TERMOQUÍMICA. Prof. Harley P. Martins Filho
|
|
|
- Natália Taveira Bardini
- 5 Há anos
- Visualizações:
Transcrição
1 TERMOQUÍMICA Prof. arley P. Martins Filho Teroquíica Medida do calor desenvolvido e u processo Identificação de E ou Cálculos c/ E ou conhecidos Estiativas do calor correspondente a outros processos Processos que libera calor: Q p = < 0 (exotéricos) Processos que consoe calor: Q p = > 0 (endotéricos) Variações de entalpia padrão e reações: Processo: Reagentes isolados no estado padrão e tep. T Produtos isolados no estado padrão e tep. T 1
2 Estado padrão de ua substância, nua certa teperatura, é o da substância pura sob pressão de 1 bar (P ø ). Exeplo: estados padrão do hidrogênio. (g): átoos e estado gasoso a 1 bar 2 (g): oléculas e estado gasoso a 1 bar 2 (l): oléculas e estado líquido a 1 bar Teperatura convencional: 298,15 K (25ºC) T de istura dos reagentes e de separação dos produtos geralente são desprezíveis e relação ao da reação Entalpias padrão de cobustão Oxidação copleta de u coposto orgânico a CO 2 (g) e 2 O(l) (e tabé N 2 (g), se nitrogênio estiver presente na olécula). Exeplo: Glicose C 6 12 O 6 (s) 6O 2 (g) 6CO 2 (g) 6 2 O(l) ø cob = kjol -1 2
3 Entalpias associadas a copostos A entalpia de u sistea é a soa das contribuições individuais de cada coposto que copõe o sistea (entalpias olares padrão ø ) Equação teroquíica: 2A 3B 4C ø = X kjol -1 ø = [4 ø (C)] [3 ø (B) 2 ø (A)] E geral, J ( J ), onde J é o coeficiente J estequioétrico (adiensional) do coposto J (positivo se produto e negativo se reagente) ø (J) e ø tê unidades kj ol -1. ø (J) = E ø (J) PV (J) = E ø (J) 1 barv (J), as não teos valores absolutos de E ø (J). Entalpia padrão de foração: variação de entalpia da reação e que o coposto é forado a partir de seus eleentos no estado de referência (estado ais estável na teperatura especificada e sob pressão de 1 bar) Exeplo: idrogênio e três estados padrão (1 bar e 25C) (g) 2 (g) estado de referência 2 (l) Exeplos de forações: Benzeno líquido: 6C(s,grafita) 3 2 (g) C 6 6 (l) ø f = 49,0 kjol -1 idróxido de sódio: Na(s) (1/2)O 2 (g) (1/2) 2 (g) NaO(s) ø f = -425,61 kjol -1 Nitrogênio atôico: (1/2)N 2 (g) N(g) ø f = 472,70 kjol -1 Enxofre onoclínico: S(s,) (rôbico) S(s,) (onoclínico) ø f = 0,33 kjol -1 3
4 Entalpia de reação e teros de entalpias de foração: Reação geral: eleentos Reagentes Produtos reação reação f f prod. reag. prod. ele. reag.. ele. prod. reag.. Para efeitos de cálculo de ø reação, são irrelevantes as entalpias dos eleentos no estado de referência. Convenciona-se então que para eleentos no estado de referência, ø = 0. Coo consequência, ø = ø f para qualquer coposto quíico (incluindo eleentos fora do estado de referência). O raciocínio é válido para qualquer propriedade de estado. Por exeplo, pode-se considerar a energia interna de foração de u coposto E f coo a sua energia interna olar, para efeitos de cálculos de E de reações. 4
5 Entalpias de foração geralente são edidas indiretaente, usando por exeplo entalpias de cobustão. Exeplo: Propano C 3 C 2 C 3 (g) 5O 2 (g) 3CO 2 (g) 4 2 O(l) ø cob = kjol -1 = 4 ø f( 2 O(l)) 3 ø f(co 2 (g)) - ø f(propano(g)) Mas as reações de foração de 2 O e CO 2 são fáceis de realizar: C(s, grafita) O 2 (g) CO 2 (g) ø = -393,51 kjol -1 = ø f(co 2 (g)) 2 (g) ½O 2 (g) 2 O(l) ø = -285,83 kjol -1 = ø f( 2 O(l)) ø f(propano(g)) = 4(-285,83) 3(-393,51) (-2220) = -104 kjol -1 Lei de ess A entalpia padrão de ua reação é igual à soa das entalpias padrões de reações interediárias e que a reação possa ser dividida. Exeplo: Cálculo da entalpia de foração de u coposto inorgânico (NaO) pela lei de ess: Na(s) (1/2)O 2 (g) (1/2) 2 (g) NaO(s) Reações interediárias: I Forar água a partir de hidrogênio e oxigênio II Reagir a água co sódio, dando NaO(aq) III Secar o NaO (inverso da solubilização) 5
6 2 (g) (1/2)O 2 (g) 2 O(l) ø = -285,83 kjol -1 Na(s) 2 O(l) NaO(aq) (1/2) 2 (g) ø = -184,28 kjol -1 NaO(aq) NaO(s) ø = 44,5 kjol -1 Na(s) (1/2)O 2 (g) (1/2) 2 (g) NaO(s) ø = -425,61 kjol -1 Energias de ligação Reação geral de dissociação: AB(g) A(g) B(g) E(AB) Espectroetria de assas co fotoionização E u espectrôetro de assas co ua fonte de luz de frequência sintonizável ede-se a frequência liiar de aparição de íons forados a partir de ua olécula neutra. A energia da reação correspondente é calculada coo h. Exeplo: a partir de BCl 3 fora-se os íons BCl 3 (/z = 116), BCl 2 (/z = 81) e BCl (/z = 46). E (ev/kj ol -1 ) BCl 3 hv BCl 3 e 11,60/1119,2 (I) BCl 2 Cl e 12,30/1186,7 (II) BCl 2Cl e 18,37/1772,4 (III) 6
7 Através de espectroscopia de absorção e infraverelho (espectroscopia vibracional) é possível se deterinar a energia de ligação de oléculas diatôicas. Exeplo: E(ClCl) = 240,0 kj ol -1 E f (Cl) = 120,0 kj ol -1. Sabendo tabé que E f (BCl 3 ) = -402,8 kj ol -1, a energia da reação (II) pode ser expressa coo 1186,7 = E f (BCl 2 ) 120,0 (-402,8) E f (BCl 2 ) = 663,9 kj ol -1 Analisando no espectrôetro de assas a olécula B 2 Cl 4 : E (ev/kj ol -1 ) B 2 Cl 4 hv BCl 2 BCl 2 e 11,32/1092,2 (IV) Sabendo que E f (B 2 Cl 4 ) = -489,90 kj ol -1, a energia da reação (IV) pode ser expressa coo 1092,2 = E f (BCl 2 ) 663,9 (-489,90) E f (BCl 2 ) = -61,6 kj ol -1 Mas agora podeos deterinar energias de ligação: BCl 3 BCl 2 Cl E(Cl BCl 2 ) = 120,0 (-61,6) (-402,8) = 461,2 kj ol -1 B 2 Cl 4 2BCl 2 E(Cl 2 B BCl 2 ) = 2(-61,6) (-489,90) = 366,7 kj ol -1 Para entalpias de ligação: = E n g RT 7
8 A dependência da reação co a teperatura Entalpia de reagentes e produtos varia diferenciadaente co T: Para ua substância estável variando de teperatura: T 2 CPdT ( T2 ) ( ) Aplicando para cada coponente de ua reação: a ( a, T ) b ( b, T2 ) 2 ( a, T ) ( b, T ) 1 1 T2 T2 C C P, P, T2 C P ( b) dt dt ( a) dt Soando todas as equações: Onde 2 T ) ( T ) C dt r( 2 r 1 C P jcp, ( j) j Se as C P, são consideradas constantes, T Lei de Kirchhoff Exeplo: para a reação 2 (g) 1/2O 2 (g) 2 O(g), ø f (25C) = - 241,82 kj ol -1. Qual a entalpia de foração a 100C? P T ) ( T ) C T r( 2 r 1 P C P (J K -1 ol -1 ) 2 O(g) 33,58 2 (g) 28,84 O 2 (g) 29,37 C P = 133,58 (1/2)29,37-128,84 = -9,94 J K -1 ol -1 ø f (100C) = -241, (-9,94)(100 25) = -241, , = -242,57 kj ol -1 8
[AE-8 2] QUIMICA: Termoquimica Prof. Douglas_26/09/2018. II. H2 1 2 O2 H2O H 68,3 kcal III. C6H12 O6 6 O2 6 CO2 6 H2O H 673,0 kcal
![[AE-8 2] QUIMICA: Termoquimica Prof. Douglas_26/09/2018. II. H2 1 2 O2 H2O H 68,3 kcal III. C6H12 O6 6 O2 6 CO2 6 H2O H 673,0 kcal [AE-8 2] QUIMICA: Termoquimica Prof. Douglas_26/09/2018. II. H2 1 2 O2 H2O H 68,3 kcal III. C6H12 O6 6 O2 6 CO2 6 H2O H 673,0 kcal](/thumbs/87/96768897.jpg) [AE-8 ]. (Uece 8) Considerando a equação de foração da glicose não balanceada C H O C6H O 6, atente às seguintes equações: I. C O CO H 94,kcal II. H O HO H 68,3 kcal III. C6H O6 6 O 6 CO 6 HO H 673, kcal
[AE-8 ]. (Uece 8) Considerando a equação de foração da glicose não balanceada C H O C6H O 6, atente às seguintes equações: I. C O CO H 94,kcal II. H O HO H 68,3 kcal III. C6H O6 6 O 6 CO 6 HO H 673, kcal
UNICID MEDICINA - Primeiro Semestre UNIVERSIDADE CIDADE DE SÃO PAULO
 UNICID 018 - MEDICINA - Prieiro Seestre UNIVERSIDADE CIDADE DE SÃ PAUL 01. petróleo bruto apresenta ipurezas, coo água salgada, areia e argila, que precisa ser retiradas por étodos físicos de separação
UNICID 018 - MEDICINA - Prieiro Seestre UNIVERSIDADE CIDADE DE SÃ PAUL 01. petróleo bruto apresenta ipurezas, coo água salgada, areia e argila, que precisa ser retiradas por étodos físicos de separação
CUSC MEDICINA - Segundo Semestre CENTRO UNIVERSITÁRIO SÃO CAMILO
 CUSC 016 - MEDICINA - Segundo Seestre CENTRO UNIVERSITÁRIO SÃO CAMILO 01. A ureia, CO(N ), presente nos fertilizantes, pode ser identificada quiicaente e u teste siples, confore a reação representada pela
CUSC 016 - MEDICINA - Segundo Seestre CENTRO UNIVERSITÁRIO SÃO CAMILO 01. A ureia, CO(N ), presente nos fertilizantes, pode ser identificada quiicaente e u teste siples, confore a reação representada pela
CUSC MEDICINA Segundo Semestre CENTRO UNIVERSITÁRIO SÃO CAMILO
 US 018 - MEDIINA Segundo Seestre ENTR UNIERSITÁRI SÃ AMIL 01. iplante de icrocápsulas do radioisótopo iodo-15 diretaente no órgão do paciente é ua das foras de radioterapia usadas no trataento do câncer
US 018 - MEDIINA Segundo Seestre ENTR UNIERSITÁRI SÃ AMIL 01. iplante de icrocápsulas do radioisótopo iodo-15 diretaente no órgão do paciente é ua das foras de radioterapia usadas no trataento do câncer
FMJ MEDICINA FACULDADE DE MEDICINA DE JUNDIAÍ
 FMJ 2017 - MEDIINA FAULDADE DE MEDIINA DE JUNDIAÍ 09. A água de coco é benéfica para a saúde, pois apresenta grande quantidade de sais inerais, principalente sódio (Na) e potássio (K). a) onsidere que
FMJ 2017 - MEDIINA FAULDADE DE MEDIINA DE JUNDIAÍ 09. A água de coco é benéfica para a saúde, pois apresenta grande quantidade de sais inerais, principalente sódio (Na) e potássio (K). a) onsidere que
4.º Teste de Física e Química A 10.º A Fev minutos /
 4.º Teste de Física e Quíica A 10.º A Fev. 2013 90 inutos / Noe: n.º Classificação Professor E.E. GRUPO I As seis questões deste grupo são todas de escolha últipla. Para cada ua delas são indicadas quatro
4.º Teste de Física e Quíica A 10.º A Fev. 2013 90 inutos / Noe: n.º Classificação Professor E.E. GRUPO I As seis questões deste grupo são todas de escolha últipla. Para cada ua delas são indicadas quatro
UNISA MEDICINA Primeiro semestre UNIVERSIDADE DE SANTO AMARO
 UNISA MEDIINA 2018 - Prieiro seestre UNIVERSIDADE DE SANT AMAR 01. A figura ostra a decoposição térica do carbonato de cobre (II), produzindo óxido de cobre (II) e dióxido de carbono, confore a equação:
UNISA MEDIINA 2018 - Prieiro seestre UNIVERSIDADE DE SANT AMAR 01. A figura ostra a decoposição térica do carbonato de cobre (II), produzindo óxido de cobre (II) e dióxido de carbono, confore a equação:
Nome : n o Classe: 2 2MB. Estequiometria
 Ensino Médio QUÍMICA Data: / /01 Atividade : Exercícios de Recuperação Paralela e Anual aula 1 Noe : n o Classe: MB Estequioetria 1. (Espcex (Aan)) O etino, tabé conhecido coo acetileno, é u alcino uito
Ensino Médio QUÍMICA Data: / /01 Atividade : Exercícios de Recuperação Paralela e Anual aula 1 Noe : n o Classe: MB Estequioetria 1. (Espcex (Aan)) O etino, tabé conhecido coo acetileno, é u alcino uito
Curso Semi-extensivo LISTA EXERCÍCIOS - 03 Disciplina: Química Professor: Eduar Fernando Rosso
 Curso Sei-extensivo LISTA EXERCÍCIOS - 03 Disciplina: Quíica Professor: Eduar Fernando Rosso assa Atôica, assa olecular e ol 01 (Ufpr 2017) E oentos de estresse, as glândulas suprarrenais secreta o horônio
Curso Sei-extensivo LISTA EXERCÍCIOS - 03 Disciplina: Quíica Professor: Eduar Fernando Rosso assa Atôica, assa olecular e ol 01 (Ufpr 2017) E oentos de estresse, as glândulas suprarrenais secreta o horônio
Termoquímica. Iniciação à Química II. Prof. Edson Nossol
 Termoquímica Iniciação à Química II Prof. Edson Nossol Uberlândia, 20/10/2017 Energia de ligação (dissociação): energia necessária para romper a ligação H (entalpia de ligação): variação de calor que acompanha
Termoquímica Iniciação à Química II Prof. Edson Nossol Uberlândia, 20/10/2017 Energia de ligação (dissociação): energia necessária para romper a ligação H (entalpia de ligação): variação de calor que acompanha
UNISA MEDICINA 2014 UNIVERSIDADE DE SANTO AMARO
 UNISA MEDIINA 2014 UNIVERSIDADE DE SANTO AMARO ONHEIMENTOS GERAIS 50. A vida no planeta Terra está baseada e dois eleentos essenciais. U deles está presente e todos os copostos orgânicos e é versátil,
UNISA MEDIINA 2014 UNIVERSIDADE DE SANTO AMARO ONHEIMENTOS GERAIS 50. A vida no planeta Terra está baseada e dois eleentos essenciais. U deles está presente e todos os copostos orgânicos e é versátil,
Nome : n o Classe: 2 1MA. Estequiometria
 Ensino Médio QUÍMICA Data: / /2012 Atividade : Exercícios de Recuperação Paralela e Anual aula 4 Noe : n o Classe: 2 1MA Estequioetria 1. (Espcex (Aan)) O etino, tabé conhecido coo acetileno, é u alcino
Ensino Médio QUÍMICA Data: / /2012 Atividade : Exercícios de Recuperação Paralela e Anual aula 4 Noe : n o Classe: 2 1MA Estequioetria 1. (Espcex (Aan)) O etino, tabé conhecido coo acetileno, é u alcino
G1 - PROVA DE QUÍMICA GERAL 08/04/06
 G1 - PROVA DE QUÍMICA GERAL 08/04/06 Noe: Gabarito Nº de Matrícula: Tura: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Dados R 0,081 at L ol -1 K -1 T (K ) T ( C) + 73,15 1 at
G1 - PROVA DE QUÍMICA GERAL 08/04/06 Noe: Gabarito Nº de Matrícula: Tura: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Dados R 0,081 at L ol -1 K -1 T (K ) T ( C) + 73,15 1 at
H inicial. ΔH = H final H inicial ΔH = [+ 10] [2(+ 34)] ΔH = 58 kj. ΔH em kj por mol de NO 2 que dimeriza? NO 2 N 2 O 4 ΔH = 58/2 kj
![H inicial. ΔH = H final H inicial ΔH = [+ 10] [2(+ 34)] ΔH = 58 kj. ΔH em kj por mol de NO 2 que dimeriza? NO 2 N 2 O 4 ΔH = 58/2 kj H inicial. ΔH = H final H inicial ΔH = [+ 10] [2(+ 34)] ΔH = 58 kj. ΔH em kj por mol de NO 2 que dimeriza? NO 2 N 2 O 4 ΔH = 58/2 kj](/thumbs/51/27357048.jpg) setor 13 130409 130409-SP Aula 5 CÁLCULO DE ΔH DE REAÇÃO ATRAVÉS DE ENTALPIAS DE FORMAÇÃO + x zero y H (kcal ou kj) A entalpia (H) de 1,0 ol de ua substância coposta é nuericaente igual ao respectivo Calor
setor 13 130409 130409-SP Aula 5 CÁLCULO DE ΔH DE REAÇÃO ATRAVÉS DE ENTALPIAS DE FORMAÇÃO + x zero y H (kcal ou kj) A entalpia (H) de 1,0 ol de ua substância coposta é nuericaente igual ao respectivo Calor
UNINOVE MEDICINA - Primeiro Semestre - Discursivas UNIVERSIDADE NOVE DE JULHO
 UNINOVE 2016 - MEDICINA - Prieiro Seestre - Discursivas UNIVERSIDADE NOVE DE JULHO 01. O anganês (Mn) te papel iportante e todos os organisos aniais e vegetais. No organiso huano, o anganês é u coponente
UNINOVE 2016 - MEDICINA - Prieiro Seestre - Discursivas UNIVERSIDADE NOVE DE JULHO 01. O anganês (Mn) te papel iportante e todos os organisos aniais e vegetais. No organiso huano, o anganês é u coponente
Termoquímica Entalpia e Lei de Hess
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Termoquímica Entalpia e Lei de Hess Sistemas a Pressão Constante Quando o volume do sistema não é constante,
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Termoquímica Entalpia e Lei de Hess Sistemas a Pressão Constante Quando o volume do sistema não é constante,
FMJ MEDICINA FACULDADE DE MEDICINA DE JUNDIAÍ
 FMJ 2016 - MEDICINA FACULDADE DE MEDICINA DE JUNDIAÍ 09. Considere o esquea de u sistea utilizado para deonstrar a condutividade elétrica de soluções e a tabela que apresenta três soluções aquosas, de
FMJ 2016 - MEDICINA FACULDADE DE MEDICINA DE JUNDIAÍ 09. Considere o esquea de u sistea utilizado para deonstrar a condutividade elétrica de soluções e a tabela que apresenta três soluções aquosas, de
UNIFEV MEDICINA - Segundo Semestre CENTRO UNIVERSITÁRIO DE VOTUPORANGA
 UNFEV 09 - MEDNA - Segundo Seestre ENTR UNVERSTÁR DE VTUPRANGA 0. Ua das técnicas de radioterapia utilizadas para o trataento de tuores de fígado consiste na ingestão de icroesferas de ácido -hidroxipropanoico,
UNFEV 09 - MEDNA - Segundo Seestre ENTR UNVERSTÁR DE VTUPRANGA 0. Ua das técnicas de radioterapia utilizadas para o trataento de tuores de fígado consiste na ingestão de icroesferas de ácido -hidroxipropanoico,
Físico-Química I. Profa. Dra. Carla Dalmolin. Termoquímica. Transformações físicas. Transformações químicas
 Físico-Química I Profa. Dra. Carla Dalmolin Termoquímica Transformações físicas Transformações químicas Termoquímica Estudo do calor trocado quando ocorrem reações químicas Sistema Sistema Vizinhança Se
Físico-Química I Profa. Dra. Carla Dalmolin Termoquímica Transformações físicas Transformações químicas Termoquímica Estudo do calor trocado quando ocorrem reações químicas Sistema Sistema Vizinhança Se
Semana 04. CANTO, E. L. Minerais, minérios, metais: de onde vêm?, para onde vão? São Paulo: Moderna, 1996 (adaptado).
 Seana 04 Seana 04 01. (Ene 2016) A iniização do tepo e custo de ua reação quíica, be coo o auento na sua taxa de conversão, caracteriza a eficiência de u processo quíico. Coo consequência, produtos pode
Seana 04 Seana 04 01. (Ene 2016) A iniização do tepo e custo de ua reação quíica, be coo o auento na sua taxa de conversão, caracteriza a eficiência de u processo quíico. Coo consequência, produtos pode
TRANSIÇÕES DE FASE DE SUBSTÂNCIAS PURAS
 RANSIÇÕES DE FASE DE SUBSÂNCIAS URAS rof. Harley. Martins Filho A explosão do space shuttle Chalenger 1 1. Fases e ições Fase de ua substância: Fora da atéria que é hoogênea e coposição quíica e propriedades
RANSIÇÕES DE FASE DE SUBSÂNCIAS URAS rof. Harley. Martins Filho A explosão do space shuttle Chalenger 1 1. Fases e ições Fase de ua substância: Fora da atéria que é hoogênea e coposição quíica e propriedades
Seu sonho, nossa meta Pa. Resposta da questão 1: [B]
![Seu sonho, nossa meta Pa. Resposta da questão 1: [B] Seu sonho, nossa meta Pa. Resposta da questão 1: [B]](/thumbs/53/31499670.jpg) RESOSTAS CAÍTULO 6-GASES Resposta da questão 1: [B] A pressão parcial do gás oxigênio ao nível do ar é igual a 1% da pressão atosférica do ar, assi teos: O 0,1100000 po 1000O 0,1100000 po 1000 a O E La
RESOSTAS CAÍTULO 6-GASES Resposta da questão 1: [B] A pressão parcial do gás oxigênio ao nível do ar é igual a 1% da pressão atosférica do ar, assi teos: O 0,1100000 po 1000O 0,1100000 po 1000 a O E La
EXAME NACIONAL 2009 ÉPOCA ESPECIAL PROPOSTA DE RESOLUÇÃO
 EXAME NACIONAL 009 ÉPOCA ESPECIAL PROPOSTA DE RESOLUÇÃO 1 11 O único facto referido no texto que justifica a elevada aplitude térica observada na Lua é a ausência de atosfera apreciável 1 (C Para u objecto
EXAME NACIONAL 009 ÉPOCA ESPECIAL PROPOSTA DE RESOLUÇÃO 1 11 O único facto referido no texto que justifica a elevada aplitude térica observada na Lua é a ausência de atosfera apreciável 1 (C Para u objecto
TERMOQUÍMICA. 1 Fenômenos endotérmicos e exotérmicos
 TERMOQUÍMICA 1 Fenômenos endotérmicos e exotérmicos a) Processos exotérmicos: Ocorrem com liberação de calor. Possuem variação de entalpia ( H) negativa. Ex: Combustão do metano (CH4) CH4 (g) + 2 O2 (g)
TERMOQUÍMICA 1 Fenômenos endotérmicos e exotérmicos a) Processos exotérmicos: Ocorrem com liberação de calor. Possuem variação de entalpia ( H) negativa. Ex: Combustão do metano (CH4) CH4 (g) + 2 O2 (g)
GABARITO - Revisão UNESP/ UNIFESP 2015
 GABARITO - Revisão UNESP/ UNIFESP 015 Resposta da questão 1: a) Coposto 1: aida. Coposto : álcool. b) A estrutura 1 apresenta isoeria óptica, pois possui carbono quiral ou assiétrico (*). O caráter ácido-básico
GABARITO - Revisão UNESP/ UNIFESP 015 Resposta da questão 1: a) Coposto 1: aida. Coposto : álcool. b) A estrutura 1 apresenta isoeria óptica, pois possui carbono quiral ou assiétrico (*). O caráter ácido-básico
Gases reais. Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departaento de Quíica Gases reais Professora: Melissa Soares Caetano Disciplina QUI 17 Gases reais Exibe desvios e relação ao
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departaento de Quíica Gases reais Professora: Melissa Soares Caetano Disciplina QUI 17 Gases reais Exibe desvios e relação ao
a) C 3 H 8 (g) 3C graf. + 4 H 2(g) C 3 H 8(g) b) C 2 H 6 O(l) 2C graf. + 3 H 2(g) + 1/2 O 2(g) C 2 H 6 O (l) c) Na 2 SO 4 (s)
 setor 30 300408 Aula 3 TERMOQUÍMICA. ENTALPIA DE FORMAÇÃO Estado Padrão = Estado físico e alotrópico mais estáveis em condição ambiente (5 C, atm). Substâncias Simples no Estado Padrão H FORM H FORM =
setor 30 300408 Aula 3 TERMOQUÍMICA. ENTALPIA DE FORMAÇÃO Estado Padrão = Estado físico e alotrópico mais estáveis em condição ambiente (5 C, atm). Substâncias Simples no Estado Padrão H FORM H FORM =
Gases reais. Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departaento de Quíica Gases reais Professora: Melissa Soares Caetano Disciplina QUI 17 Gases reais Exibe desvios e relação ao
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departaento de Quíica Gases reais Professora: Melissa Soares Caetano Disciplina QUI 17 Gases reais Exibe desvios e relação ao
ZEA0466 TERMODINÂMICA
 ZEA0466 TERMODINÂMICA SUBSTÂNCIAS PURAS Substâncias Puras Coposição quíica: Hoogênea e invariável Pode existir e ais de ua fase as a coposição quíica é a esa para todas as fases; Mistura de gases (exeplo:
ZEA0466 TERMODINÂMICA SUBSTÂNCIAS PURAS Substâncias Puras Coposição quíica: Hoogênea e invariável Pode existir e ais de ua fase as a coposição quíica é a esa para todas as fases; Mistura de gases (exeplo:
UNIFEV MEDICINA - Segundo Semestre CENTRO UNIVERSITÁRIO DE VOTUPORANGA
 UNIFEV 013 - MEDICINA - Segundo Seestre CENTRO UNIVERSITÁRIO DE VOTUPORANGA 07. Alguns gases possue aplicações e trataento estéticos e de saúde, a seguir são reportados três deles e alguas de suas aplicações.
UNIFEV 013 - MEDICINA - Segundo Seestre CENTRO UNIVERSITÁRIO DE VOTUPORANGA 07. Alguns gases possue aplicações e trataento estéticos e de saúde, a seguir são reportados três deles e alguas de suas aplicações.
PROFESSOR: EQUIPE DE QUÍMICA
 PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA ORGÂNICA 2ª SÉRIE - ENSINO MÉDIO - PARTE 2 ============================================================================================= Termoquímica
PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA ORGÂNICA 2ª SÉRIE - ENSINO MÉDIO - PARTE 2 ============================================================================================= Termoquímica
QUÍMICA 2 Volume 1 RESOLUÇÕES EXERCITANDO EM CASA
 1 QUÍMICA olue 1 RESOLUÇÕES EXERCITANDO EM CASA AULA 1 01. C [Resposta do ponto de vista da disciplina de Quíica] Cálculo do volue da grafita. 0. A Massa olar do coposto C 11H 1N O 6: 8 g/ol 8 g 6,0 10
1 QUÍMICA olue 1 RESOLUÇÕES EXERCITANDO EM CASA AULA 1 01. C [Resposta do ponto de vista da disciplina de Quíica] Cálculo do volue da grafita. 0. A Massa olar do coposto C 11H 1N O 6: 8 g/ol 8 g 6,0 10
UNIFEV MEDICINA - Segundo Semestre CENTRO UNIVERSITÁRIO DE VOTUPORANGA
 UNIFEV 01 - MEDIINA - Segundo Seestre ENTR UNIVERSITÁRI DE VTUPRANGA 07. A istura de gás oxigênio co acetileno ( H ) é utilizada na soldage de peças nas oficinas ecânicas. acetileno pode ser produzido
UNIFEV 01 - MEDIINA - Segundo Seestre ENTR UNIVERSITÁRI DE VTUPRANGA 07. A istura de gás oxigênio co acetileno ( H ) é utilizada na soldage de peças nas oficinas ecânicas. acetileno pode ser produzido
SOLUÇÃO PRATIQUE EM CASA
 SOLUÇÃO PRATIQUE EM CASA SOLUÇÃO PC1. [E] Na osose, o solvente igra da região aior pressão vapor para a enor pressão vapor. Solução 1 cloreto sódio (0,15 ol/l; esa pressão osótica das soluções presentes
SOLUÇÃO PRATIQUE EM CASA SOLUÇÃO PC1. [E] Na osose, o solvente igra da região aior pressão vapor para a enor pressão vapor. Solução 1 cloreto sódio (0,15 ol/l; esa pressão osótica das soluções presentes
CQ 050 FÍSICO QUÍMICA EXPERIMENTAL I. Revisão para a 1 a. prova
 CQ 050 FÍSICO QUÍMICA EXPERIMENAL I Revisão para a 1 a prova PRÁICA 01 DENSIDADE DOS GASES O Gás Perfeito (ideal) 1ª ipótese: as oléculas se encontra e oviento desordenado, regido pelo princípio da Mecânica
CQ 050 FÍSICO QUÍMICA EXPERIMENAL I Revisão para a 1 a prova PRÁICA 01 DENSIDADE DOS GASES O Gás Perfeito (ideal) 1ª ipótese: as oléculas se encontra e oviento desordenado, regido pelo princípio da Mecânica
Colégio Estadual Professor Ernesto Faria. Subprojeto Pibid - Química UERJ. Termoquímica
 Colégio Estadual Professor Ernesto Faria Subprojeto Pibid - Química UERJ Termoquímica REAÇÕES ENDOTÉRMICAS E EXOTÉRMICAS Processo Exotérmico Libera calor para ambiente (vizinhança) Transmite sensação de
Colégio Estadual Professor Ernesto Faria Subprojeto Pibid - Química UERJ Termoquímica REAÇÕES ENDOTÉRMICAS E EXOTÉRMICAS Processo Exotérmico Libera calor para ambiente (vizinhança) Transmite sensação de
Exercícios 1. Deduzir a relação:
 setor 1322 13220509 13220509-SP Aula 35 RELAÇÕES ENTRE ÁRIOS TIPOS DE CONCENTRAÇÃO Tipo de concentração Cou E ol/l As conversões entre esses tipos de concentração pode ser feitas: Aditindo-se 1,0 L de
setor 1322 13220509 13220509-SP Aula 35 RELAÇÕES ENTRE ÁRIOS TIPOS DE CONCENTRAÇÃO Tipo de concentração Cou E ol/l As conversões entre esses tipos de concentração pode ser feitas: Aditindo-se 1,0 L de
Universidade Federal do Acre Engenharia Agronômica PET- Programa de Ensino Tutorial. Termoquímica
 Universidade Federal do Acre Engenharia Agronômica PET- Programa de Ensino Tutorial Termoquímica Bolsista: Joyce de Q. Barbosa Tutor: Dr. José Ribamar Silva Termodinâmica Conceitos Básicos Termoquímica
Universidade Federal do Acre Engenharia Agronômica PET- Programa de Ensino Tutorial Termoquímica Bolsista: Joyce de Q. Barbosa Tutor: Dr. José Ribamar Silva Termodinâmica Conceitos Básicos Termoquímica
II Matrizes de rede e formulação do problema de fluxo de carga
 Análise de Sisteas de Energia Elétrica Matrizes de rede e forulação do problea de fluxo de carga O problea do fluxo de carga (load flow e inglês ou fluxo de potência (power flow e inglês consiste na obtenção
Análise de Sisteas de Energia Elétrica Matrizes de rede e forulação do problea de fluxo de carga O problea do fluxo de carga (load flow e inglês ou fluxo de potência (power flow e inglês consiste na obtenção
PROFª. KAÍZA CAVALCANTI
 Processos Químicos Quando ocorre uma alteração qualitativa do sistema, dos tipos de substâncias presentes ou de suas proporções. Processos Físicos Quando ocorre uma alteração qualitativa do sistema, dos
Processos Químicos Quando ocorre uma alteração qualitativa do sistema, dos tipos de substâncias presentes ou de suas proporções. Processos Físicos Quando ocorre uma alteração qualitativa do sistema, dos
P2 - PROVA DE QUÍMICA GERAL - 27/10/12
 P2 - PROVA DE QUÍMICA GERAL - 27/10/12 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados: T (K) = T ( C) + 273,15 R = 8,314
P2 - PROVA DE QUÍMICA GERAL - 27/10/12 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados: T (K) = T ( C) + 273,15 R = 8,314
Entalpia. O trabalho realizado por esta reação é denominado trabalho de pressão-volume (trabalho PV)
 Entalpia As reações químicas podem absorver ou liberar calor e também podem provocar a realização de trabalho. Quando um gás é produzido, ele pode ser utilizado para empurrar um pistão: Zn(s) + 2H + (aq)
Entalpia As reações químicas podem absorver ou liberar calor e também podem provocar a realização de trabalho. Quando um gás é produzido, ele pode ser utilizado para empurrar um pistão: Zn(s) + 2H + (aq)
P1 - PROVA DE QUÍMICA GERAL 22/03/2014
 P1 - PROV DE QUÍMIC GERL 22/03/2014 Noe: Nº de Matrícula: GRITO Tura: ssinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados R = 0,0821 at L ol -1 K -1 T (K) = T ( C) +
P1 - PROV DE QUÍMIC GERL 22/03/2014 Noe: Nº de Matrícula: GRITO Tura: ssinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados R = 0,0821 at L ol -1 K -1 T (K) = T ( C) +
UNICID MEDICINA - Primeiro Semestre UNIVERSIDADE CIDADE DE SÃO PAULO
 UNIID 019 - MEDIINA - Prieiro Seestre UNIVERSIDADE IDADE DE SÃ PAUL 01. A tabela apresenta os pontos de fusão e de ebulição de três iportantes solventes. Substância Fórula estrutural Ponto de fusão ( o
UNIID 019 - MEDIINA - Prieiro Seestre UNIVERSIDADE IDADE DE SÃ PAUL 01. A tabela apresenta os pontos de fusão e de ebulição de três iportantes solventes. Substância Fórula estrutural Ponto de fusão ( o
Diagramas Binários Introdução
 Diagraas inários Introdução Nos sisteas de u coponente, a P e T deterina as fases de equilíbrio: Equação de Clausius- Clapeyron deterina os pares de pontos (P,T) dos equilíbrios. T Nos sisteas de inários---
Diagraas inários Introdução Nos sisteas de u coponente, a P e T deterina as fases de equilíbrio: Equação de Clausius- Clapeyron deterina os pares de pontos (P,T) dos equilíbrios. T Nos sisteas de inários---
A B EQUILÍBRIO QUÍMICO. H 2 + 2ICl I 2 + 2HCl. % Ach
 A B EQUILÍBRIO QUÍMICO H 2 + 2ICl I 2 + 2HCl!. % % Ach. Ac 1 Equilíbrio Químico - Reversibilidade de reações químicas A B Exemplo: N 2 (g) + 3H 2 (g) 2NH 3 (g) equilíbrio dinâmico aa + bb yy + zz Constante
A B EQUILÍBRIO QUÍMICO H 2 + 2ICl I 2 + 2HCl!. % % Ach. Ac 1 Equilíbrio Químico - Reversibilidade de reações químicas A B Exemplo: N 2 (g) + 3H 2 (g) 2NH 3 (g) equilíbrio dinâmico aa + bb yy + zz Constante
Quase toda reação química é acompanhada de liberação ou absorção de calor (queima da gasolina, queima do etanol,
 TERMOQUÍMICA TERMOQUÍMICA Quase toda reação química é acompanhada de liberação ou absorção de calor (queima da gasolina, queima do etanol, queima do GLP). A termoquímica estuda as quantidades de calor
TERMOQUÍMICA TERMOQUÍMICA Quase toda reação química é acompanhada de liberação ou absorção de calor (queima da gasolina, queima do etanol, queima do GLP). A termoquímica estuda as quantidades de calor
a) 65,2 103 b) 32,6 103 c) 24, d) 16,3 103 e) 10,9 103
 01) (FEI-SP) A queima de 46 g de álcool etílico (C 2H 6O) libera 32,6 kcal. Sabendo que a densidade do álcool é de 0,8g/cm3, o calor liberado na queima de 28,75 litros de álcool será, em kcal, a) 65,2
01) (FEI-SP) A queima de 46 g de álcool etílico (C 2H 6O) libera 32,6 kcal. Sabendo que a densidade do álcool é de 0,8g/cm3, o calor liberado na queima de 28,75 litros de álcool será, em kcal, a) 65,2
11ª LISTA - EXERCÍCIOS DE PROVAS Energia Livre
 Pg. 1/5 1ª. Questão Considere o processo de sublimação (eq. 1) e a reação de dissociação (eq. 2) do iodo e responda o que se pede. Sublimação do iodo: I 2 (s) I 2 (g) eq. 1 Reação de dissociação do iodo:
Pg. 1/5 1ª. Questão Considere o processo de sublimação (eq. 1) e a reação de dissociação (eq. 2) do iodo e responda o que se pede. Sublimação do iodo: I 2 (s) I 2 (g) eq. 1 Reação de dissociação do iodo:
ENEM Prova resolvida Química
 ENEM 2001 - Prova resolvida Quíica 01. Nua rodovia pavientada, ocorreu o tobaento de u cainhão que transportava ácido sulfúrico concentrado. Parte da sua carga fluiu para u curso d' não poluído que deve
ENEM 2001 - Prova resolvida Quíica 01. Nua rodovia pavientada, ocorreu o tobaento de u cainhão que transportava ácido sulfúrico concentrado. Parte da sua carga fluiu para u curso d' não poluído que deve
SOLUÇÃO PRATIQUE EM CASA
 SOLUÇÃO PRATIQUE EM CASA SOLUÇÃO PC1. [C] Adicionando-se ácido clorídrico, e solução aquosa, a carbonato de cálcio, tereos a seguinte reação: HC (aq) CaCO3(s) H O( ) CO(g) CaC (aq). A diferença de assa
SOLUÇÃO PRATIQUE EM CASA SOLUÇÃO PC1. [C] Adicionando-se ácido clorídrico, e solução aquosa, a carbonato de cálcio, tereos a seguinte reação: HC (aq) CaCO3(s) H O( ) CO(g) CaC (aq). A diferença de assa
UDESC 2017/2 QUÍMICA. Comentário
 QUÍMICA Sólido: volume definido; forma definida. Líquido: volume definido; forma variável. Gasoso: volume variável; forma variável. 1 e resolução SiC 4 + 2 Mg Si + 2 MgC 2 170,1 g + 48,6 g 28,1 g Massa
QUÍMICA Sólido: volume definido; forma definida. Líquido: volume definido; forma variável. Gasoso: volume variável; forma variável. 1 e resolução SiC 4 + 2 Mg Si + 2 MgC 2 170,1 g + 48,6 g 28,1 g Massa
UNIVERSIDADE NOVE DE JULHO - UNINOVE 2019 MEDICINA - Primeiro Semestre
 UNIVRSIDAD NOV D JULO - UNINOV 2019 DICINA - Prieiro Seestre CONCINTOS GRAIS SPCÍFICOS CONCINTOS GRAIS 01. Ouro e ercúrio estão dispostos lado a lado na Classificação Periódica. No que diz respeito à estrutura
UNIVRSIDAD NOV D JULO - UNINOV 2019 DICINA - Prieiro Seestre CONCINTOS GRAIS SPCÍFICOS CONCINTOS GRAIS 01. Ouro e ercúrio estão dispostos lado a lado na Classificação Periódica. No que diz respeito à estrutura
PROF: Alex LISTA 2 DATA: 07/ 03/ 2011
 NOME: PROF: Alex LISTA DATA: 07/ 03/ 011 Teroquíica ( a Fase) 1. (Pucrj 006) Dadas as reações teroquíicas de foração NO(g) NO(g) + O(g) H 0 = 114 kj/ol de CO (reações 1a e 1b): 6 NO(g) + HO(l) 4 HNO3(aq)
NOME: PROF: Alex LISTA DATA: 07/ 03/ 011 Teroquíica ( a Fase) 1. (Pucrj 006) Dadas as reações teroquíicas de foração NO(g) NO(g) + O(g) H 0 = 114 kj/ol de CO (reações 1a e 1b): 6 NO(g) + HO(l) 4 HNO3(aq)
GABARITO R4 SETOR 1301
 GABARITO R4 QUÍMICA SETOR 1301 Resposta da questão 01: a) A foração do políero ocorre a partir do glicerol, confore indicado no texto. Possível políero de cadeia raificada: b) Quanto aior for o grau de
GABARITO R4 QUÍMICA SETOR 1301 Resposta da questão 01: a) A foração do políero ocorre a partir do glicerol, confore indicado no texto. Possível políero de cadeia raificada: b) Quanto aior for o grau de
CH 4(g) + 2 O 2(g) à CO 2(g) + 2 H 2 O (g) H = -800 kj/mol
 . (UFRO) Reações e que a energia dos reagentes é inferior à dos produtos, à esa teperatura, são: densidade do álcool é de 0,8 g/c3, o calor liberado na queia de 8,75 litros de álcool será, e kcal: a) endotéricas.
. (UFRO) Reações e que a energia dos reagentes é inferior à dos produtos, à esa teperatura, são: densidade do álcool é de 0,8 g/c3, o calor liberado na queia de 8,75 litros de álcool será, e kcal: a) endotéricas.
Centro Universitário Anchieta Engenharia Química Físico Química I Prof. Vanderlei I Paula Nome: R.A. Gabarito 4 a lista de exercícios
 Engenharia Quíica Físico Quíica I. O abaixaento da pressão de vapor do solvente e soluções não eletrolíticas pode ser estudadas pela Lei de Raoult: P X P, onde P é a pressão de vapor do solvente na solução,
Engenharia Quíica Físico Quíica I. O abaixaento da pressão de vapor do solvente e soluções não eletrolíticas pode ser estudadas pela Lei de Raoult: P X P, onde P é a pressão de vapor do solvente na solução,
ENEM Prova resolvida Química
 ENEM 2001 - Prova resolvida Quíica 01. Nua rodovia pavientada, ocorreu o tobaento de u cainhão que transportava ácido sulfúrico concentrado. Parte da sua carga fluiu para u curso d'água não poluído que
ENEM 2001 - Prova resolvida Quíica 01. Nua rodovia pavientada, ocorreu o tobaento de u cainhão que transportava ácido sulfúrico concentrado. Parte da sua carga fluiu para u curso d'água não poluído que
TERMOQUÍMICA- 3C13. As transformações físicas também são acompanhadas de calor, como ocorre na mudanda de estados físicos da matéria.
 TERMOQUÍMICA- 3C13 As transformações físicas e as reações químicas quase sempre estão envolvidas em perda ou ganho de calor. O calor é uma das formas de energia mais comum que se conhece. A Termoquimica
TERMOQUÍMICA- 3C13 As transformações físicas e as reações químicas quase sempre estão envolvidas em perda ou ganho de calor. O calor é uma das formas de energia mais comum que se conhece. A Termoquimica
Aula 6 Primeira Lei da Termodinâmica
 Aula 6 Prieira Lei da Terodinâica 1. Introdução Coo vios na aula anterior, o calor e o trabalho são foras equivalentes de transferência de energia para dentro ou para fora do sistea. 2. A Energia interna
Aula 6 Prieira Lei da Terodinâica 1. Introdução Coo vios na aula anterior, o calor e o trabalho são foras equivalentes de transferência de energia para dentro ou para fora do sistea. 2. A Energia interna
USCS MEDICINA - Primeiro Semestre - Segunda Prova UNIVERSIDADE MUNICIPAL DE SÃO CAETANO DO SUL
 USS 2017 - MEDIINA - Prieiro Seestre - Segunda Prova UNIVERSIDADE MUNIIPAL DE SÃO AETANO DO SUL 01. A figura representa ua estação de trataento de água (ETA), responsável pela produção de água potável.
USS 2017 - MEDIINA - Prieiro Seestre - Segunda Prova UNIVERSIDADE MUNIIPAL DE SÃO AETANO DO SUL 01. A figura representa ua estação de trataento de água (ETA), responsável pela produção de água potável.
BCL 0307 Transformações Químicas
 BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 05 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Qual a importância
BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 05 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Qual a importância
Um desses processos pode ser descrito pelas transformações sucessivas, representadas pelas seguintes equações químicas:
 FUVEST 1. (Fuvest 2015) A grafite de u lápis te quinze centíetros de copriento e dois ilíetros de espessura. Dentre os valores abaixo, o que ais se aproxia do núero de átoos presentes nessa grafite é Nota:
FUVEST 1. (Fuvest 2015) A grafite de u lápis te quinze centíetros de copriento e dois ilíetros de espessura. Dentre os valores abaixo, o que ais se aproxia do núero de átoos presentes nessa grafite é Nota:
25 C = 1,00 g cm. Densidade a 25 C. 1,59 cm Solubilidade em água a. 1. (Fuvest 2016) 0,1 g 100 g de
 1. (Fuvest 016) O anal do Panaá liga os oceanos Atlântico e Pacífico. Sua travessia é feita por navios de carga genericaente chaados de Panaax, cujas diensões deve seguir deterinados parâetros, para não
1. (Fuvest 016) O anal do Panaá liga os oceanos Atlântico e Pacífico. Sua travessia é feita por navios de carga genericaente chaados de Panaax, cujas diensões deve seguir deterinados parâetros, para não
Professor Armando J. De Azevedo
 Professor Armando J. De Azevedo Química Professor Armando J. De Azevedo WWW.quimicarmando.com REAÇÃO DE ADIÇÃO As reações de adição são aquelas onde um átomo proveniente de uma substância orgânica ou inorgânica
Professor Armando J. De Azevedo Química Professor Armando J. De Azevedo WWW.quimicarmando.com REAÇÃO DE ADIÇÃO As reações de adição são aquelas onde um átomo proveniente de uma substância orgânica ou inorgânica
ENZIMAS CINÉTICA ENZIMÁTICA. Classificação. Natureza da reação catalisada. Disponibilidade comercial IMPORTÂNCIA INDUSTRIAL OBJETIVOS
 OBJETIO Medir as elocidades de transforação CINÉTICA ENZIMÁTICA Aaliar a influência de condições de reação (conc. de reagentes, enzias, teperatura, ph, etc..) nas elocidades de reação Correlacionar atraés
OBJETIO Medir as elocidades de transforação CINÉTICA ENZIMÁTICA Aaliar a influência de condições de reação (conc. de reagentes, enzias, teperatura, ph, etc..) nas elocidades de reação Correlacionar atraés
P4 - PROVA DE QUÍMICA GERAL - 28/06/08
 P4 - PROVA DE QUÍMICA GERAL - 8/06/08 Nome: Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Constantes e equações: R 0,08 atm L mol -1 K -1 8,314 J mol -1
P4 - PROVA DE QUÍMICA GERAL - 8/06/08 Nome: Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Constantes e equações: R 0,08 atm L mol -1 K -1 8,314 J mol -1
Variação de entalpia nas mudanças de estado físico. Prof. Msc.. João Neto
 Variação de entalpia nas mudanças de estado físico Prof. Msc.. João Neto Processo Endotérmico Sólido Líquido Gasoso Processo Exotérmico 2 3 Processo inverso: Solidificação da água A variação de entalpia
Variação de entalpia nas mudanças de estado físico Prof. Msc.. João Neto Processo Endotérmico Sólido Líquido Gasoso Processo Exotérmico 2 3 Processo inverso: Solidificação da água A variação de entalpia
Disciplina: Química Data: 05 / 05 / Ensino Médio Série: 2º ano Turma: Valor: Média: Assunto: ROTEIRO DE RECUPERAÇÃO Etapa: I Tipo:
 Disciplina: Química Data: 05 / 05 / 2018 Ensino Médio Série: 2º ano Turma: Valor: Média: Assunto: ROTEIRO DE RECUPERAÇÃO Etapa: I Tipo: Aluno(a): Nº: Nota: Professor(a): Thito Ass. do(a) Responsável: PROGRAMA
Disciplina: Química Data: 05 / 05 / 2018 Ensino Médio Série: 2º ano Turma: Valor: Média: Assunto: ROTEIRO DE RECUPERAÇÃO Etapa: I Tipo: Aluno(a): Nº: Nota: Professor(a): Thito Ass. do(a) Responsável: PROGRAMA
Química I. Módulo 9. Questões de Aplicação H 2 + 2H 2. O 1 mol 2 mol 0,010 mol z z = 0,020 mol de Na OH 25 ml de NaOH (aq) + 2NaOH Na 2
 Química I ódulo 9 1 Determinação separada do número de s de íons H + : a olaridade do ácido ------------------------- 2 / número de hidrogênios ionizáveis do ácido-----1 olume da solução ácida (litros)-------------------
Química I ódulo 9 1 Determinação separada do número de s de íons H + : a olaridade do ácido ------------------------- 2 / número de hidrogênios ionizáveis do ácido-----1 olume da solução ácida (litros)-------------------
Lista de Exercícios Lei de Hess, Cinética Química e Equilíbrio Químico Prof. Benfica
 Lista de Exercícios Lei de Hess, Cinética Química e Equilíbrio Químico Prof. Benfica 1) A entalpia da reação (I) não pode ser medida diretamente em um calorímetro porque a reação de carbono com excesso
Lista de Exercícios Lei de Hess, Cinética Química e Equilíbrio Químico Prof. Benfica 1) A entalpia da reação (I) não pode ser medida diretamente em um calorímetro porque a reação de carbono com excesso
07. Obras célebres da literatura brasileira foram ambientadas em regiões assinaladas neste mapa:
 6 FUVEST 09/0/202 Seu é Direito nas Melhores Faculdades 07. Obras célebres da literatura brasileira fora abientadas e regiões assinaladas neste apa: Co base nas indicações do apa e e seus conhecientos,
6 FUVEST 09/0/202 Seu é Direito nas Melhores Faculdades 07. Obras célebres da literatura brasileira fora abientadas e regiões assinaladas neste apa: Co base nas indicações do apa e e seus conhecientos,
QB70C:// Química (Turmas S71/S72) Ácidos e Bases. Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 11 Atkins (5ed.
 QB70C:// Química (Turmas S71/S72) Ácidos e Bases Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 11 Atkins (5ed.) Pai, o que é chuva ácida? NaO idróxido de magnésio Mg(O)
QB70C:// Química (Turmas S71/S72) Ácidos e Bases Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 11 Atkins (5ed.) Pai, o que é chuva ácida? NaO idróxido de magnésio Mg(O)
ROTEIRO DE ESTUDO III TRIMESTRE TERMOQUÍMICA. H = -70,09 kcal/mol
 ROTEIRO DE ESTUDO III TRIMESTRE Nome: Ano: 3º E.M. Professor: CASSIO PACHECO DISCIPLINA: QUÍMICA TERMOQUÍMICA 1- A oxidação de açúcares no corpo humano produz ao redor de 4,0 kcal por grama de açúcar oxidado.
ROTEIRO DE ESTUDO III TRIMESTRE Nome: Ano: 3º E.M. Professor: CASSIO PACHECO DISCIPLINA: QUÍMICA TERMOQUÍMICA 1- A oxidação de açúcares no corpo humano produz ao redor de 4,0 kcal por grama de açúcar oxidado.
USCS MEDICINA - Primeiro Semestre - Primeira Prova UNIVERSIDADE MUNICIPAL DE SÃO CAETANO DO SUL
 USCS 2018 - MEDICINA - Prieiro Seestre - Prieira Prova UNIERSIDADE MUNICIPAL DE SÃ CAETAN D SUL 01. U professor elaborou u jogo para trabalhar co a classificação periódica dos eleentos. Seus alunos deveria
USCS 2018 - MEDICINA - Prieiro Seestre - Prieira Prova UNIERSIDADE MUNICIPAL DE SÃ CAETAN D SUL 01. U professor elaborou u jogo para trabalhar co a classificação periódica dos eleentos. Seus alunos deveria
Aula 7 Entalpia e Lei de Hess
 Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula 7 Entalpia e Lei de Hess Dr. Tiago P. Camargo Entalpia Termodinâmica Num sistema de paredes rígidas V const.
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula 7 Entalpia e Lei de Hess Dr. Tiago P. Camargo Entalpia Termodinâmica Num sistema de paredes rígidas V const.
C (grafite) + 2 H 2(g) + ½ O 2(g) CH 3 OH (l) + 238,6 kj. CO 2(g) C (grafite) + O 2(g) 393,5 kj. H 2(g) + ½ O 2(g) H 2 O (l) + 285,8 kj
 Questão 1 (PUC SP) Num calorímetro de gelo, fizeram-se reagir 5,400 g de alumínio (Al) e 16,000 g de óxido férrico, Fe 2 O 3. O calorímetro continha, inicialmente, 8,000 Kg de gelo e 8,000 Kg de água.
Questão 1 (PUC SP) Num calorímetro de gelo, fizeram-se reagir 5,400 g de alumínio (Al) e 16,000 g de óxido férrico, Fe 2 O 3. O calorímetro continha, inicialmente, 8,000 Kg de gelo e 8,000 Kg de água.
Apostila de Química 02 Termoquímica
 Apostila de Química 02 Termoquímica 1.0 Introdução A Termoquímica tem como objetivo o estudo das variações de energia que acompanham as reações químicas; Não há reação química que ocorra sem variação de
Apostila de Química 02 Termoquímica 1.0 Introdução A Termoquímica tem como objetivo o estudo das variações de energia que acompanham as reações químicas; Não há reação química que ocorra sem variação de
Gabarito - Lista de Mol 2016
 Gabarito: Resposta da questão 1: [Resposta do ponto de vista da disciplina de Quíica] a) Tereos: Para n ols de butano: 1ol C4H10 n CH 4 10 58n g 58 g CH 4 10 Para n ols de propano: 1ol CH8 n CH 8 44n g
Gabarito: Resposta da questão 1: [Resposta do ponto de vista da disciplina de Quíica] a) Tereos: Para n ols de butano: 1ol C4H10 n CH 4 10 58n g 58 g CH 4 10 Para n ols de propano: 1ol CH8 n CH 8 44n g
Um dos grandes problemas mundiais é constante necessidade de geração de energia.
 Termoquímica 1 2 Introdução Um dos grandes problemas mundiais é constante necessidade de geração de energia. A Termoquímica possibilita uma solução viável (econômica e ecológica) para esta crescente demanda.
Termoquímica 1 2 Introdução Um dos grandes problemas mundiais é constante necessidade de geração de energia. A Termoquímica possibilita uma solução viável (econômica e ecológica) para esta crescente demanda.
Exercícios sobre análise quantitativa na eletrólise- Eletroquímica
 Exercícios sobre análise quantitativa na eletrólise- Eletroquíica 01. (UEL) Nas reações de eletrólise para a obtenção de etais, as assas dos produtos depositados no cátodo pode ser calculados pela aplicação
Exercícios sobre análise quantitativa na eletrólise- Eletroquíica 01. (UEL) Nas reações de eletrólise para a obtenção de etais, as assas dos produtos depositados no cátodo pode ser calculados pela aplicação
Equilíbrio Químico. Estágio da reação química em que não existe mais tendência a mudar a composição da mistura de uma reação
 Equilíbrio Químico 1 Equilíbrio Químico Estágio da reação química em que não existe mais tendência a mudar a composição da mistura de uma reação Equilíbrio dinâmico: as reações direta e inversa ocorrem
Equilíbrio Químico 1 Equilíbrio Químico Estágio da reação química em que não existe mais tendência a mudar a composição da mistura de uma reação Equilíbrio dinâmico: as reações direta e inversa ocorrem
Papel + O 2 CO 2 + H 2 O
 DEMOSTRAÇÃO EXPERIMENTO NH 4 Cl NH 4+ + Cl - Papel + O 2 CO 2 + H 2 O Quantidade de Material Energia liberado ou consumida Definições NH 4 Cl NH 4+ + Cl - Absorção de Calor = Processo Endotérmico Papel
DEMOSTRAÇÃO EXPERIMENTO NH 4 Cl NH 4+ + Cl - Papel + O 2 CO 2 + H 2 O Quantidade de Material Energia liberado ou consumida Definições NH 4 Cl NH 4+ + Cl - Absorção de Calor = Processo Endotérmico Papel
Equilíbrio Químico. Estágio da reação química em que não existe mais tendência a mudar a composição da mistura de uma reação
 Equilíbrio Químico 1 Equilíbrio Químico Estágio da reação química em que não existe mais tendência a mudar a composição da mistura de uma reação Equilíbrio dinâmico: as reações direta e inversa ocorrem
Equilíbrio Químico 1 Equilíbrio Químico Estágio da reação química em que não existe mais tendência a mudar a composição da mistura de uma reação Equilíbrio dinâmico: as reações direta e inversa ocorrem
Exercícios Ligação Iônica
 Exercícios Ligação Iônica Questão 1 Considere o composto hipotético CaF(s). internuclear de 2,67 x 10-10 m. b) Faça o ciclo de Born-Haber para o CaF indicando todas as etapas. c) Calcule a entalpia padrão
Exercícios Ligação Iônica Questão 1 Considere o composto hipotético CaF(s). internuclear de 2,67 x 10-10 m. b) Faça o ciclo de Born-Haber para o CaF indicando todas as etapas. c) Calcule a entalpia padrão
TERMOQUÍMICA. Maira Gazzi Manfro e Giseli Menegat
 TERMOQUÍMICA Maira Gazzi Manfro e Giseli Menegat maira.manfro@caxias.ifrs.edu.br giseli.menegat@caxias.ifrs.edu.br O QUE É? TERMOQUÍMICA: é a parte da físico-química que estuda o calor envolvido nas reações
TERMOQUÍMICA Maira Gazzi Manfro e Giseli Menegat maira.manfro@caxias.ifrs.edu.br giseli.menegat@caxias.ifrs.edu.br O QUE É? TERMOQUÍMICA: é a parte da físico-química que estuda o calor envolvido nas reações
Estado Físico Características Macroscópicas Características Microscópicas
 Sistemas materiais Estados de agregação Estado Físico Características Macroscópicas Características Microscópicas Sólido forma e volume constantes. partículas com arranjo característico; formam estruturas
Sistemas materiais Estados de agregação Estado Físico Características Macroscópicas Características Microscópicas Sólido forma e volume constantes. partículas com arranjo característico; formam estruturas
O estudo do fluxo de carga
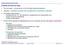 Análise de Sisteas de Potência (ASP) O estudo do fluxo de carga Fluxo de carga ferraenta de análise de redes (regie peranente) Utilização operação e tepo real e planejaento da operação e expansão nforações
Análise de Sisteas de Potência (ASP) O estudo do fluxo de carga Fluxo de carga ferraenta de análise de redes (regie peranente) Utilização operação e tepo real e planejaento da operação e expansão nforações
Lista de Exercício Para a Prova Trimestral Setor A. a) Quantas calorias, de acordo com a tabela nutricional, foram ingeridas?
 Professor: Cassio Pacheco Disciplina: Química II Trimestre 2ºAno Lista de Exercício Para a Prova Trimestral Setor A 1- Depois do cinema, um grupo de amigos foi comer aquele sandubão no Mc Donald s. O pedido
Professor: Cassio Pacheco Disciplina: Química II Trimestre 2ºAno Lista de Exercício Para a Prova Trimestral Setor A 1- Depois do cinema, um grupo de amigos foi comer aquele sandubão no Mc Donald s. O pedido
P2 - PROVA DE QUÍMICA GERAL - 12/05/12
 P2 - PROVA DE QUÍMICA GERAL - 12/05/12 Nome: GABARITO Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados: T (K) = T ( C) + 273,15 R = 8,314
P2 - PROVA DE QUÍMICA GERAL - 12/05/12 Nome: GABARITO Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados: T (K) = T ( C) + 273,15 R = 8,314
química química na abordagem do cotidiano
 Capítulo Lei de Hess e entalpias-padrão Respostas dos exercícios essenciais H C H 35 kj H total 60 kj B H 5 kj A H X H 3 0 kj Y H 4 40 kj H total 60 kj Z 3 H T H 6 30 kj U H 5 60 kj H total 30 kj S 5 a)
Capítulo Lei de Hess e entalpias-padrão Respostas dos exercícios essenciais H C H 35 kj H total 60 kj B H 5 kj A H X H 3 0 kj Y H 4 40 kj H total 60 kj Z 3 H T H 6 30 kj U H 5 60 kj H total 30 kj S 5 a)
Fotossíntese das plantas, o sol fornece energia
 Unidade 6 - Conteúdo 13 - Termoquímica As transformações físicas e as reações químicas quase sempre estão envolvidas em perda ou ganho de calor. O calor é uma das formas de energia mais comum que se conhece.
Unidade 6 - Conteúdo 13 - Termoquímica As transformações físicas e as reações químicas quase sempre estão envolvidas em perda ou ganho de calor. O calor é uma das formas de energia mais comum que se conhece.
- SOLUÇÃO = SOLUTO + SOLVENTE. COEFICIENTE DE SOLUBILIDADE ( Cs) Grandeza que depende da natureza do soluto e da temperatura.
 Soluções - MISTURA HOMOGÊNEA - SOLUÇÃO = SOLUTO + SOLVENTE menor quantidade maior quantidade COEFICIENTE DE SOLUBILIDADE ( Cs) Grandeza que depende da natureza do soluto e da temperatura. Cs = g de soluto
Soluções - MISTURA HOMOGÊNEA - SOLUÇÃO = SOLUTO + SOLVENTE menor quantidade maior quantidade COEFICIENTE DE SOLUBILIDADE ( Cs) Grandeza que depende da natureza do soluto e da temperatura. Cs = g de soluto
UNISANTA FACULDADE DE ENGENHARIA QUÍMICA 1/5 DISCIPLINA TERMODINÂMICA QUÍMICA I 1 O Semestre de 2002 PROVA P1
 UNISANTA FACULDADE DE ENGENHARIA QUÍMICA /5 DISCIPLINA TERMODINÂMICA QUÍMICA I O Seestre de 00 PROVA P Atenção:. Consultar apenas o caderno de Tabelas, Diagraas e Fórulas fornecido juntaente co a prova,
UNISANTA FACULDADE DE ENGENHARIA QUÍMICA /5 DISCIPLINA TERMODINÂMICA QUÍMICA I O Seestre de 00 PROVA P Atenção:. Consultar apenas o caderno de Tabelas, Diagraas e Fórulas fornecido juntaente co a prova,
Conteúdo 28/03/2017. Equações Químicas e Estequiometria, Balanceamento de Equações Químicas, Relação de Massa em Equações Químicas,
 Química Geral I Química - Licenciatura Prof. Udo Eckard Sinks Conteúdo 28/03/2017 Equações Químicas e Estequiometria, Balanceamento de Equações Químicas, Relação de Massa em Equações Químicas, Química
Química Geral I Química - Licenciatura Prof. Udo Eckard Sinks Conteúdo 28/03/2017 Equações Químicas e Estequiometria, Balanceamento de Equações Químicas, Relação de Massa em Equações Químicas, Química
Um dos componentes do GLP (gás liquefeito do petróleo) é o propano (C3H8). A sua combustão pode ser representada pela seguinte equação química:
 Atividade extra Exercício 1 Cecierj 2013 Um dos componentes do GLP (gás liquefeito do petróleo) é o propano (C3H8). A sua combustão pode ser representada pela seguinte equação química: C3H8(ℓ) + 5 O2 6
Atividade extra Exercício 1 Cecierj 2013 Um dos componentes do GLP (gás liquefeito do petróleo) é o propano (C3H8). A sua combustão pode ser representada pela seguinte equação química: C3H8(ℓ) + 5 O2 6
FÍSICO-QUÍMICA Prof. Jackson Alves
 FÍSICO-QUÍMICA Prof. Jackson Alves TERMOQUÍMICA Parte II Entalpia e H Processos exotérmicos e endotérmicos Equações Alotropia Entalpia (H) e Variação de entalpia ( H) Entalpia: É a energia total em um
FÍSICO-QUÍMICA Prof. Jackson Alves TERMOQUÍMICA Parte II Entalpia e H Processos exotérmicos e endotérmicos Equações Alotropia Entalpia (H) e Variação de entalpia ( H) Entalpia: É a energia total em um
PROVA MODELO 1 PROPOSTA DE RESOLUÇÃO
 PROVA MODELO PROPOSTA DE RESOLUÇÃO GRUPO I. A frase do texto que traduz u facto e que Aristóteles e Galileu era concordantes será Tal coo Aristóteles, descobriu ser uito difícil edir diretaente as trajetórias
PROVA MODELO PROPOSTA DE RESOLUÇÃO GRUPO I. A frase do texto que traduz u facto e que Aristóteles e Galileu era concordantes será Tal coo Aristóteles, descobriu ser uito difícil edir diretaente as trajetórias
