UNIVERSIDADE FEDERAL DA BAHIA DOUTORADO EM CIÊNCIA ANIMAL NOS TRÓPICOS
|
|
|
- Maria Júlia Sampaio Azenha
- 6 Há anos
- Visualizações:
Transcrição
1 UNIVERSIDADE FEDERAL DA BAHIA DOUTORADO EM CIÊNCIA ANIMAL NOS TRÓPICOS INFECÇÃO DE OVINOS POR LENTIVÍRUS CAPRINO: TRANSMISSÃO, DIAGNÓSTICO E AVALIAÇÃO CLÍNICA CARLA CAROLINE VALENÇA DE LIMA SALVADOR - BAHIA AGOSTO
2 ii CARLA CAROLINE VALENÇA DE LIMA INFECÇÃO DE OVINOS POR LENTIVÍRUS CAPRINO: TRANSMISSÃO, DIAGNÓSTICO E AVALIAÇÃO CLÍNICA Tese apresentada ao Programa de Doutorado em Ciência Animal nos Trópicos da Universidade Federal da Bahia, como requisito parcial para obtenção do título de Doutor em Ciência Animal nos Trópicos. Área de Concentração: Saúde Animal Orientador: Profa. Dra. Maria Consuêlo Caribé Ayres Coorientador: Prof. Dr. Raymundo Rizaldo Pinheiro Prof. Dr. Joselito Nunes Costa SALVADOR - BAHIA AGOSTO
3 Sistema de Bibliotecas da UFBA L732 Lima, Carla Caroline Valença de. Infecção de ovinos por lentivírus caprino: transmissão, diagnóstico e avaliação clínica / Carla Caroline Valença de Lima f.: il. Orientadora: Profª. Drª. Maria Consuêlo Caribé Ayres Co-orientador(es):Prof. Dr. Raymundo Rizaldo Pinheiro Prof. Dr. Joselito Nunes Costa Tese (doutorado em Ciência Animal nos Trópicos) - Universidade Federal da Bahia, Escola de Medicina Veterinária e Zootecnia, Salvador, Ovino Doenças Estudo de caso. 2. Caprino Doenças Estudo de caso. 3. Virologia veterinária - Avaliação. 4. Diagnóstico de laboratório I. Ayres, Maria Consuêlo Caribé. II. Pinheiro, Raymundo Rizaldo. III. Costa, Joselito Nunes. IV. Universidade Federal da Bahia. Escola de Medicina Veterinária e Zootecnia. V. Título. CDD CDU - 578:636.3
4 iii CARLA CAROLINE VALENÇA DE LIMA INFECÇÃO DE OVINOS POR LENTIVÍRUS CAPRINO: TRANSMISSÃO, DIAGNÓSTICO E AVALIAÇÃO CLÍNICA Tese defendida e aprovada pela Comissão Examinadora em 11 de agosto de Comissão Examinadora: Profa. Dra. Maria Consuêlo Caribé Ayres (UFBA) Presidente da Banca Prof. Dra. Lilian Gregory (USP) Prof. Dr. Raymundo Rizaldo Pinheiro (Embrapa Caprinos e Ovinos) Prof. Dra Lia Muniz Barreto Fernandes (UFBA) Prof. Dr. José Eugênio Guimarães (UFBA) SALVADOR - BAHIA AGOSTO
5 iv Uma das coisas mais lindas dos humanos não é a capacidade de lutar, de estar forte sempre, de resistir, de ser fortaleza ambulante. Não é aí que mora nossa força. Nossa beleza está em nossa relatividade, na fraqueza que amanhã se transcende, no choro que, sim, pode acontecer e, quando passa, lava a alma, na dor que nos deixa mais fortes, na capacidade de reconhecer sem medo, sem culpa, sem remorso, nossa humanidade, e então transcendermos. Sejamos humanos! Só não perca a esperança. Todos tem direito a dias ruins, é normal sentir que as forças acabam. Mas ela volta, melhor, depurada, enraizada. Só não perca a esperança! Ainda há muitas coisas boas no seu caminho... Portanto caminhemos. Flavio Siqueira Mensagens que chegam pela manhã Este trabalho é dedicado a todos que sabem fazer parte desta luta, que tomaram pra si as minhas dores e alegrias!
6 v AGRADECIMENTOS Ao Universo, que dentro das infinitas possibilidades sempre me conduziu a momentos de aprendizado e amor. Aos queridos companheiros de jornada, minha Grande Família, com os quais tenho o imenso prazer de conviver e aprender. Grandes jornadas certamente não são atribuídas aos grandes homens, mas a quem possui grandes companheiros, então deixo meu muito obrigada, vocês são fundamentais! Ao meu companheiro, meu eleito, homem nobre e justo, que me ensina diariamente a gratidão de ser amor! A grande equipe envolvida neste trabalho, orientadores, pesquisadores, professores, técnicos, pós-graduandos, bolsistas, estagiários, tratadores, funcionários. Este trabalho não seria o mesmo sem vocês! Deixo aqui a minha imensa gratidão e admiração por todos vocês! Aos amigos que me receberam nos diferentes locais de execução desta tese, e principalmente, nos seus corações! Foram muitas as dificuldades, mas vocês sempre me lembraram das alegrias! Às instituições executoras: Universidade Federal da Bahia (UFBA), Universidade Federal do Recôncavo da Bahia (UFRB), Embrapa Caprinos e Ovinos e Universidade Estadual do Vale do Acaraú (UVA). Ao Programa de Pós-Graduação em Ciência Animal nos Trópicos da UFBA. Às instituições de fomento à pesquisa: Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (Capes), Fundação de Amparo à Pesquisa do Estado da Bahia (Fapesb) e Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq).
7 vi Infecção de ovinos por lentivírus caprino: transmissão, diagnóstico e avaliação clínica f. Tese (Doutorado em Ciência Animal nos Trópicos). Escola de Medicina Veterinária e Zootecnia, Universidade Federal da Bahia, Salvador, 2015 RESUMO As lentiviroses dos pequenos ruminantes são enfermidades causadas por retrovírus do gênero Lentivírus. Este gênero de vírus possui um ciclo de replicação lento, e sua infecção pode ser assintomática por um longo período. Por estas características, os animais infectados apresentam manifestação clínica lenta e progressiva, de quatro principais formas: neurológica (mais frequente em animais jovens), respiratória (mais comum em ovinos), artrítica (mais presente em caprinos) e mamária, sendo chamada de artriteencefalite caprina quando acomete caprinos, e maedi-visna ou pneumonia progressiva ovina, quando em ovinos. Além disso, animais infectados muitas vezes apresentam emagrecimento progressivo, também descrito em outras lentiviroses, como a imunodeficiência felina e a anemia infecciosa equina, entretanto este mecanismo ainda foi pouco elucidado. Apesar de diversos estudos serem conduzidos com estas enfermidades, historicamente estes agentes virais eram considerados espécie-específicos, denominando o agente em ovinos como maedi-visna vírus (MVV), e em caprinos como vírus da artrite-encefalite caprina (CAEV). Entretanto, estudos filogenéticos têm demonstrado a heterogeneidade desses patógenos, e os mesmos têm sido reunidos em subtipos a partir da diferença genotípica apresentada, sendo chamados de Lentivírus de Pequenos Ruminantes (LVPR). Todavia, ainda não foi esclarecida a forma de retransmissão deste vírus entre espécies. Assim, uma vez infectando cordeiros com colostro e leite de cabras infectadas, buscou-se avaliar se estes ovinos transmitiriam o lentivírus de origem caprina (LVC) para outros ovinos. Para tal, foram realizados dois experimentos: o primeiro onde se buscou a detecção do DNA pró-viral no leite de matrizes e sêmen de carneiros; e o segundo onde se avaliou a retransmissão do LVC de ovelhas para as suas crias. No primeiro, estabeleceram-se dois grupos experimentais, um composto por 10 ovelhas, das quais foram obtidas 50 amostras de leite, e outro composto por quatro carneiros, dos quais foram obtidas 32 amostras de sêmen; todas as amostras foram testadas pela técnica de PCR nested (npcr) para a detecção de DNA pró-viral de LVC. Foram detectados DNA pró-viral de LVC em oito (16%) amostras de leite, oriundas de duas (20%) ovelhas, e em uma (3,12%) amostra de sêmen. Os produtos da amplificação foram sequenciados, confirmando-se tratar de sequência genômica do LVC. No segundo, formaram-se dois grupos experimentais: o grupo exposto (GE) foi constituído por 10 cordeiros, mantidas com suas mães, que foram infectadas experimentalmente com lentivírus caprino, positivas na npcr; e o grupo não exposto (GN), caracterizando o grupo controle, formado por cinco cordeiros, mantidos com suas matrizes, negativas para LVC. Colheram-se amostras de sangue mensalmente, do nascimento a um ano de vida, totalizando 13 amostras por animal. O GE apresentou positividade em três indivíduos, sendo dois na npcr e um nos testes imunológicos. As amostras positivas no npcr foram purificadas e sequenciadas, comprovando tratar-se de lentivírus com semelhança a cepa CAEV Cork. Desta forma, comprovou-se a transmissibilidade do lentivírus caprino entre ovinos. Além disso, um terceiro experimento foi realizado, buscando-se avaliar o comprometimento clínico dos ovinos infectados com LVC. Estabeleceram-se dois grupos experimentais: ovelhas infectadas com LVC a partir da mamada de colostro caprino (GI), e ovelhas negativas para LVC,
8 vii denominado grupo controle (GC). Os animais foram avaliados para a manifestação clínica da lentivirose, além de amostras de soro sanguíneo serem submetidas às dosagens de proteínas totais (PST), albumina (ALB), globulina (GLOB), ureia, creatinina (CREA), glicose (GLIC), triglicérides (TRIG), colesterol (COLES), aspartato aminitransferase (AST) e ɤ-glutamiltrasnferase (GGT), em 22 diferentes momentos, do nascimento aos 720 dias de vida. Os resultados demonstraram ausência de manifestação física da enfermidade, e alteração em alguns metabolitos proteicos (PST e GLOB) e diminuição da atividade da enzima GGT no primeiro ano de vida. Portanto, os ovinos retransmitem o LVC, entretanto sem comprometimento clínico da enfermidade. Palavras-chave: lentivírus de pequenos ruminantes, sêmen, leite, metabolismo, DNA proviral.
9 viii LIMA, C.C.V. Sheep infected with goat lentivirus: transmission, diagnosis and clinical evaluation f. Thesis (PhD., Animal Science in the Tropics) - School of Veterinary Medicine and Zootechny, Federal University of Bahia, Salvador, ABSTRACT The lentiviruses in small ruminants are diseases caused by retrovirus of the genus Lentivirus; This virus genus has a slow replication cycle, and its infection may be asymptomatic for a long period. For these characteristics, the infected animals have slow and progressive clinical manifestation, four main ways: neurological (more common in young animals), respiratory (more common in sheep), arthritic (more present in goats) and breast, being called arthritis -encefalite goats when it affects goats, and maedi-visna or ovine progressive pneumonia, when in sheep. Furthermore, animals infected often exhibit progressive weight loss, also described in other lentiviruses, such as feline immunodeficiency virus and equine infectious anemia virus, however this mechanism has been poorly elucidated. Despite several studies being conducted with these disorders, historically these viral agents were considered species-specific, naming the agent in sheep as maedi-visna virus (MVV), and goats as virus, caprine arthritis encephalitis (CAEV). However, phylogenetic studies have demonstrated the heterogeneity of these pathogens, and they have been gathered into subtypes from the genotypic difference presented, being called Small ruminants lentivirus (SRLV). Yet it remains unclear how to relay this virus between species. So, once infecting lambs with colostrum and milk of infected goats, we sought to evaluate whether these sheep convey the goats origin lentivirus (LVC). For this purpose two experiments were conducted: the first where we tried the detection of proviral DNA in milk matrices and semen of rams; and the second for assessment of retransmission of sheep LVC for their young. At first, set up two groups, one composed of 10 sheep were obtained of which 50 samples of milk, and the other consists of four sheep, which were obtained 32 sample of semen; All samples were tested by the technique of nested PCR (npcr) for the detection of proviral DNA LVC. Proviral DNA LVC were detected in eight (16%) samples of milk obtained from two (20%) sheep, and only one (3.12%) semen sample. The amplification products were sequenced, confirming the case of genomic sequence of the LVC. In the second, they were formed two groups consisting of 15 lambs divided into two groups: the treatment group (GE) consisted of 10 lambs kept with their mothers, who were experimentally infected with lentivirus goats, positive in the npcr; and the unexposed group (GN), featuring the control group, consisting of five lambs kept with their mothers, negative for LVC. Samples were taken monthly blood from birth to one year of life, totaling 13 samples per animal. The GE was positive in three individuals, two of the npcr and in immunological tests. Positive samples in npcr were purified and sequenced, proving that this is the similarity with lentiviruses CAEV Cork strain. Thus, it proved to transmissibility the lentivirus sheep from goats. In addition, a third experiment was carried out, seeking to evaluate the clinical signs of sheep infected with LVC. Set up two experimental groups: infected sheep with LVC from the feeding of colostrum goat (GI), and negative sheep to LVC, called control group (GC). The animals were assessed for clinical manifestation of lentiviruses, and serum samples were subjected to of total protein (PST), albumin (ALB), globulin (GLOB), urea, creatinine (CREA), glucose (GLIC), triglycerides (TRIG), cholesterol (COLES), aspartate aminitransferase (AST) and ɤ-glutamiltrasnferase (GGT) in 22 different times, from birth to 720 days of life. The results demonstrated no physical manifestation of the disease, and
10 ix changes in some protein metabolites (PST and GLOB) and activity of the enzyme GGT in the first year of life. So the sheep relay LVC, however without clinical signs of the disease. Keywords: Small ruminant lentiviruses, milk, semen, biochemistry, DNA proviral.
11 x LISTA DE TABELAS FUNDAMENTAÇÃO TEÓRICA Página Tabela 1 - Classificação taxonômica dos lentivírus de pequenos ruminantes apresentando novos subtipos propostos em estudos filogenéticos posteriores ao publicado por Shah et al. (2004a). 22 Tabela 2 - Doenças causadas por Lentivírus. 23 Tabela 1 - CAPÍTULO 1 Resultados de PCR nested em amostras de leite de ovelhas experimentalmente infectadas com lentivírus caprino, colhidas dos 30 aos 120 dias de lactação. Página 37 Tabela 2 - Resultados de PCR nested em amostras de sêmen de carneiros experimentalmente infectadas com lentivírus caprino, colhidas de abril de 2013 a abril de CAPÍTULO 2 Página Tabela 1 - Resultados dos testes de PCR nested no sangue, Immunoblotting, ELISA e Imunodifusão em gel de agarose no soro de crias ovinas expostas e não expostas a lentivirose de origem caprina. CAPITULO Página Tabela 1 - Resultados dos testes immunoblotting (IB) e PCR nested (npcr) de cordeiros infectados pelo lentivírus caprino, a partir da ingestão de colostro de cabras positivas, realizados do nascimentos aos 720 dias de idade. 72
12 xi LISTA DE FIGURAS Figura 1 - Figura 2 - Figura 3 - Figura 4 - Figura 5 - FUNDAMENTAÇÃO TEÓRICA Soropositividade para lentivírus em caprinos de diferentes regiões no Brasil. Soropositividade para lentivírus em ovinos de diferentes regiões do Brasil. Organização genômica do vírus da artrite-encefalite caprina (OLSEN, 2001). Estrutura do Lentivírus de Pequenos Ruminantes (LVPR) (SOUZA, 2008 modificado). Manifestação clínica da lentivirose de pequenos ruminantes em caprinos. Página Figura 1 - CAPÍTULO 1 Sequências parciais do gene gag de lentivírus de pequenos ruminantes: resultados obtidos da PCR nested em leite de ovelhas e sêmen de carneiros infectados com lentivirus caprino. Página 40 Figura 1 - CAPÍTULO 2 Sequências parciais do gene gag de lentivírus de pequenos ruminantes: resultados obtidos da PCR nested em ovinos infectados com lentivirus caprino. Página 57 Figura 1 - CAPÍTULO 3 Média dos valores obtidos nas dosagens séricas de proteína sérica total PST, albumina ALB e globulina GLOB, em cordeiros infectados com lentivírus caprino (GI) e cordeiros do grupo controle (GC), do nascimento aos 720 dias de vida. Página 74
13 xii Figura 2 - Figura 3 - Média dos valores obtidos nas dosagens séricas de ureia em cordeiros infectados com lentivírus caprino (GI) e cordeiros do grupo controle (GC), do nascimento aos 720 dias de vida. Média dos valores obtidos nas dosagens séricas de creatinina em cordeiros infectados com lentivírus caprino (GI) e cordeiros do grupo controle (GC), do nascimento aos 720 dias de vida. Página Figura 4 - Média dos valores obtidos nas dosagens séricas de glicose Glic, triglicérides Trig e colesterol Coles, em cordeiros infectados com lentivírus caprino (GI) e cordeiros do grupo controle (GC), do nascimento aos 720 dias de vida. 76 Figura 5 - Média dos valores obtidos nas dosagens séricas da atividade das enzimas aspartato amino-transferase (AST) e gamaglutamiltransferase (GGT), em cordeiros infectados com lentivírus caprino (GI) e cordeiros do grupo controle (GC), do nascimento aos 720 dias de vida. 77
14 xiii LISTA DE SIGLAS AIEV Vírus da anemia infecciosa equina ALB Albumina BA Bahia BIV Vírus da imunodeficiência bovina (do inglês bovine immunodeficiency virus) CA Capsídeo CAE Artrite-encefalite caprina (do inglês caprine arthritis encephalitis) CAEV Vírus da artrite-encefalite caprina (do inglês caprine arthritis encephalitis virus) Capes Coordenação de Aperfeiçoamento de Pessoal de Nível Superior CE Ceará CNPq Conselho Nacional de Desenvolvimento Científico e Tecnológico dl Decilitro DNA Ácido desoxirribonucleico (do inglês deoxyribonucleic acid) EDTA Ácido etilenodiaminotetracético (do inglês ethylenediaminetetraacetic acid) ELISA Ensaio imunoadsorvente ligado à enzima Embrapa Empresa Brasileira de Pesquisa Agropecuária ENV Envelope EUA Estados Unidos da América Fapesb Fundação de Amparo à Pesquisa do Estado da Bahia FIV Vírus da imunodeficiência felina (do inglês feline immunodeficiency virus) G Grama G Força gravitacional GE Grupo exposto GN Grupo não exposto G1 Grupo 1 G2 Grupo 2 GLOB Globulinas GO Goiás Gp Glicoproteína HIV Vírus da imunodeficiência humana (do inglês human immunodeficiency virus) IB Immunoblotting IBGE Instituto Brasileiro de Geografia e Estatística IDGA Imunodifusão em gel de agarose IFI Imunofluorescência indireta IgG Imunoglobulina G Kb Kilobase kda Kilodaltons LTR Long terminal repeats LVPR Lentivírus de pequenos ruminantes MA Matriz
15 xiv MA MG ml mm MV MVV NC npcr OIE PA PB pb PBS PCR PE PI PP PPO PST RJ RN RNA rpm RS SC SDS SIV Maranhão Minas Gerais Mililitro Milímetro Maedi-visna Vírus da Maedi-Visna Nucleocapsídeo Reação de polimerase em cadeia nested (do inglês nested polynerase chain reaction) Organização Mundial de Saúde Animal Pará Paraíba Pares de base Solução salina fosfatada (do inglês polymerase chain reaction) Reação em cadeia da polimerase Pernambuco Piauí Percentual de positividade Pneumonia progressiva ovina Proteína sérica total Rio de Janeiro Rio Grande do Norte Ácido ribonucleico (do inglês ribonucleic acid) Rotações por minuto Rio Grande do Sul Santa Catarina Dodecil sulfato de sódio (do inglês sodium dodecyl sulfate) Vírus da imunodeficiência símia (do inglês simian immunodeficiency virus) Eletroforese em gel de poliacrilamida Sergipe São Paulo Superfície Tocantins Unidades PAGE SE SP SU TO U ºC Graus Celsius µl Microlitro
16 xv SUMÁRIO Infecção de ovinos por lentivirus caprino: transmissão, diagnóstico e avaliação clínica INTRODUÇÃO GERAL... Págin a 17 FUNDAMENTAÇÃO 19 TEÓRICA Considerações históricas, ocorrência e transmissão interespécie dos lentivírus de pequenos 19 ruminantes Etiologia e patogenia dos lentivírus de pequenos ruminantes Transmissão dos lentivírus de pequenos 25 ruminantes Achados clínicos da artrite-encefalite caprina e da maedi-visna Diagnóstico e medidas de controle para as lentiviroses de pequenos ruminantes OBJETIVOS HIPÓTESE CIENTÍFICA CAPÍTULO 1 Lentivírus caprino em leite e sêmen de ovinos Págin a
17 xvi RESUMO ABSTRACT INTRODUÇÃO MATERIAL E MÉTODOS... RESULTADOS E DISCUSSÃO... CONCLUSÕES AGRADECIMENTOS REFERÊNCIAS CAPÍTULO 2 Transmissão do lentivírus caprino entre ovinos RESUMO ABSTRACT INTRODUÇÃO MATERIAL E MÉTODOS... RESULTADOS E DISCUSSÃO... Págin a
18 xvii CONCLUSÕES AGRADECIMENTOS REFERÊNCIAS CAPÍTULO 3 Avaliação clínica de ovinos infectados com o lentivírus caprino RESUMO ABSTRACT INTRODUÇÃO MATERIAL E MÉTODOS... RESULTADOS E DISCUSSÃO... CONCLUSÕES AGRADECIMENTOS REFERÊNCIAS CONSIDERAÇÕES FINAIS E IMPLICAÇÕES... Págin a REFERÊNCIAS
19 17 INTRODUÇÃO GERAL Os lentivírus são um gênero de agentes infecciosos de destaque na saúde dos animais e do homem. Abrange um vasto número de agentes responsáveis por doenças severas, como: imunodeficiências humana, símia, bovina e felina, anemia infecciosa equina, artrite-encefalite caprina (CAE) e maedi-visna (MV) ou pneumonia progressiva ovina (PPO) (LEROUX; MORNEX, 2008). Entretanto, mesmo sendo um gênero tão importante com diversos estudos na área, pouco se conhece sobre a sua patogenia, dificultando o desenvolvimento dos programas de prevenção, controle e erradicação destas enfermidades. Em se tratando dos lentivirus de pequenos ruminantes (LVPR), ou seja, do vírus da artrite encefalite caprina (CAEV) e do maedi-visna vírus (MVV), os desafios são ainda maiores, uma vez que, estes agentes não são espécie-específicos como os demais vírus desse gênero, o que implica em novas abordagens de medidas de controle (BLACKLAWS, 2012). Estudos comprovam a presença dos LVPR em vários países dos cinco continentes, realçando ainda mais o impacto econômico desta enfermidade (OIE, 2014). Em relação ao Brasil, a comprovação da presença dos LVPR em grande parte dos estados (MOOJEN et al., 1986; RAMOS et al., 1996; SARAIVA NETO et al., 1995; PINHEIRO et al., 2001; SANTIN et al., 2002; LILEMBAUN et al., 2007; SOBRINHO et al., 2008; LARA et al., 2009; SOBRINHO et al., 2010; LIMA et al., 2013a), causa preocupação quanto ao status sanitário dos rebanhos de caprinos e ovinos. Ressaltando a importância social que a atividade pecuária representa para o país, principalmente para a agricultura familiar desenvolvida na região Nordeste, com a maioria das criações voltadas ainda para subsistência, em ambientes áridos e semiáridos, onde cultivos e explorações tradicionalmente realizados em outros locais pouco se adaptam, a caprinovinocultura é responsável pela manutenção da pecuária local (SOUZA, 2004; LIMA et al., 2013a). Portanto, estudos que esclareçam os mecanismos intrínsecos à replicação, à latência viral, ao diagnóstico e à possibilidade de eliminação do vírus são necessários, a fim de se embasar medidas de prevenção, diagnóstico, controle e erradicação. Assim, este estudo buscou elucidar aspectos pertinentes à transmissão interespécies dos LVPR,
20 18 principalmente porque grande parte do rebanho de pequenos ruminantes são criados juntos, por produtores que muitas vezes negligenciam o cuidados com a enfermidade.
21 19 FUNDAMENTAÇÃO TEÓRICA 1. Considerações históricas, ocorrência e transmissão interespécie dos lentivírus de pequenos ruminantes As primeiras descrições de lentiviroses de pequenos ruminantes foram realizadas na África do Sul, em 1915; e nos Estados Unidos, em 1923, onde os ovinos apresentavam pneumonia intersticial crônica (BRODIE et al., 1998; PASICK, 1998). Em 1933, na Islândia, foram isolados casos de ovinos nativos apresentando distúrbios respiratórios e neurológicos, respectivamente Maedi e Visna, após a importação de animais infectados, da raça Karakul, oriundos da Alemanha, com o intuito de melhorar geneticamente o rebanho islandês (STRAUB, 2004). Entretanto, apenas em 1954 as duas enfermidades foram relacionadas como causadas por um único agente, denominada por Bjorn Sigurdsson como um lentivírus (CLEMENTS; ZINK, 1996; MOOJEN, 2001). Por se tratar de um mesmo agente, este foi denominado de maedi-visna vírus (MVV) (THORMAR; HELGADOTTIR, 1965). O CAEV foi observado em 1974, nos Estados Unidos, quando descrita uma leucoencefalomielite infecciosa, de possível etiologia viral, cujo sinal clínico era uma paralisia, em animais entre um e quatro meses de idade (CORK et al., 1974; CRAWFORD et al., 1980; CALLADO et al., 2001). Por ser também agente causal de alterações articulares em caprinos adultos, a doença foi denominada síndrome artrite-encefalite caprina (CAE), e em 1980 foi reconhecida como uma lentivirose (CRAWFORD; ADAMS, 1981). A partir das tentativas de melhoramento dos caprinos leiteiros, o vírus se disseminou, e além da sua presença em alguns países europeus, atingiu rebanhos no Canadá, na França, na Noruega, na Suíça e nos EUA, chegando estes países a apresentarem taxas de soropositividade entre 65 e 81% (DAWSON, 1987a). No Brasil, o primeiro relato da presença da infecção por este Lentivírus foi realizado por Moojen et al. (1986), no Rio Grande do Sul (RS), seguido de Fitterman (1988), no estado da Bahia (BA). Entretanto, estudos realizados com amostras colhidas no início da década de 80 foram identificados animais soropositivos no Rio de Janeiro (CUNHA; NASCIMENTO, 1995). Todavia, o primeiro isolamento viral no país ocorreu apenas em
22 , no RS (HÖTZEL et al., 1993), seguido de Moojen et al. (1996), ainda no RS, e apenas em 2006 foi realizado o primeiro isolamento na Bahia (TIGRE et al., 2006). A ocorrência da LVPR é observada principalmente nos rebanhos leiteiros formados pelo resultado da importação de raças, como a Anglonubiana, Saanen, Parda Alpina, Toggenburg e seus cruzamentos (FRANKE, 1998). No Brasil vários relatos indicam que os LVPR estão presentes em vários estados, como pode ser observado nas Figuras 1 (ocorrência em caprinos) e Figura 2 (ocorrência em ovinos), e dentre os estudos realizados se destacam com maior positividade os planteis de elevado padrão genético (BATISTA et al., 2004). Segundo Lilembaun et al. (2007) a doença permanece não diagnosticada em várias regiões dos países em desenvolvimento, especialmente em regiões tropicais. Figura 1 - Soropositividade para lentivírus em caprinos de diferentes regiões no Brasil. Fonte: Lima et al. (2013a). Figura 2 Soropositividade para lentivírus em ovinos de diferentes regiões do Brasil.
23 21 Fonte: SOUZA (2014) Por muitos anos agentes infecciosos isolados de ovinos foram denominados de maedi-visna vírus, enquanto que em caprinos como vírus da artrite-encefalite caprina. Entretanto, análises genômicas desses lentivírus sugerem que tenham evoluído de um genótipo ancestral comum, além de ter sido evidenciada a capacidade de cruzar barreiras interespécies e de adaptação a novos hospedeiros (LEROUX et al., 1995; ZANONI, 1998; CASTRO et al., 1999; SHAH et al., 2004a; GERMAIN; VALAS, 2006; GJERSET et al., 2007; PISONI et al., 2007; GIAMMARIOLI et al., 2011). Portanto seriam um grupo heterogêneo de agentes virológicos com abrangência de hospedeiros variável e diferentes capacidades patogênicas, passando a serem denominados lentivirus de pequenos ruminantes (LVPR), assim tratados como quasispécies virais únicas com a capacidade de infectar tanto ovinos quanto caprinos, indicando, assim a transmissão entre espécies (PASICK, 1998; BLACKLAWS et al., 2004; PISONI et al., 2005; GJERSET et al., 2007; GJERSET et al., 2009). Desta forma, surgiu uma nova classificação iniciada por Shah et al. (2004a), baseando-se nas sequências dos genes gag e pol, sugerindo quatro grupos ou genótipos
24 22 virais (A, B, C e D), com seus respectivos subtipos. Nesta classificação as sequências relacionadas ao MVV são atribuídas ao grupo A e as cepas relacionadas ao CAEV ao grupo B, e as cepas divergentes de ambos, classificadas entre os grupos C e D. Outros grupos e subtipos foram estabelecidos, a partir das novas sequências isoladas, como pode ser verificado na Tabela 1 (SOUZA et al., 2012). Tabela 1 - Classificação taxonômica dos lentivírus de pequenos ruminantes apresentando novos subtipos propostos em estudos filogenéticos posteriores ao publicado por Shah et al. (2004a). Grupos Subtipos Espécies Referências A1 Caprinos e ovinos Shah et al. (2004a) e Grego et al. (2007) A2 Caprinos e ovinos Shah et al. (2004a) A3 Caprinos e ovinos Shah et al. (2004a) A4 Caprinos e ovinos Shah et al. (2004a) A5 Caprinos Shah et al. (2004a) A6 Caprinos e ovinos Shah et al. (2004a) A A7 Caprinos Shah et al. (2004a) A8 Caprinos Grego et al. (2007) A9 Caprinos e ovinos Grego et al. (2007) A10 Caprinos e ovinos Pisoni et al. (2010) A11 Caprinos e ovinos Giammarioli et al. (2011) A12 Caprinos e ovinos Olech et al. (2012) A13 Caprinos e ovinos Olech et al. (2012) B1 Caprinos e ovinos Shah et al. (2004a) e Pisoni et al. (2005) B B2 Caprinos e ovinos Shah et al. (2004a) B3 Caprinos e ovinos Bertolotti et al. (2011) e Giammarioli et al. (2011) C - Caprinos e ovinos Shah et al. (2004a) e Gjerset et al. (2007) D - Caprinos Shah et al. (2004a) E E1 Caprinos Grego et al. (2007) e Reina et al. (2010) E2 Caprinos Grego et al. (2007) e Reina et al. (2010) Fonte: SOUZA et al. (2012) adaptado 2. Etiologia, patogenia e imunologia dos lentivírus de pequenos ruminantes Os LVPR pertencem à família Retroviridae, gênero Lentivirus, fazendo parte, portanto do grupo de retrovírus não oncogênicos (STRAUB, 2004; QUINN et al., 2005). A este mesmo gênero pertencem outros vírus de importância veterinária e humana, como os vírus da anemia infecciosa equina, o maedi-visna dos ovinos e das imunodeficiências felina (FIV), bovina (BIV), símia (SIV) e humana (HIV) (TAVARES; PEREIRA, 1999; LARA et al., 2003), como pode ser observado na Tabela 2.
25 23 Tabela 2. Doenças causadas por Lentivírus Nome do Vírus Abreviatura Hospedeiro Tropismo Vírus da anemia infecciosa equina AIEV Equinos Macrófagos Vírus da maedi-visna MVV Ovinos Macrófagos Vírus da artrite-encefalite caprina CAEV Caprinos Macrófagos Vírus da imunodeficiência felina FIV Felinos T-CD4+ / Macrófagos Vírus da imunodeficiência bovina BIV Bovinos T-CD4+ / Macrófagos Vírus da imunodeficiência símia SIV Primatas T-CD4+ / Macrófagos Vírus da imunodeficiência humana HIV 1 / 2 Humanos T-CD4+/ Macrófagos Fonte: Tavares; Pereira (1999). A família Retroviridae é composta por vírions de tamanho aproximado entre 80 e 100 nm, com simetria de capsídeo icosaédrica, envelopado e com genoma do tipo RNA linear, diplóide, de fita simples e sentido positivo. Os três principais genes contidos no genoma são gag, pol e env. O gene gag (antígeno grupo-específico) codifica proteínas estruturais internas. O gene pol (polimerase) codifica as enzimas transcriptase reversa e integrase. O gene env (envelope) codifica glicoproteínas-transmembrana e de superfície do envelope. Há também os genes que regulam a expressão do genoma viral (tat, rev e vif) (Figura 3). O vírus (Figura 4) ainda apresenta no seu envelope uma glicoproteína importante, a gp135, e no capsídeo, a p28, que induzem a formação de anticorpos nos animais. Há grande quantidade de ácido siálico na superfície do vírus, o qual protege a proteína viral da digestão das proteases e de uma rápida neutralização viral por anticorpos (QUINN et al., 2005; ICTV, 2009). Figura 3. Organização genômica do vírus da artrite-encefalite caprina (OLSEN, 2001). Figura 4. Estrutura do Lentivírus de Pequenos Ruminantes (SOUZA, 2008 modificado).
26 24 O Lentivírus de Pequenos Ruminantes apresenta tropismo por células do sistema monocítico fagocitário que promovem a distribuição e replicação viral. A interação ocorre por ligação da glicoproteína do seu envelope a receptores específicos na membrana celular do hospedeiro (PASICK, 1998; BLACKLAWS, 2012; SOUZA et al., 2012). A replicação é restrita, e permite que o vírus permaneça latente nos monócitos do hospedeiro (PUGH, 2004; PAULA et al., 2008). Isso porque, após a infecção da célula, a transcriptase reversa gera DNA de dupla fita (provírus), a partir do RNA viral, e este provírus se integra ao DNA cromossômico da célula hospedeira (DAWSON, 1987b; PASICK, 1998). Os lentivírus replicam-se no momento de maturação fagocitária. Diferente dos outros lentivírus, os LVPR não causam imunodeficiência como as outras lentiviroses, tais como HIV, SIV e FIV, pelo fato de terem predileção por infectar principalmente monócitos-macrófagos e não linfócitos. A replicação viral nos macrófagos infectados induzem uma proliferação e reatividade linfocitária, com desenvolvimento inflamatório crônico e aumento da expressão de complexo principal de histocompatibilidade classe II por macrófagos teciduais. Esta ativação nas células pode ser através da produção de citocinas por células inflamatórias ou induzida pelo próprio vírus Os macrófagos infectados induzem a uma proliferação e reatividade linfocitária inespecífica, o que justifica as reações imunomediadas que caracterizam a evolução das lentiviroses clássicas, entretanto, apesar dos indivíduos infectados não serem considerados
27 25 imunossuprimidos, pois não altera a relação de linfócitos T CD4 + e CD8 + nem de granulócitos PG68A +, não se pode excluir a possibilidade de alterações na funcionalidade de células infectadas, por modificar os padrões de citocinas liberados pelos macrófagos, que pode interferir na defesa celular, e por conseguinte permitir a infecção por outros patógenos (QUINN et al., 2005; PONTI et al., 2008; SANTOS, 2012). A doença resulta da inflamação decorrente da reação do sistema imune do hospedeiro para o vírus expressado. O desenvolvimento do anticorpo neutralizante não detém a replicação viral por causa da expressão contínua de variantes antigênicas do vírus com epítopos de neutralização que diferem no tipo específico;além de padrões de glicosilação da proteína do envelope viral, uma vez que o ácido siálico da superfície do vírus diminui a avidez do anticorpo neutralizante ao vírus. No entanto, é a resposta inflamatória à infecção que causa as alterações nos tecidos, responsáveis pela manifestação da enfermidade. As lesões são de natureza linfoproliferativa e o vírus causa uma síndrome multissistêmica, que envolve principalmente o tecido conjuntivo de revestimento sinovial, causando artrite crônica, tumefação e endurecimento do úbere, com ou sem mastite, e pneumonia intersticial crônica (RADOSTITS et al., 2002; LEROUX et al., 2010). A ocorrência de variantes antigênicas estimula não só a infecção persistente; estas mutações e seleções podem promover alteração na virulência, inclusive facilitando o cruzamento interespecífico, o que justifica a existência de subtipos virais presentes tanto em caprinos quanto em ovinos (BLACKLAWS, 2012; SOUZA et al., 2012). Outro fator a destacar é a possibilidade de compartimentalização viral, caracterizada quando na ocorrência de distinção genética dos LVPR isolados nos diversos tecidos animais, correspondentes às sub-populações virais em um mesmo indivíduo (RAMIREZ et al., 2012), dificultando ainda mais a capacidade de eliminação viral. 3. Transmissão dos LVPR Os LVPR infectam monócitos e macrófagos, e disseminam-se pelo sangue, leite ou colostro (PINHEIRO et al., 2001). A principal forma de transmissão do vírus é pela via
28 26 digestiva através da ingestão de colostro e leite de animais infectados. A presença do anticorpo no colostro não evita a infecção (PREZIUSO et al., 2004; STACHISSINI et al., 2007). A fêmea tem papel fundamental na transmissão da infecção. A introdução de fêmeas infectadas com LVPR nos rebanhos acelera a transmissão para os oiutros animais do rebanho, em virtude do contato prolongado com outras matrizes e seus filhotes, bem como na ocorrência de problemas na ordenhadeira mecânica provocando lesões no teto (PINHEIRO et al., 2001; FROTA et al., 2005). A transmissão materna fetal dos LVPR, mesmo com baixa incidência, pode ocorrer por via intrauterina e transmissão no canal vaginal no momento do parto, ou ingestão ou inalação de células infectadas pelas crias (SILVA; LIMA, 2007; KONISH et al., 2011). Sugere-se que a transmissão pode ocorrer pelo contato direto prolongado com sangue, fezes, saliva e secreções urogenitais, e pela atividade sexual, visto ter se evidanciado a particula viral nestas secreções (NORD et al., 1998; GUEDES et al., 2001; LEITNER et al., 2010). Lara et al. (2003) demonstraram, indiretamente, a presença e viabilidade do LVPR no sangue circulante, colostro e leite de caprinos infectados, bem como a possibilidade desses fluídos orgânicos infectarem animais suscetíveis por inoculação. Os cabritos quando marcados com tatuador contaminado com sangue de caprinos positivos apresentaram soroconversão. Isto evidenciou a possibilidade de transmissão horizontal iatrogênica da infecção da CAE. O vírus já foi identificado no sêmen de animais infectados, representando assim a possibilidade de transmissão por monta natural e inseminação artificial, sendo que a presença de inflamações ou infecções no órgão reprodutor pode desencadear o maior fluxo destas células inflamatórias, resultando em aumento da carga viral no sêmen. A diluição do sêmen pode diminuir a carga viral a valores abaixo do detectável em cultura, levando a resultados falso-negativos, pois a lavagem do sêmen não remove totalmente os monócitos e os macrófagos (ANDRIOLI et al., 2003; ANDRIOLI et al., 2006). É importante salientar a possibilidade de que outras rotas de infecção horizontal estejam envolvidas na transmissão do LVPR, uma vez que o vírus já foi isolado e cultivado em diferentes tipos celulares que poderiam ter papel importante na sua transmissão (SILVA; LIMA, 2007).
29 27 Deve-se considerar que em criações consorciadas, caprinos e ovinos, de forma ainda não muito clara, podem transmitir naturalmente o lentivírus (SHAH et al., 2004b; COSTA et al., 2007). Semelhante ao encontrado por Souza et al. (2015), ao comprovarem a transmissão do lentivírus caprino para ovinos, a partir do contato direto dos animais após um mês de confinamento. 4. Achados clínicos da CAE e MV A lentivirose é uma doença crônica, que ocasiona vários sinais clínicos, entre eles a artrite, a encefalite, a mastite e a pneumonia (SOUSA et al., 2005; PUGH, 2004; LARA et al., 2005). O vírus pode estar presente em todos os líquidos biológicos do organismo (FRANKE, 1998). Linfadenopatias e emagrecimento progressivo podem ser observados, de forma isolada ou simultânea (COSTA et al., 2007), entretanto alguns animais infectados podem não apresentar sinal clínico da enfermidade (GUEDES et al., 2001). As principais formas clínicas nos caprinos descritas em animais infectados pelo vírus são leucoencefalomielite, que ocorre, principalmente, em animais jovens, e artrite, mais frequente em animais adultos, além de pneumonia intersticial crônica, e mastite intersticial com endurecimento progressivo do parênquima da glândula mamária (LARA et al., 2005). A doença causa prejuízos econômicos na produção, principalmente devido ao quadro de caquexia dos animais. Casos de pneumonia e encefalite podem causar morte dos animais acometidos (TEIXEIRA et al., 2008). O emagrecimento progressivo observado em animais infectados ainda não tem o seu mecanismo totalmente esclarecido, apesar de ser atribuído à deficiência alimentar. Entretanto, verificou-se a influência da infecção no metabolismo dos animais devido às menores concentrações séricas de albumina, creatinina, ureia e glicose (DIAS, 2011). O sinal clínico mais consistente em animais acometidos com a CAE é o aumento de volumeperiarticular do carpo, que aparece em 12 a 40% nas cabras infectadas (KNOWLES et al., 1994). Já para ovinos com MV, a forma respiratória é a mais importante. Os animais acometidos manifestam dificuldade respiratória, apatia, emagrecimento, podendo desenvolver quadros de pneumonia bacteriana, secundários a infecção (DAWSON, 1987a; ANGELOPOULOU et al., 2005; BENAVIDES et al., 2013).
30 28 A forma articular da LVPR é caracterizada principalmente pelo aumento de volume da articulação, além de outros distúrbios do sistema locomotor, como claudicação e adoção de posições anômalas. A forma clínica mamária desta enfermidade é caracterizada pela presença de nódulos e endurecimento difuso no parênquima da glândula mamária, assim como a diminuição da produção de leite (FRANKE, 1998; CASTRO et al., 1999; GREGORY et al., 2009a; GREGORY et al., 2009b). A alteração pulmonar se caracteriza por pneumonia intersticial. Já a forma neurológica, mais comum em cabritos entre um a quatro meses de idade, se caracteriza pela prsença de incoordenação e paralisia (CALLADO et al., 2001). Figura 5. Manifestação clínica da lentivirose de pequenos ruminantes em caprinos. [A] Forma neurológica; [B] Forma mamária (Fonte: gentilmente cedido por Roberta L.L. de Brito); [C e D] Forma articular associada a emagrecimento progressivo (Fonte: arquivo pessoal). B A B 5. Diagnóstico e medidas de controle para a LVPR C D Devido à ausência de sinais clínicos patognomônicos e a presença de animais assintomáticos, é importante o auxílio de testes laboratoriais no diagnóstico da LVPR (LARA et al., 2005). As técnicas utilizadas se baseiam na detecção direta do vírus ou do
31 29 seu material genético, e indireto na identificação por anticorpos (PINHEIRO et al., 2001; REINA et al., 2006; CRUZ et al., 2009a; CRUZ et al., 2009b). A técnica de PCR possui alta especificidade e relativa sensibilidade, sendo recomendada em programas de controle da enfermidade em etapas mais avançadas, por conseguir detectar o início da infecção, a fase de viremia (FROTA et al., 2005). Entretanto, como a duração desta é variável, faz-se necessário o auxílio de técnicas de diagnóstico para detecção de resposta humoral (PLAZA et al., 2009). O diagnóstico sorológico é o mais utilizado, tendo como objetivo detectar a presença de anticorpos, mas a avaliação deve ser cautelosa, visto que um resultado negativo pode ser um falso negativo, pela possibilidade de soroconversão tardia ou baixas concentrações de anticorpos no sangue (FRANKE, 1998). Os métodos mais utilizados são a imunodifusão em gel de agarose (IDGA), a técnica imunoenzimática enzimelinked immunsorbent assay (ELISA), Immunobloting (IB) e a imunofluorescência indireta (IFI) (LIMA et al., 2013b). Para ser declarado livre da infecção um rebanho previamente infectado deve ser negativo em pelo menos três ou quatro testes em intervalos de seis a doze meses (NORD et al., 1998; PINHEIRO et al., 2012). Impedir a propagação da infecção de LVPR inclui a pasteurização do colostro, a segregação e a identificação de animais soropositivos (LEITNER et al., 2010). A segregação e/ou erradicação imediata dos animais constitui uma prática eficiente para limitar a propagação do vírus, que por sua vez, tem um impacto positivo na produção, incluindo alguns parâmetros do leite, aumentando os níveis de proteína e sólidos totais (TURIN et al., 2005). Vale salientar que, em programas de controle e erradicação da enfermidade implementados em sistemas de criação consorciada com caprinos e ovinos, é importante realizar o controle de ambas as espécies, pois a transmissão interespécie é uma possibilidade (SHAH et al., 2004b). OBJETIVOS - Detectar a presença do lentivírus caprino (LVC) no leite de ovelhas e no sêmen de carneiros.
32 30 - Avaliar a transmissão do lentivirus de caprinos (LVC) entre ovinos - Realizar a avaliação clínica de ovinos infectados com o lentivírus caprino HIPÓTESE CIENTÍFICA Ovinos infectados com lentivirus caprino podem transmitir a infecção, por diferentes vias, manifestando alterações clínicas da enfermidade.
33 31 CAPÍTULO 1 Lentivírus caprino em leite e sêmen de ovinos
34 32 Lentivírus caprino em leite e sêmen de ovinos RESUMO Com o objetivo de detectar a presença do lentivírus caprino (LVC) no leite de ovelhas e no sêmen de carneiros, utilizaram-se dez matrizes e quatro reprodutores infectados experimentalmente com o LVC. Foram colhidas amostras de leite das ovelhas durante os quatro meses de lactação, ocorrendo cinco coletas por animal, totalizando 50 amostras. Quanto aos carneiros, realizaram-se oito coletas de sêmen por animal, durante um ano de experimentação, totalizando-se 32 amostras. As amostras de leite e de sêmen foram submetidas à extração de DNA e à prova de reação em cadeia da polimerase do tipo nested (npcr), visando à detecção de DNA proviral do LVC. Oito (16%) amostras de leite foram positivas na npcr oriundas de duas ovelhas. Apenas uma (3,12%) amostra de sêmen apresentou positividade. Produtos da amplificação foram sequenciados, confirmando-se tratar de sequência genômica do LVC. Desta forma, demonstrou-se a presença do DNA proviral do LVC em leite e sêmen de ovinos, confirmando a viabilidade da infecção entre espécies, alertando sobre o risco de infecção se espalhe. Palavras-chave: Lentiviroses, transmissão, infecção cruzada.
35 33 Detection of caprine lentivirus in sheep milk and semen of rams ABSTRACT In order to detect the presence of the caprine lentivirus (LVC) in milk of sheep and semen of rams, ten sheep and four rams experimentally infected with LVC were used. Milk samples of sheep were collected throughout the lactation period, totaling five collections per animal and 50 samples. About the rams, there were eight semen collection sessions per animal for a year of experimentation, totaling 32 samples. DNA of milk and semen were extracted and they were submitted to Polymerase Chain Reaction of nested type (npcr), aimed at LVC proviral DNA detection. As for milk, only two sheep had positive samples in npcr totaling eight positive samples among the 50 analyzed. Regarding the semen, only one sample was positive in npcr of 32 samples analyzed. Some of the positive samples were sequenced, confirming that they were sequences of LVC. Thus, it was possible to prove the presence of proviral DNA of caprine lentivirus in milk and semen of sheep, confirming the viability of interspecies infection, warning about the risk of infection spreading. Key words: Small ruminant lentivirus, transmission, cross infection.
36 34 INTRODUÇÃO A artrite-encefalite caprina (CAE) e a maedi-visna dos ovinos (MV) são enfermidades causadas por lentivírus de pequenos ruminantes (LVPR), caracterizando-se por evolução crônica e agravamento progressivo até o óbito (BLACKLAWS, 2012). São conhecidas diferentes manifestações clínicas, sendo as principais a artrite, a pneumonia, a encefalite e a mastite, além do emagrecimento progressivo (PEREZ et al., 2014). As vias de transmissão mais importantes são por ingestão de colostro e leite contaminados, e por contato com secreções contendo o vírus, como as do trato respiratório e reprodutivo. Logo, a transmissão pode ocorrer verticalmente, entre a matriz infectada e suas crias (ALVAREZ et al., 2005); horizontalmente, pelo contato direto entre animais infectados e suscetíveis (VILLORIA et al., 2013), e de forma iatrogênica, destacando-se a mamada artificial e a utilização de sêmen em técnicas de reprodução (ALVAREZ et al., 2006; ANDRIOLI et al., 2006; SOUZA et al., 2013). Durante anos, os agentes etiológicos da CAE e da MV foram considerados como espécie-específicos. Entretanto, análises genômicas dos LVPR apontaram para a ocorrência de cepas heterogêneas, evoluídas dos protótipos virais da CAE e da MV, capazes de infectar tanto caprinos quanto ovinos (SHAH et al., 2004). Nesse sentido, a transmissão do lentivírus de caprinos para ovinos já foi comprovada (SOUZA et al., 2015), entretanto não está claro se animais infectados com cepas heterólogas têm a capacidade de transmitir a infecção. Desta forma, o objetivo deste experimento foi detectar a presença do DNA proviral de lentivirus caprino em leite e sêmen de ovinos infectados experimentalmente. MATERIAL E MÉTODOS O experimento foi realizado no Centro Nacional de Pesquisa de Caprinos e Ovinos da Empresa Brasileira de Pesquisa Agropecuária (Embrapa Caprinos e Ovinos), no município de Sobral (CE), sob aprovação do Comitê de Ética no Uso de Animais da Universidade Estadual do Vale do Acaraú/Embrapa (número 001/2012). Visando a detecção do lentivírus caprino (LVC) no leite e no sêmen de ovinos, foram estabelecidos dois grupos experimentais com animais de um ano de idade, mestiços
37 35 das raças Morada Nova e Santa Inês, mantidos isolados em baias de experimentação. O primeiro grupo constituiu de 10 fêmeas e o segundo foi formado por quatro machos. Tanto as fêmeas quanto os machos foram infectados ao nascimento com LVC, por mamada de colostro e leite de cabras infectadas. A infecção por LVC foi confirmada a partir de testes de reação em cadeia de polimerase do tipo nested (npcr) aos sete dias de vida, e durante todo o experimento os animais foram avaliados clinicamente. No grupo das fêmeas, amostras de leite foram colhidas aos 30, 60, 75, 90 e 120 dias de lactação, em tubos tipo falcon de 15mL, estéreis, após limpeza dos tetos com auxílio de gaze e álcool 70%. A ordenha foi realizada delicadamente até ser obtido o volume de 15 ml de leite de cada teto. As amostras de leite foram centrifugadas a 3.000g por 15 minutos e lavadas cinco vezes com solução salina fosfatada (PBS) para a obtenção da papa de células, baseandose na metodologia descrita por Sardi et al. (2012b). O DNA foi extraído de acordo com Grimberg et al. (1989), utilizando cloreto de lítio e proteinase K. Após a extração, as amostras foram armazenadas à -20ºC, até a realização da técnica de npcr. No grupo dos machos, foram realizadas oito coletas de sêmen por animal, durante um ano de experimentação. O sêmen foi colhido utilizando-se vagina artificial (MIES FILHO, 1962), tendo como manequim uma fêmea ovina em cio. Foram utilizadas 100µL de sêmen fresco para filtração em coluna de Sephacryl S- 40, seguindo método de Santurde et al. (1996), para retirada de impurezas. Após, 3µL de cada filtrado foi transferido para microtubos estéreis, a fim de realizar a extração de DNA, com a utilização de 200µL de solução de Chelex 100 a 5%, 2µL de proteinase K (10µg/µL) e 7µL de Dithiothreitol a 1M, incubados em banho-maria a 56 C, por 60 minutos. Depois desta etapa, as amostras foram homogeneizadas por 10 segundos, e aquecidas em banho-maria de água fervente (100 C) por oito minutos, para inativação da proteinase K. Posteriomente, realizou-se centrifugação por três minutos a G, e acondicionamento em freezer a -20 C, até a realização do teste de npcr. As amostras de DNA extraídas do leite e do sêmen foram submetidas à técnica de npcr, seguindo-se o método de Barlough et al. (1994) modificada por Andrioli et al. (2006). A reação consistiu de um volume total de 50µL, contendo tampão (10mM tris- HCl, 50mM KCl e 1,5mM MgCl2), 100µM de cada dntp, 20pmol de cada oligonucleotídeo iniciador; 2U de Taq DNA polimerase; 3µL de amostra na primeira
38 36 etapa e 1µL do produto desta na segunda etapa, sendo o volume final completado com água estéril. Em paralelo com as amostras testadas, utilizou-se um controle negativo (água estéril), e um controle positivo (material extraído de cultura de célula de membrana sinovial infectada com lentivirus, cepa B1, circulante no rebanho experimental de caprinos infectados com LVC da Embrapa Caprinos e Ovinos). Na reação foram utilizados dois pares de oligonucleotídeos iniciadores, obtidos a partir de sequência da região do gene gag, da amostra de cepa padrão CAEV-Cork (SALTARELLI et al., 1990), sendo os iniciadores P1 (5 - CAAGCAGCAGGAGGGAGAAGCTG-3 ) e P2 (5 - TCCTACCCCCATAATTTGATCCAC-3 ) usados para obter uma sequência alvo de 297pb e os iniciadores P3 (5 -GTTCCAGC AACTGCAAACAGTAGCAATG-3 ) e P4 (5 ACCTTTCTGCTTCTTCATTTAATTTCCC-3 ), objetivando a obtenção de um fragmento-alvo de 187pb (RIMSTAD et al., 1993). As reações de amplificação foram realizadas em termociclador (Programmable Thermal Controller, PTC-100, MJ Research, Inc.), constituindo um ciclo inicial de 94 C por cinco minutos; seguidos por 35 ciclos de um minuto a 94 C, um minuto a 56 C e 45 segundos a 72 C; extensão final a 72 C por sete minutos. As amostras amplificadas e os controles positivo e negativo, juntamente com o marcador de 100 bp DNA ladder, foram submetidos à eletroforese em gel de agarose a 2% em TBE (Tris, borato e EDTA 0,1X), coradas com brometo de etídio e visualizadas em transluminador de luz ultravioleta (ANDRIOLI et al., 2006). As amostras positivas na npcr foram sequênciadas na plataforma Applied Biosystems 3500 Genetic Analyzer. Estas sequências foram alinhadas com uso do Clustal W (THOMPSON et al., 1994), utilizando o programa BioEdit Sequence Alignment Editor (HALL, 1999) e comparadas com as sequências das cepas padrões CAEV Cork e MVVK1514, disponíveis no GenBank sob a numeração M33677 e M60610, respectivamente, além da sequência obtida a partir da cepa circulante na Embrapa Caprinos e Ovinos (BR/CNPC-G1), classificada como subtipo B1. RESULTADOS E DISCUSSÃO
39 37 Foi detectado DNA proviral de LVC no leite de ovelhas a partir da técnica de npcr em oito amostras das 50 analisadas (Tabela 1). Estas amostras positivas pertenceram a duas das dez ovelhas utilizadas. Tabela 1. Resultados de PCR nested em amostras de leite de dez ovelhas experimentalmente infectadas com lentivírus caprino, colhidas dos 30 aos 120 dias de lactação. Matrizes ovinas Período dias dias dias dias dias (-): Negativo; (+): Positivo. A capacidade da npcr em detectar o DNA proviral no leite foi verificada por outros estudos (GREGORY et al., 2011; SARDI et al., 2012b); entretanto os mesmos trabalharam com cabras, e ainda assim obtiveram baixa detecção frente à infecção, o que pode ser justificada pelo possível diminuto número de cópias do genoma viral presente nas células do leite, uma vez que existe variação na carga viral (BARQUERO et al., 2013). Neste experimento a detecção de DNA proviral pela npcr foi de 16%, e isto pode ser devido a baixa carga viral. Este fato se associa a variabilidade na composição celular do leite, principalmente dos monócitos, que albergam o DNA proviral, que pode ser causada por diversos fatores, influenciando na capacidade diagnóstica do npcr para LVC no leite (RAVAZZOLO et al., 2006; GOMES et al., 2010; BARBOSA et al., 2012; BLACKLAWS, 2012). A detecção de DNA proviral do LVC no leite de ovelhas comprovou a presença de células infectadas, entretanto não necessariamente a presença da partícula viral no leite, sugerindo a glândula mamária como potencial via de eliminação do LVC (RAVAZZOLO et al., 2006; GREGORY et al., 2009a). Já foi comprovado que células portadoras do DNA proviral são capazes de transmitir o vírus (HERRMANN-HOESING et al., 2007). Assim, o leite de ovelhas
40 38 infectadas com DNA pro-viral do LVC deve ser considerado quanto aos fatores de risco no controle da enfermidade. Destaca-se que não houve manifestação clínica da enfermidade nas ovelhas, inclusive os úberes se mantiveram saudáveis durante todo o período de experimentação, descartando a possibilidade de mastite indurativa, o que está de acordo com a baixa replicação viral na glândula mamária, que diminuiu a ocorrência de lesões (GREGORY et al., 2009b). Animais clinicamente saudáveis podem ter carga viral mais baixa (RAVAZZOLO et al., 2006), e isto possivelmente justifica a discreta detecção de positividade na npcr. Foi observada também a presença de DNA proviral de lentivirus caprino em uma amostra de sêmen de carneiro, das 32 avaliadas (Tabela 2). Tabela 2. Resultados de PCR nested em amostras de sêmen de quatro carneiros experimentalmente infectadas com lentivírus caprino, colhidas de abril de 2013 a abril de Coleta Carneiros (-): Negativo; (+): Positivo. A presença de DNA proviral de LVPR em sêmen já havia sido detectada em bodes naturalmente e experimentalmente infectados. Inclusive, Paula et al. (2009) verificaram uma intermitência na positividade ao npcr, ao realizar estudos com caprinos infectados com a mesma cepa deste experimento. O exame físico das ovelhas e dos carneiros não indicou qualquer alteração clínica condizente com infecção por lentivirus. Esta ausência de sintomatologia já foi relatada em outros estudos (BRITO, 2009; CAVALCANTE et al., 2013; SOUZA et al., 2015), e pode estar associada a fatores como a patogenicidade da cepa viral para a espécie ovina, uma vez que a mesma estava circulando apenas em caprinos e nestes demonstrava sintomatologia.possivelmente não estabeleceu mecanismo natural de adaptação à espécie ovina, corroborando com a ausência de manifestação clínica (GREGORY et al., 2011; RACHID et al., 2013).
41 39 Vale ressaltar que algumas quasispécies virais são comprovadamente mais adaptadas a caprinos e outras a ovinos, e que a interação nestas espécies ocorrem de forma diferente, o que deve ser considerado na interpretação dos resultados (SHAH et al., 2004; SOUZA et al., 2012; RACHID e tal., 2013). Ainda é importante ressaltar a possibilidade do vírus entrar em estado de quiescência, quando mantem o seu material genético integrado ao DNA nuclear, sem entretanto ser ativado, ou ainda em ambiente intracelular, mas sem ser integrado (CAVALCANTE et al., 2013), o que justifica a ausência de replicação, que estimularia a manifestação clínica. Quanto a discreta detecção de positividade no npcr, esta pode ser devido a baixa replicação viral nestes sítios de infecção, e portanto a capacidade de detecção do material genético nos tecidos (BARQUERO et al., 2013), apesar do tecido mamário ser sítio de predileção para a replicação do lentivírus de pequenos ruminantes (RAVAZZOLO et al., 2006; GREGORY et al., 2011). É importante ainda considerar que quanto à detecção de material genético, os lentivirus de pequenos ruminantes possuem a característica denominada intermitência, havendo alternância entre positividade e negatividade, a depender da presença de células infectadas na amostra avaliada (ALVAREZ et al., 2005; PAULA et al., 2009). Em relação às sequências genéticas obtidas com o sequenciamento das amostras positivas na npcr (Figura 1), verificou tratar-se de sequências do gene gag do lentivírus caprino, ocorrendo algumas modificações de nucleotídeos no fragmento estudado (FEITOSA et al., 2010; SOUZA et al., 2015). Com relação à homologia das sequências, verificou-se que as sequências de leite das ovelhas 04 e 07 apresentaram 98% e 97% de homologia com a CAEV Cork, e 90% e 88% com a cepa MVV K1514 respectivamente; quanto à sequência obtida do sêmen, a mesma demonstrou 100% de homologia com a CAEV Cork e 90% com a MVV K1514. Isto pode ser explicado em decorrência da seleção imposta pela compartimentalização do leite e do sêmen sobre populações de lentivírus caprino (LVC). A compartimentalização de quasispecies dos lentivírus de pequenos ruminantes (LVPR) é determinada como a distinção genética dos LVPR isolados nos diversos tecidos animais, correspondentes às sub-populações virais em um mesmo indivíduo (RAMIREZ et al., 2012).
42 40 Figura 1. Sequências parciais do gene gag de lentivírus de pequenos ruminantes: resultados obtidos da PCR nested em leite de ovelhas e sêmen de carneiros infectados com lentivirus caprino. *Seta vermelha indica troca de nucleotídeo em relação a sequencia genômica da cepa padrão CAEV Cork. A comparação dos fragmentos obtidos fornece informações importantes quanto aos sítios nucléicos modificados, e estas alterações podem estar associadas a mutações que levariam à adaptação da cepa viral ao hospedeiro. Entretanto, este experimento não foi suficiente para atestar tratar-se de mutação vinculada a adaptação. Vale ressaltar que estas modificações podem influenciar no processo de replicação viral (BARQUERO et al., 2013). Assim, verifica-se que várias são as características que influenciam a transmissão do lentivírus, visto que a disseminação da enfermidade não é espécie-específica, e estas quasispecies virais são intimamente ligadas aos mecanismos de evasão da resposta imune, decorrente de erros de transcrição do RNA viral pela transcriptase reversa, que podem ser correlacionados com as modificações nucléicas observadas neste trabalho (PASICK et al., 1998; GERMAIN e VALAS, 2006; REINA et al., 2006). CONCLUSÕES Foi detectado DNA proviral do lentivírus caprino no leite de ovelhas e no sêmen de carneiros infectados experimentalmente, sugerindo assim a viabilidade da infecção originalmente de caprinos em ovinos, apesar da ausência de manifestação clínica. As
43 41 pequenas modificações observadas nas sequencias genéticas obtidas sugerem que pode ocorrer adaptação da cepa viral à nova espécie, a partir da possibilidade de erros na transcrição gênica. A possibilidade de retransmissão da infecção reflete sobre a atenção que deve ser dada para as medidas de controle da enfermidade em pequenos ruminantes. AGRADECIMENTOS A Fundação de Amparo à Pesquisa do Estado da Bahia (Fapesb) pelo fomento ao projeto, ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq) pelo financiamento à pesquisa. À Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (Capes) pela concessão da bolsa de estudos e a Embrapa Caprinos e Ovinos pelo apoio à execução do experimento. REFERÊNCIAS ÁLVAREZ, V.; ARRANZ, J.; DALTABUIT-TEST, M.; LEGINAGOIKOA, I.; JUSTE, R.A.; AMORENA, B.; DE ANDRÉS, D.; LUJÁN, L.L.; BADIOLA, J.J.; BERRIATUA, E. Relative contribution of colostrum from Maedi-Visna virus (MVV) infected ewes to MVV-seroprevalence in lambs. Research in Veterinary Science, v.78, n.3, p , ÁLVAREZ, V.; DALTABUIT-TEST, M.; ARRANZ, J.; LEGINAGOIKOA, I.; JUSTE, R.A.; AMORENA, B.; DE ANDRÉS, D.; LUJÁN, L.L.; BADIOLA, J.J.; BERRIATUA, E. PCR detection of colostrum-associated Maedi-Visna virus (MVV) infection and relationship with ELISA-antibody status in lambs. Research in Veterinary Science, v.80, n.2, p , ANDRIOLI, A.; GOUVEIA, A.M.G.; MARTINS, A.S.; PINHEIRO, R.R.; SANTOS, D.O. Fatores de risco na transmissão do lentivírus caprino pelo sêmen. Pesquisa Agropecuária Brasileira, v.41, n.8, p , BARBOSA, D.A.; BLAGITZ, M.G.; BATISTA, C.F.; GOMES, V.; AZEDO, M.R.; SOUZA, F.N.; BENITES, N.R.; DELLA LIBERA, A.M.M.P. Contagem automática e microscópica direta de células somáticas do leite de ovelhas Santa Inês, utilizando como
44 42 corantes o Broadhurst-palley e a hematoxilina-eosina. Ciência Animal, v.22, n.3, p , BARLOUGH, J.; EAST, N.; ROWE, J.D.; HOOSEAR, K.V.; DEROCK, E.; BIGORNIA, L.; RIMSTAD, E. Double-nested polymerase chain reaction for detection of caprine arthritis-encephalitis virus proviral DNA in blood, milk, and tissues of infected goats. Journal of Virological Methods, v.50, n.1-3, p , BARQUERO, N.; GOMEZ-LUCIA, E.; ARJONA, A.; TOURAL, C.; LAS HERAS, A.; FERNÁNDEZ-GARAYZABAL, J.F.; DOMENECH, A. Evolution of specific antibodies and proviral DNA in milk of small ruminants infected by small ruminant lentivirus. Viruses, v.5, n.10, p , BLACKLAWS, B.A. Small ruminant lentiviruses: Immunopathogenesis of visna-maedi and caprine arthritis and encephalitis virus. Comparative Immunology, Microbiology and Infectious Diseases, v.35, n.3, p , BRITO, R.L.L. Implicações da artrite-encefalite caprina na reprodução, produção e na qualidade do leite de cabras. Sobral, CE: UEVA Centro de Ciências Agrárias e Biológicas. 2009, 109p. Dissertação (Mestrado). CAVALCANTE, F.R.A., ANDRIOLI, A.; PINHEIRO, R.R.; SOUZA, K.C.; VERAS, A.K.A.; LOPES, T.A.; SOUSA, S.D.; SILVA, P.A.F. Detecção do vírus da Artrite Encefalite Caprina por nested PCR e nested RT-PCR em ovócitos e fluido uterino. Arquivos do Instituto Biológico, v.80, n.4, p , FEITOSA, A.L.V.L.; TEIXEIRA, M.F.S.; PINHEIRO, R.R.; CUNHA, R.M.S.; LIMA, J.P.M.S.; ANDRIOLI, A.; DANTAS, T.V.M.; MELO, V.S.P.; PINHEIRO, D.C.S.N. Phylogenetic analysis of small ruminant lentiviruses from Northern Brazil. Small Ruminant Research, v.94, n.1-3, p , GERMAIN, K.; VALAS, S. Distribution and heterogeneity of small ruminant lentivirus envelope subtypes in naturally infected sheep. Virus Research, v. 120, n.1-2, p , GOMES, V.; AMATO, A.L.; PONTE, G.C.T.G.; BLAGITZ, M.; MADUREIRA, K.M.; DELLA LIBERA, A.M.M.P. Contagem automática e microscópica direta das células
45 43 somáticas do leite de ovelhas da raça lacaune, utilizando como corantes o Rosenfeld e verde de metil e Pironina-Y. Ciência Animal Brasileira, v. 11, n. 1, p , GREGORY, L.; LARA, M.C.C.S.H.; VILLALOBOS, E.M.C.; HASEGAWA, M.Y.; CASTRO, R.S.; RODRIGUES, J.N.M.; ARAÚJO, J.; KELLER, L.W.; DURIGON, E.L. Detecção do vírus da atrite encefalite caprina em amostras de leite de cabras pela reação em cadeia da polimerase (PCR) e Nested-PCR. ARS Veterinária, v. 25, n. 3, p , 2009a. GREGORY, L.; BIRGEL JÚNIOR, E.H.; LARA, M.C.C.S.H.; ANGELINI, M.; ARAÚJO, W.P.; RIZZO, H.; MAIORKA, P.C.; CASTRO, R.S.; KIRALY, A.C.M.; BENESI, F.J.; BIRGEL, E.H. Clinical features of indurative mastitis caused by caprine arthritis encephalitis virus. Brazilian Journal of Veterinary Pathology, v.2, n.2, p.64-68, 2009b. GREGORY, L.; LARA, M.C.C.S.H.; HASEGAWA, M.Y.; CASTRO, R.S.; FATINI, L.C.; GAETA, N.C.; RODRIGUES, J.N.M.; ARAÚJO, J.; KELLER, L.W.; DURIGON, E.L. Detecção do vírus da artrite encefalite caprina em pulmão, glândula mamária, cérebro e líquido sinovial de cabras naturalmente infectadas pela técnica de nested-pcr. Medicina Veterinária, v.5, n.1, p.7-11, GRIMBERG, J.; NOWOSCHIK, S.; BELLUSCIO, L.; MCKEE, R.; TURCK, A.; EISENBERG, A. A simple and efficient non-organic procedure for the isolation of genomic DNA from blood. Nucleic Acids Research, v.17, n.20, p.83-90, HALL, T.A. Bioedit: a user-friendly biological sequence alignment editor and analysis program for Windows 95/98/NT. Nucleic Acids Symposium Series, v.41, p.95-98, HERRMANN-HOESING, L.M.; PALMER, G.H.; KNOWLES, D.P. Evidence of proviral clearance following postpartum transmission of an ovine lentivirus. Virology, v.362, n.1, p , MIES FILHO, A. Novo modelo de vagina artificial para ovinos. Revista da Faculdade de Agronomia, v. 5, p , 1962.
46 44 PASICK, J. Maedi-Visna Virus and Caprine Arthritis-Encephalitis Virus: Distinct species or quasispecies and its implications for laboratory diagnosis. Canadian Journal of Veterinary Research, n.62, p , PAULA, N.R.O.; ANDRIOLI, A.; CARDOSO, J.F.S.; PINHEIRO, R.R.; SOUSA, F.M.L.; SOUZA, K.C.; ALVES, F.S.F.; CAMPELLO, C.C.; RICARTE, A.R.F.; TEIXEIRA, M.F.S. Profile of the Caprine arthritis-encephalitis virus (CAEV) in blood, semen from bucks naturally and experimentally infected in the semi-arid region of Brazil. Small Ruminant Research, v.85, n.1, p.27-33, PÉREZ, M.; BIESCAS, E.; REINA, R.; GLARIA, I.; MARÍN, B.; MARQUINA, A.; SALAZAR, E.; ÁLVAREZ, N.; DE ANDRÉS, D.; FANTOVA, E.; BADIOLA, J.J.; AMORENA, B.; LUJÁN, L. Small ruminant lentivirus-induced arthritis:clinicopathologic findings in sheep infected by highly replicative SRLV B2 genotype. Veterinary Pathology Online, v.52, n.1, p , RACHID, A.; CROISÉ, B.; RUSSO, P.; VIGNONI, M.; LACERENZA, D.; ROSATI, S.; KUZMAK, J.; VALAS, S. Diverse host-virus interactions following caprine arthritis-encephalitis virus infection in sheep and goats. Journal of General Virology, v.94, n.3, p , RAMÍREZ, H.; REINA, R.; BERTOLOTTI, L.; CENOZ, A.; HERNÁNDEZ, M.M.; ROMÁN, B.S.; GLARIA, I.; ANDRÉS, X.; CRESPO, H.; JÁUREGUIL, P.; BENAVIDES, J.; POLLEDO, L.; PÉREZ, V.; GARCÍA-MARÍN, J.; ROSATI, S.; AMORENA, B.; ANDRÉS, D. Study of compartmentalization in the visna clinical form of small ruminant lentivirus infection in sheep. BMC Veterinary Research, v.8, n.8, p.1-12, RAVAZZOLO, A.P.; NENCI, C.; VOGT, H.R.; WALDVOGEL, A.; OBEXER-RUFF, G.; PETERHANS, E.; BERTONI, G. Viral load, organ distribution, histopathological lesions and cytokine mrna expression in goats infected with a molecular clone of the caprine arthritis encephalitis virus. Virology, v. 350, n.1, p , REINA, R.; MORA, M.I.; GLARIA, I.; GARCÍA, I.; SOLANO, C.; LUJÁN, L.; BADIOLA, J.J.; CONTRERAS, A.; BERRIATUA, E.; JUSTE, R.; MAMOUN, R.Z.; ROLLAND, M.; AMORENA, B.; DE ANDRÉS, D. Molecular characterization and
47 45 phylogenetic study of Maedi Visna and Caprine Arthritis Encephalitis viral sequences in sheep and goats from Spain. Virus Research, v.121, n.2, p , RIMSTAD, E.; EAST, N.E.; TORTEN, M.; HIGGINS, J.; DEROCK, E.; PEDERSEN, N.C. Delayed seroconversion following naturally acquired caprine arthritis-encephalitis virus infection in goats. American Journal of Veterinary Research, v.54, n.11, p , SALTARELLI, M.; QUERAT, G.; KONINGS, D.A.M.; VIGNE, R.; CLEMENTS, J.E. Nucleotide sequence and transcriptional analysis of molecular clones of CAEV which generate infectious virus. Virology, v.179, n.1, p , SANTURDE, G., DA SILVA, N., VILLARES R., TABARES, E., SOLANA, A., BAUTISTA, J.M., CASTRO, J.M. Rapid and high sensitivity test for direct detection of bovine herpesvirus-1 genome in clinical samples. Veterinary Microbiology, v.49, p.81-92, SARDI, S.I.; TORRES, J.A.; BRANDÃO, C.F.L.; TIGRE, D.M.; CAMPOS, G.S. Early detection of goats infected with lentivirus small ruminant virus by ELISA assay. Revista de Ciências Médicas e Biológicas, v.11, n.1, p.35-40, SHAH, C.A.; BÖNI, J.; HUDER, J.B.; VOGT, H.R.; MÜHLLHER, J.; ZANONI, R.; MISEREZ, R.; LUTZ, H.; SCHÜPBACH, J. Phylogenetic analysis and reclassification of caprine and ovine lentiviruses based on 104 new isolates: evidence for regular sheepto-goat transmission and world-wide propagation through livestock trade. Virology, v.319, n.1, p.12-26, SOUZA, K.C.; PINHEIRO, R.R.; SANTOS, D.O.; BRITO, R.L.L.; RODRIGUES, A.S.; SIDER, L.H.; PAULA, N.R.O.; AVILA, A.A.; CARDOSO, J.F.S.; ANDRIOLI, A. Transmission of the caprine arthritis-encephalitis virus through artificial insemination. Small Ruminant Research, v.109, n.2-3, p , SOUZA, T.S.; PINHEIRO, R.R.; LIMA, C.C.V.; COSTA, J.N. Transmissão interespécie de lentivírus de pequenos ruminantes: Revisão e Desafios. Acta Veterinaria Brasilica, v.6, n.1, p.23-34, SOUZA, T.S.; PINHEIRO, R.R.; COSTA, J.N.; LIMA, C.C.V.; ANDRIOLI, A.; AZEVEDO, D.A.A.; SANTOS, V.W.S.; ARAUJO, J.F.; SOUSA, A.L.M.; PINHEIRO,
48 46 D.N.S.; FERNANDES, F.M.C.; COSTA NETO, A.O. Interspecific transmission of small ruminant lentiviruses from goats to sheep. Brazilian Journal of Microbiology, Ahead of print. THOMPSON, J.D.; HIGGINS, D.G.; GIBSON, T.J. Clustal W: improving the sensitivity of progressive multiple sequence alignment through sequence weighting, position specific gap penalties and weight matrix choice. Nucleic Acids Research, v.22, n.22, p , VILLORIA, M.; LEGINAGOIKOA, I.; LUJÁN, L.; PÉREZ, M.; SALAZAR, E.; BERRIATUA, E.; JUSTE, R.A.; MINGUIJÓN, E. Detection of Small Ruminant Lentivirus in environmental samples of air and water. Small Ruminant Research, v.110, n.2-3, p , 2013.
49 47 CAPÍTULO 2 Transmissão do lentivírus caprino entre ovinos
50 48 Transmissão do lentivírus caprino entre ovinos RESUMO Com o objetivo de avaliar a transmissão do lentivírus de caprinos (LVC) entre ovinos, foram utilizados 15 cordeiros distribuídos em dois grupos experimentais. O grupo exposto (GE) foi constituído por 10 cordeiros, mantidos com suas mães, que foram infectadas experimentalmente com LVC, tornando-se positivas na PCR nested (npcr). O grupo não exposto (GN) caracterizou-se como grupo controle e foi formado por cinco cordeiros, mantidos com suas matrizes, negativas para LVC pelos testes imunológicos (IDGA, ELISA e IB) e npcr. Foram colhidas amostras de sangue mensalmente, do nascimento a um ano de vida, totalizando 13 amostras por animal. O grupo GN se manteve negativo aos testes durante todo o experimento. Já no GE, três indivíduos apresentaram resultados positivos, sendo dois na npcr e um nos testes imunológicos. As amostras positivas na npcr foram purificadas e sequenciadas, comprovando tratar-se de lentivírus, grupo B1, com semelhança a cepa CAEV Cork. Quanto à via de transmissão, apesar de ser mais provável por ingestão de leite e colostro contaminado, não foi possível descartar a possibilidade de transmissão horizontal. Os resultados comprovam a transmissibilidade de cepa lentiviral caprina entre ovinos. Entretanto, os animais infectados não demonstraram sintomatologia clínica. Palavras-chave: Lentiviroses, CAEV, MVV, transmissão interespécie
51 49 Transmission of caprine lentivirus between sheep ABSTRACT In order to evaluate the transmission of caprine lentivirus (LVC) between sheep, 15 lambs were used into two experimental groups. The exposed group (GE) consisted of 10 lambs kept with their mothers, that were experimentally infected with LVC, becoming positive in the nested PCR (npcr). The unexposed group (GN) was characterized as a control group and it was formed by five lambs kept with their mothers, negative for LVC by immunological tests (AGID, ELISA and IB) and npcr. Blood samples were taken monthly from birth to one year of life, totaling 13 samples per animal. The GN group remained negative to the tests throughout the experiment. On the other hand, about GE group, only three animals had positive results, two in npcr and one in immunological tests. Positive samples in npcr were purified and sequenced, proving that this is lentivirus similar to CAEV Cork strain. As the transmission form, although it is more likely by ingestion of contaminated milk and colostrum, it has not been possible to discard the possibility of horizontal transmission. The results demonstrate the transmissibility of caprine lentiviral strain between sheep. However, infected animals showed no clinical symptoms. Keywords: Lentiviruses, CAEV, MVV, interspecies transmission
52 50 INTRODUÇÃO Os lentivírus são um grupo de vírus de marcada importância na medicina humana e medicina veterinária, por causarem síndromes degenerativas crônicas e incuráveis. Dentro deste grupo, inclui-se a lentivirose de caprinos, denominada artrite-encefalite caprina (CAE), e de ovinos, a pneumonia progressiva ovina ou maedi-visna (MV). Tanto a lentivirose de caprinos como a de ovinos apresentam múltiplas manifestações clínicas, destacando-se a articular, a neurológica, a mamária e a respiratória, além do emagrecimento progressivo (BLACKLAWS et al., 2012). As principais vias de transmissão sugeridas são pelo contato com colostro, leite, ar ou de água contaminados e a inalação de secreções respiratórias. Esta transmissão pode ser tanto verticalmente, entre a matriz e suas crias, quanto pelo contato direto entre os animais, de forma horizontal (PREZIUSO et al., 2004; SHAH et al., 2004; VILLORIA et al., 2013). Em estudos das análises genômicas dos lentivírus de pequenos ruminantes (LVPR), observou-se um grupo heterogêneo de agentes virológicos, abrangendo caprinos e ovinos, ocorrendo ainda variação de patogenicidade, caracterizando-se como quasispécies virais (PASICK, 1998; BLACKLAWS et al., 2004). A partir disso, foi realizado um estudo comprovando a transmissão do lentivirus caprino (LVC) para ovinos (SOUZA et al., 2015), entretanto sem determinar a capacidade de retransmissão desta infecção entre ovinos. Sendo assim, o presente estudo objetivou avaliar a transmissão do lentivírus caprino entre ovinos, a fim de esclarecer possíveis impactos desta infecção. MATERIAL E MÉTODOS O experiento foi conduzido no Centro Nacional de Pesquisa de Caprinos e Ovinos da Empresa Brasileira de Pesquisa Agropecuária (Embrapa Caprinos e Ovinos), situada no município de Sobral CE, sob aprovação do Comitê de Ética no Uso de Animais da Universidade Estadual do Vale do Acaraú (número 001/2012). Para tal, foram estabelecidos três espaços experimentais isolados, com distintas populações: uma constituída por cabras leiteiras, das quais foram obtidos leite e colostro a ser fornecido à população de ovinos. Um segundo rebanho que foi infectado experimentalmente pela ingestão de colostro e leite caprino contaminado com o
53 51 lentivirus; e um terceiro rebanho, constituídos pelos cordeiros filhos do segundo rebanho, dos quais foram obtidas as unidades experimentais deste estudo. A fim de verificar a transmissão do lentivírus caprino entre ovinos, foram avaliados quinze cordeiros mestiços de Santa Inês com Morada Nova; desde o nascimento até um ano de vida, mantidos em baias de isolamento, estabelecendo-se dois grupos experimentais: o grupo exposto (GE) composto por dez cordeiros mantidos com suas mães as quais foram infectadas experimentalmente, durante a fase neonatal, com lentivírus caprino, confirmado por PCR nested (npcr) e sequenciamento, a partir da mamada de leite e colostro de cabras com CAE; e o grupo não exposto (GN), caracterizado como grupo controle, formado por cinco cordeiros, mantidos com suas matrizes, negativas para LVC pelos testes de imunodifusão em gel de agarose (IDGA), ensaio imunoenzimátio (ELISA), immunoblotting (IB) e reação em cadeia da polimerase do tipo nested (npcr). Os cordeiros foram mantidos com suas mães até os 120 dias de vida, quando foi realizado o desmame, e então transferidos para novas baias de isolamento. Para avaliação da transmissão, foram obtidas duas amostras de sangue por venopunção da jugular em sistema a vácuo: uma com 5mL em tubos sem anticoagulante, para obtenção do soro sanguíneo, o qual foi utilizado nas técnicas sorológicas de IDGA, ELISA e IB; e outra com 10mL com anticoagulante (EDTA), para obtenção da papa de leucócitos a ser utilizadas na extração de DNA e posterior técnica de npcr. Os momentos de coleta foram: a primeira até os cinco dias de vida, e depois mensalmente até os doze meses de idade dos animais, totalizando 13 amostras por animal. A papa de leucócitos foi obtida por centrifugação do sangue total, tratado com cloreto de amônio, de acordo com protocolo sugerido por Feitosa et al. (2011). A partir deste material, foi realizada a extração de DNA, com uso de cloreto de lítio (GRIMBERG et al., 1989). Posteriormente, realizou-se a técnica de npcr, seguindo-se a metodologia descrita por Barlough et al. (1994) e modificada por Andrioli et al. (2006). Para cada reação foi utilizado um controle negativo, constituído de água ultrapura autoclavada, e um controle positivo, oriundo de cultura de célula de membrana sinovial infectada com lentivirus, cepa B1. Para a reação de npcr foram utilizados dois pares de oligonucleotídeos iniciadores, obtidos a partir de sequência da região do gene gag, da amostra de cepa padrão CAEV-
54 52 Cork (SALTARELLI et al., 1990), sendo os iniciadores P1 (5 - CAAGCAGCAGGAGGGAGAAGCTG-3 ) e P2 (5 - TCCTACCCCCATAATTTGATCCAC-3 ) usados para obter uma sequência alvo de 297pb. Após, utilizou-se iniciadores P3 (5 -GTTCCAGC AACTGCAAACAGTAGCAATG-3 ) e P4 (5 ACCTTTCTGCTTCTTCATTTAATTT CCC-3 ) na segunda amplificação, objetivando o fragmento-alvo de 187pb (RIMSTAD et al., 1993). As reações de amplificação foram realizadas em termociclador (Programmable Thermal Controller, PTC-100, MJ Research, Inc.), constituindo um ciclo inicial de 94 C por cinco minutos; seguidos de 35 ciclos: 94 C - um minuto, 56 C - um minuto, 72 C - 45 segundos; com extensão final a 72 C por sete minutos. As amostras amplificadas e os controles positivo e negativo, juntamente com o marcador molecular (100pb - Ladder), foram submetidos à eletroforese em gel de agarose a 2% em TBE (Tris, borato e EDTA 0,1X), corado com brometo de etídio e visualizadas em transluminador de luz ultravioleta (ANDRIOLI et al., 2006). Para comparação dos fragmentos de DNA positivos na npcr, as amostras foram sequênciadas na plataforma Applied Biosystems 3500 Genetic Analyzer. Estas sequências então foram alinhadas com uso do Clustal W (THOMPSON et al., 1994), utilizando o programa BioEdit Sequence Alignment Editor (HALL, 1999) e comparadas com as sequências das cepas padrões CAEV Cork e MVVK1514, disponíveis no GenBank sob a numeração M33677 e M60610, respectivamente, além da sequência obtida a partir da cepa circulante na Embrapa Caprinos e Ovinos (BR/CNPC-G1), classificada como subtipo B1 Além da realização de técnica molecular, também foram utilizados testes sorológicos, a fim de verificar a resposta imunológica dos cordeiros ao LVC. Para tal, foram utilizadas três diferentes técnicas, objetivando verificar a capacidade de detecção das mesmas frente a infecção: a fim de testar a viabilidade de utilização no diagnóstico, a IDGA, uma vez que é a técnica utilizada e regulamentada no país; o ELISA, a fim de aumentar a capacidade de detecção da resposta imune, por ser esta técnica mais sensível que a anterior (LIMA et al., 2013) e o Immunoblotting (IB) como técnica confirmatória, por apresentar melhor desempenho diagnóstico dentre as três (RODRIGUES et al., 2014).
55 53 Para tanto, foram produzidos antígenos a partir do cultivo secundário de membrana sinovial caprina, inoculados com cepa padrão CAEV-Cork (PINHEIRO et al., 2006; PINHEIRO et al., 2010). Para a IDGA foi utilizado antígeno ultrafiltrado (PINHEIRO et al., 2010). No ELISA, fez-se uso do antígeno obtido a partir de pellet de células tratado com dodecil sulfato de sódio (SDS), seguindo o método de Torres et al. (2009). Para o teste de IB, empregou-se o antígeno produzido a partir da ultracentrifugação em colchão de sacarose (PINHEIRO et al., 2006). Os testes de IDGA foram realizados em placas de Petri plásticas (90x15mm), contendo 13mL de gel de agarose a 1% em solução salina fosfatada (PBS). O gel foi perfurado com roseta metálica hexagonal, formando sete poços com capacidade para 25µL. No poço central foi colocado o antígeno e os poços periféricos foram preenchidos com soros testes e padrão positivo, de forma intercalada. As placas foram acondicionadas em câmara úmida, a 25ºC. Realizaram-se as leituras com 72 horas, sobre fonte de luz com fundo escuro, observando-se a formação de linhas de precipitação (PINHEIRO et al., 2010). O ELISA foi validado seguindo a metodologia descrita por Pinheiro et al. (2006) e Lima et al. (2013). Este teste foi conduzido em microplacas de polivinil de alta capacidade de adsorção, rígidas, com 96 poços, com antígeno na concentração de 0,86mg/mL. A sensibilização foi realizada com 0,5µg de antígeno por poço. Os soros foram diluídos na proporção 1:50 e testados em duplicata, e o conjugado utilizado foi o anti-igg ovino marcado com peroxidase na diluição 1: A leitura foi realizada em filtro de 490nm. Os resultados expressos obtidos em densidade óptica foram transformados em percentual do resultado médio de duas repetições com soro padrão positivo (percentual de positividade PP), variando de 0 a 100%. O ponto de corte de 25,35% foi estabelecido a partir de amostras negativas testadas por IDGA e IB (média dos PP mais três vezes o desvio padrão). Os testes de IB foram conduzidos de acordo com Pinheiro et al. (2011), com modificações. Uma vez que o extrato antigênico foi separado por eletroforese em gel de poliacrilamida (SDS-PAGE), realizou-se a transferência para membrana de nitrocelulose de forma passiva (CRUZ et al., 2003). Depois do bloqueio, a membrana foi dividida em tiras a serem incubadas com os soros testes e controles positivo e negativo, na diluição de 1:50. Foi utilizado o conjugado anti-igg ovino marcado com peroxidase na diluição de
56 54 1: Estabeleceram-se como positivos os soros cujas tiras apresentaram reação para o polipeptídeo com peso molecular próximo a 28kDa, com base no padrão de peso molecular de proteínas (OLIVEIRA et al., 2008; PINHEIRO et al., 2011; SARDI et al., 2012). RESULTADOS E DISCUSSÃO A transmissão do lentivírus caprino entre ovinos foi confirmada a partir da PCR nested em duas das crias expostas (Tabela 1). Este resultado comprovou a capacidade de replicação viral do LVC em ovinos, tornando viável a transmissão para outros ovinos. A discreta detecção de positividade do GE na npcr (2/10) pode ser justificada pela baixa adaptação da cepa viral aos ovinos, com discreta replicação viral, diminuindo a capacidade de detecção do seu material genético nos tecidos (BARQUERO et al., 2013). Quanto ao número de testes npcr positivos por animal, este resultado pode ser explicado pela intermitência viral no sangue, já identificado por outros autores em acompanhamentos de animais infectados (ALVAREZ et al., 2005; PAULA et al., 2009), o que não significa ausência de infecção. Tabela 1. Resultados dos testes de PCR nested no sangue, Immunoblotting, ELISA e Imunodifusão em gel de agarose no soro de matrizes e crias ovinas expostas e não expostas a lentivirose de origem caprina. (Continua) Grupo não exposto Grupo exposto Matrizes Testes npcr IB ELISA IDGA (-): Negativo; (+): Positivo. npcr: Reação em cadeia de polimerase nested; IB: Imunoblotting; ELISA: Ensaio imunoenzimático ligado a enzima; IDGA: Imunodifusão em gel de agarose. Tabela 1. Resultados dos testes de PCR nested no sangue, Immunoblotting, ELISA e Imunodifusão em gel de agarose no soro de matrizes e crias ovinas expostas e não expostas a lentivirose de origem caprina. (Continuação) Grupo não exposto Grupo exposto
57 55 Momento Teste dias npcr IB ELISA IDGA dias npcr IB ELISA IDGA dias npcr IB ELISA IDGA dias npcr IB ELISA IDGA dias npcr IB ELISA IDGA dias npcr IB ELISA IDGA dias npcr IB ELISA IDGA dias npcr IB ELISA IDGA dias npcr IB ELISA IDGA dias npcr IB ELISA IDGA dias npcr IB ELISA IDGA dias npcr IB ELISA IDGA dias npcr IB ELISA IDGA (-): Negativo; (+): Positivo. npcr: Reação em cadeia de polimerase nested; IB: Imunoblotting; ELISA: Ensaio imunoenzimático ligado a enzima; IDGA: Imunodifusão em gel de agarose. O comportamento do vírus no ambiente intracelular é variável, podendo este ficar em um estado denominado de quiescência, quando o DNA proviral, mesmo que integrado ao DNA celular, não seja ativado, portanto não realizando a multiplicação
58 56 viral, ou ainda dentro da célula, sem se integrar (CAVALCANTE et al., 2013; BLACKLAWS, 2012; CRUZ et al., 2013). Quanto aos testes realizados no GN, todos foram negativos, comprovando não ter havido outra fonte de infecção, além das matrizes positivas mantidas no grupo exposto. Todos os animais acompanhados no experimento não manifestaram sintomatologia clínica condizente com a enfermidade (RADOSTITS et al., 2002). Esta ausência de sinais da infecção em animais comprovadamente infectados pelos lentivírus foi observada em outros estudos (BRITO, 2009; CAVALCANTE et al., 2013; SOUZA et al., 2015), o que neste caso pode estar correlacionado em parte com a modificação da espécie para a qual a cepa viral estava adaptada, uma vez que o mesmo foi originalmente veiculado a ovinos pelo colostro e leite caprino, e foi capaz de causar sintomatologia clínica nos caprinos (RACHID et al., 2013). Em relação aos testes imunodiagnósticos, apenas um indivíduo (73) foi positivo no IB, no primeiro mês de vida, entretanto este resultado foi associado a transferência de imunoglobulinas maternas, uma vez que os anticorpos oriundos da imunidade passiva para LVPR podem ser detectados por IB, no soro sanguíneo, até os 70 dias de idade, e por Elisa e IDGA até os 50 dias (SOUZA et al., 2014). O resultado positivo no Elisa aos 300 dias foi atribuído a reação inespecífica, contituindo um falso positivo, uma vez que não foi observada positividade no teste de IB, e este ser o teste mais próximo do real status sorológico do animal (LIMA et al., 2013). A capacidade de detecção destes testes está diretamente relacionada ao nível de replicação viral que consiga gerar uma resposta imune humoral (TORRES et al., 2009). Esta limitação diagnóstica pode ser diminuída por combinação de diferentes métodos (BARQUERO et al., 2013), entretanto como visto neste experimento, a intermitência viral e sorológica precisam ser consideradas (RAVAZZOLO et al., 2006; RACHID et al., 2013). As amostras que obtiveram resultados positivos na npcr foram purificadas e sequenciadas, a fim de se realizar a comparação com as cepas originais de caprinos (Figura 1). Na observação das sequências obtidas, foi possível verificar uma diferença de 2% da sequência do cordeiro 52, com relação à cepa padrão CAEV Cork, o que indica uma variação em ovinos. Esta alteração pode ser por mutação (BARQUERO et al., 2013),
59 57 entretanto, são necessários estudos mais minuciosos para esta afirmação, principalmente porque o ovino 54 apresentou homologia de 100% com o CAEV Cork. Quanto a similaridade com a cepa MVV K1514, a cria 52 apresentou 89% de homologia, e a cria 54, 90%. Figura 1. Sequências parciais do gene gag de lentivírus de pequenos ruminantes: resultados obtidos da PCR nested em ovinos infectados com lentivirus caprino *Seta vermelha indica troca de nucleotídeo em relação a sequencia genômica da cepa padrão Caev Cork. Estes dados demonstraram que a transmissão e disseminação dos lentivírus são mais complexas do que a hipótese de serem espécie-específicos (GERMAIN e VALAS, 2006; REINA et al., 2006). Inclusive, a ocorrência das quasispecies está intimamente ligada aos mecanismos de evasão da resposta imune, principalmente a erros relacionados à transcrição do RNA viral pela transcriptase reversa (PASICK et al., 1998; BLACKLAWS, 2012). Entretanto, este fato não contradiz a questão de algumas cepas serem mais adaptadas a caprinos e outras a ovinos, e que a interação nestas espécies ocorre de forma diferente (SHAH e tal., 2004; RACHID et al., 2013). CONCLUSÕES
60 58 Foi confirmada a transmissão do lentivírus caprino entre ovinos. Este resultado se traduz no impacto epidemiológico da viabilidade e a transmissão interespécies, uma vez que o vírus foi repassado entre ovinos, apesar de não ter sido possível evidenciar a via de transmissão, se vertical a partir da mamada do leite e colostro ou intrauterina, ou horizontal, pelo contato com outras secreções entre matrizes e crias. Apesar disso, as crias infectadas durante um ano não demonstraram sintomatologia clínica. AGRADECIMENTOS A Fundação de Amparo à Pesquisa do Estado da Bahia (Fapesb) pelo fomento ao projeto, ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq) pelo financiamento à pesquisa. À Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (Capes) pela concessão da bolsa de estudos e a Embrapa Caprinos e Ovinos pelo apoio à execução do experimento. REFERÊNCIAS ÁLVAREZ, V.; ARRANZ, J.; DALTABUIT-TEST, M.; LEGINAGOIKOA, I.; JUSTE, R.A.; AMORENA, B.; DE ANDRÉS, D.; LUJÁN, L.L.; BADIOLA, J.J.; BERRIATUA, E. Relative contribution of colostrum from Maedi-Visna virus (MVV) infected ewes to MVV-seroprevalence in lambs. Research in Veterinary Science, v.78, n.3, p , ANDRIOLI, A.; GOUVEIA, A.M.G.; MARTINS, A.S.; PINHEIRO, R.R.; SANTOS, D.O. Fatores de risco na transmissão do lentivírus caprino pelo sêmen. Pesquisa Agropecuária Brasileira, v.41, n.8, p , BARLOUGH, J.; EAST, N.; ROWE, J.D.; HOOSEAR, K.V.; DEROCK, E.; BIGORNIA, L.; RIMSTAD, E. Double-nested polymerase chain reaction for detection of caprine arthritis-encephalitis virus proviral DNA in blood, milk, and tissues of infected goats. Journal of Virological Methods, v.50, n.1-3, p , BARQUERO, N.; GOMEZ-LUCIA, E.; ARJONA, A.; TOURAL, C.; LAS HERAS, A.; FERNÁNDEZ-GARAYZABAL, J.F.; DOMENECH, A. Evolution of specific
61 59 antibodies and proviral DNA in milk of small ruminants infected by small ruminant lentivirus. Viruses, v.5, n.10, p , BLACKLAWS, B.A.; BERRIATUA, E.; TORSTEINSDOTTIR, S.; WATT, N.J.; ANDRES, D.; KLEIN, D. HARKISS, G.D. Transmission of small ruminant lentiviruses. Veterinary Microbiology, v.101, p , BLACKLAWS, B.A. Small ruminant lentiviruses: Immunopathogenesis of visna-maedi and caprine arthritis and encephalitis virus. Comparative Immunology, Microbiology and Infectious Diseases, v.35, n.3, p , BRITO, R.L.L. Implicações da artrite-encefalite caprina na reprodução, produção e na qualidade do leite de cabras. Sobral, CE: UEVA Centro de Ciências Agrárias e Biológicas. 2009, 109p. Dissertação (Mestrado). CAVALCANTE, F.R.A.; ANDRIOLI, A.; PINHEIRO, R.R.; SOUZA, K.C.; VERAS, A.K.A.; LOPES, T.A.; SOUSA, S.D.; SILVA, P.A.F. Detecção do vírus da Artrite Encefalite Caprina por nested PCR e nested RT-PCR em ovócitos e fluido uterino. Arquivos do Instituto Biológico, v.80, n.4, p , CRUZ, E.T.; GONZÁLEZ, R.H.; RODRÍGUEZ, A.M.; ÁLVAREZ, H.R.; ORTEGA, M.E.T.; SCHMID, R.K.; SETIÉN, A.A. Detección de anticuerpos contra artritis encefalitis caprina (AEC) mediante inmunoelectrotransferencia. Veterinária México, v.34, n.2, p , CRUZ, J.C.M.; SINGH, D,K,; LAMARA, A.; CHEBLOUNE, Y. Small Ruminant Lentiviruses (SRLVs) Break the Species Barrier to Acquire New Host Range. Viruses, v. 5, p , FEITOSA, A.L.V.L.; TEIXEIRA, M.F.S.; PINHEIRO, R.R.; PINHEIRO, A.A.; AZEVEDO, D.A.A.; ALVES, S.M. Primeiro isolamento de lentivírus de pequenos ruminantes em caprino naturalmente infectado em rebanho do Rio Grande do Norte, Brasil. Arquivos do Instituto Biológico, v.78, n.4, p , GERMAIN, K.; VALAS, S. Distribution and heterogeneity of small ruminant lentivirus envelope subtypes in naturally infected sheep. Virus Research, v. 120, n.1-2, p , 2006.
62 60 GRIMBERG, J.; NOWOSCHIK, S.; BELLUSCIO, L.; MCKEE, R.; TURCK, A.; EISENBERG, A. A simple and efficient non-organic procedure for the isolation of genomic DNA from blood. Nucleic Acids Research, v.17, n.20, p.83-90, HALL, T.A. Bioedit: a user-friendly biological sequence alignment editor and analysis program for Windows 95/98/NT. Nucleic Acids Symposium Series, v.41, p.95-98, LIMA, C.C.V.; COSTA, J.N.; SOUZA, T.S.; MARTINEZ, P.M.; COSTA NETO, A.O.; AZEVEDO, D.A.A.; PINHEIRO, R.R.; BRITO, R.L.L. Imunodiagnóstico para a artrite-encefalite caprina em rebanhos do semiárido baiano, Brasil. Revista Brasileira de Medicina Veterinária, v.35, n.4, p , OLIVEIRA, M.M.M.; MELO, M.A.; ANDRADE, P.P.; GOMES, S.M.; CAMPOS, A.C.; NASCIMENTO, S.A.; CASTRO, R.S. Western Blot para o diagnóstico das infecções pelos lentivírus de pequenos ruminantes em caprinos: um método simples para a produção de antígeno. Arquivos do Instituto Biológico, v.75, n.3, p , PASICK, J. Maedi-Visna Virus and Caprine Arthritis-Encephalitis Virus: Distinct species or quasispecies and its implications for laboratory diagnosis. Canadian Journal of Veterinary Research, n.62, p , PAULA, N.R.O.; ANDRIOLI, A.; CARDOSO, J.F.S.; PINHEIRO, R.R.; SOUSA, F.M.L.; SOUZA, K.C.; ALVES, F.S.F.; CAMPELLO, C.C.; RICARTE, A.R.F.; TEIXEIRA, M.F.S. Profile of the Caprine arthritis-encephalitis virus (CAEV) in blood, semen from bucks naturally and experimentally infected in the semi-arid region of Brazil. Small Ruminant Research, v.85, n.1, p.27-33, PINHEIRO, R.R.; OLORTEGUI, C.D.C.; GOUVEIA, A.M.G.; ARAÚJO, S.C.; ANDRIOLI, A. Desenvolvimento de dot-blot para detecção de anticorpos para o vírus da artrite-encefalite caprina em caprinos. Revista Portuguesa de Ciências Veterinárias, v.101, n , p.51-56, PINHEIRO, R.R.; ANDRIOLI, A.; GOUVEIA, A.M.G.; ARAGÃO, M.A.C.; MARTINEZ, P.M. Avaliação de antígenos para o diagnóstico de lentivírus em rebanho
63 61 caprino sob programa de controle. Arquivos do Instituto Biológico, v.77, n.1, p , PINHEIRO, R.R.; BRITO, R.L.L.; RODRIGUES, A.S.; DIAS, R.P.; ANDRIOLI, A.; GOUVEIA, A.M.G. Protocolo de immunoblotting para diagnóstico da artrite-encefalite caprina. Comunicado Técnico 122. Sobral: Embrapa Caprinos e Ovinos, p. PREZIUSO, S.; RENZONI, G.; ALLEN, T. E.; TACCINI, E.; ROSSI, G.; DEMARTINI, J. C.; BRACA, G. Colostral transmission of Maedi-visna virus: sites of viral entry in lambs born from experimentally infected ewes. Veterinary Microbiology, v. 104, n.3-4, p , RACHID, A.; CROISÉ, B.; RUSSO, P.; VIGNONI, M.; LACERENZA, D.; ROSATI, S.; KUZMAK, J.; VALAS, S. Diverse host-virus interactions following caprine arthritis-encephalitis virus infection in sheep and goats. Journal of General Virology, v.94, n.3, p , RADOSTITS, O. H.; GAT, C. C.; BLOOD, D. C.; HINCHCLIFF; K.W. Pneumonia Progressiva Ovina (Maedi, Maedi-Visna). In: Clínica Veterinária: Um tratado de doenças dos bovinos, ovinos, suínos, caprinos e equinos. Rio de Janeiro: Guanabara Koogan. 9.ed p RAVAZZOLO, A.P.; NENCI, C.; VOGT, H.R.; WALDVOGEL, A.; OBEXER-RUFF, G.; PETERHANS, E.; BERTONI, G. Viral load, organ distribution, histopathological lesions and cytokine mrna expression in goats infected with a molecular clone of the caprine arthritis encephalitis virus. Virology, v. 350, n.1, p , REINA, R.; MORA, M.I.; GLARIA, I.; GARCÍA, I.; SOLANO, C.; LUJÁN, L.; BADIOLA, J.J.; CONTRERAS, A.; BERRIATUA, E.; JUSTE, R.; MAMOUN, R.Z.; ROLLAND, M.; AMORENA, B.; DE ANDRÉS, D. Molecular characterization and phylogenetic study of Maedi Visna and Caprine Arthritis Encephalitis viral sequences in sheep and goats from Spain. Virus Research, v.121, n.2, p , RIMSTAD, E.; EAST, N.E.; TORTEN, M.; HIGGINS, J.; DEROCK, E.; PEDERSEN, N.C. Delayed seroconversion following naturally acquired caprine arthritis-encephalitis virus infection in goats. American Journal of Veterinary Research, v.54, n.11, p , 1993.
64 62 RODRIGUES, A.S.; BRITO, R.L.L.; PINHEIRO, R.R.; DIAS, R.P.; ALVES, S.M.; SOUZA, T.S.; SOUZA, K.C.; AZEVEDO, D.A.A.; ANDRIOLI, A.; MAGALHÃES, D.C.T.; TEIXEIRA, M.F.S. Padronização do ELISA indireto e Western Blot para o diagnóstico da artrite-encefalite caprina. Arquivo Brasileiro de Medicina Veterinária e Zootecnia, v.66, n.2, p , SALTARELLI, M.; QUERAT, G.; KONINGS, D.A.M.; VIGNE, R.; CLEMENTS, J.E. Nucleotide sequence and transcriptional analysis of molecular clones of CAEV which generate infectious virus. Virology, v.179, n.1, p , SARDI, S.I.; TORRES, J.A.; BRANDÃO, C.F.L.; TIGRE, D.M.; CAMPOS, G.S. Early detection of goats infected with lentivirus small ruminant virus by ELISA assay. Revista de Ciências Médicas e Biológicas, v.11, n.1, p.35-40, SHAH, C.A.; BÖNI, J.; HUDER, J.B.; VOGT, H.R.; MÜHLLHER, J.; ZANONI, R.; MISEREZ, R.; LUTZ, H.; SCHÜPBACH, J. Phylogenetic analysis and reclassification of caprine and ovine lentiviruses based on 104 new isolates: evidence for regular sheepto-goat transmission and world-wide propagation through livestock trade. Virology, v.319, n.1, p.12-26, SOUZA, T.S.; COSTA, J.N.; PINHEIRO, R.R.; LIMA, C.C.V.; MELO, F.C.C.; ANDRIOLI, A.; AZEVEDO, D.A.A.; SANTOS, V.W.S.; OLIVEIRA, E.L.; COSTA NETO, A.O. Duração da imunidade passiva para lentivírus de pequenos ruminantes em cordeiros. Semina: Ciências Agrárias, Londrina, v. 35, n. 2, p , SOUZA, T.S.; PINHEIRO, R.R.; COSTA, J.N.; LIMA, C.C.V.; ANDRIOLI, A.; AZEVEDO, D.A.A.; SANTOS, V.W.S.; ARAUJO, J.F.; SOUSA, A.L.M.; PINHEIRO, D.N.S.; FERNANDES, F.M.C.; COSTA NETO, A.O. Interspecific transmission of small ruminant lentiviruses from goats to sheep. Brazilian Journal of Microbiology, Ahead of print. THOMPSON, J.D.; HIGGINS, D.G.; GIBSON, T.J. Clustal W: improving the sensitivity of progressive multiple sequence alignment through sequence weighting, position specific gap penalties and weight matrix choice. Nucleic Acids Research, v.22, n.22, p , 1994.
65 63 TORRES, J.A.; CAMPOS, G.S.; FREITAS, M.M.; BRANDÃO, C.F.L.; SARDI, S.I. Produção de antígeno viral para o diagnóstico da artrite-encefalite caprina utilizando um teste imunoenzimático (ELISA). Revista de Ciências Médicas e Biológicas, v.8, n.2, p , VILLORIA, M.; LEGINAGOIKOA, I.; LUJÁN, L.; PÉREZ, M.; SALAZAR, E.; BERRIATUA, E.; JUSTE, R.A.; MINGUIJÓN, E. Detection of Small Ruminant Lentivirus in environmental samples of air and water. Small Ruminant Research, v.110, n.2-3, p , 2013.
66 64 CAPÍTULO 3 Avaliação clínica de ovinos infectados com lentivírus caprino
67 65 Avaliação clínica de ovinos infectados com lentivírus caprino RESUMO Com o objetivo de realizar a avaliação clínica de ovinos experimentalmente infectados com o lentivírus caprino (LVC), foram acompanhadas ovelhas desde o nascimento até 720 dias de vida. As ovelhas foram distribuídas em dois grupos experimentais: grupo infectado - GI (seis ovelhas experimentalmente infectadas com LVC) e grupo controle - GC (cinco ovelhas negativas para LVC). Para tal, os animais foram continuamente avaliados clinicamente com o objetivo de se observar alterações causadas pela enfermidade. Incluiu-se também avaliações laboratoriais de bioquímica clínica: parâmetros do perfil proteico (Proteína Sérica Total PST, Albumina ALB, Globulina GLOB, Ureia e Creatinina - CREAT), do perfil energético (Glicose GLIC, Colesterol COLES, Triglicérides - TRIG) e de enzimas de avaliadores do metabolismo hepático (Gamaglutamiltransferase GGT e Aspartatoaminotransferase - AST). Foram realizadas 22 coletas durante o período de dois anos de experimento: do nascimento aos 720 dias de idade. Durante todo o período experimental, nenhum animal do GI manifestou qualquer alteração clínica compatível com a enfermidade. Os resultados das análises bioquímicas demonstraram diferença (p<0,05) nas concentrações de PST entre os grupos no primeiro ano de experimento, onde o GI apresentou valores superiores (p>0,05) ao GC. Esta diferença foi atribuída à superioridade de concentrações das globulinas no GI. Não houve diferenças uniformes ao longo do tempo, quanto as médias de albumina, ureia, creatinina, glicose, colesterol e triglicérides. Quanto às avaliações das atividades enzimáticas, os animais do GI apresentaram valores de GGT inferiores ao GC, dos 150 aos 330 dias de vida, entretanto sem haver diferença nos valores de AST, diminuindo a possibilidade de efeito no metabolismo hepático. Conclui-se, portanto, que a infecção experimental por LVC em ovinos não causou alteração clínica manifesta como também metabólica nos parâmetros bioquímicos analisados nesses ovinos. Palavras-chave: Sintomatologia, transmissão interespécies, bioquímica sérica.
68 66 Clinical evaluation of sheep infected with caprine lentivirus ABSTRACT In order to accomplish the clinical evaluation of sheep infected with caprine lentivirus (LVC), sheep were followed from birth to 720 days of life. The sheep were divided into two groups: infected group - GI (six sheep experimentally infected with LVC) and control group - CG (five sheep negative for LVC). To this end, the animals were evaluated clinically seeking to changes caused by the disease, and they had their biochemical measurement values performed on the protein profile (Total Serum Protein - PST, Albumin - ALB, Globulin - GLOB, Urea and Creatinine - CREAT), energy profile (Glucose - GLIC, Cholesterol COLES, Triglycerides - TRIG) and liver enzyme evaluation (Gamma Glutamyl Transferase - GGT and Aspartate Aminotransferase - AST). Twenty two samples were taken during the two years of evaluation, from birth to 720 days old. Throughout the experiment period, no animal of GI showed any clinical alteration consistent with the disease. The results of the biochemical analysis showed differences (p<0.05) in PST concentrations between the first year of experiment groups with GI presenting higher values (p>0.05) than GC. This difference was attributed to the superiority of the globulin values in GI. There were no differences in the continuous medium of albumin, urea, creatinine, glucose, cholesterol and triglycerides. As enzymatic assessments, the GI animals showed lower values to GC, from 150 to 330 days of life, but with no difference in AST values, reducing the possibility of effect on hepatic metabolism. It follows, therefore, that the LVC infection in sheep no caused physical manifestation and metabolic changes or biochemical parameters analyzed in sheep. Keywords: Clinical signs, cross-infection, biochemistry serum
69 67 INTRODUÇÃO A ovinocultura tem papel fundamental na pecuária nacional, apresentando um crescimento significativo nas últimas décadas. Entretanto, frente a este melhoramento, ocorre a disseminação de enfermidades outrora não descritas. Dentre estas, destaca-se a lentivirose de pequenos ruminantes, que é responsável por prejuízos diretos e indiretos nas criações em todo o mundo (BLACKLAWS, 2012; SOUZA et al., 2012). As lentiviroses de pequenos ruminantes são enfermidades provocadas pelos Retrovirus do gênero Lentivirus, que são quasispécies virais únicas que têm a capacidade de infectar tanto ovinos quanto caprinos (SHAH et al., 2004). Sugere-se que as principais vias de transmissão ocorrem pela ingestão de colostro, leite ou água contaminados e também pela inalação de secreções respiratórias. Esta transmissão pode ocorrer verticalmente entre a matriz e suas crias, como pelo contato direto entre os animais, de forma horizontal (BLACKLAWS et al., 2004; VILLORIA et al., 2013). Por características do próprio agente etiológico, a enfermidade apresenta curso crônico e progressivo, com alterações importantes, como a artrite, a encefalite, a mastite e a pneumonia progressiva (LARA et al., 2005; BARQUERO et al., 2013), além de linfadenopatias e emagrecimento progressivo, de forma isolada ou simultânea (COSTA et al., 2007). Entretanto, este emagrecimento observado em animais infectados ainda não tem o seu mecanismo esclarecido, apesar de ser atribuído à deficiência alimentar. Todavia, estudos realizados em caprinos identificaram influência da infecção no metabolismo orgânico, caracterizado por menores concentrações séricas de albumina, creatinina, ureia e glicose observadas em animais infectados (DIAS, 2011). As alterações clínicas são relacionadas à infiltração inflamatória crônica nos tecidos, e à persistente estimulação antigênica, podendo formar núcleos de agregação celular, principalmente com linfócitos, plasmócitos e macrófagos, na glândula mamária, nos pulmões, nas articulações e até no sistema nervoso central, neste mais frequente em animais jovens. Outros órgãos podem também ser acometidos como os rins, o fígado e o coração (PASICK, 1998; ANGELOPOULOU et al., 2006; BRELLOU et al., 2007; BENAVIDES et al., 2013). Contudo, a heterogeneidade das cepas virais pode determinar a manifestação clínica, tratando-se de cepas mais virulentas e mais adaptadas à espécie (BENAVIDES et al., 2013).
70 68 Em virtude de serem escassas as informações relacionadas à influência do lentivírus no metabolismo de ovinos, este trabalho objetiva avaliar clinicamente ovinos infectados com o lentivírus originalmente de caprinos. MATERIAL E MÉTODOS O experimento foi realizado no Centro Nacional de Pesquisa de Caprinos e Ovinos da Empresa Brasileira de Pesquisa Agropecuária (Embrapa Caprinos e Ovinos), no município de Sobral (CE), sob aprovação do Comitê de Ética no Uso de Animais da Universidade Estadual do Vale do Acaraú (número 001/2012). Foram utilizadas onze ovelhas mestiças de Santa Inês com Morada Nova, criadas intesivamente em baias experimentais, divididas em dois grupos experimentais: Grupo Infectado (GI), constituído por seis ovelhas que foram infectadas com lentivírus caprino (LVC) a partir da mamada de colostro caprino, e Grupo Controle (GC), formado por cinco ovelhas de mesmo padrão racial e idade, negativas para lentivirus de pequenos ruminantes, mantida nas mesmas condições experimentais que o GI. Ressalta-se que os dois grupos experimentais foram acompanhados quanto a sua condição de infecção pelos testes de Reação em Cadeia de Polimerase do tipo nested (npcr) e Immunoblotting (IB). Todos os animais foram monitorados de forma constante e examinados clinicamente quanto à presença de sinais clínicos associados a lentivirose de pequenos ruminantes e outras enfermidades que pudessem comprometer a sanidade dos mesmos. Estabeleceram-se 22 momentos de coleta de sangue para realização das análises bioquímicas, IB e npcr,as quais foram realizadas nos seguintes períodos: 0 ( logo após o nascimento e antes da mamada do colostro), 1, 7, 15, 30, 50, 70, 90, 120, 150, 180, 210, 240, 270, 300, 330, 390, 480, 520, 570, 630, 720 dias de vida. As amostras de sangue foram obtidas por venopunção da jugular após limpeza e antissepsia, utilizando sistema a vácuo, colhendo-se 10mL de sangue em tubos contendo ácido etilenodiaminotetracético (EDTA), para obtenção da papa de leucócitos, necessária para extração de DNA e teste de npcr; e 5mL sem anticoagulante, para serem centrifugados (3.000G) a fim de se obter o soro, acondicionado a -20 C, para realização das análises bioquímicas e IB.
71 69 O desmame dos animais de ambos os grupos foi realizado aos 90 dias de vida, os quais continuaram mantidos em baias separadas durante todo o experimento, até os 720 dias de vida, sob o mesmo manejo nutricional e sanitário. Os grupos foram avaliados clinicamente e monitorados por IB e npcr, bem como foram realizadas dosagens dos constituintes do perfil proteico (Proteína Sérica Total - PST, Albumina - ALB, Globulinas - GLOB, Ureia e Creatinina - CREAT), do perfil energético (Glicose - GLIC, Colesterol - COLES e Triglicérides - TRIG) e da atividade de enzimas avaliadoras do metabolismo hepático (aspartato aminotransferase - AST e ɤ glutamiltransferase - GGT). As amostras obtidas com anticoagulante foram centrifugadas e tratadas com cloreto de amônio para obtenção da papa de leucócitos (FEITOSA et al., 2011), a qual foi submetida a protocolo de extração de DNA (GRIMBERG et al., 1989), que então foi utilizada na npcr. A metodologia utilizada para npcr foi realizada seguindo Barlough et al. (1994) modificada po Andrioli et al. (2006). Utilizaram-se dois pares de oligonucleotídeos iniciadores, obtidos a partir de sequência da região do gene gag, da amostra de cepa padrão CAEV-Cork (SALTARELLI et al., 1990), sendo os iniciadores P1 (5 - CAAGCAGCAGGAGGGAG AAGCTG-3 ) e P2 (5 - TCCTACCCCCATAATTTGATCCAC-3 ) usados para obter um sequência alvo de 297pb. Após, se fez uso dos iniciadores P3 (5 -GTTCCAGC AACTGCAAACAGTAGCAATG-3 ) e P4 (5 ACCTTTCTGCTTCTTCATTTAATTT CCC-3 ) na segunda amplificação, objetivando o fragmento-alvo de 187pb (RIMSTAD et al., 1993). As reações de amplificação foram realizadas em termociclador (Programmable Thermal Controller, PTC-100, MJ Research, Inc.), constituindo um ciclo inicial de 94 C por cinco minutos; seguidos de 35 ciclos: 94 C - 1 minuto, 56 C - 1 minuto, 72 C - 45 segundos; com extensão final a 72 C por sete minutos. As amostras amplificadas e os controles positivo e negativo, juntamente com o marcador molecular, foram submetidos à eletroforese em gel de agarose a 2% em TBE (Tris, borato e EDTA 0,1X), coradas com brometo de etídio e visualizadas em transluminador de luz ultravioleta (ANDRIOLI et al., 2006).
72 70 As amostras de soro foram utilizadas nas dosagens bioquímicas e no teste imunológico de IB. Para tal, foi produzido antígeno a partir do cultivo secundário de membrana sinovial caprina, inoculado com cepa padrão CAEV-Cork, empregando-se a técnica de produção a partir da ultracentrifugação em colchão de sacarose (PINHEIRO et al., 2006; PINHEIRO et al., 2010). Os testes de IB foram conduzidos de acordo com Pinheiro et al. (2011) modificado por Rodrigues et al. (2014). Uma vez separando as proteinas antigênicas por eletroforese em gel de poliacrilamida (SDS-PAGE), ocorreu a transferência para membrana de nitrocelulose de forma passiva (CRUZ et al., 2003). As diluições utilizadas para soro e conjugado foram de 1:50 e 1:15.000, respectivamente. O teste foi considerado positivo quando ocorreu reação ao polipeptídeo com peso molecular aproximado de 28kDa, utilizando como controle as tiras de soros positivo e negativo, bem como o padrão de peso molecular de proteínas (OLIVEIRA et al., 2008; SARDI et al., 2012). As análises bioquímicas foram realizadas utilizando-se kits comerciais de acordo com a metodologia descrita pelo fabricante (Doles ). As determinações da proteína sérica total e da albumina foram realizadas por metodologias colorimétricas; a ureia, glicose, colesterol e triglicérides por metodos enzimáticos; e a creatinina, aspartato aminotransferase e gamaglutamiltransferase por metodos cinéticos. As concentrações séricas de ureia foram determinadas em analisadores bioquímico semi-automático Bioplus 2000 (Bioplus ) e os demais parâmetros senguíneos no sistema automatizado de bioquímica SBA 200 (Celm ). Os valores da concentração de globulina foram obtidos a partir da diferença entre a concentração da proteína sérica total e a albumina (SILVA et al., 2007). Os valores dos metabólitos obtidos nas determinações bioquímicas foram submetidos à análise estatística pela prova de Mann-Whitney, a fim de verificar diferenças entre as médias dos grupos infectado e controle, dentro de um mesmo momento avaliado. Para identificar diferenças entre as maiores e menores médias de cada grupo em cada fase, foi utilizada a prova estatística de Wilcoxon. Para todas as análises, foram considerados 95% de nível de confiança (p<0,05). RESULTADOS E DISCUSSÃO
73 71 Durante a realização do experimento nenhum dos animais apresentou sintomatologia clínica, e esta observação encontra-se de acordo com o carater lento e crônico da enfermidade (BLACKLAWS, 2012; BARQUERO et al., 2013). Os animais do grupo controle (GC) mantiveram-se negativos em todos os momentos avaliados, tanto pelo npcr quanto pelo IB. Em relação ao GI, todos os animais expostos ao LVC foram positivos na npcr (Tabela 1), confirmando a infecção dos animais. A positividade na npcr não se manteve constante e pode estar relacionada à própria patogenia do vírus, que apresenta oscilação na viremia, denominada de intermitência viral (CAVALCANTE et al., 2013; SOUZA et al., 2015). Essa oscilação na presença do DNA proviral no sangue circulante já foi descrita em outros estudos, e é associada a variação na replicação viral (ALVAREZ et al., 2005; BLACKLAWS, 2012). A presença de anticorpos nos momentos iniciais (desde as 24 horas até os 70 dias de vida) está associada à tranferência de imunidade passiva, uma vez que o grupo infectado recebeu pool de colostro de cabras infectadas que estavam respondendo a infecção, ou seja, com uma carga elevada de imunoglobulinas especificas para lentivírus (SOUZA et al., 2014). Entretanto, a presença de anticorpos no colostro não é capaz de neutralizar o vírus, podendo inclusive facilitar a penetração deste na célula, por facilitar a ligação entre a partícula viral e as células alvo, a partir de receptores específicos para a linha monocitária, aumentando assim a taxa de infecção (BLACKLAWS et al., 2012). Os resultados da média dos valores das dosagens bioquímicas realizadas, para ambos os grupos GI e GC, estão apresentados nas figuras que se seguem: Figura 1 - proteina sérica total PST, albumina ALB e globulina GLOB; Figura 2 - ureia; Figura 3- creatinina; Figura 4 - glicose (GLIC), colesterol (COLES) e triglicerides (TRIG); e Figura 5 - enzimas de avaliação hepática AST e GGT. A partir da avaliação da dinâmica de PST é possível verificar que os dois grupos apresentaram variações importantes do período do nascimento às 24 horas de vida. Isto se deve, principalmente, pela elevação dos valores de globulina, em consequência da substancial absorção de imunoglobulinas do colostro (SILVA et al., 2007; SILVA et al., 2010; ELOY et al., 2013). Contudo, nota-se que desde o 1 dia até os 330 dias do estudo, o GI apresentou valores de PST superiores (p<0,05). Inicialmente, esta dinâmica pode ser
74 72 justificada pela diferença de qualidade dos colostros ingeridos, entretanto, por este comportamento ser duradouro, pode ser associado ao status de infecção do GI. Tabela 1 Resultados dos testes immunoblotting (IB) e PCR nested (npcr) de cordeiros infectados pelo lentivírus caprino, a partir da ingestão de colostro de cabras positivas, realizados do nascimentos aos 720 dias de idade. Momentos (em dias)* Testes Animais IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr IB npcr (-) negativo; (+) positivo *Momentos a partir do nascimento. Observa-se, ainda, que desde a ingestão do colostro, os menores valores de PST foram registrados aos 50 dias, que válida a transfereância de imunidade passiva, por estar de acordo com o catabolismo das globulinas adquiridas passivamente via colostro e início
75 73 da síntese endógena, uma vez que as médias dos valores de albumina não apresentam diferença significativa entre eles (SILVA et al., 2010). Entretanto, apesar do acréscimo nos niveis de PST e GLOB em ambos os grupos a partir dos 70 dias, nota-se no GI um novo declinio, aos 150 dias de vida, sem alteração dos valores de albumina, portanto podendo tratar-se do início de uma resposta efetiva do organismo a agentes patogênicos, estando vinculado ao aumento de proteínas de fase aguda, globulinas ou proteinas do sistema complemento, que se justifica com o status da infecção no grupo, inclusive com retorno da positividade na npcr. É possível ainda perceber que a partir dos 390 dias, os grupos experimentais deixam de apresentar diferenças (p<0,05) entre os valores de PST, o que ressalta a ausência de correlação direta entre a infecção por LVC e o metabolismo proteico neste período, apesar de estudos com caprinos e felinos infectados com lentivírus apontarem para uma diminuição nos valores médios de albumina frente a animais sadios, atribuido a um menor metabolismo hepático em processos inflamatórios (RODRIGUES et al., 2007; DIAS, 2011), entretanto este comportamento só foi observado aos 720 dias. Esta diferença de dinâmica nos metabolitos proteicos frente ao observado em outros estudos pode estar associada a ausência de soroconversão maciça observada nos outros estudos, o que possivelmente altera a influência metabólica causada pelo LVPR, uma vez que algumas das lesões causadas pelo vírus devem-se à resposta imunológica frente à infecção. Quanto aos valores obtidos das médias de ureia e de creatinina, foram observadas apenas diferenças (p<0,05) pontuais, portanto não podem ser associadas a infecção entre os grupos experimentais. Entretanto, Dias (2001) verificou diminuição nos valores médios de ureia e creatinina em cabras adultas soropositivas para LVPR na realização da sua pesquisa.
76 Figura 1 Média dos valores obtidos nas dosagens séricas de proteína sérica total PST, albumina ALB e globulina GLOB, em cordeiros infectados com lentivírus caprino (GI) e cordeiros do grupo controle (GC), do nascimento aos 720 dias de vida. 74
Retrovírus Felinos. Fernando Finoketti
 Retrovírus Felinos Fernando Finoketti Porto Alegre, Rio Grande do Sul, Brasil Maio de 2014 Retrovírus - Características Capsídeo icosaédrico. Possuem envelope. Genoma composto de duas moléculas idênticas
Retrovírus Felinos Fernando Finoketti Porto Alegre, Rio Grande do Sul, Brasil Maio de 2014 Retrovírus - Características Capsídeo icosaédrico. Possuem envelope. Genoma composto de duas moléculas idênticas
UNIVERSIDADE FEDERAL DA BAHIA DOUTORADO EM CIÊNCIA ANIMAL NOS TRÓPICOS
 UNIVERSIDADE FEDERAL DA BAHIA DOUTORADO EM CIÊNCIA ANIMAL NOS TRÓPICOS TRANSMISSÃO INTERESPÉCIES DE LENTIVÍRUS DE CAPRINOS PARA OVINOS THIAGO SAMPAIO DE SOUZA SALVADOR - BAHIA AGOSTO - 2014 ii THIAGO SAMPAIO
UNIVERSIDADE FEDERAL DA BAHIA DOUTORADO EM CIÊNCIA ANIMAL NOS TRÓPICOS TRANSMISSÃO INTERESPÉCIES DE LENTIVÍRUS DE CAPRINOS PARA OVINOS THIAGO SAMPAIO DE SOUZA SALVADOR - BAHIA AGOSTO - 2014 ii THIAGO SAMPAIO
SOROPREVALÊNCIA DE MAEDI-VISNA EM OVINOS DA RAÇA SANTA INÊS NOS MUNICÍPIOS DA GRANDE VITÓRIA ES ABSTRACT
 SOROPREVALÊNCIA DE MAEDI-VISNA EM OVINOS DA RAÇA SANTA INÊS NOS MUNICÍPIOS DA GRANDE VITÓRIA ES Graziela Barioni 1, Lívia Volpe Pereira 2, Marcus Alexandre Vaillant Beltrame 3, Pauliana Tesoline 2 e Marcos
SOROPREVALÊNCIA DE MAEDI-VISNA EM OVINOS DA RAÇA SANTA INÊS NOS MUNICÍPIOS DA GRANDE VITÓRIA ES Graziela Barioni 1, Lívia Volpe Pereira 2, Marcus Alexandre Vaillant Beltrame 3, Pauliana Tesoline 2 e Marcos
Vírus da Imunodeficiência Humana
 Universidade Federal do Rio Grande do Sul Departamento de Microbiologia, Imunologia e Parasitologia Vírus da Imunodeficiência Humana Fabrício Campos Pós-doc Laboratório de Virologia Fonte: http://ultramedcampos.com.br/wp-content/uploads/2015/06/hiv.jpg
Universidade Federal do Rio Grande do Sul Departamento de Microbiologia, Imunologia e Parasitologia Vírus da Imunodeficiência Humana Fabrício Campos Pós-doc Laboratório de Virologia Fonte: http://ultramedcampos.com.br/wp-content/uploads/2015/06/hiv.jpg
Métodos de Pesquisa e Diagnóstico dos Vírus
 Métodos de Pesquisa e Diagnóstico dos Vírus Estratégias Isolamento em sistemas vivos Pesquisa de antígeno viral Pesquisa de anticorpos Pesquisa do ácido nucléico viral (DNA ou RNA) Pré requisitos para
Métodos de Pesquisa e Diagnóstico dos Vírus Estratégias Isolamento em sistemas vivos Pesquisa de antígeno viral Pesquisa de anticorpos Pesquisa do ácido nucléico viral (DNA ou RNA) Pré requisitos para
Efeito da CAE (Artrite-Encefalite Caprina) na saúde e produtividade de cabras leiteiras
 Efeito da CAE (Artrite-Encefalite Caprina) na saúde e produtividade de cabras leiteiras Roberto Soares Castro Prof. Dr. Universidade Federal Rural de Pernambuco Departamento de Medicina Veterinária - Área
Efeito da CAE (Artrite-Encefalite Caprina) na saúde e produtividade de cabras leiteiras Roberto Soares Castro Prof. Dr. Universidade Federal Rural de Pernambuco Departamento de Medicina Veterinária - Área
Avaliação da Massa Corporal e do Índice Articular Clínico em Caprinos portadores do Vírus da Artrite-Encefalite Caprina (CAEV)
 Avaliação da Massa Corporal e do Índice Articular Clínico em Caprinos portadores do Vírus da Artrite-Encefalite Caprina (CAEV) Darly Araujo de Abreu 1, Alice Andrioli 2, Roberta Lomonte Lemos de Brito
Avaliação da Massa Corporal e do Índice Articular Clínico em Caprinos portadores do Vírus da Artrite-Encefalite Caprina (CAEV) Darly Araujo de Abreu 1, Alice Andrioli 2, Roberta Lomonte Lemos de Brito
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS
 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS REBECA CAVALCANTE MARINHO ISOLAMENTO DO VÍRUS DA ARTRITE
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS REBECA CAVALCANTE MARINHO ISOLAMENTO DO VÍRUS DA ARTRITE
1/12/2008. HIV como modelo de estudo de retrovírus e patogênese. Retrovírus e oncogênese. Retrovírus e oncogênese.
 HIV como modelo de estudo de retrovírus e patogênese Retrovírus e oncogênese. Um pouco de história: 1904: Ellerman and Bang, procurando por bactérias como agentes infecciosos para leucemia em galinhas,
HIV como modelo de estudo de retrovírus e patogênese Retrovírus e oncogênese. Um pouco de história: 1904: Ellerman and Bang, procurando por bactérias como agentes infecciosos para leucemia em galinhas,
On line. Protocolos para Extração do DNA-proviral e PCR do Lentivírus Caprino em Sangue
 Comunicado Técnico On line 72 ISSN 1676-7675 Sobral, CE Dezembro, 2006 Protocolos para Extração do DNA-proviral e PCR do Lentivírus Caprino em Sangue Alice Andrioli 1 Kelma Costa de Souza 2 Raymundo Rizaldo
Comunicado Técnico On line 72 ISSN 1676-7675 Sobral, CE Dezembro, 2006 Protocolos para Extração do DNA-proviral e PCR do Lentivírus Caprino em Sangue Alice Andrioli 1 Kelma Costa de Souza 2 Raymundo Rizaldo
Anemia Infecciosa das Galinhas
 Anemia Infecciosa das Galinhas Leonardo Bozzi Miglino Programa de Pós-graduação - UFPR Mestrado Ciências Veterinárias 2010 Histórico: Isolado e descrito no Japão (1979), chamado de agente da anemia das
Anemia Infecciosa das Galinhas Leonardo Bozzi Miglino Programa de Pós-graduação - UFPR Mestrado Ciências Veterinárias 2010 Histórico: Isolado e descrito no Japão (1979), chamado de agente da anemia das
Hepatites. Inflamação do fígado. Alteração em enzimas hepáticas (alaminotransferase aspartatoaminotransferase e gamaglutamiltransferase ALT AST e GGT
 Hepatites Virais Hepatites Inflamação do fígado Alteração em enzimas hepáticas (alaminotransferase aspartatoaminotransferase e gamaglutamiltransferase ALT AST e GGT Sinais clínicos: Náuseas, dor abdominal,
Hepatites Virais Hepatites Inflamação do fígado Alteração em enzimas hepáticas (alaminotransferase aspartatoaminotransferase e gamaglutamiltransferase ALT AST e GGT Sinais clínicos: Náuseas, dor abdominal,
Detecção da infecção pelo vírus da artrite-encefalite caprina: imunodifusão em ágar e reação em cadeia da polimerase com primers degenerados
 Detecção da infecção pelo vírus da artrite-encefalite caprina: imunodifusão em ágar e reação em cadeia da polimerase com primers degenerados [Detection of caprine arthritis-encephalitis virus infection:
Detecção da infecção pelo vírus da artrite-encefalite caprina: imunodifusão em ágar e reação em cadeia da polimerase com primers degenerados [Detection of caprine arthritis-encephalitis virus infection:
UNIVERSIDADE ESTADUAL VALE DO ACARAÚ PROGRAMA DE MESTRADO EM ZOOTECNIA
 UNIVERSIDADE ESTADUAL VALE DO ACARAÚ PROGRAMA DE MESTRADO EM ZOOTECNIA ESTUDO ZOOSANITÁRIO E FATORES DE RISCO ASSOCIADOS À ARTRITE-ENCEFALITE CAPRINA NOS ESTADOS DO CEARÁ, RIO GRANDE DO NORTE E SERGIPE
UNIVERSIDADE ESTADUAL VALE DO ACARAÚ PROGRAMA DE MESTRADO EM ZOOTECNIA ESTUDO ZOOSANITÁRIO E FATORES DE RISCO ASSOCIADOS À ARTRITE-ENCEFALITE CAPRINA NOS ESTADOS DO CEARÁ, RIO GRANDE DO NORTE E SERGIPE
CARACTERÍSTICAS SEMINAIS DE CAPRINOS SADIOS E INFECTADOS PELO LENTIVÍRUS DE PEQUENOS RUMINANTES EM SOBRAL-CE
 CARACTERÍSTICAS SEMINAIS DE CAPRINOS SADIOS E INFECTADOS PELO LENTIVÍRUS DE PEQUENOS RUMINANTES EM SOBRAL-CE Elizângela Pinheiro Pereira 1 ; Rosivaldo Quirino Bezerra Junior 2 ; João Ricardo Furtado 3
CARACTERÍSTICAS SEMINAIS DE CAPRINOS SADIOS E INFECTADOS PELO LENTIVÍRUS DE PEQUENOS RUMINANTES EM SOBRAL-CE Elizângela Pinheiro Pereira 1 ; Rosivaldo Quirino Bezerra Junior 2 ; João Ricardo Furtado 3
PREVALÊNCIA SOROLÓGICA DA MAEDI-VISNA EM REBANHOS OVINOS DA MICRORREGIÃO DE JUAZEIRO - BAHIA POR MEIO DO TESTE DE IMUNODIFUSÃO EM GEL DE ÁGAR
 Prevalência sorológica da maedi-visna em rebanhos ovinos da microrregião de juazeiro... 322 DOI: 1 0.521 6/cab.v1 2i2.4454 PREVALÊNCIA SOROLÓGICA DA MAEDI-VISNA EM REBANHOS OVINOS DA MICRORREGIÃO DE JUAZEIRO
Prevalência sorológica da maedi-visna em rebanhos ovinos da microrregião de juazeiro... 322 DOI: 1 0.521 6/cab.v1 2i2.4454 PREVALÊNCIA SOROLÓGICA DA MAEDI-VISNA EM REBANHOS OVINOS DA MICRORREGIÃO DE JUAZEIRO
Comunicado Técnico. Artrite encefalite caprina viral: um alerta aos produtores. Introdução
 Comunicado Técnico 139 ISSN 1808-9984 Petrolina, PE Dezembro, 2009 Artrite encefalite caprina viral: um alerta aos produtores Daniel Maia Nogueira 1, Raymundo Rizaldo Pinheiro 2, Francisco Selmo Fernandes
Comunicado Técnico 139 ISSN 1808-9984 Petrolina, PE Dezembro, 2009 Artrite encefalite caprina viral: um alerta aos produtores Daniel Maia Nogueira 1, Raymundo Rizaldo Pinheiro 2, Francisco Selmo Fernandes
UNIVERSIDADE ESTADUAL DO MARANHÃO CENTRO DE CIÊNCIAS AGRÁRIAS CURSO DE MEDICINA VETERINÁRIA MESTRADO PROFISSIONAL EM DEFESA SANITÁRIA ANIMAL
 UNIVERSIDADE ESTADUAL DO MARANHÃO CENTRO DE CIÊNCIAS AGRÁRIAS CURSO DE MEDICINA VETERINÁRIA MESTRADO PROFISSIONAL EM DEFESA SANITÁRIA ANIMAL MICHELLE LEMOS VARGENS PREVALÊNCIA E FATORES DE RISCO ASSOCIADOS
UNIVERSIDADE ESTADUAL DO MARANHÃO CENTRO DE CIÊNCIAS AGRÁRIAS CURSO DE MEDICINA VETERINÁRIA MESTRADO PROFISSIONAL EM DEFESA SANITÁRIA ANIMAL MICHELLE LEMOS VARGENS PREVALÊNCIA E FATORES DE RISCO ASSOCIADOS
Vacinas e Vacinação 24/02/2014. Prof. Jean Berg. Defesas orgânicas. Imunoprofilaxia. Imunoprofilaxia. Resistência à infecção.
 Prof. Jean Berg Imunologia Resposta imune Mecanismo pelo qual o organismo é capaz de reconhecer e eliminar as substâncias heterólogas. Resposta imune Substâncias heterólogas Endógena células mortas Exógena
Prof. Jean Berg Imunologia Resposta imune Mecanismo pelo qual o organismo é capaz de reconhecer e eliminar as substâncias heterólogas. Resposta imune Substâncias heterólogas Endógena células mortas Exógena
Imunoensaios no laboratório clínico
 Imunoensaios no laboratório clínico Onde pesquisamos Ag e Ac?? Imunoensaios detecção e quantificação de antígeno e anticorpo: Doenças infecciosas: diagnóstico da doença diferenciação da fase da doença
Imunoensaios no laboratório clínico Onde pesquisamos Ag e Ac?? Imunoensaios detecção e quantificação de antígeno e anticorpo: Doenças infecciosas: diagnóstico da doença diferenciação da fase da doença
Vacinas e Vacinação. cüéya ]xtç UxÜz 18/5/2010. Defesas orgânicas. Imunoprofilaxia. Imunoprofilaxia. Resistência à infecção.
![Vacinas e Vacinação. cüéya ]xtç UxÜz 18/5/2010. Defesas orgânicas. Imunoprofilaxia. Imunoprofilaxia. Resistência à infecção. Vacinas e Vacinação. cüéya ]xtç UxÜz 18/5/2010. Defesas orgânicas. Imunoprofilaxia. Imunoprofilaxia. Resistência à infecção.](/thumbs/53/32296701.jpg) cüéya ]xtç UxÜz Imunologia Resposta imune Mecanismo pelo qual o organismo é capaz de reconhecer e eliminar as substâncias heterólogas. Resposta imune Substâncias heterólogas Endógena células mortas Exógena
cüéya ]xtç UxÜz Imunologia Resposta imune Mecanismo pelo qual o organismo é capaz de reconhecer e eliminar as substâncias heterólogas. Resposta imune Substâncias heterólogas Endógena células mortas Exógena
Diagnóstico Laboratorial de Infecções Virais. Profa. Claudia Vitral
 Diagnóstico Laboratorial de Infecções Virais Profa. Claudia Vitral Importância do diagnóstico laboratorial virológico Determinar a etiologia e acompanhar o curso de uma infecção viral Avaliar a eficácia
Diagnóstico Laboratorial de Infecções Virais Profa. Claudia Vitral Importância do diagnóstico laboratorial virológico Determinar a etiologia e acompanhar o curso de uma infecção viral Avaliar a eficácia
Pestvirus. Msc. Anne Caroline Ramos dos Santos
 Pestvirus Msc. Anne Caroline Ramos dos Santos Artigo Material e Métodos Animais: o Leitões de 8 semanas de idade o Livres de BVDV Vírus: o BVDV-1b não-citopático estirpe St. Oedenrode isolado de tonsila
Pestvirus Msc. Anne Caroline Ramos dos Santos Artigo Material e Métodos Animais: o Leitões de 8 semanas de idade o Livres de BVDV Vírus: o BVDV-1b não-citopático estirpe St. Oedenrode isolado de tonsila
Heterologous antibodies to evaluate the kinetics of the humoral immune response in dogs experimentally infected with Toxoplasma gondii RH strain
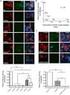 67 4.2 Estudo II Heterologous antibodies to evaluate the kinetics of the humoral immune response in dogs experimentally infected with Toxoplasma gondii RH strain Enquanto anticorpos anti-t. gondii são
67 4.2 Estudo II Heterologous antibodies to evaluate the kinetics of the humoral immune response in dogs experimentally infected with Toxoplasma gondii RH strain Enquanto anticorpos anti-t. gondii são
Exercício de Fixação: Características Gerais dos Vírus
 Exercício de Fixação: Características Gerais dos Vírus 01-2017 1- Quais foram as observações feitas por Adolf Mayer que permitiram concluir que o agente etiológico da Doença do Mosaico do tabaco era um
Exercício de Fixação: Características Gerais dos Vírus 01-2017 1- Quais foram as observações feitas por Adolf Mayer que permitiram concluir que o agente etiológico da Doença do Mosaico do tabaco era um
VÍRUS: A ESTRUTURA DO HIV E SEU CICLO DE VIDA
 VÍRUS: A ESTRUTURA DO HIV E SEU CICLO DE VIDA O vírus HIV possui duas moléculas de RNA envoltas por cápsulas proteicas (capsídeo), formando o nucleocapsídeo. Além do material genético, possui algumas enzimas,
VÍRUS: A ESTRUTURA DO HIV E SEU CICLO DE VIDA O vírus HIV possui duas moléculas de RNA envoltas por cápsulas proteicas (capsídeo), formando o nucleocapsídeo. Além do material genético, possui algumas enzimas,
Metodologia Científica
 Comunicado 132 Técnico Técnico Setembro, Metodologia Científica On line Uso de Cultura Celular de Membrana Nictitante Caprina para Produção de Antígeno de Lenti entivírus de Pequenos Ruminantes 1 Dalva
Comunicado 132 Técnico Técnico Setembro, Metodologia Científica On line Uso de Cultura Celular de Membrana Nictitante Caprina para Produção de Antígeno de Lenti entivírus de Pequenos Ruminantes 1 Dalva
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS
 1 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS ANDERSON CARVALHO DE FARIAS LEVANTAMENTO SOROLÓGICO
1 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS ANDERSON CARVALHO DE FARIAS LEVANTAMENTO SOROLÓGICO
Vírus - Caracterização Geral
 Noções de Vírus By Profª. Cynthia Vírus - Caracterização Geral Vírus = veneno ou fluído venenoso (Latim) Acelulares/ Partículas Infecciosas Composição química de nucleoproteínas (DNA ou RNA+Proteínas)
Noções de Vírus By Profª. Cynthia Vírus - Caracterização Geral Vírus = veneno ou fluído venenoso (Latim) Acelulares/ Partículas Infecciosas Composição química de nucleoproteínas (DNA ou RNA+Proteínas)
PCR Reação de Polimerase em Cadeia. Termociclador
 PCR Reação de Polimerase em Cadeia Termociclador REAÇÃO EM CADEIA DA POLIMERASE (PCR) Técnica que permite a amplificação da quantidade de DNA específico utilizando a enzima Taq DNA polimerase, sequências
PCR Reação de Polimerase em Cadeia Termociclador REAÇÃO EM CADEIA DA POLIMERASE (PCR) Técnica que permite a amplificação da quantidade de DNA específico utilizando a enzima Taq DNA polimerase, sequências
Universidade Federal Fluminense Resposta do hospedeiro às infecções virais
 Universidade Federal Fluminense Resposta do hospedeiro às infecções virais Disciplina de Virologia Departamento de Microbiologia e Parasitologia (MIP) Mecanismos de resposta inespecífica Barreiras anatômicas
Universidade Federal Fluminense Resposta do hospedeiro às infecções virais Disciplina de Virologia Departamento de Microbiologia e Parasitologia (MIP) Mecanismos de resposta inespecífica Barreiras anatômicas
Professor: David Vieira Valadão. Biologia
 Professor: David Vieira Valadão Biologia 1981 registro de casos atípicos de pneumonia entre homens homossexuais em Los Angeles (EUA). 1983 descoberta de um novo vírus em um paciente com AIDS. 1984 descoberta
Professor: David Vieira Valadão Biologia 1981 registro de casos atípicos de pneumonia entre homens homossexuais em Los Angeles (EUA). 1983 descoberta de um novo vírus em um paciente com AIDS. 1984 descoberta
Qual é a estrutura típica de um vírus?
 Vírus Qual é a estrutura típica de um vírus? CICLOS REPRODUTIVOS Em relação a reprodução dos vírus, podemos dizer que eles podem realizar um ciclo lítico ou um ciclo lisogênico. Qual é a principal
Vírus Qual é a estrutura típica de um vírus? CICLOS REPRODUTIVOS Em relação a reprodução dos vírus, podemos dizer que eles podem realizar um ciclo lítico ou um ciclo lisogênico. Qual é a principal
Introdução a Virologia. Definição - O que é vírus? Composição e estrutura Genoma e Replicação
 Introdução a Virologia Definição - O que é vírus? Composição e estrutura Genoma e Replicação O que é vírus? Agentes infecciosos ultramicroscópicos Não são células São partículas filtráveis Só apresentam
Introdução a Virologia Definição - O que é vírus? Composição e estrutura Genoma e Replicação O que é vírus? Agentes infecciosos ultramicroscópicos Não são células São partículas filtráveis Só apresentam
Aplicações de anticorpos em métodos diagnósticos
 Aula Prática Demonstrativa: Aplicações de anticorpos em métodos diagnósticos Introdução Profa. Cristina MED- 2017 Detecção de anticorpos (diagnóstico sorológico) Exemplo: detecção de anticorpos em jovem
Aula Prática Demonstrativa: Aplicações de anticorpos em métodos diagnósticos Introdução Profa. Cristina MED- 2017 Detecção de anticorpos (diagnóstico sorológico) Exemplo: detecção de anticorpos em jovem
Universidade Federal da Bahia Escola de Medicina Veterinária Mestrado em Ciência Animal nos Trópicos
 i Universidade Federal da Bahia Escola de Medicina Veterinária Mestrado em Ciência Animal nos Trópicos CARACTERÍSTICAS DOS SISTEMAS DE PRODUÇÃO DE OVINOS E PREVALÊNCIA SOROLÓGICA DA MAEDI-VISNA NA MICRORREGIÃO
i Universidade Federal da Bahia Escola de Medicina Veterinária Mestrado em Ciência Animal nos Trópicos CARACTERÍSTICAS DOS SISTEMAS DE PRODUÇÃO DE OVINOS E PREVALÊNCIA SOROLÓGICA DA MAEDI-VISNA NA MICRORREGIÃO
Ciência Animal Brasileira Suplemento 1, 2009 Anais do VIII Congresso Brasileiro de Buiatria
 PREVALÊNCIA SOROLÓGICA DA ARTRITE-ENCEFALITE CAPRINA EM REBANHOS CAPRINOS DO MUNICÍPIO DE JUAZEIRO BAHIA, BRASIL Carla Caroline Valença de Lima 1, Thiago Sampaio Souza 2, Priscila Martinez Martinez 3,
PREVALÊNCIA SOROLÓGICA DA ARTRITE-ENCEFALITE CAPRINA EM REBANHOS CAPRINOS DO MUNICÍPIO DE JUAZEIRO BAHIA, BRASIL Carla Caroline Valença de Lima 1, Thiago Sampaio Souza 2, Priscila Martinez Martinez 3,
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS
 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS LUIS ANTONIO DE OLIVEIRA ALVES PRODUÇÃO DE ANTÍGENO E
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS LUIS ANTONIO DE OLIVEIRA ALVES PRODUÇÃO DE ANTÍGENO E
AMPLIFICAÇÃO DO GENE DA PROTEÍNA E DO VÍRUS DENV ATRAVÉS DA TÉCNICA DE REAÇÃO EM CADEIA DA POLIMERASE (PCR)
 AMPLIFICAÇÃO DO GENE DA PROTEÍNA E DO VÍRUS DENV ATRAVÉS DA TÉCNICA DE REAÇÃO EM CADEIA DA POLIMERASE (PCR) Beatriz Dantas Guimarães (1); Lucas Linhares de Locio (2); Herbert Crisóstomo dos Santos Araújo
AMPLIFICAÇÃO DO GENE DA PROTEÍNA E DO VÍRUS DENV ATRAVÉS DA TÉCNICA DE REAÇÃO EM CADEIA DA POLIMERASE (PCR) Beatriz Dantas Guimarães (1); Lucas Linhares de Locio (2); Herbert Crisóstomo dos Santos Araújo
Diagnóstico do HIV Ministério da Saúde
 Ministério da Saúde Secretaria de Vigilância em Saúde Departamento de DST, AIDS e Hepatites Virais Universidade Federal de Santa Catarina Diagnóstico do HIV Ministério da Saúde Ademar Arthur Chioro dos
Ministério da Saúde Secretaria de Vigilância em Saúde Departamento de DST, AIDS e Hepatites Virais Universidade Federal de Santa Catarina Diagnóstico do HIV Ministério da Saúde Ademar Arthur Chioro dos
mundo inteiro com uma variedade de aplicações como clonagem, genotipagem e sequenciamento.
 mundo inteiro com uma variedade de aplicações como clonagem, genotipagem e sequenciamento. necessária para que você possa alcançar o melhor desempenho nesta técnica. AGAROSE A agarose é um polissacarídeo
mundo inteiro com uma variedade de aplicações como clonagem, genotipagem e sequenciamento. necessária para que você possa alcançar o melhor desempenho nesta técnica. AGAROSE A agarose é um polissacarídeo
PAULO EDUARDO BRANDÃO, PhD DEPARTAMENTO DE MEDICINA VETERINÁRIA PREVENTIVA E SAÚDE ANIMAL FACULDADE DE MEDICINA VETERINÁRIA E ZOOTECNIA UNIVERSIDADE
 PAULO EDUARDO BRANDÃO, PhD DEPARTAMENTO DE MEDICINA VETERINÁRIA PREVENTIVA E SAÚDE ANIMAL FACULDADE DE MEDICINA VETERINÁRIA E ZOOTECNIA UNIVERSIDADE DE SÃO PAULO 1. DEFINIÇÃO 2. PRINCÍPIO 3. APLICAÇÕES
PAULO EDUARDO BRANDÃO, PhD DEPARTAMENTO DE MEDICINA VETERINÁRIA PREVENTIVA E SAÚDE ANIMAL FACULDADE DE MEDICINA VETERINÁRIA E ZOOTECNIA UNIVERSIDADE DE SÃO PAULO 1. DEFINIÇÃO 2. PRINCÍPIO 3. APLICAÇÕES
EPIDEMIOLOGIA DAS INFECÇÕES VIRAIS L A B V I R - I C B S U F R G S 2015
 EPIDEMIOLOGIA DAS INFECÇÕES VIRAIS L A B V I R - I C B S U F R G S 2015 EPIDEMIOLOGIA Estudo das doenças em populações, investigando os seus determinantes, a sua dinâmica e distribuição. VÍRUS Partícula
EPIDEMIOLOGIA DAS INFECÇÕES VIRAIS L A B V I R - I C B S U F R G S 2015 EPIDEMIOLOGIA Estudo das doenças em populações, investigando os seus determinantes, a sua dinâmica e distribuição. VÍRUS Partícula
Interação Antígeno Anticorpo. Profª Heide Baida
 Interação Antígeno Anticorpo Profª Heide Baida Introdução T CD4+ memória MØ Resposta imune Ag Linfócito T CD4+ T CD4+ efetor * * * * * * * * * citocinas * * Linfócito B anticorpos B memória B Efetor (plasmócito)
Interação Antígeno Anticorpo Profª Heide Baida Introdução T CD4+ memória MØ Resposta imune Ag Linfócito T CD4+ T CD4+ efetor * * * * * * * * * citocinas * * Linfócito B anticorpos B memória B Efetor (plasmócito)
Análises moleculares - DNA
 Análises moleculares - DNA Como o mapeamento genético contribui para a genética médica? A caracterização de um gene e suas mutações aumenta a compreensão da doença Aplicações: -Desenvolvimento de diagnóstico
Análises moleculares - DNA Como o mapeamento genético contribui para a genética médica? A caracterização de um gene e suas mutações aumenta a compreensão da doença Aplicações: -Desenvolvimento de diagnóstico
Métodos imunológicos na avaliação da resposta à vacinação.
 Métodos imunológicos na avaliação da resposta à vacinação. Patrícia Neves Laboratório de Tecnologia Imunológica VDTEC/Biomanguinhos Proteção vacinal A identificação de marcadores imunológicos que se correlacionem
Métodos imunológicos na avaliação da resposta à vacinação. Patrícia Neves Laboratório de Tecnologia Imunológica VDTEC/Biomanguinhos Proteção vacinal A identificação de marcadores imunológicos que se correlacionem
TRANSFERIBILIDADE DE MARCADORES MICROSSATÉLITES DE MELÃO PARA MELANCIA
 TRANSFERIBILIDADE DE MARCADORES MICROSSATÉLITES DE MELÃO PARA MELANCIA Maia, A. K. S (1) ; Albuquerque, L. B. (1) ; Antonio, R. P. (2) ; Silveira, L. M. (3) ; Nunes, G. H. S (1) ; Silva, A. E. A (1) ;
TRANSFERIBILIDADE DE MARCADORES MICROSSATÉLITES DE MELÃO PARA MELANCIA Maia, A. K. S (1) ; Albuquerque, L. B. (1) ; Antonio, R. P. (2) ; Silveira, L. M. (3) ; Nunes, G. H. S (1) ; Silva, A. E. A (1) ;
Avaliação do padrão e número de sítios de fosforilação (EPIYA) da proteína CagA de H. pylori e risco de carcinoma gástrico e úlcera duodenal
 UNIVERSIDADE FEDERAL DE MINAS GERAIS INSTITUTO DE CIÊNCIAS BIOLÓGICAS CURSO DE PÓS-GRADUAÇÃO EM MICROBIOLOGIA Avaliação do padrão e número de sítios de fosforilação (EPIYA) da proteína CagA de H. pylori
UNIVERSIDADE FEDERAL DE MINAS GERAIS INSTITUTO DE CIÊNCIAS BIOLÓGICAS CURSO DE PÓS-GRADUAÇÃO EM MICROBIOLOGIA Avaliação do padrão e número de sítios de fosforilação (EPIYA) da proteína CagA de H. pylori
Produção de antígeno de lentivírus de pequenos ruminantes através da cultura celular de membrana nictitante caprina*
 Produção de antígeno de lentivírus de pequenos ruminantes através da cultura celular de membrana nictitante caprina* Dalva Alana Aragão de Azevedo¹ +, Juscilânia Furtado Araújo², Ana Lídia Madeira de Sousa³,
Produção de antígeno de lentivírus de pequenos ruminantes através da cultura celular de membrana nictitante caprina* Dalva Alana Aragão de Azevedo¹ +, Juscilânia Furtado Araújo², Ana Lídia Madeira de Sousa³,
Universidade de Évora ICAAM Laboratório de Microbiologia do Solo 18/07/ /07/2011
 Universidade de Évora ICAAM Laboratório de Microbiologia do Solo Ana Neves José Neto 18/07/2011-22/07/2011 Responsável: Solange Oliveira Investigadoras: Marta Laranjo Ana Alexandre Rizóbios são bactérias
Universidade de Évora ICAAM Laboratório de Microbiologia do Solo Ana Neves José Neto 18/07/2011-22/07/2011 Responsável: Solange Oliveira Investigadoras: Marta Laranjo Ana Alexandre Rizóbios são bactérias
Hepatites A e E. Hepatite E 3/7/2014. Taxonomia. Características do vírus. Não envelopado nm diâmetro Fita positiva RNA ~7.2 kb.
 Hepatites A e E Hepatite E Fábio Gregori Taxonomia Características do vírus Não envelopado 27-35 nm diâmetro Fita positiva RNA ~7.2 kb Diagnóstico Diagnóstico Infecção: a) sorodiagnóstico IgM e IgG*. b)
Hepatites A e E Hepatite E Fábio Gregori Taxonomia Características do vírus Não envelopado 27-35 nm diâmetro Fita positiva RNA ~7.2 kb Diagnóstico Diagnóstico Infecção: a) sorodiagnóstico IgM e IgG*. b)
Características Gerais dos Vírus
 Características Gerais dos Vírus Vírus Agentes causadores de infecções no homem, outros animais, vegetais e bactérias. São desprovidos de organelas e sem metabolismo próprio. Parasitas intracelulares obrigatórios.
Características Gerais dos Vírus Vírus Agentes causadores de infecções no homem, outros animais, vegetais e bactérias. São desprovidos de organelas e sem metabolismo próprio. Parasitas intracelulares obrigatórios.
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS
 1 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS SAMILLY MESQUITA ALVES SOROPREVALÊNCIA DA MAEDI - VISNA
1 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS SAMILLY MESQUITA ALVES SOROPREVALÊNCIA DA MAEDI - VISNA
Documentos 86. On line
 ISSN 1676-7959 Dezembro, 2009 Empresa Brasileira de Pesquisa Agropecuária Embrapa Caprinos e Ovinos Ministério da Agricultura, Pecuária e Abastecimento Documentos 86 On line Controle dos Casos de Mastite
ISSN 1676-7959 Dezembro, 2009 Empresa Brasileira de Pesquisa Agropecuária Embrapa Caprinos e Ovinos Ministério da Agricultura, Pecuária e Abastecimento Documentos 86 On line Controle dos Casos de Mastite
Estudo de um Polimorfismo no Gene da Cadeia Pesada β da Miosina (CPβM)
 Estudo de um Polimorfismo no Gene da Cadeia Pesada β da Miosina (CPβM) Ana Luísa Carvalho Departamento de Zoologia, Universidade de Coimbra Introdução: Neste trabalho pretende-se analisar um polimorfismo
Estudo de um Polimorfismo no Gene da Cadeia Pesada β da Miosina (CPβM) Ana Luísa Carvalho Departamento de Zoologia, Universidade de Coimbra Introdução: Neste trabalho pretende-se analisar um polimorfismo
TÍTULO: SEXAGEM FETAL:DIAGNÓTICO DO SEXO DO FETO POR REAÇÃO EM CADEIA DE POLIMERASE (PCR)
 TÍTULO: SEXAGEM FETAL:DIAGNÓTICO DO SEXO DO FETO POR REAÇÃO EM CADEIA DE POLIMERASE (PCR) CATEGORIA: EM ANDAMENTO ÁREA: CIÊNCIAS BIOLÓGICAS E SAÚDE SUBÁREA: BIOMEDICINA INSTITUIÇÃO: CENTRO UNIVERSITÁRIO
TÍTULO: SEXAGEM FETAL:DIAGNÓTICO DO SEXO DO FETO POR REAÇÃO EM CADEIA DE POLIMERASE (PCR) CATEGORIA: EM ANDAMENTO ÁREA: CIÊNCIAS BIOLÓGICAS E SAÚDE SUBÁREA: BIOMEDICINA INSTITUIÇÃO: CENTRO UNIVERSITÁRIO
Interação vírus célula Aspectos Gerais. Tatiana Castro Departamento de Microbiologia e Parasitologia (UFF)
 Interação vírus célula Aspectos Gerais Tatiana Castro Departamento de Microbiologia e Parasitologia (UFF) Interação Vírus - Célula Relacionada ao ciclo de replicação do vírus Efeitos primários da infecção
Interação vírus célula Aspectos Gerais Tatiana Castro Departamento de Microbiologia e Parasitologia (UFF) Interação Vírus - Célula Relacionada ao ciclo de replicação do vírus Efeitos primários da infecção
SOROPREVALÊNCIA DO LENTIVíRUS DE PEQUENOS RUMINANTES EM REBANHOS OVINOS E CAPRINOS DE MICRO- REGIÕES DO ESTADO DO RIO DE JANEIRO, BRASIL
 SOROPREVALÊNCIA DO LENTIVíRUS DE PEQUENOS RUMINANTES EM REBANHOS OVINOS E CAPRINOS DE MICRO- REGIÕES DO ESTADO DO RIO DE JANEIRO, BRASIL CLEUBER DE ANDRADE JÚNIOR UNIVERSIDADE ESTADUAL DO NORTE FLUMINENSE
SOROPREVALÊNCIA DO LENTIVíRUS DE PEQUENOS RUMINANTES EM REBANHOS OVINOS E CAPRINOS DE MICRO- REGIÕES DO ESTADO DO RIO DE JANEIRO, BRASIL CLEUBER DE ANDRADE JÚNIOR UNIVERSIDADE ESTADUAL DO NORTE FLUMINENSE
1.4 Metodologias analíticas para isolamento e identificação de micro-organismos em alimentos
 Áreas para Submissão de Resumos (1) Microbiologia de Alimentos Trabalhos relacionados com micro-organismos associados aos alimentos: crescimento, identificação, biossíntese, controle, interação com o hospedeiro,
Áreas para Submissão de Resumos (1) Microbiologia de Alimentos Trabalhos relacionados com micro-organismos associados aos alimentos: crescimento, identificação, biossíntese, controle, interação com o hospedeiro,
MULTIPLICAÇÃO VIRAL Danielly Cantarelli
 MULTIPLICAÇÃO VIRAL Danielly Cantarelli 1 Os vírus não possuem enzimas para a produção de energia nem para a síntese protéica Para que um vírus se multiplique, ele deve invadir uma célula hospedeira e
MULTIPLICAÇÃO VIRAL Danielly Cantarelli 1 Os vírus não possuem enzimas para a produção de energia nem para a síntese protéica Para que um vírus se multiplique, ele deve invadir uma célula hospedeira e
UNIVERSIDADE ESTADUAL DO CEARÁ SUZANA APARECIDA COSTA DE ARAÚJO
 1 UNIVERSIDADE ESTADUAL DO CEARÁ SUZANA APARECIDA COSTA DE ARAÚJO AVALIAÇÃO IN VITRO DA ATIVIDADE ANTIVIRAL DE PRODUTOS SINTÉTICOS E NATURAIS CONTRA LENTIVÍRUS DE PEQUENOS RUMINANTES FORTALEZA CE 2008
1 UNIVERSIDADE ESTADUAL DO CEARÁ SUZANA APARECIDA COSTA DE ARAÚJO AVALIAÇÃO IN VITRO DA ATIVIDADE ANTIVIRAL DE PRODUTOS SINTÉTICOS E NATURAIS CONTRA LENTIVÍRUS DE PEQUENOS RUMINANTES FORTALEZA CE 2008
Prevenção e controle das infecções virais
 Prevenção e controle das infecções virais 1 Medidas de prevenção de doenças virais Redução do risco de exposição Introdução de melhorias sanitárias (ex. infecções entéricas) Veiculação de informações para
Prevenção e controle das infecções virais 1 Medidas de prevenção de doenças virais Redução do risco de exposição Introdução de melhorias sanitárias (ex. infecções entéricas) Veiculação de informações para
Resposta imune adquirida
 Resposta imune adquirida Resposta imune adquirida Também denominada: - Resposta imune tardia - Resposta imune adaptativa É caracterizada por ocorrer em períodos mais tardios após o contato com um agente
Resposta imune adquirida Resposta imune adquirida Também denominada: - Resposta imune tardia - Resposta imune adaptativa É caracterizada por ocorrer em períodos mais tardios após o contato com um agente
RESSALVA. Atendendo solicitação do autor, o texto completo desta tese será disponibilizado somente a partir de 04/04/2016.
 RESSALVA Atendendo solicitação do autor, o texto completo desta tese será disponibilizado somente a partir de 04/04/2016. UNIVERSIDADE ESTADUAL PAULISTA UNESP CÂMPUS DE JABOTICABAL CARACTERIZAÇÃO EPIDEMIOLÓGICA
RESSALVA Atendendo solicitação do autor, o texto completo desta tese será disponibilizado somente a partir de 04/04/2016. UNIVERSIDADE ESTADUAL PAULISTA UNESP CÂMPUS DE JABOTICABAL CARACTERIZAÇÃO EPIDEMIOLÓGICA
UNIVERSIDADE FEDERAL DE MINAS GERAIS ESCOLA DE VETERINÁRIA COLEGIADO DO CURSO DE PÓS GRADUAÇÃO
 UNIVERSIDADE FEDERAL DE MINAS GERAIS ESCOLA DE VETERINÁRIA COLEGIADO DO CURSO DE PÓS GRADUAÇÃO PERFIL DAS PROPRIEDADES COMERCIAIS COM CAPRINOS EM MINAS GERAIS E SUA RELAÇÃO COM A SOROPREVALÊNCIA DO LENTIVÍRUS
UNIVERSIDADE FEDERAL DE MINAS GERAIS ESCOLA DE VETERINÁRIA COLEGIADO DO CURSO DE PÓS GRADUAÇÃO PERFIL DAS PROPRIEDADES COMERCIAIS COM CAPRINOS EM MINAS GERAIS E SUA RELAÇÃO COM A SOROPREVALÊNCIA DO LENTIVÍRUS
Hepatites. Inflamação do fígado. Alteração em enzimas hepáticas (alaminotransferase aspartatoaminotransferase e gamaglutamiltransferase ALT AST e GGT
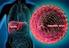 Hepatites Virais Hepatites Inflamação do fígado Alteração em enzimas hepáticas (alaminotransferase aspartatoaminotransferase e gamaglutamiltransferase ALT AST e GGT Sinais clínicos: Náuseas, dor abdominal,
Hepatites Virais Hepatites Inflamação do fígado Alteração em enzimas hepáticas (alaminotransferase aspartatoaminotransferase e gamaglutamiltransferase ALT AST e GGT Sinais clínicos: Náuseas, dor abdominal,
DESENVOLVIMENTO E PADRONIZAÇÃO DE ELISA INDIRETO PARA DIAGNÓSTICO DE MAEDI-VISNA VÍRUS DE OVINOS.
 1 Universidade Estadual do Ceará Tânia Valeska Medeiros Dantas DESENVOLVIMENTO E PADRONIZAÇÃO DE ELISA INDIRETO PARA DIAGNÓSTICO DE MAEDI-VISNA VÍRUS DE OVINOS. Fortaleza Ceará 2004 2 Universidade Estadual
1 Universidade Estadual do Ceará Tânia Valeska Medeiros Dantas DESENVOLVIMENTO E PADRONIZAÇÃO DE ELISA INDIRETO PARA DIAGNÓSTICO DE MAEDI-VISNA VÍRUS DE OVINOS. Fortaleza Ceará 2004 2 Universidade Estadual
Herpesvírus linfotrópicos: CMV e EBV. Prof. Dr. Eurico Arruda Faculdade de Medicina de Ribeirão Preto-USP
 Herpesvírus linfotrópicos: CMV e EBV Prof. Dr. Eurico Arruda Faculdade de Medicina de Ribeirão Preto-USP Caso Clínico Uma semana depois de uma famosa festa a fantasia, um aluno do 2º ano de medicina da
Herpesvírus linfotrópicos: CMV e EBV Prof. Dr. Eurico Arruda Faculdade de Medicina de Ribeirão Preto-USP Caso Clínico Uma semana depois de uma famosa festa a fantasia, um aluno do 2º ano de medicina da
Processos de interação vírus célula. e replicação viral
 Processos de interação vírus célula e replicação viral Adsorção: ligação do receptor celular e antirreceptor viral. Exemplo poliovírus: 1 Adsorção: ligação do receptor celular e antirreceptor viral. Hepatite
Processos de interação vírus célula e replicação viral Adsorção: ligação do receptor celular e antirreceptor viral. Exemplo poliovírus: 1 Adsorção: ligação do receptor celular e antirreceptor viral. Hepatite
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS
 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS ROSIVALDO QUIRINO BEZERRA JÚNIOR INFLUÊNCIA DA ARTRITE
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS ROSIVALDO QUIRINO BEZERRA JÚNIOR INFLUÊNCIA DA ARTRITE
A portaria 29, de 17 de dezembro de 2013 SVS/MS, regulamenta o diagnóstico da infecção pelo HIV, no Brasil.
 Aula 3 Base racional da portaria 29 de 17/12/2013 SVS/MS A portaria 29, de 17 de dezembro de 2013 SVS/MS, regulamenta o diagnóstico da infecção pelo HIV, no Brasil. Ao se elaborar uma portaria para normatizar
Aula 3 Base racional da portaria 29 de 17/12/2013 SVS/MS A portaria 29, de 17 de dezembro de 2013 SVS/MS, regulamenta o diagnóstico da infecção pelo HIV, no Brasil. Ao se elaborar uma portaria para normatizar
05/03/2017. Zoonose. Cocobacilos gram (-) Colônias Lisas B. suis (A e M) B. abortus (A) B. melitensis (M)
 Doença infectocontagiosa crônica provocada por bactérias do Gênero Brucellasp. Impacto econômico Queda na produção e aborto Repetição de cio / retenção de placenta Zoonose Cocobacilos gram (-) Colônias
Doença infectocontagiosa crônica provocada por bactérias do Gênero Brucellasp. Impacto econômico Queda na produção e aborto Repetição de cio / retenção de placenta Zoonose Cocobacilos gram (-) Colônias
CAROLINA MARQUES RIBEIRO PESSOA PARVOVIROSE CANINA: REVISÃO DE LITERATURA.
 CAROLINA MARQUES RIBEIRO PESSOA PARVOVIROSE CANINA: REVISÃO DE LITERATURA. SALVADOR BA 2008 CAROLINA MARQUES RIBEIRO PESSOA PARVOVIROSE CANINA: REVISÃO DE LITERATURA. Monografia apresentada a Universidade
CAROLINA MARQUES RIBEIRO PESSOA PARVOVIROSE CANINA: REVISÃO DE LITERATURA. SALVADOR BA 2008 CAROLINA MARQUES RIBEIRO PESSOA PARVOVIROSE CANINA: REVISÃO DE LITERATURA. Monografia apresentada a Universidade
EMMANUELA TINÉ DE ARRUDA AVALIAÇÃO DE UMA MICROIMUNODIFUSÃO EM GEL DE ÁGAR PARA DIAGNÓSTICO DE LENTIVÍRUS DE PEQUENOS RUMINANTES EM CAPRINOS
 EMMANUELA TINÉ DE ARRUDA AVALIAÇÃO DE UMA MICROIMUNODIFUSÃO EM GEL DE ÁGAR PARA DIAGNÓSTICO DE LENTIVÍRUS DE PEQUENOS RUMINANTES EM CAPRINOS RECIFE, PE JULHO DE 2006 EMMANUELA TINÉ DE ARRUDA AVALIAÇÃO
EMMANUELA TINÉ DE ARRUDA AVALIAÇÃO DE UMA MICROIMUNODIFUSÃO EM GEL DE ÁGAR PARA DIAGNÓSTICO DE LENTIVÍRUS DE PEQUENOS RUMINANTES EM CAPRINOS RECIFE, PE JULHO DE 2006 EMMANUELA TINÉ DE ARRUDA AVALIAÇÃO
Vírus. Leonardo Rodrigues EEEFM GRAÇA ARANHA
 Vírus Leonardo Rodrigues EEEFM GRAÇA ARANHA Virologia Virologia. Ramo da Biologia que estuda os vírus e suas propriedades. Vírus é totalmente inerte fora da sua célula hospedeira; Dependem totalmente da
Vírus Leonardo Rodrigues EEEFM GRAÇA ARANHA Virologia Virologia. Ramo da Biologia que estuda os vírus e suas propriedades. Vírus é totalmente inerte fora da sua célula hospedeira; Dependem totalmente da
Resultados. Grupo SK/aids
 40 Resultados Em virtude da quantidade e da complexidade dos dados obtidos, optou-se pela apresentação individual dos resultados na forma de Quadros que se encontram em Anexo; e para facilitar a visualização
40 Resultados Em virtude da quantidade e da complexidade dos dados obtidos, optou-se pela apresentação individual dos resultados na forma de Quadros que se encontram em Anexo; e para facilitar a visualização
Universidade Federal da Bahia Faculdade de Medicina Departamento de Anatomia Patológica e Medicina Legal Disciplina de Imunologia MED 194
 Universidade Federal da Bahia Faculdade de Medicina Departamento de Anatomia Patológica e Medicina Legal Disciplina de Imunologia MED 194 Imunologia das Viroses Monitor: Daniel Valente 1.Introdução...
Universidade Federal da Bahia Faculdade de Medicina Departamento de Anatomia Patológica e Medicina Legal Disciplina de Imunologia MED 194 Imunologia das Viroses Monitor: Daniel Valente 1.Introdução...
INFLUÊNCIA DO GENÓTIPO SOBRE A PRODUÇÃO E A COMPOSIÇÃO DO LEITE DE CABRAS MESTIÇAS
 Código 1148 INFLUÊNCIA DO GENÓTIPO SOBRE A PRODUÇÃO E A COMPOSIÇÃO DO LEITE DE CABRAS MESTIÇAS NELSON NOGUEIRA BARROS 1, VÂNIA RODRIGUES DE VASCONCELOS 1, FRANCISCO LUIZ RIBEIRO DA SILVA 1, MARCELO RENATO
Código 1148 INFLUÊNCIA DO GENÓTIPO SOBRE A PRODUÇÃO E A COMPOSIÇÃO DO LEITE DE CABRAS MESTIÇAS NELSON NOGUEIRA BARROS 1, VÂNIA RODRIGUES DE VASCONCELOS 1, FRANCISCO LUIZ RIBEIRO DA SILVA 1, MARCELO RENATO
Bases e aplicações. da tecnologia do DNA recombinante
 Bases e aplicações da tecnologia do DNA recombinante Por quê entender a Tecnologia do DNA recombinante? y y Doenças: diagnóstico, prognóstico e tratamento Compreensão dos mecanismos biológicos y y y organismos
Bases e aplicações da tecnologia do DNA recombinante Por quê entender a Tecnologia do DNA recombinante? y y Doenças: diagnóstico, prognóstico e tratamento Compreensão dos mecanismos biológicos y y y organismos
CATÁLOGO DE KITS DE EXTRAÇÃO
 CATÁLOGO DE KITS DE EXTRAÇÃO KITS DE EXTRAÇÃO BIOPUR A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
CATÁLOGO DE KITS DE EXTRAÇÃO KITS DE EXTRAÇÃO BIOPUR A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
Introdução à Bioquímica
 Introdução à Bioquímica Nucleotídeos e Ácidos Nucléicos Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física.. UNESP São José do Rio Preto - SP. Genoma! O genoma de um organismo
Introdução à Bioquímica Nucleotídeos e Ácidos Nucléicos Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física.. UNESP São José do Rio Preto - SP. Genoma! O genoma de um organismo
Casos de FHD Óbitos e Taxa de letalidade
 Casos de dengue Jan Fev Mar Abr Mai Jun Jul Ago Set Out Nov Dez Total 2003 20.471 23.612 - - - - - - - - - - 44.083 2002 94.447 188.522 237.906 128.667 60.646 23.350 12.769 10.149 6.682 7.138 9.246 9.052
Casos de dengue Jan Fev Mar Abr Mai Jun Jul Ago Set Out Nov Dez Total 2003 20.471 23.612 - - - - - - - - - - 44.083 2002 94.447 188.522 237.906 128.667 60.646 23.350 12.769 10.149 6.682 7.138 9.246 9.052
Catálogo de Kits de Extração
 Catálogo de Kits de Extração Kits de Extração Biopur A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
Catálogo de Kits de Extração Kits de Extração Biopur A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
PERFIL EPIDEMIOLÓGICO DOS CASOS DE HEPATITE A NOTIFICADOS EM UM ESTADO NORDESTINO
 PERFIL EPIDEMIOLÓGICO DOS CASOS DE HEPATITE A NOTIFICADOS EM UM ESTADO NORDESTINO Rayana Cruz de Souza; Universidade Federal da Paraíba; rayana_souza@hotmail.com Maira Ludna Duarte; Universidade Federal
PERFIL EPIDEMIOLÓGICO DOS CASOS DE HEPATITE A NOTIFICADOS EM UM ESTADO NORDESTINO Rayana Cruz de Souza; Universidade Federal da Paraíba; rayana_souza@hotmail.com Maira Ludna Duarte; Universidade Federal
Tuberculose. Definição Enfermidade infecto-contagiosa evolução crônica lesões de aspecto nodular - linfonodos e pulmão Diversos animais Zoonose
 1 2 3 Tuberculose Definição Enfermidade infecto-contagiosa evolução crônica lesões de aspecto nodular - linfonodos e pulmão Diversos animais Zoonose ETIOLOGIA Família: Mycobacteriaceae Ordem: Actinomycetalis
1 2 3 Tuberculose Definição Enfermidade infecto-contagiosa evolução crônica lesões de aspecto nodular - linfonodos e pulmão Diversos animais Zoonose ETIOLOGIA Família: Mycobacteriaceae Ordem: Actinomycetalis
RESUMO Desempenho de poedeiras em diferentes programas de luz ao início da postura
 RESUMO YURI, Flavio Manabu. Desempenho de poedeiras em diferentes programas de luz ao início da postura. 2013. 76 f. Dissertação (Mestrado em Ciência Animal Área: Produção Animal) Universidade do Estado
RESUMO YURI, Flavio Manabu. Desempenho de poedeiras em diferentes programas de luz ao início da postura. 2013. 76 f. Dissertação (Mestrado em Ciência Animal Área: Produção Animal) Universidade do Estado
Profa. Carolina G. P. Beyrodt
 Profa. Carolina G. P. Beyrodt Agente etiológico: Toxoplasma gondii (Protozoário coccídeo do Filo Apicomplexa) Histórico Isolado em 1908 de um roedor do deserto: Ctenodactylus gondii 1923 descrição do primeiro
Profa. Carolina G. P. Beyrodt Agente etiológico: Toxoplasma gondii (Protozoário coccídeo do Filo Apicomplexa) Histórico Isolado em 1908 de um roedor do deserto: Ctenodactylus gondii 1923 descrição do primeiro
Análise da qualidade do leite em pequenas propriedades de Barbacena
 Análise da qualidade do leite em pequenas propriedades de Barbacena Duarte Carvalho Minighin 1, Wallacy Augusto de Oliveira 1, Túlio Gomes Justino 1, Thaylene Maria do Amaral 1, Luis Fernando de Moraes
Análise da qualidade do leite em pequenas propriedades de Barbacena Duarte Carvalho Minighin 1, Wallacy Augusto de Oliveira 1, Túlio Gomes Justino 1, Thaylene Maria do Amaral 1, Luis Fernando de Moraes
especiais, que através do sistema do encaixe ou ajuste induzido unem-se ao
 VÍRUS: CARACTERÍSTICAS GERAIS A palavra vírus significa veneno, e é o nome dado à pequenas estruturas infecciosas dotadas de uma capa e material genético. Essas estruturas são mais pequenas do que as menores
VÍRUS: CARACTERÍSTICAS GERAIS A palavra vírus significa veneno, e é o nome dado à pequenas estruturas infecciosas dotadas de uma capa e material genético. Essas estruturas são mais pequenas do que as menores
PROGRAD / COSEAC Padrão de Respostas Biologia
 1 a QUESTÃO: Cada vez mais a técnica da reação em cadeia da polimerase (PCR - polimerase chain reaction) tem sido utilizada no diagnóstico de doenças parasitárias. Por essa técnica, regiões específicas
1 a QUESTÃO: Cada vez mais a técnica da reação em cadeia da polimerase (PCR - polimerase chain reaction) tem sido utilizada no diagnóstico de doenças parasitárias. Por essa técnica, regiões específicas
Tópicos de Imunologia Celular e Molecular (Parte 2)
 IMUNOLOGIA BÁSICA Tópicos de Imunologia Celular e Molecular (Parte 2) Prof. M. Sc. Paulo Galdino Os três outros tipos de hipersensibilidade ( II, III e IV) têm em comum uma reação exagerada do sistema
IMUNOLOGIA BÁSICA Tópicos de Imunologia Celular e Molecular (Parte 2) Prof. M. Sc. Paulo Galdino Os três outros tipos de hipersensibilidade ( II, III e IV) têm em comum uma reação exagerada do sistema
[Caprine arthritis-encephalitis virus: isolation and molecular characterization of part of the gag gene]
![[Caprine arthritis-encephalitis virus: isolation and molecular characterization of part of the gag gene] [Caprine arthritis-encephalitis virus: isolation and molecular characterization of part of the gag gene]](/thumbs/71/65096849.jpg) Arq. Bras. Med. Vet. Zootec., v.56, n.2, p.135-142, 2004 Vírus da artrite encefalite caprina: isolamento e caracterização de parte do gene gag [Caprine arthritis-encephalitis virus: isolation and molecular
Arq. Bras. Med. Vet. Zootec., v.56, n.2, p.135-142, 2004 Vírus da artrite encefalite caprina: isolamento e caracterização de parte do gene gag [Caprine arthritis-encephalitis virus: isolation and molecular
O laboratório de biologia molecular no diagnóstico e acompanhamento da infeção pelo VIH-2
 Maria de Fátima Pinto Monteiro O laboratório de biologia molecular no diagnóstico e acompanhamento da infeção pelo VIH-2 Vila Nova de Gaia 2015 O presente trabalho destina-se a instruir o processo para
Maria de Fátima Pinto Monteiro O laboratório de biologia molecular no diagnóstico e acompanhamento da infeção pelo VIH-2 Vila Nova de Gaia 2015 O presente trabalho destina-se a instruir o processo para
Resposta imune inata (natural ou nativa)
 Universidade Federal do Pampa Campus Itaqui Curso de Nutrição Imunologia Resposta imune inata (natural ou nativa) Profa. Dra. Silvana Boeira Acreditou-se por muitos anos que a imunidade inata fosse inespecífica
Universidade Federal do Pampa Campus Itaqui Curso de Nutrição Imunologia Resposta imune inata (natural ou nativa) Profa. Dra. Silvana Boeira Acreditou-se por muitos anos que a imunidade inata fosse inespecífica
Vírus Características Gerais
 Vírus Características Gerais Características Gerais Do latim veneno Agentes diminutos visíveis por microscopia eletrônica 10 a 100 vezes menores que bactérias 20-30 nm Estruturalmente muito simples Apenas
Vírus Características Gerais Características Gerais Do latim veneno Agentes diminutos visíveis por microscopia eletrônica 10 a 100 vezes menores que bactérias 20-30 nm Estruturalmente muito simples Apenas
Resposta imune adquirida do tipo celular
 Universidade Federal do Pampa Campus Itaqui Curso de Nutrição Imunologia Resposta imune adquirida do tipo celular Profa. Dra. Silvana Boeira Imunidade adquirida Imunidade adaptativa = específica = adquirida
Universidade Federal do Pampa Campus Itaqui Curso de Nutrição Imunologia Resposta imune adquirida do tipo celular Profa. Dra. Silvana Boeira Imunidade adquirida Imunidade adaptativa = específica = adquirida
Cultura microbiológica do leite na fazenda: uma nova ferramenta para o diagnóstico de mastite
 sanidade Texto: Susana N. de Macedo Cristina S. Cortinhas Marcos V. dos Santos Cultura microbiológica do leite na fazenda: uma nova ferramenta para o diagnóstico de mastite O tratamento para os casos de
sanidade Texto: Susana N. de Macedo Cristina S. Cortinhas Marcos V. dos Santos Cultura microbiológica do leite na fazenda: uma nova ferramenta para o diagnóstico de mastite O tratamento para os casos de
Vírus, um grupo a parte.
 Vírus, um grupo a parte. Vírus, um grupo a parte. Estrutura típica de um vírus: 01)Observe a figura a seguir, onde está representado, esquematicamente, o vírus HIV e analise as proposições quanto à sua
Vírus, um grupo a parte. Vírus, um grupo a parte. Estrutura típica de um vírus: 01)Observe a figura a seguir, onde está representado, esquematicamente, o vírus HIV e analise as proposições quanto à sua
