Componente Especializado da Assistência Farmacêutica. Revisão da 2ª Edição: Carolina Rodrigues Gomes e Vera Lúcia Edais Pepe
|
|
|
- Bruna da Fonseca Godoi
- 6 Há anos
- Visualizações:
Transcrição
1 Componente Especializado da Assistência Farmacêutica Autora: Tatiana Aragão Figueiredo Revisão da 2ª Edição: Carolina Rodrigues Gomes e Vera Lúcia Edais Pepe Revisoras da 1ª Edição: Ana Márcia Messeder Sebrão Fernandes, Erica Carvalho da Silva Alves da Silveira, Marcela de Araújo Calfo Inicialmente este componente era denominado por Programa de Medicamentos Excepcionais e foi criado em Em 2006, com o Pacto pela Saúde (Portaria MS/GM nº 399, de 22 de fevereiro de 2006) e o Pacto pela Vida e de Gestão (Portaria MS/GM nº 699, de 30 de março de 2006), a Assistência Farmacêutica ganha importância e passa a ser um bloco de financiamento. Este bloco de financiamento, regulamentado por meio da Portaria GM/MS n o. 204, de 29 de janeiro de 2007, já possuía 3 componentes: o componente estratégico (Ver também Nota Técnica Componente Estratégico da Assistência Farmacêutica), o componente básico (Ver Também Nota Técnica Componente Básico da Assistência Farmacêutica) e o de medicamentos de dispensação excepcional. Este último componente passa a ser denominado Componente Especializado da Assistência Farmacêutica pela Portaria GM/MS nº 2.981, de 26 de novembro de A definição e a regulamentação do Componente Especializado da Assistência Farmacêutica são de responsabilidade do Ministério da Saúde (MS). Assim, o elenco de medicamentos é formulado pela esfera federal podendo, a partir desta, ser modificado por cada estado, segundo sua complexidade assistencial. As esferas estaduais são encarregadas também de formular e implementar um sistema logístico, envolvendo as etapas de seleção, programação, aquisição, armazenamento, distribuição, dispensação e promoção do uso racional dos medicamentos de dispensação excepcional. A elaboração desta lista também é importante para a melhoria da qualidade da assistência farmacêutica, uma vez que a incorporação de medicamentos tem buscado seguir, o que tem se
2 preconizado internacionalmente, a Medicina Baseada em Evidências (MBE). Sua existência facilita a gestão da assistência farmacêutica, a uniformização de procedimentos terapêuticos e de monitoramento do tratamento, com minimização dos riscos à saúde dos pacientes e, conseqüentemente, melhoria das condições de saúde. Uma parte dos medicamentos deste componente são também chamados de alto custo e são, geralmente, onerosos demais para a população arcar com o tratamento de longo prazo, seja porque seu valor unitário é alto, seja porque, apesar de valor unitário baixo, o tratamento torna-se custoso por ser prolongado. Eles podem ser destinados ao tratamento de doenças raras ou de baixa prevalência, tais como a doença de Crohn e lúpus eritematoso sistêmico, e também para doenças de alta prevalência, como asma grave e transtorno depressivo. Nesta última circunstância, os medicamentos serão destinados aos casos, nos quais o paciente apresentou intolerância, refratariedade aos medicamentos de primeira linha do tratamento ou quando da evolução para quadro clínico de maior gravidade. Com a Portaria GM/MS nº 2.981/09, os medicamentos do componente especializado estão, agora, divididos em três grupos com características, responsabilidades e formas de organização distintas. O grupo 1 é formado por medicamentos sob responsabilidade da União, o grupo 2 por medicamentos sob responsabilidade dos Estados e Distrito Federal e o grupo 3 por medicamentos sob responsabilidade dos Municípios e Distrito Federal (Brasil, 2009). O grupo 1 é constituído por medicamentos que foram alocados seguindo os critérios: 1) maior complexidade da doença a ser tratada ambulatorialmente; 2) refratariedade ou intolerância a primeira e/ou a segunda linha de tratamento; 3) medicamentos que representam elevado impacto financeiro para o Componente e medicamentos incluídos em ações de desenvolvimento produtivo no complexo industrial da saúde. O grupo 2 é constituído por medicamentos que preenchem critérios tais como: 1) menor complexidade da doença a ser tratada ambulatorialmente em relação aos elencados no Grupo 1 e; 2) refratariedade ou
3 intolerância à primeira linha de tratamento. Já o grupo 3 é constituído por fármacos constantes na Relação Nacional de Medicamentos Essenciais vigente e indicados pelos Protocolos Clínicos e Diretrizes Terapêuticas, publicados na versão final pelo Ministério da Saúde, como a primeira linha de cuidado para o tratamento das doenças contempladas neste Componente (Brasil, 2009). A Portaria GM/MS nº 2.981/09 ressalta que a incorporação efetiva de um medicamento nos Grupos 1, 2 e 3 ocorrerá somente após a publicação na versão final dos Protocolos Clínicos e Diretrizes Terapêuticas. Esses protocolos objetivam estabelecer os critérios de diagnóstico de cada doença, critérios de inclusão e exclusão de pacientes ao tratamento, as doses corretas dos medicamentos indicados, bem como, os mecanismos de controle, acompanhamento e avaliação. Foram elaborados, até dezembro de 2010, 64 Protocolos Clínicos e Diretrizes Terapêuticas, que abrangem cerca de 110 doenças e 168 fármacos. Encontramse publicados, em forma de livro, volumes I e II, 49 destes PCDT que pode ser acessado no sítio da Secretaria de Atenção à Saúde do Ministério da Saúde ( nela=1) (Ver também Nota Técnica O Formulário Terapêutico Nacional e os Protocolos Clínicos e Diretrizes Terapêuticas: extensões da seleção de medicamentos). No que tange ao financiamento do componente, a divisão segue àquela apresentada nos grupos de medicamentos, ou seja: (1) os medicamentos do Grupo 3 serão financiados de acordo com a regulamentação do Componente Básico da Assistência Farmacêutica, (2) os medicamentos pertencentes ao grupo 2 serão financiados pelos Estados e (3) os do grupo 1 serão financiados pelo Ministério da Saúde na forma de aquisição centralizada (Grupo 1A) e na forma de transferência de recursos financeiros (Grupo 1B) (Brasil, 2009). A execução do programa segue a lógica do financiamento para os Grupos de medicamentos 2 e 3. No entanto, nos medicamentos do Grupo 1B, a aquisição, a programação, o armazenamento, a distribuição e a dispensação são de responsabilidade das Secretarias Estaduais de Saúde. O mesmo se dá para os
4 medicamentos do Grupo 1A, exceto quanto à aquisição que é atribuição do Ministério da Saúde (Brasil, 2009). Para a dispensação de algum medicamento pertencente ao Componente Especializado, deverá ocorrer uma autorização baseada na avaliação da solicitação. A avaliação da solicitação deve considerar o Laudo para a Solicitação, a Avaliação e a Autorização de Medicamentos do Componente Especializado da Assistência Farmacêutica (LME), adequadamente preenchido, a prescrição médica contendo as informações exigidas na legislação vigente e todos os documentos exigidos nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final pelo Ministério da Saúde, conforme a doença e o medicamento solicitado (Brasil, 2009). A inclusão de um medicamento no Componente Especializado está atualmente sendo realizada pela Comissão de Incorporação de Tecnologias do Ministério da Saúde (CITEC), da qual participam diversas Secretarias do Ministério da Saúde, e que tem como atribuições recomendar a incorporação ou retirada de tecnologias no Sistema Único de Saúde (SUS) e na Saúde Suplementar; propor revisão dos Protocolos Terapêuticos e Diretrizes Clínicas, bem como a realização de estudos de avaliação de tecnologias em saúde. A composição da CITEC, seu mecanismo de atuação, os critérios e fluxo da análise de inclusão de novos medicamentos e solicitação de revisão de protocolos clínicos constam da Portaria MS/GM n o 2587, de 31 de outubro de A CITEC leva em consideração, em sua análise, a relevância e o impacto da incorporação do medicamento no SUS, a existência de evidências científicas de eficácia e segurança e, quando necessário, os estudos específicos sobre a tecnologia proposta, inclusive em comparação às demais incorporadas anteriormente. A Portaria GM/MS nº 2.981/09 teve alguns de seus artigos alterados e as listas dos anexos atualizadas pela Portaria GM/MS nº 3.439, de 11 de novembro de O Ministério da Saúde tem feito importantes esforços para a elaboração de estudos que auxiliem no conhecimento sobre estes medicamentos. A Secretaria
5 de Ciência Tecnologia e Insumos Estratégicos do Ministério da Saúde (SCTIE/MS) por meio de seus Departamentos de Assistência Farmacêutica (DAF) e de Ciência e Tecnologia, a Agência Nacional de Vigilância Sanitária (ANVISA) e a Secretaria de Vigilância em Saúde (SVS) vêm envidando esforços na produção de informação sobre os medicamentos e procedimentos de importância para o SUS. Bem como, financiando a realização de revisões sistemáticas referentes medicamentos e/ou tratamento de doenças sobre os quais ainda se tem pouca informação sistematizada no País. O Boletim Brasileiro de Avaliação Tecnológica em Saúde (BRATS), disponível no site é outra iniciativa importante e tem sido elaborado em colaboração entre a ANVISA, a Agência Nacional de Saúde Suplementar (ANS) e a SCTIE/MS para difundir informações responsáveis sobre as tecnologias para todos os atores envolvidos na atenção à saúde no Brasil. Algumas situações são bastante delicadas quanto a estes medicamentos, sobretudo no que diz respeito ao julgamento técnico da eficácia e segurança de medicamentos demandados ao SUS. Muitos são os fatores envolvidos quando de indicações outras que não as de seu registro no órgão regulatório, da prescrição de medicamentos não registrados no Brasil, ou que se encontram em uso ainda experimental sem que sua eficácia e segurança estejam bem estabelecidas. Alguns estudos sugerem que pode haver atraso na incorporação de medicamentos em PCDT e mesmo no registro pela ANVISA. Por outro lado, é conhecida a pressão realizada sobre os profissionais e mesmo sobre os usuários pela propaganda de medicamentos em suas diferentes técnicas, e as estratégias para a incorporação de medicamentos às listas oficiais, garantindo um mercado consumidor, financiado pelo setor público. Nestas situações é sempre recomendável que se investigue a inexistência de medicamento equivalente em eficácia e em segurança já disponível no SUS que ainda não tenha sido utilizado para a doença em questão. Igualmente desejável é que se certifique que há evidências científicas, mesmo que internacionais, de eficácia e segurança para a
6 condição patológica para a qual se destina o medicamento (Ver também Nota Técnica de Pesquisa Clínica e Regulamentação da Importação de Medicamentos). Considerando a constante atualização das normas, e a data de finalização da Nota Técnica em janeiro de 2011, é recomendável que se consulte a página da Assistência Farmacêutica do Ministério da Saúde e/ou a base de dados Saúde Legis a fim de verificar atualizações das normas referenciadas ou regulamentações de novas áreas. Referências Bibliográficas: 1. BLATT, R. C., FARIAS, M. R. Diagnóstico do Programa de Medicamentos Excepcionais do Estado de Santa Catarina Brasil. Latin American Journal of Pharmacy, v.26, n BRASIL. Portaria Nº GM/MS 27 de outubro de Aprova o Componente de Medicamentos de Dispensação Excepcional. Disponível em: Acessado em: 12/01/ BRASIL, Portaria GM/MS nº 2.981, de 26 de novembro de Aprova o Componente Especializado da Assistência Farmacêutica. Disponível em: Acessado em: 23/03/ BRASIL, Portaria GM/MS nº 3.439, de 11 de novembro de Altera os arts. 3º, 15, 16 e 63 e os Anexos I, II, III, IV e V à Portaria nº 2.981/GM/MS, de 26 de novembro de 2009, republicada em 1º de dezembro de Disponível em: Acessado em: 11/01/ BRASIL. CONSELHO NACIONAL DE SECRETÁRIOS DE SAÚDE. Ciência e Tecnologia em Saúde / Conselho Nacional de Secretários de Saúde. Brasília: CONASS, p. (Coleção Progestores. Para entender a gestão do SUS, 7) Cap. 4, p
7 6. BRASIL. Ministério da Saúde. Acesso aos Medicamentos, Compras Governamentais e Inclusão Social, Brasília, Fórum de Competitividade da Cadeia Produtiva Farmacêutica, p. Disponível em: ecnicas/anexo_2.pdf. Acessado em: 20/01/ DANTAS, N. S. & SILVA, R. R. Medicamentos excepcionais. Brasília: Escola Superior do Ministério Público da União, p. Disponível em: Medicamentos%20Excepcionais%20-%203a%20revisao.pdf. Acessado em: 09/01/ SILVA, R. C. S. Medicamentos excepcionais no âmbito da assistência farmacêutica no Brasil. [Mestrado] Fundação Oswaldo Cruz, Escola Nacional de Saúde Pública; p.
COMPONENTES DA ASSISTÊNCIA FARMACÊUTICA NO SUS
 TEXTOS DIDÁTICOS DO CEMED Nº 2.c Compreendendo o SUS e a Assistência Farmacêutica Módulo 2 Tema 7 Aula Expositiva 4 COMPONENTES DA ASSISTÊNCIA FARMACÊUTICA NO SUS Verlanda Lima Bontempo Secretaria de Estado
TEXTOS DIDÁTICOS DO CEMED Nº 2.c Compreendendo o SUS e a Assistência Farmacêutica Módulo 2 Tema 7 Aula Expositiva 4 COMPONENTES DA ASSISTÊNCIA FARMACÊUTICA NO SUS Verlanda Lima Bontempo Secretaria de Estado
Ampliação de concentrações de somatropina para o tratamento de pacientes com síndrome de Turner e de pacientes com deficiência de hormônio de
 Ampliação de concentrações de somatropina para o tratamento de pacientes com síndrome de Turner e de pacientes com deficiência de hormônio de crescimento Hipopituitarismo Nº 297 Outubro/2017 1 2017 Ministério
Ampliação de concentrações de somatropina para o tratamento de pacientes com síndrome de Turner e de pacientes com deficiência de hormônio de crescimento Hipopituitarismo Nº 297 Outubro/2017 1 2017 Ministério
Ministério da Saúde Consultoria Jurídica/Advocacia Geral da União
 Nota Técnica N 265/2013 Brasília, agosto de 2013. Princípio Ativo: cabergolina Nome Comercial 1 : Dostinex. Sumário 1. O que é a cabergolina?... 1 2. O medicamento possui registro na Agência Nacional de
Nota Técnica N 265/2013 Brasília, agosto de 2013. Princípio Ativo: cabergolina Nome Comercial 1 : Dostinex. Sumário 1. O que é a cabergolina?... 1 2. O medicamento possui registro na Agência Nacional de
PARECER CONSULTA N 22/2017
 PARECER CONSULTA N 22/2017 PROCESSO CONSULTA CRM-ES N 38/2013 INTERESSADO: Dr. FAT ASSUNTO: Dispensação de medicamento excepcional CONSELHEIRO PARECERISTA: Dr. Thales Gouveia Limeira APROVAÇÃO PLENÁRIA:
PARECER CONSULTA N 22/2017 PROCESSO CONSULTA CRM-ES N 38/2013 INTERESSADO: Dr. FAT ASSUNTO: Dispensação de medicamento excepcional CONSELHEIRO PARECERISTA: Dr. Thales Gouveia Limeira APROVAÇÃO PLENÁRIA:
A ASSISTÊNCIA FARMACÊUTICA NA REDE DE ATENÇÃO A SAÚDE. Salvador 2017
 A ASSISTÊNCIA FARMACÊUTICA NA REDE DE ATENÇÃO A SAÚDE Salvador 2017 Assistência Farmacêutica no SUS Lei nº. 8080/ 1990: Art. 6, 1, Al. d Reconhece a assistência terapêutica integral, inclusive farmacêutica,
A ASSISTÊNCIA FARMACÊUTICA NA REDE DE ATENÇÃO A SAÚDE Salvador 2017 Assistência Farmacêutica no SUS Lei nº. 8080/ 1990: Art. 6, 1, Al. d Reconhece a assistência terapêutica integral, inclusive farmacêutica,
Componente Básico da Assistência Farmacêutica. Revisoras 2ª Edição: Carolina Rodrigues Gomes e Vera Lúcia Edais Pepe
 Componente Básico da Assistência Farmacêutica Autora: Grazielle Silva de Lima Revisoras 2ª Edição: Carolina Rodrigues Gomes e Vera Lúcia Edais Pepe Revisoras 1ª Edição: Ana Márcia Messeder Sebrão Fernandes,
Componente Básico da Assistência Farmacêutica Autora: Grazielle Silva de Lima Revisoras 2ª Edição: Carolina Rodrigues Gomes e Vera Lúcia Edais Pepe Revisoras 1ª Edição: Ana Márcia Messeder Sebrão Fernandes,
Análise Crítica da Incorporação Tecnológica no SUS: Lei /11
 Análise Crítica da Incorporação Tecnológica no SUS: Lei 12.401/11 LENIR SANTOS 16 DE AGOSTO DE 2011 SALVADOR-BA Lenir Santos 25/8/2011 1 LEI 12.401/2011 ALTERA A LEI 8080/90 Objeto da Lei: explicitar o
Análise Crítica da Incorporação Tecnológica no SUS: Lei 12.401/11 LENIR SANTOS 16 DE AGOSTO DE 2011 SALVADOR-BA Lenir Santos 25/8/2011 1 LEI 12.401/2011 ALTERA A LEI 8080/90 Objeto da Lei: explicitar o
PORTARIA CONJUNTA Nº 19, DE 3 DE JULHO DE Aprova as Diretrizes Diagnósticas e Terapêuticas do Carcinoma de Mama.
 PORTARIA CONJUNTA Nº 19, DE 3 DE JULHO DE 2018 Aprova as Diretrizes Diagnósticas e Terapêuticas do Carcinoma de Mama. O SECRETÁRIO DE ATENÇÃO À SAÚDE e o SECRETÁRIO DE CIÊNCIA, TECNOLOGIA E INSUMOS ESTRATÉGICOS,
PORTARIA CONJUNTA Nº 19, DE 3 DE JULHO DE 2018 Aprova as Diretrizes Diagnósticas e Terapêuticas do Carcinoma de Mama. O SECRETÁRIO DE ATENÇÃO À SAÚDE e o SECRETÁRIO DE CIÊNCIA, TECNOLOGIA E INSUMOS ESTRATÉGICOS,
Antirretroviral etravirina 200mg para o tratamento da infecção pelo HIV
 Antirretroviral etravirina 200mg para o tratamento da infecção pelo HIV N o 255 Março/2017 1 2017 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que
Antirretroviral etravirina 200mg para o tratamento da infecção pelo HIV N o 255 Março/2017 1 2017 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que
Acesso aos medicamentos e globalização: questões éticas e sociais.
 Acesso aos medicamentos e globalização: questões éticas e sociais. Atelier 1 As Políticas Públicas de acesso aos medicamentos. O contexto e os principais determinantes da política brasileira de. Montreal
Acesso aos medicamentos e globalização: questões éticas e sociais. Atelier 1 As Políticas Públicas de acesso aos medicamentos. O contexto e os principais determinantes da política brasileira de. Montreal
RESOLUÇÃO-RDC No- 59, DE 24 DE NOVEMBRO DE 2009
 RESOLUÇÃO-RDC No- 59, DE 24 DE NOVEMBRO DE 2009 Dispõe sobre a implantação do Sistema Nacional de Controle de Medicamentos e definição dos mecanismos para rastreamento de medicamentos, por meio de tecnologia
RESOLUÇÃO-RDC No- 59, DE 24 DE NOVEMBRO DE 2009 Dispõe sobre a implantação do Sistema Nacional de Controle de Medicamentos e definição dos mecanismos para rastreamento de medicamentos, por meio de tecnologia
10º Encontro Nacional de Inovação em Fármacos e Medicamentos (ENIFarMed)
 10º Encontro Nacional de Inovação em Fármacos e Medicamentos (ENIFarMed) DIAGNÓSTICO MEDICAMENTO TRATAMENTO ACOMPANHAMENTO MULTIDISCIPLINAR ESTUDOS NO MUNDO SOBRE MEDICAMENTOS PARA DOENÇAS RARAS 1155
10º Encontro Nacional de Inovação em Fármacos e Medicamentos (ENIFarMed) DIAGNÓSTICO MEDICAMENTO TRATAMENTO ACOMPANHAMENTO MULTIDISCIPLINAR ESTUDOS NO MUNDO SOBRE MEDICAMENTOS PARA DOENÇAS RARAS 1155
Principais causas da não autorização das solicitações de medicamentos do componente especializado da assistência farmacêutica
 Principais causas da não autorização das solicitações de medicamentos do componente especializado da assistência farmacêutica Laura Martins Valdevite 1, Camila Francisca Tavares 1, Eveline Saad De Andrade
Principais causas da não autorização das solicitações de medicamentos do componente especializado da assistência farmacêutica Laura Martins Valdevite 1, Camila Francisca Tavares 1, Eveline Saad De Andrade
ASSISTÊNCIA FARMACÊUTICA CEMEPAR. Junho/2011
 ASSISTÊNCIA FARMACÊUTICA CEMEPAR Junho/2011 ASSISTÊNCIA FARMACÊUTICA - HISTÓRICO A Assistência Farmacêutica no Brasil, como política pública, teve início em 1971, com a instituição da Central de Medicamentos
ASSISTÊNCIA FARMACÊUTICA CEMEPAR Junho/2011 ASSISTÊNCIA FARMACÊUTICA - HISTÓRICO A Assistência Farmacêutica no Brasil, como política pública, teve início em 1971, com a instituição da Central de Medicamentos
Ministério da Saúde Consultoria Jurídica/Advocacia Geral da União
 Nota Técnica N 208/2013 Brasília, agosto de 2013. Princípio Ativo: ácido nicotínico Nomes Comerciais 1 : Acinic, Metri, Cordaptive. Sumário 1. O que é o ácido nicotínico?... 2 2. O medicamento possui registro
Nota Técnica N 208/2013 Brasília, agosto de 2013. Princípio Ativo: ácido nicotínico Nomes Comerciais 1 : Acinic, Metri, Cordaptive. Sumário 1. O que é o ácido nicotínico?... 2 2. O medicamento possui registro
Comissão Intergestores Tripartite - CTI. Relação Nacional de Ações e Serviços de Saúde - RENASES- Brasília 15 de dezembro 2011
 Comissão Intergestores Tripartite - CTI Relação Nacional de Ações e Serviços de Saúde - RENASES- Brasília 15 de dezembro 2011 Seção I Decreto Nº 7508 DE 28/06/2011 CAPÍTULO IV - DA ASSISTÊNCIA À SAÚDE
Comissão Intergestores Tripartite - CTI Relação Nacional de Ações e Serviços de Saúde - RENASES- Brasília 15 de dezembro 2011 Seção I Decreto Nº 7508 DE 28/06/2011 CAPÍTULO IV - DA ASSISTÊNCIA À SAÚDE
SECRETARIA DE ATENÇÃO À SAÚDE PORTARIA CONJUNTA Nº 4, DE 23 DE JANEIRO DE 2018 Aprova as Diretrizes Diagnósticas e Terapêuticas do Carcinoma de Mama.
 SECRETARIA DE ATENÇÃO À SAÚDE PORTARIA CONJUNTA Nº 4, DE 23 DE JANEIRO DE 2018 Aprova as Diretrizes Diagnósticas e Terapêuticas do Carcinoma de Mama. O SECRETÁRIO DE ATENÇÃO À SAÚDE e o SECRETÁRIO DE CIÊNCIA,
SECRETARIA DE ATENÇÃO À SAÚDE PORTARIA CONJUNTA Nº 4, DE 23 DE JANEIRO DE 2018 Aprova as Diretrizes Diagnósticas e Terapêuticas do Carcinoma de Mama. O SECRETÁRIO DE ATENÇÃO À SAÚDE e o SECRETÁRIO DE CIÊNCIA,
FINANCIAMENTO EM SAÚDE: A QUESTÃO DOS MEDICAMENTOS
 IV Jornada de Economia da Saúde da Associação Brasileira de Economia da Saúde (ABRES) Salvador /BA 20 a 22 agosto de 2008 Profª Iola Gurgel Grupo de Pesquisa em Economia da Saúde Faculdade de Medicina
IV Jornada de Economia da Saúde da Associação Brasileira de Economia da Saúde (ABRES) Salvador /BA 20 a 22 agosto de 2008 Profª Iola Gurgel Grupo de Pesquisa em Economia da Saúde Faculdade de Medicina
Diretrizes Nacionais de Assitência ao Parto Normal
 Diretrizes Nacionais de Assitência ao Parto Normal N o 211 Março/2017 2017 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que não seja para venda
Diretrizes Nacionais de Assitência ao Parto Normal N o 211 Março/2017 2017 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que não seja para venda
Ouvidoria de saúde em ação: uma experiência inovadora sobre as práticas dos serviços do SUS
 1.10 Ouvidoria de saúde em ação: uma experiência inovadora sobre as práticas dos serviços do SUS Ombudsman health in action: an innovative experience on the practices of the SUS services Ana Piterman Odontóloga,
1.10 Ouvidoria de saúde em ação: uma experiência inovadora sobre as práticas dos serviços do SUS Ombudsman health in action: an innovative experience on the practices of the SUS services Ana Piterman Odontóloga,
PORTARIA Nº 1.554, DE 30 DE JULHO DE 2013
 PORTARIA Nº 1.554, DE 30 DE JULHO DE 2013 Dispõe sobre as regras de financiamento e execução do Componente Especializado da Assistência Farmacêutica no âmbito do Sistema Único de Saúde (SUS). O MINISTRO
PORTARIA Nº 1.554, DE 30 DE JULHO DE 2013 Dispõe sobre as regras de financiamento e execução do Componente Especializado da Assistência Farmacêutica no âmbito do Sistema Único de Saúde (SUS). O MINISTRO
BRAZIL The New Hepatitis C Treatment Protocol
 BRAZIL The New Hepatitis C Treatment Protocol Paulo Roberto Lerias de Almeida Hospital Nossa Senhora da Conceição - Pôrto Alegre Secretaria Estadual da Saúde do Rio Grande do Sul Ministério da Saúde DISCLOSURE
BRAZIL The New Hepatitis C Treatment Protocol Paulo Roberto Lerias de Almeida Hospital Nossa Senhora da Conceição - Pôrto Alegre Secretaria Estadual da Saúde do Rio Grande do Sul Ministério da Saúde DISCLOSURE
REGIMENTO INTERNO DO COMITÊ DE IMPLEMENTAÇÃO DO PROGRAMA NACIONAL DE SEGURANÇA DO PACIENTE (CIPNSP)
 PORTARIA Nº 1.978, DE 12 DE SETEMBRO DE 2014 Diário Oficial da União; Poder Executivo, Brasília, DF, 15 set. 2014. Seção I, p. 54 Aprova o Regimento Interno do Comitê de Implementação Programa Nacional
PORTARIA Nº 1.978, DE 12 DE SETEMBRO DE 2014 Diário Oficial da União; Poder Executivo, Brasília, DF, 15 set. 2014. Seção I, p. 54 Aprova o Regimento Interno do Comitê de Implementação Programa Nacional
Comitê Executivo da Saúde
 Comitê Executivo da Saúde - Histórico - Audiência Pública - Recomendação 31/2010 CNJ - Aos Tribunais: adoção de medidas para subsidiar os magistrados e demais operadores com informações técnicas; criação
Comitê Executivo da Saúde - Histórico - Audiência Pública - Recomendação 31/2010 CNJ - Aos Tribunais: adoção de medidas para subsidiar os magistrados e demais operadores com informações técnicas; criação
Assistência Farmacêutica no SUS Política de Medicamentos. Dirce Cruz Marques. agosto/2010
 Assistência Farmacêutica no SUS Política de Medicamentos Dirce Cruz Marques agosto/2010 INSERÇÃO DOS MEDICAMENTOS Políticas públicas de saúde, medicamentos, etc Pesquisa de novos fármacos Prescrição Sistema
Assistência Farmacêutica no SUS Política de Medicamentos Dirce Cruz Marques agosto/2010 INSERÇÃO DOS MEDICAMENTOS Políticas públicas de saúde, medicamentos, etc Pesquisa de novos fármacos Prescrição Sistema
SEMINÁRIO: " O SETOR DE SAÚDE COMO MODELO
 SEMINÁRIO: " O SETOR DE SAÚDE COMO MODELO PRODUTIVO E DE DESENVOLVIMENTO ECONÔMICO " Painel 2: Alternativas para reduzir a judicialização e garantir uma assistência à saúde justa e equânime aos brasileiros
SEMINÁRIO: " O SETOR DE SAÚDE COMO MODELO PRODUTIVO E DE DESENVOLVIMENTO ECONÔMICO " Painel 2: Alternativas para reduzir a judicialização e garantir uma assistência à saúde justa e equânime aos brasileiros
FARMÁCIA CIDADÃ UM AUXÍLIO PARA A ASSISTÊNCIA FARMACÊUTICA
 FARMÁCIA CIDADÃ UM AUXÍLIO PARA A ASSISTÊNCIA FARMACÊUTICA RODRÍGUES, Layla Calazans 1 OLIVEIRA, Luciara 1 ZACCHI, Pâmela Santos 1 RABELO, Sâmara Graziela 1 SAMPAIO, Poliane Barbosa 2 INTRODUÇÃO O Projeto
FARMÁCIA CIDADÃ UM AUXÍLIO PARA A ASSISTÊNCIA FARMACÊUTICA RODRÍGUES, Layla Calazans 1 OLIVEIRA, Luciara 1 ZACCHI, Pâmela Santos 1 RABELO, Sâmara Graziela 1 SAMPAIO, Poliane Barbosa 2 INTRODUÇÃO O Projeto
AVALIAÇÃO DE TECNOLOGIAS EM SAÚDE (ATS)
 AVALIAÇÃO DE TECNOLOGIAS EM SAÚDE (ATS) TECNOLOGIAS EM SAÚDE Medicamentos, equipamentos e procedimentos técnicos, sistemas organizacionais, informacionais, educacionais e de suporte, e programas e protocolos
AVALIAÇÃO DE TECNOLOGIAS EM SAÚDE (ATS) TECNOLOGIAS EM SAÚDE Medicamentos, equipamentos e procedimentos técnicos, sistemas organizacionais, informacionais, educacionais e de suporte, e programas e protocolos
// 49. ISSN Tempus, actas de saúde colet, Brasília, 8(1), 49-56, mar, 2014// Noemia TAVARES 1 Rafael PINHEIRO 2
 Assistência Farmacêutica no SUS: avanços e desafios para a efetivação da assistência terapêutica integral Pharmaceutical Services in SUS: improvements and challenges for achieving the effectiveness of
Assistência Farmacêutica no SUS: avanços e desafios para a efetivação da assistência terapêutica integral Pharmaceutical Services in SUS: improvements and challenges for achieving the effectiveness of
AULA 4 POLÍTICA NACIONAL DE MEDICAMENTOS
 FACULDADE CATÓLICA RAINHA DO SERTÃO CURSO DE FARMÁCIA DISCIPLINA: INTRODUÇÃO ÀS CIÊNCIAS FARMACÊUTICAS PROFESSOR: MÁRCIO BATISTA AULA 4 POLÍTICA NACIONAL DE MEDICAMENTOS POLÍTICA Políticas configuram decisões
FACULDADE CATÓLICA RAINHA DO SERTÃO CURSO DE FARMÁCIA DISCIPLINA: INTRODUÇÃO ÀS CIÊNCIAS FARMACÊUTICAS PROFESSOR: MÁRCIO BATISTA AULA 4 POLÍTICA NACIONAL DE MEDICAMENTOS POLÍTICA Políticas configuram decisões
POLÍTICA NACIONAL DE MEDICAMENTOS. Sociedade Brasileira de Pneumologia e Tisiologia. Dirce Cruz Marques. Bem social X mercadoria Distorção no acesso
 POLÍTICA NACIONAL DE MEDICAMENTOS Sociedade Brasileira de Pneumologia e Tisiologia Dirce Cruz Marques abril/2010 INSERÇÃO DOS MEDICAMENTOS Políticas públicas de saúde, medicamentos, etc Pesquisa de novos
POLÍTICA NACIONAL DE MEDICAMENTOS Sociedade Brasileira de Pneumologia e Tisiologia Dirce Cruz Marques abril/2010 INSERÇÃO DOS MEDICAMENTOS Políticas públicas de saúde, medicamentos, etc Pesquisa de novos
Rio de Janeiro, 08 de dezembro de 2009
 IX Encontro Nacional de Economia da Saúde Rio de Janeiro, 08 de dezembro de 2009 O Estado da Arte da Avaliação de Tecnologias no Brasil Gabrielle Troncoso Gerência de Avaliação Econômica de Novas Tecnologias
IX Encontro Nacional de Economia da Saúde Rio de Janeiro, 08 de dezembro de 2009 O Estado da Arte da Avaliação de Tecnologias no Brasil Gabrielle Troncoso Gerência de Avaliação Econômica de Novas Tecnologias
Antoine Daher Presidente da Casa Hunter
 Antoine Daher Presidente da Casa Hunter ESTUDOS NO MUNDO SOBRE MEDICAMENTOS PARA DOENÇAS RARAS 1155 estudos Fonte: www.clinicaltrials.gov ESTUDOS NA AMÉRICA LATINA SOBRE DOENÇAS RARAS 36 estudos Fonte:
Antoine Daher Presidente da Casa Hunter ESTUDOS NO MUNDO SOBRE MEDICAMENTOS PARA DOENÇAS RARAS 1155 estudos Fonte: www.clinicaltrials.gov ESTUDOS NA AMÉRICA LATINA SOBRE DOENÇAS RARAS 36 estudos Fonte:
Avaliação de Tecnologia em Saúde na Qualificação dos Gastos
 IV Jornada de Economia da Saúde Agosto 2008 Avaliação de Tecnologia em Saúde na Qualificação dos Gastos Rosimary Almeida Gerência de Avaliação de Tecnologia - GEATS Diretoria de Desenvolvimento Setorial
IV Jornada de Economia da Saúde Agosto 2008 Avaliação de Tecnologia em Saúde na Qualificação dos Gastos Rosimary Almeida Gerência de Avaliação de Tecnologia - GEATS Diretoria de Desenvolvimento Setorial
Curso ASSISTÊNCIA FARMACÊUTICA Para Técnicos de Farmácia da Rede de Atenção Básica. Dirce Cruz Marques. setembro/2011
 Curso ASSISTÊNCIA FARMACÊUTICA Para Técnicos de Farmácia da Rede de Atenção Básica Dirce Cruz Marques setembro/2011 INSERÇÃO DOS MEDICAMENTOS Políticas públicas de saúde, medicamentos, etc Pesquisa de
Curso ASSISTÊNCIA FARMACÊUTICA Para Técnicos de Farmácia da Rede de Atenção Básica Dirce Cruz Marques setembro/2011 INSERÇÃO DOS MEDICAMENTOS Políticas públicas de saúde, medicamentos, etc Pesquisa de
Política Nacional de Medicamentos
 Universidade Federal de Juiz de Fora Tese de Doutorado em Saúde Coletiva Terezinha Noemides Pires Alves IMS - UERJ Rita de Cássia Padula Alves Vieira Ruben Araújo de Mattos 1 ANÁLISE A PARTIR DO CONTEXTO,
Universidade Federal de Juiz de Fora Tese de Doutorado em Saúde Coletiva Terezinha Noemides Pires Alves IMS - UERJ Rita de Cássia Padula Alves Vieira Ruben Araújo de Mattos 1 ANÁLISE A PARTIR DO CONTEXTO,
Curitiba Outubro/2017
 Curitiba Outubro/2017 Contexto Acesso a medicamentos do Componente Especializado e Elenco Complementar da SESA-PR 22 Farmácias Regionais + Farmácia do CPM 195.063 usuários cadastrados Patologias crônicas
Curitiba Outubro/2017 Contexto Acesso a medicamentos do Componente Especializado e Elenco Complementar da SESA-PR 22 Farmácias Regionais + Farmácia do CPM 195.063 usuários cadastrados Patologias crônicas
Ciência Regulatória: a regulação como instrumento de fomento às pesquisas de novas tecnologias em saúde. Brasília, 22/06/2016
 Ciência Regulatória: a regulação como instrumento de fomento às pesquisas de novas tecnologias em saúde. JARBAS BARBOSA Diretor-Presidente ANVISA Brasília, 22/06/2016 A ANVISA Primeira Agência da área
Ciência Regulatória: a regulação como instrumento de fomento às pesquisas de novas tecnologias em saúde. JARBAS BARBOSA Diretor-Presidente ANVISA Brasília, 22/06/2016 A ANVISA Primeira Agência da área
Art. 1º Este Decreto regulamenta a Lei 8.080/90, para dispor sobre a organização, o planejamento, a assistência e a articulação interfederativa.
 Legislação do SUS DECRETO 7.508 de 28 de Junho de 2011 Prof.ª: Andréa Paula Art. 1º Este Decreto regulamenta a Lei 8.080/90, para dispor sobre a organização, o planejamento, a assistência e a articulação
Legislação do SUS DECRETO 7.508 de 28 de Junho de 2011 Prof.ª: Andréa Paula Art. 1º Este Decreto regulamenta a Lei 8.080/90, para dispor sobre a organização, o planejamento, a assistência e a articulação
Diário Oficial da União Seção 01 DOU 05 de abril de 2007
 Diário Oficial da União Seção 01 DOU 05 de abril de 2007 RESOLUÇÃO RDC Nº 28, DE 4 DE ABRIL DE 2007 Dispõe sobre a priorização da análise técnica de petições, no âmbito da Gerência-Geral de Medicamentos
Diário Oficial da União Seção 01 DOU 05 de abril de 2007 RESOLUÇÃO RDC Nº 28, DE 4 DE ABRIL DE 2007 Dispõe sobre a priorização da análise técnica de petições, no âmbito da Gerência-Geral de Medicamentos
O Formulário Terapêutico Nacional, os Protocolos Clínicos e Diretrizes Terapêuticas: extensões da seleção de medicamentos.
 O Formulário Terapêutico Nacional, os Protocolos Clínicos e Diretrizes Terapêuticas: extensões da seleção de medicamentos. Autora: Vera Lúcia Edais Pepe Revisão da 2ª Edição: Carolina Rodrigues Gomes Revisoras
O Formulário Terapêutico Nacional, os Protocolos Clínicos e Diretrizes Terapêuticas: extensões da seleção de medicamentos. Autora: Vera Lúcia Edais Pepe Revisão da 2ª Edição: Carolina Rodrigues Gomes Revisoras
JUDICIALIZAÇÃO DA SAÚDE PEMC CREMESP 14/09/2017
 JUDICIALIZAÇÃO DA SAÚDE PEMC CREMESP 14/09/2017 Lei 3268/57. Art. 2 - O Conselho Federal e os Conselhos Regionais de Medicina são os órgãos supervisores da ética profissional em toda a República e ao mesmo
JUDICIALIZAÇÃO DA SAÚDE PEMC CREMESP 14/09/2017 Lei 3268/57. Art. 2 - O Conselho Federal e os Conselhos Regionais de Medicina são os órgãos supervisores da ética profissional em toda a República e ao mesmo
ANEXO I ATRIBUIÇÕES DAS EQUIPES DE REFERÊNCIA EM SAÚDE E RESPONSABILIDADES SETORIAIS INTERFEDERATIVAS
 ANEXO I ATRIBUIÇÕES DAS EQUIPES DE REFERÊNCIA EM SAÚDE E RESPONSABILIDADES SETORIAIS INTERFEDERATIVAS 1. Atribuições das equipes de referência em saúde As equipes de referência em saúde preconizadas nesta
ANEXO I ATRIBUIÇÕES DAS EQUIPES DE REFERÊNCIA EM SAÚDE E RESPONSABILIDADES SETORIAIS INTERFEDERATIVAS 1. Atribuições das equipes de referência em saúde As equipes de referência em saúde preconizadas nesta
Nota Técnica GAF/CCTIES nº 03, 19 de março de 2014
 Nota Técnica GAF/CCTIES nº 03, 19 de março de 2014 Assunto: Padronização do Fluxo de Dispensação dos medicamentos para Tratamento de Glaucoma nas Farmácias de Medicamentos Especializados (FME) da Secretaria
Nota Técnica GAF/CCTIES nº 03, 19 de março de 2014 Assunto: Padronização do Fluxo de Dispensação dos medicamentos para Tratamento de Glaucoma nas Farmácias de Medicamentos Especializados (FME) da Secretaria
PORTARIA Nº XX, de XX de xxxxxxx de 201X. O SECRETÁRIO MUNICIPAL DE SAÚDE, no uso de suas atribuições,
 PORTARIA Nº XX, de XX de xxxxxxx de 201X Aprova a Política Municipal de Assistência Farmacêutica O SECRETÁRIO MUNICIPAL DE SAÚDE, no uso de suas atribuições, Considerando a Lei 5.991, de 17 de dezembro
PORTARIA Nº XX, de XX de xxxxxxx de 201X Aprova a Política Municipal de Assistência Farmacêutica O SECRETÁRIO MUNICIPAL DE SAÚDE, no uso de suas atribuições, Considerando a Lei 5.991, de 17 de dezembro
Doxiciclina para tratamento da Donovanose
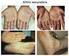 Doxiciclina para tratamento da Donovanose N o 156 Outubro/2015 1 2015 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que não seja para venda ou qualquer
Doxiciclina para tratamento da Donovanose N o 156 Outubro/2015 1 2015 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que não seja para venda ou qualquer
Considerando a Portaria do Ministério da Saúde nº /GM/MS, de 30 de outubro de 1998, que aprova a Política Nacional de Medicamentos;
 PORTARIA Nº. 552/2018 Súmula: Cria a Comissão de Farmácia e Terapêutica da Secretaria Municipal de Saúde de Tabaporã/MT e dá outras providências. O Prefeito Municipal de Tabaporã, Estado de Mato Grosso,
PORTARIA Nº. 552/2018 Súmula: Cria a Comissão de Farmácia e Terapêutica da Secretaria Municipal de Saúde de Tabaporã/MT e dá outras providências. O Prefeito Municipal de Tabaporã, Estado de Mato Grosso,
Circular 229/2013 São Paulo, 27 de maio de Provedor/Presidente Administrador
 1 Circular 229/2013 São Paulo, 27 de maio de 2013. Provedor/Presidente Administrador REF.: Lei nº 12.732, de 22/11/2012; e Portaria MS/GM nº 876, de 16/05/2013 - Primeiro tratamento do paciente com câncer
1 Circular 229/2013 São Paulo, 27 de maio de 2013. Provedor/Presidente Administrador REF.: Lei nº 12.732, de 22/11/2012; e Portaria MS/GM nº 876, de 16/05/2013 - Primeiro tratamento do paciente com câncer
Cipionato de Hidrocortisona, comprimidos de 10 mg e 20 mg, para tratamento de hiperplasia adrenal congênita de recém-nascidos diagnosticados no
 Cipionato de Hidrocortisona, comprimidos de 10 mg e 20 mg, para tratamento de hiperplasia adrenal congênita de recém-nascidos diagnosticados no programa nacional de triagem neonatal- PNTN. N o 146 Março/2015
Cipionato de Hidrocortisona, comprimidos de 10 mg e 20 mg, para tratamento de hiperplasia adrenal congênita de recém-nascidos diagnosticados no programa nacional de triagem neonatal- PNTN. N o 146 Março/2015
DELIBERAÇÃO CIB-RJ Nº 3618 DE 17 DE DEZEMBRO DE 2015
 DELIBERAÇÃO CIB-RJ Nº 3618 DE 17 DE DEZEMBRO DE 2015 PACTUA A NOTA TÉCNICA CONJUNTA SAECA/SAFIE/AS Nº 01/2015, QUE DISPÕE SOBRE O FLUXO DE DISPENSAÇÃO DE MEDICAMENTOS PARA TRATAMENTO DO GLAUCOMA, NO ÂMBITO
DELIBERAÇÃO CIB-RJ Nº 3618 DE 17 DE DEZEMBRO DE 2015 PACTUA A NOTA TÉCNICA CONJUNTA SAECA/SAFIE/AS Nº 01/2015, QUE DISPÕE SOBRE O FLUXO DE DISPENSAÇÃO DE MEDICAMENTOS PARA TRATAMENTO DO GLAUCOMA, NO ÂMBITO
ESTADO DA BAHIA PREFEITURA MUNICIPAL DE MADRE DE DEUS SECRETARIA MUNICIPAL DE SAUDE. PORTARIA SESAU Nº 002/2019 DE 10 de maio de 2019.
 Sexta-feira, 10 de Maio de 2019 Edição N 2.188 Caderno II PORTARIA SESAU Nº 002/2019 DE 10 de maio de 2019. Regulamenta o modo de atuação da Comissão de Farmácia e Terapêutica - CFT da Secretaria Municipal
Sexta-feira, 10 de Maio de 2019 Edição N 2.188 Caderno II PORTARIA SESAU Nº 002/2019 DE 10 de maio de 2019. Regulamenta o modo de atuação da Comissão de Farmácia e Terapêutica - CFT da Secretaria Municipal
PORTARIA Nº 4.283, DE 30 DE DEZEMBRO DE 2010
 ADVERTÊNCIA Este texto não substitui o publicado no Diário Oficial da União Ministério da Saúde Gabinete do Ministro PORTARIA Nº 4.283, DE 30 DE DEZEMBRO DE 2010 Aprova as diretrizes e estratégias para
ADVERTÊNCIA Este texto não substitui o publicado no Diário Oficial da União Ministério da Saúde Gabinete do Ministro PORTARIA Nº 4.283, DE 30 DE DEZEMBRO DE 2010 Aprova as diretrizes e estratégias para
A PROPOSTA DE INSERÇÃO DA ASSISTÊNCIA FARMACÊUTICA NAS REDES DE ATENÇÃO À SAÚDE NO ESTADO DE SÃO PAULO
 A PROPOSTA DE INSERÇÃO DA ASSISTÊNCIA FARMACÊUTICA NAS REDES DE ATENÇÃO À SAÚDE NO ESTADO DE SÃO PAULO Profa. Dra. Diretor Técnico de Departamento de Saúde Núcleo de Assistência Farmacêutica SES - SP Insistimos
A PROPOSTA DE INSERÇÃO DA ASSISTÊNCIA FARMACÊUTICA NAS REDES DE ATENÇÃO À SAÚDE NO ESTADO DE SÃO PAULO Profa. Dra. Diretor Técnico de Departamento de Saúde Núcleo de Assistência Farmacêutica SES - SP Insistimos
PORTARIA Nº 698/GM DE 30 DE MARÇO DE O MINISTRO DE ESTADO DA SAÚDE, no uso de suas atribuições, e
 PORTARIA Nº 698/GM DE 30 DE MARÇO DE 2006. Define que o custeio das ações de saúde é de responsabilidade das três esferas de gestão do SUS, observado o disposto na Constituição Federal e na Lei Orgânica
PORTARIA Nº 698/GM DE 30 DE MARÇO DE 2006. Define que o custeio das ações de saúde é de responsabilidade das três esferas de gestão do SUS, observado o disposto na Constituição Federal e na Lei Orgânica
PUBLICADA A PRIMEIRA PORTARIA BRASILEIRA SOBRE FARMÁCIA HOSPITALAR
 PUBLICADA A PRIMEIRA PORTARIA BRASILEIRA SOBRE FARMÁCIA HOSPITALAR Os farmacêuticos hospitalares brasileiros iniciam o ano de 2011, tendo como marco político a publicação da Portaria do Ministro da Saúde
PUBLICADA A PRIMEIRA PORTARIA BRASILEIRA SOBRE FARMÁCIA HOSPITALAR Os farmacêuticos hospitalares brasileiros iniciam o ano de 2011, tendo como marco político a publicação da Portaria do Ministro da Saúde
AS PLANTAS MEDICINAIS E A FITOTERAPIA NO SISTEMA OFICIAL DE SAÚDE 1º Seminário Internacional de Práticas Integrativas e Complementares em Saúde
 MINISTÉRIO DA SAÚDE SECRETARIA DE CIÊNCIA, TECNOLOGIA E INSUMOS ESTRATÉGICOS DEPARTAMENTO DE ASSISTÊNCIA FARMACÊUTICA E INSUMOS ESTRATÉGICOS AS PLANTAS MEDICINAIS E A FITOTERAPIA NO SISTEMA OFICIAL DE
MINISTÉRIO DA SAÚDE SECRETARIA DE CIÊNCIA, TECNOLOGIA E INSUMOS ESTRATÉGICOS DEPARTAMENTO DE ASSISTÊNCIA FARMACÊUTICA E INSUMOS ESTRATÉGICOS AS PLANTAS MEDICINAIS E A FITOTERAPIA NO SISTEMA OFICIAL DE
Ampliação de uso do naproxeno para osteoartrite de joelho e quadril
 Ampliação de uso do naproxeno para osteoartrite de joelho e quadril N o 298 Agosto/2017 1 2017 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que
Ampliação de uso do naproxeno para osteoartrite de joelho e quadril N o 298 Agosto/2017 1 2017 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que
O papel dos laboratórios oficiais no acesso a medicamentos no SUS
 O papel dos laboratórios oficiais no acesso a medicamentos no SUS Os desafios da expansão de produção de fármacos para os componentes as Assistência Farmacêutica No Brasil, o desabastecimento de medicamentos
O papel dos laboratórios oficiais no acesso a medicamentos no SUS Os desafios da expansão de produção de fármacos para os componentes as Assistência Farmacêutica No Brasil, o desabastecimento de medicamentos
RELATÓRIO PARA A. SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS
 RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS RELATÓRIO PARA A SOCIEDADE Este relatório é uma versão resumida do relatório técnico
RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS RELATÓRIO PARA A SOCIEDADE Este relatório é uma versão resumida do relatório técnico
III Fórum Nacional de Produtos para Saúde Brasília, setembro Inovação é acesso. Fabiana Raynal Floriano DGITS/SCTIE/MS
 III Fórum Nacional de Produtos para Saúde Brasília, setembro 2016 Inovação é acesso Fabiana Raynal Floriano DGITS/SCTIE/MS INOVAÇÃO Definição: introdução de novidade ou aperfeiçoamento no ambiente produtivo
III Fórum Nacional de Produtos para Saúde Brasília, setembro 2016 Inovação é acesso Fabiana Raynal Floriano DGITS/SCTIE/MS INOVAÇÃO Definição: introdução de novidade ou aperfeiçoamento no ambiente produtivo
SUMÁRIO ATENÇÃO E ASSISTÊNCIA FARMACÊUTICAS CAPÍTULO 1 CÓDIGO DE ÉTICA DA PROFISSÃO FARMACÊUTICA E ATUAÇÃO NA FARMÁCIA COMERCIAL CAPÍTULO 2
 SUMÁRIO ATENÇÃO E ASSISTÊNCIA FARMACÊUTICAS CAPÍTULO 1 1. Introdução...12 2. Leis, Portarias e Resoluções que Abordam a Atenção e Assistência Farmacêutica 12 1. Política Nacional de Medicamentos - Portaria
SUMÁRIO ATENÇÃO E ASSISTÊNCIA FARMACÊUTICAS CAPÍTULO 1 1. Introdução...12 2. Leis, Portarias e Resoluções que Abordam a Atenção e Assistência Farmacêutica 12 1. Política Nacional de Medicamentos - Portaria
PREFEITURA MUNICIPAL DE GUAÇUÍ Estado do Espírito Santo
 Decreto n.º 10.430, de 21 de novembro de 2017 APROVA A INSTRUÇÃO NORMATIVA SSP Nº 03/2017. legais; A Prefeita Municipal de Guaçuí,, no uso de suas atribuições CONSIDERANDO o Processo nº 4.401/2017, da
Decreto n.º 10.430, de 21 de novembro de 2017 APROVA A INSTRUÇÃO NORMATIVA SSP Nº 03/2017. legais; A Prefeita Municipal de Guaçuí,, no uso de suas atribuições CONSIDERANDO o Processo nº 4.401/2017, da
Agência Nacional de Vigilância Sanitária. Consulta Pública n 344, de 06 de junho de 2017 D.O.U de 07/06/2017
 Agência Nacional de Vigilância Sanitária www.anvisa.gov.br Consulta Pública n 344, de 06 de junho de 2017 D.O.U de 07/06/2017 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso das
Agência Nacional de Vigilância Sanitária www.anvisa.gov.br Consulta Pública n 344, de 06 de junho de 2017 D.O.U de 07/06/2017 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso das
Padrão de Terminologia/TISS
 Padrão de Terminologia no âmbito da Saúde Suplementar Parte integrante da TISS Padrão de Terminologia/TISS Agência Nacional de Saúde Suplementar Autarquia vinculada ao Ministério da Saúde Finalidade institucional
Padrão de Terminologia no âmbito da Saúde Suplementar Parte integrante da TISS Padrão de Terminologia/TISS Agência Nacional de Saúde Suplementar Autarquia vinculada ao Ministério da Saúde Finalidade institucional
Ministério da Saúde PORTARIA DE CONSOLIDAÇÃO Nº 2, DE 28 DE SETEMBRO DE 2017
 ADVERTÊNCIA Este texto não substitui o publicado no Diário Oficial da União Ministério da Saúde Gabinete do Ministro PORTARIA DE CONSOLIDAÇÃO Nº 2, DE 28 DE SETEMBRO DE 2017 Consolidação das normas sobre
ADVERTÊNCIA Este texto não substitui o publicado no Diário Oficial da União Ministério da Saúde Gabinete do Ministro PORTARIA DE CONSOLIDAÇÃO Nº 2, DE 28 DE SETEMBRO DE 2017 Consolidação das normas sobre
Exposição de Motivos da Revisão do Rol de Procedimentos da ANS Introdução
 Exposição de Motivos da Revisão do Rol de Procedimentos da ANS - 2007 Introdução A Agência Nacional de Saúde Suplementar (ANS) tem, dentre suas atribuições estabelecidas pela Lei 9.961, de 28 de janeiro
Exposição de Motivos da Revisão do Rol de Procedimentos da ANS - 2007 Introdução A Agência Nacional de Saúde Suplementar (ANS) tem, dentre suas atribuições estabelecidas pela Lei 9.961, de 28 de janeiro
ALTERA O CADASTRAMENTO DOS CENTROS DE REFERÊNCIA EM SAÚDE DO TRABALHADOR NO SCNES
 Circular 489/2013 São Paulo, 29 de Outubro de 2013. PROVEDOR(A) ADMINISTRADOR(A) ALTERA O CADASTRAMENTO DOS CENTROS DE REFERÊNCIA EM SAÚDE DO TRABALHADOR NO SCNES Diário Oficial da União Nº 208, Seção
Circular 489/2013 São Paulo, 29 de Outubro de 2013. PROVEDOR(A) ADMINISTRADOR(A) ALTERA O CADASTRAMENTO DOS CENTROS DE REFERÊNCIA EM SAÚDE DO TRABALHADOR NO SCNES Diário Oficial da União Nº 208, Seção
Política Nacional de Atenção Básica. Portaria nº 648/GM de 28 de Março de 2006
 Política Nacional de Atenção Básica Portaria nº 648/GM de 28 de Março de 2006 ! A Atenção Básica caracteriza-se por um conjunto de ações de saúde no âmbito individual e coletivo que abrangem a promoção
Política Nacional de Atenção Básica Portaria nº 648/GM de 28 de Março de 2006 ! A Atenção Básica caracteriza-se por um conjunto de ações de saúde no âmbito individual e coletivo que abrangem a promoção
ACESSO A MEDICAMENTOS DE ALTO CUSTO NO BRASIL: O COMPONENTE ESPECIALIZADO DA ASSISTÊNCIA FARMACÊUTICA
 ACESSO A MEDICAMENTOS DE ALTO CUSTO NO BRASIL: O COMPONENTE ESPECIALIZADO DA ASSISTÊNCIA FARMACÊUTICA Marina R M Rover 1 SUS Política Nacional de Assistência Farmacêutica Componentes: Componente Especializado
ACESSO A MEDICAMENTOS DE ALTO CUSTO NO BRASIL: O COMPONENTE ESPECIALIZADO DA ASSISTÊNCIA FARMACÊUTICA Marina R M Rover 1 SUS Política Nacional de Assistência Farmacêutica Componentes: Componente Especializado
Diário Oficial Imprensa Nacional.
 Diário Oficial Imprensa Nacional. REPÚBLICA FEDERATIVA DO BRASIL BRASÍLIA - DF Nº 229 1º/12/09 p.71 MINISTÉRIO DA SAÚDE GABINETE DO MINISTRO PORTARIA Nº 2.981, DE 26 DE NOVEMBRO DE 2009(*) Aprova o Componente
Diário Oficial Imprensa Nacional. REPÚBLICA FEDERATIVA DO BRASIL BRASÍLIA - DF Nº 229 1º/12/09 p.71 MINISTÉRIO DA SAÚDE GABINETE DO MINISTRO PORTARIA Nº 2.981, DE 26 DE NOVEMBRO DE 2009(*) Aprova o Componente
Uso Racional de Medicamentos. Felipe Dias Carvalho Consultor Nacional de Desenvolvimento e Inovação Tecnológica em Saúde OPAS/OMS
 Uso Racional de Medicamentos Felipe Dias Carvalho Consultor Nacional de Desenvolvimento e Inovação Tecnológica em Saúde OPAS/OMS Conceito URM - OMS Existe uso racional quando os pacientes recebem medicamentos
Uso Racional de Medicamentos Felipe Dias Carvalho Consultor Nacional de Desenvolvimento e Inovação Tecnológica em Saúde OPAS/OMS Conceito URM - OMS Existe uso racional quando os pacientes recebem medicamentos
NOTA CONASEMS PORTARIA n. 748 de 27/03/2018 DOU 28/03/2018
 NOTA CONASEMS PORTARIA n. 748 de 27/03/2018 DOU 28/03/2018 O Financiamento da Saúde, de acordo com a Constituição Federal de 1988, é responsabilidade das três esferas de Governo, com recursos oriundos
NOTA CONASEMS PORTARIA n. 748 de 27/03/2018 DOU 28/03/2018 O Financiamento da Saúde, de acordo com a Constituição Federal de 1988, é responsabilidade das três esferas de Governo, com recursos oriundos
Ministério da Saúde Gabinete do Ministro PORTARIA Nº 2.915, DE 12 DE DEZEMBRO DE 2011
 Ministério da Saúde Gabinete do Ministro PORTARIA Nº 2.915, DE 12 DE DEZEMBRO DE 2011 Institui a Rede Brasileira de Avaliação de Tecnologias em Saúde (REBRATS). O MINISTRO DE ESTADO DA SAÚDE, no uso das
Ministério da Saúde Gabinete do Ministro PORTARIA Nº 2.915, DE 12 DE DEZEMBRO DE 2011 Institui a Rede Brasileira de Avaliação de Tecnologias em Saúde (REBRATS). O MINISTRO DE ESTADO DA SAÚDE, no uso das
PORTARIA Nº 195, DE 6 DE FEVEREIRO DE 2019
 PORTARIA Nº 195, DE 6 DE FEVEREIRO DE 2019 Prorroga a estratégia de ampliação do acesso aos Procedimentos Cirúrgicos Eletivos no âmbito do Sistema Único de Saúde (SUS). O MINISTRO DE ESTADO DA SAÚDE, no
PORTARIA Nº 195, DE 6 DE FEVEREIRO DE 2019 Prorroga a estratégia de ampliação do acesso aos Procedimentos Cirúrgicos Eletivos no âmbito do Sistema Único de Saúde (SUS). O MINISTRO DE ESTADO DA SAÚDE, no
ENFERMAGEM LEGISLAÇÃO EM SAÚDE
 ENFERMAGEM LEGISLAÇÃO EM SAÚDE Sistema Único de Saúde - SUS: Constituição Federal, Lei Orgânica da Saúde - Lei nº 8.080 de 1990 e outras normas Parte 5 Profª. Tatiane da Silva Campos LEI Nº 8.080, DE 19
ENFERMAGEM LEGISLAÇÃO EM SAÚDE Sistema Único de Saúde - SUS: Constituição Federal, Lei Orgânica da Saúde - Lei nº 8.080 de 1990 e outras normas Parte 5 Profª. Tatiane da Silva Campos LEI Nº 8.080, DE 19
Publicada no DOU em 31/12/2010 PORTARIA Nº 4.283, DE 30 DE DEZEMBRO DE 2010
 Publicada no DOU em 31/12/2010 PORTARIA Nº 4.283, DE 30 DE DEZEMBRO DE 2010 Aprova as diretrizes e estratégias fortalecimento e aprimoramento das ações e serviços de farmácia no âmbito dos hospitais. O
Publicada no DOU em 31/12/2010 PORTARIA Nº 4.283, DE 30 DE DEZEMBRO DE 2010 Aprova as diretrizes e estratégias fortalecimento e aprimoramento das ações e serviços de farmácia no âmbito dos hospitais. O
CONGRESSO DE SECRETÁRIOS MUNICIPAIS DE SAÚDE DE SÃO PAULO. Implicações na prática da Assistência à Saúde no SUS. Mar/2012
 CONGRESSO DE SECRETÁRIOS MUNICIPAIS DE SAÚDE DE SÃO PAULO Implicações na prática da Assistência à Saúde no SUS Mar/2012 O SUS HOJE IDSUS aponta problemas de acesso e de qualidade do sistema na maioria
CONGRESSO DE SECRETÁRIOS MUNICIPAIS DE SAÚDE DE SÃO PAULO Implicações na prática da Assistência à Saúde no SUS Mar/2012 O SUS HOJE IDSUS aponta problemas de acesso e de qualidade do sistema na maioria
Responsabilidades e Diretrizes para execução e financiamento de ações de Vigilância em Saúde
 Responsabilidades e Diretrizes para execução e financiamento de ações de Vigilância em Saúde Departamento de Gestão da Vigilância em Saúde-DEGEVS Secretaria de Vigilância em Saúde Ministério da Saúde dagvs@saude.gov.br
Responsabilidades e Diretrizes para execução e financiamento de ações de Vigilância em Saúde Departamento de Gestão da Vigilância em Saúde-DEGEVS Secretaria de Vigilância em Saúde Ministério da Saúde dagvs@saude.gov.br
Estudos de avaliação de tecnologias em saúde e a incorporação de novas tecnologias no sistema de saúde
 ABRES 2014 - XI Encontro Nacional de Economia da Saúde & VI Encontro Latino Americano de Economia da Saúde Estudos de avaliação de tecnologias em saúde e a incorporação de novas tecnologias no sistema
ABRES 2014 - XI Encontro Nacional de Economia da Saúde & VI Encontro Latino Americano de Economia da Saúde Estudos de avaliação de tecnologias em saúde e a incorporação de novas tecnologias no sistema
Circular 220/2016 São Paulo, 12 de Maio de 2016.
 Circular 220/2016 São Paulo, 12 de Maio de 2016. PROVEDOR(A) ADMINISTRADOR(A) PORTARIA No- 498, DE 11 DE MAIO DE 2016. Diário Oficial da União Nº 90, quinta-feira, 12 de Maio de 2016. Prezados Senhores,
Circular 220/2016 São Paulo, 12 de Maio de 2016. PROVEDOR(A) ADMINISTRADOR(A) PORTARIA No- 498, DE 11 DE MAIO DE 2016. Diário Oficial da União Nº 90, quinta-feira, 12 de Maio de 2016. Prezados Senhores,
Regimento Interno da Comissão de Farmácia e Terapêutica
 Regimento Interno da Comissão de Farmácia e Terapêutica Da natureza e finalidade Art. 1º - A Comissão de Farmácia e Terapêutica (CFT) é instância de caráter consultivo e deliberativo da Direção Médica
Regimento Interno da Comissão de Farmácia e Terapêutica Da natureza e finalidade Art. 1º - A Comissão de Farmácia e Terapêutica (CFT) é instância de caráter consultivo e deliberativo da Direção Médica
Financiamento. Consultório na Rua PORTARIA Nº 123, DE 25 DE JANEIRO DE Sem portaria convivência e cultura. Estabelece, no âmbito Especializada/
 Rede De (RAPS) Componentes da RAPS Pontos da RAPS Nº da Portaria de Financiamento Caracterização da portaria Atenção Básica Unidade Básica de PORTARIA 2488/11 Institui a Política Saúde Nacional de Atenção
Rede De (RAPS) Componentes da RAPS Pontos da RAPS Nº da Portaria de Financiamento Caracterização da portaria Atenção Básica Unidade Básica de PORTARIA 2488/11 Institui a Política Saúde Nacional de Atenção
Reunião Plenária do Conselho Federal de Medicina
 Reunião Plenária do Conselho Federal de Medicina Brasília DF, 29 de maio de 2.014 Tarcísio José Palhano Assessor da Presidência do Conselho Federal de Farmácia (CFF) Coordenador Técnico-Científico do Centro
Reunião Plenária do Conselho Federal de Medicina Brasília DF, 29 de maio de 2.014 Tarcísio José Palhano Assessor da Presidência do Conselho Federal de Farmácia (CFF) Coordenador Técnico-Científico do Centro
DELIBERAÇÃO CIB-SUS/MG Nº 2.512, DE 19 DE JULHO DE 2017.
 DELIBERAÇÃO CIB-SUS/MG Nº 2.512, DE 19 DE JULHO DE 2017. Aprova o Protocolo Estadual para Dispensação de Insumos para Monitoramento de Diabetes no âmbito do SUS-MG. A Comissão Intergestores Bipartite do
DELIBERAÇÃO CIB-SUS/MG Nº 2.512, DE 19 DE JULHO DE 2017. Aprova o Protocolo Estadual para Dispensação de Insumos para Monitoramento de Diabetes no âmbito do SUS-MG. A Comissão Intergestores Bipartite do
Prefeitura Municipal de Esteio Oficina 6 : A organização de protocolos e gestão macro da Vigilância Sanitária
 Prefeitura Municipal de Esteio Oficina 6 : A organização de protocolos e gestão macro da Vigilância Sanitária Palestrante: Ana Paula Macedo Vigilância Sanitária Entende-se por vigilância sanitária um conjunto
Prefeitura Municipal de Esteio Oficina 6 : A organização de protocolos e gestão macro da Vigilância Sanitária Palestrante: Ana Paula Macedo Vigilância Sanitária Entende-se por vigilância sanitária um conjunto
CURSO DE FORMAÇÃO CONTINUADA PARA PROFESSORES E PROFISSIONAIS DE SAÚDE A PRESCRIÇÃO E O ACESSO AOS MEDICAMENTOS NO SUS
 CURSO DE FORMAÇÃO CONTINUADA PARA PROFESSORES E PROFISSIONAIS DE SAÚDE A PRESCRIÇÃO E O ACESSO AOS MEDICAMENTOS NO SUS Elizangela Braga Andrade Orientadora: Profª. Drª. Paulete Goldenberg 1- INTRODUÇÃO:
CURSO DE FORMAÇÃO CONTINUADA PARA PROFESSORES E PROFISSIONAIS DE SAÚDE A PRESCRIÇÃO E O ACESSO AOS MEDICAMENTOS NO SUS Elizangela Braga Andrade Orientadora: Profª. Drª. Paulete Goldenberg 1- INTRODUÇÃO:
 RESOLUÇÃO-RDC N 21, DE 10 DE ABRIL DE 2013 Altera a RDC nº 45, de 23 de junho de 2008, que dispõe sobre o procedimento administrativo relativo à prévia anuência da Anvisa para a concessão de patentes para
RESOLUÇÃO-RDC N 21, DE 10 DE ABRIL DE 2013 Altera a RDC nº 45, de 23 de junho de 2008, que dispõe sobre o procedimento administrativo relativo à prévia anuência da Anvisa para a concessão de patentes para
do Trabalhador e da Trabalhadora
 Ministério da Saúde Secretaria de Vigilância em Saúde Departamento de Vigilância em Saúde Ambiental e Saúde do Trabalhador Coordenação Geral de Saúde do Trabalhador Política Nacional de Saúde do Trabalhador
Ministério da Saúde Secretaria de Vigilância em Saúde Departamento de Vigilância em Saúde Ambiental e Saúde do Trabalhador Coordenação Geral de Saúde do Trabalhador Política Nacional de Saúde do Trabalhador
PORTARIA No , DE 11 DE NOVEMBRO DE 2009
 PORTARIA No- 2.728, DE 11 DE NOVEMBRO DE 2009 Dispõe sobre a Rede Nacional de Atenção Integral à Saúde do Trabalhador (RENAST) e dá outras providências. O MINISTRO DE ESTADO DA SAÚDE, no uso das atribuições
PORTARIA No- 2.728, DE 11 DE NOVEMBRO DE 2009 Dispõe sobre a Rede Nacional de Atenção Integral à Saúde do Trabalhador (RENAST) e dá outras providências. O MINISTRO DE ESTADO DA SAÚDE, no uso das atribuições
As novas tecnologias e seus impactos no mercado de Saúde Suplementar
 As novas tecnologias e seus impactos no mercado de Saúde Suplementar Tecnologias em saúde: considerações iniciais O que é tecnologia em saúde? Medicamentos, equipamentos, dispositivos e procedimentos medico-cirúrgicos
As novas tecnologias e seus impactos no mercado de Saúde Suplementar Tecnologias em saúde: considerações iniciais O que é tecnologia em saúde? Medicamentos, equipamentos, dispositivos e procedimentos medico-cirúrgicos
AULA 3 DIREITO À SAÚDE SISTEMA ÚNICO DE SAÚDE
 FACULDADE CATÓLICA RAINHA DO SERTÃO CURSO DE FARMÁCIA DISCIPLINA: INTRODUÇÃO ÀS CIÊNCIAS FARMACÊUTICAS PROFESSOR: MÁRCIO BATISTA AULA 3 DIREITO À SAÚDE SISTEMA ÚNICO DE SAÚDE DIREITO À SAÚDE DIREITO À
FACULDADE CATÓLICA RAINHA DO SERTÃO CURSO DE FARMÁCIA DISCIPLINA: INTRODUÇÃO ÀS CIÊNCIAS FARMACÊUTICAS PROFESSOR: MÁRCIO BATISTA AULA 3 DIREITO À SAÚDE SISTEMA ÚNICO DE SAÚDE DIREITO À SAÚDE DIREITO À
Política Nacional de Atenção Integral às Pessoas com Doenças Raras no SUS. Brasília, 29 de maio de 2014
 Política Nacional de Atenção Integral às Pessoas com Doenças Raras no SUS Brasília, 29 de maio de 2014 Doenças raras OMS: afeta até 65 pessoas/100 mil indivíduos (1,3:2.000). Acometem de 6% a 8% da população.
Política Nacional de Atenção Integral às Pessoas com Doenças Raras no SUS Brasília, 29 de maio de 2014 Doenças raras OMS: afeta até 65 pessoas/100 mil indivíduos (1,3:2.000). Acometem de 6% a 8% da população.
PORTARIA Nº 196, DE 6 DE FEVEREIRO DE 2012
 Legislações - GM Ter, 7 de Fevereiro de 22 : PORTARIA Nº 96, DE 6 DE FEVEREIRO DE 22 Aprova a diretriz para acompanhamento e tratamento de pacientes portadores de implantes mamários das marcas PIP (Poly
Legislações - GM Ter, 7 de Fevereiro de 22 : PORTARIA Nº 96, DE 6 DE FEVEREIRO DE 22 Aprova a diretriz para acompanhamento e tratamento de pacientes portadores de implantes mamários das marcas PIP (Poly
Programa Nacional para a Prevenção e o Controle das Hepatites Virais - Portaria 263 de 5/2/2002
 Programa Nacional para a Prevenção e o Controle das Hepatites Virais - Portaria 263 de 5/2/2002 Ementa: criação de mecanismos para organizar, articular e integrar as ações voltadas à prevenção e ao controle
Programa Nacional para a Prevenção e o Controle das Hepatites Virais - Portaria 263 de 5/2/2002 Ementa: criação de mecanismos para organizar, articular e integrar as ações voltadas à prevenção e ao controle
Política Nacional de Saúde do Trabalhador e da Trabalhadora
 Ministério da Saúde Secretaria de Vigilância em Saúde Departamento de Vigilância em Saúde Ambiental e Saúde do Trabalhador Coordenação Geral de Saúde do Trabalhador Política Nacional de Saúde do Trabalhador
Ministério da Saúde Secretaria de Vigilância em Saúde Departamento de Vigilância em Saúde Ambiental e Saúde do Trabalhador Coordenação Geral de Saúde do Trabalhador Política Nacional de Saúde do Trabalhador
Conselho Federal de Farmácia
 1 RESOLUÇÃO Nº 549, de 25 de agosto de 2011 Ementa: Dispõe sobre as atribuições do farmacêutico no exercício da gestão de produtos para a saúde, e dá outras providências. O Conselho Federal de Farmácia,
1 RESOLUÇÃO Nº 549, de 25 de agosto de 2011 Ementa: Dispõe sobre as atribuições do farmacêutico no exercício da gestão de produtos para a saúde, e dá outras providências. O Conselho Federal de Farmácia,
100 QUESTÕES DE SAÚDE PÚBLICA PARA AGENTE COMUNITÁRIO
 Caro Leitor, A equipe técnica do Concurseiro da Saúde empenha-se em desenvolver apostilas e materiais atualizados de acordo com as leis recentemente publicadas a fim de estar sempre em consonância com
Caro Leitor, A equipe técnica do Concurseiro da Saúde empenha-se em desenvolver apostilas e materiais atualizados de acordo com as leis recentemente publicadas a fim de estar sempre em consonância com
SECRETARIA DE SAÚDE SECRETARIA EXECUTIVA DE COORDENAÇÃO GERAL DIRETORIA GERAL DE PLANEJAMENTO GERÊNCIA DE GESTÃO ESTRATÉGICA E PARTICIPATIVA
 NOTA TÉCNICA Nº 04 ORIENTAÇÕES GERAIS SOBRE O RELATÓRIO QUADRIMESTRAL DE ACORDO COM A LEI COMPLEMENTAR Nº141 DE 13 DE JANEIRO DE 2012 Introdução: Até 2011, a forma de prestar contas sobre as ações, recursos
NOTA TÉCNICA Nº 04 ORIENTAÇÕES GERAIS SOBRE O RELATÓRIO QUADRIMESTRAL DE ACORDO COM A LEI COMPLEMENTAR Nº141 DE 13 DE JANEIRO DE 2012 Introdução: Até 2011, a forma de prestar contas sobre as ações, recursos
Revisão da RDC 54/2013 Rastreabilidade de Medicamentos
 Diretoria de Gestão Institucional DIGES Revisão da RDC 54/2013 Rastreabilidade de Medicamentos Brasília, 07/12/2016 AUDIÊNCIA PÚBLICA Objetivos do SNCM: Ferramenta útil contra a falsificação e o roubo
Diretoria de Gestão Institucional DIGES Revisão da RDC 54/2013 Rastreabilidade de Medicamentos Brasília, 07/12/2016 AUDIÊNCIA PÚBLICA Objetivos do SNCM: Ferramenta útil contra a falsificação e o roubo
