Últimas Novidades Terminologia MedDRA Versão 18.0
|
|
|
- Afonso Minho Gameiro
- 7 Há anos
- Visualizações:
Transcrição
1 Últimas Novidades Terminologia MedDRA Versão 18.0
2 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA) [Federação Internacional de Associações de Fabricantes de Produtos Farmacêuticos] em nome da ICH [Conferência Internacional de Harmonização].. Isenção de responsabilidade e declaração de copyright Este documento está protegido por copyright e pode utilizar-se, reproduzir-se, incorporar-se em outros trabalhos, adaptar-se, modificar-se, traduzir-se ou distribuir-se sob uma licença pública desde que se reconheça sempre no documento a titularidade de copyright da ICH. Em caso de qualquer adaptação, modificação ou tradução do documento, devem tomar-se medidas razoáveis para categorizar, demarcar ou identificar claramente que modificações se fizeram ou se basearam no documento original. Qualquer impressão de que a adaptação, a modificação ou a tradução do documento original é endossada ou patrocinada pela ICH deve ser evitada. O documento é fornecido tal como está" sem nenhum tipo de garantia. Em caso nenhum nem a ICH nem os autores do documento original serão responsáveis por qualquer reclamação, danos ou qualquer outra responsabilidade proveniente da utilização deste documento. As autorizações acima citadas não são aplicáveis ao conteúdo fornecido por terceiros. Por conseguinte, para documentos em que se confere o copyright a terceiros, deve obter-se autorização para a reprodução do titular deste copyright. ii
3 Índice Índice 1. DESCRIÇÃO GERAL DO DOCUMENTO PEDIDOS DE MODIFICAÇÕES PARA A VERSÃO MODIFICAÇÕES DA TERMINOLOGIA MODIFICAÇÕES COMPLEXAS MODIFICAÇÕES DA TRADUÇÃO Revisão da tradução em francês NOVOS DESENVOLVIMENTOS NA VERSÃO ACTUALIZAÇÕES DE CONCEITOS DE UTILIZAÇÃO DE PRODUTOS GRUPO SOC 27 A SER IMPLEMENTADO NA VERSÃO 19.0 DA TERMINOLOGIA MedDRA ÂMBITO DA TERMINOLOGIA MedDRA: REVISÕES DO GUIA INTRODUTÓRIO NOVO NAVEGADOR BASEADO NA WEB (WBB) PERGUNTAS MedDRA ESTANDARDIZADAS (SMQS) PEDIDOS DE PROACTIVIDADE Termos para utilização de fármacos Termos para local Classificação de termos para coluna e espinhal e coluna vertebral Biomarcadores farmacogenómicos em rotulagem de medicamentos RESUMO DAS MODIFICAÇÕES RESUMO DO IMPACTO SOBRE A TERMINOLOGIA RESUMO DO IMPACTO SOBRE OS REGISTOS DOS FICHEIROS DA TERMINOLOGIA MedDRA CONTAGEM DOS TERMOS DA TERMINOLOGIA MedDRA NOMES DE TERMOS PT E LLT MODIFICADOS RAZÕES PARA AS MODIFICAÇÕES DE ESTADO DOS TERMOS LLT LISTA DE FIGURAS Figure 2-1. Modificações de termos por Grupo SOC... 3 LISTA DE QUADROS Quadro 2-1 Novo termo HLGT... 4 Quadro 2-2 Novos termos HLT... 4 Quadro 2-3 Termos HLT fundidos... 5 Quadro 3-1 SMQ com novo nome... 9 iii
4 Índice Quadro 3-2 Exemplos de termos para local acrescentados à terminologia MedDRA Quadro 3-3 Exemplo de modificações de termos para coluna e espinhal e coluna vertebral Quadro 3-4 Exemplos de termos para novos biomarcadores farmacogenómicos Quadro 4-1 Resumo do impacto nos grupos SOC e termos HLGT e HLT Quadro 4-2 Resumo do impacto nos termos PT Quadro 4-3 Resumo do impacto nos termos LLT Quadro 4-4 Resumo do impacto nas SMQ Quadro 4-5 Resumo do impacto sobre os registos dos ficheiros da terminologia MedDRA Quadro 4-6 Contagem de termos da terminologia MedDRA Quadro 4-7 Nomes de termos PT e LLT modificados Quadro 4-8 Mudanças de estado de termos LLT iv
5 Descrição Geral do Documento 1. DESCRIÇÃO GERAL DO DOCUMENTO Este documento Últimas Novidades contém informações sobre a origem e os tipos de modificações que foram feitos à terminologia do Dicionário Médico para Actividades Regulamentares (Medical Dictionary for Regulatory Activities - MedDRA) entre a versão 17.1 e a versão A secção número 2, Pedidos de Modificações para a Versão 18.0, oferece um resumo das informações sobre o número de pedidos de modificações processadas para a versão. A secção número 3, Novos Desenvolvimentos na Versão 18.0, destaca as modificações existentes na versão 18.0 relacionadas com a apresentação dos pedidos de modificação, novas iniciativas e informações sobre as Perguntas MedDRA Estandardizadas (SMQs). A secção número 4, Resumo das Modificações, apresenta detalhes sobre: A história dos termos; O impacto desta versão na terminologia (em quadros); O impacto nos registos dos ficheiros da terminologia MedDRA; As contagens dos termos da terminologia MedDRA e das SMQ; Os nomes dos termos de nível mais baixo (LLT) e dos termos preferidos (PT) modificados; Todos os termos LLT na terminologia MedDRA que tiveram uma modificação do estado actual. Toda a documentação actualizada relacionada com esta versão está incluída nos meios de distribuição em formato de documento transportável (PDF) da Adobe ou, para alguns documentos, Microsoft Excel. Para ver a relação completa, consultar o ficheiro!!readm.txt. A Secção de Assistência da Organização de Manutenção e Serviços de Apoio (MSSO Help Desk) pode ser contactada através do número de telefone (AT&T Internacional gratuito) ou em mssohelp@meddra.org. 1
6 Pedidos de Modificações para a Versão PEDIDOS DE MODIFICAÇÕES PARA A VERSÃO MODIFICAÇÕES DA TERMINOLOGIA As modificações efectuadas à terminologia MedDRA resultam simultaneamente dos pedidos de modificação provenientes dos utilizadores, dos pedidos de proactividade apresentados pelos utilizadores da terminologia MedDRA e dos pedidos de modificação internos. Os pedidos de modificação internos resultam das actividades de manutenção da MSSO, assim como de actividades especiais do grupo de trabalho no qual a MSSO participa. A versão 18.0 da terminologia MedDRA é uma versão de modificação complexa, o que significa que as modificações podem ser feitas a todos os níveis da hierarquia da terminologia MedDRA. Os pedidos de modificação compreendem tanto actualizações da terminologia MedDRA como modificações às SMQ. Nesta versão foram processados, ao todo, 2069 pedidos de modificação; 1758 pedidos de modificação foram aprovados e implementados e 280 pedidos de modificação foram rejeitados. Existem, além disso, 31 pedidos de modificação que ficaram em suspenso e sujeitos a um estudo mais a fundo para a sua resolução para além desta versão As informações sobre modificações específicas (por exemplo, novos termos acrescentados, termos LLT promovidos, termos PT relegados, modificações de termos PT principais dentro de grupos SOC, etc.), que ocorreram desde a versão anterior da terminologia MedDRA, podem obter-se através do Relatório da Versão (Version Report) incluído na respectiva versão em inglês da terminologia MedDRA para download. Além disso, para identificar as modificações, os utilizadores podem utilizar a ferramenta de análise online da terminologia MedDRA em MedDRA Version Analysis Tool (MVAT) que compara quaisquer duas versões da terminologia MedDRA, incluindo versões não consecutivas. O resultado da MVAT é semelhante ao Relatório da Versão. A ferramenta MVAT é gratuita para os utilizadores da terminologia MedDRA como parte da sua assinatura. Entre publicações da terminologia MedDRA, a MSSO disponibiliza ficheiros de weekly supplemental update [actualização semanal suplementar] que são modificações aprovadas que serão implementadas para a próxima versão da terminologia MedDRA. Os ficheiros suplementares podem ser úteis para que os utilizadores compreendam as modificações que serão implementadas na próxima publicação. Uma explicação de todas as modificações consideradas (aprovadas e não aprovadas) para a versão 18.0 da terminologia MedDRA está acessível, tanto como um Relatório Detalhado cumulativo, que está incluído na versão em inglês da terminologia MedDRA para download. Os utilizadores podem examinar todos os pedidos de modificações considerados pela MSSO, desde a versão 5.1 da terminologia MedDRA até à presente, através da aplicação WebCR. A Figura 2-1 (apresentada abaixo) resume todas as modificações feitas por Grupos SOC [System Organ Class Grupos Sistémicos] e pode ser útil para avaliar o impacto 2
7 Pedidos de Modificações para a Versão 18.0 das modificações a uma área específica da terminologia MedDRA. Os dados provêm da diferença nas contagens de termos PT/LLT primários e secundários, HLT e HLGT para a versão 18.0 mostrados no Quadro 4-6 e as informações correspondentes para a versão Além disso, na Figura 2-1 incluem-se as modificações a nomes de termos e as modificações de estados de termos LLT. Consultar a secção 4 para obter um resumo das modificações na versão 18.0 da terminologia MedDRA. Afecções congénitas, familiares e genéticas Afecções do ouvido e do labirinto Afecções dos tecidos cutâneos e subcutâneos Afecções hepatobiliares Afecções musculosqueléticas e dos tecidos conjuntivos Afecções oculares Circunstâncias sociais Complicações de intervenções relacionadas com lesões e Doenças cardíacas Doenças do metabolismo e da nutrição Doenças do sangue e do sistema linfático Doenças do sistema imunitário Doenças do sistema nervoso Doenças dos órgãos genitais e da mama Doenças endócrinas Doenças gastrointestinais Doenças renais e urinárias Doenças respiratórias, torácicas e do mediastino Exames complementares de diagnóstico Infecções e infestações Neoplasias benignas malignas e não especificadas (incl.quistos e Perturbações do foro psiquiátrico Perturbações gerais e alterações no local de administração Procedimentos cirúrgicos e médicos Situações na gravidez, no puerpério e perinatais Vasculopatias Figure 2-1. Modificações de termos por Grupo SOC 2.2 MODIFICAÇÕES COMPLEXAS As propostas de modificações complexas consideradas durante a versão 18.0 incluem as que foram apresentadas pelos utilizadores, as iniciativas especiais e as que foram identificadas internamente pela MSSO durante a avaliação dos pedidos de modificação. As propostas de modificações complexas foram apresentadas no website da MSSO para receber as observações da comunidade de utilizadores, de 7 de Julho de 2014 a 1 de Agosto de Todas as modificações complexas foram submetidas a mais 3
8 Pedidos de Modificações para a Versão 18.0 revisões internas e discussões de consenso que resultaram no conjunto de 16 modificações complexas finalmente aprovado. As modificações complexas implementadas na Versão 18.0 estão resumidas a seguir. Consultar Documentos Relacionados na secção Change Request section do website da MedDRA para obter detalhes específicos. Ao nível de grupos SOC: Não se fizeram modificações a termos de grupos SOC existentes. Ao nível de termos HLGT: Acrescentou-se um novo grupo de termos de alto nível (HLGT - High Level Grouping Terms) e não se fundiu nenhum HLGT em consequência das modificações complexas na versão As modificações são as seguintes: Novo termo HLGT Novo termo HLGT Problemas de utilização de produto para grupo SOC Complicações de intervenções relacionadas com lesões e intoxicações Quadro 2-1 Novo termo HLGT Ao nível de termos HLT: Acrescentaram-se oito novos termos de alto nível (HLT High Level Terms) e fundiram-se sete termos HLT em consequência das modificações complexas na versão As modificações são as seguintes: Novos termos HLT Novo termo HLT Hérnias abdominais NC Fracturas de membro Fracturas e luxações de membro Usos fora do rótulo/indicação Sobredosagens NC Posicionamento de paciente Problemas de utilização de produto NC Subdosagens NC para grupo SOC Doenças gastrointestinais Afecções musculosqueléticas e dos tecidos conjuntivos Complicações de intervenções relacionadas com lesões e intoxicações Complicações de intervenções relacionadas com lesões e intoxicações Complicações de intervenções relacionadas com lesões e intoxicações Procedimentos cirúrgicos e médicos Complicações de intervenções relacionadas com lesões e intoxicações Complicações de intervenções relacionadas com lesões e intoxicações Quadro 2-2 Novos termos HLT 4
9 Termos HLT fundidos Pedidos de Modificações para a Versão 18.0 Termos HLT fundidos para termos HLT SOC Hérnias da cavidade abdominal NC Hérnias abdominais NC Doenças gastrointestinais Hérnias abdominais, localização não especificada Fracturas do membro inferior Fracturas e luxações do membro inferior Sobredosagens Hérnias abdominais NC Fracturas de membro Fracturas e luxações de membro Sobredosagens NC Doenças gastrointestinais Afecções musculosqueléticas e dos tecidos conjuntivos Complicações de intervenções relacionadas com lesões e intoxicações Complicações de intervenções relacionadas com lesões e intoxicações Fracturas do membro superior Fracturas de membro Afecções musculosqueléticas e dos tecidos conjuntivos Fracturas e luxações do membro superior Fracturas e luxações de membro Complicações de intervenções relacionadas com lesões e intoxicações Quadro 2-3 Termos HLT fundidos 2.3 MODIFICAÇÕES DA TRADUÇÃO Revisão da tradução em francês Num esforço para rever e melhorar a terminologia MedDRA em francês, a MSSO está a realizar uma revisão da tradução dos termos de inglês para francês. Este processo constitui um esforço em curso cuja duração se prevê ser ao longo de várias publicações da terminologia MedDRA. Para ajudar os utilizadores da terminologia MedDRA em francês a compreender as mudanças que já ocorreram, a MSSO incluiu uma folha de cálculo na versão 18.0 em francês da terminologia MedDRA para download, a qual contém uma lista de todas as modificações que foram feitas. Esta folha de cálculo indica que modificações à tradução são de natureza conceptual (isto é, implicam um significado diferente) em relação às que são correcções de menor importância, tais como de ortografia ou modificações de sinais diacríticos. Esta folha de cálculo será incluída em todas as futuras versões da terminologia MedDRA em francês, até ao fim da revisão. Consultar a secção de pedidos de modificação em Change Request section no website da MSSO se desejar fazer pedidos para melhorar a tradução de um termo ou termos a uma versão da terminologia MedDRA noutra língua que não seja a língua inglesa. 5
10 Novos Desenvolvimentos na Versão NOVOS DESENVOLVIMENTOS NA VERSÃO ACTUALIZAÇÕES DE CONCEITOS DE UTILIZAÇÃO DE PRODUTOS Vários utilizadores da terminologia MedDRA solicitaram modificações complexas e relacionadas, incluindo pedidos de novos termos, a fim de melhor organizar a colocação dos conceitos de utilização de produtos incluindo os conceitos de erro de medicação, sobredosagem e subdosagem, assim como os conceitos de má utilização e os conceitos de uso fora do rótulo/indicação. A MSSO examinou os comentários recebidos sobre essas propostas e, em colaboração com o Grupo de Trabalho M1 de Pontos a Considerar M1 da ICH, desenvolveu uma estrutura para melhor organizar os conceitos relacionados com a utilização de produtos. Os pontos que se seguem descrevem sucintamente a abordagem seguida. Consultar o documento Modificações Complexas Implementadas na Versão 18.0 na secção de Change Request (Pedidos de Modificações) do website da terminologia MedDRA para obter pormenores. Um novo termo HLGT Problemas de utilização de produto foi acrescentado ao grupo SOC Complicações de intervenções relacionadas com lesões e intoxicações para agrupar conceitos relacionados com a utilização de produtos (erros de medicação, má utilização, uso fora do rótulo/indicação, sobredosagens e subdosagens) num único local para facilitar a codificação e a recuperação, sem a necessidade de ligações multiaxiais extensas. O novo termo HLGT Problemas de utilização de produto contém quatro novos termos HLT: o O termo HLT Problemas de utilização de produto NC abarca uma mistura de conceitos de má utilização, uso intencional e outros conceitos de utilização ou uso não específicos. Este novo termo HLT terá dois novos conceitos de termos PT para além dos termos PT existentes de utilização ou uso não específicos: O termo PT Problema de utilização de produto abarca conceitos de utilização ou uso não especifico de produtos que não são especificamente identificados como erros de medicação, utilização fora de rótulo/indicação, má utilização, etc. O termo PT Problema de utilização intencional de produto abarca conceitos de problemas de utilização que se sabe serem intencionais, mas que não são especificamente identificados como sendo má utilização ou utilização fora de rótulo/indicação. o O termo HLT Sobredosagens NC abarca conceitos de sobredosagem que não são necessariamente má administrações e substitui o termo HLT Sobredosagens. o O termo HLT Subdosagens NC abarca conceitos de subdosagem que não são necessariamente má administrações. o O termo HLT Usos fora do rótulo/indicação abarca conceitos de uso de medicamentos fora da indicação. 6
11 Novos Desenvolvimentos na Versão GRUPO SOC 27 A SER IMPLEMENTADO NA VERSÃO 19.0 DA TERMINOLOGIA MedDRA O Conselho de Gestão da Terminologia MedDRA da ICH aprovou a criação de um grupo SOC 27 adicional (o vigésimo sétimo) na terminologia MedDRA. O vigésimo sétimo grupo SOC (que ainda tem de ser denominado) vai ser criado para abranger conceitos não clínicos e não relacionados com pacientes. Estes termos cobrem problemas relacionados com produtos médicos e são importantes do ponto de vista regulamentar, visto que podem ter um efeito indirecto sobre a segurança do paciente. Inicialmente, o grupo SOC 27 incluirá termos para problemas de qualidade de produtos que sejam definidos como anomalias que possam ser introduzidas durante a fabricação/rotulagem, empacotamento, transporte, manuseamento ou armazenamento de produtos médicos. O termo existente HLGT Problemas de qualidade do produto será transferido do grupo SOC Perturbações gerais e alterações no local de administração para o novo grupo SOC e complementar-se-á com novos termos especificamente relacionados com o processo de fabricação. O impacto sobre as organizações que não estão envolvidas na fabricação do produto nem na qualidade do produto espera-se que seja mínimo. Espera-se que o grupo SOC 27 seja implementado em Março de 2016, na versão 19.0 da terminologia MedDRA. A MSSO fornecerá informações mais detalhadas acerca do grupo SOC 27 através de documentos, webinars, s informativos e outras comunicações bastante antes da data de implementação planeada para Para esclarecimentos sobre o grupo SOC 27, contactar a Secção de Assistência (Help Desk) da Organização de Manutenção e Serviços de Apoio (MSSO). 3.3 ÂMBITO DA TERMINOLOGIA MedDRA: REVISÕES DO GUIA INTRODUTÓRIO Serão feitas revisões à secção 1.5 (Âmbito da terminologia) no Guia Introdutório da Terminologia MedDRA Versão A redacção revista refere-se aos tipos de produtos e conceitos médicos que a terminologia MedDRA mantém e ao potencial de expansão da terminologia em áreas de novos tópicos. Estas revisões são o resultado das recomendações do painel de peritos sobre o âmbito da terminologia MedDRA que são aprovadas pelo Conselho de Gestão da terminologia MedDRA. A redacção relevante é extraída e apresentada a seguir. A terminologia MedDRA aplica-se a todas as fases de desenvolvimento de produtos farmacêuticos para uso humano, excepto da toxicologia animal. O âmbito da terminologia MedDRA abrange conceitos médicos, relacionados com a saúde e regulamentares referentes aos ditos produtos. A terminologia também aborda os efeitos que os dispositivos podem ter sobre a saúde e o mau funcionamento dos mesmos (por exemplo: o termo preferido (PT) Infecção relacionada com o dispositivo e o termo PT Mau funcionamento de dispositivo). Além disso, a terminologia também pode apoiar outros tipos de produtos que são regulamentados pelo menos num sector, tal como de alimentos ou de cosméticos. Em consulta com o Conselho de Gestão da Terminologia MedDRA, a terminologia pode aumentar quanto ao seu âmbito, a fim de abranger conceitos adicionais médicos, relacionados com a saúde e regulamentares, os quais são desenvolvidos com base em 7
12 Novos Desenvolvimentos na Versão 18.0 esforços de colaboração que envolvem peritos relevantes. Áreas de novos tópicos a acrescentar serão sujeitas ao habitual processo de pedidos da MSSO. 3.4 NOVO NAVEGADOR BASEADO NA WEB (WBB) A MSSO tem o prazer de anunciar o novo navegador da terminologia MedDRA ou seja o MedDRA Web-Based Browser (WBB) que está disponível desde 1 de Dezembro de Para usar a aplicação são necessárias a identificação e a palavra chave do utilizador da terminologia MedDRA. O novo WBB tem características semelhantes ao actual navegador MedDRA Desktop Browser, para além de outras novas. Os utilizadores poderão: Navegar através da hierarquia da terminologia MedDRA e das SMQ Pesquisar termos e códigos da terminologia MedDRA e das SMQ Visualizar simultaneamente várias línguas fornecidas Utilizar o Research Bin (caixa de pesquisa) para reunir termos para fins de análise e de pesquisa Visualizar os antecedentes do termo Visualizar informações detalhadas sobre o termo Exportar os resultados da pesquisa para uma folha de cálculo Obter acesso às características especiais da tradução da terminologia MedDRA para japonês O WBB é gratuito para todos os utilizadores da terminologia MedDRA como parte de cada assinatura MedDRA. Para aprender a como entrar no WBB e utilizá-lo, é necessário visualizar ou fazer o download de um videocast da secção Training Materials (material de formação) no website da terminologia MedDRA sob Tools (ferramentas). Além disso, está disponível um user guide (guia do utilizador). 3.5 PERGUNTAS MedDRA ESTANDARDIZADAS (SMQs) Foram incluídas duas novas SMQ de nível 1 na publicação da versão 18.0 da terminologia MedDRA: a SMQ Insuficiência respiratória e a SMQ Tendinopatias e afecções dos ligamentos. Existem agora 98 SMQ de nível 1 em produção até esta versão. Para obter mais informações acerca das novas SMQ, incluindo os seus critérios de inclusão e exclusão, consultar o Guia Introdutório das Perguntas MedDRA Estandardizadas (SMQ) Versão Para além das novas SMQ, foram atribuídos novos nomes a quatro SMQ relacionadas com doenças vasculares do sistema nervoso central, na versão 18.0 da terminologia MedDRA. Os termos relacionados com medula espinhal estão incluídos nestas SMQ para além dos termos relacionados com o cérebro e, por conseguinte, a atribuição de novos nomes a estas SMQ reflete melhor as partes anatómicas cobertas. Consultar o quadro que se segue para obter as SMQ com o novo nome. 8
13 Novos Desenvolvimentos na Versão 18.0 Nome anterior da SMQ Doenças cerebrovasculares (SMQ) Doenças cerebrovasculares, não especificadas como hemorrágicas ou isquémicas (SMQ) Doenças cerebrovasculares isquémicas (SMQ) Doenças cerebrovasculares hemorrágicas (SMQ) Novo nome da SMQ Doenças vasculares do sistema nervoso central (SMQ) Doenças vasculares do sistema nervoso central, não especificadas como hemorrágicas ou isquémicas (SMQ) Doenças vasculares isquémicas do sistema nervoso central (SMQ) Doenças vasculares hemorrágicas do sistema nervoso central (SMQ) Quadro 3-1 SMQ com novo nome 3.6 PEDIDOS DE PROACTIVIDADE O processo de proactividade ou manutenção proactiva permite aos utilizadores da terminologia MedDRA propor modificações gerais à terminologia MedDRA fora do processo estabelecido de pedidos de modificação para resolver inconsistências, fazer correcções ou sugerir melhoramentos. Durante o período do processo de pedidos de modificação para a versão 18.0, a MSSO avaliou cinco propostas de proactividade apresentadas pelos utilizadores da terminologia MedDRA. Das cinco propostas, quatro foram implementadas e uma não foi aprovada. Consultar os detalhes que se seguem sobre os pedidos implementados. A MSSO publica e actualiza uma lista de todas as propostas recebidas e a situação destas na secção de Change Request (Pedidos de Modificações) do website da terminologia MedDRA. A MSSO está interessada em ouvir quaisquer ideias que os utilizadores possam ter sobre melhoramentos proactivos à terminologia MedDRA. Enviem as vossas ideias sobre melhoramentos proactivos à terminologia MedDRA por para a MSSO Help Desk. Sejam tão específicos quanto seja possível ao descrever as vossas ideias e incluam uma justificação que explique porque é que pensam que as vossas propostas devem ser implementadas Termos para utilização de fármacos Um utilizador da terminologia MedDRA solicitou que fosse examinado um conjunto de termos para utilização de fármacos com vista a uma possível inclusão na terminologia MedDRA. Com base numa revisão feita pela MSSO, verificou-se que a maior parte dos conceitos solicitados já estavam representados na terminologia MedDRA quer como correspondências directas ou conceitos aproximados. Três novos termos foram acrescentados (o termo PT Participante em ensaio clínico, o termo PT Planificação de gravidez, e o termo LLT Interrupção da cadeia de fornecimento de medicamentos). O 9
14 Novos Desenvolvimentos na Versão 18.0 estado do termo LLT Sem medicação foi modificado para desactualizado devido ao facto deste conceito ambíguo se poder referir a um determinado paciente que está a ficar sem medicação ou a um problema de uma cadeia de fornecimento Termos para local Em dois pedidos separados, foi solicitado à MSSO que considerasse acrescentar mais conceitos de local (por exemplo, local de administração) à terminologia MedDRA, a fim de fornecer mais opções de codificação aos utilizadores da terminologia MedDRA. Com base nesta revisão, foram acrescentados 224 novos conceitos principalmente ao grupo SOC Perturbações gerais e alterações no local de administração. A abordagem da MSSO consistiu em acrescentar um conjunto de termos de local de administração semelhantes aos termos de local de injecção já existentes e preencher algumas lacunas a termos de local de injecção idênticos, conforme apropriado em relação a termos para local de vacinação, local de infusão, local de aplicação e local do dispositivo médico. Ligações secundárias adequadas foram acrescentadas para novos termos com base nas regras e convenções da terminologia MedDRA descritas no Guia Introdutório da Terminologia MedDRA. Consultar o quadro abaixo para a obtenção de alguns exemplos de termos acrescentados. Termo PT Flebite no local de aplicação Hiperestesia no local de infusão Lesão no local do dispositivo médico Eczema no local de vacinação Termo LLT Vermelhidão articular no local de administração Vermelhidão articular no local de aplicação Termo HLT* primário Reacções do local de aplicação e instilação Reacções no local de infusão Complicações ligadas ao dispositivo NC Reacções no local de vacinação Termo PT Eritema articular no local de administração Eritema articular no local de aplicação Quadro 3-2 Exemplos de termos para local acrescentados à terminologia MedDRA *O SOC Perturbações gerais e alterações no local de administração é o grupo SOC primário Classificação de termos para coluna e espinhal e coluna vertebral A MSSO recebeu pedidos para examinar a escolha específica de um termo ou da colocação específica de vários conceitos da terminologia MedDRA relacionados com a anatomia das costas que não são sempre coerentes relativamente a estruturas ósseas ou a tecidos nervosos e moles. Muitos destes termos são derivações de vértebra, coluna vertebral e costas. Com base num número total de 1366 termos LLT, PT, HLT e HLGT aplicáveis da terminologia MedDRA que foram examinados, foram implementados 12 pedidos de modificação, para assegurar uma utilização coerente destes termos. As modificações referiram-se à coerência de definição do termo, estado 10
15 Novos Desenvolvimentos na Versão 18.0 do termo e relações hierárquicas. Consultar o exemplo que se segue: o termo LLT Hematoma espinhal foi modificado para desactualizado devido a ser um termo ambíguo; espinhal podia referir-se à medula espinhal ou à estrutura óssea/vértebra. (Consultar também a Secção 4.5). Versão 17.1 da terminologia MedDRA Versão 18.0 da terminologia MedDRA Termo LLT Estado Termo LLT Estado Hematoma espinhal Actual Hematoma espinhal Desactualizado Quadro 3-3 Exemplo de modificações de termos para coluna e espinhal e coluna vertebral A Secção 5.1 do Guia Introdutório da terminologia MedDRA será actualizada para incluir uma afirmação explicando que, para os fins da terminologia MedDRA, os termos para coluna e espinhal são considerados conceitos sinónimos de vertebral e espinhal em vez de medula espinhal, a não ser que "espinhal represente claramente um conceito neurológico, tal como o termo PT Claudicação da medula espinhal Biomarcadores farmacogenómicos em rotulagem de medicamentos Um utilizador da terminologia MedDRA solicitou que a MSSO considerasse acrescentar à terminologia MedDRA termos adicionais pertinentes do ponto de vista médico para biomarcadores farmacogenómicos, a fim de oferecer mais opções de codificação e análise. Após examinar a proposta, a MSSO acrescentou à terminologia MedDRA 72 novos termos farmacogenómicos pertinentes do ponto de vista médico e fez modificações a quatro termos já existentes. Consultar o quadro que se segue para obter exemplos. Novo termo PT Termo HLT primário Grupo SOC primário Ensaio do HLA-B*5701 positivo Super-expressão da proteína HER-2 Análises de marcadores celulares Mutações genéticas adquiridas e outras alterações Exames complementares de diagnóstico Perturbações gerais e alterações no local de administração Novo termo LLT Termo PT Grupo SOC primário ESR1 positivo PgR positiva Oestrogen receptor assay positive Progesterone receptor assay positive Exames complementares de diagnóstico Exames complementares de diagnóstico Quadro 3-4 Exemplos de termos para novos biomarcadores farmacogenómicos 11
16 Resumo das Modificações 4. RESUMO DAS MODIFICAÇÕES 4.1 RESUMO DO IMPACTO SOBRE A TERMINOLOGIA Os quadros seguintes (consultar os quadros 4-1 a 4-5) resumem o impacto sobre a terminologia MedDRA na versão Estes quadros destinam-se apenas a servir de referência. Para obter informações detalhadas sobre as modificações na versão 18.0, consultar o Relatório da Versão da terminologia MedDRA localizado na versão em língua inglesa para telecarregamento em English language download. Modificações em SOC, HLGT, HLT Nível Acção de pedidos de modificação Modificação final Versão 17.1 Versão 18.0 SOC Total de grupos SOC Novos termos HLGT HLGT Termos HLGT fundidos Total de termos HLGT Novos termos HLT HLT Termos HLT fundidos Total de termos HLT Quadro 4-1 Resumo do impacto nos grupos SOC e termos HLGT e HLT 1 A modificação final total dos termos HLGT ou HLT é igual ao número de novos termos HLGT ou HLT menos o número dos respectivos termos HLGT ou HLT fundidos. Modificações em termos PT Nível Acção de pedidos de modificação Versão 17.1 Versão 18.0 PT Novos termos PT Termos LLT promovidos
17 Resumo das Modificações Nível Acção de pedidos de modificação Versão 17.1 Versão 18.0 Termos PT relegados Modificação final Total de termos PT Quadro 4-2 Resumo do impacto nos termos PT 1 A modificação final dos termos PT é igual ao número dos novos termos PT mais o número de termos LLT promovidos, menos o número de termos PT relegados. Modificações em termos LLT Nível Acção de pedidos de modificação Modificação final Versão 17.1 Versão 18.0 LLT Total de termos LLT Quadro 4-3 Resumo do impacto nos termos LLT 1 O total de termos LLT inclui termos PT, dado que estes também são representados como termos LLT. Novos SMQ Nível Modificação final Versão 17.1 Versão Quadro 4-4 Resumo do impacto nas SMQ 13
18 Resumo das Modificações 4.2 RESUMO DO IMPACTO SOBRE OS REGISTOS DOS FICHEIROS DA TERMINOLOGIA MedDRA O quadro seguinte resume o impacto da terminologia MedDRA na versão Este quadro destina-se apenas a servir de referência. INTL_ORD.ASC SOC.ASC SOC_HLGT.ASC HLGT.ASC HLGT_HLT.ASC HLT.ASC HLT_PT.ASC Acrescentado 0 Suprimido 0 Modificado 0 Acrescentado 0 Suprimido 0 Modificado 0 Acrescentado 1 Suprimido 0 Modificado 0 Acrescentado 1 Suprimido 0 Modificado 0 Acrescentado 8 Suprimido 7 Modificado 0 Acrescentado 8 Suprimido 7 Modificado 0 Acrescentado Suprimido 189 Modificado 0 Acrescentado MDHIER.ASC Suprimido 224 Modificado 0 Acrescentado 580 PT.ASC Suprimido 43 Modificado 17 LLT.ASC Acrescentado
19 Resumo das Modificações SMQ_LIST.ASC 1 SMQ_CONTENT.ASC Suprimido 0 Modificado Acrescentado Suprimido 0 Modificado 212 Acrescentado Suprimido 0 Modificado Quadro 4-5 Resumo do impacto sobre os registos dos ficheiros da terminologia MedDRA 1 O número de SMQ acrescentado inclui o nível superior (nível 1) e as SMQ subordinadas (sub-smq). 4.3 CONTAGEM DOS TERMOS DA TERMINOLOGIA MedDRA O quadro abaixo mostra as contagens dos termos por grupo SOC para os termos HLGT, HLT, termos PT e LLT primários e secundários e termos PT e LLT primários. Grupos SOC Termos LLT* (primários) 1 Termos PT (primários) 1 Termos LLT* (primários e secundários) 2 Termos PT (primários e secundários) 2 Termos HLT 3 Termos HLGT 3 Doenças do sangue e do sistema linfático Afecções cardíacas Afecções congénitas, familiares e genéticas Afecções do ouvido e do labirinto Doenças endócrinas
20 Resumo das Modificações Grupos SOC Termos LLT* (primários) 1 Termos PT (primários) 1 Termos LLT* (primários e secundários) 2 Termos PT (primários e secundários) 2 Termos HLT 3 Termos HLGT 3 Afecções oculares Afecções gastrointestinais Perturbações gerais e alterações no local de administração Afecções hepatobiliares Doenças do sistema imunitário Infecções e infestações Complicações de intervenções relacionadas com lesões e intoxicações Exames complementare s de diagnóstico Doenças do metabolismo e da nutrição Afecções musculosquelética s e dos tecidos conjuntivos
21 Resumo das Modificações Grupos SOC Termos LLT* (primários) 1 Termos PT (primários) 1 Termos LLT* (primários e secundários) 2 Termos PT (primários e secundários) 2 Termos HLT 3 Termos HLGT 3 Neoplasias benignas malignas e não especificadas (incl quistos e pólipos) Doenças do sistema nervoso Situações na gravidez, no puerpério e perinatais Perturbações do foro psiquiátrico Doenças renais e urinárias Doenças dos órgãos genitais e da mama Doenças respiratórias, torácicas e do mediastino Afecções dos tecidos cutâneos e subcutâneos Circunstâncias sociais Procedimentos cirúrgicos e médicos
22 Resumo das Modificações Grupos SOC Termos LLT* (primários) 1 Termos PT (primários) 1 Termos LLT* (primários e secundários) 2 Termos PT (primários e secundários) 2 Termos HLT 3 Termos HLGT 3 Vasculopatias Total Quadro 4-6 Contagem de termos da terminologia MedDRA 11 A contagem primária só inclui o número de termos que têm ligação primária com o grupo SOC designado, quer seja ao nível LLT ou ao nível PT. As somas dos termos primários LLT e PT coincidem com os dos Quadros 4-2 e A contagem total inclui o número de termos que têm tanto ligação primária, como secundária com o grupo SOC designado, quer ao nível LLT ou ao nível PT. Por conseguinte, as somas do total de termos LLT e PT são superiores às dos Quadros 4-2 e As contagens dos termos HLT e HLGT não constituem necessariamente valores exclusivos, dada a estrutura multiaxial da terminologia MedDRA (consultar a secção 2.2 do Guia Introdutório para obter uma explicação de multi-axialidade). Há alguns termos HLT que são contados em mais do que um grupo SOC. Por exemplo, o termo HLT Anomalias congénitas do tecido conjuntivo e o termo HLGT Afecções musculosqueléticas e dos tecidos conjuntivos congénitas contaram-se tanto no grupo SOC de Afecções congénitas, familiares e genéticas como no grupo SOC de Afecções musculosqueléticas e do tecido conjuntivo. As somas dos termos HLT e HLGT são superiores às incluídas no Quadro NOMES DE TERMOS PT E LLT MODIFICADOS Como parte das actividades de manutenção contínuas da terminologia MedDRA, podem modificar-se (atribuição de um novo nome) os termos PT e LLT existentes para corrigir erros de ortografia, espaços duplos, maiúsculas e outros erros válidos que satisfaçam os critérios de atribuição de novos nomes na terminologia MedDRA. Este recurso de atribuição de novos nomes retém o código original do termo da terminologia MedDRA e mantém o seu significado original. Este processo facilita a reutilização do mesmo código da terminologia MedDRA para os termos PT ou LLT com um novo nome. O quadro que se segue inclui os termos aos quais foi atribuído um novo nome na versão 18.0 da terminologia MedDRA em inglês. 18
23 Resumo das Modificações Código Nível Nome do termo na versão 17.1 Nome do termo na versão LLT Fístula bilio-cutânea Fístula bilio-cutânea PT Neoplasia de células dendríticas plasmocitóides blásticas Neoplasia de células dendríticas plasmocitóides blásticas PT Ensaio de receptor C-KIT Ensaio de receptor C-KIT PT Síndrome de Eagle Síndrome de Eagle * LLT Ressecção do complexo auréolamamilo Ressecção do complexo auréolamamilo LLT Anomalia de Peters Anomalia de Peters LLT Síndrome de Wells Síndrome de Wells Quadro 4-7 Nomes de termos PT e LLT modificados * Este foi o único termo que sofreu alteração em português, dado que ao contrário do inglês todos os outros termos estavam correctos em português 4.5 RAZÕES PARA AS MODIFICAÇÕES DE ESTADO DOS TERMOS LLT O quadro seguinte reflecte os nove termos que sofreram uma mudança de estado ao nível dos termos LLT na versão 18.0 da terminologia MedDRA, assim como as razões para esta modificação. Termos de nível mais baixo (LLT) Dor de barriga Degenerescência macular senil não exsudativa da retina Dor de barriga Adenomegalia Estado modificado para Actual Actual Actual Desactualizado Razões Uma modificação para o estado actual acrescenta este termo coloquial comum, a fim de melhorar as opções de codificação em inglês e noutras línguas. Os dois termos LLT existentes o LLT Degenerescência macular senil não exsudativa da retina e o termo com hífen em inglês são aceites como redacções correctas da expressão. Uma modificação para o estado actual acrescenta este termo coloquial comum, a fim de melhorar as opções de codificação em inglês e noutras línguas. O conceito pode ser representado por um dos vários termos LLT existentes sob o termo PT Linfadenopatia, tal como o termo LLT Gânglios linfáticos inchados. 19
24 Resumo das Modificações Termos de nível mais baixo (LLT) Estado modificado para Razões Excisão da mama Fractura exposta a nível C5-C7 com lesão traumática medular NE Sem medicação Hematoma espinhal Hematoma espinhal Desactualizado Desactualizado Desactualizado Desactualizado Desactualizado Ainda que na prática clínica o termo excisão da mama" se refira principalmente à excisão de uma parte da mama, também pode ser interpretado como um sinónimo de mastectomia. Por esse motivo, para clarificação do conceito, o termo LLT Excisão da mama será modificado para desactualizado e substituído por um novo termo LLT Excisão de nódulo mamário sob o termo PT Remoção de nódulo mamário Este termo LLT representa um conceito de combinação que não está em conformidade com as convenções ta terminologia MedDRA. Esta modificação foi feita com base no pedido de proactividade para examinar a classificação de termos com espinhal versus condições das vértebras. Consultar a secção "Sem medicação" pode ser considerado ambíguo, dado que se poderia referir a um determinado paciente que está a ficar sem medicação ou a um problema de uma cadeia de fornecimento. Hematoma espinhal é um termo ambíguo porque espinhal se pode referir quer à medula espinhal ou à estrutura óssea/vértebras. Esta modificação foi feita com base no pedido de proactividade para examinar a classificação de termos com espinhal versus condições das vértebras. Consultar a secção Hematoma espinhal é um termo ambíguo porque espinhal se pode referir quer à medula espinhal ou à estrutura óssea/vértebras. Esta modificação foi feita com base no pedido de proactividade para examinar a classificação de termos com espinhal versus condições das vértebras. Consultar a secção Quadro 4-8 Mudanças de estado de termos LLT 20
Últimas Novidades Terminologia MedDRA Versão 18.1
 Últimas Novidades Terminologia MedDRA Versão 18.1 Setembro 2015 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations
Últimas Novidades Terminologia MedDRA Versão 18.1 Setembro 2015 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations
Últimas Novidades Terminologia MedDRA Versão 21.1
 C Últimas Novidades Terminologia MedDRA Versão 21.1 Setembro 2018 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é registada pela International Federation of Pharmaceutical Manufacturers and
C Últimas Novidades Terminologia MedDRA Versão 21.1 Setembro 2018 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é registada pela International Federation of Pharmaceutical Manufacturers and
Últimas Novidades Terminologia MedDRA Versão 17.1
 Últimas Novidades Terminologia MedDRA Versão 17.1 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
Últimas Novidades Terminologia MedDRA Versão 17.1 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
Últimas Novidades Terminologia MedDRA Versão 14.1
 Últimas Novidades Terminologia MedDRA Versão 14.1 Reconhecimentos RECONHECIMENTOS MedDRA é uma marca registada da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA) [Federação
Últimas Novidades Terminologia MedDRA Versão 14.1 Reconhecimentos RECONHECIMENTOS MedDRA é uma marca registada da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA) [Federação
Últimas Novidades Terminologia MedDRA Versão 20.1
 c Últimas Novidades Terminologia MedDRA Versão 20.1 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
c Últimas Novidades Terminologia MedDRA Versão 20.1 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
Últimas Novidades Terminologia MedDRA Versão 22.0
 C Últimas Novidades Terminologia MedDRA Versão 22.0 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é registada pela International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
C Últimas Novidades Terminologia MedDRA Versão 22.0 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é registada pela International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
Últimas Novidades Terminologia MedDRA Versão 20.0
 c Últimas Novidades Terminologia MedDRA Versão 20.0 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
c Últimas Novidades Terminologia MedDRA Versão 20.0 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
Últimas Novidades Terminologia MedDRA Versão 15.1
 Últimas Novidades Terminologia MedDRA Versão 15.1 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
Últimas Novidades Terminologia MedDRA Versão 15.1 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
Últimas Novidades Terminologia MedDRA Versão 19.1
 Últimas Novidades Terminologia MedDRA Versão 19.1 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
Últimas Novidades Terminologia MedDRA Versão 19.1 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
O Que Há de Novo MedDRA Versão MSSO-DI Março de 2016
 c O Que Há de Novo MedDRA Versão 19.0 Agradecimentos AGRADECIMENTOS A marca registada MedDRA é propriedade da IFPMA, em nome do ICH. Isenção de Responsabilidades e Declaração de Direitos Reservados Este
c O Que Há de Novo MedDRA Versão 19.0 Agradecimentos AGRADECIMENTOS A marca registada MedDRA é propriedade da IFPMA, em nome do ICH. Isenção de Responsabilidades e Declaração de Direitos Reservados Este
Últimas Novidades Terminologia MedDRA Versão 14.0
 Últimas Novidades Terminologia MedDRA Versão 14.0 Reconhecimentos RECONHECIMENTOS MedDRA é uma marca registada da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA) [Federação
Últimas Novidades Terminologia MedDRA Versão 14.0 Reconhecimentos RECONHECIMENTOS MedDRA é uma marca registada da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA) [Federação
RECUPERAÇÃO E APRESENTAÇÃO DE DADOS DA TERMINOLOGIA MedDRA : PONTOS A CONSIDERAR
 RECUPERAÇÃO E APRESENTAÇÃO DE DADOS DA TERMINOLOGIA MedDRA : PONTOS A CONSIDERAR Guia Endossado pelo ICH para os Utilizadores da Terminologia MedDRA sobre Saída de Dados Versão Condensada 2018 Reconhecimentos
RECUPERAÇÃO E APRESENTAÇÃO DE DADOS DA TERMINOLOGIA MedDRA : PONTOS A CONSIDERAR Guia Endossado pelo ICH para os Utilizadores da Terminologia MedDRA sobre Saída de Dados Versão Condensada 2018 Reconhecimentos
Organização de Manutenção e Serviços de Apoio (MSSO) Recomendações para Implementação e Utilização da Terminologia MedDRA
 MELHORES PRÁTICAS da Terminologia MedDRA Organização de Manutenção e Serviços de Apoio (MSSO) Recomendações para Implementação e Utilização da Terminologia MedDRA Reconhecimentos Reconhecimentos A marca
MELHORES PRÁTICAS da Terminologia MedDRA Organização de Manutenção e Serviços de Apoio (MSSO) Recomendações para Implementação e Utilização da Terminologia MedDRA Reconhecimentos Reconhecimentos A marca
Últimas Novidades Terminologia MedDRA Versão 17.0
 Últimas Novidades Terminologia MedDRA Versão 17.0 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
Últimas Novidades Terminologia MedDRA Versão 17.0 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
Últimas Novidades Terminologia MedDRA Versão 15.0
 Últimas Novidades Terminologia MedDRA Versão 15.0 Reconhecimentos RECONHECIMENTOS MedDRA é uma marca registada da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA) [Federação
Últimas Novidades Terminologia MedDRA Versão 15.0 Reconhecimentos RECONHECIMENTOS MedDRA é uma marca registada da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA) [Federação
Documento de Ficheiro em Formato de Distribuição MedDRA Versão 16.0
 Documento de Ficheiro em Formato de Distribuição MedDRA Versão 16.0 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and
Documento de Ficheiro em Formato de Distribuição MedDRA Versão 16.0 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and
Guia Introdutório MedDRA Versão 13.1
 Guia Introdutório MedDRA Versão 13.1 Aviso ao Leitor Aviso ao Leitor Este Guia Introdutório está redigido em português e foi preparado para ser utilizado unicamente com a versão do MedDRA em português.
Guia Introdutório MedDRA Versão 13.1 Aviso ao Leitor Aviso ao Leitor Este Guia Introdutório está redigido em português e foi preparado para ser utilizado unicamente com a versão do MedDRA em português.
SELECÇÃO DE TERMOS DA TERMINOLOGIA MedDRA : PONTOS A CONSIDERAR
 SELECÇÃO DE TERMOS DA TERMINOLOGIA MedDRA : PONTOS A CONSIDERAR Guia Endossado pelo ICH para os Utilizadores da Terminologia MedDRA Versão Condensada 2018 Reconhecimentos A marca comercial MedDRA é registada
SELECÇÃO DE TERMOS DA TERMINOLOGIA MedDRA : PONTOS A CONSIDERAR Guia Endossado pelo ICH para os Utilizadores da Terminologia MedDRA Versão Condensada 2018 Reconhecimentos A marca comercial MedDRA é registada
Últimas Novidades Terminologia MedDRA Versão 13.0
 Últimas Novidades Terminologia MedDRA Versão 13.0 Reconhecimentos RECONHECIMENTOS MedDRA é uma marca registada da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA) [Federação
Últimas Novidades Terminologia MedDRA Versão 13.0 Reconhecimentos RECONHECIMENTOS MedDRA é uma marca registada da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA) [Federação
Últimas Novidades Terminologia MedDRA Versão 13.1
 Últimas Novidades Terminologia MedDRA Versão 13.1 Reconhecimentos RECONHECIMENTOS MedDRA é uma marca registada da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA) [Federação
Últimas Novidades Terminologia MedDRA Versão 13.1 Reconhecimentos RECONHECIMENTOS MedDRA é uma marca registada da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA) [Federação
Últimas Novidades Terminologia MedDRA Versão 16.1
 Últimas Novidades Terminologia MedDRA Versão 16.1 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
Últimas Novidades Terminologia MedDRA Versão 16.1 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
GDH CID-9-MC A CID-9-MC é um sistema de Classificação de Doenças, que se baseia na 9ª Revisão, Modificação Clínica, da Classificação Internacional de
 SISTEMA DE CLASSIFICAÇÃO DE DOENTES EM GRUPOS DE DIAGNÓSTICOS HOMOGÉNEOS GDH GDH CID-9-MC A CID-9-MC é um sistema de Classificação de Doenças, que se baseia na 9ª Revisão, Modificação Clínica, da Classificação
SISTEMA DE CLASSIFICAÇÃO DE DOENTES EM GRUPOS DE DIAGNÓSTICOS HOMOGÉNEOS GDH GDH CID-9-MC A CID-9-MC é um sistema de Classificação de Doenças, que se baseia na 9ª Revisão, Modificação Clínica, da Classificação
Documentação de Ficheiros ASCII e Consecutivos MedDRA Versão 14.1
 Documentação de Ficheiros ASCII e Consecutivos MedDRA Versão 14.1 Reconhecimentos RECONHECIMENTOS MedDRA é uma marca registada da International Federation of Pharmaceutical Manufacturers and Associations
Documentação de Ficheiros ASCII e Consecutivos MedDRA Versão 14.1 Reconhecimentos RECONHECIMENTOS MedDRA é uma marca registada da International Federation of Pharmaceutical Manufacturers and Associations
Últimas Novidades Terminologia MedDRA Versão 16.0
 Últimas Novidades Terminologia MedDRA Versão 16.0 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
Últimas Novidades Terminologia MedDRA Versão 16.0 Reconhecimentos RECONHECIMENTOS A marca registada MedDRA é propriedade da International Federation of Pharmaceutical Manufacturers and Associations (IFPMA)
FOLHETO INFORMATIVO FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR. Pandermil 10 mg/g Creme. Hidrocortisona
 FOLHETO INFORMATIVO FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR Pandermil 10 mg/g Creme Hidrocortisona Leia atentamente este folheto antes de utilizar o medicamento. - Conserve este folheto. Pode
FOLHETO INFORMATIVO FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR Pandermil 10 mg/g Creme Hidrocortisona Leia atentamente este folheto antes de utilizar o medicamento. - Conserve este folheto. Pode
Anexo III. Alterações nas secções relevantes do resumo das caraterísticas do medicamento e do folheto informativo
 Anexo III Alterações nas secções relevantes do resumo das caraterísticas do medicamento e do folheto informativo Nota: As alterações ao Resumo das Características do Medicamento e ao Folheto Informativo
Anexo III Alterações nas secções relevantes do resumo das caraterísticas do medicamento e do folheto informativo Nota: As alterações ao Resumo das Características do Medicamento e ao Folheto Informativo
Jornal Oficial da União Europeia L 304/1. (Actos cuja publicação é uma condição da sua aplicabilidade)
 23.11.2005 Jornal Oficial da União Europeia L 304/1 I (Actos cuja publicação é uma condição da sua aplicabilidade) REGULAMENTO (CE) N. o 1905/2005 DO CONSELHO de 14 de Novembro de 2005 que altera o Regulamento
23.11.2005 Jornal Oficial da União Europeia L 304/1 I (Actos cuja publicação é uma condição da sua aplicabilidade) REGULAMENTO (CE) N. o 1905/2005 DO CONSELHO de 14 de Novembro de 2005 que altera o Regulamento
Instruções aos requerentes para Registo Simplificado de Medicamentos Homeopáticos
 Instruções aos requerentes para Registo Simplificado de Medicamentos Homeopáticos 1 REGRAS A OBSERVAR PELOS REQUERENTES DE REGISTO SIMPLIFICADO DE MEDICAMENTOS HOMEOPÁTICOS 2 A. Legislação Decreto-Lei
Instruções aos requerentes para Registo Simplificado de Medicamentos Homeopáticos 1 REGRAS A OBSERVAR PELOS REQUERENTES DE REGISTO SIMPLIFICADO DE MEDICAMENTOS HOMEOPÁTICOS 2 A. Legislação Decreto-Lei
FOLHETO INFORMATIVO FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR. Pandermil 10 mg/g Pomada. Hidrocortisona
 FOLHETO INFORMATIVO FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR Pandermil 10 mg/g Pomada Hidrocortisona Leia atentamente este folheto antes de utilizar o medicamento. - Conserve este folheto. Pode
FOLHETO INFORMATIVO FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR Pandermil 10 mg/g Pomada Hidrocortisona Leia atentamente este folheto antes de utilizar o medicamento. - Conserve este folheto. Pode
REGULAMENTO DE EXECUÇÃO (UE) /... DA COMISSÃO. de
 COMISSÃO EUROPEIA Bruxelas, 24.3.2017 C(2017) 1812 final REGULAMENTO DE EXECUÇÃO (UE) /... DA COMISSÃO de 24.3.2017 relativo às modalidades para os procedimentos de inspeção de boas práticas clínicas,
COMISSÃO EUROPEIA Bruxelas, 24.3.2017 C(2017) 1812 final REGULAMENTO DE EXECUÇÃO (UE) /... DA COMISSÃO de 24.3.2017 relativo às modalidades para os procedimentos de inspeção de boas práticas clínicas,
DECISÃO DE EXECUÇÃO (UE) /... DA COMISSÃO. de
 COMISSÃO EUROPEIA Bruxelas, 18.7.2018 C(2018) 4543 final DECISÃO DE EXECUÇÃO (UE) /... DA COMISSÃO de 18.7.2018 relativa à adoção e atualização da lista de qualificações/aptidões, competências e profissões
COMISSÃO EUROPEIA Bruxelas, 18.7.2018 C(2018) 4543 final DECISÃO DE EXECUÇÃO (UE) /... DA COMISSÃO de 18.7.2018 relativa à adoção e atualização da lista de qualificações/aptidões, competências e profissões
Proposta de. REGULAMENTO (CE) n.º / DA COMISSÃO
 Proposta de REGULAMENTO (CE) n.º / DA COMISSÃO de [ ] que altera o Regulamento (CE) n.º 2042/2003 da Comissão, relativo à aeronavegabilidade permanente das aeronaves e dos produtos, peças e equipamentos
Proposta de REGULAMENTO (CE) n.º / DA COMISSÃO de [ ] que altera o Regulamento (CE) n.º 2042/2003 da Comissão, relativo à aeronavegabilidade permanente das aeronaves e dos produtos, peças e equipamentos
CA Desktop Migration Manager
 CA Desktop Migration Manager Notas da Versão Service Pack 12.8.01 A presente documentação, que inclui os sistemas de ajuda incorporados e os materiais distribuídos eletronicamente (doravante denominada
CA Desktop Migration Manager Notas da Versão Service Pack 12.8.01 A presente documentação, que inclui os sistemas de ajuda incorporados e os materiais distribuídos eletronicamente (doravante denominada
Jornal Oficial da União Europeia L 170/7
 1.7.2005 Jornal Oficial da União Europeia L 170/7 REGULAMENTO (CE) N. o 1002/2005 DA COMISSÃO de 30 de Junho de 2005 que altera o Regulamento (CE) n. o 1239/95 no que diz respeito, por um lado, à concessão
1.7.2005 Jornal Oficial da União Europeia L 170/7 REGULAMENTO (CE) N. o 1002/2005 DA COMISSÃO de 30 de Junho de 2005 que altera o Regulamento (CE) n. o 1239/95 no que diz respeito, por um lado, à concessão
A QUEM INTERESSA ESTE PROCEDIMENTO OPERACIONAL
 Pág.: 1 / 8 ÍNDICE 1. OBJECTIVO E ÂMBITO 2. DOCUMENTAÇÃO DE REFERÊNCIA 3. MODO DE PROCEDER 3.1. Introdução 3.2. Recolha de Currículos dos Candidatos 3.3. Organização Interna dos Currículos 3.3.1. Arquivo
Pág.: 1 / 8 ÍNDICE 1. OBJECTIVO E ÂMBITO 2. DOCUMENTAÇÃO DE REFERÊNCIA 3. MODO DE PROCEDER 3.1. Introdução 3.2. Recolha de Currículos dos Candidatos 3.3. Organização Interna dos Currículos 3.3.1. Arquivo
Código Subsidiário do I-REC - Documento 04. Emissão de I-RECs. versão 1.4
 Código Subsidiário do I-REC - Documento 04 Emissão de I-RECs versão 1.4 Código Subsidiário do I-REC - Documento 04 Emissão de I-RECs Versão 1.4 Sumário 1. Introdução 4 1.1 O I-REC Service 4 1.2 O Código
Código Subsidiário do I-REC - Documento 04 Emissão de I-RECs versão 1.4 Código Subsidiário do I-REC - Documento 04 Emissão de I-RECs Versão 1.4 Sumário 1. Introdução 4 1.1 O I-REC Service 4 1.2 O Código
TECNOLOGIAS DA INFORMAÇÃO E COMUNICAÇÃO SISTEMAS DE GESTÃO DE BASE DE DADOS CONCEITOS BÁSICOS
 TECNOLOGIAS DA INFORMAÇÃO E COMUNICAÇÃO CONCEITOS BÁSICOS Necessidade das base de dados Permite guardar dados dos mais variados tipos; Permite um rápido e fácil acesso aos dados; Acelera os processos de
TECNOLOGIAS DA INFORMAÇÃO E COMUNICAÇÃO CONCEITOS BÁSICOS Necessidade das base de dados Permite guardar dados dos mais variados tipos; Permite um rápido e fácil acesso aos dados; Acelera os processos de
PRIVACIDADE E SEGURANÇA
 PRIVACIDADE E SEGURANÇA A Blueticket Serviços de Bilhética SA, entidade responsável pela exploração deste website, empresa 100% detida pela Arena Atlântico, SA, encara seriamente a privacidade e a proteção
PRIVACIDADE E SEGURANÇA A Blueticket Serviços de Bilhética SA, entidade responsável pela exploração deste website, empresa 100% detida pela Arena Atlântico, SA, encara seriamente a privacidade e a proteção
Capítulo 17b (Ex-CAPÍTULO 9) EFEITOS TARDIOS
 Capítulo 17b (Ex-CAPÍTULO 9) EFEITOS TARDIOS 9.1. DEFINIÇÃO DE EFEITO TARDIO Define-se "efeito tardio" como o efeito residual, geralmente inactivo, de duração indefinida após o fim da fase aguda da doença
Capítulo 17b (Ex-CAPÍTULO 9) EFEITOS TARDIOS 9.1. DEFINIÇÃO DE EFEITO TARDIO Define-se "efeito tardio" como o efeito residual, geralmente inactivo, de duração indefinida após o fim da fase aguda da doença
1. "O Cliente aceita fornecer um ambiente correspondente aos requisitos especificados para a Máquina."
 Comunicado Internacional de Informação para Clientes - Instalação de Máquinas IBM O objectivo do presente comunicado consiste em definir os termos IBM e descrever as práticas globais da IBM associadas
Comunicado Internacional de Informação para Clientes - Instalação de Máquinas IBM O objectivo do presente comunicado consiste em definir os termos IBM e descrever as práticas globais da IBM associadas
Unidade de Informação Financeira. Guia de preenchimento da Declaração de Identificação de Pessoas Designadas ( DIPD )
 Unidade de Informação Financeira Guia de preenchimento da Declaração de Identificação de Pessoas Designadas ( DIPD ) Índice 1. Objectivo da Declaração de Identificação de Pessoas Designadas (DIPD)... 3
Unidade de Informação Financeira Guia de preenchimento da Declaração de Identificação de Pessoas Designadas ( DIPD ) Índice 1. Objectivo da Declaração de Identificação de Pessoas Designadas (DIPD)... 3
Direitos autorais 2000 pelo Grupo de Trabalho de Harmonização Global GHTF/SG1/N29R16:2005 DOCUMENTO FINAL
 GHTF/SG1/N29R16:2005 DOCUMENTO FINAL Título: Documento informativo acerca da definição do termo produto médico Grupo de autoria: Grupo de Estudo 1 do GHTF Respaldado por: Grupo de Trabalho de Harmonização
GHTF/SG1/N29R16:2005 DOCUMENTO FINAL Título: Documento informativo acerca da definição do termo produto médico Grupo de autoria: Grupo de Estudo 1 do GHTF Respaldado por: Grupo de Trabalho de Harmonização
Jornal Oficial da União Europeia
 16.1.2004 L 10/5 REGULAMENTO (CE) N. o 65/2004 DA COMISSÃO de 14 de Janeiro de 2004 que estabelece um sistema para criação e atribuição de identificadores únicos aos organismos geneticamente modificados
16.1.2004 L 10/5 REGULAMENTO (CE) N. o 65/2004 DA COMISSÃO de 14 de Janeiro de 2004 que estabelece um sistema para criação e atribuição de identificadores únicos aos organismos geneticamente modificados
DENOMINAÇÃO, FORMA FARMACÊUTICA, DOSAGEM DO MEDICAMENTO, ESPÉCIES-ALVO, VIAS DE ADMINISTRAÇÃO E TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
 ANEXO I DENOMINAÇÃO, FORMA FARMACÊUTICA, DOSAGEM DO MEDICAMENTO, ESPÉCIES-ALVO, VIAS DE ADMINISTRAÇÃO E TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO 1/7 Requerente/Titular da Autorização de Introdução
ANEXO I DENOMINAÇÃO, FORMA FARMACÊUTICA, DOSAGEM DO MEDICAMENTO, ESPÉCIES-ALVO, VIAS DE ADMINISTRAÇÃO E TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO 1/7 Requerente/Titular da Autorização de Introdução
Como Verificar o estado da factura
 1 / 5 Como Verificar o estado da factura 1. Inicie a sessão na sua conta OB10. - Se necessitar de ajuda para o fazer, consulte o guia "Como iniciar sessão". 2. Seleccione Facturação - Clique em "Facturação"
1 / 5 Como Verificar o estado da factura 1. Inicie a sessão na sua conta OB10. - Se necessitar de ajuda para o fazer, consulte o guia "Como iniciar sessão". 2. Seleccione Facturação - Clique em "Facturação"
DECLARAÇÕES EUROPEIAS DA FARMÁCIA HOSPITALAR. SECÇÃO 1: Declaração de Princípios Introdutórios e Gestão
 DECLARAÇÕES EUROPEIAS DA FARMÁCIA HOSPITALAR As páginas que se seguem constituem as Declarações Europeias da Farmácia Hospitalar. As declarações expressam os objetivos comuns definidos para cada sistema
DECLARAÇÕES EUROPEIAS DA FARMÁCIA HOSPITALAR As páginas que se seguem constituem as Declarações Europeias da Farmácia Hospitalar. As declarações expressam os objetivos comuns definidos para cada sistema
APROVADO EM INFARMED. Folheto informativo: Informação para o utilizador. Pandermil 10 mg/g Creme. Hidrocortisona
 Folheto informativo: Informação para o utilizador Pandermil 10 mg/g Creme Hidrocortisona Leia com atenção todo este folheto antes de começar a utilizar este pois contém informação importante para si. Utilize
Folheto informativo: Informação para o utilizador Pandermil 10 mg/g Creme Hidrocortisona Leia com atenção todo este folheto antes de começar a utilizar este pois contém informação importante para si. Utilize
Instituições Superiores de Controlo Enquadramento para a Medição do Desempenho
 Instituições Superiores de Controlo Enquadramento para a Medição do Desempenho CHECKLIST DA GARANTIA DA QUALIDADE DOS TERMOS DE REFERÊNCIA Versão Preliminar 1.1 Outubro 2014 Secretariado de Doadores INTOSAI
Instituições Superiores de Controlo Enquadramento para a Medição do Desempenho CHECKLIST DA GARANTIA DA QUALIDADE DOS TERMOS DE REFERÊNCIA Versão Preliminar 1.1 Outubro 2014 Secretariado de Doadores INTOSAI
O QUE É? O RABDOMIOSARCOMA
 O QUE É? O RABDOMIOSARCOMA Músculo O RABDOMIOSARCOMA O QUE SIGNIFICA ESTADIO? O QUE É O RABDOMIOSARCOMA? O rabdomiosarcoma é um tumor dos tecidos moles (tecidos que suportam e ligam as várias partes do
O QUE É? O RABDOMIOSARCOMA Músculo O RABDOMIOSARCOMA O QUE SIGNIFICA ESTADIO? O QUE É O RABDOMIOSARCOMA? O rabdomiosarcoma é um tumor dos tecidos moles (tecidos que suportam e ligam as várias partes do
Dando cumprimento às obrigações comunitárias do Estado Português, o presente diploma procede à transposição da referida directiva.
 Transpõe para a ordem jurídica nacional a Directiva n.º 2003/63/CE, da Comissão, de 25 de Junho, que altera a Directiva n.º 2001/83/CE, do Parlamento Europeu e do Conselho, que estabelece um código comunitário
Transpõe para a ordem jurídica nacional a Directiva n.º 2003/63/CE, da Comissão, de 25 de Junho, que altera a Directiva n.º 2001/83/CE, do Parlamento Europeu e do Conselho, que estabelece um código comunitário
Projecto X-arq: módulo de gestão : Caso prático do seu desenvolvimento no Arquivo Municipal de Lisboa. Rui Paixão. Câmara Municipal de Lisboa
 Projecto X-arq: módulo de gestão : Caso prático do seu desenvolvimento no Arquivo Municipal de Lisboa Rui Paixão Câmara Municipal de Lisboa rui.alexandre.paixao@cm-lisboa.pt Palavras-chave: sistema informático,
Projecto X-arq: módulo de gestão : Caso prático do seu desenvolvimento no Arquivo Municipal de Lisboa Rui Paixão Câmara Municipal de Lisboa rui.alexandre.paixao@cm-lisboa.pt Palavras-chave: sistema informático,
ELABORADO VERIFICADO APROVADO
 Pág. n.º 1/9 LISTA DE ALTERAÇÕES Descrição da alteração Páginas Edição Data Clarificação do posicionamento hierárquico dos regulamentos municipais no âmbito do SGQ, bem como as responsabilidades pela sua
Pág. n.º 1/9 LISTA DE ALTERAÇÕES Descrição da alteração Páginas Edição Data Clarificação do posicionamento hierárquico dos regulamentos municipais no âmbito do SGQ, bem como as responsabilidades pela sua
Jornal Oficial da União Europeia L 109/11
 19.4.2008 Jornal Oficial da União Europeia L 109/11 REGULAMENTO (CE) N. o 353/2008 DA COMISSÃO de 18 de Abril de 2008 que estabelece normas de execução relativas aos pedidos de autorização de alegações
19.4.2008 Jornal Oficial da União Europeia L 109/11 REGULAMENTO (CE) N. o 353/2008 DA COMISSÃO de 18 de Abril de 2008 que estabelece normas de execução relativas aos pedidos de autorização de alegações
Anexo I. Conclusões científicas e fundamentos da alteração dos termos da(s) autorização(ões) de introdução no mercado
 Anexo I Conclusões científicas e fundamentos da alteração dos termos da(s) autorização(ões) de introdução no mercado 1 Conclusões científicas Tendo em conta o relatório de avaliação do PRAC sobre os relatórios
Anexo I Conclusões científicas e fundamentos da alteração dos termos da(s) autorização(ões) de introdução no mercado 1 Conclusões científicas Tendo em conta o relatório de avaliação do PRAC sobre os relatórios
15º - AUDHOSP ANO 2016
 15º - AUDHOSP ANO 2016 CID 11 DEBORAH PIMENTA FERREIRA Médica Equipe Assessoria Técnica de Tecnologia da Informação SMS/SP Set/2016 Breve introdução à CID A CID (Classificação Estatística Internacional
15º - AUDHOSP ANO 2016 CID 11 DEBORAH PIMENTA FERREIRA Médica Equipe Assessoria Técnica de Tecnologia da Informação SMS/SP Set/2016 Breve introdução à CID A CID (Classificação Estatística Internacional
XI Encuentro de Autoridades Competentes en Medicamentos de los Países Iberoamericanos (EAMI) de junio de 2016, Cuba
 Prof. Doutor Henrique Luz Rodrigues Presidente do Conselho Diretivo do INFARMED, I.P. XI Encuentro de Autoridades Competentes en Medicamentos de los Países Iberoamericanos (EAMI) 21-24 de junio de 2016,
Prof. Doutor Henrique Luz Rodrigues Presidente do Conselho Diretivo do INFARMED, I.P. XI Encuentro de Autoridades Competentes en Medicamentos de los Países Iberoamericanos (EAMI) 21-24 de junio de 2016,
Por Constantino W. Nassel
 NORMA ISO 9000 SISTEMA DE GESTÃO DA QUALIDADE ISO 9001:2000 REQUISITOS E LINHAS DE ORIENTAÇÃO PARA IMPLEMENTAÇÃO Por Constantino W. Nassel CONTEÚDOS O que é a ISO? O que é a ISO 9000? Histórico Normas
NORMA ISO 9000 SISTEMA DE GESTÃO DA QUALIDADE ISO 9001:2000 REQUISITOS E LINHAS DE ORIENTAÇÃO PARA IMPLEMENTAÇÃO Por Constantino W. Nassel CONTEÚDOS O que é a ISO? O que é a ISO 9000? Histórico Normas
ADENDA AO MANUAL SOBRE A APLICAÇÃO PRÁTICA DO REGULAMENTO INN
 ADENDA AO MANUAL SOBRE A APLICAÇÃO PRÁTICA DO REGULAMENTO INN Trata-se de uma adenda à primeira edição do Manual sobre a aplicação prática do Regulamento (CE) n.º 1005/2008 do Conselho, de 29 de Setembro
ADENDA AO MANUAL SOBRE A APLICAÇÃO PRÁTICA DO REGULAMENTO INN Trata-se de uma adenda à primeira edição do Manual sobre a aplicação prática do Regulamento (CE) n.º 1005/2008 do Conselho, de 29 de Setembro
PT 1 PT COMISSÃO DAS COMUNIDADES EUROPEIAS BRUXELAS, 20/10/2009 ORÇAMENTO GERAL SECÇÃO III COMISSÃO, TÍTULOS 07, 17, 40
 COMISSÃO S COMUNIDES EUROPEIAS ORÇAMENTO GERAL - 2009 SECÇÃO III COMISSÃO, TÍTULOS 07, 17, 40 BRUXELAS, 20/10/2009 TRANSFERÊNCIA DE DOTAÇÕES N. DEC 41/2009 DESPESAS NÃO OBRIGATÓRIAS EUR ORIGEM S DOTAÇÕES
COMISSÃO S COMUNIDES EUROPEIAS ORÇAMENTO GERAL - 2009 SECÇÃO III COMISSÃO, TÍTULOS 07, 17, 40 BRUXELAS, 20/10/2009 TRANSFERÊNCIA DE DOTAÇÕES N. DEC 41/2009 DESPESAS NÃO OBRIGATÓRIAS EUR ORIGEM S DOTAÇÕES
Decisão da Comissão de /693/UE
 Relatório sobre a aplicação da Directiva 2004/42 do Parlamento Europeu e do Conselho de 21 de Abril de 2004 Decisão da Comissão de 22.07.2010 2010/693/UE Período de abrangência 2010 Lisboa 2011 Índice
Relatório sobre a aplicação da Directiva 2004/42 do Parlamento Europeu e do Conselho de 21 de Abril de 2004 Decisão da Comissão de 22.07.2010 2010/693/UE Período de abrangência 2010 Lisboa 2011 Índice
(Atos não legislativos) REGULAMENTOS
 31.8.2016 L 234/1 II (Atos não legislativos) REGULAMENTOS REGULAMENTO DELEGADO (UE) 2016/1437 DA COMISSÃO de 19 de maio de 2016 que complementa a Diretiva 2004/109/CE do Parlamento Europeu e do Conselho
31.8.2016 L 234/1 II (Atos não legislativos) REGULAMENTOS REGULAMENTO DELEGADO (UE) 2016/1437 DA COMISSÃO de 19 de maio de 2016 que complementa a Diretiva 2004/109/CE do Parlamento Europeu e do Conselho
VALOR VIDA. Produto: ZDVI1 NOVO ALTERAÇÃO. Mod. K281/001 - Junho Pág. 1/5
 VALOR VIDA Produto: ZDVI1 NOVO ALTERAÇÃO Tipo de Prémio: Nivelado Anual Renovável: Pág. 1/5 PRIMEIRO SEGURADO - Preencher apenas se diferente do Tomador do Seguro SEGUNDO SEGURADO - Preencher apenas se
VALOR VIDA Produto: ZDVI1 NOVO ALTERAÇÃO Tipo de Prémio: Nivelado Anual Renovável: Pág. 1/5 PRIMEIRO SEGURADO - Preencher apenas se diferente do Tomador do Seguro SEGUNDO SEGURADO - Preencher apenas se
Estado-Membro Titular da Autorização de Introdução no Mercado Nome de fantasia Dosagem Forma farmacêutica Via de administração
 ANEXO I LISTA DAS DENOMINAÇÕES, FORMA FARMACÊUTICA, DOSAGEM, VIA DE ADMINISTRAÇÃO DO MEDICAMENTO, TITULARES DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO NOS ESTADOS-MEMBROS 1 Estado-Membro Titular da Autorização
ANEXO I LISTA DAS DENOMINAÇÕES, FORMA FARMACÊUTICA, DOSAGEM, VIA DE ADMINISTRAÇÃO DO MEDICAMENTO, TITULARES DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO NOS ESTADOS-MEMBROS 1 Estado-Membro Titular da Autorização
Enviar dinheiro em segurança
 Enviar dinheiro em segurança É este o seu caso? Vai enviar dinheiro para uma pessoa ou para uma empresa, e: está a utilizar uma empresa que não é um banco nem uma sociedade de crédito imobiliário. Nesse
Enviar dinheiro em segurança É este o seu caso? Vai enviar dinheiro para uma pessoa ou para uma empresa, e: está a utilizar uma empresa que não é um banco nem uma sociedade de crédito imobiliário. Nesse
Condições gerais de utilização Website
 Condições gerais de utilização Website www.hra-pregnancy-registry.com Os presentes termos e condições gerais de utilização têm por objetivo definir os direitos e as obrigações de todos os utilizadores,
Condições gerais de utilização Website www.hra-pregnancy-registry.com Os presentes termos e condições gerais de utilização têm por objetivo definir os direitos e as obrigações de todos os utilizadores,
PARECER n.º 01/2006 DA AGÊNCIA EUROPEIA PARA A SEGURANÇA DA AVIAÇÃO
 PARECER n.º 01/2006 DA AGÊNCIA EUROPEIA PARA A SEGURANÇA DA AVIAÇÃO relativo a um Regulamento da Comissão que altera o Regulamento (CE) n.º 1592/2002 do Parlamento Europeu e do Conselho relativo a regras
PARECER n.º 01/2006 DA AGÊNCIA EUROPEIA PARA A SEGURANÇA DA AVIAÇÃO relativo a um Regulamento da Comissão que altera o Regulamento (CE) n.º 1592/2002 do Parlamento Europeu e do Conselho relativo a regras
SAÚDE SOLUÇÃO PARA O CONTROLO DA LEGISLAÇÃO. Destinatários. Benefícios
 SOLUÇÃO PARA O CONTROLO DA LEGISLAÇÃO Destinatários Todas as Instituições Prestadoras de Cuidados de Saúde Instituições certificadas ( ISO 9001 ) Prestadores de Serviços Complementares de Diagnóstico e
SOLUÇÃO PARA O CONTROLO DA LEGISLAÇÃO Destinatários Todas as Instituições Prestadoras de Cuidados de Saúde Instituições certificadas ( ISO 9001 ) Prestadores de Serviços Complementares de Diagnóstico e
GUIA PARA O PREENCHIMENTO DOS FORMULÁRIOS SISTEMA DE GESTÃO PARA EMBALAGENS NÃO REUTILIZÁVEIS
 GUIA PARA O PREENCHIMENTO DOS FORMULÁRIOS SISTEMA DE GESTÃO PARA EMBALAGENS NÃO REUTILIZÁVEIS Versão: 1.0 Data: 05-06-2009 Índice Acesso e estados dos Formulários... 3 Escolha do Formulário e submissão...
GUIA PARA O PREENCHIMENTO DOS FORMULÁRIOS SISTEMA DE GESTÃO PARA EMBALAGENS NÃO REUTILIZÁVEIS Versão: 1.0 Data: 05-06-2009 Índice Acesso e estados dos Formulários... 3 Escolha do Formulário e submissão...
Legislação Farmacêutica Compilada. Decreto-Lei n.º 94/95, de 9 de Maio. INFARMED - Gabinete Jurídico e Contencioso 129
 Regime jurídico da introdução no mercado, do fabrico, da comercialização, da rotulagem e da publicidade dos produtos homeopáticos para uso humano (Revogado pelo Decreto-Lei n.º 176/2006, de 30 de Agosto)
Regime jurídico da introdução no mercado, do fabrico, da comercialização, da rotulagem e da publicidade dos produtos homeopáticos para uso humano (Revogado pelo Decreto-Lei n.º 176/2006, de 30 de Agosto)
Como utilizar o presente manual
 Como utilizar o presente manual O presente manual orienta o utilizador ao longo do processo de pedido de licença relativa ao rótulo ecológico da UE, em conformidade com os requisitos dos critérios aplicáveis.
Como utilizar o presente manual O presente manual orienta o utilizador ao longo do processo de pedido de licença relativa ao rótulo ecológico da UE, em conformidade com os requisitos dos critérios aplicáveis.
Manual do Revisor Oficial de Contas. Directriz de Revisão/Auditoria 800
 Directriz de Revisão/Auditoria 800 Dezembro de 2001 Relatório do Revisor/Auditor sobre Trabalhos com Finalidade Especial ÍNDICE Parágrafos INTRODUÇÃO 1-3 CONSIDERAÇÕES GERAIS 4-10 RELATÓRIOS SOBRE DEMONSTRAÇÕES
Directriz de Revisão/Auditoria 800 Dezembro de 2001 Relatório do Revisor/Auditor sobre Trabalhos com Finalidade Especial ÍNDICE Parágrafos INTRODUÇÃO 1-3 CONSIDERAÇÕES GERAIS 4-10 RELATÓRIOS SOBRE DEMONSTRAÇÕES
Um SGBD permite que cada utilizador tenha uma vista diferente (abstrata) do conteúdo da base de dados;
 1 Bioinformatica Conceitos Básicos Camadas de abstração Um SGBD permite que cada utilizador tenha uma vista diferente (abstrata) do conteúdo da base de dados; Cada utilizador necessita de ter acesso a
1 Bioinformatica Conceitos Básicos Camadas de abstração Um SGBD permite que cada utilizador tenha uma vista diferente (abstrata) do conteúdo da base de dados; Cada utilizador necessita de ter acesso a
GARANTIA Período de Garantia Como acionar a Garantia
 Garantia G004270 GARANTIA A Mundo Reader, S.L., ( Mundo Reader ) oferece a presente Garantia Limitada aos compradores do(s) produto(s) bq incluído(s) no pacote de venda ( Produto ). A Mundo Reader garante-lhe
Garantia G004270 GARANTIA A Mundo Reader, S.L., ( Mundo Reader ) oferece a presente Garantia Limitada aos compradores do(s) produto(s) bq incluído(s) no pacote de venda ( Produto ). A Mundo Reader garante-lhe
ANEXO ANEXO I MODELO DE CARTA QUE ACOMPANHA UM PEDIDO DE CONSULTA PARA A DETERMINAÇÃO DO ESTATUTO DE NOVO ALIMENTO
 EN ANEXO ANEXO I MODELO DE CARTA QUE ACOMPANHA UM PEDIDO DE CONSULTA PARA A DETERMINAÇÃO DO ESTATUTO DE NOVO ALIMENTO Autoridade competente do Estado-Membro Data: Assunto: Pedido de consulta para determinação
EN ANEXO ANEXO I MODELO DE CARTA QUE ACOMPANHA UM PEDIDO DE CONSULTA PARA A DETERMINAÇÃO DO ESTATUTO DE NOVO ALIMENTO Autoridade competente do Estado-Membro Data: Assunto: Pedido de consulta para determinação
NEUROCIRURGIA o que é neurocirurgia?
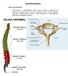 NEUROCIRURGIA o que é neurocirurgia? Neurocirurgia é a especialidade médica que se ocupa do tratamento de doenças do sistema nervoso central e periférico (como tumores, doenças vasculares, degenerativas),
NEUROCIRURGIA o que é neurocirurgia? Neurocirurgia é a especialidade médica que se ocupa do tratamento de doenças do sistema nervoso central e periférico (como tumores, doenças vasculares, degenerativas),
Test. este Xpert MTB/RIF. Ferramenta de avaliação e monitorização clínica Visita de avaliação global
 Test este Xpert MTB/RIF Ferramenta de avaliação e monitorização clínica Visita de avaliação global Esta ferramenta destina-se a ser utilizado por pessoal / consultores que realizam visitas de monitorização
Test este Xpert MTB/RIF Ferramenta de avaliação e monitorização clínica Visita de avaliação global Esta ferramenta destina-se a ser utilizado por pessoal / consultores que realizam visitas de monitorização
Hidrocortisona Bluepharma, pela sua ação refrescante e secante, está indicado nas situações agudas e exsudativas.
 Folheto informativo: Informação para o utilizador Hidrocortisona Bluepharma 10 mg/g Creme Hidrocortisona Leia com atenção todo este folheto antes de começar a utilizar este medicamento, pois contém informação
Folheto informativo: Informação para o utilizador Hidrocortisona Bluepharma 10 mg/g Creme Hidrocortisona Leia com atenção todo este folheto antes de começar a utilizar este medicamento, pois contém informação
Internações Hospitalares. Primeira Base de Dados da Parceria Close-Up com SINDUSFARMA
 Internações Hospitalares Primeira Base de Dados da Parceria Close-Up com SINDUSFARMA 2 Bases de Dados Planejadas para 2018 Internações Hospitalares CEAF Componente Especializado da Administração Farmaceutica
Internações Hospitalares Primeira Base de Dados da Parceria Close-Up com SINDUSFARMA 2 Bases de Dados Planejadas para 2018 Internações Hospitalares CEAF Componente Especializado da Administração Farmaceutica
ANEXO I. Perguntas e Respostas sobre a revisão benefício-risco do piroxicam
 ANEXO I Perguntas e Respostas sobre a revisão benefício-risco do piroxicam A Agência Europeia de Medicamentos (EMEA) completou recentemente a avaliação da segurança do anti-inflamatório não esteróide (AINE)
ANEXO I Perguntas e Respostas sobre a revisão benefício-risco do piroxicam A Agência Europeia de Medicamentos (EMEA) completou recentemente a avaliação da segurança do anti-inflamatório não esteróide (AINE)
GUIA PARA O PREENCHIMENTO DOS FORMULÁRIOS - ENTIDADE GESTORA SOGILUB
 GUIA PARA O PREENCHIMENTO DOS FORMULÁRIOS - ENTIDADE GESTORA SOGILUB Versão: 1.0 Data: 05-06-2009 Índice Acesso e estados dos Formulários... 3 Escolha do Formulário e submissão... 4 Bases para a navegação
GUIA PARA O PREENCHIMENTO DOS FORMULÁRIOS - ENTIDADE GESTORA SOGILUB Versão: 1.0 Data: 05-06-2009 Índice Acesso e estados dos Formulários... 3 Escolha do Formulário e submissão... 4 Bases para a navegação
TRAUMATISMO RAQUIMEDULAR
 TRAUMATISMO RAQUIMEDULAR Definição Entende-se por traumatismo raquimedular lesão de qualquer causa externa na coluna vertebral, incluindo ou não medula ou raízes nervosas, em qualquer dos seus segmentos
TRAUMATISMO RAQUIMEDULAR Definição Entende-se por traumatismo raquimedular lesão de qualquer causa externa na coluna vertebral, incluindo ou não medula ou raízes nervosas, em qualquer dos seus segmentos
PT Unida na diversidade PT A8-0188/298. Alteração. Marco Zullo em nome do Grupo EFDD
 7.9.2017 A8-0188/298 298 Anexo I Secção IV Parte A Serviços de comunicação social audiovisual e equipamentos com capacidades informáticas avançadas conexos, para uso dos consumidores Serviços de comunicação
7.9.2017 A8-0188/298 298 Anexo I Secção IV Parte A Serviços de comunicação social audiovisual e equipamentos com capacidades informáticas avançadas conexos, para uso dos consumidores Serviços de comunicação
GUIA PARA O PREENCHIMENTO DOS FORMULÁRIOS ENTIDADE GESTORA VALORMED
 GUIA PARA O PREENCHIMENTO DOS FORMULÁRIOS ENTIDADE GESTORA VALORMED Versão: 1.0 Data: 05-06-2009 Índice Acesso e estados dos Formulários... 3 Escolha do Formulário e submissão... 4 Bases para a navegação
GUIA PARA O PREENCHIMENTO DOS FORMULÁRIOS ENTIDADE GESTORA VALORMED Versão: 1.0 Data: 05-06-2009 Índice Acesso e estados dos Formulários... 3 Escolha do Formulário e submissão... 4 Bases para a navegação
Este medicamento pertence ao grupo farmacoterapêutico 9.4 Medicamentos para tratamento da artrose.
 Folheto informativo: Informação para o utilizador Glucosamina Tedec 1500 mg pó para solução oral Sulfato de glucosamina Leia com atenção todo este folheto antes de começar a tomar este medicamento pois
Folheto informativo: Informação para o utilizador Glucosamina Tedec 1500 mg pó para solução oral Sulfato de glucosamina Leia com atenção todo este folheto antes de começar a tomar este medicamento pois
ÍNDICE. Parágrafo Introdução
 NORMA INTERNACIONAL DE 720 AS RESPONSABILIDADES DO AUDITOR RELATIVAS A OUTRA INFORMAÇÃO EM DOCUMENTOS QUE CONTENHAM DEMONSTRAÇÕES FINANCEIRAS AUDITADAS (Aplicável a auditorias de demonstrações financeiras
NORMA INTERNACIONAL DE 720 AS RESPONSABILIDADES DO AUDITOR RELATIVAS A OUTRA INFORMAÇÃO EM DOCUMENTOS QUE CONTENHAM DEMONSTRAÇÕES FINANCEIRAS AUDITADAS (Aplicável a auditorias de demonstrações financeiras
SISTEMA DE GESTÃO DA QUALIDADE
 Gestão Documental OF.Q-P001-00 P 1 / 7 A. OBJECTIVO Definir as regras formais para redacção dos modelos que documentam os Sistemas de Gestão da Qualidade tutelados pela Ordem dos Farmacêuticos. B. ÂMBITO
Gestão Documental OF.Q-P001-00 P 1 / 7 A. OBJECTIVO Definir as regras formais para redacção dos modelos que documentam os Sistemas de Gestão da Qualidade tutelados pela Ordem dos Farmacêuticos. B. ÂMBITO
PLANO DE TRANSIÇÃO E ALTERAÇÕES
 SISTEMA COMUNITÁRIO DE ECOGESTÃO E AUDITORIA Regulamento (UE) 2018/2026, de 19 de dezembro de 2018 PLANO DE TRANSIÇÃO E ALTERAÇÕES janeiro de 2019 PLANO DE TRANSIÇÃO No passado dia 20 de dezembro de 2018
SISTEMA COMUNITÁRIO DE ECOGESTÃO E AUDITORIA Regulamento (UE) 2018/2026, de 19 de dezembro de 2018 PLANO DE TRANSIÇÃO E ALTERAÇÕES janeiro de 2019 PLANO DE TRANSIÇÃO No passado dia 20 de dezembro de 2018
ELABORADO VERIFICADO APROVADO
 Pág. n.º 1/9 LISTA DE ALTERAÇÕES Descrição da alteração Páginas Edição Data ELABORADO VERIFICADO APROVADO Pág. n.º 2/9 1. OBJECTIVO: Descrever a forma de gerir e controlar os documentos e registos do Sistema
Pág. n.º 1/9 LISTA DE ALTERAÇÕES Descrição da alteração Páginas Edição Data ELABORADO VERIFICADO APROVADO Pág. n.º 2/9 1. OBJECTIVO: Descrever a forma de gerir e controlar os documentos e registos do Sistema
Jornal Oficial da União Europeia L 166/3
 27.6.2008 Jornal Oficial da União Europeia L 166/3 REGULAMENTO (CE) N. o 605/2008 DA COMISSÃO de 20 de Junho de 2008 que estabelece as regras de execução das disposições relativas ao certificado de controlo
27.6.2008 Jornal Oficial da União Europeia L 166/3 REGULAMENTO (CE) N. o 605/2008 DA COMISSÃO de 20 de Junho de 2008 que estabelece as regras de execução das disposições relativas ao certificado de controlo
Código Mundial Antidopagem
 Código Mundial Antidopagem LISTA INTERNACIONAL DE SUBSTÂNCIAS E MÉTODOS PROIBIDOS PARA 2004 NORMA INTERNACIONAL A presente Lista entrará em vigor em 1 de Janeiro de 2004 O PROCESSO Nos termos do Código
Código Mundial Antidopagem LISTA INTERNACIONAL DE SUBSTÂNCIAS E MÉTODOS PROIBIDOS PARA 2004 NORMA INTERNACIONAL A presente Lista entrará em vigor em 1 de Janeiro de 2004 O PROCESSO Nos termos do Código
Enxerto injectável MIIG Estão incluídos na presente embalagem os idiomas seguintes:
 Enxerto injectável MIIG 150816-0 Estão incluídos na presente embalagem os idiomas seguintes: Inglês (en) Alemão (de) Holandês (nl) Francês (fr) Espanhol (es) Italiano (it) Português (pt) 中文 - Chinês (ch)
Enxerto injectável MIIG 150816-0 Estão incluídos na presente embalagem os idiomas seguintes: Inglês (en) Alemão (de) Holandês (nl) Francês (fr) Espanhol (es) Italiano (it) Português (pt) 中文 - Chinês (ch)
Documentação e Ajudas
 Interfaces Pessoa Máquina Documentação e Ajudas Cap. 12 Manuais e Documentação 20 Melhor e Pior? Melhor e Pior? Resumo Aula Anterior Multiplicidade de Dispositivos de Interação Entrada de Texto Introdução
Interfaces Pessoa Máquina Documentação e Ajudas Cap. 12 Manuais e Documentação 20 Melhor e Pior? Melhor e Pior? Resumo Aula Anterior Multiplicidade de Dispositivos de Interação Entrada de Texto Introdução
COMISSÃO DAS COMUNIDADES EUROPEIAS. Projecto de. REGULAMENTO (CE) n.º /2001 da COMISSÃO
 COMISSÃO DAS COMUNIDADES EUROPEIAS Bruxelas, 22.5.2001 Projecto de REGULAMENTO (CE) n.º /2001 da COMISSÃO de [ ] que estabelece regras pormenorizadas para a aplicação do Regulamento (CE) n.º 2494/95 do
COMISSÃO DAS COMUNIDADES EUROPEIAS Bruxelas, 22.5.2001 Projecto de REGULAMENTO (CE) n.º /2001 da COMISSÃO de [ ] que estabelece regras pormenorizadas para a aplicação do Regulamento (CE) n.º 2494/95 do
PAVIMENTOS ALIGEIRADOS DE PRANCHAS PREFABRICADAS DE BETÃO PRÉ-ESFORÇADO
 DEPARTAMENTO DE EDIFÍCIOS Núcleo de Tecnologia da Construção Proc. 0802/11/17791 PAVIMENTOS ALIGEIRADOS DE PRANCHAS PREFABRICADAS DE BETÃO PRÉ-ESFORÇADO Ficha de caracterização da produção. Parte 1 Estudo
DEPARTAMENTO DE EDIFÍCIOS Núcleo de Tecnologia da Construção Proc. 0802/11/17791 PAVIMENTOS ALIGEIRADOS DE PRANCHAS PREFABRICADAS DE BETÃO PRÉ-ESFORÇADO Ficha de caracterização da produção. Parte 1 Estudo
Jornal Oficial da União Europeia L 64/15
 11.3.2011 Jornal Oficial da União Europeia L 64/15 REGULAMENTO (UE) N. o 234/2011 DA COMISSÃO de 10 de Março de 2011 que executa o Regulamento (CE) n. o 1331/2008 do Parlamento Europeu e do Conselho que
11.3.2011 Jornal Oficial da União Europeia L 64/15 REGULAMENTO (UE) N. o 234/2011 DA COMISSÃO de 10 de Março de 2011 que executa o Regulamento (CE) n. o 1331/2008 do Parlamento Europeu e do Conselho que
Despacho n.º B/2001, de 31 de Maio 1 (DR, 2.ª série n.º 148, de 28 de Junho de 2001)
 1 (DR, 2.ª série n.º 148, de 28 de Junho de 2001) Regulamentação das autorizações de utilização especial de medicamentos (Revogado pelo Despacho n.º 9114/2002, de15 de Março) O despacho n.º 17 495/2000,
1 (DR, 2.ª série n.º 148, de 28 de Junho de 2001) Regulamentação das autorizações de utilização especial de medicamentos (Revogado pelo Despacho n.º 9114/2002, de15 de Março) O despacho n.º 17 495/2000,
