CAROLINE FERNANDES DOS SANTOS
|
|
|
- Giovanni Custódio das Neves
- 8 Há anos
- Visualizações:
Transcrição
1 CAROLINE FERNANDES DOS SANTOS Agonistas PPAR (rosiglitazona, bezafibrato e fenofibrato) e alterações bioquímicas e estruturais em órgãos-alvo de camundongos C57BL/6 alimentados com dieta hiperlipídica rica em sacarose Tese apresentada como requisito parcial para a obtenção do título de Doutor em Ciências no Programa de Pós-Graduação em Biologia Humana e Experimental, Universidade do Estado do Rio de Janeiro. Orientador: Professor Doutor Carlos Alberto Mandarim-de-Lacerda Rio de Janeiro, RJ 2010
2 CAROLINE FERNANDES DOS SANTOS Agonistas PPAR (rosiglitazona, bezafibrato e fenofibrato) e alterações bioquímicas e estruturais em órgãos-alvo de camundongos C57BL/6 alimentados com dieta hiperlipídica rica em sacarose Apresentada em: 7 de junho de 2010 Banca Examinadora: Prof. Dr. Carlos Alberto Mandarim-de-Lacerda (orientador) Rio de Janeiro, RJ 2010
3 DEDICATÓRIA À minha família, aos amigos queridos, ao meu orientador.
4 AGRADECIMENTOS Aos meus pais, pelo apoio e amor incondicional. Por terem ajudado sua filha de 17 anos a ir para a cidade grande cursar uma universidade e conquistar o mundo! À Prof. Dra. Leila Maria Meirelles Pereira, pelo incentivo no meu 2 período de faculdade em Ciências Biológicas a iniciar o estágio de Iniciação Científica no Laboratório de Morfometria e Morfologia Cardiovascular (LMMC) da Uerj, laboratório onde me encontrei e permaneço até hoje. Ao Prof. Dr. Carlos Alberto Mandarim de Lacerda, por toda a orientação ao longo desses nove anos, desde a Iniciação Científica, passando pelo Mestrado e agora Doutorado, pelo incentivo constante a auto-superação, ao aprendizado de novas técnicas e a aquisição de novos conhecimentos. E não posso esquecer também do zelo pelo planejamento do protocolo experimental e na aplicação das técnicas, pois nada é mais forte que a sua parte mais fraca. E é claro, se ao longo do meu caminho enxerguei mais longe, foi porque eu estava apoiada no ombro de um gigante. À Prof. Dra. Márcia Barbosa Águila, por ter me acolhido e adotado como orientanda. Seu conhecimento sobre dietas experimentais foi fundamental para a execução do trabalho. Ao nutricionista Rafael Evangelista, que participou deste trabalho como aluno de Iniciação Científica, por toda a ajuda. Além do aprendizado das técnicas, espero que esse trabalho tenha contribuído com a sua formação tanto profissional quanto científica. À técnica Thatiany Marinho, por toda a assistência durante o desenvolvimento deste trabalho. Obrigada por seccionar meu material e pela ajuda na compra do material necessário para a realização da imunohistoquímica. Fico muito feliz que você tenha escolhido seguir a carreira de Biólogo, lhe desejo muito sucesso nessa sua nova empreitada.
5 Aos amigos de longa data Leonardo Mendonça e Mariana Catta-Preta, por toda a ajuda, apoio e produtivas discussões sobre nossos trabalhos ao longo de nossos mestrado e doutorado. Vocês sempre estiveram presentes e sempre me ajudaram, creio que sempre estarão, e sei que posso contar com vocês sempre que necessário. Aos amigos de curta data cultivados ao longo do doutorado, Thiago Torres, Sandra Barbosa, Lyana Parente, Daniele Bezerra e Fernanda Amorim, que também sempre me apoiaram verdadeiramente, assim como contribuíram inúmeras vezes com profundas discussões sobre o andamento de nossos trabalhos. À equipe LMMC news e Titanic, por descontrair nosso ambiente de trabalho com atualizações diárias dos acontecimentos inéditos. Nosso barco pode ficar à deriva, mas não afundará nunca! Aos secretários Ciro Reis e Simone por estarem sempre dispostos a resolver nossos pepinos como cancelar uma disciplina aqui, resolver assuntos de bolsa ali... Obrigada por terem paciência comigo durante o processo de pedido da bolsa PDEE Capes. Ao Prof. Dr. Kamal Rahmouni por ter me acolhido em seu laboratório durante o doutorado sandwich. Também agradeço ao Donald Morgan e ao Deng-Fuo Guo pelo ensino das técnicas de fisiologia e biologia molecular, além dos demais integrantes do laboratório Leonard Brooks, Shannon Harlan e Kenjiro Muta. À Elisa Mandarim por ter me apresentado à Iowa City e me ajudado nos primeiros meses de adaptação à cidade. Aos amigos conquistados durante o doutorado sandwich Milena Pires, Robert Corso, Marlon Hernadez, Luciana Cunha, Evan Roz, Gustavo Koberstein, Ian DeVolder e Aline Hilzendeger, pelos momentos de descontração, pelo apoio e por terem tornado a minha estadia longe de casa mais fácil. À todos os componentes do LMMC por todo o apoio e torcida ao longo do desenvolvimento deste projeto.
6 Só sabemos com exatidão quando sabemos pouco à medida que adquirimos conhecimento. Instala-se a dúvida. Johann Goethe
7 RESUMO FERNANDES-SANTOS Caroline. Agonistas PPAR (rosiglitazona, bezafibrato e fenofibrato) e alterações bioquímicas e estruturais em órgãos-alvo de camundongos C57BL/6 alimentados com dieta hiperlipídica rica em sacarose. Tese (Doutorado em Ciências, Biologia Humana e Experimental) IBRAG, Universidade do Estado do Rio de Janeiro, Rio de Janeiro, Este trabalho teve o objetivo de estudar o efeito de medicamentos com diferentes ações agonista PPAR (rosiglitazona, fenofibrato e bezafibrato) sobre o perfil lipídico, glicídico e alterações na massa corporal e morfologia do tecido adiposo e pancreático em modelo de diabetes e sobrepeso induzido por dieta. Camundongos C57BL/6 (2 meses de idade) foram alimentados com dieta padrão (SC, n=10) ou dieta hiperlipídica rica em sacarose (HFHS, n=40) por 6 semanas. Logo após, os animais HFHS foram subdividos em: HFHS não tratado e HFHS tratado com rosiglitazona (HFHS-Ro), fenofibrato (HFHS-Fe) ou bezafibrato (HFHS-Bz) (5 semanas). Os camundongos alimentados com dieta HFHS apresentaram maior glicemia e insulina de jejum (+33% e +138%, respectivamente), intolerância à glicose, resistência à insulina, aumento da massa corporal (MC) (+20%) e adiposidade, hipertrofia de adipócitos e redução da imunocoloração para adiponectina no tecido adiposo. No pâncreas houve aumento da massa (+28%), acúmulo de gordura (+700%), hipertrofia da ilhota (+38%) e redução da imunocoloração para GLUT-2 (-60%). A rosiglitazona diminuiu a glicemia e insulina de jejum, porém induziu o ganho de MC e hipertrofia cardíaca. O fenofibrato estabilizou a MC, enquanto o bezafibrato levou a perda de MC. Apenas o bezafibrato impediu a hipertrofia da ilhota. A imunocoloração para GLUT-2 foi aumentada por todos os medicamentos, e não houve alterações na imunocoloração para o PPARα. Sinais morfológicos de pancreatite foram vistos no grupo HFHS-Fe, apesar dos níveis normais de amilase e lipase séricos. A rosiglitazona exacerbou a infiltração intrapancreática de gordura (+75% vs. HFHS), e o bezafibrato aumento a imunocoloração para o PPARβ/δ nas ilhotas pancreáticas. Em conclusão, o bezafibrato apresentou um efeito mais amplo sobre as alterações metabólicas, morfológicas e biométricas decorrentes da dieta HFHS, sugerindo que a inibição das três isoformas do PPAR seria melhor do que a inibição de apenas uma isoforma. A rosiglitazona exacerbou o ganho de MC, a infiltração de gordura no pâncreas e induziu hipertrofia cardíaca, assim, é necessário cautela ao prescrever este medicamento a um paciente obeso. Palavras chaves: Receptor ativador de proliferação peroxissomal, dieta hiperlipídica rica em sacarose, doença pancreática gordurosa não-alcoólica, fibratos, rosiglitazona, adiponectina.
8 ABSTRACT This work aimed to evaluate the effect of peroxisome proliferator-activated receptor (PPAR) agonists (rosiglitazone, fenofibrate and bezafibrate) on lipid and glucose metabolism, body mass, and adipose and pancreatic tissue morphology in a model of diet-induced type 2 diabetes and overweight in mice. Two-month-old male C57BL/6 mice were fed a standard chow (SC, n=10) or a high-fat high-sucrose chow (HFHS, n=40) for 6 weeks, and then HFHS-fed mice were subdivided by treatment: untreated HFHS and HFHS treated with rosiglitazone (HFHS-Ro), fenofibrate (HFHS-Fe), or bezafibrate (HFHS-Bz) (5 weeks on medication). HFHS-fed mice have altered fasting glucose (+33%) and insulin (+138%), GI, IR, increased body mass (+20%) and fat pad weight, adipocyte hypertrophy, and decreased adiponectin immunostain. They also presented increased pancreatic (+28%) mass, intrapancreatic fat (+700%), islet hypertrophy (+38%), and decreased GLUT-2 immunostain (-60%). Rosiglitazone reduced fasting glucose and insulin but induced weight gain and heart hypertrophy. Fenofibrate impaired body mass gain, while bezafibrate induced weight loss. Only bezafibrate impaired islet hypertrophy. GLUT-2 immunostain was improved by all treatments, and there were no alterations in PPAR-α stain. There were morphological signs of pancreatitis in fenofibrate-treated mice, although there was no alteration in serum amylase and lipase. Rosiglitazone exacerbated pancreatic fat infiltration (+75% vs. HFHS group), and bezafibrate increased PPAR-β expression in pancreatic islets. In conclusion, bezafibrate showed a wider range of action on metabolic, morphologic, and biometric alterations due to HFHS intake, suggesting that inhibiting the three PPAR isoforms is better than inhibiting each isoform alone. Rosiglitazone exacerbated body mass gain, pancreatic fat infiltration and induced heart hypertrophy as well, thus, precaution has to be taken in prescribing rosiglitazone to obese patients. Key words: Peroxisome proliferator-activated receptor, high-fat high-sucrose diet, nonalcoholic fatty pancreatic disease, fibrates, rosiglitazone, adiponectin.
9 LISTA DE ILUSTRAÇÕES Figura Página 1 Lipotoxicidade na síndrome metabólica Regulação da glicemia pela insulina Tecido adiposo: células e adipocinas Padrões de distribuição da gordura corporal na obesidade Ativação do PPAR e transcrição gênica Morfometria do adipócito Quantificação da densidade de volume de gordura pancreática Quantificação da imunocoloração nas ilhotas pancreáticas Eficiência alimentar dos diferentes grupos experimentais, nos períodos pré-tratamento e pós-tratamento Evolução da massa corporal ao longo do experimento Teste oral de tolerância à glicose Hipertrofia cardíaca Adipócitos na gordura retroperitoneal Regressão linear e correlação de Pearson entre o diâmetro do adipócito da gordura retroperitoneal e a resistência à insulina (avaliada pelo HOMA-IR) Imunocoloração para adiponectina no tecido adiposo retroperitoneal Fotomicrografias do tecido pancreático mostrando os achados mais frequentes Fotomicrografias de ilhotas pancreáticas coradas com diferentes anticorpos... 77
10 LISTA DE TABELAS Tabela Página 1 Componentes da Síndrome Metabólica segundo o NCEP-ATP III Modelos de Doenças Metabólicas induzidas por Dieta Composição das dietas Ingestão de Ração, Energia e Água Metabolismo Lipídico e Glicídico e Função Pancreática Gorduras Viscerais e Subcutânea e Diâmetro do Adipócito Regressão linear e correlação entre o diâmetro do adipócito de diferentes depósitos de gordura e parâmetros do metabolismo glicídico Quantificação da Imunocoloração para Adiponectina no Tecido Adiposo (sistema semiquantitativo por escore) Massa Pancreática, Diâmetro da Ilhota e Gordura Pancreática Quantificação da Densidade de Imunomarcação nas Ilhotas Pancreáticas... 78
11 LISTA DE ABREVIATURAS E SIGLAS Sigla Definição Sigla Definição AGL Ácido graxo livre LGK Glicoquinase hepática AIN93 Guia nutricional para roedores LPL Lipase lipoproteica AMPK Adenosina monofosfato quinase MCP-1 Proteína quimiotática do macrófago 1 APOA1 Apolipoproteína A-1 NaCl Cloreto de sódio ASC Área sob a curva NCEP- ATPIII Programa Nacional de Educação do Colesterol Terceiro Painel de Tratamento do Adulto ATP Adenosina trifosfato NR1C1 sinônimo de PPARα bgk Glicoquinase pancreática NR1C2 sinônimo de PPARβ/δ BRIN-BD11 Linhagem clonal de células β NR1C3 sinônimo de PPARγ BSA Albumina de soro bovino ob/ob Camundongo deficiente em leptina Bz Bezafibrato OMS Organização Mundial de Saúde C/EBPS CCAAT/enhancer biding protein PACAP Polipeptídeo ativador da adenilato ciclase Ca 2+ Íon cálcio PAI-1 Inibidor do ativador de plasminogênio-1 CCL2 Quimiocina CC ligante 2 PBS Salina tamponada com fosfato CT Colesterol total Pp Pontos parciais db/db Camundongo com excesso de leptina PPAR Receptor ativador de proliferação celular DM2 Diabetes tipo II PPRE Elemento responsivo ao PPAR EGIR Grupo Europeu de Estudo da Resistência à Insulina PT Pontos totais EPM Erro padrão da média RA Ácido retinóico Fe Fenofibrato RI Resistência à insulina GIP Peptídeo insulinotrópico dependente de glicose RNAm RNA mensageiro GK Glicoquinase Ro Rosiglitazona GLP-1 Peptídeo semelhante ao glucagon 1 ROS Espécies reativas de oxigênio GLUT Transportador da glicose RXR Receptor do ácido retinóico HDL Lipoproteína de alta densidade SC Grupo dieta controle HFHS Grupo dieta rica em lipídios e sacarose SD Rato Sprague Dawley HOMA-IR Índice de resistência à insulina Sub:Vis Relação entre gordura subcutânea e visceral HSL Lipase sensível a hormônio TG Triglicerídeo IL-1b Interleucina 1β TNF-α Fator de necrose tumoral α
12 Sigla Definição Sigla Definição IL-6 Interleucina 6 TOTG Teste oral de tolerância à glicose INS-1 Linhagem clonal de células β TZD Tiazolidinediona IR Receptor da insulina VEGF Fator vascular de crescimento endotelial K + Íon potássio VIP Peptídeo intestinal vasoativo LDL Lipoproteína de baixa densidade Vv[gord] Densidade de volume de gordura
13 SUMÁRIO Página INTRODUÇÃO 15 1 OBJETIVOS Objetivo Geral Objetivos Específicos 17 2 REVISÃO DA LITERATURA Síndrome Metabólica Metabolismo da Glicose e Sensibilidade à Insulina Tecido Adiposo, Adipócitos e Adipocinas Tecido Adiposo Visceral versus Subcutâneo Doença Gordurosa Pancreática Não-Alcoólica Receptores Ativadores de Proliferação Peroxissomal Modelos Experimentais de Doenças Metabólicas 42 3 MATERIAIS E MÉTODOS Obtenção da Amostra e Grupos Experimentais Ingestão de Ração, Água, Energia e Eficiência Alimentar Metabolismo Glicídico e Lipídico e Função Pancreática Hipertrofia Cardíaca Morfometria do Tecido Adiposo Morfometria e Estereologia do Pâncreas 51
14 3.7 Imunohistoquímica do Tecido Adiposo e Pâncreas Análise Estatística 55 4 RESULTADOS Ingestão de Ração, Energia e Água e Eficiência Alimentar Massa Corporal Lipídios Séricos Insulina e Glicose séricos Coração Gorduras Visceral e Subcutânea e Diâmetro do Adipócito Expressão de Adiponectina no Tecido Adiposo Massa do Pâncreas, Gordura pancreática e Ilhotas pancreáticas Expressão de Insulina, Glucagon, GLUT-2 PPARα e PPARδ/β nas Ilhotas Pancreáticas 76 5 DISCUSSÃO Considerações Finais 88 6 CONCLUSÃO 89 REFERÊNCIAS 90 ANEXO - Parecer do Comitê de Ética em Experimentação Animal APÊNDICE 1 - Artigo publicado na revista Nutrition APÊNDICE 2 - Artigo publicado na revista Pancreas
15 15 INTRODUÇÃO A obesidade, o diabetes e as doenças cardiovasculares são cada vez mais comuns na sociedade moderna. Estas patologias estão frequentemente associadas à ingestão da dieta ocidental rica em lipídios saturados combinado a um estilo de vida sedentário. Este hábito alimentar vai contra o genótipo econômico, que promove o armazenamento de energia nas células adiposas na forma de triacilglicerol a fim de atingir a demanda energética em tempos de necessidade (Prentice e Moore, 2005). A obesidade é uma doença heterogênea em relação à distribuição regional do tecido adiposo. Existem dois depósitos principais de tecido adiposo, um visceral, e um subcutâneo. O tecido adiposo subcutâneo é definido como a gordura localizada entre a pele e o músculo, enquanto o tecido adiposo visceral localiza-se no interior das cavidades corporais, principalmente abdominal (Catalan et al., 2009). Evidências mostram que a obesidade visceral está associada a um risco aumentado para comorbidades associadas à obesidade, enquanto a gordura subcutânea estaria associada a um risco reduzido de doenças cardiovasculares (Wajchenberg, 2000; Wajchenberg et al., 2002; Despres e Lemieux, 2006). Além disso, o tecido adiposo visceral é mais ativo metabolicamente do que o subcutâneo, assim como também há diferença entre as moléculas secretadas por eles (Fried et al., 1998; Russell et al., 1998; Lihn et al., 2004; Hotamisligil, 2006). Alguns trabalhos mostram que o tecido pancreático pode ser foco de acúmulo ectópico de gordura (Ogilvie, 1933; Matsumoto et al., 1995; Katz et al., 1999), mas até recentemente, descrições sobre a influência da obesidade sobre o acúmulo de gordura no pâncreas ainda não tinham sido feitas. Mathur e col. foram os primeiros a descrever uma condição denominada doença pancreática gordurosa não alcoólica, a qual se caracteriza pelo aumento da massa pancreática e gordura intralobular e interlobular (especialmente triglicerídeos e ácidos graxos livres), além do aumento da produção de citocinas inflamatórias (Mathur et al., 2007). A pancreatite é outra
16 16 doença que compromete a função pancreática normal, e sua patogênese ainda não é bem entendida. Entretanto, evidências sugerem que há uma conexão potencial entre a ingestão de dieta rica em lipídios e o dano pancreático crônico (Chowdhury et al., 2000; Yan et al., 2006; Zhang et al., 2008). Os receptores ativadores de proliferação peroxissomal (PPAR) fazem parte de uma família de fatores de transcrição intimamente conectada ao metabolismo celular de lipídios, carboidratos e proteínas, além de promoverem a diferenciação celular. Eles existem em três isotipos: PPARα, PPARβ/δ e PPARγ (Dreyer et al., 1992). O PPARα é expresso em tecidos metabolicamente ativos como o fígado, coração, rim e músculo esquelético, o PPARβ/δ é expresso de forma ampla, e a expressão do PPARγ é encontrada de forma predominante no tecido adiposo, macrófagos, colo e placenta (Rosen e Spiegelman, 2000). Medicamentos capazes de modular a expressão do PPAR como as tiazolidinedionas (TZD) e os fibratos são bem conhecidos pelos clínicos. Os TZDs são ativadores PPARγ e ajudam a aumentar a sensibilidade dos tecidos à ação da insulina em pacientes diabéticos. Os fibratos são ativadores PPARα e reduzem a produção hepática de triglicerídeos pelo aumento da oxidação de ácidos graxos. Não há medicamentos com ação agonista PPARβ/δ no mercado, apesar de existirem fortes evidências de que sua ativação reduz o tamanho do adipócito e a massa adiposa corporal total (Luquet et al., 2003; Wang et al., 2003), tornando-os armas potentes no combate a obesidade. Há um grande potencial para que medicamentos capazes de ativar mais de um isotipo do PPAR (duplo-agonistas PPARα/γ ou pan-agonistas PPARα/β/δ/γ) sejam utilizados como instrumento de combate à doenças metabólicas. Infelizmente, alguns deles possuem efeitos colaterais como, por exemplo, o aumento de eventos cardiovasculares adversos (muraglitazar, infarto do miocárdio, acidente vascular encefálico e ataque isquêmico transitório; tesaglitazar, aumento da creatina sérica) (Fagerberg et al., 2005; Nissen et al., 2005). Sabe-se hoje que o bezafibrato agonista PPARα também possui alta afinidade pelos isotipos β e γ e, por essa razão, ele é classificado como um pan-agonista PPAR (Krey et al., 1997; Willson et al., 2000). O bezafibrato tem sido amplamente utilizado no tratamento da dislipidemia em
17 17 humanos com um bom perfil de segurança (Goa et al., 1996). Além disso, estudos clínicos têm mostrado suas propriedades anti-diabéticas (Tenenbaum et al., 2005; Tenenbaum et al., 2006). A ação dos TZDs e fibratos sobre o metabolismo glicídico e lipídico são bem conhecidas, porém a comparação entre a ação de um pan-agonista PPAR e agonistas PPAR únicos (que ativam apenas um isotipo do PPAR) sobre alterações na massa corporal, tecido adiposo e pâncreas in vivo decorrentes da ingestão de uma dieta rica em lipídios e sacarose merece atenção. 1 OBJETIVOS 1.1 Objetivo Geral Estudar o efeito de medicamentos com diferentes ações agonista PPAR (rosiglitazona, fenofibrato e bezafibrato) sobre o perfil lipídico, glicídico e alterações na massa corporal e morfologia do tecido adiposo e pancreático em modelo de diabetes e sobrepeso induzido por dieta. 1.2 Objetivos Específicos Induzir o diabetes tipo II e o sobrepeso em camundongos C57BL/6 através da administração de dieta rica em lipídios e sacarose; Comparar o efeito da rosiglitazona, fenofibrato e bezafibrato sobre: o Metabolismo glicídico e lipídico; o Massa corporal, morfologia do tecido adiposo e expressão de adiponectina; o Morfologia pancreática e expressão de insulina, glucagon, GLUT2, PPARα e PPARβ/δ.
18 18 2 REVISÃO DA LITERATURA 2.1 Síndrome Metabólica A síndrome metabólica é caracterizada por um conjunto de fatores de risco cardiovascular, usualmente relacionados à deposição central de gordura e à resistência à insulina, sendo responsável pelo aumento da taxa de mortalidade geral em 1,5 vezes e da mortalidade cardiovascular em 2,5 vezes. A predisposição genética (Bouchard, 1995), a alimentação inadequada (Liese et al., 1998) e a inatividade física (Lakka et al., 2003) estão entre os principais fatores que contribuem para o surgimento dessa síndrome. Há uma indicação consensual de que o aumento da pressão arterial, os distúrbios do metabolismo glicídico e lipídico e o excesso de massa corporal estão, de forma definitiva, associados ao aumento da morbimortalidade cardiovascular, fato observado não só nos países desenvolvidos, mas também, e de forma preocupante, nos países em desenvolvimento e subdesenvolvidos (SBH, 2004). A combinação de alterações metabólicas conhecida atualmente como síndrome metabólica foi primeiramente descrita por Kylin em 1923 como sendo a associação entre a hipertensão arterial, a hiperglicemia e a gota (Kylin, 1923). Duas décadas depois, Vague notou que a adiposidade concentrada na porção superior do corpo (andróide, descrita em maior detalhe na seção Tecido Adiposo Visceral versus Subcutâneo ) era o tipo mais frequentemente associado com as anormalidades metabólicas vistas no diabetes e na doença cardiovascular (Vague, 1947). Em 1988, Reaven utilizou o termo Síndrome X e estabeleceu firmemente a importância clínica desta síndrome, apesar da obesidade não ter sido incluída (Reaven, 1988). Em 1989, Kaplan renomeou a síndrome como Quarteto Mortal, e outros atribuíram o nome de Síndrome da Resistência à Insulina (Kaplan, 1989; Haffner et al., 1992). Hoje, o nome Síndrome Metabólica é a descrição mais utilizada e mais bem aceita para a caracterização desta constelação de distúrbios metabólicos que atuam não apenas
19 19 como fatores de risco cardiovascular, mas também predizem o alto risco de desenvolvimento do diabetes (se este já não estiver presente). Vários grupos tentaram desenvolver uma definição única para a síndrome metabólica. As definições mais amplamente aceitas foram propostas pela Organização Mundial de Saúde (OMS), pelo Grupo Europeu de Estudo da Resistência à Insulina (EGIR) e pelo Programa Nacional de Educação do Colesterol Terceiro Painel de Tratamento do Adulto (NCEP-ATP III) (Balkau e Charles, 1999; World Health Organisation, 1999; NCEP, 2002). Todos os grupos concordam com os componentes que são o centro da síndrome metabólica: obesidade, resistência à insulina, dislipidemia e hipertensão arterial. Entretanto, eles estabelecem diferentes critérios clínicos para a identificação de cada componente, sendo seus valores ligeiramente diferentes, quando as três recomendações são comparadas entre si. A definição da OMS preconiza como ponto de partida a avaliação da resistência à insulina ou do distúrbio do metabolismo da glicose, o que dificulta a sua utilização. Por outro lado, a definição do NCEP-ATP III foi desenvolvida para uso clínico e não exige a comprovação de resistência à insulina, facilitando a sua utilização (SBH, 2004). Segundo o NCEP-ATP III, a síndrome metabólica representa uma combinação de pelo menos três componentes dos apresentados na Tabela 1, e devido a sua simplicidade e praticidade, ela é a definição recomendada pela I Diretriz Brasileira de Diagnóstico e Tratamento da Síndrome Metabólica (SBH, 2004). Apesar de não fazerem parte dos critérios de diagnóstico da síndrome metabólica, várias condições clínicas e fisiopatológicas estão frequentemente associadas a ela, tais como: síndrome de ovários policísticos, acanthosis nigricans, doença hepática gordurosa não-alcoólica, microalbuminúria, estados pró-trombóticos, estados próinflamatórios e de disfunção endotelial e hiperuricemia (Bloomgarden, 2004). É importante destacar o aumento da prevalência da obesidade em todo o Brasil e uma tendência de aumento especialmente preocupante do problema em crianças em idade escolar, em adolescentes e nos estratos de menor renda (Monteiro et al., 1995). A adoção precoce por toda a população de estilos de vida que promovam a manutenção da saúde, como a ingestão de uma dieta adequada e a prática regular de
20 20 atividade física, preferencialmente desde a infância, são componentes básicos para a prevenção da síndrome metabólica. As características clínicas da síndrome metabólica estão associadas a um risco aumentado de desenvolvimento de doença cardiovascular (Alexander et al., 2003), incluindo um maior risco de doença arterial coronariana para um determinado nível de LDL colesterol (2001), assim como morte prematura (Trevisan et al., 1998). O estabelecimento de um critério para a definição da síndrome é útil, uma vez que cada componente individual atua de forma sinérgica de forma a amplificar o risco; porém, estes mesmo componentes também são fatores de risco independentes para o desenvolvimento da doença cardiovascular aterosclerótica. Tabela 1. Componentes da Síndrome Metabólica segundo o NCEP-ATP III 1 Componentes Níveis Obesidade Abdominal (circunferência da cintura) Homem > 102 cm Mulher > 88 cm Triglicerídeos 150 mg/dl HDL colesterol Homens < 40 mg/dl Mulheres < 50 mg/dl Pressão Arterial 130 mmhg ou 85 mmhg Glicemia de Jejum 110 mg/dl 1 Adaptado de NCEP-ATPIII 2001 (2001).
21 21 Apesar da obesidade por si só não ser um componente no diagnóstico da síndrome metabólica, há evidências suficientes de que a gordura visceral intra-abdominal a qual aumenta com a idade (Bouchard et al., 1993) esteja intimamente ligada a resistência à insulina. Esta relação fisiopatológica é consistente ao se notar a ênfase sobre a circunferência abdominal e a relação cintura-quadril (World Health Organisation, 1999), parâmetros amplamente utilizados como critério de diagnóstico de risco cardiovascular decorrente da obesidade, ao invés do uso do índice de massa corporal. Mesmo em indivíduos que possuem massa corporal normal, o aumento da circunferência abdominal está associado a um risco cardiovascular aumentado. As anormalidades do metabolismo lipídico estão frequentemente presentes em indivíduos com síndrome metabólica, formando uma tríade de dislipidemia aterogênica que consiste em hipertrigliceridemia, baixos níveis de HDL colesterol e altos níveis de LDL (Howard e Howard, 1994; Betteridge, 1997). Mais especificamente, as partículas de LDL pequenas e densas que são mais aterogênicas estão presentes em proporção aumentada. Além disso, níveis aumentados de partículas remanescentes com capacidade aterogênica ricas em triglicerídeo e colesterol também são encontrados. Assim, a hipertrigliceridemia tem sido estudada como um defeito metabólico central que leva a uma cascata de eventos, que no final produz um perfil lipídico pró-aterogênico. Este tipo de dislipidemia encontrada na síndrome metabólica também está comumente presente em pacientes com diabetes tipo 2. Também é importante ressaltar que os indivíduos não diabéticos com síndrome metabólica apresentam um risco elevado de desenvolvimento de diabetes tipo 2 (Laaksonen et al., 2002; Lorenzo et al., 2003). A pressão arterial aumentada é um componente frequente na síndrome metabólica, e a hipertensão arterial é mais frequentemente vista em indivíduos com resistência à insulina ou obesidade (Reaven, 1988). Diversos estudos têm mostrado que mesmo ganhos modestos de massa corporal podem precipitar o surgimento da hipertensão arterial (Must et al., 1999). Assim como acontece no infarto do miocárdio, também há uma associação positiva e significante entre a presença da síndrome metabólica e o acidente vascular encefálico (Ninomiya et al., 2004).
22 22 Um dos maiores desafios na síndrome metabólica é entender os mecanismos celulares e moleculares que fazem a conexão entre a constelação de anormalidades metabólicas e seus efeitos fisiopatológicos que mais tardiamente se manifestarão na forma de doença. Diversas evidências apontam o aumento da massa de tecido adiposo como o mecanismo primário por trás desta síndrome. Assim como nos humanos que apresentam formas raras de obesidade monogênica, os modelos de obesidade genética em roedores frequentemente manifestam resistência à insulina, hiperglicemia e hipertrigliceridemia. Algumas características peculiares à adiposidade aumentada têm sido apontadas como causas das alterações referenciadas acima. Entre elas podemos destacar: (1) níveis elevados de ácidos graxos livres, levando a resistência periférica à insulina (Boden, 1997); (2) esteatose tecidual (p. ex., no músculo esquelético, fígado e ilhotas pancreáticas) e consequente lipotoxicidade (prejuízo na sinalização da insulina nestes tecidos) (Fig. 1) (Unger, 1995) e; (3) níveis reduzidos de adiponectina (adipocina ligada à sensibilidade à insulina) e níveis elevados de resistina (adipocina ligada à resistência à insulina) (Berg et al., 2001; Banerjee et al., 2004). Na síndrome metabólica, o acúmulo excessivo de ácidos graxos livres (AGL) em tecidos que não o tecido adiposo resulta em disfunção celular (p. ex., alterações no transporte de glicose estimulado pela insulina ou secreção diminuída de insulina) (Fig. 1). O acúmulo excessivo de AGL também pode levar à morte celular por apoptose. Os efeitos do acúmulo de AGL depende do tipo celular, da natureza do lipídio e do grau e duração da exposição aos níveis elevados de lipídios. A lipotoxicidade pode ser melhorada ou prevenida se o lipídio é redirecionado ao tecido adiposo (p. ex., através da estimulação da via dos receptores ativadores de proliferação peroxissomal [PPAR] γ) ou se ele é secretado na forma de lipoproteína. De forma alternativa, o direcionamento dos AGL aos depósitos de triglicerídeos ou para a β-oxidação aumentada (p. ex., através da estimulação das vias de sinalização do PPARα) pode proteger contra a lipotoxicidade. Agentes como os salicilatos, os inibidores da síntese de ceramidas ou as proteínas degradadoras de espécies reativas de oxigênio (ROS scavengers) podem bloquear algumas vias de sinalização específicas e vias do metabolismo de ácidos graxos que são críticas para a lipotoxicidade.
23 23 PPARγ Leptina PPARα Figura 1. Lipotoxicidade na síndrome metabólica. O aumento excessivo de ácidos graxos livres pode levar, em último caso, a disfunção celular (p. ex., alterações no transporte de glicose estimulado pela insulina ou secreção de insulina diminuída, dependendo do tipo celular) e, finalmente, a disfunção celular e morte por apoptose. Maiores explicações no texto acima. Abreviações: TG, triglicerídeo; PPAR, receptor ativador de proliferação peroxissomal. Adaptado de Schaeffer e col (Schaffer, 2003).
24 Metabolismo da Glicose e Sensibilidade à Insulina Apesar de a glicemia apresentar uma variação entre os estados alimentado e jejum, a glicose plasmática permanece dentro de um intervalo fisiológico limitado que varia de 4 a 7 mmol/l ( 72 a 126 mg/dl) em indivíduos sadios. Este controle é feito pelo balanço entre a absorção intestinal de glicose, sua produção hepática e sua captação e metabolismo nos tecidos periféricos. A insulina aumenta a captação da glicose nos tecidos periféricos e inibe sua produção hepática, servindo assim como um regulador primário de sua concentração sanguínea (Fig. 2). Ela também promove o armazenamento de substratos no tecido adiposo, fígado e músculo esquelético pela estimulação da lipogênese, glicogênese e síntese de proteínas, respectivamente, assim como inibe a lipólise, glicogenólise e quebra de proteínas (Scheen, 2004). Em condições normais, a insulina promove a captação de glicose nas células adiposas e musculares pela estimulação da translocação do transportador da glicose tipo 4 (GLUT4) de sítios intracelulares para a membrana plasmática. O GLUT4 se localiza na membrana de vesículas intracelulares, que estão em constante movimento de reservatórios intracelulares em direção à membrana plasmática e vice-versa. A insulina aumenta o transporte da glicose através do aumento da taxa de exocitose das vesículas que contêm o GLUT4, e pela ligeira diminuição da taxa de internalização das mesmas (Pessin et al., 1999). Estudos sugerem que estas vesículas se movem ao longo de trilhos de microtúbulos em direção a superfície celular, onde a vesícula então se ancora e se funde a membrana, permitindo a exposição extracelular da proteína GLUT4 (Guilherme et al., 2000).
25 25 Figura 2. Regulação da glicemia pela insulina. O aumento nos níveis plasmáticos de glicose é percebido pelas células β da ilhota pancreática, que secretam insulina. No adipócito e no músculo esquelético, a ligação da insulina ao seu receptor IR estimula a translocação do GLUT4 para a membrana e consequente captação de glicose para armazenamento. No fígado, a estimulação do receptor IR leva a uma série de eventos que no final inibem a produção hepática de glicose. Adaptado de Muoio e col (Muoio e Newgard, 2005).
26 26 Até 75% da captação de glicose dependente de insulina ocorre no músculo esquelético, enquanto o tecido adiposo contribui apenas com uma pequena fração (Klip e Paquet, 1990). De forma interessante, camundongos com o receptor da insulina silenciado no músculo esquelético possuem tolerância normal à glicose (Bruning et al., 1998), enquanto esta mesma alteração no tecido adiposo leva a intolerância à glicose, aparentemente devido a indução de resistência à insulina no músculo e no fígado (Abel et al., 2001). Tanto a obesidade quanto a lipoatrofia resultam em resistência à insulina e predispõem ao diabetes mellitus tipo 2 (DM2), demonstrando que o tecido adiposo é crucial na regulação do metabolismo glicídico (Gavrilova et al., 2000). Apesar da insulina não estimular a captação da glicose no fígado, ela é capaz de bloquear a glicogenólise e a gliconeogênese, assim como estimular a síntese de glicogênio. Muitos tecidos estão envolvidos na manutenção da homeostase da glicose. Entre eles, o fígado e as células β pancreáticas são os mais importantes porque eles podem sentir e responder a alterações nos níveis sanguíneos de glicose. O aparato de sensibilidade à glicose é composto pelo transportador de glicose tipo 2 (GLUT2) e pela glicoquinase (GK) (Schuit et al., 2001; Cerf, 2007). Enquanto o gene do GLUT2 possui um promotor único, o gene da GK possui dois promotores separados e funcionalmente distintos, que expressam isoformas da GK específicas para cada tecido: GK do fígado (LGK) e GK da célula β pancreática (βgk) (Magnuson, 1990). A glicose é captada pela célula através do GLUT2, e a GK mantém a glicose no citoplasma através de sua fosforilação (Schuit et al., 2001). Em indivíduos saudáveis a secreção de insulina estimulada pela glicose é bifásica. O aumento dos níveis de glicose no citoplasma da célula β induz a primeira fase de secreção da insulina, através de sua liberação de grânulos secretores presentes no citoplasma. A entrada de glicose na célula β é percebida pela βgk, que a fosforila em glicose-6-fosfato, gerando ATP. O fechamento dos canais de K + dependentes de ATP resulta na despolarização da membrana plasmática e ativação dos canais de Ca 2+ dependentes de voltagem, levando ao aumento intracelular da concentração de Ca 2+, e consequente secreção de insulina em pulsos (segunda fase de secreção) (Soria et al., 2004). Outros mediadores da secreção de insulina incluem a ativação de fosfolipases
27 27 e proteína quinase C (p. ex., pela acetilcolina), e a estimulação da atividade da adenilato ciclase e ativação da proteína quinase A. Este último mecanismo pode ser ativado por hormônios como peptídeos intestinais vasoativos (VIP), polipeptídeo ativador da adenilato ciclase (PACAP), peptídeo semelhante ao glucagon 1 (GLP-1) e peptídeo insulinotrópico dependente de glicose (GIP). Estes fatores parecem desempenhar um papel importante na segunda fase de secreção de insulina estimulada pela glicose, após o reabastecimento dos grânulos secretores intracelulares (Bratanova-Tochkova et al., 2002). O aparato de sensibilidade à glicose do fígado exerce forte influência na utilização da glicose e na síntese do glicogênio. A glicose é conhecida por regular a transcrição de diversos genes envolvidos nas vias metabólicas hepáticas (Girard et al., 1997; Nordlie et al., 1999), como o gene da L-piruvato quinase, da ácido graxo sintase e do GLUT2. O aumento intracelular da glicose-6-fosfato leva a glicólise e síntese de glicogênio (Aiston et al., 1999). Mesmo pequenas alterações na expressão da LGK levam a um impacto mensurável sobre a concentração sanguínea de glicose (Ferre et al., 1996; Hariharan et al., 1997; Niswender et al., 1997). Adicionalmente, camundongos silenciados especificamente para o GLUT2 hepático apresentam expressão diminuída da LGK (Burcelin et al., 2000). Assim, a LGK e o GLUT2 desempenham papéis chaves no metabolismo hepático da glicose. Os principais problemas relacionados ao DM2 são a resistência à insulina e a deterioração progressiva da função da célula β (Saltiel, 2001). A resistência à insulina pode ser desencadeada por diversos fatores como a idade, defeitos genéticos, fatores ambientais e a obesidade. Ela é caracterizada por uma alteração na sinalização normal da insulina nas células que captam a glicose. Há insulina, mas a resposta celular a sua presença está diminuída e assim, a captação da glicose é menor. Como resultado, aumenta o estímulo de secreção de insulina pela célula β, uma vez que parte da glicose ainda permanece no sangue. Se esta célula conseguir sentir os níveis de glicose e secretar insulina de forma suficiente a compensar a resistência à insulina (hiperinsulinemia compensatória), o DM2 não ocorre. O DM2 só se desenvolve quando ocorrem de forma concomitante a resistência à insulina e a insuficiência da célula β. A característica essencial da insuficiência da célula β é o aumento da
28 28 secreção basal de insulina e a diminuição da secreção de insulina estimulada pela glicose, resultantes da perda da habilidade da célula β em responder aos níveis circulantes de glicose (Muoio e Newgard, 2008). Tanto a hiperglicemia quanto a hiperlipidemia crônica podem exercer efeitos deletérios sobre a função da célula β, fenônemos denominados glicotoxicidade e lipotoxicidade, respectivamente. Progressivamente, ambos contribuem para a deteriorização da homeostase da glicose no DM2. O mecanismo da glicotoxicidade envolve diversos fatores de transcrição que são, pelo menos em parte, mediados pela geração de estresse oxidativo crônico (Matsuoka et al., 1997; Tajiri et al., 1997; Ihara et al., 1999). Ela desempenha efeitos lentos e progressivamente irreversíveis sobre a função da célula β pancreática: efeitos reversíveis até certo ponto, e então se tornam irreversíveis (Moran et al., 1997; Gleason et al., 2000). Além das alterações funcionais, a hiperglicemia crônica induz a diminuição da massa de células β através de apoptose (Pick et al., 1998; Donath et al., 1999). Os ácidos graxos combustível essencial da célula β no estado normal também se tornam tóxicos à célula β quando presentes cronicamente em níveis elevados. A exposição prolongada das células β aos ácidos graxos aumenta a secreção basal de insulina inibindo, porém, a secreção de insulina estimulada pela glicose. A lipotoxicidade é mediada provavelmente pelo acúmulo de um sinal citosólico derivado da via de esterificação do ácido graxo. Os ácidos graxos inibem a expressão do gene da insulina na presença de níveis elevados de glicose (Gremlich et al., 1997; Ritz-Laser et al., 1999; Jacqueminet et al., 2000), em parte devido à regulação negativa do fator de transcrição pancreático-duodenal homeobox-1 (Gremlich et al., 1997). Ácidos graxos em excesso também levam a morte da célula β por apoptose tanto in vitro (Cnop et al., 2001; Maedler et al., 2001), quanto in vivo (Pick et al., 1998; Shimabukuro et al., 1998). Tem sido proposto que a hiperglicemia crônica, independente da hiperlipidemia, é tóxica para a função da célula β, enquanto a hiperlipidemia crônica seria deletéria apenas quando concomitante a hiperglicemia (Poitout e Robertson, 2002).
29 Tecido Adiposo, Adipócitos e Adipocinas A homeostase da ingestão e do gasto energético é regulada pela deposição e liberação de ácidos graxos do tecido adiposo (na forma de triacilglicerol), um órgão que até recentemente não era considerado nas pesquisas que relacionavam o balanço energético com a obesidade. Entretanto, esta idéia mudou radicalmente nos últimos anos, e o tecido adiposo se tornou foco de intensa pesquisa. Existem algumas razões para essa mudança de pensamento: 1) a obesidade é definida como a expansão do tecido adiposo, assim ele deveria ser considerado como ponto central no estudo da doença; 2) o tecido adiposo branco é o sítio primário de produção dos hormônios envolvidos no balanço energético, como a leptina e; 3) o tecido adiposo secreta inúmeros fatores envolvidos numa constelação de processos metabólicos e fisiológicos, sendo que alguns destes fatores estão implicados em patologias associadas a obesidade, particularmente a resistência à insulina e a síndrome metabólica (Rajala e Scherer, 2003; Trayhurn e Wood, 2004). A simplicidade aparente do tecido adiposo branco e marrom, tanto histologicamente quanto metabolicamente, é a principal razão pela qual este órgão foi negligenciado até recentemente. O triacilglicerol constitui até 85% do peso do tecido, e por isso acreditava-se que sua função estava limitada a síntese e quebra de lipídios, mas sabe-se hoje que esta simplicidade é ilusória. Ao nível celular, existe uma considerada heterogeneidade, onde os adipócitos maduros contribuem com não mais do que metade do conteúdo celular. Entre as demais células estão, por exemplo, os fibroblastos, células endoteliais, pre-adipócitos e macrófagos (Weisberg et al., 2003; Xu et al., 2003). O tecido adiposo branco é um órgão secretor, particularmente pela secreção de ácidos graxos durante o jejum. Ele também secreta outros lipídios como o colesterol e o retinol (armazenados, mas não sintetizados pelo adipócito), hormônios esteróides e prostaglandinas (Trayhurn e Beattie, 2001). Além disso, os adipócitos secretam a enzima lipase lipoprotéica (LPL), que quebra o triacilglicerol circulante em ácido graxo, para que seja posteriormente armazenado no adipócito. Os adipócitos são células de renovação lenta em pessoas não obesas, e a expansão do tecido adiposo durante o desenvolvimento (da idade jovem a meia idade) é
30 30 principalmente resultado do seu aumento uniforme em tamanho por hipertrofia (Kissebah e Krakower, 1994; Wajchenberg, 2000). No homem existe um aumento no número de adipócitos no depósito subcutâneo da região abdominal, o mesmo não ocorrendo na mulher. A obesidade que se desenvolve na criança e no adolescente é geralmente hiperplásica, ou seja, há um aumento no número de células adiposas (Kissebah e Krakower, 1994; Wajchenberg, 2000; Karelis et al., 2004). Por outro lado, a maior parte da obesidade no adulto está relacionada a expansão hipertrófica dos adipócitos pré-existentes (Kissebah e Krakower, 1994; Wajchenberg, 2000). Estudos sobre a celularidade do tecido adiposo mostram que os adipócitos se tornam gravemente resistentes à insulina se armazenam mais de 1,0 μg de lipídio/célula, e um novo recrutamento de adipócitos normalmente ocorre quando o conteúdo lipídico da célula atinge 0,7-0,8 μg/célula (Krotkiewski et al., 1983). O recrutamento de adipócitos ocorre pela proliferação e diferenciação dos préadipócitos, um processo que é caracterizado pela ativação e inativação de genes específicos através da indução de fatores de transcrição como o a CCAAT/enhancer biding protein (C/EBPs) e o receptor ativador de proliferação peroxissomal γ (PPARγ) (Gregoire et al., 1998). A atividade biológica do tecido adiposo muda conforme seu estoque de lipídio aumenta. Comparado aos adipócitos pequenos, os adipócitos grandes são mais resistentes à insulina e são mais lipolíticos, secretam mais citocinas inflamatórias, secretam menos adiponectina (Le Lay et al., 2001; Sopasakis et al., 2004), e são achados de forma mais frequente em indivíduos com distúrbios metabólicos relacionados a obesidade (Krotkiewski et al., 1983; Weyer et al., 2000). Dessa forma, a composição de células no tecido adiposo, assim como a proporção entre a quantidade de adipócitos grandes e pequenos, são fatores importantes na determinação da atividade metabólica e da resposta às alterações ambientais daquele depósito específico. O tecido adiposo secreta moléculas peptídicas e não peptídicas que são coletivamente denominadas adipocinas (Fig. 3). Elas funcionam como hormônios, regulando a atividade biológica de tecidos e órgãos vizinhos e distantes (Smith et al., 2005). Algumas adipocinas são sintetizadas exclusivamente pelos adipócitos (p. ex., adiponectina), enquanto outras são sintetizadas pelos outros tipos celulares
31 31 presentes no tecido adiposo. A diversidade entre as adipocinas é grande, tanto em termos de estrutura protéica quanto em função. Entre elas podemos encontrar citocinas clássicas (p. ex., fator de necrose tumoral α, TNF-α; interleucina 6, IL-6), quimiocinas (p. ex., proteína quimiotática do monócito, MCP-1), proteínas do sistema complemento (p. ex., adipsina) e proteínas envolvidas na homeostase vascular (p. ex., inibidor do ativador do plasminogênio-1, PAI-1), na regulação da pressão arterial (angiotensinogênio), no metabolismo lipídico (p. ex., proteína de transferência de ésteres de colesterol, proteína ligante do retinol), na homeostase da glicose (p. ex., adiponectina e resistina) e na angiogênese (p. ex., fator vascular de crescimento endotelial, VEGF) (Rajala e Scherer, 2003; Trayhurn e Wood, 2004). Entre as adipocinas mais recentemente descobertas estão a proteína ligadora de retinol 4 (RBP-4), Nampt/PBEF/Visfatin, lipocalina 2 (LCN-2), omentina, chemerina, osteopondina e vaspina (Catalan et al., 2009). Geralmente a taxa de secreção das adipocinas ocorre de acordo com a quantidade de gordura estocada no adipócito, um fenômeno que representa um meio de ajustar a atividade celular de forma a manter a fisiologia e a morfologia ótima do tecido adiposo. Por exemplo, o aumento da produção de TNF-α e IL-6 pelo tecido adiposo na obesidade estimula a atividade da lipase sensível a hormônio (HSL), diminui a expressão de GLUT4, assim como a produção e a atividade da LPL, limitando a entrada adicional de lipídios nos adipócitos hipertrofiados (Wajchenberg, 2000; Smith et al., 2005). A leptina e a adiponectina são as adipocinas mais estudadas até o momento, e sabe-se que ambas exercem efeitos regulatórios no hipotálamo, fígado, ilhotas pancreáticas e músculo esquelético (Smith et al., 2005). A leptina funciona como um sinal de feedback negativo na regulação da massa corporal. Uma redução nos níveis de leptina sinaliza que o armazenamento de energia está insuficiente. Isto induz a ingestão de energia e a redução do seu gasto e aumenta a transformação de energia em gordura, levando a um balanço energético positivo que, consequentemente, eleva os níveis de leptina (Friedman, 2002). Entretanto, a obesidade está frequentemente associada com hiperleptinemia, refletindo um estado de resistência à ação da leptina em indivíduos obesos, uma vez que eles permanecem com peso elevado apesar dos altos níveis de leptina circulante (Caro et al., 1996). Adicionalmente, a leptina aumenta a atividade nervosa simpática renal na obesidade, levando ao conceito de
32 32 resistência seletiva à leptina, onde a resistência parece estar limitada as suas ações metabólicas com preservação, porém, da sua ação sobre a atividade simpática renal (Correia et al., 2002; Rahmouni et al., 2002; Rahmouni et al., 2005). A adiponectina é uma citocina anti-inflamatória que possui ação tanto de sensibilização à insulina quanto anti-aterosclerótica. Semelhante à leptina, a produção de adiponectina também responde ao estado energético sistêmico. Entretanto, enquanto a adiposidade eleva os níveis plasmáticos de leptina, ela reduz significativamente os níveis de adiponectina (Weyer et al., 2001). Apesar do efeito oposto em relação ao acúmulo de gordura, tanto a adiponectina quanto a leptina regulam a via AMP quinase (AMPK) de forma a aumentar a oxidação de ácidos graxos nos tecidos alvos, tanto através de uma ação direta sobre a via AMPK (Minokoshi et al., 2002; Yamauchi et al., 2002) quanto pela modulação da atividade nervosa simpática (Qi et al., 2004). Na obesidade, a inflamação e a resistência à insulina no tecido adiposo são promovidas pelos macrófagos residentes (Weisberg et al., 2003; Xu et al., 2003; Arkan et al., 2005; Cancello e Clement, 2006; Lesniewski et al., 2007). Eles secretam mediadores pró-inflamatórios como o TNF-α, IL-6 e MCP-1, os quais estão envolvidos no desenvolvimento da resistência à insulina em humanos e em camundongos obesos (Senn et al., 2002; Klover et al., 2005; Cancello e Clement, 2006; Kanda et al., 2006; Sell et al., 2007). Em ambos, os macrófagos infiltram no tecido adiposo na forma de monócitos circulantes em resposta ao aumento de MCP-1, produzindo proteinases que degradam a matriz extracelular necessária ao seu remodelamento, associado à hipertrofia do adipócito e a expansão do tecido adiposo (Huber et al., 2007). Os macrófagos também secretam mais TNF-α, IL-6 e MCP-1, gerando assim um ciclo vicioso (Strissel et al., 2007).
33 Figura 3. Tecido adiposo: células e adipocinas. A expansão do tecido adiposo durante o ganho de peso leva ao recrutamento de macrófagos através de vários sinais como o CCL2. Estes macrófagos se localizam principalmente ao redor dos adipócitos apoptóticos. Vários mediadores sintetizados pelos adipócitos e macrófagos residentes podem contribuir para a inflamação local e sistêmica. Abreviações: TNF, fator de necrose tumoral; IL-6, interleucina 6; CCL2, quimiocina CC ligante 2. Adaptado de Tilg e col (Tilg e Moschen, 2006). 33
34 Tecido Adiposo Visceral versus Subcutâneo Na obesidade moderada, a distribuição regional do tecido adiposo parece ser um indicador importante de alterações metabólicas e cardiovasculares, uma vez que uma correlação inconstante entre o índice de massa corporal e estes distúrbios tem sido encontrada (Mann, 1974; Keys, 1981; Kannel, 1985; Larsson, 1991). Ao longo das últimas duas décadas os estudos têm reenfatizado a hipótese postulada anteriormente por Vague em 1947 (Vague, 1947) de que a obesidade não é uma condição homogênea e que a distribuição regional do tecido adiposo é importante na compreensão da relação entre a obesidade e os distúrbios no metabolismo glicídico e lipídico (Bouchard et al., 1993). Muitos estudos prospectivos mostraram que o excesso de gordura na região superior do corpo (central ou abdominal) considerada por Vague como obesidade andróide ou masculina se correlaciona de forma mais frequente com o aumento da mortalidade e risco de doenças como o diabetes, hiperlipidemia, hipertensão arterial e aterosclerose das artérias coronárias, encefálicas e de vasos periféricos, quando comparada ao tipo ginecóide de distribuição da gordura (porção inferior do corpo ou glúteo-femoral ou depósito periférico) (Lapidus et al., 1984; Larsson et al., 1984; Ohlson et al., 1985; Ducimetiere et al., 1986; Donahue et al., 1987) (Fig. 4). Figura 4. Padrões de distribuição da gordura corporal na obesidade. Em (A) é mostrado o padrão de distribuição andróide ou masculino ou central, onde o acúmulo de gordura predomina na região superior do corpo, ao nível da linha da cintura. Em (B), padrão ginecóide ou feminino, com predomínio de acúmulo de gordura na região glúteo-femoral. Adaptado de Adams, risk_of_diabetes.increased_by_liver_disease.php
35 35 Foram realizados diversos estudos epidemiológicos na Suécia e nos Estados Unidos no início da década de 1980 utilizando a espessura da dobra cutânea, a circunferência abdominal e/ou relação cintura-quadril como marcadores substitutos ao índice de massa corporal para se avaliar a adiposidade corporal. Estes estudos confirmaram uma associação entre a obesidade abdominal (andróide ou central) e o risco de desenvolvimento de doença cardiovascular e diabetes (Kissebah e Krakower, 1994; Wajchenberg, 2000). Todavia, as medidas antropométricas não distinguem entre o acúmulo de gordura abdominal subcutânea e abdominal intra-abdominal. Assim, análises posteriores por tomografia computadorizada e ressonância magnética da região abdominal ao nível da quarta e quinta vértebras lombares revelaram o acúmulo de gordura visceral com sendo a característica crítica que distingue indivíduos metabolicamente saudáveis (mas obesos) de pessoas obesas com desordens metabólicas e de indivíduos metabolicamente obesos, mas com peso normal (Sims, 2001). Desde então, a obesidade visceral tem sido implicada como fator de risco independente para o desenvolvimento de resistência à insulina e intolerância à glicose, capaz de levar ao desenvolvimento de DM2 e de doenças cardiovasculares em diferentes grupos étnicos (Kissebah e Krakower, 1994; Wajchenberg, 2000). A gordura da porção superior do corpo (central) corresponde ao depósito visceral localizado na cavidade abdominal adicionado ao depósito de gordura subcutâneo localizado imediatamente abaixo da pele e sobre a musculatura abdominal na porção superior do abdome (Smith et al., 2001). A gordura visceral é representada pela gordura situada na região intra-abdominal, composta pelos omentos maior e menor e pelo tecido adiposo mesentérico. A gordura visceral contribui com cerca de 20% da gordura corporal total no homem e corresponde, porém, a apenas 6% na mulher prémenopausa (Ross et al., 1992). A gordura da porção inferior do corpo (ginecóide) é representada principalmente pelo tecido adiposo subcutâneo nas regiões glútea e femoral, que é metabolicamente menos ativa do que o tecido adiposo da porção superior do corpo. O depósito subcutâneo glúteo-femoral também pode proteger contra o desenvolvimento de distúrbios metabólicos (Frayn, 2002). Ambos os depósitos visceral e subcutâneo servem como repositores de energia de forma a manter o equilíbrio sistêmico do gasto e da ingestão energética. Entretanto,
36 36 eles possuem algumas diferenças constitutivas em termos de morfologia e fisiologia que são características do seu papel fisiológico primário (Kissebah e Krakower, 1994; Wajchenberg, 2000). Os adipócitos do depósito adiposo visceral possuem uma taxa de lipólise basal baixa, mas esta se torna muito alta quando estimulados por catecolaminas, comparado a células oriundas dos depósitos subcutâneos abdominal, glúteo e femoral. Isto se deve ao grande número de receptores β-adrenérgicos e ao baixo número de receptores α-adrenérgicos nos adipócitos da gordura visceral (Mauriege et al., 1987; Hellmer et al., 1992; Vikman et al., 1996). A gordura visceral também possui uma alta taxa de captação de ácidos graxos não esterificados e triacilglicerol (Marin et al., 1992; Jensen et al., 2003). No homem, por exemplo, o tecido adiposo omental capta aproximadamente 50% mais lipídios do que o tecido adiposo subcutâneo (Marin et al., 1992; Jensen et al., 2003). Em relação às citocinas inflamatórias, sua função varia de acordo com a localização anatômica do depósito de gordura de onde são provenientes. As citocinas secretadas pelo depósito visceral exercem um maior efeito sobre o metabolismo hepático de carboidratos e lipídios e estimulam a secreção de proteínas inflamatórias pelo fígado (Baumann e Gauldie, 1990; Fernandez-Real et al., 2001). Dessa forma, citocinas inflamatórias provenientes do tecido adiposo visceral induziriam resistência hepática à insulina e inflamação sistêmica crônica (Frayn, 2002; Ravussin e Smith, 2002). Por outro lado, as citocinas produzidas pelo depósito subcutâneo exercem um efeito maior sobre o desenvolvimento e a função da célula adiposa a nível local (Sopasakis et al., 2004), apesar de também exercerem efeitos sistêmicos sobre o músculo esquelético, por exemplo. Em relação à leptina e adiponectina, o nível de expressão e secreção de leptina é aproximadamente três vezes maior no tecido adiposo subcutâneo comparado ao visceral, e é proporcional a quantidade de triacilglicerol armazenada no adipócito (Tritos e Mantzoros, 1997) e, consequentemente, ao tamanho do adipócito (Hamilton et al., 1995; Montague et al., 1997; Wajchenberg, 2000). Em contraste, a gordura visceral secreta mais adiponectina do que a gordura subcutânea que, por sua vez, é mais sensível à ação da insulina e dos sensibilizadores de insulina (tiazolidinedionas) (Motoshima et al., 2002).
37 Doença Gordurosa Pancreática Não-Alcoólica Uma das consequências da obesidade é a infiltração de gordura em diversos órgãos incluindo o coração, rins, fígado e músculo esquelético (acúmulo ectópico de gordura). Sob estresse oxidativo, citocinas são liberadas pelo tecido adiposo levando a um processo inflamatório e a disfunção do órgão. No fígado, a infiltração de gordura tem sido denominada como doença gordurosa hepática não-alcoólica, a qual pode levar cronicamente a esteatohepatite não-alcoólica e cirrose (Wanless e Shiota, 2004; McCullough, 2006). Infelizmente, não existem dados relatando a influência da obesidade sobre o acúmulo de gordura no pâncreas ou produção de citocinas no mesmo e, assim, a doença gordurosa pancreática não-alcoólica até recentemente ainda não havia sido descrita (Mathur et al., 2007). Apesar da inexistência de uma descrição mais detalhada da doença gordurosa pancreática não-alcoólica, algumas evidências mostrando uma correlação entre a obesidade e o acúmulo de gordura no pâncreas têm sido relatadas há algum tempo na literatura. Em 1920, Schaefer relatou uma correlação entre o peso do pâncreas e a massa corporal no indivíduo adulto (Schaefer, 1926). Em 1933, Ogilvie e col. encontraram 9% de gordura pancreática em cadáveres magros comparado a 17% em cadáveres obesos (Ogilvie, 1933). Nas décadas de 1960 e 1970, a gordura no pâncreas foi correlacionada com a idade, obesidade e o DM2 (Walters, 1966). Estudos recentes com tomografia computadorizada e ressonância magnética também mostram uma correlação entre a gordura pancreática e a obesidade (Matsumoto et al., 1995; Kovanlikaya et al., 2005). A pancreatite aguda é uma das doenças que mais frequentemente acometem o pâncreas e sua patogênese ainda não é completamente compreendida. Entretanto, evidências mostram que há uma autodigestão da glândula causada por um evento desconhecido, que converte as enzimas digestivas inativas em sua forma ativa no interior do pâncreas, levando a ruptura da membrana celular, edema, hemorragia intersticial, necrose e ativação adicional de outras pró-enzimas, que podem levar a destruição total dos ácinos pancreáticos (Vasseur et al., 2004). Já foi observado em humanos que a gravidade da pancreatite é aumentada em pacientes obesos
38 38 comparado a indivíduos magros, sugerindo também uma correlação entre a pancreatite e a obesidade (Segersvard et al., 2001; Papachristou et al., 2006). Comparado a camundongos magros, camundongos obesos com deficiência de leptina possuem mais gordura pancreática intralobular e interlobular avaliada histologicamente (Mathur et al., 2007; Fraulob et al., 2010). Os camundongos obesos também apresentam mais TNF-α e IL-1β em seu pâncreas. Em um estudo comparando camundongos magros (C57BL/6J, leptina normal) com camundongos obesos ob/ob ou db/db (ob/ob, deficiente em leptina e db/db, excesso de leptina, mas não possui seu receptor), foi administrado salina ou ceruleína para indução de pancreatite edematosa (Zyromski et al., 2008). Os camundongos obesos apresentaram uma pancreatite grave (histologicamente), sendo que os camundongos obesos hiperleptinêmicos (db/db) apresentaram uma pancreatite mais grave do que os camundongos ob/ob. Complementando os dados acima, ratos obesos por ingestão de dieta hiperlipídica apresentam lipotoxicidade pancreática e maior peroxidação lipídica, associada a danos morfológicos semelhantes a pancreatite, assim como aumento da síntese de colágeno por células estreladas ativadas (Zhang et al., 2008). Assim, estes estudos sugerem que a doença gordurosa pancreática não-alcoólica pode levar a uma esteatopancreatite não-alcoólica. Entretanto, trabalhos adicionais são necessários para elucidar o papel fisiopatológico da obesidade nesta nova condição, uma vez que o pâncreas possui uma função vital na homeostase da glicose e no desenvolvimento do DM2 no indivíduo obeso. 2.6 Receptores Ativadores de Proliferação Peroxissomal Os receptores ativadores de proliferação peroxissomal (PPARs) são fatores de transcrição ativados por ligantes que pertencem à superfamília de receptores nucleares hormonais. O PPARα (NR1C1) (Committee, 1999) foi o primeiro a ser descrito como um receptor ativador de proliferação peroxissomal, daí seu nome (Issemann e Green, 1990). Dois isotipos relacionados, o PPARβ/δ (NR1C2) e o PPARγ (NR1C3) foram posteriormente encontrados e caracterizados (Dreyer et al., 1992). O
39 39 sequenciamento do genoma de mamíferos indicou que existem apenas três isotipos do PPAR, e cada um deles é codificado por um gene separado. Cada isotipo do PPAR possui um padrão de expressão tecidual característico (Kliewer et al., 1994; Braissant et al., 1996). O PPARα é altamente expresso em órgãos que desempenham um papel significante no catabolismo de ácidos graxos, como o tecido adiposo marrom, fígado, coração, rim e intestino (Mandard et al., 2004). Sua expressão também é detectada em muitas células vasculares como as células endoteliais, células musculares lisas, monócitos e macrófagos (Chinetti et al., 1998; Inoue et al., 1998; Staels et al., 1998; Diep et al., 2000). Entre os três isotipos, o PPARβ/δ é o que possui o mais amplo espectro de expressão. Funções importantes têm sido atribuídas ao PPARβ/δ na pele, intestino, placenta, músculo esquelético, tecido adiposo e encéfalo (Braissant et al., 1996; Bastie et al., 1999; Peters et al., 2000; Michalik et al., 2001; Barak et al., 2002), contudo seu nível de expressão é relativamente maior no encéfalo, tecido adiposo e pele (Braissant et al., 1996). O gene do PPARγ possui três promotores, permitindo a expressão de três isoformas, PPARγ1 e PPARγ2 e PPARγ3 (Fajas et al., 1997; Fajas et al., 1998). O RNAm do PPARγ1 e PPARγ3 originam a mesma proteína PPARγ1. Uma alta expressão do PPARγ2 é encontrada nos diferentes tecidos adiposos (Dreyer et al., 1992; Chawla et al., 1994; Tontonoz et al., 1994b), enquanto o PPARγ1 possui uma expressão mais ampla como, por exemplo, no intestino, encéfalo, células vasculares e tipos específicos de células imunes e inflamatórias (Tontonoz et al., 1994a; Zhu et al., 1995). O PPARγ3 é encontrado nos macrófagos, intestino grosso e tecido adiposo branco (Braissant et al., 1996; Fajas et al., 1998; Ricote et al., 1998a). Diferente dos receptores de hormônios esteróides que atuam como homodímeros, a regulação transcripcional pelo PPAR necessita da heterodimerização com o receptor X retinóico (RXR or NR2B), que pertence à mesma superfamília de receptores nucleares (Fig. 5) (Kliewer et al., 1992; Keller et al., 1993). O heretodímero PPAR/RXR pode se formar na ausência de um ligante. Quando ativado por um ligante, ele modula a transcrição através de sua ligação a uma sequência específica do DNA denominada elemento responsivo ao PPAR (PPRE) (Kliewer et al., 1992; Tugwood et al., 1992; Feige et al., 2005). O PPRE é composto de dois sítios que ocorrem como
40 40 repetições consenso da sequência AGGTCA, e entreposto a eles há um único nucleotídeo fazendo o espaçamento. Este elemento responsivo normalmente está presente em cópia única ou múltiplas cópias na região promotora de seus genes alvos, mas também pode estar localizado na região proximal de certos genes responsivos ao PPAR (Di-Poi et al., 2002). O PPAR e o RXR se ligam aos sítios 5 e 3 do PPRE, respectivamente, e a região 5 medeia a seletividade de ligação entre os diferentes isotipos do PPAR (DiRenzo et al., 1997; Ijpenberg et al., 1997; Juge-Aubry et al., 1997). O controle transcripcional pelos heterodímeros PPAR/RXR requer a interação com complexos coreguladores tanto um coativador para estimulação ou um corepressor para inibição da expressão de genes alvos (Dowell et al., 1999; Stanley et al., 2003; Guan et al., 2005; Yu et al., 2005). Figura 5. Ativação do PPAR e transcrição gênica. A ativação do receptor PPAR leva a sua acumulação no núcleo, onde ele forma um heretodímero com o RXR. O heterodímero PPAR/RXR se liga a sequência PPRE do DNA, induzindo a transcrição gênica dos diferentes isotipos do PPAR. Abreviações: PPAR, receptor ativador de proliferação peroxissomal; RA, ácido retinóico; RXR receptor X retinóico; PPRE, elemento responsivo ao PPAR. Adaptado de Bishop-Bailey e col (Bishop-Bailey, 2000).
41 41 Consistente com a sua distribuição em tecidos com altas taxas catabólicas de ácidos graxos e alta atividade peroxissomal, o principal papel do PPARα é a regulação da homeostase energética (Lefebvre et al., 2006). No fígado em especial, o PPARα ativa o catabolismo dos ácidos graxos, estimula a gliconeogênese, a síntese de corpos cetônicos, e está envolvido no controle da montagem das lipoproteínas (Staels et al., 1995; Vu-Dac et al., 1995; Kersten et al., 1999; Reddy e Hashimoto, 2001). O PPARα também estimula a síntese do heme e o catabolismo do colesterol. Adicionalmente, ele atenua a resposta inflamatória e participa do controle do metabolismo de aminoácidos e da síntese da uréia (Devchand et al., 1996; Staels et al., 1998; Kersten et al., 2001). O aumento da oxidação de ácidos graxos devido à ativação do PPARα diminui os níveis circulantes de triglicerídeos, a esteatose hepática e muscular e reduz a adiposidade, que leva a melhora da sensibilidade à insulina (Guerre-Millo et al., 2000; Chou et al., 2002; Kim et al., 2003). De forma não surpreendente, os medicamentos da classe dos fibratos p. ex., gemfibrozil, clofibrato, fenofibrato e bezafibrato que são amplamente utilizados no tratamento da hipertrigliceridemia são ativadores do PPARα. Os agonistas PPARα têm demonstrado também uma atividade antiinflamatória significativa, e isto parece estar relacionado às suas ações protetoras no sistema cardiovascular (Berger et al., 2005). Apesar de amplamente expresso nos tecidos do corpo, as funções do PPARβ/δ não são ainda completamente conhecidas. Hoje já se sabe que ele é necessário ao desenvolvimento normal da placenta e do intestino, e também está envolvido no controle da homeostase energética pela estimulação de genes envolvidos no catabolismo de ácidos graxos e na termogênese adaptativa (Wang et al., 2003; Nadra et al., 2006; Varnat et al., 2006). O PPARβ/δ também possui um papel importante no controle da proliferação, diferenciação e sobrevivência celular, assim como no reparo tecidual (Letavernier et al., 2005; Michalik e Wahli, 2006). O tratamento com o GW (agonista PPARβ/δ de alta afinidade) tem mostrado que a ativação do PPARβ/δ é capaz de aumentar o HDL colesterol (Leibowitz et al., 2000; Oliver et al., 2001), impede a progressão da lesão aterosclerótica em camundongos (Lee et al., 2003) e induz a perda de peso (Wang et al., 2003). Adicionalmente, os ligantes
42 42 PPARβ/δ têm sido propostos como potentes sensibilizadores de insulina, uma vez que eles melhoram a intolerância à glicose (Tanaka et al., 2003; Wang et al., 2004). O PPARγ é o protagonista na diferenciação do tecido adiposo e na manutenção das funções específicas do adipócito, como o armazenamento de lipídios no tecido adiposo branco e a dissipação de energia no tecido adiposo marrom (Tontonoz et al., 1993; He et al., 2003; Koutnikova et al., 2003). Além disso, ele é necessário à sobrevivência dos adipócitos diferenciados (Imai et al., 2004). Adicionalmente, o PPARγ está envolvido no metabolismo da glicose através da melhora da sensibilidade à insulina e assim representa uma ligação molecular entre o metabolismo de carboidratos e lipídios (Rosen et al., 1999; Rieusset et al., 2002; Savage et al., 2003). Da mesma forma que o PPARα, a ativação do PPARγ parece limitar a inflamação, adicionando um interesse em seu possível papel sobre a contenção da aterosclerose, além do diabetes (Ricote et al., 1998b). Entre os compostos sintéticos que ativam seletivamente o PPARγ estão as tiazolidinedionas, que são sensibilizadores de insulina utilizados para tratar a hiperglicemia no DM2 (Mayerson et al., 2002; Bajaj et al., 2003; Bays et al., 2004). 2.7 Modelos Experimentais de Doenças Metabólicas Modelos animais apropriados são cruciais no estudo da patogênese e terapia das doenças metabólicas, mas ainda não é claro que critério deve ser utilizado na definição do modelo animal ideal. Do ponto de vista científico e ético, a exigência mínima é a de que não apenas o fenótipo, mas também a patogênese da condição do animal se assemelhe à doença humana em estudo. Considerando a natureza poligênica da síndrome metabólica humana, os estudos com modelos de obesidade monogênica ou induzida farmacologicamente devem ser interpretados com cuidado, uma vez que na maioria das vezes é difícil definir o quanto um resultado é decorrente do fenótipo obesidade ou do modelo genético/farmacológico em questão (Buettner et al., 2007).
43 43 Como alternativa, os pesquisadores têm utilizado dietas ricas em lipídios, denominadas dietas hiperlipídicas (high-fat diets) (Oakes et al., 1997), com a finalidade de gerar modelos de obesidade em roedores. O primeiro relato de tal intervenção nutricional data da década de Estudos subsequentes mostraram que as dietas hiperlipídicas promovem hiperglicemia e resistência à insulina e, assim, diversos pesquisadores têm examinado seus efeitos sobre a fisiologia muscular esquelética e hepática, e sobre a sinalização da insulina. Baseado nesta experiência, o uso de dietas hiperlipídicas é geralmente bem aceito na geração de modelos válidos de síndrome metabólica humana em roedores que apresentam como fenótipo a resistência à insulina e uma função comprometida da célula β (Oakes et al., 1997; Ahren et al., 1999; Lingohr et al., 2002). Entretanto, há um problema importante relacionado à dieta hiperlipídica, que concerne à definição do termo hiperlipídica propriamente dito. Apesar das inúmeras publicações na base de artigos PubMed 2 usarem o termo high-fat diet, nem o conteúdo lipídico (quantidade), nem a composição lipídica (qualidade) das dietas é padronizado. A AIN-93 é um guia que determina a quantidade e a qualidade ideal de macro e micronutrientes na dieta de roedores de laboratório (Reeves et al., 1993). Segunda esta publicação, recomenda-se que a dieta padrão de manutenção de roedores (AIN-93M) contenha 9,5% de lipídios em sua composição energética (= 40 g/kg de ração), sendo sua fonte o óleo de soja. Porém, não existe uma recomendação para a elaboração de dietas hiperlipídicas, resultando em inúmeras variações na literatura, com dietas contendo 20%, 40% ou até 60% de sua energia derivada do lipídio, assim como dietas elaboradas com lipídios de origem animal (banha de porco, sebo) ou vegetal (milho ou palma). Isto leva inevitavelmente a resultados variáveis e conflitantes, de difícil comparação. Outro agravante é o de que a maioria das pesquisas em obesidade utiliza dietas com ingredientes purificados (mais correto), enquanto alguns estudos adicionam gordura à ração comercial. Isto pode levar a inadequações nutricionais, uma vez que quando a gordura é adicionada, outros nutrientes são diluídos (proteínas, vitaminas, minerais e fibras). A adição de uma quantidade excessiva de gordura pode na verdade gerar uma dieta deficiente em proteínas, que claramente não é a intenção ao se criar uma dieta hiperlipídica. 2 (
44 44 O efeito da dieta hiperlipídica sobre a massa corporal depende tanto da quantidade de lipídio quanto do tempo de ingestão da dieta. A maioria dos roedores se torna obeso quando alimentado com dietas com teor lipídico entre 30%-60%, mas a resposta na tolerância à glicose, resistência à insulina, triglicerídeos, etc, depende da linhagem, idade (Levin et al., 1997; Rossmeisl et al., 2003) e fonte do lipídio (Ikemoto et al., 1996; Buettner et al., 2006). Na Tabela 2 são apresentados alguns modelos de doenças metabólicas induzidos por dieta em roedores. Tomando como base o camundongo C57BL/6, o modelo mais indicado para o estudo do DM2 seria através da oferta de uma dieta hiperlipídica rica em sacarose (Surwit et al., 1988).
45 45 Tabela 2. Modelos de doenças metabólicas induzidas por dieta Tipo de dieta Linhagem Fenótipo Comentário Lipídio 30-60% SD, Wistar Obesidade Diferença aparente na massa corporal após 2-10 semanas de dieta. O tipo de lipídio influencia o ganho de massa corporal (Chang et al., 1990; Ghibaudi et al., 2002; Levin e Dunn-Meynell, 2006). Frutose 60% SD, Wistar Hipertensão, insulina, CT, TG, HDL, LDL Hipertensão se desenvolve após 6-8 semanas de dieta (Sanchez- Lozada et al., 2007; de Moura et al., 2008). Sacarose 60-70% SD, Wistar RI, TG Ambos ocorrem após 2 semanas de dieta (Pagliassotti et al., 1996; Pagliassotti et al., 2000). Lipídio 45-60% C57BL/6 Obesidade, diabetes, RI, CT Massa corporal aumenta já na 1ª semana; hiperglicemia ocorre após 4 semanas (Rossmeisl et al., 2003; Gallou-Kabani et al., 2007; Fraulob et al., 2010). Dieta hiperlipídica (ác. graxo saturado), 1% colesterol, 0,25% ácido cólico C57BL/6 Aterosclerose CT Hipercolesterolemia e aterosclerose moderada ocorrem após semanas de dieta (Nishina et al., 1990; Nishina et al., 1993). Lipídio 36%, Sacarose 37% C57BL/6 Obesidade, diabetes, RI O aumento da glicemia de jejum é mais pronunciado quando a sacarose é adicionada à dieta hiperlipíca (Surwit et al., 1988). A porcentagem indicada dos macronutrientes é calculada com base na energia total da dieta (em kcal). Abreviações: SD, rato Sprague Dawley; CT, colesterol total; TG, triglicerídeo; HDL, lipoproteína de alta densidade; LDL, lipoproteína de baixa densidade; RI, resistência à insulina (Gajda et al., 2007).
46 46 MATERIAIS E MÉTODOS O protocolo de manuseio e experimentação foi aprovado pelo Comitê local de Ética para Uso e Cuidado de Animais de Laboratório (Anexo 1). Este estudo foi realizado em acordo com o Guia para Uso e Cuidado de Animais Laboratoriais (US National Institutes of Health 85-23, revisada em 1996). 3.1 Obtenção da Amostra e Grupos Experimentais Neste estudo foram utilizados camundongos C57BL/6 machos com dois meses de idade, obtidos previamente da Universidade Federal de São Paulo (USP/CEDEME). Eles foram mantidos em condições controladas de umidade, temperatura, luz e exaustão (umidade 60±10%, 21±2 C, ciclo de 12 h claro/escuros e ciclo de exaustão de 15 min/h). Os animais foram agrupados conforme descrito abaixo: SC controle não diabético e sem sobrepeso, alimentado com dieta padrão para roedores (standard chow) por 6 semanas (n=10); HFHS controle diabético e com sobrepeso, alimentado com dieta rica em lipídios e sacarose (high-fat high-sucrose diet) por 6 semanas (n=40). Passadas 6 semanas, os animais do grupo HFHS foram subdivididos conforme o tratamento, que durou 5 semanas, sem interrupção da dieta: HFHS dieta HFHS, sem tratamento (n=10); HFHS-Ro dieta HFHS + rosiglitazona (0,01% na ração) (n=10); HFHS-Fe dieta HFHS + fenofibrato (0,18% na ração) (n=10); HFHS-Bz dieta HFHS + bezafibrato (0,4% na ração) (n=10).
47 47 O experimento totalizou 11 semanas. Os medicamentos foram administrados na ração. As dietas foram elaboradas com nutrientes purificados pela empresa Rhoster (Rhoster, Ribeirão Preto, SP, Brasil, em acordo com as recomendações da AIN93M (Reeves et al., 1993). Suas formulações encontram-se descritas na Tabela 3: Tabela 3. Composição das dietas. SC HFHS Ingredientes (g/kg) Caseína 140,0 160,0 Amido de milho 620,7 220,7 Sacarose 100,0 300,0 Fibras 50,0 50,0 Óleo de soja 40,0 40,0 Banha - 180,0 Mix de vitaminas* 10,0 10,0 Mix de minerais** 35,0 35,0 Colina 2,5 2,5 Antioxidante 0,008 0,008 Energia kcal/g 3,81 4,71 Proteína, % 14,9 13,7 Lipídio, % 9,4 42,0 Carboidrato, % 75,7 44,2 * Vitaminas presentes no mix estão em acordo com a AIN-93M. ** Minerais presentes no mix estão em acordo com a AIN-93M. Abreviações: SC, dieta padrão; HFHS, dieta hiperlipídica rica em sacarose.
48 Ingestão de Ração, Água, Energia e Eficiência Alimentar A livre ingestão de ração e água foi permitida aos animais. Ao longo do experimento, a massa corporal foi aferida semanalmente e a ingestão de água e ração diariamente. A ingestão de ração (g/dia) foi multiplicada pela energia da ração (Kcal/g) para se obter a ingestão de energia diária por camundongo. A eficiência alimentar foi calculada como [(ganho de massa corporal/kcal ingerida) x 100]. Todos estes parâmetros foram calculados para o período pré-tratamento (semana 0 a 6) e pós-tratamento (semana 6 a 11). O cálculo da dose diária de medicamento ingerido foi feito com base na ingestão diária de ração e na massa corporal, correspondendo a 9,4±0,09 mg/kg/dia para a rosiglitazona, 163,0±3.0 mg/kg/dia para o fenofibrato e 382,0±7,0 mg/kg/dia para o bezafibrato. 3.3 Metabolismo Glicídico e Lipídico e Função Pancreática Na semana 6, sangue foi coletado após 6 horas de jejum através da veia submandibular para análise dos níveis séricos de glicose (glicômetro, Accu-Chek Go, Roche, São Paulo, SP, Brasil) e insulina (insulin ImmuChem coated tube radioimmunoassay kit, MP Biomedicals, Califórnia, USA). Na semana 10 foi realizado teste oral de tolerância à glicose (TOTG), onde glicose a 25% diluída em salina estéril (0,9% NaCl) foi administrada através de gavagem orogástrica após jejum de 6 horas (dose de 1g/kg de massa corporal). Sangue foi coletado através de uma incisão na ponta da cauda do animal para dosagem da glicose plasmática antes da gavagem e após 15, 30 e 60 minutos. A área sob a curva (ASC) foi calculada usando a regra do trapézio para analisar a intolerância à glicose. Na eutanásia (semana 11), sangue foi novamente coletado (punção cardíaca pelo átrio direito) após 6 horas de jejum para análise da glicose (glicômetro) e insulina
49 49 (radioimunoensaio) de jejum. Os lipídios séricos (triglicerídeos, colesterol total e HDL colesterol), amilase e lipase também foram analisados, através de ensaio colorimétrico (Bioclin, Belo Horizonte, MG, Brasil). O LDL colesterol foi calculado através da equação de Friedwald, LDL = [CT - HDL - (TG/5)], onde CT representa o colesterol total e TG o triglicerídeo (Friedwald et al., 1972). A resistência à insulina foi avaliada pelo HOMA-IR (homeostasis model assessment index) onde: HOMA-IR = [insulina (µu/ml) x glicose (mmol/l)] / 22,5 (Matthews et al., 1985). 3.4 Hipertrofia Cardíaca Para a análise da hipertrofia cardíaca o coração foi removido no momento da eutanásia, pesado e seu peso foi corrigido pelo comprimento da tíbia (côndilo ao maléolo medial) a fim de se remover o efeito do tamanho do animal sobre este parâmetro (Yin et al., 1982). 3.5 Morfometria do Tecido Adiposo Foram utilizadas as gorduras epididimal, retroperitoneal e inguinal para analisar a morfologia dos adipócitos. A gordura subcutânea localizada entre a porção inferior da caixa torácica e a porção mediana da coxa foi considerada como gordura inguinal (Surwit et al., 1995). A gordura conectada a parede abdominal posterior, ao redor dos rins e na parte abdominal do ureter foi considerada gordura retroperitoneal. A gordura abdominal localizada na porção inferior do abdome conectada ao epidídimo foi considerada como gordura epididimal. A relação entre a gordura visceral e a subcutânea foi calculada como: Sub:Vis = [gordura inguinal] / [gordura epididimal + retroperitoneal]. Após pesadas, as gorduras foram fixadas em formalina 4%, incluídas em Paraplast plus (Sigma-Aldrich Co., St. Louis, MO, USA), seccionadas em 5 µm de espessura e
50 50 coradas com hematoxilina e eosina. Foram obtidas imagens digitais dos cortes histológicos, e aproximadamente 250 adipócitos por grupo tiveram seu diâmetro aferido usando o software Image-Pro Plus versão 5.0 (Media Cybernetics, Silver Spring, USA) (Fig. 6). Figura 6. Morfometria do adipócito. No software Image-Pro Plus, uma imagem digital do tecido adiposo foi adquirida e duas medidas de diâmetro por adipócito foram realizadas, para o cálculo do diâmetro médio. No quadro à direita estão os valores dos diâmetros mensurados.
51 Morfometria e Estereologia do Pâncreas O pâncreas foi pesado logo após ser retirado do corpo do animal, fixado em formalina 4% por 24h e então seguiu a rotina de processamento histológico do laboratório para inclusão em Paraplast plus (Sigma Co., St. Louis, MO, USA). O tecido incluído foi seccionado em cortes histológicos não consecutivos de 5 μm de espessura, e posteriormente corado em hematoxilina e eosina. Imagens digitais do tecido pancreático foram adquiridas utilizando o software Image-Pro Plus versão 5.0 (Media Cybernetcs, Silver Spring, MD, USA). O maior e o menor diâmetro de cada ilhota foram mensurados a fim de se calcular o diâmetro médio da ilhota. Pelo menos 25 ilhotas foram analisadas por camundongo, totalizando 125 ilhotas por grupo. A densidade de gordura no pâncreas (interlobular + intralobular + perilobular) foi calculada através da análise estereológica por contagem de pontos. Uma imagem do tecido pancreático em pequeno aumento foi projetada em um monitor Sony (Sony Triniton, Pencoed, UK) acoplado ao microscópio Leica (Leica DMRBE, Wetzlar, Germany) através de uma videocâmera (Kappa, Gleichen, Germany), e um sistema teste contendo 36 pontos foi sobreposto a imagem do tecido (Fig. 7). Os pontos que tocavam as células adiposas foram considerados. A densidade de volume de gordura pancreática foi calculada como Vv[gord] = Pp/PT, onde Pp representa os pontos que tocavam as células adiposas e PT representa o número total de pontos do sistema teste (Mandarim-de-Lacerda, 2003).
52 Figura 7. Quantificação da densidade de volume de gordura pancreática. Este parâmetro foi calculado a partir da relação entre os pontos (representado pelo centro de cada cruz) que tocam as células adiposas e o número total de pontos do sistema teste. 52
53 Imunohistoquímica do Tecido Adiposo e Pâncreas Os tecidos adiposo e pancreático utilizados na imunohistoquímica passaram pelo mesmo processamento histológico utilizado na análise morfométrica e estereológica. As lâminas foram tratadas com xilol e posteriormente com álcool etílico em concentrações decrescentes e água destilada. A recuperação antigênica foi feita em tampão citrato ph 6,0 a 60 C. A peroxidase endógena foi inibida com peróxido de hidrogênio 3% e as ligações não específicas foram inibidas com PBS/BSA 5%. Os cortes foram incubados com os anticorpos descritos a seguir: Tecido adiposo: anti-adiponectina (A6354, Sigma) Pâncreas: anti-insulina (A0564, DAKO), anti-glucacon (A0565, DAKO), anti-glut2 (AB1342, Chemicon), anti-pparα (sc-9000, Santa Cruz Biotechnology) e anti- PPARβ/δ (sc-1987, Santa Cruz Biotechnology). A ligação do anticorpo primário foi amplificada pelo sistema avidinaestreptavidina (K0679; Universal DakoCytomation LSAB + Kit, Peroxidase), e a reação foi visualizada após incubação com 3,3 diaminobenzidina tetraclorido (DAB, K3466, DakoCytomation). Os cortes foram então contracorados com hematoxilina de Mayer, banhados em água destilada, desidratados em concentrações crescentes de álcool etílico, banhados em xilol e, finalmente, as lamínulas foram sobrepostas à lâmina usando Enthelan. No tecido adiposo, a quantificação da imunocoloração para adiponectina foi classificada usando um sistema de escore semi-quantitativo: 0, sem expressão; +, expressão fraca; ++ expressão moderada; +++ expressão forte. No pâncreas, imagens digitais das ilhotas imunocoradas foram obtidas usando o mesmo equipamento utilizado para a análise morfométrica. Uma ferramenta de seleção foi utilizada para identificar as áreas da ilhota com coloração imunopositiva (Fig. 8). Esta seleção foi segmentada em uma nova imagem digital em preto e branco, sem tons intermediários, onde a cor branca representava as áreas imunopositivas e a cor preta representava o restante do tecido pancreático. O limite externo da ilhota foi delimitado usando a ferramenta AOI irregular, e no interior desta área delimitada, a
54 54 área ocupada pela cor branca foi quantificada usando a ferramenta de histograma da imagem. Esta área foi expressa na forma de densidade de coloração por ilhota (%) (Mandarim-de-Lacerda et al., 2010). Figura 8. Quantificação da imunocoloração nas ilhotas pancreáticas. Em (a), ilhota pancreática corada com anticorpo anti-insulina (em marrom). Em (b), segmentação da imagem a em uma nova imagem em preto e branco, onde a cor branca representa a imunocoloração para insulina e a cor preta o restante do tecido. A área que representa a ilhota é delimitada (linha verde) e, assim, a quantidade de cor branca é quantificada pelo histograma da imagem e expressa como percentagem da área total da ilhota.
55 Análise Estatística Os dados são apresentados na forma de média ± erro padrão da média (EPM). Um n=10 por grupo foi mantido ao longo do experimento, entretanto apenas um n=5 foi utilizado para cada parâmetro analisado. Os dados foram testados em relação a normalidade e a homocedasticidade das variâncias. As diferenças entre os grupos estudados foram analisadas através de análise de variância seguida de pós-teste de Tukey. As diferenças para um mesmo grupo, em momentos diferentes (prétratamento versus pós-tratamento), foram testadas usando teste t-pareado. A correlação e regressão linear foram calculadas para o diâmetro do adipócito versus o HOMA-IR e a área sob a curva do TOTG (Statistica version 7, Statsoft, Tulsa, OK, USA). Um P menor do que 0,05 foi considerado estatisticamente significativo.
56 56 RESULTADOS 4.1 Ingestão de Ração, Energia e Água e Eficiência Alimentar Até a semana 6, o grupo HFHS ingeriu 10% a menos de ração do que o grupo SC, porém a ingestão energética foi maior (+10%, P<0,0001), sem diferença na ingestão hídrica (Tabela 4). Os grupos HFHS-Fe e HFHS-Bz ingeriram a mesma quantidade de ração do grupo HFHS, porém o tratamento com a rosiglitazona resultou em hiperfagia (+15% comparado ao grupo HFHS, P<0,0001). A eficiência alimentar dos animais alimentados com dieta HFHS foi maior do que no grupo SC no período pré-tratamento (aproximadamente +116%, P<0,01) (Fig. 9). Este comportamento se manteve no grupo HFHS sem tratamento no período póstratamento. A eficiência alimentar no grupo HFHS-Ro foi exacerbada pelo medicamento (+494% e +94%, respectivamente, comparado aos grupos SC e HFHS, P<0,001). Ambos os fibratos diminuíram a eficiência energética, de forma a torná-la negativa. No período pós-tratamento houve aumento da ingestão hídrica pelo grupo HFHS comparado ao SC (+14%, P<0,05), a qual foi diminuída pela administração de rosiglitazona (-10% comparado ao grupo HFHS, P<0,05) (Tabela 4). Não foi observada diarréia ou qualquer alteração física nos animais.
57 57 Tabela 4. Ingestão de Ração, Energia e Água Ração (g/dia/animal) Energia (Kcal/dia/animal) Água (ml/dia/animal) Pré-tratamento SC 3,0±0,04 11,5±0,2 4,5±0,2 HFHS 2,7±0,02 a 12,7±0,1 a 4,5±0,1 Pós-tratamento SC 2,7±0,03 a 10,5±0,1 ab 3,5±0,1 ab HFHS 2,7±0,05 a 12,7±0,3 *a 4,0±0,1 *b HFHS-Ro 3,1±0,03 * b 14,5±0,2 * ab 3,6±0,1 ab HFHS-Fe 2,7±0,05 a 12,6±0,2 * a 4,1±0,1 * HFHS-Bz 2,6±0,05 a 12,2±0,3 * 4,3±0,1 * Os dados são apresentados na forma de média ± EPM. Grupos: SC, dieta padrão; HFHS, dieta rica em lipídios e sacarose; HFHS-Ro, HFHS tratado com rosiglitazona; HFHS-Fe, HFHS tratado com fenofibrato e; HFHS-Bz, HFHS tratado com bezafibrato. Os símbolos representam diferença estatística com: (a) SC e (b) HFHS, no período pré-tratamento; (*) SC, ( ) HFHS e ( ) HFHS-Ro, no período pós-tratamento, P<0,05.
58 58 Figura 9. Eficiência alimentar dos diferentes grupos experimentais, nos períodos pré-tratamento e póstratamento. Grupos: SC, dieta padrão; HFHS, dieta rica em lipídios e sacarose; HFHS-Ro, HFHS tratado com rosiglitazona; HFHS-Fe, HFHS tratado com fenofibrato e; HFHS-Bz, HFHS tratado com bezafibrato. Os símbolos representam diferença estatística com: (a) mesmo grupo, no período pré-tratamento; (*) SC, ( ) HFHS e ( ) HFHS-Ro, no período pós-tratamento, P<0, Massa Corporal Os animais iniciaram o experimento sem diferenças na massa corporal (22,2 g ± 0,2 g aos 2 meses de idade) (Fig. 10). A dieta HFHS induziu ganho de massa corporal, onde na semana 6 os animais apresentaram massa corporal 17% maior do que o grupo SC (P<0,0001). A massa corporal do grupo HFHS sem tratamento continuou aumentando até o fim do experimento, alcançando 34,3 g ± 1,0 g. A administração de rosiglitazona exacerbou o ganho de massa corporal (+49% e +17% comparado aos grupos SC e HFHS, respectivamente, P<0,01). O fenofibrato impediu a evolução do ganho de massa corporal e o bezafibrato induziu perda de massa (-9% comparado à massa corporal do mesmo grupo na semana 6, P<0,01).
59 Figura 10. Evolução da massa corporal ao longo do experimento. As dietas foram administradas por 11 semanas e os medicamentos da 6ª à 11ª semana. Grupos: SC, dieta padrão; HFHS, dieta rica em lipídios e sacarose; HFHS-Ro, HFHS tratado com rosiglitazona; HFHS-Fe, HFHS tratado com fenofibrato e; HFHS- Bz, HFHS tratado com bezafibrato. Os símbolos representam diferença estatística com: (*) SC, ( ) HFHS, ( ) HFHS-Ro e ( ) HFHS-Fe, P<0,05. 59
60 Lipídios séricos O colesterol total e o HDL colesterol apresentaram-se elevados após 11 semanas de ingestão da dieta HFHS, comparado aos animais que receberam dieta padrão (+46% for CT, P<0,001 e +22% for HDL, P<0,05) (Tabela 5). O colesterol total foi menor nos grupos HFHS-Ro e HFHS-Bz comparado ao grupo HFHS (-12%, P<0,05 e -14%, P<0,05, respectivamente). Os três tratamentos reduziram o HDL colesterol, sendo o bezafibrato o mais eficiente (-45%, P<0,0001). A dieta HFHS não alterou os níveis de triglicerídeos, porém o tratamento com os fibratos reduziu este parâmetro, comparado aos grupos SC e HFHS (P<0,05). O LDL colesterol foi aumentado pela dieta HFHS (+93%, P<0,001), porém o tratamento com rosiglitazona o manteve similar ao grupo SC, enquanto os fibratos aumentaram o LDL, quando comparado tanto ao grupo SC quanto ao grupo HFHS (P<0,0001). 4.4 Insulina e Glicose séricos A ingestão da dieta HFHS levou ao aumento da glicemia de jejum em cerca de 32% comparado ao grupo SC (P<0,0001) (Tabela 5). Esta diferença foi observada durante todo o experimento. A rosiglitazona impediu o aumento da glicemia de jejum, enquanto o bezafibrato teve efeito hipoglicemiante, uma vez que o grupo HFHS-Bz apresentou glicemia de jejum inferior a glicemia apresentada pelo grupo HFHS na semana 6 (-18%, P<0,001). Não houve melhora da glicemia de jejum pelo fenofibrato. No teste oral de tolerância à glicose, a área sob a curva foi maior no grupo HFHS comparado ao SC (+30%, P<0,0001), indicando intolerância à glicose nesses animais. Os animais que receberam rosiglitazona ou bezafibrato apresentaram redução da área sob a curva, comparado aos animais HFHS não tratados (P<0,01) (Fig. 11). O fenofibrato não alterou de forma significativa a área sob a curva no grupo HFHS-Fe, a qual se apresentou semelhante ao grupo HFHS.
61 61 A insulina de jejum aumentou após a ingestão da dieta HFHS (+57% na semana 6, P<0,05, e +138% na semana 11 comparado ao grupo SC, P<0,001) (Tabela 5). Todos os medicamentos impediram a elevação dos níveis de insulina quando comparados ao grupo HFHS (-32% para a rosiglitazona, P<0,001; -58% para o fenofibrato, P<0,0001; e -63% para o bezafibrato). Ao final do experimento, a insulina de jejum nos animais que receberam fenofibrato ou bezafibrato foi semelhante à do grupo SC. A resistência à insulina foi vista nos animais HFHS não tratados nas semanas 6 e 11, comparado ao grupo SC, acessado através do HOMA-IR (+97% e +201%, respectivamente, P<0,0001) (Tabela 5). Todos os medicamentos impediram o desenvolvimento da resistência à insulina. A amilase e lipase séricas não diferiram de forma significativa entre os grupos estudados (Tabela 5).
62 62 Tabela 5. Metabolismo Lipídico e Glicídico e Função Pancreática. SC HFHS HFHS-Ro HFHS-Fe HFHS-Bz Pré-tratamento Glicose, mmol/l 7,5±0,3 9,9±0,2 a Insulina, ng/dl 0,7±0,07 1,1±0,12 a HOMA-IR 5,9±0,3 11,6±1,0 a Pós-tratamento Glicose, mmol/l 9,1±0,3 a 12,1±0,7 *b 9,2±0,4 10,5±0,7 a 8,1±0,3 b Insulina, ng/dl 0,8±0,11 1,9±0,13 *b 1,3±0,11 * a 0,8±0,05 0,7±0,06 HOMA-IR 9,2±0,6 27,7±2,4 *ab 12,9±1,4 a 9,9±1,1 6,7±0,6 Triglicerídeos, mg/dl 147±11 156±12 122±10 108±4 * 110±7 * Colesterol total, mg/dl 136±4 199±5 * 176±5 * 192±3 * 172±9 * HDL, mg/dl 68±5 83±2 * 68±4 55±3 46±2 * Amilase, U/L 666±25 654±18 697±6 661±17 656±4 Lipase, U/L 608±8 628±2 613±15 595±15 625±27 Os dados são apresentados na forma de média ± EPM. Abreviações: SC, dieta padrão; HFHS, dieta rica em lipídios e sacarose; HFHS-Ro, HFHS tratado com rosiglitazona; HFHS-Fe, HFHS tratado com fenofibrato; HFHS-Bz, HFHS tratado com bezafibrato; HOMA-IR, índice de resistência à insulina e; HDL, lipoproteína de alta densidade. Os símbolos representam diferença estatística com: (a) SC e (b) HFHS, no período pré-tratamento; (*) SC, ( ) HFHS, ( ) HFHS-Ro e ( ) HFHS-Fe, no período póstratamento, P<0,05.
63 Figura 11. Teste oral de tolerância à glicose. As curvas glicêmicas de resposta à sobrecarga de glicose são mostradas em (A) e as áreas sob as curvas são mostradas em (B). Grupos: SC, dieta padrão; HFHS, dieta rica em lipídios e sacarose; HFHS-Ro, HFHS tratado com rosiglitazona; HFHS-Fe, HFHS tratado com fenofibrato e; HFHS-Bz, HFHS tratado com bezafibrato. Os símbolos representam diferença estatística com: (*) SC, ( ) HFHS, ( ) HFHS-Ro e ( ) HFHS-Fe, P<0,05. 63
64 Coração A dieta HFHS não induziu hipertrofia cardíaca (Fig. 12). Entretanto, a relação coração:tíbia foi 43% maior no grupo HFHS-Ro comparado ao grupo SC (P<0,0001), indicando hipertrofia cardíaca. Os fibratos não apresentaram ação sobre este parâmetro. Figura 12. Hipertrofia cardíaca. Relação entre o peso do coração e o comprimento da tíbia nos diferentes grupos experimentais. Grupos: SC, dieta padrão; HFHS, dieta rica em lipídios e sacarose; HFHS-Ro, HFHS tratado com rosiglitazona; HFHS-Fe, HFHS tratado com fenofibrato e; HFHS-Bz, HFHS tratado com bezafibrato. Os símbolos representam diferença estatística com: (*) SC, ( ) HFHS e ( ) HFHS-Ro, P<0,05.
65 Gorduras Viscerais e Subcutânea e Diâmetro do Adipócito Houve aumento da massa das gorduras epididimal (+176%), retroperitoneal (+211%) e inguinal (+219%) nos animais HFHS não tratados comparado ao grupo SC (P<0,001) (Tabela 6). As gorduras epididimal e inguinal se apresentaram, respectivamente, 33% (P<0,05) e 75% (P<0,0001) maior no grupo HFHS-Ro comparado aos animais HFHS não tratados. Já nos grupos HFHS-Fe e HFHS-Bz elas apresentaram massa similar à do grupo SC. Apenas a rosiglitazona teve ação sobre a relação gordura Sub:Vis (+54% comparado ao grupo SC, P<0,001). A administração da dieta HFHS induziu a hipertrofia dos adipócitos das gorduras epididimal (+26%, P<0,001), retroperitoneal (+58%, P<0,0001) e inguinal (+54%, P<0,001) (Tabela 6 e Fig. 13). O tamanho do diâmetro dos adipócitos no grupo HFHS- Ro foi similar aos animais do grupo HFHS, enquanto os fibratos apresentaram adipócitos de tamanho similar ao grupo SC.
66 66 Tabela 6. Gorduras Viscerais e Subcutânea e Diâmetro do Adipócito SC HFHS HFHS-Ro HFHS-Fe HFHS-Bz Gordura, g Epididimal 0,49±0,04 1,35±0,13 * 1,80±0,19 * 0,52±0,04 0,61±0,05 Retroperitoneal 0,18±0,03 0,56±0,04 * 0,60±0,05 * 0,17±0,02 0,16±0,01 Inguinal 0,37±0,05 1,18±0,12 * 2,07±0,29 * 0,46±0,04 0,50±0,04 Sub:Vis 0,50±0,03 0,63±0,03 0,77±0,07 * 0,66±0,05 0,65±0,03 Adipócito, µm Epididimal 61,9±3,5 77,7±2,1 * 82,5±3,8 * 59,4±2,6 54,9±2,2 Retroperitoneal 59,8±4,7 94,4±3,8 * 89,2±1,7 * 60,6±2,0 56,8±2,9 Inguinal 43,1±3,5 66,4±4,3 * 62,6±3,4 * 47,4±3,9 48,3±1,4 Os dados são apresentados na forma de média ± EPM. Abreviações: SC, dieta padrão; HFHS, dieta rica em lipídios e sacarose; HFHS-Ro, HFHS tratado com rosiglitazona; HFHS-Fe, HFHS tratado com fenofibrato; HFHS-Bz, HFHS tratado com bezafibrato; Sub, gordura subcutânea e; Vis, gordura visceral. Os símbolos representam diferença estatística com: (*) SC, ( ) HFHS e ( ) HFHS-Ro, P<0,05.
67 Figura 13. Adipócitos na gordura retroperitoneal. Grupos: (a) dieta padrão, SC; (b) dieta rica em lipídios e sacarose, HFHS; (c) HFHS tratado com rosiglitazona; (d) HFHS tratado com fenofibrato e; (e) HFHS tratado com bezafibrato. Observe os adipócitos hipertrofiados em (b) e (c) e adipócitos com morfologia similar ao grupo SC em (d) e (e). 67
68 68 A correlação entre o diâmetro do adipócito e a glicemia e insulina de jejum, intolerância à glicose (ASC do TOTG) e resistência à insulina (HOMA-IR) é mostrada na Tabela 7. A glicemia de jejum não apresentou correlação com o diâmetro do adipócito. A insulina de jejum apresentou correlação com o diâmetro do adipócito em todos os depósitos de gordura, sendo esta correlação mais forte com os adipócitos da gordura retroperitoneal. A intolerância à glicose apresentou fraca correlação com o diâmetro do adipócito para todos os depósitos de gordura, enquanto a resistência à insulina apresentou maior correlação com o diâmetro dos adipócitos da gordura retroperitoneal (Figura 14).
69 69 Tabela 7. Regressão linear e correlação entre o diâmetro do adipócito de diferentes depósitos de gordura e parâmetros do metabolismo glicídico Slope Interseção em Y r P Glicose G. inguinal 0,8 ± 1,1 46 ± 11 0,15 NS G. epididimal 1,3 ± 1,2 54 ± 11 0,23 NS G. retroperitoneal 2,9 ± 1,6 44 ± 16 0,35 NS Insulina G. inguinal 15,3 ± 3,9 37 ± 5 0,64 <0,0001 G. epididimal 17,2 ± 4,1 48 ± 5 0,66 <0,0001 G. retroperitoneal 29,4 ± 4,6 40 ± 6 0,81 <0,0001 ASC do TOTG G. inguinal 0,05 ± 0,02 17 ± 14 0,50 <0,05 G. epididimal 0,06 ± 0,02 27 ± 15 0,51 <0,05 G. retroperitoneal 0,10 ± 0,03 6 ± 19 0,60 <0,01 HOMA-IR G. inguinal 0,77 ± 0,25 44 ± 4 0,53 <0,001 G. epididimal 0,84 ± 0,28 56 ± 4 0,53 <0,001 G. retroperitoneal 1,60 ± 0,31 51 ± 5 0,73 <0,00001 Os dados são apresentados na forma de média ± EPM. O slope representa o coeficiente angular da reta de regressão linear. Abreviações: r, coeficiente de correlação de Pearson; P, significância do coeficiente de correlação; NS, sem significância estatística; ASC, área sob a curva e; TOTG, teste de tolerância oral à glicose.
70 Figura 14. Regressão linear e correlação de Pearson entre o diâmetro do adipócito da gordura retroperitoneal e a resistência à insulina (avaliada pelo HOMA-IR). Abreviações: SC, dieta padrão; HFHS, dieta rica em lipídios e sacarose; HFHS-Ro, HFHS tratado com rosiglitazona; HFHS-Fe, HFHS tratado com fenofibrato e; HFHS-Bz, HFHS tratado com bezafibrato. 70
71 Expressão de Adiponectina no Tecido Adiposo A ingestão da dieta HFHS resultou na diminuição da imunocoloração para adiponectina no tecido adiposo inguinal e retroperitoneal, quando comparado à dieta controle SC (Tabela 8 e Fig. 15). Na gordura inguinal, todos os tratamentos mantiveram a imunocoloração para adiponectina semelhante ao grupo SC, enquanto na gordura retroperitoneal a rosiglitazona apresentou imunocoloração mais forte quando comparada aos fibratos. Tabela 8. Quantificação da imunocoloração para adiponectina no tecido adiposo (sistema semiquantitativo por escore) Grupos SC HFHS HFHS-Ro HFHS-Fe HFHS-Bz G. inguinal G. retroperitoneal Escores: (+) expressão fraca; (++), expressão moderada; (+++) expressa forte. Abreviações: G., gordura; SC, dieta padrão; HFHS, dieta rica em lipídios e sacarose; HFHS-Ro, HFHS tratado com rosiglitazona; HFHS-Fe, HFHS tratado com fenofibrato e; HFHS-Bz, HFHS tratado com bezafibrato.
72 Figura 15. Imunocoloração para adiponectina no tecido adiposo retroperitoneal (em marrom). (a) dieta padrão, SC; (b) dieta rica em lipídios e sacarose, HFHS; (c) HFHS tratado com rosiglitazona; (d), HFHS tratado com fenofibrato; (e) HFHS tratado com bezafibrato e; (f) controle negativo da reação. Comparado ao grupo SC (a), a imunocoloração para adiponectina está diminuída no grupo HFHS (b). Os grupos tratados (c, d, e) apresentaram imunocoloração mais forte do que o grupo HFHS (b). Entre os tratados, a rosiglitazona apresentou a maior intensidade de imunocoloração (c). 72
73 Massa do Pâncreas, Gordura pancreática e Ilhotas pancreáticas Os achados mais relevantes no que concerne a morfologia pancreática estão ilustrados na Fig. 16. O grupo HFHS não tratado apresentou aumento da massa pancreática (+28% comparado ao grupo SC, P<0,05) (Tabela 9), e esta alteração foi prevenida pelo tratamento com ambos os fibratos (-24% no HFHS-Fe, P<0,05 e -41% no HFHS-Bz, P<0,001, comparado ao grupo HFHS), mas não pela rosiglitazona. O diâmetro da ilhota aumentou após a ingestão da dieta HFHS (+38%, P<0,001), indicando hipertrofia da ilhota. Entre os medicamentos, apenas o bezafibrato inibiu este processo. Os ácinos nos grupos HFHS não tratado e HFHS-Fe apresentaram certo grau de degeneração (necrose da célula acinar) e infiltrado de células inflamatórias (Fig. 16). A dieta HFHS induziu o acúmulo de gordura no pâncreas nos espaços interlobular, intralobular e perilobular (+700% de gordura no grupo HFHS comparado ao grupo SC, P<0,001). A rosiglitazona exacerbou o acúmulo de gordura no pâncreas (+75% comparado ao HFHS, P<0,05), enquanto os fibratos não tiveram ação sobre este parâmetro.
74 74 Tabela 9. Massa Pancreática, Diâmetro da Ilhota e Gordura Pancreática Parâmetros Grupos SC HFHS HFHS-Ro HFHS-Fe HFHS-Bz Pâncreas, mg 246±17 315±13 * 271±17 240±12 187±18 Ilhota, μm 102±4 141±5 * 145±5 * 123±5 * 109±3 Gordura, % 0,2±0,1 1,6±0,4 * 2,8±0,2 * 1,2±0,3 1,0±0,2 Os dados são apresentados na forma de média ± EPM. Abreviações: SC, dieta padrão; HFHS, dieta rica em lipídios e sacarose; HFHS-Ro, HFHS tratado com rosiglitazona; HFHS-Fe, HFHS tratado com fenofibrato e; HFHS-Bz, HFHS tratado com bezafibrato. Os símbolos representam diferença estatística com: (*) SC, ( ) HFHS e ( ) HFHS-Ro, P<0,05.
75 Figura 16. Fotomicrografias do tecido pancreático mostrando os achados mais frequentes. (A) SC, tecido pancreático normal; (B) HFHS, alguns adipócitos podem ser vistos no pâncreas exócrino e ao redor dos vasos de grande calibre; (C) HFHS-Ro, grande infiltrado de adipócitos entre os lóbulos pancreáticos (interlobular) e no tecido exócrino (intralobular); (D) HFHS-Ro, adipócitos eram comumente encontrados no pâncreas exócrino; (E) SC, tecido pancreático normal; (F) HFHS, infiltrado inflamatório (setas cheia); (G) HFHS, início de degeneração acinar (seta vazia) e; (H) HFHS-Fe, grau avançado de degeneração acinar e deposição de matriz extracelular (seta vazia). Os cortes foram corados em HeE. As barras de calibração em (A) correspondem às figuras A-D e a barra em (B) corresponde às figuras E-H. Abreviações: SC, dieta padrão; HFHS, dieta rica em lipídios e sacarose; HFHS-Ro, HFHS tratado com rosiglitazona e; HFHS-Fe, HFHS tratado com fenofibrato.. 75
76 Expressão de Insulina, Glucagon, GLUT2, PPARα e PPARβ/δ nas Ilhotas Pancreáticas As ilhotas dos animais do grupo HFHS apresentaram densidade aumentada de imunocoloração para insulina (+134%, P<0,0001) e densidade diminuída de imunocoloração para o glucagon e GLUT2 (-60%, P<0,001 e -39%, P<0,05, respectivamente), quando comparado ao grupo SC (Tabela 10 e Fig. 17). A densidade de imunocoloração para o GLUT2 foi mantida nos níveis do grupo SC após o tratamento com a rosiglitazona, fenofibrato e bezafibrato. No grupo HFHS-Bz, a densidade de imunocoloração para insulina se manteve maior do que a do grupo SC (+85%, P<0,001), enquanto os grupos HFHS-Ro e HFHS-Fe não apresentaram diferenças com o mesmo. Apenas a rosiglitazona foi capaz de manter a densidade de imunocoloração para o glucagon semelhante ao grupo SC (+127% no grupo HFHS-Ro comparado ao grupo HFHS, P<0,001). A densidade de imunocoloração para o PPARα e PPARβ/δ não foi afetada pela dieta ou tratamento, com exceção do bezafibrato, que aumento a densidade de imunocoloração para o PPARβ/δ nas ilhotas pancreáticas dos animais do grupo HFHS-Bz (+56% quando comparado ao grupo SC, P<0,01).
77 Figura 17. Fotomicrografias de ilhotas pancreáticas imunocoradas com diferentes anticorpos. Cada coluna representa um grupo de estudo, e cada linha um anticorpo. Abreviações: SC, dieta padrão; HFHS, dieta rica em lipídios e sacarose; HFHS-Ro, HFHS tratado com rosiglitazona; HFHS-Fe, HFHS tratado com fenofibrato e; HFHS-Bz, HFHS tratado com bezafibrato. 77
78 78 Tabela 10. Quantificação da Densidade de Imunocoloração nas Ilhotas Pancreáticas Parâmetro Grupos SC HFHS HFHS-Ro HFHS-Fe HFHS-Bz Densidade/ilhota, % Insulina 8,5±1,0 19,9±1,2 * 7,5±0,8 10,1±0,8 15,7±1,5 * Glucagon 6,5±0,8 2,6±0,4 * 5,9±0,7 3,3±0,4 * 3,7±0,6 * GLUT2 7,6±0,5 4,6±0,4 * 7,6±0,7 8,0±0,6 9,8±0,9 PPARα 10,2±1,4 9,3±0,9 9,6±1,4 11,4±1,3 9,8±0,7 PPARβ/δ 19,7±2,1 27,3±2,3 27,1±1,8 25,1±1,8 30,7±2,0 * Os dados são apresentados na forma de média ± EPM. Abreviações: SC, dieta padrão; HFHS, dieta rica em lipídios e sacarose; HFHS-Ro, HFHS tratado com rosiglitazona; HFHS-Fe, HFHS tratado com fenofibrato e; HFHS-Bz, HFHS tratado com bezafibrato. Os símbolos representam diferença estatística com: (*) SC, ( ) HFHS, ( ) HFHS-Ro e ( ) HFHS-Bz, P<0,05.
79 79 DISCUSSÃO As principais alterações induzidas pela ingestão da dieta HFHS em camundongos C57BL/6 no presente estudo foram: hiperglicemia, intolerância à glicose, hiperinsulinemia, resistência à insulina, hipercolesterolemia, sobrepeso, hipertrofia de adipócitos e lesão pancreática. Algumas destas alterações estão presentes na síndrome metabólica humana como, por exemplo, as alterações do metabolismo glicídico e a massa corporal elevada. A lesão pancreática induzida pela dieta HFHS apresentou como características o aumento da massa pancreática, a infiltração de células adiposas (intra e interlobular) e inflamatórias e a degeneração acinar. O infiltrado de células adiposas caracteriza a doença pancreática gordurosa nãoalcóolica. Outro achado relevante foi a hipertrofia da ilhota pancreática, com concomitante aumento da imunocoloração para insulina e diminuição da imunocoloração para o GLUT2. O tratamento com bezafibrato apresentou maior ação sobre as alterações metabólicas induzidas pela dieta HFHS, uma vez que a melhora na intolerância à glicose e na sensibilidade à insulina foram mais pronunciadas nos animais HFHS-Bz, comparado aos demais tratamentos. Além disso, o bezafibrato apresentou um efeito antiobesidade, uma vez que ele diminuiu a massa corporal dos animais alimentados com a dieta HFHS, assim como impediu a hipertrofia dos adipócitos das gorduras inguinal, retroperitoneal e epididimal. O efeito antiobesidade do bezafibrato foi compartilhado apenas com o fenofibrato, porém este medicamento não agiu de forma satisfatória sobre a intolerância à glicose. Por outro lado, a rosiglitazona exacerbou o ganho de massa corporal induzido pela dieta HFHS e como consequência houve hipertrofia cardíaca. Em relação ao pâncreas, os achados mais relevantes são o acúmulo exacerbado de gordura intrapancreática pela rosiglitazona, sinais morfológicos de pancreatite nos animais tratados com fenofibrato, aumento da
80 80 imunocoloração para o PPARβ/δ nas células endócrinas pelo bezafibrato e um aumento da imunocoloração para o GLUT2 pelos três medicamentos. Tem sido mostrado que a rosiglitazona trata de forma eficiente a intolerância à glicose e a resistência à insulina. Esta ação é promovida pelo aumento da expressão do GLUT4 no tecido adiposo, redução da lipotoxicidade dos ácidos graxos livres sobre as células β pancreáticas, redução da secreção de TNF-α pelos adipócitos e aumento da secreção de adiponectina (Olefsky, 2000; Kramer et al., 2001; Kim et al., 2004). Por outro lado, a rosiglitazona pode induzir ganho de massa corporal pelo aumento da massa de tecido adiposo e edema periférico como resultado da retenção renal de sódio (Fuchtenbusch et al., 2000; Mudaliar et al., 2003). Assim, ainda é tema de debate se o ganho de peso induzido pela rosiglitazona em pacientes diabéticos com doença cardiovascular e/ou obesidade associados agravaria esta situação a longoprazo. Foi publicado que a rosiglitazona pode duplicar o risco de insuficiência cardíaca e aumentar em 42% o risco de infarto do miocárdio (Singh et al., 2007). Alguns trabalhos indicam que o tratamento com tiazolidinedionas pode causar hipertrofia cardíaca (Carley et al., 2004; Wu et al., 2004; Chang et al., 2008) e, ratificando este dado, este fenômeno também foi encontrado no presente estudo no grupo HFHS-Ro. Assim, a hipertrofia cardíaca induzida pela rosiglitazona poderia exercer efeitos adversos sobre a função cardiovascular durante o tratamento crônico de pacientes com DM2 ou hipertensão arterial sistêmica. Entretanto, o quanto a indução da hipertrofia cardíaca ocorre em humanos após o uso a longo-prazo de tiazolidinedionas ainda é esconhecido. Alterações nos níveis plasmáticos de LDL e HDL colesterol são fatores de risco importantes para o desenvolvimento da aterosclerose e da doença arterial coronariana (Gordon et al., 1977; Harper e Jacobson, 1999; Brewer, 2004), especialmente em pacientes com síndrome metabólica. O aumento do HDL colesterol é uma característica comum à maioria das linhagens de camundongos quando alimentadas com uma dieta hiperlipídica (Paigen, 1995), de forma contrária ao que acontece na síndrome metabólica humana, que é caracterizada por níveis reduzidos de HDL colesterol (Alberti et al., 2006). Nos humanos, os fibratos reduzem o triglicerídeo plasmático e aumentam o HDL (Fruchart et al., 2001; Fruchart e Duriez,
81 ), e apesar da rosiglitazona apresentar efeito similar, ela aumenta o LDL (Parulkar et al., 2001; Miyazaki et al., 2003; Deeg et al., 2007; Gastaldelli et al., 2007). Alterações no HDL cholesterol pela rosiglitazona não foram vistas no presente estudo, porém os fibratos diminuíram o HDL colesterol, efeito diferente do que é usualmente visto em humanos. O efeito oposto da ativação do PPARα sobre o HDL plasmático em camundongos comparado ao que acontece nos humanos é provavelmente devido a uma regulação diferenciada da apolipoproteína A-1, (APOA1), que forma o núcleo do HDL colesterol. Enquanto a ativação do PPARα aumenta os níveis plasmáticos e a expressão hepática do RNAm da APOA1 em humanos (Berthou et al., 1996), o efeito oposto é observado em roedores (Staels et al., 1992). Além disso, a rosiglitazona diminuiu o LDL colesterol, enquanto os fibratos aumentaram o mesmo, efeito que também provavelmente se deve a diferenças espécie-específicas na regulação das apolipoproteínas. As reduções do LDL e o HDL colesterol foram os principais responsáveis pelo baixo colesterol total nos animais tratados com rosiglitazona ou bezafibrato. A atividade biológica do adipócito muda conforme o seu armazenamento de lipídios aumenta. Comparado aos adipócitos pequenos, os adipócitos grandes são mais resistentes à ação da insulina, secretam mais citocinas inflamatórias e menos adiponectina (Le Lay et al., 2001; Sopasakis et al., 2004), e são mais frequentemente encontrados em pessoas com distúrbios metabólicos relacionados a obesidade (Krotkiewski et al., 1983; Weyer et al., 2000). A resistência à insulina e a inflamação, por sua vez, podem levar ao diabetes tipo II, doença cardiovascular, aumento do risco de câncer e outros problemas associados à obesidade (Powell, 2007). Assim, a composição celular do tecido adiposo é o principal determinante de sua atividade metabólica em resposta às alterações ambientais (Yang e Smith, 2007). A correlação positiva encontrada no presente estudo entre a sensibilidade à insulina (HOMA-IR) e o diâmetro o adipócito ratifica essa afirmação, uma vez que ela mostra que quanto maior o diâmetro do adipócito, maior a resistência à insulina. O presente estudo mostra prevalência de adipócitos pequenos após a terapia com fibratos em todos os depósitos de gordura analisados, o que pode explicar a melhora da resistência à insulina nos grupos HFHS-Fe e HFHS-Bz. A imunocoloração
82 82 aumentada para adiponectina também ratifica a menor resistência à insulina. As gorduras epididimal e inguinal apresentaram-se mais pesadas nos animais tratados com rosiglitazona comparado ao grupo HFHS não tratado, e este achado indica claramente que a rosiglitazona induziu a hiperplasia dos adipócitos nestes dois depósitos, uma vez que não foi vista diferença no diâmetro dos adipócitos entre estes dois grupos. A relação entre o peso das gorduras subcutânea e visceral indica um maior incremento de massa na gordura subcutânea pela rosiglitazona. Devido à expressão abundante de PPARγ no tecido adiposo, acredita-se que a melhora metabólica desempenhada pelos TZDs se deve principalmente a indução da adipogênese para recrutamento de adipócitos novos e pequenos, com maior capacidade de armazenamento de lipídios e secreção de adiponectina, e este fenômeno ocorreria principalmente no tecido adiposo subcutâneo. Entretanto, o ganho excessivo de massa adiposa após tratamentos a longo-prazo pode desempenhar consequências prejudiciais à saúde, particularmente em pessoas nas quais o sobrepeso ou obesidade já está instalado antes do tratamento (Yang e Smith, 2007). Os pesquisadores estão agora prestando atenção na localização da gordura ao invés da obesidade como um todo, uma vez que os depósitos de gordura visceral e subcutâneo possuem funções distintas. Os depósitos viscerais liberam citocinas as quais exercem efeito principal no metabolismo hepático de carboidratos e lipídios e estimulam a secreção hepática de proteínas inflamatórias (Baumann e Gauldie, 1990; Fernandez-Real et al., 2001). As citocinas liberadas pelos depósitos de gordura subcutâneos afetam principalmente o desenvolvimento e função local do adipócito (Sopasakis et al., 2004). A expressão e secreção de leptina são maiores na gordura subcutânea, enquanto, em contraste, a gordura visceral secreta mais adiponectina e é mais sensível a captação da glicose estimulada pela insulina (Tritos e Mantzoros, 1997; Virtanen et al., 2002; Lundgren et al., 2004). No presente estudo, a correlação entre o diâmetro do adipócito e o HOMA-IR foi maior na gordura retroperitoneal comparado às gorduras epididimal e inguinal, sugerindo que os depósitos de gordura podem desempenhar papéis diferentes na sensibilidade à insulina. Morfologicamente, uma estrutura em forma de coroa, representada por células gigantes multinucleadas (resultante da agregação de macrófagos) ao redor dos adipócitos indica a morte do
83 83 adipócito (Cinti et al., 2005), e esta estrutura foi vista com frequência apenas na gordura retroperitoneal dos animais tratados com rosiglitazona. Além disso, a imunocoloração para adiponectina foi maior na gordura retroperitoneal comparada à inguinal após o tratamento com rosiglitazona. Estas ações depósito-específicas (gordura retroperitoneal) reforçam a idéia de funções diferentes para cada tipo depósito de gordura. Os fibratos impediram o armazenamento de energia na forma de gordura independente do consumo de energia, uma vez que a ingestão diária de energia nos animais de ambos os grupos HFHS-Fe e HFHS-Bz não foi diferente do grupo HFHS não tratado. É sabido que o fenofibrato pode causar hipofagia (Carmona et al., 2005), mas isto não ocorreu no presente estudo. Assim, a menor massa corporal e adiposa vista no grupo HFHS-Fe não foi resultado de uma ingestão alimentar reduzida. Provavelmente, os fibratos aumentaram o gasto energético, resultando assim na ausência de ganho de massa corporal. Uma vez que o aumento da oxidação de ácidos graxos é o principal efeito do fenofibrato, a diminuição nos processos de captação e síntese de ácidos graxos, associado com a mobilização dos lipídios no tecido adiposo (Ferreira et al., 2006) pode explicar a parada no ganho de massa corporal e adiposidade por este medicamento. A ativação do PPARβ/δ pelo bezafibrato também pode aumentar a capacidade de oxidação de ácidos graxos no músculo esquelético, a qual é acompanhada pela redistribuição do fluxo de ácidos graxos do tecido adiposo em direção ao músculo esquelético (Wang et al., 2003; Fredenrich e Grimaldi, 2005). O somatório da ativação do PPARα e PPARβ/δ pelo bezafibrato poderia talvez ser a razão da perda de peso nos camundongos tratados com bezafibrato. Na maioria dos trabalhos experimentais, os fibratos são administrados na ração. A concentração do bezafibrato costuma variar entre 0,2 e 0,5% (p/p) (Peters et al., 2003; Kjorholt et al., 2005), enquanto a concentração do fenofibrato varia entre 0,1 e 0,5% (p/p) (Koh et al., 2003; Choi et al., 2005). É provável que a diferença na resposta da massa corporal entre os fibratos no presente estudo não seja devida a quantidade de medicamento administrada, mas sim devido a uma ativação diferencial dos isotipos do PPAR por estes medicamentos, uma vez que as quantidades utilizadas no presente estudo estão dentro do intervalo utilizado na maioria dos trabalhos.
84 84 Em relação ao pâncreas, o acúmulo ectópico de gordura no grupo HFHS não tratado se localizou principalmente nos espaços interlobular (ao redor dos vasos de maior calibre e ductos) e perilobular (na periferia do lóbulo pancreático). Os animais tratados apresentaram este mesmo padrão, com exceção da rosiglitazona, que também apresentou um aumento marcante na infiltração de células adiposas no espaço intralobular (entre os ácinos exócrinos). A exacerbação do acúmulo de gordura no pâncreas dos animais HFHS-Ro é provavelmente resultado da maior massa adiposa encontrada nestes animais comparado ao grupo HFHS não tratado, em lugar de uma ação específica do medicamento sobre o tecido pancreático. O bezafibrato induziu perda de peso nos animais do grupo HFHS-Bz, e apesar de não apresentar diferença estatística, o acúmulo de gordura em seu pâncreas foi ligeiramente menor do que no grupo HFHS não tratado, reforçando mais uma vez uma possível correlação positiva entre a massa adiposa corporal e a infiltração pancreática de gordura. A presença de pequenas quantidades de gordura no pâncreas é comum em pessoas obesas ou em idade avançada (Walters, 1966; Haaga e Alfidi, 1977; Itai et al., 1995), ou em camundongos alimentados com dieta hiperlipídica (Fraulob et al., 2010; Nascimento et al., 2010) e esta condição é revertida após a perda de peso (Patel et al., 1980). Entretanto, o acúmulo excessivo de gordura no pâncreas pode ter significância patológica, uma vez que ele pode deprimir a função exócrina substancialmente, resultando em má-absorção. Não foram encontradas alterações na lipase e amilase sérica entre os grupos estudados, sugerindo que a função exócrina ainda estava preservada. Entretanto, os animais HFHS e HFHS-Fe não tratados já apresentavam sinais microscópicos de lesão acinar compatível com pancreatite. Apesar dos fibratos poderem causar pancreatite como efeito colateral (Sgro e Escousse, 1991; Brown, 2007), apenas os animais tratados com fenofibrato apresentaram certo grau de lesão acinar. Não existem trabalhos que analisem o papel in vivo das células adiposas intrapancreáticas na função endócrina e/ou exócrina do pâncreas. Entretanto, é sabido que sob condições de estresse oxidativo, citocinas secretadas pelos adipócitos são liberadas localmente e levam a um processo inflamatório com disfunção do órgão
85 85 (Mathur et al., 2007), e camundongos obesos tem significativamente mais TNF-α e IL- 1β em seu pâncreas (Pitt, 2007). Adicionalmente, o próprio ácido graxo livre circulante em níveis elevados está implicado na disfunção da célula β, causando um aumento da secreção basal de insulina e prejuízo na secreção de insulina estimulada pela glicose (Grill e Bjorklund, 2000; Yoshikawa et al., 2001b; Prentki et al., 2002). A rosiglitazona é capaz de melhorar tanto a secreção basal de insulina quanto a secreção de insulina estimulada pela glicose em ilhotas cultivadas em meio contendo palmitato (Tian et al., 2006). Entretanto, apesar desse efeito protetor, é possível que as citocinas inflamatórias liberadas pelas células adiposas intrapancreaáticas in vivo atenuem a extensão dos efeitos benéficos da rosiglitazona sobre a função da célula β. Os isotipos do PPAR são expressos nas ilhotas pancreáticas de roedores e humanos, onde o PPARβ/δ apresenta a maior expressão, seguido do PPARα e PPARγ (Braissant et al., 1996). Entretanto, o papel de cada isotipo na regulação da função das células endócrinas pancreáticas ainda não é completamente entendido. No presente estudo foi visto uma fraca expressão do PPARα no grupo SC, a qual não foi alterada no grupo que recebeu a dieta HFHS. Esta falta de ação sobre a expressão do PPARα está em acordo com um trabalho prévio que mostrou que ilhotas pancreáticas em cultura com palmitato por 8 horas apresentam aumento da expressão de RNAm para o PPARα, mas após longos períodos de incubação a expressão do PPARα, assim como do RNAm para o GLUT2, são inibidos (Yoshikawa et al., 2001b). De forma interessante, no presente estudo o tratamento com ambos os fibratos não aumentou a densidade de coloração do PPARα na ilhota pancreática, apesar de os fibratos serem conhecidos por sua capacidade de ativar a expressão do RNAm e proteína do PPARα (Krey et al., 1997; Yoshikawa et al., 2001a; Inoue et al., 2002). Camundongos PPARα -/- ob/ob desenvolvem uma hiperglicemia severa e dependente da idade, além de disfunção da célula β caracterizada pela redução da área média da ilhota pancreática e prejuízo da secreção de insulina estimulada pela glicose in vivo e in vitro (Lalloyer et al., 2006), sugerindo um papel para o PPARα na função normal das células β. Por outro lado, Yoshikawa e col. mostraram que a exposição da ilhota pancreática de rato ao bezafibrato diminui a secreção de insulina estimulada pela glicose (Yoshikawa et al., 2001a). No presente estudo, o aumento da densidade de imunocoloração para
86 86 insulina na ilhota pancreática do grupo HFHS-Bz mostra que estes animais sintetizam bastante insulina, mas talvez aja alguma alteração em sua secreção, uma vez que a insulina sérica destes animais é baixa. O PPARβ/δ apresentou expressão moderada no grupo SC, e sua expressão foi afetada apenas pelo tratamento com bezafibrato. Trabalhos recentes têm mostrado que o bezafibrato pode atuar como agonista dos três isotipos do PPAR (Krey et al., 1997; Inoue et al., 2002), e no presente estudo foi demonstrado pela primeira vez que o bezafibrato ativa a expressão do PPARβ/δ nas células endócrinas da ilhota pancreática. Higashiyama e col. mostraram que a expressão do PPARβ/δ nas ilhotas pancreáticas de camundongos é restrita ao citoplasma das células δ (Higashiyama et al., 2007), porém em outro estudo, Braissant e col. mostraram um padrão de imunocoloração do PPARβ/δ em ilhotas de rato semelhante ao visto no presente estudo (Braissant et al., 1996). No presente estudo não foi feito a identificação do tipo celular PPARβ/δ-positivo como feito por Higashiyama e col. (Higashiyama et al., 2007), mas pode-se afirmar, baseando-se no padrão de imunocoloração, que as células β expressam a proteína PPARβ/δ. O papel do PPARβ/δ nas células endócrinas da ilhota pancreática ainda é desconhecido e estudos adicionais são necessários. No presente estudo, apenas o bezafibrato foi capaz de prevenir a hipertrofia das ilhotas pancreáticas, e outros trabalhos têm mostrado que ele é capaz de inibir a inflamação pancreática, prevenir a degeneração pancreática (Jia e Otsuki, 2003) e suprimir a expressão da α-actina de músculo liso (Jia et al., 2004), preservando assim a morfologia do tecido pancreático. O quanto estes efeitos são devidos à ativação dos diferentes isotipos do PPAR ou são apenas resultado da melhora do perfil metabólico sistêmico ainda permanece a ser elucidado. As células endócrinas da ilhota pancreática expressam normalmente tanto o RNAm quanto a proteína do PPARγ (Dubois et al., 2000). Adicionalmente, os ácidos graxos livres inibem a expressão do RNAm do PPARγ2 em ilhotas pancreáticas in vivo, e esse efeito é inibido pela rosiglitazona (Lupi et al., 2004), assim a ativação do PPARγ nas células endócrinas pancreáticas pode explicar parcialmente a conexão entre a rosiglitazona e a melhora na homeostase da glicose. Apesar de o PPARγ ser expresso nas células BRIN-BD11 (uma linhagem clonal de células β), estas células são
87 87 relativamente resistentes à ativação pela rosiglitazona quando esta é administrada em concentrações terapêuticas (Welters et al., 2004), assim é difícil dizer se a melhora na função da célula β reportada após o tratamento está relacionada a ação direta da rosiglitazona sobre a função da célula β ou um efeito secundário da ativação do PPARγ em outros tecidos. Adicionalmente, a deleção seletiva do PPARγ nas células β de camundongos não afeta a homeostase da glicose (Rosen et al., 2003), assim a ação antidiabética da rosiglitazona talvez independa da modulação da expressão do PPARγ na célula β. O GLUT2 e a glicoquinase trabalham como sensores de glicose para a secreção de insulina estimulada pela glicose na célula β em condições fisiológicas. Em células β de diabéticos, a expressão do RNAm para o GLUT2 está diminuída, e como consequência a secreção basal de insulina está aumentada (Kim e Ahn, 2004). No presente estudo, a dieta HFHS reduziu a densidade de imunocoloração para GLUT2 na ilhota, enquanto todos os tratamentos mantiveram este parâmetro semelhante ao grupo SC, sugerindo indiretamente que estes medicamentos melhoraram a função da célula β. Sun e col. mostraram que a ativação do PPARα nas células β de ratos pelo fenofibrato aumenta a expressão do RNAm para o GLUT2 (Sun et al., 2008). Adicionalmente, há melhora da secreção de insulina estimulada pela glicose que antes estava diminuída por exposição à ácidos graxos em células isoladas de ilhotas de rato e em células INS-1 (Sun et al., 2008), efeitos também compartilhados pela rosiglitazona (Lalloyer et al., 2006). Por outro lado, Yoshikawa e col. mostraram que a exposição de ilhotas pancreáticas de rato ao bezafibrato diminui a secreção de insulina dependente de glicose (Yoshikawa et al., 2001a). Quando o bezafibrato é adicionado à terapia com pioglitazona porém, há aumento da secreção de insulina estimulada pela glicose quando comparado ao tratamento com pioglitazona isolado, apesar de não haver diferença identificável na imunocoloração para o GLUT2 entre estes dois grupos (Yajima et al., 2003).
88 Considerações finais O tratamento combinado com agonistas PPARα e PPARγ parece promissor no combate à resistência à insulina, dislipidemia aterogênica e obesidade em pacientes com síndrome metabólica. Além disso, a adição da propriedade agonista PPARβ/δ poderia prevenir o desenvolvimento do sobrepeso que tipicamente acompanha a administração de agonistas PPARγ puro como a rosiglitazona, ou até mesmo combater a obesidade. Estudos adicionais sobre a biologia dos PPARs irão aumentar a nossa compreensão com relação a sua significância a nível fisiológicoe farmacológicas, e fornecerão conhecimento adicional para o desenvolvimento de ligantes PPAR superiores e com melhores índices terapêuticos. O bezafibrato é candidato potencial como molde para o desenvolvimento de pan-agonistas PPAR mais eficientes, e que não apresentem os efeitos adversos vistos com os duploagonitas PPAR muraglitazar e tesaglitazar.
89 89 CONCLUSÃO O bezafibrato apresenta um efeito mais amplo sobre as alterações metabólicas, morfológicas e biométricas decorrentes da ingestão de dieta rica em lipídios e sacarose em camundongos C57BL/6, sugerindo que a inibição dos três isotipos do PPAR seja melhor do que a inibição de apenas um isotipo. Além disso, ele também é capaz de aumentar a imunocoloração para o PPARβ/δ nas células endócrinas pancreáticas. A rosiglitazona exacerba o ganho de massa corporal, a infiltração de gordura no pâncreas e induz hipertrofia cardíaca, o que deve ser levado em conta, na medicina, quando da prescrição deste medicamento a pacientes obesos.
90 90 Referências Clinical Guidelines on the Identification, Evaluation, and Treatment of Overweight and Obesity in Adults--The Evidence Report. National Institutes of Health. Obes Res 1998; 6 Suppl 2:51S-209S. Executive Summary of The Third Report of The National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, And Treatment of High Blood Cholesterol In Adults (Adult Treatment Panel III). Jama 2001; 285: Abel ED, Peroni O, Kim JK, Kim YB, Boss O, Hadro E, Minnemann T, Shulman GI, Kahn BB. Adiposeselective targeting of the GLUT4 gene impairs insulin action in muscle and liver. Nature 2001; 409: Ahren B, Gudbjartsson T, Al-Amin AN, Martensson H, Myrsen-Axcrona U, Karlsson S, Mulder H, Sundler F. Islet perturbations in rats fed a high-fat diet. Pancreas 1999; 18: Aiston S, Trinh KY, Lange AJ, Newgard CB, Agius L. Glucose-6-phosphatase overexpression lowers glucose 6-phosphate and inhibits glycogen synthesis and glycolysis in hepatocytes without affecting glucokinase translocation. Evidence against feedback inhibition of glucokinase. J Biol Chem 1999; 274: Alberti KG, Zimmet P, Shaw J. Metabolic syndrome--a new world-wide definition. A Consensus Statement from the International Diabetes Federation. Diabet Med 2006; 23: Alexander CM, Landsman PB, Teutsch SM, Haffner SM. NCEP-defined metabolic syndrome, diabetes, and prevalence of coronary heart disease among NHANES III participants age 50 years and older. Diabetes 2003; 52: Arkan MC, Hevener AL, Greten FR, Maeda S, Li ZW, Long JM, Wynshaw-Boris A, Poli G, Olefsky J, Karin M. IKK-beta links inflammation to obesity-induced insulin resistance. Nat Med 2005; 11: Bajaj M, Suraamornkul S, Pratipanawatr T, Hardies LJ, Pratipanawatr W, Glass L, Cersosimo E, Miyazaki Y, DeFronzo RA. Pioglitazone reduces hepatic fat content and augments splanchnic glucose uptake in patients with type 2 diabetes. Diabetes 2003; 52: Balkau B, Charles MA. Comment on the provisional report from the WHO consultation. European Group for the Study of Insulin Resistance (EGIR). Diabet Med 1999; 16: Banerjee RR, Rangwala SM, Shapiro JS, Rich AS, Rhoades B, Qi Y, Wang J, Rajala MW, Pocai A, Scherer PE, Steppan CM, Ahima RS, Obici S, Rossetti L, Lazar MA. Regulation of fasted blood glucose by resistin. Science 2004; 303: Barak Y, Liao D, He W, Ong ES, Nelson MC, Olefsky JM, Boland R, Evans RM. Effects of peroxisome proliferator-activated receptor delta on placentation, adiposity, and colorectal cancer. Proc Natl Acad Sci U S A 2002; 99: Bastie C, Holst D, Gaillard D, Jehl-Pietri C, Grimaldi PA. Expression of peroxisome proliferatoractivated receptor PPARdelta promotes induction of PPARgamma and adipocyte differentiation in 3T3C2 fibroblasts. J Biol Chem 1999; 274: Baumann H, Gauldie J. Regulation of hepatic acute phase plasma protein genes by hepatocyte stimulating factors and other mediators of inflammation. Mol Biol Med 1990; 7:
91 91 Bays H, Mandarino L, DeFronzo RA. Role of the adipocyte, free fatty acids, and ectopic fat in pathogenesis of type 2 diabetes mellitus: peroxisomal proliferator-activated receptor agonists provide a rational therapeutic approach. J Clin Endocrinol Metab 2004; 89: Berg AH, Combs TP, Du X, Brownlee M, Scherer PE. The adipocyte-secreted protein Acrp30 enhances hepatic insulin action. Nat Med 2001; 7: Berger JP, Akiyama TE, Meinke PT. PPARs: therapeutic targets for metabolic disease. Trends Pharmacol Sci 2005; 26: Berthou L, Duverger N, Emmanuel F, Langouet S, Auwerx J, Guillouzo A, Fruchart JC, Rubin E, Denefle P, Staels B, Branellec D. Opposite regulation of human versus mouse apolipoprotein A- I by fibrates in human apolipoprotein A-I transgenic mice. J Clin Invest 1996; 97: Betteridge DJ. LDL heterogeneity: implications for atherogenicity in insulin resistance and NIDDM. Diabetologia 1997; 40 Suppl 2:S Bishop-Bailey D. Peroxisome proliferator-activated receptors in the cardiovascular system. Br J Pharmacol 2000; 129: Bloomgarden ZT. Definitions of the insulin resistance syndrome: the 1st World Congress on the Insulin Resistance Syndrome. Diabetes Care 2004; 27: Boden G. Role of fatty acids in the pathogenesis of insulin resistance and NIDDM. Diabetes 1997; 46:3-10. Bouchard C. Genetics and the metabolic syndrome. Int J Obes Relat Metab Disord 1995; 19 Suppl 1:S Bouchard C, Despres JP, Mauriege P. Genetic and nongenetic determinants of regional fat distribution. Endocr Rev 1993; 14: Braissant O, Foufelle F, Scotto C, Dauca M, Wahli W. Differential expression of peroxisome proliferator-activated receptors (PPARs): tissue distribution of PPAR-alpha, -beta, and -gamma in the adult rat. Endocrinology 1996; 137: Bratanova-Tochkova TK, Cheng H, Daniel S, Gunawardana S, Liu YJ, Mulvaney-Musa J, Schermerhorn T, Straub SG, Yajima H, Sharp GW. Triggering and augmentation mechanisms, granule pools, and biphasic insulin secretion. Diabetes 2002; 51 Suppl 1:S Brewer HB, Jr. Increasing HDL Cholesterol Levels. N Engl J Med 2004; 350: Brown WV. Expert commentary: the safety of fibrates in lipid-lowering therapy. Am J Cardiol 2007; 99:19C-21C. Bruning JC, Michael MD, Winnay JN, Hayashi T, Horsch D, Accili D, Goodyear LJ, Kahn CR. A muscle-specific insulin receptor knockout exhibits features of the metabolic syndrome of NIDDM without altering glucose tolerance. Mol Cell 1998; 2: Buettner R, Parhofer KG, Woenckhaus M, Wrede CE, Kunz-Schughart LA, Scholmerich J, Bollheimer LC. Defining high-fat-diet rat models: metabolic and molecular effects of different fat types. J Mol Endocrinol 2006; 36: Buettner R, Scholmerich J, Bollheimer LC. High-fat diets: modeling the metabolic disorders of human obesity in rodents. Obesity (Silver Spring) 2007; 15: Burcelin R, del Carmen Munoz M, Guillam MT, Thorens B. Liver hyperplasia and paradoxical regulation of glycogen metabolism and glucose-sensitive gene expression in GLUT2-null hepatocytes. Further evidence for the existence of a membrane-based glucose release pathway. J Biol Chem 2000; 275:
92 92 Cancello R, Clement K. Is obesity an inflammatory illness? Role of low-grade inflammation and macrophage infiltration in human white adipose tissue. Bjog 2006; 113: Carley AN, Semeniuk LM, Shimoni Y, Aasum E, Larsen TS, Berger JP, Severson DL. Treatment of type 2 diabetic db/db mice with a novel PPARgamma agonist improves cardiac metabolism but not contractile function. Am J Physiol Endocrinol Metab 2004; 286:E Carmona MC, Louche K, Nibbelink M, Prunet B, Bross A, Desbazeille M, Dacquet C, Renard P, Casteilla L, Penicaud L. Fenofibrate prevents Rosiglitazone-induced body weight gain in ob/ob mice. Int J Obes (Lond) 2005; 29: Caro JF, Kolaczynski JW, Nyce MR, Ohannesian JP, Opentanova I, Goldman WH, Lynn RB, Zhang PL, Sinha MK, Considine RV. Decreased cerebrospinal-fluid/serum leptin ratio in obesity: a possible mechanism for leptin resistance. Lancet 1996; 348: Catalan V, Gomez-Ambrosi J, Rodriguez A, Salvador J, Fruhbeck G. Adipokines in the treatment of diabetes mellitus and obesity. Expert Opin Pharmacother 2009; 10: Cerf ME. High fat diet modulation of glucose sensing in the beta-cell. Med Sci Monit 2007; 13:RA Chang CH, McNamara LA, Wu MS, Muise ES, Tan Y, Wood HB, Meinke PT, Thompson JR, Doebber TW, Berger JP, McCann ME. A novel selective peroxisome proliferator-activator receptorgamma modulator-sppargammam5 improves insulin sensitivity with diminished adverse cardiovascular effects. Eur J Pharmacol 2008; 584: Chang S, Graham B, Yakubu F, Lin D, Peters JC, Hill JO. Metabolic differences between obesityprone and obesity-resistant rats. Am J Physiol 1990; 259:R Chawla A, Schwarz EJ, Dimaculangan DD, Lazar MA. Peroxisome proliferator-activated receptor (PPAR) gamma: adipose-predominant expression and induction early in adipocyte differentiation. Endocrinology 1994; 135: Chinetti G, Griglio S, Antonucci M, Torra IP, Delerive P, Majd Z, Fruchart JC, Chapman J, Najib J, Staels B. Activation of proliferator-activated receptors alpha and gamma induces apoptosis of human monocyte-derived macrophages. J Biol Chem 1998; 273: Choi KC, Ryu OH, Lee KW, Kim HY, Seo JA, Kim SG, Kim NH, Choi DS, Baik SH, Choi KM. Effect of PPAR-alpha and -gamma agonist on the expression of visfatin, adiponectin, and TNF-alpha in visceral fat of OLETF rats. Biochem Biophys Res Commun 2005; 336: Chou CJ, Haluzik M, Gregory C, Dietz KR, Vinson C, Gavrilova O, Reitman ML. WY14,643, a peroxisome proliferator-activated receptor alpha (PPARalpha ) agonist, improves hepatic and muscle steatosis and reverses insulin resistance in lipoatrophic A-ZIP/F-1 mice. J Biol Chem 2002; 277: Chowdhury P, Nishikawa M, Blevins GW, Jr., Rayford PL. Response of rat exocrine pancreas to high-fat and high-carbohydrate diets. Proc Soc Exp Biol Med 2000; 223: Cinti S, Mitchell G, Barbatelli G, Murano I, Ceresi E, Faloia E, Wang S, Fortier M, Greenberg AS, Obin MS. Adipocyte death defines macrophage localization and function in adipose tissue of obese mice and humans. J Lipid Res 2005; 46: Cnop M, Hannaert JC, Hoorens A, Eizirik DL, Pipeleers DG. Inverse relationship between cytotoxicity of free fatty acids in pancreatic islet cells and cellular triglyceride accumulation. Diabetes 2001; 50: Committee NRN. A unified nomenclature system for the nuclear receptor superfamily. Cell 1999; 97:
93 93 Correia ML, Haynes WG, Rahmouni K, Morgan DA, Sivitz WI, Mark AL. The concept of selective leptin resistance: evidence from agouti yellow obese mice. Diabetes 2002; 51: de Moura RF, Ribeiro C, de Oliveira JA, Stevanato E, de Mello MA. Metabolic syndrome signs in Wistar rats submitted to different high-fructose ingestion protocols. Br J Nutr 2008:1-7. Deeg MA, Buse JB, Goldberg RB, Kendall DM, Zagar AJ, Jacober SJ, Khan MA, Perez AT, Tan MH. Pioglitazone and rosiglitazone have different effects on serum lipoprotein particle concentrations and sizes in patients with type 2 diabetes and dyslipidemia. Diabetes Care 2007; 30: Despres JP, Lemieux I. Abdominal obesity and metabolic syndrome. Nature 2006; 444: Devchand PR, Keller H, Peters JM, Vazquez M, Gonzalez FJ, Wahli W. The PPARalpha-leukotriene B4 pathway to inflammation control. Nature 1996; 384: Di-Poi N, Tan NS, Michalik L, Wahli W, Desvergne B. Antiapoptotic role of PPARbeta in keratinocytes via transcriptional control of the Akt1 signaling pathway. Mol Cell 2002; 10: Diep QN, Touyz RM, Schiffrin EL. Docosahexaenoic acid, a peroxisome proliferator-activated receptor-alpha ligand, induces apoptosis in vascular smooth muscle cells by stimulation of p38 mitogen-activated protein kinase. Hypertension 2000; 36: DiRenzo J, Soderstrom M, Kurokawa R, Ogliastro MH, Ricote M, Ingrey S, Horlein A, Rosenfeld MG, Glass CK. Peroxisome proliferator-activated receptors and retinoic acid receptors differentially control the interactions of retinoid X receptor heterodimers with ligands, coactivators, and corepressors. Mol Cell Biol 1997; 17: Donahue RP, Abbott RD, Bloom E, Reed DM, Yano K. Central obesity and coronary heart disease in men. Lancet 1987; 1: Donath MY, Gross DJ, Cerasi E, Kaiser N. Hyperglycemia-induced beta-cell apoptosis in pancreatic islets of Psammomys obesus during development of diabetes. Diabetes 1999; 48: Dowell P, Ishmael JE, Avram D, Peterson VJ, Nevrivy DJ, Leid M. Identification of nuclear receptor corepressor as a peroxisome proliferator-activated receptor alpha interacting protein. J Biol Chem 1999; 274: Dreyer C, Krey G, Keller H, Givel F, Helftenbein G, Wahli W. Control of the peroxisomal betaoxidation pathway by a novel family of nuclear hormone receptors. Cell 1992; 68: Dubois M, Pattou F, Kerr-Conte J, Gmyr V, Vandewalle B, Desreumaux P, Auwerx J, Schoonjans K, Lefebvre J. Expression of peroxisome proliferator-activated receptor gamma (PPARgamma) in normal human pancreatic islet cells. Diabetologia 2000; 43: Ducimetiere P, Richard J, Cambien F. The pattern of subcutaneous fat distribution in middle-aged men and the risk of coronary heart disease: the Paris Prospective Study. Int J Obes 1986; 10: Fagerberg B, Edwards S, Halmos T, Lopatynski J, Schuster H, Stender S, Stoa-Birketvedt G, Tonstad S, Halldorsdottir S, Gause-Nilsson I. Tesaglitazar, a novel dual peroxisome proliferatoractivated receptor alpha/gamma agonist, dose-dependently improves the metabolic abnormalities associated with insulin resistance in a non-diabetic population. Diabetologia 2005; 48: Fajas L, Auboeuf D, Raspe E, Schoonjans K, Lefebvre AM, Saladin R, Najib J, Laville M, Fruchart JC, Deeb S, Vidal-Puig A, Flier J, Briggs MR, Staels B, Vidal H, Auwerx J. The organization, promoter analysis, and expression of the human PPARgamma gene. J Biol Chem 1997; 272:
94 94 Fajas L, Fruchart JC, Auwerx J. PPARgamma3 mrna: a distinct PPARgamma mrna subtype transcribed from an independent promoter. FEBS Lett 1998; 438: Feige JN, Gelman L, Tudor C, Engelborghs Y, Wahli W, Desvergne B. Fluorescence imaging reveals the nuclear behavior of peroxisome proliferator-activated receptor/retinoid X receptor heterodimers in the absence and presence of ligand. J Biol Chem 2005; 280: Fernandez-Real JM, Vayreda M, Richart C, Gutierrez C, Broch M, Vendrell J, Ricart W. Circulating interleukin 6 levels, blood pressure, and insulin sensitivity in apparently healthy men and women. J Clin Endocrinol Metab 2001; 86: Ferre T, Riu E, Bosch F, Valera A. Evidence from transgenic mice that glucokinase is rate limiting for glucose utilization in the liver. Faseb J 1996; 10: Ferreira AVM, Parreira GG, Green A, Botion LM. Effects of fenofibrate on lipid metabolism in adipose tissue of rats. Metabolism 2006; 55: Fraulob JC, Ogg-Diamantino R, Fernandes-Santos C, Aguila MB, Mandarim de Lacerda CA. A mouse model of metabolic syndrome: insulin resistance, fatty liver and non-alcoholic fatty pancreas disease (NAFPD) in C57BL/6 mice fed a high fat diet. J Clin Biochem Nutr 2010; 46:1-12. Frayn KN. Adipose tissue as a buffer for daily lipid flux. Diabetologia 2002; 45: Fredenrich A, Grimaldi PA. PPAR delta: an uncompletely known nuclear receptor. Diabetes Metab 2005; 31: Fried SK, Bunkin DA, Greenberg AS. Omental and subcutaneous adipose tissues of obese subjects release interleukin-6: depot difference and regulation by glucocorticoid. J Clin Endocrinol Metab 1998; 83: Friedman JM. The function of leptin in nutrition, weight, and physiology. Nutr Rev 2002; 60:S1-14; discussion S68-84, Friedwald WT, Levy RS, Fredrickson DS. Estimation of the concentration of low-density lipoprotein cholesterol in plasma without use of the preparative ultracentrifuge. Clin Chem 1972; 18: Fruchart JC, Duriez P. Mode of action of fibrates in the regulation of triglyceride and HDLcholesterol metabolism. Drugs Today (Barc) 2006; 42: Fruchart JC, Staels B, Duriez P. The role of fibric acids in atherosclerosis. Curr Atheroscler Rep 2001; 3: Fuchtenbusch M, Standl E, Schatz H. Clinical efficacy of new thiazolidinediones and glinides in the treatment of type 2 diabetes mellitus. Exp Clin Endocrinol Diabetes 2000; 108: Gajda AM, Pellizzon MA, Matthew RR, Ulman EA Diet-Induced Metabolic Syndrome in Rodent Models. In: Animal Lab News. Gallou-Kabani C, Vige A, Gross MS, Rabes JP, Boileau C, Larue-Achagiotis C, Tome D, Jais JP, Junien C. C57BL/6J and A/J mice fed a high-fat diet delineate components of metabolic syndrome. Obesity (Silver Spring) 2007; 15: Gastaldelli A, Ferrannini E, Miyazaki Y, Matsuda M, Mari A, DeFronzo RA. Thiazolidinediones improve beta-cell function in type 2 diabetic patients. Am J Physiol Endocrinol Metab 2007; 292:E Gavrilova O, Marcus-Samuels B, Graham D, Kim JK, Shulman GI, Castle AL, Vinson C, Eckhaus M, Reitman ML. Surgical implantation of adipose tissue reverses diabetes in lipoatrophic mice. J Clin Invest 2000; 105:
95 95 Ghibaudi L, Cook J, Farley C, van Heek M, Hwa JJ. Fat intake affects adiposity, comorbidity factors, and energy metabolism of sprague-dawley rats. Obes Res 2002; 10: Girard J, Ferre P, Foufelle F. Mechanisms by which carbohydrates regulate expression of genes for glycolytic and lipogenic enzymes. Annu Rev Nutr 1997; 17: Gleason CE, Gonzalez M, Harmon JS, Robertson RP. Determinants of glucose toxicity and its reversibility in the pancreatic islet beta-cell line, HIT-T15. Am J Physiol Endocrinol Metab 2000; 279:E Goa KL, Barradell LB, Plosker GL. Bezafibrate. An update of its pharmacology and use in the management of dyslipidaemia. Drugs 1996; 52: Gordon T, Castelli WP, Hjortland MC, Kannel WB, Dawber TR. High density lipoprotein as a protective factor against coronary heart disease. The Framingham Study. Am J Med 1977; 62: Gregoire FM, Smas CM, Sul HS. Understanding adipocyte differentiation. Physiol Rev 1998; 78: Gremlich S, Bonny C, Waeber G, Thorens B. Fatty acids decrease IDX-1 expression in rat pancreatic islets and reduce GLUT2, glucokinase, insulin, and somatostatin levels. J Biol Chem 1997; 272: Grill V, Bjorklund A. Dysfunctional insulin secretion in type 2 diabetes: role of metabolic abnormalities. Cell Mol Life Sci 2000; 57: Guan HP, Ishizuka T, Chui PC, Lehrke M, Lazar MA. Corepressors selectively control the transcriptional activity of PPARgamma in adipocytes. Genes Dev 2005; 19: Guerre-Millo M, Gervois P, Raspe E, Madsen L, Poulain P, Derudas B, Herbert JM, Winegar DA, Willson TM, Fruchart JC, Berge RK, Staels B. Peroxisome proliferator-activated receptor alpha activators improve insulin sensitivity and reduce adiposity. J Biol Chem 2000; 275: Guilherme A, Emoto M, Buxton JM, Bose S, Sabini R, Theurkauf WE, Leszyk J, Czech MP. Perinuclear localization and insulin responsiveness of GLUT4 requires cytoskeletal integrity in 3T3-L1 adipocytes. J Biol Chem 2000; 275: Haaga JR, Alfidi RJ. Computed tomographic scanning of the pancreas. Radiol Clin North Am 1977; 15: Haffner SM, Valdez RA, Hazuda HP, Mitchell BD, Morales PA, Stern MP. Prospective analysis of the insulin-resistance syndrome (syndrome X). Diabetes 1992; 41: Hamilton BS, Paglia D, Kwan AY, Deitel M. Increased obese mrna expression in omental fat cells from massively obese humans. Nat Med 1995; 1: Hariharan N, Farrelly D, Hagan D, Hillyer D, Arbeeny C, Sabrah T, Treloar A, Brown K, Kalinowski S, Mookhtiar K. Expression of human hepatic glucokinase in transgenic mice liver results in decreased glucose levels and reduced body weight. Diabetes 1997; 46: Harper CR, Jacobson TA. New perspectives on the management of low levels of high-density lipoprotein cholesterol. Arch Intern Med 1999; 159: He W, Barak Y, Hevener A, Olson P, Liao D, Le J, Nelson M, Ong E, Olefsky JM, Evans RM. Adiposespecific peroxisome proliferator-activated receptor gamma knockout causes insulin resistance in fat and liver but not in muscle. Proc Natl Acad Sci U S A 2003; 100:
96 96 Hellmer J, Marcus C, Sonnenfeld T, Arner P. Mechanisms for differences in lipolysis between human subcutaneous and omental fat cells. J Clin Endocrinol Metab 1992; 75: Higashiyama H, Billin AN, Okamoto Y, Kinoshita M, Asano S. Expression profiling of peroxisome proliferator-activated receptor-delta (PPAR-delta) in mouse tissues using tissue microarray. Histochem Cell Biol 2007; 127: Hotamisligil GS. Inflammation and metabolic disorders. Nature 2006; 444: Howard BV, Howard WJ. Dyslipidemia in non-insulin-dependent diabetes mellitus. Endocr Rev 1994; 15: Huber J, Loffler M, Bilban M, Reimers M, Kadl A, Todoric J, Zeyda M, Geyeregger R, Schreiner M, Weichhart T, Leitinger N, Waldhausl W, Stulnig TM. Prevention of high-fat diet-induced adipose tissue remodeling in obese diabetic mice by n-3 polyunsaturated fatty acids. Int J Obes (Lond) 2007; 31: Ihara Y, Toyokuni S, Uchida K, Odaka H, Tanaka T, Ikeda H, Hiai H, Seino Y, Yamada Y. Hyperglycemia causes oxidative stress in pancreatic beta-cells of GK rats, a model of type 2 diabetes. Diabetes 1999; 48: Ijpenberg AI, Jeannin E, Wahli W, Desvergne B. Polarity and specific sequence requirements of peroxisome proliferator-activated receptor (PPAR)/retinoid X receptor heterodimer binding to DNA. A functional analysis of the malic enzyme gene PPAR response element. J Biol Chem 1997; 272: Ikemoto S, Takahashi M, Tsunoda N, Maruyama K, Itakura H, Ezaki O. High-fat diet-induced hyperglycemia and obesity in mice: differential effects of dietary oils. Metabolism 1996; 45: Imai T, Takakuwa R, Marchand S, Dentz E, Bornert JM, Messaddeq N, Wendling O, Mark M, Desvergne B, Wahli W, Chambon P, Metzger D. Peroxisome proliferator-activated receptor gamma is required in mature white and brown adipocytes for their survival in the mouse. Proc Natl Acad Sci U S A 2004; 101: Inoue I, Itoh F, Aoyagi S, Tazawa S, Kusama H, Akahane M, Mastunaga T, Hayashi K, Awata T, Komoda T, Katayama S. Fibrate and statin synergistically increase the transcriptional activities of PPARalpha/RXRalpha and decrease the transactivation of NFkappaB. Biochem Biophys Res Commun 2002; 290: Inoue I, Shino K, Noji S, Awata T, Katayama S. Expression of peroxisome proliferator-activated receptor alpha (PPAR alpha) in primary cultures of human vascular endothelial cells. Biochem Biophys Res Commun 1998; 246: Issemann I, Green S. Activation of a member of the steroid hormone receptor superfamily by peroxisome proliferators. Nature 1990; 347: Itai Y, Saida Y, Kurosaki Y, Kurosaki A, Fujimoto T. Focal fatty masses of the pancreas. Acta Radiol 1995; 36: Jacqueminet S, Briaud I, Rouault C, Reach G, Poitout V. Inhibition of insulin gene expression by long-term exposure of pancreatic beta cells to palmitate is dependent on the presence of a stimulatory glucose concentration. Metabolism 2000; 49: Jensen MD, Sarr MG, Dumesic DA, Southorn PA, Levine JA. Regional uptake of meal fatty acids in humans. Am J Physiol Endocrinol Metab 2003; 285:E Jia D, Otsuki M. Bezafibrate, a peroxisome proliferator-activated receptor (PPAR)-alpha activator, prevents pancreatic degeneration in obese and diabetic rats. Pancreas 2003; 26:
97 97 Jia D, Yamamoto M, Otani M, Otsuki M. Bezafibrate on lipids and glucose metabolism in obese diabetic Otsuka Long-Evans Tokushima fatty rats. Metabolism 2004; 53: Juge-Aubry C, Pernin A, Favez T, Burger AG, Wahli W, Meier CA, Desvergne B. DNA binding properties of peroxisome proliferator-activated receptor subtypes on various natural peroxisome proliferator response elements. Importance of the 5'-flanking region. J Biol Chem 1997; 272: Kanda H, Tateya S, Tamori Y, Kotani K, Hiasa K, Kitazawa R, Kitazawa S, Miyachi H, Maeda S, Egashira K, Kasuga M. MCP-1 contributes to macrophage infiltration into adipose tissue, insulin resistance, and hepatic steatosis in obesity. J Clin Invest 2006; 116: Kannel WB. Lipids, diabetes, and coronary heart disease: insights from the Framingham Study. Am Heart J 1985; 110: Kaplan NM. The deadly quartet. Upper-body obesity, glucose intolerance, hypertriglyceridemia, and hypertension. Arch Intern Med 1989; 149: Karelis AD, St-Pierre DH, Conus F, Rabasa-Lhoret R, Poehlman ET. Metabolic and body composition factors in subgroups of obesity: what do we know? J Clin Endocrinol Metab 2004; 89: Katz DS, Hines J, Math KR, Nardi PM, Mindelzun RE, Lane MJ. Using CT to reveal fat-containing abnormalities of the pancreas. AJR Am J Roentgenol 1999; 172: Keller H, Dreyer C, Medin J, Mahfoudi A, Ozato K, Wahli W. Fatty acids and retinoids control lipid metabolism through activation of peroxisome proliferator-activated receptor-retinoid X receptor heterodimers. Proc Natl Acad Sci U S A 1993; 90: Kersten S, Mandard S, Escher P, Gonzalez FJ, Tafuri S, Desvergne B, Wahli W. The peroxisome proliferator-activated receptor alpha regulates amino acid metabolism. Faseb J 2001; 15: Kersten S, Seydoux J, Peters JM, Gonzalez FJ, Desvergne B, Wahli W. Peroxisome proliferatoractivated receptor alpha mediates the adaptive response to fasting. J Clin Invest 1999; 103: Keys A. Overweight, obesity, coronary heart disease, and mortality: the W.O. Atwater Memorial Lecture, Prog Clin Biol Res 1981; 67: Kim H, Haluzik M, Asghar Z, Yau D, Joseph JW, Fernandez AM, Reitman ML, Yakar S, Stannard B, Heron-Milhavet L, Wheeler MB, LeRoith D. Peroxisome proliferator-activated receptor-alpha agonist treatment in a transgenic model of type 2 diabetes reverses the lipotoxic state and improves glucose homeostasis. Diabetes 2003; 52: Kim H, Haluzik M, Gavrilova O, Yakar S, Portas J, Sun H, Pajvani UB, Scherer PE, LeRoith D. Thiazolidinediones improve insulin sensitivity in adipose tissue and reduce the hyperlipidaemia without affecting the hyperglycaemia in a transgenic model of type 2 diabetes. Diabetologia 2004; 47: Kim HI, Ahn YH. Role of peroxisome proliferator-activated receptor-gamma in the glucose-sensing apparatus of liver and beta-cells. Diabetes 2004; 53 Suppl 1:S Kissebah AH, Krakower GR. Regional adiposity and morbidity. Physiol Rev 1994; 74: Kjorholt C, Akerfeldt MC, Biden TJ, Laybutt DR. Chronic hyperglycemia, independent of plasma lipid levels, is sufficient for the loss of beta-cell differentiation and secretory function in the db/db mouse model of diabetes. Diabetes 2005; 54:
98 98 Kliewer SA, Forman BM, Blumberg B, Ong ES, Borgmeyer U, Mangelsdorf DJ, Umesono K, Evans RM. Differential expression and activation of a family of murine peroxisome proliferatoractivated receptors. Proc Natl Acad Sci U S A 1994; 91: Kliewer SA, Umesono K, Noonan DJ, Heyman RA, Evans RM. Convergence of 9-cis retinoic acid and peroxisome proliferator signalling pathways through heterodimer formation of their receptors. Nature 1992; 358: Klip A, Paquet MR. Glucose transport and glucose transporters in muscle and their metabolic regulation. Diabetes Care 1990; 13: Klover PJ, Clementi AH, Mooney RA. Interleukin-6 depletion selectively improves hepatic insulin action in obesity. Endocrinology 2005; 146: Koh EH, Kim MS, Park JY, Kim HS, Youn JY, Park HS, Youn JH, Lee KU. Peroxisome proliferatoractivated receptor (PPAR)-alpha activation prevents diabetes in OLETF rats: comparison with PPAR-gamma activation. Diabetes 2003; 52: Koutnikova H, Cock TA, Watanabe M, Houten SM, Champy MF, Dierich A, Auwerx J. Compensation by the muscle limits the metabolic consequences of lipodystrophy in PPAR gamma hypomorphic mice. Proc Natl Acad Sci U S A 2003; 100: Kovanlikaya A, Mittelman SD, Ward A, Geffner ME, Dorey F, Gilsanz V. Obesity and fat quantification in lean tissues using three-point Dixon MR imaging. Pediatr Radiol 2005; 35: Kramer D, Shapiro R, Adler A, Bush E, Rondinone CM. Insulin-sensitizing effect of rosiglitazone (BRL-49653) by regulation of glucose transporters in muscle and fat of Zucker rats. Metabolism 2001; 50: Krey G, Braissant O, L'Horset F, Kalkhoven E, Perroud M, Parker MG, Wahli W. Fatty acids, eicosanoids, and hypolipidemic agents identified as ligands of peroxisome proliferatoractivated receptors by coactivator-dependent receptor ligand assay. Mol Endocrinol 1997; 11: Krotkiewski M, Bjorntorp P, Sjostrom L, Smith U. Impact of obesity on metabolism in men and women. Importance of regional adipose tissue distribution. J Clin Invest 1983; 72: Kylin E. Studien ueber das Hypertonie-Hyperglyka "mie-hyperurika" miesyndrom. Zentralblatt Fuer Innere Med 1923; 44: Laaksonen DE, Lakka HM, Niskanen LK, Kaplan GA, Salonen JT, Lakka TA. Metabolic syndrome and development of diabetes mellitus: application and validation of recently suggested definitions of the metabolic syndrome in a prospective cohort study. Am J Epidemiol 2002; 156: Lakka TA, Laaksonen DE, Lakka HM, Mannikko N, Niskanen LK, Rauramaa R, Salonen JT. Sedentary lifestyle, poor cardiorespiratory fitness, and the metabolic syndrome. Med Sci Sports Exerc 2003; 35: Lalloyer F, Vandewalle B, Percevault F, Torpier G, Kerr-Conte J, Oosterveer M, Paumelle R, Fruchart JC, Kuipers F, Pattou F, Fievet C, Staels B. Peroxisome proliferator-activated receptor alpha improves pancreatic adaptation to insulin resistance in obese mice and reduces lipotoxicity in human islets. Diabetes 2006; 55: Lapidus L, Bengtsson C, Larsson B, Pennert K, Rybo E, Sjostrom L. Distribution of adipose tissue and risk of cardiovascular disease and death: a 12 year follow up of participants in the
99 99 population study of women in Gothenburg, Sweden. Br Med J (Clin Res Ed) 1984; 289: Larsson B. Obesity, fat distribution and cardiovascular disease. Int J Obes 1991; 15 Suppl 2: Larsson B, Svardsudd K, Welin L, Wilhelmsen L, Bjorntorp P, Tibblin G. Abdominal adipose tissue distribution, obesity, and risk of cardiovascular disease and death: 13 year follow up of participants in the study of men born in Br Med J (Clin Res Ed) 1984; 288: Le Lay S, Krief S, Farnier C, Lefrere I, Le Liepvre X, Bazin R, Ferre P, Dugail I. Cholesterol, a cell sizedependent signal that regulates glucose metabolism and gene expression in adipocytes. J Biol Chem 2001; 276: Lee CH, Chawla A, Urbiztondo N, Liao D, Boisvert WA, Evans RM, Curtiss LK. Transcriptional repression of atherogenic inflammation: modulation by PPARdelta. Science 2003; 302: Lefebvre P, Chinetti G, Fruchart JC, Staels B. Sorting out the roles of PPAR alpha in energy metabolism and vascular homeostasis. J Clin Invest 2006; 116: Leibowitz MD, Fievet C, Hennuyer N, Peinado-Onsurbe J, Duez H, Bergera J, Cullinan CA, Sparrow CP, Baffic J, Berger GD, Santini C, Marquis RW, Tolman RL, Smith RG, Moller DE, Auwerx J. Activation of PPARdelta alters lipid metabolism in db/db mice. FEBS Lett 2000; 473: Lesniewski LA, Hosch SE, Neels JG, de Luca C, Pashmforoush M, Lumeng CN, Chiang SH, Scadeng M, Saltiel AR, Olefsky JM. Bone marrow-specific Cap gene deletion protects against high-fat diet-induced insulin resistance. Nat Med 2007; 13: Letavernier E, Perez J, Joye E, Bellocq A, Fouqueray B, Haymann JP, Heudes D, Wahli W, Desvergne B, Baud L. Peroxisome proliferator-activated receptor beta/delta exerts a strong protection from ischemic acute renal failure. J Am Soc Nephrol 2005; 16: Levin BE, Dunn-Meynell AA. Differential effects of exercise on body weight gain and adiposity in obesity-prone and -resistant rats. Int J Obes (Lond) 2006; 30: Levin BE, Dunn-Meynell AA, Balkan B, Keesey RE. Selective breeding for diet-induced obesity and resistance in Sprague-Dawley rats. Am J Physiol 1997; 273:R Liese AD, Mayer-Davis EJ, Haffner SM. Development of the multiple metabolic syndrome: an epidemiologic perspective. Epidemiol Rev 1998; 20: Lihn AS, Bruun JM, He G, Pedersen SB, Jensen PF, Richelsen B. Lower expression of adiponectin mrna in visceral adipose tissue in lean and obese subjects. Mol Cell Endocrinol 2004; 219:9-15. Lingohr MK, Buettner R, Rhodes CJ. Pancreatic beta-cell growth and survival--a role in obesitylinked type 2 diabetes? Trends Mol Med 2002; 8: Lorenzo C, Okoloise M, Williams K, Stern MP, Haffner SM. The metabolic syndrome as predictor of type 2 diabetes: the San Antonio heart study. Diabetes Care 2003; 26: Lundgren M, Buren J, Ruge T, Myrnas T, Eriksson JW. Glucocorticoids down-regulate glucose uptake capacity and insulin-signaling proteins in omental but not subcutaneous human adipocytes. J Clin Endocrinol Metab 2004; 89: Lupi R, Del Guerra S, Marselli L, Bugliani M, Boggi U, Mosca F, Marchetti P, Del Prato S. Rosiglitazone prevents the impairment of human islet function induced by fatty acids: evidence for a role of PPARgamma2 in the modulation of insulin secretion. Am J Physiol Endocrinol Metab 2004; 286:E
100 100 Luquet S, Lopez-Soriano J, Holst D, Fredenrich A, Melki J, Rassoulzadegan M, Grimaldi PA. Peroxisome proliferator-activated receptor delta controls muscle development and oxidative capability. Faseb J 2003; 17: Maedler K, Spinas GA, Dyntar D, Moritz W, Kaiser N, Donath MY. Distinct effects of saturated and monounsaturated fatty acids on beta-cell turnover and function. Diabetes 2001; 50: Magnuson MA. Glucokinase gene structure. Functional implications of molecular genetic studies. Diabetes 1990; 39: Mandard S, Muller M, Kersten S. Peroxisome proliferator-activated receptor alpha target genes. Cell Mol Life Sci 2004; 61: Mandarim-de-Lacerda CA. Stereological tools in biomedical research. An Acad Bras Cienc 2003; 75: Mandarim-de-Lacerda CA, Fernandes-Santos C, Aguila MB Image analysis and quantitative morphology. In: Hewitson TD, Darby JA, editors. Histology protocols: methods in molecular biology. New Jersey: Humana Press. p Mann GV. The influence of obesity on health (second of two parts). N Engl J Med 1974; 291: Marin P, Andersson B, Ottosson M, Olbe L, Chowdhury B, Kvist H, Holm G, Sjostrom L, Bjorntorp P. The morphology and metabolism of intraabdominal adipose tissue in men. Metabolism 1992; 41: Mathur A, Marine M, Lu D, Swartz-Basile DA, Saxena R, Zyromski NJ, Pitt HA. Nonalcoholic fatty pancreas disease. HPB (Oxford) 2007; 9: Matsumoto S, Mori H, Miyake H, Takaki H, Maeda T, Yamada Y, Oga M. Uneven fatty replacement of the pancreas: evaluation with CT. Radiology 1995; 194: Matsuoka T, Kajimoto Y, Watada H, Kaneto H, Kishimoto M, Umayahara Y, Fujitani Y, Kamada T, Kawamori R, Yamasaki Y. Glycation-dependent, reactive oxygen species-mediated suppression of the insulin gene promoter activity in HIT cells. J Clin Invest 1997; 99: Matthews DR, Hosker JP, Rudenski AS, Naylor BA, Treacher DF, Turner RC. Homeostasis model assessment: insulin resistance and beta-cell function from fasting plasma glucose and insulin concentrations in man. Diabetologia 1985; 28: Mauriege P, Galitzky J, Berlan M, Lafontan M. Heterogeneous distribution of beta and alpha-2 adrenoceptor binding sites in human fat cells from various fat deposits: functional consequences. Eur J Clin Invest 1987; 17: Mayerson AB, Hundal RS, Dufour S, Lebon V, Befroy D, Cline GW, Enocksson S, Inzucchi SE, Shulman GI, Petersen KF. The effects of rosiglitazone on insulin sensitivity, lipolysis, and hepatic and skeletal muscle triglyceride content in patients with type 2 diabetes. Diabetes 2002; 51: McCullough AJ. Pathophysiology of nonalcoholic steatohepatitis. J Clin Gastroenterol 2006; 40 Suppl 1:S Michalik L, Desvergne B, Tan NS, Basu-Modak S, Escher P, Rieusset J, Peters JM, Kaya G, Gonzalez FJ, Zakany J, Metzger D, Chambon P, Duboule D, Wahli W. Impaired skin wound healing in peroxisome proliferator-activated receptor (PPAR)alpha and PPARbeta mutant mice. J Cell Biol 2001; 154:
101 101 Michalik L, Wahli W. Involvement of PPAR nuclear receptors in tissue injury and wound repair. J Clin Invest 2006; 116: Minokoshi Y, Kim YB, Peroni OD, Fryer LG, Muller C, Carling D, Kahn BB. Leptin stimulates fattyacid oxidation by activating AMP-activated protein kinase. Nature 2002; 415: Miyazaki Y, He H, Mandarino LJ, DeFronzo RA. Rosiglitazone improves downstream insulin receptor signaling in type 2 diabetic patients. Diabetes 2003; 52: Montague CT, Prins JB, Sanders L, Digby JE, O'Rahilly S. Depot- and sex-specific differences in human leptin mrna expression: implications for the control of regional fat distribution. Diabetes 1997; 46: Monteiro CA, Mondini L, de Souza AL, Popkin BM. The nutrition transition in Brazil. Eur J Clin Nutr 1995; 49: Moran A, Zhang HJ, Olson LK, Harmon JS, Poitout V, Robertson RP. Differentiation of glucose toxicity from beta cell exhaustion during the evolution of defective insulin gene expression in the pancreatic islet cell line, HIT-T15. J Clin Invest 1997; 99: Motoshima H, Wu X, Sinha MK, Hardy VE, Rosato EL, Barbot DJ, Rosato FE, Goldstein BJ. Differential regulation of adiponectin secretion from cultured human omental and subcutaneous adipocytes: effects of insulin and rosiglitazone. J Clin Endocrinol Metab 2002; 87: Mudaliar S, Chang AR, Henry RR. Thiazolidinediones, peripheral edema, and type 2 diabetes: incidence, pathophysiology, and clinical implications. Endocr Pract 2003; 9: Muoio DM, Newgard CB. Metabolism: A is for adipokine. Nature 2005; 436: Muoio DM, Newgard CB. Mechanisms of disease: molecular and metabolic mechanisms of insulin resistance and beta-cell failure in type 2 diabetes. Nat Rev Mol Cell Biol 2008; 9: Must A, Spadano J, Coakley EH, Field AE, Colditz G, Dietz WH. The disease burden associated with overweight and obesity. Jama 1999; 282: Nadra K, Anghel SI, Joye E, Tan NS, Basu-Modak S, Trono D, Wahli W, Desvergne B. Differentiation of trophoblast giant cells and their metabolic functions are dependent on peroxisome proliferator-activated receptor beta/delta. Mol Cell Biol 2006; 26: Nascimento FA, Barbosa-da-Silva S, Fernandes-Santos C, Mandarim-de-Lacerda CA, Aguila MB. Adipose tissue, liver and pancreas structural alterations in C57BL/6 mice fed high-fat-highsucrose diet supplemented with fish oil (n-3 fatty acid rich oil). Exp Toxicol Pathol 2010; 62: NCEP. Third report of the national cholesterol education program (NCEP) expert panel on detection, evaluation, and treatment of high blood cholesterol in adults (adut treatment panel III) National institute of health Ninomiya JK, L'Italien G, Criqui MH, Whyte JL, Gamst A, Chen RS. Association of the metabolic syndrome with history of myocardial infarction and stroke in the Third National Health and Nutrition Examination Survey. Circulation 2004; 109: Nishina PM, Lowe S, Verstuyft J, Naggert JK, Kuypers FA, Paigen B. Effects of dietary fats from animal and plant sources on diet-induced fatty streak lesions in C57BL/6J mice. J Lipid Res 1993; 34: Nishina PM, Verstuyft J, Paigen B. Synthetic low and high fat diets for the study of atherosclerosis in the mouse. J Lipid Res 1990; 31:
102 102 Nissen SE, Wolski K, Topol EJ. Effect of muraglitazar on death and major adverse cardiovascular events in patients with type 2 diabetes mellitus. Jama 2005; 294: Niswender KD, Shiota M, Postic C, Cherrington AD, Magnuson MA. Effects of increased glucokinase gene copy number on glucose homeostasis and hepatic glucose metabolism. J Biol Chem 1997; 272: Nordlie RC, Foster JD, Lange AJ. Regulation of glucose production by the liver. Annu Rev Nutr 1999; 19: Oakes ND, Cooney GJ, Camilleri S, Chisholm DJ, Kraegen EW. Mechanisms of liver and muscle insulin resistance induced by chronic high-fat feeding. Diabetes 1997; 46: Ogilvie RF. The islands of Langerhans in 19 cases of obesity. J Pathol Bact 1933; 37: Ohlson LO, Larsson B, Svardsudd K, Welin L, Eriksson H, Wilhelmsen L, Bjorntorp P, Tibblin G. The influence of body fat distribution on the incidence of diabetes mellitus years of follow-up of the participants in the study of men born in Diabetes 1985; 34: Olefsky JM. Treatment of insulin resistance with peroxisome proliferator-activated receptor gamma agonists. J Clin Invest 2000; 106: Oliver WR, Jr., Shenk JL, Snaith MR, Russell CS, Plunket KD, Bodkin NL, Lewis MC, Winegar DA, Sznaidman ML, Lambert MH, Xu HE, Sternbach DD, Kliewer SA, Hansen BC, Willson TM. A selective peroxisome proliferator-activated receptor delta agonist promotes reverse cholesterol transport. Proc Natl Acad Sci U S A 2001; 98: Pagliassotti MJ, Gayles EC, Podolin DA, Wei Y, Morin CL. Developmental stage modifies dietinduced peripheral insulin resistance in rats. Am J Physiol Regul Integr Comp Physiol 2000; 278:R Pagliassotti MJ, Prach PA, Koppenhafer TA, Pan DA. Changes in insulin action, triglycerides, and lipid composition during sucrose feeding in rats. Am J Physiol 1996; 271:R Paigen B. Genetics of responsiveness to high-fat and high-cholesterol diets in the mouse. Am J Clin Nutr 1995; 62:458S-462S. Papachristou GI, Papachristou DJ, Avula H, Slivka A, Whitcomb DC. Obesity increases the severity of acute pancreatitis: performance of APACHE-O score and correlation with the inflammatory response. Pancreatology 2006; 6: Parulkar AA, Pendergrass ML, Granda-Ayala R, Lee TR, Fonseca VA. Nonhypoglycemic effects of thiazolidinediones. Ann Intern Med 2001; 134: Patel S, Bellon EM, Haaga J, Park CH. Fat replacement of the exocrine pancreas. AJR Am J Roentgenol 1980; 135: Pessin JE, Thurmond DC, Elmendorf JS, Coker KJ, Okada S. Molecular basis of insulin-stimulated GLUT4 vesicle trafficking. Location! Location! Location! J Biol Chem 1999; 274: Peters JM, Aoyama T, Burns AM, Gonzalez FJ. Bezafibrate is a dual ligand for PPARalpha and PPARbeta: studies using null mice. Biochim Biophys Acta 2003; 1632: Peters JM, Lee SS, Li W, Ward JM, Gavrilova O, Everett C, Reitman ML, Hudson LD, Gonzalez FJ. Growth, adipose, brain, and skin alterations resulting from targeted disruption of the mouse peroxisome proliferator-activated receptor beta(delta). Mol Cell Biol 2000; 20: Pick A, Clark J, Kubstrup C, Levisetti M, Pugh W, Bonner-Weir S, Polonsky KS. Role of apoptosis in failure of beta-cell mass compensation for insulin resistance and beta-cell defects in the male Zucker diabetic fatty rat. Diabetes 1998; 47:
103 103 Pitt HA. Hepato-pancreato-biliary fat: the good, the bad and the ugly. HPB (Oxford) 2007; 9: Poitout V, Robertson RP. Minireview: Secondary beta-cell failure in type 2 diabetes--a convergence of glucotoxicity and lipotoxicity. Endocrinology 2002; 143: Powell K. Obesity: the two faces of fat. Nature 2007; 447: Prentice AM, Moore SE. Early programming of adult diseases in resource poor countries. Arch Dis Child 2005; 90: Prentki M, Joly E, El-Assaad W, Roduit R. Malonyl-CoA signaling, lipid partitioning, and glucolipotoxicity: role in beta-cell adaptation and failure in the etiology of diabetes. Diabetes 2002; 51 Suppl 3:S Qi Y, Takahashi N, Hileman SM, Patel HR, Berg AH, Pajvani UB, Scherer PE, Ahima RS. Adiponectin acts in the brain to decrease body weight. Nat Med 2004; 10: Rahmouni K, Haynes WG, Morgan DA, Mark AL. Selective resistance to central neural administration of leptin in agouti obese mice. Hypertension 2002; 39: Rahmouni K, Morgan DA, Morgan GM, Mark AL, Haynes WG. Role of selective leptin resistance in diet-induced obesity hypertension. Diabetes 2005; 54: Rajala MW, Scherer PE. Minireview: The adipocyte--at the crossroads of energy homeostasis, inflammation, and atherosclerosis. Endocrinology 2003; 144: Ravussin E, Smith SR. Increased fat intake, impaired fat oxidation, and failure of fat cell proliferation result in ectopic fat storage, insulin resistance, and type 2 diabetes mellitus. Ann N Y Acad Sci 2002; 967: Reaven GM. Banting lecture Role of insulin resistance in human disease. Diabetes 1988; 37: Reddy JK, Hashimoto T. Peroxisomal beta-oxidation and peroxisome proliferator-activated receptor alpha: an adaptive metabolic system. Annu Rev Nutr 2001; 21: Reeves PG, Nielsen FH, Fahey GC, Jr. AIN-93 purified diets for laboratory rodents: final report of the American Institute of Nutrition ad hoc writing committee on the reformulation of the AIN- 76A rodent diet. J Nutr 1993; 123: Ricote M, Huang J, Fajas L, Li A, Welch J, Najib J, Witztum JL, Auwerx J, Palinski W, Glass CK. Expression of the peroxisome proliferator-activated receptor gamma (PPARgamma) in human atherosclerosis and regulation in macrophages by colony stimulating factors and oxidized low density lipoprotein. Proc Natl Acad Sci U S A 1998a; 95: Ricote M, Li AC, Willson TM, Kelly CJ, Glass CK. The peroxisome proliferator-activated receptorgamma is a negative regulator of macrophage activation. Nature 1998b; 391: Rieusset J, Touri F, Michalik L, Escher P, Desvergne B, Niesor E, Wahli W. A new selective peroxisome proliferator-activated receptor gamma antagonist with antiobesity and antidiabetic activity. Mol Endocrinol 2002; 16: Ritz-Laser B, Meda P, Constant I, Klages N, Charollais A, Morales A, Magnan C, Ktorza A, Philippe J. Glucose-induced preproinsulin gene expression is inhibited by the free fatty acid palmitate. Endocrinology 1999; 140: Rosen ED, Kulkarni RN, Sarraf P, Ozcan U, Okada T, Hsu CH, Eisenman D, Magnuson MA, Gonzalez FJ, Kahn CR, Spiegelman BM. Targeted elimination of peroxisome proliferator-activated receptor gamma in beta cells leads to abnormalities in islet mass without compromising glucose homeostasis. Mol Cell Biol 2003; 23:
104 104 Rosen ED, Sarraf P, Troy AE, Bradwin G, Moore K, Milstone DS, Spiegelman BM, Mortensen RM. PPAR gamma is required for the differentiation of adipose tissue in vivo and in vitro. Mol Cell 1999; 4: Rosen ED, Spiegelman BM. Molecular regulation of adipogenesis. Annu Rev Cell Dev Biol 2000; 16: Ross R, Leger L, Morris D, de Guise J, Guardo R. Quantification of adipose tissue by MRI: relationship with anthropometric variables. J Appl Physiol 1992; 72: Rossmeisl M, Rim JS, Koza RA, Kozak LP. Variation in type 2 diabetes--related traits in mouse strains susceptible to diet-induced obesity. Diabetes 2003; 52: Russell CD, Petersen RN, Rao SP, Ricci MR, Prasad A, Zhang Y, Brolin RE, Fried SK. Leptin expression in adipose tissue from obese humans: depot-specific regulation by insulin and dexamethasone. Am J Physiol 1998; 275:E Saltiel AR. New perspectives into the molecular pathogenesis and treatment of type 2 diabetes. Cell 2001; 104: Sanchez-Lozada LG, Tapia E, Jimenez A, Bautista P, Cristobal M, Nepomuceno T, Soto V, Avila- Casado C, Nakagawa T, Johnson RJ, Herrera-Acosta J, Franco M. Fructose-induced metabolic syndrome is associated with glomerular hypertension and renal microvascular damage in rats. Am J Physiol Renal Physiol 2007; 292:F Savage DB, Tan GD, Acerini CL, Jebb SA, Agostini M, Gurnell M, Williams RL, Umpleby AM, Thomas EL, Bell JD, Dixon AK, Dunne F, Boiani R, Cinti S, Vidal-Puig A, Karpe F, Chatterjee VK, O'Rahilly S. Human metabolic syndrome resulting from dominant-negative mutations in the nuclear receptor peroxisome proliferator-activated receptor-gamma. Diabetes 2003; 52: SBH. I Diretriz Brasileira de Diagnóstico e Tratamento da Síndrome Metabólica. Hipertensão 2004; 7: Schaefer JH. The normal weight of the pancreas in the adult human being: a biometric study.. Anat Rec 1926; 32: Schaffer JE. Lipotoxicity: when tissues overeat. Curr Opin Lipidol 2003; 14: Scheen AJ. Pathophysiology of insulin secretion. Ann Endocrinol (Paris) 2004; 65: Schuit FC, Huypens P, Heimberg H, Pipeleers DG. Glucose sensing in pancreatic beta-cells: a model for the study of other glucose-regulated cells in gut, pancreas, and hypothalamus. Diabetes 2001; 50:1-11. Segersvard R, Sylvan M, Herrington M, Larsson J, Permert J. Obesity increases the severity of acute experimental pancreatitis in the rat. Scand J Gastroenterol 2001; 36: Sell H, Kaiser U, Eckel J. Expression of chemokine receptors in insulin-resistant human skeletal muscle cells. Horm Metab Res 2007; 39: Senn JJ, Klover PJ, Nowak IA, Mooney RA. Interleukin-6 induces cellular insulin resistance in hepatocytes. Diabetes 2002; 51: Sgro C, Escousse A. [Side effects of fibrates (except liver and muscle)]. Therapie 1991; 46: Shimabukuro M, Higa M, Zhou YT, Wang MY, Newgard CB, Unger RH. Lipoapoptosis in beta-cells of obese prediabetic fa/fa rats. Role of serine palmitoyltransferase overexpression. J Biol Chem 1998; 273:
105 105 Sims EA. Are there persons who are obese, but metabolically healthy? Metabolism 2001; 50: Singh S, Loke YK, Furberg CD. Long-term risk of cardiovascular events with rosiglitazone: a metaanalysis. Jama 2007; 298: Smith DH, Dubiel R, Jones M. Use of 24-hour ambulatory blood pressure monitoring to assess antihypertensive efficacy: a comparison of olmesartan medoxomil, losartan potassium, valsartan, and irbesartan. Am J Cardiovasc Drugs 2005; 5: Smith SR, Lovejoy JC, Greenway F, Ryan D, dejonge L, de la Bretonne J, Volafova J, Bray GA. Contributions of total body fat, abdominal subcutaneous adipose tissue compartments, and visceral adipose tissue to the metabolic complications of obesity. Metabolism 2001; 50: Sopasakis VR, Sandqvist M, Gustafson B, Hammarstedt A, Schmelz M, Yang X, Jansson PA, Smith U. High local concentrations and effects on differentiation implicate interleukin-6 as a paracrine regulator. Obes Res 2004; 12: Soria B, Quesada I, Ropero AB, Pertusa JA, Martin F, Nadal A. Novel players in pancreatic islet signaling: from membrane receptors to nuclear channels. Diabetes 2004; 53 Suppl 1:S Staels B, Koenig W, Habib A, Merval R, Lebret M, Torra IP, Delerive P, Fadel A, Chinetti G, Fruchart JC, Najib J, Maclouf J, Tedgui A. Activation of human aortic smooth-muscle cells is inhibited by PPARalpha but not by PPARgamma activators. Nature 1998; 393: Staels B, van Tol A, Andreu T, Auwerx J. Fibrates influence the expression of genes involved in lipoprotein metabolism in a tissue-selective manner in the rat. Arterioscler Thromb 1992; 12: Staels B, Vu-Dac N, Kosykh VA, Saladin R, Fruchart JC, Dallongeville J, Auwerx J. Fibrates downregulate apolipoprotein C-III expression independent of induction of peroxisomal acyl coenzyme A oxidase. A potential mechanism for the hypolipidemic action of fibrates. J Clin Invest 1995; 95: Stanley TB, Leesnitzer LM, Montana VG, Galardi CM, Lambert MH, Holt JA, Xu HE, Moore LB, Blanchard SG, Stimmel JB. Subtype specific effects of peroxisome proliferator-activated receptor ligands on corepressor affinity. Biochemistry 2003; 42: Strissel KJ, Stancheva Z, Miyoshi H, Perfield JW, 2nd, DeFuria J, Jick Z, Greenberg AS, Obin MS. Adipocyte death, adipose tissue remodeling, and obesity complications. Diabetes 2007; 56: Sun Y, Zhang L, Gu HF, Han W, Ren M, Wang F, Gong B, Wang L, Guo H, Xin W, Zhao J, Gao L. Peroxisome proliferator-activated receptor-alpha regulates the expression of pancreatic/duodenal homeobox-1 in rat insulinoma (INS-1) cells and ameliorates glucoseinduced insulin secretion impaired by palmitate. Endocrinology 2008; 149: Surwit RS, Feinglos MN, Rodin J, Sutherland A, Petro AE, Opara EC, Kuhn CM, Rebuffe-Scrive M. Differential effects of fat and sucrose on the development of obesity and diabetes in C57BL/6J and A/J mice. Metabolism 1995; 44: Surwit RS, Kuhn CM, Cochrane C, McCubbin JA, Feinglos MN. Diet-induced type II diabetes in C57BL/6J mice. Diabetes 1988; 37: Tajiri Y, Moller C, Grill V. Long-term effects of aminoguanidine on insulin release and biosynthesis: evidence that the formation of advanced glycosylation end products inhibits B cell function. Endocrinology 1997; 138:
106 106 Tanaka T, Yamamoto J, Iwasaki S, Asaba H, Hamura H, Ikeda Y, Watanabe M, Magoori K, Ioka RX, Tachibana K, Watanabe Y, Uchiyama Y, Sumi K, Iguchi H, Ito S, Doi T, Hamakubo T, Naito M, Auwerx J, Yanagisawa M, Kodama T, Sakai J. Activation of peroxisome proliferator-activated receptor delta induces fatty acid beta-oxidation in skeletal muscle and attenuates metabolic syndrome. Proc Natl Acad Sci U S A 2003; 100: Tenenbaum A, Fisman EZ, Boyko V, Benderly M, Tanne D, Haim M, Matas Z, Motro M, Behar S. Attenuation of progression of insulin resistance in patients with coronary artery disease by bezafibrate. Arch Intern Med 2006; 166: Tenenbaum A, Motro M, Fisman EZ, Adler Y, Shemesh J, Tanne D, Leor J, Boyko V, Schwammenthal E, Behar S. Effect of bezafibrate on incidence of type 2 diabetes mellitus in obese patients. Eur Heart J 2005; 26: Tian JY, Li G, Gu YY, Zhang HL, Zhou WZ, Wang X, Zhu HD, Luo TH, Luo M. Role and mechanism of rosiglitazone on the impairment of insulin secretion induced by free fatty acids on isolated rat islets. Chin Med J (Engl) 2006; 119: Tilg H, Moschen AR. Adipocytokines: mediators linking adipose tissue, inflammation and immunity. Nat Rev Immunol 2006; 6: Tontonoz P, Graves RA, Budavari AI, Erdjument-Bromage H, Lui M, Hu E, Tempst P, Spiegelman BM. Adipocyte-specific transcription factor ARF6 is a heterodimeric complex of two nuclear hormone receptors, PPAR gamma and RXR alpha. Nucleic Acids Res 1994a; 22: Tontonoz P, Hu E, Graves RA, Budavari AI, Spiegelman BM. mppar gamma 2: tissue-specific regulator of an adipocyte enhancer. Genes Dev 1994b; 8: Tontonoz P, Kim JB, Graves RA, Spiegelman BM. ADD1: a novel helix-loop-helix transcription factor associated with adipocyte determination and differentiation. Mol Cell Biol 1993; 13: Trayhurn P, Beattie JH. Physiological role of adipose tissue: white adipose tissue as an endocrine and secretory organ. Proc Nutr Soc 2001; 60: Trayhurn P, Wood IS. Adipokines: inflammation and the pleiotropic role of white adipose tissue. Br J Nutr 2004; 92: Trevisan M, Liu J, Bahsas FB, Menotti A. Syndrome X and mortality: a population-based study. Risk Factor and Life Expectancy Research Group. Am J Epidemiol 1998; 148: Tritos NA, Mantzoros CS. Leptin: its role in obesity and beyond. Diabetologia 1997; 40: Tugwood JD, Issemann I, Anderson RG, Bundell KR, McPheat WL, Green S. The mouse peroxisome proliferator activated receptor recognizes a response element in the 5' flanking sequence of the rat acyl CoA oxidase gene. Embo J 1992; 11: Unger RH. Lipotoxicity in the pathogenesis of obesity-dependent NIDDM. Genetic and clinical implications. Diabetes 1995; 44: Vague J. La differénciation sexuelle, facteur determinant des formes de l obésite. Presse méd 1947; 55: Varnat F, Heggeler BB, Grisel P, Boucard N, Corthesy-Theulaz I, Wahli W, Desvergne B. PPARbeta/delta regulates paneth cell differentiation via controlling the hedgehog signaling pathway. Gastroenterology 2006; 131: Vasseur S, Folch-Puy E, Hlouschek V, Garcia S, Fiedler F, Lerch MM, Dagorn JC, Closa D, Iovanna JL. p8 improves pancreatic response to acute pancreatitis by enhancing the expression of the antiinflammatory protein pancreatitis-associated protein I. J Biol Chem 2004; 279:
107 107 Vikman HL, Savola JM, Raasmaja A, Ohisalo JJ. Alpha 2A-adrenergic regulation of cyclic AMP accumulation and lipolysis in human omental and subcutaneous adipocytes. Int J Obes Relat Metab Disord 1996; 20: Virtanen KA, Lonnroth P, Parkkola R, Peltoniemi P, Asola M, Viljanen T, Tolvanen T, Knuuti J, Ronnemaa T, Huupponen R, Nuutila P. Glucose uptake and perfusion in subcutaneous and visceral adipose tissue during insulin stimulation in nonobese and obese humans. J Clin Endocrinol Metab 2002; 87: Vu-Dac N, Schoonjans K, Kosykh V, Dallongeville J, Fruchart JC, Staels B, Auwerx J. Fibrates increase human apolipoprotein A-II expression through activation of the peroxisome proliferator-activated receptor. J Clin Invest 1995; 96: Wajchenberg BL. Subcutaneous and visceral adipose tissue: their relation to the metabolic syndrome. Endocr Rev 2000; 21: Wajchenberg BL, Giannella-Neto D, da Silva ME, Santos RF. Depot-specific hormonal characteristics of subcutaneous and visceral adipose tissue and their relation to the metabolic syndrome. Horm Metab Res 2002; 34: Walters MN. Adipose atrophy of the exocrine pancreas. J Pathol Bacteriol 1966; 92: Wang YX, Lee CH, Tiep S, Yu RT, Ham J, Kang H, Evans RM. Peroxisome-proliferator-activated receptor delta activates fat metabolism to prevent obesity. Cell 2003; 113: Wang YX, Zhang CL, Yu RT, Cho HK, Nelson MC, Bayuga-Ocampo CR, Ham J, Kang H, Evans RM. Regulation of muscle fiber type and running endurance by PPARdelta. PLoS Biol 2004; 2:e294. Wanless IR, Shiota K. The pathogenesis of nonalcoholic steatohepatitis and other fatty liver diseases: a four-step model including the role of lipid release and hepatic venular obstruction in the progression to cirrhosis. Semin Liver Dis 2004; 24: Weisberg SP, McCann D, Desai M, Rosenbaum M, Leibel RL, Ferrante AW, Jr. Obesity is associated with macrophage accumulation in adipose tissue. J Clin Invest 2003; 112: Welters HJ, McBain SC, Tadayyon M, Scarpello JH, Smith SA, Morgan NG. Expression and functional activity of PPARgamma in pancreatic beta cells. Br J Pharmacol 2004; 142: Weyer C, Foley JE, Bogardus C, Tataranni PA, Pratley RE. Enlarged subcutaneous abdominal adipocyte size, but not obesity itself, predicts type II diabetes independent of insulin resistance. Diabetologia 2000; 43: Weyer C, Funahashi T, Tanaka S, Hotta K, Matsuzawa Y, Pratley RE, Tataranni PA. Hypoadiponectinemia in obesity and type 2 diabetes: close association with insulin resistance and hyperinsulinemia. J Clin Endocrinol Metab 2001; 86: Willson TM, Brown PJ, Sternbach DD, Henke BR. The PPARs: from orphan receptors to drug discovery. J Med Chem 2000; 43: World Health Organisation DoNDS Definition, Diagnosis and Classification of Diabetes Mellitus and its Complications. In. Wu L, Wang R, De Champlain J, Wilson TW. Beneficial and deleterious effects of rosiglitazone on hypertension development in spontaneously hypertensive rats. Am J Hypertens 2004; 17:
108 108 Xu H, Barnes GT, Yang Q, Tan G, Yang D, Chou CJ, Sole J, Nichols A, Ross JS, Tartaglia LA, Chen H. Chronic inflammation in fat plays a crucial role in the development of obesity-related insulin resistance. J Clin Invest 2003; 112: Yajima K, Hirose H, Fujita H, Seto Y, Fujita H, Ukeda K, Miyashita K, Kawai T, Yamamoto Y, Ogawa T, Yamada T, Saruta T. Combination therapy with PPARgamma and PPARalpha agonists increases glucose-stimulated insulin secretion in db/db mice. Am J Physiol Endocrinol Metab 2003; 284:E Yamauchi T, Kamon J, Minokoshi Y, Ito Y, Waki H, Uchida S, Yamashita S, Noda M, Kita S, Ueki K, Eto K, Akanuma Y, Froguel P, Foufelle F, Ferre P, Carling D, Kimura S, Nagai R, Kahn BB, Kadowaki T. Adiponectin stimulates glucose utilization and fatty-acid oxidation by activating AMP-activated protein kinase. Nat Med 2002; 8: Yan MX, Li YQ, Meng M, Ren HB, Kou Y. Long-term high-fat diet induces pancreatic injuries via pancreatic microcirculatory disturbances and oxidative stress in rats with hyperlipidemia. Biochem Biophys Res Commun 2006; 347: Yang X, Smith U. Adipose tissue distribution and risk of metabolic disease: does thiazolidinedioneinduced adipose tissue redistribution provide a clue to the answer? Diabetologia 2007; 50: Yin FC, Spurgeon HA, Rakusan K, Weisfeldt ML, Lakatta EG. Use of tibial length to quantify cardiac hypertrophy: application in the aging rat. Am J Physiol 1982; 243:H Yoshikawa H, Tajiri Y, Sako Y, Hashimoto T, Umeda F, Nawata H. Effects of bezafibrate on beta-cell function of rat pancreatic islets. Eur J Pharmacol 2001a; 426: Yoshikawa H, Tajiri Y, Sako Y, Hashimoto T, Umeda F, Nawata H. Effects of free fatty acids on betacell functions: a possible involvement of peroxisome proliferator-activated receptors alpha or pancreatic/duodenal homeobox. Metabolism 2001b; 50: Yu C, Markan K, Temple KA, Deplewski D, Brady MJ, Cohen RN. The nuclear receptor corepressors NCoR and SMRT decrease peroxisome proliferator-activated receptor gamma transcriptional activity and repress 3T3-L1 adipogenesis. J Biol Chem 2005; 280: Zhang X, Cui Y, Fang L, Li F. Chronic high-fat diets induce oxide injuries and fibrogenesis of pancreatic cells in rats. Pancreas 2008; 37:e Zhu Y, Qi C, Korenberg JR, Chen XN, Noya D, Rao MS, Reddy JK. Structural organization of mouse peroxisome proliferator-activated receptor gamma (mppar gamma) gene: alternative promoter use and different splicing yield two mppar gamma isoforms. Proc Natl Acad Sci U S A 1995; 92: Zyromski NJ, Mathur A, Pitt HA, Lu D, Gripe JT, Walker JJ, Yancey K, Wade TE, Swartz-Basile DA. A murine model of obesity implicates the adipokine milieu in the pathogenesis of severe acute pancreatitis. Am J Physiol Gastrointest Liver Physiol 2008.
109 ANEXOS 109
110 110 UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE BIOLOGIA ROBERTO ALCANTARA GOMES COMISSÃO DE ÉTICA PARA O CUIDADO E USO DE ANIMAIS EXPERIMENTAIS CERTIFICADO Certificamos que o Protocolo nº CEA/176/2008 sobre Alterações metabólicas, estruturais e moleculares em órgãos-alvo de camundongos C57BL/6J com regime alimentar hiperlipídico e diferentes tratamentos sob a responsabilidade de Carlos Alberto Mandarim-de-Lacerda está de acordo com os Princípios Éticos na Experimentação Animal adotados pelo Colégio Brasileiro de Experimentação Animal (COBEA), tendo sido aprovado pela Comissão de Ética Para o Cuidado e Uso de Animais Experimentais do Instituto de Biologia Roberto Alcântara Gomes da UERJ (CEA), em 22/03/2008. Este certificado expira em 22/03/2010, podendo ser renovado. Rio de Janeiro, 22 de Março de 2008.
Células A (25%) Glucagon Células B (60%) Insulina Células D (10%) Somatostatina Células F ou PP (5%) Polipeptídeo Pancreático 1-2 milhões de ilhotas
 Instituto Biomédico Departamento de Fisiologia e Farmacologia Disciplina: Fisiologia II Curso: Medicina Veterinária Pâncreas Endócrino Prof. Guilherme Soares Ilhotas Células A (25%) Glucagon Células B
Instituto Biomédico Departamento de Fisiologia e Farmacologia Disciplina: Fisiologia II Curso: Medicina Veterinária Pâncreas Endócrino Prof. Guilherme Soares Ilhotas Células A (25%) Glucagon Células B
TRATAMENTO MEDICAMENTOSO DO DIABETES MELLITUS: SULFONILUREIAS E BIGUANIDAS
 UNIVERSIDADE DE UBERABA LIGA DE DIABETES 2013 TRATAMENTO MEDICAMENTOSO DO DIABETES MELLITUS: SULFONILUREIAS E BIGUANIDAS PALESTRANTES:FERNANDA FERREIRA AMUY LUCIANA SOUZA LIMA 2013/2 CRITÉRIOS PARA ESCOLHA
UNIVERSIDADE DE UBERABA LIGA DE DIABETES 2013 TRATAMENTO MEDICAMENTOSO DO DIABETES MELLITUS: SULFONILUREIAS E BIGUANIDAS PALESTRANTES:FERNANDA FERREIRA AMUY LUCIANA SOUZA LIMA 2013/2 CRITÉRIOS PARA ESCOLHA
EXERCÍCIO E DIABETES
 EXERCÍCIO E DIABETES Todos os dias ouvimos falar dos benefícios que os exercícios físicos proporcionam, de um modo geral, à nossa saúde. Pois bem, aproveitando a oportunidade, hoje falaremos sobre a Diabetes,
EXERCÍCIO E DIABETES Todos os dias ouvimos falar dos benefícios que os exercícios físicos proporcionam, de um modo geral, à nossa saúde. Pois bem, aproveitando a oportunidade, hoje falaremos sobre a Diabetes,
Regulação do metabolismo do glicogênio
 Regulação do metabolismo do glicogênio A U L A 27 objetivos Ao final desta aula, você deverá ser capaz de: Aprender sobre as vias de regulação do metabolismo de glicogênio. Reforçar os conceitos adquiridos
Regulação do metabolismo do glicogênio A U L A 27 objetivos Ao final desta aula, você deverá ser capaz de: Aprender sobre as vias de regulação do metabolismo de glicogênio. Reforçar os conceitos adquiridos
METABOLISMO DE LIPÍDEOS
 METABOLISMO DE LIPÍDEOS 1. Β-oxidação de ácidos graxos - Síntese de acetil-coa - ciclo de Krebs - Cadeia transportadora de elétrons e fosforilação oxidativa 2. Síntese de corpos cetônicos 3. Síntese de
METABOLISMO DE LIPÍDEOS 1. Β-oxidação de ácidos graxos - Síntese de acetil-coa - ciclo de Krebs - Cadeia transportadora de elétrons e fosforilação oxidativa 2. Síntese de corpos cetônicos 3. Síntese de
Curso: Integração Metabólica
 Curso: Integração Metabólica Aula 9: Sistema Nervoso Autônomo Prof. Carlos Castilho de Barros Sistema Nervoso Sistema Nervoso Central Sistema Nervoso Periférico Sensorial Motor Somático Autônomo Glândulas,
Curso: Integração Metabólica Aula 9: Sistema Nervoso Autônomo Prof. Carlos Castilho de Barros Sistema Nervoso Sistema Nervoso Central Sistema Nervoso Periférico Sensorial Motor Somático Autônomo Glândulas,
A SAÚDE DO OBESO Equipe CETOM
 A SAÚDE DO OBESO Dr. Izidoro de Hiroki Flumignan Médico endocrinologista e sanitarista Equipe CETOM Centro de Estudos e Tratamento para a Obesidade Mórbida. Diretor do Instituto Flumignano de Medicina
A SAÚDE DO OBESO Dr. Izidoro de Hiroki Flumignan Médico endocrinologista e sanitarista Equipe CETOM Centro de Estudos e Tratamento para a Obesidade Mórbida. Diretor do Instituto Flumignano de Medicina
REGULAÇÃO HORMONAL DO METABOLISMO
 REGULAÇÃO HORMONAL DO METABOLISMO A concentração de glicose no sangue está sempre sendo regulada A glicose é mantida em uma faixa de 60 a 90 g/100ml de sangue (~4,5mM) Homeostase da glicose Necessidade
REGULAÇÃO HORMONAL DO METABOLISMO A concentração de glicose no sangue está sempre sendo regulada A glicose é mantida em uma faixa de 60 a 90 g/100ml de sangue (~4,5mM) Homeostase da glicose Necessidade
Unidade 1 Adaptação e Lesão Celular
 DISCIPLINA DE PATOLOGIA Prof. Renato Rossi Jr Unidade 1 Adaptação e Lesão Celular Objetivo da Unidade: Identificar e compreender os mecanismos envolvidos nas lesões celulares reversíveis e irreversíveis.
DISCIPLINA DE PATOLOGIA Prof. Renato Rossi Jr Unidade 1 Adaptação e Lesão Celular Objetivo da Unidade: Identificar e compreender os mecanismos envolvidos nas lesões celulares reversíveis e irreversíveis.
Biomassa de Banana Verde Integral- BBVI
 Biomassa de Banana Verde Integral- BBVI INFORMAÇÕES NUTRICIONAIS Porção de 100g (1/2 copo) Quantidade por porção g %VD(*) Valor Energético (kcal) 64 3,20 Carboidratos 14,20 4,73 Proteínas 1,30 1,73 Gorduras
Biomassa de Banana Verde Integral- BBVI INFORMAÇÕES NUTRICIONAIS Porção de 100g (1/2 copo) Quantidade por porção g %VD(*) Valor Energético (kcal) 64 3,20 Carboidratos 14,20 4,73 Proteínas 1,30 1,73 Gorduras
Hormonas e mensageiros secundários
 Hormonas e mensageiros secundários Interrelação entre os tecidos Comunicação entre os principais tecidos Fígado tecido adiposo hormonas sistema nervoso substratos em circulação músculo cérebro 1 Um exemplo
Hormonas e mensageiros secundários Interrelação entre os tecidos Comunicação entre os principais tecidos Fígado tecido adiposo hormonas sistema nervoso substratos em circulação músculo cérebro 1 Um exemplo
RESUMOS SIMPLES...156
 155 RESUMOS SIMPLES...156 156 RESUMOS SIMPLES CARNEIRO, NELSON HILÁRIO... 159 CARNEIRO, NELSON HILÁRIO... 157 CORTE, MARIANA ZANGIROLAME... 159 CORTE, MARIANA ZANGIROLAME... 157 GARCIA JUNIOR, JAIR RODRIGUES...
155 RESUMOS SIMPLES...156 156 RESUMOS SIMPLES CARNEIRO, NELSON HILÁRIO... 159 CARNEIRO, NELSON HILÁRIO... 157 CORTE, MARIANA ZANGIROLAME... 159 CORTE, MARIANA ZANGIROLAME... 157 GARCIA JUNIOR, JAIR RODRIGUES...
Os efeitos endocrinológicos na cirurgia da obesidade.
 Os efeitos endocrinológicos na cirurgia da obesidade. Dr. Izidoro de Hiroki Flumignan Médico endocrinologista e sanitarista Equipe CETOM Centro de Estudos e Tratamento para a Obesidade Mórbida. Diretor
Os efeitos endocrinológicos na cirurgia da obesidade. Dr. Izidoro de Hiroki Flumignan Médico endocrinologista e sanitarista Equipe CETOM Centro de Estudos e Tratamento para a Obesidade Mórbida. Diretor
Diabetes Mellitus em animais de companhia. Natália Leonel Ferreira 2º ano Medicina Veterinária
 Diabetes Mellitus em animais de companhia Natália Leonel Ferreira 2º ano Medicina Veterinária O que é Diabetes Mellitus? É uma doença em que o metabolismo da glicose fica prejudicado pela falta ou má absorção
Diabetes Mellitus em animais de companhia Natália Leonel Ferreira 2º ano Medicina Veterinária O que é Diabetes Mellitus? É uma doença em que o metabolismo da glicose fica prejudicado pela falta ou má absorção
ALTERAÇÕES METABÓLICAS NA GRAVIDEZ
 ALTERAÇÕES METABÓLICAS NA GRAVIDEZ CUSTO ENERGÉTICO DA GRAVIDEZ CRESCIMENTO E DESENVOLVIMENTO FETAL SÍNTESE DE TECIDO MATERNO 80.000 kcal ou 300 Kcal por dia 2/4 médios 390 Kcal depósito de gordura- fase
ALTERAÇÕES METABÓLICAS NA GRAVIDEZ CUSTO ENERGÉTICO DA GRAVIDEZ CRESCIMENTO E DESENVOLVIMENTO FETAL SÍNTESE DE TECIDO MATERNO 80.000 kcal ou 300 Kcal por dia 2/4 médios 390 Kcal depósito de gordura- fase
VI CURSO DE ATUALIZAÇÃO EM DIABETES DIETOTERAPIA ACADÊMICA LIGA DE DIABETES ÂNGELA MENDONÇA
 VI CURSO DE ATUALIZAÇÃO EM DIABETES DIETOTERAPIA ACADÊMICA ÂNGELA MENDONÇA LIGA DE DIABETES A intervenção nutricional pode melhorar o controle glicêmico. Redução de 1.0 a 2.0% nos níveis de hemoglobina
VI CURSO DE ATUALIZAÇÃO EM DIABETES DIETOTERAPIA ACADÊMICA ÂNGELA MENDONÇA LIGA DE DIABETES A intervenção nutricional pode melhorar o controle glicêmico. Redução de 1.0 a 2.0% nos níveis de hemoglobina
Butylene Glycol; Water (Aqua); Dihydromyricetin. Modelador do tecido adiposo: a solução cosmética para o tratamento da gordura localizada.
 Produto INCI Definição MYRICELINE Butylene Glycol; Water (Aqua); Dihydromyricetin Modelador do tecido adiposo: a solução cosmética para o tratamento da gordura localizada. Propriedades Os tratamentos cosméticos
Produto INCI Definição MYRICELINE Butylene Glycol; Water (Aqua); Dihydromyricetin Modelador do tecido adiposo: a solução cosmética para o tratamento da gordura localizada. Propriedades Os tratamentos cosméticos
DIABETES MELLITUS. Ricardo Rodrigues Cardoso Educação Física e Ciências do DesportoPUC-RS
 DIABETES MELLITUS Ricardo Rodrigues Cardoso Educação Física e Ciências do DesportoPUC-RS Segundo a Organização Mundial da Saúde, existem atualmente cerca de 171 milhões de indivíduos diabéticos no mundo.
DIABETES MELLITUS Ricardo Rodrigues Cardoso Educação Física e Ciências do DesportoPUC-RS Segundo a Organização Mundial da Saúde, existem atualmente cerca de 171 milhões de indivíduos diabéticos no mundo.
Saiba quais são os diferentes tipos de diabetes
 Saiba quais são os diferentes tipos de diabetes Diabetes é uma doença ocasionada pela total falta de produção de insulina pelo pâncreas ou pela quantidade insuficiente da substância no corpo. A insulina
Saiba quais são os diferentes tipos de diabetes Diabetes é uma doença ocasionada pela total falta de produção de insulina pelo pâncreas ou pela quantidade insuficiente da substância no corpo. A insulina
A patroa quer emagrecer
 A patroa quer emagrecer A UU L AL A Andando pela rua, você passa em frente a uma farmácia e resolve entrar para conferir seu peso na balança. E aí vem aquela surpresa: uns quilinhos a mais, ou, em outros
A patroa quer emagrecer A UU L AL A Andando pela rua, você passa em frente a uma farmácia e resolve entrar para conferir seu peso na balança. E aí vem aquela surpresa: uns quilinhos a mais, ou, em outros
Disciplina de Fisiologia Veterinária. GH e PROLACTINA. Prof. Fabio Otero Ascoli
 Disciplina de Fisiologia Veterinária GH e PROLACTINA Prof. Fabio Otero Ascoli GH Sinônimos: Hormônio do crescimento ou somatotrópico ou somatotropina Histologia: Em torno de 30 a 40% das células da hipófise
Disciplina de Fisiologia Veterinária GH e PROLACTINA Prof. Fabio Otero Ascoli GH Sinônimos: Hormônio do crescimento ou somatotrópico ou somatotropina Histologia: Em torno de 30 a 40% das células da hipófise
ORIENTAÇÕES PARA O PROFESSOR PRESENCIAL
 ORIENTAÇÕES PARA O PROFESSOR PRESENCIAL Componente Curriculares Educação Física Professores Ministrantes: Kim Raone e Marcus Marins Série/ Ano letivo: 2º ano/ 2014 Data: 26/03/2014 AULA 5.1 Conteúdo: Doenças
ORIENTAÇÕES PARA O PROFESSOR PRESENCIAL Componente Curriculares Educação Física Professores Ministrantes: Kim Raone e Marcus Marins Série/ Ano letivo: 2º ano/ 2014 Data: 26/03/2014 AULA 5.1 Conteúdo: Doenças
Capacidade de organizar os produtos da digestão usando a energia extraída dos mesmos produtos da digestão (REGULAÇÃO)
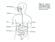 Capacidade de organizar os produtos da digestão usando a energia extraída dos mesmos produtos da digestão (REGULAÇÃO) As proteínas são digeridas até aminoácidos, as gorduras (triglicérides) até glicerol
Capacidade de organizar os produtos da digestão usando a energia extraída dos mesmos produtos da digestão (REGULAÇÃO) As proteínas são digeridas até aminoácidos, as gorduras (triglicérides) até glicerol
Visão geral dos antidiabéticos orais tradicionais: secretagogos, inibidores da alfa-glicosidase e sensibilizadores de insulina
 Visão geral dos antidiabéticos orais tradicionais: secretagogos, inibidores da alfa-glicosidase e sensibilizadores de insulina INTRODUÇÃO O controle da hiperglicemia em longo prazo é essencial para a manutenção
Visão geral dos antidiabéticos orais tradicionais: secretagogos, inibidores da alfa-glicosidase e sensibilizadores de insulina INTRODUÇÃO O controle da hiperglicemia em longo prazo é essencial para a manutenção
Disciplina: FISIOLOGIA CELULAR CONTROLE DA HOMEOSTASE, COMUNICAÇÃO E INTEGRAÇÃO DO CORPO HUMANO (10h)
 Ementário: Disciplina: FISIOLOGIA CELULAR CONTROLE DA HOMEOSTASE, COMUNICAÇÃO E INTEGRAÇÃO DO CORPO HUMANO (10h) Ementa: Organização Celular. Funcionamento. Homeostasia. Diferenciação celular. Fisiologia
Ementário: Disciplina: FISIOLOGIA CELULAR CONTROLE DA HOMEOSTASE, COMUNICAÇÃO E INTEGRAÇÃO DO CORPO HUMANO (10h) Ementa: Organização Celular. Funcionamento. Homeostasia. Diferenciação celular. Fisiologia
M E T B O L I S M O CATABOLISMO ANABOLISMO
 METABOLISMO É o conjunto das reações químicas que ocorrem num organismo vivo com o fim de promover a satisfação de necessidades estruturais e energéticas. ...metabolismo Do ponto de vista físico-químico,
METABOLISMO É o conjunto das reações químicas que ocorrem num organismo vivo com o fim de promover a satisfação de necessidades estruturais e energéticas. ...metabolismo Do ponto de vista físico-químico,
DIABETES MELLITUS. Prof. Claudia Witzel
 DIABETES MELLITUS Diabetes mellitus Definição Aumento dos níveis de glicose no sangue, e diminuição da capacidade corpórea em responder à insulina e ou uma diminuição ou ausência de insulina produzida
DIABETES MELLITUS Diabetes mellitus Definição Aumento dos níveis de glicose no sangue, e diminuição da capacidade corpórea em responder à insulina e ou uma diminuição ou ausência de insulina produzida
Colesterol O que é Isso? Trabalhamos pela vida
 Colesterol O que é Isso? X O que é o Colesterol? Colesterol é uma gordura encontrada apenas nos animais Importante para a vida: Estrutura do corpo humano (células) Crescimento Reprodução Produção de vit
Colesterol O que é Isso? X O que é o Colesterol? Colesterol é uma gordura encontrada apenas nos animais Importante para a vida: Estrutura do corpo humano (células) Crescimento Reprodução Produção de vit
O que é O que é. colesterol?
 O que é O que é colesterol? 1. O que é colesterol alto e por que ele é ruim? Apesar de a dislipidemia (colesterol alto) ser considerada uma doença extremamente prevalente no Brasil e no mundo, não existem
O que é O que é colesterol? 1. O que é colesterol alto e por que ele é ruim? Apesar de a dislipidemia (colesterol alto) ser considerada uma doença extremamente prevalente no Brasil e no mundo, não existem
Congresso do Desporto Desporto, Saúde e Segurança
 Congresso do Desporto Desporto, Saúde e Segurança Projecto Mexa-se em Bragança Organização: Pedro Miguel Queirós Pimenta Magalhães E-mail: mexaseembraganca@ipb.pt Web: http://www.mexaseembraganca.ipb.pt
Congresso do Desporto Desporto, Saúde e Segurança Projecto Mexa-se em Bragança Organização: Pedro Miguel Queirós Pimenta Magalhães E-mail: mexaseembraganca@ipb.pt Web: http://www.mexaseembraganca.ipb.pt
Figura 1: peridrociclopentanofenantreno
 COLESTEROL A n a L a u r a B u e n o Esteróides são álcoois de alto peso molecular. São compostos lipossolúveis muito importantes na fisiologia humana. Os esteróis possuem uma estrutura básica chamada
COLESTEROL A n a L a u r a B u e n o Esteróides são álcoois de alto peso molecular. São compostos lipossolúveis muito importantes na fisiologia humana. Os esteróis possuem uma estrutura básica chamada
ALTERAÇÕES METABÓLICAS NO PERFIL LIPÍDICO E GLICÊMICO DE PACIENTES HIV POSITIVOS QUE FAZEM USO DE ANTIRETROVIRAIS
 ALTERAÇÕES METABÓLICAS NO PERFIL LIPÍDICO E GLICÊMICO DE PACIENTES HIV POSITIVOS QUE FAZEM USO DE ANTIRETROVIRAIS Greice Rodrigues Bittencourt Introdução A terapia antiretroviral contemporânea (TARV) baseado
ALTERAÇÕES METABÓLICAS NO PERFIL LIPÍDICO E GLICÊMICO DE PACIENTES HIV POSITIVOS QUE FAZEM USO DE ANTIRETROVIRAIS Greice Rodrigues Bittencourt Introdução A terapia antiretroviral contemporânea (TARV) baseado
Diabetes Gestacional
 Diabetes Gestacional Introdução O diabetes é uma doença que faz com que o organismo tenha dificuldade para controlar o açúcar no sangue. O diabetes que se desenvolve durante a gestação é chamado de diabetes
Diabetes Gestacional Introdução O diabetes é uma doença que faz com que o organismo tenha dificuldade para controlar o açúcar no sangue. O diabetes que se desenvolve durante a gestação é chamado de diabetes
ENFRENTAMENTO DA OBESIDADE ABORDAGEM TERAPÊUTICA
 ENFRENTAMENTO DA OBESIDADE ABORDAGEM TERAPÊUTICA Obesidade 300 mil mortes / ano; 100 bi dólares / ano; O excesso de peso (IMC >25) acomete de 15% a 60% da população de todos os países civilizados. EUA...
ENFRENTAMENTO DA OBESIDADE ABORDAGEM TERAPÊUTICA Obesidade 300 mil mortes / ano; 100 bi dólares / ano; O excesso de peso (IMC >25) acomete de 15% a 60% da população de todos os países civilizados. EUA...
RESENHA: Novas perspectivas na luta contra a dependência química provocada pela cocaína.
 RESENHA: Novas perspectivas na luta contra a dependência química provocada pela cocaína. FONTE: Yao, L. et al. (2010) Nature Medicine 16 (9), 1024. Contribuição de Rodolfo do Couto Maia (Doutorando do
RESENHA: Novas perspectivas na luta contra a dependência química provocada pela cocaína. FONTE: Yao, L. et al. (2010) Nature Medicine 16 (9), 1024. Contribuição de Rodolfo do Couto Maia (Doutorando do
Bases Moleculares da Obesidade e Diabetes. IGF- I System. Carlos Cas(lho de Barros
 Bases Moleculares da Obesidade e Diabetes IGF- I System Carlos Cas(lho de Barros Visão Geral do Sistema IGF-I - É o maior mediador do crescimento intra uterino e pós natal - Receptor IGF- I crescimento
Bases Moleculares da Obesidade e Diabetes IGF- I System Carlos Cas(lho de Barros Visão Geral do Sistema IGF-I - É o maior mediador do crescimento intra uterino e pós natal - Receptor IGF- I crescimento
AGENTE DE FÉ E DO CORAÇÃO PASTORAL NACIONAL DA SAÚDE 04 de outubro de 2013. Dislipidemias
 AGENTE DE FÉ E DO CORAÇÃO PASTORAL NACIONAL DA SAÚDE 04 de outubro de 2013 Dislipidemias Raul D. Santos Unidade Clínica de Lípides InCor-HCFMUSP Faculdade de Medicina da USP Metabolismo do colesterol,
AGENTE DE FÉ E DO CORAÇÃO PASTORAL NACIONAL DA SAÚDE 04 de outubro de 2013 Dislipidemias Raul D. Santos Unidade Clínica de Lípides InCor-HCFMUSP Faculdade de Medicina da USP Metabolismo do colesterol,
0800 30 30 03 www.unimedbh.com.br
 ANS - Nº 34.388-9 0800 30 30 03 www.unimedbh.com.br Março 2007 Programa de Atenção ao Diabetes O que é diabetes? AUnimed-BH preocupa-se com a saúde e o bem-estar dos seus clientes, por isso investe em
ANS - Nº 34.388-9 0800 30 30 03 www.unimedbh.com.br Março 2007 Programa de Atenção ao Diabetes O que é diabetes? AUnimed-BH preocupa-se com a saúde e o bem-estar dos seus clientes, por isso investe em
3ªsérie B I O L O G I A
 3.1 QUESTÃO 1 Três consumidores, A, B e C, compraram, cada um deles, uma bebida em embalagem longa vida, adequada às suas respectivas dietas. As tabelas abaixo trazem informações nutricionais sobre cada
3.1 QUESTÃO 1 Três consumidores, A, B e C, compraram, cada um deles, uma bebida em embalagem longa vida, adequada às suas respectivas dietas. As tabelas abaixo trazem informações nutricionais sobre cada
Câncer de Próstata. Fernando Magioni Enfermeiro do Trabalho
 Câncer de Próstata Fernando Magioni Enfermeiro do Trabalho O que é próstata? A próstata é uma glândula que só o homem possui e que se localiza na parte baixa do abdômen. Ela é um órgão muito pequeno, tem
Câncer de Próstata Fernando Magioni Enfermeiro do Trabalho O que é próstata? A próstata é uma glândula que só o homem possui e que se localiza na parte baixa do abdômen. Ela é um órgão muito pequeno, tem
Tratamento de diabetes: insulina e anti-diabéticos. Profa. Dra. Fernanda Datti
 Tratamento de diabetes: insulina e anti-diabéticos Profa. Dra. Fernanda Datti Pâncreas Ilhotas de Langerhans células beta insulina células alfa glucagon células gama somatostatina regulação das atividades
Tratamento de diabetes: insulina e anti-diabéticos Profa. Dra. Fernanda Datti Pâncreas Ilhotas de Langerhans células beta insulina células alfa glucagon células gama somatostatina regulação das atividades
EPIGENÉTICA E NUTRIÇÃO MATERNA. Augusto Schneider Faculdade de Nutrição Universidade Federal de Pelotas
 EPIGENÉTICA E NUTRIÇÃO MATERNA Augusto Schneider Faculdade de Nutrição Universidade Federal de Pelotas EPIGENÉTICA Estudo da variação herdável que ocorre sem mudança na sequência do DNA Mudanças de longo
EPIGENÉTICA E NUTRIÇÃO MATERNA Augusto Schneider Faculdade de Nutrição Universidade Federal de Pelotas EPIGENÉTICA Estudo da variação herdável que ocorre sem mudança na sequência do DNA Mudanças de longo
Estrutura adrenal. Função da medula adrenal. Função da medula adrenal. Funções do córtex adrenal. Funções do córtex adrenal. Funções do córtex adrenal
 Estrutura adrenal Função da medula adrenal O córtex compreende a zona glomerulosa, secretora dos minelocorticóides, e a zona reticulada, secretora de glicocorticóides e dos androgênios adrenais. A medula
Estrutura adrenal Função da medula adrenal O córtex compreende a zona glomerulosa, secretora dos minelocorticóides, e a zona reticulada, secretora de glicocorticóides e dos androgênios adrenais. A medula
DOENÇA HEPÁTICA GORDUROSA NÃO ALCOÓLICA TRATAMENTO COM DROGAS
 DOENÇA HEPÁTICA GORDUROSA NÃO ALCOÓLICA TRATAMENTO COM DROGAS HELMA PINCHEMEL COTRIM FACULDADE DE MEDICINA UNIVERSIDADE FEDERAL DA BAHIA DOENÇA HEPÁTICA GORDUROSA NÃO ALCOÓLICA TRATAMENTO QUAIS OS OBJETIVOS?
DOENÇA HEPÁTICA GORDUROSA NÃO ALCOÓLICA TRATAMENTO COM DROGAS HELMA PINCHEMEL COTRIM FACULDADE DE MEDICINA UNIVERSIDADE FEDERAL DA BAHIA DOENÇA HEPÁTICA GORDUROSA NÃO ALCOÓLICA TRATAMENTO QUAIS OS OBJETIVOS?
Diminua seu tempo total de treino e queime mais gordura
 Diminua seu tempo total de treino e queime mais gordura Neste artigo vou mostrar o principal tipo de exercício para acelerar a queima de gordura sem se matar durante horas na academia. Vou mostrar e explicar
Diminua seu tempo total de treino e queime mais gordura Neste artigo vou mostrar o principal tipo de exercício para acelerar a queima de gordura sem se matar durante horas na academia. Vou mostrar e explicar
Alimentos de Soja - Uma Fonte de Proteína de Alta Qualidade
 Alimentos de Soja - Uma Fonte de Proteína de Alta Qualidade Documento de posição do Comité Consultivo Científico da ENSA Introdução As proteínas são um importante nutriente necessário para o crescimento
Alimentos de Soja - Uma Fonte de Proteína de Alta Qualidade Documento de posição do Comité Consultivo Científico da ENSA Introdução As proteínas são um importante nutriente necessário para o crescimento
Retinopatia Diabética
 Retinopatia Diabética A diabetes mellitus é uma desordem metabólica crónica caracterizada pelo excesso de níveis de glicose no sangue. A causa da hiper glicemia (concentração de glicose igual ou superior
Retinopatia Diabética A diabetes mellitus é uma desordem metabólica crónica caracterizada pelo excesso de níveis de glicose no sangue. A causa da hiper glicemia (concentração de glicose igual ou superior
Curso: Integração Metabólica
 Curso: Integração Metabólica Aula 7: Suprarrenal e tireoide Prof. Carlos Castilho de Barros Algumas pessoas podem apresentar distúrbios que provocam a obesidade. Estórias como Eu como pouco mas continuo
Curso: Integração Metabólica Aula 7: Suprarrenal e tireoide Prof. Carlos Castilho de Barros Algumas pessoas podem apresentar distúrbios que provocam a obesidade. Estórias como Eu como pouco mas continuo
Alterações Metabolismo Carboidratos DIABETES
 5.5.2009 Alterações Metabolismo Carboidratos DIABETES Introdução Diabetes Mellitus é uma doença metabólica, causada pelo aumento da quantidade de glicose sanguínea A glicose é a principal fonte de energia
5.5.2009 Alterações Metabolismo Carboidratos DIABETES Introdução Diabetes Mellitus é uma doença metabólica, causada pelo aumento da quantidade de glicose sanguínea A glicose é a principal fonte de energia
Teste seus conhecimentos: Caça-Palavras
 Teste seus conhecimentos: Caça-Palavras Batizada pelos médicos de diabetes mellitus, a doença ocorre quando há um aumento do açúcar no sangue. Dependendo dos motivos desse disparo, pode ser de dois tipos.
Teste seus conhecimentos: Caça-Palavras Batizada pelos médicos de diabetes mellitus, a doença ocorre quando há um aumento do açúcar no sangue. Dependendo dos motivos desse disparo, pode ser de dois tipos.
Tópicos da Aula. Classificação CHO. Processo de Digestão 24/09/2012. Locais de estoque de CHO. Nível de concentração de glicose no sangue
 Universidade Estadual Paulista DIABETES E EXERCÍCIO FÍSICO Profª Dnda Camila Buonani da Silva Disciplina: Atividade Física e Saúde Tópicos da Aula 1. Carboidrato como fonte de energia 2. Papel da insulina
Universidade Estadual Paulista DIABETES E EXERCÍCIO FÍSICO Profª Dnda Camila Buonani da Silva Disciplina: Atividade Física e Saúde Tópicos da Aula 1. Carboidrato como fonte de energia 2. Papel da insulina
Água e Solução Tampão
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
CONTROLE E INTEGRAÇÂO
 CONTROLE E INTEGRAÇÂO A homeostase é atingida através de uma série de mecanismos reguladores que envolve todos os órgãos do corpo. Dois sistemas, entretanto, são destinados exclusivamente para a regulação
CONTROLE E INTEGRAÇÂO A homeostase é atingida através de uma série de mecanismos reguladores que envolve todos os órgãos do corpo. Dois sistemas, entretanto, são destinados exclusivamente para a regulação
8.2 - Mecanismos envolvidos na alteração do metabolismo hepático entre os estado bem alimentado e o estado de jejum
 UNIDADE 8 - INTERRELAÇÕES METABÓLICAS 8.1 - Ciclo Jejum-alimentação 8.2 - Mecanismos envolvidos na alteração do metabolismo hepático entre os estado bem alimentado e o estado de jejum 8.3 - Inter-relações
UNIDADE 8 - INTERRELAÇÕES METABÓLICAS 8.1 - Ciclo Jejum-alimentação 8.2 - Mecanismos envolvidos na alteração do metabolismo hepático entre os estado bem alimentado e o estado de jejum 8.3 - Inter-relações
COMPOSIÇÃO QUÍMICA DA CARNE. Profª Sandra Carvalho
 COMPOSIÇÃO QUÍMICA DA CARNE Profª Sandra Carvalho A carne magra: 75% de água 21 a 22% de proteína 1 a 2% de gordura 1% de minerais menos de 1% de carboidratos A carne magra dos diferentes animais de abate
COMPOSIÇÃO QUÍMICA DA CARNE Profª Sandra Carvalho A carne magra: 75% de água 21 a 22% de proteína 1 a 2% de gordura 1% de minerais menos de 1% de carboidratos A carne magra dos diferentes animais de abate
exercício físico na obesidade e síndrome metabólica
 exercício físico na obesidade e síndrome metabólica CONCEITOS Atividade Física é qualquer movimento corporal produzido pelos músculos esqueléticos que resultam em gasto energético; Exercício é uma atividade
exercício físico na obesidade e síndrome metabólica CONCEITOS Atividade Física é qualquer movimento corporal produzido pelos músculos esqueléticos que resultam em gasto energético; Exercício é uma atividade
47 Por que preciso de insulina?
 A U A UL LA Por que preciso de insulina? A Medicina e a Biologia conseguiram decifrar muitos dos processos químicos dos seres vivos. As descobertas que se referem ao corpo humano chamam mais a atenção
A U A UL LA Por que preciso de insulina? A Medicina e a Biologia conseguiram decifrar muitos dos processos químicos dos seres vivos. As descobertas que se referem ao corpo humano chamam mais a atenção
Prescrição Dietética
 Prescrição Dietética Quantitativo Cálculo de Dietas Cálculo de dietas estimar as necessidades energéticas de um indivíduo (atividade física, estágio da vida e composição corporal) Necessidades energéticas
Prescrição Dietética Quantitativo Cálculo de Dietas Cálculo de dietas estimar as necessidades energéticas de um indivíduo (atividade física, estágio da vida e composição corporal) Necessidades energéticas
à diabetes? As complicações resultam da de açúcar no sangue. São frequentes e graves podendo (hiperglicemia).
 diabetes Quando Acidente a glicemia vascular (glicose cerebral no sangue) (tromboses), sobe, o pâncreas uma das principais O que Quais é a diabetes? as complicações associadas à diabetes? produz causas
diabetes Quando Acidente a glicemia vascular (glicose cerebral no sangue) (tromboses), sobe, o pâncreas uma das principais O que Quais é a diabetes? as complicações associadas à diabetes? produz causas
CAPÍTULO 6 TECIDO MUSCULAR
 CAPÍTULO 6 TECIDO MUSCULAR 1 Características Histológicas O tecido muscular é constituído por células alongadas que possuem grande quantidade de filamentos citoplasmáticos com proteínas contráteis. Esse
CAPÍTULO 6 TECIDO MUSCULAR 1 Características Histológicas O tecido muscular é constituído por células alongadas que possuem grande quantidade de filamentos citoplasmáticos com proteínas contráteis. Esse
Colesterol 3. Que tipos de colesterol existem? 3. Que factores afectam os níveis de colesterol? 4. Quando está o colesterol demasiado elevado?
 Colesterol Colesterol 3 Que tipos de colesterol existem? 3 Que factores afectam os níveis de colesterol? 4 Quando está o colesterol demasiado elevado? 4 Como reduzir o colesterol e o risco de doença cardiovascular?
Colesterol Colesterol 3 Que tipos de colesterol existem? 3 Que factores afectam os níveis de colesterol? 4 Quando está o colesterol demasiado elevado? 4 Como reduzir o colesterol e o risco de doença cardiovascular?
UNIVERSIDADE DE SANTA CRUZ DO SUL - UNISC DEPARTAMENTO DE FARMÁCIA DISCIPLINA DE FISIOLOGIA GERAL HORMÔNIOS MASCULINOS
 UNIVERSIDADE DE SANTA CRUZ DO SUL - UNISC DEPARTAMENTO DE FARMÁCIA DISCIPLINA DE FISIOLOGIA GERAL HORMÔNIOS MASCULINOS Andiara Onizzolo Marques Isadora Schmachtenberg Manoela Zaccani Maristela Ullrich
UNIVERSIDADE DE SANTA CRUZ DO SUL - UNISC DEPARTAMENTO DE FARMÁCIA DISCIPLINA DE FISIOLOGIA GERAL HORMÔNIOS MASCULINOS Andiara Onizzolo Marques Isadora Schmachtenberg Manoela Zaccani Maristela Ullrich
FUNDAMENTOS DA ESTEATOSE HEPÁTICA
 FUNDAMENTOS DA ESTEATOSE HEPÁTICA GORDURA BRANCA X MARROM SINDROME METABÓLICA RESISTÊNCIA INSULÍNICA HIPERINSULINISMO ÍNDICE GLICÊMICO Dr. Izidoro de Hiroki Flumignan & EQUIPE MULTIDISCIPLINAR MEDICINA
FUNDAMENTOS DA ESTEATOSE HEPÁTICA GORDURA BRANCA X MARROM SINDROME METABÓLICA RESISTÊNCIA INSULÍNICA HIPERINSULINISMO ÍNDICE GLICÊMICO Dr. Izidoro de Hiroki Flumignan & EQUIPE MULTIDISCIPLINAR MEDICINA
Por outro lado, na avaliação citológica e tecidual, o câncer tem seis fases, conhecidas por fases biológicas do câncer, conforme se segue:
 8 - O câncer também tem fases de desenvolvimento? Sim, o câncer tem fases de desenvolvimento que podem ser avaliadas de diferentes formas. Na avaliação clínica feita por médicos é possível identificar
8 - O câncer também tem fases de desenvolvimento? Sim, o câncer tem fases de desenvolvimento que podem ser avaliadas de diferentes formas. Na avaliação clínica feita por médicos é possível identificar
DOENÇAS CARDÍACAS NA INSUFICIÊNCIA RENAL
 DOENÇAS CARDÍACAS NA INSUFICIÊNCIA RENAL As doenças do coração são muito freqüentes em pacientes com insuficiência renal. Assim, um cuidado especial deve ser tomado, principalmente, na prevenção e no controle
DOENÇAS CARDÍACAS NA INSUFICIÊNCIA RENAL As doenças do coração são muito freqüentes em pacientes com insuficiência renal. Assim, um cuidado especial deve ser tomado, principalmente, na prevenção e no controle
azul NOVEMBRO azul Saúde também é coisa de homem. Doenças Cardiovasculares (DCV)
 Doenças Cardiovasculares (DCV) O que são as Doenças Cardiovasculares? De um modo geral, são o conjunto de doenças que afetam o aparelho cardiovascular, designadamente o coração e os vasos sanguíneos. Quais
Doenças Cardiovasculares (DCV) O que são as Doenças Cardiovasculares? De um modo geral, são o conjunto de doenças que afetam o aparelho cardiovascular, designadamente o coração e os vasos sanguíneos. Quais
5 Alimentos que Queimam Gordura www.mmn-global.com/aumenteseumetabolismo IMPRIMIR PARA UMA MAIS FÁCIL CONSULTA
 IMPRIMIR PARA UMA MAIS FÁCIL CONSULTA ÍNDICE Alimentos que Queimam Gordura TORANJA CHA VERDE E CHA VERMELHO AVEIA BROCOLOS SALMÃO TORANJA A dieta da Toranja já vem sendo discutida por algum tempo, mas
IMPRIMIR PARA UMA MAIS FÁCIL CONSULTA ÍNDICE Alimentos que Queimam Gordura TORANJA CHA VERDE E CHA VERMELHO AVEIA BROCOLOS SALMÃO TORANJA A dieta da Toranja já vem sendo discutida por algum tempo, mas
Saúde da mulher em idade fértil e de crianças com até 5 anos de idade dados da PNDS 2006
 Saúde da mulher em idade fértil e de crianças com até 5 anos de idade dados da PNDS 2006 José Cechin Superintendente Executivo Francine Leite Carina Burri Martins Esse texto compara as morbidades referidas
Saúde da mulher em idade fértil e de crianças com até 5 anos de idade dados da PNDS 2006 José Cechin Superintendente Executivo Francine Leite Carina Burri Martins Esse texto compara as morbidades referidas
Por não serem solúveis na água, os lípidos circulam no plasma sob a forma de lipoproteínas. Os ácidos gordos livres circulam ligados à albumina.
 LIPOPROTEÍNAS E DISLIPIDÉMIAS Por não serem solúveis na água, os lípidos circulam no plasma sob a forma de lipoproteínas. Os ácidos gordos livres circulam ligados à albumina. Transporte dos lípidos Classificação
LIPOPROTEÍNAS E DISLIPIDÉMIAS Por não serem solúveis na água, os lípidos circulam no plasma sob a forma de lipoproteínas. Os ácidos gordos livres circulam ligados à albumina. Transporte dos lípidos Classificação
Perfil Lipídico. Prof. Fernando Ananias FUNÇÃO DOS LIPÍDIOS
 Perfil Lipídico Prof. Fernando Ananias FUNÇÃO DOS LIPÍDIOS Maior reserva corporal de energia tecidos muscular e subcutâneo Proteção contra traumatismo: 4% Isolamento térmico Transportadores de vitaminas
Perfil Lipídico Prof. Fernando Ananias FUNÇÃO DOS LIPÍDIOS Maior reserva corporal de energia tecidos muscular e subcutâneo Proteção contra traumatismo: 4% Isolamento térmico Transportadores de vitaminas
Convivendo bem com a doença renal. Guia de Nutrição e Diabetes Você é capaz, alimente-se bem!
 Convivendo bem com a doença renal Guia de Nutrição e Diabetes Você é capaz, alimente-se bem! Nutrição e dieta para diabéticos: Introdução Mesmo sendo um paciente diabético em diálise, a sua dieta ainda
Convivendo bem com a doença renal Guia de Nutrição e Diabetes Você é capaz, alimente-se bem! Nutrição e dieta para diabéticos: Introdução Mesmo sendo um paciente diabético em diálise, a sua dieta ainda
Dra. Kátia R. P. de Araújo Sgrillo. sgrillo.ita@ftc.br
 Dra. Kátia R. P. de Araújo Sgrillo sgrillo.ita@ftc.br Lipídeos são compostos guardados em grandes quantidades como triglicerídeos neutros e representam 90% da dieta. São altamente insolúveis, podendo ser
Dra. Kátia R. P. de Araújo Sgrillo sgrillo.ita@ftc.br Lipídeos são compostos guardados em grandes quantidades como triglicerídeos neutros e representam 90% da dieta. São altamente insolúveis, podendo ser
RELEPTIN Irvingia gabonensis extrato
 RELEPTIN Irvingia gabonensis extrato Redução de peso, colesterol e glicemia. Reduz medidas pela queima de gordura ao mesmo tempo em que controla a dislipidemia, reduzindo o colesterol LDL e triglicérides
RELEPTIN Irvingia gabonensis extrato Redução de peso, colesterol e glicemia. Reduz medidas pela queima de gordura ao mesmo tempo em que controla a dislipidemia, reduzindo o colesterol LDL e triglicérides
CORRELAÇÃO DA INSUFICIÊNCIA RENAL E ANEMIA EM PACIENTES NORMOGLICEMICOS E HIPERGLICEMICOS EM UM LABORATÓRIO DA CIDADE DE JUAZEIRO DO NORTE, CE
 CORRELAÇÃO DA INSUFICIÊNCIA RENAL E ANEMIA EM PACIENTES NORMOGLICEMICOS E HIPERGLICEMICOS EM UM LABORATÓRIO DA CIDADE DE JUAZEIRO DO NORTE, CE Janaína Esmeraldo Rocha, Faculdade Leão Sampaio, janainaesmeraldo@gmail.com
CORRELAÇÃO DA INSUFICIÊNCIA RENAL E ANEMIA EM PACIENTES NORMOGLICEMICOS E HIPERGLICEMICOS EM UM LABORATÓRIO DA CIDADE DE JUAZEIRO DO NORTE, CE Janaína Esmeraldo Rocha, Faculdade Leão Sampaio, janainaesmeraldo@gmail.com
Dia Mundial da Diabetes - 14 Novembro de 2012 Controle a diabetes antes que a diabetes o controle a si
 Dia Mundial da Diabetes - 14 Novembro de 2012 Controle a diabetes antes que a diabetes o controle a si A função da insulina é fazer com o que o açúcar entre nas células do nosso corpo, para depois poder
Dia Mundial da Diabetes - 14 Novembro de 2012 Controle a diabetes antes que a diabetes o controle a si A função da insulina é fazer com o que o açúcar entre nas células do nosso corpo, para depois poder
O corpo humano está organizado desde o mais simples até o mais complexo, ou seja, do átomo microscópico ao complexo organismo humano macroscópico.
 1 O corpo humano está organizado desde o mais simples até o mais complexo, ou seja, do átomo microscópico ao complexo organismo humano macroscópico. Note essa organização na figura abaixo. - Átomos formam
1 O corpo humano está organizado desde o mais simples até o mais complexo, ou seja, do átomo microscópico ao complexo organismo humano macroscópico. Note essa organização na figura abaixo. - Átomos formam
Nestas últimas aulas irei abordar acerca das vitaminas. Acompanhe!
 Aula: 31 Temática: Vitaminas parte I Nestas últimas aulas irei abordar acerca das vitaminas. Acompanhe! Introdução O termo vitamina refere-se a um fator dietético essencial requerido por um organismo em
Aula: 31 Temática: Vitaminas parte I Nestas últimas aulas irei abordar acerca das vitaminas. Acompanhe! Introdução O termo vitamina refere-se a um fator dietético essencial requerido por um organismo em
Saúde e Desporto. Manuel Teixeira Veríssimo Hospitais da Universidade de Coimbra. Relação do Desporto com a Saúde
 Saúde e Desporto Manuel Teixeira Veríssimo Hospitais da Universidade de Coimbra Relação do Desporto com a Saúde Dum modo geral aceita-se que o desporto dá saúde Contudo, o desporto também comporta malefícios
Saúde e Desporto Manuel Teixeira Veríssimo Hospitais da Universidade de Coimbra Relação do Desporto com a Saúde Dum modo geral aceita-se que o desporto dá saúde Contudo, o desporto também comporta malefícios
PlanetaBio Resolução de Vestibulares UFRJ 2007 www.planetabio.com
 1-O gráfico a seguir mostra como variou o percentual de cepas produtoras de penicilinase da bactéria Neisseria gonorrhoeae obtidas de indivíduos com gonorréia no período de 1980 a 1990. A penicilinase
1-O gráfico a seguir mostra como variou o percentual de cepas produtoras de penicilinase da bactéria Neisseria gonorrhoeae obtidas de indivíduos com gonorréia no período de 1980 a 1990. A penicilinase
Complicações Metabólicas da Terapia Anti-retroviral
 Complicações Metabólicas da Terapia Anti-retroviral Dra. Daisy Maria Machado Universidade Federal de São Paulo Centro de Referência e Treinamento em DST-AIDS 2004 Terapia Anti-retroviral HAART: Redução
Complicações Metabólicas da Terapia Anti-retroviral Dra. Daisy Maria Machado Universidade Federal de São Paulo Centro de Referência e Treinamento em DST-AIDS 2004 Terapia Anti-retroviral HAART: Redução
EXERCÍCIOS ON LINE DE CIÊNCIAS 8 AN0
 EXERCÍCIOS ON LINE DE CIÊNCIAS 8 AN0 1- Que órgão do sistema nervoso central controla nosso ritmo respiratório? Bulbo 2- Os alvéolos são formados por uma única camada de células muito finas. Explique como
EXERCÍCIOS ON LINE DE CIÊNCIAS 8 AN0 1- Que órgão do sistema nervoso central controla nosso ritmo respiratório? Bulbo 2- Os alvéolos são formados por uma única camada de células muito finas. Explique como
Azul. Novembro. cosbem. Mergulhe nessa onda! A cor da coragem é azul. Mês de Conscientização, Preveção e Combate ao Câncer De Próstata.
 cosbem COORDENAÇÃO DE SAÚDE E BEM-ESTAR Novembro Azul Mês de Conscientização, Preveção e Combate ao Câncer De Próstata. Mergulhe nessa onda! A cor da coragem é azul. NOVEMBRO AZUL Mês de Conscientização,
cosbem COORDENAÇÃO DE SAÚDE E BEM-ESTAR Novembro Azul Mês de Conscientização, Preveção e Combate ao Câncer De Próstata. Mergulhe nessa onda! A cor da coragem é azul. NOVEMBRO AZUL Mês de Conscientização,
Em 2013 perderam-se 4 683 anos potenciais de vida devido à diabetes mellitus
 Dia Mundial da diabetes 14 de novembro 1983-2013 EMBARGO ATTÉ 13 DE NOVEMBRO DE 2014,, ÀS 11 HORAS Em 2013 perderam-se 4 683 anos potenciais de vida devido à diabetes mellitus Em 2013, as doenças endócrinas,
Dia Mundial da diabetes 14 de novembro 1983-2013 EMBARGO ATTÉ 13 DE NOVEMBRO DE 2014,, ÀS 11 HORAS Em 2013 perderam-se 4 683 anos potenciais de vida devido à diabetes mellitus Em 2013, as doenças endócrinas,
Pesquisa revela uma das causas de morte prematura na Rússia: a vodca
 Pesquisa revela uma das causas de morte prematura na Rússia: a vodca Post 02 Fevereiro 2014 By UNIAD Revista Veja - Álcool Estudo concluiu que risco de morte entre homens russos com menos de 55 anos pode
Pesquisa revela uma das causas de morte prematura na Rússia: a vodca Post 02 Fevereiro 2014 By UNIAD Revista Veja - Álcool Estudo concluiu que risco de morte entre homens russos com menos de 55 anos pode
Incretinomiméticos e inibidores de DPP-IV
 Bruno de Oliveira Sawan Rodrigo Ribeiro Incretinomiméticos e inibidores de DPP-IV Liga de Diabetes - UNIUBE GLP-1 GLP-1 é normalmente produzido pelas células neuroendócrinas L da mucosa intestinal Sua
Bruno de Oliveira Sawan Rodrigo Ribeiro Incretinomiméticos e inibidores de DPP-IV Liga de Diabetes - UNIUBE GLP-1 GLP-1 é normalmente produzido pelas células neuroendócrinas L da mucosa intestinal Sua
CAROLINE FERNANDES DOS SANTOS
 CAROLINE FERNANDES DOS SANTOS Agonistas PPAR (rosiglitazona, bezafibrato e fenofibrato) e alterações bioquímicas e estruturais em órgãos-alvo de camundongos C57BL/6 alimentados com dieta hiperlipídica
CAROLINE FERNANDES DOS SANTOS Agonistas PPAR (rosiglitazona, bezafibrato e fenofibrato) e alterações bioquímicas e estruturais em órgãos-alvo de camundongos C57BL/6 alimentados com dieta hiperlipídica
Bioenergética. Profa. Kalyne de Menezes Bezerra Cavalcanti
 Bioenergética Profa. Kalyne de Menezes Bezerra Cavalcanti Natal/RN Fevereiro de 2011 Substratos para o exercício O corpo utiliza nutrientes carboidratos, gorduras e proteínas consumidos diariamente para
Bioenergética Profa. Kalyne de Menezes Bezerra Cavalcanti Natal/RN Fevereiro de 2011 Substratos para o exercício O corpo utiliza nutrientes carboidratos, gorduras e proteínas consumidos diariamente para
Que tipos de Diabetes existem?
 Que tipos de Diabetes existem? -Diabetes Tipo 1 -também conhecida como Diabetes Insulinodependente -Diabetes Tipo 2 - Diabetes Gestacional -Outros tipos de Diabetes Organismo Saudável As células utilizam
Que tipos de Diabetes existem? -Diabetes Tipo 1 -também conhecida como Diabetes Insulinodependente -Diabetes Tipo 2 - Diabetes Gestacional -Outros tipos de Diabetes Organismo Saudável As células utilizam
Fisiologia do Sistema Endócrino-I
 Curso Preparatório para Residência em Enfermagem-2012 Fisiologia do Sistema Endócrino-I Prof. Fernando Ramos Gonçalves -Msc Glândulas endócrinas: Funções: Secreções de substâncias (hormônios) que atuam
Curso Preparatório para Residência em Enfermagem-2012 Fisiologia do Sistema Endócrino-I Prof. Fernando Ramos Gonçalves -Msc Glândulas endócrinas: Funções: Secreções de substâncias (hormônios) que atuam
Coach Marcelo Ruas Relatório Grátis do Programa 10 Semanas para Barriga Tanquinho
 Coach Marcelo Ruas Relatório Grátis do Programa 10 Semanas para Barriga Tanquinho Alimento I Toranja A dieta da Toranja já vem sendo discutida por algum tempo, mas não se sabia ao certo porque a Toranja
Coach Marcelo Ruas Relatório Grátis do Programa 10 Semanas para Barriga Tanquinho Alimento I Toranja A dieta da Toranja já vem sendo discutida por algum tempo, mas não se sabia ao certo porque a Toranja
INTRODUÇÃO À FISIOLOGIA. Profª. Juliana Delatim Simonato Rocha Lab. de Ecofisiologia Animal LEFA - CIF/CCB
 INTRODUÇÃO À FISIOLOGIA Profª. Juliana Delatim Simonato Rocha Lab. de Ecofisiologia Animal LEFA - CIF/CCB 1 Fisiologia é... Literalmente... Conhecimento da natureza O estudo do funcionamento dos organismos
INTRODUÇÃO À FISIOLOGIA Profª. Juliana Delatim Simonato Rocha Lab. de Ecofisiologia Animal LEFA - CIF/CCB 1 Fisiologia é... Literalmente... Conhecimento da natureza O estudo do funcionamento dos organismos
NECESSIDADES NUTRICIONAIS DO EXERCÍCIO
 Departamento de Fisiologia Curso: Educação Física NECESSIDADES NUTRICIONAIS DO EXERCÍCIO Aluno: Anderson de Oliveira Lemos Matrícula: 9612220 Abril/2002 Estrutura de Apresentação Líquidos Eletrólitos Energia
Departamento de Fisiologia Curso: Educação Física NECESSIDADES NUTRICIONAIS DO EXERCÍCIO Aluno: Anderson de Oliveira Lemos Matrícula: 9612220 Abril/2002 Estrutura de Apresentação Líquidos Eletrólitos Energia
Epidemiologia DIABETES MELLITUS
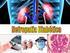 Epidemiologia DIABETES MELLITUS 300 milhões / mundo ( 5,9% população adulta) / Brasil : > 10 milhões Aumento progressivo : Longevidade, Síndrome metabólica Mortalidade anual : 3,8 milhões AVC, IAM... Amputação
Epidemiologia DIABETES MELLITUS 300 milhões / mundo ( 5,9% população adulta) / Brasil : > 10 milhões Aumento progressivo : Longevidade, Síndrome metabólica Mortalidade anual : 3,8 milhões AVC, IAM... Amputação
Coração Saudável! melhor dele?
 As doenças cardiovasculares (DCV s) - incluem as doenças coronarianas e o acidente vascular cerebral (AVC) também conhecido como derrame afetam pessoas de todas as idades, até mesmo mulheres e crianças.
As doenças cardiovasculares (DCV s) - incluem as doenças coronarianas e o acidente vascular cerebral (AVC) também conhecido como derrame afetam pessoas de todas as idades, até mesmo mulheres e crianças.
INSTITUIÇÃO: CENTRO UNIVERSITÁRIO DAS FACULDADES METROPOLITANAS UNIDAS
 TÍTULO: DIABETES MELLITUS TIPO II E O ANTIDIABÉTICO METFORMINA CATEGORIA: EM ANDAMENTO ÁREA: CIÊNCIAS BIOLÓGICAS E SAÚDE SUBÁREA: BIOMEDICINA INSTITUIÇÃO: CENTRO UNIVERSITÁRIO DAS FACULDADES METROPOLITANAS
TÍTULO: DIABETES MELLITUS TIPO II E O ANTIDIABÉTICO METFORMINA CATEGORIA: EM ANDAMENTO ÁREA: CIÊNCIAS BIOLÓGICAS E SAÚDE SUBÁREA: BIOMEDICINA INSTITUIÇÃO: CENTRO UNIVERSITÁRIO DAS FACULDADES METROPOLITANAS
Porque se cuidar é coisa de homem. Saúde do homem
 Porque se cuidar é coisa de homem. Saúde do homem SAÚDE DO HOMEM Por preconceito, muitos homens ainda resistem em procurar orientação médica ou submeter-se a exames preventivos, principalmente os de
Porque se cuidar é coisa de homem. Saúde do homem SAÚDE DO HOMEM Por preconceito, muitos homens ainda resistem em procurar orientação médica ou submeter-se a exames preventivos, principalmente os de
Diabetes - Introdução
 Diabetes - Introdução Diabetes Mellitus, conhecida simplesmente como diabetes, é uma disfunção do metabolismo de carboidratos, caracterizada pelo alto índice de açúcar no sangue (hiperglicemia) e presença
Diabetes - Introdução Diabetes Mellitus, conhecida simplesmente como diabetes, é uma disfunção do metabolismo de carboidratos, caracterizada pelo alto índice de açúcar no sangue (hiperglicemia) e presença
