DETECÇÃO E IDENTIFICAÇÃO MOLECULAR DE BACTÉRIAS ENTÉRICAS CAUSADORAS DE DIARREIA PARA DIAGNÓSTICO IN VITRO
|
|
|
- Maria do Loreto Azenha Flores
- 6 Há anos
- Visualizações:
Transcrição
1 CLART EnteroBac DETECÇÃO E IDENTIFICAÇÃO MOLECULAR DE BACTÉRIAS ENTÉRICAS CAUSADORAS DE DIARREIA PARA DIAGNÓSTICO IN VITRO 1
2 CLART e CLART-Strip são marcas registadas de GENOMICA Para mais informações e questões, não hesite em visitar GENOMICA, S.A.U. Alcarria, 7, Coslada, Madrid, Espanha Tel: , Fax: Versão 1 Junho de
3 ÍNDICE: 1. GLOSSÁRIO DE TERMOS 2. DESCRIÇÃO 3. COMPONENTES E CONSERVAÇÃO DO KIT 3.1. Reagentes de extração, purificação e amplificação 3.2. Reagentes de visualização 3.3. Outros componentes 4. MATERIAL ADICIONAL 4.1. Reagentes e material 4.2. Equipamento 5. PROCEDIMENTOS E RECOMENDAÇÕES DE MANIPULAÇÃO 5.1. Recomendações gerais 5.2. Precauções para a extração 5.3. Precauções para a visualização 6. AMOSTRAS: AMOSTRAS FECAIS 7. PROTOCOLOS DE TRABALHO 7.1. Extração automática do ADN de microrganismos presentes em amostras fecais 7.2. Reação de amplificação 7.3. Visualização do produto amplificado 8. LEITURA DE RESULTADOS 9. INTERPRETAÇÃO DE RESULTADOS 10. ESPECIFICAÇÕES TÉCNICAS E DE FUNCIONAMENTO 11. BIBLIOGRAFIA 3
4 1. GLOSSÁRIO DE TERMOS Consultar Instruções de Utilização Prazo de validade Dispositivo para diagnóstico in vitro Lote 20ºC 25ºC Conservar à temperatura ambiente 4ºC 8ºC Conservar entre 4 ºC e 8 ºC - 30ºC -18ºC Conservar entre -30 ºC e -18 ºC 4
5 2. DESCRIÇÃO CLART EnteroBac deteta a presença das seguintes bactérias entéricas causadoras de diarreia: Salmonella spp. (todas as espécies descritas) Shigella spp. (S. dysenteriae, S. Sonnei, S. boydii e S. flexneri) Yersinia enterocolítica Yersinia spp. (Y. pestis, Y. pseudotuberculosis, Y. enterocolítica) Campylobacter spp. (C. lari, C. laridis, C. upsaliensis, C. jejuni, C. coli) Campylobacter jejuni Campylobacter coli Escherichia coli enteropatogénica EPEC: (E. coli enterohemorrágica, E. coli enteroinvasiva, E. coli enterotoxigénica e E. coli enteropatogénica) Clostridium difficile B Aeromonas spp, produtores de aerolisina A deteção dos diferentes microrganismos é conseguida através da amplificação por PCR de uma codificação específica de regiões para as enterotoxinas e fatores de virulência para os microrganismos incluídos no kit e para genes constitutivos de Salmonella spp. e Campylobacter spp. A amplificação foi realizada em dois tipos diferentes de tubos de PCR. Os tubos de Mix 1 são brancos e permitem a amplificação e subsequente deteção de Shigella spp, Yersinia enterocolítica, Yersinia spp., Campylobacter coli, Campylobacter jejuni, Escherichia coli EPEC, Clostridium difficile B e Aeromonas produtoras de aerolisina. Os tubos de Mix 2 são verdes e contém tudo o que é necessário para a amplificação e deteção de Salmonella spp. e Campylobacter spp. A plataforma baseia-se numa micro matriz de baixa densidade, fixa na base de uma tira de 8 poços (CLART Strip-CS) (Figura 1), proporcionando um meio muito eficiente e fácil de usar o sistema. Esta tecnologia permite a deteção simultânea de múltiplos marcadores moleculares para uso diagnóstico, ao mesmo tempo que proporciona os controlos necessários para assegurar a fiabilidade dos resultados. Além disso, este sistema simplifica consideravelmente os processos de hibridização e visualização, quando comparado com os sistemas clássicos de micro matriz. 5
6 Figura 1: Plataformas CLART em forma de tira de 8 poços (CS). A hibridização do produto de PCR amplificado é detetada pela criação de um precipitado insolúvel nos locais de micro matriz, onde os produtos amplificados foram recolhidos por sondas. Este facto é conseguido utilizando oligonucleotídeos marcados com biotina. Os produtos de amplificação biotinilados hibridizam-se nas suas sondas específicas, ligadas à superfície de micro matriz, e imobilizam-se. Estes produtos biotinilados imobilizados são reconhecidos pela estreptavidina de um conjugado de estreptavidina-peroxidase, proporcionando assim atividade de peroxidase aos produtos hibridizados. Posteriormente, a atividade de peroxidase metabolizará a o-dianisidina e produzirá um produto insolúvel que se precipitará nos locais onde ocorreu a hibridização (Figura 2). Matriz de sondas Marcação Biotina Hibridização Conjugação Conjugado do catalisador Reação de revelação Substrato precipitado 6
7 Figura 2: Diagrama do método de visualização. As sondas, imobilizadas sobre a superfície, captam os seus produtos amplificados complementares marcados com biotina. Com a ajuda da biotina, o conjugado liga-se, neste caso, à estreptavidina-hrp (HorseRadish Peroxidase = Peroxidase de Armorácia). Devido à ação da HRP, o substrato de o- dianisidina produz uma precipitação no local de hibridização. 3. COMPONENTES E CONSERVAÇÃO DO KIT CLART EnteroBac Kit contém reagentes suficientes para a extração e análise de ADN de 48 amostras clínicas. Estes reagentes estão acondicionados em duas caixas distintas, dependendo da temperatura a que devem ser conservados. Todos os reagentes fornecidos são estáveis nas condições adequadas até ao prazo de validade indicado Tubos de amplificação Os tubos de amplificação contêm 45 µl de mistura de reação. Estão prontos a serem utilizados e devem ser conservados a -20ºC. Só o número necessário de tubos deve ser descongelado sobre gelo quando forem precisos, enquanto os restantes devem ser mantidos a 20ºC. No kit, estão incluídos dois tubos de amplificação diferentes: - Mix 1: Tubo branco. Amplificação de Shigella spp, Yersinia spp., Campylobacter coli, Campylobacter jejuni, Escherichia coli EPEC, Clostridium difficile e Aeromonas produtoras de aerolisina. Neste mix, estão incluídos um controlo de amplificação interno e um controlo de extração. - Mix 2: Tubo verde. Amplificação de Salmonella spp. e Campylobacter spp. Está incluído um controlo de amplificação interno diferente do controlo interno do Mix 1. - CE ADN (controlo de extração). Controlo de extração de ADN humano genómico. Nota: o kit inclui uma tira adesiva indicadora de temperatura. Se aparecer uma luz vermelha na janela de visualização da tira indicadora de temperatura, o kit não deve ser utilizado porque a temperatura de conservação pode ter sido ultrapassada Reagentes de visualização ADVERTÊNCIA: Após a receção, as micro matrizes devem ser conservadas à temperatura ambiente. Micro matrizes: Tiras de poços CS (incluindo as sondas específicas). Estas são entregues num envelope selado. Após a abertura, o envelope deve ser fechado e conservado a temperatura ambiente, protegido da luz. RE (Revelador). Conservar a 4ºC. 7
8 SH (Solução de hibridização). Conservar a 4ºC. DC (Solvente do conjugado). Conservar a 4ºC. CJ (Conjugado). Conservar a 4ºC. Centrifugar ligeiramente antes de utilizar. TL (tampão de lavagem). Conservar a 4ºC. Suporte e tampa para a tira de 8 poços Outros componentes - CAR (Clinical Array Reader): o que permite a leitura e interpretação automática até 12 CS, ou seja, um total de 96 amostras. Esta plataforma é fabricada exclusivamente para a GENOMICA, para só ser utilizada com os seus kits. - Adaptador do suporte para colocar sobre a bandeja do CAR, de modo a encaixar a placa de microtitulação antes da leitura. - Software: É específico para CLART EnteroBac, desenhado e validado por GENOMICA. Instalado e pronto a utilizar. CAR (Clinical Array Reader) Figura 3: Leitor CAR. 4. MATERIAL ADICIONAL 4.1. Reagentes e material 8
9 Água destilada Luvas descartáveis Deslocamento positivo ou pontas de pipeta com filtro Recipiente com gelo picado Tubos Eppendorf esterilizados (1,5 ml) Suportes para tubos de 1,5 ml Suportes para tubos de 0,5 ml/0,2 ml Equipamentos Microcentrífuga Termociclador Três micropipetas ajustáveis (1-20 µl, µl e µl) para utilização no laboratório de extração. Três micropipetas ajustáveis (1-20 µl, µl e µl) para utilização no laboratório de visualização. Termoblocos (a 37 C, 55 C e 100ºC) com um agitador ajustável e compatível com os tubos Eppendorf. Vórtex Sistema a vácuo 5. PROCEDIMENTOS E RECOMENDAÇÕES DE MANIPULAÇÃO Muito importante: ler cuidadosamente esta secção antes de iniciar qualquer trabalho Recomendações gerais 1. O procedimento deve ser realizado em duas áreas separadas fisicamente. Isto evitará a contaminação de amostras com os produtos anteriormente amplificados. Cada área deve ter os seus próprios materiais de trabalho identificados (pipetas, pontas, tubos, suportes, luvas, etc.) que nunca devem sair da respetiva área. Área Pré-PCR: as amostras são preparadas e o ADN é extraído. Manipulações das amostras fecais deve ser feito dentro da cabina de segurança. Área Pós-PCR: os produtos são amplificados e, depois, visualizados. O material desta área nunca deve entrar em contacto com o material da área pré-pcr. DEPOIS DE TRABALHAR NA ÁREA PÓS-PCR, NÃO RETORNE À ÁREA PRÉ- PCR. 2. Use sempre luvas. Recomenda-se a troca frequente de luvas, embora seja obrigatório trocá-las antes de começar a trabalhar em cada uma das áreas supramencionadas. 9
10 Devem ser utilizadas luvas novas para a preparação dos tubos de amplificação e sempre que se adicionar ADN aos tubos. 3. Limpe as áreas de trabalho (bancadas de laboratório, coberturas, grelhas, pipetas, termociclador) cuidadosamente com desinfetante diluído a 10% após o processamento de cada lote de amostra; é obrigatório desinfetar todas as áreas de trabalho para evitar contaminações. 4. Utilize sempre pontas de pipetas com filtro ou pipetas de deslocamento positivo para evitar contaminações. 5. Utilize materiais de laboratórios esterilizados (em autoclave) e descartáveis. 6. Nunca misture reagentes de dois tubos diferentes, mesmo que pertençam ao mesmo lote. 7. Feche imediatamente os tubos dos reagentes depois da utilização, para evitar a contaminação. 8. Elimine as pontas das micropipetas depois da utilização. 9. Mantenha sempre os tubos afastados uns dos outros durante a manipulação com especial cuidado, durante as fases de extração. 10. A GENOMICA não assume qualquer responsabilidade em relação aos resultados obtidos sem seguir as instruções contidas neste manual Precauções para a extração Muitos dos microrganismos no kit CLART EnteroBac fazem parte da flora normal do trato digestivo humano, pelo que é preciso ser extremamente cuidadoso aquando do processamento da amostra clínica. Use sempre luvas. Calce as luvas, tendo o cuidado para os dedos só tocarem nas extremidades. Limpe as superfícies de trabalho com lixívia diluída a 10%. Ligue o fluxo laminar e a luz UV, pelo menos, 20 minutos antes da extração. A preparação das amostras antes da extração deve ser feita dentro da cabina Precauções para a visualização 1. Evite que a ponta da pipeta ou o sistema a vácuo toque no fundo do tubo onde se encontra a micro matriz. 10
11 2. Recomenda-se a adição de todas as soluções sobre a parede local da CS nunca diretamente sobre o fundo. 3. Só se deve adicionar a solução de hibridização imediatamente antes de adicionar os produtos de PCR. 4. Aquando da utilização da CS, ficará um ligeiro volume residual para evitar a secagem da matriz. 5. Após a incubação com o conjugado, é muito importante lavar cuidadosamente a CS para evitar que qualquer conjugado remanescente reaja com o revelador. 6. Evite bolhas sobre a superfície da micro matriz, quando adicionar as diferentes soluções. 7. Mantenha a base da CS limpa para evitar a possível interferência, aquando da leitura dos resultados. 8. Quando visualizar a imagem no leitor, confirme o aparecimento de marcadores de posição e que não há bolhas ou manchas a interferir na leitura. Se necessário, limpe a base do tubo com papel de celulose ou tape suavemente o tubo com o dedo. 6. AMOSTRAS: AMOSTRAS FECAIS O kit CLART EnteroBac foi concebido e validado para ser utilizado em amostras fecais (1). A GENOMICA não se responsabiliza pelos resultados quando se utilizarem outras amostras. 7. PROTOCOLO DE TRABALHO 7.1. Extração Automática de ADN 1. Preparação da amostra antes da extração (realizada fora do equipamento). Recomendado para todos os equipamentos automáticos. Transfira 1 g de amostra fecal e ressuspenda em 2 ml de solução salina (cloreto de sódio a 0,9%). Centrifugue durante 2 minutos a rpm. Nota: As manipulações das amostras fecais devem ser feitas na cobertura de segurança. 11
12 Retire o sobrenadante para um tubo de 1,5 ml esterilizado e elimine o agregado. Centrifugue a rpm durante 5 minutos, para concentrar o agregado bacteriano. Elimine o sobrenadante e ressuspenda em 1,5 ml de solução salina (cloreto de sódio a 0,9%). Ressuspenda vigorosamente. Transfira 275 µl para um novo tubo. Adicione 25 µl de CE ADN (controlo de extração). Transfira a mistura para o extrator. 2. Lise interna e extração de ADN num equipamento de extrator automático. Siga o guia de utilizador do computador. O volume de eluição selecionado é 110 µl. Este volume pode variar dependendo da instrumentação do extrator automático utilizado. Se o aparelho tiver vários programas de lavagem, selecione a opção mais abrangente (como por exemplo, protocolo específico B no Nuclisens easymag da biomérieux). 3. Depois da extração, retire 110 µl do ADN eluído com a micro pipeta e introduza-os nos tubos Eppendorf de 1,5 ml. Utilize 5 µl em cada tubo de amplificação e conserve o resto a -20 C. O rendimento mínimo estimado da extração de ADN necessário para a amplificação bemsucedida é 5 ng/µl Reação de amplificação Recomendações específicas para a amplificação: Trabalhe na área de pré-pcr, utilize sempre a cobertura e siga as recomendações descritas em 5.1. Adicione o ADN aos tubos de amplificação sempre sob cobertura. Durante o processo, mantenha os tubos separados no gelo. 1. Descongele um tubo de reação Mix 1 e Mix 2 para cada amostra e mantenhaos no gelo. Não utilize temperaturas superiores a 37ºC para descongelar. 2. Centrifugue os tubos de reação numa microcentrífuga, de modo a que todo o líquido vá para o fundo (se não houver adaptadores disponíveis para segurar nos tubos de reação, estes podem ser colocados em tubos maiores sem tampas). 3. Adicione 5 µl do ADN extraído de cada amostra aos tubos Mix 1 e Mix 2 e ressuspenda várias vezes com uma micro pipeta. Deixe os tubos no gelo. 12
13 5. Programe o termociclador da seguinte forma: 1 ciclo 95ºC 5 minutos 45 ciclos 95ºC 30 segundos 53ºC 30 segundos 72ºC 1 minuto 1 ciclo 72ºC 10 minutos 4ºC (mantido) até à recolha dos tubos (opcional) 6. Inicie o programa e coloque os tubos Mix 1 e Mix 2 no termociclador quando o bloco estiver acima dos 90ºC. Isto minimiza quaisquer amplificações não específicas devido à hibridização que ocorre abaixo da temperatura de reação. O processo de amplificação dura cerca de 3 horas e meia, embora este tempo possa variar dependendo do termociclador utilizado Protocolo de Visualização para CLART Strip (CS) Recomendações específicas antes de iniciar o processo de visualização: O PROTOCOLO DESCRITO ABAIXO DEVE SER REALIZADO NA ÁREA PÓS-PCR. NUNCA LEVE O PRODUTO AMPLIFICADO PARA A ÁREA PRÉ-PCR. 1. No início do ensaio: Ligue o Leitor CAR (Clinical Arrays Reader) para permitir a autocalibração do aparelho. Introduza a identificação das amostras. É importante ter o equipamento já preparado para ler as amostras no fim do ensaio, de modo a que estas fiquem expostas a um tempo de revelação excessivo. 2. Ligue o termomisturador a uma temperatura de 56ºC, pelo menos 30 minutos antes de iniciar o processo de hibridização. 3. Conserve a SH (Solução de Hibridização) à temperatura ambiente. 4. Prepare a solução de lavagem antes de cada ensaio. Não utilize soluções anteriores ou quaisquer restos de outros ensaios. 5. Antes de iniciar o programa de desnaturação, lave o termociclador com lixívia diluída a 10%. Durante o processo de desnaturação, coloque os tubos de amplificação separados no termociclador. A desnaturação não deve ultrapassar os 10 minutos. 13
14 6. Não é necessário utilizar pontas com filtro durante o processo de visualização, exceto quando se adiciona produtos amplificados a cada poço. No entanto, deve ser utilizada uma ponta diferente para cada amostra e para cada reagente. Esta precaução também se deve aplicar ao tampão TL. 7. Os pentes de 8 pontas utilizados com as bombas de aspiração devem ser eliminados após a utilização ou descontaminados com uma solução de lixívia diluída a 10% após cada ensaio. Certifique-se de que a bomba de vácuo funciona corretamente e não deixa resíduos de líquido nos poços. 8. Todos os tampões devem ser aspirados cuidadosamente dos poços sem tocar no fundo. VISUALIZAÇÃO 1. Desnaturação: utilize o termociclador para desnaturar as amostras. Regule o programa para 15 minutos, a 95º C. Coloque os produtos amplificados no termociclador e incube durante 10 minutos, a 95º C. Passados 10 minutos, retire os tubos do termociclador (ainda a 95 o C) e coloque-os imediatamente no gelo. 2. Prepare a solução TL diluída: Para 8 poços (uma tira), adicione o seguinte: 1 ml de solução TL + 9 ml de água destilada. Isto constituirá os 10 ml de solução TL necessária para uma tira. 3. Pré-lavagem da CS: Adicione 200 µl de solução TL diluída a cada matriz e ressuspenda 10 a 15 vezes com a pipeta. Elimine a solução TL diluída usando uma pipeta ou, de preferência, um sistema a vácuo. Este passo é necessário para lavar as CSs já embaladas, antes de adicionar a amostra. A CS não deve conter resíduos da solução de lavagem. Em circunstância alguma, deve deixar-se que as CSs sequem durante um longo período. 4. Hibridização: A solução de hibridização (SH) deve ser aquecida a 56 C de modo a dissolver os sais cristalizados. Adicione 100 µl de tampão SH (evitando o aparecimento de espuma) + 5 µl de produto desnaturado do tubo Mix 1 e do tubo Mix 2 a cada poço. Misture adequadamente com a pipeta evitando tocar na matriz e incube a tira, coberta por uma tampa de plástico transparente, no 14
15 termomisturador durante 30 minutos, a 56 C, com uma centrifugação de 550 rpm. Para obter resultados corretos, os produtos amplificados dos tubos Mix 1 e Mix 2 devem ser visualizados na mesma matriz. Retire as CSs e elimine a solução SH usando uma pipeta ou um sistema a vácuo. Programe o bloco de aquecimento para 30 C e deixe-o a funcionar para que possa ser utilizado mais tarde no passo 6. Pode retirar a tampa do bloco de aquecimento para o deixar arrefecer mais depressa. 5. Lavagem dupla: use pontas diferentes para cada poço em ambas as lavagens. Lave duas vezes a CS com 200 µl de solução TL diluída em cada poço, misturando 10 a 15 vezes com a pipeta. Elimine a solução TL diluída usando uma pipeta ou um sistema a vácuo, deixando um volume remanescente. No caso do bloco de aquecimento não ter atingido uma temperatura de 30 C quando chegar a este passo, deixe as CSs cheias com solução TL diluída até o bloco de aquecimento chegar à temperatura necessária. 6. Bloqueio e conjugado: Prepare a solução CJ diluída 15 minutos antes de o tempo de hibridização acabar e mantenha-a no gelo até à sua utilização. Recomenda-se a centrifugação do tampão CJ durante 10 segundos antes da utilização. Prepare o tampão CJ diluído: Para uma tira (8 poços), adicione o seguinte: 1 ml de tampão DC 9 µl de tampão CJ No vórtex, agitar durante breves instantes a solução CJ diluída. Retirar o tampão TL diluído sem secar a matriz e adicione 100 µl de tampão CJ diluído para cada poço. Incube a 30 C, a 550 rpm, durante 15 minutos exatamente no termomisturador. Após esta incubação, pegue na tira e remova imediatamente o tampão CJ diluído com a bomba. (Regule o termomisturador para 25 C e sem centrifug ação para o passo 8. Retire a tampa para acelerar o arrefecimento). 7. Tripla Lavagem: Adicione de imediato 200 µl de solução TL diluída por poço. Misture bem 10 a 15 vezes com a pipeta e retire o tampão TL diluído com a bomba sem deixar secar a matriz. Repita esta lavagem duas vezes e deixe a CS com 200 µl de tampão TL a RT durante 5-10 minutos ou até o termomisturador atingir os 25 C. 15
16 É muito importante que o tampão CJ diluído seja completamente lavado. Qualquer resíduo de tampão pode reagir com o tampão RE produzindo um sinal não específico. 8. Relevar com tampão RE: retire o tampão TL diluído sem deixar secar a matriz e adicione 100 µl de tampão RE por poço. Incube a 25 C no termomisturador durante 10 minutos sem agitação. Atenção! É muito importante utilizar o termomisturador sem agitação neste passo. 9. Retire o tampão RE com a bomba. A matriz deve ser seca, nesta altura. 10. Leitor CAR (Clinical Array Reader): De modo a analisar as amostras, um adaptador especial deve ser colocado sobre a bandeja do CAR. Depois, coloque a placa normalmente na bandeja e o CAR procederá à análise automática das matrizes. 8. LEITURA DE RESULTADOS O processamento dos dados obtidos em cada análise é completamente automático. O equipamento de leitura/análise fornecerá um relatório com os resultados. No ecrã, aparecerá uma tabela com três colunas. A coluna da esquerda mostra o grupo microbiano propício a ser detetado, a coluna central apresentará um resultado positivo ou negativo para cada grupo microbiano e a coluna da direita mostrará se os controlos da amplificação e da extração de ADN foram realizados em conformidade. 9. INTERPRETAÇÃO DOS RESULTADOS Um dos principais inconvenientes da amplificação genómica é a utilização de amostras de ADN de fraca qualidade (fragmentos de ADN demasiado curtos, degradação do ADN ou perda do ADN durante a extração) ou a presença de inibidores da polimerase do ADN (como por exemplo, a hemoglobina, resíduos de cera parafina, sais, etc.) nas amostras a analisar, interferindo assim na amplificação genómica e resultando em falsos negativos. No entanto, CLART EnteroBac elimina os falsos negativos através da utilização de controlos internos nos mesmos tubos (Mix 1 e Mix 2) em que a amostra é analisada e são amplificados ao mesmo tempo que o ADN microbiano. No tubo Mix 1 existem oligonucleotídeos específicos que amplificam o controlo de extração (CE ADN), que é adicionado à amostra antes da extração. A presença na matriz de ADN genómico indica que o processo de extração foi adequado, eliminando assim resultados negativos falsos devido a erros na extração. 16
17 Para obter resultados corretos, a amostra tem de ser amplificada nos tubos Mix 1 e Mix 2, e os produtos amplificados devem ser visualizados na mesma matriz. Em cada conjunto de análise, deve ser incluído um controlo de extração negativo para confirmar que as amostras não foram contaminadas durante a extração, amplificação e visualização, dando assim origem a um falso positivo. Cada tubo contém as seguintes bases de amplificação: Mix 1: Mix 2: Duas bases que amplifiquem um controlo de extração Duas bases que amplifiquem um plasmídeo modificado, incluído no tubo de amplificação e usado como um controlo para a amplificação da reação PCR. Oligonucleotídeos específicos do alvo, concebidos para detetar agentes patogénicos microbianos. Duas bases que amplifiquem um plasmídeo modificado, incluído no tubo de amplificação e usado como um controlo para a amplificação da reação PCR. Este plasmídeo é diferente do incluído no tubo Mix 1. Oligonucleotídeos específicos do alvo, concebidos para detetar agentes patogénicos microbianos. O tubo de reação foi concebido para favorecer a amplificação de microrganismos, comparativamente aos outros dois controlos. Entre estes dois controlos, a amplificação do ADN genómico será realizada de preferência, comparando o controlo da reação de amplificação. A razão para este design é: O controlo genómico do ADN só seria essencial para confirmar um resultado negativo, uma vez que confirma que a extração do ADN da amostra fecal foi realizada com sucesso. O controlo PCR só seria essencial quando não se encontrar amplificação no tubo porque ajudará a distinguir entre um PCR inibido e uma amostra onde não há ADN. Em certas condições (como por exemplo, elevada concentração de ADN microbiano), pode ocorrer uma amplificação negativa dos dois controlos, ou de algum deles, exibindo uma leitura: SEM SINAL. Há duas possibilidades que podem levar a um resultado não válido: 17
18 Extração não válida: A amplificação do alvo microbiano e/ou a amplificação da extração e controlos de amplificação podem ser prejudicadas devido à presença de inibidores de amplificação ou devido a um erro mecânico durante a extração. O processo terá de ser repetido na totalidade. Amplificação não válida: A presença microbiana num tubo e a ausência de amplificação no outro indica um procedimento de extração válido, mas indica a presença de um problema durante a amplificação. A amplificação com ambos os tubos tem de ser repetida. Há três possibilidades que podem levar a um resultado inconclusivo: Nos casos em que as réplicas de uma sonda da matriz sejam muito diferentes umas das outras. Nas infeções múltiplas com mais de 3 bactérias. Quando a intensidade do sinal da absorção não normalizada se encontra no limite de deteção da técnica, cuja amplitude é determinada pelo software para cada tipo de microrganismo. 10. ESPECIFICAÇÕES TÉCNICAS E DE FUNCIONAMENTO Conhecidas fontes de interferência Certas substâncias podem interferir com o kit CLART EnteroBac. São principalmente substâncias que inibem a mistura enzimática e, por conseguinte, inibem a reação de amplificação. Os fatores mais comuns são os seguintes: Utilização de amostra inadequadas. A análise de qualquer tipo de amostras clínicas diferentes das especificadas no manual do kit CLART EnteroBac, assim como a recolha incorreta de amostras, pode originar um resultado de análise inconclusivo ou inválido, devido à falta de amplificação, em consequência da falta de amostra ou de reação inibida. A conservação inadequada de amostras pode influenciar o resultado da análise. Se as amostras estão sujeitas a condições que podem resultar na degradação do ADN, o resultado da análise pode levar a um falso negativo Especificações técnicas: 18
19 Parâmetros analíticos: Sensibilidade analítica. A sensibilidade analítica dos microrganismos apresentados no kit (2) foi determinada através da amplificação de uma série de diluições de ADN de plasmídeos recombinantes com o produto fragmentado de amplificação específico (incluindo a parte complementar da sonda específica de deteção) para cada microrganismo. O passo de visualização foi realizado em CLART Strips, obtendo os mesmos resultados agora resumidos na seguinte Tabela 1. Microrganismo Yersinia enterocolítica Escherichia coli (enteropatogénica) Campylobacter jejuni Shigella Salmonella Clostridium difficile Campylobacter coli Aeromonas aerolisina + Nº de cópias do plasmídeo para a reação PCR Tabela 1. Número de cópias de plasmídeo recombinante necessário para obter 100% de sensibilidade na deteção de cada um dos microrganismos. Especificidade analítica. Foram realizadas experiências de especificidade com 8 plasmídeos recombinantes (2), mostrando que não há uma deteção não específica de outros microrganismos. Por conseguinte, é considerado que a técnica analítica atinge uma especificidade de 100%. Parâmetros de diagnóstico Para determinar os parâmetros diagnósticos do kit CLART EnteroBac, foram realizados estudos comparativos com a caracterização da cultura fecal (1, 2). Estas comparações foram feitas em colaboração com dois hospitais espanhóis e um hospital português. Serviço de Microbiologia do Hospital Universitário Germans Trías i Pujol, Badalona, Barcelona. Serviço de Microbiologia do Hospital Universitário Ramon y Cajal, Madrid. 19
20 Foi processado um total de 334 amostras de amostras fecais. A seguinte tabela ilustra os dados de sensibilidade diagnóstica e especificidade para as espécies microbianas detetadas no kit CLART EnteroBac. Os resultados de CLART EnteroBac foram comparados com os resultados da técnica de referência (cultura fecal + caracterização). Em caso de discrepâncias, os resultados da sequenciação foram considerados como resultados válidos. Nesses casos específicos, onde esta informação não estava disponível, as discrepâncias foram avaliadas por uma Nested-PCR e posterior sequenciação do ADN. Sensib Especificid N = 334 ilidade ade PPV NPV Campylobacter 90,0 100,0 100,0 94,0 Salmonella 83,2 99,0 98,3 89,4 Clostridium difficile 83,0 100,0 100,0 97,7 Escherichia coli enteropatogénica 100,0 100,0 100,0 100,0 Shigella ,0 100,0 99,7 Tabela 2. Sensibilidade e especificidade diagnóstica de CLART EnteroBac para cada microrganismo. PPV: valor previsto positivo. NPV: valor previsto negativo. Nesta validação, foram processadas 15 amostras de Aeromonas spp., nenhuma delas positiva para a toxina aerolisina (alvo neste kit), pelo que os parâmetros diagnósticos para este microrganismo não foram determinados. Devido à baixa prevalência de Yersinia nas amostras utilizadas nesta validação, só foram processadas 5 amostras com este microrganismo, não sendo suficiente para calcular parâmetros diagnósticos fiáveis. Especificidade diagnóstica. A técnica também foi validada com culturas fecais negativas e com amostras fecais com presença de microrganismos não sujeitos à identificação por CLART EnteroBac, e os resultados não revelaram reatividade cruzada, chegando a uma especificidade diagnóstica mínima de 99%. Reprodutibilidade e repetibilidade diagnóstica Os dados obtidos são os seguintes: Reprodutibilidade: 91,8 % (n=49 amostras) 20
21 Repetibilidade: 97,2 % (n= 48 amostras) As amostras foram processadas desde o passo da extração. Deteção de infeções múltiplas Os resultados de CLART EnteroBac mostram a presença de infeções múltiplas (duas ou mais microrganismos) em 15,9% das amostras fecais analisadas contra 2,4% das infeções múltiplas detetadas nas amostras fecais por caracterização da cultura, sustentando a maior sensibilidade de CLART EnteroBac para deteção de infeções múltiplas versus os métodos clássicos de identificação da cultura. 21
22 BIBLIOGRAFIA 1. Alvarez, M., Buesa, J., Castillo. J. and J. Vila. Microbiologic diagnostic of enteric diseases nd Ed. (24). Eds. Cercenado E. and R. Cantón. Proceedings in clinical microbiology. Spanish Society of CIinical Microbiology (SEIMC). 2. Manjón, N., Moscoso, J., Margolles, Y., García, M., Morosini, M. I., Salazar, O., Cospedal R., Cantón, R., and M. L. Villahermosa Design and optimization of microarray based in vitro assay, for the rapid identification of bacterial pathogens responsible of infectious diarrhea Infectious diseases and Clínical Microbiology. Vol 29, th Congress of the Spanish Society of Clinical Microbiology (SEIMC). Malaga, Spain. June 1 st -4 th
CLART SeptiBac + DETECÇÃO E IDENTIFICAÇÃO MOLECULAR DE BACTÉRIAS GRAM- POSITIVAS E FUNGOS CAUSADORES DE SEPTICEMIA PARA DIAGNÓSTICO IN VITRO
 CLART SeptiBac + DETECÇÃO E IDENTIFICAÇÃO MOLECULAR DE BACTÉRIAS GRAM- POSITIVAS E FUNGOS CAUSADORES DE SEPTICEMIA PARA DIAGNÓSTICO IN VITRO 1 CLART SeptiBac + Amplificação CLART SeptiBac + Deteção 48
CLART SeptiBac + DETECÇÃO E IDENTIFICAÇÃO MOLECULAR DE BACTÉRIAS GRAM- POSITIVAS E FUNGOS CAUSADORES DE SEPTICEMIA PARA DIAGNÓSTICO IN VITRO 1 CLART SeptiBac + Amplificação CLART SeptiBac + Deteção 48
CLART CMA KRAS BRAF PI3K
 CLART CMA KRAS BRAF PI3K DETEÇÃO E IDENTIFICAÇÃO GENÉTICA DE MUTAÇÕES PONTUAIS EM 3 DOS GENES PERTENCENTES À VIA DO EGFR (RECETOR DO FATOR DE CRESCIMENTO EPIDÉRMICO) ASSOCIADOS AO CANCRO COLORRETAL KRAS,
CLART CMA KRAS BRAF PI3K DETEÇÃO E IDENTIFICAÇÃO GENÉTICA DE MUTAÇÕES PONTUAIS EM 3 DOS GENES PERTENCENTES À VIA DO EGFR (RECETOR DO FATOR DE CRESCIMENTO EPIDÉRMICO) ASSOCIADOS AO CANCRO COLORRETAL KRAS,
Ficha de protocolo do QIAsymphony SP
 Fevereiro de 2017 Ficha de protocolo do QIAsymphony SP circdna_2000_dsp_v1 e circdna_4000_dsp_v1 Este documento é a ficha de protocolo do QIAsymphony circdna_2000_dsp_v1 e circdna_4000_dsp_v1, versão 1,
Fevereiro de 2017 Ficha de protocolo do QIAsymphony SP circdna_2000_dsp_v1 e circdna_4000_dsp_v1 Este documento é a ficha de protocolo do QIAsymphony circdna_2000_dsp_v1 e circdna_4000_dsp_v1, versão 1,
Protocolo de extração de DNA de tecido vegetal: (Doyle & Doyle, 1987)
 Protocolo de extração de DNA de tecido vegetal: (Doyle & Doyle, 1987) PROCEDIMENTOS 1. Preparo do Material» Primeiro verifique se todas as soluções estão preparadas;» Ligue o banho-maria a 65ºC;» Prepare
Protocolo de extração de DNA de tecido vegetal: (Doyle & Doyle, 1987) PROCEDIMENTOS 1. Preparo do Material» Primeiro verifique se todas as soluções estão preparadas;» Ligue o banho-maria a 65ºC;» Prepare
Antes de iniciar o procedimento, preparar o Tampão de Lise: adicionar 1 ml da solução MI2 ao tubo com Lisozima e agitar brevemente.
 90043-50 Kit de Extração EliGene MTB Instruções de Uso USO PRETENDIDO O «Kit de Extração EliGene MTB» é destinado ao isolamento do DNA de espécies de Mycobacterium e eventualmente de outros organismos
90043-50 Kit de Extração EliGene MTB Instruções de Uso USO PRETENDIDO O «Kit de Extração EliGene MTB» é destinado ao isolamento do DNA de espécies de Mycobacterium e eventualmente de outros organismos
Detecção de IL-1 por ELISA sanduíche. Andréa Calado
 Detecção de IL-1 por ELISA sanduíche Andréa Calado andreabelfort@hotmail.com ELISA O teste identifica e quantifica Ag ou Ac, utilizando um dos dois conjugados com enzimas; PRINCIPAIS TIPOS: INDIRETO:
Detecção de IL-1 por ELISA sanduíche Andréa Calado andreabelfort@hotmail.com ELISA O teste identifica e quantifica Ag ou Ac, utilizando um dos dois conjugados com enzimas; PRINCIPAIS TIPOS: INDIRETO:
Extracção de ADN de mancha de sangue por Chelex 100. Protocolo experimental:
 Extracção de ADN de mancha de sangue por Chelex 100 1. Num tubo eppendorf misturar 1ml de água desionizada estéril com uma mancha de sangue com aproximadamente 3mm²; 2. Incubar à temperatura ambiente no
Extracção de ADN de mancha de sangue por Chelex 100 1. Num tubo eppendorf misturar 1ml de água desionizada estéril com uma mancha de sangue com aproximadamente 3mm²; 2. Incubar à temperatura ambiente no
Protocolo laboratorial para purificação manual de ADN de amostra com 0,5 ml
 Protocolo laboratorial para purificação manual de ADN de amostra com 0,5 ml Para a purificação do ADN genómico através das famílias de kits de recolha Oragene e ORAcollect. Visite o nosso website em www.dnagenotek.com
Protocolo laboratorial para purificação manual de ADN de amostra com 0,5 ml Para a purificação do ADN genómico através das famílias de kits de recolha Oragene e ORAcollect. Visite o nosso website em www.dnagenotek.com
CATÁLOGO DE KITS DE EXTRAÇÃO
 CATÁLOGO DE KITS DE EXTRAÇÃO KITS DE EXTRAÇÃO BIOPUR A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
CATÁLOGO DE KITS DE EXTRAÇÃO KITS DE EXTRAÇÃO BIOPUR A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
Catálogo de Kits de Extração
 Catálogo de Kits de Extração Kits de Extração Biopur A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
Catálogo de Kits de Extração Kits de Extração Biopur A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
Procedimento Operacional Padrão - POP
 Página 1 de 10 Biobanco Procedimento Operacional Padrão para: Extração de RNA total de sangue POP: V. 1.0 Nome: Extração de RNA total de sangue Efetiva: dezembro, 22 autora: Erika Regina Manuli Aprovação
Página 1 de 10 Biobanco Procedimento Operacional Padrão para: Extração de RNA total de sangue POP: V. 1.0 Nome: Extração de RNA total de sangue Efetiva: dezembro, 22 autora: Erika Regina Manuli Aprovação
Extração de DNA/RNA Viral. Instruções de uso K204
 Extração de DNA/RNA Viral Instruções de uso K204 Revisão: Novembro/2018 ÍNDICE Finalidade... 3 Princípio de Ação... 3 Apresentação... 3 Reagentes... 4 Equipamentos e Insumos Operacionais... 4 Condições
Extração de DNA/RNA Viral Instruções de uso K204 Revisão: Novembro/2018 ÍNDICE Finalidade... 3 Princípio de Ação... 3 Apresentação... 3 Reagentes... 4 Equipamentos e Insumos Operacionais... 4 Condições
Folha de protocolo do QIAsymphony SP
 Folha de protocolo do QIAsymphony SP Protocolo DNA_Blood_200_V7_DSP Informações gerais Para utilização em diagnóstico in vitro. Este protocolo destina-se à purificação de ADN total genómico e mitocondrial
Folha de protocolo do QIAsymphony SP Protocolo DNA_Blood_200_V7_DSP Informações gerais Para utilização em diagnóstico in vitro. Este protocolo destina-se à purificação de ADN total genómico e mitocondrial
mundo inteiro com uma variedade de aplicações como clonagem, genotipagem e sequenciamento.
 mundo inteiro com uma variedade de aplicações como clonagem, genotipagem e sequenciamento. necessária para que você possa alcançar o melhor desempenho nesta técnica. AGAROSE A agarose é um polissacarídeo
mundo inteiro com uma variedade de aplicações como clonagem, genotipagem e sequenciamento. necessária para que você possa alcançar o melhor desempenho nesta técnica. AGAROSE A agarose é um polissacarídeo
Cargo: D-43 - Tecnólogo Laboratório Meio ambiente
 da Prova Prática QUESTÃO 1: Cargo: D-43 - Tecnólogo Laboratório Meio ambiente A titulometria volumétrica envolve a medida de volume de uma solução de concentração conhecida, necessária para reagir essencial
da Prova Prática QUESTÃO 1: Cargo: D-43 - Tecnólogo Laboratório Meio ambiente A titulometria volumétrica envolve a medida de volume de uma solução de concentração conhecida, necessária para reagir essencial
Folha de protocolo do QIAsymphony SP
 Folha de protocolo do QIAsymphony SP Protocolo DNA_Buffy_Coat_400_V6_DSP Informações gerais Para utilização em diagnóstico in vitro. Este protocolo destina-se à purificação de ADN total genómico e mitocondrial
Folha de protocolo do QIAsymphony SP Protocolo DNA_Buffy_Coat_400_V6_DSP Informações gerais Para utilização em diagnóstico in vitro. Este protocolo destina-se à purificação de ADN total genómico e mitocondrial
ZytoDot CEN 7 Probe. Para a deteção dos satélites alfa humanos do cromossoma 7 por meio de hibridação in situ cromogénica (CISH)
 ZytoDot CEN 7 Probe C-3008-400 40 (0,4 ml) Para a deteção dos satélites alfa humanos do cromossoma 7 por meio de hibridação in situ cromogénica (CISH).... Para utilização em diagnóstico in vitro em conformidade
ZytoDot CEN 7 Probe C-3008-400 40 (0,4 ml) Para a deteção dos satélites alfa humanos do cromossoma 7 por meio de hibridação in situ cromogénica (CISH).... Para utilização em diagnóstico in vitro em conformidade
CLART PAPILOMAVIRUS HUMANO 2 GENOTIPAGEM DE PAPILOMAVIRUS HUMANO POR IDENTIFICAÇÃO GENÓMICA PARA DIAGNÓSTICO IN VITRO
 CLART PAPILOMAVIRUS HUMANO 2 GENOTIPAGEM DE PAPILOMAVIRUS HUMANO POR IDENTIFICAÇÃO GENÓMICA PARA DIAGNÓSTICO IN VITRO 1 CLART HPV2 está sob a proteção de 2 famílias de patentes que correspondem aos pedidos
CLART PAPILOMAVIRUS HUMANO 2 GENOTIPAGEM DE PAPILOMAVIRUS HUMANO POR IDENTIFICAÇÃO GENÓMICA PARA DIAGNÓSTICO IN VITRO 1 CLART HPV2 está sob a proteção de 2 famílias de patentes que correspondem aos pedidos
ZytoDot. Para a deteção dos satélites alfa humanos do cromossoma 17 por meio de hibridação in situ cromogénica (CISH)
 ZytoDot CEN 17 Probe C-3006-400 40 (0,4 ml) Para a deteção dos satélites alfa humanos do cromossoma 17 por meio de hibridação in situ cromogénica (CISH).... Para utilização em diagnóstico in vitro em conformidade
ZytoDot CEN 17 Probe C-3006-400 40 (0,4 ml) Para a deteção dos satélites alfa humanos do cromossoma 17 por meio de hibridação in situ cromogénica (CISH).... Para utilização em diagnóstico in vitro em conformidade
Procedimento Operacional Padrão - POP
 Página 1 de 10 IMT-POP-BB-0 Biobanco Procedimento Operacional Padrão para: Extração de DNA de sangue total POP: V. 1.0 Nome: Extração de DNA em sangue total Efetiva: dezembro, 22 autora: Erika Regina Manuli
Página 1 de 10 IMT-POP-BB-0 Biobanco Procedimento Operacional Padrão para: Extração de DNA de sangue total POP: V. 1.0 Nome: Extração de DNA em sangue total Efetiva: dezembro, 22 autora: Erika Regina Manuli
NextGeneration ECO One-Step RT-qPCR Kit
 DNA EXPRESS BIOTECNOLOGIA NextGeneration ECO One-Step RT-qPCR Kit Kit para uso em RT-PCR em tempo real quantitativo (RT-qPCR) em único tubo contendo NextGeneration Transcriptase Reversa M-MLV RNAse Minus
DNA EXPRESS BIOTECNOLOGIA NextGeneration ECO One-Step RT-qPCR Kit Kit para uso em RT-PCR em tempo real quantitativo (RT-qPCR) em único tubo contendo NextGeneration Transcriptase Reversa M-MLV RNAse Minus
Instruções de uso. RealStar Rotavirus RT-PCR Kit /2017 PT
 Instruções de uso RealStar Rotavirus RT-PCR Kit 1.0 01/2017 PT RealStar Rotavirus RT-PCR Kit 1.0 Para utilização com Mx 3005P QPCR System (Stratagene) VERSANT kpcr Molecular System AD (Siemens Healthcare)
Instruções de uso RealStar Rotavirus RT-PCR Kit 1.0 01/2017 PT RealStar Rotavirus RT-PCR Kit 1.0 Para utilização com Mx 3005P QPCR System (Stratagene) VERSANT kpcr Molecular System AD (Siemens Healthcare)
2. Aplicabilidade: Bioquímicos/biomédicos do setor de imunologia
 1. Sinonímia: HIV triagem, HIV teste rápido 2. Aplicabilidade: Bioquímicos/biomédicos do setor de imunologia 3. Aplicação clínica Utilizado para investigar a infecção pelo vírus da imunodeficiência humana.
1. Sinonímia: HIV triagem, HIV teste rápido 2. Aplicabilidade: Bioquímicos/biomédicos do setor de imunologia 3. Aplicação clínica Utilizado para investigar a infecção pelo vírus da imunodeficiência humana.
PROTOCOLO OPERACIONAL PARA TRANSFERÊNCIA DE CÉLULAS BACTERIANAS PARA MEIO LÍQUIDO
 Ministério da Agricultura e do Abastecimento Empresa Brasileira de Pesquisa Agropecuária-EMBRAPA Centro Nacional de Pesquisa de Agrobiologia-CNPAB ISSN 0104-6187 PROTOCOLO OPERACIONAL PARA TRANSFERÊNCIA
Ministério da Agricultura e do Abastecimento Empresa Brasileira de Pesquisa Agropecuária-EMBRAPA Centro Nacional de Pesquisa de Agrobiologia-CNPAB ISSN 0104-6187 PROTOCOLO OPERACIONAL PARA TRANSFERÊNCIA
Folha de protocolo QIAsymphony SP
 Folha de protocolo QIAsymphony SP Tissue_LC_200_V7_DSP e Tissue_HC_200_V7_DSP Informações gerais Para utilização em diagnóstico in vitro Este protocolo destina-se à purificação do ADN total de tecidos
Folha de protocolo QIAsymphony SP Tissue_LC_200_V7_DSP e Tissue_HC_200_V7_DSP Informações gerais Para utilização em diagnóstico in vitro Este protocolo destina-se à purificação do ADN total de tecidos
Instruções de Uso XGEN RNA REFERÊNCIA/p210 Kit de RNA Referência para Quantificação de cdna de BCR/ABL p210
 Instruções de Uso XGEN RNA REFERÊNCIA/p210 Kit de RNA Referência para Quantificação de cdna de BCR/ABL p210 1. USO PRETENDIDO O kit XGEN RNA REFERÊNCIA/p210 é destinado para a avaliação de desempenho do
Instruções de Uso XGEN RNA REFERÊNCIA/p210 Kit de RNA Referência para Quantificação de cdna de BCR/ABL p210 1. USO PRETENDIDO O kit XGEN RNA REFERÊNCIA/p210 é destinado para a avaliação de desempenho do
MANUAL DO UTILIZADOR. Aspirador de Secreções DeVilbiss 7305P 24 HORAS
 MANUAL DO UTILIZADOR www.praxair-crd.pt Aspirador de Secreções DeVilbiss 7305P 24 HORAS 800 201 519 Aspirador de Secreções DeVilbiss 7305P 3 Aspirador de Secreções DeVilbiss 7305 ÍNDICE DESCRIÇÃO DO EQUIPAMENTO
MANUAL DO UTILIZADOR www.praxair-crd.pt Aspirador de Secreções DeVilbiss 7305P 24 HORAS 800 201 519 Aspirador de Secreções DeVilbiss 7305P 3 Aspirador de Secreções DeVilbiss 7305 ÍNDICE DESCRIÇÃO DO EQUIPAMENTO
Progensa PCA3 Urine Specimen Transport Kit
 Progensa PCA3 Urine Specimen Transport Kit Instruções para o médico Para uso em diagnóstico in vitro. Exclusivamente para exportação dos EUA. Instruções 1. Pode ser útil pedir ao paciente que beba uma
Progensa PCA3 Urine Specimen Transport Kit Instruções para o médico Para uso em diagnóstico in vitro. Exclusivamente para exportação dos EUA. Instruções 1. Pode ser útil pedir ao paciente que beba uma
Preparação Manual de Amostras Utilizando o ABBOTT msample Preparation System DNA para RealTime High Risk HPV
 Preparação Manual de Amostras Utilizando o ABBOTT msample Preparation System DNA para RealTime High Risk HPV Nº. de lista 03N92-06 Abbott Max-Planck-Ring 2 65205 Wiesbaden Alemanha +49-6122-580 Abbott
Preparação Manual de Amostras Utilizando o ABBOTT msample Preparation System DNA para RealTime High Risk HPV Nº. de lista 03N92-06 Abbott Max-Planck-Ring 2 65205 Wiesbaden Alemanha +49-6122-580 Abbott
Prática de Laboratório 1
 Prática de Laboratório 1 12 pontos Preparação do ácido 2-iodobenzóico [Tempo aprox: 1 hr] Essa prática de laboratório envolve a preparação do acido 2-iodobenzóico a partir do acido 2-aminobenzóico. O procedimento
Prática de Laboratório 1 12 pontos Preparação do ácido 2-iodobenzóico [Tempo aprox: 1 hr] Essa prática de laboratório envolve a preparação do acido 2-iodobenzóico a partir do acido 2-aminobenzóico. O procedimento
BeoLab Livro de consulta
 BeoLab 8002 Livro de consulta Utilização diária 3 Quando terminar a instalação das colunas conforme descrito nas páginas seguintes, ligue todo o sistema à alimentação eléctrica. A luz indicadora fica
BeoLab 8002 Livro de consulta Utilização diária 3 Quando terminar a instalação das colunas conforme descrito nas páginas seguintes, ligue todo o sistema à alimentação eléctrica. A luz indicadora fica
Abbott. Preparação manual de amostras para o ensaio Abbott RealTime HCV Genotype II B2N /R Abbott Laboratories/Printed in Germany
 Abbott mtm Preparação manual de amostras para o ensaio Abbott RealTime HCV Genotype II Abbott Molecular Inc. 1300 E. Touhy Ave. Des Plaines, IL 60018 www.abbottmolecular.com ABBOTT Max-Planck-Ring 2 65205
Abbott mtm Preparação manual de amostras para o ensaio Abbott RealTime HCV Genotype II Abbott Molecular Inc. 1300 E. Touhy Ave. Des Plaines, IL 60018 www.abbottmolecular.com ABBOTT Max-Planck-Ring 2 65205
Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio.
 ATIVIDADE 2 - CÁLCULO DE CONCENTRAÇÃO Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio. Exercício 2. Calcule
ATIVIDADE 2 - CÁLCULO DE CONCENTRAÇÃO Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio. Exercício 2. Calcule
Instruções de uso. RealStar Norovirus RT-PCR Kit /2017 PT
 Instruções de uso RealStar Norovirus RT-PCR Kit 2.0 01/2017 PT RealStar Norovirus RT-PCR Kit 2.0 Para utilização com m2000rt (Abbott Diagnostics) Mx 3005P QPCR System (Stratagene) VERSANT kpcr Molecular
Instruções de uso RealStar Norovirus RT-PCR Kit 2.0 01/2017 PT RealStar Norovirus RT-PCR Kit 2.0 Para utilização com m2000rt (Abbott Diagnostics) Mx 3005P QPCR System (Stratagene) VERSANT kpcr Molecular
LABORATÓRIO ANÁLISE. PROCEDIMENTO OPERACIONAL PADRÃO. ANALITICO
 Edição Análise Crítica Aprovação Data / / Data: / / Data: / / ASS.: ASS.: ASS.: NOME: Rozileide Agostinho NOME:Rozileide Agostinho NOME: Marcelo Villar FUNÇÃO/CARGO: Controle de Documentos e Dados FUNÇÃO/CARGO:
Edição Análise Crítica Aprovação Data / / Data: / / Data: / / ASS.: ASS.: ASS.: NOME: Rozileide Agostinho NOME:Rozileide Agostinho NOME: Marcelo Villar FUNÇÃO/CARGO: Controle de Documentos e Dados FUNÇÃO/CARGO:
CLART PneumoVir CARACTERIZAÇÃO DE VÍRUS QUE CAUSAM INFECÇÕES RESPIRATÓRIAS HUMANAS ATRAVÉS DA IDENTIFICAÇÃO GENÓMICA PARA DIAGNÓSTICO IN VITRO
 CLART PneumoVir CARACTERIZAÇÃO DE VÍRUS QUE CAUSAM INFECÇÕES RESPIRATÓRIAS HUMANAS ATRAVÉS DA IDENTIFICAÇÃO GENÓMICA PARA DIAGNÓSTICO IN VITRO CLART Pneumovir Extracção Purificação 24 determinações Refª
CLART PneumoVir CARACTERIZAÇÃO DE VÍRUS QUE CAUSAM INFECÇÕES RESPIRATÓRIAS HUMANAS ATRAVÉS DA IDENTIFICAÇÃO GENÓMICA PARA DIAGNÓSTICO IN VITRO CLART Pneumovir Extracção Purificação 24 determinações Refª
Instruções de uso. RealStar Clostridium difficile PCR Kit /2017 PT
 Instruções de uso RealStar Clostridium difficile PCR Kit 1.0 01/2017 PT RealStar Clostridium difficile PCR Kit 1.0 Para utilização com m2000rt (Abbott Diagnostics) Mx 3005P QPCR System (Stratagene) VERSANT
Instruções de uso RealStar Clostridium difficile PCR Kit 1.0 01/2017 PT RealStar Clostridium difficile PCR Kit 1.0 Para utilização com m2000rt (Abbott Diagnostics) Mx 3005P QPCR System (Stratagene) VERSANT
FISIOLOGIA ANIMAL II
 DEPARTAMENTO DE ZOOLOGIA FACULDADE DE CIÊNCIAS E TECNOLOGIA UNIVERSIDADE DE COIMBRA FISIOLOGIA ANIMAL II AULA 5 Teste ELISA para o VIH PAULO SANTOS 2006 1 OBJECTIVOS Consolidar conhecimentos relativos
DEPARTAMENTO DE ZOOLOGIA FACULDADE DE CIÊNCIAS E TECNOLOGIA UNIVERSIDADE DE COIMBRA FISIOLOGIA ANIMAL II AULA 5 Teste ELISA para o VIH PAULO SANTOS 2006 1 OBJECTIVOS Consolidar conhecimentos relativos
artus BK Virus QS-RGQ Kit
 artus BK Virus QS-RGQ Kit Características de desempenho artus BK Virus QS-RGQ Kit, versão 1, 4514363 Verificar a disponibilidade de novas revisões de rotulagem eletrónica em www.qiagen.com/products/artusbkvirusrgpcrkit.aspx
artus BK Virus QS-RGQ Kit Características de desempenho artus BK Virus QS-RGQ Kit, versão 1, 4514363 Verificar a disponibilidade de novas revisões de rotulagem eletrónica em www.qiagen.com/products/artusbkvirusrgpcrkit.aspx
HEMOCENTRO RP TÉCNICA
 P. 1/9 1. OBJETIVO Genotipar os Alelos HLA em alta resolução. 2. APLICAÇÃO Aplica-se a amostras de DNA de pacientes e doadores. 3. RESPONSABILIDADE Assistentes de Laboratório, Técnicos, Aprimorandos, Bolsistas
P. 1/9 1. OBJETIVO Genotipar os Alelos HLA em alta resolução. 2. APLICAÇÃO Aplica-se a amostras de DNA de pacientes e doadores. 3. RESPONSABILIDADE Assistentes de Laboratório, Técnicos, Aprimorandos, Bolsistas
Em nossos experimento serão utilizadas células SH SY5Y, uma sublinhagem de células de neuroblastoma SK-N-SH, figura 1.
 Procedimentos Em nossos experimento serão utilizadas células SH SY5Y, uma sublinhagem de células de neuroblastoma SK-N-SH, figura 1. As células serão submetidas a estresse oxidativo por meio do tratamento
Procedimentos Em nossos experimento serão utilizadas células SH SY5Y, uma sublinhagem de células de neuroblastoma SK-N-SH, figura 1. As células serão submetidas a estresse oxidativo por meio do tratamento
Características de desempenho
 Características de desempenho Kit QIAamp DSP DNA FFPE Tissue, Versão 1 60404 Gestão de versão Este documento é designado de Características de desempenho do Kit QIAamp DSP DNA FFPE Tissue, versão 1, R3.
Características de desempenho Kit QIAamp DSP DNA FFPE Tissue, Versão 1 60404 Gestão de versão Este documento é designado de Características de desempenho do Kit QIAamp DSP DNA FFPE Tissue, versão 1, R3.
Apostila de aula prática REAÇÃO EM CADEIA PELA POLIMERASE (PCR)
 1 Universidade Federal Fluminense Instituto Biomédico Departamento de Microbiologia e Parasitologia Curso: Medicina Veterinária Disciplina: Virologia III (MIP00071) Apostila de aula prática REAÇÃO EM CADEIA
1 Universidade Federal Fluminense Instituto Biomédico Departamento de Microbiologia e Parasitologia Curso: Medicina Veterinária Disciplina: Virologia III (MIP00071) Apostila de aula prática REAÇÃO EM CADEIA
Termocicladores. versão
 Termocicladores Os Termocicladores são equipamentos usados em Biologia Molecular que realizam os ciclos de temperaturas necessários para uma reação em cadeia da polimerização ou amplificação de DNA. Os
Termocicladores Os Termocicladores são equipamentos usados em Biologia Molecular que realizam os ciclos de temperaturas necessários para uma reação em cadeia da polimerização ou amplificação de DNA. Os
ID Gene Bluetongue Duplex
 1279 Certified management system ID Gene Bluetongue Duplex Ref: IDBTV-50 / IDBTV-100 50 / 100 testes PCR Real Time para a detecção qualitativa do Vírus da Língua Azul (BTV) Amostra adequada: sangue total
1279 Certified management system ID Gene Bluetongue Duplex Ref: IDBTV-50 / IDBTV-100 50 / 100 testes PCR Real Time para a detecção qualitativa do Vírus da Língua Azul (BTV) Amostra adequada: sangue total
BD ProbeTec ET. Instruções do Equipamento Periférico para Micobactérias
 BD ProbeTec ET Instruções do Equipamento Periférico para Micobactérias 2003/07 Becton, Dickinson and Company N de Documento: L 006357(B) 7 Loveton Circle Sparks, Maryland 21152 USA Tel: 800.638.8663 BENEX
BD ProbeTec ET Instruções do Equipamento Periférico para Micobactérias 2003/07 Becton, Dickinson and Company N de Documento: L 006357(B) 7 Loveton Circle Sparks, Maryland 21152 USA Tel: 800.638.8663 BENEX
Normas básicas de segurança no laboratório de química
 Atitude Responsável Vestuário Vista sempre uma bata que o proteja adequadamente. Não a use fora da área dos laboratórios. Use sempre óculos de segurança Espaço Conheça a localização de saídas de emergência,
Atitude Responsável Vestuário Vista sempre uma bata que o proteja adequadamente. Não a use fora da área dos laboratórios. Use sempre óculos de segurança Espaço Conheça a localização de saídas de emergência,
Solidificação e fusão da água
 Solidificação e fusão da água A temperatura de solidificação é a temperatura à qual a substância passa de líquido a sólido. Temperatura de ebulição é a temperatura à qual a substância passa de sólido a
Solidificação e fusão da água A temperatura de solidificação é a temperatura à qual a substância passa de líquido a sólido. Temperatura de ebulição é a temperatura à qual a substância passa de sólido a
Para 1L de meio triptona ou peptona 16g (1,6%) extrato de levedura 10g (1%) NaCl 5g (0,5%)
 Preparação de meio líquido - triptona ou peptona - extrato de levedura 1º Dissolver a triptona e o extrato; 2º Acrescentar o cloreto de sódio e acertar o volume; 3º Após tudo dissolvido e com volume correto,
Preparação de meio líquido - triptona ou peptona - extrato de levedura 1º Dissolver a triptona e o extrato; 2º Acrescentar o cloreto de sódio e acertar o volume; 3º Após tudo dissolvido e com volume correto,
Condição de estoque: 20 C. Apresentação: qpcr SYBR Green mix 2 x µl (para 200 reações
 qpcr-sybr-green mix / ROX Condição de estoque: 20 C. Apresentação: qpcr SYBR Green mix 2 x 1.250 µl (para 200 reações de 24 µl) MgCl 2 1,25 ml Padrões de amplificação de DNA e oligos em três concentrações:
qpcr-sybr-green mix / ROX Condição de estoque: 20 C. Apresentação: qpcr SYBR Green mix 2 x 1.250 µl (para 200 reações de 24 µl) MgCl 2 1,25 ml Padrões de amplificação de DNA e oligos em três concentrações:
Métodos Analíticos de Controle de Alergênicos em Alimentos Juliana Ramos - R-Biopharm Brasil
 Reunião de vendas II/14 Campinas SP 26. 28. de Agosto 2014 Métodos Analíticos de Controle de Alergênicos em Alimentos Juliana Ramos - R-Biopharm Brasil Alergias Alimentares Alergias Alimentares 170 alimentos
Reunião de vendas II/14 Campinas SP 26. 28. de Agosto 2014 Métodos Analíticos de Controle de Alergênicos em Alimentos Juliana Ramos - R-Biopharm Brasil Alergias Alimentares Alergias Alimentares 170 alimentos
CentoCard. Simplifica a sua logística Cartão-filtro para a coleta de amostras de pacientes
 CentoCard Simplifica a sua logística Cartão-filtro para a coleta de amostras de pacientes CentoCard Simpliica a sua logística Cartão-iltro para a coleta de amostras de pacientes Enviar amostras biológicas
CentoCard Simplifica a sua logística Cartão-filtro para a coleta de amostras de pacientes CentoCard Simpliica a sua logística Cartão-iltro para a coleta de amostras de pacientes Enviar amostras biológicas
FORNO ELÉTRICO EPV-8009
 Manual de Instruções FORNO ELÉTRICO EPV-8009 SOMENTE PARA USO DOMÉSTICO Leia atentamente as informações contidas neste manual antes de usar o aparelho. INFORMAÇÕES DE SEGURANÇA: 1. Antes de utilizar o
Manual de Instruções FORNO ELÉTRICO EPV-8009 SOMENTE PARA USO DOMÉSTICO Leia atentamente as informações contidas neste manual antes de usar o aparelho. INFORMAÇÕES DE SEGURANÇA: 1. Antes de utilizar o
S8 Resumo das informações mais importantes
 S8 Resumo das informações mais importantes S8 Resumo das informações mais importantes J Este manual breve não substitui o Manual de instruções S8. Primeiro, leia e respeite as instruções de segurança e
S8 Resumo das informações mais importantes S8 Resumo das informações mais importantes J Este manual breve não substitui o Manual de instruções S8. Primeiro, leia e respeite as instruções de segurança e
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 )
 SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
J6/J600 Resumo das informações mais importantes
 J6/J600 Resumo das informações mais importantes J6/J600 Resumo das informações mais importantes J Este manual breve não substitui o Manual de instruções J6/J600. Primeiro, leia e respeite as instruções
J6/J600 Resumo das informações mais importantes J6/J600 Resumo das informações mais importantes J Este manual breve não substitui o Manual de instruções J6/J600. Primeiro, leia e respeite as instruções
Informações ao Consumidor. Teste Ca Veromar
 Informações ao Consumidor Teste Ca Veromar O cálcio é quinto elemento mais abundante na água do mar. Tem grande importância para os animais marinhos, estando presente nas estruturas rígidas de corais,
Informações ao Consumidor Teste Ca Veromar O cálcio é quinto elemento mais abundante na água do mar. Tem grande importância para os animais marinhos, estando presente nas estruturas rígidas de corais,
TÉCNICA SIMPLIFICADA DE COLHEITA DE MATERIAL EM ANIMAIS PARA O DIAGNÓSTICO DA RAIVA
 TÉCNICA SIMPLIFICADA DE COLHEITA DE MATERIAL EM ANIMAIS PARA O DIAGNÓSTICO DA RAIVA (Fotos gentilmente cedidas pelo KwaZulu-Natal Rabies Project e pelo Serengueti Carnivore Disease Project) Preparação
TÉCNICA SIMPLIFICADA DE COLHEITA DE MATERIAL EM ANIMAIS PARA O DIAGNÓSTICO DA RAIVA (Fotos gentilmente cedidas pelo KwaZulu-Natal Rabies Project e pelo Serengueti Carnivore Disease Project) Preparação
Protocolo de pré-desinfecção/lavagem manual e de esterilização das pontas e limas SATELEC
 Protocolo de pré-desinfecção/lavagem manual e de esterilização das pontas e limas SATELEC Avisos: Não utilize esfregões ou produtos de limpeza abrasivos. Evite usar soluções que contenham iodo ou uma elevada
Protocolo de pré-desinfecção/lavagem manual e de esterilização das pontas e limas SATELEC Avisos: Não utilize esfregões ou produtos de limpeza abrasivos. Evite usar soluções que contenham iodo ou uma elevada
INSTRUÇÕES DE USO. Padrões Moleculares Helix Elite USO PRETENDIDO RESUMO E EXPLICAÇÃO PRINCÍPIOS COMPOSIÇÃO
 INSTRUÇÕES DE USO Padrões Moleculares Helix Elite USO PRETENDIDO Os Padrões Moleculares sintéticos Helix Elite devem ser utilizados como material de controle positivo em aplicações moleculares. RESUMO
INSTRUÇÕES DE USO Padrões Moleculares Helix Elite USO PRETENDIDO Os Padrões Moleculares sintéticos Helix Elite devem ser utilizados como material de controle positivo em aplicações moleculares. RESUMO
EXTRAÇÃO DE DNA DE SANGUE (LEUCÓCITOS)
 EXTRAÇÃO DE DNA DE SANGUE (LEUCÓCITOS) A) Obtenção de Leucócitos 1. Coletar 5mL de sangue em tubos contendo EDTA potássio (50uL de EDTA (k 3) a 15%). O EDTA é uma substância anticoagulante. Existem outras
EXTRAÇÃO DE DNA DE SANGUE (LEUCÓCITOS) A) Obtenção de Leucócitos 1. Coletar 5mL de sangue em tubos contendo EDTA potássio (50uL de EDTA (k 3) a 15%). O EDTA é uma substância anticoagulante. Existem outras
O LABORATÓRIO DE MICROBIOLOGIA
 O LABORATÓRIO DE MICROBIOLOGIA Instalações Sala de manipulações cores claras, iluminação natural (preferencialmente) s/ correntes de ar. Superfícies de trabalho revestidas por materiais lisos, resistentes,
O LABORATÓRIO DE MICROBIOLOGIA Instalações Sala de manipulações cores claras, iluminação natural (preferencialmente) s/ correntes de ar. Superfícies de trabalho revestidas por materiais lisos, resistentes,
Conjunto de slides educacionais
 Conjunto de slides educacionais Objectivos de aprendizagem e conteúdo Objectivos de aprendizagem: Familiarização com as principais diferenças de NovoSeven estável à temperatura ambiente, Compreensão dos
Conjunto de slides educacionais Objectivos de aprendizagem e conteúdo Objectivos de aprendizagem: Familiarização com as principais diferenças de NovoSeven estável à temperatura ambiente, Compreensão dos
Protocolo. Extração de Proteínas Totais de Planta. Método Fenol Modificado de:
 Protocolo Extração de Proteínas Totais de Planta Método Fenol Modificado de: Hurkman W. J. and Tanaka C. K. (1986). Solubilization of Plant Membrane Proteins for Analysis by Two-Dimensional Gel Electrophoresis.
Protocolo Extração de Proteínas Totais de Planta Método Fenol Modificado de: Hurkman W. J. and Tanaka C. K. (1986). Solubilization of Plant Membrane Proteins for Analysis by Two-Dimensional Gel Electrophoresis.
Hibridação in situ por fluorescência FISH
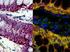 Universidade Estadual de Londrina Departamento de Biologia Geral Laboratório de Citogenética Animal - LACA Hibridação in situ por fluorescência FISH O protocolo descrito a seguir foi baseado nos procedimentos
Universidade Estadual de Londrina Departamento de Biologia Geral Laboratório de Citogenética Animal - LACA Hibridação in situ por fluorescência FISH O protocolo descrito a seguir foi baseado nos procedimentos
Z6 Resumo das informações mais importantes
 PROFESSIONAL AROMA GRINDER Z6 Resumo das informações mais importantes J Este manual breve não substitui o Manual de instruções Z6. Primeiro, leia e respeite as instruções de segurança e advertências para
PROFESSIONAL AROMA GRINDER Z6 Resumo das informações mais importantes J Este manual breve não substitui o Manual de instruções Z6. Primeiro, leia e respeite as instruções de segurança e advertências para
Célia Fagundes da Cruz
 LABORATÓRIO CENTRAL DO ESTADO DO PARANÁ - LACEN/PR Célia Fagundes da Cruz Julho/2012 SUPERINTENDÊNCIA DE VIGILÂNCIA EM SAÚDE - SVS LABORATÓRIO CENTRAL DO ESTADO DO PARANÁ - LACEN/PR LACEN/PR: 117 anos
LABORATÓRIO CENTRAL DO ESTADO DO PARANÁ - LACEN/PR Célia Fagundes da Cruz Julho/2012 SUPERINTENDÊNCIA DE VIGILÂNCIA EM SAÚDE - SVS LABORATÓRIO CENTRAL DO ESTADO DO PARANÁ - LACEN/PR LACEN/PR: 117 anos
Procedimento Operacional Padrão EBRACLEAN
 EBRACLEAN Solução desincrustante e biocida para limpeza e lavagem especial do sistema hidráulico de analisadores hematológicos. AMOSTRA Não se aplica EBRACLEAN MS: 10159820133 Analisadores hematológicos
EBRACLEAN Solução desincrustante e biocida para limpeza e lavagem especial do sistema hidráulico de analisadores hematológicos. AMOSTRA Não se aplica EBRACLEAN MS: 10159820133 Analisadores hematológicos
AMBICARE INDUSTRIAL Tratamento de Resíduos, S.A. HYDROSCOUT (USEPA SW-846 DRAFT METHOD 9001) Pág 1 de 5
 HYDROSCOUT (USEPA SW-846 DRAFT METHOD 9001) Pág 1 de 5 HYDROSCOUT Cada embalagem de reagentes contém: 1 40 tubos de plástico com tampa branca e septo cinzento, com uma ampola cinzenta. 2 40 ampolas de
HYDROSCOUT (USEPA SW-846 DRAFT METHOD 9001) Pág 1 de 5 HYDROSCOUT Cada embalagem de reagentes contém: 1 40 tubos de plástico com tampa branca e septo cinzento, com uma ampola cinzenta. 2 40 ampolas de
CONTROLE Rh Monoclonal
 CONTROLE Rh Monoclonal PROTHEMO Produtos Hemoterápicos Ltda. Controle negativo das classificações Rh - Hr PARA TESTES EM LÂMINA OU TUBO Somente para Uso Diagnóstico IN VITRO Conservar entre: 2-8 C Não
CONTROLE Rh Monoclonal PROTHEMO Produtos Hemoterápicos Ltda. Controle negativo das classificações Rh - Hr PARA TESTES EM LÂMINA OU TUBO Somente para Uso Diagnóstico IN VITRO Conservar entre: 2-8 C Não
TECHNOLOGY Awareness - Cost-Effective by Design
 AWARENESS TECHNOLOGY 2017 Analisadores Químicos Analisadores EIA Analisadores ISE Equipamento EIA/CLIA Luminómetros Analisadores Automáticos Awareness - Cost-Effective by Design 01 ANALISADORES QUÍMICOS
AWARENESS TECHNOLOGY 2017 Analisadores Químicos Analisadores EIA Analisadores ISE Equipamento EIA/CLIA Luminómetros Analisadores Automáticos Awareness - Cost-Effective by Design 01 ANALISADORES QUÍMICOS
E8/E80/E800 Resumo das informações mais importantes
 E8/E80/E800 Resumo das informações mais importantes J Este manual breve não substitui o Manual de instruções E8/E80/ E800. Primeiro, leia e respeite as instruções de segurança e advertências para evitar
E8/E80/E800 Resumo das informações mais importantes J Este manual breve não substitui o Manual de instruções E8/E80/ E800. Primeiro, leia e respeite as instruções de segurança e advertências para evitar
Teste Simplificado para Detecção de Coliformes Totais
 NOV 2011 BLH-IFF/NT- 40.11 Rede Nacional de Bancos de Leite Humano PNQBLH Programa Nacional de Qualidade em Bancos de Leite Humano Sede: FIOCRUZ/IFF-BLH Av. Rui Barbosa, 716 Flamengo Rio de Janeiro CEP:
NOV 2011 BLH-IFF/NT- 40.11 Rede Nacional de Bancos de Leite Humano PNQBLH Programa Nacional de Qualidade em Bancos de Leite Humano Sede: FIOCRUZ/IFF-BLH Av. Rui Barbosa, 716 Flamengo Rio de Janeiro CEP:
produtos one step ahead missão visão valores capital humano
 o n e s t e p a h e a d A Certest Biotec é uma empresa especializada em biotecnologia com uma vasta experiência no desenvolvimento de produtos de diagnóstico in vitro em aplicações humanas, veterinárias
o n e s t e p a h e a d A Certest Biotec é uma empresa especializada em biotecnologia com uma vasta experiência no desenvolvimento de produtos de diagnóstico in vitro em aplicações humanas, veterinárias
KITS DE EXTRAÇÃO DNA E RNA
 ACERTE COM PRECISÃO KITS DE EXTRAÇÃO DNA E RNA A Linha Biopur para extração e purificação de DNA e RNA possui kits variados com tecnologia para procedimentos manual (Mini Spin e Mini Cent) e para automação
ACERTE COM PRECISÃO KITS DE EXTRAÇÃO DNA E RNA A Linha Biopur para extração e purificação de DNA e RNA possui kits variados com tecnologia para procedimentos manual (Mini Spin e Mini Cent) e para automação
2. Aplicabilidade: Bioquímicos/biomédicos do setor de imunologia
 1. Sinonímia: HIV triagem, HIV teste rápido. 2. Aplicabilidade: Bioquímicos/biomédicos do setor de imunologia 3. Aplicação clínica Utilizado para investigar a infecção pelo vírus da imunodeficiência humana.
1. Sinonímia: HIV triagem, HIV teste rápido. 2. Aplicabilidade: Bioquímicos/biomédicos do setor de imunologia 3. Aplicação clínica Utilizado para investigar a infecção pelo vírus da imunodeficiência humana.
Protocolo de pré-desinfecção/lavagem manual e de esterilização do conjunto peça de mão e cabo Piezotome SATELEC
 Protocolo de pré-desinfecção/lavagem manual e de esterilização do conjunto peça de mão e cabo Piezotome SATELEC Avisos Não utilize esfregões ou produtos de limpeza abrasivos. Evite usar soluções que contenham
Protocolo de pré-desinfecção/lavagem manual e de esterilização do conjunto peça de mão e cabo Piezotome SATELEC Avisos Não utilize esfregões ou produtos de limpeza abrasivos. Evite usar soluções que contenham
AMPLIFICAÇÃO CFTR. Instruções de Uso
 AMPLIFICAÇÃO CFTR Instruções de Uso USO PRETENDIDO O kit de Amplificação CFTR, para uso in vitro, destina-se à amplificação multiplex dos ácidos nucleicos respectivamente às regiões 8 (éxon/íntron4, íntron5,
AMPLIFICAÇÃO CFTR Instruções de Uso USO PRETENDIDO O kit de Amplificação CFTR, para uso in vitro, destina-se à amplificação multiplex dos ácidos nucleicos respectivamente às regiões 8 (éxon/íntron4, íntron5,
E S T U D O D E U M E L É C T R O D O S E L E T I V O D E I Ã O N I T R A T O
 E S T U D O D E U M E L É C T R O D O S E L E T I V O D E I Ã O N I T R A T O OBJETIVO Pretende-se com este trabalho experimental que os alunos avaliem as características de um eléctrodo sensível a ião
E S T U D O D E U M E L É C T R O D O S E L E T I V O D E I Ã O N I T R A T O OBJETIVO Pretende-se com este trabalho experimental que os alunos avaliem as características de um eléctrodo sensível a ião
INSTALAÇÃO DE PISOS COLADOS (BASE DE CORTIÇA)
 INSTALAÇÃO DE PISOS COLADOS (BASE DE CORTIÇA) INFORMAÇÃO GERAL Os revestimentos Corklife colados destinam-se apenas a uso exclusivo no interior. Leia as seguintes instruções antes de instalar. Guarde as
INSTALAÇÃO DE PISOS COLADOS (BASE DE CORTIÇA) INFORMAÇÃO GERAL Os revestimentos Corklife colados destinam-se apenas a uso exclusivo no interior. Leia as seguintes instruções antes de instalar. Guarde as
TÉCNICAS PARASITOLÓGICAS DE TF-TEST (THREE FECAL TEST) CONVENTIONAL E MODIFIED
 TÉCNICAS PARASITOLÓGICAS DE TF-TEST (THREE FECAL TEST) CONVENTIONAL E MODIFIED I. COMENTÁRIOS A técnica parasitológica de TF-Test Conventional, utilizando o kit comercial TF- Test, foi avaliada para o
TÉCNICAS PARASITOLÓGICAS DE TF-TEST (THREE FECAL TEST) CONVENTIONAL E MODIFIED I. COMENTÁRIOS A técnica parasitológica de TF-Test Conventional, utilizando o kit comercial TF- Test, foi avaliada para o
FISPQ (Ficha de Informações de Segurança de Produtos Químicos) KALIPTO ÓLEO DE PINHO KALIPTO ÓLEO DE EUCALIPTO
 Página 1 de 6 1 - IDENTIFICAÇÃO DO PRODUTO E DA EMPRESA Nome: Kalipto Óleo de Pinho Código interno: 9300 Nome: Kalipto Óleo de Eucalipto Código interno: 9301 Empresa: BOMBRIL S/A TELEFONE DE EMERGÊNCIA:
Página 1 de 6 1 - IDENTIFICAÇÃO DO PRODUTO E DA EMPRESA Nome: Kalipto Óleo de Pinho Código interno: 9300 Nome: Kalipto Óleo de Eucalipto Código interno: 9301 Empresa: BOMBRIL S/A TELEFONE DE EMERGÊNCIA:
HEMOCENTRO RP TÉCNICA
 P. 1/6 1. OBJETIVO Amplificar os genes HLA-A, B, C, DRB1, e DQA1/DQB1 para posterior identificação dos seus respectivos grupos alélicos. *1 2. APLICAÇÃO Aplica-se às amostras de DNA genômico de doadores
P. 1/6 1. OBJETIVO Amplificar os genes HLA-A, B, C, DRB1, e DQA1/DQB1 para posterior identificação dos seus respectivos grupos alélicos. *1 2. APLICAÇÃO Aplica-se às amostras de DNA genômico de doadores
AVALIAÇÃO DOS FATORES QUE INFLUENCIAM A VELOCIDADE DAS REAÇÕES QUÍMICAS: CONCENTRAÇÃO DE REAGENTES E TEMPERATURA DE REAÇÃO.
 AVALIAÇÃO DOS FATORES QUE INFLUENCIAM A VELOCIDADE DAS REAÇÕES QUÍMICAS: CONCENTRAÇÃO DE REAGENTES E TEMPERATURA DE REAÇÃO. Aula 11 Glauber Silva Godoi META Desenvolver no aluno a capacidade de avaliar
AVALIAÇÃO DOS FATORES QUE INFLUENCIAM A VELOCIDADE DAS REAÇÕES QUÍMICAS: CONCENTRAÇÃO DE REAGENTES E TEMPERATURA DE REAÇÃO. Aula 11 Glauber Silva Godoi META Desenvolver no aluno a capacidade de avaliar
FISPQ (Ficha de Informações de Segurança de Produtos Químicos) Q BRILHO CERA AUTO BRILHO
 Página 1 de 6 1. IDENTIFICAÇÃO DO PRODUTO E DA EMPRESA Nome do Produto: Q BRILHO CERA AUTO BRILHO Códigos internos: Incolor 12/750 ml: 7530 12/500 ml: 7531 - Refil Vermelha 12/750 ml: 7532 12/500 ml: 7537
Página 1 de 6 1. IDENTIFICAÇÃO DO PRODUTO E DA EMPRESA Nome do Produto: Q BRILHO CERA AUTO BRILHO Códigos internos: Incolor 12/750 ml: 7530 12/500 ml: 7531 - Refil Vermelha 12/750 ml: 7532 12/500 ml: 7537
VALIDAÇÃO DE MÉTODOS ANALÍTICOS
 VALIDAÇÃO DE MÉTODOS ANALÍTICOS RE nº 899, de 2003 da ANVISA - Guia para validação de métodos analíticos e bioanalíticos; Validation of analytical procedures - UNITED STATES PHARMACOPOEIA - última edição;
VALIDAÇÃO DE MÉTODOS ANALÍTICOS RE nº 899, de 2003 da ANVISA - Guia para validação de métodos analíticos e bioanalíticos; Validation of analytical procedures - UNITED STATES PHARMACOPOEIA - última edição;
NORMAS TÉCNICAS REDEBLH-BR PARA BANCOS DE LEITE HUMANO:
 NORMAS TÉCNICAS REDEBLH-BR PARA BANCOS DE LEITE HUMANO: Controle Sanitário de Leite Humano Ordenhado BLH-IFF/NT- 40.05 Teste Simplificado para Detecção de Coliformes Totais FEV 2005 BLH-IFF/NT- 40.05 Rede
NORMAS TÉCNICAS REDEBLH-BR PARA BANCOS DE LEITE HUMANO: Controle Sanitário de Leite Humano Ordenhado BLH-IFF/NT- 40.05 Teste Simplificado para Detecção de Coliformes Totais FEV 2005 BLH-IFF/NT- 40.05 Rede
INSTRUÇÕES DE INSTALAÇÃO PARA CORKLIFE DEKWALL
 INSTRUÇÕES DE INSTALAÇÃO PARA CORKLIFE DEKWALL INFORMAÇÃO GERAL Corklife Dekwall destina-se apenas a espaços interiores. Leia as seguintes instruções antes de instalar. Guarde as réguas na embalagem original
INSTRUÇÕES DE INSTALAÇÃO PARA CORKLIFE DEKWALL INFORMAÇÃO GERAL Corklife Dekwall destina-se apenas a espaços interiores. Leia as seguintes instruções antes de instalar. Guarde as réguas na embalagem original
Instruções de uso. RealStar HEV RT-PCR Kit /2017 PT
 Instruções de uso RealStar HEV RT-PCR Kit 1.0 01/2017 PT RealStar HEV RT-PCR Kit 1.0 Para utilização com m2000rt (Abbott Diagnostics) Mx 3005P QPCR System (Stratagene) VERSANT kpcr Molecular System AD
Instruções de uso RealStar HEV RT-PCR Kit 1.0 01/2017 PT RealStar HEV RT-PCR Kit 1.0 Para utilização com m2000rt (Abbott Diagnostics) Mx 3005P QPCR System (Stratagene) VERSANT kpcr Molecular System AD
MSDS (Material Safety Data Sheet) Lysoform Suave
 Página 1 de 5 1 - IDENTIFICAÇÃO DO PRODUTO E DA EMPRESA: Nome: Códigos internos: Empresa: BOMBRIL S/A INFORMAÇÃO AO CLIENTE: TELEFONE DE EMERGÊNCIA: 0800 014 8110 2 - COMPOSIÇÃO E INFORMAÇÕES SOBRE OS
Página 1 de 5 1 - IDENTIFICAÇÃO DO PRODUTO E DA EMPRESA: Nome: Códigos internos: Empresa: BOMBRIL S/A INFORMAÇÃO AO CLIENTE: TELEFONE DE EMERGÊNCIA: 0800 014 8110 2 - COMPOSIÇÃO E INFORMAÇÕES SOBRE OS
IQ-UFG. Curso Experimental de Química Geral e Inorgânica. Prof. Dr. Anselmo
 IQ-UFG Curso Experimental de Química Geral e Inorgânica Aula 02 Reconhecimento de Vidrarias e Introdução às Técnicas de Laboratório Prof. Dr. Anselmo Vidrarias e equipamentos usuais em laboratórios de
IQ-UFG Curso Experimental de Química Geral e Inorgânica Aula 02 Reconhecimento de Vidrarias e Introdução às Técnicas de Laboratório Prof. Dr. Anselmo Vidrarias e equipamentos usuais em laboratórios de
CYCLER CHECK. Kit de teste para a validação da uniformidade da temperatura em termocicladores. pronto a usar, pré-aliquotado. REF (4 testes)
 PT Instruções de utilização CYCLER CHECK Kit de teste para a validação da uniformidade da temperatura em termocicladores pronto a usar, pré-aliquotado REF 7104 (10 testes) REF 71044 (4 testes) Índice 1.
PT Instruções de utilização CYCLER CHECK Kit de teste para a validação da uniformidade da temperatura em termocicladores pronto a usar, pré-aliquotado REF 7104 (10 testes) REF 71044 (4 testes) Índice 1.
Aula Prática 04 Preparação de Emulsão de Brometo de Prata Não Lavada Emulsões 6 de Outubro de 2008
 Aula Prática 04 Preparação de Emulsão de Brometo de Prata Não Lavada Emulsões 6 de Outubro de 2008 Licenciatura em Fotografia, 3º ano, 2008-2009 Escola Superior de Tecnologia de Tomar Objectivos Primeiro
Aula Prática 04 Preparação de Emulsão de Brometo de Prata Não Lavada Emulsões 6 de Outubro de 2008 Licenciatura em Fotografia, 3º ano, 2008-2009 Escola Superior de Tecnologia de Tomar Objectivos Primeiro
Protocolo de pré-desinfecção/lavagem manual e de esterilização das chaves SATELEC
 CHAVES Protocolo de pré-desinfecção/lavagem manual e de esterilização das chaves SATELEC Avisos: Não utilize esfregões ou produtos de limpeza abrasivos. Evite usar soluções que contenham iodo ou uma elevada
CHAVES Protocolo de pré-desinfecção/lavagem manual e de esterilização das chaves SATELEC Avisos: Não utilize esfregões ou produtos de limpeza abrasivos. Evite usar soluções que contenham iodo ou uma elevada
Este protocolo diz respeito às peças de mão Suprasson, Newtron e Newtron LED
 PEÇAS DE MÃO DESTARTARIZADORAS: SUPRASSON/NEWTRON/NEWTRON LED Protocolo de pré-desinfecção/lavagem manual e de esterilização das peças de mão destartarizadoras SATELEC Este protocolo diz respeito às peças
PEÇAS DE MÃO DESTARTARIZADORAS: SUPRASSON/NEWTRON/NEWTRON LED Protocolo de pré-desinfecção/lavagem manual e de esterilização das peças de mão destartarizadoras SATELEC Este protocolo diz respeito às peças
Microbiologia alimentar Medronho. Maria João de Almeida Pessoa Trigo. Escola Secundária Fonseca de Benevides, Lisboa 4 de Fevereiro de 2014
 Microbiologia alimentar Medronho Maria João de Almeida Pessoa Trigo Escola Secundária Fonseca de Benevides, Lisboa 4 de Fevereiro de 2014 NORMAS DE SEGURANÇA Principais Normas de Segurança em Laboratório
Microbiologia alimentar Medronho Maria João de Almeida Pessoa Trigo Escola Secundária Fonseca de Benevides, Lisboa 4 de Fevereiro de 2014 NORMAS DE SEGURANÇA Principais Normas de Segurança em Laboratório
Z8 Resumo das informações mais importantes
 Z8 Resumo das informações mais importantes J Este manual breve não substitui o Manual de instruções Z8. Primeiro, leia e respeite as instruções de segurança e advertências para evitar perigos. Lavar o
Z8 Resumo das informações mais importantes J Este manual breve não substitui o Manual de instruções Z8. Primeiro, leia e respeite as instruções de segurança e advertências para evitar perigos. Lavar o
LÍDER MUNDIAL EM AUTOMAÇÃO. Pipetagem de alta performance para a sua rotina
 LÍDER MUNDIAL EM AUTOMAÇÃO Pipetagem de alta performance para a sua rotina Tecnologia de Pipetagem Avançada As plataformas de pipetagem da Hamilton são desenvolvidas com tecnologia de ponta e apresentam
LÍDER MUNDIAL EM AUTOMAÇÃO Pipetagem de alta performance para a sua rotina Tecnologia de Pipetagem Avançada As plataformas de pipetagem da Hamilton são desenvolvidas com tecnologia de ponta e apresentam
