LABORATÓRIOS DE QUÍMICA-FÍSICA E PROCESSOS
|
|
|
- Rachel Rocha Mascarenhas
- 7 Há anos
- Visualizações:
Transcrição
1 LABORATÓRIOS DE QUÍMICA-FÍSICA E PROCESSOS S-102 S-105 S-108 HCL (37%) S-101 Solução de Proteína P-1 / V-101 Precipitação S-103 P-2 / NFD-101 Filtração S-104 S-106 P-3 / FDR-101 Secagem (Freeze Drying) S-107 PROBLEMAS PROPOSTOS Módulo de Processos SuperPro Designer Mestrado Integrado em Engenharia Biológica Prof. José A. Leonardo Santos Departamento de Engenharia Química e Biológica 2008/2009
2 PROBLEMA 1 Na preparação de um meio de cultura para fermentação pretende-se efectuar a seguinte mistura: - Sacarose, com um caudal de 10,0 kg/min e à temperatura de 15ºC; - Uma solução aquosa com 10% (m/m) de glicerol, com um caudal de 50 L/min e à temperatura de 20ºC; e - Água, com um caudal de 60 L/min e à temperatura de 40ºC. 1. Para a corrente resultante desta mistura determinar: A) O caudal volumétrico (m 3 /h). Dados para o reservatório: B) A composição. Tempo de residência = 20 min C) A temperatura. Altura/Diâmetro = 2,5 D) Volume do reservatório. 2. Calcular o calor que é necessário fornecer à mistura para que a sua temperatura seja de 37ºC, Calcular o caudal da água de aquecimento. PROBLEMA 2 Uma corrente de 100 kg/h de biomassa húmida (contendo 40% de água) a 20ºC, passa através de um secador (spray drying), onde é removida 80% da água inicialmente presente. Sabendo que este secador é alimentado com ar seco a 0,5 bar e a 80ºC, determine: A) A percentagem de água na biomassa seca. B) O caudal mássico e volumétrico (PTT) de ar seco à entrada. C) As dimensões (altura e diâmetro) e número de unidades de secadores necessários. Dados: Tempo de operação anual = 7920 h (altura/diâmetro) secador = 2,0 Diâmetro máximo do secador = 1,2 m Velocidade de evaporação = 80 kg/m 3.h Ar seco utilizado = 15,0 kg/kg de água evaporada Temperatura dos sólidos secos à saída = 50ºC IST/DEQB 1
3 PROBLEMA 3 Pretende-se diluir e purificar continuamente uma solução aquosa stock de glucose. Esta solução apresenta a seguinte composição mássica: glucose 36%; impurezas insolúveis 4% e água 60%. Uma corrente desta solução, a 15ºC e com um caudal de 100 kg/h, é misturada com água, a 40ºC e com um caudal de 400 L/h. A mistura à saída do misturador deve estar à temperatura de 37ºC. Após esta operação, a mistura é filtrada para remoção total das impurezas. 400 L/h Água 40ºC 100 kg/h 15ºC Glucose 36% Água - 60% Impurezas - 4% Misturador 37ºC Filtro Glucose Água Impurezas + solução Indicar: A) A concentração de glucose à saída do filtro. B) Calor fornecido no tanque de mistura e o caudal de fluido de aquecimento. C) A dimensão característica (volume do tanque de mistura e área de filtração do filtro) e o número de unidades de cada peça de equipamento. Dados: Tempo de operação = 320 dias/ano = 7680 horas/ano Impurezas: Propriedades idênticas à da água com peso molecular de 100 g/mol Diâmetro médio dos agregados formados pelas impurezas = 0,15 µm Tanque de mistura: Tempo de residência = 10 min = 0,167 h Volume útil = 0,80 volume total Fluido de aquecimento (ÁGUA QUENTE): Temperatura de entrada = 80ºC Temperatura de saída = 60ºC Filtro: Área de filtração máxima = 2,0 m 2 Fluxo médio de filtração = 150 L/(h m 2 ) Concentração dos insolúveis no bolo de filtração = 0,50 (V/V) IST/DEQB 2
4 PROBLEMA 4 Células de uma bactéria geneticamente modificada, imobilizadas em k-carragénio, são utilizadas para converter glucose em ácido glutâmico (C 5 H 9 NO 4 ). As células imobilizadas não crescem mas conseguem metabolizar a glucose à temperatura de 25 C, de acordo com a reacção: C 6 H 12 O 6 + NH O2 C 5 H 9 NO 4 + CO H 2 O Hº R = kcal/kg de glucose O fermentador é alimentado continuamente por uma corrente líquida (composta por uma solução aquosa de glucose (4% mássica)) a 25 C e com um caudal de 100 kg/min (esterilizado com vapor a 130ºC), e por uma corrente gasosa (composta por ar e amoníaco (6% mássica)) a 15 C, 2 bar abs e com um caudal de 40 kg/min (esterilizada por filtração). O arrefecimento do fermentador é efectuado através da circulação de água fria numa camisa de refrigeração. Determinar: A) O caudal de solução e a concentração de ácido glutâmico. B) Os consumos energéticos do processo. C) As dimensões principais de todas as peças de equipamento. Dados: Tempo de operação = 330 dias/ano = 7920,0 horas/ano Ácido glutâmico: Propriedades semelhantes às das proteínas (massa molecular = 147,12 g/mol). Tanque de mistura: Temperatura de saída = 25ºC Tempo de residência = 10 min = 0,167 h Volume útil = 0,80 volume total Volume máximo = 2,0 m 3 H/D = 2,5 Esterilizador Temperatura de esterilização = 130ºC. Temperatura de pré-aquecimento = 100ºC Temperatura final = 25ºC IST/DEQB 3
5 Viscosidade da mistura = 0,95 cp Agente de aquecimento = vapor (152ºC) Agente de arrefecimento = água fria (5º/10ºC) Filtros A mistura ar/amoníaco é esterilizada por filtração. Caudal máximo = 1,0 m 3 /s Fermentador (contínuo, estequiométrico) Tempo de residência = 6,0 h Volume útil = 0,75 volume total Temperatura de saída = 25ºC Fluido de arrefecimento: água fria (10º/20ºC) Conversão da glucose = 95% Volume máximo = 25,0 m 3 H/D = 3,0 Tanque de armazenamento Tempo de residência = 3,0 h Volume útil = 0,80 volume total Temperatura de saída = 8ºC Fluido de arrefecimento: solução aquosa de NaCl (salmoura) (-10º/0ºC) Volume máximo = 10,0 m 3 H/D = 3,0 IST/DEQB 4
6 PROBLEMA 5 O formaldeído pode ser formado, num reactor catalítico, a partir de metanol através da reacção: CH 3 OH HCHO + H 2 Considerando que esta reacção tem uma conversão de 60% e que se pretende produzir 1,0 ton/h de formaldeído, estabelecer o balanço de massas ao reactor, quando: A) O metanol não consumido não é reutilizado. B) O metanol da corrente efluente do reactor é sujeita a uma separação completa e reciclado para a entrada do reactor. PROBLEMA 6 A produção de óxido de etileno (C 2 H 4 O) realizada por oxidação catalítica do etileno: 2 C 2 H 4 + O 2 2 C 2 H 4 O ocorrendo, para as condições da reacção, uma reacção secundária de combustão do etileno: C 2 H O 2 2 CO H 2 O Após as separações, os reagentes não consumidos são reciclados para o reactor, de acordo com o diagrama de blocos seguinte. O 2 C 2 H 4 O 2 C 2 H 4 Misturador C 2 H 4 40% O 2-60% Reactor Separadores H 2 O C 2 H 4 O CO 2 Sabendo que à entrada do reactor (reactor tubular, PFR) o oxigénio encontra-se com uma percentagem molar de 60% (63,1164% mássico), que a conversão do etileno é de 80% e que o selectividade é de 75%, calcule os caudais volumétricos (PTS) frescos de oxigénio e etileno de forma a produzir-se 1,5 ton/h de óxido de etileno. IST/DEQB 5
7 PROBLEMA 7 Pretende-se proceder à purificação descontínua (batch) de uma proteína, promovendo a sua precipitação total através do abaixamento do ph (Proteína Proteína PP). Para tal, é adicionado uma solução aquosa de HCl a 37% (% mássica) à solução de proteína, ocorrendo simultaneamente a neutralização total do hidróxido de sódio, segundo a reacção: NaOH + HCl NaCl + H 2 O Hº R = kcal/kg de NaOH A proteína precipitada (Proteína PP) é separada por filtração e depois seca, de acordo com o diagrama de blocos seguinte: HCl (37% mássico) Água de lavagem Vapor de água Proteína 12% Tanque de Precipitação Filtro Secador Proteína PP 92% NaOH - 2% Água - 84% Filtrado Água - 8% (% mássica) Impurezas 2% (% mássica) Para 1000 kg de solução inicial de proteína por batch, estabelecer o balanço de massas e de energia ao processo indicando: A) Os consumos de solução de HCl e de água de lavagem do filtrado. B) Os consumos energéticos no secador. C) As dimensões principais das três peças de equipamento. D) Duração de um ciclo e o número de ciclos por ano. DADOS: Proteína precipitada propriedades iguais ás proteínas solúveis. Impurezas - propriedades iguais ás da água, com massa molecular de 392 g/mol Tanque de precipitação Massa de solução de HCl = 6% da massa da solução de proteína inicial. As proteínas é o único componente que precipita. Caudais de alimentação (ou de carga): Solução de proteína = 120 kg/min ; Solução de HCl = 10 kg/min Setup time (*) : Solução de proteína = 15 min ; Solução de HCl = 0 min (*) - Tempo gasto antes de cada operação na preparação dessa operação (inclui limpeza, preparação do equipamento, etc.) IST/DEQB 6
8 Tempo de precipitação = 30 min Tempo de agitação igual ao tempo de precipitação Temperatura de saída = 25ºC Fluido de arrefecimento: água fria (5/10ºC) Volume máximo = 2 m 3 H/D = 2,5 Caudal de transferência do tanque para o filtro (transfer out). = Caudal de filtração Filtro Tipo de filtro: filtro de Nutsche Tempo de filtração = 60 min Fluxo de filtração = 80 L/hm 2 (= caudal por unidade de área da membrana) Porosidade do bolo (precipitado) de filtração = 0,40 v/v Lavagem do precipitado: Volume de água = 3 vezes o volume de precipitado (ou bolo de filtração) Tempo de lavagem = 30 min Fluxo de filtração = 150 L/hm 2 Área máxima de filtração = 8,0 m 2 Caudal de transferência do filtro para o secador (transfer out) = 400 kg/h Secador (Freeze Dryer ) Componente volátil: água LOD final (loss on drying)(*) = 8% (*) teor de água num sólido seco Tempo de operação = 90 min Temperatura do sólido seco = 10ºC Capacidade máxima de sublimação = 100 kg Fluido de aquecimento: vapor (152ºC); Massa de vapor = 3,0 kg de vapor/kg evaporado Lavagem do equipamento (CIP - cleaning in place) Tanque de precipitação: 1º passo: Água 20 min; 25ºC; 3,0 L/m 2 min; recircular 2 vezes 2º passo: NaOH (0,5 M) 10 min; 40ºC; 3,0 L/m 2 min; recircular 1 vezes 3º passo: Água 20 min; 25ºC; 3,0 L/m 2 min; recircular 2 vezes Nota: este procedimento deveria ser efectuado para todas as peças de equipamento. No entanto, a título exemplificativo, só vai ser efectuado para o tanque de precipitação. IST/DEQB 7
9 PROBLEMA 8 Pretende-se obter um extracto bruto de um enzima (com um baixo grau de pureza), de uma forma descontínua. Este enzima é produzido intracelularmente por uma bactéria (Escherichia coli), sendo o processo dividido em duas etapas: produção da bactéria por fermentação e recuperação do enzima. ETAPA A Fermentação da Escherichia coli Pretende-se produzir, de 2600 kg/batch de Escherichia coli, utilizando glucose como fonte de carbono e amónia como fonte de azoto, de acordo com a seguinte reacção: 1,77 NH ,00 C 6 H 12 O ,57 O 2 + 4,20 Sais 12,79 Biomassa + 22,38 CO ,37 H 2 O (coeficientes mássicos) O meio de fermentação necessário para a produção desta bactéria é preparado num tanque, onde são misturados kg de água com 7200 kg de (glucose (86,5%) + sais (13,5%)). Após esterilização contínua, esta solução é introduzida no fermentador juntamente com ar e com 400 kg de amónia gasosa. Todas estas correntes se encontram inicialmente a 25ºC e à pressão atmosférica. Nota: Considerar que os sais têm um peso molecular de 100 g/mol, sendo as restantes propriedades iguais às da água. Dados sobre as operações unitárias desta etapa: Tanque misturador Volume máximo = 100 m 3 Volume útil / volume total = 0,8 H/D = 2,5 Temperatura de saída = 25º Caudais de alimentação: Água = 2000 kg/min Nutrientes = 500 kg/min Caudal de transf. = Caudal do esterilizador Setup time : Água = 5 min Nutrientes = 10 min Esterilizador (modelo tipo plug flow ) Temperatura de esterilização = 140ºC Temperatura de pré-aquecimento = 110ºC Temperatura final = 37ºC Tempo de operação = 4 h Viscosidade do fluido = 0,9 cp Energia de activação = 67,7 kcal/mol IST/DEQB 8
10 ln(factor de frequência) = 84 s -1 Diâmetro da tubagem = 10 cm (rating modo ) Comprimento da tubagem = 3 m (rating modo ) Compressor Pressão = 5,0 bar Eficiência global = 70% Temperatura máxima à saída = 40ºC Potência máxima = 1000 kw Filtros (para o ar e para os gases de fermentação) Caudal máximo = 0,8 m 3 /s Fermentador Caudal de adição da amónia = 20 kg/min Temperatura = 37ºC Potência específica = 3,0 kw/m 3 Arejamento = 0,5 vvm Tempo de fermentação = 24 h 25ºC HR 2 Reacção: Conversão = 98% ; = 3750kcal/kg O Volume máximo = 350 m 3 H/D = 3,0 Volume útil / volume total = 0,75 Tempo de espera entre a fermentação e transferência para a centrífuga = 30 min ETAPA B Recuperação do Enzima Após as fermentação as células são concentradas por centrifugação e sujeitas a desintegração através de um homogenizador de alta pressão. Após a libertação do enzima o extracto é sujeito a uma microfiltração para remoção dos fragmentos celulares. Dados sobre as operações unitárias desta etapa: Centrífuga de discos (disck stack centrifuge ) Partículas sólidas: Solução ( água): - D min = 1,0 µm - ρ = 980 kg/m 3 - ρ = 1020 kg/m 3 - µ = 1,0 cp IST/DEQB 9
11 Eficiência de sedimentação = 40% (quando se aplica a lei de Stokes a eficiência é de 100%) Tempo de centrifugação = 6,0 h Recuperação de biomassa = 98% Temperatura à saída = 30ºC Concentração de sólidos nos concentrado = 250 g/l Área equivalente de sedimentação (Σ) = m 2 Tanque de arrefecimento Temperatura de saída = 10ºC Arrefecimento: - Eficiência = 90% - Capacidade calorífica do equipamento = 10 kcal/ºc - Tempo de operação = tempo de tranf. da centrífuga + tempo de transf. para o desintegrador Volume máximo = 50 m 3 Volume útil / volume total = 0,8 H/D = 2,5 Honogenizador de alta pressão (ruptura celular) Número de passagens = 2 Composição da biomassa: - Debris = 30% - Ácidos nucleicos (M = g/mol) = 20% - Proteínas (M = g/mol) = 45% - Enzima (M = g/mol) = 5% Percentagem de desintegração = 98% Desnaturação do enzima = 10% Tempo de operação = 8,0 h Temperatura de saída = 20ºC Caudal máximo = 3000 L/h Tanque Tempo de espera entre a ruptura e a microfiltração = 30 min Temperatura = 20ºC Restantes dados idênticos ao tanque misturador inicial IST/DEQB 10
12 Microfiltro Tempo de operação = 6,0 horas Fluxo de filtrado = 30,0 L/hm 2 Factor de concentração (volume inicial/volume final do concentrado) = 2,5 Concentração máxima de sólidos = 600 g/l Coeficientes de rejeição: - Biomassa = 100% - Debris = 100% - Ácidos nucleicos = 98% - Proteínas = 85% - Enzima = 15,0% Desnaturação do enzima = 3,0% Tanque Arrefecimento: temperatura = 15ºC; tempo = 60 min Caudal de transferência para o diafiltro = 100 kg/min Restantes dados idênticos ao tanque misturador inicial Diafiltro Tempo de operação = 4,0 horas Fluxo de filtrado = 15,0 L/hm 2 Factor de concentração (volume inicial/volume final do concentrado) = 15,0 Concentração máxima de sólidos = 600 g/l Coeficientes de rejeição: - Ácidos nucleicos = 100% - Proteínas = 100% - Enzima = 100% Desnaturação do enzima = 10,0% Secador (Freeze Dryer ) Componente volátil: água LOD final (loss on drying)(*) = 12% (*) teor de água num sólido seco Tempo de operação = 120 min Temperatura do sólido seco = 10ºC IST/DEQB 11
13 Capacidade máxima de sublimação = 200 kg Fluido de aquecimento: vapor (152ºC); Massa de vapor = 3,0 kg de vapor/kg evaporado QUESTÕES A) Estabelecer os balanços de massa e de energia. B) Indicar o rendimento global do processo C) Indicar a produção de enzima impuro e o número de batchs anuais. D) Indicar a(s) principal(ais) dimensão(ões) para todas as peças de equipamento. Flowsheet do processo S -101 Ág ua S Nutrientes S P -1 / V-101 Mis tura dor S P -2 / ST-101 Es te riliza do r S Amónia S P -6 / AF-102 Filtro de Gases S -111 S -106 S P -5 / V-103 S Ar S e co S P -3 / G -101 Comp re s s or S P -4 / AF-101 Filtro de Ar S Fe rme nta do r P -7 / DS -101 Centrífuga de discos S S P -8 / V-102 Tanque de Arrefecimento P -9 / HG-101 Homo ge n iza dor S S S S P -14 / FDR -101 S e c a g e m S S P -13 / DF-101 Dia filtra ç ã o S P -12 / V-105 Ta n qu e S S P -11 / MF-101 Mic rofiltro S P -10 / V-104 Ta n qu e IST/DEQB 12
PROCESSOS EM ENGENHARIA BIOLÓGICA
 PROCESSOS EM ENGENHARIA BIOLÓGICA S-101 S-102 S-103 P-1 / V-101 P-2 / ST-101 S-104 Tanque de mistura Esterilizador S-108 P-6 / AF-102 S-109 S-105 Filtro de gases P-3 / G-101 S-106 S-107 P-4 / AF-101 Compressor
PROCESSOS EM ENGENHARIA BIOLÓGICA S-101 S-102 S-103 P-1 / V-101 P-2 / ST-101 S-104 Tanque de mistura Esterilizador S-108 P-6 / AF-102 S-109 S-105 Filtro de gases P-3 / G-101 S-106 S-107 P-4 / AF-101 Compressor
Engenharia Biológica Integrada. Exame de
 Engenharia Biológica Integrada Exame de 17.06.2003 1) Um dado metabolito é produzido por fermentação aeróbia seguido de extracção de acordo com a seguinte descrição: - Preparação de uma suspensão vegetativa
Engenharia Biológica Integrada Exame de 17.06.2003 1) Um dado metabolito é produzido por fermentação aeróbia seguido de extracção de acordo com a seguinte descrição: - Preparação de uma suspensão vegetativa
Exercício. Questão 48 Engenheiro de Processamento Petrobras 02/2010
 Operações Unitárias Apresentação Grandezas Físicas Questão 48 Engenheiro de Processamento Petrobras 02/2010 O número de cavitação (Ca) é um número adimensional empregado na investigação da cavitação em
Operações Unitárias Apresentação Grandezas Físicas Questão 48 Engenheiro de Processamento Petrobras 02/2010 O número de cavitação (Ca) é um número adimensional empregado na investigação da cavitação em
Curso: Engenharia Biotecnológica (2 Ano) Disciplina: Engenharia de Bioprocessos I
 Docente: Prof. Raúl Barros Curso: Engenharia Biotecnológica (2 Ano) Disciplina: Engenharia de Bioprocessos I Ano Lectivo: 2006/2007 2 Semestre Notas sobre os trabalhos individuais: A realização de trabalhos
Docente: Prof. Raúl Barros Curso: Engenharia Biotecnológica (2 Ano) Disciplina: Engenharia de Bioprocessos I Ano Lectivo: 2006/2007 2 Semestre Notas sobre os trabalhos individuais: A realização de trabalhos
PROCESSOS DE ENGENHARIA QUÍMICA E BIOLÓGICA I
 PROCESSOS DE ENGENHARIA QUÍMICA E BIOLÓGICA I S-105 Purga S-104 S-101 Reagentes P-4 / FSP-101 S-106 S-108 S-10 Produto P-1 / V-101 Reacção S-103 P- / DE-101 Pré-Filtração P-3 / UF-101 Ultrafiltração S-107
PROCESSOS DE ENGENHARIA QUÍMICA E BIOLÓGICA I S-105 Purga S-104 S-101 Reagentes P-4 / FSP-101 S-106 S-108 S-10 Produto P-1 / V-101 Reacção S-103 P- / DE-101 Pré-Filtração P-3 / UF-101 Ultrafiltração S-107
Engenharia das Reacções - Exercícios -
 Engenharia das Reacções - Exercícios - 1 Estudou-se a reacção de recombinação de átomos de iodo na presença de árgon: 2 I (g) + Ar (g) I 2 (g) + Ar (g) As velocidade iniciais de formação de I 2 são apresentadas
Engenharia das Reacções - Exercícios - 1 Estudou-se a reacção de recombinação de átomos de iodo na presença de árgon: 2 I (g) + Ar (g) I 2 (g) + Ar (g) As velocidade iniciais de formação de I 2 são apresentadas
R: a) t r = 2,23 h b) nº bateladas = 7 c) N Rt = 179,4 kmol por dia
 Reator batelada 1- Uma solução aquosa de acetato de etila deve ser saponificada com uma solução diluída de hidróxido de sódio. A concentração inicial de acetato é 5 g/l e a densidade de mistura reacional
Reator batelada 1- Uma solução aquosa de acetato de etila deve ser saponificada com uma solução diluída de hidróxido de sódio. A concentração inicial de acetato é 5 g/l e a densidade de mistura reacional
1. A fermentação é um processo químico complexo do fabrico de vinho no qual a glucose é convertida em etanol e dióxido de carbono:
 EB: QUÍMICA GERAL/ EQB: QUÍMICA GERAL I Capítulo 4. Reacções químicas II Ficha de exercícios 1. A fermentação é um processo químico complexo do fabrico de vinho no qual a glucose é convertida em etanol
EB: QUÍMICA GERAL/ EQB: QUÍMICA GERAL I Capítulo 4. Reacções químicas II Ficha de exercícios 1. A fermentação é um processo químico complexo do fabrico de vinho no qual a glucose é convertida em etanol
PQI 3211 LISTA DE EXERCÍCIOS BALANÇOS MATERIAIS COM REAÇÕES QUÍMICAS
 PQI 3211 LISTA DE EXERCÍCIOS BALANÇOS MATERIAIS COM REAÇÕES QUÍMICAS Para problemas com múltiplas unidades de processamento, realize a análise do número de graus de liberdade para cada unidade, para o
PQI 3211 LISTA DE EXERCÍCIOS BALANÇOS MATERIAIS COM REAÇÕES QUÍMICAS Para problemas com múltiplas unidades de processamento, realize a análise do número de graus de liberdade para cada unidade, para o
Capítulo 5 Processos com Reciclagem, By-Pass e Purga
 Capítulo 5 Processos com Reciclagem, By-Pass e Purga Uma reciclagem envolve o retorno de material (ou energia), presente à saída do processo, para o início do processo, de modo a que seja novamente processado.
Capítulo 5 Processos com Reciclagem, By-Pass e Purga Uma reciclagem envolve o retorno de material (ou energia), presente à saída do processo, para o início do processo, de modo a que seja novamente processado.
PRODUÇÃO DE CLORIDRATO DE DEMECLOCICLINA
 PRODUÇÃO DE CLORIDRATO DE DEMECLOCICLINA OBJECTIVO: Aplicação do programa SuperPro Designer na simulação de um projecto para a produção de 50 ton/ano de cloridrato de demeclociclina, com um valor comercial
PRODUÇÃO DE CLORIDRATO DE DEMECLOCICLINA OBJECTIVO: Aplicação do programa SuperPro Designer na simulação de um projecto para a produção de 50 ton/ano de cloridrato de demeclociclina, com um valor comercial
PROCESSOS DE ENGENHARIA QUÍMICA
 PRCESSS DE ENGENHARIA QUÍMICA Mestrado Integrado em Engenharia Química Capítulo 3 BALANÇS DE ENERGIA ENVLVEND ENTALPIAS DE SLUÇÃ E MISTURA Mª Fátima Costa Farelo Licínio Mendes Ferreira 3 - BALANÇS DE
PRCESSS DE ENGENHARIA QUÍMICA Mestrado Integrado em Engenharia Química Capítulo 3 BALANÇS DE ENERGIA ENVLVEND ENTALPIAS DE SLUÇÃ E MISTURA Mª Fátima Costa Farelo Licínio Mendes Ferreira 3 - BALANÇS DE
INSTITUTO SUPERIOR TÉCNICO
 INSTITUTO SUPERIOR TÉCNICOT Departamento de Engenharia Química e Biológica Separação e Purificação de Produtos Biológicos CENTRIFUGAÇÃO Centrifugação Velocidade de centrifugação vs diâmetro partícula Velocidade
INSTITUTO SUPERIOR TÉCNICOT Departamento de Engenharia Química e Biológica Separação e Purificação de Produtos Biológicos CENTRIFUGAÇÃO Centrifugação Velocidade de centrifugação vs diâmetro partícula Velocidade
ENGENHARIA BIOLÓGICA INTEGRADA II
 ENGENHARIA BIOLÓGICA INTEGRADA II TRANSFERÊNCIA DE OXIGÉNIO EM TANQUES INDUSTRIAIS Helena Pinheiro Torre Sul, Piso 8, Gabinete 8.6.19 Ext. 3125 helena.pinheiro@tecnico.ulisboa.pt & Luis Fonseca ENGENHARIA
ENGENHARIA BIOLÓGICA INTEGRADA II TRANSFERÊNCIA DE OXIGÉNIO EM TANQUES INDUSTRIAIS Helena Pinheiro Torre Sul, Piso 8, Gabinete 8.6.19 Ext. 3125 helena.pinheiro@tecnico.ulisboa.pt & Luis Fonseca ENGENHARIA
Atividade de Autoavaliação Recuperação 2 os anos Rodrigo ago/09
 Química Atividade de Autoavaliação Recuperação 2 os anos Rodrigo ago/09 Re Resolução 1. O carbeto de cálcio CaC 2 (s) (massa molar = 64 g mol 1 ), também conhecido como carbureto, pode ser obtido aquecendo-se
Química Atividade de Autoavaliação Recuperação 2 os anos Rodrigo ago/09 Re Resolução 1. O carbeto de cálcio CaC 2 (s) (massa molar = 64 g mol 1 ), também conhecido como carbureto, pode ser obtido aquecendo-se
Operações Unitárias Parte II
 Operações Unitárias Parte II Apresentação Aula anterior: - Grandezas físicas; - Balanço de massa; - Balanço de energia; - Conversão; - Reciclo; - Rendimento; - Fração convertida; - Umidade relativa; -
Operações Unitárias Parte II Apresentação Aula anterior: - Grandezas físicas; - Balanço de massa; - Balanço de energia; - Conversão; - Reciclo; - Rendimento; - Fração convertida; - Umidade relativa; -
Operações de separação mecânica Filtração
 Operações de separação mecânica Filtração Operações Unitárias I Ano Lectivo 2016/2017 Joana Rodrigues Operações de separação mecânica Sedimentação (Decantação) Partículas no estado sólido ou gotas de líquido
Operações de separação mecânica Filtração Operações Unitárias I Ano Lectivo 2016/2017 Joana Rodrigues Operações de separação mecânica Sedimentação (Decantação) Partículas no estado sólido ou gotas de líquido
Exemplos. Prof. Marcelo Henrique. Exemplo 1 Produção de suco concentrado de laranja
 Exemplos Prof. Marcelo Henrique Exemplo 1 Produção de suco concentrado de laranja O suco natural de laranja contém 13,5% m/m de sólidos e o restante de água. Já o suco concentrado de laranja comercial
Exemplos Prof. Marcelo Henrique Exemplo 1 Produção de suco concentrado de laranja O suco natural de laranja contém 13,5% m/m de sólidos e o restante de água. Já o suco concentrado de laranja comercial
EB: QUÍMICA GERAL/ EQB: QUÍMICA GERAL I
 EB: QUÍMICA GERAL/ EQB: QUÍMICA GERAL I Capítulo 6. Termoquímica Ficha de exercícios 1. Uma amostra de azoto gasoso expande-se do seu volume inicial de 1.6 L para 5.4 L, a temperatura constante. Calcule
EB: QUÍMICA GERAL/ EQB: QUÍMICA GERAL I Capítulo 6. Termoquímica Ficha de exercícios 1. Uma amostra de azoto gasoso expande-se do seu volume inicial de 1.6 L para 5.4 L, a temperatura constante. Calcule
Química B Intensivo V. 1
 1 Química B Intensivo V. 1 Exercícios 01) B 02) B a) Falsa. O leite in natura é uma mistura heterogênea e não apresenta as mesmas propriedades em toda a extensão da amostra. b) Verdadeira. A gelatina é
1 Química B Intensivo V. 1 Exercícios 01) B 02) B a) Falsa. O leite in natura é uma mistura heterogênea e não apresenta as mesmas propriedades em toda a extensão da amostra. b) Verdadeira. A gelatina é
Prova de Acesso de Química para Maiores de 23 Anos 2009/2010
 Nome Completo : B. I. n.º Prova de Acesso de Química para Maiores de 23 Anos 2009/2010 21 Julho 2009, 10:00 13:00 h Respostas às perguntas de escolha múltipla: assinale a resposta certa quando lhe for
Nome Completo : B. I. n.º Prova de Acesso de Química para Maiores de 23 Anos 2009/2010 21 Julho 2009, 10:00 13:00 h Respostas às perguntas de escolha múltipla: assinale a resposta certa quando lhe for
INSTITUTO POLITÉCNICO DE TOMAR ESCOLA SUPERIOR DE TECNOLOGIA. Departamento de Engenharia Química e do Ambiente. QUÍMICA I (1º Ano/1º Semestre)
 INSTITUTO POLITÉCNICO DE TOMAR ESCOLA SUPERIOR DE TECNOLOGIA Departamento de Engenharia Química e do Ambiente QUÍMICA I (1º Ano/1º Semestre) 4ª Série de Exercícios EQUILÍBRIO QUÍMICO Tomar (2003) 1 Equilíbrio
INSTITUTO POLITÉCNICO DE TOMAR ESCOLA SUPERIOR DE TECNOLOGIA Departamento de Engenharia Química e do Ambiente QUÍMICA I (1º Ano/1º Semestre) 4ª Série de Exercícios EQUILÍBRIO QUÍMICO Tomar (2003) 1 Equilíbrio
TRATAMENTO DE EFLUENTES LÍQUIDOS POR MEMBRANAS. Eng. Walter Plácido
 TRATAMENTO DE EFLUENTES LÍQUIDOS POR MEMBRANAS 1 Eng. Walter Plácido Bacteriológicas Considerações Custos Químicas e volumétricas Eficácia (disponibilidade e rendimento) Nível da tecnologia SISTEMAS MEMBRANARES
TRATAMENTO DE EFLUENTES LÍQUIDOS POR MEMBRANAS 1 Eng. Walter Plácido Bacteriológicas Considerações Custos Químicas e volumétricas Eficácia (disponibilidade e rendimento) Nível da tecnologia SISTEMAS MEMBRANARES
Teste de Laboratórios de Química I e soluções
 É OBRIGATÓRIO IDENTIFICAR TODAS AS FOLHAS DE EXAME AS FOLHAS NÃO IDENTIFICADAS SÃO ANULADAS Teste de Laboratórios de Química I e soluções 4 de Janeiro de 2013 Duração: 1h 30m Mestrado Integrado em Engenharia
É OBRIGATÓRIO IDENTIFICAR TODAS AS FOLHAS DE EXAME AS FOLHAS NÃO IDENTIFICADAS SÃO ANULADAS Teste de Laboratórios de Química I e soluções 4 de Janeiro de 2013 Duração: 1h 30m Mestrado Integrado em Engenharia
Química Analítica I Tratamento dos dados analíticos Soluções analíticas
 Química Analítica I Tratamento dos dados analíticos Soluções analíticas Profª Simone Noremberg Kunz 2 Mol Medidas em química analítica É a quantidade de uma espécie química que contém 6,02x10 23 partículas
Química Analítica I Tratamento dos dados analíticos Soluções analíticas Profª Simone Noremberg Kunz 2 Mol Medidas em química analítica É a quantidade de uma espécie química que contém 6,02x10 23 partículas
s e õ ç lu o S a ic ím u Q G A. P 1
 1. 2. Uma solução comercial de soro fisiológico tem concentração de NaCl de 0,9% (massa/volume). Soluções com essa concentração podem ser consideradas como tendo densidade unitária. a) expresse essa concentração
1. 2. Uma solução comercial de soro fisiológico tem concentração de NaCl de 0,9% (massa/volume). Soluções com essa concentração podem ser consideradas como tendo densidade unitária. a) expresse essa concentração
6 MATERIAIS E EQUIPAMENTOS
 79 6 MATERIAIS E EQUIPAMENTOS 6.1. Amostra O spent potliner, estudado neste trabalho, foi fornecido pela Valesul Alumínio S.A., empresa que produz e comercializa alumínio primário e ligas para a indústria
79 6 MATERIAIS E EQUIPAMENTOS 6.1. Amostra O spent potliner, estudado neste trabalho, foi fornecido pela Valesul Alumínio S.A., empresa que produz e comercializa alumínio primário e ligas para a indústria
Lista de Exercícios Solução em Sala
 Lista de Exercícios Solução em Sala 1) Um conjunto pistão-cilindro área de seção transversal igual a 0,01 m². A massa do pistão é 101 kg e ele está apoiado nos batentes mostrado na figura. Se a pressão
Lista de Exercícios Solução em Sala 1) Um conjunto pistão-cilindro área de seção transversal igual a 0,01 m². A massa do pistão é 101 kg e ele está apoiado nos batentes mostrado na figura. Se a pressão
DISCIPLINA DE TERMODINÂMICA APLICADA À BIOTECNOLOGIA.
 Balanços em sistemas com reação química são um pouco mais complicados. Para resolver problemas com reação, relações estequiométricas devem ser usadas em junção com as equações de balanço de massa. Estes
Balanços em sistemas com reação química são um pouco mais complicados. Para resolver problemas com reação, relações estequiométricas devem ser usadas em junção com as equações de balanço de massa. Estes
ENGENHARIA BIOLÓGICA INTEGRADA II
 ENGENHARIA BIOLÓGICA INTEGRADA II AGITAÇÃO EM TANQUES INDUSTRIAIS Helena Pinheiro Torre Sul, Piso 8, Gabinete 8.6.19 Ext. 3125 helena.pinheiro@tecnico.ulisboa.pt & Luis Fonseca ENGENHARIA BIOLÓGICA INTEGRADA
ENGENHARIA BIOLÓGICA INTEGRADA II AGITAÇÃO EM TANQUES INDUSTRIAIS Helena Pinheiro Torre Sul, Piso 8, Gabinete 8.6.19 Ext. 3125 helena.pinheiro@tecnico.ulisboa.pt & Luis Fonseca ENGENHARIA BIOLÓGICA INTEGRADA
Aula 6: Estequiometria. Eduarda Boing Pinheiro
 Aula 6: Estequiometria Eduarda Boing Pinheiro Na natureza nada se cria, nada se perde, tudo se transforma. Antoine Lavoisier 2 Balanceamento químico: A mesma quantidade de cada elemento está presente no
Aula 6: Estequiometria Eduarda Boing Pinheiro Na natureza nada se cria, nada se perde, tudo se transforma. Antoine Lavoisier 2 Balanceamento químico: A mesma quantidade de cada elemento está presente no
MESTRADO INTEGRADO EM ENGENHARIA QUÍMICA ANO LECTIVO 2014/2015 SUPERVISOR: PROF. JOÃO BASTOS MONITORA: DIANA PEREIRA
 MESTRADO INTEGRADO EM ENGENHARIA QUÍMICA ANO LECTIVO 2014/2015 SUPERVISOR: PROF. JOÃO BASTOS MONITORA: DIANA PEREIRA Índice Propriedades físicas e químicas da Soda Cáustica Aspetos Económicos Aplicações
MESTRADO INTEGRADO EM ENGENHARIA QUÍMICA ANO LECTIVO 2014/2015 SUPERVISOR: PROF. JOÃO BASTOS MONITORA: DIANA PEREIRA Índice Propriedades físicas e químicas da Soda Cáustica Aspetos Económicos Aplicações
Capítulo 6 Processos Envolvendo Vapores
 Capítulo 6 Processos Envolvendo Vapores Pressão de vapor Define-se vapor como um componente no estado gasoso que se encontra a pressão e temperatura inferiores às do ponto crítico. Assim, um vapor pode
Capítulo 6 Processos Envolvendo Vapores Pressão de vapor Define-se vapor como um componente no estado gasoso que se encontra a pressão e temperatura inferiores às do ponto crítico. Assim, um vapor pode
EVAPORAÇÃO. Profa. Marianne Ayumi Shirai EVAPORAÇÃO
 Universidade Tecnológica Federal do Paraná Campus Londrina Operações Unitárias na Indústria de Alimentos EVAPORAÇÃO Profa. Marianne Ayumi Shirai EVAPORAÇÃO É a remoção parcial da água de mistura de líquidos,
Universidade Tecnológica Federal do Paraná Campus Londrina Operações Unitárias na Indústria de Alimentos EVAPORAÇÃO Profa. Marianne Ayumi Shirai EVAPORAÇÃO É a remoção parcial da água de mistura de líquidos,
2. A pressão atmosférica no cume do monte McKinley é 606 mmhg num determinado dia. Qual é o valor dessa pressão em atm e kpa?
 EB: QUÍMICA GERAL/ EQB: QUÍMICA GERAL I Capítulo 5. Gases Ficha de Exercícios 1. Converta 562 mmhg em atm. 2. A pressão atmosférica no cume do monte McKinley é 606 mmhg num determinado dia. Qual é o valor
EB: QUÍMICA GERAL/ EQB: QUÍMICA GERAL I Capítulo 5. Gases Ficha de Exercícios 1. Converta 562 mmhg em atm. 2. A pressão atmosférica no cume do monte McKinley é 606 mmhg num determinado dia. Qual é o valor
PARTE III Balanço de massa
 PARTE III Balanço de massa 1. Procedimentos para cálculo de Balanço de Massa i. Escolha como base de cálculo uma quantidade ou vazão de uma das correntes do processo. ii. Desenhe o fluxograma e rotule
PARTE III Balanço de massa 1. Procedimentos para cálculo de Balanço de Massa i. Escolha como base de cálculo uma quantidade ou vazão de uma das correntes do processo. ii. Desenhe o fluxograma e rotule
OPERAÇÕES UNITÁRIAS II
 COLÉGIO META OPERAÇÕES UNITÁRIAS II Prof. ABEL SCUPELITI ARTILHEIRO SÃO PAULO 2012 1 OPERAÇÕES UNITÁRIAS II BALANÇO MATERIAL O Balanço Material é utilizado para projetos e análises de equipamentos de novas
COLÉGIO META OPERAÇÕES UNITÁRIAS II Prof. ABEL SCUPELITI ARTILHEIRO SÃO PAULO 2012 1 OPERAÇÕES UNITÁRIAS II BALANÇO MATERIAL O Balanço Material é utilizado para projetos e análises de equipamentos de novas
ÁREA DE ESTUDO: CÓDIGO 16 TERMODINÂMICA APLICADA, MECÂNICA DOS FLUIDOS E OPERAÇÕES UNITÁRIAS
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO CEARÁ DIRETORIA DE GESTÃO DE PESSOAS COMISSÃO COORDENADORA DE CONCURSOS CONCURSO PÚBLICO PROFESSOR EFETIVO EDITAL Nº 10/DGP-IFCE/2010 ÁREA DE ESTUDO:
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO CEARÁ DIRETORIA DE GESTÃO DE PESSOAS COMISSÃO COORDENADORA DE CONCURSOS CONCURSO PÚBLICO PROFESSOR EFETIVO EDITAL Nº 10/DGP-IFCE/2010 ÁREA DE ESTUDO:
PAGQuímica 2011/1 Exercícios de Equilíbrio Químico
 PAGQuímica 2011/1 Exercícios de Equilíbrio Químico 1. Para o equilíbrio gasoso entre NO e O 2 formando NO 2 (2 NO (g) + O 2 (g) 2 NO 2 (g)), a constante de equilíbrio é Kc = 6,45 x 10 5. a) em que concentração
PAGQuímica 2011/1 Exercícios de Equilíbrio Químico 1. Para o equilíbrio gasoso entre NO e O 2 formando NO 2 (2 NO (g) + O 2 (g) 2 NO 2 (g)), a constante de equilíbrio é Kc = 6,45 x 10 5. a) em que concentração
Componente de Química
 Componente de Química Unidade 1 Química e Indústria: equilíbrios e desequilíbrios A Química, o amoníaco e muito mais A Revolução Industrial Desenvolvimento sustentável versus desenvolvimento insustentável
Componente de Química Unidade 1 Química e Indústria: equilíbrios e desequilíbrios A Química, o amoníaco e muito mais A Revolução Industrial Desenvolvimento sustentável versus desenvolvimento insustentável
ATENÇÃO: assinale ou apresente cuidadosamente as respostas e apresente TODOS os cálculos efectuados.
 Prova de Acesso de Química Maiores de 23 Anos Candidatura 2016-2017 14 de Junho de 2017 10h00 12h30 Nome CCnº ATENÇÃO: assinale ou apresente cuidadosamente as respostas e apresente TODOS os cálculos efectuados.
Prova de Acesso de Química Maiores de 23 Anos Candidatura 2016-2017 14 de Junho de 2017 10h00 12h30 Nome CCnº ATENÇÃO: assinale ou apresente cuidadosamente as respostas e apresente TODOS os cálculos efectuados.
CONCEITOS BÁSICOS EM ENGENHARIA QUÍMICA
 CONCEITOS BÁSICOS EM ENGENHARIA QUÍMICA O QUE SÃO PROCESSOS QUÍMICOS? Definições básicas Processos Químicos Modos Operacionais Vazões Escoamentos CONCEITOS BÁSICOS EM ENGENHARIA QUÍMICA Operação Descontínua
CONCEITOS BÁSICOS EM ENGENHARIA QUÍMICA O QUE SÃO PROCESSOS QUÍMICOS? Definições básicas Processos Químicos Modos Operacionais Vazões Escoamentos CONCEITOS BÁSICOS EM ENGENHARIA QUÍMICA Operação Descontínua
COLÉGIO DA POLÍCIA MILITAR
 COLÉGIO DA POLÍCIA MILITAR ASSESSORIA TÉCNICA Processo Avaliativo Recuperação - 3º Bimestre/2015 Disciplina: QUÍMICA 3ª série EM A/B Nome do aluno Nº Turma A Recuperação deve ser entregue no dia 08/09/2015.
COLÉGIO DA POLÍCIA MILITAR ASSESSORIA TÉCNICA Processo Avaliativo Recuperação - 3º Bimestre/2015 Disciplina: QUÍMICA 3ª série EM A/B Nome do aluno Nº Turma A Recuperação deve ser entregue no dia 08/09/2015.
FICHA DE TRABALHO DE FÍSICA E QUÍMICA A FEVEREIRO 2012
 FICHA DE TRABALHO DE FÍSICA E QUÍMICA A FEVEREIRO 2012 APSA Nº14 11º Ano de Escolaridade 1. Qual a massa de hidróxido de sódio necessária para reagir completamente com 49,05 g de ácido sulfúrico de acordo
FICHA DE TRABALHO DE FÍSICA E QUÍMICA A FEVEREIRO 2012 APSA Nº14 11º Ano de Escolaridade 1. Qual a massa de hidróxido de sódio necessária para reagir completamente com 49,05 g de ácido sulfúrico de acordo
PROCESSOS DE ENGENHARIA QUÍMICA E BIOLÓGICA I
 PROCESSOS DE ENGENHARIA QUÍMICA E BIOLÓGICA I S-105 Purga S-104 S-101 Reagentes P-4 / FSP-101 S-106 S-108 S-102 Produto P-1 / V-101 Reacção S-103 P-2 / DE-101 Pré-Filtração P-3 / UF-101 Ultrafiltração
PROCESSOS DE ENGENHARIA QUÍMICA E BIOLÓGICA I S-105 Purga S-104 S-101 Reagentes P-4 / FSP-101 S-106 S-108 S-102 Produto P-1 / V-101 Reacção S-103 P-2 / DE-101 Pré-Filtração P-3 / UF-101 Ultrafiltração
PAG Química Equilíbrio Químico 1. Para o equilíbrio gasoso entre NO e O 2 formando NO 2 (2 NO (g) + O 2 (g) 2 NO 2 (g)), a constante de equilíbrio é
 1. Para o equilíbrio gasoso entre NO e O 2 formando NO 2 (2 NO (g) + O 2 (g) 2 NO 2 (g)), a constante de equilíbrio é Kc = 6,45 x 10 5. a) em que concentração de O 2 as concentrações de NO 2 e de NO são
1. Para o equilíbrio gasoso entre NO e O 2 formando NO 2 (2 NO (g) + O 2 (g) 2 NO 2 (g)), a constante de equilíbrio é Kc = 6,45 x 10 5. a) em que concentração de O 2 as concentrações de NO 2 e de NO são
PROCESSOS EM ENGENHARIA BIOLÓGICA
 MESTRADO INTEGRADO EM ENGENHARIA BIOLÓGICA 3º ANO / 1º SEMESTRE 2016/2017 S-101 S-102 S-103 P-1 / V-101 P-2 / ST-101 S-104 Tanque de mistura Esterilizador S-108 P-6 / AF-102 S-109 S-105 Filtro de gases
MESTRADO INTEGRADO EM ENGENHARIA BIOLÓGICA 3º ANO / 1º SEMESTRE 2016/2017 S-101 S-102 S-103 P-1 / V-101 P-2 / ST-101 S-104 Tanque de mistura Esterilizador S-108 P-6 / AF-102 S-109 S-105 Filtro de gases
1.1. A partir de 10 mol de ácido nítrico qual é a massa de nitrato de amónio que se obtém?
 Escola Secundária de Lagoa Física e Química A 11º Ano Turma A Paula Melo Silva Ficha de Trabalho 5 Cálculos estequiométricos 1. O ácido nítrico é uma das mais importantes substâncias inorgânicas industriais.
Escola Secundária de Lagoa Física e Química A 11º Ano Turma A Paula Melo Silva Ficha de Trabalho 5 Cálculos estequiométricos 1. O ácido nítrico é uma das mais importantes substâncias inorgânicas industriais.
TRANSPORTE DE MASSA. Alda Simões CEQ / MEF / 2015
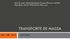 Livro de apoio: Christie Geankoplis, Transport Processes and Unit Operations, 3rd ed, 1993, Prentice Hall, cap 6 TRANSPORTE DE MASSA CEQ / MEF / 2015 Alda Simões Transporte molecular de massa Lei de Fick
Livro de apoio: Christie Geankoplis, Transport Processes and Unit Operations, 3rd ed, 1993, Prentice Hall, cap 6 TRANSPORTE DE MASSA CEQ / MEF / 2015 Alda Simões Transporte molecular de massa Lei de Fick
MÁQUINAS TÉRMICAS
 UNIVERSIDADE DE AVEIRO DEPARTAMENTO DE ENGENHARIA MECÂNICA EXERCÍCIOS DAS AULAS PRÁTICAS MÁQUINAS TÉRMICAS 2010-2011 DOCENTES RESPONSÁVEIS DEM Fernando Neto DEM João Oliveira DISCIPLINA Código 40544 Ano
UNIVERSIDADE DE AVEIRO DEPARTAMENTO DE ENGENHARIA MECÂNICA EXERCÍCIOS DAS AULAS PRÁTICAS MÁQUINAS TÉRMICAS 2010-2011 DOCENTES RESPONSÁVEIS DEM Fernando Neto DEM João Oliveira DISCIPLINA Código 40544 Ano
PQI 3103 LISTA DE EXERCÍCIOS II 2018 BALANÇOS MATERIAIS SISTEMAS EM REGIME PERMANENTE SEM REAÇÕES QUÍMICAS
 Pág. 1/6 PQI 3103 LISTA DE EXERCÍCIOS II 2018 BALANÇOS MATERIAIS SISTEMAS EM REGIME PERMANENTE SEM REAÇÕES QUÍMICAS Exercícios para apoio ao estudo não é necessário entregar a solução da lista Observação:
Pág. 1/6 PQI 3103 LISTA DE EXERCÍCIOS II 2018 BALANÇOS MATERIAIS SISTEMAS EM REGIME PERMANENTE SEM REAÇÕES QUÍMICAS Exercícios para apoio ao estudo não é necessário entregar a solução da lista Observação:
Faculdade de Engenharia Química (FEQUI) Operações Unitárias 2 4ª Lista de Exercícios (parte B Extração Líquido-Líquido)
 Faculdade de Engenharia Química (FEQUI) Operações Unitárias 2 4ª Lista de Exercícios (parte B Extração Líquido-Líquido) Profº Carlos Henrique Ataíde (novembro de 2013) 1ª) Concurso Petrobras Químico (a)
Faculdade de Engenharia Química (FEQUI) Operações Unitárias 2 4ª Lista de Exercícios (parte B Extração Líquido-Líquido) Profº Carlos Henrique Ataíde (novembro de 2013) 1ª) Concurso Petrobras Químico (a)
Processo Oxo Prof. Marcos Villela Barcza
 Processo Oxo Prof. Marcos Villela Barcza Processo Oxo (Hidroformilação) 1- Introdução: Olefinas reagem com gás de síntese (CO e H2) em presença de catalisadores para formar aldeídos contendo um carbono
Processo Oxo Prof. Marcos Villela Barcza Processo Oxo (Hidroformilação) 1- Introdução: Olefinas reagem com gás de síntese (CO e H2) em presença de catalisadores para formar aldeídos contendo um carbono
Exercícios e exemplos de sala de aula Parte 1
 PME2398 Termodinâmica e suas Aplicações 1 o semestre / 2013 Prof. Bruno Carmo Exercícios e exemplos de sala de aula Parte 1 Propriedade das substâncias puras: 1- Um tanque rígido com volume de 1m 3 contém
PME2398 Termodinâmica e suas Aplicações 1 o semestre / 2013 Prof. Bruno Carmo Exercícios e exemplos de sala de aula Parte 1 Propriedade das substâncias puras: 1- Um tanque rígido com volume de 1m 3 contém
PROCESSOS QUÍMICOS INDUSTRIAIS II. (Parte II)
 PROCESSOS QUÍMICOS INDUSTRIAIS II REAÇÕES QUÍMICAS E BALANÇO MATERIAL (Parte II) PROCESSOS UNITÁRIOS REAÇÕES QUÍMICAS Transformações Químicas Aspectos Qualitativos - Tipos de reação - Espécies em solução
PROCESSOS QUÍMICOS INDUSTRIAIS II REAÇÕES QUÍMICAS E BALANÇO MATERIAL (Parte II) PROCESSOS UNITÁRIOS REAÇÕES QUÍMICAS Transformações Químicas Aspectos Qualitativos - Tipos de reação - Espécies em solução
QUÍMICA CÁLCULOS ESTEQUIOMÉTRICOS
 QUÍMICA CÁLCULOS ESTEQUIOMÉTRICOS CÁLCULOS ESTEQUIOMÉTRICOS Os cálculos estequiométricos correspondem aos cálculos de massa, de quantidade de matéria e em alguns casos, de volumes das substâncias envolvidas
QUÍMICA CÁLCULOS ESTEQUIOMÉTRICOS CÁLCULOS ESTEQUIOMÉTRICOS Os cálculos estequiométricos correspondem aos cálculos de massa, de quantidade de matéria e em alguns casos, de volumes das substâncias envolvidas
P1 - PROVA DE QUÍMICA GERAL 10/09/05
 P1 - PROVA DE QUÍMICA GERAL 10/09/05 Nome: Nº de Matrícula: Gabarito Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados R 0,0821 atm L mol -1 K -1 K C + 273,15
P1 - PROVA DE QUÍMICA GERAL 10/09/05 Nome: Nº de Matrícula: Gabarito Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados R 0,0821 atm L mol -1 K -1 K C + 273,15
PHA 3418 Tecnologia de Separação por Membranas para Tratamento de Água e Efluentes
 PHA 3418 Tecnologia de Separação por Membranas para Tratamento de Água e Efluentes AULA 2 CLASSIFICAÇÃO DOS PROCESSOS DE SEPARAÇÃO POR MEMBRANAS Prof.: José Carlos Mierzwa Processos de Separação por Membranas
PHA 3418 Tecnologia de Separação por Membranas para Tratamento de Água e Efluentes AULA 2 CLASSIFICAÇÃO DOS PROCESSOS DE SEPARAÇÃO POR MEMBRANAS Prof.: José Carlos Mierzwa Processos de Separação por Membranas
Exemplo 2: A baixas temperaturas a lei de velocidade da reação A + B C + D é r A =
 Determine a energia de ativação desta reação. Exemplo 1: Para a reação SO 2 + 1 2 O 2 SO 3, se a velocidade de formação de SO 3 é de 2 mol m -3 s -1, então as velocidades de desaparecimento de SO 2, de
Determine a energia de ativação desta reação. Exemplo 1: Para a reação SO 2 + 1 2 O 2 SO 3, se a velocidade de formação de SO 3 é de 2 mol m -3 s -1, então as velocidades de desaparecimento de SO 2, de
Curso: Engenharia Biotecnológica (3 Ano) Disciplina: Engenharia de Bioprocessos II
 Docente: Prof. Raúl Barros Curso: Engenharia Biotecnológica ( Ano) Disciplina: Engenharia de Bioprocessos II Ano Lectivo: 00/007 Semestre Notas sobre os trabalhos individuais: A realização de trabalhos
Docente: Prof. Raúl Barros Curso: Engenharia Biotecnológica ( Ano) Disciplina: Engenharia de Bioprocessos II Ano Lectivo: 00/007 Semestre Notas sobre os trabalhos individuais: A realização de trabalhos
Química Analítica IV QUI semestre 2012 Profa. Maria Auxiliadora Costa Matos ANÁLISE GRAVIMÉTRICA
 Química Analítica IV QUI070 1 semestre 2012 Profa. Maria Auxiliadora Costa Matos ANÁLISE GRAVIMÉTRICA 1 GRAVIMETRIA OU ANÁLISE GRAVIMETRICA Processo de isolar ou de pesar um composto definido de um elemento
Química Analítica IV QUI070 1 semestre 2012 Profa. Maria Auxiliadora Costa Matos ANÁLISE GRAVIMÉTRICA 1 GRAVIMETRIA OU ANÁLISE GRAVIMETRICA Processo de isolar ou de pesar um composto definido de um elemento
Instalações Térmicas. 3º ano 6º semestre Aula 20
 Instalações Térmicas º ano 6º semestre Aula 0 Aula 0: Balanços Térmicos e Consumo de combustível - Prática Tópicos Características de Funcionamento do Forno Condições Térmicas Balanço de Calor Consumo
Instalações Térmicas º ano 6º semestre Aula 0 Aula 0: Balanços Térmicos e Consumo de combustível - Prática Tópicos Características de Funcionamento do Forno Condições Térmicas Balanço de Calor Consumo
FORMULÁRIO DE DIVULGAÇÃO DO CONTEÚDO DA PROVA FINAL E RECUPERAÇÃO FINAL
 FORMULÁRIO DE DIVULGAÇÃO DO CONTEÚDO DA PROVA FINAL E RECUPERAÇÃO FINAL A) SÉRIE/ANO: 2º Ano Médio B) DISCIPLINA: Química - Enio C) CONTEÚDO A SER EXIGIDO/ORIENTAÇÃO PARA O ESTUDO: SOLUÇÕES: Coeficiente
FORMULÁRIO DE DIVULGAÇÃO DO CONTEÚDO DA PROVA FINAL E RECUPERAÇÃO FINAL A) SÉRIE/ANO: 2º Ano Médio B) DISCIPLINA: Química - Enio C) CONTEÚDO A SER EXIGIDO/ORIENTAÇÃO PARA O ESTUDO: SOLUÇÕES: Coeficiente
Mestrado em Engenharia Química 1º ano Simulação de Processos Químicos. Caso de Estudo # 1 - Reactor batch para reacções múltiplas.
 Caso de Estudo # 1 - Reactor batch para reacções múltiplas. Considere um reactor batch utilizado no esquema de reacções múltiplas seguinte: A k 1 B k 2 k 3 C Considere que todas as reacções são elementares
Caso de Estudo # 1 - Reactor batch para reacções múltiplas. Considere um reactor batch utilizado no esquema de reacções múltiplas seguinte: A k 1 B k 2 k 3 C Considere que todas as reacções são elementares
MINERALIZAÇÃO E DESMINERALIZAÇÃO DA ÁGUA
 MINERALIZAÇÃO E DESMINERALIZAÇÃO DA ÁGUA Dissolução; Solubilidade; Produto de solubilidade; Precipitação; Mineralização e desmineralização das águas. Água do Mar Ó mar salgado, Quanto do teu sal são lágrimas
MINERALIZAÇÃO E DESMINERALIZAÇÃO DA ÁGUA Dissolução; Solubilidade; Produto de solubilidade; Precipitação; Mineralização e desmineralização das águas. Água do Mar Ó mar salgado, Quanto do teu sal são lágrimas
4001 Transesterificação do óleo de mamona em ricinoleato de metila
 4001 Transesterificação do óleo de mamona em ricinoleato de metila Classificação Tipos de reações e classes de substâncias. Reação do grupo carbonila de derivados do ácido carboxílico, trans-esterificação,
4001 Transesterificação do óleo de mamona em ricinoleato de metila Classificação Tipos de reações e classes de substâncias. Reação do grupo carbonila de derivados do ácido carboxílico, trans-esterificação,
PROCESSOS QUÍMICOS INDUSTRIAIS I APRESENTAÇÃO DA DISCIPLINA
 PROCESSOS QUÍMICOS INDUSTRIAIS I APRESENTAÇÃO DA DISCIPLINA UNIDADES DIDÁTICAS 1. Introdução ao estudo dos Processos Químicos Industriais. Relacionamento com a Indústria Química. 2. Derivados inorgânicos
PROCESSOS QUÍMICOS INDUSTRIAIS I APRESENTAÇÃO DA DISCIPLINA UNIDADES DIDÁTICAS 1. Introdução ao estudo dos Processos Químicos Industriais. Relacionamento com a Indústria Química. 2. Derivados inorgânicos
GASES INDUSTRIAIS. QUÍMICA APLICADA QAP 0001 Prof.: Sivaldo Leite Correia, Dr. Doutorando: Samoel Schwaab
 GASES INDUSTRIAIS QUÍMICA APLICADA QAP 0001 Prof.: Sivaldo Leite Correia, Dr. Doutorando: Samoel Schwaab Introdução Gases Industriais; Grupo de gases comercialmente fabricados e vendidos; Contribuições
GASES INDUSTRIAIS QUÍMICA APLICADA QAP 0001 Prof.: Sivaldo Leite Correia, Dr. Doutorando: Samoel Schwaab Introdução Gases Industriais; Grupo de gases comercialmente fabricados e vendidos; Contribuições
ESCOLA SALESIANA DE MANIQUE FICHA DE AVALIAÇÃO DE QUÍMICA ANO LECTIVO 2010/2011
 ESCOLA SALESIANA DE MANIQUE FICHA DE AVALIAÇÃO DE QUÍMICA ANO LECTIVO 2010/2011 Nome: 12.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. A maioria das reacções químicas ocorre com
ESCOLA SALESIANA DE MANIQUE FICHA DE AVALIAÇÃO DE QUÍMICA ANO LECTIVO 2010/2011 Nome: 12.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. A maioria das reacções químicas ocorre com
Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente.
 SOLUÇÕES Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente. Fase: numa mistura, é cada uma das porções que apresenta aspecto homogéneo ou uniforme. CLASSIFICAÇÃO
SOLUÇÕES Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente. Fase: numa mistura, é cada uma das porções que apresenta aspecto homogéneo ou uniforme. CLASSIFICAÇÃO
564 E V A P O R A Ç Ã O
 564 E V A P O R A Ç Ã O FIGURA 10-5: Esquema de cálculo de um evaporador de multiefeitos (caso de um evaporador triplo, em que i 1, 2, 3). V i e L i são, respectivamente, os caudais de vapor provenientes
564 E V A P O R A Ç Ã O FIGURA 10-5: Esquema de cálculo de um evaporador de multiefeitos (caso de um evaporador triplo, em que i 1, 2, 3). V i e L i são, respectivamente, os caudais de vapor provenientes
CIENCIAS DE ENGENHARIA QUÍMICA MEF
 CIENCIAS DE ENGENHARIA QUÍMICA MEF DINÂMICA DE FLUIDOS EXERCÍCIOS 2015 1. Converta pé-poundal para erg e erg/s para watt, recorrendo apenas às conversões 1 ft 0,3048 m e 1 lbm 0,454 kg. 2. Considerando
CIENCIAS DE ENGENHARIA QUÍMICA MEF DINÂMICA DE FLUIDOS EXERCÍCIOS 2015 1. Converta pé-poundal para erg e erg/s para watt, recorrendo apenas às conversões 1 ft 0,3048 m e 1 lbm 0,454 kg. 2. Considerando
2º Trimestre Sala de Estudo Data: 22/05/18 Ensino Médio 3º ano classe: A_B Profª Danusa Nome: nº
 2º Trimestre Sala de Estudo Data: 22/05/18 Ensino Médio 3º ano classe: A_B Profª Danusa Nome: nº Conteúdo: Cálculo Estequiométrico Avançado Questão 01 - (UFRR/2017) O produto vendido comercialmente como
2º Trimestre Sala de Estudo Data: 22/05/18 Ensino Médio 3º ano classe: A_B Profª Danusa Nome: nº Conteúdo: Cálculo Estequiométrico Avançado Questão 01 - (UFRR/2017) O produto vendido comercialmente como
LISTA DE EXERCÍCIOS DE RECUPERAÇÃO 1º TRIMESTRE QUÍMICA
 LISTA DE EXERCÍCIOS DE RECUPERAÇÃO 1º TRIMESTRE QUÍMICA ALUNO(a): Nº: SÉRIE: 2ª TURMA: UNIDADE: VV JC JP PC DATA: / /2017 Obs.: Esta lista deve ser entregue resolvida no dia da prova de recuperação. Valor:
LISTA DE EXERCÍCIOS DE RECUPERAÇÃO 1º TRIMESTRE QUÍMICA ALUNO(a): Nº: SÉRIE: 2ª TURMA: UNIDADE: VV JC JP PC DATA: / /2017 Obs.: Esta lista deve ser entregue resolvida no dia da prova de recuperação. Valor:
Solubilidade, estequiometria, misturas e gases
 Solubilidade, estequiometria, misturas e gases 1) O cientista italiano Amedeo Avogadro, na tentativa de compreender relações de volumes nas reações dos gases, propôs uma hipótese, estabelecendo que (CNTP
Solubilidade, estequiometria, misturas e gases 1) O cientista italiano Amedeo Avogadro, na tentativa de compreender relações de volumes nas reações dos gases, propôs uma hipótese, estabelecendo que (CNTP
Um processo de produção de um metabolito secundário consiste das seguintes fases:
 1 Diagramas do Processo Um processo de produção de um metabolito secundário consiste das seguintes fases: 1. Fermentação aeróbia para produção do produto e biomassa. 2. Extracção directa do produto do
1 Diagramas do Processo Um processo de produção de um metabolito secundário consiste das seguintes fases: 1. Fermentação aeróbia para produção do produto e biomassa. 2. Extracção directa do produto do
ENGENHARIA BIOLÓGICA INTEGRADA II
 ENGENHARIA BIOLÓGICA INTEGRADA II EXEMPLOS ADICIONAIS Helena Pinheiro Torre Sul, Piso 8, Gabinete 8.6.19 Ext. 3125 helena.pinheiro@tecnico.ulisboa.pt EXEMPLO 1 Um reactor air-lift de circulação interna
ENGENHARIA BIOLÓGICA INTEGRADA II EXEMPLOS ADICIONAIS Helena Pinheiro Torre Sul, Piso 8, Gabinete 8.6.19 Ext. 3125 helena.pinheiro@tecnico.ulisboa.pt EXEMPLO 1 Um reactor air-lift de circulação interna
CAPÍTULO II BALANÇOS DE MASSA E DE ENERGIA EM SISTEMAS GÁS/VAPOR 2.1 CARACTERIZAÇÃO DE SISTEMAS GÁS/VAPOR
 Neste capítulo iremos abordar balanços de massa e de energia para os sistemas constituídos por misturas gás/vapor. Este estudos irão focar fundamentalmente o sistema gás/vapor de maior interesse industrial
Neste capítulo iremos abordar balanços de massa e de energia para os sistemas constituídos por misturas gás/vapor. Este estudos irão focar fundamentalmente o sistema gás/vapor de maior interesse industrial
Energética Industrial
 Universidade do Minho Departamento de Engenharia Mecânica Energética Industrial Problemas propostos José Carlos Fernandes Teixeira 1) 1.5 kg de gelo à temperatura de 260 K, funde-se, à pressão de 1 bar,
Universidade do Minho Departamento de Engenharia Mecânica Energética Industrial Problemas propostos José Carlos Fernandes Teixeira 1) 1.5 kg de gelo à temperatura de 260 K, funde-se, à pressão de 1 bar,
01/08/2010. química).
 UNIDADES DIDÁTICAS PROCESSOS QUÍMICOS I APRESENTAÇÃO DA DISCIPLINA 1. Introdução ao estudo dos Processos Químicos Industriais. Relacionamento com a Indústria Química. 2. Derivados inorgânicos do nitrogênio.
UNIDADES DIDÁTICAS PROCESSOS QUÍMICOS I APRESENTAÇÃO DA DISCIPLINA 1. Introdução ao estudo dos Processos Químicos Industriais. Relacionamento com a Indústria Química. 2. Derivados inorgânicos do nitrogênio.
UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO
 UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO 08/11/2010 PROVA ESCRITA Assinatura do candidato: Área de concentração:
UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO 08/11/2010 PROVA ESCRITA Assinatura do candidato: Área de concentração:
III.1 Classificação das Misturas: Soluções e Dispersões.
 III SOLUÇÕES III.1 Classificação das Misturas: Soluções e Dispersões. Frequentemente as substâncias químicas (elementos e compostos) encontram-se misturadas umas às outras. O sangue, a água do mar, o solo
III SOLUÇÕES III.1 Classificação das Misturas: Soluções e Dispersões. Frequentemente as substâncias químicas (elementos e compostos) encontram-se misturadas umas às outras. O sangue, a água do mar, o solo
Prof. Engº Pery C. G. de Castro. Revisado em outubro de 2009 PARTE - V CONSTRUÇÃO
 Prof. Engº Pery C. G. de Castro Revisado em outubro de 2009 PARTE - V CONSTRUÇÃO 1 CONSTRUÇÃO O principal problema da reciclagem de misturas asfálticas a quente é a secagem e aquecimento do RAP. Se for
Prof. Engº Pery C. G. de Castro Revisado em outubro de 2009 PARTE - V CONSTRUÇÃO 1 CONSTRUÇÃO O principal problema da reciclagem de misturas asfálticas a quente é a secagem e aquecimento do RAP. Se for
Capítulo by Pearson Education
 QUÍMICA A Ciência Central 9ª Edição Aspectos adicionais dos equilíbrios aquosos David P. White O efeito do íon comum A solubilidade de um sal parcialmente solúvel diminui quando um íon comum é adicionado.
QUÍMICA A Ciência Central 9ª Edição Aspectos adicionais dos equilíbrios aquosos David P. White O efeito do íon comum A solubilidade de um sal parcialmente solúvel diminui quando um íon comum é adicionado.
2017 Obtenção da amida do ácido cinâmico através da reação do cloreto do ácido cinâmico com amônia
 217 Obtenção da amida do ácido cinâmico através da reação do cloreto do ácido cinâmico com amônia O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Classificação Tipos de reação e classes de
217 Obtenção da amida do ácido cinâmico através da reação do cloreto do ácido cinâmico com amônia O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Classificação Tipos de reação e classes de
ESTEQUIOMETRIA. Estudo das reações. Descrevendo uma reação química. Indicadores de uma reação química:
 ESTEQUIOMETRIA Estudo das reações Indicadores de uma reação química: Produção de um gás Liberação ou absorção de calor Formação de um precipitado Mudança de cor 3 Descrevendo uma reação química Reagentes
ESTEQUIOMETRIA Estudo das reações Indicadores de uma reação química: Produção de um gás Liberação ou absorção de calor Formação de um precipitado Mudança de cor 3 Descrevendo uma reação química Reagentes
ESTEQUIOMETRIA. Estudo das reações. Indicadores de uma reação química:
 ESTEQUIOMETRIA Estudo das reações Indicadores de uma reação química: Produção de um gás Liberação ou absorção de calor Formação de um precipitado Mudança de cor 3 Descrevendo uma reação química Reagentes
ESTEQUIOMETRIA Estudo das reações Indicadores de uma reação química: Produção de um gás Liberação ou absorção de calor Formação de um precipitado Mudança de cor 3 Descrevendo uma reação química Reagentes
ESTEQUIOMETRIA. Estudo das reações. Descrevendo uma reação química. Indicadores de uma reação química:
 ESTEQUIOMETRIA Estudo das reações Indicadores de uma reação química: Produção de um gás Liberação ou absorção de calor Formação de um precipitado Mudança de cor 3 Descrevendo uma reação química Representação
ESTEQUIOMETRIA Estudo das reações Indicadores de uma reação química: Produção de um gás Liberação ou absorção de calor Formação de um precipitado Mudança de cor 3 Descrevendo uma reação química Representação
RECUPERAÇÃO DE INSUMOS E SUBPRODUTOS DA PRODUÇÃO DE BIODIESEL. Processo de recuperação do Metanol e da Glicerina.
 RECUPERAÇÃO DE INSUMOS E SUBPRODUTOS DA PRODUÇÃO DE BIODIESEL Processo de recuperação do Metanol e da Glicerina. O processo completo de produção de biodiesel partindo-se do óleo degomado é constituído
RECUPERAÇÃO DE INSUMOS E SUBPRODUTOS DA PRODUÇÃO DE BIODIESEL Processo de recuperação do Metanol e da Glicerina. O processo completo de produção de biodiesel partindo-se do óleo degomado é constituído
BB-DIESEL BIODIESEL SOLUTIONS
 Unidade de produção de biodiesel O biodiesel é um metil-éster que resulta de uma reacção entre um álcool (geralmente o metanol) e óleos vegetais ou gorduras animais em ambiente alcalino. Para que a reacção
Unidade de produção de biodiesel O biodiesel é um metil-éster que resulta de uma reacção entre um álcool (geralmente o metanol) e óleos vegetais ou gorduras animais em ambiente alcalino. Para que a reacção
sua configuração eletrônica por níveis e subníveis mais provável;
 http://www.ime.ebr/~sd3/vestibular/provas9900/quimica/ 1 a QUESTÃO Valor: 1,0 Para um possível elemento X de nº atômico Z=119, determine: d. sua configuração eletrônica por níveis e subníveis mais provável;
http://www.ime.ebr/~sd3/vestibular/provas9900/quimica/ 1 a QUESTÃO Valor: 1,0 Para um possível elemento X de nº atômico Z=119, determine: d. sua configuração eletrônica por níveis e subníveis mais provável;
Catálise heterogênea. Catalisador sólido. Reação na interface sólido-fluido
 Catálise heterogênea Catalisador sólido Reação na interface sólido-fluido Tipos de catalisadores Poroso: elevada área superficial Tipos de catalisadores Peneiras moleculares: capacidade de distinção entre
Catálise heterogênea Catalisador sólido Reação na interface sólido-fluido Tipos de catalisadores Poroso: elevada área superficial Tipos de catalisadores Peneiras moleculares: capacidade de distinção entre
Qui. Allan Rodrigues Xandão (Gabriel Pereira)
 Semana 15 Allan Rodrigues Xandão (Gabriel Pereira) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. 23
Semana 15 Allan Rodrigues Xandão (Gabriel Pereira) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. 23
BALANÇO DE MASSA E ENERGIA EM PROCESSOS QUÍMICOS LISTA DE EXERCÍCIOS CORRESPONDENTES ÀS AULAS 2 E 3
 BALANÇO DE MASSA E ENERGIA EM PROCESSOS QUÍMICOS LISTA DE EXERCÍCIOS CORRESPONDENTES ÀS AULAS 2 E 3 Pág. 2/6 4. Trezentos galões americanos de uma mistura contendo 75,0% em massa de etanol e 25% de água
BALANÇO DE MASSA E ENERGIA EM PROCESSOS QUÍMICOS LISTA DE EXERCÍCIOS CORRESPONDENTES ÀS AULAS 2 E 3 Pág. 2/6 4. Trezentos galões americanos de uma mistura contendo 75,0% em massa de etanol e 25% de água
PADRÃO DE RESPOSTA - QUÍMICA - Grupo J
 PADRÃO DE RESPOSTA - QUÍMICA - Grupo J 1 a QUESTÃO: (2,0 pontos) Avaliador Revisor Num recipiente de 3,0 L de capacidade, as seguintes pressões parciais foram medidas: N 2 = 0,500 atm; H 2 = 0,400 atm;
PADRÃO DE RESPOSTA - QUÍMICA - Grupo J 1 a QUESTÃO: (2,0 pontos) Avaliador Revisor Num recipiente de 3,0 L de capacidade, as seguintes pressões parciais foram medidas: N 2 = 0,500 atm; H 2 = 0,400 atm;
ESCOLA SECUNDÁRIA DE CASQUILHOS
 ESCOLA SECUNDÁRIA DE CASQUILHOS 8.º Teste sumativo de FQA 16. março. 015 10.º Ano Turma A Professora: Maria do Anjo Albuquerque Versão 1 Duração da prova: 90 minutos. Este teste é constituído por 7 páginas
ESCOLA SECUNDÁRIA DE CASQUILHOS 8.º Teste sumativo de FQA 16. março. 015 10.º Ano Turma A Professora: Maria do Anjo Albuquerque Versão 1 Duração da prova: 90 minutos. Este teste é constituído por 7 páginas
Módulo inicial Materiais: Diversidade e Constituição. Química 10.º ano Ano lectivo 2007/2008
 Química 10.º ano Ano lectivo 2007/2008 Escola Secundária José Saramago Marta Paulino e Ângela Patrício O que é um Material? É algo que tem massa e ocupa espaço. Classificação Materiais: Componentes Origem
Química 10.º ano Ano lectivo 2007/2008 Escola Secundária José Saramago Marta Paulino e Ângela Patrício O que é um Material? É algo que tem massa e ocupa espaço. Classificação Materiais: Componentes Origem
ENGENHARIA QUÍMICA 3º
 ENGENHARIA QUÍMICA 3º ano 2005/2006 OPERAÇÕES EM SISTEMAS MULTIFÁSICOS Exercícios IST, DEQB, Fevereiro de 2006 I. Caracterização de Sistemas Subdivididos Problema I.1 Por peneiração de um sal obtiveram-se
ENGENHARIA QUÍMICA 3º ano 2005/2006 OPERAÇÕES EM SISTEMAS MULTIFÁSICOS Exercícios IST, DEQB, Fevereiro de 2006 I. Caracterização de Sistemas Subdivididos Problema I.1 Por peneiração de um sal obtiveram-se
