Sendo O a forma oxidada do analito e R a forma reduzida.
|
|
|
- Igor Coelho Silva
- 9 Há anos
- Visualizações:
Transcrição
1 2 Voltametria Os métodos eletroanalíticos fazem uso das propriedades elétricas mensuráveis (corrente, potencial e carga) de um analito quando este é submetido a uma diferença de potencial entre eletrodos em uma cela eletroquímica. Essas medidas podem então ser relacionadas com algum parâmetro químico intrínseco do analito 41. Existe uma gama variada de técnicas eletroanalíticas que têm sido utilizadas para várias aplicações, entre elas no monitoramento ambiental, no controle de qualidade de produtos e processos industriais e nas análises biomédicas. Os métodos eletroanalíticos oferecem uma série de vantagens tais como (i) seletividade e especificidade das determinações resultante da oxiredução das espécies analíticas de interesse em um potencial aplicado específico; (ii) seletividade decorrente dos processos de oxiredução do analito em eletrodo de trabalho feito com material específico; (iii) grande sensibilidade e baixos limites de detecção resultante das técnicas de pré-concentração e modos de aquisição de sinal que proporciona ambiente com baixo sinal de fundo 42. A voltametria é uma técnica eletroanalítica que se baseia nos fenômenos que ocorrem na interface entre a superfície do eletrodo de trabalho e a camada fina de solução adjacente a essa superfície. Essa técnica é classificada como dinâmica, pois a cela eletroquímica é operada na presença de corrente elétrica (i > 0) que, por sua vez, é medida em função da aplicação controlada de um potencial 43. Assim, nessa técnica, as informações sobre o analito são obtidas por meio da medição da magnitude da corrente elétrica que surge no eletrodo de trabalho ao se aplicar um potencial entre um eletrodo de trabalho e um eletrodo auxiliar. O parâmetro ajustado é o potencial (E) e o parâmetro medido é a corrente resultante (i) O registro da corrente em função do potencial, é denominado voltamograma, e a magnitude da corrente obtida pela transferência de elétrons durante um processo de oxiredução (Equação 1), pode ser relacionada com a quantidade de analito presente na interface do eletrodo e conseqüentemente, na cela eletroquímica.
2 29 O + ne - R (1) Sendo O a forma oxidada do analito e R a forma reduzida. Um eletrodo atrai predominantemente espécies carregadas positivamente ou negativamente, que podem ou não reagir na sua superfície. Espécies neutras também interagem com o eletrodo via adsorção. Logo, a reação eletródica é composta por uma série de etapas e para se descrever qualquer processo eletródico deve ser considerado primeiro, o transporte das espécies até a superfície do eletrodo e segundo, a reação que ocorre no eletrodo. Assim, a corrente (ou velocidade de reação eletródica) é governada por processos como (i) transferência de massa (transferência da espécie do corpo da solução para a interface eletrodosuperfície); (ii) transferência de carga (transferência de elétrons na superfície do eletrodo; (iii) reações químicas que precedem ou sucedem a transferência de elétrons que podem por sua vez ser homogêneos (protonação, dimerização, etc) ou heterogêneos (decomposições catalíticas, adsorção, desorção, cristalização). É indispensável que o transporte de massa seja contínuo, pois, caso contrário, a concentração da espécie eletroativa de interesse na superfície do eletrodo irá decrescer rapidamente, inviabilizando a relação com a concentração do analito no seio da solução. Existem três formas pela qual o transporte de massa pode correr, a migração, a convecção e a difusão. Em voltametria, as condições experimentais são ajustadas para que o transporte por migração (movimento de íons através da solução causada pela atração ou repulsão entre as espécies iônicas em solução e o eletrodo de trabalho) e convecção (movimentação das espécies causadas por perturbação mecânica do fluxo da solução) sejam minimizados. No caso da migração, o uso de excesso de eletrólito não reativo na solução ou eletrólito suporte (concentração de 50 a 100 vezes maior que a concentração da espécie eletroativa de interesse) impede a formação de um campo elétrico devido a um gradiente de cargas. Já o transporte convectivo é minimizado cessando o distúrbio mecânico da solução (agitação mecânica e borbulhamento de gás) antes de se aplicar o potencial de trabalho. Assim, em voltametria, o transporte de massa é feito basicamente por difusão, que é a movimentação espontânea da espécie química devido à formação de um gradiente de concentração do analito de interesse. Por exemplo, considerando a
3 30 reação redox (Equação1) no sentido direto, à medida que a espécie oxidada (O) começa a ser reduzida, há um decréscimo da concentração de O na superfície do eletrodo, e espontaneamente surgirá um fluxo de O do seio da solução para a interface eletrodo-solução devido a criação do gradiente de concentração. A transferência de carga e consequentemente as reações eletródicas (processos de oxidação e redução) ocorrem na interface eletrodo-solução gerando corrente elétrica. A corrente total é constituída de duas componentes. A corrente faradaica, relativa à reação de oxiredução da espécie em estudo no eletrodo e a corrente capacitiva, que é a corrente necessária para carregar a dupla camada elétrica existente na interface eletrodo-solução. A interface eletrodo-solução é uma região bem diferente de todo o restante da solução e é onde a maior diferença de potencial ocorre podendo ser descrita pela síntese de Stern dos modelos de Helmholtz, Gouy e Chapman. A dupla camada pode ser representa esquematicamente pela Figura 3. Figura 3 - Representação esquemática da dupla camada segundo a síntese de Stern dos modelos de Helmholtz e Gouy-chapman. Quando a superfície do eletrodo de trabalho, imerso na solução de eletrólito suporte, se encontra carregado (positivamente ou negativamente) ela irá alterar a camada de solução imediatamente vizinha da superfície do eletrodo 44. Seguindo
4 31 este raciocínio, Helmholtz, postulou que esta distribuição de cargas ao longo do eletrodo iria produzir uma orientação das moléculas do solvente imediatamente vizinhas ao eletrodo de forma a criar uma contra camada elétrica cuja carga total e densidade de carga seria igual ao eletrodo de trabalho, porém possuiria sinal oposto, de forma a manter a neutralidade elétrica do sistema. Esta interface formada por duas lâminas de carga oposta em sinais é denominada de dupla camada elétrica, sendo bastante compacta, ou seja, as moléculas do solvente na camada adjacente não possuem mobilidade estando especificamente adsorvidas no eletrodo (plano interno de Helmholtz ou camada interna). Além dessa camada, estaria uma região na qual as moléculas da espécie eletroativa de interesse solvatados estariam presentes, porém, devido ao seu raio de hidratação, não conseguem atingir a superfície do eletrodo. Este plano se estende a partir da fronteira da camada interna até a fronteira da região denominada seio da solução. Essa região é denominada plano externo de Helmholtz, camada externa ou camada difusa. Nessa camada externa, que é mais larga que a camada interna, as moléculas do analito solvatados possuem certa mobilidade, e sofrem atração do eletrodo por interações de longa distância. A concentração de analito na camada difusa é proporcional à concentração de analito no seio da solução, o que tem a importante consequência de proporcionar um aspecto analítico quantitativo na medida de corrente gerado pela interação do analito com o eletrodo. A largura da camada externa depende da composição da solução e é limitada por convecção, variando entre 0,3 a 0,5 mm num ambiente sem agitação mecânica. Quando a solução é mantida sob agitação, a largura dessa camada decresce significantemente para valores entre 0,01 a 0,001 mm. Além desta camada externa, existiria o seio da solução, onde as moléculas não sofrem nenhum tipo de interação com o eletrodo. Normalmente a transferência de carga se dá quando analito atinge a camada externa (difusa), mas em alguns casos, onde ocorre adsorção específica, o analito pode chegar até a camada interna (compacta) substituindo moléculas do solvente e se adsorvendo especificamente ao eletrodo. A corrente observada na interação do analito com o eletrodo (oxiredução) é a faradaica (denominada assim por obedecer a lei de Faraday), e é proporcional à concentração de analito ativo no seio da solução. O outro tipo de corrente, a corrente capacitiva, não é proporcional à concentração do analito e nem obedece à lei de faraday (não-faradaica), é apenas
5 32 uma corrente que é gerada devido a presença de um acúmulo de elétrons na superfície do eletrodo, aumentando a carga da dupla camada elétrica (corrente transiente causada por mudanças na superfície do eletrodo e da solução). Muito dos ganhos instrumentais obtidos nos últimos anos tem sido em função da diminuição da contribuição da corrente não-faradaica na corrente total medida. Para que seja possível determinar um analito por voltametria é necessário que o analito em questão seja eletroativo, ou seja, que ele oxide ou reduza em uma região de potencial aplicado na qual a transferência de elétrons seja favorável termodinamicamente ou cinéticamente, criando-se um fluxo de elétrons 45. Nesse caso, a corrente faradaica deve ser medida em um ambiente de baixo ruído, que é formado pelas correntes não-faradaicas e por correntes faradaicas provenientes de processos de oxiredução provenientes de outras espécies na solução da cela de trabalho (eletrólito de suporte e solvente, componentes da amostra, gases dissolvidos). No primeiro caso, as correntes não-faradaicas podem ser minimizadas pelo uso de eletrodos de pequena área superficial e pelo uso de um modo de aquisição de sinal (corrente) mais apropriados. No caso das correntes faradaicas não-específicas do analito, o uso de eletrodo polarizado garante que nenhuma transferência de carga possa ocorrer entre o eletrodo e a solução de eletrólito suporte em função do potencial aplicado. Muito embora nenhum eletrodo seja idealmente polarizado (transferência de carga na interface eletrodoeletrólito suporte nula em todo o intervalo de potencial), eletrólitos suporte proporcionam comportamento polarizado para alguns eletrodos num intervalo limitado de potencial (janela de potencial de trabalho) 46. A seletividade do eletrodo em condições experimentais específicas também evita que a corrente faradaica proveniente de substâncias potencialmente interferentes se manifestem. O potencial aplicado no eletrodo de trabalho atua como a força motriz para a reação eletroquímica. É o potencial controlado que possibilita a espécie presente na solução ser oxidada ou reduzida na superfície do eletrodo. Na medida que o potencial se torna mais negativo, o eletrodo se torna uma fonte de elétrons favorecendo a redução das espécies na interface solução-eletrodo. No caso de um potencial mais positivo a oxidação das espécies será favorecida. Por esta razão, quando se faz uma varredura de potencial no sentido negativo usa-se a denominação de varredura catódica, enquanto que uma varredura de potencial no sentido positivo é a varredura anódica.
6 33 A corrente elétrica surge quando o potencial aplicado atinge um valor tal que permite a reação de oxiredução do analito acontecer. Se essa corrente elétrica é proporcional à quantidade das espécies que reagem, pode-se fazer uso desse fenômeno do ponto de vista analítico quantitativo. A corrente faradaica, i, proveniente da oxiredução do analito na superfície do eletrodo é, dada por: i = zf dn/dt (2) Onde: z é um número inteiro de sinal e magnitude da carga iônica da espécie eletroativa F é a constante de Faraday (96.484,6 C) dn/dt é a taxa de variação de mols da espécie eletroativa Se considerarmos a taxa de variação dn/dt como o produto entre o fluxo de espécies eletroativas (J) e a área da seção reta (A), tem-se que a corrente instantânea é: i = zfaj (3) Ao contrário da polarografia clássica com eletrodo gotejante, na voltametria com eletrodo estático, onde a área do eletrodo se mantém constante, tem-se que A é independente do tempo. Na voltametria, as espécies ativas chegam no eletrodo primariamente por difusão, pois outras formas de transporte de massa são propositalmente limitadas. Nesse caso J é dependente do tempo e é descrito pela primeira lei de Fick, que descreve J como o produto entre o coeficiente de difusão, D, multiplicado pela variação de concentração na interface eletrodo-solução (onde à distância, x, entre a superfície do eletrodo e a solução é zero) J = D dc 0 /dx (4) Assim a corrente é limitada por difusão ou está sob controle difusional. Sendo as espécies envolvidas no processo são iônicas (fluxo envolvendo transferência de carga) e a corrente pode ser expressa por:
7 34 i = zfa D dc 0 /dx (5) Similarmente, se o fluxo de espécies para o eletrodo não envolve transferência de carga (transferência de cátions ou ânions) mas é adsortivo, temos um processo heterogêneo cineticamente controlado. A adsorção é um processo heterogêneo e o fluxo de espécies eletroativas pode ser descrito como uma etapa cinética de primeira ordem (Equação 6) Nesse caso tem-se também uma relação onde a corrente é proporcional à concentração da espécie de interesse. i = zfak h c 0 (6) Onde: k h é uma constante de velocidade heterogênea c 0 é concentração superficial de espécies na superfície do eletrodo em um dado instante. Como na camada externa, existe um gradiente de concentração aproximadamente constante (Figura 4), o que dc/dx é igual à diferença entre a concentração de analito na dupla camada e a concentração no seio da solução (c c 0 ) dividido por dx, que equivale à largura da camada difusa (δ), assim: dc 0 /dx = (c c 0 )/ δ (7) Logo, substituindo (7) em (5), tem-se: i = zfa D (c c 0 )/ δ ( 8) Quando a corrente é limitada por difusão, o material que chega à superfície do eletrodo é imediatamente reduzido ou oxidado mantendo sua concetração, c 0, do nula. Assim, a Equação 8 pode ser simplificada para: i = - zfa D Ox c Ox / δ (9) no caso do processo anódico, e para: i = zfa D Red c Red / δ (10) no caso de um processo catódico. Desde que δ é limitado por convecção, pode ser considerada constante.
8 35 Para sistemas controlados pelas leis da termodinâmica, o potencial do eletrodo (E) pode ser usado para estabelecer a concentração da espécie eletroativa na superfície do eletrodo, de acordo com a equação de Nernst: E = E o + 2,3RT/nF x log (c Ox /c Red ) (11) Sendo: E 0 o potencial padrão da reação R a constante dos gases (4,18 J mol -1 K -1 ) T a temperatura absoluta n o número de mols elétrons transferido na reação. c Ox e c Red são as concentrações superficiais das espécies oxidada e reduzida respectivamente Figura 4 Camada de difusão de Nernst. A concentração no seio da solução é C B e a largura da camada de difusão é δ. A corrente resultante de uma reação de oxiredução é faradaica (a reação de n mols de substância envolve a transferência de n x coulombs), e esta reação não é homogênea em toda a solução, pois todo este processo acontece na interface entre a solução e o eletrodo de trabalho. A corrente irá então depender de dois fatores: (1 o ) A velocidade na qual as espécies se movem do seio da solução para a superfície do eletrodo (transporte de massa) e (2 O ) a velocidade na qual os elétrons são transferidos do eletrodo para a espécie em solução e vice-versa (transferência de carga) 47.
9 36 Como vimos que a concentração das espécies ativas são proporcionais à corrente, temos aproximadamente que: E = E o + 2,3RT/nF x log [(-i Ox δ/zfad Ox ) i Red δ/zfad Red )] (12) Como D Ox é aproximadamente igual a D Red, temos: E = E o + 2,3RT/nF x log (-i Ox /i Red ) (13) Assim, tem-se a relação entre o potencial aplicado e a corrente de difusão ou faradaica que por sua vez pode ser relacionada com a concentração das espécies de interesse. A forma na qual o potencial é aplicado, e por conseqüência a forma como o sinal analítico (corrente) é adquirido, irá denominar o tipo de técnica voltamétrica em questão. As formas mais comuns de aplicação deste potencial estão representados na Figura 5, bem como a forma de resposta da corrente resultante segundo revisão de Barek 48. O modo de aquisição repercute na sensibilidade do método principalmente devido à magnitude da corrente capacitiva observada para cada caso e também na seletividade devido ao formato do voltamograma e à largura dos pulsos de resposta medidos. Além do modo de aquisição, os métodos voltamétricos variam de acordo com as etapas utilizadas antes ou durante a medida do sinal, tais como a pré-concentração de analito (proveniente da capacidade do analito em reagir ou adsorver com o material do eletrodo de trabalho) ou direção ou inversão da direção da varredura de potencial. A escolha da técnica voltamétrica a ser utilizada está relacionada com o tipo e a qualidade de informação quantitativa/qualitativa que se quer obter a respeito do analito ou do processo que envolve a interação entre o analito e o eletrodo de trabalho. Maiores detalhes sobre os diferentes modos de aquisição são descritos a seguir.
10 37 Tipo de voltametria varredura linear Sinal de excitação Corrente resultante i pulso diferencial i onda quadrada i Voltametria cíclica i E Figura 5- Forma de aplicação do potencial para cada tipo de voltametria
11 Voltametria de varredura linear Na voltametria de varredura linear, também chamada por alguns autores de cronoamperometria de varredura de potencial linear 48, o potencial aplicado ao eletrodo de trabalho varia linearmente com o tempo (Figura 6A), esta técnica possibilita a aplicação de velocidades de varredura relativamente altas (até 1000 mv s -1 ), no entanto não é um técnica muito sensível. A B Figura 6- Representação esquemática da voltametria com varredura linear: a) Variação do potencial como o tempo, b) variação da corrente como o tempo, d) variação da corrente como o potencial. A corrente é lida de forma direta, em função do potencial aplicado, desta forma a corrente total lida possui contribuições tanto da corrente faradaica (desejável) quanto da corrente capacitiva (ruído), o que prejudica em muito a aplicação desta técnica para aplicações quantitativas. Os limites de detecção obtidos por essa técnica, nas estimativas mais otimistas, são da ordem de 10-6 mol L -1
12 Voltametria de pulso diferencial. Na voltametria de pulso diferencial, pulsos de amplitude fixos sobrepostos a uma rampa de potencial crescente são aplicados ao eletrodo de trabalho. A Figura 7 mostra os dois sinais de excitação mais comuns para aparelhos comerciais de polarografia 43. No primeiro tipo (Figura 7A), ocorre a sobreposição de pulsos periódicos sobre uma rampa linear, esta forma de excitação é utilizado em equipamentos analógicos. O segundo tipo (Figura 7B) é usado em equipamentos digitais, nestes equipamentos combina-se um pulso de saída com um sinal em degrau. A 50 ms B Potencial S2 E S2 S1 S1 tempo Figura 7 Sinais de excitação para voltametria de pulso diferencial A corrente é medida duas vezes, uma antes da aplicação do pulso (S1) e outra ao final do pulso (S2). A primeira corrente é instrumentalmente subtraída da segunda, e a diferença das correntes é plotada versus o potencial aplicado, o voltamograma resultante consiste de picos de corrente de forma gaussiana, cuja área deste pico é diretamente proporcional à concentração do analito, de acordo com a seguinte equação: 1/ 2 nfad C 1 σ i p = (14) πt 1+ σ m
13 40 Sendo: i p = corrente do pico (µa) n = número de elétrons envolvido na reação redox F = constante de Faraday (coulombs) A = área do eletrodo (cm 2 ) t m = tempo entre o segunda e a primeira leitura de corrente (s) D = coeficiente de difusão (cm 2 s -1 ) C = concentração do analito (mmol L -1 ) σ = exp(nf/rt E/2), E = amplitude do pulso O pico de potencial (E p ) pode também ser usado para identificar as espécies, uma vez que estes picos aparecem próximos ao potencial de meia-onda da correspondente análise polarográfica: E p = E 1/2 - E/2 (15) O objetivo de se fazer duas leituras da corrente e se trabalhar com a diferença entre elas é fazer a correção da corrente capacitiva. À medida que se aplica o pulso, ocorre um acréscimo da contribuição da corrente capacitiva e da corrente faradaica, mas a corrente capacitiva diminui exponencialmente, enquanto que a corrente faradaica diminui linearmente, assim, escolhendo um tempo apropriado para se fazer a segunda leitura, faz-se a leitura da corrente total a um valor de corrente onde a contribuição da corrente capacitiva (não-faradaica) pode ser desconsiderada. Assim, desvinculando o valor da primeira leitura de corrente da segunda, obtém-se uma minimização da contribuição da corrente de fundo 41. Esta correção de correntes possibilitada pelo modo de pulso diferencial permite obter limites de detecção da ordem de 10-8 mol L -1.
14 Voltametria de onda quadrada Na voltametria de onda quadrada (do inglês, square-wave) uma onda quadrada simétrica de amplitude E p sobreposta a uma rampa de potencial na forma de escada (staircase) caracterizada pela amplitude E s, largura a e período τ é aplicada ao eletrodo de trabalho 49, como representado na Figura 8. A corrente é amostrada duas vezes, uma ao final do pulso direto, quando a direção do pulso é igual à direção da varredura, e outro ao final do pulso reverso (que ocorre no meio do degrau da onda staircase), onde a direção do pulso é contrária à direção da varredura. Assim como na voltametria de pulso diferencial, esta dupla amostragem da corrente garante uma minimização da contribuição da corrente capacitiva sobre a corrente total lida. O voltamograma resultante consiste da diferença entre estas duas correntes versus a rampa de potencial aplicado. Na Figura 8 está também representada o pico corrente resultante da voltametria de onda quadrada, o pico é caracterizado por um potencial E 1/2 e largura W 1/2. A sensibilidade desta técnica é comparável com a proveniente da voltametria de pulso diferencial. A maior vantagem desta técnica é a velocidade de aquisição dos dados. Freqüências de 1 a 100 ciclos de onda quadrada por segundo permitem o uso de velocidades de varredura de potencial extremamente rápidas. Enquanto na voltametria de pulso diferencial a velocidade de varredura varia de 1 a 10 mv s -1, na voltametria de onda quadrada esta velocidade varia de 100 a 1000 mv s -1, isto diminui o tempo de análise de cerca de 3 a 5 minutos para alguns poucos segundos (3 a 10 s) sem haver perda da resolução dos picos.
15 Figura 8 Representação esquemática da voltametria de onda quadrada. 42
16 Voltametria cíclica A voltametria cíclica é a técnica mais comumente usada para adquirir informações qualitativas sobre os processos eletroquímicos. A eficiência desta técnica resulta de sua habilidade de rapidamente fornecer informações sobre a termodinâmica de processos redox, da cinética de reações heterogêneas de transferência de elétrons e sobre reações químicas acopladas a processos adsortivos 41. Inicia-se a aplicação do potencial de um valor no qual nenhuma redução ocorre, com o aumento do potencial para regiões mais negativas (catódica) ocorre a redução do composto em solução, gerando um pico de corrente proporcional à concentração deste composto, quando o potencial já tiver atingido um valor no qual nenhuma reação de redução ocorre, o potencial é varrido no sentido inverso, até o valor inicial, e no caso de uma reação reversível, os produtos que tiverem sido gerados no sentido direto (e se localizam ainda próximos à superfície do eletrodo) serão oxidados, gerando um pico simétrico ao pico da redução. O tipo de voltamograma gerado depende do tipo de mecanismo redox que o composto em questão sofre no eletrodo, o que faz da voltametria cíclica uma ferramenta valiosa para estudos mecanísticos. Existem dois componentes principais que determinam as reações que ocorrem no eletrodo, existe a transferência difusional de massa do analito em solução para a superfície do eletrodo, e a transferência heterogênea de carga entre o analito e o eletrodo, em alguns casos ainda pode ocorrer reações químicas acopladas a algum destes processos. A equação de Butler-Volmer 84, equação básica da cinética eletroquímica, expressa estas relações. i nf = Ca (0, t) K s αna F o exp[ ( E pc E )] Cb(0, t) K RT s (1 α) na exp[ RT ( E pc E o )]( 16) Para uma reação reversível, ou seja, uma reação que ocorre com velocidade suficientemente alta para estabelecer um equilíbrio dinâmico na interface, a equação de Butler-Volmer se reduz na equação de Nerst (11), pois como a cinética da reação de transferência de carga é rápida (Ks > 10-1 cm s -1 ) apenas a etapa de transferência de massa irá ditar as regras do processo. A corrente do pico (em amperes) neste caso, é dada por:
17 44 3 1/ 2 1/ 2 ( 2,69x10 5 ) n 2 / AD0 v C0 i pc = (17) Sendo que n é o número de elétrons envolvidos no processo, A é a área do eletrodo (cm 2 ), Do é o coeficiente de difusão (cm 2 s -1 ) e Co é a concentração da espécie em solução (mol cm -3 ), v é a velocidade de varredura (V s -1 ). Para uma reação reversível a corrente de pico varia linearmente com a raíz quadrada da velocidade de varredura. Outros critérios para reversibilidade são a razão da corrente de pico anódico e catódico igual a unidade e independente de v, o potencial de pico não variando com a velocidade de varredura de potencial e a razão i p /v 1/2 constante e independe de v 50. Quando a velocidade de transferência de carga é lenta comparada com a velocidade de varredura (Ks<10-5 cm/s) as concentrações das espécies oxidadas (O) e reduzida (R) não serão mais função apenas do potencial, não possuindo portanto um comportamento nerstiano. Neste caso, os termos α (coeficiente de transferência) e Ks (velocidade de transferência de carga) devem ser considerados. Nestas circunstâncias, a equação que descreve a corrente de pico (i pc ) é dada por: ipc 5 1/ 2 1/ 2 1/ 2 = ( 2,99x10 ) n( αn) AC0 D0 v (18) Nestes casos, o voltamograma costuma apresentar apenas pico anódico, que irá deslocar-se como aumento da velocidade de varredura. Além disso, este pico varia também com α e Ks. Para uma reação eletródica quase-reversível (10-1 > Ks > 10-5 cm/s) a corrente é controlada tanto pela etapa de transferência de massa como pela etapa de transferência de carga. A equação de Nernst é apenas aproximadamente satisfeita. A forma de aplicação do potencial na voltametria cíclica está representado na Figura 9, o potencial é varrido linearmente com o tempo no eletrodo de trabalho estacionário, em uma solução sem agitação, usando um potencial em forma de triângulo (Figura 9a). Dependendo da informação desejada, simples ou múltiplos ciclos podem ser utilizados. Durante a varredura do potencial, o potenciostato mede a corrente resultante desta corrente versus o potencial aplicado. Em alguns casos, instrumentos digitais não possuem este mesmo padrão de aplicação de potencial. Porém, o potencial é aplicado na forma de escada 86 (staircase) como pode ser visto na Figura 9b, com degraus de potenciais pequenos (da ordem de 10 mv) e tempo de duração pequena (50 ms), onde a corrente é lida
18 45 apenas no final deste intervalo. Esse método stair case substitui a contento a varredura linear. O objetivo desta variação é conseguir uma minimização da contribuição da corrente capacitiva na corrente total. Como as etapas de potencial são pequenas, as equações para as respostas da voltametria cíclica staircase são consideradas como idênticas das provenientes da voltametria cíclica de varredura linear. A) potencial Ciclo 1 tempo B) Ciclo 1 potencial tempo Figura 9 formas de aplicação do potencial para a voltametria cíclica: a) potencial com varredura linear e b) potencial do tipo escada.
19 Voltametria de redissolução. Na voltametria de redissolução, uma reação eletroquímica entre o analito (ou um complexo do analito) com o eletrodo de trabalho deve ocorrer antes da varredura e aquisição de sinal iniciar. Devido à essa reação, o analito pode ser préconcentrado no eletrodo de trabalho. Como consequência, um aumento da magnitude da corrente medida é obtido, com diminuição significativa do limites de detecção alcançados para estas espécies químicas. Esta etapa normalmente ocorre sob aplicação de um potencial controlado durante um tempo determinado, e com condições hidrodinâmicas (transporte de massa) controlados e reprodutíveis 51. Após esta etapa de pré-concentração, é feita uma varredura de potencial no qual o analito é redissolvido (do inglês, stripping) para a solução. A análise voltamétrica por redissolução possui duas variantes, a catódica e a anódica. A voltametria de redissolução anódica (ASV, do inglês) é mais utilizada para a análise de íons metálicos através da deposição catódica Quando esta análise ocorre em eletrodo de gota pendente de mercúrio (EGPM), a reação que ocorre entre o analito e o eletrodo é: A n+ + ne - + Hg A(Hg) (19) Em eletrodos sólidos, a reação que ocorre é: A n+ + ne - A (20) Sendo A o analito. Esse tipo de interação é mais comum para os íons metálicos, mas também ocorre no caso de algumas substâncias orgânicas (por exemplo a adenina) que atingem o eletrodo de mercúrio por difusão e convecção (uma vez que nesta etapa ainda existe agitação da solução). A concentração de analito no amalgama, C Hg é regida pela lei de Faraday. = i td l C Hg (21) nfvhg
20 47 Sendo: i l a corrente limite para a difusão de metal td o tempo de deposição V Hg o volume do eletrodo de mercúrio A quantidade de analito depositado representa uma pequena (porém reprodutível) fração do analito presente na solução. Terminada a etapa de deposição, a agitação da solução é encerrada para se terminar com o transporte de massa conectivo, e o potencial é então varrido anodicamente, de forma linear ou pulsada (pulso diferencial ou onda quadrada). No caso dos metais, durante esta varredura anódica, os metais amalgamados são reoxidados, sendo redissolvidos do eletrodo para a solução, numa seqüência que respeita os seus potenciais padrões. A reação que representa esta reação é: A(Hg) A n+ + ne - (EGPM) (22a) ou A A n+ + n e- (eletrodo sólido) (22b) A corrente de pico depende de vários parâmetros das etapas de deposição e redissolução, assim como das características do analito e da geometria do eletrodo. Para o eletrodo de gota pendente de mercúrio, a expressão para a corrente de pico é: i d = 2,72x10 5 n 3/2 AD 1/2 v 1/2 C Hg (23) Sendo A um fator de frequencia e D o coeficiente de difusão do analito no eletrólito suporte utilizado. A voltametria de redissolução catódica (CSV) é utilizada para determinar uma grande variedade de compostos orgânicos e inorgânicos Nesta voltametria, aplica-se um potencial relativamente positivo ao eletrodo de trabalho na presença do analito, e este irá reagir com o eletrodo, formando um sal insolúvel sobre o material eletródico. Esta reação pode ser representada da seguinte forma:
21 48 M M n+ + ne - M n+ + A n- MA (24a) (24b) Sendo M o material eletródico, A o analito e MA o sal insolúvel formado na superfície do eletrodo. A varredura se dá no sentido catódico (negativo), e o analito é redissolvido da seguinte forma: MA + ne - M + A n- (25) Como esta técnica envolve a formação de um filme sob a superfície do eletrodo, é até mesmo comum que a curva de calibração perca a linearidade em relativas altas concentrações, devido a saturação da superfície do eletrodo. A sensibilidade da voltametria de redissolução catódica depende da quantidade de material que pode ser depositada no eletrodo. Esta quantidade é uma função da cinética de formação e da sensibilidade do composto formado, do coeficiente de difusão do íon no filme, e da densidade do filme. A sensibilidade depende também da velocidade de dissociação do composto formado.
22 Voltametria adsortiva de redissolução (AdSV) Uma possibilidade de se conseguir deposição do analito sobre o eletrodo de trabalho e um conseqüente ganho no limite de detecção da técnica mesmo quando o analito não reage eletroliticamente com o material do eletrodo é utilizando a voltametria adsortiva de redissolução. Esta técnica é baseada na capacidade que alguns compostos orgânicos e inorgânicos possuem de adsorverem na superfície do material eletródico. Esta adsorção pode ocorrer espontaneamente na superfície de um eletrodo comum, ou pode-se fazer uso de um eletrodo quimicamente modificado para se conseguir tal adsorção Em ambos os casos, a acumulação não é baseada em processos faradaicos, o analito se mantém ligado ao eletrodo por ligações covalentes, troca iônica e outras ligações eletrostáticas. Normalmente, esta adsorção se dá na camada difusa do modelo de Stern. Como em todo processo de adsorção, a quantidade de analito acumulada na superfície do eletrodo é uma função de muitos fatores, como solvente, material do eletrodo, força iônica, ph, transporte de massa, potencial ou temperatura. O processo deve ser reprodutível e ocorrer sem passivação do eletrodo (cuidado este obviamente desnecessário quando o eletrodo de trabalho é uma gota de mercúrio). Como este procedimento também envolve a formação de um filme sobre a superfície do mercúrio, também é comum a perda de linearidade em concentrações relativamente altas (em torno de 10-6 mol L -1 ). Para remediar isto, pode-se usar menores tempos de acumulação, menores velocidades de agitação da solução ou mesmo diluição das soluções. Na literatura são encontradas várias aplicações de voltametria adsortiva de redissolução para análise de compostos de importância clínico-biológica
ELETROQUÍMICA. Prof a. Dr a. Carla Dalmolin
 ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin TÉCNICAS DE DEGRAU E VARREDURA DE POTENCIAL Degrau e Impulso Degrau: alteração instantânea no potencial ou na corrente de um sistema eletroquímico A análise da
ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin TÉCNICAS DE DEGRAU E VARREDURA DE POTENCIAL Degrau e Impulso Degrau: alteração instantânea no potencial ou na corrente de um sistema eletroquímico A análise da
ELETROQUÍMICA. Prof a. Dr a. Carla Dalmolin
 ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin CINÉTICA E MECANISMOS DAS REAÇÕES ELETROQUÍMICAS Eletrodo Transferência de Elétrons O + e R 5. Transferência de elétrons k c O 1. Difusão k d,o k a O Para uma
ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin CINÉTICA E MECANISMOS DAS REAÇÕES ELETROQUÍMICAS Eletrodo Transferência de Elétrons O + e R 5. Transferência de elétrons k c O 1. Difusão k d,o k a O Para uma
CQ049 FQ Eletroquímica. prof. Dr. Marcio Vidotti Terça / Quarta: 15:30 17:30
 CQ049 FQ Eletroquímica prof. Dr. Marcio Vidotti [email protected] www.quimica.ufpr.br/mvidotti Terça / Quarta: 15:30 17:30 Espontaneidade de reações eletroquímicas redução A + e - A - oxidação A A + + e
CQ049 FQ Eletroquímica prof. Dr. Marcio Vidotti [email protected] www.quimica.ufpr.br/mvidotti Terça / Quarta: 15:30 17:30 Espontaneidade de reações eletroquímicas redução A + e - A - oxidação A A + + e
ELETROQUÍMICA. Prof a. Dr a. Carla Dalmolin
 ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin CONCEITOS BÁSICOS Eletroquímica Fenômenos químicos associados à transferência de cargas elétricas Duas semi-reações de transferência de carga em direções opostas
ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin CONCEITOS BÁSICOS Eletroquímica Fenômenos químicos associados à transferência de cargas elétricas Duas semi-reações de transferência de carga em direções opostas
Eletroquímica. Métodos/Técnicas - Eletroquímicas. Físico-química III/DAQBI/UTFPR - João Batista Floriano. Técnicas Eletroquímicas
 Métodos/Técnicas - s Técnicas s Interface Eletrodo/ solução Métodos Estacionários (I = 0) Métodos Dinâmicos (I 0) Solução Eletrolítica Titração Potenciométrica Potenciometria Potencial Controlado Potencial
Métodos/Técnicas - s Técnicas s Interface Eletrodo/ solução Métodos Estacionários (I = 0) Métodos Dinâmicos (I 0) Solução Eletrolítica Titração Potenciométrica Potenciometria Potencial Controlado Potencial
Polarização e cinética de eletrodo
 Polarização e cinética de eletrodo RESUMO DA POLARIZAÇÃO O eletrodo sai da condição de equilíbrio pela passagem de corrente pelo circuito externo; A cinética da reação interfacial é mais lenta que o fluxo
Polarização e cinética de eletrodo RESUMO DA POLARIZAÇÃO O eletrodo sai da condição de equilíbrio pela passagem de corrente pelo circuito externo; A cinética da reação interfacial é mais lenta que o fluxo
TRANSPORTE DE MASSA Eletroquímica Aula 6 Prof a. Dr a. Carla Dalmolin
 TRANSPORTE DE MASSA Eletroquímica Aula 6 Prof a. Dr a. Carla Dalmolin Velocidade de Reação de Eletrodo v = k a [R] k c [O] Dependem do transporte de espécies Difusão: movimento térmico de espécies neutras
TRANSPORTE DE MASSA Eletroquímica Aula 6 Prof a. Dr a. Carla Dalmolin Velocidade de Reação de Eletrodo v = k a [R] k c [O] Dependem do transporte de espécies Difusão: movimento térmico de espécies neutras
Noções Básicas de Eletroquímica
 Noções Básicas de Eletroquímica Dupla Camada Elétrica Genericamente Representa o ambiente iônico nas vizinhanças de uma superfície carregada; Uma dupla camada elétrica se forma todas as vezes que condutores
Noções Básicas de Eletroquímica Dupla Camada Elétrica Genericamente Representa o ambiente iônico nas vizinhanças de uma superfície carregada; Uma dupla camada elétrica se forma todas as vezes que condutores
Eletroquímica. Métodos/Técnicas - Eletroquímicas. Físico-química III/DAQBI/UTFPR - João Batista Floriano. Técnicas Eletroquímicas
 Métodos/Técnicas - s Técnicas s Interface Eletrodo/ solução Solução Eletrolítica Dupla Camada Elétrica Métodos Estacionários (I = 0) Métodos Dinâmicos (I 0) Titração Potenciométrica Potenciometria Potencial
Métodos/Técnicas - s Técnicas s Interface Eletrodo/ solução Solução Eletrolítica Dupla Camada Elétrica Métodos Estacionários (I = 0) Métodos Dinâmicos (I 0) Titração Potenciométrica Potenciometria Potencial
Métodos voltamétricos
 VOLTAMETRIA Métodos voltamétricos Dentre o grupo de técnicas que se baseiam na aplicação de um programa de potencial aplicado aos eletrodos e a corrente faradaica que resulta neste processo, destacam-se:
VOLTAMETRIA Métodos voltamétricos Dentre o grupo de técnicas que se baseiam na aplicação de um programa de potencial aplicado aos eletrodos e a corrente faradaica que resulta neste processo, destacam-se:
Métodos Eletroanalíticos. Voltametria
 Métodos Eletroanalíticos Voltametria Tipos de métodos eletroanalíticos Métodos Eletroanalíticos Métodos Interfaciais Métodos Não-Interfaciais Estáticos Dinâmicos Condutimetria Titulações Condutimétricas
Métodos Eletroanalíticos Voltametria Tipos de métodos eletroanalíticos Métodos Eletroanalíticos Métodos Interfaciais Métodos Não-Interfaciais Estáticos Dinâmicos Condutimetria Titulações Condutimétricas
Tipos de métodos eletroanalíticos
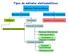 Tipos de métodos eletroanalíticos Métodos Eletroanalíticos Métodos Interfaciais Métodos Não-Interfaciais Estáticos Dinâmicos Sensores Condutimétricos Sensores Potenciométricos Potencial Controlado Sensores
Tipos de métodos eletroanalíticos Métodos Eletroanalíticos Métodos Interfaciais Métodos Não-Interfaciais Estáticos Dinâmicos Sensores Condutimétricos Sensores Potenciométricos Potencial Controlado Sensores
QUI 070 Química Analítica V Análise Instrumental. Aula 7 Química Eletroanalítica
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 070 Química Analítica V Análise Instrumental Aula 7 Química Eletroanalítica Julio C. J. Silva Juiz de Fora,
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 070 Química Analítica V Análise Instrumental Aula 7 Química Eletroanalítica Julio C. J. Silva Juiz de Fora,
Métodos Eletroanalíticos. Condutometria
 Métodos Eletroanalíticos Condutometria Tipos de métodos eletroanalíticos Métodos Eletroanalíticos Métodos Interfaciais Métodos Não-Interfaciais Estáticos Dinâmicos Condutimetria Titulações Condutimétricas
Métodos Eletroanalíticos Condutometria Tipos de métodos eletroanalíticos Métodos Eletroanalíticos Métodos Interfaciais Métodos Não-Interfaciais Estáticos Dinâmicos Condutimetria Titulações Condutimétricas
CÉLULAS ELETROLÍTICAS
 QUÍMICAELETROANALÍTICA CÉLULAS ELETROLÍTICAS REPRESENTAÇÃOESQUEMÁTICA dois limites, um em cada extremidade da ponte salina Cu Cu 2+ (0,0200 mol L -1 ) Ag + (0,0200 mol L -1 ) Ag limite entres fases, ou
QUÍMICAELETROANALÍTICA CÉLULAS ELETROLÍTICAS REPRESENTAÇÃOESQUEMÁTICA dois limites, um em cada extremidade da ponte salina Cu Cu 2+ (0,0200 mol L -1 ) Ag + (0,0200 mol L -1 ) Ag limite entres fases, ou
CORROSÃO E ELETRODEPOSIÇÃO
 CORROSÃO E ELETRODEPOSIÇÃO Princípios de Eletroquímica Prof. Dr. Artur de Jesus Motheo Departamento de FísicoF sico-química Instituto de Química de são Carlos Universidade de São Paulo 1 Princípios de
CORROSÃO E ELETRODEPOSIÇÃO Princípios de Eletroquímica Prof. Dr. Artur de Jesus Motheo Departamento de FísicoF sico-química Instituto de Química de são Carlos Universidade de São Paulo 1 Princípios de
CQ049 FQ Eletroquímica.
 CQ049 FQ Eletroquímica prof. Dr. Marcio Vidotti LEAP Laboratório de Eletroquímica e Polímeros [email protected] www.quimica.ufpr.br/mvidotti A Eletroquímica pode ser dividida em duas áreas: Iônica: Está
CQ049 FQ Eletroquímica prof. Dr. Marcio Vidotti LEAP Laboratório de Eletroquímica e Polímeros [email protected] www.quimica.ufpr.br/mvidotti A Eletroquímica pode ser dividida em duas áreas: Iônica: Está
Aula 9 FÍSICO-QUÍMICA DE SUPERFÍCIES PARTE 2: PROCESSOS EM ELETRODOS. Kleber Bergamaski
 Aula 9 FÍSICO-QUÍMICA DE SUPERFÍCIES PARTE 2: PROCESSOS EM ELETRODOS META Apresentar os principais conceitos à físico-química de superfícies envolvidos nos processos de eletrodos. Entendimento da interface
Aula 9 FÍSICO-QUÍMICA DE SUPERFÍCIES PARTE 2: PROCESSOS EM ELETRODOS META Apresentar os principais conceitos à físico-química de superfícies envolvidos nos processos de eletrodos. Entendimento da interface
AULA 5 Adsorção, isotermas e filmes monomoleculares. Prof a Elenice Schons
 AULA 5 Adsorção, isotermas e filmes monomoleculares Prof a Elenice Schons ADSORÇÃO É um processo de acumulação e concentração seletiva de um ou mais constituintes contidos num gás ou líquido sobre superfícies
AULA 5 Adsorção, isotermas e filmes monomoleculares Prof a Elenice Schons ADSORÇÃO É um processo de acumulação e concentração seletiva de um ou mais constituintes contidos num gás ou líquido sobre superfícies
QUI 070 Química Analítica V Análise Instrumental. Aula 7 Química Eletroanalítica
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 070 Química Analítica V Análise Instrumental Aula 7 Química Eletroanalítica Julio C. J. Silva Juiz de Fora,
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 070 Química Analítica V Análise Instrumental Aula 7 Química Eletroanalítica Julio C. J. Silva Juiz de Fora,
Eletroanalítica: Condutometria (ou Condutimetria)
 Universidade Federal do ABC Disciplina: Eletroanalítica e Técnicas de Separação (NH 3101) Eletroanalítica: Condutometria (ou Condutimetria) Bruno Lemos Batista Santo André - SP 2018 Site da disciplina
Universidade Federal do ABC Disciplina: Eletroanalítica e Técnicas de Separação (NH 3101) Eletroanalítica: Condutometria (ou Condutimetria) Bruno Lemos Batista Santo André - SP 2018 Site da disciplina
4. Resultados e Discussão
 Absorbância 4. Resultados e Discussão 4.1. Obtenção da curva de calibração A obtenção da curva de calibração, absorbância vs. concentração de Paraquat, é necessária para a análise química do pesticida.
Absorbância 4. Resultados e Discussão 4.1. Obtenção da curva de calibração A obtenção da curva de calibração, absorbância vs. concentração de Paraquat, é necessária para a análise química do pesticida.
DEPARTAMENTO DE ENGENHARIA METALÚRGICA. Cinética das Reações Heterogêneas
 DEPARTAMENTO DE ENGENHARIA METALÚRGICA Cinética das Reações Heterogêneas 1 Processos heterogêneos em metalurgia extrativa Os estudos termodinâmicos permitem a determinação da posição de equilíbrio alcançada
DEPARTAMENTO DE ENGENHARIA METALÚRGICA Cinética das Reações Heterogêneas 1 Processos heterogêneos em metalurgia extrativa Os estudos termodinâmicos permitem a determinação da posição de equilíbrio alcançada
QUÍMICA ELETROANALÍTICA
 QUÍMICA ELETROANALÍTICA A química Eletroanalítica compreende um conjunto de métodos analíticos qualitativos e quantitativos baseados nas propriedades elétricas de uma solução contendo o analito quando
QUÍMICA ELETROANALÍTICA A química Eletroanalítica compreende um conjunto de métodos analíticos qualitativos e quantitativos baseados nas propriedades elétricas de uma solução contendo o analito quando
Eletroquímica. Coulometria
 Eletroquímica Coulometria Tipos de métodos eletroanalíticos Métodos Eletroanalíticos Métodos Interfaciais Métodos Não-Interfaciais Estáticos Dinâmicos Condutimetria Titulações Condutimétricas Potenciometria
Eletroquímica Coulometria Tipos de métodos eletroanalíticos Métodos Eletroanalíticos Métodos Interfaciais Métodos Não-Interfaciais Estáticos Dinâmicos Condutimetria Titulações Condutimétricas Potenciometria
QUI 154 Química Analítica V Análise Instrumental. Aula 4 Potenciometria
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 154 Química Analítica V Análise Instrumental Aula 4 Potenciometria Julio C. J. Silva Juiz de Fora, 1 o sem
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 154 Química Analítica V Análise Instrumental Aula 4 Potenciometria Julio C. J. Silva Juiz de Fora, 1 o sem
MÉTODOS ELETROANALÍTICOS PARTE II
 Aula 7 MÉTODOS ELETROANALÍTICOS PARTE II META Apresentar os fundamentos da titulação potenciométrica; apresentar a localização do ponto fi nal da titulação potenciométrica; apresentar os fundamentos da
Aula 7 MÉTODOS ELETROANALÍTICOS PARTE II META Apresentar os fundamentos da titulação potenciométrica; apresentar a localização do ponto fi nal da titulação potenciométrica; apresentar os fundamentos da
QUI 070 Química Analítica V Análise Instrumental. Aula 4 Química Eletroanalítica
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 070 Química Analítica V Análise Instrumental Aula 4 Química Eletroanalítica Julio C. J. Silva 2o semestre
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 070 Química Analítica V Análise Instrumental Aula 4 Química Eletroanalítica Julio C. J. Silva 2o semestre
ELETROQUÍMICA. Prof a. Dr a. Carla Dalmolin
 ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin MÉTODOS DE IMPEDÂNCIA Espectroscopia de Impedância Eletroquímica Aplicada à caracterização de processos de eletrodo e de interfaces complexas Deve ser utilizada
ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin MÉTODOS DE IMPEDÂNCIA Espectroscopia de Impedância Eletroquímica Aplicada à caracterização de processos de eletrodo e de interfaces complexas Deve ser utilizada
1- Números de oxidação (Nox) Indicam a espécie que perde elétrons e a que ganha elétrons, ou seja, é a carga elétrica da espécie química.
 Eletroquímica É um ramo da Química que estuda as reações químicas que ocorrem, em um meio envolvendo um condutor (um metal ou um semicondutor) e um condutor iônico (o eletrólito), envolvendo trocas de
Eletroquímica É um ramo da Química que estuda as reações químicas que ocorrem, em um meio envolvendo um condutor (um metal ou um semicondutor) e um condutor iônico (o eletrólito), envolvendo trocas de
REAÇÕES DE ÓXIDO-REDUÇÃO
 REAÇÕES DE ÓXIDO-REDUÇÃO A Química Analítica moderna tem por base a medida dos Sinais Analíticos, relacionados às transformações de propriedades dos materiais ao longo de uma Análise Química. Entre estes
REAÇÕES DE ÓXIDO-REDUÇÃO A Química Analítica moderna tem por base a medida dos Sinais Analíticos, relacionados às transformações de propriedades dos materiais ao longo de uma Análise Química. Entre estes
Profª Eleonora Slide de aula. Revisão: Termodinâmica e Bioenergética
 Revisão: Termodinâmica e Bioenergética Revisão:Termodinâmica As leis da termodinâmica governam o comportamento de s bioquímicos As leis da termodinâmica são princípios gerais aplicados a todos os processos
Revisão: Termodinâmica e Bioenergética Revisão:Termodinâmica As leis da termodinâmica governam o comportamento de s bioquímicos As leis da termodinâmica são princípios gerais aplicados a todos os processos
Condutividade Elétrica
 FQE1 Exp. 1 Condutividade Elétrica 1. Introdução A condução elétrica é um fenômeno de transporte em que a carga elétrica (elétrons ou íons) se move através do sistema. A condutividade elétrica, também
FQE1 Exp. 1 Condutividade Elétrica 1. Introdução A condução elétrica é um fenômeno de transporte em que a carga elétrica (elétrons ou íons) se move através do sistema. A condutividade elétrica, também
Cálculo da Força Eletromotriz de uma Pilha
 30 2.10.1 Cálculo da Força Eletromotriz de uma Pilha Vamos calcular a fem (E) a 25 o C da célula abaixo: Zn ZnSO 4 (1,0 molal) CuSO 4 (0,1 molal) Cu A semi-reação no cátodo é Cu 2+ + 2e Cu, A semi-reação
30 2.10.1 Cálculo da Força Eletromotriz de uma Pilha Vamos calcular a fem (E) a 25 o C da célula abaixo: Zn ZnSO 4 (1,0 molal) CuSO 4 (0,1 molal) Cu A semi-reação no cátodo é Cu 2+ + 2e Cu, A semi-reação
DIFUSÃO. Conceitos Gerais
 DIFUSÃO Conceitos Gerais CAPA Os tratamentos térmicos são um conjunto de operações que têm por objetivo modificar as propriedades dos aços e de outros materiais através de um conjunto de operações que
DIFUSÃO Conceitos Gerais CAPA Os tratamentos térmicos são um conjunto de operações que têm por objetivo modificar as propriedades dos aços e de outros materiais através de um conjunto de operações que
Química Analítica Avançada
 Química Analítica Avançada Volumetria de Óxido-redução Profa. Lilian Silva LMBRANDO Reações de Oxi-redução Oxidação e redução 0 0 +1-1 0 0 +1-1 Reações redox e semi-células Zn 0 + Cu 2+ Zn 2+ + Cu 0 semi-célula
Química Analítica Avançada Volumetria de Óxido-redução Profa. Lilian Silva LMBRANDO Reações de Oxi-redução Oxidação e redução 0 0 +1-1 0 0 +1-1 Reações redox e semi-células Zn 0 + Cu 2+ Zn 2+ + Cu 0 semi-célula
Fonte: Netz e Ortega, 2002.
 1 Atividade A atividade é uma espécie de concentração efetiva. Para entender o que é uma concentração efetiva, podemos raciocinar do seguinte modo: As interações entre as moléculas em uma mistura fazem
1 Atividade A atividade é uma espécie de concentração efetiva. Para entender o que é uma concentração efetiva, podemos raciocinar do seguinte modo: As interações entre as moléculas em uma mistura fazem
ELETROQUÍMICA. 1. Introdução
 ELETROQUÍMICA 1. Introdução Em geral, uma célula eletroquímica é um dispositivo em que uma corrente elétrica o fluxo de elétrons através de um circuito é produzida por uma reação química espontânea ou
ELETROQUÍMICA 1. Introdução Em geral, uma célula eletroquímica é um dispositivo em que uma corrente elétrica o fluxo de elétrons através de um circuito é produzida por uma reação química espontânea ou
INTRODUÇÃO A MÉTODOS CROMATOGRÁFICOS
 INTRODUÇÃO A MÉTODOS CROMATOGRÁFICOS 1 Histórico da cromatografia moderna Mikhail Tsweett (1872-1919) Botânico russo: usou uma coluna empacotada contendo carbonato de cálcio como fase estacionária para
INTRODUÇÃO A MÉTODOS CROMATOGRÁFICOS 1 Histórico da cromatografia moderna Mikhail Tsweett (1872-1919) Botânico russo: usou uma coluna empacotada contendo carbonato de cálcio como fase estacionária para
Oxidação térmica e processos PECVD
 5 Oxidação térmica e processos PECVD 2012 5.1. Introdução Contexto (das aulas) Contexto (nosso processo) 5.2. Oxidação Térmica do Silício 5.3. Deposição de SiO 2 por PECVD 1 Contexto da aula Obtenção de
5 Oxidação térmica e processos PECVD 2012 5.1. Introdução Contexto (das aulas) Contexto (nosso processo) 5.2. Oxidação Térmica do Silício 5.3. Deposição de SiO 2 por PECVD 1 Contexto da aula Obtenção de
PMT AULAS 1 E 2 Augusto Camara Neiva. PMT Augusto Neiva
 PMT3130 2017 - AULAS 1 E 2 Augusto Camara Neiva 1 2 3 4 AS AULAS NÃO SEGUIRÃO LINEARMENTE A APOSTILA HOJE: ELETROQUÍMICA 5 MOLÉCULA DE ÁGUA A molécula de água é polar e, portanto, a água pode alojar íons
PMT3130 2017 - AULAS 1 E 2 Augusto Camara Neiva 1 2 3 4 AS AULAS NÃO SEGUIRÃO LINEARMENTE A APOSTILA HOJE: ELETROQUÍMICA 5 MOLÉCULA DE ÁGUA A molécula de água é polar e, portanto, a água pode alojar íons
ELETRODO OU SEMIPILHA:
 ELETROQUÍMICA A eletroquímica estuda a corrente elétrica fornecida por reações espontâneas de oxirredução (pilhas) e as reações não espontâneas que ocorrem quando submetidas a uma corrente elétrica (eletrólise).
ELETROQUÍMICA A eletroquímica estuda a corrente elétrica fornecida por reações espontâneas de oxirredução (pilhas) e as reações não espontâneas que ocorrem quando submetidas a uma corrente elétrica (eletrólise).
Volumetria de Óxido-redução
 Volumetria de Óxido-redução LMBRANDO Reações de Oxi-redução Oxidação e redução 0 0 +1-1 0 0 +1-1 Reações redox e semi-células Zn 0 + Cu 2+ Zn 2+ + Cu 0 semi-célula do zinco: Zn 0 Zn 2+ + 2e - semi-célula
Volumetria de Óxido-redução LMBRANDO Reações de Oxi-redução Oxidação e redução 0 0 +1-1 0 0 +1-1 Reações redox e semi-células Zn 0 + Cu 2+ Zn 2+ + Cu 0 semi-célula do zinco: Zn 0 Zn 2+ + 2e - semi-célula
2. POLAROGRAFIA 2.1 CONCEITOS GERAIS
 2. POLAROGRAFIA 2.1 CONCEITOS GERAIS A eletroanalítica é um ramo do conhecimento da química em que são estabelecidas relações diretas entre as concentrações do analito e alguma propriedade elétrica como
2. POLAROGRAFIA 2.1 CONCEITOS GERAIS A eletroanalítica é um ramo do conhecimento da química em que são estabelecidas relações diretas entre as concentrações do analito e alguma propriedade elétrica como
Minicurso: Medição de ph e Íons por Potenciometria
 Minicurso: por Potenciometria Instrutor: Nilton Pereira Alves São José dos Campos 29/05/2010 1/37 Instrutor: Nilton Pereira Alves Técnico químico ECOMPO SJC - SP Bacharel em Química Oswaldo Cruz SP Mestre
Minicurso: por Potenciometria Instrutor: Nilton Pereira Alves São José dos Campos 29/05/2010 1/37 Instrutor: Nilton Pereira Alves Técnico químico ECOMPO SJC - SP Bacharel em Química Oswaldo Cruz SP Mestre
HIDROMETALURGIA E ELETROMETALURGIA. Prof. Carlos Falcão Jr.
 HIDROMETALURGIA E ELETROMETALURGIA Prof. Carlos Falcão Jr. de um sólido em fase aquosa natureza do sólido (iônico, covalente ou metálico) processo: físico químico eletroquímico de redução eletrolítico
HIDROMETALURGIA E ELETROMETALURGIA Prof. Carlos Falcão Jr. de um sólido em fase aquosa natureza do sólido (iônico, covalente ou metálico) processo: físico químico eletroquímico de redução eletrolítico
Eletroquímica. Condutometria
 Eletroquímica Condutometria Tipos de métodos eletroanalíticos Métodos Eletroanalíticos Métodos Interfaciais Métodos Não-Interfaciais Estáticos Dinâmicos Condutometria Titulações Condutométricas Potenciometria
Eletroquímica Condutometria Tipos de métodos eletroanalíticos Métodos Eletroanalíticos Métodos Interfaciais Métodos Não-Interfaciais Estáticos Dinâmicos Condutometria Titulações Condutométricas Potenciometria
Cinética Química. Prof. Alex Fabiano C. Campos. Rapidez Média das Reações
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
INTRODUÇÃO À ELETROQUÍMICA Prof. Dr. Patricio R. Impinnisi Departamento de engenharia elétrica UFPR
 INTRODUÇÃO À ELETROQUÍMICA Prof. Dr. Patricio R. Impinnisi Departamento de engenharia elétrica UFPR REAÇÕES ELETROQUÍMICAS Vamos inicialmente estudar estes sistemas para identificar os princípios fundamentais
INTRODUÇÃO À ELETROQUÍMICA Prof. Dr. Patricio R. Impinnisi Departamento de engenharia elétrica UFPR REAÇÕES ELETROQUÍMICAS Vamos inicialmente estudar estes sistemas para identificar os princípios fundamentais
CONSELHO REGIONAL DE QUÍMICA - IV REGIÃO (SP)
 CONSELHO REGIONAL DE QUÍMICA - IV REGIÃO (SP) Medição de ph e íons por potenciometria Ministrante: Nilton Pereira Alves Quimlab Química Contatos: [email protected] Apoio São José dos Campos, 29 de
CONSELHO REGIONAL DE QUÍMICA - IV REGIÃO (SP) Medição de ph e íons por potenciometria Ministrante: Nilton Pereira Alves Quimlab Química Contatos: [email protected] Apoio São José dos Campos, 29 de
Transporte Iônico e o Potencial de Membrana
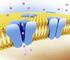 Transporte Iônico e o Potencial de Membrana Até o momento, consideramos apenas o transporte de solutos neutros (sem carga elétrica) através da membrana celular. A partir de agora, vamos passar a estudar
Transporte Iônico e o Potencial de Membrana Até o momento, consideramos apenas o transporte de solutos neutros (sem carga elétrica) através da membrana celular. A partir de agora, vamos passar a estudar
FLOCULAÇÃO E DISPERSÃO DAS ARGILAS
 1 FLOCULAÇÃO E DISPERSÃO DAS ARGILAS PROF. GILSON MOURA FILHO/SER/UFAL CURSO DE PÓSGRADUAÇÃO EM AGRONOMIA DISCIPLINA: FÍSICA DO SOLO 1. FORÇAS E ENERGIA NO SISTEMA SOLOÁGUA Forças de coesão e adesão Forças
1 FLOCULAÇÃO E DISPERSÃO DAS ARGILAS PROF. GILSON MOURA FILHO/SER/UFAL CURSO DE PÓSGRADUAÇÃO EM AGRONOMIA DISCIPLINA: FÍSICA DO SOLO 1. FORÇAS E ENERGIA NO SISTEMA SOLOÁGUA Forças de coesão e adesão Forças
INTRODUÇÃO À ELETROQUÍMICA Prof. Dr. Patricio R. Impinnisi Departamento de engenharia elétrica UFPR
 INTRODUÇÃO À ELETROQUÍMICA Prof. Dr. Patricio R. Impinnisi Departamento de engenharia elétrica UFPR REAÇÕES ELETROQUÍMICAS Uma reação eletroquímica é um processo químico heterogêneo (que envolve uma interface
INTRODUÇÃO À ELETROQUÍMICA Prof. Dr. Patricio R. Impinnisi Departamento de engenharia elétrica UFPR REAÇÕES ELETROQUÍMICAS Uma reação eletroquímica é um processo químico heterogêneo (que envolve uma interface
Eletrodo redox. Eletrodos construídos com metais inertes: platina, ouro, paládio. do sistema de óxido-redução presente na solução.
 Eletrodo redox Para sistemas de óxido-redução. Eletrodos construídos com metais inertes: platina, ouro, paládio Atuam como fontes ou depósito de elétrons transferidos a partir do sistema de óxido-redução
Eletrodo redox Para sistemas de óxido-redução. Eletrodos construídos com metais inertes: platina, ouro, paládio Atuam como fontes ou depósito de elétrons transferidos a partir do sistema de óxido-redução
O refrigerante normal por possuir açúcar em sua composição apresenta uma maior massa, logo possuindo uma maior uma maior densidade. Lembrando d = m/v.
 26 A O refrigerante normal por possuir açúcar em sua composição apresenta uma maior massa, logo possuindo uma maior uma maior densidade. Lembrando d = m/v. 27 D I Errada. Na mesma temperatura o liquido
26 A O refrigerante normal por possuir açúcar em sua composição apresenta uma maior massa, logo possuindo uma maior uma maior densidade. Lembrando d = m/v. 27 D I Errada. Na mesma temperatura o liquido
REAÇÕES QUÍMICAS PRODUZINDO CORRENTE ELÉTRICA CORRENTE ELÉTRICA PRODUZINDO REAÇÃO QUÍMICA PROF. RODRIGO BANDEIRA
 REAÇÕES QUÍMICAS PRODUZINDO CORRENTE ELÉTRICA CORRENTE ELÉTRICA PRODUZINDO REAÇÃO QUÍMICA A relação entre as reações químicas e a corrente elétrica é estudada por um ramo da química chamado ELETROQUÍMICA
REAÇÕES QUÍMICAS PRODUZINDO CORRENTE ELÉTRICA CORRENTE ELÉTRICA PRODUZINDO REAÇÃO QUÍMICA A relação entre as reações químicas e a corrente elétrica é estudada por um ramo da química chamado ELETROQUÍMICA
AULA DE RECUPERAÇÃO PROF. NEIF NAGIB
 AULA DE RECUPERAÇÃO PROF. NEIF NAGIB ELETROQUÍMICA Estuda os fenômenos envolvidos na produção de corrente elétrica a partir da transferência de elétrons em reações de óxido-redução, e a utilização de corrente
AULA DE RECUPERAÇÃO PROF. NEIF NAGIB ELETROQUÍMICA Estuda os fenômenos envolvidos na produção de corrente elétrica a partir da transferência de elétrons em reações de óxido-redução, e a utilização de corrente
Química Geral e Inorgânica. QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin. Eletroquímica
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Eletroquímica Reações Redox Reações onde ocorre a transferência de elétrons entre átomos Fluxo de elétrons
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Eletroquímica Reações Redox Reações onde ocorre a transferência de elétrons entre átomos Fluxo de elétrons
Reações químicas aplicas ao processamento de materiais cerâmicos
 Reações químicas aplicas ao processamento de materiais cerâmicos Em vários casos, no processo de fabricação de peças cerâmicas, as reações entre os diferentes constituintes dos corpos cerâmicos são interrompidas
Reações químicas aplicas ao processamento de materiais cerâmicos Em vários casos, no processo de fabricação de peças cerâmicas, as reações entre os diferentes constituintes dos corpos cerâmicos são interrompidas
Físico-Química I. Profa. Dra. Carla Dalmolin. Misturas Simples. Termodinâmica das Misturas Propriedades das Soluções Atividade
 Físico-Química I Profa. Dra. Carla Dalmolin Misturas Simples Termodinâmica das Misturas Propriedades das Soluções Atividade Misturas Simples Misturas de substâncias que não reagem Modelo simples para posteriormente
Físico-Química I Profa. Dra. Carla Dalmolin Misturas Simples Termodinâmica das Misturas Propriedades das Soluções Atividade Misturas Simples Misturas de substâncias que não reagem Modelo simples para posteriormente
Estudo das reações químicas para geração de energia.
 Estudo das reações químicas para geração de energia. Células Galvânicas (Pilhas e Baterias): Conversão de Energia Química em Energia Elétrica (Reações Espontâneas) Células Eletrolíticas: Conversão de Energia
Estudo das reações químicas para geração de energia. Células Galvânicas (Pilhas e Baterias): Conversão de Energia Química em Energia Elétrica (Reações Espontâneas) Células Eletrolíticas: Conversão de Energia
Células eletrolíticas são mecanismos que provocam uma reação não espontânea de oxi-redução pelo fornecimento de energia elétrica ELETRÓLISE ÍGNEA
 ELETRÓLISE Células eletrolíticas são mecanismos que provocam uma reação não espontânea de oxi-redução pelo fornecimento de energia elétrica ELETRÓLISE ÍGNEA É o processo de decomposição de uma substância
ELETRÓLISE Células eletrolíticas são mecanismos que provocam uma reação não espontânea de oxi-redução pelo fornecimento de energia elétrica ELETRÓLISE ÍGNEA É o processo de decomposição de uma substância
CQ110 : Princípios de FQ
 Fenômenos de Interface Devido às diferentes interações, as moléculas superficiais possuem uma maior energia, dessa forma, para deslocar uma molécula do interior do sistema para sua superfície, uma energia
Fenômenos de Interface Devido às diferentes interações, as moléculas superficiais possuem uma maior energia, dessa forma, para deslocar uma molécula do interior do sistema para sua superfície, uma energia
E cel = E catodo - E anodo E cel = 0,337 ( 0,763) E cel = 1,100 V. ZnSO 4(aq) 1,0 mol L -1 CuSO 4(aq) 1,0 mol L -1
 QMC5351 Química Analítica Instrumental POTENCIOMETRIA Análise Potenciométrica Conceitos Iniciais CÉLULA ELETROQUÍMICA sistema onde dois eletrodos, cada um deles imerso em uma solução eletrolítica (interligadas
QMC5351 Química Analítica Instrumental POTENCIOMETRIA Análise Potenciométrica Conceitos Iniciais CÉLULA ELETROQUÍMICA sistema onde dois eletrodos, cada um deles imerso em uma solução eletrolítica (interligadas
ELETROQUÍMICA. paginapessoal.utfpr.edu.br/lorainejacobs. Profª Loraine Jacobs DAQBI
 ELETROQUÍMICA [email protected] paginapessoal.utfpr.edu.br/lorainejacobs Profª Loraine Jacobs DAQBI CORRENTE ELÉTRICA Pode ser produzida por: Geradores elétricos : Transformam energia mecânica
ELETROQUÍMICA [email protected] paginapessoal.utfpr.edu.br/lorainejacobs Profª Loraine Jacobs DAQBI CORRENTE ELÉTRICA Pode ser produzida por: Geradores elétricos : Transformam energia mecânica
MÉTODOS COULOMÉTRICOS
 MÉTODOS COULOMÉTRICOS São realizados por meio da medida de quantidade de carga elétrica requerida para converter uma amostra de um analito quantitativamente a um diferente estado de oxidação. A coulometria
MÉTODOS COULOMÉTRICOS São realizados por meio da medida de quantidade de carga elétrica requerida para converter uma amostra de um analito quantitativamente a um diferente estado de oxidação. A coulometria
3. Origem das cargas elétricas no solo
 3. Origem das cargas elétricas no solo 3.1. Origem das cargas elétricas Há no solo, em geral, predominância de cargas negativas sobre positivas. Essa predominância, bastante significativa em solos de regiões
3. Origem das cargas elétricas no solo 3.1. Origem das cargas elétricas Há no solo, em geral, predominância de cargas negativas sobre positivas. Essa predominância, bastante significativa em solos de regiões
Catálise heterogênea. Catalisador sólido. Reação na interface sólido-fluido
 Catálise heterogênea Catalisador sólido Reação na interface sólido-fluido Tipos de catalisadores Poroso: elevada área superficial Tipos de catalisadores Peneiras moleculares: capacidade de distinção entre
Catálise heterogênea Catalisador sólido Reação na interface sólido-fluido Tipos de catalisadores Poroso: elevada área superficial Tipos de catalisadores Peneiras moleculares: capacidade de distinção entre
MOVIMENTO DE ÁTOMOS E IONS NOS MATERIAIS DIFUSÃO
 Prof. Júlio César Giubilei Milan UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE ENGENHARIA MECÂNICA MOVIMENTO DE ÁTOMOS E IONS NOS MATERIAIS DIFUSÃO CMA CIÊNCIA
Prof. Júlio César Giubilei Milan UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE ENGENHARIA MECÂNICA MOVIMENTO DE ÁTOMOS E IONS NOS MATERIAIS DIFUSÃO CMA CIÊNCIA
APLICAÇÕES DOS POTENCIAIS PADRÃO DE ELETRODO
 APLICAÇÕES DOS POTENCIAIS PADRÃO DE ELETRODO POTENCIAL TERMODINÂMICO! definido como o potencial do catodo menos o potencial do anodo (semi-reações escritas como redução; despreza queda ôhmica e potencial
APLICAÇÕES DOS POTENCIAIS PADRÃO DE ELETRODO POTENCIAL TERMODINÂMICO! definido como o potencial do catodo menos o potencial do anodo (semi-reações escritas como redução; despreza queda ôhmica e potencial
Cinética eletroquímica
 Cinética eletroquímica Parte 1 Até agora falamos em potencial de equilíbrio: isto é termodinâmica. Agora vamos nos preocupar com velocidades... Em uma reação eletroquímica em equilíbrio tem-se: A + ze
Cinética eletroquímica Parte 1 Até agora falamos em potencial de equilíbrio: isto é termodinâmica. Agora vamos nos preocupar com velocidades... Em uma reação eletroquímica em equilíbrio tem-se: A + ze
Difusão em Sólidos TM229 - DEMEC Prof Adriano Scheid
 Difusão em Sólidos TM229 - DEMEC Prof Adriano Scheid O que é Difusão? É o fenômeno de transporte de material pelo movimento de átomos. Importância? Diversas reações e processos que ocorrem nos materiais
Difusão em Sólidos TM229 - DEMEC Prof Adriano Scheid O que é Difusão? É o fenômeno de transporte de material pelo movimento de átomos. Importância? Diversas reações e processos que ocorrem nos materiais
RT ln zf. Reações Eletroquímicas Equilíbrio. Equação de Nernst. ox, rev. Constantes úteis:
 Reações Eletroquímicas Equilíbrio Constantes úteis: Equação de Nernst ou: ou: R = 8,621 x 10-5 ev/k ; T = 25ºC = 298 K ; ln x = 2,303 log x 1F = 1 ev/v R = 8,314510 J/mol.K 1F = 96485 C R = 1,987 cal/mol.k
Reações Eletroquímicas Equilíbrio Constantes úteis: Equação de Nernst ou: ou: R = 8,621 x 10-5 ev/k ; T = 25ºC = 298 K ; ln x = 2,303 log x 1F = 1 ev/v R = 8,314510 J/mol.K 1F = 96485 C R = 1,987 cal/mol.k
LCE0182 Química Analítica Quantitativa. Informações Gerais. Wanessa Melchert Mattos.
 LCE0182 Química Analítica Quantitativa Informações Gerais Wanessa Melchert Mattos [email protected] Aprovação Para que o aluno possa ser aprovado exige-se média mínima de 5,0 em notas e 70% de frequência
LCE0182 Química Analítica Quantitativa Informações Gerais Wanessa Melchert Mattos [email protected] Aprovação Para que o aluno possa ser aprovado exige-se média mínima de 5,0 em notas e 70% de frequência
Exercício de Revisão III Unidade. Eletroquímica
 1 Exercício de Revisão III Unidade Eletroquímica 1) O que difere uma célula galvânica e uma célula eletrolítica? 2) Considere a pilha: Zn(s)/Zn 2+ // Ag + /Ag(s) a) Proponha um esquema de funcionamento
1 Exercício de Revisão III Unidade Eletroquímica 1) O que difere uma célula galvânica e uma célula eletrolítica? 2) Considere a pilha: Zn(s)/Zn 2+ // Ag + /Ag(s) a) Proponha um esquema de funcionamento
Cinética Química. Prof. Alex Fabiano C. Campos
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Aula EQUILÍBRIO DE OXIDAÇÃO E REDUÇÃO METAS
 EQUILÍBRIO DE OXIDAÇÃO E REDUÇÃO METAS Apresentar a definição de oxidação e redução; apresentar a definição e classificação de celula eletroquímica; apresentar a equação de nernst; apresentar outros equilíbrios
EQUILÍBRIO DE OXIDAÇÃO E REDUÇÃO METAS Apresentar a definição de oxidação e redução; apresentar a definição e classificação de celula eletroquímica; apresentar a equação de nernst; apresentar outros equilíbrios
TIPOS DE MÉTODOS ELETROANALÍTICOS
 CONDUTOMETRIA TIPOS DE MÉTODOS ELETROANALÍTICOS CONDUTOMETRIA Baseia-se em medições de condutância das soluções iônicas(seio da solução). A condução de eletricidade através das soluções iônicas é devida
CONDUTOMETRIA TIPOS DE MÉTODOS ELETROANALÍTICOS CONDUTOMETRIA Baseia-se em medições de condutância das soluções iônicas(seio da solução). A condução de eletricidade através das soluções iônicas é devida
Primeira Lista de Exercícios de Biofísica II. c n
 Primeira Lista de Exercícios de Biofísica II 1. Considere uma célula composta por um corpo celular ao qual está preso um longo e fino processo tubular (por exemplo, o axônio de um neurônio ou o flagelo
Primeira Lista de Exercícios de Biofísica II 1. Considere uma célula composta por um corpo celular ao qual está preso um longo e fino processo tubular (por exemplo, o axônio de um neurônio ou o flagelo
QUI109 QUÍMICA GERAL (Ciências Biológicas) 3ª aula /
 QUI109 QUÍMICA GERAL (Ciências Biológicas) 3ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) Massa / Mol Massa é uma medida invariável da quantidade de matéria
QUI109 QUÍMICA GERAL (Ciências Biológicas) 3ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) Massa / Mol Massa é uma medida invariável da quantidade de matéria
ESTUDO ELETROANALÍTICO DO CARRAPATICIDA FIPRONIL PELA TÉCNICA DE VOLTAMETRIA CÍCLICA. Resumo 800
 ESTUDO ELETROANALÍTICO DO CARRAPATICIDA FIPRONIL PELA TÉCNICA DE VOLTAMETRIA CÍCLICA Resumo 800 Este trabalho objetivou a caracterização eletroquímica do carrapaticida fipronil, por meio da técnica de
ESTUDO ELETROANALÍTICO DO CARRAPATICIDA FIPRONIL PELA TÉCNICA DE VOLTAMETRIA CÍCLICA Resumo 800 Este trabalho objetivou a caracterização eletroquímica do carrapaticida fipronil, por meio da técnica de
INTRODUÇÃO À ELETROQUÍMICA
 QFL0230 2014 INTRODUÇÃO À ELETROQUÍMICA REAÇÕES DE OXIDAÇÃOREDUÇÃO (REDOX)! transferência de e de um reagente para o outro Ce 4+ + Fe 2+ D Ce 3+ + Fe 3+ SEMIREAÇÕES: e Ce 4+ + 1 e D Ce 3+, redução agente
QFL0230 2014 INTRODUÇÃO À ELETROQUÍMICA REAÇÕES DE OXIDAÇÃOREDUÇÃO (REDOX)! transferência de e de um reagente para o outro Ce 4+ + Fe 2+ D Ce 3+ + Fe 3+ SEMIREAÇÕES: e Ce 4+ + 1 e D Ce 3+, redução agente
Exercício 3) A formação de cargas elétrica em objetos quotidianos é mais comum em dias secos ou úmidos? Justifique a sua resposta.
 Exercícios Parte teórica Exercício 1) Uma esfera carregada, chamada A, com uma carga 1q, toca sequencialmente em outras 4 esferas (B, C, D e E) carregadas conforme a figura abaixo. Qual será a carga final
Exercícios Parte teórica Exercício 1) Uma esfera carregada, chamada A, com uma carga 1q, toca sequencialmente em outras 4 esferas (B, C, D e E) carregadas conforme a figura abaixo. Qual será a carga final
Voltametria Ciclica: Fundamentos Básicos e Aplicações
 Voltametria Ciclica: Fundamentos Básicos e Aplicações rof. Alzir Azevedo Batista Universidade Federal de São Carlos - Brasil Introdução A técnica de voltametria c cclica é mais própria para fins qualitativos
Voltametria Ciclica: Fundamentos Básicos e Aplicações rof. Alzir Azevedo Batista Universidade Federal de São Carlos - Brasil Introdução A técnica de voltametria c cclica é mais própria para fins qualitativos
CATÁLISE ENZIMÁTICA. CINÉTICA Controle da velocidade de reações. CINÉTICA Equilíbrio e Estado Estacionário
 CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
