3.Métodos Físicos de Separação
|
|
|
- Malu de Sousa Varejão
- 10 Há anos
- Visualizações:
Transcrição
1 3.Métodos Físicos de Separação Mestrado em Química para o Ensino 55
2 Mestrado em Química para o Ensino 56
3 3.Métodos Físicos de Separação 3.1. Substâncias e Misturas de Substâncias A classificação da matéria é uma primeira etapa para se perceber em que medida o tipo de matéria vai condicionar a sua aplicação e utilização no quotidiano, inclusivamente nos processos físicos de separação. Para os químicos, a classificação dos materiais tendo em conta a sua composição é muito importante. O esquema representado na figura 3.1 resume, de modo geral, a classificação da matéria de acordo com a composição química. Matéria Sim Não É uniforme Mistura homogénea Sim Pode ser separada por processos físicos? Não Substância pura Mistura heterogénea Substância Composta Sim Pode ser decomposta em componentes mais simples por processos químicos? Não Substância Elementar Fig 3. 1-Classificação da matéria (adaptado de: Reger Daniel et. al, Química: Princípios e Aplicações; 1997) Mestrado em Química para o Ensino 57
4 Tal como se observa na Figura 2.5, a matéria divide-se em substâncias puras e misturas. A grande maioria dos materiais que nos rodeiam são misturas de substâncias. Uma mistura é então a matéria que é constituída por duas ou mais substâncias em proporções que podem variar e sem que entre essas substâncias exista qualquer tipo de interacção química. As misturas são constituídas por componentes com propriedades físicas distintas, podendo, deste modo, proceder-se à sua separação. É frequente que quando duas substâncias entram em contacto possam reagir quimicamente. Quando tal acontece, o resultado não é uma mistura, mas uma nova substância que se formou por reacção química, que apresentará novas características, perdendo as suas características iniciais. Um outro conceito que surge em oposição às misturas é substância. Habitualmente designa-se por substância uma amostra que não pode ser separada nos seus diversos constituintes por processos físicos. Em química a utilização do conceito substância está associado a pureza. Em determinados casos é fácil identificar e classificar uma amostra como sendo uma mistura. No entanto, em outros casos é necessário recorrer a equipamentos por vezes complexos e a um exame cuidadoso de modo a classificar a amostra em substância. (Reger; Goode; Mercer; 1997) Classificação de misturas A maior parte da matéria que encontramos no nosso dia-a-dia é composta por uma mistura de substâncias. É importante referir que os componentes das misturas assumem uma variedade de dimensões e como tal é possível efectuar a distinção entre misturas homogéneas e heterogéneas, figura 2.6, de acordo com a uniformidade ou não, em toda a sua extensão. Misturas de substâncias Heterogéneas Homogéneas Fig Classificação das misturas Mestrado em Química para o Ensino 58
5 Uma mistura homogénea é aquela que apresenta o mesmo aspecto ( homo = igual ) não sendo possível efectuar a distinção dos seus componentes existindo uma única fase. Uma mistura heterogénea é uma mistura que apresenta aspecto diferente ao longo da sua extensão ( hetero = diferente ) sendo possível distinguir alguns ou até mesmo todos os componentes de uma mistura à vista desarmada. Os componentes encontram-se em pelo menos duas fases. É possível identificar ainda um outro tipo de mistura que se designa por mistura coloidal. Esta mistura é por vezes confundida com as misturas homogéneas, no entanto a sua observação detalhada ao microscópio permite inseri-la mais proximamente das misturas heterogéneas. São misturas que estão no limite entre o homogéneo e o heterogéneo. Por vezes não é fácil determinar se uma amostra é ou não uma mistura e como tal a identificação e análise é uma sequência de testes baseados nas propriedades que as substâncias apresentam. Estas propriedades são divididas em três grandes grupos: propriedades organolépticas, físicas e químicas. Propriedades organolépticas são aquelas que impressionam os sentidos, como a cor, odor, sabor, aspecto sentido pelo tacto e timbre (estas duas últimas propriedades são pouco significativas para a identificação). Propriedades físicas são aquelas que envolvem interacções da matéria com a energia, sendo específicas (características de um único tipo de matéria) desde que o material seja puro. As propriedades físicas podem ser: ponto de fusão, ponto de ebulição, densidade, calor especifico e dureza. Propriedades químicas relativas às transformações da matéria: neutralização, fotólise, solubilidade, pirólise, oxidação-redução, acção sobre indicadores. A observação dos componentes de uma mistura pode ser efectuada de maneiras distintas tais como a observação ao microscópio ou à vista desarmada. A utilização de processos indirectos é também muitas vezes utilizada, através de vários procedimentos experimentais. Estes procedimentos permitem distinguir misturas de substâncias puras. Um procedimento comum diz respeito às substâncias puras, que apresentam pontos de fusão e de ebulição constantes. No entanto, é necessário cuidado pois existem casos de misturas em que os mesmos também se verificam, como é o caso das misturas eutéticas (ponto de fusão constante) ou misturas azeotrópicas (ponto de ebulição constante). Mestrado em Química para o Ensino 59
6 Classificação de substâncias. As substâncias puras podem ainda dividir-se em substâncias compostas e elementares. As substâncias compostas são constituídas por mais do que uma espécie química como é o caso da água, cuja constituição é o hidrogénio e o oxigénio. As substâncias elementares têm na sua constituição uma única espécie química, tal como o caso do oxigénio. Substâncias Elementares Compostas Apresentam unidades estruturais: átomos ou moléculas que em conjunto com outras iguais formam a substância. Compostos moleculares: unidade estrutural é a molécula, e resulta da combinação química de elementos diferentes, e em conjunto com outras formam a substância Compostos iónicos: a unidade estrutural é o menor conjunto de iões, electricamente neutro. Fig Classificação de substâncias Mestrado em Química para o Ensino 60
7 3.2. Técnicas de Separação e Purificação Muitas das substâncias puras que existem na natureza só se encontram sob a forma de misturas e como tal é necessário proceder à sua separação, pois a obtenção de substâncias com grau de pureza elevado é muito importante. Existe uma grande variedade de métodos que permitem realizar a separação dos componentes de uma mistura homogénea e heterogénea. A seguir apresentam-se os métodos de separação mais utilizados e de que modo são aplicados a misturas. A utilização de cada uma destas técnicas envolve a manutenção das propriedades que caracterizam as substâncias. A escolha da técnica depende das características e do estado físico dos constituintes que fazem parte da mistura (Reger; Goode; Mercer; 1997). Relativamente às separações de misturas heterogéneas deve-se ter em atenção que estas misturas têm várias fases que podem estar em diferentes estados físicos. Se a mistura que se pretende separar for constituída por uma ou mais fases sólidas as técnicas devem estar de acordo com as características dos componentes. É importante ter em atenção também a finalidade da separação Misturas heterogéneas Para estas misturas as técnicas de separação são específicas e como tal descrevem-se seguidamente: I Separação de componentes sólidos de uma mistura sólida Caso o componente que constitui a mistura tenha propriedades magnéticas pode utilizar-se para efectuar uma separação magnética (Fig 3.4). Esta técnica permite separar materiais que são atraídos por ímanes. Este tipo de técnica é frequentemente utilizado na indústria química para separar o ferro de outros metais. Mestrado em Química para o Ensino 61
8 Fig Separação magnética (Extraído de Nunes; Cruz; Acção (Re) Acção; 2006) Uma outra técnica que permite separar componentes sólidos é a peneiração. Este procedimento tem em consideração as dimensões do material sólido. É possível utilizando peneiras cuja estrutura é uma rede fina com malhas que variam de acordo com o tamanho do produto a separar. Uma das aplicações desta técnica ressalta no dia-a-dia na construção civil e na indústria da panificação. Uma outra técnica frequentemente utilizada é a sublimação que apenas é possível quando um dos componentes da mistura sublima facilmente como é o caso do iodo, gelo seco ou naftaleno. II Separação de um sólido insolúvel de uma mistura sólido líquido Decantação é a técnica frequentemente utilizada para se separar um sólido depositado no fundo de um recipiente que contém um líquido. O sólido é denominado sedimento. O líquido é cuidadosa e lentamente transferido para um outro copo com a ajuda de uma vareta, tal como é possível observar na figura 3.5. Mestrado em Química para o Ensino 62
9 Fig Decantação (Extraído de Nunes, N.; Cruz.A.C.; Acção (Re) Acção; 2006) III Separação de partículas sólidas insolúveis num líquido ou numa solução A separação de partículas em suspensão pode ser efectuada recorrendo a uma filtração. Das várias técnicas de filtração é de referir a filtração por gravidade e a filtração a pressão reduzida. Filtração por gravidade Este tipo de filtração ocorre devido ao efeito da gravidade sobre a mistura que se pretende separar. A mistura deve ser constituída por uma fase sólida e uma fase líquida. Deve fazer-se passar a mistura por uma barreira porosa que habitualmente é o papel de filtro (mas também podendo ser utilizados outros materiais que permitam reter as partículas sólidas). O filtro servirá para reter as partículas sólidas. Estas partículas adquirem o nome de resíduo, enquanto que a mistura líquida que contém partículas de menor dimensão atravessa o papel de filtro formando o filtrado. Um dos problemas desta técnica é a obstrução do filtro pelas pequenas partículas bem como a elevada viscosidade (Reger; Goode; Mercer; 1997). Nesta técnica é importante a preparação do papel de filtro. O tamanho do filtro deve ser o mais adequado à quantidade de sólido que se pretende separar, não devendo ocupar mais de 1/3 da capacidade do papel de filtro, para que seja possível efectuar a lavagem do mesmo posteriormente. Os filtros preparados podem ser de pregas ou lisos. Os filtros de pregas são os mais indicados quando se pretende recolher o líquido, pois têm maior área e maior Mestrado em Química para o Ensino 63
10 velocidade de filtração. Os filtros lisos são mais utilizados quando pretendemos recolher o resíduo sólido. Após a preparação o papel deve adaptar-se ao funil, devendo molhar-se com o solvente. Este procedimento permite a minimização das perdas e maior aderência do papel ao funil. Filtração a pressão reduzida Este tipo de filtração é utilizada quando se pretende efectuar uma filtração mais rápida que a anterior ou então quando as partículas sólidas da mistura apresentam dimensões muito pequenas. Para a realização desta filtração é necessário utilizar um Kitasato, um funil de Büchner e uma bomba de vácuo. Deverá colocar-se entre a trompa de vácuo e o recipiente de recolha de filtrado um segundo Kitasato como segurança, evitando a entrada de água no filtrado caso ocorram variações de pressão. Após efectuado o vácuo no sistema, o sistema aspira a mistura, obrigando o líquido a passar através do filtro. As partículas sólidas ficam retidas no papel de filtro. Deve ter-se o cuidado de só desligar o sistema de vácuo quando se fizer entrar ar no sistema através do Kitasato de segurança. Centrifugação Tal como foi dito anteriormente, depois de se efectuar uma filtração ficam partículas de pequenas dimensões em solução, que devem ser separadas utilizando para tal uma outra técnica que se denomina centrifugação. O processo baseia-se na utilização de uma centrifugadora (manual ou mais sofisticada) onde se colocam vários tubos de ensaio, que rodam a alta velocidade (Fig 3.6). A separação é efectuada entre partículas de massa diferente. Formam-se depósitos de sólidos no fundo dos tubos de ensaio, separando-se o líquido por decantação. Este processo pode também ser utilizado para separar componentes de misturas coloidais. Mestrado em Química para o Ensino 64
11 Fig Centrifugação (Extraído de Nunes; Cruz; Acção (Re) Acção; 2006) IV Separação de líquidos imiscíveis A técnica que permite a separação de dois ou mais líquidos imiscíveis designa-se decantação em funil. A mistura é colocada num funil de decantação, de modo que as diferentes camadas se separem. Inicialmente é recolhido o líquido que apresenta maior densidade (que é o líquido da camada inferior) para um gobelé. Um exemplo comum em que pode ser utilizado este tipo de separação é a mistura água / azeite (Fig 3.7). Fig Decantação em funil (Extraído de Nunes; Cruz; Acção (Re) Acção; 2006) Mestrado em Química para o Ensino 65
12 Misturas homogéneas I Separação de um soluto de uma solução Para a recuperação de um sólido (soluto) que se encontra dissolvido numa solução pode recorrer-se à ebulição do solvente, que consiste em levar à ebulição o solvente, passando este para o estado gasoso. A sua utilização pode ser por exemplo para separar o cloreto de sódio de uma solução aquosa de cloreto de sódio. Uma outra técnica de separação de um sólido dissolvido numa solução saturada é a cristalização. Esta técnica consiste em deixar evaporar lentamente o solvente à temperatura ambiente, obtendo-se os cristais do sólido que se pretende recuperar. É uma técnica habitualmente utilizada nas salinas para obtenção do sal a partir da água do mar. II Separação de diferentes solutos de uma solução Existem técnicas que se baseiam nas diferenças de afinidade para outros materiais, essas diferenças manifestam-se no dia-a-dia por exemplo nas manchas na roupa provocadas pelos diversos alimentos (Reger, D., Goode, S., Mercer, E.; 1997). Estas manchas são removíveis com níveis de dificuldade diferentes, dependendo da constituição do alimento. O princípio de remoção assenta na técnica de separação designada por cromatografia. A cromatografia surge no mundo da química como uma poderosa técnica e é frequentemente utilizada. Esta técnica utiliza dois materiais: um estacionário e o outro em movimento, designados respectivamente por fase estacionária e fase móvel. A fundamentação da técnica assenta na migração diferencial dos componentes de uma mistura, como consequência da interacção das duas fases imiscíveis. A cromatografia pode ser utilizada na identificação de compostos, efectuando comparação com outros padrões, ou para purificação de compostos, separando os componentes de misturas. Existem diversos tipos de cromatografia, podendo esta ser em papel, cromatografia em camada fina (CCD), cromatografia gasosa (CG) e cromatografia líquida de alta eficiência (HPLC). A escolha do tipo de cromatografia depende do material que se pretende separar. Mestrado em Química para o Ensino 66
13 De entre todos os tipos de cromatografia o mais simples é a cromatografia em papel. O papel representará a fase estacionária (aquosa, uma vez que o papel apresenta na sua constituição moléculas de celulose) e a fase móvel é o solvente orgânico. A mistura é colocada na zona inferior do pedaço de papel e a extremidade por sua vez imersa na fase líquida móvel. À medida que a fase móvel se desloca sobre a fase estacionária os componentes serão arrastados de acordo com a afinidade, tal como se observa na figura 3.8, ou seja, os componentes que não são fortemente atraídos para o papel são arrastados com o líquido enquanto que os que são fortemente atraídos pelo papel movem-se mais lentamente o que provocará a separação (Ibid, 1997, p.27). Fig Cromatografia em papel (Extraído de Reger Daniel et. al, Química: Princípios e Aplicações; 1997) III Separação de componentes de uma mistura de dois ou mais líquidos ou de um sólido dissolvido num líquido A destilação é utilizada para separar soluções de líquidos com pontos de ebulição diferentes (com pelo menos 25 ºC de diferença) ou soluções líquidas em que um dos componentes é volátil. A operação decorre quando a solução é submetida a um aumento de temperatura ou diminuição da pressão. É a combinação destes dois factores que facilita a ocorrência da destilação. Reconhecem-se dois tipos de destilação: a destilação simples e a destilação fraccionada. Mestrado em Química para o Ensino 67
14 Fig 3. 9-Destilação simples (Extraído de Reger Daniel et. al, Química: Princípios e Aplicações, 1997) Destilação Simples É sabido que as substâncias puras apresentam pontos de ebulição bem definidos, mas o mesmo não se pode dizer das substâncias impuras. Com base neste conhecimento é possível separar e caracterizar determinados componentes de uma mistura, que apresentem diferentes volatilidades. A separação dos vários componentes de uma mistura líquida (ou mistura de um sólido dissolvido num liquido), pode ser efectuada utilizando a montagem apresentada na figura 3.9. Na destilação simples de uma mistura de dois ou mais líquidos com pontos de ebulição diferentes, o primeiro líquido recolhido será mais rico no componente que apresenta menor ponto de ebulição (ou seja o mais volátil). Este é arrefecido no condensador, que é percorrido externamente por água, condensando. No entanto, o vapor irá conter uma certa quantidade dos restantes componentes da mistura. O líquido recolhido pode ser novamente destilado caso se pretenda, obtendo-se nesse caso um líquido mais enriquecido no componente mais volátil (ibid, 1997, p.25). Destilação Fraccionada Após a destilação simples de uma mistura líquida o destilado irá conter sempre uma percentagem dos outros componentes mesmo que em pequena quantidade. Para que se obtenham substâncias puras pode recorrer-se à destilação fraccionada. A destilação fraccionada é relativamente diferente da destilação simples, neste caso o vapor proveniente do balão de destilação é encaminhado para uma coluna de grande comprimento, entre o balão de destilação e o condensador, denominada coluna de Mestrado em Química para o Ensino 68
15 fraccionamento, onde em ciclos sucessivos condensa e evapora (refluxo). Os vapores que atingem o topo da coluna são enriquecidos no componente mais volátil, que por arrefecimento da coluna vão condensar. (ibid, 1997, p.25) Uma vez que o trajecto percorrido é maior que na destilação simples, verifica-se uma sucessão de estados de equilíbrio condensação /vaporização. Tal permite aumentar a eficácia da separação. Numa primeira etapa o vapor do líquido mais volátil atinge o topo da coluna de fraccionamento, predominando nas primeiras fracções de destilado que se recolhe. Durante esta etapa a temperatura permanece constante. Após a destilação completa do componente a temperatura deverá subir e quando se mantiver constante de novo, verificar-se-á a destilação do segundo componente. Este procedimento repete-se até que todos os componentes sejam extraídos da mistura. Cuidados a ter antes de iniciar a destilação Antes de iniciar qualquer destilação, seja ela simples ou fraccionada, é necessário tomar algumas precauções tais como: Verificar o ajuste de todos os esmerilados das ligações. Verificar o sentido de circulação da água no condensador, que deve ser contrário ao sentido de circulação do destilado. Adicionar reguladores de ebulição, podendo ser pedaços de porcelana ou esferas de vidro, de modo a evitar uma ebulição tumultuosa ou o sobreaquecimento da mistura. Confirmar a quantidade de liquido que se colocou no balão, não devendo ultrapassar metade da capacidade do balão evitando-se assim a projecção de líquido. A velocidade do aquecimento deverá ser lenta, uma vez que só se consegue um bom equilíbrio entre o líquido e o vapor quando existe um contacto prolongado entre as duas fases. Mestrado em Química para o Ensino 69
16 separações. A tabela 3.1 resume todos os processos físicos mais utilizados para realizar as Misturas homogéneas Misturas heterogéneas Métodos Cristalização Ebulição do solvente Destilação simples Destilação fraccionada Evaporação Cromatografia Separação magnética Sublimação Peneiração Extracção por solvente Decantação Filtração Centrifugação Decantação em ampola Tabela3. 1-Processos físicos de separação Mestrado em Química para o Ensino 70
17 3.3. Separações de Substâncias e a Integração nos Currículos Princípios orientadores do ensino básico Os princípios orientadores da disciplina de Ciências Físico-Químicas para o ensino básico surgem como a integração no projecto educativo de cada escola previsto pelo Ministério da Educação em A proposta destas orientações curriculares prende-se com a intenção de criar novas formas de dinamizar as aulas, implementando novas experiências educativas. Segundo as recomendações do Conselho Nacional de Educação (CNE) (parecer nº2/2000) A autonomia pedagógica, nomeadamente através de projectos educativos é também condição de flexibilização curricular, para que os professores ajam mais como produtores do que como consumidores de currículo. Com estes novos currículos pretende-se sensibilizar os alunos para questões do mundo actual, estimulando o interesse dos alunos para o estudo das ciências. As orientações curriculares surgem como proposta que engloba duas disciplinas: as Ciências Físico-Químicas e as Ciências Naturais, existindo entre ambas uma interdisciplinaridade de saberes. Considera-se importante a implementação de um currículo que pretende desenvolver competências específicas para a literacia científica. Ao nível do ensino básico sugere-se as seguintes competências: 1. Conhecimento (substantivo, processual ou metodológico, epistemológico) 2. Raciocínio 3. Comunicação 4. Atitudes Organização Geral do Programa De acordo com o sugerido pelo Ministério da Educação (adiante M.E.) os princípios orientadores do ensino básico englobam todos os níveis de ensino, 7º, 8º e 9º ano. Nas orientações curriculares para os três ciclos do Ensino Básico propõe-se a organização em temas gerais tais como: Mestrado em Química para o Ensino 71
18 Terra no Espaço Terra em transformação Sustentabilidade na Terra Viver melhor na Terra. A visão e abordagem destes temas incide sobretudo numa perspectiva Ciência- Tecnologia-Sociedade-Ambiente (adiante CTS-A) e tal como mencionado nas orientações curriculares possibilita alargar os horizontes da aprendizagem, proporcionando aos alunos não só o acesso aos produtos da ciência mas também aos seus processos, através das potencialidades e limites da ciência e das suas aplicações Tecnológicas na Sociedade. Os temas apresentam seguimento. Embora incidindo sobre aspectos diferentes, todos promovem a aplicação das ciências e em particular das Ciências Físico-Químicas a situações concretas do quotidiano, na resolução de questões que só são devidamente explicadas com conteúdos científicos. A abordagem do tema Separações Físicas surge inserido no tema Terra em Transformação, mais especificamente na constituição do mundo material, tal como se verifica na figura Mestrado em Química para o Ensino 72
19 Fig Organização dos temas gerais do Ensino Básico (adaptado do ministério da Educação, 2001) A abordagem do estudo das separações de substâncias de uma mistura, centra-se na questão Como é constituído o mundo material?. Associado a este tema de separações físicas, encontram-se outros conceitos tais como: substâncias, mistura de substâncias e propriedades físicas das substâncias cujo estudo é necessário para a compreensão do processo de separações. Destacam-se para este tema objectivos específicos tais como (M.E; 2001): Compreensão da existência de diferentes materiais, propriedades distintas e de diferentes utilizações; Distinção entre substância e mistura de substâncias; Utilização das diferentes técnicas de separação a casos concretos de misturas. Mestrado em Química para o Ensino 73
20 Princípios orientadores do ensino secundário. O tema Processos Físicos de Separação é aplicado especificamente ao nível do ensino básico. No entanto, os processos físicos de separação são abordados novamente no 10º ano de escolaridade. Esta TIPS (ou uma adaptação mais exigente) também pode ser aplicada ao nível do ensino secundário no intuito de efectuar uma breve revisão de conceitos e, como tal, explicita-se seguidamente como se poderia enquadrar no programa do Ensino Secundário. Como resultado da Revisão Curricular do Ensino Secundário surge a homologação do programa de Física e Química A em No Ensino Secundário o tema em questão enquadra-se no módulo inicial: Materiais: diversidade e constituição, pretendendo-se a explicação do mundo material e artificialmente construído (M.E, 2001), reforçando a ideia que se estabeleceu no ensino básico de que o mundo à nossa volta é constituído por substâncias. O principal objectivo deste módulo é a consolidação de conhecimentos que, embora adquiridos no ensino básico, são fundamentais para a aprendizagem de posteriores conceitos Os objectivos de aprendizagem para este tema, iniciado com as questões: Materiais: Qual a origem?; Que constituição e composição?; Como se separam constituintes?, são (M.E.; 2001): Utilização do conceito de substância para descrever o mundo material, podendo existir isoladamente ou com a formação de misturas; Caracterização de misturas e de substâncias; Explicitação dos diversos passos de modo a dar resposta a questões resolúveis experimentalmente; Relacionar a técnica com o princípio subjacente; Aplicar técnicas adequadas à separação de misturas e princípios subjacentes; Percepção das limitações das técnicas, enquanto processos de componentes de misturas; Ao nível do ensino secundário é fundamentalmente privilegiado o trabalho laboratorial. O seguinte esquema permite identificar de que modo os processos físicos de separação estão integrados na reestruturação dos novos temas. Mestrado em Química para o Ensino 74
21 Fig3. 1- Contextualização dos conceitos relacionados com os processos físicos de separação (adaptado do Ministério da Educação, 2001). Fig Organização dos temas gerais Fisica-Química A (adaptado do ministério da Educação, 2001) Mestrado em Química para o Ensino 75
22 Mestrado em Química para o Ensino 76
Decantação sólido - líquido
 Processos de separação Decantação sólido - líquido Possível devido à diferença de densidades dos componentes da mistura. Permite a separação de líquidos imiscíveis (que não se misturam) ou um sólido precipitado
Processos de separação Decantação sólido - líquido Possível devido à diferença de densidades dos componentes da mistura. Permite a separação de líquidos imiscíveis (que não se misturam) ou um sólido precipitado
SEPARAÇÃO DE MISTURAS HETEROGÊNEAS. (Processos mecânicos de separação) Sistema sólido - sólido
 SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas
SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas
23-05-2012. Sumário. Materiais. Processos de separação dos componentes duma mistura
 Sumário 6º Teste de avaliação. Processos de separação dos componentes de uma mistura. Separação de componentes de misturas: Heterogéneas sólidas; Heterogéneas sólidas-líquidas; Heterogéneas líquidas; Homogéneas
Sumário 6º Teste de avaliação. Processos de separação dos componentes de uma mistura. Separação de componentes de misturas: Heterogéneas sólidas; Heterogéneas sólidas-líquidas; Heterogéneas líquidas; Homogéneas
Como distinguir misturas homogéneas de misturas heterogéneas. Uma mistura é constituída por dois ou mais componentes
 Como distinguir misturas homogéneas de misturas heterogéneas Uma mistura é constituída por dois ou mais componentes Homogéneas As pizzas são misturas heterogéneas Heterogéneas coloidais A espuma para o
Como distinguir misturas homogéneas de misturas heterogéneas Uma mistura é constituída por dois ou mais componentes Homogéneas As pizzas são misturas heterogéneas Heterogéneas coloidais A espuma para o
Separação de Misturas
 1. Introdução Separação de Misturas As misturas são comuns em nosso dia a dia. Como exemplo temos: as bebidas, os combustíveis, e a própria terra em que pisamos. Poucos materiais são encontrados puros.
1. Introdução Separação de Misturas As misturas são comuns em nosso dia a dia. Como exemplo temos: as bebidas, os combustíveis, e a própria terra em que pisamos. Poucos materiais são encontrados puros.
Química SUBSTÂNCIAS, MISTURAS E PROCESSO DE SEPARAÇÃO DE MISTURAS
 SUBSTÂNCIAS, MISTURAS E PROCESSO DE SEPARAÇÃO DE MISTURAS SUBSTÂNCIAS QUÍMICAS Átomos ligados entre si são chamados de moléculas, e representam substâncias químicas. Cada molécula é identificada por uma
SUBSTÂNCIAS, MISTURAS E PROCESSO DE SEPARAÇÃO DE MISTURAS SUBSTÂNCIAS QUÍMICAS Átomos ligados entre si são chamados de moléculas, e representam substâncias químicas. Cada molécula é identificada por uma
SUBSTÂNCIAS E MISTURAS. Professor: Antonio Sorrentino
 SUBSTÂNCIAS E MISTURAS Professor: Antonio Sorrentino Substância pura e tipos de misturas Substâncias puras: Apresentam propriedades físicas bem definidas. Têm pontos de fusão e de ebulição. Ponto de fusão:
SUBSTÂNCIAS E MISTURAS Professor: Antonio Sorrentino Substância pura e tipos de misturas Substâncias puras: Apresentam propriedades físicas bem definidas. Têm pontos de fusão e de ebulição. Ponto de fusão:
PROCESSOS DE SEPARAÇÃO DE MISTURAS. 1- quais os métodos mais indicados para separa os componentes das misturas abaixo:
 EXERCÍCIOS DE REVISÃO PROCESSOS DE SEPARAÇÃO DE MISTURAS 1- quais os métodos mais indicados para separa os componentes das misturas abaixo: a) areia e ferro na forma de lâmina separação magnética b) água
EXERCÍCIOS DE REVISÃO PROCESSOS DE SEPARAÇÃO DE MISTURAS 1- quais os métodos mais indicados para separa os componentes das misturas abaixo: a) areia e ferro na forma de lâmina separação magnética b) água
Introdução. Gerais. Funcionais. Propriedades. da Matéria Organolépticas. Específicas. Químicas. Físicas. Química. Rômulo
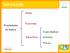 Introdução Gerais Propriedades Funcionais da Matéria Organolépticas Específicas s Físicas Propriedades Gerais São propriedades comuns a todo tipo de matéria massa extensão impenetrabilidade divisibilidade
Introdução Gerais Propriedades Funcionais da Matéria Organolépticas Específicas s Físicas Propriedades Gerais São propriedades comuns a todo tipo de matéria massa extensão impenetrabilidade divisibilidade
LOGO. Separação de misturas. Profa. Samara Garcia Profa. Núria Galacini Março/Abril/2012
 LOGO Separação de misturas Profa. Samara Garcia Profa. Núria Galacini Março/Abril/2012 Misturas Homogêneas Destilação simples (sólido + líquido): Por aquecimento, só o líquido entra em ebulição, vaporiza-se
LOGO Separação de misturas Profa. Samara Garcia Profa. Núria Galacini Março/Abril/2012 Misturas Homogêneas Destilação simples (sólido + líquido): Por aquecimento, só o líquido entra em ebulição, vaporiza-se
SEPARAÇÃO DE MISTURAS
 SEPARAÇÃO DE MISTURAS Os materiais encontrados na natureza são, em geral, misturas de várias substâncias. Mesmo em laboratório, quando tentamos preparar uma só substância, acabamos, normalmente, chegando
SEPARAÇÃO DE MISTURAS Os materiais encontrados na natureza são, em geral, misturas de várias substâncias. Mesmo em laboratório, quando tentamos preparar uma só substância, acabamos, normalmente, chegando
Separação de Misturas II Parte
 Separação de Misturas II Parte Fracionamento de misturas heterogêneas Catação ou escolha É um método rudimentar de separação de mistura baseado na diferença de tamanho e de aspecto das partículas de uma
Separação de Misturas II Parte Fracionamento de misturas heterogêneas Catação ou escolha É um método rudimentar de separação de mistura baseado na diferença de tamanho e de aspecto das partículas de uma
A Matéria e Diagrama de Fases. Profº André Montillo www.montillo.com.br
 A Matéria e Diagrama de Fases Profº André Montillo www.montillo.com.br Substância: É a combinação de átomos de elementos diferentes em uma proporção de um número inteiro. O átomo não é criado e não é destruído,
A Matéria e Diagrama de Fases Profº André Montillo www.montillo.com.br Substância: É a combinação de átomos de elementos diferentes em uma proporção de um número inteiro. O átomo não é criado e não é destruído,
Roteiro de Estudos 2 trimestre 2015 Disciplina: Química 9º ANOS
 Roteiro de Estudos 2 trimestre 2015 Disciplina: Química 9º ANOS Professor: Ricardo Augusto Marques da Costa O que devo saber: UNIDADE 2 Os estados físicos da matéria. Estados físicos da matéria e suas
Roteiro de Estudos 2 trimestre 2015 Disciplina: Química 9º ANOS Professor: Ricardo Augusto Marques da Costa O que devo saber: UNIDADE 2 Os estados físicos da matéria. Estados físicos da matéria e suas
Matéria e Estados da Matéria
 Matéria e Estados da Matéria A matéria é o material físico do universo. Matéria é tudo que tem massa e ocupa certo lugar no espaço. Na antiguidade, o homem chegou a acreditar que toda matéria existente
Matéria e Estados da Matéria A matéria é o material físico do universo. Matéria é tudo que tem massa e ocupa certo lugar no espaço. Na antiguidade, o homem chegou a acreditar que toda matéria existente
Introdução à Química Inorgânica
 Introdução à Química Inorgânica Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira Química A Química é uma ciência que está diretamente ligada à nossa vida cotidiana. A produção do pão,
Introdução à Química Inorgânica Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira Química A Química é uma ciência que está diretamente ligada à nossa vida cotidiana. A produção do pão,
PROPRIEDADES DA MATÉRIA
 Profª Msc.Anna Carolina A. Ribeiro PROPRIEDADES DA MATÉRIA RELEMBRANDO Matéria é tudo que tem massa e ocupa lugar no espaço. Não existe vida nem manutenção da vida sem matéria. Corpo- Trata-se de uma porção
Profª Msc.Anna Carolina A. Ribeiro PROPRIEDADES DA MATÉRIA RELEMBRANDO Matéria é tudo que tem massa e ocupa lugar no espaço. Não existe vida nem manutenção da vida sem matéria. Corpo- Trata-se de uma porção
 Termos Técnicos Ácidos Classe de substâncias que têm ph igual ou maior que 1 e menor que 7. Exemplo: sumo do limão. Átomos Todos os materiais são formados por pequenas partículas. Estas partículas chamam-se
Termos Técnicos Ácidos Classe de substâncias que têm ph igual ou maior que 1 e menor que 7. Exemplo: sumo do limão. Átomos Todos os materiais são formados por pequenas partículas. Estas partículas chamam-se
Aluno (a): Professor:
 3º BIM P1 LISTA DE EXERCÍCIOS CIÊNCIAS 6º ANO Aluno (a): Professor: Turma: Turno: Data: / / Unidade: ( ) Asa Norte ( ) Águas Lindas ( )Ceilândia ( ) Gama ( )Guará ( ) Pistão Norte ( ) Recanto das Emas
3º BIM P1 LISTA DE EXERCÍCIOS CIÊNCIAS 6º ANO Aluno (a): Professor: Turma: Turno: Data: / / Unidade: ( ) Asa Norte ( ) Águas Lindas ( )Ceilândia ( ) Gama ( )Guará ( ) Pistão Norte ( ) Recanto das Emas
2. Assinale a alternativa que apresenta, na seqüência, os termos corretos que preenchem as lacunas da seguinte afirmativa:
 COLÉGIO JOÃO PAULO I QUÍMICA 8ª Série Nome: Turma: Data: Professor (a): Nota Máxima: 6,0 Nota: 1. Assinale a ÚNICA proposição CORRETA que contém o melhor método para separar os três componentes de uma
COLÉGIO JOÃO PAULO I QUÍMICA 8ª Série Nome: Turma: Data: Professor (a): Nota Máxima: 6,0 Nota: 1. Assinale a ÚNICA proposição CORRETA que contém o melhor método para separar os três componentes de uma
O interesse da Química é analisar as...
 O interesse da Química é analisar as... PROPRIEDADES CONSTITUINTES SUBSTÂNCIAS E MATERIAIS TRANSFORMAÇÕES ESTADOS FÍSICOS DOS MATERIAIS Os materiais podem se apresentar na natureza em 3 estados físicos
O interesse da Química é analisar as... PROPRIEDADES CONSTITUINTES SUBSTÂNCIAS E MATERIAIS TRANSFORMAÇÕES ESTADOS FÍSICOS DOS MATERIAIS Os materiais podem se apresentar na natureza em 3 estados físicos
Água como solvente. Objectivos de Aprendizagem. No final desta lição, você será capaz de:
 Lição N o 3 Água como solvente Objectivos de Aprendizagem No final desta lição, você será capaz de: Mencionar as propriedades físicas da água. Descrever a composição química da água. Material de apoio
Lição N o 3 Água como solvente Objectivos de Aprendizagem No final desta lição, você será capaz de: Mencionar as propriedades físicas da água. Descrever a composição química da água. Material de apoio
UNIVERSIDADE NOVA DE LISBOA Faculdade de Ciências e Tecnologia
 UNIVERSIDADE NVA DE LISBA Faculdade de Ciências e Tecnologia Síntese de ácido acetilsalicílico (aspirina). Análise por TLC do produto obtido. 1. Cromatografia Misturas de compostos podem ser separados
UNIVERSIDADE NVA DE LISBA Faculdade de Ciências e Tecnologia Síntese de ácido acetilsalicílico (aspirina). Análise por TLC do produto obtido. 1. Cromatografia Misturas de compostos podem ser separados
23-05-2012. Sumário. Materiais. Algumas propriedades físicas e químicas dos materiais
 Sumário Correção do TPC. Algumas propriedades físicas características de substâncias. Os estados físicos da matéria e as mudanças de estado; Temperatura de fusão e temperatura de ebulição; Densidade. Estados
Sumário Correção do TPC. Algumas propriedades físicas características de substâncias. Os estados físicos da matéria e as mudanças de estado; Temperatura de fusão e temperatura de ebulição; Densidade. Estados
Propriedades da matéria e mudanças de estado físico
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Propriedades da matéria e mudanças de estado físico Professor: José Tiago Pereira Barbosa 1 Propriedades da Matéria A matéria é
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Propriedades da matéria e mudanças de estado físico Professor: José Tiago Pereira Barbosa 1 Propriedades da Matéria A matéria é
Matéria: Química Assunto: Materiais Prof. Gilberto Ramos
 Matéria: Química Assunto: Materiais Prof. Gilberto Ramos Química Materiais, suas propriedades e usos Estados Físicos Estado vem do latim status (posição,situação, condição,modo de estar). O estado físico
Matéria: Química Assunto: Materiais Prof. Gilberto Ramos Química Materiais, suas propriedades e usos Estados Físicos Estado vem do latim status (posição,situação, condição,modo de estar). O estado físico
Ciências Físico-Químicas Ano Lectivo 2010/2011
 Ciências Físico-Químicas Ano ectivo 2010/2011 Nome 7.º Ano Turma Número Mudanças de estado físico, ponto de fusão, ponto de ebulição e concentração mássica 1. Indique, justificando, se a temperatura a
Ciências Físico-Químicas Ano ectivo 2010/2011 Nome 7.º Ano Turma Número Mudanças de estado físico, ponto de fusão, ponto de ebulição e concentração mássica 1. Indique, justificando, se a temperatura a
Atividade 1: Grandezas Químicas
 COLÉGIO SHALOM Ensino Fundamental 9 Ano Prof.º: Hélen Cristina Disciplina Química Aluno (a):. No. Trabalho de Recuperação Data: / / Valor: Nota: Orientações: -Responder manuscrito; -Cópias de colegas,
COLÉGIO SHALOM Ensino Fundamental 9 Ano Prof.º: Hélen Cristina Disciplina Química Aluno (a):. No. Trabalho de Recuperação Data: / / Valor: Nota: Orientações: -Responder manuscrito; -Cópias de colegas,
Curso de Farmácia. Operações Unitárias em Indústria Prof.a: Msd Érica Muniz 6 /7 Período DESTILAÇÃO
 Curso de Farmácia Operações Unitárias em Indústria Prof.a: Msd Érica Muniz 6 /7 Período DESTILAÇÃO 1 Introdução A destilação como opção de um processo unitário de separação, vem sendo utilizado pela humanidade
Curso de Farmácia Operações Unitárias em Indústria Prof.a: Msd Érica Muniz 6 /7 Período DESTILAÇÃO 1 Introdução A destilação como opção de um processo unitário de separação, vem sendo utilizado pela humanidade
RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL
 RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL 5 ESTUDO DA MATÉRIA 1 DEFINIÇÕES Matéria é tudo que ocupa lugar no espaço e tem massa. Nem tudo que existe no universo e matéria. Por exemplo, o calor e
RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL 5 ESTUDO DA MATÉRIA 1 DEFINIÇÕES Matéria é tudo que ocupa lugar no espaço e tem massa. Nem tudo que existe no universo e matéria. Por exemplo, o calor e
PROF. KELTON WADSON OLIMPÍADA 8º SÉRIE ASSUNTO: TRANSFORMAÇÕES DE ESTADOS DA MATÉRIA.
 PROF. KELTON WADSON OLIMPÍADA 8º SÉRIE ASSUNTO: TRANSFORMAÇÕES DE ESTADOS DA MATÉRIA. 1)Considere os seguintes dados obtidos sobre propriedades de amostras de alguns materiais. Com respeito a estes materiais,
PROF. KELTON WADSON OLIMPÍADA 8º SÉRIE ASSUNTO: TRANSFORMAÇÕES DE ESTADOS DA MATÉRIA. 1)Considere os seguintes dados obtidos sobre propriedades de amostras de alguns materiais. Com respeito a estes materiais,
Preparação de Soluções
 Colégio Paulo VI Preparação de Soluções TÉCNICAS LABORATORIAIS DE QUÍMICA I Ana Filipa Sousa nº2 10ºA Abril 2002 2 ÍNDICE Nomenclatura 4 1. Introdução x 2. Teoria e Método x 3. Material x 4. Produtos x
Colégio Paulo VI Preparação de Soluções TÉCNICAS LABORATORIAIS DE QUÍMICA I Ana Filipa Sousa nº2 10ºA Abril 2002 2 ÍNDICE Nomenclatura 4 1. Introdução x 2. Teoria e Método x 3. Material x 4. Produtos x
Ciclo: 3º Ano: 7º Disciplina: Físico-Química. Atividades / Estratégias. Nº aulas previstas. Avaliação
 código 171608 AGRUPAMENTO DE ESCOLAS D. DOMINGOS JARDO Direção Regional de Educação de Lisboa Ciclo: º Ano: 7º Disciplina: Físico-Química Conteúdos I - O Universo 1. O que existe no Universo 1.1 Estrutura
código 171608 AGRUPAMENTO DE ESCOLAS D. DOMINGOS JARDO Direção Regional de Educação de Lisboa Ciclo: º Ano: 7º Disciplina: Físico-Química Conteúdos I - O Universo 1. O que existe no Universo 1.1 Estrutura
UTILIZAÇÃO DOS NOVOS LABORATÓRIOS ESCOLARES
 ESCOLA SECUNDÁRIA CAMILO CASTELO BRANCO V. N. FAMALICÃO ACÇÃO DE FORMAÇÃO UTILIZAÇÃO DOS NOVOS LABORATÓRIOS ESCOLARES Correcção Formador: Professor Vítor Duarte Teodoro Formanda: Maria do Céu da Mota Rocha
ESCOLA SECUNDÁRIA CAMILO CASTELO BRANCO V. N. FAMALICÃO ACÇÃO DE FORMAÇÃO UTILIZAÇÃO DOS NOVOS LABORATÓRIOS ESCOLARES Correcção Formador: Professor Vítor Duarte Teodoro Formanda: Maria do Céu da Mota Rocha
PROPRIEDADES DOS MATERIAIS QUÍMICA GERAL
 PROPRIEDADES DOS MATERIAIS QUÍMICA GERAL PROPRIEDADES DA MATÉRIA CONCEITOS BÁSICOS MATÉRIA: tudo o que tem massa e ocupa lugar no espaço. CORPO/OBJETO: porção limitada da matéria. MASSA: quantidade matéria,
PROPRIEDADES DOS MATERIAIS QUÍMICA GERAL PROPRIEDADES DA MATÉRIA CONCEITOS BÁSICOS MATÉRIA: tudo o que tem massa e ocupa lugar no espaço. CORPO/OBJETO: porção limitada da matéria. MASSA: quantidade matéria,
Propriedades físicas e químicas das substâncias
 Propriedades físicas e químicas das substâncias Na Natureza há uma grande diversidade de materais. Muitos desses materais são substâncias mas será que são puras? Há substâncias que, mesmo misturadas com
Propriedades físicas e químicas das substâncias Na Natureza há uma grande diversidade de materais. Muitos desses materais são substâncias mas será que são puras? Há substâncias que, mesmo misturadas com
Início 15.09.11 03.01.12 10.04.12 Final 16.12.11 23.03.12 08.06.12 Interrupções - 20 22 Fev 2012 -
 TOTAL Outras Atividades Tema B: Terra em Transformação Tema A: Terra no Espaço Departamento de Matemática e Ciências Experimentais PLANIFICAÇÃO 7º Ano de Ciências Físico-Químicas Ano Letivo 2011 / 2012
TOTAL Outras Atividades Tema B: Terra em Transformação Tema A: Terra no Espaço Departamento de Matemática e Ciências Experimentais PLANIFICAÇÃO 7º Ano de Ciências Físico-Químicas Ano Letivo 2011 / 2012
Analisar e aplicar os princípios da extração sólido-líquido e líquido-líquido na separação e purificação de produtos.
 12.1 Objetivo Específico Analisar e aplicar os princípios da extração sólido-líquido e líquido-líquido na separação e purificação de produtos. 12.2 Introdução A extração é uma técnica para purificação
12.1 Objetivo Específico Analisar e aplicar os princípios da extração sólido-líquido e líquido-líquido na separação e purificação de produtos. 12.2 Introdução A extração é uma técnica para purificação
Processos em Engenharia: Processos de Separação
 Processos em Engenharia: Processos de Separação Prof. Daniel Coutinho [email protected] Departamento de Automação e Sistemas DAS Universidade Federal de Santa Catarina UFSC DAS 5101 - Aula 10 p.1/44
Processos em Engenharia: Processos de Separação Prof. Daniel Coutinho [email protected] Departamento de Automação e Sistemas DAS Universidade Federal de Santa Catarina UFSC DAS 5101 - Aula 10 p.1/44
SEPARAÇÃO DE MISTURAS Exercícios
 SEI Ensina - MILITAR Química SEPARAÇÃO DE MISTURAS Exercícios 1.A água potável é um recurso natural considerado escasso em diversas regiões do nosso planeta. Mesmo em locais onde a água é relativamente
SEI Ensina - MILITAR Química SEPARAÇÃO DE MISTURAS Exercícios 1.A água potável é um recurso natural considerado escasso em diversas regiões do nosso planeta. Mesmo em locais onde a água é relativamente
Propriedades físicas e químicas das substâncias
 Ciências Físico-Químicas - 7º ano Propriedades físicas e M. Neli G. C. Cavaleiro M. Domingas Beleza Há substâncias que, mesmo misturadas com outras, facilmente identificamos através de características
Ciências Físico-Químicas - 7º ano Propriedades físicas e M. Neli G. C. Cavaleiro M. Domingas Beleza Há substâncias que, mesmo misturadas com outras, facilmente identificamos através de características
M A T E R I A I S D E L A B O R A T Ó R I O. Prof. Agamenon Roberto
 M A T E R I A I S D E L A B O R A T Ó R I O Prof. Agamenon Roberto Prof. Agamenon Roberto MATERIAS DE LABORATÓRIO 2 TUBO DE ENSAIO: Tubo de vidro fechado em uma das extremidades, empregado para fazer reações
M A T E R I A I S D E L A B O R A T Ó R I O Prof. Agamenon Roberto Prof. Agamenon Roberto MATERIAS DE LABORATÓRIO 2 TUBO DE ENSAIO: Tubo de vidro fechado em uma das extremidades, empregado para fazer reações
Mudanças de Fase. Estado de agregação da matéria
 Mudanças de Fase Estado de agregação da matéria Investigando melhor... Para produzirmos gelo é preciso levar água até o congelador. Para produzirmos vapor é preciso levar água à chama de um fogão. Por
Mudanças de Fase Estado de agregação da matéria Investigando melhor... Para produzirmos gelo é preciso levar água até o congelador. Para produzirmos vapor é preciso levar água à chama de um fogão. Por
Podes dissolver o sal que quiseres num copo de água?
 8 Podes dissolver o sal que quiseres num copo de água? E8-1 o que necessitas sal de cozinha areia ou pedaços de calcário ou cacos pequenos de louças, de tijolos, etc. água da torneira dois copos iguais
8 Podes dissolver o sal que quiseres num copo de água? E8-1 o que necessitas sal de cozinha areia ou pedaços de calcário ou cacos pequenos de louças, de tijolos, etc. água da torneira dois copos iguais
ATIVIDADES RECUPERAÇÃO PARALELA
 ATIVIDADES RECUPERAÇÃO PARALELA Nome: Nº Ano: 6º Data: 14/11/2012 Bimestre: 4 Professor: Vanildo Disciplina: Química Orientações para estudo: Esta atividade deverá ser entregue no dia da avaliação de recuperação,
ATIVIDADES RECUPERAÇÃO PARALELA Nome: Nº Ano: 6º Data: 14/11/2012 Bimestre: 4 Professor: Vanildo Disciplina: Química Orientações para estudo: Esta atividade deverá ser entregue no dia da avaliação de recuperação,
SEPARAÇÃO DE MISTURAS
 SEPARAÇÃO DE MISTURAS Os seguintes processos permitem a separação dos vários constituintes de uma mistura. Cada um destes processos tem uma utilização bem definida, dependendo do tipo e das propriedades
SEPARAÇÃO DE MISTURAS Os seguintes processos permitem a separação dos vários constituintes de uma mistura. Cada um destes processos tem uma utilização bem definida, dependendo do tipo e das propriedades
Aula 2: O estudo da matéria
 KROTON S.A. UNIC EDUCACIONAL LTDA. ENGENHARIA DE PRODUÇÃO 2015/1 Aula 2: O estudo da matéria A Matéria Conceitos; Tudo que tem massa e ocupa lugar no espaço. - O que é massa? - Como se afere a massa de
KROTON S.A. UNIC EDUCACIONAL LTDA. ENGENHARIA DE PRODUÇÃO 2015/1 Aula 2: O estudo da matéria A Matéria Conceitos; Tudo que tem massa e ocupa lugar no espaço. - O que é massa? - Como se afere a massa de
Motivação 2- Viagem de Kemi : Substâncias e misturas - Não misture!
 TÍTULO: Separação de misturas: Separar para quê? Por quê? MOTIVAÇÃO 1: Figura 1: Imagens disponível em: https://encrypted- tbn1.gstatic.com/images?q=tbn:and9gcteufd9xe2nxk6cm617o- 1PnafWL2Ta3RCwzGRldDclRzyYB-HBFekHOlo
TÍTULO: Separação de misturas: Separar para quê? Por quê? MOTIVAÇÃO 1: Figura 1: Imagens disponível em: https://encrypted- tbn1.gstatic.com/images?q=tbn:and9gcteufd9xe2nxk6cm617o- 1PnafWL2Ta3RCwzGRldDclRzyYB-HBFekHOlo
MATÉRIA Mestranda Daniele Potulski Disciplina Química da Madeira I
 PROPRIEDADES DA MATÉRIA Mestranda Daniele Potulski Disciplina Química da Madeira I Química É a ciência que estuda a constituição da matéria; ESTRUTURA INTERNA RELAÇÕES ENTRE OS DIVERSOS TIPOS DE MATERIAIS
PROPRIEDADES DA MATÉRIA Mestranda Daniele Potulski Disciplina Química da Madeira I Química É a ciência que estuda a constituição da matéria; ESTRUTURA INTERNA RELAÇÕES ENTRE OS DIVERSOS TIPOS DE MATERIAIS
QUÍMICA TECNOLÓGICA I
 Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG QUÍMICA TECNOLÓGICA I Prof a. Dr a. Flaviana Tavares Vieira [email protected] Alquimia
Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG QUÍMICA TECNOLÓGICA I Prof a. Dr a. Flaviana Tavares Vieira [email protected] Alquimia
Ficha Informativa n.º 4 Materiais
 AGRUPAMENTO VERTICAL DE ESCOLAS DE FRAZÃO ESCOLA E.B. 2,3 DE FRAZÃO CIÊNCIAS FÍSICO-QUÍMICAS 9º ANO DE ESCOLARIDADE ANO LETIVO 2011/2012 Ficha Informativa n.º 4 Materiais Nome: Data: / /2012 INTRODUÇÃO
AGRUPAMENTO VERTICAL DE ESCOLAS DE FRAZÃO ESCOLA E.B. 2,3 DE FRAZÃO CIÊNCIAS FÍSICO-QUÍMICAS 9º ANO DE ESCOLARIDADE ANO LETIVO 2011/2012 Ficha Informativa n.º 4 Materiais Nome: Data: / /2012 INTRODUÇÃO
PROCEDIMENTO EXPERIMENTAL A MACROESCALA
 PROCEDIMENTO EXPERIMENTAL A MACROESCALA Parte I Produção do óxido de cobre Ponto de Partida 1- Preparar uma amostra de 300 mg de cobre a partir de um fio de cobre ou de uma folha de cobre. 2- Colocar a
PROCEDIMENTO EXPERIMENTAL A MACROESCALA Parte I Produção do óxido de cobre Ponto de Partida 1- Preparar uma amostra de 300 mg de cobre a partir de um fio de cobre ou de uma folha de cobre. 2- Colocar a
Fase Identifica um estado uniforme de
 DIAGRAMAS DE FASES Definições Fase Identifica um estado uniforme de matéria, não só no que se refere à composição química, mas também no que se refere ao estado físico. Número de fases numa mistura P 1
DIAGRAMAS DE FASES Definições Fase Identifica um estado uniforme de matéria, não só no que se refere à composição química, mas também no que se refere ao estado físico. Número de fases numa mistura P 1
1 - Etapas do método científico.
 1 - Etapas do método científico. Realizar experimentos apropriados para responder a questões; A partir da observação, estabelecer relações. Princípios: Proposições ou generalizações de regularidades, semelhanças
1 - Etapas do método científico. Realizar experimentos apropriados para responder a questões; A partir da observação, estabelecer relações. Princípios: Proposições ou generalizações de regularidades, semelhanças
Profa. Maria Fernanda - Química [email protected]
 Profa. Maria Fernanda - Química [email protected] Estudo de caso Reúnam-se em grupos de máximo 5 alunos e proponha uma solução para o seguinte caso: A morte dos peixes ornamentais. Para isso
Profa. Maria Fernanda - Química [email protected] Estudo de caso Reúnam-se em grupos de máximo 5 alunos e proponha uma solução para o seguinte caso: A morte dos peixes ornamentais. Para isso
10-10-2000. Francisco José Simões Roque, nº9 11ºA
 Estudo da composição dos solos A turfa 10-10-2000 Francisco José Simões Roque, nº9 11ºA INTRODUÇÃO Os solos são sistemas trifásicos pois são constituídos por componentes sólidos, líquidos e gasosos. Cerca
Estudo da composição dos solos A turfa 10-10-2000 Francisco José Simões Roque, nº9 11ºA INTRODUÇÃO Os solos são sistemas trifásicos pois são constituídos por componentes sólidos, líquidos e gasosos. Cerca
TRATAMENTO DA ÁGUA PARA GERADORES DE VAPOR
 Universidade Federal do Paraná Curso de Engenharia Industrial Madeireira MÁQUINAS TÉRMICAS AT-101 Dr. Alan Sulato de Andrade [email protected] 1 INTRODUÇÃO: A água nunca está em estado puro, livre de
Universidade Federal do Paraná Curso de Engenharia Industrial Madeireira MÁQUINAS TÉRMICAS AT-101 Dr. Alan Sulato de Andrade [email protected] 1 INTRODUÇÃO: A água nunca está em estado puro, livre de
 Principal material de laboratório e a sua função Balão de Erlenmeyer/matrás Gobelé/copo Balão de fundo plano Proveta Balão volumétrico Caixa de Petri Kitasato Balão de destilação Vidro de relógio Tubos
Principal material de laboratório e a sua função Balão de Erlenmeyer/matrás Gobelé/copo Balão de fundo plano Proveta Balão volumétrico Caixa de Petri Kitasato Balão de destilação Vidro de relógio Tubos
ESTADOS FÍSICOS DA MATÉRIA
 ESTADOS FÍSICOS DA MATÉRIA A matéria pode se apresentar em diferentes estados físicos, como sólido, líquido e gasoso. Algumas propriedades da matéria dependem de seu estado físico. O estado sólido Em determinada
ESTADOS FÍSICOS DA MATÉRIA A matéria pode se apresentar em diferentes estados físicos, como sólido, líquido e gasoso. Algumas propriedades da matéria dependem de seu estado físico. O estado sólido Em determinada
Beja com Ciência Relatório 1. Beja com Ciência
 Relatório Tema: Iniciação à ciência Atividade Data Horas despendidas 27/0/4 2 28/0/4 3 Regras básicas de comportamento em laboratório. 29/0/4 Saber ler e identificar os rótulos presentes em 30/0/4 5 laboratório
Relatório Tema: Iniciação à ciência Atividade Data Horas despendidas 27/0/4 2 28/0/4 3 Regras básicas de comportamento em laboratório. 29/0/4 Saber ler e identificar os rótulos presentes em 30/0/4 5 laboratório
Aluno (a): Nº. Disciplina: Química Goiânia, / / 2014
 Lista de Exercícios Aluno (a): Nº. Professora: Núbia de Andrade Série: 1º ano (Ensino médio) Turma: Disciplina: Química Goiânia, / / 2014 01) A mudança de fase denominada sublimação ocorre quando a) o
Lista de Exercícios Aluno (a): Nº. Professora: Núbia de Andrade Série: 1º ano (Ensino médio) Turma: Disciplina: Química Goiânia, / / 2014 01) A mudança de fase denominada sublimação ocorre quando a) o
Nesta experiência vamos ver que o conceito de temperatura pode ser subjectivo.
 Estudo do Meio Físico-Natural I P06 - Termodinâmica 1 Objectivo Realizar várias experiências relacionadas com termodinâmica. 2 Quente ou frio? Nesta experiência vamos ver que o conceito de temperatura
Estudo do Meio Físico-Natural I P06 - Termodinâmica 1 Objectivo Realizar várias experiências relacionadas com termodinâmica. 2 Quente ou frio? Nesta experiência vamos ver que o conceito de temperatura
CONTEÚDOS OBJETIVOS PERÍODO
 ESCOLA BÁSICA2,3 EUGÉNIO DOS SANTOS 2013 2014 página 1 ESCOLA BÁSICA DO 2.º E 3.º CICLOS EUGÉNIO DOS SANTOS PLANIFICAÇÃO E METAS DE APRENDIZAGEM DA DISCIPLINA DE CIÊNCIAS FÍSICO-QUÍMICAS 8.º ANO DE ESCOLARIDADE
ESCOLA BÁSICA2,3 EUGÉNIO DOS SANTOS 2013 2014 página 1 ESCOLA BÁSICA DO 2.º E 3.º CICLOS EUGÉNIO DOS SANTOS PLANIFICAÇÃO E METAS DE APRENDIZAGEM DA DISCIPLINA DE CIÊNCIAS FÍSICO-QUÍMICAS 8.º ANO DE ESCOLARIDADE
Janine Coutinho Canuto
 Janine Coutinho Canuto Termologia é a parte da física que estuda o calor. Muitas vezes o calor é confundido com a temperatura, vamos ver alguns conceitos que irão facilitar o entendimento do calor. É a
Janine Coutinho Canuto Termologia é a parte da física que estuda o calor. Muitas vezes o calor é confundido com a temperatura, vamos ver alguns conceitos que irão facilitar o entendimento do calor. É a
Introdução à Química. Prof. Fernando R. Xavier
 Introdução à Química Prof. Fernando R. Xavier UDESC 2013 Qual a idade da química? É possível identificar a presença da química desde a idade do bronze (3,300 a.c.). Ex.: Agricultura, conserva de alimentos,
Introdução à Química Prof. Fernando R. Xavier UDESC 2013 Qual a idade da química? É possível identificar a presença da química desde a idade do bronze (3,300 a.c.). Ex.: Agricultura, conserva de alimentos,
Diagramas de Fase. Objetivos:
 1 Diagramas de Fase Objetivos: Interpretar diagramas de fases de substâncias puras Deslocamento da fronteira entre as fases Interpretar diagramas de fases de compostos Diagramas de misturas líquidas Diagramas
1 Diagramas de Fase Objetivos: Interpretar diagramas de fases de substâncias puras Deslocamento da fronteira entre as fases Interpretar diagramas de fases de compostos Diagramas de misturas líquidas Diagramas
COLÉGIO NOSSA SENHORA DA PIEDADE. Programa de Recuperação Paralela. 2ª Etapa 2014. 1ª série Turma: FG
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 2ª Etapa 2014 Disciplina: QUÍMICA Professora: Maria Luiza 1ª série Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 2ª Etapa 2014 Disciplina: QUÍMICA Professora: Maria Luiza 1ª série Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
Preparação e padronização de uma solução 0,10 mol/l de ácido clorídrico
 Universidade Estadual de Goiás UnUCET - Anápolis Química Industrial Química Experimental II Preparação e padronização de uma solução 0,10 mol/l de ácido clorídrico Alunos: Bruno Ramos; Wendel Thiago; Thales
Universidade Estadual de Goiás UnUCET - Anápolis Química Industrial Química Experimental II Preparação e padronização de uma solução 0,10 mol/l de ácido clorídrico Alunos: Bruno Ramos; Wendel Thiago; Thales
Propriedades da matéria (Continuação)
 Propriedades da matéria (Continuação) Densidade m/v Experimentos / discussão Exercício 1) Um bloco de metal tem volume de 200 ml e massa de 1792 g. a) Qual a densidade desse metal, expressa em g / cm3?
Propriedades da matéria (Continuação) Densidade m/v Experimentos / discussão Exercício 1) Um bloco de metal tem volume de 200 ml e massa de 1792 g. a) Qual a densidade desse metal, expressa em g / cm3?
CALORIMETRIA, MUDANÇA DE FASE E TROCA DE CALOR Lista de Exercícios com Gabarito e Soluções Comentadas
 COLÉGIO PEDRO II PRÓ-REITORIA DE PÓS-GRADUAÇÃO, PESQUISA, EXTENSÃO E CULTURA PROGRAMA DE RESIDÊNCIA DOCENTE RESIDENTE DOCENTE: Marcia Cristina de Souza Meneguite Lopes MATRÍCULA: P4112515 INSCRIÇÃO: PRD.FIS.0006/15
COLÉGIO PEDRO II PRÓ-REITORIA DE PÓS-GRADUAÇÃO, PESQUISA, EXTENSÃO E CULTURA PROGRAMA DE RESIDÊNCIA DOCENTE RESIDENTE DOCENTE: Marcia Cristina de Souza Meneguite Lopes MATRÍCULA: P4112515 INSCRIÇÃO: PRD.FIS.0006/15
MATÉRIA- PROPRIEDADES DA MATÉRIA- SUBSTÂNICAS (Pura e Composta)- MISTURAS- ANÁLISE IMEDIATA.
 ATENÇÃO: Não sou o detentor dos direitos e também não tenho a intenção de violá-los de nenhuma imagem, exemplo prático ou material de terceiros que porventura venham a ser utilizados neste ou em qualquer
ATENÇÃO: Não sou o detentor dos direitos e também não tenho a intenção de violá-los de nenhuma imagem, exemplo prático ou material de terceiros que porventura venham a ser utilizados neste ou em qualquer
Escola Superior de Educação João de Deus
 Regulamento do 2.º Ciclo de Estudos Conducente ao Grau de Mestre em Educação pela Arte Artigo 1.º Objectivos Os objectivos dos cursos de mestrado (2.º ciclo), da Escola Superior de Educação João de Deus
Regulamento do 2.º Ciclo de Estudos Conducente ao Grau de Mestre em Educação pela Arte Artigo 1.º Objectivos Os objectivos dos cursos de mestrado (2.º ciclo), da Escola Superior de Educação João de Deus
Actividade laboratorial (Biologia e Geologia 11º ano)
 Actividade laboratorial (Biologia e Geologia 11º ano) INFLUÊNCIA DO CO 2 NA DISSOLUÇÃO DE CALCÁRIOS (Parte II Proposta de Resolução do Guião) O que se pretende 1. Seleccionar o material necessário ao estudo
Actividade laboratorial (Biologia e Geologia 11º ano) INFLUÊNCIA DO CO 2 NA DISSOLUÇÃO DE CALCÁRIOS (Parte II Proposta de Resolução do Guião) O que se pretende 1. Seleccionar o material necessário ao estudo
Química Geral PROF. LARISSA ROCHA ALMEIDA - CURSINHO VITORIANO 1
 Química Geral AULA 1 PROPRIEDADES GERAIS DA MATÉRIA E CONCEITOS INICIAIS PROF. LARISSA ROCHA ALMEIDA - CURSINHO VITORIANO 1 Tópicos Matéria Energia Diagrama de Mudança de Fases Ciclo da Água Universo e
Química Geral AULA 1 PROPRIEDADES GERAIS DA MATÉRIA E CONCEITOS INICIAIS PROF. LARISSA ROCHA ALMEIDA - CURSINHO VITORIANO 1 Tópicos Matéria Energia Diagrama de Mudança de Fases Ciclo da Água Universo e
ESTUDO DA MATÉRIA. QUÍMICA: é o ramo da ciência que estuda a matéria, suas propriedades, estruturas e transformações.
 QUÍMICA: é o ramo da ciência que estuda a matéria, suas propriedades, estruturas e transformações. MATÉRIA: é tudo que tem massa e ocupa lugar no espaço. Exemplo: O ar Um balão de festas (bexiga) aumenta
QUÍMICA: é o ramo da ciência que estuda a matéria, suas propriedades, estruturas e transformações. MATÉRIA: é tudo que tem massa e ocupa lugar no espaço. Exemplo: O ar Um balão de festas (bexiga) aumenta
Exercícios de Propriedades Coligativas e Coloides
 Exercícios de Propriedades Coligativas e Coloides 1. Considere o gráfico da pressão máxima de vapor em função da temperatura para um solvente puro e para uma solução desse solvente contendo um soluto molecular
Exercícios de Propriedades Coligativas e Coloides 1. Considere o gráfico da pressão máxima de vapor em função da temperatura para um solvente puro e para uma solução desse solvente contendo um soluto molecular
Exercícios Sobre MudanÇas de estados físicos e diagramas
 Exercícios Sobre MudanÇas de estados físicos e diagramas 01. (Uepg) Quanto às características das substâncias puras e das misturas, assinale o que for correto. 01) Misturas sólidas homogêneas não podem
Exercícios Sobre MudanÇas de estados físicos e diagramas 01. (Uepg) Quanto às características das substâncias puras e das misturas, assinale o que for correto. 01) Misturas sólidas homogêneas não podem
Química 12º Ano. Unidade 2 Combustíveis, Energia e Ambiente. Actividades de Projecto Laboratorial. Janeiro 2005. Jorge R. Frade, Ana Teresa Paiva
 Efeitos da composição em temperaturas de fusão e de ebulição Química 12º Ano Unidade 2 Combustíveis, Energia e Ambiente Actividades de Projecto Laboratorial Janeiro 2005 Jorge R. Frade, Ana Teresa Paiva
Efeitos da composição em temperaturas de fusão e de ebulição Química 12º Ano Unidade 2 Combustíveis, Energia e Ambiente Actividades de Projecto Laboratorial Janeiro 2005 Jorge R. Frade, Ana Teresa Paiva
 Exame de Laboratórios de Bioquímica e Biofísica Licenciatura em Bioquímica 1ª Época 27 de Junho de 2006 Por favor responda às questões da 1ª parte e 2ª partes em folhas separadas 1ª Parte 1. Suponha que
Exame de Laboratórios de Bioquímica e Biofísica Licenciatura em Bioquímica 1ª Época 27 de Junho de 2006 Por favor responda às questões da 1ª parte e 2ª partes em folhas separadas 1ª Parte 1. Suponha que
24 O uso dos manuais de Matemática pelos alunos de 9.º ano
 24 O uso dos manuais de Matemática pelos alunos de 9.º ano Mariana Tavares Colégio Camões, Rio Tinto João Pedro da Ponte Departamento de Educação e Centro de Investigação em Educação Faculdade de Ciências
24 O uso dos manuais de Matemática pelos alunos de 9.º ano Mariana Tavares Colégio Camões, Rio Tinto João Pedro da Ponte Departamento de Educação e Centro de Investigação em Educação Faculdade de Ciências
QUÍMICA QUESTÃO 41 QUESTÃO 42
 Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
A) a existência do oceano líquido é uma hipótese possível, pois um sal solúvel só forma uma mistura homogênea com a água, quando ela está líquida.
 TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
Departamento de Química Inorgânica 2. SOLUÇÕES
 2. SOLUÇÕES I. INTRODUÇÃO Soluções são misturas homogêneas de dois ou mais componentes, sendo que estes estão misturados uniformemente em nível molecular. Em nosso cotidiano temos diversos exemplos de
2. SOLUÇÕES I. INTRODUÇÃO Soluções são misturas homogêneas de dois ou mais componentes, sendo que estes estão misturados uniformemente em nível molecular. Em nosso cotidiano temos diversos exemplos de
Reconhecimento e explicação da importância da evolução tecnológica no nosso conhecimento atual sobre o Universo.
 ESCOLA BÁSICA2,3 EUGÉNIO DOS SANTOS 2013 2014 página 1 ESCOLA BÁSICA DO 2.º E 3.º CICLOS EUGÉNIO DOS SANTOS PLANIFICAÇÃO E METAS DE APRENDIZAGEM DA DISCIPLINA DE CIÊNCIAS FÍSICO-QUÍMICAS 7.º ANO DE ESCOLARIDADE
ESCOLA BÁSICA2,3 EUGÉNIO DOS SANTOS 2013 2014 página 1 ESCOLA BÁSICA DO 2.º E 3.º CICLOS EUGÉNIO DOS SANTOS PLANIFICAÇÃO E METAS DE APRENDIZAGEM DA DISCIPLINA DE CIÊNCIAS FÍSICO-QUÍMICAS 7.º ANO DE ESCOLARIDADE
ESTADOS DA MATÉRIA. O átomo é composto por outras partículas ainda menores.
 ESTADOS DA MATÉRIA A matéria que temos a nossa volta é formada de moléculas que são constituídas por átomos. Uma combinação destes átomos forma as substâncias que conhecemos, porém, devemos salientar que
ESTADOS DA MATÉRIA A matéria que temos a nossa volta é formada de moléculas que são constituídas por átomos. Uma combinação destes átomos forma as substâncias que conhecemos, porém, devemos salientar que
Enquadramento 02. Justificação 02. Metodologia de implementação 02. Destinatários 02. Sessões formativas 03
 criação de empresas em espaço rural guia metodológico para criação e apropriação 0 Enquadramento 02 Justificação 02 de implementação 02 Destinatários 02 Sessões formativas 03 Módulos 03 1 e instrumentos
criação de empresas em espaço rural guia metodológico para criação e apropriação 0 Enquadramento 02 Justificação 02 de implementação 02 Destinatários 02 Sessões formativas 03 Módulos 03 1 e instrumentos
Solidificação: é o processo em que uma substância passa do estado líquido para o estado sólido.
 EXERCÍCIOS PREPARATÓRIOS 1. (G1) Explique o significado das palavras a seguir. Observe o modelo. Solidificação: é o processo em que uma substância passa do estado líquido para o estado sólido. Vaporização:
EXERCÍCIOS PREPARATÓRIOS 1. (G1) Explique o significado das palavras a seguir. Observe o modelo. Solidificação: é o processo em que uma substância passa do estado líquido para o estado sólido. Vaporização:
Água e Solução Tampão
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
SUBSTÂNCIAS E MISTURAS
 SUBSTÂNCIAS E MISTURAS 1. ELEMENTO QUÍMICO É um conjunto de átomos de mesmo número atômico(z). 1 2 3 H H H 1 1 1 2. SUBSTÂNCIA Z Todo material formado por um tipo apenas de componente (molécula ou aglomerado
SUBSTÂNCIAS E MISTURAS 1. ELEMENTO QUÍMICO É um conjunto de átomos de mesmo número atômico(z). 1 2 3 H H H 1 1 1 2. SUBSTÂNCIA Z Todo material formado por um tipo apenas de componente (molécula ou aglomerado
ARTIGO TÉCNICO. Os objectivos do Projecto passam por:
 A metodologia do Projecto SMART MED PARKS ARTIGO TÉCNICO O Projecto SMART MED PARKS teve o seu início em Fevereiro de 2013, com o objetivo de facultar uma ferramenta analítica de confiança para apoiar
A metodologia do Projecto SMART MED PARKS ARTIGO TÉCNICO O Projecto SMART MED PARKS teve o seu início em Fevereiro de 2013, com o objetivo de facultar uma ferramenta analítica de confiança para apoiar
Resumos. 1) Aula L1 - O Lixo e Conceitos Químicos a. Aulas. 1) Aula L1 - Lixo e Conceitos Gerais. 2) Aula L2 - Estados Físicos da Matéria
 Resumo Teórico 1 Fala Gás Nobre! Tudo bem? Já assistimos todos os vídeos sobre o Lixo. Estamos cada vez mais próximos do sucesso. Por isso quero te entregar esse material que contém o resumo das aulas
Resumo Teórico 1 Fala Gás Nobre! Tudo bem? Já assistimos todos os vídeos sobre o Lixo. Estamos cada vez mais próximos do sucesso. Por isso quero te entregar esse material que contém o resumo das aulas
Introdução. a cultura científica e tecnológica.
 Introdução A cultura científica e tecnológica é cada vez mais reconhecida como uma condição estratégica para o desenvolvimento de uma cidadania ativa, traduzindo-se numa sociedade mais qualificada e no
Introdução A cultura científica e tecnológica é cada vez mais reconhecida como uma condição estratégica para o desenvolvimento de uma cidadania ativa, traduzindo-se numa sociedade mais qualificada e no
- CROMATOGRAFIA EM CAMADA FINA (CCF)
 - CROMATOGRAFIA EM CAMADA FINA (CCF) Técnica de identificação e separação de compostos orgânicos Aplicações: - Identificação de componentes de uma mistura - Acompanhamento da evolução de uma reação - Análise
- CROMATOGRAFIA EM CAMADA FINA (CCF) Técnica de identificação e separação de compostos orgânicos Aplicações: - Identificação de componentes de uma mistura - Acompanhamento da evolução de uma reação - Análise
Disciplina de Didáctica da Química I
 Disciplina de Didáctica da Química I Texto de Apoio Concepções Alternativas em Equilíbrio Químico Autores: Susana Fonseca, João Paiva 3.2.3 Concepções alternativas em Equilíbrio Químico Tal como já foi
Disciplina de Didáctica da Química I Texto de Apoio Concepções Alternativas em Equilíbrio Químico Autores: Susana Fonseca, João Paiva 3.2.3 Concepções alternativas em Equilíbrio Químico Tal como já foi
GUIA PARA O PREENCHIMENTO DOS FORMULÁRIOS ENTIDADE GESTORA ERP PORTUGAL
 GUIA PARA O PREENCHIMENTO DOS FORMULÁRIOS ENTIDADE GESTORA ERP PORTUGAL Versão: 1.0 Data: 05-06-2009 Índice Acesso e estados dos Formulários... 3 Escolha do Formulário e submissão... 4 Bases para a navegação
GUIA PARA O PREENCHIMENTO DOS FORMULÁRIOS ENTIDADE GESTORA ERP PORTUGAL Versão: 1.0 Data: 05-06-2009 Índice Acesso e estados dos Formulários... 3 Escolha do Formulário e submissão... 4 Bases para a navegação
1.º PERÍODO. n.º de aulas previstas DOMÍNIOS SUBDOMÍNIOS/CONTEÚDOS OBJETIVOS. De 36 a 41
 DE FÍSICO-QUÍMICA - 7.º ANO Ano Letivo 2014 2015 PERFIL DO ALUNO O aluno é capaz de: o Conhecer e compreender a constituição do Universo, localizando a Terra, e reconhecer o papel da observação e dos instrumentos
DE FÍSICO-QUÍMICA - 7.º ANO Ano Letivo 2014 2015 PERFIL DO ALUNO O aluno é capaz de: o Conhecer e compreender a constituição do Universo, localizando a Terra, e reconhecer o papel da observação e dos instrumentos
Mudanças de estado da água: fusão, solidificação, evaporação, ebulição, condensação...
 PROFESSOR: EQUIPE DE CIÊNCIAS BANCO DE QUESTÕES - CIÊNCIAS - 6º ANO - ENSINO FUNDAMENTAL ============================================================================================= Mudanças de estado
PROFESSOR: EQUIPE DE CIÊNCIAS BANCO DE QUESTÕES - CIÊNCIAS - 6º ANO - ENSINO FUNDAMENTAL ============================================================================================= Mudanças de estado
Propriedades da Matéria
 Professor: Robinho AULA 1 QMC E Propriedades da Matéria Matéria Massa Volume AR Matéria/Propriedades Pág. 263 DENSIDADE d = m V Matéria/Propriedades Pág. 263 Med (UFSC 2011)Uma medalha, supostamente de
Professor: Robinho AULA 1 QMC E Propriedades da Matéria Matéria Massa Volume AR Matéria/Propriedades Pág. 263 DENSIDADE d = m V Matéria/Propriedades Pág. 263 Med (UFSC 2011)Uma medalha, supostamente de
Areias e Ambientes Sedimentares
 Areias e Ambientes Sedimentares As areias são formadas a partir de rochas. São constituídas por detritos desagregados de tamanhos compreendidos entre 0,063 e 2 milímetros. Areias: Ambiente fluvial As areias
Areias e Ambientes Sedimentares As areias são formadas a partir de rochas. São constituídas por detritos desagregados de tamanhos compreendidos entre 0,063 e 2 milímetros. Areias: Ambiente fluvial As areias
SPIRO, T. G.; STIGLIANI, W. M. Química ambiental. São Paulo: Pearson. 2009 (adaptado).
 1. (Enem 2014) O principal processo industrial utilizado na produção de fenol é a oxidação do cumeno (isopropilbenzeno). A equação mostra que esse processo envolve a formação do hidroperóxido de cumila,
1. (Enem 2014) O principal processo industrial utilizado na produção de fenol é a oxidação do cumeno (isopropilbenzeno). A equação mostra que esse processo envolve a formação do hidroperóxido de cumila,
