Disciplina de Didáctica da Química I
|
|
|
- Maria do Loreto Sá Dreer
- 10 Há anos
- Visualizações:
Transcrição
1 Disciplina de Didáctica da Química I Texto de Apoio Concepções Alternativas em Equilíbrio Químico Autores: Susana Fonseca, João Paiva
2 3.2.3 Concepções alternativas em Equilíbrio Químico Tal como já foi referido, são vários os estudos que identificam dificuldades de compreensão do Equilíbrio Químico, bem como ideias alternativas que os alunos evidenciam em resposta a questões relacionadas com esta temática. Hackling e Garnett (1985) registaram as seguintes concepções alternativas: - A velocidade da reacção directa aumenta à medida que a reacção decorre; - Existe uma relação aritmética simples entre as concentrações de reagentes e de produtos, como por exemplo, igual concentração de ambos os reagentes ou de reagentes e produtos; - Depois de adicionar um reagente, a quantidade desse reagente permanece a mesma;
3 - Ao adicionar um reagente a velocidade da reacção inversa diminui, o mesmo acontecendo quando se aumenta a temperatura numa reacção endotérmica, ou quando se diminui o volume numa reacção com maior número de moles nos produtos; - Quando um equilíbrio é restabelecido, as velocidades das reacções directa e inversa são as mesmas que no equilíbrio inicial; - Alterações de volume e de concentração provocam alterações no valor da constante de equilíbrio e a temperatura não provoca efeitos directamente na constante de equilíbrio; - Um catalisador pode afectar de modo diferente a velocidade das reacções directa e inversa. Maskill e Cachapuz (1989), utilizaram testes de associação de palavras para identificar as ideias desenvolvidas pelos alunos e verificaram que: - Os alunos desenvolvem uma visão do tipo balanço do Equilíbrio Químico (mais estático do que dinâmico); - A ideia de reversibilidade é entendida como a possibilidade de mover num sentido ou noutro, mas de forma alternada e linear; - Incapacidade em relacionar a velocidade da reacção com a teoria das colisões; - Nas reacções em fase gasosa, a pressão é associada a força, mais do que a colisões entre partículas ou ao seu movimento; - Não compreensão do verdadeiro significado do termo concentração e sua influência no equilíbrio; - Está presente a ideia de que quanto mais rápida a reacção, maior a quantidade de produtos produzida; - As quantidades de reagentes e produtos são iguais no estado de equilíbrio. Bergquist e Heikkinen (1990), situam as concepções alternativas dos alunos em quatro áreas gerais de dificuldade: a) Os estudantes demonstram dificuldades acerca das quantidades de substância e das concentrações: - tentando calcular concentrações quando estas já são dadas; - expressando incerteza acerca de quando usar o volume; 82
4 - assumindo que a razão entre os coeficientes estequiométricos se aplica nas concentrações de produtos e reagentes no equilíbrio; - assumindo que as quantidades molares são iguais, mesmo quando um dos reagentes está em excesso. b) Os alunos mostram confusão acerca do aparecimento e desaparecimento de material, assumindo: - que as concentrações variam quando o equilíbrio é estabelecido; - que uma reacção é reversível e completa; - que a reacção no sentido directo deve ser concluída antes que a reacção no sentido inverso comece; - que a adição de mais reagente varia apenas a concentração de produto. c) Os estudantes demonstram confusão acerca da constante de equilíbrio: - descrevendo-a como variando em valor a temperatura constante; - assumindo que o seu valor varia com a alteração das concentrações de reagentes ou produtos. d) Os estudantes demonstram incompreensão do princípio de Le Chatelier: - tentando ajustar um sistema que já está em equilíbrio; - tentando apenas alterar a concentração do reagente adicionado; - tentando alterar a concentração de todas as espécies presentes, excepto as do reagente adicionado; - expressando incerteza sobre como variações de temperatura, volume ou pressão (incluindo a adição de gases inertes), alteram as concentrações de equilíbrio. Banerjee (1995), verificou que: - Sempre que é dada uma constante de equilíbrio, os alunos consideram que todas as concentrações fornecidas (por exemplo as iniciais) são também as de equilíbrio; - Embora os alunos usem o termo constante de equilíbrio, têm dificuldade em compreender a existência de um equilíbrio em reacções que virtualmente se completam ou que ocorrem em muito pequena extensão; - Quando a temperatura diminui numa reacção exotérmica a velocidade da reacção directa aumenta (confundindo assim extensão e velocidade da reacção, devido à tentativa de aplicar erradamente o princípio de Le Chatelier à velocidade de reacção); 83
5 - Valores elevados da constante de equilíbrio implicam reacções muito rápidas; - Dificuldade em compreender o papel dos catalisadores no equilíbrio; - Dificuldade na interpretação da equação da energia de Gibbs; - Confusão entre energia de Gibbs, reversibilidade, espontaneidade e equilíbrio. Solaz e Quílez (2001), identificam uma série de concepções alternativas que associam a utilizações erróneas do princípio de Le Chatelier: - A adição de reagentes, a pressão e temperatura constantes, implica sempre o deslocamento do equilíbrio no sentido de formação dos produtos; - A adição de sólidos em equilíbrios heterogéneos altera o equilíbrio; - A adição de um gás inerte a um Equilíbrio Químico nunca o perturba, uma vez que o gás não reage; - A adição de gás inerte, a volume e temperatura constantes, aumenta a pressão total e esta alteração é minimizada pelo deslocamento no sentido em que há diminuição do número total de moles de espécies gasosas; - A adição de gás inerte, a pressão e temperatura constantes, perturba o equilíbrio, aumentando a pressão, como tal, a alteração é minimizada pelo deslocamento no sentido em que há diminuição do número total de moles de espécies gasosas; - A adição de um gás inerte, a pressão e temperatura constantes, não perturba o equilíbrio, porque o volume aumenta mas isso não afecta o equilíbrio, pois a pressão é mantida constante; as fracções molares dos gases em reacção não variam; - A adição de gases inertes, a pressão e temperatura constantes, numa reacção do tipo A (g) B (g) + C (g) diminui a pressão parcial de A, o que provoca um deslocamento no sentido dos reagentes. Van Driel e Gräber (2002) reuniram concepções alternativas detectadas, ao longo dos anos, noutros estudos. Entre as concepções alternativas reunidas, encontram-se muitas das já referidas anteriormente. De qualquer modo, para que se compreenda que estas ideias dos alunos são verificadas de forma consistente em vários artigos, inscrevem-se em seguida as concepções alternativas e dificuldades compiladas por estes autores: - Não distinção entre reacções irreversíveis e reversíveis; - A reacção directa completa-se antes da reacção inversa começar; - Não distinção entre rapidez e extensão; 84
6 - A velocidade da reacção directa aumenta ao longo do tempo; - Não ocorre reacção durante o equilíbrio; - O equilíbrio é visto como um pêndulo oscilante; - Visão compartimentada do equilíbrio, acreditando que existe um lado esquerdo e um lado direito que actuam independentemente; - Massa e concentração significam o mesmo para as espécies presentes no equilíbrio; - Existe uma relação simples entre reagentes e produtos no equilíbrio, sendo o mais comum a ideia de que no equilíbrio a concentração de reagentes é igual à de produtos. - Incompreensão do princípio de Le Chatelier de forma significativa, procurando aplicálo sem a sua compreensão; - Tentativa de aplicar o princípio de Le Chatelier em situações fora da âmbito em que o mesmo é valido, como a adição de gases inertes ou substâncias liquidas e sólidas; - Aplicação da formulação geral do princípio de Le Chatelier a alterações de pressão ou volume, de igual forma; - Na formação de um novo equilíbrio a velocidade das reacções é igual ao anterior equilíbrio; - Quando a temperatura de um sistema é alterada, a evolução pode ser prevista sem saber se a reacção é exotérmica ou endotérmica; - Os estudantes com visão compartimentada acreditam que as alterações ao equilíbrio produzem efeitos apenas de um dos lados da equação; - A constante de equilíbrio altera-se com alterações de concentração ou volume; - A constante de equilíbrio é independente da temperatura; - O catalisador afecta de modo diferente as velocidades da reacção directa e inversa, implicando alterações no valor da constante de equilíbrio; - Um valor mais elevado da constante de equilíbrio, implica uma reacção mais rápida; - Erros no cálculo do equilíbrio devido a falta de compreensão da estequiometria; - Não associação das alterações no equilíbrio com modificações da energia e entropia do sistema. Furió, Calatayud, Bárcenas e Padilla (2000) detectaram que a fixação com que o princípio de Le Chatelier é aplicado, leva a que frequentemente os alunos encarem a adição de um reagente sólido como a de qualquer outro. Do mesmo modo, nas adições de gás inerte não são considerados todos os factores influenciadores, como se a adição é efectuada a volume ou a pressão constantes. 85
7 Banerjee (1991a) efectuou um estudo em que determinou a existência de concepções alternativas em Equilíbrio Químico não só em alunos mas também em professores. Entre as concepções alternativas detectadas, encontra-se o facto dos professores e alunos falharem a percepção de que o princípio de Le Chatelier só é limitado a informação qualitativa. Os professores e os alunos demonstram dificuldades conceptuais quando aplicam raciocínios demasiado intuitivos usando este princípio. Verificaram também que, em muitos casos, alunos e professores tinham a ideia que ao descer a temperatura numa reacção exotérmica, a velocidade da reacção directa aumenta (na realidade como a temperatura diminui, ambas as reacções diminuem de velocidade, mas a mais prejudicada é a inversa que necessita de mais energia). O problema neste caso, é que, mais uma vez, está a procurar-se aplicar o princípio onde já não é válido, ou seja, ao campo das velocidades. A Tabela 3.1 organiza as concepções alternativas e dificuldades atrás referidas, procurado constituir uma síntese, por forma a melhor interpretar e distinguir as ideias identificadas. 86
8 Temas Reacções Reversíveis Concepções Alternativas e Dificuldades Não distinção das implicações de uma reacção ser reversível ou irreversível; A reacção no sentido directo tem ser concluída, antes que a reacção no sentido inverso comece; Reversibilidade é a possibilidade de mover num sentido ou noutro, mas de forma alternada e linear. Quantificação do Equilíbrio Cálculos Envolventes Constante de Equilíbrio Alterações das quantidades de Reagentes e Produtos Alterações de Pressão / Volume Calcular concentrações quando estas já são dadas; Não saber quando usar o volume nos cálculos; As quantidades molares são iguais, mesmo quando um dos reagentes está em excesso; Massa e concentração significam o mesmo para as espécies presentes no equilíbrio. O seu valor mantém-se com alterações de temperatura; O seu valor varia com a alteração das concentrações de reagentes ou produtos; Existe uma relação aritmética simples entre as concentrações de reagentes e de produtos, como igual concentração de ambos os reagentes ou de reagentes e produtos; A razão entre os coeficientes estequiométricos aplica-se nas concentrações de equilíbrio; Sempre que é dada uma constante de equilíbrio, as concentrações dadas são também as de equilíbrio; As concentrações variam quando o equilíbrio é estabelecido; Embora os alunos usem o termo constante de equilíbrio, têm dificuldade em compreender a existência de um equilíbrio em reacções que virtualmente se completam ou que ocorrem em muito pequena extensão; Com a adição de mais reagente varia apenas a concentração de produto; Com a adição de reagente altera-se apenas a concentração do reagente adicionado; Com a adição de reagente altera-se a concentração de todas as espécies presentes, excepto as do reagente adicionado; Depois de adicionar um reagente, a quantidade desse reagente permanece a mesma; A adição de reagentes, a pressão e temperatura constantes, implica sempre o deslocamento do equilíbrio no sentido de formação de produtos. Incerteza sobre como a variação de o volume ou pressão altera as concentrações de equilíbrio; Confusão desta situação com a alteração de pressão por adição de gás inerte. Perturbações ao Equilíbrio Alterações de Temperatura Outras Perturbações Perturbação em Geral Quando a temperatura de um sistema é alterada, a evolução pode ser prevista sem saber se a reacção é exotérmica ou endotérmica; Incerteza sobre como a variação de temperatura altera as concentrações de equilíbrio. A adição de um gás inerte ao Equilíbrio Químico nunca o perturba, uma vez que não se verifica reacção; A adição de gás inerte, a volume e temperatura constantes, aumenta a pressão total e esta alteração é minimizada pelo deslocamento no sentido em que há diminuição do número de moles; A adição de um gás inerte a pressão e temperatura constantes não perturba o equilíbrio; A adição de gases inertes a pressão e temperatura constantes numa reacção do tipo A (g) B (g) + C (g) diminui a pressão parcial de A, o que provoca um deslocamento no sentido dos reagentes; A adição de gás inerte a pressão e temperatura constantes perturba o equilíbrio, aumentando a pressão, como tal a alteração é minimizada pelo deslocamento no sentido em que há diminuição do número de moles; A adição de sólidos em equilíbrios heterogéneos altera o equilíbrio. Tentativa de ajustar um sistema que já está em equilíbrio; As alterações ao equilíbrio produzem efeitos apenas de um dos lados da equação. 87
9 Temas (continuação) Princípio de Le Chatelier Equilíbrio Dinâmico Concepções Alternativas e Dificuldades (continuação) Aplicação à adição de gases inertes, substâncias líquidas e sólidas; Aplicação a alterações de extensão e velocidade da reacção simultaneamente; Aplicação a alterações de volume sem compreensão que é a alteração de pressão que o sistema procura contrariar; Incompreensão do princípio de forma significativa, procurando aplicá-lo sem a sua compreensão. Não ocorre reacção durante o equilíbrio; Visão oscilante do Equilíbrio Químico (mais estático do que dinâmico); Existe um lado esquerdo e um lado direito no equilíbrio, que actuam independentemente; Dificuldade em compreender o equilíbrio em reacções que virtualmente se completam ou que praticamente não ocorrem. Cinética e Equilíbrio Termodinâmica Catalisadores Perturbações do Equilíbrio Ideias Gerais Um catalisador pode afectar de modo diferente a velocidade das reacções directa e inversa. O catalisador afecta de modo diferente as velocidades da reacção directa e inversa implicando alterações no valor da constante de equilíbrio. Quando a temperatura diminui numa reacção exotérmica, a velocidade da reacção directa aumenta; Ao adicionar um reagente, a velocidade da reacção inversa diminui, o mesmo acontecendo quando se aumenta a temperatura numa reacção endotérmica, ou quando se diminui o volume numa reacção com maior número de moles nos produtos; Incapacidade em relacionar a velocidade da reacção com a teoria das colisões; A pressão é associada a força, mais do que a colisões entre partículas ou ao seu movimento; Quanto mais rápida a reacção, maior a quantidade de produto produzida; Um valor mais elevado da constante de equilíbrio implica uma reacção mais rápida; A velocidade da reacção directa aumenta ao longo do tempo; Quando um equilíbrio é restabelecido, as velocidades das reacções directa e inversa são as mesmas que no equilíbrio inicial. Não associação das alterações no equilíbrio a modificações da energia e entropia do sistema; Dificuldade na interpretação da equação da energia de Gibbs; Confusão entre energia de Gibbs, reversibilidade, espontaneidade e equilíbrio. Tabela 3.1- Síntese de Concepções Alternativas e Dificuldades em Equilíbrio Químico. 88
Introdução. Muitas reações ocorrem completamente e de forma irreversível como por exemplo a reação da queima de um papel ou palito de fósforo.
 Introdução Muitas reações ocorrem completamente e de forma irreversível como por exemplo a reação da queima de um papel ou palito de fósforo. Existem também sistemas, em que as reações direta e inversa
Introdução Muitas reações ocorrem completamente e de forma irreversível como por exemplo a reação da queima de um papel ou palito de fósforo. Existem também sistemas, em que as reações direta e inversa
- A velocidade da reação direta (V1) é igual à velocidade da reação inversa (V2) V 1 = V 2
 EQUILÍBRIO QUÍMICO Equilíbrio Químico - Equilíbrio químico é a parte da físico-química que estuda as reações reversíveis e as condições para o estabelecimento desta atividade equilibrada. A + B C + D -
EQUILÍBRIO QUÍMICO Equilíbrio Químico - Equilíbrio químico é a parte da físico-química que estuda as reações reversíveis e as condições para o estabelecimento desta atividade equilibrada. A + B C + D -
EQUILÍBRIO QUÍMICO 1
 EQUILÍBRIO QUÍMICO 1 1- Introdução Uma reação química é composta de duas partes separadas por uma flecha, a qual indica o sentido da reação. As espécies químicas denominadas como reagentes ficam à esquerda
EQUILÍBRIO QUÍMICO 1 1- Introdução Uma reação química é composta de duas partes separadas por uma flecha, a qual indica o sentido da reação. As espécies químicas denominadas como reagentes ficam à esquerda
CINÉTICA QUÍMICA. QUÍMICA 1 2º ANO Prof.ª ELAINE CRISTINA. Educação para toda a vida. Colégio Santo Inácio. Jesuítas
 CINÉTICA QUÍMICA QUÍMICA 1 2º ANO Prof.ª ELAINE CRISTINA CLASSIFICAÇÃO DAS REAÇÕES CINÉTICAS I - Quanto à velocidade Rápidas: neutralizações em meio aquoso, combustões,... Lentas: fermentações, formação
CINÉTICA QUÍMICA QUÍMICA 1 2º ANO Prof.ª ELAINE CRISTINA CLASSIFICAÇÃO DAS REAÇÕES CINÉTICAS I - Quanto à velocidade Rápidas: neutralizações em meio aquoso, combustões,... Lentas: fermentações, formação
P2 - PROVA DE QUÍMICA GERAL - 20/05/06
 - ROVA DE QUÍMICA GERAL - 0/05/06 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão a,5 a,5 3 a,5 4 a,5 Total 0,0 Constantes: R 8,34 J mol - K - 0,08 atm L mol - K - atm L 0,35
- ROVA DE QUÍMICA GERAL - 0/05/06 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão a,5 a,5 3 a,5 4 a,5 Total 0,0 Constantes: R 8,34 J mol - K - 0,08 atm L mol - K - atm L 0,35
Equilíbrio Químico. Prof. Alex Fabiano C. Campos
 6/09/010 Equilíbrio Químico rof. Alex Fabiano C. Campos rocessos Reversíveis e Irreversíveis Algumas reações são irreversíveis, ou seja, uma vez obtios os proutos não há previsão espontânea e regeneração
6/09/010 Equilíbrio Químico rof. Alex Fabiano C. Campos rocessos Reversíveis e Irreversíveis Algumas reações são irreversíveis, ou seja, uma vez obtios os proutos não há previsão espontânea e regeneração
CALOR, TEMPERATURA E CAPACIDADES CALORÍFICAS. C = q/ T. C = n. C m
 CALOR, TEMPERATURA E CAPACIDADES CALORÍFICAS Nem todas as substâncias têm a mesma capacidade calorífica, isto é, para a mesma energia calorífica recebida, a elevação de temperatura é diferente. C capacidade
CALOR, TEMPERATURA E CAPACIDADES CALORÍFICAS Nem todas as substâncias têm a mesma capacidade calorífica, isto é, para a mesma energia calorífica recebida, a elevação de temperatura é diferente. C capacidade
PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA DE QUÍMICA
 PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA DE QUÍMICA TEMAS 1. Estrutura da matéria 1.1 Elementos, átomos e iões 1.2
PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA DE QUÍMICA TEMAS 1. Estrutura da matéria 1.1 Elementos, átomos e iões 1.2
P3 - PROVA DE QUÍMICA GERAL - 16/06/12
 P3 - PROVA DE QUÍMICA GERAL - 6/06/ Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Dados gerais: G = H - TS G= - n F E G = G o + RT ln Q ΔE ΔE [A] [A] 0 Questão Valor Grau Revisão kt a,5 a,5 3 a,5
P3 - PROVA DE QUÍMICA GERAL - 6/06/ Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Dados gerais: G = H - TS G= - n F E G = G o + RT ln Q ΔE ΔE [A] [A] 0 Questão Valor Grau Revisão kt a,5 a,5 3 a,5
Transições de Fase de Substâncias Simples
 Transições de Fase de Substâncias Simples Como exemplo de transição de fase, vamos discutir a liquefação de uma amostra de gás por um processo de redução de volume a temperatura constante. Consideremos,
Transições de Fase de Substâncias Simples Como exemplo de transição de fase, vamos discutir a liquefação de uma amostra de gás por um processo de redução de volume a temperatura constante. Consideremos,
Utilização do SOLVER do EXCEL
 Utilização do SOLVER do EXCEL 1 Utilização do SOLVER do EXCEL José Fernando Oliveira DEEC FACULDADE DE ENGENHARIA DA UNIVERSIDADE DO PORTO MAIO 1998 Para ilustrar a utilização do Solver na resolução de
Utilização do SOLVER do EXCEL 1 Utilização do SOLVER do EXCEL José Fernando Oliveira DEEC FACULDADE DE ENGENHARIA DA UNIVERSIDADE DO PORTO MAIO 1998 Para ilustrar a utilização do Solver na resolução de
Se um sistema troca energia com a vizinhança por trabalho e por calor, então a variação da sua energia interna é dada por:
 Primeira Lei da Termodinâmica A energia interna U de um sistema é a soma das energias cinéticas e das energias potenciais de todas as partículas que formam esse sistema e, como tal, é uma propriedade do
Primeira Lei da Termodinâmica A energia interna U de um sistema é a soma das energias cinéticas e das energias potenciais de todas as partículas que formam esse sistema e, como tal, é uma propriedade do
Começo por apresentar uma breve definição para projecto e para gestão de projectos respectivamente.
 The role of Project management in achieving Project success Ao longo da desta reflexão vou abordar os seguintes tema: Definir projectos, gestão de projectos e distingui-los. Os objectivos da gestão de
The role of Project management in achieving Project success Ao longo da desta reflexão vou abordar os seguintes tema: Definir projectos, gestão de projectos e distingui-los. Os objectivos da gestão de
Aula 05. Princípios da Termodinâmica. Termodinâmica. Energia das Reações Químicas. Filosofia do Sucesso (Napoleon Hill)
 Filosofia do Sucesso (Napoleon Hill) Se você pensa que é um derrotado, você será derrotado. Se não pensar, quero a qualquer custo, não conseguirá nada. Mesmo que você queira vencer, mas pensa que não vai
Filosofia do Sucesso (Napoleon Hill) Se você pensa que é um derrotado, você será derrotado. Se não pensar, quero a qualquer custo, não conseguirá nada. Mesmo que você queira vencer, mas pensa que não vai
FATORES QUE AFETAM AS VELOCIDADES DAS REAÇÕES. 2. As concentrações dos reagentes. 3. A temperatura na qual a reação ocorre.
 CINÉTICA QUÍMICA FATORES QUE AFETAM AS VELOCIDADES DAS REAÇÕES 1. O estado físico dos reagentes. 2. As concentrações dos reagentes. 3. A temperatura na qual a reação ocorre. 4. A presença de um catalisador.
CINÉTICA QUÍMICA FATORES QUE AFETAM AS VELOCIDADES DAS REAÇÕES 1. O estado físico dos reagentes. 2. As concentrações dos reagentes. 3. A temperatura na qual a reação ocorre. 4. A presença de um catalisador.
Análise Dimensional Notas de Aula
 Primeira Edição Análise Dimensional Notas de Aula Prof. Ubirajara Neves Fórmulas dimensionais 1 As fórmulas dimensionais são formas usadas para expressar as diferentes grandezas físicas em função das grandezas
Primeira Edição Análise Dimensional Notas de Aula Prof. Ubirajara Neves Fórmulas dimensionais 1 As fórmulas dimensionais são formas usadas para expressar as diferentes grandezas físicas em função das grandezas
Equilíbrio Químico. Processos Reversíveis e Irreversíveis
 Equilíbrio Químico rocessos Reversíveis e Irreversíveis rocessos Reversíveis e I Algumas reações são irreversíveis, ou seja, uma vez obtios os proutos não há previsão espontânea e regeneração os reagentes.
Equilíbrio Químico rocessos Reversíveis e Irreversíveis rocessos Reversíveis e I Algumas reações são irreversíveis, ou seja, uma vez obtios os proutos não há previsão espontânea e regeneração os reagentes.
COLÉGIO SANTA TERESINHA R. Madre Beatriz 135 centro Tel. (33) 3341-1244 www.colegiosantateresinha.com.br
 PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
Cinética Química Aplicada (LOQ 4003)
 - Universidade de São Paulo - Escola de Engenharia de Lorena Cinética Química Aplicada (LOQ 4003) 1º semestre de 2014 Prof. Dr. João Paulo Alves Silva [email protected] Aula anterior Equação de Velocidade
- Universidade de São Paulo - Escola de Engenharia de Lorena Cinética Química Aplicada (LOQ 4003) 1º semestre de 2014 Prof. Dr. João Paulo Alves Silva [email protected] Aula anterior Equação de Velocidade
O Que Tem Sido Apresentado em Livros Didáticos?
 Princípio de Le Chatelier O Que Tem Sido Apresentado em Livros Didáticos? Renato Canzian e Flavio Antonio Maximiano Neste trabalho, é apresentada uma análise sobre como os aspectos relacionados ao deslocamento
Princípio de Le Chatelier O Que Tem Sido Apresentado em Livros Didáticos? Renato Canzian e Flavio Antonio Maximiano Neste trabalho, é apresentada uma análise sobre como os aspectos relacionados ao deslocamento
Modelo Cascata ou Clássico
 Modelo Cascata ou Clássico INTRODUÇÃO O modelo clássico ou cascata, que também é conhecido por abordagem top-down, foi proposto por Royce em 1970. Até meados da década de 1980 foi o único modelo com aceitação
Modelo Cascata ou Clássico INTRODUÇÃO O modelo clássico ou cascata, que também é conhecido por abordagem top-down, foi proposto por Royce em 1970. Até meados da década de 1980 foi o único modelo com aceitação
IBM1018 Física Básica II FFCLRP USP Prof. Antônio Roque Aula 6. O trabalho feito pela força para deslocar o corpo de a para b é dado por: = =
 Energia Potencial Elétrica Física I revisitada 1 Seja um corpo de massa m que se move em linha reta sob ação de uma força F que atua ao longo da linha. O trabalho feito pela força para deslocar o corpo
Energia Potencial Elétrica Física I revisitada 1 Seja um corpo de massa m que se move em linha reta sob ação de uma força F que atua ao longo da linha. O trabalho feito pela força para deslocar o corpo
ENZIMAS E METABOLISMO
 ENZIMAS E METABOLISMO Metabolismo Celular é o conjunto de todas as reacções químicas celulares acompanhadas de transferência de energia. ANABOLISMO conjunto de reacções químicas que conduzem à biossíntese
ENZIMAS E METABOLISMO Metabolismo Celular é o conjunto de todas as reacções químicas celulares acompanhadas de transferência de energia. ANABOLISMO conjunto de reacções químicas que conduzem à biossíntese
Mobilidade na FEUP Deslocamento Vertical
 Mobilidade na FEUP Deslocamento Vertical Relatório Grupo 515: Carolina Correia Elder Vintena Francisco Martins Salvador Costa Sara Palhares 2 Índice Introdução...4 Objectivos...5 Método...6 Dados Obtidos...7
Mobilidade na FEUP Deslocamento Vertical Relatório Grupo 515: Carolina Correia Elder Vintena Francisco Martins Salvador Costa Sara Palhares 2 Índice Introdução...4 Objectivos...5 Método...6 Dados Obtidos...7
ESCOLA SECUNDÁRIA DR. SOLANO DE ABREU ABRANTES TURMA: I ANO: 12º ANO LETIVO 2011/2012 ATIVIDADES ESTRATÉGIAS. Diagnose da turma. Trabalho individual
 ESCOLA SECUNDÁRIA DR. SOLANO DE ABREU ABRANTES Curso Profissional de Técnico de Higiene e Segurança do Trabalho e Ambiente DISCIPLINA: FÌSICA E QUÌMICA TURMA: I ANO: 12º ANO LETIVO 2011/2012 COMPETÊNCIAS
ESCOLA SECUNDÁRIA DR. SOLANO DE ABREU ABRANTES Curso Profissional de Técnico de Higiene e Segurança do Trabalho e Ambiente DISCIPLINA: FÌSICA E QUÌMICA TURMA: I ANO: 12º ANO LETIVO 2011/2012 COMPETÊNCIAS
USP EEL - Escola de Engenharia de Lorena Reatores Aula 1 Introdução a Engenharia de Reatores
 1 - Introdução A cinética química e o projeto de reatores estão no coração de quase todos os produtos químicos industriais. É, principalmente, o conhecimento da cinética química e o projeto do reator que
1 - Introdução A cinética química e o projeto de reatores estão no coração de quase todos os produtos químicos industriais. É, principalmente, o conhecimento da cinética química e o projeto do reator que
CINÉTICA QUÍMICA CINÉTICA QUÍMICA EQUAÇÃO DE ARRHENIUS
 CINÉTICA QUÍMICA CINÉTICA QUÍMICA EQUAÇÃO DE ARRHENIUS A DEPENDÊNCIA DA VELOCIDADE DE REAÇÃO COM A TEMPERATURA A velocidade da maioria das reações químicas aumenta à medida que a temperatura também aumenta.
CINÉTICA QUÍMICA CINÉTICA QUÍMICA EQUAÇÃO DE ARRHENIUS A DEPENDÊNCIA DA VELOCIDADE DE REAÇÃO COM A TEMPERATURA A velocidade da maioria das reações químicas aumenta à medida que a temperatura também aumenta.
Tipologia, número de itens e cotação. Tipologia dos itens Número de Itens cotação 2 6 Resposta curta 1 8 3 20 Resposta restrita 2 12 3 20 Cálculo 3 12
 E s c o l a S e c u n d á r i a d e A l c á c e r d o S a l Ano letivo 2011/2012 Física e Química A Bloco II Teste Sumativo 5A Critérios de classificação ( 31/05/2012) Tipologia, número de itens e cotação
E s c o l a S e c u n d á r i a d e A l c á c e r d o S a l Ano letivo 2011/2012 Física e Química A Bloco II Teste Sumativo 5A Critérios de classificação ( 31/05/2012) Tipologia, número de itens e cotação
Matriz - Prova de recuperação modular- Cursos profissionais Física e Química- Módulo Q3- Reações Químicas Duração da Prova: 90 min (prova escrita)
 Matriz - Prova de recuperação modular- Cursos profissionais Física e Química- Módulo Q3- Reações Químicas Duração da Prova: 90 min (prova escrita) O presente documento divulga informação relativa à prova
Matriz - Prova de recuperação modular- Cursos profissionais Física e Química- Módulo Q3- Reações Químicas Duração da Prova: 90 min (prova escrita) O presente documento divulga informação relativa à prova
Leonnardo Cruvinel Furquim TERMOQUÍMICA
 Leonnardo Cruvinel Furquim TERMOQUÍMICA Termoquímica Energia e Trabalho Energia é a habilidade ou capacidade de produzir trabalho. Mecânica; Elétrica; Calor; Nuclear; Química. Trabalho Trabalho mecânico
Leonnardo Cruvinel Furquim TERMOQUÍMICA Termoquímica Energia e Trabalho Energia é a habilidade ou capacidade de produzir trabalho. Mecânica; Elétrica; Calor; Nuclear; Química. Trabalho Trabalho mecânico
Equilíbrio Químico. Hiram Araujo. Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons.
 Hiram Araujo Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode Introdução
Hiram Araujo Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode Introdução
SERÁ NECESSÁRIA UMA FORÇA PARA
 Ano Lectivo 2010/2011 Professora Fátima Pires FÍSICO-QUÍMICA SERÁ NECESSÁRIA UMA FORÇA PARA QUE UM CORPO SE MOVA? Avaliação: Professora: Observações: 11ºB «Será necessária uma força para que um corpo se
Ano Lectivo 2010/2011 Professora Fátima Pires FÍSICO-QUÍMICA SERÁ NECESSÁRIA UMA FORÇA PARA QUE UM CORPO SE MOVA? Avaliação: Professora: Observações: 11ºB «Será necessária uma força para que um corpo se
Escola de Engenharia de Lorena USP - Cinética Química Capítulo 05 Reações Irreversiveis a Volume Varíavel
 1 - Calcule a fração de conversão volumétrica (ε A) para as condições apresentadas: Item Reação Condição da Alimentação R: (ε A ) A A 3R 5% molar de inertes 1,5 B (CH 3 ) O CH 4 + H + CO 30% em peso de
1 - Calcule a fração de conversão volumétrica (ε A) para as condições apresentadas: Item Reação Condição da Alimentação R: (ε A ) A A 3R 5% molar de inertes 1,5 B (CH 3 ) O CH 4 + H + CO 30% em peso de
Cinética Química. Professora (Estagiária): Magda Vieira Professora Supervisora: Kátia Aquino. Profa. Kátia Aquino
 Cinética Química Professora (Estagiária): Magda Vieira Professora Supervisora: Kátia Aquino Profa. Kátia Aquino 1 As reações também possuem suas velocidades próprias Muito rápida: combustão http://www.franciscoevangelista.com/2012/07/incendio-residencial-com-vitima-fatal.html
Cinética Química Professora (Estagiária): Magda Vieira Professora Supervisora: Kátia Aquino Profa. Kátia Aquino 1 As reações também possuem suas velocidades próprias Muito rápida: combustão http://www.franciscoevangelista.com/2012/07/incendio-residencial-com-vitima-fatal.html
Universidade Federal de São Paulo Instituto de Ciência e Tecnologia Bacharelado em Ciência e Tecnologia
 Universidade Federal de São Paulo Instituto de Ciência e Tecnologia Bacharelado em Ciência e Tecnologia Oscilações 1. Movimento Oscilatório. Cinemática do Movimento Harmônico Simples (MHS) 3. MHS e Movimento
Universidade Federal de São Paulo Instituto de Ciência e Tecnologia Bacharelado em Ciência e Tecnologia Oscilações 1. Movimento Oscilatório. Cinemática do Movimento Harmônico Simples (MHS) 3. MHS e Movimento
1. O Fluxo de Caixa para á Análise Financeira
 ANÁLISE DE FLUXOS A DEMONSTRAÇÃO DO FLUXO DE CAIXA ESTGV-IPV Mestrado em Finanças Empresariais 1. O Fluxo de Caixa para á Análise Financeira A análise baseada nos fluxos visa ultrapassar algumas das limitações
ANÁLISE DE FLUXOS A DEMONSTRAÇÃO DO FLUXO DE CAIXA ESTGV-IPV Mestrado em Finanças Empresariais 1. O Fluxo de Caixa para á Análise Financeira A análise baseada nos fluxos visa ultrapassar algumas das limitações
4.2 Modelação da estrutura interna
 4.2 Modelação da estrutura interna AST434: C4-25/83 Para calcular a estrutura interna de uma estrela como o Sol é necessário descrever como o gás que o compõe se comporta. Assim, determinar a estrutura
4.2 Modelação da estrutura interna AST434: C4-25/83 Para calcular a estrutura interna de uma estrela como o Sol é necessário descrever como o gás que o compõe se comporta. Assim, determinar a estrutura
As Propriedades das Misturas (Aulas 18 a 21)
 As Propriedades das Misturas (Aulas 18 a 21) I Introdução Em Química, solução é o nome dado a dispersões cujo tamanho das moléculas dispersas é menor que 1 nanometro (10 Angstrons). A solução ainda pode
As Propriedades das Misturas (Aulas 18 a 21) I Introdução Em Química, solução é o nome dado a dispersões cujo tamanho das moléculas dispersas é menor que 1 nanometro (10 Angstrons). A solução ainda pode
Gabarito da Prova de Oficinas dos Velhos Ano 2008
 Gabarito da Prova de Oficinas dos Velhos Ano 2008 12 de maio de 2008 1 (a) O objetivo principal da oficina de espectroscopia é que os aprendizes aprendessem, rápido, a interpretar espectros e linhas espectrais,
Gabarito da Prova de Oficinas dos Velhos Ano 2008 12 de maio de 2008 1 (a) O objetivo principal da oficina de espectroscopia é que os aprendizes aprendessem, rápido, a interpretar espectros e linhas espectrais,
Pressão Estática, de Estagnação e Dinâmica
 Pressão Estática, de Estagnação e Dinâmica p V gz cte p 1 V z cte A pressão p que aparece na equação de Bernoulli é a pressão termodinâmica, comumente chamada de pressão estática. Para medirmos p, poderíamos
Pressão Estática, de Estagnação e Dinâmica p V gz cte p 1 V z cte A pressão p que aparece na equação de Bernoulli é a pressão termodinâmica, comumente chamada de pressão estática. Para medirmos p, poderíamos
Investimento Directo Estrangeiro e Salários em Portugal Pedro Silva Martins*
 Investimento Directo Estrangeiro e Salários em Portugal Pedro Silva Martins* Os fluxos de Investimento Directo Estrangeiro (IDE) para Portugal tornaram-se uma componente importante da economia portuguesa
Investimento Directo Estrangeiro e Salários em Portugal Pedro Silva Martins* Os fluxos de Investimento Directo Estrangeiro (IDE) para Portugal tornaram-se uma componente importante da economia portuguesa
Descobertas do electromagnetismo e a comunicação
 Descobertas do electromagnetismo e a comunicação Porque é importante comunicar? - Desde o «início dos tempos» que o progresso e o bem estar das sociedades depende da sua capacidade de comunicar e aceder
Descobertas do electromagnetismo e a comunicação Porque é importante comunicar? - Desde o «início dos tempos» que o progresso e o bem estar das sociedades depende da sua capacidade de comunicar e aceder
DISTÂNCIAS DE SEGURANÇA
 FICHA TÉCNICA DISTÂNCIAS DE SEGURANÇA Níveis GDE Temas Transversais Síntese informativa Nível 1 Nível Atitudinal; Nível 3 Nível Táctico Tema 2 - Atitudes e Comportamentos; Tema 5 - Conhecimento das Regras
FICHA TÉCNICA DISTÂNCIAS DE SEGURANÇA Níveis GDE Temas Transversais Síntese informativa Nível 1 Nível Atitudinal; Nível 3 Nível Táctico Tema 2 - Atitudes e Comportamentos; Tema 5 - Conhecimento das Regras
UNIVERSIDADE FEDERAL DO PARANÁ PROGRAMA DE PÓS GRADUAÇÃO EM ENGENHARIA DE ALIMENTOS ANÁLISES TÉRMICAS DE ALIMENTOS
 UNIVERSIDADE FEDERAL DO PARANÁ PROGRAMA DE PÓS GRADUAÇÃO EM ENGENHARIA DE ALIMENTOS ANÁLISES TÉRMICAS DE ALIMENTOS Regina Cristina A. De Lima TRANSIÇÕES DE FASE 1. Introdução Uma fase é um estado específico
UNIVERSIDADE FEDERAL DO PARANÁ PROGRAMA DE PÓS GRADUAÇÃO EM ENGENHARIA DE ALIMENTOS ANÁLISES TÉRMICAS DE ALIMENTOS Regina Cristina A. De Lima TRANSIÇÕES DE FASE 1. Introdução Uma fase é um estado específico
UM CONCEITO FUNDAMENTAL: PATRIMÔNIO LÍQUIDO FINANCEIRO. Prof. Alvaro Guimarães de Oliveira Rio, 07/09/2014.
 UM CONCEITO FUNDAMENTAL: PATRIMÔNIO LÍQUIDO FINANCEIRO Prof. Alvaro Guimarães de Oliveira Rio, 07/09/2014. Tanto as pessoas físicas quanto as jurídicas têm patrimônio, que nada mais é do que o conjunto
UM CONCEITO FUNDAMENTAL: PATRIMÔNIO LÍQUIDO FINANCEIRO Prof. Alvaro Guimarães de Oliveira Rio, 07/09/2014. Tanto as pessoas físicas quanto as jurídicas têm patrimônio, que nada mais é do que o conjunto
Lição 3. Instrução Programada
 Lição 3 É IMPORTANTE A ATENTA LEITURA DAS INSTRUÇÕES FORNECIDAS NAS LIÇÕES 1 e 2. NOSSO CURSO NÃO SE TRATA DE UM CURSO POR COR RESPONDENCIA; NÃO NOS DEVERÃO SER MAN- DADAS FOLHAS COM AS QUESTÕES PARA SEREM
Lição 3 É IMPORTANTE A ATENTA LEITURA DAS INSTRUÇÕES FORNECIDAS NAS LIÇÕES 1 e 2. NOSSO CURSO NÃO SE TRATA DE UM CURSO POR COR RESPONDENCIA; NÃO NOS DEVERÃO SER MAN- DADAS FOLHAS COM AS QUESTÕES PARA SEREM
DEPARTAMENTO DE ENGENHARIA ELÉTRICA DEE CURSO DE ENGENHARIA ELÉTRICA
 LABORATÓRIO 6: Máquina Síncrona em Barramento Infinito Objetivo: Verificar, experimentalmente, como é feita a ligação de um gerador síncrono no barramento infinito. Teoria: As necessidades de energia elétrica
LABORATÓRIO 6: Máquina Síncrona em Barramento Infinito Objetivo: Verificar, experimentalmente, como é feita a ligação de um gerador síncrono no barramento infinito. Teoria: As necessidades de energia elétrica
Variação de entalpia nas mudanças de estado físico. Prof. Msc.. João Neto
 Variação de entalpia nas mudanças de estado físico Prof. Msc.. João Neto Processo Endotérmico Sólido Líquido Gasoso Processo Exotérmico 2 3 Processo inverso: Solidificação da água A variação de entalpia
Variação de entalpia nas mudanças de estado físico Prof. Msc.. João Neto Processo Endotérmico Sólido Líquido Gasoso Processo Exotérmico 2 3 Processo inverso: Solidificação da água A variação de entalpia
Explorações de alunos
 A partir dos exemplos sugeridos e explorados pelos alunos pretende-se que possam conjecturar que, dadas duas funções reais de variável real f e g, o domínio da função quociente pode ser dado por: f f g
A partir dos exemplos sugeridos e explorados pelos alunos pretende-se que possam conjecturar que, dadas duas funções reais de variável real f e g, o domínio da função quociente pode ser dado por: f f g
SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA
 SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA QUESTÃO 01 Em uma determinada transformação foi constatado que poderia ser representada
SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA QUESTÃO 01 Em uma determinada transformação foi constatado que poderia ser representada
TERMOGRAVIMETRIA A análise termogravimétrica (TG) é uma técnica térmica onde a massa da amostra é registada em função da temperatura ou do tempo.
 TERMOGRAVIMETRIA A análise termogravimétrica (TG) é uma técnica térmica onde a massa da amostra é registada em função da temperatura ou do tempo. TERMOGRAVIMETRIA São frequentemente usados três modos distintos
TERMOGRAVIMETRIA A análise termogravimétrica (TG) é uma técnica térmica onde a massa da amostra é registada em função da temperatura ou do tempo. TERMOGRAVIMETRIA São frequentemente usados três modos distintos
CONSERVAÇÃO DA ENERGIA MECÂNICA
 Departamento de Física da Faculdade de Ciências da Universidade de Lisboa T3 Física Experimental I - 2007/08 CONSERVAÇÃO DA ENERGIA MECÂNICA 1. Objectivo Verificar a conservação da energia mecânica de
Departamento de Física da Faculdade de Ciências da Universidade de Lisboa T3 Física Experimental I - 2007/08 CONSERVAÇÃO DA ENERGIA MECÂNICA 1. Objectivo Verificar a conservação da energia mecânica de
Diagrama de transição de Estados (DTE)
 Diagrama de transição de Estados (DTE) O DTE é uma ferramenta de modelação poderosa para descrever o comportamento do sistema dependente do tempo. A necessidade de uma ferramenta deste tipo surgiu das
Diagrama de transição de Estados (DTE) O DTE é uma ferramenta de modelação poderosa para descrever o comportamento do sistema dependente do tempo. A necessidade de uma ferramenta deste tipo surgiu das
P3 - PROVA DE QUÍMICA GERAL - 13/11/07
 P3 - PROVA DE QUÍMICA GERAL - 3//07 Nome: GABARITO Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão Dados gerais: G = - n F E o a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 0,0 RT ΔE = ΔE lnq nf G
P3 - PROVA DE QUÍMICA GERAL - 3//07 Nome: GABARITO Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão Dados gerais: G = - n F E o a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 0,0 RT ΔE = ΔE lnq nf G
ENEM 2014/2015 Física (Prova Amarela) Prof. Douglas Almeida
 Questão 46 Nesta questão, o candidato precisa saber que um filtro de luz realiza a refração seletiva, deixando passar as cores que o compõe e absorvendo substancialmente as outras cores. Assim, para absorver
Questão 46 Nesta questão, o candidato precisa saber que um filtro de luz realiza a refração seletiva, deixando passar as cores que o compõe e absorvendo substancialmente as outras cores. Assim, para absorver
Capítulo 16. Gravitação. Página 231
 Capítulo 16 Gravitação Página 231 O peso de um corpo é consequência da força de gravidade com que o corpo é atraído pela Terra ou por outro astro. É medido com dinamômetro. Não levando em conta os efeitos
Capítulo 16 Gravitação Página 231 O peso de um corpo é consequência da força de gravidade com que o corpo é atraído pela Terra ou por outro astro. É medido com dinamômetro. Não levando em conta os efeitos
Prova Escrita de Física e Química A
 EXAME NACIONAL DO ENSINO SECUNDÁRIO Decreto-Lei n.º 19/2012, de 5 de julho Prova Escrita de Física e Química A 10.º e 11.º Anos de Escolaridade Prova 715/1.ª Fase Critérios de Classificação 1 Páginas 201
EXAME NACIONAL DO ENSINO SECUNDÁRIO Decreto-Lei n.º 19/2012, de 5 de julho Prova Escrita de Física e Química A 10.º e 11.º Anos de Escolaridade Prova 715/1.ª Fase Critérios de Classificação 1 Páginas 201
Ao descolarmos de uma grande altitude a densidade diminui, o que acontece à sustentação?
 O que é a aerodinâmica? Aerodinâmica é o estudo do ar em movimento e das forças que actuam em superfícies sólidas, chamadas asas, que se movem no ar. Aerodinâmica deriva do grego "aer", ar, e "dynamis",
O que é a aerodinâmica? Aerodinâmica é o estudo do ar em movimento e das forças que actuam em superfícies sólidas, chamadas asas, que se movem no ar. Aerodinâmica deriva do grego "aer", ar, e "dynamis",
Modelo de Intervenção em Crises., Modelo Centrado em Tarefas
 Modelo de Intervenção em Crises, Modelo Centrado em Tarefas o O que é uma crise? * E porque acontece? *alteração que se dá no equilíbrio do indivíduo, quando este numa dada altura da sua vida dá por si
Modelo de Intervenção em Crises, Modelo Centrado em Tarefas o O que é uma crise? * E porque acontece? *alteração que se dá no equilíbrio do indivíduo, quando este numa dada altura da sua vida dá por si
Matéria: Química Assunto: Materiais Prof. Gilberto Ramos
 Matéria: Química Assunto: Materiais Prof. Gilberto Ramos Química Materiais, suas propriedades e usos Estados Físicos Estado vem do latim status (posição,situação, condição,modo de estar). O estado físico
Matéria: Química Assunto: Materiais Prof. Gilberto Ramos Química Materiais, suas propriedades e usos Estados Físicos Estado vem do latim status (posição,situação, condição,modo de estar). O estado físico
Capítulo 2. A 1ª Lei da Termodinâmica
 Capítulo 2. A 1ª Lei da Termodinâmica Parte 1: trabalho, calor e energia; energia interna; trabalho de expansão; calor; entalpia Baseado no livro: Atkins Physical Chemistry Eighth Edition Peter Atkins
Capítulo 2. A 1ª Lei da Termodinâmica Parte 1: trabalho, calor e energia; energia interna; trabalho de expansão; calor; entalpia Baseado no livro: Atkins Physical Chemistry Eighth Edition Peter Atkins
Prova de Química e Biologia
 Provas Especialmente Adequadas Destinadas a Avaliar a Capacidade para a Frequência dos Cursos Superiores do IPVC dos Maiores de 23 Anos Prova de Química e Biologia Prova modelo Prova Específica de Química
Provas Especialmente Adequadas Destinadas a Avaliar a Capacidade para a Frequência dos Cursos Superiores do IPVC dos Maiores de 23 Anos Prova de Química e Biologia Prova modelo Prova Específica de Química
CAPÍTULO 4 - BALANÇOS MATERIAIS. Existem dois tipos fundamentais de entidade em termodinâmica, estados de um sistema, e os processos de um sistema.
 Existem dois tipos fundamentais de entidade em termodinâmica, estados de um sistema, e os processos de um sistema. Sempre que duas ou mais propriedades de um sistema variam, diz-se que ocorreu um processo.
Existem dois tipos fundamentais de entidade em termodinâmica, estados de um sistema, e os processos de um sistema. Sempre que duas ou mais propriedades de um sistema variam, diz-se que ocorreu um processo.
Anexo A Categorização das respostas dos alunos às questões antes de ensino e pós-ensino na Actividade de Aprendizagem 1
 Anexos CD Anexo A Categorização das respostas dos alunos às questões antes de ensino e pós-ensino na Actividade de Aprendizagem 1 Qual é o efeito da variação de temperatura no estado físico da água líquida?
Anexos CD Anexo A Categorização das respostas dos alunos às questões antes de ensino e pós-ensino na Actividade de Aprendizagem 1 Qual é o efeito da variação de temperatura no estado físico da água líquida?
Efeito Osmótico de Soluções de Concentração Diferente na Membrana de um Ovo de Codorniz
 Efeito Osmótico de Soluções de Concentração Diferente na Membrana de um Ovo de Codorniz Rui Pedro Lousa das Neves Bioquímica Grupo 3 Coimbra 05/05/99 Introdução Se entre dois meios com diferentes concentrações
Efeito Osmótico de Soluções de Concentração Diferente na Membrana de um Ovo de Codorniz Rui Pedro Lousa das Neves Bioquímica Grupo 3 Coimbra 05/05/99 Introdução Se entre dois meios com diferentes concentrações
PROVA DE QUÍMICA - 1998 Segunda Etapa
 PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
Escola Secundária Dom Manuel Martins
 Escola Secundária Dom Manuel Martins Setúbal Prof. Carlos Cunha 4ª Ficha de Avaliação FÍSICO QUÍMICA A ANO LECTIVO 2008 / 2009 ANO 2 N. º NOME: TURMA: B CLASSIFICAÇÃO Devido ao crescimento da população
Escola Secundária Dom Manuel Martins Setúbal Prof. Carlos Cunha 4ª Ficha de Avaliação FÍSICO QUÍMICA A ANO LECTIVO 2008 / 2009 ANO 2 N. º NOME: TURMA: B CLASSIFICAÇÃO Devido ao crescimento da população
Início 15.09.11 03.01.12 10.04.12 Final 16.12.11 23.03.12 08.06.12 Interrupções - 20 22 Fev 2012 -
 TOTAL Outras Atividades Tema B: Terra em Transformação Tema A: Terra no Espaço Departamento de Matemática e Ciências Experimentais PLANIFICAÇÃO 7º Ano de Ciências Físico-Químicas Ano Letivo 2011 / 2012
TOTAL Outras Atividades Tema B: Terra em Transformação Tema A: Terra no Espaço Departamento de Matemática e Ciências Experimentais PLANIFICAÇÃO 7º Ano de Ciências Físico-Químicas Ano Letivo 2011 / 2012
Energia, tecnologia e política climática: perspectivas mundiais para 2030 MENSAGENS-CHAVE
 Energia, tecnologia e política climática: perspectivas mundiais para 2030 MENSAGENS-CHAVE Cenário de referência O estudo WETO apresenta um cenário de referência que descreve a futura situação energética
Energia, tecnologia e política climática: perspectivas mundiais para 2030 MENSAGENS-CHAVE Cenário de referência O estudo WETO apresenta um cenário de referência que descreve a futura situação energética
Leis de Newton. Dinâmica das partículas Física Aplicada http://www.walmorgodoi.com
 Leis de Newton Dinâmica das partículas Física Aplicada http://www.walmorgodoi.com Antes de Galileu Durante séculos, o estudo do movimento e suas causas tornou-se o tema central da filosofia natural. Antes
Leis de Newton Dinâmica das partículas Física Aplicada http://www.walmorgodoi.com Antes de Galileu Durante séculos, o estudo do movimento e suas causas tornou-se o tema central da filosofia natural. Antes
TIC Unidade 2 Base de Dados. Informação é todo o conjunto de dados devidamente ordenados e organizados de forma a terem significado.
 Conceitos relativos à Informação 1. Informação O que á a informação? Informação é todo o conjunto de dados devidamente ordenados e organizados de forma a terem significado. 2. Dados Em informática designa-se
Conceitos relativos à Informação 1. Informação O que á a informação? Informação é todo o conjunto de dados devidamente ordenados e organizados de forma a terem significado. 2. Dados Em informática designa-se
NCRF 19 Contratos de construção
 NCRF 19 Contratos de construção Esta Norma Contabilística e de Relato Financeiro tem por base a Norma Internacional de Contabilidade IAS 11 - Contratos de Construção, adoptada pelo texto original do Regulamento
NCRF 19 Contratos de construção Esta Norma Contabilística e de Relato Financeiro tem por base a Norma Internacional de Contabilidade IAS 11 - Contratos de Construção, adoptada pelo texto original do Regulamento
Capítulo 4 Trabalho e Energia
 Capítulo 4 Trabalho e Energia Este tema é, sem dúvidas, um dos mais importantes na Física. Na realidade, nos estudos mais avançados da Física, todo ou quase todos os problemas podem ser resolvidos através
Capítulo 4 Trabalho e Energia Este tema é, sem dúvidas, um dos mais importantes na Física. Na realidade, nos estudos mais avançados da Física, todo ou quase todos os problemas podem ser resolvidos através
Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron:
 Equação de Estado de Van der Waals Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron: P i V i = nrt em que colocamos
Equação de Estado de Van der Waals Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron: P i V i = nrt em que colocamos
DEPENDÊNCIA DA VELOCIDADE COM A TEMPERATURA Camilo Andrea Angelucci
 DPNDÊNCIA DA VLOCIDAD COM A TMPRATURA Camilo Andrea Angelucci MTA Apresentar os conceitos da infl uência da temperatura na velocidade das reações químicas. OBJTIVOS Ao fi nal desta aula, o aluno deverá:
DPNDÊNCIA DA VLOCIDAD COM A TMPRATURA Camilo Andrea Angelucci MTA Apresentar os conceitos da infl uência da temperatura na velocidade das reações químicas. OBJTIVOS Ao fi nal desta aula, o aluno deverá:
Pisa 2012: O que os dados dizem sobre o Brasil
 Pisa 2012: O que os dados dizem sobre o Brasil A OCDE (Organização para Cooperação e Desenvolvimento Econômico) divulgou nesta terça-feira os resultados do Programa Internacional de Avaliação de Alunos,
Pisa 2012: O que os dados dizem sobre o Brasil A OCDE (Organização para Cooperação e Desenvolvimento Econômico) divulgou nesta terça-feira os resultados do Programa Internacional de Avaliação de Alunos,
Profa. Dra. Vivian C. C. Hyodo
 Profa. Dra. Vivian C. C. Hyodo A Energia e suas Fontes Fontes de Energia Renováveis Fontes de Energia Não-Renováveis Conclusões Energia: Capacidade de realizar trabalho Primeira Lei da Termodinâmica: No
Profa. Dra. Vivian C. C. Hyodo A Energia e suas Fontes Fontes de Energia Renováveis Fontes de Energia Não-Renováveis Conclusões Energia: Capacidade de realizar trabalho Primeira Lei da Termodinâmica: No
Linguagem da Termodinâmica
 Linguagem da Termodinâmica Termodinâmica N A = 6,022 10 23 Ramo da Física que estuda sistemas que contêm um grande nº de partículas constituintes (átomos, moléculas, iões,...), a partir da observação das
Linguagem da Termodinâmica Termodinâmica N A = 6,022 10 23 Ramo da Física que estuda sistemas que contêm um grande nº de partículas constituintes (átomos, moléculas, iões,...), a partir da observação das
Capítulo 3. Avaliação de Desempenho. 3.1 Definição de Desempenho
 20 Capítulo 3 Avaliação de Desempenho Este capítulo aborda como medir, informar e documentar aspectos relativos ao desempenho de um computador. Além disso, descreve os principais fatores que influenciam
20 Capítulo 3 Avaliação de Desempenho Este capítulo aborda como medir, informar e documentar aspectos relativos ao desempenho de um computador. Além disso, descreve os principais fatores que influenciam
Introdução. Procura, oferta e intervenção. Cuidados continuados - uma visão económica
 Cuidados continuados - uma visão económica Pedro Pita Barros Faculdade de Economia Universidade Nova de Lisboa Introdução Área geralmente menos considerada que cuidados primários e cuidados diferenciados
Cuidados continuados - uma visão económica Pedro Pita Barros Faculdade de Economia Universidade Nova de Lisboa Introdução Área geralmente menos considerada que cuidados primários e cuidados diferenciados
saber identificar as ideias principais, organizá las e relacioná las com as anteriores;
 Leitura na diagonal É um tipo de leitura rápida, em que o objectivo é procurar uma informação específica ou identificar as ideias principais de um texto, que te vai permitir organizar melhor o teu estudo.
Leitura na diagonal É um tipo de leitura rápida, em que o objectivo é procurar uma informação específica ou identificar as ideias principais de um texto, que te vai permitir organizar melhor o teu estudo.
SISTEMAS DE INFORMAÇÃO PARA GESTÃO
 07-05-2013 1 SISTEMAS DE INFORMAÇÃO PARA GESTÃO Aula I Docente: Eng. Hercílio Duarte 07-05-2013 2 Objectivo Sistemas Modelos Dados Vs. Informação Introdução aos sistemas de Informação 07-05-2013 3 Introdução
07-05-2013 1 SISTEMAS DE INFORMAÇÃO PARA GESTÃO Aula I Docente: Eng. Hercílio Duarte 07-05-2013 2 Objectivo Sistemas Modelos Dados Vs. Informação Introdução aos sistemas de Informação 07-05-2013 3 Introdução
Química Analítica Avançada: Volumetria de Neutralização. Prof a Lilian Silva 2011
 Química Analítica Avançada: Volumetria de Neutralização Prof a Lilian Silva 2011 INTRODUÇÃO À VOLUMETRIA TITULAÇÃO Processo no qual uma solução padrão ou solução de referência é adicionada a uma solução
Química Analítica Avançada: Volumetria de Neutralização Prof a Lilian Silva 2011 INTRODUÇÃO À VOLUMETRIA TITULAÇÃO Processo no qual uma solução padrão ou solução de referência é adicionada a uma solução
Como organizar um processo de planejamento estratégico
 Como organizar um processo de planejamento estratégico Introdução Planejamento estratégico é o processo que fixa as grandes orientações que permitem às empresas modificar, melhorar ou fortalecer a sua
Como organizar um processo de planejamento estratégico Introdução Planejamento estratégico é o processo que fixa as grandes orientações que permitem às empresas modificar, melhorar ou fortalecer a sua
5. Métodos ágeis de desenvolvimento de software
 Engenharia de Software 5. Métodos ágeis de desenvolvimento de software Nuno Miguel Gil Fonseca [email protected] Desenvolver e entregar software o mais rapidamente possível é hoje em dia um dos
Engenharia de Software 5. Métodos ágeis de desenvolvimento de software Nuno Miguel Gil Fonseca [email protected] Desenvolver e entregar software o mais rapidamente possível é hoje em dia um dos
Guia de Estudo Folha de Cálculo Microsoft Excel
 Tecnologias da Informação e Comunicação Guia de Estudo Folha de Cálculo Microsoft Excel Estrutura geral de uma folha de cálculo: colunas, linhas, células, endereços Uma folha de cálculo electrónica ( electronic
Tecnologias da Informação e Comunicação Guia de Estudo Folha de Cálculo Microsoft Excel Estrutura geral de uma folha de cálculo: colunas, linhas, células, endereços Uma folha de cálculo electrónica ( electronic
Princípios de Bioenergética
 Universidade Federal do Ceará Centro de Ciências Departamento de Bioquímica e Biologia Molecular Disciplina de Introdução a Bioquímica Princípios de Bioenergética 1. Conceitos Básicos 1.1. Conceito de
Universidade Federal do Ceará Centro de Ciências Departamento de Bioquímica e Biologia Molecular Disciplina de Introdução a Bioquímica Princípios de Bioenergética 1. Conceitos Básicos 1.1. Conceito de
Fase Identifica um estado uniforme de
 DIAGRAMAS DE FASES Definições Fase Identifica um estado uniforme de matéria, não só no que se refere à composição química, mas também no que se refere ao estado físico. Número de fases numa mistura P 1
DIAGRAMAS DE FASES Definições Fase Identifica um estado uniforme de matéria, não só no que se refere à composição química, mas também no que se refere ao estado físico. Número de fases numa mistura P 1
CONTEÚDOS OBJETIVOS PERÍODO
 ESCOLA BÁSICA2,3 EUGÉNIO DOS SANTOS 2013 2014 página 1 ESCOLA BÁSICA DO 2.º E 3.º CICLOS EUGÉNIO DOS SANTOS PLANIFICAÇÃO E METAS DE APRENDIZAGEM DA DISCIPLINA DE CIÊNCIAS FÍSICO-QUÍMICAS 8.º ANO DE ESCOLARIDADE
ESCOLA BÁSICA2,3 EUGÉNIO DOS SANTOS 2013 2014 página 1 ESCOLA BÁSICA DO 2.º E 3.º CICLOS EUGÉNIO DOS SANTOS PLANIFICAÇÃO E METAS DE APRENDIZAGEM DA DISCIPLINA DE CIÊNCIAS FÍSICO-QUÍMICAS 8.º ANO DE ESCOLARIDADE
Força atrito. Forças. dissipativas
 Veículo motorizado 1 Trabalho Ocorrem variações predominantes de Por ex: Forças constantes Sistema Termodinâmico Onde atuam Força atrito É simultaneamente Onde atuam Sistema Mecânico Resistente Ocorrem
Veículo motorizado 1 Trabalho Ocorrem variações predominantes de Por ex: Forças constantes Sistema Termodinâmico Onde atuam Força atrito É simultaneamente Onde atuam Sistema Mecânico Resistente Ocorrem
Exactidão da medição
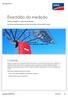 Exactidão da medição Valores energéticos e grau de rendimento dos inversores fotovoltaicos do tipo Sunny Boy e Sunny Mini Central Conteúdo Qualquer operador de um sistema fotovoltaico deseja estar o mais
Exactidão da medição Valores energéticos e grau de rendimento dos inversores fotovoltaicos do tipo Sunny Boy e Sunny Mini Central Conteúdo Qualquer operador de um sistema fotovoltaico deseja estar o mais
ANÁLISE QUÍMICA INSTRUMENTAL
 ANÁLISE QUÍMICA INSTRUMENTAL CROMATOGRAFIA 2 1 6 Ed. Cap. 10 268-294 6 Ed. Cap. 6 Pg.209-219 6 Ed. Cap. 28 Pg.756-829 6 Ed. Cap. 21 Pg.483-501 3 Separação Química Princípios de uma separação. Uma mistura
ANÁLISE QUÍMICA INSTRUMENTAL CROMATOGRAFIA 2 1 6 Ed. Cap. 10 268-294 6 Ed. Cap. 6 Pg.209-219 6 Ed. Cap. 28 Pg.756-829 6 Ed. Cap. 21 Pg.483-501 3 Separação Química Princípios de uma separação. Uma mistura
Lista de Exercícios 4 Indústrias Químicas Resolução pelo Monitor: Rodrigo Papai de Souza
 Lista de Exercícios 4 Indústrias Químicas Resolução pelo Monitor: Rodrigo Papai de Souza 1) a-) Calcular a solubilidade do BaSO 4 em uma solução 0,01 M de Na 2 SO 4 Dissolução do Na 2 SO 4 : Dado: BaSO
Lista de Exercícios 4 Indústrias Químicas Resolução pelo Monitor: Rodrigo Papai de Souza 1) a-) Calcular a solubilidade do BaSO 4 em uma solução 0,01 M de Na 2 SO 4 Dissolução do Na 2 SO 4 : Dado: BaSO
COMO CALCULAR A PERFORMANCE DOS FUNDOS DE INVESTIMENTOS - PARTE II
 COMO CALCULAR A PERFORMANCE DOS FUNDOS DE INVESTIMENTOS - PARTE II O que é o Índice de Treynor? Índice de Treynor x Índice de Sharpe Restrições para as análises de Sharpe e Trynor A utilização do risco
COMO CALCULAR A PERFORMANCE DOS FUNDOS DE INVESTIMENTOS - PARTE II O que é o Índice de Treynor? Índice de Treynor x Índice de Sharpe Restrições para as análises de Sharpe e Trynor A utilização do risco
Ciências Físico - Químicas. Planificação de uma Actividade Laboratorial No contexto dos Novos Programas
 ESCOLA SECUNDÁRIA NUNO ÁLVARES CASTELO BRANCO Ciências Físico - Químicas Planificação de uma Actividade Laboratorial No contexto dos Novos Programas Trabalho elaborado por: Célia Maria Antunes Dias Castelo
ESCOLA SECUNDÁRIA NUNO ÁLVARES CASTELO BRANCO Ciências Físico - Químicas Planificação de uma Actividade Laboratorial No contexto dos Novos Programas Trabalho elaborado por: Célia Maria Antunes Dias Castelo
ESTUDO DA CINÉTICA DE HIDRÓLISE ÁCIDA DO COMPOSTO Trans-[(Co(en) 2 Cl 2 )Cl]
![ESTUDO DA CINÉTICA DE HIDRÓLISE ÁCIDA DO COMPOSTO Trans-[(Co(en) 2 Cl 2 )Cl] ESTUDO DA CINÉTICA DE HIDRÓLISE ÁCIDA DO COMPOSTO Trans-[(Co(en) 2 Cl 2 )Cl]](/thumbs/26/8060460.jpg) TRABALHO 3 ESTUDO DA CINÉTICA DE HIDRÓLISE ÁCIDA DO COMPOSTO Trans-[(Co(en) 2 Cl 2 )Cl] 1. OBJECTIVO Estudo da cinética da reacção de hidrólise ácida do composto Trans-[Co(en) 2 Cl 2 ]Cl. Determinação
TRABALHO 3 ESTUDO DA CINÉTICA DE HIDRÓLISE ÁCIDA DO COMPOSTO Trans-[(Co(en) 2 Cl 2 )Cl] 1. OBJECTIVO Estudo da cinética da reacção de hidrólise ácida do composto Trans-[Co(en) 2 Cl 2 ]Cl. Determinação
Manual de Utilizador. Disciplina de Projecto de Sistemas Industriais. Escola Superior de Tecnologia. Instituto Politécnico de Castelo Branco
 Escola Superior de Tecnologia Instituto Politécnico de Castelo Branco Departamento de Informática Curso de Engenharia Informática Disciplina de Projecto de Sistemas Industriais Ano Lectivo de 2005/2006
Escola Superior de Tecnologia Instituto Politécnico de Castelo Branco Departamento de Informática Curso de Engenharia Informática Disciplina de Projecto de Sistemas Industriais Ano Lectivo de 2005/2006
Segurança e Higiene no Trabalho
 Guia Técnico Segurança e Higiene no Trabalho Volume III Análise de Riscos um Guia Técnico de Copyright, todos os direitos reservados. Este Guia Técnico não pode ser reproduzido ou distribuído sem a expressa
Guia Técnico Segurança e Higiene no Trabalho Volume III Análise de Riscos um Guia Técnico de Copyright, todos os direitos reservados. Este Guia Técnico não pode ser reproduzido ou distribuído sem a expressa
Estudaremos aqui como essa transformação pode ser entendida a partir do teorema do trabalho-energia.
 ENERGIA POTENCIAL Uma outra forma comum de energia é a energia potencial U. Para falarmos de energia potencial, vamos pensar em dois exemplos: Um praticante de bungee-jump saltando de uma plataforma. O
ENERGIA POTENCIAL Uma outra forma comum de energia é a energia potencial U. Para falarmos de energia potencial, vamos pensar em dois exemplos: Um praticante de bungee-jump saltando de uma plataforma. O
Termodinâmica Química Lista 2: 1 a Lei da Termodinâmica. Resolução comentada de exercícios selecionados
 Termodinâmica Química Lista 2: 1 a Lei da Termodinâmica. Resolução comentada de exercícios selecionados Prof. Fabrício R. Sensato Semestre 4º Engenharia: Materiais Período: Matutino/diurno Regimes: Normal/DP
Termodinâmica Química Lista 2: 1 a Lei da Termodinâmica. Resolução comentada de exercícios selecionados Prof. Fabrício R. Sensato Semestre 4º Engenharia: Materiais Período: Matutino/diurno Regimes: Normal/DP
