Química B Intensivo V. 1
|
|
|
- Nathalia Cortês Oliveira
- 9 Há anos
- Visualizações:
Transcrição
1 GABARIT Química B Intensivo V. 1 Exercícios 01) C 02) E Quando substâncias são colocadas em um mesmo sistema, a mais densa "afunda" e a menos densa "flutua". Assim, em relação à água, de densidade 1g/mL, flutuariam as substâncias de densidade menor água: gasolina (0,80) e óleo comestível (0,90). Densidade do mercúrio d = m v d = 1370 g d = 137 g/ml 100 ml Densidade do cubo A: d = 14 g 2 ml d = 7 g/ml Densidade do cubo B: d = 20 g = 10 g/ml 2 ml s dois cubos são menos densos que o mercúrio e, assim, flutuarão. 03) 28 volume ocupado pela areia sem ar deve ser calculado pelo aumento do volume na água: Água: 25 ml Água + areia: 39 ml Volume ocupado pela areia: = 14 ml Volume inicial de areia: 25 ml (areia + ar) Volume do ar: 25 ml 14 ml (areia pura) = 11 ml Densidade da areia: d = m v d = 40, 6 g = 2,9 g/ml 14 ml Soma final: ,9 = 27,9 28 (número inteiro mais próximo) 04) E Para o cálculo da densidade da mistura, utiliza-se a média ponderada: d = d = 100 d = d = 808 g/l Valores maiores que 808 g/l representam uma mistura com mais de 4% de água, o que é ilegal. valor de 805 g/l representa menos que 4% de água e mais de 96% de álcool, ou seja, o combustível é mais puro. Isso pode ocorrer. que não pode é o combustível ter mais água que o estipulado. 05) a) Porque água (polar) e gasolina (apolar) não se misturam. b) 21% c) Não, pois o percentual da mistura está dentro da margem permitida. A diferença nos volumes ocorre pois o álcool, por ter maior afinidade com a água, passa da gasolina para a fase aquosa da mistura. Assim, calcula-se o volume de álcool: 30 ml 23,7 ml = 6,3 ml gasolina gasolina + pura álcool % de álcool: 30 ml 100% 6,3 ml x% x = x = 21%, dentro da margem permitida (18 24%) sistema apresenta duas fases: gasolina (apolar) e água + álcool (polar). 06) líquido, gasoso, líquido, líquido, gasoso. Uma substância estaráno estado físico sólido quando a temperatura em que estiver for menor que seu ponto de fusão (sólido para líquido). Será liquida quando estiver em temperatura maior que o ponto de fusão e menor que o ponto de ebulição e será gasosa quando estiver em ttemperatura maior que seu ponto de ebulição. SÓLID Ponto de fusão LÍQUID Ponto de ebulição GASS Química B 1
2 GABARIT 07) E Para 50 C (deserto da Arábia): Clorofórmio: 50 C é maior que 63 C e menor que 61 C líquido; Éter etílico: 50 C é maior que 116 C e que 34 C gasoso; Etanol: 50 C é maior que 117 C e menor que 78 C líquido; Fenol: 50 C é maior que 41 C e menor que 182 C líquido; Pentano: 50 C é maior que 130 C e que 36 C gasoso. CH 3 CH Temperatura do ambiente: 150 C (temperatura do óleo). Ácido acético evapora acima de 118 C (ponto de ebulição). Estado físico: gasoso. Br 2 Temperatura do ambiente: 0 C (temperatura da água com gelo). Bromo congela abaixo de 7 C (ponto de fusão) e evapora acima de 59 C (ponto de ebulição). Estado físico: líquido (temperatura do ambiente entre os pontos de fusão e ebulição). 08) Nenhuma 09) E 1. Errada o processo I é a sublimação; 2. Errada o processo II (solidificação) ocorre com liberação de calor; 3. Errada na condensação as moléculas se aprximam, há diminuição de volume com consequente aumento de densidade. Densidade e volume são inversamente proporcionais; 4. Errada moléculas no estado gasoso são mais sensíveis a variação de volume por efeito de pressão; 5. Errada moléculas no estado gasoso são mais sensíveis a variação de volume por efeito de pressão; 6. Errada o vapor d'água ocorre em maior temperatura. Assim, possui maior energia que a água líquida ou sólida. I. 45 C é maior que 63,5 C (P.F.) e menor que 61,7 C (P.E.) líquido; II. 45 C é maior que 34,5 C (P.E.) gasoso; III. 45 C é menor que 54 C (P.F.) sólido; IV. 45 C é maior que 43 C (P.F.) e menor que 181,8 C (P.E.) líquido. 10) B 11) A 12) B 13) B 14) B a) Errada. I e IV são líquidas na temperatura apresentada. b) Errada. Estão nos estados líquido, gasoso, sólido e líquido. c) Errada. Estão nos estados gasoso e sólido. d) Errada. Estão nos estados líquido, gasoso, sólido e líquido. e) Certa. I. Ponto de fusão e ponto de ebulição variam mistura comum; II. Ponto de fusão e ponto de ebulição fixos substância pura; III. Ponto de fusão variável e ponto de ebulição fixo mistura azeotrópica. Curva AA': ponto de fusão e ponto de ebulição fixos substância pura; Curva BB': variação de temperatura durante a mudança de estado físico mistura (quando homogênea, é chamada simplesmente de solução). A sublimação, que comumente ocorre com a naftalina, é a passagem do estado físico sólido diretamente para o estado físico gasoso, sem aparente passagem pelo estado líquido. Processo endotérmico ocorre com absorção de calor. Processo exotérmico ocorre com liberação de calor. a) Errada. liquefação (gasoso para líquido) exotérmico; solidificação (líquido para sólido) exotérmico. b) Certa. fusão (sólido para líquido) endotérmico; condensação (gassoso para líquido) exotérmico. c) Errada. condensação (gasoso para líquido) exotérmico; sublimação (solido para gasoso) endotérmico. d) Errada. evaporação (líquido para gasoso) endotérmico; fusão (sólido para líquido) endotérmico. e) Errada. solidificação (líquido para sólido) exotérmico; evaporação (líquido para gasoso) endotéremico. a) Certa. Vaporização é o nome que se dá para a mudança do estado líquido para o gasoso. b) Errada. A água pode evaporar em temperaturas diferentes, quando se varia a pressão. 2 Química B
3 GABARIT 15) B 16) A 17) E 18) C c) Certa. Vaporização é a passagem do líquido para o gasoso. Ebulição é um tipo de vaporização com aquecimento artificial. d) Certa. A calefação é a passagem do líquido para o gasoso (vaporização) de forma praticamente instantânea. e) Certa. A vaporização ocorre com absorção de energia (processo endotérmico). a) Errada. As transformações são físicas com mudança de estado físico apenas. b) Certa. A passagem de sólido para vapor diretamente se chama sublimação. c) Errada. A eliminação de água não altera as características químicas do alimento. d) Errada. s alimentos desidratados podem ser reconstituídos com a reintrodução de água. A intenção do processo é que não ocorra alterações nas características do alimento, quando reidratado; e) Errada. Variações na pressão modificam os pontos de fusão e ebulição. a) Certa. A ferrugem é uma reação química em que o ferro reage com o oxigênio do ar dando origem a um óxido (formação de novas substâncias). b) Errada. A passagem de estado físico caracteriza fenômeno físico (sem formação de novas substâncias). c) Errada. A lata amassada não caracteriza processo químico, e sim físico. d) Errada. A transformação da água em gelo, solidificação, é um fenômeno físico. ponto de ebulição é a temperatura na qual ocorre a mudança de estado físico, com passagem do estado líquido para o vapor. Com a mudança, as ligações intermoleculares são rompidas, mas não as ligações intramoleculares. Assim, sem a formação de novas substâncias, é caracterizado como um fenômeno físico. 1) Errada. Um pedaço de isopor flutuando é um fenômeno físico (sem alteração da matéria). 2) Certa. açúcar ao caramelar sofre reação química com formação de novas substâncias. 3) Certa. A liberação de gás é um sinal claro de reação química entre o ferro e o ácido. 4) Errada. A dissolução do sal não caracteriza reação química, apenas a separação dos íons por efeito da dissolução em água. 5) Errada. A atração do prego pelo imã é um processo físico, sem alteração na matéria. 19) B 20) E 21) A 22) B 1) Químico o crescimento de pelos e unhas é fenômeno químico pois envolve a formação da queratina através de reação química. 2) Físico a passagem de moléculas não implica reação química. 3) Químico a digestão envolve uma série de reações químicas, com formação de novas substâncias. 4) Químico formam-se novas substâncias. 5) Físico na emulsificação tem-se uma ação semelhante à de um detergente, fazendo com que a gordura forme uma emulsão com água, porém sem reação química. que ocorre é que as moléculas dos sais biliares possuem uma parte polar, onde captam a água, e uma parte apolar, onde captam a gordura. A gordura e a água não reagem entre si. 6) Químico ocorre reação química na formação do sistema tampão. 7) Físico como outras filtrações, a filtração que ocorre nos glomérulos renais não envolve reação química. a) Errada todas são substâncias simples; b) Errada substância simples, elemento e substância composta; c) Errada elementos, substância composta e elemento; d) Errada substância composta, substância simples e cubstância simples; e) Certa elemento, substância simples e substância composta. Número de elementos: cada tipo diferente de bolinha 4 tipos (clara, escura, riscada, e escura maior); Número de átomos: total de bolinhas 12; Número de substâncias: cada tipo diferente de molécula 4 (há duas moléculas que são iguais); Número de moléculas: cada conjunto de bolinhas representa uma molécula 5. Mistura: leite (II) formado por várias substâncias diferentes; Composto ou substância composta: brometo de potássio (III) é substância pura, formada por mais de um elemento químico (bromo e potássio); Elemento: prata (I) formado apenas por átomos de prata. Sequência: II, III, I. Química B 3
4 GABARIT 23) C 24) E 25) A 26) E 27) A a) Errada água ( ), gás clorídrico (HC ) e gás carbônico (C 2 ) são substâncias compostas; b) Errada gás carbônico (C 2 ) é substância composta; c) Certa todas substâncias simples (, 2, C 2, 3 ) d) Errada água ( ) e gás carbônico (C 2 ) são substâncias compostas; e) Errada gás carbônico (C 2 ) e gás clorídrico (HC ) são substâncias compostas; a) Errada grafite e fósforo vermelho formam substâncias puras; b) Errada ferro, enxofre e mercúrio substâncias puras; c) Errada açúcar e metanol são substâncias compostas; d) Errada álcool absoluto e gás amoníaco são substâncias compostas; e) Certa todas são misturas. I. gelo (1 fase), água (1 fase), óleo (1 fase) = 3 fases (apenas 2 componentes); II. água (1 fase), gás (1 fase), gelo (1 fase) = 3 fases (apenas 2 componentes); III. gelo (1 fase), óleo (1 fase), salmoura leve (1 fase), granito (3 fases) = 6 fases (6 componentes). bs.: A salmoura é a mistura de sal e água. A informação salmoura leve serve para a dedução de que a mistura é homogênea, de modo que todo o sal está dissolvido, ou seja, possui uma única fase. granito possui três fases pois é formado por 3 minerais: quartzo, mica e feldspato. Cada substância diferente é um componente: Açúcar, limalha de ferro (ferro em pó ), nitrogênio, água e vapor d'água = 4 componentes (lembrando que água e vapor d'água são o mesmo componente mesma substância); Fases: limalha de ferro (1 fase), açúcar dissolvido em água (1 fase), nitrogênio e vapor d água (1 fase) = 3 fases; sistema é heterogêneo pois possui mais de uma fase (trifásico). Areia: 1 fase Sal, açúcar, água: 1 fase Diesel (óleo): 1 fase Total: 3 fases 28) D 29) A 30) D 31) B 32) E 33) D I. N 2 e 2 mistura homogênea ou solução (toda mistura de gases é homogênea). II. Enxofre e água mistura heterogênea (não se misturam). III. Glicose sólida substância pura composta. IV. Álcool de supermercado mistura homogênea (o álcool de supermercado tem água na composição e proporção variável. mais comum é o 92,8 GL com 92,8% de álcool e o restante de água). I. Leite mistura homogênea de vários componentes. II. Água substância pura composta (formada por dois elementos). III. Sopa de galinha mistura heterogênea (água, galinha, etc). IV. Soro caseiro mistura homogênea de água, açúcar e sal. a) Errada. São 2 átomos de hidrogênio e 1 átomo de oxigênio ( ). b) Errada. Gás carbônico (molécula de C 2 ) possui 1 átomo de carbono e 2 átomos de oxigênio. c) Errada. zônio ( 3 ) é constituído de 3 átomos de oxigênio. d) Certa. Elementos: Fe, C, N. e) Errada. Ácido sulfúrico ( S 4 ) possui 2 átomos de hidrogênio, 1 átomo de enxofre e 4 átomos de oxigênio. a) Errada. No lado esquerdo estão os reagentes e no lado direito os produtos. b) Certa. c) Errada. Si 2 é a fórmula de uma substância composta (formada por 2 elementos). d) Errada. Ambas são fórmulas. símbolo é usado para representar um elemento. Um conjunto de símbolos compõe a fórmula de uma molécula. e) Errada. São fórmulas de substâncias compostas. Na alotropia, substâncias simples diferentes possuem a mesma composição química (formadas pelo mesmo tipo de elemento químico). Exemplo: fósforo vermelho: Pn (atomicidade indeterminada); fósforo branco: P 4. 2 = oxigênio. Atomicidade: 2 3 = ozônio. Atomicidade: 3 4 Química B
5 GABARIT 34) B Na recristalização, a água é evaporada e sal e açúcar, um de cada vez, precipitam (recristalização). 35) E a) Errada funil de büchner é usado para separação sólido-líquido; b) Errada centífuga é usada para separações sólido-líquido; c) Errada cadinho é um recipienteusado para macerar ou triturar sólidos ou ainda extrair substâncias com solvente; d) Errada papel filtro é usado em separações sólido-líquido ou sólido-gasoso; e) Certa o funil de separação separa misturas heterogêneas entre líquidos. 36) a) Mistura I: areia. b) Mistura III: sal de cozinha. 37) A a) A filtração em funil com papel permite seprara uma mistura hetogênea sólido-líquido. Dentro as opções apresentadas, apenas a proposta I, areia e água, tem essa característica. A água passará pelo papel juntamente com o etanol e o sal de cozinha dissolvido, deixando a areia como resíduo. b) Na solução resultante há uma única substância sólida dissolvida, o sal. Ao evaporar os líquidos (água e etanol), restará o sal como resíduo final. Líquido menos denso (ex: Azeite) Funil ou ampola de decantação Líquido mais denso (ex: Água) (3) A sublimação permite a evaporação da naftalina por aquecimento, deixando a areia como resíduo; (2) A decantação com o auxílio de um funil de separação permite escoar a água e o óleo separadamente, separando-os; (1) Para realizar a imantação, é necessário que um componente da mistura tenha propriedades metálicas e o outro não. É o que ocorre com a limalha de ferro (metal) e o enxofre (ametal); (5) Na fusão fracionada, a liga metálica é aquecida e o metal cujo ponto de fusão é menor funde primeiro deixando o outro metal na fase sólidda, onde poderão ser separados por filtração; (4) Com a adição de água em quantidade, sal e açúcar são dissolvidos. Em seguida, inicia-se uma evaporação lenta de solvente, onde a substância de menor coeficiente de solubilidade começa a cristalizar primeiro. Após a cristalização, uma filtração separa a mistura sólido-líquido. Química B 5
6 GABARIT 38) E Ciclo da água na natureza: Formação de nuvens: passagem do líquido para o gasoso através da evaporação; Precipitação da chuva: passagem do gasoso para o líquido através da condensação. Processo semelhante ocorre na destilação, onde ocorre sequencialmente evaporação e condensação. 42) B 16 Certa após a filtração, o sistema resultante é uma mistura homogênea, chamada de solução. a) Errada base, ácido, ácido; b) Certa todos ácidos; c) Errada ácido, hidrocarboneto, hidreto metálico; d) Errada hidreto metálico, hidrocarboneto, hidrocarboneto; e) Errada hidrocarboneto, base, ácido. 43) C 44) C Vinagre apresenta sabor azedo, pois é ácido, ou seja, possui maior quantidade de H + (cátion) do que H (ânion). Somente ionizam os hidrogênios ligados aos átomos de oxigênio. HC 4 um hidrogênio ionizável monoácido; 39) D a) Errada a filtração separa misturas sólido-líquido ou sólido-gasoso; b) Errada a decantação pode seprar líquidos imiscíveis (mistura heterogênea); c) Errada a peneiração separa misturas sólido-sólido; d) Certa a destilação é o processo apropriado para separar misturas homogêneas de líquidos, como o caso do álcool e acetona; e) Errada a filtração a vácuo assim como a filtração comum separa misturas sólidos-líquido ou sólido-gasoso. Mn 4 dois hidrogênios ionizáveis diácido; H 3 P 3 dois hidrogênios ionizáveis diácido; 40) B fracionamento do petróleo que ocorre por destilação fracionada é baseado nos diferentes pontos de ebulição dos componentes da mistura. Com o aquecimento, cada componente evapora em uma temperatura diferente, permitindo assim a separação. H 4 Sb 2 7 quatro hidrogênios ionizáveis tetrácido; 41) Errada o café é uma mistura de diversas substâncias; 02. Certa a água quente extrai substâncias do café, mudado a cor e sabor; 04. Certa através da filtração o excesso de café fica retido no filtro; 08. Errada a filtração é um fenômeno físico de separação, sem alterar a composição química dos componentes da mistura; 6 Química B
7 GABARIT 45) 16 46) D 01. Errada independentemente de o ácido ser fraco ou forte, sempre sofrerá alteração em presença de uma base; 02. Errada qualquer ácido mantém-se incolor em fenolftaleína. Ela torna-se avermelhada apenas em meio básico; 04. Errada ácidos que tornam a solução altamente condutora de corrente elétrica são fortes; 08. Errada na ionização, a proporção entre a concentração de H + e A não é determinada pela força. Ex.: HA H + + A ou A 2H + + A, etc. 16. Certa quando a concentração de HA é maior que a de H +, isso quer dizer que o ácido está pouco ionizado. Por consequência, é um ácido fraco. Dica de obtenção da força ácida sem dispor do grau de ionização: Regra de Pauling: 50) A 51) C IV. Certa HC (92%), S 4 (61%); V. Errada são ácidos facos e por isso formam soluções com baixa condutividade elétrica. A afirmativa II é suficiente para deduzir que a substância tem comportamento de uma base (reage com ácido formando sal e água). A afirmativa III confirma essa hipótese, pois bases tornam a fenolftaleína vermelha. a) Certa base; b) Errada sal; c) Errada sal; d) Errada óxido. 52) A sabor adstringente é uma característica organoléptica típica das bases. a) Errada ácido; b) Errada sal; c) Certa base; d) Errada sacarose; e) Errada ácido. 47) C 48) B a) Errada K 2 é óxido básico; b) Errada HF é hidrácido moderado; c) Certa hidrácido fraco, hidrácido forte, base fraca, óxido ácido e óxido básico; d) Errada H 3 B 3 é oxiácido KH é base forte; e) Errada NH 3 é base fraca, Ba é óxido básico e S 3 é óxido ácido. Quanto maior o valor da constante ácida (Ka), mais ionizado estará o ácido. Assim, maior será a sua força. 6, < II 49) E 3, < V 1, < I 1, < IV rdem crescente de Ka (rdem crescente de acidez) 1, III I. Certa ácidos em água ionizam; II. Certa de acordo com Arrhenius, ácidos em água ionizam, liberando exclusivamente o cátion H + ; III. Certa são formados por ligação covalente apenas; 53) C A hidroxila é um ânion que tem por valência 1. Assim, pelo número de hidroxilas, pode-se saber a valência do cátion que forma a base: Assim, o metal deve ser da família IIA ou de família B desde que tenha valência 2 +. a) Certa magnésio IIA; b) Errada enxofre VIA (é ametal); c) Errada sódio IA; d) Errada alumínio IIIA; e) Errada prata IB (valência 1 + ) As bases solúveis (fortes) são as de metais da família IA. As bases parcialmente solúveis (fortes) são as de metais da família IIA. Exceção: Mg( ) fraca. Química B 7
8 GABARIT 54) B 55) D a) Errada Cu (família B fraca), Mg (família IIA fraca); b) Errada K (família IA forte), Ba (família IIA forte); c) Certa Na (família IA forte), Mg (família IIA fraca); d) Errada Ba (família IIA forte), Fe (família B fraca); e) Errada Al (família IIIA fraca), Na (família IA forte). (3) ácido nítrico HN 3 (X) ácido clórico HC 3 (4) ácido fosfórico H 3 P 4 (X) ácido sulfúrico S 4 (2) ácido sulfuroso S 3 (X) hidróxido ferroso Fe(H) 2 (1) hidróxido férrico Fe(H) 3 (X) hidróxido de nitrogênio não existe com esse nome (5) hidróxido de amônio NH 4 H Fórmulas (1ª coluna) que não tiveram os nomes mencionados na 2ª coluna: HC ácido clorídrico S ácido sulfídrico Hidrácidos possuem o nome terminado em ídrico. Escala de ph: 57) E Reações de neutralização: 2HN 3 + Fe(H) 2 Fe(N 3 ) ácido nítrico hidróxido ferroso nitrato ferroso água 3HN 3 + Fe(H) 3 Fe(N 3 ) ácido nítrico hidróxido férrico nitrato férrico água HN 3 + NaH NaN 3 ácido nítrico hidróxido nitrato água de sódio de sódio 58) B 59) D HN 2 + NaH NaN 2 ácido hidróxido nitrito água nitroso de sódio de sódio 3HN 2 + Fe(H) 3 Fe(N 2 ) ácido nitroso hidróxido férrico nitrito férrico água Neutralização total: 3HC + A (H) 3 A C ácido hidróxido cloreto de água clorídrico de alumínio alumínio HBr + Fe(H) 2 Fe(H)Br ácido hidróxido hidróxi brometo água bromídrico ferroso ferroso 60) A S 4 + 2NaH Na 2 S ácido sulfúrico hidróxido de sulfato de sódio água sódio 56) A Cerveja: Vermelho alaranjado ph de 4,1 a 5 ácido; Refrigerante: Vermelho alaranjado ph de 1,8 a 3 ácido; Suco de limão: Vermelho alaranjado ph de 2,1 a 2,4 ácido; Vinagre: Vermelho alaranjado ph de 2,5 a 3,5 ácido; Amoníaco: Azul ph de 11,8 a 12,3 alcalino; Leite de magnésia: Azul ph de 8 a 10 alcalino. a) Certa solução de ph 1: adquire cor vermelha, solução de ph 4: adquire cor rosa; b) Errada soluções de ph 4 e 6 adquirem cor rosa e não podem ser diferenciadas; c) Errada soluções de ph 7 e 8 adquirem cor roxa e não podem ser diferenciadas; d) Errada soluções de ph 10 e 11 adquirem cor azul e não podem ser diferenciadas; e) Errada soluções de ph 13 e 14 adquirem cor amarela e não podem ser diferenciadas. S 4 + NaH NaHS 4 ácido sulfúrico hidróxido hidrogeno água de sódio sulfato de sódio 61) D 62) D a) Errada o KC (cloreto de potássio) é um sal; b) Errada como sal, forma íons em solução aquosa, conduzindo assim a corrente elétrica; c) Errada é um sal formado por metal e ametal e, portanto, um composto iônico; d) Certa forma íons em grande quantidade, sendo assim um bom condutor de corrente elétrica; e) Errada é um sal. Reações de neutralização de origem: HC + NaH NaC ácido hidróxido cloreto água clorídrico de sódio de sódio HBr + KH KBr ácido hidróxido brometo água bromídrico de potássio de potássio 8 Química B
9 GABARIT HI + NaH NaI ácido hidróxido iodeto água iodídrico de sódio de sódio 63) E 64) E 65) A 66) D 67) E 2HC + Mg(H) 2 MgC ácido hidróxido cloreto de água clorídrico de magnésio magnésio 2H 3 P 4 + 3Ca(H) 2 Ca 3 (P 4 ) ácido fosfórico hidróxido de cálcio fosfato de cálcio água 3 C 3 + 2Fe(H) 3 Fe 2 (C 3 ) ácido carbônico hidróxido férrico, carbonato férrico, água ou ou hidróxido de ferro III carbonato de ferro III Ácido de referência: HC ácido hipocloroso HC ácido clorídrico Sal: C hipoclorito C cloreto A S 4 ácido sulfúrico (oxiácido) B KCN cianeto de potássio (sal do ácido cianídrico e hidróxido de potássio) C K 2 S 4 sulfato de potássio (sal do ácido sulfúrico e hidróxido de potássio) D HCN ácido cianídrico (hidrácido) 69) B Metais alcalinoterrosos formam cátions bivalentes: M 2+ Sulfetos (enxofre é da família VIA) formam ânions bivalentes: S 2 (recebem 2 elétrons). Fluoretos (flúor é da família VIIA) formam ânions monovalentes: F (recebem 1 elétron). 70) 18 71) D M 2+ + S 2 MS M F MF Errada decantação é um método para a separação de misturas heterogêneas; 02. Certa A 2 (S 4 ) 3. Não há hidrogênio ou hidroxila na fórmula, pois foi formada em reação de neutralização total de A (H) 3 e S 4 ; 04. Errada a fórmula se forma da seguinte maneira: 2A S 4 2 A 2 (S 4 ) 3 ; 08. Errada é considerada insolúvel (solubilidade de 1,5 mg/l aproximadamente); 16. Certa vem do hidróxido de sódio (NaH) com o ácido hipocloroso (HC ). NaHC 3 é comumente usado e constitui a fórmula de diversos medicamentos como Sal de Fruta Eno, Estomazil e Sonrisal. Apesar de ser um sal ácido, o bicarbonato de sódio pode neutralizar a acidez estomacal segundo a reação: Reações de neutralização de origem: HC + KH KC ácido hidróxido cloreto água clorídrico de de potássio potássio 68) A 2H 3 P 4 + 3Ca(H) 2 Ca 3 (P 4 ) ácido fosfórico hidróxido de cálcio fosfato de cálcio água HN 3 ácido nítrico NH 4 H hidróxido de amônio a) Certa ânion C (halogênio família VIIA) e cátion Mg 2+ (alcalinoterroso família IIA); b) Errada são ácido e sal, respectivamente. enunciado menciona sal e base; c) Errada são ácido e base, respectivamente. enunciado menciona sal e base; d) Errada são base e ácido, respectivamente. enunciado menciona sal e base; e) Errada são ácido e base, respectivamente. enunciado menciona sal e base. 72) E 73) D A neutralização ocorre, pois o ácido formado (carbônico) é ácido fraco na medida em que se decompõe espontaneamente em água e gás carbônico. Mg(H) 2 o hidróxido de magnésio também é comumente usado para neutralizar a acidez estomacal por ação direta da hidroxila neutralizando os hidrogênios ácidos; CH 3 CH ácido acético. Não pode ser usado, pois é um ácido. gás que mais contribui para o aumento do efeito estufa é o gás carbônico (C 2 ), que pertence à função óxido. C 2 C 3 Gás carbônico é óxido ácido, pois em água forma o ácido carbônico. Química B 9
10 GABARIT 74) C 75) C 76) B 77) C 78) D 79) D a) Errada óxidos podem reagir com água; b) Errada é um óxido (composto binário em que o elemento mais eletronegativo é o oxigênio); c) Certa óxido básico + água base; d) Errada é um óxido básico; e) Errada é óxido básico e por isso pode neutralizar um ácido. Para se considerar um óxido como ácido, esse íxido deve satisfazer a uma das condições: em água origina ácido; é capaz de neutralizar uma base formando sal e água. I. Certa em água forma ácido sulfuroso; II. Certa reage com base (NaH) formando sal e água; III. Errada reage com ácido formando sal e água (é óxido básico). I. Óxido ácido C 2 C 3 II. Óxido básico Ca Ca(H) 2 III. Óxido básico Na 2 2NaH IV. Óxido ácido S 2 S 3 V. Óxido básico Sr Sr(H) 2 Óxido de alumínio: 2A A 2 3 Óxido de cromo III: 2Cr Cr 2 3 Óxido de zinco: Zn Zn Óxido de magnésio: Mg Mg Óxido de ferro III: 2Fe Fe 2 3 Hidróxido ferroso: Fe(H) 2 também chamado hidróxido de ferro II. férrico é Fe(H) 3. Usa-se o sufixo ico para o de maior número de oxidação e oso para o de menor NX; Ácido sulfídrico: S (hidrácidos ácidos sem oxigênio utilizam o sufixo ídrico); Ácido sulfúrico: S 4 (oxiácidos ácidos com oxigênio utilizam os sufixos ico e oso); Óxido de carbono: C (mais comumente monóxido de carbono, para diferenciá-lo do dióxido de carbono C 2 ). b) Certa 2S S 3 c) Certa entre outros danos, a corrosão provocada pelos ácidos sulfuroso e sulfúrico é causada pela chuva ácida, especialmente no mármore; d) Errada são óxidos ácidos, pois em água formam os ácidos sulfuroso e sulfúrico, respectivamente; e) Certa 2S S 3 80) 03 81) A 01. Certa NaC (hipoclorito de sódio constitui a água sanitária), Ca (óxido de cálcio cal viva), CH 3 CH (ácido etanoico constitui o vinagre), C 2 (dióxido de carbono no estado sólido é o gelo seco), Mg(H) 2 (hidróxido de magnésio conhecido como leite de magnésio); 02. Certa ácido acético é ácido e dióxido de carbono é óxido ácido, pois em água origina o ácido carbônico; 04. Errada a solubilidade do hidróxido de magnésio é muito pequena, por isso é uma base fraca; 08. Errada provém de uma base forte (NaH) e por isso, em água, pode originar: HC (ácido fraco e pouco ionizado) + Na + + H (base forte e,, muito dissociada). A presença dos íons garante a condutibilidade elétrica. S 4 ácido sulfúrico (ácido); NaH hidróxido de sódio (base); MgC 2 cloreto de magnésio (sal); 2 peróxido de hidrogênio (água oxigenada) (óxido). 82) 07 83) C 01. Certa ao reagir com a água a cal virgem (Ca) forma a base hidróxido de cálcio (cal hidratada), que neutraliza a acidez do solo; 02. Certa o hidróxido de cálcio neutraliza íons H + presentes no solo; 04. Certa o hidróxido de cálcio neutraliza íons H + presentes no solo; 08. Errada cal virgem (Ca) é um óxido básico, pois em água forma uma base (Ca(H) 2 ); 16. Errada a calagem diminui a acidez do solo, tornando o ph maior. A: Principal responsável pela chuva ácida S 2 (dióxido de enxofre); B: Usado em produtos de limpeza NH 3 (amônia); C: Principal responsável pelo efeito estufa: C 2 (gás carbônico); D: Filtra os raios ultravioleta: 3 (ozônio). a) Certa S 3 S 4 (ácido sulfúrico); 10 Química B
Química B Semiextensivo V. 2
 GABARIT Química B Semiextensivo V. 2 Exercícios 01) E 02) C 03) C 04) D a) Errada um soluto puro, mesmo de natureza iônica, não conduz corrente elétrica, pois para que isso ocorra é necessário que os íons
GABARIT Química B Semiextensivo V. 2 Exercícios 01) E 02) C 03) C 04) D a) Errada um soluto puro, mesmo de natureza iônica, não conduz corrente elétrica, pois para que isso ocorra é necessário que os íons
Química B Semiextensivo V. 1
 Química B Semiextensivo V. 1 Exercícios 01) A 02) C 03) A 04) E d = m v Densidade e massa são diretamente proporcionais, ou seja, quanto maior a massa da substância, maior será sua densidade. Já o volume
Química B Semiextensivo V. 1 Exercícios 01) A 02) C 03) A 04) E d = m v Densidade e massa são diretamente proporcionais, ou seja, quanto maior a massa da substância, maior será sua densidade. Já o volume
Apostila de Química 19 Funções Inorgânicas
 1.0 Dissociação Apostila de Química 19 Funções Inorgânicas Teoria da dissociação (Arrhenius, 1903) Determinadas substâncias, quando dissolvidas em água, são capazes de originar cátions e ânions (íons livres).
1.0 Dissociação Apostila de Química 19 Funções Inorgânicas Teoria da dissociação (Arrhenius, 1903) Determinadas substâncias, quando dissolvidas em água, são capazes de originar cátions e ânions (íons livres).
FUNÇÕES INORGÂNICAS Profº JAISON
 FUNÇÕES INORGÂNICAS Profº JAISON TEORIA DE ARRHENIUS 1.Eletrólitos e não eletrólitos As substâncias cujas soluções aquosas apresentam íons livres conduzem eletricidade, portanto, são chamadas de eletrólitos.
FUNÇÕES INORGÂNICAS Profº JAISON TEORIA DE ARRHENIUS 1.Eletrólitos e não eletrólitos As substâncias cujas soluções aquosas apresentam íons livres conduzem eletricidade, portanto, são chamadas de eletrólitos.
Química B Extensivo V. 5
 GABARIT Química B Extensivo V. 5 Exercícios 01) 08) B 0) c) Ca óxido de cálcio d) C dióxido de cloro e) A óxido de alumínio b) HC hipocloroso c) H S sulfídrico d) HI iodídrico e) Mn óxido de manganês IV
GABARIT Química B Extensivo V. 5 Exercícios 01) 08) B 0) c) Ca óxido de cálcio d) C dióxido de cloro e) A óxido de alumínio b) HC hipocloroso c) H S sulfídrico d) HI iodídrico e) Mn óxido de manganês IV
Aulas Multimídias Santa Cecília Profª Thiago Quick Disciplina: Química Série: 9º ano EF
 Aulas Multimídias Santa Cecília Profª Thiago Quick Disciplina: Química Série: 9º ano EF ÁCIDOS FUNÇÕES INORGÂNICAS São substâncias que não possuem carbono em sua composição, com exceção de algumas substâncias
Aulas Multimídias Santa Cecília Profª Thiago Quick Disciplina: Química Série: 9º ano EF ÁCIDOS FUNÇÕES INORGÂNICAS São substâncias que não possuem carbono em sua composição, com exceção de algumas substâncias
Reações Químicas. Balanceamento de Reações Químicas Exemplo: + H 2 O 3. Fe 2. Fe + H 2
 Reações Químicas Balanceamento de Reações Químicas Exemplo: Fe 2 O 3 + H 2 Fe + H 2 O Reações Químicas Balanceamento de Reações Químicas Exemplo: Fe 3 O 4 + C Fe + CO Reações Químicas Balanceamento de
Reações Químicas Balanceamento de Reações Químicas Exemplo: Fe 2 O 3 + H 2 Fe + H 2 O Reações Químicas Balanceamento de Reações Químicas Exemplo: Fe 3 O 4 + C Fe + CO Reações Químicas Balanceamento de
ÁCIDOS ÁCIDOS CONCEITO PROPRIEDADES CLASSIFICAÇÃO NOMENCLATURA 10/11/2015. HCl (aq) H + (aq) + Cl - (aq) H 3 PO 4(aq) 3 H + (aq) + PO 4
 FUNÇÕES INORGÂNICAS São substâncias que não possuem carbono em sua composição, com exceção de algumas substâncias como, por exemplo, o CO 2, CO, Carbono grafite, diamante, H 2 CO 3, HCN, sais carbonatos
FUNÇÕES INORGÂNICAS São substâncias que não possuem carbono em sua composição, com exceção de algumas substâncias como, por exemplo, o CO 2, CO, Carbono grafite, diamante, H 2 CO 3, HCN, sais carbonatos
LOGO. Funções Inorgânicas e Tipos de Reações. Profa. Samara Garcia
 LOGO Funções Inorgânicas e Tipos de Reações Profa. Samara Garcia ÁCIDOS Definição segundo Arrhenius: são substâncias que em solução aquosa sofrem ionização, liberando como cátions somente íons H + (H 3
LOGO Funções Inorgânicas e Tipos de Reações Profa. Samara Garcia ÁCIDOS Definição segundo Arrhenius: são substâncias que em solução aquosa sofrem ionização, liberando como cátions somente íons H + (H 3
Funções inorgânicas ácidos de Arrhenius
 Funções inorgânicas ácidos de Arrhenius Ácidos são substâncias que, em solução aquosa, sofrem ionização, liberando como cátion somente H +. Ex:. HNO 3 H + + NO 3 Se colocarmos a água como reagente podemos
Funções inorgânicas ácidos de Arrhenius Ácidos são substâncias que, em solução aquosa, sofrem ionização, liberando como cátion somente H +. Ex:. HNO 3 H + + NO 3 Se colocarmos a água como reagente podemos
Capítulo 6 - LIGAÇÕES QUÍMICAS-resoluções
 Capítulo 6 - LIGAÇÕES QUÍMICAS-resoluções 1-C X e T devem ter a mesma carga com sinais contrários: +1 e -1, +2 e -2 ou +3 e -3. 2-B A) Fe 2 S 3 B) CsCl C) CaI 2 D) Al 2 3 E) Ba 3 N 2 Quanto maior a diagonal
Capítulo 6 - LIGAÇÕES QUÍMICAS-resoluções 1-C X e T devem ter a mesma carga com sinais contrários: +1 e -1, +2 e -2 ou +3 e -3. 2-B A) Fe 2 S 3 B) CsCl C) CaI 2 D) Al 2 3 E) Ba 3 N 2 Quanto maior a diagonal
O que é uma propriedade funcional da matéria? Acidez Alcalinidade Salinidade. Funções químicas
 O que é uma propriedade funcional da matéria? Acidez Alcalinidade Salinidade Funções químicas Função química Conjunto de compostos que possuem comportamento semelhantes Ácidos bases Sais Óxidos Mas você
O que é uma propriedade funcional da matéria? Acidez Alcalinidade Salinidade Funções químicas Função química Conjunto de compostos que possuem comportamento semelhantes Ácidos bases Sais Óxidos Mas você
GABARITO. Química B Extensivo V. 6. Exercícios 06) A. I. Adição ou síntese. Dois reagentes (N 2. ). III. Adição ou síntese. Dois reagentes (P 2 07) A
 GABARIT Química B Extensivo V 6 Exercícios 01) A a) Certa S + 2 S 2 Na síntese total, os reagentes são substâncias simples + Ca(H) 2 Ca + 2 Reação de neutralização do solo b) Errada S 3 é óxido ácido,
GABARIT Química B Extensivo V 6 Exercícios 01) A a) Certa S + 2 S 2 Na síntese total, os reagentes são substâncias simples + Ca(H) 2 Ca + 2 Reação de neutralização do solo b) Errada S 3 é óxido ácido,
COMPOSTOS INORGÂNICOS Profº Jaison Mattei
 COMPOSTOS INORGÂNICOS Profº Jaison Mattei Ácidos (teoria de Arrhenius) Ácidos são substâncias moleculares que, ao serem dissolvidas em água se dissociam, originando o íon hidrônio (H 3 O + ). Exemplos:
COMPOSTOS INORGÂNICOS Profº Jaison Mattei Ácidos (teoria de Arrhenius) Ácidos são substâncias moleculares que, ao serem dissolvidas em água se dissociam, originando o íon hidrônio (H 3 O + ). Exemplos:
UFSC. Resposta: = 40. Comentário
 Resposta: 08 + 32 = 40 01. Incorreta. O butano não possui isomeria óptica, pois não possui carbono assimétrico. 02. Incorreta. Ao serem liberados para a atmosfera os gases sofrem expansão de volume. 04.
Resposta: 08 + 32 = 40 01. Incorreta. O butano não possui isomeria óptica, pois não possui carbono assimétrico. 02. Incorreta. Ao serem liberados para a atmosfera os gases sofrem expansão de volume. 04.
9º Ano/Turma: Data / / ) Observe os sistemas onde as esferas representam átomos. Sobre esses sistemas, a afirmação incorreta é:
 Estudante: Educadora: Daiana Araújo 9º Ano/Turma: Data / /2015 C.Curricular: Ciências/ Química 1) Observe os sistemas onde as esferas representam átomos. Sobre esses sistemas, a afirmação incorreta é:
Estudante: Educadora: Daiana Araújo 9º Ano/Turma: Data / /2015 C.Curricular: Ciências/ Química 1) Observe os sistemas onde as esferas representam átomos. Sobre esses sistemas, a afirmação incorreta é:
SAIS E ÓXIDOS FUNÇÕES INORGÂNICAS
 SAIS E ÓXIDOS FUNÇÕES INORGÂNICAS SAIS Os sais são comuns em nosso cotidiano: SAIS São compostos iônicos que possuem, pelo menos um cátion diferente do H + e um ânion diferente do OH -. Exemplos: NaCl
SAIS E ÓXIDOS FUNÇÕES INORGÂNICAS SAIS Os sais são comuns em nosso cotidiano: SAIS São compostos iônicos que possuem, pelo menos um cátion diferente do H + e um ânion diferente do OH -. Exemplos: NaCl
Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas:
 Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas: Resposta da questão 1: a) Cromo (Cr), manganês (Mn), alumínio ( (A l ) ) e Ferro (Fe). b) A distribuição: 2 2 6 2 6 2 5 1s 2s
Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas: Resposta da questão 1: a) Cromo (Cr), manganês (Mn), alumínio ( (A l ) ) e Ferro (Fe). b) A distribuição: 2 2 6 2 6 2 5 1s 2s
CuSO 4 K 2 Cr 2 O 7. Funções Inorgânicas. NaOH. NaCl
 CuSO 4 K 2 Cr 2 O 7 Funções Inorgânicas NaOH NaCl Função química corresponde a um conjunto de substâncias que apresentam propriedades químicas semelhantes. ÁCIDO: H + + ÂNION BASE: CÁTION + OH SAL: CÁTION
CuSO 4 K 2 Cr 2 O 7 Funções Inorgânicas NaOH NaCl Função química corresponde a um conjunto de substâncias que apresentam propriedades químicas semelhantes. ÁCIDO: H + + ÂNION BASE: CÁTION + OH SAL: CÁTION
QUÍMICA LIGAÇÕES QUÍMICAS PROF. SAUL SANTANA
 QUÍMICA LIGAÇÕES QUÍMICAS PROF. SAUL SANTANA Ligação Química O conceito de configuração eletrônica e o desenvolvimento da Tabela Periódica permitiu aos químicos uma base lógica para explicar a formação
QUÍMICA LIGAÇÕES QUÍMICAS PROF. SAUL SANTANA Ligação Química O conceito de configuração eletrônica e o desenvolvimento da Tabela Periódica permitiu aos químicos uma base lógica para explicar a formação
Funções Químicas: Ácidos, bases, sais e óxidos
 Funções Químicas: Ácidos, bases, sais e óxidos Funções Químicas Grupo de substâncias compostas que possuem propriedades químicas semelhantes; As funções químicas são divididas de acordo com a divisão clássica
Funções Químicas: Ácidos, bases, sais e óxidos Funções Químicas Grupo de substâncias compostas que possuem propriedades químicas semelhantes; As funções químicas são divididas de acordo com a divisão clássica
O que é uma propriedade funcional da matéria? Acidez Alcalinidade Salinidade. Funções químicas
 O que é uma propriedade funcional da matéria? Acidez Alcalinidade Salinidade Funções químicas Função química Conjunto de compostos que possuem comportamento semelhantes Ácidos bases Sais Óxidos Mas você
O que é uma propriedade funcional da matéria? Acidez Alcalinidade Salinidade Funções químicas Função química Conjunto de compostos que possuem comportamento semelhantes Ácidos bases Sais Óxidos Mas você
QUÍMICA 1ª Série Ensino Médio
 LISTA 02 CENTRO EDUCACIONAL SIGMA QUÍMICA 1ª Série Ensino Médio Materiais Puros e Impuros Método de separação de Misturas Estados de agregação da matéria Números do átomo e distribuição eletrônica Leis
LISTA 02 CENTRO EDUCACIONAL SIGMA QUÍMICA 1ª Série Ensino Médio Materiais Puros e Impuros Método de separação de Misturas Estados de agregação da matéria Números do átomo e distribuição eletrônica Leis
Arrhenius. Teoria da Disssociação eletrolítica de Arrhenius
 Teoria da Disssociação eletrolítica de Arrhenius Quando uma substância dissolve na água ela vai se dividindo em partículas cada vez menores. Se essa divisão para nas moléculas a solução não conduz a corrente
Teoria da Disssociação eletrolítica de Arrhenius Quando uma substância dissolve na água ela vai se dividindo em partículas cada vez menores. Se essa divisão para nas moléculas a solução não conduz a corrente
1 - O elemento flúor forma compostos com hidrogênio, carbono, potássio e magnésio, respectivamente. Os compostos covalentes ocorrem com:
 Sem limite para crescer Colégio: Nome: nº Professor(a): Data: / /2013 EXERCÍCIOS QUÍMICA 1ª SÉRIE E.M. Turma: 1 - O elemento flúor forma compostos com hidrogênio, carbono, potássio e magnésio, respectivamente.
Sem limite para crescer Colégio: Nome: nº Professor(a): Data: / /2013 EXERCÍCIOS QUÍMICA 1ª SÉRIE E.M. Turma: 1 - O elemento flúor forma compostos com hidrogênio, carbono, potássio e magnésio, respectivamente.
Reações inorgânicas Atividades 2
 Reações inorgânicas Atividades 2 Introdução Os exercícios propostos abaixo abordam o conteúdo de reações inorgânicas, com os principais tipos dessas reações, dessa vez com os nomes das substâncias, para
Reações inorgânicas Atividades 2 Introdução Os exercícios propostos abaixo abordam o conteúdo de reações inorgânicas, com os principais tipos dessas reações, dessa vez com os nomes das substâncias, para
Ácidos e Bases. Funções Inorgânicas
 Ácidos e Bases Funções Inorgânicas Funções Inorgânicas As substâncias podem ser classificadas em duas classes: Substâncias orgânicas: aquelas que contém carbono. Substâncias inorgânicas: aquelas formadas
Ácidos e Bases Funções Inorgânicas Funções Inorgânicas As substâncias podem ser classificadas em duas classes: Substâncias orgânicas: aquelas que contém carbono. Substâncias inorgânicas: aquelas formadas
CONTEÚDO E HABILIDADES DINÂMICA LOCAL INTERATIVA INTERATIVIDADE FINAL AULA QUÍMICA. Unidade III. Ligações químicas e funções inorgânicas.
 Unidade III Ligações químicas e funções inorgânicas. 2 Aula 11.2 Conteúdo: Função Inorgânica: sais e óxidos. 3 Habilidades: Compreender os códigos e símbolos próprios da Química atual. 4 REVISÃO 5 Xampu
Unidade III Ligações químicas e funções inorgânicas. 2 Aula 11.2 Conteúdo: Função Inorgânica: sais e óxidos. 3 Habilidades: Compreender os códigos e símbolos próprios da Química atual. 4 REVISÃO 5 Xampu
TEORIA DA REPULSÃO DOS PARES DE ELÉTRONS DA CAMADA DE VALÊNCIA (TEORIA RPECV)
 GEOMETRIA MOLECULAR TEORIA DA REPULSÃO DOS PARES DE ELÉTRONS DA CAMADA DE VALÊNCIA (TEORIA RPECV) A teoria da repulsão dos pares de elétrons da camada de valência afirma que o arranjo geométrico dos átomos
GEOMETRIA MOLECULAR TEORIA DA REPULSÃO DOS PARES DE ELÉTRONS DA CAMADA DE VALÊNCIA (TEORIA RPECV) A teoria da repulsão dos pares de elétrons da camada de valência afirma que o arranjo geométrico dos átomos
Lembrete: Antes de começar a copiar cada unidade, coloque o cabeçalho da escola e a data! CIÊNCIAS - UNIDADE 4 REAÇÕES E FUNÇÕES QUÍMICAS
 Lembrete: Antes de começar a copiar cada unidade, coloque o cabeçalho da escola e a data! Use canetas coloridas ou escreva palavras destacadas, para facilitar na hora de estudar. E capriche! Não se esqueça
Lembrete: Antes de começar a copiar cada unidade, coloque o cabeçalho da escola e a data! Use canetas coloridas ou escreva palavras destacadas, para facilitar na hora de estudar. E capriche! Não se esqueça
REVISÃO DE ÁCIDOS E BASES
 REVISÃO DE ÁCIDOS E BASES COMPOSTOS COVALENTES NÃO CONDUZEM CORRENTE ELÉTRICA POR EXEMPLO A ÁGUA É NECESSÁRIO ADICIONAR COMPOSTOS IÔNICOS À ÁGUA OS COMPOSTOS IÔNICOS DESFAZEM A LIGAÇÃO DE SEUS ÍONS QUE
REVISÃO DE ÁCIDOS E BASES COMPOSTOS COVALENTES NÃO CONDUZEM CORRENTE ELÉTRICA POR EXEMPLO A ÁGUA É NECESSÁRIO ADICIONAR COMPOSTOS IÔNICOS À ÁGUA OS COMPOSTOS IÔNICOS DESFAZEM A LIGAÇÃO DE SEUS ÍONS QUE
QUÍMICA PROFº JAISON MATTEI
 QUÍMICA PROFº JAISON MATTEI 1. A água da chuva é naturalmente ácida devido à presença do gás carbônico encontrado na atmosfera. Esse efeito pode ser agravado com a emissão de gases contendo enxofre, sendo
QUÍMICA PROFº JAISON MATTEI 1. A água da chuva é naturalmente ácida devido à presença do gás carbônico encontrado na atmosfera. Esse efeito pode ser agravado com a emissão de gases contendo enxofre, sendo
Funções inorgânicas : Sais e Óxidos
 Funções inorgânicas : Sais e Óxidos Sais Bicarbonato de sódio (NaHCO 3 ) Utilizado em antiácidos Carbonato de cálcio (CaCO 3 ) Encontrado no mármore, no calcário, nas cascas de ovos etc Sulfato de cálcio
Funções inorgânicas : Sais e Óxidos Sais Bicarbonato de sódio (NaHCO 3 ) Utilizado em antiácidos Carbonato de cálcio (CaCO 3 ) Encontrado no mármore, no calcário, nas cascas de ovos etc Sulfato de cálcio
Nome do ácido H x EO y. ácido [nome de E] + ico. ácido [nome de E] + oso
![Nome do ácido H x EO y. ácido [nome de E] + ico. ácido [nome de E] + oso Nome do ácido H x EO y. ácido [nome de E] + ico. ácido [nome de E] + oso](/thumbs/54/34456988.jpg) ÁCIDOS Ácido de Arrhenius - Substância que, em solução aquosa, libera como cátions somente íons H + (ou H 3 O + ). Ácido não-oxigenado (H x E): Exemplo: HCl - ácido clorídrico ácido + [nome de E] + ídrico
ÁCIDOS Ácido de Arrhenius - Substância que, em solução aquosa, libera como cátions somente íons H + (ou H 3 O + ). Ácido não-oxigenado (H x E): Exemplo: HCl - ácido clorídrico ácido + [nome de E] + ídrico
A Água e Suas Relações. Funções Inorgânicas Ácidos, Bases e Sais
 A Água e Suas Relações Funções Inorgânicas Ácidos, Bases e Sais Introdução: É constituída por 2 gases: Hidrogênio Oxigênio Água Na proporção 2:1, ou seja 2 átomos de hidrogênio e 1 átomo de oxigênio Sua
A Água e Suas Relações Funções Inorgânicas Ácidos, Bases e Sais Introdução: É constituída por 2 gases: Hidrogênio Oxigênio Água Na proporção 2:1, ou seja 2 átomos de hidrogênio e 1 átomo de oxigênio Sua
QUÍMICA. Soluções e Substâncias Inorgânicas
 QUÍMICA Soluções e Substâncias Inorgânicas Substâncias Inorgânicas e suas características: Ácidos, Bases, Sais e Óxidos. Reações de Neutralização - Parte 2 Prof ª. Giselle Blois Exercícios: Substâncias
QUÍMICA Soluções e Substâncias Inorgânicas Substâncias Inorgânicas e suas características: Ácidos, Bases, Sais e Óxidos. Reações de Neutralização - Parte 2 Prof ª. Giselle Blois Exercícios: Substâncias
REVISÃO: FUNÇÕES INORGÂNICAS. Prof. Guilherme F. Martins
 REVISÃO: FUNÇÕES INORGÂNICAS Prof. Guilherme F. Martins ÁCIDOS Segundo Arrhenius é toda substância que em meio aquoso libera por ionização, como única espécie de carga positiva, o íon H + (próton). Obs.
REVISÃO: FUNÇÕES INORGÂNICAS Prof. Guilherme F. Martins ÁCIDOS Segundo Arrhenius é toda substância que em meio aquoso libera por ionização, como única espécie de carga positiva, o íon H + (próton). Obs.
As substâncias químicas podem ser agrupadas de acordo com suas PROPRIEDADES COMUNS. Estas propriedades comuns são chamadas de PROPRIEDADES FUNCIONAIS
 As substâncias químicas podem ser agrupadas de acordo com suas PROPRIEDADES COMUNS Estas propriedades comuns são chamadas de PROPRIEDADES FUNCIONAIS Em função dessas propriedades podemos agrupar as substâncias
As substâncias químicas podem ser agrupadas de acordo com suas PROPRIEDADES COMUNS Estas propriedades comuns são chamadas de PROPRIEDADES FUNCIONAIS Em função dessas propriedades podemos agrupar as substâncias
Separação de misturas
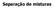 Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
Respostas Caderno de Exercícios 1
 Respostas Caderno de Exercícios 1 Respostas Caderno de Exercícios capítulo 1 1. D 2. E 3. C 4. C 5. A 6. A 7. E 8. B 9. D 10. C 11. B 12. A 13. C 14. B 15. D 16. A 17. D 18. D 19. C 20. a) Água; carbonato
Respostas Caderno de Exercícios 1 Respostas Caderno de Exercícios capítulo 1 1. D 2. E 3. C 4. C 5. A 6. A 7. E 8. B 9. D 10. C 11. B 12. A 13. C 14. B 15. D 16. A 17. D 18. D 19. C 20. a) Água; carbonato
3ª Série / Vestibular. As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar que, na reação:
 3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
O b) SO 2. CaSO 3 + CO 2
 31 c QUÍMICA petróleo pode conter alto teor de enxofre, que deve ser removido nas refinarias de petróleo. Mesmo assim, na queima de combustíveis fósseis, forma-se dióxido de enxofre. Esse óxido liberado
31 c QUÍMICA petróleo pode conter alto teor de enxofre, que deve ser removido nas refinarias de petróleo. Mesmo assim, na queima de combustíveis fósseis, forma-se dióxido de enxofre. Esse óxido liberado
Função química Conjunto
 Função química Conjunto de compostos que possuem comportamento semelhantes As principais funções inorgânicas são : Os ácidos As bases Os sais Os óxidos Mas você sabe identificar? Ácidos Do ponto de vista
Função química Conjunto de compostos que possuem comportamento semelhantes As principais funções inorgânicas são : Os ácidos As bases Os sais Os óxidos Mas você sabe identificar? Ácidos Do ponto de vista
QUÍMICA. Professora Caroline Azevedo
 QUÍMICA Professora Caroline Azevedo FUNÇÕES INORGÂNICAS Ácidos Segundo Arrhenius, toda substância que em solução aquosa sofre ionização produzindo como cátion, apenas o íon H +, é um ácido. Ex. H 2 O +
QUÍMICA Professora Caroline Azevedo FUNÇÕES INORGÂNICAS Ácidos Segundo Arrhenius, toda substância que em solução aquosa sofre ionização produzindo como cátion, apenas o íon H +, é um ácido. Ex. H 2 O +
Química A Semi-Extensivo V. 3
 Química A Semi-Extensivo V. Exercícios 01) B a) b) c),5,5 N d) e) d.d.p. = 0 1,0,8 Li Br,0,5 d.d.p. =,8 1,0 = 1,8 polar = d.d.p. d.d.p. = 0,5 d.d.p. = 0,7 1,0,8 Li Br d.d.p. = 0 1,0 Li (g) molécula apolar
Química A Semi-Extensivo V. Exercícios 01) B a) b) c),5,5 N d) e) d.d.p. = 0 1,0,8 Li Br,0,5 d.d.p. =,8 1,0 = 1,8 polar = d.d.p. d.d.p. = 0,5 d.d.p. = 0,7 1,0,8 Li Br d.d.p. = 0 1,0 Li (g) molécula apolar
... 2) Escreva a fórmula e os nomes dos sete ácidos padrões.
 Lista de Exercícios Ácidos Bases e sais 1) Nas colunas abaixo, associe as fórmulas aos seus nomes: I. H 2 S(aq) ( ) ácido bromídrico II. HCl (aq) ( ) ácido fluorídrico III. HCN(aq) ( ) ácido iodídrico
Lista de Exercícios Ácidos Bases e sais 1) Nas colunas abaixo, associe as fórmulas aos seus nomes: I. H 2 S(aq) ( ) ácido bromídrico II. HCl (aq) ( ) ácido fluorídrico III. HCN(aq) ( ) ácido iodídrico
O ALUNO DEVERÁ VIR PARA A AULA DE RECUPERAÇÃO COM A LISTA PRONTA PARA TIRAR DÚVIDAS.
 Lista de exercícios para a prova de recuperação final 1º ano EM Conteúdo. O ALUNO DEVERÁ VIR PARA A AULA DE RECUPERAÇÃO COM A LISTA PRONTA PARA TIRAR DÚVIDAS. - Misturas e substâncias - Tabela e propriedades
Lista de exercícios para a prova de recuperação final 1º ano EM Conteúdo. O ALUNO DEVERÁ VIR PARA A AULA DE RECUPERAÇÃO COM A LISTA PRONTA PARA TIRAR DÚVIDAS. - Misturas e substâncias - Tabela e propriedades
26/08/15 SUBSTÂNCIAS E MISTURAS. Prof. Ms. Mayanderson (Xuxu)
 SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
Funções Inorgânicas. Funções Inorgânicas. Ácidos. Teoria da dissociação iônica de Arrhenius 10/11/17. Prof. Mayanderson
 Funções Inorgânicas n Função química é um conjunto de substâncias com propriedades químicas semelhantes, denominadas propriedades funcionais. Funções Inorgânicas Prof. Mayanderson n Ácidos; n Bases; n
Funções Inorgânicas n Função química é um conjunto de substâncias com propriedades químicas semelhantes, denominadas propriedades funcionais. Funções Inorgânicas Prof. Mayanderson n Ácidos; n Bases; n
29/03/ TRANSFORMAÇÕES QUÍMICAS PROVA 1 GABARITO - prova tipo A
 29/03/2016 - TRANSFORMAÇÕES QUÍMICAS PROVA 1 GABARITO - prova tipo A Texto para as questões 1 a 10: O permanganato de potássio (KMnO 4 ) é um forte agente oxidante. Em laboratório, pode ser empregado para
29/03/2016 - TRANSFORMAÇÕES QUÍMICAS PROVA 1 GABARITO - prova tipo A Texto para as questões 1 a 10: O permanganato de potássio (KMnO 4 ) é um forte agente oxidante. Em laboratório, pode ser empregado para
FUNÇÕES INORGÂNICAS. Maira Gazzi Manfro e Giseli Menegat
 FUNÇÕES INORGÂNICAS Maira Gazzi Manfro e Giseli Menegat [email protected] [email protected] O que são funções inorgânicas? Funções inorgânicas são agrupamentos de compostos
FUNÇÕES INORGÂNICAS Maira Gazzi Manfro e Giseli Menegat [email protected] [email protected] O que são funções inorgânicas? Funções inorgânicas são agrupamentos de compostos
INTRODUÇÃO À QUÍMICA
 INTRODUÇÃO À QUÍMICA O QUE É QUÍMICA? É a ciência que estuda a matéria, suas propriedades, transformações e interações, bem como a energia envolvida nestes processos. QUAL A IMPORTÂNCIA DA QUÍMICA? Entender
INTRODUÇÃO À QUÍMICA O QUE É QUÍMICA? É a ciência que estuda a matéria, suas propriedades, transformações e interações, bem como a energia envolvida nestes processos. QUAL A IMPORTÂNCIA DA QUÍMICA? Entender
06) Considere a aparelhagem desenhada a seguir, empregada para testes de condutividade elétrica. O teste deu positivo com qual dos líquidos?
 TEORIA DE ARRHENIUS 01) (Puc-SP) Dados os compostos A: CH 3 COONa (Sal: acetato de sódio) B: CH 3 COOH (ácido acético) C: CH 3 CH 2 OH (álcool etílico) D: C 6 H 12 O 6 (glicose) Pede-se: a) Quais os que
TEORIA DE ARRHENIUS 01) (Puc-SP) Dados os compostos A: CH 3 COONa (Sal: acetato de sódio) B: CH 3 COOH (ácido acético) C: CH 3 CH 2 OH (álcool etílico) D: C 6 H 12 O 6 (glicose) Pede-se: a) Quais os que
PROVA DE QUÍMICA. Tendo em vista as propriedades coligativas dessas soluções, é CORRETO afirmar
 17 PROVA DE QUÍMICA Q U E S T Ã O 2 6 Z e X são elementos químicos que apresentam respectivamente 2 e 6 elétrons no nível de valência. A fórmula química resultante da combinação entre átomos dos elementos
17 PROVA DE QUÍMICA Q U E S T Ã O 2 6 Z e X são elementos químicos que apresentam respectivamente 2 e 6 elétrons no nível de valência. A fórmula química resultante da combinação entre átomos dos elementos
Conceitos importantes: a) Matéria : Tudo o que possui massa e ocupa lugar no espaço.
 SISTEMAS QUÍMICOS E SUAS TRANSFORMAÇÕES Prof. Ms. Mayanderson (Xuxu) QUÍMICA: A química estuda a natureza, as propriedades, a composição e as transformações da matéria. Ela está em nosso cotidiano e, ao
SISTEMAS QUÍMICOS E SUAS TRANSFORMAÇÕES Prof. Ms. Mayanderson (Xuxu) QUÍMICA: A química estuda a natureza, as propriedades, a composição e as transformações da matéria. Ela está em nosso cotidiano e, ao
Exercícios Métodos de Separação. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017
 Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO:
 LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: Aguarde a ORDEM do fiscal para abrir este caderno de provas. Não será permitida a saída do candidato antes de esgotado o prazo mínimo de 60 minutos. Este caderno
LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: Aguarde a ORDEM do fiscal para abrir este caderno de provas. Não será permitida a saída do candidato antes de esgotado o prazo mínimo de 60 minutos. Este caderno
SOLUÇÃO PRATIQUE EM CASA
 SOLUÇÃO PC1. Incorreta. Seria pura se apresentasse apenas moléculas de água em sua composição, porém, a água potável apresenta diversos tipos de sais dissolvidos. Correta. A água do mar pode se tornar
SOLUÇÃO PC1. Incorreta. Seria pura se apresentasse apenas moléculas de água em sua composição, porém, a água potável apresenta diversos tipos de sais dissolvidos. Correta. A água do mar pode se tornar
CIÊNCIAS PROVA 3º BIMESTRE 9º ANO PROJETO CIENTISTAS DO AMANHÃ
 PREFEITURA DA CIDADE DO RIO DE JANEIRO SECRETARIA MUNICIPAL DE EDUCAÇÃO SUBSECRETARIA DE ENSINO COORDENADORIA DE EDUCAÇÃO CIÊNCIAS PROVA 3º BIMESTRE 9º ANO PROJETO CIENTISTAS DO AMANHÃ 2010 01. A tabela
PREFEITURA DA CIDADE DO RIO DE JANEIRO SECRETARIA MUNICIPAL DE EDUCAÇÃO SUBSECRETARIA DE ENSINO COORDENADORIA DE EDUCAÇÃO CIÊNCIAS PROVA 3º BIMESTRE 9º ANO PROJETO CIENTISTAS DO AMANHÃ 2010 01. A tabela
Tarefa 22 Professor Gustavo
 6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
LISTA DE EXERCÍCIOS 1º ANO
 GAB LISTA - 11 a) Elemento: Carbono; número de massa do isótopo do carbono com 8 nêutrons:14 b) Moléculas com ligações polares: (figura 01) Moléculas com ligações apolares: (figura 02) a) Observe a figura
GAB LISTA - 11 a) Elemento: Carbono; número de massa do isótopo do carbono com 8 nêutrons:14 b) Moléculas com ligações polares: (figura 01) Moléculas com ligações apolares: (figura 02) a) Observe a figura
Em meio aquoso sofrem dissociação liberando íons na água, o que torna o meio condutor de corrente elétrica.
 Aula 7 Funções Inorgânicas (sais e óxidos) Sal Os sais são compostos que possuem um cátion qualquer (só não pode ser exclusivamente o H +, senão será um ácido) e um ânion qualquer(só não pode ser exclusivamente
Aula 7 Funções Inorgânicas (sais e óxidos) Sal Os sais são compostos que possuem um cátion qualquer (só não pode ser exclusivamente o H +, senão será um ácido) e um ânion qualquer(só não pode ser exclusivamente
09) Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão:
 01) Indique a alternativa que completa corretamente as lacunas do seguinte período: Um elemento químico é representado pelo seu..., é identificado pelo número de... e pode apresentar diferentes números
01) Indique a alternativa que completa corretamente as lacunas do seguinte período: Um elemento químico é representado pelo seu..., é identificado pelo número de... e pode apresentar diferentes números
Exercícios Sobre Ocorrência de ReaÇões
 Exercícios Sobre Ocorrência de ReaÇões Dados: Força de ácidos e bases Ácidos fortes α 50 % Ácidos semifortes ou moderados 5 % α 50% Ácidos fracos α 5% Classificação dos hidrácidos mais conhecidos: Hidrácidos
Exercícios Sobre Ocorrência de ReaÇões Dados: Força de ácidos e bases Ácidos fortes α 50 % Ácidos semifortes ou moderados 5 % α 50% Ácidos fracos α 5% Classificação dos hidrácidos mais conhecidos: Hidrácidos
Associação Catarinense das Fundações Educacionais ACAFE PARECER DOS RECURSOS
 11) Assinale a alternativa correta. A O nitrogênio principal componente do ar atmosférico é uma substância composta forma-da pelo elemento nitrogênio, 10 N. B A água pura é uma substância líquida nas condições
11) Assinale a alternativa correta. A O nitrogênio principal componente do ar atmosférico é uma substância composta forma-da pelo elemento nitrogênio, 10 N. B A água pura é uma substância líquida nas condições
ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017
 ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017 1º ano Nome Nº Turma Data 15/12 Nota 08 Disciplina QUÍMICA TRABALHO Prof. ORLANDO Valor 30 ESTUDOS INDEPENDENTES DE RECUPERAÇÃO 01) Na química temos
ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017 1º ano Nome Nº Turma Data 15/12 Nota 08 Disciplina QUÍMICA TRABALHO Prof. ORLANDO Valor 30 ESTUDOS INDEPENDENTES DE RECUPERAÇÃO 01) Na química temos
1. Estados físicos da matéria Mudanças de estado Substâncias puras Misturas 4 Exercícios Densidade 6 1.
 1. Estados físicos da matéria 3 1.1 Mudanças de estado 3 1.2 Substâncias puras 4 1.3 Misturas 4 Exercícios 5 1.4 Densidade 6 1.5 Transformação da matéria 6 1.6 Alotropia 6 1.7 Diagramas de fases 6 1.8
1. Estados físicos da matéria 3 1.1 Mudanças de estado 3 1.2 Substâncias puras 4 1.3 Misturas 4 Exercícios 5 1.4 Densidade 6 1.5 Transformação da matéria 6 1.6 Alotropia 6 1.7 Diagramas de fases 6 1.8
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano
 EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
Química A Extensivo V. 6
 Extensivo V. 6 Resolva 1.01) D NaH forte iônica 1.0) 8 NH H Aula 1 Pb( H) fraca covalente 01. Incorreto. Base covalente 0. Incorreto. Base fraca; α pequeno 0. Correto. Papel tornassol azul 08. Correto.
Extensivo V. 6 Resolva 1.01) D NaH forte iônica 1.0) 8 NH H Aula 1 Pb( H) fraca covalente 01. Incorreto. Base covalente 0. Incorreto. Base fraca; α pequeno 0. Correto. Papel tornassol azul 08. Correto.
SIMPLES SUBSTÂNCIA PURA COMPOSTA HOMOGÊNEO MISTURA HOMOGÊNEA SISTEMA SUBSTÂNCIA PURA HETEROGÊNEO MISTURA HETEROGÊNEA
 Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico que contenha ou não matéria,
Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico que contenha ou não matéria,
02- Quais das propriedades a seguir são as mais indicadas para verificar se é pura uma certa amostra sólida de uma substância conhecida?
 PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
FUVEST 1981 Primeira fase e Segunda fase
 FUVEST 1981 Primeira fase e Segunda fase CONHECIMENTOS GERAIS 5. Nas condições ambientes, pastilhas de hidróxido de sódio, expostas ao ar durante várias horas, transformam-se em um líquido claro. Este
FUVEST 1981 Primeira fase e Segunda fase CONHECIMENTOS GERAIS 5. Nas condições ambientes, pastilhas de hidróxido de sódio, expostas ao ar durante várias horas, transformam-se em um líquido claro. Este
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
Funções da Química Inorgânica I
 Funções da Química Inorgânica I Introdução às funções e Ácidos. Química 1ª Série Profº Edilzo Filho Natal, Setembro de 2015. Introdução às funções inorgânicas Funções Orgânicas versus Funções Inorgânicas.
Funções da Química Inorgânica I Introdução às funções e Ácidos. Química 1ª Série Profº Edilzo Filho Natal, Setembro de 2015. Introdução às funções inorgânicas Funções Orgânicas versus Funções Inorgânicas.
REAÇÕES QUÍMICAS REAGENTES E PRODUTOS DE REAÇÃO
 REAÇÕES QUÍMICAS Os materiais podem sofrer transformações químicas ou transformações físicas. As transformações químicas são aquelas em que ocorre a formação de novas substâncias com propriedades diferentes
REAÇÕES QUÍMICAS Os materiais podem sofrer transformações químicas ou transformações físicas. As transformações químicas são aquelas em que ocorre a formação de novas substâncias com propriedades diferentes
Gabarito de Química Frente 2
 Gabarito de Química Frente 2 Módulo 05 01. E Calculo do nox: 1) HNO 3 1 + X + 3 x (- 2) = 0 X= + 5 +1 2 X 2) HNO 2 1 + Y + 2 x (- 2) = 0 Y= + 3 +1 Y 2 3) NH 3 Z + 3 x (+1) = 0 Z = - 3 Z 02.A +1 Para calcular
Gabarito de Química Frente 2 Módulo 05 01. E Calculo do nox: 1) HNO 3 1 + X + 3 x (- 2) = 0 X= + 5 +1 2 X 2) HNO 2 1 + Y + 2 x (- 2) = 0 Y= + 3 +1 Y 2 3) NH 3 Z + 3 x (+1) = 0 Z = - 3 Z 02.A +1 Para calcular
Professor: José Tiago Pereira Barbosa
 Professor: José Tiago Pereira Barbosa Química Orgânica Inorgânica Compostos que possuem átomos de Carbono Compostos que não possuem átomos de Carbono* *Alguns compostos contendo carbono são estudados
Professor: José Tiago Pereira Barbosa Química Orgânica Inorgânica Compostos que possuem átomos de Carbono Compostos que não possuem átomos de Carbono* *Alguns compostos contendo carbono são estudados
PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK
 PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK Substância Pura: Um único tipo de substância Simples: formada por átomos de um único elemento. Composta: formada por átomos de mais de um elemento.
PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK Substância Pura: Um único tipo de substância Simples: formada por átomos de um único elemento. Composta: formada por átomos de mais de um elemento.
Química B Extensivo V. 2
 Química B Extensivo V. 2 Exercícios Sistema Componentes Fases Classificação Água + gelo 1 2 Heterogêneo Água + 3 cubos de gelo 1 2 Heterogêneo Açúcar + sal 2 2 Heterogêneo Areia + enxofre + sal 3 3 Heterogêneo
Química B Extensivo V. 2 Exercícios Sistema Componentes Fases Classificação Água + gelo 1 2 Heterogêneo Água + 3 cubos de gelo 1 2 Heterogêneo Açúcar + sal 2 2 Heterogêneo Areia + enxofre + sal 3 3 Heterogêneo
Sistemas, Substâncias puras e Misturas Separação de Misturas
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
Reações envolvendo substâncias em solução aquosa: (reações por via úmida) e reações por via seca (substâncias não dissolvidas em solventes)
 Reações envolvendo substâncias em solução aquosa: (reações por via úmida) e reações por via seca (substâncias não dissolvidas em solventes) OBJETIVO: é possível fazer generalizações a respeito da ocorrência
Reações envolvendo substâncias em solução aquosa: (reações por via úmida) e reações por via seca (substâncias não dissolvidas em solventes) OBJETIVO: é possível fazer generalizações a respeito da ocorrência
SIMULADO de QUÍMICA 1 os anos 2008 TODOS COLÉGIOS
 SIMULADO de QUÍMICA 1 os anos 2008 TODOS COLÉGIOS 1) Em relação às partículas atômicas, a alternativa falsa é: a) a massa do próton é igual a massa do elétron. b) a massa do elétron é menor que a massa
SIMULADO de QUÍMICA 1 os anos 2008 TODOS COLÉGIOS 1) Em relação às partículas atômicas, a alternativa falsa é: a) a massa do próton é igual a massa do elétron. b) a massa do elétron é menor que a massa
Tarefa 09 à 12 Professor Willian. Com base no gráfico, assinale a alternativa que apresenta a afirmativa CORRETA.
 9º ano Química Tarefa 09 à 12 Professor Willian 01. Dois materiais sólidos, A e B, são aquecidos a uma velocidade de 10ºC.min 1. A figura a seguir representa o diagrama de aquecimento desses dois materiais.
9º ano Química Tarefa 09 à 12 Professor Willian 01. Dois materiais sólidos, A e B, são aquecidos a uma velocidade de 10ºC.min 1. A figura a seguir representa o diagrama de aquecimento desses dois materiais.
01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas:
 01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas: a) I é correta. d) I e II são corretas. b) II é correta. e) II e III são corretas. c) III é correta. 05) (UFPE-PE)
01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas: a) I é correta. d) I e II são corretas. b) II é correta. e) II e III são corretas. c) III é correta. 05) (UFPE-PE)
Luis Eduardo C. Aleotti. Química. Aula 26 - Funções Inorgânicas II: Ácidos
 Luis Eduardo C. Aleotti Química Aula 26 - Funções Inorgânicas II: Ácidos SAIS O que é? - H + proveniente de um ácido deixa o meio ácido. - OH - proveniente de uma base deixa o meio básico. - O que acontece
Luis Eduardo C. Aleotti Química Aula 26 - Funções Inorgânicas II: Ácidos SAIS O que é? - H + proveniente de um ácido deixa o meio ácido. - OH - proveniente de uma base deixa o meio básico. - O que acontece
Questão 10: Sobre as moléculas de CO 2 e SO 2, cujas estruturas estão representadas a seguir, é CORRETO afirmar que: S O O C O
 QUESTÕES OBJETIVAS Questão 9: Nitrogênio e fósforo são elementos essenciais para a nutrição das plantas e por isso alguns de seus compostos são utilizados na maioria dos fertilizantes. Sobre esses elementos
QUESTÕES OBJETIVAS Questão 9: Nitrogênio e fósforo são elementos essenciais para a nutrição das plantas e por isso alguns de seus compostos são utilizados na maioria dos fertilizantes. Sobre esses elementos
A nomenclatura dos sais é feita escrevendo-se o nome do ânion, a palavra de e o nome do cátion: (nome do ânion) de (nome do cátion)
 QUÍMICA GERAL - AULA 6 - SAIS E ÓXIDOS DATA: 18/09/2015 PROF. ANA - SAIS NEUTRALIZAÇÃO TOTAL Quando misturamos uma solução aquosa de HCl e uma solução aquosa de NaOH ocorre uma reação entre os íons H +
QUÍMICA GERAL - AULA 6 - SAIS E ÓXIDOS DATA: 18/09/2015 PROF. ANA - SAIS NEUTRALIZAÇÃO TOTAL Quando misturamos uma solução aquosa de HCl e uma solução aquosa de NaOH ocorre uma reação entre os íons H +
QUÍMICA QUESTÃO O oxigênio e o enxofre podem ser encontrados como moléculas O 2 QUESTÃO 32
 T 20 QUÍMCA QUESTÃ 3 Com exceção dos gases nobres, os elementos químicos, em condições ambientais, podem ser encontrados sob diferentes formas: como metais ou ligas, substâncias moleculares, substâncias
T 20 QUÍMCA QUESTÃ 3 Com exceção dos gases nobres, os elementos químicos, em condições ambientais, podem ser encontrados sob diferentes formas: como metais ou ligas, substâncias moleculares, substâncias
Resumão do Hondinha. Reações químicas. Reações químicas
 Resumão do Hondinha Reações químicas Em uma reação química ocorre a transformação de substâncias com determinadas propriedades iniciais (reagentes) em outras com propriedades diferentes (produtos). As
Resumão do Hondinha Reações químicas Em uma reação química ocorre a transformação de substâncias com determinadas propriedades iniciais (reagentes) em outras com propriedades diferentes (produtos). As
Gabaritos Resolvidos Energia Química Semiextensivo V4 Frente C
 01) E Quanto maior a constante ácida, maior a força do ácido (acidez). Assim, HF < HCl < HBr < HI Ordem crescente de acidez (mais fraco para o mais forte) a) Errada é o HI (ácido mais forte); b) Errada
01) E Quanto maior a constante ácida, maior a força do ácido (acidez). Assim, HF < HCl < HBr < HI Ordem crescente de acidez (mais fraco para o mais forte) a) Errada é o HI (ácido mais forte); b) Errada
O que é uma propriedade funcional da matéria? Acidez Alcalinidade Salinidade. Funções químicas
 O que é uma propriedade funcional da matéria? Acidez Alcalinidade Salinidade Funções químicas Função química Conjunto de compostos que possuem comportamento semelhantes Ácidos bases Sais Óxidos Mas você
O que é uma propriedade funcional da matéria? Acidez Alcalinidade Salinidade Funções químicas Função química Conjunto de compostos que possuem comportamento semelhantes Ácidos bases Sais Óxidos Mas você
EXERCÍCIOS DE QUÍMICA
 INTRODUÇÃO AO ESTUDO DA QUÍMICA FENÔMENOS FÍSICOS E QUÍMICOS SUBSTÂNCIAS PURAS E MISTURAS ATOMICIDADE - ALOTROPIA 1. (UFPE) Em quais das passagens a seguir está ocorrendo transformação química? (1) O reflexo
INTRODUÇÃO AO ESTUDO DA QUÍMICA FENÔMENOS FÍSICOS E QUÍMICOS SUBSTÂNCIAS PURAS E MISTURAS ATOMICIDADE - ALOTROPIA 1. (UFPE) Em quais das passagens a seguir está ocorrendo transformação química? (1) O reflexo
Ionização Ácido é toda substância que em solução aquosa libera íon H +
 Ácidos Ionização Ácido é toda substância que em solução aquosa libera íon H + Equação de Ionização de ácidos: HCl H + + Cl - H 2 SO 4 2H + + SO 4-2 H 3 PO 4 3H + + PO 4-3 Classificação a)quanto ao número
Ácidos Ionização Ácido é toda substância que em solução aquosa libera íon H + Equação de Ionização de ácidos: HCl H + + Cl - H 2 SO 4 2H + + SO 4-2 H 3 PO 4 3H + + PO 4-3 Classificação a)quanto ao número
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017
 III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
BIMESTRAL QUÍMICA - 1ºBIMESTRE
 BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
Propriedades da matéria
 Propriedades da matéria Gerais específicas Funcionais O que é uma propriedade funcional da matéria? Grupos de substâncias cujas características e propriedades se assemelham Função química Ácidos bases
Propriedades da matéria Gerais específicas Funcionais O que é uma propriedade funcional da matéria? Grupos de substâncias cujas características e propriedades se assemelham Função química Ácidos bases
QUÍMICA FUNÇÕES INORGÂNICAS ÁCIDOS. Professor: Rafael Odorico
 QUÍMICA FUNÇÕES INORGÂNICAS ÁCIDOS FUNÇÕES QUÍMICAS Algumas substâncias químicas com propriedades semelhantes foram agrupadas em funções químicas. Função Química conjunto de compostos com propriedades
QUÍMICA FUNÇÕES INORGÂNICAS ÁCIDOS FUNÇÕES QUÍMICAS Algumas substâncias químicas com propriedades semelhantes foram agrupadas em funções químicas. Função Química conjunto de compostos com propriedades
Gabarito Química Volume 1
 Gabarito Química Volume 1 Química 1 Capítulo 1 01. D 05. A 06. C 07. A 08. C 09. E 10. C 11. E 12. D 13. D 14. C 15. D 16. A 17. A 19. A 21. B 23. C 24. D 25. B 26. D 27. A 28. C 29. D 30. E 31. C 33.
Gabarito Química Volume 1 Química 1 Capítulo 1 01. D 05. A 06. C 07. A 08. C 09. E 10. C 11. E 12. D 13. D 14. C 15. D 16. A 17. A 19. A 21. B 23. C 24. D 25. B 26. D 27. A 28. C 29. D 30. E 31. C 33.
resoluções de exercícios
 resoluções de exercícios QUÍMIA I apítulo Água 04 Funções Inorgânicas BL 01 H ácido sulfúrico é classificado como ácido fixo, ou seja, menos volátil BL 0 A) Incorreta é uma substância composta de elementos
resoluções de exercícios QUÍMIA I apítulo Água 04 Funções Inorgânicas BL 01 H ácido sulfúrico é classificado como ácido fixo, ou seja, menos volátil BL 0 A) Incorreta é uma substância composta de elementos
