Faremos uma breve introdução sobre proteínas usando os livros textos que constam nas referências: Lehninger et al., 1993; Stryer, 1995 e Dose, 1982.
|
|
|
- Elisa Pinto Ramires
- 8 Há anos
- Visualizações:
Transcrição
1 3. Proteínas Faremos uma breve introdução sobre proteínas usando os livros textos que constam nas referências: Lehninger et al., 1993; Stryer, 1995 e Dose, Estrutura de Proteínas Em animais superiores, as proteínas são os compostos orgânicos mais abundantes, representam cerca de 50 % do peso seco dos tecidos. Do ponto de vista funcional, seu papel é fundamental, não existindo processo biológico que não dependa da presença ou da atividade deste tipo de biomolécula. As proteínas desempenham inúmeras funções distintas, como por exemplo: enzimas, hormônios, proteínas transportadoras, anticorpos e receptores de muitas células. Todas as proteínas contêm carbono, hidrogênio, oxigênio e nitrogênio e muitas possuem enxofre. Há variações na composição de diferentes proteínas, porém a quantidade de nitrogênio, representa, em média, 16 % da massa total da molécula. Dessa forma pode-se calcular a quantidade aproximada de proteína em uma amostra medindo-se a quantidade de nitrogênio da mesma. As proteínas são moléculas poliméricas de grande tamanho, pertencendo à categoria das macromoléculas, constituídas por um grande número de unidades monoméricas estruturais os aminoácidos que formam grandes cadeias. Devido a esse grande tamanho, quando são dispersas em um solvente adequado, formam soluções coloidais, que possuem características especiais que as distinguem das soluções de moléculas pequenas. Por meio da hidrólise podemos clivá-las em seqüências menores de aminoácidos, pois centenas ou milhares de aminoácidos podem participar na formação de uma grande molécula polimérica de uma proteína. As proteínas são formadas através de ligações peptídicas entre os diversos tipos de aminoácidos e podemos classificá-las em duas grandes categorias:
2 26 - Proteínas globulares: são proteínas em que as cadeias de aminoácidos se voltam sobre elas mesmas, formando um conjunto compacto que tem forma esferóide ou elipsóide, em que os três eixos da molécula tendem a ser de tamanhos similares. Em geral, são proteínas de grande atividade funcional, como por exemplo, as enzimas, os anticorpos, os hormônios, a hemoglobina; são solúveis em meios aquosos. - Proteínas fibrosas: são proteínas em que as cadeias de aminoácidos se ordenam de maneira paralela, formando fibras ou lâminas estendidas, nas quais o eixo longitudinal predomina sobre os transversais. Em geral, são pouco solúveis em água e participam na formação de estruturas de sustentação, como as fibras do tecido conjuntivo e outras formações de tecidos de grande resistência mecânica. A estrutura molecular das proteínas é muito complexa, por essa razão é conveniente dividi-la em níveis distintos de organização: Figura 3.1 Níveis de organização da estrutura molecular de uma proteína. - Estrutura primária: refere-se ao número e identidade dos aminoácidos que compõem a molécula e ao ordenamento ou seqüência dessas unidades na cadeia polipeptídica. A união peptídica somente permite a formação de estruturas lineares e por isso, as cadeias não apresentam ramificações.
3 27 - Estrutura secundária: a medida que o comprimento das cadeias vai aumentando e em função das condições físico-químicas do meio, se cria a estrutura secundária, que é a disposição espacial regular, repetitiva, que a cadeia polipeptídica pode adotar, geralmente mantida por ligações de hidrogênio. Podemos ter: - a) Hélice-alfa: as cadeias de aminoácidos têm vários centros polares e, devido a isto, a fibra enrola-se dando lugar a uma hélice que se estabiliza formando ligações intramoleculares com pontes de hidrogênio. Figura 3.2 Exemplo de uma estrutura do tipo hélice-alfa. - b) Folha-beta: as cadeias de peptídeos se unem formando filas paralelas que se estabilizam de maneira intermolecular mediante pontes de hidrogênio.
4 28 Figura 3.3 Exemplo de uma estrutura do tipo folha-beta. - Estrutura terciária: é a estrutura da maioria das proteínas globulares, aparece a partir das hélices, que voltam a enrolar-se. É uma estrutura tridimensional completa que forma-se a partir das forças de atração ou repulsão eletrostática, das pontes de hidrogênio, das forças de Van der Waals e das pontes dissulfeto existentes entre os resíduos de aminoácidos que formam as cadeias.
5 29 Figura 3.4 Exemplo de estrutura terciária de uma proteína. - Estrutura quaternária: são estruturas de caráter oligomérico, que estão compostas por várias moléculas separadas, mas entrelaçadas em estrutura terciária. Se aplica somente a proteínas constituídas por duas ou mais cadeias polipeptídicas e se refere a disposição espacial dessas cadeias e as ligações que se estabelecem entre elas pontes de hidrogênio, atrações eletrostáticas, interações hidrofóbicas, pontes dissulfeto entre cisteínas de cadeias diferentes. Um exemplo deste tipo de estrutura é a hemoglobina que é composta por quatro subunidades semelhantes à mioglobina. 3.2 Albumina e Insulina Albumina sérica é uma das proteínas mais estudadas e é a mais abundante no plasma com uma concentração típica de 5g / 100ml. Muitos pesquisadores têm estudado a estrutura e as propriedades da albumina sérica e suas interações com
6 30 outras proteínas com o intuito de compreender todas as suas funções no organismo (Friedli, 2005). A albumina sérica é a mais abundante proteína no sistema circulatório e contribui em 80% para a manutenção da pressão osmótica do sangue. É também um dos principais responsáveis pela manutenção do ph do sangue. Nos mamíferos, a albumina é sintetizada inicialmente como preproalbumina pelo fígado. Após a remoção do peptídeo sinal, tem-se a proalbumina que será modificada pela remoção de seis resíduos de propeptídeo do novo terminal N. A albumina enviada para a circulação sangüínea possui uma meia-vida de 19 dias. Como a albumina é sintetizada no fígado, a diminuição de sua quantidade no plasma pode ser produto de uma doença hepática, mas também pode ser o resultado de uma doença renal que permita que a albumina escape pela urina. Sua diminuição pode também estar relacionada a desnutrição ou uma dieta pobre em proteínas. Existem resultados contraditórios e muitas discussões sobre a determinação da estrutura da albumina, porém com base em experimentos de hidrodinâmica e espalhamento de raios-x, a albumina sérica aproxima-se de um elipsóide de 140 x 40 Angstrons com três domínios homólogos. Albuminas são caracterizadas por conterem um número pequeno de resíduos de triptofano e metionina e um alto número de cistina e aminoácidos carregados, ácidos aspártico e glutâmico, lisina e arginina. O conteúdo de glicina e isoleucina é menor que a média encontrada em proteínas. Tanto a albumina bovina (BSA) quanto a humana (HSA) possuem apenas um resíduo de cisteína livre, Cys34. Os outros formam 17 pontes dissulfeto ajudando a manter a estrutura terciária. A albumina bovina (BSA) possui 2 resíduos de triptofano, Trp134 e Trp212 e a humana (HSA) apenas um, Trp214. A Fig. 3.5 abaixo mostra a estrutura de cadeias de duas moléculas de HSA (PDB, 1BM0), onde os resíduos Cys34 e Trp214 aparecem como esferas.
7 31 Figura 3.5 Estrutura quaternária da HSA com os resíduos de cisteína e triptofano em destaque. (Construída a partir das coordenadas 1BM0, disponíveis no PDB, Protein Data Bank) Talvez, a mais interessante propriedade da albumina seja sua capacidade de ligar-se reversivelmente a uma grande variedade de ligantes. A albumina é a principal transportadora de ácidos graxos, que são insolúveis no plasma sangüíneo. Também possui muitas outras funções, como seqüestrar radicais livres de oxigênio e inativar vários metabólitos lipofílicos tóxicos como a bilirrubina. A albumina tem uma grande afinidade por ácidos graxos, hematina, bilirrubina e por pequenos compostos aromáticos negativamente carregados. Forma ligações covalentes com fosfato piridoxil, cisteína, glutationa e vários metais como cobre, níquel, mercúrio, prata e ouro. No plasma circulante, aproximadamente 30 % dos grupos SH livres, Cys34, são oxidados por cisteína e glutationa. Como a albumina é uma proteína transportadora multifuncional, acredita-se que ela possa ser uma transportadora ou reservatório de óxido nítrico, e possa estar relacionada com importantes processos fisiológicos ainda não compreendidos envolvendo o NO. A insulina é uma proteína composta de duas cadeias polipeptídicas, chamadas de cadeia A e cadeia B. As cadeias A e B são mantidas unidas por duas pontes dissulfeto; há uma outra ponte dissulfeto no interior da cadeia A. Não há
8 32 cisteína livre. Na maioria das espécies, a cadeia A consiste de 21 resíduos de aminoácidos e a cadeia B, de 30. Na molécula de insulina não há resíduos de triptofano. A Fig. 3.6 mostra a estrutura de cadeias de duas moléculas de insulina (PDB, 1GUJ), onde os resíduos de cisteína formam pontes dissulfeto, estão apresentados na estrutura esfera-bastão. Figura 3.6 Duas moléculas de insulina com as pontes dissulfeto em destaque. (Construída a partir das coordenadas 1GUJ, disponíveis no PDB, Protein Data Bank) Apesar da seqüência de aminoácidos da insulina variar entre espécies, certos segmentos da molécula são altamente conservados, incluindo as posições das três pontes dissulfeto, os finais da cadeia A e os resíduos C-terminal da cadeia B. Estas similaridades na seqüência de aminoácidos da insulina levam a uma conformação tridimensional que é muito parecida entre as espécies. Dessa forma uma molécula de insulina de um animal tem uma atividade biológica muito semelhante quando inoculada em outro animal de espécie diferente. Por isso, a insulina do porco foi muito usada no tratamento de pacientes humanos diabéticos. O nível de glicose sangüínea nos mamíferos é controlado principalmente por dois hormônios protéicos produzidos no pâncreas pelas ilhotas de Langerhans: a insulina e o glucagon. A função da insulina é estimular a entrada de glicose do sangue para o interior das células sempre que houver hiperglicemia, como após as refeições. A ligação da insulina aos seus receptores na membrana da célula, desencadeia uma série de reações bioquímicas em cascata, fosforilações e desfosforilações a partir do receptor de tirosina cinase, que aumentarão o número
9 33 de receptores de glicose na membrana da célula, conhecidos como receptores GLUT. Já o glucagon estimula a liberação de glicose especialmente no fígado e no tecido adiposo em casos de hipoglicemia, como nos intervalos entre as refeições. Os indivíduos que não produzem insulina suficiente para o controle da glicemia sangüínea são portadores de diabetes do tipo 1 juvenil e dependem da administração de insulina. Os portadores de diabetes tipo 2 em geral são adultos que produzem insulina em quantidade suficiente ou aumentada, mas suas células não são sensíveis a ela. Através do trabalho de Frederick Sanger, a insulina foi o primeiro hormônio peptídico a ter sua seqüência de aminoácidos conhecida (Miranda e Loffredo, 2005). 3.3 Modificação de Proteínas por Óxidos de Nitrogênio Em células, os principais alvos de espécies reativas derivadas de óxido nítrico são proteínas e resíduos de aminoácidos que contém cisteína e tirosina. Stamler at al. (1992) demonstraram que proteínas S-nitrosiladas são formadas sob condições fisiológicas e possuem efeitos de vasodilatação e inibição plaquetária. Essas observações sugeriram que grupos S-nitrosotióis pertencentes a proteínas podem servir como intermediários no metabolismo celular do NO e apresentam a possibilidade de um mecanismo celular adicional regulatório. Usando BSA e NaNO 2 em meio ácido e espectroscopia de absorção, esses autores obtiveram a confirmação da formação de S-nitrosotióis em proteínas. Nitrito de sódio (NaNO 2 ) em meio ácido (HCl) produz HNO 2 e pequenas quantidades de N 2 O 3 e NOCl, todos agentes de nitrosação. S-nitrosothiols podem ser facilmente sintetizados em laboratório pela reação entre tióis e ácido nitroso (formado por nitrito em HCl, por exemplo). HNO2 + RSH RSNO + H2O. Esse caminho não ocorre em ph fisiológico e é relevante em condições de acidez extrema (ph < 3). No laboratório este método é adequado para tióis de pequena massa molecular, como glutationa e cisteína, mas não proteínas por causa da desnaturação ácida e porque outros grupos funcionais, como aminas, álcoois e aromáticos, são susceptíveis a modificações por nitrito acidificado (Hogg, 2002). Para síntese de S-nitrosotióis de proteínas, um método mais adequado envolve a
10 34 transferência espontânea do grupo nitroso de um S-nitrosotiol de baixa massa molecular. No entanto, essa reação é reversível, sendo a constante de equilíbrio ~1. S-nitrosotióis possuem dois picos de absorção máxima, um na região de nm e outro muito menor em ~ 550 nm. Para S-nitroso BSA, foram obtidos picos em 335 e 545 nm com coeficientes de absorção molar de 3869 M 1. cm 1 e 47 M 1. cm 1, respectivamente (Stamler et al., 1992). Zhang et al. (1996) estudaram a nitrosação da BSA com NaNO 2 em meio ácido em comparação com a nitrosação de carboximetil-bsa, em que o grupo tiol está covalentemente ligado. Obtiveram resultados que indicaram que outros grupos além de cisteína estavam reagindo com HNO 2 e formavam cromóforos com espectro de absorção semelhante ao de S-nitrosotióis. Através de medidas espectrofotométricas de 16 modelos de dipeptídeos, que continham o resíduo de glicina e mais um resíduo variável, mostraram que o dipeptídeo glicina-triptofano era o único que apresentava significativa nitrosação nestas condições e que o grupo NO ligava-se ao nitrogênio do anel indol do triptofano. Comparando estes resultados com os obtidos para BSA nativa e bloqueada concluíram que resíduos de triptofano eram nitrosados nesta proteína, e não apenas resíduos de cisteína. Rassaf et al. (2002) mostraram a presença concomitante de proteínas do tipo N-nitroso e S-nitroso no plasma humano. Usando quimioluminescência em fase gasosa e cromatografia líquida, mediram os níveis basais no plasma de metabólitos relacionados ao NO em 18 voluntários saudáveis. Eles descobriram que em adição aos produtos oxidativos do metabolismo do NO, nitrito (0,20 + 0,02 µm) e nitrato (14,4 + 1,7 µm), o plasma humano médio contém aproximadamente 5 vezes mais concentrações de espécies de N-nitroso (32,3 + 5,0 nm) que S-nitrosotióis (7,2 + 1,1 nm). As quantidades de N-nitroso e S- nitroso aparecem associadas com frações de albumina, mostrando a presença de um composto formado por uma molécula de alto peso molecular do tipo N-nitroso na circulação humana, levantando a questão sobre sua origem e potencial papel fisiológico. Harohalli et al. (2002) estudaram os padrões de liberação de NO em BSA e HSA nitrosadas e os compararam a várias formas de HSA mutantes recombinantes nitrosadas. Todas as espécies de albuminas foram nitrosadas com
11 35 NO 2 em meio ácido. Eles encontraram padrões de liberação de NO a partir de BSA nitrosada de acordo com artigos anteriores que indicam que Cys-34 é o principal alvo de nitrosação, porém em HSA nitrosada o principal alvo de nitrosação foi um resíduo de aminoácido diferente de Cys-34. Utilizando as diferentes espécies recombinantes de HSA nitrosadas produzidas concluíram que o Trp-214 é o principal alvo de nitrosação em HSA. Mutações em Trp-214 levaram a um aumento na nitrosação de Cys-34, indicando uma possível competição entre estes dois resíduos para reação com N 2 O 3, a espécie reativa de nitrosação formada em soluções aquosas ácidas de NO 2. Os valores médios de tempo para triptofano nitrosado foram determinados a partir das medidas de NO liberado na ausência de Hg 2+. Os autores encontraram min para a BSA e min para HSA, ambas comerciais (Sigma). Kirsch et al. (2003) estudaram a N-nitrosação de derivados de triptofano com o N terminal bloqueado na presença de sistemas geradores de N 2 O 3, como os doadores de NO na presença de oxigênio em ph 7,4. Nessas condições, a N- nitrosação de N-acetil-triptofano e lisina-triptofano-lisina foi provada, respectivamente, por espectroscopia UV-vis e por espectrometria 15 N NMR. Os dados dos autores mostraram conclusivamente que N 2 O 3 provoca a nitrosação da função amina secundária (N indol ) do anel indol do triptofano N-bloqueado com alta reatividade em valores de ph fisiológicos. Noble e Williams (2000) estudaram a formação e as reações de proteínas do tipo S-nitroso. A nitrosação da BSA por ácido nitroso ocorre em dois estágios: um rápido, consistente com uma reação de S-nitrosação da unidade de cisteína livre, seguido de um lento, que é consistente com uma reação de N-nitrosação de um resíduo de triptofano. Os autores obtiveram resultados de cinética química para ambos estágios que sugerem, em teoria, que proteínas do tipo S-nitroso podem atuar como reservatório de NO. Suzuki et al. (2004) realizaram experimentos sobre reações de peroxinitrito e outras espécies reativas de nitrogênio com N-acetil-L-triptofano sobre várias condições e mostraram que resíduos de triptofano podem ser nitrados, nitrosados e oxidados por espécies reativas de nitrogênio, necessitando de estudos posteriores para correlacionar perda de função de proteínas e tipo de modificações sofridas nos resíduos de triptofano.
12
ESTRUTURA DAS PROTEÍNAS
 ESTRUTURA DAS PROTEÍNAS Aminoácidos ligam-se por ligações peptídicas = reação de condensação entre: OH do grupo carboxila de um aminoácido H do grupo amina do outro aminoácido ( liberação de uma molécula
ESTRUTURA DAS PROTEÍNAS Aminoácidos ligam-se por ligações peptídicas = reação de condensação entre: OH do grupo carboxila de um aminoácido H do grupo amina do outro aminoácido ( liberação de uma molécula
Água e Solução Tampão
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
Professor Fernando Stuchi M ETABOLISMO DE C ONSTRUÇÃO
 M ETABOLISMO DE C ONSTRUÇÃO P ROTEÍNAS P ROPRIEDADE BÁSICA São grandes moléculas (macromoléculas) constituídas por aminoácidos, através de ligações peptídicas. É o composto orgânico mais abundante no corpo
M ETABOLISMO DE C ONSTRUÇÃO P ROTEÍNAS P ROPRIEDADE BÁSICA São grandes moléculas (macromoléculas) constituídas por aminoácidos, através de ligações peptídicas. É o composto orgânico mais abundante no corpo
DETERMINAÇÃO DA ESTRUTURA TRIDIMENSIONAL DE PROTEÍNAS POR DIFRAÇÃO DE RAIOS-X
 DETERMINAÇÃO DA ESTRUTURA TRIDIMENSIONAL DE PROTEÍNAS POR DIFRAÇÃO DE RAIOS-X Disciplina: Engenharia de Proteínas Ma. Flávia Campos Freitas Vieira NÍVEIS ESTRUTURAIS DAS PROTEÍNAS Fonte: Lehninger, 2010.
DETERMINAÇÃO DA ESTRUTURA TRIDIMENSIONAL DE PROTEÍNAS POR DIFRAÇÃO DE RAIOS-X Disciplina: Engenharia de Proteínas Ma. Flávia Campos Freitas Vieira NÍVEIS ESTRUTURAIS DAS PROTEÍNAS Fonte: Lehninger, 2010.
Professor Carlos - Proteinas
 14085. (Fuvest 2001) Os três compostos abaixo têm uso farmacológico Considere as afirmações: I Nas moléculas dos três compostos, há ligações peptídicas. II A porcentagem em massa de oxigênio na dropropizina
14085. (Fuvest 2001) Os três compostos abaixo têm uso farmacológico Considere as afirmações: I Nas moléculas dos três compostos, há ligações peptídicas. II A porcentagem em massa de oxigênio na dropropizina
Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I. Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas.
 Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I Acompanhe! Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas. Introdução: A proteína é o composto orgânico mais abundante
Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I Acompanhe! Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas. Introdução: A proteína é o composto orgânico mais abundante
As bactérias operárias
 A U A UL LA As bactérias operárias Na Aula 47 você viu a importância da insulina no nosso corpo e, na Aula 48, aprendeu como as células de nosso organismo produzem insulina e outras proteínas. As pessoas
A U A UL LA As bactérias operárias Na Aula 47 você viu a importância da insulina no nosso corpo e, na Aula 48, aprendeu como as células de nosso organismo produzem insulina e outras proteínas. As pessoas
Questões. Biologia Professor: Rubens Oda 24/11/2014. #VaiTerEspecífica. 1 (UEMG 2014) Considere, a seguir, a recorrência de uma heredopatia.
 Questões 1 (UEMG 2014) Considere, a seguir, a recorrência de uma heredopatia. De acordo com o heredograma e outros conhecimentos sobre o assunto, é CORRETO afirmar que a) normalidade ocorre na ausência
Questões 1 (UEMG 2014) Considere, a seguir, a recorrência de uma heredopatia. De acordo com o heredograma e outros conhecimentos sobre o assunto, é CORRETO afirmar que a) normalidade ocorre na ausência
Hoje estudaremos a bioquímica dos ácidos nucléicos. Acompanhe!
 Aula: 2 Temática: Ácidos Nucléicos Hoje estudaremos a bioquímica dos ácidos nucléicos. Acompanhe! Introdução: Os ácidos nucléicos são as moléculas com a função de armazenamento e expressão da informação
Aula: 2 Temática: Ácidos Nucléicos Hoje estudaremos a bioquímica dos ácidos nucléicos. Acompanhe! Introdução: Os ácidos nucléicos são as moléculas com a função de armazenamento e expressão da informação
As proteínas transportadoras
 As proteínas transportadoras 10 A U L A objetivos Ao final desta aula, você deverá compreender o que são: Proteínas transportadoras: carreadores e canais. Aquaporinas. Biologia Celular As proteínas transportadoras
As proteínas transportadoras 10 A U L A objetivos Ao final desta aula, você deverá compreender o que são: Proteínas transportadoras: carreadores e canais. Aquaporinas. Biologia Celular As proteínas transportadoras
Regulação do metabolismo do glicogênio
 Regulação do metabolismo do glicogênio A U L A 27 objetivos Ao final desta aula, você deverá ser capaz de: Aprender sobre as vias de regulação do metabolismo de glicogênio. Reforçar os conceitos adquiridos
Regulação do metabolismo do glicogênio A U L A 27 objetivos Ao final desta aula, você deverá ser capaz de: Aprender sobre as vias de regulação do metabolismo de glicogênio. Reforçar os conceitos adquiridos
Proteínas. As proteínas são o centro da acção em todos os processos biológicos. Voet & Voet Biochemistry
 Proteínas As proteínas são o centro da acção em todos os processos biológicos. Voet & Voet Biochemistry As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (~50% do peso sêco)
Proteínas As proteínas são o centro da acção em todos os processos biológicos. Voet & Voet Biochemistry As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (~50% do peso sêco)
As membranas são os contornos das células, compostos por uma bicamada lipídica
 Células e Membranas As membranas são os contornos das células, compostos por uma bicamada lipídica Organelas são compartimentos celulares limitados por membranas A membrana plasmática é por si só uma organela.
Células e Membranas As membranas são os contornos das células, compostos por uma bicamada lipídica Organelas são compartimentos celulares limitados por membranas A membrana plasmática é por si só uma organela.
ANTICORPOS. CURSO: Farmácia DISCIPLINA: Microbiologia e Imunologia Clínica PROFESSORES: Guilherme Dias Patto Silvia Maria Rodrigues Querido
 CURSO: Farmácia DISCIPLINA: Microbiologia e Imunologia Clínica PROFESSORES: Guilherme Dias Patto Silvia Maria Rodrigues Querido ANTICORPOS Anticorpo é uma globulina sintetizada por linfócitos B e principalmente
CURSO: Farmácia DISCIPLINA: Microbiologia e Imunologia Clínica PROFESSORES: Guilherme Dias Patto Silvia Maria Rodrigues Querido ANTICORPOS Anticorpo é uma globulina sintetizada por linfócitos B e principalmente
UFABC Bacharelado em Ciência & Tecnologia
 UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades e funções de proteínas: Mioglobina / Hemoglobina
UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades e funções de proteínas: Mioglobina / Hemoglobina
Princípios moleculares dos processos fisiológicos
 2012-04-30 UNIVERSIDADE AGOSTINHO NETO FACULDADE DE CIÊNCIAS DEI-BIOLOGIA ---------------------------------------------- Aula 5: Princípios moleculares dos processos fisiológicos (Fisiologia Vegetal, Ano
2012-04-30 UNIVERSIDADE AGOSTINHO NETO FACULDADE DE CIÊNCIAS DEI-BIOLOGIA ---------------------------------------------- Aula 5: Princípios moleculares dos processos fisiológicos (Fisiologia Vegetal, Ano
M E T B O L I S M O CATABOLISMO ANABOLISMO
 METABOLISMO É o conjunto das reações químicas que ocorrem num organismo vivo com o fim de promover a satisfação de necessidades estruturais e energéticas. ...metabolismo Do ponto de vista físico-químico,
METABOLISMO É o conjunto das reações químicas que ocorrem num organismo vivo com o fim de promover a satisfação de necessidades estruturais e energéticas. ...metabolismo Do ponto de vista físico-químico,
Nestas últimas aulas irei abordar acerca das vitaminas. Acompanhe!
 Aula: 31 Temática: Vitaminas parte I Nestas últimas aulas irei abordar acerca das vitaminas. Acompanhe! Introdução O termo vitamina refere-se a um fator dietético essencial requerido por um organismo em
Aula: 31 Temática: Vitaminas parte I Nestas últimas aulas irei abordar acerca das vitaminas. Acompanhe! Introdução O termo vitamina refere-se a um fator dietético essencial requerido por um organismo em
Cap. 4: Componentes orgânicos celulares As moléculas multifuncionais. Equipe de Biologia
 ap. 4: omponentes orgânicos celulares As moléculas multifuncionais Equipe de Biologia De que são formados os seres vivos? Substâncias orgânicas arboidratos Lipídios Proteínas Vitaminas Ácidos nucleicos
ap. 4: omponentes orgânicos celulares As moléculas multifuncionais Equipe de Biologia De que são formados os seres vivos? Substâncias orgânicas arboidratos Lipídios Proteínas Vitaminas Ácidos nucleicos
Hormonas e mensageiros secundários
 Hormonas e mensageiros secundários Interrelação entre os tecidos Comunicação entre os principais tecidos Fígado tecido adiposo hormonas sistema nervoso substratos em circulação músculo cérebro 1 Um exemplo
Hormonas e mensageiros secundários Interrelação entre os tecidos Comunicação entre os principais tecidos Fígado tecido adiposo hormonas sistema nervoso substratos em circulação músculo cérebro 1 Um exemplo
ANÁLISE QUÍMICA INSTRUMENTAL
 ANÁLISE QUÍMICA INSTRUMENTAL CROMATOGRAFIA 2 1 6 Ed. Cap. 10 268-294 6 Ed. Cap. 6 Pg.209-219 6 Ed. Cap. 28 Pg.756-829 6 Ed. Cap. 21 Pg.483-501 3 Separação Química Princípios de uma separação. Uma mistura
ANÁLISE QUÍMICA INSTRUMENTAL CROMATOGRAFIA 2 1 6 Ed. Cap. 10 268-294 6 Ed. Cap. 6 Pg.209-219 6 Ed. Cap. 28 Pg.756-829 6 Ed. Cap. 21 Pg.483-501 3 Separação Química Princípios de uma separação. Uma mistura
INTERAÇÃO DOS RAIOS-X COM A MATÉRIA
 INTERAÇÃO DOS RAIOS-X COM A MATÉRIA RAIOS-X + MATÉRIA CONSEQUÊNCIAS BIOLÓGICAS EFEITOS DAZS RADIAÇÕES NA H2O A molécula da água é a mais abundante em um organismo biológico, a água participa praticamente
INTERAÇÃO DOS RAIOS-X COM A MATÉRIA RAIOS-X + MATÉRIA CONSEQUÊNCIAS BIOLÓGICAS EFEITOS DAZS RADIAÇÕES NA H2O A molécula da água é a mais abundante em um organismo biológico, a água participa praticamente
Síntese Artificial de Peptídeos
 Síntese Artificial de Peptídeos Rebeca Bayeh Seminário apresentado para a disciplina Princípios Físicos Aplicados à Fisiologia (PGF530) Prof. Dr. Adriano Mesquita Alencar Segundo semestre de 2013 Motivação
Síntese Artificial de Peptídeos Rebeca Bayeh Seminário apresentado para a disciplina Princípios Físicos Aplicados à Fisiologia (PGF530) Prof. Dr. Adriano Mesquita Alencar Segundo semestre de 2013 Motivação
Criado e Desenvolvido por: RONNIELLE CABRAL ROLIM Todos os direitos são reservados 2015. www.tioronni.com
 Criado e Desenvolvido por: RONNIELLE CABRAL ROLIM Todos os direitos são reservados 2015. www.tioronni.com ÁCIDOS NUCLEICOS ÁCIDOS NUCLÉICOS: são substâncias formadoras de genes, constituídas por um grande
Criado e Desenvolvido por: RONNIELLE CABRAL ROLIM Todos os direitos são reservados 2015. www.tioronni.com ÁCIDOS NUCLEICOS ÁCIDOS NUCLÉICOS: são substâncias formadoras de genes, constituídas por um grande
CONTROLE E INTEGRAÇÂO
 CONTROLE E INTEGRAÇÂO A homeostase é atingida através de uma série de mecanismos reguladores que envolve todos os órgãos do corpo. Dois sistemas, entretanto, são destinados exclusivamente para a regulação
CONTROLE E INTEGRAÇÂO A homeostase é atingida através de uma série de mecanismos reguladores que envolve todos os órgãos do corpo. Dois sistemas, entretanto, são destinados exclusivamente para a regulação
Equipe de Biologia. Biologia
 Aluno (a): Série: 3ª Turma: TUTORIAL 5B Ensino Médio Equipe de Biologia Data: Biologia Ácidos nucléicos Os ácidos nucléicos são moléculas gigantes (macromoléculas), formadas por unidades monoméricas menores
Aluno (a): Série: 3ª Turma: TUTORIAL 5B Ensino Médio Equipe de Biologia Data: Biologia Ácidos nucléicos Os ácidos nucléicos são moléculas gigantes (macromoléculas), formadas por unidades monoméricas menores
Figura 1: peridrociclopentanofenantreno
 COLESTEROL A n a L a u r a B u e n o Esteróides são álcoois de alto peso molecular. São compostos lipossolúveis muito importantes na fisiologia humana. Os esteróis possuem uma estrutura básica chamada
COLESTEROL A n a L a u r a B u e n o Esteróides são álcoois de alto peso molecular. São compostos lipossolúveis muito importantes na fisiologia humana. Os esteróis possuem uma estrutura básica chamada
EXERCÍCIO E DIABETES
 EXERCÍCIO E DIABETES Todos os dias ouvimos falar dos benefícios que os exercícios físicos proporcionam, de um modo geral, à nossa saúde. Pois bem, aproveitando a oportunidade, hoje falaremos sobre a Diabetes,
EXERCÍCIO E DIABETES Todos os dias ouvimos falar dos benefícios que os exercícios físicos proporcionam, de um modo geral, à nossa saúde. Pois bem, aproveitando a oportunidade, hoje falaremos sobre a Diabetes,
METABOLISMO DE LIPÍDEOS
 METABOLISMO DE LIPÍDEOS 1. Β-oxidação de ácidos graxos - Síntese de acetil-coa - ciclo de Krebs - Cadeia transportadora de elétrons e fosforilação oxidativa 2. Síntese de corpos cetônicos 3. Síntese de
METABOLISMO DE LIPÍDEOS 1. Β-oxidação de ácidos graxos - Síntese de acetil-coa - ciclo de Krebs - Cadeia transportadora de elétrons e fosforilação oxidativa 2. Síntese de corpos cetônicos 3. Síntese de
Estrutura tridimensional de proteínas. Prof. Dr. Fernando Berton Zanchi
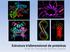 Estrutura tridimensional de proteínas Prof. Dr. Fernando Berton Zanchi Níveis de Estruturas Protéicas A conformação espacial das proteínas As proteínas não são traços rígidos porque suas ligações químicas
Estrutura tridimensional de proteínas Prof. Dr. Fernando Berton Zanchi Níveis de Estruturas Protéicas A conformação espacial das proteínas As proteínas não são traços rígidos porque suas ligações químicas
O processo da Expressão Gênica
 Coordenadoria de Educação e Difusão de Ciências Rua 9 de Julho, 1205 - São Carlos - São Paulo e-mail: cbme@if.sc.usp.br- Telefone: (16) 3373-9159 http://cbme.ifsc.usp.br http://cbme.usp.br O processo da
Coordenadoria de Educação e Difusão de Ciências Rua 9 de Julho, 1205 - São Carlos - São Paulo e-mail: cbme@if.sc.usp.br- Telefone: (16) 3373-9159 http://cbme.ifsc.usp.br http://cbme.usp.br O processo da
ÁCIDOS NUCLEÍCOS RIBOSSOMO E SÍNTESE PROTEÍCA
 ÁCIDOS NUCLEÍCOS RIBOSSOMO E SÍNTESE PROTEÍCA ÁCIDOS NUCLÉICOS: Moléculas orgânicas complexas, formadas polimerização de nucleotídeos (DNA e RNA) pela Contêm a informação que determina a seqüência de aminoácidos
ÁCIDOS NUCLEÍCOS RIBOSSOMO E SÍNTESE PROTEÍCA ÁCIDOS NUCLÉICOS: Moléculas orgânicas complexas, formadas polimerização de nucleotídeos (DNA e RNA) pela Contêm a informação que determina a seqüência de aminoácidos
As forças atrativas entre duas moléculas são significativas até uma distância de separação d, que chamamos de alcance molecular.
 Tensão Superficial Nos líquidos, as forças intermoleculares atrativas são responsáveis pelos fenômenos de capilaridade. Por exemplo, a subida de água em tubos capilares e a completa umidificação de uma
Tensão Superficial Nos líquidos, as forças intermoleculares atrativas são responsáveis pelos fenômenos de capilaridade. Por exemplo, a subida de água em tubos capilares e a completa umidificação de uma
QUÍMICA CELULAR NUTRIÇÃO TIPOS DE NUTRIENTES NUTRIENTES ENERGÉTICOS 4/3/2011 FUNDAMENTOS QUÍMICOS DA VIDA
 NUTRIÇÃO QUÍMICA CELULAR PROFESSOR CLERSON CLERSONC@HOTMAIL.COM CIESC MADRE CLÉLIA CONCEITO CONJUNTO DE PROCESSOS INGESTÃO, DIGESTÃO E ABSORÇÃO SUBSTÂNCIAS ÚTEIS AO ORGANISMO ESPÉCIE HUMANA: DIGESTÃO ONÍVORA
NUTRIÇÃO QUÍMICA CELULAR PROFESSOR CLERSON CLERSONC@HOTMAIL.COM CIESC MADRE CLÉLIA CONCEITO CONJUNTO DE PROCESSOS INGESTÃO, DIGESTÃO E ABSORÇÃO SUBSTÂNCIAS ÚTEIS AO ORGANISMO ESPÉCIE HUMANA: DIGESTÃO ONÍVORA
UFABC Bacharelado em Ciência & Tecnologia
 UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Energia de interação entre macromoléculas Interações em meio
UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Energia de interação entre macromoléculas Interações em meio
Proteínas. Enzima que Colagénio Insulina degrada a insulina (hormona)
 Proteínas O seu nome deriva da palavra Grega proteios, que significa de principal importância. As proteínas desempenham um papel fundamental nos sistemas biológicos, estando associadas a todas as formas
Proteínas O seu nome deriva da palavra Grega proteios, que significa de principal importância. As proteínas desempenham um papel fundamental nos sistemas biológicos, estando associadas a todas as formas
7.012 Conjunto de Problemas 5
 Nome Seção 7.012 Conjunto de Problemas 5 Pergunta 1 Enquanto estudava um problema de infertilidade, você tentou isolar um gene hipotético de coelho que seria responsável pela prolífica reprodução desses
Nome Seção 7.012 Conjunto de Problemas 5 Pergunta 1 Enquanto estudava um problema de infertilidade, você tentou isolar um gene hipotético de coelho que seria responsável pela prolífica reprodução desses
REVISÃO QUÍMICA. Profº JURANDIR QUÍMICA
 REVISÃO QUÍMICA Profº JURANDIR QUÍMICA DADOS 01. (ENEM 2004) Em setembro de 1998, cerca de 10.000 toneladas de ácido sulfúrico (H 2 SO 4 ) foram derramadas pelo navio Bahamas no litoral do Rio Grande
REVISÃO QUÍMICA Profº JURANDIR QUÍMICA DADOS 01. (ENEM 2004) Em setembro de 1998, cerca de 10.000 toneladas de ácido sulfúrico (H 2 SO 4 ) foram derramadas pelo navio Bahamas no litoral do Rio Grande
BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2010_2011_1º Teste 25/10/2010
 BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2010_2011_1º Teste 25/10/2010 (Duração: 1,5 h) Nome do Aluno: Nº: Curso: Cada uma das questões de escolha múltipla (1 à 40) tem a cotação de 0,5 valores. Será descontado
BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2010_2011_1º Teste 25/10/2010 (Duração: 1,5 h) Nome do Aluno: Nº: Curso: Cada uma das questões de escolha múltipla (1 à 40) tem a cotação de 0,5 valores. Será descontado
O fluxo da informação é unidirecional
 Curso - Psicologia Disciplina: Genética Humana e Evolução Resumo Aula 3- Transcrição e Tradução Dogma central TRANSCRIÇÃO DO DNA O fluxo da informação é unidirecional Processo pelo qual uma molécula de
Curso - Psicologia Disciplina: Genética Humana e Evolução Resumo Aula 3- Transcrição e Tradução Dogma central TRANSCRIÇÃO DO DNA O fluxo da informação é unidirecional Processo pelo qual uma molécula de
ENZIMAS. Células podem sintetizar enzimas conforme a sua necessidade.
 ENZIMAS As enzimas são proteínas, catalisadores (aumenta a velocidade de uma determinada reação química) biológicos (proteínas) de alta especificidade. Praticamente todas as reações que caracterizam o
ENZIMAS As enzimas são proteínas, catalisadores (aumenta a velocidade de uma determinada reação química) biológicos (proteínas) de alta especificidade. Praticamente todas as reações que caracterizam o
Projeto Genoma e Proteoma
 Projeto Genoma e Proteoma Grupo 3: *Artur S. Nascimento *Bárbara S. Costa *Beatrice Barbosa *Tamyres S. E. Guimarães *Yara Cavalcante O que é genoma? O genoma é o conjunto de todo o material genético que
Projeto Genoma e Proteoma Grupo 3: *Artur S. Nascimento *Bárbara S. Costa *Beatrice Barbosa *Tamyres S. E. Guimarães *Yara Cavalcante O que é genoma? O genoma é o conjunto de todo o material genético que
Dra. Kátia R. P. de Araújo Sgrillo. sgrillo.ita@ftc.br
 Dra. Kátia R. P. de Araújo Sgrillo sgrillo.ita@ftc.br O metabolismo de carboidratos em humanos pode ser dividido nas seguintes categorias: 1. Glicólise 2. Ciclo de Krebs 3. Glicogênese 4. Glicogenólise
Dra. Kátia R. P. de Araújo Sgrillo sgrillo.ita@ftc.br O metabolismo de carboidratos em humanos pode ser dividido nas seguintes categorias: 1. Glicólise 2. Ciclo de Krebs 3. Glicogênese 4. Glicogenólise
DURAÇÃO DA PROVA: 03 HORAS
 INSTRUÇÕES: PRCESS SELETIV 2013/2 - CPS PRVA DISCURSIVA DE QUÍMICA CURS DE GRADUAÇÃ EM MEDICINA 1. Só abra a prova quando autorizado. 2. Veja se este caderno contém 5 (cinco) questões discursivas. Caso
INSTRUÇÕES: PRCESS SELETIV 2013/2 - CPS PRVA DISCURSIVA DE QUÍMICA CURS DE GRADUAÇÃ EM MEDICINA 1. Só abra a prova quando autorizado. 2. Veja se este caderno contém 5 (cinco) questões discursivas. Caso
PROVA DE QUÍMICA - 1998 Segunda Etapa
 PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
Mary Santiago Silva 05/05/2010
 Espectrometria de Massas Interpretação do Espectro de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Fragmentação em espectro de massas por EI oferece importante informação
Espectrometria de Massas Interpretação do Espectro de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Fragmentação em espectro de massas por EI oferece importante informação
Bioquímica. Purificação de proteínas
 Bioquímica Purificação de proteínas Estratégia geral - Liberação da proteína do material biológico - Podem ser separados por fracionamento celular - Pode-se separar proteínas por características: Solubilidade
Bioquímica Purificação de proteínas Estratégia geral - Liberação da proteína do material biológico - Podem ser separados por fracionamento celular - Pode-se separar proteínas por características: Solubilidade
Resposta: Interbits SuperPro Web
 1. (Fuvest 2012) Uma mutação, responsável por uma doença sanguínea, foi identificada numa família. Abaixo estão representadas sequências de bases nitrogenadas, normal e mutante; nelas estão destacados
1. (Fuvest 2012) Uma mutação, responsável por uma doença sanguínea, foi identificada numa família. Abaixo estão representadas sequências de bases nitrogenadas, normal e mutante; nelas estão destacados
DIFERENTES DIETAS ALIMENTARES E SUAS RELAÇÕES COM O DESENVOLVIMENTO.
 V EPCC Encontro Internacional de Produção Científica Cesumar 23 a 26 de outubro de 2007 DIFERENTES DIETAS ALIMENTARES E SUAS RELAÇÕES COM O DESENVOLVIMENTO. Izamara Maria Fachim Rauber 1 IZAMARA_MARIA_FACHIM_RAUBER.doc,
V EPCC Encontro Internacional de Produção Científica Cesumar 23 a 26 de outubro de 2007 DIFERENTES DIETAS ALIMENTARES E SUAS RELAÇÕES COM O DESENVOLVIMENTO. Izamara Maria Fachim Rauber 1 IZAMARA_MARIA_FACHIM_RAUBER.doc,
TURMA DE REVISÃO - EMESCAM 1º SEMESTRE 2012 - QUÍMICA
 TURMA DE REVISÃO - EMESCAM 1º SEMESTRE 2012 - QUÍMICA Prof. Borges EXERCÍCIOS DE AMINOÁCIDOS 1. (Fuvest) A hidrólise de um peptídeo rompe a ligação peptídica, originando aminoácidos. Quantos aminoácidos
TURMA DE REVISÃO - EMESCAM 1º SEMESTRE 2012 - QUÍMICA Prof. Borges EXERCÍCIOS DE AMINOÁCIDOS 1. (Fuvest) A hidrólise de um peptídeo rompe a ligação peptídica, originando aminoácidos. Quantos aminoácidos
Dra. Maria Izabel Gallão. Matriz Extracelular
 Matriz Extracelular - a matriz extracelular (MEC) corresponde aos complexos macromoleculares relativamente estáveis, formados por moléculas de diferentes naturezas que são produzidas, exportadas e complexadas
Matriz Extracelular - a matriz extracelular (MEC) corresponde aos complexos macromoleculares relativamente estáveis, formados por moléculas de diferentes naturezas que são produzidas, exportadas e complexadas
Questões complementares
 Questões complementares 1. Definir célula e os tipos celulares existentes. Caracterizar as diferenças existentes entre os tipos celulares. 2. Existe diferença na quantidade de organelas membranares entre
Questões complementares 1. Definir célula e os tipos celulares existentes. Caracterizar as diferenças existentes entre os tipos celulares. 2. Existe diferença na quantidade de organelas membranares entre
UNIDADE 4 - ESTRUTURA CRISTALINA
 UNIDADE 4 - ESTRUTURA CRISTALINA 4.1. INTRODUÇÃO Em geral, todos os metais, grande parte dos cerâmicos e certos polímeros cristalizam-se quando se solidificam. Os átomos se arranjam em uma estrutura tridimensional
UNIDADE 4 - ESTRUTURA CRISTALINA 4.1. INTRODUÇÃO Em geral, todos os metais, grande parte dos cerâmicos e certos polímeros cristalizam-se quando se solidificam. Os átomos se arranjam em uma estrutura tridimensional
Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2
 11 Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2 4 ), para que a água esteja em conformidade com
11 Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2 4 ), para que a água esteja em conformidade com
2 - Biodisponibilidade. Biodisponibilidade Velocidade e extensão de absorção de um fármaco a partir de uma forma de administração
 2 - Biodisponibilidade TOXICOCINÉTICA Biodisponibilidade Velocidade e extensão de absorção de um fármaco a partir de uma forma de administração Fator de Biodisponibilidade (F) Fração da dose administrada
2 - Biodisponibilidade TOXICOCINÉTICA Biodisponibilidade Velocidade e extensão de absorção de um fármaco a partir de uma forma de administração Fator de Biodisponibilidade (F) Fração da dose administrada
Estrutura e função dos ácidos nucléicos. Profa. Melissa de Freitas Cordeiro-Silva
 Estrutura e função dos ácidos nucléicos Profa. Melissa de Freitas Cordeiro-Silva > Polímeros de nucleotídeos Funções: DNA (ácido desoxirribonucléico) : > Armazenar as informações necessárias para a construção
Estrutura e função dos ácidos nucléicos Profa. Melissa de Freitas Cordeiro-Silva > Polímeros de nucleotídeos Funções: DNA (ácido desoxirribonucléico) : > Armazenar as informações necessárias para a construção
Biomassa de Banana Verde Integral- BBVI
 Biomassa de Banana Verde Integral- BBVI INFORMAÇÕES NUTRICIONAIS Porção de 100g (1/2 copo) Quantidade por porção g %VD(*) Valor Energético (kcal) 64 3,20 Carboidratos 14,20 4,73 Proteínas 1,30 1,73 Gorduras
Biomassa de Banana Verde Integral- BBVI INFORMAÇÕES NUTRICIONAIS Porção de 100g (1/2 copo) Quantidade por porção g %VD(*) Valor Energético (kcal) 64 3,20 Carboidratos 14,20 4,73 Proteínas 1,30 1,73 Gorduras
Capacidade de organizar os produtos da digestão usando a energia extraída dos mesmos produtos da digestão (REGULAÇÃO)
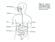 Capacidade de organizar os produtos da digestão usando a energia extraída dos mesmos produtos da digestão (REGULAÇÃO) As proteínas são digeridas até aminoácidos, as gorduras (triglicérides) até glicerol
Capacidade de organizar os produtos da digestão usando a energia extraída dos mesmos produtos da digestão (REGULAÇÃO) As proteínas são digeridas até aminoácidos, as gorduras (triglicérides) até glicerol
POLÍMEROS POLIETILENO DE BAIXA DENSIDADE
 POLÍMEROS Os polímeros são macromoléculas formada pela união de pequenas unidades que se repetem, os monômeros. Existem basicamente dois tipos de polimerização: adição e condensação. Na polimeirzação por
POLÍMEROS Os polímeros são macromoléculas formada pela união de pequenas unidades que se repetem, os monômeros. Existem basicamente dois tipos de polimerização: adição e condensação. Na polimeirzação por
COMPOSIÇÃO QUÍMICA DA CARNE. Profª Sandra Carvalho
 COMPOSIÇÃO QUÍMICA DA CARNE Profª Sandra Carvalho A carne magra: 75% de água 21 a 22% de proteína 1 a 2% de gordura 1% de minerais menos de 1% de carboidratos A carne magra dos diferentes animais de abate
COMPOSIÇÃO QUÍMICA DA CARNE Profª Sandra Carvalho A carne magra: 75% de água 21 a 22% de proteína 1 a 2% de gordura 1% de minerais menos de 1% de carboidratos A carne magra dos diferentes animais de abate
BIOQUÍMICA DA ÁGUA. Disciplina: Bioquímica, Prof. Dr. Vagne Oliveira E-mail: vagne_melo_oliveira@outlook.com
 BIOQUÍMICA DA ÁGUA Disciplina: Bioquímica, Prof. Dr. Vagne Oliveira E-mail: vagne_melo_oliveira@outlook.com ÁGUA Substância mais abundante nos seres vivos; É uma substância líquida, incolor, inodora e
BIOQUÍMICA DA ÁGUA Disciplina: Bioquímica, Prof. Dr. Vagne Oliveira E-mail: vagne_melo_oliveira@outlook.com ÁGUA Substância mais abundante nos seres vivos; É uma substância líquida, incolor, inodora e
METABOLISMO. Nesta 3 a parte da disciplina nosso principal objetivo é compreender os mecanismos pelos quais as células regulam o seu metabolismo
 METABOLISMO Nesta 3 a parte da disciplina nosso principal objetivo é compreender os mecanismos pelos quais as células regulam o seu metabolismo Mas o que é metabolismo? Metabolismo é o nome que damos ao
METABOLISMO Nesta 3 a parte da disciplina nosso principal objetivo é compreender os mecanismos pelos quais as células regulam o seu metabolismo Mas o que é metabolismo? Metabolismo é o nome que damos ao
A) Escreva a equação que representa a semi-reação de redução e seu respectivo potencial padrão.
 QUÍMICA QUESTÃ 01 Aparelhos eletrônicos sem fio, tais como máquinas fotográficas digitais e telefones celulares, utilizam, como fonte de energia, baterias recarregáveis. Um tipo comum de bateria recarregável
QUÍMICA QUESTÃ 01 Aparelhos eletrônicos sem fio, tais como máquinas fotográficas digitais e telefones celulares, utilizam, como fonte de energia, baterias recarregáveis. Um tipo comum de bateria recarregável
MEDICINA VETERINÁRIA. Disciplina: Genética Animal. Prof a.: D rd. Mariana de F. Gardingo Diniz
 MEDICINA VETERINÁRIA Disciplina: Genética Animal Prof a.: D rd. Mariana de F. Gardingo Diniz TRANSCRIÇÃO DNA A transcrição é o processo de formação de uma molécula de RNA a partir de uma molécula molde
MEDICINA VETERINÁRIA Disciplina: Genética Animal Prof a.: D rd. Mariana de F. Gardingo Diniz TRANSCRIÇÃO DNA A transcrição é o processo de formação de uma molécula de RNA a partir de uma molécula molde
Metais em água. metais tem um papel crucial em. como espécies hidroxiladas, ex.: FeOH(H 2 O)
 Metais em água Para a estabilização dos elétrons mais externos os cátions metálicos em água são ligados (coordenados) a outras espécies. Assim, os metais em soluções aquosas procuram a máxima estabilidade
Metais em água Para a estabilização dos elétrons mais externos os cátions metálicos em água são ligados (coordenados) a outras espécies. Assim, os metais em soluções aquosas procuram a máxima estabilidade
Curso: Integração Metabólica
 Curso: Integração Metabólica Aula 9: Sistema Nervoso Autônomo Prof. Carlos Castilho de Barros Sistema Nervoso Sistema Nervoso Central Sistema Nervoso Periférico Sensorial Motor Somático Autônomo Glândulas,
Curso: Integração Metabólica Aula 9: Sistema Nervoso Autônomo Prof. Carlos Castilho de Barros Sistema Nervoso Sistema Nervoso Central Sistema Nervoso Periférico Sensorial Motor Somático Autônomo Glândulas,
MEDICINA VETERINÁRIA. Disciplina: Genética Animal. Prof a.: Drd. Mariana de F. G. Diniz
 MEDICINA VETERINÁRIA Disciplina: Genética Animal Prof a.: Drd. Mariana de F. G. Diniz Gene, é a unidade fundamental da hereditariedade. Cada gene é formado por uma sequência específica de ácidos nucléicos
MEDICINA VETERINÁRIA Disciplina: Genética Animal Prof a.: Drd. Mariana de F. G. Diniz Gene, é a unidade fundamental da hereditariedade. Cada gene é formado por uma sequência específica de ácidos nucléicos
CAPÍTULO 6 TECIDO MUSCULAR
 CAPÍTULO 6 TECIDO MUSCULAR 1 Características Histológicas O tecido muscular é constituído por células alongadas que possuem grande quantidade de filamentos citoplasmáticos com proteínas contráteis. Esse
CAPÍTULO 6 TECIDO MUSCULAR 1 Características Histológicas O tecido muscular é constituído por células alongadas que possuem grande quantidade de filamentos citoplasmáticos com proteínas contráteis. Esse
Bases Moleculares da Hereditariedade
 UNIVERSIDADE FEDERAL DO PIAUÍ CENTRO DE CIÊNCIAS AGRÁRIAS PROG. DE PÓS GRAD. EM GENET. E MELHORAMENTO NÚCLEO DE ESTUDOS EM GENET. E MELHORAMENTO Bases Moleculares da Hereditariedade Ministrante: João Paulo
UNIVERSIDADE FEDERAL DO PIAUÍ CENTRO DE CIÊNCIAS AGRÁRIAS PROG. DE PÓS GRAD. EM GENET. E MELHORAMENTO NÚCLEO DE ESTUDOS EM GENET. E MELHORAMENTO Bases Moleculares da Hereditariedade Ministrante: João Paulo
O QUE SÃO SUBSTÂNCIAS INORGÂNICAS? QUAL A FUNÇÃO BIOLÓGICA DE CADA UMA?
 O QUE SÃO SUBSTÂNCIAS ORGÂNICAS? O QUE SÃO SUBSTÂNCIAS INORGÂNICAS? QUAL A FUNÇÃO BIOLÓGICA DE CADA UMA? SUBSTÂNCIAS ORGÂNICAS: CARBONO, HIDROGÊNIO, OXIGÊNIO E NITROGÊNIO FORMAM CADEIAS LONGAS E COMPLEXAS
O QUE SÃO SUBSTÂNCIAS ORGÂNICAS? O QUE SÃO SUBSTÂNCIAS INORGÂNICAS? QUAL A FUNÇÃO BIOLÓGICA DE CADA UMA? SUBSTÂNCIAS ORGÂNICAS: CARBONO, HIDROGÊNIO, OXIGÊNIO E NITROGÊNIO FORMAM CADEIAS LONGAS E COMPLEXAS
47 Por que preciso de insulina?
 A U A UL LA Por que preciso de insulina? A Medicina e a Biologia conseguiram decifrar muitos dos processos químicos dos seres vivos. As descobertas que se referem ao corpo humano chamam mais a atenção
A U A UL LA Por que preciso de insulina? A Medicina e a Biologia conseguiram decifrar muitos dos processos químicos dos seres vivos. As descobertas que se referem ao corpo humano chamam mais a atenção
Projeto Embuá Unidade de Aprendizagem: ENERGIA
 Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
Mitocôndrias e Cloroplastos
 Universidade Federal de Sergipe Centro de Ciências Biológicas e da Saúde Departamento de Morfologia Biologia Celular Mitocôndrias e Cloroplastos Características gerais de mitocôndrias e cloroplastos Mitocôndrias
Universidade Federal de Sergipe Centro de Ciências Biológicas e da Saúde Departamento de Morfologia Biologia Celular Mitocôndrias e Cloroplastos Características gerais de mitocôndrias e cloroplastos Mitocôndrias
Bioenergética. Profa. Kalyne de Menezes Bezerra Cavalcanti
 Bioenergética Profa. Kalyne de Menezes Bezerra Cavalcanti Natal/RN Fevereiro de 2011 Substratos para o exercício O corpo utiliza nutrientes carboidratos, gorduras e proteínas consumidos diariamente para
Bioenergética Profa. Kalyne de Menezes Bezerra Cavalcanti Natal/RN Fevereiro de 2011 Substratos para o exercício O corpo utiliza nutrientes carboidratos, gorduras e proteínas consumidos diariamente para
BASES MACROMOLECULARES DA CONSTITUIÇÃO CELULAR
 BASES MACROMOLECULARES DA CONSTITUIÇÃO CELULAR As moléculas que constituem as células são formadas pelos mesmos átomos encontrados nos seres inanimados. Todavia, na origem e evolução das células, alguns
BASES MACROMOLECULARES DA CONSTITUIÇÃO CELULAR As moléculas que constituem as células são formadas pelos mesmos átomos encontrados nos seres inanimados. Todavia, na origem e evolução das células, alguns
23/03/2015. Moléculas orgânicas - Carboidratos
 Moléculas orgânicas - Carboidratos São formados por C, H, O. São Conhecidos como: Hidratos de Carbono Glucídios Glicídios Açúcares Sacarídeos Funções: Energética (glicose); Glicogênio : reserva energética
Moléculas orgânicas - Carboidratos São formados por C, H, O. São Conhecidos como: Hidratos de Carbono Glucídios Glicídios Açúcares Sacarídeos Funções: Energética (glicose); Glicogênio : reserva energética
Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS
 Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS REGRA DO OCTETO Cada átomo tem um número de elétrons diferente e estes e - (elétrons) estão distribuídos
Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS REGRA DO OCTETO Cada átomo tem um número de elétrons diferente e estes e - (elétrons) estão distribuídos
PROF.: FERNANDA BRITO Disciplina Farmacologia. fernandabrito@vm.uff.br
 PROF.: FERNANDA BRITO Disciplina Farmacologia fernandabrito@vm.uff.br EXEMPLOS DE ESQUEMAS COMPARTIMENTAIS DO CORPO TGI COMPARTIMENTO CENTRAL CÉREBRO FÍGADO ELIMINAÇÃO METABÓLICA EXCREÇÃO RENAL OUTROS
PROF.: FERNANDA BRITO Disciplina Farmacologia fernandabrito@vm.uff.br EXEMPLOS DE ESQUEMAS COMPARTIMENTAIS DO CORPO TGI COMPARTIMENTO CENTRAL CÉREBRO FÍGADO ELIMINAÇÃO METABÓLICA EXCREÇÃO RENAL OUTROS
Forças intermoleculares, Disciplina de Química Geral Profa. Marcia Margarete Meier
 , líquidos e sólidos 1 Uma comparação entre líquidos e sólidos As propriedades físicas das substâncias entendidas em termos de teoria cinética molecular : Os gases são altamente compressíveis, assumem
, líquidos e sólidos 1 Uma comparação entre líquidos e sólidos As propriedades físicas das substâncias entendidas em termos de teoria cinética molecular : Os gases são altamente compressíveis, assumem
IESA-ESTUDO DIRIGIDO 1º SEMESTRE 8º ANO - MANHÃ E TARDE- DISCIPLINA: CIÊNCIAS PROFESSORAS: CELIDE E IGNÊS. Aluno(a): Turma:
 IESA-ESTUDO DIRIGIDO 1º SEMESTRE 8º ANO - MANHÃ E TARDE- DISCIPLINA: CIÊNCIAS PROFESSORAS: CELIDE E IGNÊS Aluno(a): Turma: Querido (a) aluno (a), Este estudo dirigido foi realizado para que você revise
IESA-ESTUDO DIRIGIDO 1º SEMESTRE 8º ANO - MANHÃ E TARDE- DISCIPLINA: CIÊNCIAS PROFESSORAS: CELIDE E IGNÊS Aluno(a): Turma: Querido (a) aluno (a), Este estudo dirigido foi realizado para que você revise
Células A (25%) Glucagon Células B (60%) Insulina Células D (10%) Somatostatina Células F ou PP (5%) Polipeptídeo Pancreático 1-2 milhões de ilhotas
 Instituto Biomédico Departamento de Fisiologia e Farmacologia Disciplina: Fisiologia II Curso: Medicina Veterinária Pâncreas Endócrino Prof. Guilherme Soares Ilhotas Células A (25%) Glucagon Células B
Instituto Biomédico Departamento de Fisiologia e Farmacologia Disciplina: Fisiologia II Curso: Medicina Veterinária Pâncreas Endócrino Prof. Guilherme Soares Ilhotas Células A (25%) Glucagon Células B
Organização do Material Genético nos Procariontes e Eucariontes
 Organização do Material Genético nos Procariontes e Eucariontes Organização do Material Genético nos Procariontes e Eucariontes Procariontes Eucariontes Localização Organização Forma Disperso no citoplasma
Organização do Material Genético nos Procariontes e Eucariontes Organização do Material Genético nos Procariontes e Eucariontes Procariontes Eucariontes Localização Organização Forma Disperso no citoplasma
O corpo humano está organizado desde o mais simples até o mais complexo, ou seja, do átomo microscópico ao complexo organismo humano macroscópico.
 1 O corpo humano está organizado desde o mais simples até o mais complexo, ou seja, do átomo microscópico ao complexo organismo humano macroscópico. Note essa organização na figura abaixo. - Átomos formam
1 O corpo humano está organizado desde o mais simples até o mais complexo, ou seja, do átomo microscópico ao complexo organismo humano macroscópico. Note essa organização na figura abaixo. - Átomos formam
A patroa quer emagrecer
 A patroa quer emagrecer A UU L AL A Andando pela rua, você passa em frente a uma farmácia e resolve entrar para conferir seu peso na balança. E aí vem aquela surpresa: uns quilinhos a mais, ou, em outros
A patroa quer emagrecer A UU L AL A Andando pela rua, você passa em frente a uma farmácia e resolve entrar para conferir seu peso na balança. E aí vem aquela surpresa: uns quilinhos a mais, ou, em outros
9/30/2014. Por que engenheiros biomédicos precisam estudar anatomia e fisiologia? Introdução. Fisiologia. Anatomia
 Por que engenheiros biomédicos precisam estudar anatomia e fisiologia? Introdução à Anatomia e Fisiologia EN2319-Bases Biológicas para Engenharia I Reginaldo K Fukuchi Universidade Federal do ABC Por que
Por que engenheiros biomédicos precisam estudar anatomia e fisiologia? Introdução à Anatomia e Fisiologia EN2319-Bases Biológicas para Engenharia I Reginaldo K Fukuchi Universidade Federal do ABC Por que
Volumetria ácido-base (continuação) Prof a Alessandra Smaniotto QMC 5325 - Química Analítica - Farmácia Turmas 02102A e 02102B
 Volumetria ácido-base (continuação) Prof a Alessandra Smaniotto QMC 5325 - Química Analítica - Farmácia Turmas 02102A e 02102B Curvas de titulação ² A curva de titulação é a representação gráfica de como
Volumetria ácido-base (continuação) Prof a Alessandra Smaniotto QMC 5325 - Química Analítica - Farmácia Turmas 02102A e 02102B Curvas de titulação ² A curva de titulação é a representação gráfica de como
AS LEIS DE NEWTON PROFESSOR ANDERSON VIEIRA
 CAPÍTULO 1 AS LEIS DE NEWTON PROFESSOR ANDERSON VIEIRA Talvez o conceito físico mais intuitivo que carregamos conosco, seja a noção do que é uma força. Muito embora, formalmente, seja algo bastante complicado
CAPÍTULO 1 AS LEIS DE NEWTON PROFESSOR ANDERSON VIEIRA Talvez o conceito físico mais intuitivo que carregamos conosco, seja a noção do que é uma força. Muito embora, formalmente, seja algo bastante complicado
Questão 61. Questão 63. Questão 62. alternativa B. alternativa B. alternativa D
 Questão 61 A limpeza de pisos de mármore normalmente é feita com solução de ácido clorídrico comercial (ácido muriático). Essa solução ácida ataca o mármore, desprendendo gás carbônico, segundo a reação
Questão 61 A limpeza de pisos de mármore normalmente é feita com solução de ácido clorídrico comercial (ácido muriático). Essa solução ácida ataca o mármore, desprendendo gás carbônico, segundo a reação
Membranas Biológicas e Transporte
 Universidade Federal do Ceará Centro de Ciências Departamento de Bioquímica e Biologia Molecular Disciplina de Introdução a Bioquímica Membranas Biológicas e Transporte 1. Introdução 2. Os Constituintes
Universidade Federal do Ceará Centro de Ciências Departamento de Bioquímica e Biologia Molecular Disciplina de Introdução a Bioquímica Membranas Biológicas e Transporte 1. Introdução 2. Os Constituintes
AVALIAÇÃO DA QUALIDADE E VALOR NUTRICIONAL DE ÓLEOS E GORDURAS
 Data: Agosto/2003 AVALIAÇÃO DA QUALIDADE E VALOR NUTRICIONAL DE ÓLEOS E GORDURAS Óleos e gorduras são constituintes naturais dos ingredientes grãos usados nas formulações de rações para animais. Podem
Data: Agosto/2003 AVALIAÇÃO DA QUALIDADE E VALOR NUTRICIONAL DE ÓLEOS E GORDURAS Óleos e gorduras são constituintes naturais dos ingredientes grãos usados nas formulações de rações para animais. Podem
Informação Técnica 10.08.01 E 09.2003 Offset Serviços. Molhagem em impressão offset Fatos importantes para o uso nos aditivos de molhagem offset 1/5
 Informação Técnica 10.08.01 E 09.2003 Offset Serviços Molhagem em impressão offset Fatos importantes para o uso nos aditivos de molhagem offset 1/5 O processo de impressão offset Offset continua a ser
Informação Técnica 10.08.01 E 09.2003 Offset Serviços Molhagem em impressão offset Fatos importantes para o uso nos aditivos de molhagem offset 1/5 O processo de impressão offset Offset continua a ser
Apostila de Química Geral
 Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
Núcleo Celular. Biomedicina primeiro semestre de 2012 Profa. Luciana Fontanari Krause
 Núcleo Celular Biomedicina primeiro semestre de 2012 Profa. Luciana Fontanari Krause Núcleo Celular Eucarioto: núcleo delimitado por membrana nuclear (carioteca) Portador dos fatores hereditários e controlador
Núcleo Celular Biomedicina primeiro semestre de 2012 Profa. Luciana Fontanari Krause Núcleo Celular Eucarioto: núcleo delimitado por membrana nuclear (carioteca) Portador dos fatores hereditários e controlador
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo
 Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
FISIOLOGIA RENAL EXERCÍCIOS DE APRENDIZAGEM
 EXERCÍCIOS DE APRENDIZAGEM FISIOLOGIA RENAL 01. A sudorese (produção de suor) é um processo fisiológico que ajuda a baixar a temperatura do corpo quando está muito calor ou quando realizamos uma atividade
EXERCÍCIOS DE APRENDIZAGEM FISIOLOGIA RENAL 01. A sudorese (produção de suor) é um processo fisiológico que ajuda a baixar a temperatura do corpo quando está muito calor ou quando realizamos uma atividade
INTRODUÇÃO À FISIOLOGIA. Profª. Juliana Delatim Simonato Rocha Lab. de Ecofisiologia Animal LEFA - CIF/CCB
 INTRODUÇÃO À FISIOLOGIA Profª. Juliana Delatim Simonato Rocha Lab. de Ecofisiologia Animal LEFA - CIF/CCB 1 Fisiologia é... Literalmente... Conhecimento da natureza O estudo do funcionamento dos organismos
INTRODUÇÃO À FISIOLOGIA Profª. Juliana Delatim Simonato Rocha Lab. de Ecofisiologia Animal LEFA - CIF/CCB 1 Fisiologia é... Literalmente... Conhecimento da natureza O estudo do funcionamento dos organismos
PlanetaBio Resolução de Vestibulares UFRJ 2007 www.planetabio.com
 1-O gráfico a seguir mostra como variou o percentual de cepas produtoras de penicilinase da bactéria Neisseria gonorrhoeae obtidas de indivíduos com gonorréia no período de 1980 a 1990. A penicilinase
1-O gráfico a seguir mostra como variou o percentual de cepas produtoras de penicilinase da bactéria Neisseria gonorrhoeae obtidas de indivíduos com gonorréia no período de 1980 a 1990. A penicilinase
COLÉGIO MÓDULO DISCIPLINA BIOLOGIA UFBA I UNIDADE PROFESSOR SÉRGIO MAGALHÃES
 COLÉGIO MÓDULO DISCIPLINA BIOLOGIA UFBA I UNIDADE PROFESSOR SÉRGIO MAGALHÃES 01 V(01) Isótopos radioativos são importantes para elucidação de compostos químicos que são imprescindíveis aos seres vivos.
COLÉGIO MÓDULO DISCIPLINA BIOLOGIA UFBA I UNIDADE PROFESSOR SÉRGIO MAGALHÃES 01 V(01) Isótopos radioativos são importantes para elucidação de compostos químicos que são imprescindíveis aos seres vivos.
 Sistema Endócrino Sistema Endócrino Sistema Endócrino Sistema Endócrino Sistema Endócrino Sistema Endócrino Mensagem Química: Hormônios Os hormônios são substâncias químicas liberadas na corrente sanguínea
Sistema Endócrino Sistema Endócrino Sistema Endócrino Sistema Endócrino Sistema Endócrino Sistema Endócrino Mensagem Química: Hormônios Os hormônios são substâncias químicas liberadas na corrente sanguínea
Estrutura e Função de Ácidos Nucléicos
 UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA QBQ0313 Estrutura e Função de Ácidos Nucléicos Flavia Carla Meotti Os Ácidos Nucléicos Função: armazenamento e transmissão da informação
UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA QBQ0313 Estrutura e Função de Ácidos Nucléicos Flavia Carla Meotti Os Ácidos Nucléicos Função: armazenamento e transmissão da informação
