OLIMPÍADA BRASILEIRA DE QUÍMICA Fase VI (final)
|
|
|
- Heloísa Botelho Borja
- 5 Há anos
- Visualizações:
Transcrição
1 OLIMPÍADA BRASILEIRA DE QUÍMICA Fase VI (final) QUESTÃO 1 Boa parte das propriedades dos metais depende da forma como seus átomos encontram-se arranjados no espaço. A maioria dos metais comuns apresenta arranjos atômicos cúbicos. Os sistemas de arranjos cúbicos podem ser classificados em três diferentes tipos de repetição: cúbico simples, o qual não é observado nos metais devido o baixo empacotamento atômico; cúbico de corpo centrado, observado no crômio metálico, por exemplo, e cúbico de faces centradas, observado, por exemplo, no cobre metálico. Uma maneira de se calcular o espaço ocupado em cada célula unitária é através do fator de empacotamento (FE), que pode ser obtido dividindo o volume dos átomos da célula pelo volume da célula unitária. a) Sabendo disso, calcule o FE no cobre metálico, raio atômico 1,278 Å. Compare esse valor com o FE do crômio metálico, cujo lado da face da célula unitária apresenta um comprimento de 2,887 Å. As referidas estruturas cristalinas podem ser determinadas através de análise por raio X. Quando um feixe de raios X é dirigido através de um material cristalino, esses raios são difratados pelos planos dos átomos do cristal. O ângulo de difração depende do comprimento de onda dos raios X e das distâncias entre planos adjacentes. Estas distâncias entre planos adjacentes correspondem aos espaçamentos de repetição dos átomos em uma determinada direção. Os planos podem ser traçados tendo-se como base os eixos x, y, z. b) Tendo lembrado disso, determine o raio atômico do níquel, que possui estrutura cúbica de faces centradas, sabendo que para se determinar o espaçamento entre os planos 200 no níquel, usam-se raios X de comprimento de onda 0,58 Å e que o ângulo de reflexão é 9,5. QUESTÃO 2 1 de 6 01/11/12 11:14
2 Uma determinada substância sofre decomposição segundo uma cinética de primeira ordem, e sua dependência em relação à temperatura segue uma lei empiríca chamada de equação de Arrhenius. Os tempos de meia-vida determinados a 95ºC e 85ºC foram 15,4 minutos e 57,8 minutos, respectivamente. A partir destes dados: a) Calcule a energia de ativação e, supondo que esta permaneça constante, independente da temperatura, estime o tempo de meia-vida a 25 ºC. b) Estime também a energia de ativação por meio de um gráfico do logarítmo natural da constante de velocidade versus o inverso da temperatura (em Kelvin). Dados: Equação de Arrhenius: R = 8,314 J.K -1.mol -1 QUESTÃO 3 O lantânio presente em 5,00 g de monazita foi convenientemente extraído na forma de La 3+ e concentrado em 100 ml de solução. Após precipitação quantitativa do metal na forma de oxalato, La 2 (C 2 O 4 ) 3, o sal foi filtrado, lavado e redissolvido em quantidade adequada (~20 ml) de ácido sulfúrico 1,00 mol/l em erlenmeyer de 125 ml. Na titulação desta solução com solução de KMnO 4 0,0064 mol/l, foram gastos 36,1 ml. Determine: a) A concentração de La 3+ na solução inicial b) O teor de lantânio na monazita Dados: Massas atômicas (aproximadas), g/mol: La = 138,9 Mn = 54,9 K = 39,0 O = 16,0 C = 12,0 S = 32,0 2 de 6 01/11/12 11:14
3 QUESTÃO 4 O íon Fe(III) pode formar complexos com as geometrias tetraédrica e octaédrica. Entretanto, a maioria dos complexos de Fe(III) apresenta geometria octaédrica e são complexos de spin baixo. O íon Co(III) forma complexos apenas octaédricos e, 99% destes, são de spin baixo. Já o íon Co(II) pode formar complexos tetraédricos e octaédricos de spin alto. De acordo com as informações acima e baseado na Teoria do Campo Cristalino (TCC), explique essa diferença de comportamento entre esses íons. QUESTÃO 5 A oxepina pode ser preparada no laboratório, não por oxidação direta do benzeno, mas, através da seqüência de reações químicas apresentadas abaixo. Complete esta seqüência, indicando as estruturas, com especificação da estereoquímica, quando for o caso, dos intermediários A, B e C. 3 de 6 01/11/12 11:14
4 DBN = 1,5-diaza-biciclo[4.3.0]nona-5-eno QUESTÃO 6 Uma substância X que dá teste positivo com FeCl 3, mostra no seu espectro de massa o pico do íon molecular situado a 194 unidades de massa. Sua hidrólise catalisada por ácido fornece a substância Y que é solúvel em solução de NaHCO 3 a 10%. O espectro de RMN 1 H de X, obtido em CD 3 OD a 500 MHz, apresenta os seguintes sinais: d (ppm) MULTIPLICIDADE E J (HZ) INTEGRAÇÃO 3,75 S 3,12 6,30 D, J=15 1,20 6,75 D, J=8 1,03 6,94 DD, J=2 E 8 1,03 7,03 D, J=2 1,02 7,56 D, J=15 1,00 s = singlete; d = dublete; dd = dublete de dublete. O espectro de RMN 13 C normal (desacoplado) de X apresenta dez sinais, o DEPT 135 seis sinais e o DEPT 90 cinco sinais, conforme especificado: Carbono normal d (ppm) DEPT 135 DEPT 90 52,1 positivo não aparece 114,9 positivo positivo 115,3 positivo positivo 116,6 positivo positivo 123,1 positivo positivo 4 de 6 01/11/12 11:14
5 127,8 não aparece não aparece 146,9 positivo positivo 147,1 não aparece não aparece 149,7 não aparece não aparece 169,9 não aparece não aparece Com base nestas informações, responda: a) Qual é a fórmula molecular de X? b) Quais as estruturas das substâncias X e Y? c) Que outra substância, além de Y, é formada na hidrólise de X? d) Qual(is) do(s) sinal(is) do espectro de RMN 1 H de X não aparece no espectro de Y? Dados: Alguns valores de deslocamentos químicos de 1 H H aromático: H olefínico: H de ácido carboxílico: CH -O-: 3 RCH -O-: 2 R CH-O-: 2 R C=CH-CO: 2 RCH=C-CO: :; 6-9 ppm; 4,2-7,6 ppm; ppm; 3,3-3,8 ppm; 3,5-4,4 ppm: 3,8-5,2 ppm; 5,8-6,7 ppm; 6,5-7,8 ppm. Alguns valores de deslocamentos químicos de 13 C 5 de 6 01/11/12 11:14
6 C de carbonila: C aromático: C olefínico: ppm; ppm; ppm: 6 de 6 01/11/12 11:14
EXAME SELETIVO PARA 38 th INTERNATIONAL CHEMISTRY OLYMPIAD CORÉIA, JULHO DE 2006
 Seletiva para a 37th International Chemistry Olimpiad EXAME SELETIVO PARA 38 th INTERNATIONAL CHEMISTRY OLYMPIAD CORÉIA, JULHO DE 2006 PROGRAMA NACIONAL OLIMPÍADAS DE QUÍMICA Apoio: ABRIL 2006 Olimpíada
Seletiva para a 37th International Chemistry Olimpiad EXAME SELETIVO PARA 38 th INTERNATIONAL CHEMISTRY OLYMPIAD CORÉIA, JULHO DE 2006 PROGRAMA NACIONAL OLIMPÍADAS DE QUÍMICA Apoio: ABRIL 2006 Olimpíada
FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS
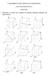 FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS 1 Determine os índices e/ou desenhe as direções cristalinas indicadas nas figuras abaixo. 2 Determineos índices dos planos cristalinos
FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS 1 Determine os índices e/ou desenhe as direções cristalinas indicadas nas figuras abaixo. 2 Determineos índices dos planos cristalinos
LISTA DE EXERCÍCIOS 6 1 (UNIDADE III INTRODUÇÃO À CIÊNCIA DOS MATERIAIS)
 UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO CENTRO DE ENGENHARIAS DEPARTAMENTO DE ENGENHARIA E TECNOLOGIA DISCIPLINA: QUÍMICA APLICADA À ENGENHARIA PROFESSOR: FREDERICO RIBEIRO DO CARMO Estrutura cristalina
UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO CENTRO DE ENGENHARIAS DEPARTAMENTO DE ENGENHARIA E TECNOLOGIA DISCIPLINA: QUÍMICA APLICADA À ENGENHARIA PROFESSOR: FREDERICO RIBEIRO DO CARMO Estrutura cristalina
EXAME DE SELEÇÃO PARA O PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA DA UNIVERSIDADE FEDERAL DO CEARÁ (PPGQ-UFC)/2015.2
 Universidade Federal do Ceará Centro de Ciências Programa de Pós-Graduação em Química Caixa Postal 12.200 Tel. (085)3366.9981 CEP 60.450-970 Fortaleza - Ceará - Brasil EXAME DE SELEÇÃO PARA O PROGRAMA
Universidade Federal do Ceará Centro de Ciências Programa de Pós-Graduação em Química Caixa Postal 12.200 Tel. (085)3366.9981 CEP 60.450-970 Fortaleza - Ceará - Brasil EXAME DE SELEÇÃO PARA O PROGRAMA
Número de Identificação: Data: / / Sobre o equilíbrio químico de solubilidade têm-se as seguintes situações:
 Questões de Química Analítica Questão 1 QA: Sobre o equilíbrio químico de solubilidade têm-se as seguintes situações: A) As concentrações de íons magnésio, cálcio e níquel(ii) e alumínio (III) em uma solução,
Questões de Química Analítica Questão 1 QA: Sobre o equilíbrio químico de solubilidade têm-se as seguintes situações: A) As concentrações de íons magnésio, cálcio e níquel(ii) e alumínio (III) em uma solução,
Programa de Pós-Graduação em Química
 1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Nível: DOUTORADO Duração da Prova: 4 horas São José do Rio Preto, 16 de Março de 2015. QUESTÕES DE QUÍMICA 2/12 Código de Matrícula:
1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Nível: DOUTORADO Duração da Prova: 4 horas São José do Rio Preto, 16 de Março de 2015. QUESTÕES DE QUÍMICA 2/12 Código de Matrícula:
UNIVERSIDADE FEDERAL DO CEARÁ CENTRO DE CIÊNCIAS OLIMPÍADA BRASILEIRA DE QUÍMICA 2004 FASE VI
 UNIVERSIDADE FEDERAL DO CEARÁ CENTRO DE CIÊNCIAS OLIMPÍADA BRASILEIRA DE QUÍMICA 2004 FASE VI Questão 1 Em uma análise química desejava-se determinar o teor percentual de zinco em 96,57g de uma amostra
UNIVERSIDADE FEDERAL DO CEARÁ CENTRO DE CIÊNCIAS OLIMPÍADA BRASILEIRA DE QUÍMICA 2004 FASE VI Questão 1 Em uma análise química desejava-se determinar o teor percentual de zinco em 96,57g de uma amostra
I - 4 Au (s) + O 2(g) + 2 H 2 O (l) + 8 CN - -
 QUESTÕES OBJETIVAS Questão 9: O processo do cianeto pode ser utilizado para extrair ouro de rochas. Esse processo consiste em, inicialmente, tratar as rochas trituradas com cianeto, havendo formação do
QUESTÕES OBJETIVAS Questão 9: O processo do cianeto pode ser utilizado para extrair ouro de rochas. Esse processo consiste em, inicialmente, tratar as rochas trituradas com cianeto, havendo formação do
UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO
 UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO 08/11/2010 PROVA ESCRITA Assinatura do candidato: Área de concentração:
UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO 08/11/2010 PROVA ESCRITA Assinatura do candidato: Área de concentração:
UNIVERSIDADE FEDERAL DE PELOTAS CENTRO DE CIÊNCIAS QUÍMICAS, FARMACÊUTICAS E DE ALIMENTOS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA
 PROVA DE FÍSICO-QUÍMICA - 2017/02 Questão 1: Um mol de CO 2 ocupa um volume de 1,32 L e temperatura de 48ºC. Calcule a pressão do sistema supondo em a) um sistema ideal, b) um sistema real e em c) diga
PROVA DE FÍSICO-QUÍMICA - 2017/02 Questão 1: Um mol de CO 2 ocupa um volume de 1,32 L e temperatura de 48ºC. Calcule a pressão do sistema supondo em a) um sistema ideal, b) um sistema real e em c) diga
O aluno deverá elaborar resumos teóricos dos textos do livro e de outras fontes sobre os tópicos do conteúdo.
 Disciplina QUÍMICA Curso ENSINO MÉDIO Professor GUILHERME Série 1ª SÉRIE ROTEIRO DE ESTUDOS DE RECUPERAÇÃO E REVISÃO 1º SEMESTRE / 2012 Aluno (a): Número: 1 - Conteúdo: Ácidos e bases propriedades, conceito
Disciplina QUÍMICA Curso ENSINO MÉDIO Professor GUILHERME Série 1ª SÉRIE ROTEIRO DE ESTUDOS DE RECUPERAÇÃO E REVISÃO 1º SEMESTRE / 2012 Aluno (a): Número: 1 - Conteúdo: Ácidos e bases propriedades, conceito
Sugestões de estudo para a P1
 Sugestões de estudo para a P1 1) Considere a curva de energia potencial da ligação entre dois átomos (E) apresentada ao lado, e as três afirmações a Seguir: I. Na distância interatômica r o as forças de
Sugestões de estudo para a P1 1) Considere a curva de energia potencial da ligação entre dois átomos (E) apresentada ao lado, e as três afirmações a Seguir: I. Na distância interatômica r o as forças de
SISTEMA HEXAGONAL SIMPLES
 SISTEMA HEXAGONAL SIMPLES Os metais não cristalizam no sistema hexagonal simples porque o fator de empacotamento é muito baixo Entretanto, cristais com mais de um tipo de átomo cristalizam neste sistema
SISTEMA HEXAGONAL SIMPLES Os metais não cristalizam no sistema hexagonal simples porque o fator de empacotamento é muito baixo Entretanto, cristais com mais de um tipo de átomo cristalizam neste sistema
PROVA DE INGRESSO NO CURSO DE MESTRADO ACADÊMICO EM QUÍMICA PROCESSO DE SELEÇÃO: segundo semestre de 2007
 UIVERSIDADE FEDERAL DO PARAÁ DEPARTAMETO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE IGRESSO O CURSO DE MESTRADO ACADÊMICO EM QUÍMICA PROCESSO DE SELEÇÃO: segundo semestre de 2007 09 de Julho
UIVERSIDADE FEDERAL DO PARAÁ DEPARTAMETO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE IGRESSO O CURSO DE MESTRADO ACADÊMICO EM QUÍMICA PROCESSO DE SELEÇÃO: segundo semestre de 2007 09 de Julho
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de Informações e instruções para a resolução da prova
 Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de 2014 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de 2014 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de Informações e instruções para a resolução da prova
 Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de 2015 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de 2015 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO MÉDIO - FASE 2
 III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com
DETERMINAÇÃO DE ALGUNS PARÂMETROS CINÉTICOS DA REAÇÃO DE DECOMPOSIÇÃO DO PERÓXIDO DE HIDROGÊNIO.
 DETERMINAÇÃO DE ALGUNS PARÂMETROS CINÉTICOS DA REAÇÃO DE DECOMPOSIÇÃO DO PERÓXIDO DE HIDROGÊNIO. Glauber Silva Godoi Aula 13 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros
DETERMINAÇÃO DE ALGUNS PARÂMETROS CINÉTICOS DA REAÇÃO DE DECOMPOSIÇÃO DO PERÓXIDO DE HIDROGÊNIO. Glauber Silva Godoi Aula 13 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros
Olimpíada Brasileira de Química
 Olimpíada Brasileira de Química - 2006 Fase III MODALIDADE A Olimpíada Brasileira de Química PARTE I - QUESTÕES MÚLTIPLA ESCOLHA QUESTÃO 1 As espécies Fe 2+ e Fe 3+, provenientes de isótopos distintos
Olimpíada Brasileira de Química - 2006 Fase III MODALIDADE A Olimpíada Brasileira de Química PARTE I - QUESTÕES MÚLTIPLA ESCOLHA QUESTÃO 1 As espécies Fe 2+ e Fe 3+, provenientes de isótopos distintos
Determine o abaixamento relativo da pressão de vapor do solvente quando ) são dissolvidos em 117,2 ml de etanol a 25 o C.
 1 a QUESTÃO Valor: 1,0 Considerando os elementos químicos Be, B, F, Ca e Cs, classifique-os em ordem crescente de acordo com as propriedades periódicas indicadas: a. raio atômico; b. primeira energia de
1 a QUESTÃO Valor: 1,0 Considerando os elementos químicos Be, B, F, Ca e Cs, classifique-os em ordem crescente de acordo com as propriedades periódicas indicadas: a. raio atômico; b. primeira energia de
Serviço Público Federal Universidade Federal do Pará Instituto de Ciências Exatas e Naturais Programa de Pós-Graduação em Química
 Questão 1: (1,25 pontos) Uma preparação farmacêutica contendo cromo (III) foi analisada tratando-se 2,63 g da amostra com 5,00 ml de solução 0,0103 mol/l de EDTA. A quantidade de EDTA que não reagiu foi
Questão 1: (1,25 pontos) Uma preparação farmacêutica contendo cromo (III) foi analisada tratando-se 2,63 g da amostra com 5,00 ml de solução 0,0103 mol/l de EDTA. A quantidade de EDTA que não reagiu foi
Prova de Conhecimentos Específicos 1 a QUESTÃO: (1,0 ponto)
 Prova de Conhecimentos Específicos 1 a QUESTÃO: (1,0 ponto) Fluoreto de alumínio é insolúvel em ácido fluorídrico líquido, mas se dissolve quando fluoreto de sódio está presente. Quando fluoreto de boro
Prova de Conhecimentos Específicos 1 a QUESTÃO: (1,0 ponto) Fluoreto de alumínio é insolúvel em ácido fluorídrico líquido, mas se dissolve quando fluoreto de sódio está presente. Quando fluoreto de boro
PROCESSO DE SELEÇÃO 2017 TURMA 2018 ANTES DE RESPONDER ÀS QUESTÕES DESTA PROVA, LEIA ATENTAMENTE ESTAS INSTRUÇÕES:
 Código do candidato PROCESSO DE SELEÇÃO 2017 TURMA 2018 ANTES DE RESPONDER ÀS QUESTÕES DESTA PROVA, LEIA ATENTAMENTE ESTAS INSTRUÇÕES: Escreva o seu código de identificação em todas as folhas de resposta
Código do candidato PROCESSO DE SELEÇÃO 2017 TURMA 2018 ANTES DE RESPONDER ÀS QUESTÕES DESTA PROVA, LEIA ATENTAMENTE ESTAS INSTRUÇÕES: Escreva o seu código de identificação em todas as folhas de resposta
Tabela Periódica dos Elementos
 MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DO PIAUÍ CENTRO DE CIÊNCIAS DA NATUREZA Pró-Reitoria de Pesquisa e Pós-Graduação Coordenação do Programa de Pós-Graduação em Química EXAME SELETIVO PARA INGRESSO
MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DO PIAUÍ CENTRO DE CIÊNCIAS DA NATUREZA Pró-Reitoria de Pesquisa e Pós-Graduação Coordenação do Programa de Pós-Graduação em Química EXAME SELETIVO PARA INGRESSO
Introdução a Engenharia e Ciência dos Materiais
 Introdução a Engenharia e Ciência dos Materiais Estrutura Cristalina Prof. Vera L Arantes 2014 25/3/2014 ESTRUTURA CRISTALINA 2 ARRANJO ATÔMICO Por que estudar? As propriedades de alguns materiais estão
Introdução a Engenharia e Ciência dos Materiais Estrutura Cristalina Prof. Vera L Arantes 2014 25/3/2014 ESTRUTURA CRISTALINA 2 ARRANJO ATÔMICO Por que estudar? As propriedades de alguns materiais estão
TP064 - CIÊNCIA DOS MATERIAIS PARA EP. FABIANO OSCAR DROZDA
 TP064 - CIÊNCIA DOS MATERIAIS PARA EP FABIANO OSCAR DROZDA fabiano.drozda@ufpr.br 1 AULA 03 ESTRUTURA DOS SÓLIDOS CRISTALINOS 2 BREVE REVISÃO AULA PASSADA LIGAÇÕES QUÍMICAS Ligações primárias ou fortes
TP064 - CIÊNCIA DOS MATERIAIS PARA EP FABIANO OSCAR DROZDA fabiano.drozda@ufpr.br 1 AULA 03 ESTRUTURA DOS SÓLIDOS CRISTALINOS 2 BREVE REVISÃO AULA PASSADA LIGAÇÕES QUÍMICAS Ligações primárias ou fortes
ESTRUTURA DOS SÓLIDOS CRISTALINOS. Mestranda: Marindia Decol
 ESTRUTURA DOS SÓLIDOS CRISTALINOS Mestranda: Marindia Decol Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
ESTRUTURA DOS SÓLIDOS CRISTALINOS Mestranda: Marindia Decol Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
Olimpíada Brasileira de Química 2013 Fase VI
 Programa Nacional Olimpíadas de Química Olimpíada Brasileira de Química 2013 Fase VI PROBLEMA 1: Complexos de cobalto são muito usados nos conhecidos galinhos do tempo, que são bibelôs que mudam de cor,
Programa Nacional Olimpíadas de Química Olimpíada Brasileira de Química 2013 Fase VI PROBLEMA 1: Complexos de cobalto são muito usados nos conhecidos galinhos do tempo, que são bibelôs que mudam de cor,
FÍSICA DA MATÉRIA CONDENSADA 2009/10 Folha 1 I Redes e Estruturas Cristalinas
 FÍSICA DA MATÉRIA CONDENSADA 2009/10 Folha 1 I Redes e Estruturas Cristalinas 1 - Indicar a rede subjacente aos desenhos das figuras la) e lb). Encontrar três conjuntos de vectores fundamentais primitivos
FÍSICA DA MATÉRIA CONDENSADA 2009/10 Folha 1 I Redes e Estruturas Cristalinas 1 - Indicar a rede subjacente aos desenhos das figuras la) e lb). Encontrar três conjuntos de vectores fundamentais primitivos
Tabela Periódica dos Elementos
 MINISTÉRI DA EDUCAÇÃ UNIVERSIDADE FEDERAL D PIAUÍ CENTR DE CIÊNCIAS DA NATUREZA Pró-reitoria de Pesquisa e Pós-Graduação Coordenação do Programa de Pós-Graduação em Química EXAME SELETIV PARA INGRESS N
MINISTÉRI DA EDUCAÇÃ UNIVERSIDADE FEDERAL D PIAUÍ CENTR DE CIÊNCIAS DA NATUREZA Pró-reitoria de Pesquisa e Pós-Graduação Coordenação do Programa de Pós-Graduação em Química EXAME SELETIV PARA INGRESS N
ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA.
 ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA. Glauber Silva Godoi Aula 14 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros cinéticos de uma reação a partir
ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA. Glauber Silva Godoi Aula 14 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros cinéticos de uma reação a partir
ESTRUTURA DOS SÓLIDOS CRISTALINOS CAP. 03
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE ENGENHARIA MECÂNICA ESTRUTURA DOS SÓLIDOS CRISTALINOS CAP. 03 CMA CIÊNCIA DOS MATERIAIS 2º Semestre de 2014 Prof.
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE ENGENHARIA MECÂNICA ESTRUTURA DOS SÓLIDOS CRISTALINOS CAP. 03 CMA CIÊNCIA DOS MATERIAIS 2º Semestre de 2014 Prof.
PROPRIEDADES DOS SÓLIDOS ESTRUTURA E TIPO DE LIGAÇÕES
 PROPRIEDADES DOS SÓLIDOS ESTRUTURA E TIPO DE LIGAÇÕES 1 REPRESENTAÇÃO Diferentes estados da matéria gás pouca ordem, movimentos rápidos. Sólido cristalino altamente ordenado líquido polar mais ordenado,
PROPRIEDADES DOS SÓLIDOS ESTRUTURA E TIPO DE LIGAÇÕES 1 REPRESENTAÇÃO Diferentes estados da matéria gás pouca ordem, movimentos rápidos. Sólido cristalino altamente ordenado líquido polar mais ordenado,
O diagrama abaixo relaciona a solubilidade de dois sais A e B com a temperatura.
 13 PRVA D E Q U Í M I C A Q U E S T Ã 21 diagrama abaixo relaciona a solubilidade de dois sais A e B com a temperatura. Com relação ao diagrama, é INCRRET afirmar que: a) a 100ºC, a solubilidade de B é
13 PRVA D E Q U Í M I C A Q U E S T Ã 21 diagrama abaixo relaciona a solubilidade de dois sais A e B com a temperatura. Com relação ao diagrama, é INCRRET afirmar que: a) a 100ºC, a solubilidade de B é
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de Informações e instruções para a resolução da prova
 Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de 2013 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de 2013 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Resolução da Questão 1 Item I (Texto Definitivo)
 Questão Considerando que, por meio do cálculo integral, é possível calcular áreas delimitadas por gráficos de curvas, atenda, necessariamente, o que se pede nos itens de I a IV a seguir. I Calcule os pontos
Questão Considerando que, por meio do cálculo integral, é possível calcular áreas delimitadas por gráficos de curvas, atenda, necessariamente, o que se pede nos itens de I a IV a seguir. I Calcule os pontos
30 Exercícios Resolvidos CAPÍTULO 3 ESTRUTURA CRISTALINA
 IFRS - Mestrado em Tecnologia e Engenharia de Materiais DISCIPLINA: Ciência dos Materiais PROFESSOR: Juliano Toniollo ALUNO: PAULO CESAR FRITZEN 30 Exercícios Resolvidos CAPÍTULO 3 ESTRUTURA CRISTALINA
IFRS - Mestrado em Tecnologia e Engenharia de Materiais DISCIPLINA: Ciência dos Materiais PROFESSOR: Juliano Toniollo ALUNO: PAULO CESAR FRITZEN 30 Exercícios Resolvidos CAPÍTULO 3 ESTRUTURA CRISTALINA
ESTEQUIOMETRIA stoicheion metron
 Nada mais é do que a ciência responsável por equacionar e quantificar as transformações químicas, permitindo assim, determinar quase que com exatidão o que ocorre experimentalmente. O termo Estequiometria
Nada mais é do que a ciência responsável por equacionar e quantificar as transformações químicas, permitindo assim, determinar quase que com exatidão o que ocorre experimentalmente. O termo Estequiometria
21. Considere a seguinte expressão de constante de equilíbrio em termos de pressões parciais: K p =
 PASES 2 a ETAPA TRIÊNIO 2003-2005 1 O DIA GABARITO 1 13 QUÍMICA QUESTÕES DE 21 A 30 21. Considere a seguinte expressão de constante de equilíbrio em termos de pressões parciais: K p = 1 p CO2 Dentre as
PASES 2 a ETAPA TRIÊNIO 2003-2005 1 O DIA GABARITO 1 13 QUÍMICA QUESTÕES DE 21 A 30 21. Considere a seguinte expressão de constante de equilíbrio em termos de pressões parciais: K p = 1 p CO2 Dentre as
Exame 2º Ano Modalidade B
 Questão 01 O Bismuto é um elemento muito usado na indústria de cosméticos, devido sua baixa toxicidade. O isótopo mais estável do Bismuto apresenta número de massa 209 e dar origem ao íon Bi 3+ (forma
Questão 01 O Bismuto é um elemento muito usado na indústria de cosméticos, devido sua baixa toxicidade. O isótopo mais estável do Bismuto apresenta número de massa 209 e dar origem ao íon Bi 3+ (forma
XII Olimpíada Baiana de Química Exame 2017
 Questão 01 (Peso 1) Questões objetivas (QUESTÕES DE 01 A 30) A fórmula estrutural condensada, CH 3 CH 2 CH 2 COOCH 3, representa: A) um éster B) uma amida C) um aldeído D) um anidrido E) um ácido carboxílico
Questão 01 (Peso 1) Questões objetivas (QUESTÕES DE 01 A 30) A fórmula estrutural condensada, CH 3 CH 2 CH 2 COOCH 3, representa: A) um éster B) uma amida C) um aldeído D) um anidrido E) um ácido carboxílico
Atividades de Recuperação Paralela de Química A
 Atividades de Recuperação Paralela de Química A 3ª série Ensino Médio. Conteúdos para estudos: Setor A: calcular ph e poh de soluções; equacionar hidrólises de sais ácidos e básicos; calcular a solubilidade
Atividades de Recuperação Paralela de Química A 3ª série Ensino Médio. Conteúdos para estudos: Setor A: calcular ph e poh de soluções; equacionar hidrólises de sais ácidos e básicos; calcular a solubilidade
OLIMPÍADA BRASILEIRA DE QUÍMICA 2001 FASE III
 UNIVERSIDADE FEDERAL DO CEARÁ CENTRO DE CIÊNCIAS OLIMPÍADA BRASILEIRA DE QUÍMICA 2001 FASE III PROBLEMA 1 Anestésico local Uma substância A, medicinalmente usada em preparações para uso tópico como anestésico
UNIVERSIDADE FEDERAL DO CEARÁ CENTRO DE CIÊNCIAS OLIMPÍADA BRASILEIRA DE QUÍMICA 2001 FASE III PROBLEMA 1 Anestésico local Uma substância A, medicinalmente usada em preparações para uso tópico como anestésico
UNIDADE 6 Defeitos do Sólido Cristalino
 UNIDADE 6 Defeitos do Sólido Cristalino 1. Em condições de equilíbrio, qual é o número de lacunas em 1 m de cobre a 1000 o C? Dados: N: número de átomos por unidade de volume N L : número de lacunas por
UNIDADE 6 Defeitos do Sólido Cristalino 1. Em condições de equilíbrio, qual é o número de lacunas em 1 m de cobre a 1000 o C? Dados: N: número de átomos por unidade de volume N L : número de lacunas por
Desenhe a estrutura espacial do gás carbônico, da amônia, do metano, do etileno, do acetileno e do benzeno.
 Exemplos de Questões de Conteúdo Geral Questão 1 Responda os seguintes itens: a) Na classificação periódica, o elemento químico de configuração [Ar] 4s 2 3d 10 4p 5 está localizado em que período? Qual
Exemplos de Questões de Conteúdo Geral Questão 1 Responda os seguintes itens: a) Na classificação periódica, o elemento químico de configuração [Ar] 4s 2 3d 10 4p 5 está localizado em que período? Qual
Avaliação para Seleção de Mestrado em Agroquímica I. Número ou código do(a) candidato(a): INSTRUÇÕES
 Universidade Federal de Viçosa Departamento de Química Programa de Pós-Graduação em Agroquímica Avaliação para Seleção de Mestrado em Agroquímica - 2012-I Número ou código do(a) candidato(a): INSTRUÇÕES
Universidade Federal de Viçosa Departamento de Química Programa de Pós-Graduação em Agroquímica Avaliação para Seleção de Mestrado em Agroquímica - 2012-I Número ou código do(a) candidato(a): INSTRUÇÕES
Físico-Química Experimental Exp. 10. Cinética Química
 Cinética Química 1. Introdução Cinética química é o estudo da progressão das reações químicas, o que determina suas velocidades e como controlá-las. Ao estudar a termodinâmica de uma reação, leva-se em
Cinética Química 1. Introdução Cinética química é o estudo da progressão das reações químicas, o que determina suas velocidades e como controlá-las. Ao estudar a termodinâmica de uma reação, leva-se em
QUI109 QUÍMICA GERAL (Ciências Biológicas) 4ª aula /
 QUI109 QUÍMICA GERAL (Ciências Biológicas) 4ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) REAÇÃO EM SOLUÇÃO AQUOSA São reações envolvendo compostos iônicos
QUI109 QUÍMICA GERAL (Ciências Biológicas) 4ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) REAÇÃO EM SOLUÇÃO AQUOSA São reações envolvendo compostos iônicos
5ª AVALIAÇÃO TRADICICIONAL 5ª AVALIAÇÃO TRADICIONAL/2017 3ª SÉRIE / PRÉ-VESTIBULAR PROVA DISCURSIVA DE QUÍMICA RESOLUÇÃO ATENÇÃO!
 5ª AVALIAÇÃO TRADICIONAL/2017 3ª SÉRIE / PRÉ-VESTIBULAR PROVA DISCURSIVA DE QUÍMICA RESOLUÇÃO ATENÇÃO! Duração total das provas Discursivas + REDAÇÃO: 5 1/2 horas 1 1ª Questão (Douglas) 5ª AVALIAÇÃO TRADICICIONAL
5ª AVALIAÇÃO TRADICIONAL/2017 3ª SÉRIE / PRÉ-VESTIBULAR PROVA DISCURSIVA DE QUÍMICA RESOLUÇÃO ATENÇÃO! Duração total das provas Discursivas + REDAÇÃO: 5 1/2 horas 1 1ª Questão (Douglas) 5ª AVALIAÇÃO TRADICICIONAL
QUÍMICA TITULAÇÃO ,0 ml de uma solução de NaOH neutralizam totalmente 10,0 ml de uma solução de HNO
 QUÍMICA Prof. Daniel Pires TITULAÇÃO 1. Um suco de laranja industrializado tem seu valor de ph determinado pelo controle de qualidade. Na análise, 20 ml desse suco foram neutralizados com 2 ml de NaOH
QUÍMICA Prof. Daniel Pires TITULAÇÃO 1. Um suco de laranja industrializado tem seu valor de ph determinado pelo controle de qualidade. Na análise, 20 ml desse suco foram neutralizados com 2 ml de NaOH
Departamento de Química Inorgânica IQ / UFRJ IQG 128 / IQG CINÉTICA QUÍMICA
 Departamento de Química Inorgânica IQ / UFRJ IQG 18 / IQG 31 6. CINÉTICA QUÍMICA I. INTRODUÇÃO O ozônio é um dos componentes naturais da estratosfera, onde absorve parte significativa da radiação ultravioleta.
Departamento de Química Inorgânica IQ / UFRJ IQG 18 / IQG 31 6. CINÉTICA QUÍMICA I. INTRODUÇÃO O ozônio é um dos componentes naturais da estratosfera, onde absorve parte significativa da radiação ultravioleta.
ESTRUTURA DOS SÓLIDOS
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais ESTRUTURA DOS SÓLIDOS PMT 2100 - Introdução à Ciência dos Materiais para Engenharia 2º semestre de
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais ESTRUTURA DOS SÓLIDOS PMT 2100 - Introdução à Ciência dos Materiais para Engenharia 2º semestre de
Física da Matéria Condensada
 Física da Matéria Condensada II Redes e estruturas cristalinas 1. Indique a rede subjacente aos desenhos das figuras 1 e 2. Encontre três conjuntos de vectores fundamentais primitivos para a fig. 1 e dois
Física da Matéria Condensada II Redes e estruturas cristalinas 1. Indique a rede subjacente aos desenhos das figuras 1 e 2. Encontre três conjuntos de vectores fundamentais primitivos para a fig. 1 e dois
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de Informações e instruções para a resolução da prova
 Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de 2014 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de 2014 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de Informações e instruções para a resolução da prova
 Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de 2013 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de 2013 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
EXAME DE SELEÇÃO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA DO INSTITUTO DE QUÍMICA-ARARAQUARA-UNESP 24/01/2012 CURSOS: MESTRADO E DOUTORADO
 EXAME DE SELEÇÃO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA DO INSTITUTO DE QUÍMICA-ARARAQUARA-UNESP 24/01/2012 CURSOS: MESTRADO E DOUTORADO Questão 1. Mostre, fazendo uso de mecanismos e reagentes adequados,
EXAME DE SELEÇÃO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA DO INSTITUTO DE QUÍMICA-ARARAQUARA-UNESP 24/01/2012 CURSOS: MESTRADO E DOUTORADO Questão 1. Mostre, fazendo uso de mecanismos e reagentes adequados,
3ª Série / Vestibular. As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar que, na reação:
 3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
Físico-química Farmácia 2014/02
 Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
CADERNO DE RESPOSTA RESPOSTAS ESPERADAS PELAS BANCAS ELABORADORAS 2ª FASE PROVA DISCURSIVA ESPECÍFICA CURSOS
 PROCESSO SELETIVO UEG 2013/1 Domingo, 25 de novembro de 2012. CADERNO DE RESPOSTA 2ª FASE PROVA DISCURSIVA ESPECÍFICA Grupo: Ciências Exatas e da Terra, Engenharia e outros - CETE III Curso Superior de
PROCESSO SELETIVO UEG 2013/1 Domingo, 25 de novembro de 2012. CADERNO DE RESPOSTA 2ª FASE PROVA DISCURSIVA ESPECÍFICA Grupo: Ciências Exatas e da Terra, Engenharia e outros - CETE III Curso Superior de
Química II 1º Exame B 4 de Junho de ª Parte
 Química II 1º Exame B 4 de Junho de 2018 Nome nº MEQ MEBiol Sala Duração: 3h 1: 2: 3: 4: 5: 6: 7: 8: 9: 10: Total: Responda às perguntas 1B a 5B na folha do enunciado Responda às perguntas 6B a 16B em
Química II 1º Exame B 4 de Junho de 2018 Nome nº MEQ MEBiol Sala Duração: 3h 1: 2: 3: 4: 5: 6: 7: 8: 9: 10: Total: Responda às perguntas 1B a 5B na folha do enunciado Responda às perguntas 6B a 16B em
PADRÃO DE RESPOSTA - QUÍMICA - Grupo J
 PADRÃO DE RESPOSTA - QUÍMICA - Grupo J 1 a QUESTÃO: (2,0 pontos) Avaliador Revisor Num recipiente de 3,0 L de capacidade, as seguintes pressões parciais foram medidas: N 2 = 0,500 atm; H 2 = 0,400 atm;
PADRÃO DE RESPOSTA - QUÍMICA - Grupo J 1 a QUESTÃO: (2,0 pontos) Avaliador Revisor Num recipiente de 3,0 L de capacidade, as seguintes pressões parciais foram medidas: N 2 = 0,500 atm; H 2 = 0,400 atm;
Resolução da Questão 1 Item I (Texto Definitivo)
 Questão Considerando que, por meio do cálculo integral, é possível calcular áreas delimitadas por gráficos de curvas, atenda, necessariamente, o que se pede nos itens de I a IV a seguir. I Calcule os pontos
Questão Considerando que, por meio do cálculo integral, é possível calcular áreas delimitadas por gráficos de curvas, atenda, necessariamente, o que se pede nos itens de I a IV a seguir. I Calcule os pontos
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Lei de Velocidade Integrada Mostra a variação das concentrações
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Lei de Velocidade Integrada Mostra a variação das concentrações
ARRANJOS ATÔMICOS. Química Aplicada. Profº Vitor de Almeida Silva
 ARRANJOS ATÔMICOS Química Aplicada Profº Vitor de Almeida Silva 1. Arranjo Periódico de Átomos SÓLIDO: Constituído por átomos (ou grupo de átomos) que se distribuem de acordo com um ordenamento bem definido;
ARRANJOS ATÔMICOS Química Aplicada Profº Vitor de Almeida Silva 1. Arranjo Periódico de Átomos SÓLIDO: Constituído por átomos (ou grupo de átomos) que se distribuem de acordo com um ordenamento bem definido;
Universidade Federal da Paraíba. Centro de Ciências Exatas e da Natureza Programa de Pós-graduação em Química
 Universidade ederal da Paraíba Centro de Ciências Exatas e da Natureza Programa de Pós-graduação em Química PROVA DE SELEÇÃO PARA INGRESSO NO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA (PERÍODO 2019.1) DATA:
Universidade ederal da Paraíba Centro de Ciências Exatas e da Natureza Programa de Pós-graduação em Química PROVA DE SELEÇÃO PARA INGRESSO NO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA (PERÍODO 2019.1) DATA:
UNIDADE 4 Estrutura dos Sólidos Cristalinos
 UNIDADE 4 Estrutura dos Sólidos Cristalinos 1. Calcular a densidade teórica (em g/cm 3 ) dos seguintes metais: a) Fe- b) Al DADOS Estrutura Cristalina Raio Atômico (nm) Massa Molar (g/mol) Fe- CCC 0,1241
UNIDADE 4 Estrutura dos Sólidos Cristalinos 1. Calcular a densidade teórica (em g/cm 3 ) dos seguintes metais: a) Fe- b) Al DADOS Estrutura Cristalina Raio Atômico (nm) Massa Molar (g/mol) Fe- CCC 0,1241
A Dualidade Onda-Partícula
 A Dualidade Onda-Partícula O fato de que as ondas têm propriedades de partículas e viceversa se chama Dualidade Onda-Partícula. Todos os objetos (macroscópicos também!) são onda e partícula ao mesmo tempo.
A Dualidade Onda-Partícula O fato de que as ondas têm propriedades de partículas e viceversa se chama Dualidade Onda-Partícula. Todos os objetos (macroscópicos também!) são onda e partícula ao mesmo tempo.
Prova Escrita de Conhecimentos Gerais em Química
 Universidade de Brasília (UnB) Instituto de Química (IQ) Programa de Pós-Graduação em Química (PPGQ) Código: (uso da Secretaria) 06/02/2017 SELEÇÃO DE CANDIDATOS AO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA
Universidade de Brasília (UnB) Instituto de Química (IQ) Programa de Pós-Graduação em Química (PPGQ) Código: (uso da Secretaria) 06/02/2017 SELEÇÃO DE CANDIDATOS AO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA
Química. A) Considerando-se que o pk a1 é aproximadamente 2, quais os valores de pk a2 e pk a3?
 Química 01. O gráfico a seguir representa a variação do p de 50 ml de uma solução aquosa de um ácido 3 X em função do volume de NaO 0,30 moll -1 adicionado. A) Considerando-se que o pk a1 é aproximadamente
Química 01. O gráfico a seguir representa a variação do p de 50 ml de uma solução aquosa de um ácido 3 X em função do volume de NaO 0,30 moll -1 adicionado. A) Considerando-se que o pk a1 é aproximadamente
Universidade Federal da Paraíba. Centro de Ciências Exatas e da Natureza Programa de Pós-graduação em Química
 Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Programa de Pós-graduação em Química PROVA DE SELEÇÃO PARA INGRESSO NO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA (PERÍODO 2019.2) DATA:
Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Programa de Pós-graduação em Química PROVA DE SELEÇÃO PARA INGRESSO NO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA (PERÍODO 2019.2) DATA:
MÓDULOS 45 e 46 QUÍMICA. Cristais. Ciências da Natureza, Matemática e suas Tecnologias 1. CONCEITO DE CELA OU CÉLULA UNITÁRIA
 II Ciências da Natureza, Matemática e suas Tecnologias QUÍMICA MÓDULOS 45 e 46 Cristais. CONCEITO DE CELA OU CÉLULA UNITÁRIA É a menor unidade que se repete em um cristal, isto é, o retículo cristalino
II Ciências da Natureza, Matemática e suas Tecnologias QUÍMICA MÓDULOS 45 e 46 Cristais. CONCEITO DE CELA OU CÉLULA UNITÁRIA É a menor unidade que se repete em um cristal, isto é, o retículo cristalino
Física dos Materiais FMT0502 ( )
 Física dos Materiais FMT0502 (4300502) 1º Semestre de 2010 Instituto de Física Universidade de São Paulo Professor: Antonio Dominguesdos Santos E-mail: adsantos@if.usp.br Fone: 3091.6886 http://plato.if.usp.br/~fmt0502n/
Física dos Materiais FMT0502 (4300502) 1º Semestre de 2010 Instituto de Física Universidade de São Paulo Professor: Antonio Dominguesdos Santos E-mail: adsantos@if.usp.br Fone: 3091.6886 http://plato.if.usp.br/~fmt0502n/
estrutura atômica cristalino
 Aula 0b estrutura atômica cristalina ZEA 1038 Ciência e Tecnologia dos Materiais Prof. João Adriano Rossignolo Profa. Eliria M.J.A. Pallone estrutura atômica cristalino 1 CRISTAL ESTRUTURA CRISTALINA Muitos
Aula 0b estrutura atômica cristalina ZEA 1038 Ciência e Tecnologia dos Materiais Prof. João Adriano Rossignolo Profa. Eliria M.J.A. Pallone estrutura atômica cristalino 1 CRISTAL ESTRUTURA CRISTALINA Muitos
Capítulo 5 Estrutura dos materiais
 Capítulo 5 Estrutura dos materiais *. O Molibdénio (Mo) apresenta estrutura cristalina cúbica de corpo centrado (CCC) sendo o seu raio atómico e o seu peso atómico 0,nm e 95,94g/mol, respectivamente. Número
Capítulo 5 Estrutura dos materiais *. O Molibdénio (Mo) apresenta estrutura cristalina cúbica de corpo centrado (CCC) sendo o seu raio atómico e o seu peso atómico 0,nm e 95,94g/mol, respectivamente. Número
PAG Química Cinética 1.
 1. 2. 3. errata: a reação é em mais de uma etapa, os gráficos devem apresentar pelo menos duas!! 4. 5. Explique se cada uma das alternativas abaixo é correta ou não, para reações químicas que ocorrem
1. 2. 3. errata: a reação é em mais de uma etapa, os gráficos devem apresentar pelo menos duas!! 4. 5. Explique se cada uma das alternativas abaixo é correta ou não, para reações químicas que ocorrem
Centro de Ciências da Natureza DEPARTAMENTO DE QUÍMICA OLIMPÍADAS DE QUÍMICA
 Centro de Ciências da Natureza DEPARTAMENTO DE QUÍMICA OLIMPÍADAS DE QUÍMICA Olímpiada Brasileira de Química 2012 FASE VI 06.04.2013 Questão 1 (18 pontos) Os complexos de níquel normalmente se apresentam
Centro de Ciências da Natureza DEPARTAMENTO DE QUÍMICA OLIMPÍADAS DE QUÍMICA Olímpiada Brasileira de Química 2012 FASE VI 06.04.2013 Questão 1 (18 pontos) Os complexos de níquel normalmente se apresentam
NOME: QFL ª Prova (15 pontos) Tabela de deslocamentos químicos de 13 C em sistemas orgânicos
 NOME: QFL 2144 2008 3ª Prova (15 pontos) Tabela de deslocamentos químicos de 13 C em sistemas orgânicos Fragmentações e fragmentos comuns em espectrometria de massa Íon fragmento Neutro Perdido Massa do
NOME: QFL 2144 2008 3ª Prova (15 pontos) Tabela de deslocamentos químicos de 13 C em sistemas orgânicos Fragmentações e fragmentos comuns em espectrometria de massa Íon fragmento Neutro Perdido Massa do
Bioquímica Inorgânica. 1º exame 18 de Junho de 2014
 Nº Nome Bioquímica Inorgânica 1º exame 18 de Junho de 2014 Duração: 3h00. Leia todo o enunciado antes de começar a responder. Justifique as respostas. RESPONDA APENAS NOS ESPAÇOS ASSINALADOS. I (1,5) Alguns
Nº Nome Bioquímica Inorgânica 1º exame 18 de Junho de 2014 Duração: 3h00. Leia todo o enunciado antes de começar a responder. Justifique as respostas. RESPONDA APENAS NOS ESPAÇOS ASSINALADOS. I (1,5) Alguns
Programa de Pós-Graduação em Química UNIFAL-MG PROVA ESCRITA DE CONHECIMENTOS GERAIS EM QUÍMICA
 Programa de Pós-Graduação em Química UNIFAL-MG PROVA ESCRITA DE CONHECIMENTOS GERAIS EM QUÍMICA Orientações Importantes: 1) IDENTIFIQUE TODAS AS FOLHAS DA PROVA COM SEU NÚMERO DE INSCRIÇÃO. 2) EM HIPÓTESE
Programa de Pós-Graduação em Química UNIFAL-MG PROVA ESCRITA DE CONHECIMENTOS GERAIS EM QUÍMICA Orientações Importantes: 1) IDENTIFIQUE TODAS AS FOLHAS DA PROVA COM SEU NÚMERO DE INSCRIÇÃO. 2) EM HIPÓTESE
Ciência de Materiais. LEGI. Ano lectivo ESTRUTURA CRISTALINA
 1. I) Desenhe em cubos unitários os planos com os seguintes índices de Miller: a) ( 1 0 1) b) ( 0 3 1) c) ( 1 2 3) II) Desenhe em cubos unitários as direcções com os seguintes índices: a) [ 1 0 1] b) [
1. I) Desenhe em cubos unitários os planos com os seguintes índices de Miller: a) ( 1 0 1) b) ( 0 3 1) c) ( 1 2 3) II) Desenhe em cubos unitários as direcções com os seguintes índices: a) [ 1 0 1] b) [
Química Inorgânica Avançada
 Química Inorgânica Avançada - UFS 1 Química Inorgânica Avançada Prof. Dr. Antônio Reinaldo Cestari Discente: Ailton Soares SÃO CRISTÓVÃO-SE 16/OUTUBRO/2014 Química Inorgânica Avançada - UFS 2 Química Inorgânica
Química Inorgânica Avançada - UFS 1 Química Inorgânica Avançada Prof. Dr. Antônio Reinaldo Cestari Discente: Ailton Soares SÃO CRISTÓVÃO-SE 16/OUTUBRO/2014 Química Inorgânica Avançada - UFS 2 Química Inorgânica
FUVEST 1984 Primeira fase e Segunda fase
 FUVEST 1984 Primeira fase e Segunda fase Professora Sonia 9. A melhor maneira de separar os três componentes de uma mistura de areia com solução aquosa de sal é: CONHECIMENTOS GERAIS 5. O peso atômico
FUVEST 1984 Primeira fase e Segunda fase Professora Sonia 9. A melhor maneira de separar os três componentes de uma mistura de areia com solução aquosa de sal é: CONHECIMENTOS GERAIS 5. O peso atômico
Capítulo 1 - Cristais
 1. Cristais 1.1. Introdução O materiais no estado sólido podem apresentar estruturas cristalinas ou amorfas. Na estrutura cristalina os átomo (moléculas) apresentam um ordenamento periódico nas posições
1. Cristais 1.1. Introdução O materiais no estado sólido podem apresentar estruturas cristalinas ou amorfas. Na estrutura cristalina os átomo (moléculas) apresentam um ordenamento periódico nas posições
UDESC 2014/2 QUÍMICA. 15) Resposta: B. Comentário
 QUÍMICA 15) Resposta: B a) Correta. b) Incorreta. O modelo atômico constituído por núcleo positivo e eletrosfera de carga negativa é de autoria de Rutherford. c) Correta. d) Correta. e) Correta. 16) Resposta:
QUÍMICA 15) Resposta: B a) Correta. b) Incorreta. O modelo atômico constituído por núcleo positivo e eletrosfera de carga negativa é de autoria de Rutherford. c) Correta. d) Correta. e) Correta. 16) Resposta:
PROVA PARA INGRESSO NO MESTRADO. Programa de Pós Graduação em Química 14/06/2017 NOME
 PROVA PARA INGRESSO NO MESTRADO Programa de Pós Graduação em Química 14/06/2017 NOME Instruções para a prova: Coloque seu nome nesta folha antes de continuar; Marcar com um X, no quadro abaixo, as questões
PROVA PARA INGRESSO NO MESTRADO Programa de Pós Graduação em Química 14/06/2017 NOME Instruções para a prova: Coloque seu nome nesta folha antes de continuar; Marcar com um X, no quadro abaixo, as questões
Universidade Federal da Paraíba. Centro de Ciências Exatas e da Natureza Programa de Pós-graduação em Química
 Universidade ederal da Paraíba Centro de Ciências Exatas e da Natureza Programa de Pós-graduação em Química PROVA DE SELEÇÃO PARA INGRESSO NO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA (PERÍODO 218.2) DATA:
Universidade ederal da Paraíba Centro de Ciências Exatas e da Natureza Programa de Pós-graduação em Química PROVA DE SELEÇÃO PARA INGRESSO NO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA (PERÍODO 218.2) DATA:
Gabarito Prova de Conhecimentos em Química Mestrado/Doutorado 1/2018 PPGQ/IQ/UnB
 Gabarito Prova de Conhecimentos em Química Mestrado/Doutorado 1/2018 PPGQ/IQ/UnB Questão 1 - Em 1888, Rydberg mostrou que o espectro de linhas do átomo de hidrogênio poderia ser descrito pela expressão
Gabarito Prova de Conhecimentos em Química Mestrado/Doutorado 1/2018 PPGQ/IQ/UnB Questão 1 - Em 1888, Rydberg mostrou que o espectro de linhas do átomo de hidrogênio poderia ser descrito pela expressão
Avaliação para Seleção de Mestrado em Agroquímica II. Número ou código do(a) candidato(a): INSTRUÇÕES
 Universidade Federal de Viçosa Departamento de Química Programa de Pós-Graduação em Agroquímica Avaliação para Seleção de Mestrado em Agroquímica - 2016.II Número ou código do(a) candidato(a): INSTRUÇÕES
Universidade Federal de Viçosa Departamento de Química Programa de Pós-Graduação em Agroquímica Avaliação para Seleção de Mestrado em Agroquímica - 2016.II Número ou código do(a) candidato(a): INSTRUÇÕES
Capítulo 5 Estrutura dos materiais
 Capítulo 5 Estrutura dos materiais *. O vanádio (V) apresenta estrutura cúbica de corpo centrado (CCC), sendo o parâmetro da rede 0,04nm e o peso atómico 50,94g/mol. O número de Avogadro é N 0 0 A =, /
Capítulo 5 Estrutura dos materiais *. O vanádio (V) apresenta estrutura cúbica de corpo centrado (CCC), sendo o parâmetro da rede 0,04nm e o peso atómico 50,94g/mol. O número de Avogadro é N 0 0 A =, /
Prova 3 Química QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. QUESTÕES OBJETIVAS GABARITO 4
 Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Assinale a alternativa incorreta.
Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Assinale a alternativa incorreta.
Prova 3 Química QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. QUESTÕES OBJETIVAS GABARITO 1
 Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 A quantidade de Na 2 CO 3.10H 2
Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 A quantidade de Na 2 CO 3.10H 2
Prova 3 Química QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. QUESTÕES OBJETIVAS GABARITO 2
 Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Considere que, a 25 o C, temos
Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Considere que, a 25 o C, temos
Prova 3 Química QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. QUESTÕES OBJETIVAS GABARITO 3
 Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Assinale a alternativa correta.
Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Assinale a alternativa correta.
UNIVERSIDADE ESTADUAL DO SUDOESTE DA BAHIA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA EXAME GERAL EM QUÍMICA EDITAL N 163/2017
 UNIVERSIDADE ESTADUAL DO SUDOESTE DA BAHIA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA EXAME GERAL EM QUÍMICA EDITAL N 163/2017 Seleção para o 1º Semestre de 2018 16 de janeiro de 2018 CADERNO DE QUESTÕES Tempo
UNIVERSIDADE ESTADUAL DO SUDOESTE DA BAHIA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA EXAME GERAL EM QUÍMICA EDITAL N 163/2017 Seleção para o 1º Semestre de 2018 16 de janeiro de 2018 CADERNO DE QUESTÕES Tempo
Teoria da Ligação de Valência (TLV)
 Universidade Federal de Sergipe Departamento de Química Química Inorgânica Teoria da Ligação de Valência (TLV) Docente: Reinaldo Cestari Discente: Daiane Requião São Cristóvão - 2014 Elaboração Walter
Universidade Federal de Sergipe Departamento de Química Química Inorgânica Teoria da Ligação de Valência (TLV) Docente: Reinaldo Cestari Discente: Daiane Requião São Cristóvão - 2014 Elaboração Walter
AVALIAÇÃO DOS FATORES QUE INFLUENCIAM A VELOCIDADE DAS REAÇÕES QUÍMICAS: PRESENÇA
 AVALIAÇÃO DOS FATORES QUE INFLUENCIAM A VELOCIDADE DAS REAÇÕES QUÍMICAS: PRESENÇA DE CATALISADOR E SUPERFÍCIE DE CONTATO. Aula 12 Glauber Silva Godoi META Desenvolver no aluno a capacidade de avaliar os
AVALIAÇÃO DOS FATORES QUE INFLUENCIAM A VELOCIDADE DAS REAÇÕES QUÍMICAS: PRESENÇA DE CATALISADOR E SUPERFÍCIE DE CONTATO. Aula 12 Glauber Silva Godoi META Desenvolver no aluno a capacidade de avaliar os
Pb 2e Pb E 0,13 v. Ag 2e Ag E +0,80 v. Zn 2e Zn E 0,76 v. Al 3e Al E 1,06 v. Mg 2e Mg E 2,4 v. Cu 2e Cu E +0,34 v
 QUÍMICA 1ª QUESTÃO Umas das reações possíveis para obtenção do anidrido sulfúrico é a oxidação do anidrido sulfuroso por um agente oxidante forte em meio aquoso ácido, como segue a reação. Anidrido sulfuroso
QUÍMICA 1ª QUESTÃO Umas das reações possíveis para obtenção do anidrido sulfúrico é a oxidação do anidrido sulfuroso por um agente oxidante forte em meio aquoso ácido, como segue a reação. Anidrido sulfuroso
CONCURSO DE ADMISSÃO AO CURSO DE FORMAÇÃO E GRADUAÇÃO QUÍMICA FOLHA DE QUESTÕES
 CONCURSO DE ADMISSÃO AO CURSO DE FORMAÇÃO E GRADUAÇÃO QUÍMICA FOLHA DE QUESTÕES 2007 1 a QUESTÃO Valor: 1,0 A A configuração eletrônica de um átomo X é [ X ]. Determine: Z a) os valores de Z e de n, para
CONCURSO DE ADMISSÃO AO CURSO DE FORMAÇÃO E GRADUAÇÃO QUÍMICA FOLHA DE QUESTÕES 2007 1 a QUESTÃO Valor: 1,0 A A configuração eletrônica de um átomo X é [ X ]. Determine: Z a) os valores de Z e de n, para
2005 by Pearson Education. Capítulo 04
 QUÍMICA A Ciência Central 9ª Edição Capítulo 4 Reações em soluções aquosas e estequiometria de soluções David P. White Propriedades gerais das soluções aquosas Propriedades eletrolíticas As soluções aquosas
QUÍMICA A Ciência Central 9ª Edição Capítulo 4 Reações em soluções aquosas e estequiometria de soluções David P. White Propriedades gerais das soluções aquosas Propriedades eletrolíticas As soluções aquosas
