HISTÓRIA DA MATÉRIA. Leucipo e Demócretes (V a.c.) Aristóteles (III a.c.)
|
|
|
- Brian Ferreira Farias
- 6 Há anos
- Visualizações:
Transcrição
1 HISTÓRIA DA MATÉRIA Leucipo e Demócretes (V a.c.) Tudo que existe é composto de elementos indivisíveis Átomo a = negação; tomo = divisível Entidades discretas, infinitamente duras, não modificáveis, eternas e indivísveis Aristóteles (III a.c.) Contra o atomicismo Senso comum: sólidos são sólidos, líquidos são líquidos, e não um monte de pequenas partículas que ninguém vê! Influência dura mais de 000 anos: conceito de átomo é esquecido
2 John Dalton (1808) Reintroduz o átomo Elementos são constituídos de átomos idênticos e indivisíveis Átomos de um mesmo elemento possuem mesmo tamanho e massa Átomos de diferentes elementos se distinguem apenas por sua massa Átomos não podem ser criados ou destruídos por processos químicos (indestrutíveis) Reações químicas átomos dos materiais iniciais são reorganizados em proporções definidas Átomos podem se combinar (síntese) e se separar (análise) Teoria explica perfeitamente os teoremas introduzidos (resultados experimentais) Unidade de massa atômica massa do átomo de hidrogênio 1 u (uma, amu) = 1 Da = 1, kg Nova pergunta comum: de que é feito o átomo?
3 Michael Faraday (183) Eletrólise dividir através da eletricidade H O (l) O (g) + 4H + (aq) + 4e - 4H O (l) + 4e - H (g) + 4OH - (aq) gás O V.V gás H Lei de Faraday: em uma eletrólise, o número de moles liberado em um eletrodo é proporcional à carga que flui pela solução eletrolítica bolhas de O bolhas de H bateria ou fonte DC número moles = relação entre massa e massa molar (mol) H O + e - e - ânodo cátodo
4 George Johnstone Stoney (1874) Existência de transportadores de cargas elétricas ligados ao átomo elétrons William Crookes (1879) Raios catódicos são constituídos de corpúsculos Philipp Lenard (1890) Experimentos sistemáticos para analisar os raios catódicos Jean Baptiste Perrin (1895) Raios catódicos são constituídos de corpúsculos com carga elétrica negativa Novo desafio: determinar a massa m e a carga q do corpúsculo
5 Joseph John Thomson (1897) Descobre o elétron Supõe que os elétrons (raios catódicos) já estão presentes nos átomos do cátodo Encontra a relação q/m para o elétron q/m = 1, C/kg Joseph John Thomson (1904) 1 o modelo atômico Modelo do pudim de ameixas ( Plumpudding ) Átomo massa uniformemente distribuída, de carga positiva, dentro da qual estão incrustados os pequenos elétrons de carga negativa Átomo excitado: elétrons vibram, emitindo radiação Robert Andrews Millikan (1910) Encontra a carga q do elétron q = 1, C m = 9, kg
6 Ernest Rutherford (1911) Mostra que o modelo de J. J. Thomson é incorreto; substitui por novo modelo o modelo atômico Modelo planetário Átomo pequeno núcleo positivamente carregado rodeado por uma núvem de elétrons negativos Núcleo possui praticamente toda a massa do átomo Núvem de elétrons ocupa praticamente todo o volume do átomo Elétrons orbitam ao redor do núcleo acelerados (MCU) Modelo tem uma falha séria: os elétrons continuamente acelerados deveriam emitir energia (radiação) devido à perda de energia sua trajetória se tornaria espiral os elétrons deveriam colapsar contra o núcleo Outra falha: não explica os espectros de linhas (discretos) obtidos experimentalmente
7 Niels Bohr (1915) Novo modelo atômico Modelo planetário Idêntico ao modelo de Rutherford, porém postulando determinadas propriedades Argumento: modelo explica bem os resultados experimentais!! Postulados de Bohr: as órbitas dos elétrons não podem ser quaiquer somente certas órbitas são permitidas o elétron em sua órbita não emite energia somente ao passar de uma órbita a outra o elétron irá emitir (ou absorver) energia Órbitas eletrônicas são discretas e estáveis
8 Arnold Sommerfeld (1916) Extende o modelo de Bohr Modelo de Bohr-Sommerfeld Órbitas elípticas Ernest Rutherford (1919) Descobre o próton como constituinte do núcleo atômico Identifica o próton como sendo o núcleo do átomo de hidrogênio Próton = o primeiro pois o 1 H é o menor e mais simples átomo James Chadwick (193) Descobre o neutron
9 Espectros atômicos Sólidos em altas T Espectro contínuo Gás monoatômico (rarefeito) Espectro discreto Experimento (emissão) Elétrons são acelerados pela ddp V em uma ampola de gás rarefeito Eletrons colidem com átomos do gás, cedendo-lhes energia e levando-os a estados excitados Átomos retornam ao estado normal, emitindo radiação Radiação passa pela fenda colimadora e é decomposta, no prisma, em seus diversos comprimentos de onda fenda lâmpada de hidrogênio prisma Cada tipo de átomo tem seu espectro característico detector
10 Espectro da lâmpada de hidrogênio Espectro regular incentiva a busca de uma equação Balmer (1885) n λ = 3646 n 4 Série de Balmer Rydberg (1890) 1 λ (A 1 ) = n 4 n = n = R H 1 1 n R H = 10, m 1 cte. de Rydberg Séries para o hidrogênio 1 λ = R H n n =, 3, 1 λ = R 1 H 1 n n = 3, 4, 1 λ = R H n n = 4, 5, 1 λ = R 1 H 4 1 n n = 5, 6, 1 λ = R H n n = 6, 7, Série de Lyman ultravioleta Série de Balmer ultravioleta próximo e visível Série de Paschen infravermelho Série de Bracket infravermelho Série de Pfund infravermelho
11 Átomos dos elementos alcalinos Li, Na, K, Fórmulas das séries tem mesmo formato geral 1 λ = R 1 m a 1 n b onde R = constante de Rydberg para o elemento considerado a e b = ctes. para a série observada m = inteiro fixo para a série observada n = inteiro variável
12 Espectros de emissão Elétrons colidem contra as moléculas de um gás Gás aquecido (excitado) emite luz em seus comprimentos de onda característicos Espectros de absorção Luz incide sobre o gás frio (normal) Gás absorve em comprimentos de onda característicos, deixando o restante passar Espectros de emissão versus de absorção Observa-se experimentalmente que todas as linhas (faltantes) do espectro de absorção aparecem no espectro de emissão, porém o contrário não ocorre: faltam linhas!!
13 Modelo do átomo de Thomson Modelo do pudim de ameixas (1904) Elétrons imersos na carga positiva Átomo no estado fundamental elétrons fixos em suas posições de equilíbrio Átomo no estado excitado elétrons vibram em torno de suas posições de equilíbrio Teoria do eletromagnetismo corpo carregado acelerado emite radiação modelo com elétron vibrando explica qualitativamente a emissão de radiação por átomos excitados falta concordância quantitativa Ex: átomo de hidrogênio F e = 1 q + q 4πε o r q + = ρv = ρ 4 3 πa3 q = e r = a F e = ρe 3ε o a = cte. a = mä oscilador harmônico πν = ω = cte m = ρ e 3ε o m
14 Elétron irá oscilar com frequência ν = 1 π ρ 3ε o e m Valor de e/m (Thomson); valor de e (Millikan) Valor de N A (n o de Avogadro) através de experimentos de eletrólise (Dalton) Valor de r A (raio atômico) a partir da densidade de um sólido, seu peso atômico e N A Átomo é neutro q + = +e ρ = e V = e 3 3 4πr ν = 1 A π Do eletromagnetismo 1 4πε o e r A 3 e m 1 4πε o = Nm C Substituindo, obtemos a frequência e o comprimento de onda da radiação emitida pelo átomo de hidrogênio ν =, s -1 λ = 1180 A Átomo de hidrogênio irradia apenas em uma frequência, no ultravioleta longínquo
15 Experimento de Rutherford Fonte de partículas : feixe paralelo e estreito (colimado por um diafragma) Alvo: folha muito fina de um metal (ouro) Feixe de partículas atravessa o alvo apenas diminui um pouco sua velocidade Partícula sofre deflexões ao atravessar a folha (força Coulombiana) partículas espalhadas grande parte das partículas não é defletida Deflexão da partícula depende dos detalhes da trajetória diferente para diferentes partículas do feixe feixe de partículas folha fina de ouro Feixe emergente divergente Medida da divergência medir o número de partículas espalhadas em cada região angular de a + d Detector camada de composto cristalino ZnS (produz pequena cintilação quando atingido por uma partícula ) microscópio (contagem das partículas) fonte de partículas tela fluorescente circular Partículas : átomo de hélio duplamente ionizado m α = 4m pr óton ; q α = e ; m pr óton = 1836 m elétron
16 Queremos calcular: N()d número de partículas espalhadas em um ângulo entre e + d Modelo de Thomson: elétrons em uma esfera de carga positiva elétrons de um átomo causam múltiplas delexões da partícula φ 1 deflexão quadrática média por um único átomo N átomos do alvo causam múltiplas deflexões da partícula θ 1 deflexão quadrática média total (espalhamento quadrático médio total) deflexão é aleatória θ 1 = N φ 1 N teoria estatística: N θ dθ = N 0 e θ θ dθ = Iθ θ (distribuição (random walk) θ e θ dθ Gaussiana)
17 Deflexão máxima no modelo de Thomson Momento da partícula antes e depois da deflexão Δp α = p αi sin φ Deflexão máxima max sofrida pela partícula ao interagir com o átomo será sin φ max = Δp α,max p αi Precisamos, portanto, calcular a fração de momento perdida durante a interação da partícula com o átomo: contribuição dos elétrons contribuição da carga positiva (uniformemente distribuída)
18 Contribuição dos elétrons em um átomo supondo colisão frontal antes da colisão E = m α v αi p = m α v αi depois da colisão E = m α v αf + m ev ef p = m α v αf + m e v ef conservação de energia e momento: m α v αi v ef = v αi v αf v ef v αi v αf = m α v αf + m ev ef m α v αi = m α v αf + m e v ef v ef = v αi + v αf m α m e m α m e v αi v αf = v ef v αi v αf = v ef m α m e v αi v αf = v ef = v αi + v αf v αi v αf = m e v m αi + v αf 0 v αi v αf v ef v αi α momento (velocidade) adquirido pelo corpo inicialmente em repouso é sempre máximo em uma colisão frontal v ef,max = v αi p ef,max = m e v αi perda máxima de momento da partícula por contribuição dos elétrons Δp α,max = m e v αi
19 Contribuição da carga positiva uniformemente distribuída em um átomo força que atua sobre a partícula devido ao elemento de carga dq df = 1 q α dq 4πε o r = 1 edq 4πε o r força total sobre a partícula devido à carga positiva F = df = e 4πε o força máxima que atua sobre a partícula devido à carga positiva de um átomo F max = 1 4πε o e Z r A perda de momento da partícula dependerá do tempo de interação t Δp α = FΔt tempo de interação máximo tempo máximo em que a partícula permanece dentro do átomo Δt max = r A v αi dq r e Q 4πε o r = A ( ) v αi v αf e Ze 4πε o r A perda máxima de momento da partícula por contribuição da carga positiva Δp α,max = F max Δt max = 1 4πε o e Z r A v αi
20 Calculando as duas contribuições 1 = Nm 4πε o C r A = m K α = 5 MeV = , J (típico) Z 100 metal típico e = 1, C m e = 1 m e = 1 1 m α 4 m p perda máxima de momento da partícula por contribuição da carga positiva Δp α,max = F max Δt max = 1 e Z 4πε o r A v αi sin φ max = Δp α,max = 1 e Z p αi 4πε o r A m α v = 1 e Z 1 = φ αi 4πε o r A K max = rad αi perda máxima de momento da partícula por contribuição dos elétrons Δp α,max = m e v αi sin φ max = Δp α,max p αi = m ev αi m α v αi = m e m α = φ max = rad ângulo de deflexão máximo de uma partícula ao passar por um átomo φ max ~10 4 rad
21 Calculando a deflexão máxima devido a vários átomos θ 1 = N φ 1 Supondo folha de expessura 10-4 cm (diâmetro do átomo.r A =.10-8 cm) N = 0, átomos N 10 átomos φ 1 φ max 10 4 rad N θ dθ I = θ θ e θ θ dθ = θe θ.10 4 θ 1 10 rad 1 ângulo médio do espalhamento é θ 1 1 para 0 equação reproduz bem os resultados experimentais para = (90 ) equação N θ = π I observado experimentalmente = πe π N θ = π I Modelo de Thomson não explica o espalhamento!!! 10 4
22 Modelo do átomo de Rutherford Modelo planetário (1911) Todas as cargas positivas estão concentradas em uma pequena região (núcleo) Contribuição dos elétrons ao espalhamento pode ser desprezada ( φ max ~10 4 rad ) Alvo de folha metálica (átomos pesados) massa do núcleo é muito maior doque das partículas núcleo permanece fixo durante o espalhamento Partículas não penetram na região nuclear partículas e núcleo são cargas puntuais repulsão Coulombiana Velocidade das partículas : v c /0 mecânica não relativística
23 Espalhamento da partícula pelo núcleo puntual pesado
24 Energia nos extremos (- e +) K = m iv 0 K + = m iv 0 Momento angular L = r p nos extremos (- e +) r = rx + by p = m i v 0 x L = m i v 0 b L + = m i v 0 b Conservação de energia m i v 0 = m iv 0 v 0 = v 0 Conservação do momento angular m i bv 0 = m i b v 0 b = b
25 Queremos calcular: N()d número de partículas que defletem com um ângulo entre e + d Estratégia Analisar o espalhamento de uma partícula com parâmetro de impacto entre b e b + db Essa partícula será espalhada entre e + d Usando a Lei de Coulomb, a equação para o momento angular e a Lei de Newton, encontrar uma relação entre b e Observar que, pela simetria, teremos um anel de impacto de área da = bdb Supor que a folha metálica seja fina o suficiente, de forma que uma partícula seja defletida apenas por um átomo ao atravessá-la em uma folha de área a e expessura t o número de átomos em um volume V = at da folha será igual ao número de anéis de área da na área a da folha Calcular o número de anéis de área da, e a probabilidade P(b)db de ocorrer um impacto entre uma partícula e um núcleo Obter a probabilidade P()d de ocorrer um impacto entre uma partícula e núcleo Para um feixe de I partículas, obter o número de partículas defletidas com um ângulo entre e + d
26 Força de repulsão Coulombiana entre partícula e núcleo em qualquer instante de tempo t F = 1 zze 4πε 0 r r = 1 zze 4πε 0 r cos φ x + sin φ y F y = 1 zze 4πε 0 r sin φ (precisamos encontrar r ) Momento linear da partícula em qualquer instante de tempo t p = m i v = m i v r r + v t θ = m dr dφ i r + r dt dt θ Momento angular da partícula em qualquer instante de tempo t L = r p = m i r dr dφ r + r dt dt θ = m ir dφ dt 1 r = m i dφ L dt = 1 dφ v 0 b dt r θ Substituindo na força F y = 1 zze dφ sin φ 4πε 0 v 0 b dt
27 Usando a ª Lei de Newton F y = m i dv y dt dv y dt = 1 zze dφ sin φ 4πε 0 m i v 0 b dt dv y = 1 zze sin φ dφ 4πε 0 m i v 0 b Integrando sobre todo o espaço limites v y = 0 φ = 0 v y + = v 0 sin θ φ + = 180 θ v 0 sin θ 0 dv y = 1 4πε 0 zze m i v 0 b 180 θ 0 sin φ dφ v 0 sin θ = 1 4πε 0 zze m i v 0 b cos 180 θ + cos 0 v 0 = 1 4πε 0 zze m i v 0 b 1 + cos θ sin θ 1 + cos θ sin θ = 4πε 0 m i v 0 b zze
28 Usando as relações trigonométricas cos θ = cos θ sin θ sin θ = sin θ cos θ 1 + cos θ sin θ = cos θ sin θ = cot θ Substituindo cot θ = 4πε 0 m i v 0 b zze Lembrando que a energia cinética do feixe de partículas é dada por K feixe = E = m iv 0 Substituindo, encontramos a relação entre b e cot θ = 8πε 0 K feixe zze b
29 Considerando o caso da colisão frontal, sendo D a distância de maior aproximação ao núcleo Conservação de energia E = K feixe = m iv 0 E D = E elec D = 1 zze 4πε 0 D K feixe = m iv 0 = 1 zze 4πε 0 D D = 1 4πε 0 zze K feixe = 1 4πε 0 zze m i v 0 Reescrevendo a relação entre b e em função de D cot θ = b D onde D = 1 4πε 0 zze K feixe
30 Uma partícula que incide com um parâmetro de impacto entre b e b + db será espalhada entre e + d Por simetria, teremos um anel de impacto, levando a um anel de espalhamento
31 Folha metálica (alvo) expessura t área A = mn volume V = At densidade atômica Considerando que a folha é muito fina uma partícula é defletida apenas por um átomo Área do anel de impacto da = πbdb Número de anéis de área da = Número de átomos n a n a = ρv = ρmnt Probabilidade de ocorrer o impacto de uma partícula P b db = número de anéis área do anel área da folha = n ada A P b db = πρt bdb
32 Substituindo a equação de b encontrada anteriormente cos θ b = D cot θ = D sin θ db = D 1 4 sin θ dθ P b db = πρt D cos θ sin θ D 1 4 sin θ dθ = πρtd 4 cos θ sin 3 θ dθ Reescrevendo a equação, usando a relação trigonométrica cos θ = cos θ sin θ sin θ = sin θ cos θ cos θ sin θ = cos θ sin θ cos θ = sin θ cos θ sin 3 θ = cos θ sin θ sin 4 θ sin θ = sin 4 θ P b db = πρtd 8 sin θ sin 4 θ dθ
33 Conforme b aumenta, diminui P b db = P θ dθ P θ dθ = πρtd 8 sin θ sin 4 θ dθ Essa é a probabilidade de que uma partícula seja defletida entre e + d Mas a radiação possui I partículas Portanto, o número de partículas que sofrem uma deflexão entre e + d será N θ dθ = IP θ dθ N θ dθ I = πρtd 8 sin θ sin 4 θ dθ Comparando Thomson e Rutherford Rutherford N θ I sin θ sin 4 θ N θ = 5 N θ = 1 ~10 3 Thomson N θ I θe θ.10 4 N θ = 5 N θ = 1 ~10 31 Espalhamento com o ângulo decresce muito mais rapidamente no modelo de Thomson!!!
34 Geiger e Marsden (1911): testam a equação obtida por Rutherford em uma série de experimentos dependência com, t e K feixe são plenamente satisfeitas Modelo de Rutherford: fornece um limite para o tamanho do núcleo, desde que não ocorra penetração na região nuclear da partícula Z grande r nucleo D = 1 4πε 0 zze K feixe Para átomos com Z pequeno, divergências experimentais mostram que ocorre penetração nuclear da partícula Modelo de Rutherford deixa de funcionar Falhas do Modelo de Rutherford Partículas carregadas e aceleradas emitem radiação e perdem energia elétron deveria espiralar e colapsar com o núcleo A energia irradiada nesse processo deve ser um contínuo não explica os espectros atômicos (linhas - discreto)
35 Principal diferença entre os Modelos de Thomson e de Rutherford Modelo de Thomson elétrons em uma esfera de carga positiva maioria das partículas não é defletida algumas partículas são levemente defletida pelos elétrons Modelo de Rutherford elétrons em torno de uma carga positiva central e puntual, de grande massa maioria das partículas não é defletida algumas partículas são levemente defletida pelos elétrons e pelo núcleo algumas partículas serão fortemente defletida pelo núcleo
36 Modelo do átomo de Bohr Postulados (1915) explicam os resultados experimentais! i. Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) segundo as leis clássicas do movimento implica na existência do núcleo atômico ii. iii. iv. Elétron só pode se mover em uma órbita na qual seu momento angular L é um múltiplo inteiro de ( = h/) L = nħ = n h n = 1,, 3, π quantiza o momento angular Apesar de constantemente acelerado, o elétron que se move em uma dessas órbitas estáveis não emite radiação eletromagnética energia E permanece constante elimina o problema da instabilidade Elétron emite radiação ao mudar, de forma descontínua, de uma órbita estável (E i ) para outra órbita estável (E f ) a radiação emitida terá frequência ν = E i E f h se baseia no postulado de Einstein ( ) E = hν
37 Analisando os postulados com mais detalhes i. ii. F Coulomb = F centr ípeta 1 eze 4πε 0 r = mv r L = mvr = 1 4πε 0 mze r L = nħ n = 1,, 3, L = nħ = 1 mze r 4πε 0 r = 4πε 0ħ mze n n = 1,, 3, L = Lmvr = 1 4πε 0 mze r nħv = 1 4πε 0 Ze órbita estável define o raio das órbitas estáveis (estados estacionários) v = 1 Ze 1 4πε 0 ħ n n = 1,, 3, define a velocidade do elétron nas órbitas estáveis
38 iii. E = K + V V = 1 Ze 4πε 0 r K = mv = 1 Ze 4πε 0 r E = 1 Ze 4πε 0 r E = 1 Ze 4πε 0 ħ m 1 n n = 1,, 3, define a energia das órbitas estáveis iv. ν = E i E f h ν = 1 πħ = E i E f πħ 1 Ze 4πε 0 ħ m 1 n i 1 n f definindo a constante: R = me4 1 4πcħ 3 4πε 0 ν = cr Z 1 n f 1 n i n = 1,, 3, define a frequência da radiação emitida k = ν c = R Z 1 n f 1 n i n = 1,, 3, define o número de onda da radiação emitida
39 Para o átomo de Hidrogênio (Z = 1) em seu estado fundamental (n = 1) Raio atômico r = 4πε 0ħ me = 0,53 A Velocidade do elétron v = 1 4πε 0 e ħ =, m/s Energia E = 1 e 4πε 0 ħ m =, J = 13,6 ev Transições no átomo de Hidrogênio (Z = 1) para n f = k = 1 λ = R 1 1 n i n i = 3, 4, 5, Série de Balmer, caso R = R H cálculos conferem o resultado!
40 Espectros de absorção átomo de Hidrogênio Átomo está inicialmente no estado fundamental Ao incidir radiação, os fótons contendo energia hν = E f E i serão absorvidos Ocorrerão transições eletrônicas, porém sempre com n i = 1 Somente as linhas da Série de Lyman serão observadas Espectros de emissão átomo de Hidrogênio Átomo é irradiado, passando a estados excitados Ao retornar ao estado fundamental, poderão ocorrer transições eletrônicas para as órbitas intermediárias permitidas Ocorrerão transições, com n i > 1 e n f 1 Todas as Séries (Lyman, Balmer, Paschen, Bracket, Pfund,...) podem ser observadas Modelo de Bohr explica as diferenças observadas entre espectros de absorção e de emissão!
41 Espectros de absorção para um gás de Hidrogênio em alta temperatura Devido a colisões internas, alguns átomos podem passar ao estado excitado n i = Série de Balmer, além da Série de Lyman, poderá ser observada Estimando a população de átomos no 1 o estado excitado distribuição de Boltzmann n 1 = e E 1 KT n e E = e E1 E KT KT onde K = 1, J/K = cte. de Boltzmann Energia do estado fundamental Energia do 1 o estado excitado E 1 = 1 e 4πε 0 ħ E = 1 e 4πε 0 ħ E 1 E = 1, K K n Supondo gás a T = K = 0,31 31% dos átomos estarão no 1 o estado excitado n Linhas da Série de Balmer serão observadas m m 1 1 =, J 1 = 0, J Aplicação: estimar a temperatura na superfície de estrelas (atmosferas estrelares)
42 Interpretação das regras de quantização Modelo de Bohr concordância experimental Postulados de Bohr natureza misteriosa Quantização grande mistério!! Bohr: quantização do momento angular do elétron se movendo em trajetória circular ao redor do núcleo Planck: quantização para a energia total de um ente (por ex. elétron realizando MHS) Regras de Quantização de Wilson e Sommerfeld (1916) Conjunto de regras para a quantização de qualquer sistema físico para o qual as coordenadas são funções periódicas no tempo Incluem quantização de Bohr e Planck como casos especiais Interpretação de de Broglie (194) L = nħ = nh π (Bohr) L = mvr = pr = h πr = nλ n = 1,, 3, (de Broglie) λ r As órbitas possíveis são aquelas nas quais a circunferência da órbita pode conter exatamente um número inteiro de comprimentos de onda de de Broglie
43 Crítica à antiga teoria quântica Bem sucedida explica Efeito fotoelétrico Radiação de corpo negro Efeito Compton Calor específico em sólidos a baixas temperaturas Espectros do átomo de hidrogênio (inclusive estrutura fina) Espectros de átomos dos elementos alcalinos (similares ao 1 H: átomos de 1 elétron) Falhas NÃO pode ser aplicada a átomos com mais de 1 elétron nem mesmo para o segundo átomo mais simples: o hélio NÃO fornece infos sobre a intensidade das linhas nos espectros SOMENTE pode ser aplicada a sistemas periódicos, e existem MUITOS sistemas físicos interessantes que NÃO SÃO periódicos
HISTÓRIA DA MATÉRIA. Leucipo e Demócretes (V a.c.) Aristóteles (III a.c.)
 HISTÓRIA DA MATÉRIA Leucipo e Demócretes (V a.c.) Tudo que existe é composto de elementos indivisíveis Átomo a = negação; tomo = divisível Entidades discretas, infinitamente duras, não modificáveis, eternas
HISTÓRIA DA MATÉRIA Leucipo e Demócretes (V a.c.) Tudo que existe é composto de elementos indivisíveis Átomo a = negação; tomo = divisível Entidades discretas, infinitamente duras, não modificáveis, eternas
Uma breve história do mundo dos quanta. Érica Polycarpo Equipe de Física Coordenação: Prof. Marta Barroso
 Uma breve história do mundo dos Érica Polycarpo Equipe de Física Coordenação: Prof. Marta Barroso Tópicos da Terceira Aula Espectros atômicos Evolução dos modelos atômicos Thomson Rutherford Bohr Princípio
Uma breve história do mundo dos Érica Polycarpo Equipe de Física Coordenação: Prof. Marta Barroso Tópicos da Terceira Aula Espectros atômicos Evolução dos modelos atômicos Thomson Rutherford Bohr Princípio
A natureza corpuscular da matéria
 A natureza corpuscular da matéria Vimos as evidências da natureza corpuscular da radiação: quantização dos osciladores Planck quantização da luz Einstein fótons como partículas Compton Evidências da natureza
A natureza corpuscular da matéria Vimos as evidências da natureza corpuscular da radiação: quantização dos osciladores Planck quantização da luz Einstein fótons como partículas Compton Evidências da natureza
Prof. Dr. Lucas Barboza Sarno da Silva
 Prof. Dr. Lucas Barboza Sarno da Silva O Efeito Compton Einstein, em 1919, concluiu que um fóton de energia E se desloca em uma única direção (diferentemente de uma onda esférica) e é portador de um momento
Prof. Dr. Lucas Barboza Sarno da Silva O Efeito Compton Einstein, em 1919, concluiu que um fóton de energia E se desloca em uma única direção (diferentemente de uma onda esférica) e é portador de um momento
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 4 MODELOS ATÔMICOS Primeira Edição junho de 2005 CAPÍTULO 4 MODELOS ATÔMICOS ÍNDICE 4.1- Modelo de Thomson 4.2- Modelo de Rutherford 4.2.1-
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 4 MODELOS ATÔMICOS Primeira Edição junho de 2005 CAPÍTULO 4 MODELOS ATÔMICOS ÍNDICE 4.1- Modelo de Thomson 4.2- Modelo de Rutherford 4.2.1-
Prof. Dr. Lucas Barboza Sarno da Silva
 Prof. Dr. Lucas Barboza Sarno da Silva Espectros atômicos Toda substância a uma certa temperatura emite radiação térmica, caracterizada por uma distribuição contínua de comprimentos de onda. A forma da
Prof. Dr. Lucas Barboza Sarno da Silva Espectros atômicos Toda substância a uma certa temperatura emite radiação térmica, caracterizada por uma distribuição contínua de comprimentos de onda. A forma da
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 MODELOS ATÔMICOS E A VELHA TEORIA QUÂNTICA Edição de junho de 2014 CAPÍTULO 3 MODELOS ATÔMICOS E A VELHA TEORIA QUÂNTICA ÍNDICE 3.1-
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 MODELOS ATÔMICOS E A VELHA TEORIA QUÂNTICA Edição de junho de 2014 CAPÍTULO 3 MODELOS ATÔMICOS E A VELHA TEORIA QUÂNTICA ÍNDICE 3.1-
ONDAS ELETROMAGNÉTICAS ÁTOMO DE BOHR. QFL-4010 Prof. Gianluca C. Azzellini
 ONDAS ELETROMAGNÉTICAS ÁTOMO DE BOHR Ondas Eletromagnéticas ONDAS ELETROMAGNÉTICAS ASPECTOS GERAIS A= amplitude (m) λ= comprimento de onda (m) ν= frequência (Hz= s -1 ) c= velocidade da luz=,998x10 8
ONDAS ELETROMAGNÉTICAS ÁTOMO DE BOHR Ondas Eletromagnéticas ONDAS ELETROMAGNÉTICAS ASPECTOS GERAIS A= amplitude (m) λ= comprimento de onda (m) ν= frequência (Hz= s -1 ) c= velocidade da luz=,998x10 8
5. Modelo atômico de Bohr
 5. Modelo atômico de Bohr Sumário Espectros atômicos Modelo de Bohr para o átomo de hidrogênio Níveis de energia e raias espectrais Experiência de Franck-Hertz O princípio da correspondência Correção do
5. Modelo atômico de Bohr Sumário Espectros atômicos Modelo de Bohr para o átomo de hidrogênio Níveis de energia e raias espectrais Experiência de Franck-Hertz O princípio da correspondência Correção do
Modelos Atômicos. Eisberg (cap. 4) e Tipler (cap. 4)
 P2 no dia 15-MAI Modelos Atômicos Eisberg (cap. 4) e Tipler (cap. 4) Perguntas 1. Do que os átomos são constituídos? 2. Qual o tamanho típico do átomo? 3. Como os constituintes se distribuem? Um pouco
P2 no dia 15-MAI Modelos Atômicos Eisberg (cap. 4) e Tipler (cap. 4) Perguntas 1. Do que os átomos são constituídos? 2. Qual o tamanho típico do átomo? 3. Como os constituintes se distribuem? Um pouco
Universidade Federal do Rio de Janeiro Instituto de Física Física IV 2019/1 Lista de Exercícios do Capítulo 5 Origens da Teoria Quântica
 Universidade Federal do Rio de Janeiro Instituto de Física Física IV 2019/1 Lista de Exercícios do Capítulo 5 Origens da Teoria Quântica 1) Calcule a energia de um quantum de luz de comprimento de onda
Universidade Federal do Rio de Janeiro Instituto de Física Física IV 2019/1 Lista de Exercícios do Capítulo 5 Origens da Teoria Quântica 1) Calcule a energia de um quantum de luz de comprimento de onda
Laboratório de Física Moderna Espectrosocopia Aula 01. Marcelo Gameiro Munhoz
 Laboratório de Física Moderna Espectrosocopia Aula 01 Marcelo Gameiro Munhoz munhoz@if.usp.br 1 Contextualização Para iniciar nosso experimento, vamos compreender o contexto que o cerca Qual o tipo de
Laboratório de Física Moderna Espectrosocopia Aula 01 Marcelo Gameiro Munhoz munhoz@if.usp.br 1 Contextualização Para iniciar nosso experimento, vamos compreender o contexto que o cerca Qual o tipo de
TEORIAS ATÔMICAS. Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807)
 TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
RAIOS-X (RAIOS RÖNTGEN)
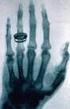 RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
RAIOS-X (RAIOS RÖNTGEN)
 RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
Sumário. O átomo de H e a estrutura atómica
 Sumário Das Estrelas ao átomo Unidade temática 1 O átomo de hidrogénio e a estrutura atómica. Quantização de energia. : De Dalton ao modelo quântico. APSA 6 Espectro atómico do átomo de hidrogénio. Porque
Sumário Das Estrelas ao átomo Unidade temática 1 O átomo de hidrogénio e a estrutura atómica. Quantização de energia. : De Dalton ao modelo quântico. APSA 6 Espectro atómico do átomo de hidrogénio. Porque
Laboratório de Física Moderna Espectroscopia do H. Marcelo Gameiro Munhoz
 Laboratório de Física Moderna Espectroscopia do H Marcelo Gameiro Munhoz munhoz@if.usp.br 1 Contextualização Para iniciar nosso experimento, vamos compreender o contexto que o cerca Qual o tipo de fenômeno
Laboratório de Física Moderna Espectroscopia do H Marcelo Gameiro Munhoz munhoz@if.usp.br 1 Contextualização Para iniciar nosso experimento, vamos compreender o contexto que o cerca Qual o tipo de fenômeno
Principais Postulados de Dalton (1803)
 Teoria Atômica da Matéria Breve Histórico Leucipo e Demócrito ( 400 a.c.) descontinuidade da matéria (átomo). Alquimia ( 300 a.c. 1500 d.c.) civilizações árabes e gregas. Paracelsus ( 1500 d.c.) Iatroquímica.
Teoria Atômica da Matéria Breve Histórico Leucipo e Demócrito ( 400 a.c.) descontinuidade da matéria (átomo). Alquimia ( 300 a.c. 1500 d.c.) civilizações árabes e gregas. Paracelsus ( 1500 d.c.) Iatroquímica.
MODELOS ATÔMICOS BIK0102: ESTRUTURA DA MATÉRIA. Professor Hugo Barbosa Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace MODELOS ATÔMICOS Professor Hugo Barbosa Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Ondas (uma breve revisão...) Uma onda é uma perturbação
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace MODELOS ATÔMICOS Professor Hugo Barbosa Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Ondas (uma breve revisão...) Uma onda é uma perturbação
FÍSICA MODERNA I AULA 08
 Universidade de São Paulo Instituto de Física FÍSICA MODERNA I AULA 08 Profa. Márcia de Almeida Rizzutto Pelletron sala 4 rizzutto@if.usp.br o. Semestre de 04 Monitor: Gabriel M. de Souza Santos Página
Universidade de São Paulo Instituto de Física FÍSICA MODERNA I AULA 08 Profa. Márcia de Almeida Rizzutto Pelletron sala 4 rizzutto@if.usp.br o. Semestre de 04 Monitor: Gabriel M. de Souza Santos Página
Ciências Exatas UFPR Palotina
 Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula 3 Teoria Atômica, Massas Atômicas e Moleculares e Íons Prof. Isac G. Rosset Ciências Exatas UFPR Palotina Prof. Isac G. Rosset
Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula 3 Teoria Atômica, Massas Atômicas e Moleculares e Íons Prof. Isac G. Rosset Ciências Exatas UFPR Palotina Prof. Isac G. Rosset
Principais modelos atômicos. Principais modelos atômicos Modelo Atômico de Rutherford (1911)
 Principais modelos atômicos Modelo Atômico de Thomson (898) Com a descoberta dos prótons e elétrons, Thomson propôs um modelo de átomo no qual os elétrons e os prótons, estariam uniformemente distribuídos,
Principais modelos atômicos Modelo Atômico de Thomson (898) Com a descoberta dos prótons e elétrons, Thomson propôs um modelo de átomo no qual os elétrons e os prótons, estariam uniformemente distribuídos,
Prof. Dr. Lucas Barboza Sarno da Silva
 Prof. Dr. Lucas Barboza Sarno da Silva O Efeito Compton Einstein, em 1919, concluiu que um fóton de energia E se desloca em uma única direção (diferentemente de uma onda esférica) e é portador de um momento
Prof. Dr. Lucas Barboza Sarno da Silva O Efeito Compton Einstein, em 1919, concluiu que um fóton de energia E se desloca em uma única direção (diferentemente de uma onda esférica) e é portador de um momento
ELÉTRONS EM ÁTOMOS. Depois do modelo de Rutherford: Como é o comportamento dos elétrons nos átomos? Rutherford: estrutura planetária, com o
 ELÉTRONS EM ÁTOMOS Depois do modelo de Rutherford: Como é o comportamento dos elétrons nos átomos? Rutherford: estrutura planetária, com o núcleo correspondendo ao sol no nosso sistema solar e os elétrons
ELÉTRONS EM ÁTOMOS Depois do modelo de Rutherford: Como é o comportamento dos elétrons nos átomos? Rutherford: estrutura planetária, com o núcleo correspondendo ao sol no nosso sistema solar e os elétrons
O Efeito Fotoelétrico
 O Efeito Fotoelétrico O efeito fotoelétrico é a emissão de elétrons por um material, geralmente metálico, quando exposto a uma radiação eletromagnética (como a luz) suficientemente energética, ou seja,
O Efeito Fotoelétrico O efeito fotoelétrico é a emissão de elétrons por um material, geralmente metálico, quando exposto a uma radiação eletromagnética (como a luz) suficientemente energética, ou seja,
Valter L. Líbero EFC
 Valter L. Líbero EFC - 2012 1- Teoria Atômica 2- Interação Matéria Radiação 3- Relatividade Referências: Tipler e Llewellyn J. P. McEvoy E Oscar Zarate O Conceito de Átomo Demócrito (o grego), 450 ac:
Valter L. Líbero EFC - 2012 1- Teoria Atômica 2- Interação Matéria Radiação 3- Relatividade Referências: Tipler e Llewellyn J. P. McEvoy E Oscar Zarate O Conceito de Átomo Demócrito (o grego), 450 ac:
Radiação térmica e a hipótese de Planck
 Radiação térmica e a hipótese de Planck o que é radiação térmica e como é medida (radiância, radiância espectral,...); Lei de Kirchhoff para a radiação (taxas de emissão e de absorção): E v A v = J(v,T
Radiação térmica e a hipótese de Planck o que é radiação térmica e como é medida (radiância, radiância espectral,...); Lei de Kirchhoff para a radiação (taxas de emissão e de absorção): E v A v = J(v,T
QUÍMICA I. Teoria atômica Capítulo 6. Aula 2
 QUÍMICA I Teoria atômica Capítulo 6 Aula 2 Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com a matéria. A radiação eletromagnética se movimenta
QUÍMICA I Teoria atômica Capítulo 6 Aula 2 Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com a matéria. A radiação eletromagnética se movimenta
O átomo de Rutherford
 O átomo de Rutherford ~10-14 m Núcleo de carga +Ze rodeado por Z elétrons (modelo planetário). Z é chamado número atômico (H: Z = 1, He: Z = 2, etc.). O número atômico determina as propriedades físicas
O átomo de Rutherford ~10-14 m Núcleo de carga +Ze rodeado por Z elétrons (modelo planetário). Z é chamado número atômico (H: Z = 1, He: Z = 2, etc.). O número atômico determina as propriedades físicas
Física 4. Guia de Estudos P2
 Física 4 Guia de Estudos P2 1. Efeito Doppler relativístico O efeito Doppler relativístico é a aparente mudança de frequência da onda eletromagnética quando há movimento relativo entre fonte e observador.
Física 4 Guia de Estudos P2 1. Efeito Doppler relativístico O efeito Doppler relativístico é a aparente mudança de frequência da onda eletromagnética quando há movimento relativo entre fonte e observador.
Instituto de Física USP. Física Moderna I. Aula 15. Professora: Mazé Bechara
 Instituto de Física USP Física Moderna I Aula 15 Professora: Mazé Bechara Aula 15 Espectros de linhas e o Modelo atômico de Thomson. O experimento de Rutherford - 1911 1. Características dos espectros
Instituto de Física USP Física Moderna I Aula 15 Professora: Mazé Bechara Aula 15 Espectros de linhas e o Modelo atômico de Thomson. O experimento de Rutherford - 1911 1. Características dos espectros
Modelos atômicos Professor: Hugo Cesário
 Modelos atômicos Professor: Hugo Cesário Átomo/Filosofia Filosofia Tales de Mileto (600 a.c.) Do que tudo é feito? água Empédocles (450 a.c.) Quatro raízes Raízes unidas pelo amor e separadas pela discórdia
Modelos atômicos Professor: Hugo Cesário Átomo/Filosofia Filosofia Tales de Mileto (600 a.c.) Do que tudo é feito? água Empédocles (450 a.c.) Quatro raízes Raízes unidas pelo amor e separadas pela discórdia
Estrutura eletrônica da matéria - resumo
 Estrutura eletrônica da matéria - resumo A NATUREZA ONDULATÓRIA DA LUZ COMO A RADIAÇÃO ELETROMAGNÉTICA SE MOVE À VELOCIDADE DA LUZ, O COMPRIMENTO DE ONDA E A FREQUÊNCIA ESTÃO RELACIONADOS: νλ=c ONDE ν(ni)
Estrutura eletrônica da matéria - resumo A NATUREZA ONDULATÓRIA DA LUZ COMO A RADIAÇÃO ELETROMAGNÉTICA SE MOVE À VELOCIDADE DA LUZ, O COMPRIMENTO DE ONDA E A FREQUÊNCIA ESTÃO RELACIONADOS: νλ=c ONDE ν(ni)
Universidade Federal do Tocantins
 Universidade Federal do Tocantins Modelos atômicos Prof. Dr. Edenilson dos Santos Niculau enicolau@uft.edu.br Blog: profedenilsonniculau.wordpress.com 2 Sumário MODELOS ATÔMICOS Estrutura atômica Teoria
Universidade Federal do Tocantins Modelos atômicos Prof. Dr. Edenilson dos Santos Niculau enicolau@uft.edu.br Blog: profedenilsonniculau.wordpress.com 2 Sumário MODELOS ATÔMICOS Estrutura atômica Teoria
MODELOS ATÔMICOS BIK0102: ESTRUTURA DA MATÉRIA. Professor Hugo Barbosa Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace MODELOS ATÔMICOS Professor Hugo Barbosa Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Ondas (uma breve revisão...) Uma onda é uma perturbação
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace MODELOS ATÔMICOS Professor Hugo Barbosa Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Ondas (uma breve revisão...) Uma onda é uma perturbação
Modelos atômicos (quânticos) Bohr Sommerfeld Professor: Hugo Cesário
 Modelos atômicos (quânticos) Bohr Sommerfeld Professor: Hugo Cesário Rutherford Niels Bohr Max Planck Sommerfeld Modelos atômicos quânticos Problemas de Rutherford: Modelo entrou em choque com os conceitos
Modelos atômicos (quânticos) Bohr Sommerfeld Professor: Hugo Cesário Rutherford Niels Bohr Max Planck Sommerfeld Modelos atômicos quânticos Problemas de Rutherford: Modelo entrou em choque com os conceitos
Instituto de Física USP. Física V - Aula 15. Professora: Mazé Bechara
 Instituto de Física USP Física V - Aula 15 Professora: Mazé Bechara Aula 15 Espectros de absorção e emissão atômica e modelo atômico de Thomson. 1. Evidências experimentais da existência de estrutura nos
Instituto de Física USP Física V - Aula 15 Professora: Mazé Bechara Aula 15 Espectros de absorção e emissão atômica e modelo atômico de Thomson. 1. Evidências experimentais da existência de estrutura nos
Física Moderna I Aula 09. Marcelo G Munhoz Edifício HEPIC, sala 202, ramal
 Física Moderna I Aula 09 Marcelo G Munhoz Edifício HEPIC, sala 202, ramal 916940 munhoz@if.usp.br 1 Estabilidade do átomo proposto por Rutherford Este modelo proposto por Rutherford tinha um sério problema
Física Moderna I Aula 09 Marcelo G Munhoz Edifício HEPIC, sala 202, ramal 916940 munhoz@if.usp.br 1 Estabilidade do átomo proposto por Rutherford Este modelo proposto por Rutherford tinha um sério problema
2. A ORIGEM DA CONSTANTE DE NEGRO
 QUANTIZAÇÃO . INTRODUÇÃO O No final do século XIX acreditava-se, em geral, que todos os fenômenos naturais poderiam ser descritos mediante: Leis de Newton, Leis da Termodinâmica, e Leis do Eletromagnetismo.
QUANTIZAÇÃO . INTRODUÇÃO O No final do século XIX acreditava-se, em geral, que todos os fenômenos naturais poderiam ser descritos mediante: Leis de Newton, Leis da Termodinâmica, e Leis do Eletromagnetismo.
ESTRUTURA ATÔMICA DA MATÉRIA (PARTE 3 MODELOS ATÔMICOS)
 01. Gregos (Demócrito e Leucipo) "A matéria é formada de pequenas partículas indivisíveis denominadas átomos." (a = não tomo = parte) QUÍMICA INORGÂNICA - CAPÍTULO 2 ESTRUTURA ATÔMICA DA MATÉRIA (PARTE
01. Gregos (Demócrito e Leucipo) "A matéria é formada de pequenas partículas indivisíveis denominadas átomos." (a = não tomo = parte) QUÍMICA INORGÂNICA - CAPÍTULO 2 ESTRUTURA ATÔMICA DA MATÉRIA (PARTE
Quantização. Quantização da energia (Planck, 1900) hc h. Efeito fotoelétrico (Einstein, 1905) Espectros atômicos (linhas discretas) v 2
 Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
Distribuição da radiação* ESPECTRO
 ESPECTROSCOPIA intensidade INFORMAÇÃO Distribuição da radiação* ESPECTRO Através do espectro de um objeto astronômico pode-se conhecer informações sobre temperatura, pressão, densidade, composição química,
ESPECTROSCOPIA intensidade INFORMAÇÃO Distribuição da radiação* ESPECTRO Através do espectro de um objeto astronômico pode-se conhecer informações sobre temperatura, pressão, densidade, composição química,
MODELO ATÔMICO: DO SIMPLES AO ELABORADO UMA TENTATIVA DE DESVENDAR OS MISTÉRIOS DA MATÉRIA
 MODELO ATÔMICO: DO SIMPLES AO ELABORADO UMA TENTATIVA DE DESVENDAR OS MISTÉRIOS DA MATÉRIA Leucipo Demócrito Epicuro (de 400-250 a.c): a matéria seria constituída de átomos e espaços vazios; Aristóteles
MODELO ATÔMICO: DO SIMPLES AO ELABORADO UMA TENTATIVA DE DESVENDAR OS MISTÉRIOS DA MATÉRIA Leucipo Demócrito Epicuro (de 400-250 a.c): a matéria seria constituída de átomos e espaços vazios; Aristóteles
Sumário. O átomo de H e a estrutura atómica
 Sumário Das Estrelas ao átomo Unidade temática 1 O átomo de hidrogénio e a estrutura atómica. Quantização de energia. APSA 6 Espectro atómico do átomo de hidrogénio. Porque é que o espectro do átomo de
Sumário Das Estrelas ao átomo Unidade temática 1 O átomo de hidrogénio e a estrutura atómica. Quantização de energia. APSA 6 Espectro atómico do átomo de hidrogénio. Porque é que o espectro do átomo de
Tubos de Crookes e a descoberta do elétron
 Tubos de Crookes e a descoberta do elétron (A) Efeito de um obstáculo no caminho dos raios catódicos. Raios Catódicos High voltage source of high voltage shadow Resultados independem do gás usado para
Tubos de Crookes e a descoberta do elétron (A) Efeito de um obstáculo no caminho dos raios catódicos. Raios Catódicos High voltage source of high voltage shadow Resultados independem do gás usado para
Aula 3. Espectros atômicos e modelo atômico de Rutherford. UFABC - Física Quântica - Curso Prof. Germán Lugones
 UFABC - Física Quântica - Curso 2017.3 Prof. Germán Lugones Aula 3 Espectros atômicos e modelo atômico de Rutherford Uma versão de alta resolução do espectro do nosso Sol. Cada uma das 50 faixas cobre
UFABC - Física Quântica - Curso 2017.3 Prof. Germán Lugones Aula 3 Espectros atômicos e modelo atômico de Rutherford Uma versão de alta resolução do espectro do nosso Sol. Cada uma das 50 faixas cobre
Uma breve história do mundo dos quanta. Érica Polycarpo Equipe de Física Coordenação: Prof. Marta Barroso
 Uma breve história do mundo dos Érica Polycarpo Equipe de Física Coordenação: Prof. Marta Barroso Tópicos da Segunda Aula Abordagem histórica Radiação de corpo negro Efeito fotoelétrico Espalhamento Compton
Uma breve história do mundo dos Érica Polycarpo Equipe de Física Coordenação: Prof. Marta Barroso Tópicos da Segunda Aula Abordagem histórica Radiação de corpo negro Efeito fotoelétrico Espalhamento Compton
UFABC - Física Quântica - Curso Prof. Germán Lugones. Aula 4. O modelo atômico de Bohr
 UFABC - Física Quântica - Curso 2017.3 Prof. Germán Lugones Aula 4 O modelo atômico de Bohr 1 O modelo de Bohr Em 1913, Niels Bohr propôs um modelo do átomo de hidrogênio que combinava o trabalho de Planck,
UFABC - Física Quântica - Curso 2017.3 Prof. Germán Lugones Aula 4 O modelo atômico de Bohr 1 O modelo de Bohr Em 1913, Niels Bohr propôs um modelo do átomo de hidrogênio que combinava o trabalho de Planck,
Modelos atômicos. Química Fundamental I. Prof. Edson Nossol
 Modelos atômicos Química Fundamental I Prof. Edson Nossol Uberlândia, 26/04/2017 Demócrito (V a.c.): matéria partículas muito pequenas e indivisíveis (átomos) Dalton (1808): químico, matemático e filósofo
Modelos atômicos Química Fundamental I Prof. Edson Nossol Uberlândia, 26/04/2017 Demócrito (V a.c.): matéria partículas muito pequenas e indivisíveis (átomos) Dalton (1808): químico, matemático e filósofo
Hipóteses atomísticas
 Modelos atômicos 1 Hipóteses atômicas Primeiras idéias sobre a constituição da matéria séculos VII a IV a.c. Hipóteses atomísticas observáveis. Aristóteles e outros filósofos século IV a.c. - toda matéria
Modelos atômicos 1 Hipóteses atômicas Primeiras idéias sobre a constituição da matéria séculos VII a IV a.c. Hipóteses atomísticas observáveis. Aristóteles e outros filósofos século IV a.c. - toda matéria
A teoria quântica antiga AULA
 3 AULA METAS: Mostrar as dificuldades enfrentadas pela física clássica na explicação da estabilidade dos átomos e da estrutura dos espectros atômicos. Introduzir o modelo de Bohr para o átomo de um elétron.
3 AULA METAS: Mostrar as dificuldades enfrentadas pela física clássica na explicação da estabilidade dos átomos e da estrutura dos espectros atômicos. Introduzir o modelo de Bohr para o átomo de um elétron.
Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento angular bem definido
 ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
O átomo de Dalton O átomo de Thomson O átomo de Rutherford O átomo moderno Isótopos Abundância isotópica e determinação de massas atômicas O átomo de
 Estrutura atômica O átomo de Dalton O átomo de Thomson O átomo de Rutherford O átomo moderno Isótopos Abundância isotópica e determinação de massas atômicas O átomo de Bohr 2 1 Por que estudar os átomos???
Estrutura atômica O átomo de Dalton O átomo de Thomson O átomo de Rutherford O átomo moderno Isótopos Abundância isotópica e determinação de massas atômicas O átomo de Bohr 2 1 Por que estudar os átomos???
Física IV para Engenharia Elétrica. 2º Semestre de Instituto de Física - Universidade de São Paulo
 1 Física IV para Engenharia Elétrica 2º Semestre de 2014 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdirg@if.usp.br Aula -6: Modelo atômico 2 Interpretação quântica
1 Física IV para Engenharia Elétrica 2º Semestre de 2014 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdirg@if.usp.br Aula -6: Modelo atômico 2 Interpretação quântica
Física D Extensivo V. 8
 Física D Extensivo V. 8 Exercícios 0) C f R X > f WZ 0) B 03) E 04) E raios X > luz Raios X são radiações eletromagnéticas com um comprimento de onda muito curto, aproximadamente de 0,06 até 0 Å. Formam-se
Física D Extensivo V. 8 Exercícios 0) C f R X > f WZ 0) B 03) E 04) E raios X > luz Raios X são radiações eletromagnéticas com um comprimento de onda muito curto, aproximadamente de 0,06 até 0 Å. Formam-se
SUGESTÕES DE EXERCÍCIOS PARA A SEGUNDA AVALIAÇÃO
 FÍSICA IV PROF. DR. DURVAL RODRIGUES JUNIOR SUGESTÕES DE EXERCÍCIOS PARA A SEGUNDA AVALIAÇÃO Como na Biblioteca do Campus I e do Campus II temos bom número de cópias do Halliday e poucas do Serway, os
FÍSICA IV PROF. DR. DURVAL RODRIGUES JUNIOR SUGESTÕES DE EXERCÍCIOS PARA A SEGUNDA AVALIAÇÃO Como na Biblioteca do Campus I e do Campus II temos bom número de cópias do Halliday e poucas do Serway, os
Modelos atômicos. Curso de Química. Prof. Rui Medeiros. quimicadorui.com.br
 Modelos atômicos Curso de Química Prof. Rui Medeiros quimicadorui.com.br Módulo Extra - 2017 2 CURSO DE QUÍMICA PROFESSOR RUI MEDEIROS MÓDULO EXTRA - 2017 Modelos atômicos ü A representação esquemática
Modelos atômicos Curso de Química Prof. Rui Medeiros quimicadorui.com.br Módulo Extra - 2017 2 CURSO DE QUÍMICA PROFESSOR RUI MEDEIROS MÓDULO EXTRA - 2017 Modelos atômicos ü A representação esquemática
Estrutura da Matéria BIK Prof. Fernando Carlos Giacomelli (Turma A)
 Estrutura da Matéria BIK0102-15 Prof. Fernando Carlos Giacomelli (Turma A) fernando.giacomelli@ufabc.edu.br Bloco A - Sala 613-3 Torre 3 - CCNH - Santo André Dualidade Onda-Partícula: Descrição Clássica
Estrutura da Matéria BIK0102-15 Prof. Fernando Carlos Giacomelli (Turma A) fernando.giacomelli@ufabc.edu.br Bloco A - Sala 613-3 Torre 3 - CCNH - Santo André Dualidade Onda-Partícula: Descrição Clássica
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
MODELO ATÔMICO DE BOHR 1913
 MODELO ATÔMICO DE BOHR 1913 Niels Bohr (1885-1961) +sico dinamarquês, trabalhou com Rutherford Modelo atômico de Rutherford Lembre que: havia dificuldades para explicar: u u Como um átomo poderia ser estável
MODELO ATÔMICO DE BOHR 1913 Niels Bohr (1885-1961) +sico dinamarquês, trabalhou com Rutherford Modelo atômico de Rutherford Lembre que: havia dificuldades para explicar: u u Como um átomo poderia ser estável
J.J. Thomson N. Bohr E. Schrödinger. J. Dalton E. Rutherford. Demócrito e Leucipo. A. Sommerfeld. Evolução histórica
 J.J. Thomson N. Bohr E. Schrödinger Demócrito e Leucipo J. Dalton E. Rutherford Evolução histórica A. Sommerfeld Demócrito e Leucipo (modelo filosofal) Do que a matéria é constituída? A matéria é descontínua.
J.J. Thomson N. Bohr E. Schrödinger Demócrito e Leucipo J. Dalton E. Rutherford Evolução histórica A. Sommerfeld Demócrito e Leucipo (modelo filosofal) Do que a matéria é constituída? A matéria é descontínua.
Quantização da Carga, Luz e Energia
 Quantização da Carga, Luz e Energia Prof. Jaime Urban 1 / 13 Quantização da Carga Elétrica Primeiras medidas de e e de e/m Michael Faraday (1791-1867) Condução da eletricidade em ĺıquidos - Lei da eletrólise
Quantização da Carga, Luz e Energia Prof. Jaime Urban 1 / 13 Quantização da Carga Elétrica Primeiras medidas de e e de e/m Michael Faraday (1791-1867) Condução da eletricidade em ĺıquidos - Lei da eletrólise
Escola Politécnica FAP GABARITO DA P2 24 de outubro de 2006
 P2 Física IV Escola Politécnica - 2006 FAP 2204 - GABARITO DA P2 24 de outubro de 2006 Questão 1 A. O comprimento de onda de corte para ejetar elétron da superfície do metal lantânio é = 3760 Å. (a) (0,5
P2 Física IV Escola Politécnica - 2006 FAP 2204 - GABARITO DA P2 24 de outubro de 2006 Questão 1 A. O comprimento de onda de corte para ejetar elétron da superfície do metal lantânio é = 3760 Å. (a) (0,5
SEL FUNDAMENTOS FÍSICOS DOS PROCESSOS DE FORMAÇÃO DE IMAGENS MÉDICAS. Prof. Homero Schiabel (Sub-área de Imagens Médicas)
 SEL 5705 - FUNDAMENTOS FÍSICOS DOS PROCESSOS DE FORMAÇÃO DE IMAGENS MÉDICAS Prof. Homero Schiabel (Sub-área de Imagens Médicas) 5. INTERAÇÃO DOS RAIOS X COM A MATÉRIA 5.1. Atenuação e Absorção ATENUAÇÃO:
SEL 5705 - FUNDAMENTOS FÍSICOS DOS PROCESSOS DE FORMAÇÃO DE IMAGENS MÉDICAS Prof. Homero Schiabel (Sub-área de Imagens Médicas) 5. INTERAÇÃO DOS RAIOS X COM A MATÉRIA 5.1. Atenuação e Absorção ATENUAÇÃO:
Introd. Física Médica
 Introd. Física Médica O Efeito Foto Elétrico (EFE) Introdução a Física Médica O Efeito Foto Elétrico (EFE) Introdução a Fís sica Médica Heinrich HERTZ descobriu o Efeito FotoElétrico (1887): Quando a luz
Introd. Física Médica O Efeito Foto Elétrico (EFE) Introdução a Física Médica O Efeito Foto Elétrico (EFE) Introdução a Fís sica Médica Heinrich HERTZ descobriu o Efeito FotoElétrico (1887): Quando a luz
A Antiga Mecânica Quântica
 A Antiga Mecânica Quântica Química Quântica Prof a. Dr a. Carla Dalmolin Dualidade Partícula Onda O Princípio da Incerteza Quantização da Energia E = hν Aplicações bem sucedidas: Radiação do Corpo Negro
A Antiga Mecânica Quântica Química Quântica Prof a. Dr a. Carla Dalmolin Dualidade Partícula Onda O Princípio da Incerteza Quantização da Energia E = hν Aplicações bem sucedidas: Radiação do Corpo Negro
QUESTÕES DE FÍSICA MODERNA
 QUESTÕES DE FÍSICA MODERNA 1) Em diodos emissores de luz, conhecidos como LEDs, a emissão de luz ocorre quando elétrons passam de um nível de maior energia para um outro de menor energia. Dois tipos comuns
QUESTÕES DE FÍSICA MODERNA 1) Em diodos emissores de luz, conhecidos como LEDs, a emissão de luz ocorre quando elétrons passam de um nível de maior energia para um outro de menor energia. Dois tipos comuns
I. Paulino* Mecânica Quântica I ( ) - Capítulo 01. *UAF/CCT/UFCG - Brasil. Origens da Mecânica Quântica Teoria Quântica Exercícios
 AS ORIGENS DA MECÂNICA QUÂNTICA Mecânica Quântica I (1108045) - Capítulo 01 I. Paulino* *UAF/CCT/UFCG - Brasil 2014.2 1 / 63 Origens da Mecânica Quântica Partículas e ondas Radiação do corpo negro Efeito
AS ORIGENS DA MECÂNICA QUÂNTICA Mecânica Quântica I (1108045) - Capítulo 01 I. Paulino* *UAF/CCT/UFCG - Brasil 2014.2 1 / 63 Origens da Mecânica Quântica Partículas e ondas Radiação do corpo negro Efeito
O espectro eletromagnético. foton
 Estrutura Atômica I O espectro eletromagnético Modelos atômicos O experimento de Faraday e a natureza elétrica da matéria Os experimentos de Thomson e a descoberta do elétron O experimento de Millikan
Estrutura Atômica I O espectro eletromagnético Modelos atômicos O experimento de Faraday e a natureza elétrica da matéria Os experimentos de Thomson e a descoberta do elétron O experimento de Millikan
Uma breve história do mundo dos quanta Érica Polycarpo & Marta F. Barroso
 Unidade 3 Bohr e de Broglie: a antiga teoria quântica CEDERJ / EXTENSÃO FÍSICA Érica Polycarpo & Marta F. Barroso Sumário: Apresentação Espectros atômicos e a evolução dos modelos para o átomo As ondas
Unidade 3 Bohr e de Broglie: a antiga teoria quântica CEDERJ / EXTENSÃO FÍSICA Érica Polycarpo & Marta F. Barroso Sumário: Apresentação Espectros atômicos e a evolução dos modelos para o átomo As ondas
Lista de Exercícios - Física Quântica - UNIDADE 1
 Lista de Exercícios - Física Quântica - UNIDADE 1 Problemas e questões baseados no D. Halliday, R. Resnick e J. Walker, Fundamentos de Física, 6ª ed. - Capítulos 39, 40 e 41. Questões 1. Como pode a energia
Lista de Exercícios - Física Quântica - UNIDADE 1 Problemas e questões baseados no D. Halliday, R. Resnick e J. Walker, Fundamentos de Física, 6ª ed. - Capítulos 39, 40 e 41. Questões 1. Como pode a energia
TEORIA ATÔMICA. Química Geral
 TEORIA ATÔMICA Química Geral 1 Modelo Atômico de Dalton John Dalton 1766 1844: Físico, Químico e Meteorologista inglês Primeira tentativa de relacionar mudanças químicas a eventos que ocorrem ao nível
TEORIA ATÔMICA Química Geral 1 Modelo Atômico de Dalton John Dalton 1766 1844: Físico, Químico e Meteorologista inglês Primeira tentativa de relacionar mudanças químicas a eventos que ocorrem ao nível
ESTRUTURA ATÔMICA. Modelos Atômicos
 ESTRUTURA ATÔMICA Modelos Atômicos 1.Modelo atômico de Dalton 2.Modelo atômico de Thomson 3.Modelo atômico de Rutherford 4.Modelo atômico de Rutherford-Bohr 5.Modelo atômico atual MODELOS ATÔMICOS 1808
ESTRUTURA ATÔMICA Modelos Atômicos 1.Modelo atômico de Dalton 2.Modelo atômico de Thomson 3.Modelo atômico de Rutherford 4.Modelo atômico de Rutherford-Bohr 5.Modelo atômico atual MODELOS ATÔMICOS 1808
Profa: GRAÇA PORTO. Quibi. Química - Graça Porto
 Profa: GRAÇA PORTO WWW. Quibi. COM Leucipo de Mileto ( 440 a.c.) & Demócrito (460 a.c. - 370 a.c. ) A idéia de dividirmos uma porção qualquer de matéria até chegarmos a uma partícula que não possa mais
Profa: GRAÇA PORTO WWW. Quibi. COM Leucipo de Mileto ( 440 a.c.) & Demócrito (460 a.c. - 370 a.c. ) A idéia de dividirmos uma porção qualquer de matéria até chegarmos a uma partícula que não possa mais
Propriedades corpusculares da radiação e.m.
 Propriedades corpusculares da radiação e.m. Fenômenos que evidenciam a natureza corpuscular da radiação eletromagnética: efeito fotoelétrico; produção de raios-x (bremsstrahlung) espalhamento Compton produção
Propriedades corpusculares da radiação e.m. Fenômenos que evidenciam a natureza corpuscular da radiação eletromagnética: efeito fotoelétrico; produção de raios-x (bremsstrahlung) espalhamento Compton produção
Atomística. Matéria. Sistemas. Órgãos. Tecidos. Células. Moléculas Átomos
 Atomística Matéria Sistemas Órgãos Tecidos Células Moléculas Átomos Atomística Tales de Mileto (640 a.c. e 2610 a.h.): Descobriu as cargas elétricas Empédocles (V a.c. e XXV a.h.) água terra fogo ar Atomística
Atomística Matéria Sistemas Órgãos Tecidos Células Moléculas Átomos Atomística Tales de Mileto (640 a.c. e 2610 a.h.): Descobriu as cargas elétricas Empédocles (V a.c. e XXV a.h.) água terra fogo ar Atomística
Aula-11. (quase) Tudo sobre os átomos
 Aula-11 (quase) Tudo sobre os átomos Algumas propriedades: Átomos são estáveis (quase sempre) Os átomos se combinam (como o fazem é descrito pela mecânica quântica) Os átomos podem ser agrupados em famílias
Aula-11 (quase) Tudo sobre os átomos Algumas propriedades: Átomos são estáveis (quase sempre) Os átomos se combinam (como o fazem é descrito pela mecânica quântica) Os átomos podem ser agrupados em famílias
Energia certa significa: quando a energia do fóton corresponde à diferença nos níveis de energia entre as duas órbitas permitidas do átomo de H.
 ESPECTROSCOPIA II A relação da luz com as linhas espectrais O que acontece se átomos de H forem bombardeados por fótons? R. Existem três possibilidades: 1) a maioria dos fótons passa sem nenhuma interação
ESPECTROSCOPIA II A relação da luz com as linhas espectrais O que acontece se átomos de H forem bombardeados por fótons? R. Existem três possibilidades: 1) a maioria dos fótons passa sem nenhuma interação
Química Geral prof. Eduardo. Modelos Atômicos. Módulo QG 04 Apst. 1
 Química Geral prof. Eduardo Modelos Atômicos Módulo QG 04 Apst. 1 Empédocles (492 432 a.c.) Existem quatro elementos básicos na natureza. Aristóteles teles (384 322 a.c.) Frio, quente, úmido, seco. Ar,
Química Geral prof. Eduardo Modelos Atômicos Módulo QG 04 Apst. 1 Empédocles (492 432 a.c.) Existem quatro elementos básicos na natureza. Aristóteles teles (384 322 a.c.) Frio, quente, úmido, seco. Ar,
Introdução à Astrofísica. Espectroscopia. Rogemar A. Riffel
 Introdução à Astrofísica Espectroscopia Rogemar A. Riffel Radiação de Corpo Negro Corpo negro: corpo que absorve toda a radiação que incide sobre ele, sem refletir nada; - Toda a radiação emitida pelo
Introdução à Astrofísica Espectroscopia Rogemar A. Riffel Radiação de Corpo Negro Corpo negro: corpo que absorve toda a radiação que incide sobre ele, sem refletir nada; - Toda a radiação emitida pelo
13/Maio/2016 Aula 20. Átomo de hidrogénio Modelo de Bohr Modelo quântico. Números quânticos. 11/Maio/2016 Aula 19
 11/Maio/2016 Aula 19 Aplicações: - nanotecnologias; - microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. 13/Maio/2016 Aula 20 Átomo de hidrogénio Modelo de Bohr Modelo quântico. Números
11/Maio/2016 Aula 19 Aplicações: - nanotecnologias; - microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. 13/Maio/2016 Aula 20 Átomo de hidrogénio Modelo de Bohr Modelo quântico. Números
Disciplina: Física IV Física Moderna
 Disciplina: Física IV Física Moderna Instrutor: Prof. Carlos Eduardo Souza - Cadu Sala: A2-15 (IF, andar 1P) Email: carloseduardosouza@id.uff.br Site do curso: http://cursos.if.uff.br/fisicaiv_xxi_0216/
Disciplina: Física IV Física Moderna Instrutor: Prof. Carlos Eduardo Souza - Cadu Sala: A2-15 (IF, andar 1P) Email: carloseduardosouza@id.uff.br Site do curso: http://cursos.if.uff.br/fisicaiv_xxi_0216/
ATOMÍSTICA PROF. ADRIANO ALVES
 ATOMÍSTICA PROF. ADRIANO ALVES Demócrito Aristóteles Dalton Thomson Bohr Rutherford Sommerfeld Heisenberg Schrödinger De Broglie DALTON 1. Toda matéria é formada de partículas fundamentais, os átomos.
ATOMÍSTICA PROF. ADRIANO ALVES Demócrito Aristóteles Dalton Thomson Bohr Rutherford Sommerfeld Heisenberg Schrödinger De Broglie DALTON 1. Toda matéria é formada de partículas fundamentais, os átomos.
Mecânica Quântica:
 Mecânica Quântica: 206-207 a Série. Considere o modelo de Bohr para o átomo de hidrogénio. (vide le Bellac, ex..5.2).. Mostre que o raio de Bohr, o menor raio que verica a condição 2πr = nλ, é dado por
Mecânica Quântica: 206-207 a Série. Considere o modelo de Bohr para o átomo de hidrogénio. (vide le Bellac, ex..5.2).. Mostre que o raio de Bohr, o menor raio que verica a condição 2πr = nλ, é dado por
Hipóteses atomísticas
 Modelos atômicos 1 Hipóteses atômicas Primeiras idéias sobre a constituição da matéria séculos VII a IV a.c. Hipóteses atomísticas observáveis. Aristóteles e outros flósofos século IV a.c. - toda matéria
Modelos atômicos 1 Hipóteses atômicas Primeiras idéias sobre a constituição da matéria séculos VII a IV a.c. Hipóteses atomísticas observáveis. Aristóteles e outros flósofos século IV a.c. - toda matéria
Universidade Federal do Tocantins
 Universidade Federal do Tocantins Modelos atômicos: Introdução Prof. Dr. Edenilson dos Santos Niculau enicolau@uft.edu.br Blog: profedenilsonniculau.wordpress.com 2 Sumário MODELOS ATÔMICOS Estrutura atômica
Universidade Federal do Tocantins Modelos atômicos: Introdução Prof. Dr. Edenilson dos Santos Niculau enicolau@uft.edu.br Blog: profedenilsonniculau.wordpress.com 2 Sumário MODELOS ATÔMICOS Estrutura atômica
Séries de Lyman, Balmer, Paschen, etc. e Modelo de Bohr
 Séries de Lyman, Balmer, Paschen, etc. e Modelo de Bohr Problemas com a Física Clássica Fatos que a Física Clássica não podia explicar Observação de linhas nos espectros atômicos; A estrutura nuclear do
Séries de Lyman, Balmer, Paschen, etc. e Modelo de Bohr Problemas com a Física Clássica Fatos que a Física Clássica não podia explicar Observação de linhas nos espectros atômicos; A estrutura nuclear do
Física Moderna I Aula 09. Marcelo G Munhoz Pelletron, sala 245, ramal 6940
 Física Moderna I Aula 09 Marcelo G Munhoz Pelletron, sala 245, ramal 6940 munhoz@if.usp.br 1904 - O Modelo Atômico de Thomson Philosophical Magazine, 7 (1904), 237 A parir da descoberta dos elétrons (carga
Física Moderna I Aula 09 Marcelo G Munhoz Pelletron, sala 245, ramal 6940 munhoz@if.usp.br 1904 - O Modelo Atômico de Thomson Philosophical Magazine, 7 (1904), 237 A parir da descoberta dos elétrons (carga
Física IV Escola Politécnica GABARITO DA P2 13 de outubro de 2016
 Física IV - 4323204 Escola Politécnica - 2016 GABARITO DA P2 13 de outubro de 2016 Questão 1 Uma partícula 1 com massa de repouso m 0 e energia total igual a duas vezes sua energia de repouso colide com
Física IV - 4323204 Escola Politécnica - 2016 GABARITO DA P2 13 de outubro de 2016 Questão 1 Uma partícula 1 com massa de repouso m 0 e energia total igual a duas vezes sua energia de repouso colide com
Radiação Eletromagnética (II) Sandra dos Anjos IAG/USP
 Radiação Eletromagnética (II) Espectro Solar Modelos Atômicos Absorção e Emissão de Fótons A Natureza da Formação de Linhas Espectrais Composição Química dos Astros Propagação da Luz Intensidade da Radiação
Radiação Eletromagnética (II) Espectro Solar Modelos Atômicos Absorção e Emissão de Fótons A Natureza da Formação de Linhas Espectrais Composição Química dos Astros Propagação da Luz Intensidade da Radiação
pessoal.utfpr.edu.br/renan
 Aula 2: Espectro de emissão do hidrogênio: Balmer e Rydberg O átomo de Bohr Princípio da incerteza Partícula na caixa Prof. Renan Borsoi Campos pessoal.utfpr.edu.br/renan O espectro eletromagnético da
Aula 2: Espectro de emissão do hidrogênio: Balmer e Rydberg O átomo de Bohr Princípio da incerteza Partícula na caixa Prof. Renan Borsoi Campos pessoal.utfpr.edu.br/renan O espectro eletromagnético da
4. Teoria atômica da matéria
 4. Teoria atômica da matéria Sumário Modelos atômicos: de Demócrito a Dalton Determinação da razão e/m para o elétron Determinação da carga do elétron Modelo de Thomson Espalhamento de partículas alfa
4. Teoria atômica da matéria Sumário Modelos atômicos: de Demócrito a Dalton Determinação da razão e/m para o elétron Determinação da carga do elétron Modelo de Thomson Espalhamento de partículas alfa
Natureza ondulatória da luz
 Natureza ondulatória da luz Planck (900): a energia só pode ser liberada (ou absorvida) por átomos em certos pedaços de tamanhos mínimos, chamados quanta (quantum, no singular). A relação entre a energia
Natureza ondulatória da luz Planck (900): a energia só pode ser liberada (ou absorvida) por átomos em certos pedaços de tamanhos mínimos, chamados quanta (quantum, no singular). A relação entre a energia
Física IV Escola Politécnica GABARITO DA P3 25 de novembro de 2014
 Física IV - 4320402 Escola Politécnica - 2014 GABARITO DA P3 25 de novembro de 2014 Questão 1 Um elétron em repouso espalha um fóton incidente que possui comprimento de onda λ. Observa-se que o fóton espalhado
Física IV - 4320402 Escola Politécnica - 2014 GABARITO DA P3 25 de novembro de 2014 Questão 1 Um elétron em repouso espalha um fóton incidente que possui comprimento de onda λ. Observa-se que o fóton espalhado
Atomística. Prof. Fernando R. Xavier
 Atomística Prof. Fernando R. Xavier UDESC 2013 Nem sempre foi tão fácil observar um átomo... Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson 400 a.c. até 1897 d.c. O Modelo de
Atomística Prof. Fernando R. Xavier UDESC 2013 Nem sempre foi tão fácil observar um átomo... Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson 400 a.c. até 1897 d.c. O Modelo de
18/Maio/2016 Aula 21. Introdução à Física Nuclear. Estrutura e propriedades do núcleo. 13Maio/2016 Aula 20
 13Maio/2016 Aula 20 Átomo de hidrogénio Modelo de Bohr Modelo quântico. Números quânticos. 18/Maio/2016 Aula 21 Introdução à Física Nuclear Estrutura e propriedades do núcleo 1 Aula anterior Átomos modelo
13Maio/2016 Aula 20 Átomo de hidrogénio Modelo de Bohr Modelo quântico. Números quânticos. 18/Maio/2016 Aula 21 Introdução à Física Nuclear Estrutura e propriedades do núcleo 1 Aula anterior Átomos modelo
