Adsorção em interfaces sólido/solução
|
|
|
- Geraldo Campelo Beltrão
- 7 Há anos
- Visualizações:
Transcrição
1 Adsorção em interfaces sólido/solução 1
2 Adsorção em interfaces sólido/solução 2
3 Adsorção em interfaces sólido/solução Adsorção vs Absorção 3
4 Adsorção em interfaces sólido/solução Muitos processos químicos de adsorção ocorrem com migração do adsorbato (espécie em solução) para os sítios mais internos do adsorvente (sólido). Atualmente, o termo mais correto, que engloba processos de adsorção e absorção é o termo SORÇÃO (SORPTION). O termo DESSORÇÃO (DESORPTION) é utilizado quando ocorre a saída do adsorbato dos sítios de adsorção (locais onde ocorrem 4 as interações.
5 Adsorção em interfaces sólido/solução 5
6 Adsorção em interfaces sólido/solução Etapas que compõem um processo cinético na interface sólido/solução: Theoretical description of the kinetics of solute adsorption at..., Applied Surface Science, 253 (2007)
7 Adsorção em interfaces sólido/solução Dinâmica dos processos de adsorção Cinética de adsorção A metodologia de adsorção por Batch (agitação contínua) utiliza um sistema fechado, contendo uma quantidade bem definida de uma solução (tipicamente aquosa) em presença de uma quantidade bem definida do material sólido (adsorvente). À medida que aumenta o tempo de contato adsorvente/solução, os sítios de adsorção são ocupados progressivamente. A ocupação efetiva dos sítios depende de vários fatores. 7
8 Adsorção em interfaces sólido/solução Como se estuda a cinética de adsorção de processos em interfaces sólido/solução? Pela construção de ISOTERMAS DE ADSORÇÃO (ADSORPTION ISOTHERMS; SORPTION ISOTHERMS) Review Sorption isotherms: A review on physical bases, modeling and measurement, Applied Geochemistry 22 (2007)
9 Principais tipos e características de isotermas de adsorção (sorção): Calculo da quantidade adsorvida em estudos cinéticos em interfaces Sólido/solução: Q t ( Ci C m t ). V Q t = Quantidade adsorvida do adsorvente (mg (adsorb.) /g (adsorv.) mol (adsorb.) /g (adsorv.)) C i = Concentração inicial do adsorbato em solução (mg/l ou mol/l). C t = Concentração do adsorbato em solução após um determinado tempo de contato (mg/l ou mol/l). V = Volume da solução (L) m = massa do adsorvente (g) ou 9
10 Quantidade adsorvida (unidade apropriada) Cinética de adsorção Temperatura 25 C Tempo de contato (unidade de tempo, min, h, etc) Exemplo de uma curva cinética de adsorção na interface sólido/solução 10
11 Quais os principais fatores que influenciam na cinética de adsorção sólido/solução? 11
12 1- Concentração inicial do adsorbato em solução De forma genérica, a adsorção se estabelece até se que uma certa fração de sítios disponíveis sejam ocupados, até atingir o equilíbrio: Adsorvente (solv.) + adsorbato (solv.) = adsorvente-adsorbato + solv., K 1 12
13 1- Concentração inicial do adsorbato em solução Quando se aumenta a concentração inicial da solução, uma quantidade maior de sítios de adsorção é ocupada, deslocando-se o equilíbrio para a direita, levando o sistema para uma nova condição de equilíbrio, K 2, K 3,... O aumento da concentração inicial supera a resistência à transferência de massa da solução para a fase sólida. 13
14 1- Concentração inicial do adsorbato em solução Theoretical description of the kinetics of solute adsorption at..., Applied Surface Science, 253 (2007)
15 2- Valor do ph da solução O ph da solução afeta a carga dos sítios de adsorção do adsorvente, seus graus de ionização, o tipo e a quantidade do adsorbato em solução. Na maioria dos casos, as adsorbatos estão presentes no meio aquoso na forma de cátions ou ânions. 15
16 Cr(VI) forms several species, the relative proportions of which depend on both ph and total Cr(VI) concentration. In the ph between 1 and 6 HCrO 4 is the predominant form up to the Cr(VI) concentration 10-2 mol/l when it starts to condense yielding the orange-red dichromate ion. A simplified Pourbaix diagram for chromium (Cr) species dominating in diluted aerated aqueous solutions in the absence of any complexing agents, other than H 2 O or OH. The broken vertical lines represent the normal ph range in natural waters, whereas the grey zone shows the domain of Cr(OH) 3 (s) stability for 10 6 mol/l of total Cr. J. Kotas, Z. Stasicka, Environmental Pollution, 107 (2000)
17 2- Valor do ph da solução Espécies aniônicas são adsorvidas, preferencialmente, quando o ph do meio é baixo (tipicamente < 6), pois os sítios de adsorção encontram-se protonados e, consequentemente, com cargas residuais positivas. Espécies catiônicas são adsorvidas em ph s > 7, devido à deposição de íons OH - ou desprotonação dos sítios de adsorção. Meio ácido: M-OH + H + [M-OH 2 ] + Meio básico: M-OH + OH - [M-O] - + H 2 O 17
18 4- Massa do adsorvente q e ( Ci C m t ). V % Re moção (( C C ) / C ) x100 i t i Fig. 5 shows the effect of adsorbent mass on the adsorption. The results showed that increasing the carbon mass increased the percent removal (R%) but decreased the adsorption capacity. There are two factors, which can contribute to this adsorbent mass effect: (i) as the dosage of adsorbent is increased, the adsorption sites remain unsaturated during the adsorption reaction leading to drop in adsorption capacity; (ii) the aggregation/agglomeration of adsorbent particles at higher mass, which would lead to a decrease in the surface area and an increase in the diffusional path length. Journal of Hazardous Materials 166 (2009)
19 5- Tamanho das partículas do adsorvente À medida que o tamanho das partículas aumenta, diminui a quantidade adsorvida. 19
20 6- Velocidade de agitação A velocidade de agitação apresenta pouca influência na quantidade adsorvida. 20
21 7 Temperatura do meio de adsorção A adsorção aumenta com a temperatura = Processo endotérmico 21
22 7 Temperatura do meio de adsorção A adsorção diminui com a temperatura = Processo exotérmico 22
23 7 Temperatura do meio de adsorção Via de regra, os processos de adsorção nas interfaces sólido/solução são, em princípio, exotérmicos. Contudo, muitos processos de natureza exotérmica e/ou endotérmica ocorrem simultaneamente. Processo exotérmico: Adsorvente (solv.) + adsorbato (solv.) = adsorvente-adsorbato + solv. + calor Processo endotérmico: Adsorvente (solv.) + adsorbato (solv.) + calor = adsorvente-adsorbato + solv. 23
24 7 Temperatura do meio de adsorção As quantidades adsorvidas aumentam com a temperatura quando: A- Ocorre extensa difusão do adsorbato para os poros menores do adsorvente. Termodinamicamente, a difusão necessita retirar energia do ambiente para que as moléculas do adsorbato ganhem energia suficiente para que a difusão ocorre apreciavelmente. Quanto maior for a magnitude da difusão, maior será a contribuição endotérmica no processo de adsorção. 24
25 7 Temperatura do meio de adsorção E/OU B- O adsorbato e os sítios de adsorção possuem energias de solvatação muito elevadas. Para que haja aproximação efetiva para que ocorra adsorção, é preciso que parte das moléculas que solvatam os sítios de adsorção e que estão nas esferas mais próximas do adsorbato sejam removidas. Termodinamicamente, esse processo também necessita retirada de energia do sistema para que ocorra efetivamente. Quanto maiores forem as energias de solvatação dos sítios de adsorção e das moléculas solvatantes do adsorbato, maior será a contribuição endotérmica no processo de adsorção. 25
Física Aplicada 2016/17 MICF FFUP ADSORÇÃO DE LÍQUIDOS EM SUPERFÍCIES SÓLIDAS
 ADSORÇÃO DE LÍQUIDOS EM SUPERFÍCIES SÓLIDAS ADSORÇÃO DE LÍQUIDOS NA SUPERFÍCIE DE UM SÓLIDO When the distance between the solid surfaces is decreased, the oscillatory molecular density shows up. RECORDE
ADSORÇÃO DE LÍQUIDOS EM SUPERFÍCIES SÓLIDAS ADSORÇÃO DE LÍQUIDOS NA SUPERFÍCIE DE UM SÓLIDO When the distance between the solid surfaces is decreased, the oscillatory molecular density shows up. RECORDE
INTERFACE SÓLIDO - LÍQUIDO
 INTERFACE SÓLIDO - LÍQUIDO ADSORÇÃO DE LÍQUIDOS EM SUPERFÍCIES SÓLIDAS Física Aplicada 2017/18 MICF FFUP 1 ADSORÇÃO DE LÍQUIDOS NA SUPERFÍCIE DE UM SÓLIDO Na interface sólido-líquido as moléculas têm tendência
INTERFACE SÓLIDO - LÍQUIDO ADSORÇÃO DE LÍQUIDOS EM SUPERFÍCIES SÓLIDAS Física Aplicada 2017/18 MICF FFUP 1 ADSORÇÃO DE LÍQUIDOS NA SUPERFÍCIE DE UM SÓLIDO Na interface sólido-líquido as moléculas têm tendência
ESTUDO DA INFLUÊNCIA DO ph NA ADSORÇÃO DE CROMO (VI) EM CARVÃO ATIVADO GRANULAR
 ESTUDO DA INFLUÊNCIA DO ph NA ADSORÇÃO DE CROMO (VI) EM CARVÃO ATIVADO GRANULAR OLIVEIRA, R. F. 1 FÉRIS, L. A. 1 1 Universidade Federal do Rio Grande do Sul, Departamento de Engenharia Química E-mail para
ESTUDO DA INFLUÊNCIA DO ph NA ADSORÇÃO DE CROMO (VI) EM CARVÃO ATIVADO GRANULAR OLIVEIRA, R. F. 1 FÉRIS, L. A. 1 1 Universidade Federal do Rio Grande do Sul, Departamento de Engenharia Química E-mail para
INFLUÊNCIA DO ph NA SORÇÃO DE ÍONS METÁLICOS EM SÍLICA GEL
 INFLUÊNCIA DO ph NA SORÇÃO DE ÍONS METÁLICOS EM SÍLICA GEL H. M. C. FAGNANI 1, R. C. FERREIRA 1, M. A. S. D. BARROS 1, P. A. ARROYO 1 1 Universidade Estadual de Maringá, Departamento de Engenharia Química
INFLUÊNCIA DO ph NA SORÇÃO DE ÍONS METÁLICOS EM SÍLICA GEL H. M. C. FAGNANI 1, R. C. FERREIRA 1, M. A. S. D. BARROS 1, P. A. ARROYO 1 1 Universidade Estadual de Maringá, Departamento de Engenharia Química
ADSORÇÃO. PMT Físico-Química para Engenharia Metalúrgica e de Materiais II - Neusa Alonso-Falleiros 1
 DSORÇÃO Referências: LUPIS, C. H. P. Chemical Thermodynamics of Materials. New York : North-Holland, 1983. p. Capítulo XIV: dsorption. DeHOFF, ROBERT T. Thermodynamics in Materials Science. New York :
DSORÇÃO Referências: LUPIS, C. H. P. Chemical Thermodynamics of Materials. New York : North-Holland, 1983. p. Capítulo XIV: dsorption. DeHOFF, ROBERT T. Thermodynamics in Materials Science. New York :
DETERMINAÇÃO DOS PARÂMETROS CINÉTICOS DE ADSORÇÃO DE ÍONS DOS METAIS DE TRANSIÇÃO UTILIZANDO O MODELO DE AVRAMI
 MIRANDA, W. D.; ALCÂNTARA, E. F. C. Determinação dos parâmetros cinéticos de adsorção de íons dos metais de transição utilizando o modelo de Avrami. In: CONGRESSO DE PESQUISA ENSINO E EXTENSÃO DA UFG CONPEEX,
MIRANDA, W. D.; ALCÂNTARA, E. F. C. Determinação dos parâmetros cinéticos de adsorção de íons dos metais de transição utilizando o modelo de Avrami. In: CONGRESSO DE PESQUISA ENSINO E EXTENSÃO DA UFG CONPEEX,
AULA 5 Adsorção, isotermas e filmes monomoleculares. Prof a Elenice Schons
 AULA 5 Adsorção, isotermas e filmes monomoleculares Prof a Elenice Schons ADSORÇÃO É um processo de acumulação e concentração seletiva de um ou mais constituintes contidos num gás ou líquido sobre superfícies
AULA 5 Adsorção, isotermas e filmes monomoleculares Prof a Elenice Schons ADSORÇÃO É um processo de acumulação e concentração seletiva de um ou mais constituintes contidos num gás ou líquido sobre superfícies
O EFEITO DA ADIÇÃO DE CLORETO DE SÓDIO NO COMPORTAMENTO DAS ISOTERMAS DE ADSORÇÃO DE CORANTE AZUL REATIVO BF-5G EM CARVÃO ATIVADO DE OSSO
 O EFEITO DA ADIÇÃO DE CLORETO DE SÓDIO NO COMPORTAMENTO DAS ISOTERMAS DE ADSORÇÃO DE CORANTE AZUL REATIVO BF-5G EM CARVÃO ATIVADO DE OSSO V. E. HORITA 1, C. H. MAEDA 1, D. S. de CARVALHO 1, P. A. ARROYO
O EFEITO DA ADIÇÃO DE CLORETO DE SÓDIO NO COMPORTAMENTO DAS ISOTERMAS DE ADSORÇÃO DE CORANTE AZUL REATIVO BF-5G EM CARVÃO ATIVADO DE OSSO V. E. HORITA 1, C. H. MAEDA 1, D. S. de CARVALHO 1, P. A. ARROYO
UTILIZAÇÃO DE ADSORVENTE ALTERNATIVO DE BAIXO CUSTO PARA REMOÇÃO DO CORANTE TARTRAZINA
 UTILIZAÇÃO DE ADSORVENTE ALTERNATIVO DE BAIXO CUSTO PARA REMOÇÃO DO CORANTE TARTRAZINA E. L. FOLETTO*,1, C. T. WEBER 1, G. C. COLLAZZO 2, M. A. MAZUTTI 1, R. C. KUHN 1 ; G. L. DOTTO 1 1 Departamento de
UTILIZAÇÃO DE ADSORVENTE ALTERNATIVO DE BAIXO CUSTO PARA REMOÇÃO DO CORANTE TARTRAZINA E. L. FOLETTO*,1, C. T. WEBER 1, G. C. COLLAZZO 2, M. A. MAZUTTI 1, R. C. KUHN 1 ; G. L. DOTTO 1 1 Departamento de
AVALIAÇÃO DA CINÉTICA DE ADSORÇÃO DE ÍONS CROMO (VI) EM NANOFIBRAS DE QUITOSANA/NYLON 6
 AVALIAÇÃO DA CINÉTICA DE ADSORÇÃO DE ÍONS CROMO (VI) EM NANOFIBRAS DE QUITOSANA/NYLON 6 C. Schonhart 1 ; G. Kummer 1 ; G. L. Dotto 1 ; D. A. Bertuol 1 ; E. H. Tanabe 1 1 Departamento de Engenharia Química
AVALIAÇÃO DA CINÉTICA DE ADSORÇÃO DE ÍONS CROMO (VI) EM NANOFIBRAS DE QUITOSANA/NYLON 6 C. Schonhart 1 ; G. Kummer 1 ; G. L. Dotto 1 ; D. A. Bertuol 1 ; E. H. Tanabe 1 1 Departamento de Engenharia Química
INFLUÊNCIA DA PRESENÇA DE SAIS NA ADSORÇÃO DO CORANTE VERMELHO PROCION UTILIZANDO ALUMINA ATIVADA
 INFLUÊNCIA DA PRESENÇA DE SAIS NA ADSORÇÃO DO CORANTE VERMELHO PROCION UTILIZANDO ALUMINA ATIVADA N. Favarin 1, E.C. Peres¹, E, G.L. Dotto 1 1 Universidade Federal de Santa Maria, Departamento de Engenharia
INFLUÊNCIA DA PRESENÇA DE SAIS NA ADSORÇÃO DO CORANTE VERMELHO PROCION UTILIZANDO ALUMINA ATIVADA N. Favarin 1, E.C. Peres¹, E, G.L. Dotto 1 1 Universidade Federal de Santa Maria, Departamento de Engenharia
REMOÇÃO DE CÁTIONS METÁLICOS UTILIZANDO ZEÓLITA HBEA
 Congresso Técnico Científico da Engenharia e da Agronomia CONTECC 2016 Rafain Palace Hotel & Convention Center- Foz do Iguaçu - PR 29 de agosto a 1 de setembro de 2016 REMOÇÃO DE CÁTIONS METÁLICOS UTILIZANDO
Congresso Técnico Científico da Engenharia e da Agronomia CONTECC 2016 Rafain Palace Hotel & Convention Center- Foz do Iguaçu - PR 29 de agosto a 1 de setembro de 2016 REMOÇÃO DE CÁTIONS METÁLICOS UTILIZANDO
Remoção de Cr(VI) de soluções aquosas pelo filme de óxido de ferro/nanotubo de carbono/quitosana reticulada
 Nº do Trabalho: 2017-A5-11552 Título: Remoção de Cr(VI) de soluções aquosas pelo filme de óxido de ferro/nanotubo de carbono/quitosana reticulada Autores: SOUZA, C. H. F. (carlos.h.souza@ufv.br; Universidade
Nº do Trabalho: 2017-A5-11552 Título: Remoção de Cr(VI) de soluções aquosas pelo filme de óxido de ferro/nanotubo de carbono/quitosana reticulada Autores: SOUZA, C. H. F. (carlos.h.souza@ufv.br; Universidade
ESTUDO COMPARATIVO DE ADSORÇÃO DO Cr(VI) PELAS FIBRAS DE QUITOSANA E QUITOSANA MAGNÉTICA
 ESTUDO COMPARATIVO DE ADSORÇÃO DO Cr(VI) PELAS FIBRAS DE QUITOSANA E QUITOSANA MAGNÉTICA RESUMO Mitiko Yamaura* (IPEN, PD) Glaucia Mayumi Shima (IPEN, IC) *myamaura@ipen.br Neste trabalho apresenta-se
ESTUDO COMPARATIVO DE ADSORÇÃO DO Cr(VI) PELAS FIBRAS DE QUITOSANA E QUITOSANA MAGNÉTICA RESUMO Mitiko Yamaura* (IPEN, PD) Glaucia Mayumi Shima (IPEN, IC) *myamaura@ipen.br Neste trabalho apresenta-se
Adsorção do corante Rodamina B de soluções aquosas por zeólita sintética de cinzas pesadas de carvão
 Adsorção do corante Rodamina B de soluções aquosas por zeólita sintética de cinzas pesadas de carvão RAQUEL R. ALCÂNTARA a*, JULIANA C. IZIDORO a, DENISE A. FUNGARO a. *rreisa@hotmail.com a. Instituto
Adsorção do corante Rodamina B de soluções aquosas por zeólita sintética de cinzas pesadas de carvão RAQUEL R. ALCÂNTARA a*, JULIANA C. IZIDORO a, DENISE A. FUNGARO a. *rreisa@hotmail.com a. Instituto
Uso de vermiculita revestida com quitosana como agente adsorvente dos íons sintéticos de chumbo (Pb ++ )
 Uso de vermiculita revestida com quitosana como agente adsorvente dos íons sintéticos de chumbo (Pb ++ ) Anne.P. O. da Silva, Josette.L.de S. Melo, Jailson V. de Melo São Paulo/Brazil May /2011 Introdução
Uso de vermiculita revestida com quitosana como agente adsorvente dos íons sintéticos de chumbo (Pb ++ ) Anne.P. O. da Silva, Josette.L.de S. Melo, Jailson V. de Melo São Paulo/Brazil May /2011 Introdução
Adsorção de Solução. ( é um fenômeno de superfície e é relacionada a tensão superficial de soluções )
 Adsorção de Solução Adsorção é a acumulação de uma substância em uma interface. Ocorre com todos os tipos de interface, tais como gás-sólido, solução-sólido, solução-gás, solução α -solução β ( é um fenômeno
Adsorção de Solução Adsorção é a acumulação de uma substância em uma interface. Ocorre com todos os tipos de interface, tais como gás-sólido, solução-sólido, solução-gás, solução α -solução β ( é um fenômeno
ADSORÇÃO DE AZUL DE METILENO SOBRE CARVÃO ATIVO
 QFL 1444 - FÍSICO-QUÍMICA EXPERIMENTAL 2018 1 ADSORÇÃO DE AZUL DE METILENO SOBRE CARVÃO ATIVO Absorção Adsorção Danilo Marques Alves nº USP 9922662 Gabriela Ayres n USP 9792498 Livia Yukari Tanaka nº USP
QFL 1444 - FÍSICO-QUÍMICA EXPERIMENTAL 2018 1 ADSORÇÃO DE AZUL DE METILENO SOBRE CARVÃO ATIVO Absorção Adsorção Danilo Marques Alves nº USP 9922662 Gabriela Ayres n USP 9792498 Livia Yukari Tanaka nº USP
PALIGORSQUITA ATIVADA TERMICAMENTE VISANDO A ADSORÇÃO DE Pb +2. Ministro Petrônio Portela - Bairro: Ininga, CEP /Teresina PI
 PALIGORSQUITA ATIVADA TERMICAMENTE VISANDO A ADSORÇÃO DE Pb +2 Silva, M. P. (1) ; Santos, M. S. F. (2), Xavier, K. C. M. (1) ; Carvalho, M. W. N. C. (3) ; Osajima, J. A. (1) ; Silva Filho, E. C. (1) socorroferreira@ufpi.edu.br
PALIGORSQUITA ATIVADA TERMICAMENTE VISANDO A ADSORÇÃO DE Pb +2 Silva, M. P. (1) ; Santos, M. S. F. (2), Xavier, K. C. M. (1) ; Carvalho, M. W. N. C. (3) ; Osajima, J. A. (1) ; Silva Filho, E. C. (1) socorroferreira@ufpi.edu.br
INFLUÊNCIA DO ph NA ADSORÇÃO DE ÍONS Cr (VI) UTILIZANDO ESPONJA DE QUITOSANA
 INFLUÊNCIA DO ph NA ADSORÇÃO DE ÍONS Cr (VI) UTILIZANDO ESPONJA DE QUITOSANA E. L. ARAÚJO 1, C.E. G.COMIOTTO 1, M. A. LOPES 1,T. R. S. CADAVAL Jr 1 e L. A. de A. PINTO 1 1 Universidade Federal do Rio Grande,
INFLUÊNCIA DO ph NA ADSORÇÃO DE ÍONS Cr (VI) UTILIZANDO ESPONJA DE QUITOSANA E. L. ARAÚJO 1, C.E. G.COMIOTTO 1, M. A. LOPES 1,T. R. S. CADAVAL Jr 1 e L. A. de A. PINTO 1 1 Universidade Federal do Rio Grande,
MECANISMO DE ADSORÇÃO DE PARACETAMOL EM CARVÕES DE ORIGEM NACIONAL
 MECANISMO DE ADSORÇÃO DE PARACETAMOL EM CARVÕES DE ORIGEM NACIONAL R. C. FERREIRA 1, T. F. V. de OLIVEIRA 1, O. M. COUTO JUNIOR 1, M. A. S. D. de BARROS 1, K. Q. de CARVALHO 2, 1 Universidade Estadual
MECANISMO DE ADSORÇÃO DE PARACETAMOL EM CARVÕES DE ORIGEM NACIONAL R. C. FERREIRA 1, T. F. V. de OLIVEIRA 1, O. M. COUTO JUNIOR 1, M. A. S. D. de BARROS 1, K. Q. de CARVALHO 2, 1 Universidade Estadual
FÍSICA DAS SUPERFÍCIES
 FÍSICA DAS SUPERFÍCIES Produção de vácuo forte Preparação de máscaras de gás (usam carvão ativado para gases perigosos Controlo de humidade com gel de sílica Remoção das impurezas de diversos produtos
FÍSICA DAS SUPERFÍCIES Produção de vácuo forte Preparação de máscaras de gás (usam carvão ativado para gases perigosos Controlo de humidade com gel de sílica Remoção das impurezas de diversos produtos
CARGAS ELÉTRICAS DO SOLO. Atributos físicos e químicos do solo -Aula 12- Prof. Alexandre Paiva da Silva INTRODUÇÃO CARGAS ELÉTRICAS E FOTOSSÍNTESE:
 CARGAS ELÉTRICAS DO SOLO Atributos físicos e químicos do solo -Aula 12- Prof. Alexandre Paiva da Silva INTRODUÇÃO CARGAS ELÉTRICAS E FOTOSSÍNTESE: Vida na Terra Propriedade de uma dispersão coloidal Argilas
CARGAS ELÉTRICAS DO SOLO Atributos físicos e químicos do solo -Aula 12- Prof. Alexandre Paiva da Silva INTRODUÇÃO CARGAS ELÉTRICAS E FOTOSSÍNTESE: Vida na Terra Propriedade de uma dispersão coloidal Argilas
21º CBECIMAT - Congresso Brasileiro de Engenharia e Ciência dos Materiais 09 a 13 de Novembro de 2014, Cuiabá, MT, Brasil
 UTILIZAÇÃO DE HIDROGÉIS NANOCOMPÓSITOS DE AMIDO ENXERTADO COM POLI (ACRILATO DE SÓDIO) E NANOWHISKERS DE CELULOSE PARA REMOÇÃO DE CORANTE AZUL DE METILENO R. F. Gomes, A. C. N. de Azevedo, M. G. Vaz, D.
UTILIZAÇÃO DE HIDROGÉIS NANOCOMPÓSITOS DE AMIDO ENXERTADO COM POLI (ACRILATO DE SÓDIO) E NANOWHISKERS DE CELULOSE PARA REMOÇÃO DE CORANTE AZUL DE METILENO R. F. Gomes, A. C. N. de Azevedo, M. G. Vaz, D.
Catálise homogênea e heterogênea
 Catálise homogênea e heterogênea Definição de catálise 1 - Uma substância que altera a velocidade de uma reação sem ser usada é chamada de catalisador. - O fenômeno de aumentar a taxa de reação pelo uso
Catálise homogênea e heterogênea Definição de catálise 1 - Uma substância que altera a velocidade de uma reação sem ser usada é chamada de catalisador. - O fenômeno de aumentar a taxa de reação pelo uso
FUNCIONALIZAÇÃO DA CELULOSE COM CISTEAMINA: SÍNTESE, CARACTERIZAÇÃO E ADSORÇÃO
 FUNCIONALIZAÇÃO DA CELULOSE COM CISTEAMINA: SÍNTESE, CARACTERIZAÇÃO E ADSORÇÃO Bezerra, R. D. S., Silva, F. S., Ferreira, F. J. L., Silva, L. S., Osajima, J. A., Silva Filho, E. C. Autor para correspondência:
FUNCIONALIZAÇÃO DA CELULOSE COM CISTEAMINA: SÍNTESE, CARACTERIZAÇÃO E ADSORÇÃO Bezerra, R. D. S., Silva, F. S., Ferreira, F. J. L., Silva, L. S., Osajima, J. A., Silva Filho, E. C. Autor para correspondência:
4. RESULTADOS E DISCUSSÕES 4.1Comprimento de onda do corante Telon Violet
 ADSORÇÃO DE CORANTE ÁCIDO UTILIZANDO RESÍDUO DE FIBRA DE VIDRO ACID DYE ADSORPTION USING FIBERGLASS WASTE Ferreira, Raquel Pisani Baldinotti Campus de Sorocaba Engenharia Ambiental raquelpisani@hotmail.com
ADSORÇÃO DE CORANTE ÁCIDO UTILIZANDO RESÍDUO DE FIBRA DE VIDRO ACID DYE ADSORPTION USING FIBERGLASS WASTE Ferreira, Raquel Pisani Baldinotti Campus de Sorocaba Engenharia Ambiental raquelpisani@hotmail.com
ESTUDO DA ADSORÇÃO DE FENOL EM CARVÃO ATIVADO E ZEÓLITA USY
 Congresso Técnico Científico da Engenharia e da Agronomia CONTECC 2018 Maceió - AL 21 a 24 de agosto de 2018 ESTUDO DA ADSORÇÃO DE FENOL EM CARVÃO ATIVADO E ZEÓLITA USY FABRICIO VENTURA BARSI 1 *; MARINA
Congresso Técnico Científico da Engenharia e da Agronomia CONTECC 2018 Maceió - AL 21 a 24 de agosto de 2018 ESTUDO DA ADSORÇÃO DE FENOL EM CARVÃO ATIVADO E ZEÓLITA USY FABRICIO VENTURA BARSI 1 *; MARINA
Processos Superficiais Adsorção
 Adsorção em Sólidos - quando se mistura um sólido finamente dividido em uma solução diluída de corante, observamos que a intensidade da coloração decresce pronunciadamente; - se é sólido e gás a pressão
Adsorção em Sólidos - quando se mistura um sólido finamente dividido em uma solução diluída de corante, observamos que a intensidade da coloração decresce pronunciadamente; - se é sólido e gás a pressão
PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA
 PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA INFORMAÇÕES IMPORTANTES: - IDENTIFIQUE TODAS AS FOLHAS DESTA PROVA COM SEU NÚMERO DE INSCRIÇÃO. Obs.: EM HIPÓTESE NENHUMA USE SEU NOME NAS FOLHAS COMO IDENTIFICAÇÃO.
PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA INFORMAÇÕES IMPORTANTES: - IDENTIFIQUE TODAS AS FOLHAS DESTA PROVA COM SEU NÚMERO DE INSCRIÇÃO. Obs.: EM HIPÓTESE NENHUMA USE SEU NOME NAS FOLHAS COMO IDENTIFICAÇÃO.
PQI-2321 Tópicos de Química para Engenharia Ambiental I
 PQI-2321 Tópicos de Química para Engenharia Ambiental I Adsorção Aula 01 Prof. Moisés Teles moises.teles@usp.br Departamento de Engenharia Química Escola Politécnica da USP Introdução Exemplos. Bicarbonato
PQI-2321 Tópicos de Química para Engenharia Ambiental I Adsorção Aula 01 Prof. Moisés Teles moises.teles@usp.br Departamento de Engenharia Química Escola Politécnica da USP Introdução Exemplos. Bicarbonato
VIABILIDADE DO USO DA CASCA DE BANANA COMO ADSORVENTE DE ÍONS DE URÂNIO
 05 International Nuclear Atlantic Conference - INAC 05 Santos, SP, Brazil, August 28 to September 2, 05 ASSOCIAÇÃO BRASILEIRA DE ENERGIA NUCLEAR - ABEN ISBN: 85-99141-01-5 VIABILIDADE DO USO DA CASCA DE
05 International Nuclear Atlantic Conference - INAC 05 Santos, SP, Brazil, August 28 to September 2, 05 ASSOCIAÇÃO BRASILEIRA DE ENERGIA NUCLEAR - ABEN ISBN: 85-99141-01-5 VIABILIDADE DO USO DA CASCA DE
EXPERIMENTO 3 ADSORÇÃO Determinação da Isoterma de adsorção do azul de metileno em fibra de algodão
 EXPERIMETO 3 ADSORÇÃO Determinação da Isoterma de adsorção do azul de metileno em fibra de algodão Adsorção é o acúmulo de uma substância numa interface, que é a superfície ou região limítrofe entre duas
EXPERIMETO 3 ADSORÇÃO Determinação da Isoterma de adsorção do azul de metileno em fibra de algodão Adsorção é o acúmulo de uma substância numa interface, que é a superfície ou região limítrofe entre duas
Lista de Exercícios. Data limite para entrega da lista: 14/09/2018
 Lista de Exercícios Nome: n.º Santos, de de 2018. Série: 2.ª Turmas: A, B, C Ensino: Médio Prof. Paulo Henrique (PH) Bimestre: 3.º Data limite para entrega da lista: 14/09/2018 Valor: 4,0(quatro) 1) Por
Lista de Exercícios Nome: n.º Santos, de de 2018. Série: 2.ª Turmas: A, B, C Ensino: Médio Prof. Paulo Henrique (PH) Bimestre: 3.º Data limite para entrega da lista: 14/09/2018 Valor: 4,0(quatro) 1) Por
REMOÇÃO DE DICLOFENACO DE POTÁSSIO USANDO CARVÃO ATIVADO COMERCIAL COM ALTA ÁREA DE SUPERFÍCIE
 REMOÇÃO DE DICLOFENACO DE POTÁSSIO USANDO CARVÃO ATIVADO COMERCIAL COM ALTA ÁREA DE SUPERFÍCIE J. F. de Oliveira; E. C. Peres; A. Sulkovski; E. L.Foletto Departamento de Engenharia Química Universidade
REMOÇÃO DE DICLOFENACO DE POTÁSSIO USANDO CARVÃO ATIVADO COMERCIAL COM ALTA ÁREA DE SUPERFÍCIE J. F. de Oliveira; E. C. Peres; A. Sulkovski; E. L.Foletto Departamento de Engenharia Química Universidade
USO DE RESÍDUO DE ERVA MATE MODIFICADA NA ADSORÇÃO DE CORANTE TÊXTIL
 USO DE RESÍDUO DE ERVA MATE MODIFICADA NA ADSORÇÃO DE CORANTE TÊXTIL B. M. Vicentin 1 ; G. X. Araújo 2 ; R. D. C. Rocha 3 1- Programa De Pós-Graduação Em Tecnologia De Processos Químicos E Bioquímicos
USO DE RESÍDUO DE ERVA MATE MODIFICADA NA ADSORÇÃO DE CORANTE TÊXTIL B. M. Vicentin 1 ; G. X. Araújo 2 ; R. D. C. Rocha 3 1- Programa De Pós-Graduação Em Tecnologia De Processos Químicos E Bioquímicos
Estudo da remoção de Cd 2+, Cr 3+ e Pb 2+ de soluções aquosas empregando a zeólita natural escolecita: uma abordagem cinética e termodinâmica
 http://revistas.unlp.edu.ar/index.php/domus/issue/current/showtoc Estudo da remoção de Cd 2+, Cr 3+ e Pb 2+ de soluções aquosas empregando a zeólita natural escolecita: uma abordagem cinética e termodinâmica
http://revistas.unlp.edu.ar/index.php/domus/issue/current/showtoc Estudo da remoção de Cd 2+, Cr 3+ e Pb 2+ de soluções aquosas empregando a zeólita natural escolecita: uma abordagem cinética e termodinâmica
4. Materiais e métodos
 68 4. Materiais e métodos Neste capítulo serão apresentados os equipamentos usados para a realização do estudo da biossorção de íons metálicos Pb 2+ e Mn 2+ contidos em soluções aquosas, utilizando como
68 4. Materiais e métodos Neste capítulo serão apresentados os equipamentos usados para a realização do estudo da biossorção de íons metálicos Pb 2+ e Mn 2+ contidos em soluções aquosas, utilizando como
CELULOSE FOSFATADA COM ÁCIDO METAFOSFÓRICO PARA REMOÇÃO DE CORANTES
 CELULOSE FOSFATADA COM ÁCIDO METAFOSFÓRICO PARA REMOÇÃO DE CORANTES S. C. C. Silva, F. C. Silva 1, M. M. F. Silva 2, L. C. B. Lima 1, M. R. M. C. Santos 1, J. A. Osajima 1, E. C. da Silva Filho 1 1 Programa
CELULOSE FOSFATADA COM ÁCIDO METAFOSFÓRICO PARA REMOÇÃO DE CORANTES S. C. C. Silva, F. C. Silva 1, M. M. F. Silva 2, L. C. B. Lima 1, M. R. M. C. Santos 1, J. A. Osajima 1, E. C. da Silva Filho 1 1 Programa
SCIENTIA PLENA VOL. 6, NUM
 SCIENTIA PLENA VOL. 6, NUM. 12 2010 www.scientiaplena.org.br Estudo Comparativo de Adsorção do Corante Preto Sulphcolor utilizando o Carvão Ativo Convencional com o Bagaço da Cana-deaçúcar In Natura e
SCIENTIA PLENA VOL. 6, NUM. 12 2010 www.scientiaplena.org.br Estudo Comparativo de Adsorção do Corante Preto Sulphcolor utilizando o Carvão Ativo Convencional com o Bagaço da Cana-deaçúcar In Natura e
REMOÇÃO DE PARACETAMOL USANDO CARVÃO ATIVADO COMERCIAL DE CASCA DE COCO BABAÇU
 REMOÇÃO DE PARACETAMOL USANDO CARVÃO ATIVADO COMERCIAL DE CASCA DE COCO BABAÇU E. C. Severo 1 ; V. S. Foletto 2 ; A. C. Steffen 3 ; E. R. Abaide 3 ; E. L. Foletto 1 1- Departamento de Engenharia uímica
REMOÇÃO DE PARACETAMOL USANDO CARVÃO ATIVADO COMERCIAL DE CASCA DE COCO BABAÇU E. C. Severo 1 ; V. S. Foletto 2 ; A. C. Steffen 3 ; E. R. Abaide 3 ; E. L. Foletto 1 1- Departamento de Engenharia uímica
EFICIÊNCIA DO CARVÃO ATIVADO DE BABAÇU NA REMOÇÃO DO CORANTE AMARELO TARTRAZINA EM SOLUÇÃO AQUOSA
 EFICIÊNCIA DO CARVÃO ATIVADO DE BABAÇU NA REMOÇÃO DO CORANTE AMARELO TARTRAZINA EM SOLUÇÃO AQUOSA I. M. RECK 1, R. M. PAIXÃO 2, L. A. M. PINTO 1, R. BERGAMASCO 2, A. M. S. VIEIRA 1 e R. GOMES 3 1 Universidade
EFICIÊNCIA DO CARVÃO ATIVADO DE BABAÇU NA REMOÇÃO DO CORANTE AMARELO TARTRAZINA EM SOLUÇÃO AQUOSA I. M. RECK 1, R. M. PAIXÃO 2, L. A. M. PINTO 1, R. BERGAMASCO 2, A. M. S. VIEIRA 1 e R. GOMES 3 1 Universidade
INFLUÊNCIA DA REMEDIAÇÃO ELETROCINÉTICA N0 AUMENTO DO CICLO DE VIDA DE CATALISADORES DESATIVADOS POR PROCESSO FCC
 INFLUÊNCIA DA REMEDIAÇÃO ELETROCINÉTICA N0 AUMENTO DO CICLO DE VIDA DE CATALISADORES DESATIVADOS POR PROCESSO FCC L.S. SANCHES 1, R. B. G. VALT 1, M. J. S. PONTE 1, K. C. SANTOS 2 E A. BROSKA 2 1-Universidade
INFLUÊNCIA DA REMEDIAÇÃO ELETROCINÉTICA N0 AUMENTO DO CICLO DE VIDA DE CATALISADORES DESATIVADOS POR PROCESSO FCC L.S. SANCHES 1, R. B. G. VALT 1, M. J. S. PONTE 1, K. C. SANTOS 2 E A. BROSKA 2 1-Universidade
Adsorção de Ácido Laranja 8 de solução aquosa sobre zeólitas sintetizadas a partir de cinzas leves de carvão modificadas por surfactante
 Adsorção de Ácido Laranja 8 de solução aquosa sobre zeólitas sintetizadas a partir de cinzas leves de carvão modificadas por surfactante THARCILA C. R. BERTOLINI *, CARINA P. MAGDALENA, JULIANA C. IZIDORO,
Adsorção de Ácido Laranja 8 de solução aquosa sobre zeólitas sintetizadas a partir de cinzas leves de carvão modificadas por surfactante THARCILA C. R. BERTOLINI *, CARINA P. MAGDALENA, JULIANA C. IZIDORO,
ACH4064 Linguagem Química e Reações Químicas 2
 ACH4064 Linguagem Química e Reações Químicas 2 Profa Dra Káthia M. Honório - kmhonorio@usp.br (sala 322C 3o andar Prédio I1) Prof. Dr. Paulo Rogério Miranda Correia - prmc@usp.br (sala 320D 3o andar Prédio
ACH4064 Linguagem Química e Reações Químicas 2 Profa Dra Káthia M. Honório - kmhonorio@usp.br (sala 322C 3o andar Prédio I1) Prof. Dr. Paulo Rogério Miranda Correia - prmc@usp.br (sala 320D 3o andar Prédio
3ª Série / Vestibular. As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar que, na reação:
 3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
Resumo. Luciana de Jesus Barros; Layne Sousa dos Santos. Orientadores: Elba Gomes dos Santos, Luiz Antônio Magalhães Pontes
 Estudo da remoção do Metal Ferro por Adsorção em Mesocarpo do Coco Luciana de Jesus Barros; Layne Sousa dos Santos Orientadores: Elba Gomes dos Santos, Luiz Antônio Magalhães Pontes Resumo Neste trabalho,
Estudo da remoção do Metal Ferro por Adsorção em Mesocarpo do Coco Luciana de Jesus Barros; Layne Sousa dos Santos Orientadores: Elba Gomes dos Santos, Luiz Antônio Magalhães Pontes Resumo Neste trabalho,
Remoção de Cu e Co contido em soluções aquosas por Biossorção
 Leonardo Martins da Silva Remoção de Cu e Co contido em soluções aquosas por Biossorção Dissertação de Mestrado Dissertação apresentada como requisito parcial para obtenção do título de Mestre pelo Programa
Leonardo Martins da Silva Remoção de Cu e Co contido em soluções aquosas por Biossorção Dissertação de Mestrado Dissertação apresentada como requisito parcial para obtenção do título de Mestre pelo Programa
natural escolecita: uma abordagem cinética e termodinâmica Karla Carolina Saqueto, Nemésio Neves Batista Salvador, Marcos Valério Battisti, Ana
 Estudo da remoção de Cd 2+, Cr 3+ e Pb 2+ de soluções aquosas empregando a zeólita natural escolecita: uma abordagem cinética e termodinâmica Karla Carolina Saqueto, Nemésio Neves Batista Salvador, Marcos
Estudo da remoção de Cd 2+, Cr 3+ e Pb 2+ de soluções aquosas empregando a zeólita natural escolecita: uma abordagem cinética e termodinâmica Karla Carolina Saqueto, Nemésio Neves Batista Salvador, Marcos
Eixo Temático ET Tratamento de Efluentes Sanitários e Industriais
 Anais do Congresso Brasileiro de Gestão Ambiental e Sustentabilidade - Vol. 2: Congestas 2014 377 Eixo Temático ET-07-002 - Tratamento de Efluentes Sanitários e Industriais RECUPERAÇÃO TÉRMICA DE ADSORVENTES
Anais do Congresso Brasileiro de Gestão Ambiental e Sustentabilidade - Vol. 2: Congestas 2014 377 Eixo Temático ET-07-002 - Tratamento de Efluentes Sanitários e Industriais RECUPERAÇÃO TÉRMICA DE ADSORVENTES
ADSORÇÃO DE ÍNDIGO DE CARMIM EM BIOMASSA SECA DE Pistia stratiotes
 ADSORÇÃO DE ÍNDIGO DE CARMIM EM BIOMASSA SECA DE Pistia stratiotes R.M. Ferreira 1,2 (PG); N. M. de Oliveira 1 (PG); L.L. Lima 1 (IC); A. L. D. M. Campista 1 (IC); D. M. A. Stapelfeldt 1 (PQ) 1 Departamento
ADSORÇÃO DE ÍNDIGO DE CARMIM EM BIOMASSA SECA DE Pistia stratiotes R.M. Ferreira 1,2 (PG); N. M. de Oliveira 1 (PG); L.L. Lima 1 (IC); A. L. D. M. Campista 1 (IC); D. M. A. Stapelfeldt 1 (PQ) 1 Departamento
- SOLUÇÃO = SOLUTO + SOLVENTE. COEFICIENTE DE SOLUBILIDADE ( Cs) Grandeza que depende da natureza do soluto e da temperatura.
 Soluções - MISTURA HOMOGÊNEA - SOLUÇÃO = SOLUTO + SOLVENTE menor quantidade maior quantidade COEFICIENTE DE SOLUBILIDADE ( Cs) Grandeza que depende da natureza do soluto e da temperatura. Cs = g de soluto
Soluções - MISTURA HOMOGÊNEA - SOLUÇÃO = SOLUTO + SOLVENTE menor quantidade maior quantidade COEFICIENTE DE SOLUBILIDADE ( Cs) Grandeza que depende da natureza do soluto e da temperatura. Cs = g de soluto
Cinética e Equilíbrio da Sorção de Corante Direto Preto Krom KJR em Carvão Ativado de Ossos
 Cinética e Equilíbrio da Sorção de Corante Direto Preto Krom KJR em Carvão Ativado de Ossos Claudio J. Glitz Jr. 1*, Fabiano B. Scheufele 1, Aparecido N. Módenes 2 (1) Curso de Graduação em Engenharia
Cinética e Equilíbrio da Sorção de Corante Direto Preto Krom KJR em Carvão Ativado de Ossos Claudio J. Glitz Jr. 1*, Fabiano B. Scheufele 1, Aparecido N. Módenes 2 (1) Curso de Graduação em Engenharia
Termodinâmica e Cinética de reações orgânicas. Profa. Alceni Augusta Werle Profa. Tania Marcia do Sacramento Melo
 Termodinâmica e Cinética de reações orgânicas Profa. Alceni Augusta Werle Profa. Tania Marcia do Sacramento Melo 1 1 INTRODUÇÃO reagentes produtos Termodinâmica é a área da química que estuda as concentrações
Termodinâmica e Cinética de reações orgânicas Profa. Alceni Augusta Werle Profa. Tania Marcia do Sacramento Melo 1 1 INTRODUÇÃO reagentes produtos Termodinâmica é a área da química que estuda as concentrações
Professor Haroldo. Equilíbrio Químico
 Professor Haroldo Equilíbrio Químico - Irreversibilidade de Processos: Um processo irreversível é aquele que só ocorre em um sentido. A B Exemplo: Papel cinzas. - Reversibilidade de Processos: Um processo
Professor Haroldo Equilíbrio Químico - Irreversibilidade de Processos: Um processo irreversível é aquele que só ocorre em um sentido. A B Exemplo: Papel cinzas. - Reversibilidade de Processos: Um processo
ESTUDO DA REMOÇÃO DE FENOL EM ÁGUAS RESIDUÁRIAS SINTÉTICAS ATRAVÉS DE ADSORÇÃO EM CARVÃO VEGETAL
 ESTUDO DA REMOÇÃO DE FENOL EM ÁGUAS RESIDUÁRIAS SINTÉTICAS ATRAVÉS DE ADSORÇÃO EM CARVÃO VEGETAL A. Simonatto 1 ; A. L. B. Meneghini 1 ; A. Dervanoski 1 ; G. D. L. P. Vargas 1 ; T. C. da Silva 1 ; C. J.
ESTUDO DA REMOÇÃO DE FENOL EM ÁGUAS RESIDUÁRIAS SINTÉTICAS ATRAVÉS DE ADSORÇÃO EM CARVÃO VEGETAL A. Simonatto 1 ; A. L. B. Meneghini 1 ; A. Dervanoski 1 ; G. D. L. P. Vargas 1 ; T. C. da Silva 1 ; C. J.
QUÍMICA Cinética Química Velocidade de Reação, Energia de Ativação, Concentração, Pressão, Temperatura e Catalisador - Parte 4 Prof ª.
 QUÍMICA Cinética Química Concentração, Pressão, Temperatura e Catalisador - Parte 4 Prof ª. Giselle Blois CONCENTRAÇÃO DOS REAGENTES: O aumento da concentração dos reagentes acarreta em um aumento da velocidade
QUÍMICA Cinética Química Concentração, Pressão, Temperatura e Catalisador - Parte 4 Prof ª. Giselle Blois CONCENTRAÇÃO DOS REAGENTES: O aumento da concentração dos reagentes acarreta em um aumento da velocidade
AVALIAÇÃO DA APLICABILIDADE DE ESCAMAS DE SARDINHA VERDADEIRA SARDINELLA BRASILIENSIS NA REMOÇÃO DE CROMO HEXAVALENTE PELO PROCESSO DE ADSORÇÃO.
 AVALIAÇÃO DA APLICABILIDADE DE ESCAMAS DE SARDINHA VERDADEIRA SARDINELLA BRASILIENSIS NA REMOÇÃO DE CROMO HEXAVALENTE PELO PROCESSO DE ADSORÇÃO. GONÇALVES, G. T¹; CORRÊA, R 1.; CORRÊA, A. X. da R¹. 1-
AVALIAÇÃO DA APLICABILIDADE DE ESCAMAS DE SARDINHA VERDADEIRA SARDINELLA BRASILIENSIS NA REMOÇÃO DE CROMO HEXAVALENTE PELO PROCESSO DE ADSORÇÃO. GONÇALVES, G. T¹; CORRÊA, R 1.; CORRÊA, A. X. da R¹. 1-
4. Resultados e Discussão
 Absorbância 4. Resultados e Discussão 4.1. Obtenção da curva de calibração A obtenção da curva de calibração, absorbância vs. concentração de Paraquat, é necessária para a análise química do pesticida.
Absorbância 4. Resultados e Discussão 4.1. Obtenção da curva de calibração A obtenção da curva de calibração, absorbância vs. concentração de Paraquat, é necessária para a análise química do pesticida.
ADSORÇÃO. Adsorção é a fixação de uma substância em uma interface, seja ela sólido-gás, sólido-líquido, líquido-gás (vapor).
 ADSORÇÃO Adsorção é a fixação de uma substância em uma interface, seja ela sólido-gás, sólido-líquido, líquido-gás (vapor). Adsorção física não ocorre ligação química entre substrato e adsorbato. O adsorbato
ADSORÇÃO Adsorção é a fixação de uma substância em uma interface, seja ela sólido-gás, sólido-líquido, líquido-gás (vapor). Adsorção física não ocorre ligação química entre substrato e adsorbato. O adsorbato
Adsorção de íons Zn 2+ pelo bagaço da uva Isabel em meio aquoso
 Adsorção de íons Zn 2+ pelo bagaço da uva Isabel em meio aquoso Lucas Gelain 1, Márjore Antunes 2, Marcelo Giovanela 3 1 Universidade de Caxias do Sul (UCS) (lgelain@ucs.br) 2 UCS (marjore86@gmail.com)
Adsorção de íons Zn 2+ pelo bagaço da uva Isabel em meio aquoso Lucas Gelain 1, Márjore Antunes 2, Marcelo Giovanela 3 1 Universidade de Caxias do Sul (UCS) (lgelain@ucs.br) 2 UCS (marjore86@gmail.com)
UTILIZAÇÃO DE SEMENTES DE LARANJA COMO ADSOVENTE NA REMOÇÃO DO CORANTE AZUL DE METILENO
 UTILIZAÇÃO DE SEMENTES DE LARANJA COMO ADSOVENTE NA REMOÇÃO DO CORANTE AZUL DE METILENO DAIANE CÁSSIA PEREIRA ABREU 1, BIANCA MESQUITA COELHO BOTREL 2, SABRINA MESQUITA COELHO 3, ADELIR APARECIDA SACZK
UTILIZAÇÃO DE SEMENTES DE LARANJA COMO ADSOVENTE NA REMOÇÃO DO CORANTE AZUL DE METILENO DAIANE CÁSSIA PEREIRA ABREU 1, BIANCA MESQUITA COELHO BOTREL 2, SABRINA MESQUITA COELHO 3, ADELIR APARECIDA SACZK
QUI219 QUÍMICA ANALÍTICA (Farmácia) Prof. Mauricio X. Coutrim
 QUI219 QUÍMICA ANALÍTICA (Farmácia) Prof. Mauricio X. Coutrim (mcoutrim@iceb.ufop.br) SOLUÇÕES AQUOSAS Equilíbrios químicos A água e os eletrólitos (solutos que forma íons quando dissolvidos em água):
QUI219 QUÍMICA ANALÍTICA (Farmácia) Prof. Mauricio X. Coutrim (mcoutrim@iceb.ufop.br) SOLUÇÕES AQUOSAS Equilíbrios químicos A água e os eletrólitos (solutos que forma íons quando dissolvidos em água):
Uso de Vermiculita Revestida com Quitosana como Agente Adsorvente dos Íons Sintéticos de Chumbo (Pb ++ )
 Uso de Vermiculita Revestida com Quitosana como Agente Adsorvente dos Íons Sintéticos de Chumbo (Pb ++ ) A. P. O. da Silva a, J. L. S. Melo b, J. V. de Melo c a. Universidade Federal do Rio Grande do Norte,
Uso de Vermiculita Revestida com Quitosana como Agente Adsorvente dos Íons Sintéticos de Chumbo (Pb ++ ) A. P. O. da Silva a, J. L. S. Melo b, J. V. de Melo c a. Universidade Federal do Rio Grande do Norte,
ANÁLISE DA INFLUÊNCIA DA ACIDEZ E DA TEMPERATURA DO SISTEMA SOBRE REMOÇÃO DE CROMO TOTAL UTILIZANDO RESINA MISTA.
 ANÁLISE DA INFLUÊNCIA DA ACIDEZ E DA TEMPERATURA DO SISTEMA SOBRE REMOÇÃO DE CROMO TOTAL UTILIZANDO RESINA MISTA. M. A. BARROS 1, T. S. CARMO 2 e M. R. FRANCO JUNIOR 3 1 Universidade Federal de Uberlândia,
ANÁLISE DA INFLUÊNCIA DA ACIDEZ E DA TEMPERATURA DO SISTEMA SOBRE REMOÇÃO DE CROMO TOTAL UTILIZANDO RESINA MISTA. M. A. BARROS 1, T. S. CARMO 2 e M. R. FRANCO JUNIOR 3 1 Universidade Federal de Uberlândia,
DIFERENTES TIPOS DE ADSORVENTES EMPREGADOS NA REMOÇÃO DE NITRATOS EM ÁGUAS: UMA REVISÃO
 DIFERENTES TIPOS DE ADSORVENTES EMPREGADOS NA REMOÇÃO DE NITRATOS EM ÁGUAS: UMA REVISÃO Arielly Samara Santos Batista 1 ; Fábia Rafaella Silva Alves 2 ; Wedja Marcelino da Silva 3 ; Denise Domingos da
DIFERENTES TIPOS DE ADSORVENTES EMPREGADOS NA REMOÇÃO DE NITRATOS EM ÁGUAS: UMA REVISÃO Arielly Samara Santos Batista 1 ; Fábia Rafaella Silva Alves 2 ; Wedja Marcelino da Silva 3 ; Denise Domingos da
ESTUDO AVALIATIVO DA CAPACIDADE DE ADSORÇÃO DO METAL PESADO CHUMBO (II) EM VERMICULITA REVESTIDA COM QUITOSANA
 ESTUDO AVALIATIVO DA CAPACIDADE DE ADSORÇÃO DO METAL PESADO CHUMBO (II) EM VERMICULITA REVESTIDA COM QUITOSANA Anne P.O.da Silva 1*, Jailson V.de Melo 1,Josette L.de S.Melo 1 UFRN- Universidade Federal
ESTUDO AVALIATIVO DA CAPACIDADE DE ADSORÇÃO DO METAL PESADO CHUMBO (II) EM VERMICULITA REVESTIDA COM QUITOSANA Anne P.O.da Silva 1*, Jailson V.de Melo 1,Josette L.de S.Melo 1 UFRN- Universidade Federal
Cinética Química. Prof. Alex Fabiano C. Campos
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Potencial de Eletrodo Parte I
 Potencial de Eletrodo Parte I 1. Gentil V. Corrosão. 3 edição. 2. Denaro A. R. Fundamentos de eletroquímica. Ed Edgar Blucher Ltda e Ed. Universidade de São Paulo, Brasil, 1974. 3. Ander P. e Sonnessa
Potencial de Eletrodo Parte I 1. Gentil V. Corrosão. 3 edição. 2. Denaro A. R. Fundamentos de eletroquímica. Ed Edgar Blucher Ltda e Ed. Universidade de São Paulo, Brasil, 1974. 3. Ander P. e Sonnessa
CORANTE REATIVO VERMELHO REMAZOL RGB EM CARVÃO ATIVADO COMERCIAL E LODO GASEIFICADO PROVENIENTE DE ESTAÇÃO DE TRATAMENTO DE EFLUENTE TÊXTIL
 ADSORÇÃO DE CORANTE REATIVO VERMELHO REMAZOL RGB EM CARVÃO ATIVADO COMERCIAL E LODO GASEIFICADO PROVENIENTE DE ESTAÇÃO DE TRATAMENTO DE EFLUENTE TÊXTIL W.UTECH JÚNIOR 1, R. F. dos SANTOS¹, J. J. SORNAS¹,
ADSORÇÃO DE CORANTE REATIVO VERMELHO REMAZOL RGB EM CARVÃO ATIVADO COMERCIAL E LODO GASEIFICADO PROVENIENTE DE ESTAÇÃO DE TRATAMENTO DE EFLUENTE TÊXTIL W.UTECH JÚNIOR 1, R. F. dos SANTOS¹, J. J. SORNAS¹,
Titulo do Trabalho SISTEMA ESTRUTURADO ARGILOMINERAL 8-HIDROXIQUINOLINA EMPREGADO PARA REMOÇÃO DE ÍONS Pb(II) DE MEIO AQUOSO
 Titulo do Trabalho SISTEMA ESTRUTURADO ARGILOMINERAL 8-HIDROXIQUINOLINA EMPREGADO PARA REMOÇÃO DE ÍONS Pb(II) DE MEIO AQUOSO Nome do Autor (a) Principal Bruno Della Rovere Binhardi. Nome (s) do Co-autor
Titulo do Trabalho SISTEMA ESTRUTURADO ARGILOMINERAL 8-HIDROXIQUINOLINA EMPREGADO PARA REMOÇÃO DE ÍONS Pb(II) DE MEIO AQUOSO Nome do Autor (a) Principal Bruno Della Rovere Binhardi. Nome (s) do Co-autor
E-books PCNA. Vol. 1 QUÍMICA ELEMENTAR CAPÍTULO 8 EQUILÍBRO QUÍMICO
 E-books PCNA Vol. 1 QUÍMICA ELEMENTAR CAPÍTULO 8 EQUILÍBRO QUÍMICO 2 QUÍMICA ELEMENTAR CAPÍTULO 8 APRESENTAÇÃO... 4 CAPÍTULO 8... 5 1. INTRODUÇÃO... 5 2. REAÇÃO REVERSÍVEL... 6 3. CLASSIFICAÇÃO DO EQUILÍBRIO...
E-books PCNA Vol. 1 QUÍMICA ELEMENTAR CAPÍTULO 8 EQUILÍBRO QUÍMICO 2 QUÍMICA ELEMENTAR CAPÍTULO 8 APRESENTAÇÃO... 4 CAPÍTULO 8... 5 1. INTRODUÇÃO... 5 2. REAÇÃO REVERSÍVEL... 6 3. CLASSIFICAÇÃO DO EQUILÍBRIO...
Qui. Professores: Allan Rodrigues Xandão Monitor: Renan Micha
 Semana 19 Professores: Allan Rodrigues Xandão Monitor: Renan Micha Ao adicionarmos solutos não voláteis a um solv EXERCÍCIOS DE AULA 1. 2NaHCO 3(s) Na 2CO 3(s) + CO 2(g) + H 2O (g) Relativamente à equação
Semana 19 Professores: Allan Rodrigues Xandão Monitor: Renan Micha Ao adicionarmos solutos não voláteis a um solv EXERCÍCIOS DE AULA 1. 2NaHCO 3(s) Na 2CO 3(s) + CO 2(g) + H 2O (g) Relativamente à equação
 Lista de exercícios - Bloco 2 - Aula 25 a 28 - Equilíbrio Químico - Conceitos gerais e cálculo (Kc e Kp) 1. (Unicid - Medicina 2017) Considere os equilíbrios: 1. 2 SO 2 (g) + O 2 (g) 2 SO 3 (g) 25 Kc =
Lista de exercícios - Bloco 2 - Aula 25 a 28 - Equilíbrio Químico - Conceitos gerais e cálculo (Kc e Kp) 1. (Unicid - Medicina 2017) Considere os equilíbrios: 1. 2 SO 2 (g) + O 2 (g) 2 SO 3 (g) 25 Kc =
Cinética Química. Prof. Alex Fabiano C. Campos. Rapidez Média das Reações
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Professor: Fábio Silva SOLUÇÕES
 Professor: Fábio Silva SOLUÇÕES Solvente: Substância que apresenta o mesmo estado de agregação da solução; Substância encontrada em maior quantidade. SOLUÇÃO É uma mistura homogênea de dois ou mais componentes.
Professor: Fábio Silva SOLUÇÕES Solvente: Substância que apresenta o mesmo estado de agregação da solução; Substância encontrada em maior quantidade. SOLUÇÃO É uma mistura homogênea de dois ou mais componentes.
Equilíbrio de Precipitação
 Capítulo 4 Equilíbrio de Precipitação Prof a Alessandra Smaniotto QMC 5325 - Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B Introdução Os equilíbrios ácido -base são exemplos de
Capítulo 4 Equilíbrio de Precipitação Prof a Alessandra Smaniotto QMC 5325 - Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B Introdução Os equilíbrios ácido -base são exemplos de
EQUILÍBRIOS: QUÍMICO E IÔNICO Profº Jaison Mattei
 EQUILÍBRIOS: QUÍMICO E IÔNICO Profº Jaison Mattei Reações completas ou irreversíveis São reações nas quais os reagentes são totalmente convertidos em produtos, não havendo sobra de reagente, ao final da
EQUILÍBRIOS: QUÍMICO E IÔNICO Profº Jaison Mattei Reações completas ou irreversíveis São reações nas quais os reagentes são totalmente convertidos em produtos, não havendo sobra de reagente, ao final da
ADSORÇÃO DE Cr(VI) EM HIDROGEL DE QUITOSANA
 ADSORÇÃO DE Cr(VI) EM HIDROGEL DE QUITOSANA P. B. Vilela 1 ; A. Dalalibera 2 ; E. C. Duminelli 2 ; V. A. Becegato 1 ; A. T. Paulino 1,3 1- Departamento de Engenharia Ambiental e Sanitária Programa de Pós-Graduação
ADSORÇÃO DE Cr(VI) EM HIDROGEL DE QUITOSANA P. B. Vilela 1 ; A. Dalalibera 2 ; E. C. Duminelli 2 ; V. A. Becegato 1 ; A. T. Paulino 1,3 1- Departamento de Engenharia Ambiental e Sanitária Programa de Pós-Graduação
Utilização de lama vermelha tratada com peróxido de BLUE 19
 Utilização de lama vermelha tratada com peróxido de hidrogênio i e ativada por tratamento térmico como meio adsorvedor do corante Reativo Kelli Cristina de Souza BLUE 19 Orientadora: Prof. Dra. Maria Lúcia
Utilização de lama vermelha tratada com peróxido de hidrogênio i e ativada por tratamento térmico como meio adsorvedor do corante Reativo Kelli Cristina de Souza BLUE 19 Orientadora: Prof. Dra. Maria Lúcia
Estudo da cinética e do equilíbrio de adsorção da cefamicina C presente na fase de topo (PEG) do SDFA em resina de troca iônica
 Estudo da cinética e do uilíbrio de adsorção da cefamicina C presente na fase de topo (PEG) do SDFA em resina de troca iônica L. M. BRITES 1 e M. B. PASOTTO 2 1 Centro Universitário da FEI, Departamento
Estudo da cinética e do uilíbrio de adsorção da cefamicina C presente na fase de topo (PEG) do SDFA em resina de troca iônica L. M. BRITES 1 e M. B. PASOTTO 2 1 Centro Universitário da FEI, Departamento
REMOÇÃO DE CORANTES TÊXTEIS INDUSTRIAIS POR ADSORÇÃO EM NANOFOLHAS DE GRAFENO
 REMOÇÃO DE CORANTES TÊXTEIS INDUSTRIAIS POR ADSORÇÃO EM NANOFOLHAS DE GRAFENO B. S. Damasceno 1, E. H. C. de Oliveira 2, L. K. de Assis 3, M. N. Carvalho 4, M. G. Ghislandi 5 Lote 21, Quadra 21, Setor
REMOÇÃO DE CORANTES TÊXTEIS INDUSTRIAIS POR ADSORÇÃO EM NANOFOLHAS DE GRAFENO B. S. Damasceno 1, E. H. C. de Oliveira 2, L. K. de Assis 3, M. N. Carvalho 4, M. G. Ghislandi 5 Lote 21, Quadra 21, Setor
Professor da Escola de Engenharia Mauá (EEM/CEUN-IMT).
 ESTUDO CINÉTICO DA ADSORÇÃO DO CORANTE INDIGO BLUE (2,2 - BIS - 2,3 - DIIDRO - 3 - OXOINDOLILIDENO) EM FIBRAS DE CASCA DE COCO VERDE (COCOS NUCIFERA L) Lívia Fiorotto Zeferino 1, Patrícia Antonio de Menezes
ESTUDO CINÉTICO DA ADSORÇÃO DO CORANTE INDIGO BLUE (2,2 - BIS - 2,3 - DIIDRO - 3 - OXOINDOLILIDENO) EM FIBRAS DE CASCA DE COCO VERDE (COCOS NUCIFERA L) Lívia Fiorotto Zeferino 1, Patrícia Antonio de Menezes
AULA DE VÉSPERA 2ª FASE UECE / GABARITO Professor: Michel Henri
 AULA DE VÉSPERA ª FASE UECE / GABARITO Professor: Michel Henri Resposta da questão 1: [E] A equação de Henderson-Hasselbach é válida com melhor aproximação entre ph 4 e ph 10, devido às simplificações
AULA DE VÉSPERA ª FASE UECE / GABARITO Professor: Michel Henri Resposta da questão 1: [E] A equação de Henderson-Hasselbach é válida com melhor aproximação entre ph 4 e ph 10, devido às simplificações
AVALIAÇÃO DA CAPACIDADE DE ADSORÇÃO DE BTEX POR NANOESTRUTURA ADSORVENTE CONFECCIONADA COM ARGILA ESMECTITA DE ORIGEM BRASILEIRA
 AVALIAÇÃO DA CAPACIDADE DE ADSORÇÃO DE BTEX POR NANOESTRUTURA ADSORVENTE CONFECCIONADA COM ARGILA ESMECTITA DE ORIGEM BRASILEIRA J. M. da Costa, G. M.G. Farias², E. F. A. Rebouças³, C. Dalmolin 4 e W.
AVALIAÇÃO DA CAPACIDADE DE ADSORÇÃO DE BTEX POR NANOESTRUTURA ADSORVENTE CONFECCIONADA COM ARGILA ESMECTITA DE ORIGEM BRASILEIRA J. M. da Costa, G. M.G. Farias², E. F. A. Rebouças³, C. Dalmolin 4 e W.
Remoção de Boro de Águas e Efluentes de Petróleo por Adsorção
 Javier Paúl Montalvo Andia Remoção de Boro de Águas e Efluentes de Petróleo por Adsorção Tese de Doutorado Tese apresentada como requisito parcial para obtenção do título de Doutor pelo Programa de Engenharia
Javier Paúl Montalvo Andia Remoção de Boro de Águas e Efluentes de Petróleo por Adsorção Tese de Doutorado Tese apresentada como requisito parcial para obtenção do título de Doutor pelo Programa de Engenharia
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DA PARAÍBA
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DA PARAÍBA PLANO DE ENSINO DADOS DA DISCIPLINA Nome da Disciplina: QUÍMICA II Curso: Controle Ambiental Carga Horária: 80hs Total de Aulas Semanais:
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DA PARAÍBA PLANO DE ENSINO DADOS DA DISCIPLINA Nome da Disciplina: QUÍMICA II Curso: Controle Ambiental Carga Horária: 80hs Total de Aulas Semanais:
CURSO DE CIÊNCIAS BIOLÓGICAS. DISCIPLINA: Química Geral. Assunto: Equilíbrio Químico Docente: Prof a. Dr a. Luciana M. Saran
 CURSO DE CIÊNCIAS BIOLÓGICAS DISCIPLINA: Química Geral Assunto: Equilíbrio Químico Docente: Prof a. Dr a. Luciana M. Saran 1 1. Introdução Existem dois tipos de reações: a) aquelas em que, após determinado
CURSO DE CIÊNCIAS BIOLÓGICAS DISCIPLINA: Química Geral Assunto: Equilíbrio Químico Docente: Prof a. Dr a. Luciana M. Saran 1 1. Introdução Existem dois tipos de reações: a) aquelas em que, após determinado
CARACTERIZAÇÃO E APLICAÇÃO DE CARBONO ATIVADO NA REMOÇÃO DE CORANTES ANIÔNICOS.
 Blucher Chemical Engineering Proceedings Dezembro de 2014, Volume 1, Número 1 X Congresso Brasileiro de Engenharia Química Iniciação Científica Influência da pesquisa em Engenharia Química no desenvolvimento
Blucher Chemical Engineering Proceedings Dezembro de 2014, Volume 1, Número 1 X Congresso Brasileiro de Engenharia Química Iniciação Científica Influência da pesquisa em Engenharia Química no desenvolvimento
USO DE RESÍDUOS TRATADOS PARA ADSORÇÃO DO CORANTE AZUL BRILHANTE REMAZOL EM EFLUENTE SINTÉTICO
 USO DE RESÍDUOS TRATADOS PARA ADSORÇÃO DO CORANTE AZUL BRILHANTE REMAZOL EM EFLUENTE SINTÉTICO J. P. S. FERNANDES 1, A. L. A. CORREA 2, L. B. PIMENTA 2, J. T. CLARO 2, C. A. F. PEREIRA 3 1 Instituto Federal
USO DE RESÍDUOS TRATADOS PARA ADSORÇÃO DO CORANTE AZUL BRILHANTE REMAZOL EM EFLUENTE SINTÉTICO J. P. S. FERNANDES 1, A. L. A. CORREA 2, L. B. PIMENTA 2, J. T. CLARO 2, C. A. F. PEREIRA 3 1 Instituto Federal
ELETROQUÍMICA. Prof a. Dr a. Carla Dalmolin
 ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin CONCEITOS BÁSICOS Eletroquímica Fenômenos químicos associados à transferência de cargas elétricas Duas semi-reações de transferência de carga em direções opostas
ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin CONCEITOS BÁSICOS Eletroquímica Fenômenos químicos associados à transferência de cargas elétricas Duas semi-reações de transferência de carga em direções opostas
QUI 070 Química Analítica IV Análise Quantitativa. Volumetria de Precipitação
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 070 Química Analítica IV Análise Quantitativa Volumetria de Precipitação Lilian Silva Juiz de Fora, 2011 VOLUMETRIA
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 070 Química Analítica IV Análise Quantitativa Volumetria de Precipitação Lilian Silva Juiz de Fora, 2011 VOLUMETRIA
AVALIAÇÃO DA REMOÇÃO DE CROMO UTLIZANDO RESINA MISTA
 AVALIAÇÃO DA REMOÇÃO DE CROMO UTLIZANDO RESINA MISTA Maria A. Barros, e Moilton R. Franco Junior Bolsista de doutorado CAPES, discente do curso de Pós Graduação em Engenharia Química Professor da Faculdade
AVALIAÇÃO DA REMOÇÃO DE CROMO UTLIZANDO RESINA MISTA Maria A. Barros, e Moilton R. Franco Junior Bolsista de doutorado CAPES, discente do curso de Pós Graduação em Engenharia Química Professor da Faculdade
COLÓIDES. Prof. Harley P. Martins filho SISTEMAS COLOIDAIS. Colóide: dispersão de pequenas partículas de um material em outro
 COLÓIDES Prof. Harley P. Martins filho SISTEMAS COLOIDAIS Colóide: dispersão de pequenas partículas de um material em outro Faixa de tamanho das partículas coloidais 10-9 a 10-6 m Classificação geral:
COLÓIDES Prof. Harley P. Martins filho SISTEMAS COLOIDAIS Colóide: dispersão de pequenas partículas de um material em outro Faixa de tamanho das partículas coloidais 10-9 a 10-6 m Classificação geral:
QUÍMICA. Equilíbrio Químico. Sistemas Homogêneos: Constantes: Kc e Kp. Deslocamento do Equilíbrio: Fatores - Parte 3. Prof ª.
 QUÍMICA Equilíbrio Químico Sistemas Homogêneos: Constantes: Kc e Kp. - Parte 3 Prof ª. Giselle Blois Exercício: Sistemas Homogêneos: Constantes: Kc e Kp. 1. (PUC-RS) Um equilíbrio envolvido na formação
QUÍMICA Equilíbrio Químico Sistemas Homogêneos: Constantes: Kc e Kp. - Parte 3 Prof ª. Giselle Blois Exercício: Sistemas Homogêneos: Constantes: Kc e Kp. 1. (PUC-RS) Um equilíbrio envolvido na formação
FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS
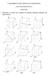 FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS 1 Determine os índices e/ou desenhe as direções cristalinas indicadas nas figuras abaixo. 2 Determineos índices dos planos cristalinos
FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS 1 Determine os índices e/ou desenhe as direções cristalinas indicadas nas figuras abaixo. 2 Determineos índices dos planos cristalinos
BIOADSORÇÃO E DESSORÇÃO DOS ÍONS Cd 2+ E Zn 2+ PELO RESÍDUO DA EXTRAÇÃO DO ALGINATO DA ALGA MARINHA Sargassum filipendula
 BIOADSORÇÃO E DESSORÇÃO DOS ÍONS Cd 2+ E Zn 2+ PELO RESÍDUO DA EXTRAÇÃO DO ALGINATO DA ALGA MARINHA Sargassum filipendula M. T. MUNARO 1, C. BERTAGNOLLI 2, M. G. C. da SILVA 3, S. J. KLEINÜBING 3 e E.
BIOADSORÇÃO E DESSORÇÃO DOS ÍONS Cd 2+ E Zn 2+ PELO RESÍDUO DA EXTRAÇÃO DO ALGINATO DA ALGA MARINHA Sargassum filipendula M. T. MUNARO 1, C. BERTAGNOLLI 2, M. G. C. da SILVA 3, S. J. KLEINÜBING 3 e E.
PLANEJAMENTO EXPERIMENTAL NO ESTUDO DA REMOÇÃO DO VIOLETA CRISTAL UTILIZANDO CAULIM COMO ADSORVENTE.
 PLANEJAMENTO EXPERIMENTAL NO ESTUDO DA REMOÇÃO DO VIOLETA CRISTAL UTILIZANDO CAULIM COMO ADSORVENTE. N. Caponi; J. S. Salla; S. L. Jahn; G. L. Dotto; E. L. Foletto Departamento de Engenharia Química Universidade
PLANEJAMENTO EXPERIMENTAL NO ESTUDO DA REMOÇÃO DO VIOLETA CRISTAL UTILIZANDO CAULIM COMO ADSORVENTE. N. Caponi; J. S. Salla; S. L. Jahn; G. L. Dotto; E. L. Foletto Departamento de Engenharia Química Universidade
Colégio João Paulo I. Questões complementares de Cinética Química. Prof. Cristiano Rupp
 Colégio João Paulo I Questões complementares de Cinética Química Prof. Cristiano Rupp 1- A quimotripsina é uma enzima que catalisa a clivagem heterolítica das ligações peptídicas, processo que faz parte
Colégio João Paulo I Questões complementares de Cinética Química Prof. Cristiano Rupp 1- A quimotripsina é uma enzima que catalisa a clivagem heterolítica das ligações peptídicas, processo que faz parte
ADSORÇÃO DE ÍONS COBRE (Cu 2+ ) EM SOLUÇÃO AQUOSA SINTÉTICA UTILIZANDO RESÍDUO DE BÚZIO NATURAL
 ADSORÇÃO DE ÍONS COBRE (Cu 2+ ) EM SOLUÇÃO AQUOSA SINTÉTICA UTILIZANDO RESÍDUO DE BÚZIO NATURAL L.M. CORREIA 1, A. L. CARNEIRO 1, C.L.C. JÚNIOR 1, R.S. VIEIRA 1 Universidade Federal do Ceará, Departamento
ADSORÇÃO DE ÍONS COBRE (Cu 2+ ) EM SOLUÇÃO AQUOSA SINTÉTICA UTILIZANDO RESÍDUO DE BÚZIO NATURAL L.M. CORREIA 1, A. L. CARNEIRO 1, C.L.C. JÚNIOR 1, R.S. VIEIRA 1 Universidade Federal do Ceará, Departamento
