Configuração Eletrônica
|
|
|
- Lídia Schmidt Vilarinho
- 7 Há anos
- Visualizações:
Transcrição
1 Configuração Eletrônica 1) (ITA) Considere as seguintes espécies químicas no estado gasoso, bem como os respectivos átomos assinalados pelos algarismos romanos: Os orbitais híbridos dos átomos assinalados por I, II, III e IV são respectivamente: A) sp 2, sp 3, dsp 3 e d 2 sp 3. B) sp 2, sp 2, sp 3 e dsp 3. C) sp 3, dsp3, d 2 sp 3 e sp 3. D) sp 3, sp 2, dsp 3 e d 2 sp 3. E) sp, dsp 3, sp 3 e dsp 3. 2) (UPE) Entre as alternativas abaixo, relacionadas com as ligações químicas, escolha a verdadeira. A) Os orbitais híbridos sp 3 d 2 direcionam-se para os vértices de uma pirâmide pentagonal. B) O ângulo entre os átomos de hidrogênio na molécula do gás sulfídrico é maior que entre os átomos de hidrogênio na molécula da água. C) O CF6 2- tem uma geometria octaédrica com os átomos de flúor direcionados para os vértices do octaedro. D) O paramagnetismo da molécula do oxigênio experimentalmente comprovado, sinaliza para uma estrutura de Lewis com elétrons desemparelhados. E) A molécula do oxigênio é diamagnética e não paramagnética, de tal forma que a estrutura de Lewis, na qual todos os elétrons aparecem em pares, está correta. 3) (UECE) Até sua morte, em 1940, Thomson manteve-se afinado com a Física de seu tempo e seu nome permanecerá na história como o cientista que corajosamente dividiu o indivisível e provocou uma mudança de paradigma na história do átomo, tomado como partícula indivisível desde o tempo dos gregos. Com relação ao átomo, assinale a alternativa correta. Em uma camada com n = 4, existem 3 subcamadas Quando n = 6, são possíveis 5 valores do número quântico l Para um elétron em uma subcamada 6d, são permitidos 6 valores de ml Com os números quânticos n = 4, l = 2 e ml = 0, podem existir 6 elétrons 4) (UFSCar) Considere as seguintes propriedades: configuração eletrônica da camada de valência ns 2 np 3 ; boa condutividade elétrica; baixa energia de ionização; alta afinidade eletrônica. A sequência de elementos que apresentam as propriedades relacionadas, na ordem dada, é A) N, Pt, Cl e F.. B) Ca, Cu, K e Br. C) Al, Au, Cl e Na. D) P, Cu, Na e Cl E) As, Cl, K e Br. 5) (ITA) Considere as seguintes configurações eletrônicas de espécies no estado gasoso: I. 1s 2 2s 2 2p 1. II. 1s 2 2s 2 2p 3. III. 1s 2 2s 2 2p 4. IV. 1s 2 2s 2 2p 5. V. 1s 2 2s 2 2p 5 3s 1. Assinale a alternativa ERRADA. A) As configurações I e IV podem representar estados fundamentais de cátions do segundo período da Tabela Periódica. B) As configurações II e III podem representar tanto um estado fundamental como um estado excitado de átomos neutros do segundo período da Tabela Periódica. C) A configuração V pode representar um estado excitado de um átomo neutro do segundo período da Tabela Periódica. D) As configurações II e IV podem representar estados excitados de átomos neutros do segundo período da Tabela Periódica. E) As configurações II, III e V podem representar estados excitados de átomos neutros do segundo período da Tabela Periódica. Resposta: D 6) (FGV - SP) O titânio e seus compostos são amplamente empregados tanto na área metalúrgica como na produção de cosméticos e fármacos. No Brasil, são extraídos os minérios na forma de óxidos, rutilo (TiO2) e ilmenita (FeTiO3). O titânio apresenta o mesmo estado de oxidação nesses dois minérios. O número de oxidação do titânio e a configuração eletrônica da camada de valência do ferro no estado de oxidação em que se encontra na ilmenita são, respectivamente, a) +2 e 3d 6 4s 2. b) +2 e 3d 4 4s 2. c) +3 e 3d 5. d) +4 e 3d 6. e) +4 e 3d 4. 1
2 7) (Vunesp) Os átomos dos elementos X, Y e Z apresentam as seguintes configurações eletrônicas no seu estado fundamental: X 1s 2 2s 2 2p 5 Y 1s 2 2s 2 2p 6 3s 1 Z 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5 É correto afirmar que: a) dentre os citados, o átomo do elemento X tem o maior raio atômico. b) o elemento Y é um metal alcalino e o elemento Z é um halogênio. c) dentre os citados, o átomo do elemento Z tem a maior afinidade eletrônica. d) o potencial de ionização do elemento X é menor do que o do átomo do elemento Z. e) o elemento Z pertence ao grupo 15 (VA) e está no quarto período da classificação periódica. 8) (UERJ) Certo herbicida, cujo uso indiscriminado contamina o solo, pode ser degradado por radiação gama, produzindo, dentre outras, a substância orgânica representada a seguir. O emissor de radiação gama utilizado é o elemento cuja configuração eletrônica, no estado fundamental, é [Ar] 3d7 4s2, e que possui 33 nêutrons em seu núcleo. Indique o isótopo utilizado como emissor gama e escreva os nomes dos compostos que, além de possuírem átomos de cloro ligados a átomos de carbono vizinhos, sejam isômeros de posição da substância orgânica representada. 9) (UFRJ) A solubilidade de vários sais em água em função da temperatura é apresentada no diagrama a seguir: O composto I é formado por átomos cujos subníveis de maior energia, dos estados fundamentais, são 4 s 1 e 5 p 5. O composto II tem o maior calor de dissolução. O composto III é formado por átomos pertencentes ao mesmo período da tabela periódica. O composto IV se decompõe em altas temperaturas, formando nitrito de sódio e oxigênio. Com base nos comentários, no diagrama e na tabela periódica, dê o nome dos compostos I, II, III e IV. 10) (ESPCEX) Considere a distribuição energética crescente, pelos orbitais, dos elétrons de um átomo representativo de elemento de número atômico 26. O último elétron distribuído terá o número quântico magnético igual a zero A)-1 B)-2 C)+1 D)+2 11) (UFRN) Leia as declarações abaixo e, em seguida, assinale a alternativa que apresenta as declarações corretas: l. A eletronegatividade não existe como propriedade do elemento químico isolado: ocorre a partir da relação entre os átomos dos elementos quando os mesmos se ligam. 2. O primeiro potencial de ionização é a energia liberada quando se retira o elétron de maior energia de um átomo gasoso em seu estado fundamental. 3. Os elementos químicos de configuração eletrônica 1s 2 2s 2 2p 6 3s 1 e 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 apresentam baixa energia de ionização. 4. Em um período, considerando-se os elementos representativos, quanto maior a carga nuclear, menor o raio atômico. a) 1, 3 e 4 b) 1, 2 e 3 c) 1, 2 e 4 d) 2, 3 e 4 e) 1, 2 e 4 12) (UFF/1) Conhece-se, atualmente, mais de cem elementos químicos que são, em sua maioria, elementos naturais e, alguns poucos, sintetizados pelo homem. Esses elementos estão reunidos na Tabela Periódica segundo suas características e propriedades químicas. Em particular, os Halogênios apresentam: A) o elétron diferenciador no antepenúltimo nível B) subnível f incompleto C) o elétron diferenciador no penúltimo nível D) subnível p incompleto E) subnível d incompleto 2
3 13) (UFF) Estão representadas por X, Y e Z as configurações eletrônicas fundamentais de três átomos neutros: X 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 Y 1s 2 2s 2 2p 3 Z 1s 2 2s 2 2p 6 3s 2 3p 5 Pode-se concluir que: (A) A espécie formada por X e Z é predominantemente iônica e de fórmula X 2 Z. (B) A espécie formada por Y e Z é predominantemente covalente e de fórmula YZ. (C) A espécie formada por X e Z é predominantemente iônica e de fórmula XZ 2. (D) A espécie formada por X e Y é predominantemente covalente e de fórmula X 2 Y 3. (E) A espécie formada por Y e Z é predominantemente iônica e de fórmula YZ 3. 14) (UECE) O metal mais abundante, em massa, no corpo humano, tem, no estado fundamental, a seguinte configuração eletrônica: Nível 1: completo Nível 2: completo Nível 3: 8 elétrons Nível 4: 2 elétrons A alternativa que indica corretamente esse elemento é: A) Ferro (Z = 26) C) Potássio (Z = 19) B) Cálcio (Z = 20) D) Magnésio (Z = 12) 15) (UFMG) Considerando as partículas constituintes do íon Mg 2+ e a posição do elemento no quadro periódico, pode-se afirmar que esse íon A) apresenta dois níveis completamente preenchidos. B) apresenta números iguais de prótons e elétrons. C) tem um núcleo com 14 prótons. D) tem a mesma configuração eletrônica que o átomo de argônio. 16) (UFC) Uma das estratégias da indústria cosmética na fabricação de desodorantes baseia-se no uso de substâncias que obstruem os poros da pele humana, inibindo a sudorese local. Dentre as substâncias utilizadas, inclui-se o sulfato de alumínio hexahidratado, Al2(SO4)3.6H2O. A configuração eletrônica correta do alumínio, tal como se encontra nessa espécie química, é: a) Idêntica à do elemento neônio b) 1s 2 2s 2 2p 6 3s 2 3p 1 c) Idêntica a do íon Ca 2+ d) 1s 2 2s 2 2p 3 e) (1s 2 2s 2 2p 6 ) 2 17) (UFPR) Uma das estratégias da indústria cosmética na fabricação de desodorantes baseia-se no uso de substâncias que obstruem os poros da pele humana, inibindo a sudorese local. Dentre as substâncias utilizadas, inclui-se o sulfato de alumínio hexahidratado, Al2(SO4)3.6H2O. A configuração eletrônica correta do alumínio, tal como se encontra nessa espécie química, é: idêntica à do elemento neônio 1s 2 2s 2 2p 6 3s 2 3p 1 idêntica a do íon Ca 2+ 1s 2 2s 2 2p 3 (1s 2 2s 2 2p 6 ) 2 18) (Fuvest) As espécies Fe 2+ e Fe 3+, provenientes de isótopos distintos do ferro, diferem entre si, quanto ao número a) atômico e ao número de oxidação. b) atômico e ao raio iônico. c) de prótons e ao número de elétrons. d) de elétrons e ao número de nêutrons. e) de prótons e ao número de nêutrons. 19) (UFPE) Considere os átomos X, Y e Z. O átomo X é um metal alcalino, Y representa um elemento do grupo VA (ou 15) da tabela periódica e Z é um halogênio. Considere que todos os três átomos pertençam ao mesmo período (2 ou 3 ). A partir destas informações julgue as afirmativas abaixo: 0-0) o átomo X possui maior afinidade eletrônica que o átomo Z 1-1) dos três átomos, o átomo Z possui a maior energia de ionização 2-2) os átomos X e Z formarão sólidos cristalinos iônicos 3-3) o íon X + possui raio maior que o íon Y 3 4-4) os átomos Y e Z formam moléculas com ligações covalentes polares 20) (Mack) Uma distribuição eletrônica possível para um elemento X, que pertence à mesma família do elemento bromo, cujo número atômico é igual a 35, é: A) 1s 2, 2s 2, 2p 5 B) 1s 2, 2s 2, 2p 6, 3s 2, 3p 1 C) 1s 2, 2s 2, 2p 2 D) 1s 2, 2s 2, 2p 6, 3s 1 E) 1s 2, 2s 2, 2p 6, 3s 2, 3p 6, 4s 2, 3d 5 21) (UFRJ) O carbono apresenta diferentes formas cristalinas alotrópicas. O diamante, de ocorrência natural rara, tem a mesma estrutura cristalina do silício e do germânio, os quais podem ser empregados na fabricação de dispositivos semicondutores. Recentemente, foi descoberto como produzir diamante com pureza suficiente 3
4 para, também, ser utilizado na fabricação de semicondutores. Identifique, entre os três elementos químicos mencionados, aquele que pertence ao terceiro período da tabela periódica. Escreva seu símbolo e o número total de elétrons do seu nível mais energético. 22) (UFRN) Sejam os elementos Li, Be, C, N e O. A sequência correta da eletronegatividade é: A) Li Be C N O B) O Li N Be C C) Li O N Be C D) O N C Be Li E) N O Be Li O 23) (Uniube) Dos íons, abaixo, aquele(s) que possui(em) o seu último elétron representado em 2 p 6, de acordo com o diagrama de Pauling, é (são): I) 11Na + II) 19K + III) 20Ca 2+ IV) 9F - Assinale a afirmativa correta: A) II, III e IV B) I e IV C) I e III D) II e III 24) (FaE) Ao se transformar em íon estável, um átomo de magnésio (Z = 12) e um átomo de oxigênio (Z = 8), respectivamente: a) perdem-se e ganham-se dois elétrons. b) perde-se e ganha-se um elétron. c) ganham-se e perdem-se três elétrons. d) ganham-se e perdem-se dois elétrons. 25) (PUC - RS/1) 1) Quando se salpica um pouco de cloreto de sódio ou bórax diretamente nas chamas de uma lareira, obtêm-se chamas coloridas. Isso acontece porque nos átomos dessas substâncias os elétrons excitados A) absorvem energia sob forma de luz, neutralizado a carga nuclear e ficando eletricamente neutros. B) retornam a níveis energéticos inferiores, devolvendo energia absorvida sob forma de luz. C) recebem um quantum de energia e distribuem-se ao redor do núcleo em órbitas mais internas. D) emitem energia sob forma de luz e são promovidos para órbitas mais externas. E) saltam para níveis energéticos superiores superando a carga nuclear e originando um ânion. 26) (PUC - RS/1) Considerando-se o cátion de um átomo X que apresenta 11 prótons, 12 nêutrons e 10 elétrons, pode-se afirmar que tal cátion A) pode ser representado por X 2+. B) é maior que o átomo X. C) apresenta número atômico igual a 10. D) é isoeletrônico do ânion O 2-. E) apresenta configuração eletrônica semelhante ao gás nobre argônio. 27) (Unirio) "Anualmente cerca de dez milhões de pilhas, além de 500 mil baterias de telefone celular, são jogadas fora na cidade do Rio de Janeiro. (...) elas têm elementos tóxicos, como o chumbo, mercúrio, zinco e manganês, que provocam graves problemas de saúde. O Globo, 05/01/98. Dos quatro elementos citados, aqueles que possuem, em sua distribuição eletrônica, elétrons desemparelhados são: A) Pb e Zn. B) Pb e Mn. C) Hg e Pb. D) Hg e Zn. E) Zn e Mn. 28) (PUC - RJ) Sobre a estrutura atômica, configuração eletrônica e periodicidade química, é correto afirmar que: a) quando o elétron é excitado e ganha energia, ele salta de uma órbita mais externa para outra mais interna. b) sendo o orbital a região mais provável de se encontrar o elétron, um orbital do subnível p poderá conter no máximo seis elétrons. c) o íon Sr 2+ possui configuração eletrônica 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6. d) devido à sua carga nuclear, o raio atômico do sódio é menor do que o do cloro. e) a energia para remover um elétron do átomo de Mg (1 a energia de ionização) é maior do que aquela necessária para remover um elétron do íon de Mg 1+ (2 a energia de ionização). 4
5 Gabarito 1) Alternativa: A 2) Alternativa: D 3) Alternativa: D 4) Alternativa: D 5) Alternativa: D 6) Alternativa: D 7) Alternativa: B 8) Co 60 2,3 - dicloro-fenol ou 2,3 - dicloro-hidróxi-benzeno 3,4 - dicloro-fenol ou 3,4 - dicloro-hidróxi-benzeno 22) Alternativa: D 23) Alternativa: B 24) Alternativa: A 25) Alternativa: B 26) Alternativa: D 27) Alternativa: B 28) Alternativa: C 9) Resposta: I = Iodeto de Potássio II = Nitrato de Prata III = Cloreto de Sódio IV = Nitrato de Sódio 10) Alternativa: C 11) Alternativa: A 12) Alternativa: D 13) Alternativa: C 14) Alternativa: B 15) Alternativa: A 16) Alternativa: A 17) Resposta: A 18) Alternativa: D 19) Resposta: FVVFV 20) Alternativa: A 21) Resposta: Silício (Si). Número de elétrons no nível mais energético: 4 5
Exercícios de Química Configuração Eletrônica
 Exercícios de Química Configuração Eletrônica 1) (UFPR-1999) Uma das estratégias da indústria cosmética na fabricação de desodorantes baseia-se no uso de substâncias que obstruem os poros da pele humana,
Exercícios de Química Configuração Eletrônica 1) (UFPR-1999) Uma das estratégias da indústria cosmética na fabricação de desodorantes baseia-se no uso de substâncias que obstruem os poros da pele humana,
Distribuição Eletrônica- Aula Cursinho TRIU- 21/05/12. Elétrons. K (n=1) L(n=2) M(n=3) N(n=4) O(n=4) P(n=5) Q(n=6) 2 8 18 32 32 18 8
 Cursinho pré-vestibular- TRIU Prof: Luciana Assis Terra Distribuição Eletrônica- Aula Cursinho TRIU- 21/05/12 Átomo Núcleo Eletrosfera Elétrons Eletrosfera Camadas (níveis) Subcamadas (subníveis) Obs:
Cursinho pré-vestibular- TRIU Prof: Luciana Assis Terra Distribuição Eletrônica- Aula Cursinho TRIU- 21/05/12 Átomo Núcleo Eletrosfera Elétrons Eletrosfera Camadas (níveis) Subcamadas (subníveis) Obs:
LISTA DE EXERCÍCIOS - Tabela Periódica Prof. MSc. Fernanda Palladino
 LISTA DE EXERCÍCIOS - Tabela Periódica Prof. MSc. Fernanda Palladino 1) Indique o período e o grupo dos elementos abaixo : a) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 b) 1s 2 2s 2 2p 6 3s 2 c) 1s 2 2s 2 2p 6 d) 1s
LISTA DE EXERCÍCIOS - Tabela Periódica Prof. MSc. Fernanda Palladino 1) Indique o período e o grupo dos elementos abaixo : a) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 b) 1s 2 2s 2 2p 6 3s 2 c) 1s 2 2s 2 2p 6 d) 1s
EXERCÍCIOS CONFIGURAÇÃO ELETRÔNICA E PROPRIEDADES ATÔMICAS E TENDÊNCIAS PERIÓDICAS
 EXERCÍCIOS CONFIGURAÇÃO ELETRÔNICA E PROPRIEDADES ATÔMICAS E TENDÊNCIAS PERIÓDICAS Questão 1 O cloreto de tionila, SOCl 2, é um importante agente de coloração e um importante agente oxidande em química
EXERCÍCIOS CONFIGURAÇÃO ELETRÔNICA E PROPRIEDADES ATÔMICAS E TENDÊNCIAS PERIÓDICAS Questão 1 O cloreto de tionila, SOCl 2, é um importante agente de coloração e um importante agente oxidande em química
Faculdade Pitágoras de Londrina Disciplina: Química Geral Prof. Me. Thiago Orcelli. Aluno:
 1 Faculdade Pitágoras de Londrina Disciplina:. Aluno: Turma: Exercícios de Fixação englobando conteúdos das Aulas 1-4. Orientação: Escolha um livro de Química Geral disponível na biblioteca e resolva os
1 Faculdade Pitágoras de Londrina Disciplina:. Aluno: Turma: Exercícios de Fixação englobando conteúdos das Aulas 1-4. Orientação: Escolha um livro de Química Geral disponível na biblioteca e resolva os
EXERCÍCIOS DE QUÍMICA 1º ENSINO MÉDIO. 01. Utilizando o esquema de Lewis, dê o íon-fórmula dos compostos constituídos por:
 EXERCÍCIOS DE QUÍMICA 1º ENSINO MÉDIO 01. Utilizando o esquema de Lewis, dê o íon-fórmula dos compostos constituídos por: a) Ca (Z = 20) e F (Z = 9) b) Na (Z = 11) e S (Z = 16) c) K (Z = 19) e O (Z = 8)
EXERCÍCIOS DE QUÍMICA 1º ENSINO MÉDIO 01. Utilizando o esquema de Lewis, dê o íon-fórmula dos compostos constituídos por: a) Ca (Z = 20) e F (Z = 9) b) Na (Z = 11) e S (Z = 16) c) K (Z = 19) e O (Z = 8)
ESTRUTURA ELETRÔNICA DOS ÁTOMOS
 ESTRUTURA ELETRÔNICA DOS ÁTOMOS MECÂNICA QUÂNTICA E OS ORBITAIS ATÔMICOS 1926 Físico austríaco Erwin Schrödinger Equação de onda de Schrödinger Incorpora tanto o comportamento ondulatório como o de partícula
ESTRUTURA ELETRÔNICA DOS ÁTOMOS MECÂNICA QUÂNTICA E OS ORBITAIS ATÔMICOS 1926 Físico austríaco Erwin Schrödinger Equação de onda de Schrödinger Incorpora tanto o comportamento ondulatório como o de partícula
Estudos de Recuperação para Oportunidade Adicional 2010-2º TRIMESTRE Tabela Periódica, Ligações Químicas e Nox
 1 Aluno(a): Nº.: Série: Turma: Data: / / Estudos de Recuperação para Oportunidade Adicional 2010-2º TRIMESTRE Tabela Periódica, Ligações Químicas e Nox 01 - O ferro faz parte da molécula de hemoglobina
1 Aluno(a): Nº.: Série: Turma: Data: / / Estudos de Recuperação para Oportunidade Adicional 2010-2º TRIMESTRE Tabela Periódica, Ligações Químicas e Nox 01 - O ferro faz parte da molécula de hemoglobina
www.professormazzei.com Classificação Periódica Folha 03 - Prof.: João Roberto Mazzei
 Questão 01 Considera-se que quatorze elementos químicos metálicos são essenciais para o correto funcionamento do organismo, portanto indispensáveis para manter a saúde. Os referidos elementos estão listados
Questão 01 Considera-se que quatorze elementos químicos metálicos são essenciais para o correto funcionamento do organismo, portanto indispensáveis para manter a saúde. Os referidos elementos estão listados
Tabela Periódica (localização e propriedades)
 Tabela Periódica (localização e propriedades Questão 01 Três átomos cujos números atômicos são 8, 11 e 17 estão classificados na tabela periódica, respectivamente, como a um gás nobre, um metal alcalino
Tabela Periódica (localização e propriedades Questão 01 Três átomos cujos números atômicos são 8, 11 e 17 estão classificados na tabela periódica, respectivamente, como a um gás nobre, um metal alcalino
Colégio Saint Exupéry
 Colégio Saint Exupéry Apostila QUÍMICA No nosso dia-a-dia o ato de classificar as coisas é algo corriqueiro. Em um faqueiro colocamos em um mesmo espaço as facas, em outro os garfos, etc. Agrupar coisas
Colégio Saint Exupéry Apostila QUÍMICA No nosso dia-a-dia o ato de classificar as coisas é algo corriqueiro. Em um faqueiro colocamos em um mesmo espaço as facas, em outro os garfos, etc. Agrupar coisas
9º ANO ENSINO FUNDAMENTAL -2015
 COLÉGIO NOSSA SENHORA DE LOURDES trimestral Disciplina: Professor (a): QUÍMICA LUIS FERNANDO Roteiro de estudos para recuperação 9º ANO ENSINO FUNDAMENTAL -2015 Conteúdo: Referência para estudo: Sites
COLÉGIO NOSSA SENHORA DE LOURDES trimestral Disciplina: Professor (a): QUÍMICA LUIS FERNANDO Roteiro de estudos para recuperação 9º ANO ENSINO FUNDAMENTAL -2015 Conteúdo: Referência para estudo: Sites
Aula II - Tabela Periódica
 Aula II - Tabela Periódica Tutora: Marcia Mattos Pintos Rio Grande, 16 agosto de 2014. Revisão Átomo: Unidade fundamental da matéria; Partes do átomo: núcleo e eletrosfera. Carga Elétrica das partículas
Aula II - Tabela Periódica Tutora: Marcia Mattos Pintos Rio Grande, 16 agosto de 2014. Revisão Átomo: Unidade fundamental da matéria; Partes do átomo: núcleo e eletrosfera. Carga Elétrica das partículas
Química A Extensivo V. 3
 Química A Extensivo V. 3 Exercícios 01) Respostas: a) Z = 17 1s 2 2s 2 2p 6 3s 2 3p 5 Cl 3 período b) Z = 20 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 Ca 4 período c) Z = 32 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p
Química A Extensivo V. 3 Exercícios 01) Respostas: a) Z = 17 1s 2 2s 2 2p 6 3s 2 3p 5 Cl 3 período b) Z = 20 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 Ca 4 período c) Z = 32 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p
Química. Resolução das atividades complementares. Q33 Distribuição eletrônica
 Resolução das atividades complementares 3 Química Q33 Distribuição eletrônica p. 6 1 (Uniube-MG) Um átomo cuja configuração eletrônica é 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 tem como número atômico: a) 10 c)
Resolução das atividades complementares 3 Química Q33 Distribuição eletrônica p. 6 1 (Uniube-MG) Um átomo cuja configuração eletrônica é 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 tem como número atômico: a) 10 c)
Distribuição Eletrônica Tabela Periódica
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Distribuição Eletrônica Tabela Periódica Orbitais e Números Quânticos N o Quântico Principal Camada Subcamada
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Distribuição Eletrônica Tabela Periódica Orbitais e Números Quânticos N o Quântico Principal Camada Subcamada
C L A S S I F I C A Ç Ã O P E R I Ó D I C A D O S E L E M E N T O S Q U Í M I C O S
 C L A S S I F I C A Ç Ã O P E R I Ó D I C A D O S E L E M E N T O S Q U Í M I C O S PROF. AGAMENON ROBERTO < 2014 CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS QUÍMICOS INTRODUÇÃO No nosso dia-a-dia o ato de classificar
C L A S S I F I C A Ç Ã O P E R I Ó D I C A D O S E L E M E N T O S Q U Í M I C O S PROF. AGAMENON ROBERTO < 2014 CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS QUÍMICOS INTRODUÇÃO No nosso dia-a-dia o ato de classificar
mais vapores do vinho. É, portanto, uma mistura homogênea.
 Resolução das atividades complementares Química p. I. Falsa. As amostras A e B contêm a mesma substância (naftalina). Essas amostras se fundem, portanto, na mesma temperatura. II. Falsa. A temperatura
Resolução das atividades complementares Química p. I. Falsa. As amostras A e B contêm a mesma substância (naftalina). Essas amostras se fundem, portanto, na mesma temperatura. II. Falsa. A temperatura
OLIMPÍADA PIAUIENSE DE QUÍMICA - 2014 Modalidade EF
 OLIMPÍADA PIAUIENSE DE QUÍMICA - 2014 Modalidade EF INSTRUÇÕES 1 Esta prova contém oito questões no total, sendo duas questões abertas e seis questões de múltipla escolha. 2 Antes de iniciar a prova, confira
OLIMPÍADA PIAUIENSE DE QUÍMICA - 2014 Modalidade EF INSTRUÇÕES 1 Esta prova contém oito questões no total, sendo duas questões abertas e seis questões de múltipla escolha. 2 Antes de iniciar a prova, confira
Pode-se dizer que na molécula H Cl as eletrosferas dos átomos H e Cl são, respectivamente, iguais às eletrosferas dos átomos dos gases nobres:
 Questão 01) Um elemento químico A, de número atômico 11, um elemento químico B, de número atômico 8, e um elemento químico C, de número atômico 1, combinam-se formando o composto ABC. As ligações entre
Questão 01) Um elemento químico A, de número atômico 11, um elemento químico B, de número atômico 8, e um elemento químico C, de número atômico 1, combinam-se formando o composto ABC. As ligações entre
WELLINGTON ESTUDO DA TABELA PERIODICA
 WELLINGTON ESTUDO DA TABELA PERIODICA O PRINCÍPIO... Dos atuais 115 elementos químicos conhecidos,cerca de 60 já haviam sido isolados e estudados em 1869,quando o químico russo Dmitri Mendeleev se destacou
WELLINGTON ESTUDO DA TABELA PERIODICA O PRINCÍPIO... Dos atuais 115 elementos químicos conhecidos,cerca de 60 já haviam sido isolados e estudados em 1869,quando o químico russo Dmitri Mendeleev se destacou
ATOMÍSTICA. 18- O ânion NO 3 é isoeletrônico do átomo T. Qual o número atômico de T? A) 15 B) 16 C) 31 D) 32 E) 63
 MODELOS ATÔMICOS 1- (UFMG) Com relação ao modelo atômico de Bohr, a afirmativa FALSA é A) cada órbita eletrônica corresponde a um estado estacionário de energia. B) o elétron emite energia ao passar de
MODELOS ATÔMICOS 1- (UFMG) Com relação ao modelo atômico de Bohr, a afirmativa FALSA é A) cada órbita eletrônica corresponde a um estado estacionário de energia. B) o elétron emite energia ao passar de
10- (UNESP) Nesta tabela periódica, os algarismos romanos substituem os símbolos dos elementos.
 TABELA PERIÓDICA 1- (UNITAU) Considere as seguintes afirmações: I - Quanto menor o raio do íon, maior será sua quantidade de elétrons quando comparado com seu átomo. II - O potencial de ionização aumenta
TABELA PERIÓDICA 1- (UNITAU) Considere as seguintes afirmações: I - Quanto menor o raio do íon, maior será sua quantidade de elétrons quando comparado com seu átomo. II - O potencial de ionização aumenta
1. (G1 - ifsul 2016) Para o processo de purificação da água, são adicionadas substâncias como sulfato de alumínio, A 2(SO 4) 3,
 1. (G1 - ifsul 2016) Para o processo de purificação da água, são adicionadas substâncias como sulfato de alumínio, A 2(SO 4) 3, para formação de flocos com a sujeira da água; cloro, C 2, para desinfecção;
1. (G1 - ifsul 2016) Para o processo de purificação da água, são adicionadas substâncias como sulfato de alumínio, A 2(SO 4) 3, para formação de flocos com a sujeira da água; cloro, C 2, para desinfecção;
Disciplina: Química Átomos e Moléculas e Tabela Periódica
 Disciplina: Química Átomos e Moléculas e Tabela Periódica CURSO DE GRADUAÇÃO Prof. MSc: Fernanda Palladino Belo Horizonte, 12 de março de 2013 Atomos Estrutura e as Principais características do átomo.
Disciplina: Química Átomos e Moléculas e Tabela Periódica CURSO DE GRADUAÇÃO Prof. MSc: Fernanda Palladino Belo Horizonte, 12 de março de 2013 Atomos Estrutura e as Principais características do átomo.
www.professormazzei.com - ATOMÍSTICA Folha 04 João Roberto Mazzei
 Questão 01 Rutherford idealizou um modelo atômico com duas regiões distintas. Esse modelo pode ser comparado a um estádio de futebol com a bola no centro: a proporção entre o tamanho do estádio em relação
Questão 01 Rutherford idealizou um modelo atômico com duas regiões distintas. Esse modelo pode ser comparado a um estádio de futebol com a bola no centro: a proporção entre o tamanho do estádio em relação
Modelos atômicos. Modelo de Bohr
 Modelos atômicos Modelo de Bohr O modelo de Bohr apresenta limitações significativas, não servindo para explicar vários dos fenômenos nos quais estão envolvidos elétrons. As deficiências do modelo de Bohr
Modelos atômicos Modelo de Bohr O modelo de Bohr apresenta limitações significativas, não servindo para explicar vários dos fenômenos nos quais estão envolvidos elétrons. As deficiências do modelo de Bohr
Turma: Terça-feira ( ) Quarta-feira diurno ( ) Quarta-feira noturno ( ) Quinta-feira ( ) Sexta-feira ( ) Nome do aluno ID Assinatura
 005 Lista de exercícios que deve ser entregue no dia da prova (conteúdo: propriedades da matéria, unidades de medidas, estrutura atômica, propriedades eletrônicas e tabela periódica Química para Engenharia
005 Lista de exercícios que deve ser entregue no dia da prova (conteúdo: propriedades da matéria, unidades de medidas, estrutura atômica, propriedades eletrônicas e tabela periódica Química para Engenharia
Períodos (linhas contínuas) Por isso a tabela é chamada de periódica. Algumas propriedades se comportam de maneira periódica.
 Química (profª Simone) Aula 4 - Tabela Periódica Você já colecionou algo? Quando essa coleção vai aumentando surge à necessidade de organização. Os químicos ao longo dos tempos foram descobrindo cada vez
Química (profª Simone) Aula 4 - Tabela Periódica Você já colecionou algo? Quando essa coleção vai aumentando surge à necessidade de organização. Os químicos ao longo dos tempos foram descobrindo cada vez
Distribuição Eletrônica Números Quânticos
 Distribuição Eletrônica Números Quânticos 01. (UFPR-91) Relativamente à configuração eletrônica 2s 2 2p 6 3s 2, são corretas as afirmações: 01. É uma configuração impossível, já que existem elétrons no
Distribuição Eletrônica Números Quânticos 01. (UFPR-91) Relativamente à configuração eletrônica 2s 2 2p 6 3s 2, são corretas as afirmações: 01. É uma configuração impossível, já que existem elétrons no
LIGAÇÕES QUÍMICAS Folha 04 João Roberto Mazzei
 01. Assinale a fórmula de Lewis da molécula HCN. a) H x C xn b) H x C x N c) H x C x N x d) H x C x x N e) Hx C x xn 0. Assinale a alternativa que apresenta, ao mesmo tempo, ligações covalentes e iônicas.
01. Assinale a fórmula de Lewis da molécula HCN. a) H x C xn b) H x C x N c) H x C x N x d) H x C x x N e) Hx C x xn 0. Assinale a alternativa que apresenta, ao mesmo tempo, ligações covalentes e iônicas.
ESTRUTURA GERAL DO ÁTOMO. NÚCLEO - Prótons: p + - Nêutrons: n o. ELETROSFERA - Elétrons: e - o 3) CARGA ATÔMICA E CARGA IÔNICA
 QUÍMICA GERAL ATOMÍSTICA Professor: Ramon Lamar ESTRUTURA GERAL DO ÁTOMO NÚCLEO - Prótons: p + - Nêutrons: n o ELETROSFERA - Elétrons: e - o ) NÚMERO ATÔMICO Corresponde ao número total de prótons presente
QUÍMICA GERAL ATOMÍSTICA Professor: Ramon Lamar ESTRUTURA GERAL DO ÁTOMO NÚCLEO - Prótons: p + - Nêutrons: n o ELETROSFERA - Elétrons: e - o ) NÚMERO ATÔMICO Corresponde ao número total de prótons presente
Educação para toda a vida
 LIGAÇÕES IÔNICAS E COVALENTES Noções sobre Ligações Químicas Regra do Octeto Ligação Iônica ou Eletrovalente Ligação Covalente ou Molecular Ligação Metálica Teoria do Octeto Todos os elementos buscam formas
LIGAÇÕES IÔNICAS E COVALENTES Noções sobre Ligações Químicas Regra do Octeto Ligação Iônica ou Eletrovalente Ligação Covalente ou Molecular Ligação Metálica Teoria do Octeto Todos os elementos buscam formas
Ligação iônica. Prof. Leandro Zatta
 Ligação iônica Prof. Leandro Zatta A molecule is an aggregate of two or more atoms in a definite arrangement held together by chemical forces. H 2 H 2 O NH 3 CH 4 A diatomic molecule contains only two
Ligação iônica Prof. Leandro Zatta A molecule is an aggregate of two or more atoms in a definite arrangement held together by chemical forces. H 2 H 2 O NH 3 CH 4 A diatomic molecule contains only two
Tabela Periódica Parte 2. Classificação dos elementos
 Aula 6 07/04/2016 Tabela Periódica Parte 2 Classificação dos elementos - De acordo com as propriedades físicas dos elementos, eles são subdividos em: Metais: Esses são a maioria dos elementos da tabela
Aula 6 07/04/2016 Tabela Periódica Parte 2 Classificação dos elementos - De acordo com as propriedades físicas dos elementos, eles são subdividos em: Metais: Esses são a maioria dos elementos da tabela
Material Extra de Química
 Material Extra de Química TABELA PERIÓDICA E PROPRIEDADES PERIÓDICAS d) Energia de Ionização: _ NÍVEL BÁSICO 01. Os elementos da tabela periódica encontram-se em ordem crescente de: a) Número de massa.
Material Extra de Química TABELA PERIÓDICA E PROPRIEDADES PERIÓDICAS d) Energia de Ionização: _ NÍVEL BÁSICO 01. Os elementos da tabela periódica encontram-se em ordem crescente de: a) Número de massa.
Exame de Recuperação Curso Profissional de Técnico de Gestão e Programação de Sistemas Informáticos
 Exame de Recuperação Curso Profissional de Técnico de Gestão e Programação de Sistemas Informáticos DISCIPLINA: Física e Química Módulo: Q1 2015/2016 10 ºAno de escolaridade Data: 30 de outubro de 2015
Exame de Recuperação Curso Profissional de Técnico de Gestão e Programação de Sistemas Informáticos DISCIPLINA: Física e Química Módulo: Q1 2015/2016 10 ºAno de escolaridade Data: 30 de outubro de 2015
www.professormazzei.com FUNÇÕES INORGÂNICAS Folha 02 João Roberto Fortes Mazzei
 01. Durante um experimento, seu professor de química pediu que você identificasse as soluções aquosas presentes em cada um dos béqueres (A, B, C) apresentados na figura a seguir. Dois béqueres do experimento
01. Durante um experimento, seu professor de química pediu que você identificasse as soluções aquosas presentes em cada um dos béqueres (A, B, C) apresentados na figura a seguir. Dois béqueres do experimento
PROPRIEDADES PERIÓDICAS
 PROPRIEDADES PERIÓDICAS EXERCÍCIOS DE APLICAÇÃO 01 (PUC-RS) Com relação à classificação periódica dos elementos, pode-se afirmar que o: a) hidrogênio é um metal alcalino localizado na 1ª coluna. b) nitrogênio
PROPRIEDADES PERIÓDICAS EXERCÍCIOS DE APLICAÇÃO 01 (PUC-RS) Com relação à classificação periódica dos elementos, pode-se afirmar que o: a) hidrogênio é um metal alcalino localizado na 1ª coluna. b) nitrogênio
Questão 01 - (UNIFOR CE/2016)
 Instituto Lúcia Vasconcelos - Concursos Públicos e Vestibulares Fone: (62) 3093-1415 Questão 01 - (UNIFOR CE/2016) A charge abaixo apresenta o pensamento filosófico usado na inspiração para a ideia de
Instituto Lúcia Vasconcelos - Concursos Públicos e Vestibulares Fone: (62) 3093-1415 Questão 01 - (UNIFOR CE/2016) A charge abaixo apresenta o pensamento filosófico usado na inspiração para a ideia de
ESTRUTURA DO ÁTOMO. 3. (G1 - cftmg 2016) Sobre as propriedades do íon sulfeto ( ) verdadeiro ou (F) para falso.
 1. (Udesc 2014) O enunciado Em um mesmo átomo, não podem existir dois elétrons com o mesmo conjunto de números quânticos refere-se a(ao): a) Princípio da Exclusão de Pauli. b) Princípio da Conservação
1. (Udesc 2014) O enunciado Em um mesmo átomo, não podem existir dois elétrons com o mesmo conjunto de números quânticos refere-se a(ao): a) Princípio da Exclusão de Pauli. b) Princípio da Conservação
Resolução da Prova de Química Vestibular Inverno UPF 2003 Prof. Emiliano Chemello
 Resolução da Prova de Química Vestibular Inverno UPF 2003 Professor Emiliano Chemello www.quimica.net/emiliano emiliano@quimica.net Questões Resoluções Os óxidos básicos (Oxigênio ligado a um metal de
Resolução da Prova de Química Vestibular Inverno UPF 2003 Professor Emiliano Chemello www.quimica.net/emiliano emiliano@quimica.net Questões Resoluções Os óxidos básicos (Oxigênio ligado a um metal de
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 01 TURMA ANUAL. 05. Item A
 RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS 01. Item B AULA 01 TURMA ANUAL I Correto. Ao passar para um nível mais interno o elétron emite energia na forma de luz. II Falso. Rutherford não propôs um átomo maciço,
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS 01. Item B AULA 01 TURMA ANUAL I Correto. Ao passar para um nível mais interno o elétron emite energia na forma de luz. II Falso. Rutherford não propôs um átomo maciço,
Química A Extensivo V. 4
 Química A Extensivo V. 4 Exercícios Para iniciar o estudo das ligações químicas é interessante conhecer o esquema de formulação a partir das famílias. Veja: Quando se tem as famílias A dos elementos que
Química A Extensivo V. 4 Exercícios Para iniciar o estudo das ligações químicas é interessante conhecer o esquema de formulação a partir das famílias. Veja: Quando se tem as famílias A dos elementos que
ORIENTAÇÃO DE ESTUDOS
 ORIENTAÇÃO DE ESTUDOS RECUPERAÇÃO SEMESTRAL 1º Ano do Ensino Médio Disciplina: Química 1. Considere a tabela a seguir, onde estão relacionados os pontos de fusão e de ebulição de algumas substâncias sob
ORIENTAÇÃO DE ESTUDOS RECUPERAÇÃO SEMESTRAL 1º Ano do Ensino Médio Disciplina: Química 1. Considere a tabela a seguir, onde estão relacionados os pontos de fusão e de ebulição de algumas substâncias sob
ROTEIRO DE ESTUDOS DE QUÍMICA 2 etapa/14 1 Série Ensino Médio
 ROTEIRO DE ESTUDOS DE QUÍMICA 2 etapa/14 1 Série Ensino Médio Aluno (a): Turma n Modelo de Bohr e distribuição eletrônica em níveis e subníveis. Classificação Periódica dos Elementos Químicos Propriedades
ROTEIRO DE ESTUDOS DE QUÍMICA 2 etapa/14 1 Série Ensino Médio Aluno (a): Turma n Modelo de Bohr e distribuição eletrônica em níveis e subníveis. Classificação Periódica dos Elementos Químicos Propriedades
Evolução dos Modelos Atômicos
 Evolução dos Modelos Atômicos 1. (Puc - RS) O átomo, na visão de Thomson, é constituído de a) níveis e subníveis de energia. b) cargas positivas e negativas. c) núcleo e eletrosfera. d) grandes espaços
Evolução dos Modelos Atômicos 1. (Puc - RS) O átomo, na visão de Thomson, é constituído de a) níveis e subníveis de energia. b) cargas positivas e negativas. c) núcleo e eletrosfera. d) grandes espaços
Introdução à Eletroquímica. 1. Gentil V. Corrosão. 3 edição. 2. Cotton F. A. e Wilkinson G. Basic Inorganic Chemistry, John Wiley & Son, USA, 1976.
 Introdução à Eletroquímica 1. Gentil V. Corrosão. 3 edição. 2. Cotton F. A. e Wilkinson G. Basic Inorganic Chemistry, John Wiley & Son, USA, 1976. INTRODUÇÃO Eletroquímica: estuda as relações entre efeitos
Introdução à Eletroquímica 1. Gentil V. Corrosão. 3 edição. 2. Cotton F. A. e Wilkinson G. Basic Inorganic Chemistry, John Wiley & Son, USA, 1976. INTRODUÇÃO Eletroquímica: estuda as relações entre efeitos
Evolução dos Modelos Atômicos A DESCOBERTA DO ÁTOMO
 Evolução dos Modelos Atômicos A DESCOBERTA DO ÁTOMO A DESCOBERTA DAS PARTÍCULAS SUBATÔMICAS Após Dalton ter apresentado sua teoria atômica, em 1808, na qual sugeria que os átomos eram indivisíveis, maciços
Evolução dos Modelos Atômicos A DESCOBERTA DO ÁTOMO A DESCOBERTA DAS PARTÍCULAS SUBATÔMICAS Após Dalton ter apresentado sua teoria atômica, em 1808, na qual sugeria que os átomos eram indivisíveis, maciços
CONFIGURAÇÕES ELETRÔNICAS E PERIODICIDADE QUÍMICA
 CONFIGURAÇÕES ELETRÔNICAS E PERIODICIDADE QUÍMICA A tabela periódica é o guia para a ordem na qual os orbitais são preenchidos. Ela está estruturada de forma que os elementos com o mesmo padrão de configurações
CONFIGURAÇÕES ELETRÔNICAS E PERIODICIDADE QUÍMICA A tabela periódica é o guia para a ordem na qual os orbitais são preenchidos. Ela está estruturada de forma que os elementos com o mesmo padrão de configurações
Previsão das cargas iônicas O número de elétrons que um átomo perde está relacionado com a sua posição na tabela periódica.
 Aula 4 Formação de cátions e ânions Ligações químicas Ións e compostos iônicos Em geral: átomos metálicos tendem a perder elétrons para se transformarem em cátions; íons não-metálicos tendem a ganhar elétrons
Aula 4 Formação de cátions e ânions Ligações químicas Ións e compostos iônicos Em geral: átomos metálicos tendem a perder elétrons para se transformarem em cátions; íons não-metálicos tendem a ganhar elétrons
Proposta de Resolução
 A educação para a cidadania e o sucesso escolar e social dos alunos AGRUPAMENTO DE ESCOLAS DE AVEIRO 160933 Direção Regional de Educação do Centro Ficha de Trabalho Módulo Q1 Física e Química CURSO PROFISSIONAL
A educação para a cidadania e o sucesso escolar e social dos alunos AGRUPAMENTO DE ESCOLAS DE AVEIRO 160933 Direção Regional de Educação do Centro Ficha de Trabalho Módulo Q1 Física e Química CURSO PROFISSIONAL
Tabela Periódica - Avançada
 1. (UERJ/2011) Considere as quatro caixas abaixo, que contêm diferentes materiais residuais de uma indústria: eletronegatividade do outro d) ser um não- e sua última camada 3s 2 3p 2 3p 2. 3. (FUVEST SP/2010)
1. (UERJ/2011) Considere as quatro caixas abaixo, que contêm diferentes materiais residuais de uma indústria: eletronegatividade do outro d) ser um não- e sua última camada 3s 2 3p 2 3p 2. 3. (FUVEST SP/2010)
REVISÃO VESTIBULAR TABELA PERIÓDICA
 REVISÃO VESTIBULAR TABELA PERIÓDICA Histórico da tabela periódica Organizar os elementos químicos em grupos com a finalidade de facilitar o estudo das substâncias derivadas destes, tem sido tarefa árdua,
REVISÃO VESTIBULAR TABELA PERIÓDICA Histórico da tabela periódica Organizar os elementos químicos em grupos com a finalidade de facilitar o estudo das substâncias derivadas destes, tem sido tarefa árdua,
Ligações Químicas s 2 p 6
 ÉRIE RUM A ITA ENIN PRÉ-UNIVERITÁRI PRFER(A) ÉRGI MAT ALUN(A) EDE Nº TC TURMA TURN DATA / / QUÍMICA Ligações Químicas s p 6 Conceitos De todos os elementos químicos conhecidos, somente os gases nobres
ÉRIE RUM A ITA ENIN PRÉ-UNIVERITÁRI PRFER(A) ÉRGI MAT ALUN(A) EDE Nº TC TURMA TURN DATA / / QUÍMICA Ligações Químicas s p 6 Conceitos De todos os elementos químicos conhecidos, somente os gases nobres
Química Inorgânica Aula 3
 Química Inorgânica Aula 3 Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira LIGAÇÕES QUÍMICAS O que são Ligações Químicas? São as ligações que se estabelecem entre a união de dois átomos.
Química Inorgânica Aula 3 Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira LIGAÇÕES QUÍMICAS O que são Ligações Químicas? São as ligações que se estabelecem entre a união de dois átomos.
Prof. M.Sc. Maron Stanley S. O. Gomes
 Ligações químicas, símbolos e a regra do octeto Prof. M.Sc. Maron Stanley S.. Gomes Ligação química: é a força atrativa que mantém dois ou mais átomos unidos. Ligação covalente: resulta do compartilhamento
Ligações químicas, símbolos e a regra do octeto Prof. M.Sc. Maron Stanley S.. Gomes Ligação química: é a força atrativa que mantém dois ou mais átomos unidos. Ligação covalente: resulta do compartilhamento
A Ciência Central. David P. White
 QUÍMICA A Ciência Central 9ª Edição Capítulo 8 Conceitos básicos b de ligação química David P. White Ligações químicas, símbolos s de Lewis e a regra do octeto Ligação química: é a força atrativa que mantém
QUÍMICA A Ciência Central 9ª Edição Capítulo 8 Conceitos básicos b de ligação química David P. White Ligações químicas, símbolos s de Lewis e a regra do octeto Ligação química: é a força atrativa que mantém
CLASSIFICAÇÃO PERIÓDICA
 CLASSIFICAÇÃO PERIÓDICA 1. O elemento cloro apresenta dois isótopos mais abundantes na natureza, um com 18 nêutrons e o outro com 20 nêutrons. a) Determine os números de massa desses dois isótopos do cloro.
CLASSIFICAÇÃO PERIÓDICA 1. O elemento cloro apresenta dois isótopos mais abundantes na natureza, um com 18 nêutrons e o outro com 20 nêutrons. a) Determine os números de massa desses dois isótopos do cloro.
Profª.. Carla da Silva Meireles
 Estrutura eletrônica dos átomos Profª.. Carla da Silva Meireles O que fazem os elétrons? Como eles se mantém em órbita? As leis da física eram insatisfatórias para descrever movimento de partículas tão
Estrutura eletrônica dos átomos Profª.. Carla da Silva Meireles O que fazem os elétrons? Como eles se mantém em órbita? As leis da física eram insatisfatórias para descrever movimento de partículas tão
M A S S A S E M E D I D A S
 M A S S A S E M E D I D A S PROF. AGAMENON ROBERTO < 2010 > Prof. Agamenon Roberto ATOMÍSTICA www.agamenonquimica.com 2 MASSAS E MEDIDAS UNIDADE DE MASSA ATÔMICA (u.m.a.) Para pesar ou medir algo se torna
M A S S A S E M E D I D A S PROF. AGAMENON ROBERTO < 2010 > Prof. Agamenon Roberto ATOMÍSTICA www.agamenonquimica.com 2 MASSAS E MEDIDAS UNIDADE DE MASSA ATÔMICA (u.m.a.) Para pesar ou medir algo se torna
Polaridade e Geometria Molecular
 Polaridade e Geometria Molecular Prof. Leandro Zatta Prof. Leandro Zatta 1 Conceitos Prof. Leandro Zatta 2 Eletronegatividade Polaridade de ligação Momentos de dipolo Geometria molecular Modelo de ligação
Polaridade e Geometria Molecular Prof. Leandro Zatta Prof. Leandro Zatta 1 Conceitos Prof. Leandro Zatta 2 Eletronegatividade Polaridade de ligação Momentos de dipolo Geometria molecular Modelo de ligação
TP064 - CIÊNCIA DOS MATERIAIS PARA EP. FABIANO OSCAR DROZDA
 TP064 - CIÊNCIA DOS MATERIAIS PARA EP FABIANO OSCAR DROZDA fabiano.drozda@ufpr.br 1 AULA 02 ESTRUTURA ATÔMICA e LIGAÇÃO ATÔMICA CAPÍTULO 02 CALLISTER 5 a Ed. 2 ESTRUTURA ATÔMICA Modelo atômico de Bohr
TP064 - CIÊNCIA DOS MATERIAIS PARA EP FABIANO OSCAR DROZDA fabiano.drozda@ufpr.br 1 AULA 02 ESTRUTURA ATÔMICA e LIGAÇÃO ATÔMICA CAPÍTULO 02 CALLISTER 5 a Ed. 2 ESTRUTURA ATÔMICA Modelo atômico de Bohr
5- Formam substância iônica do tipo AB 2 A) III e I B) III e II C) IV e I D) V e I E) V e II
 LIGAÇÕES QUÍMICAS 1- Uma ligação de caráter acentuadamente iônico se estabelece quando os átomos participantes da ligação: A) possuem números de oxidação acentuadamente diferentes. B) apresentam elétrons
LIGAÇÕES QUÍMICAS 1- Uma ligação de caráter acentuadamente iônico se estabelece quando os átomos participantes da ligação: A) possuem números de oxidação acentuadamente diferentes. B) apresentam elétrons
4.1. Tabela Periódica e a configuração electrónica dos elementos
 4.1. Tabela Periódica e a configuração electrónica dos elementos Breve história O químico alemão Johann Döbereiner, por volta de 1830, descobriu que havia conjuntos de três elementos com propriedades semelhantes
4.1. Tabela Periódica e a configuração electrónica dos elementos Breve história O químico alemão Johann Döbereiner, por volta de 1830, descobriu que havia conjuntos de três elementos com propriedades semelhantes
II OLimpíada Brasileira de Química Júnior - Fase II
 II OLimpíada Brasileira de Química Júnior - Fase II 17/10/2009 - II OBQjr 2009 INSTRUÇÕES: II Olimpíada Brasileira de Química Júnior Exames - Fase II 1. A prova consta de 25 questões, cada uma contém quatro
II OLimpíada Brasileira de Química Júnior - Fase II 17/10/2009 - II OBQjr 2009 INSTRUÇÕES: II Olimpíada Brasileira de Química Júnior Exames - Fase II 1. A prova consta de 25 questões, cada uma contém quatro
VIII OSEQUIM Olimpíada Sergipana de Química 1ª. Etapa Modalidade A
 Bom dia aluno! Está é a prova da primeira etapa da OSEQUIM, Olimpíada Sergipana de Química 2014, modalidade A, para alunos que se encontram cursando o 1º. Ano do ensino médio em 2014. Confira se a sua
Bom dia aluno! Está é a prova da primeira etapa da OSEQUIM, Olimpíada Sergipana de Química 2014, modalidade A, para alunos que se encontram cursando o 1º. Ano do ensino médio em 2014. Confira se a sua
PROF: Alex LISTA 13 DATA: 30/07/2013 Para estudar: Tabela Periódica
 NOME: PROF: Alex LISTA 13 DATA: 30/07/2013 Para estudar: Tabela Periódica 01 - (UEPB) A Tabela Periódica dos s químicos é uma das maiores descobertas científicas do mundo. Pode ser comparada em importância
NOME: PROF: Alex LISTA 13 DATA: 30/07/2013 Para estudar: Tabela Periódica 01 - (UEPB) A Tabela Periódica dos s químicos é uma das maiores descobertas científicas do mundo. Pode ser comparada em importância
Metais. Grande número de entidades iguais mantidas coesas em um retículo cristalino.
 Ligações Metálicas Grande número de entidades iguais mantidas coesas em um retículo cristalino. Metais Não pode ser explicado pela teoria das ligações covalentes o arranjo dos metais não segue o padrão
Ligações Metálicas Grande número de entidades iguais mantidas coesas em um retículo cristalino. Metais Não pode ser explicado pela teoria das ligações covalentes o arranjo dos metais não segue o padrão
Ligações Iônicas. Tipos de Ligações
 Ligações Iônicas Tipos de Ligações Existem diversos tipos de ligações para se considerar quando analisar a composição química de um composto. Uma ligação pode ser definida como uma força que prende grupos
Ligações Iônicas Tipos de Ligações Existem diversos tipos de ligações para se considerar quando analisar a composição química de um composto. Uma ligação pode ser definida como uma força que prende grupos
TABELA PERIÓDICA FAMÍLIAS DOS ELEMENTOS QUÍMICOS
 TABELA PERIÓDICA A grande diversidade de elementos químicos levou à sua organização de acordo com as suas propriedades físicas e químicas. A Tabela Periódica que hoje conhecemos foi sofrendo alterações
TABELA PERIÓDICA A grande diversidade de elementos químicos levou à sua organização de acordo com as suas propriedades físicas e químicas. A Tabela Periódica que hoje conhecemos foi sofrendo alterações
Questão Aula. Curso Profissional de Técnico de Gestão e Programação de Sistemas Informáticos
 Questão Aula Curso Profissional de Técnico de Gestão e Programação de Sistemas Informáticos DISCIPLINA: Física e Química Módulo: Q1 2015/2016 10 ºAno de escolaridade Duração: 90 minutos Nome: N.º 8 páginas
Questão Aula Curso Profissional de Técnico de Gestão e Programação de Sistemas Informáticos DISCIPLINA: Física e Química Módulo: Q1 2015/2016 10 ºAno de escolaridade Duração: 90 minutos Nome: N.º 8 páginas
QUÍMICA GERAL PROF. PAULO VALIM
 QUÍMICA GERAL PROF. PAULO VALIM 5 LIGAÇÕES QUÍMICAS Gás Nobre para catalisar sua reação, vamos disponibilizar alguns exercícios com gabarito ao final de cada capítulo de estudo. Eles não fazem parte dos
QUÍMICA GERAL PROF. PAULO VALIM 5 LIGAÇÕES QUÍMICAS Gás Nobre para catalisar sua reação, vamos disponibilizar alguns exercícios com gabarito ao final de cada capítulo de estudo. Eles não fazem parte dos
II Correto. Quanto maior a distância entre as cargas, mais fraca é a ligação e menos energia é empregada na sua quebra.
 01. Item B I Correto. A energia para quebrar a ligação H (568 kj/mol) é a maior da tabela. Isto torna mais difícil a sua quebra, portanto ionizando menos o ácido que passa a ser o mais fraco entre os listados.
01. Item B I Correto. A energia para quebrar a ligação H (568 kj/mol) é a maior da tabela. Isto torna mais difícil a sua quebra, portanto ionizando menos o ácido que passa a ser o mais fraco entre os listados.
Aula 2: Estrutura Atômica
 Aula 2: Estrutura Atômica Histórico u Grécia Antiga: Alquimistas (400 a.c.) - Matéria consiste de partículas distintas indivisíveis (átomos) - Ausência de evidências experimentais u Teoria Atômica dos
Aula 2: Estrutura Atômica Histórico u Grécia Antiga: Alquimistas (400 a.c.) - Matéria consiste de partículas distintas indivisíveis (átomos) - Ausência de evidências experimentais u Teoria Atômica dos
1
 Níveis de dificuldade das Questões Fácil Pontifícia Universidade Católica do Rio Grande do Sul Médio Difícil Resolução da Prova de Química Vestibular Verão PUCRS 2005 Prof. Emiliano Chemello www.quimica.net/emiliano
Níveis de dificuldade das Questões Fácil Pontifícia Universidade Católica do Rio Grande do Sul Médio Difícil Resolução da Prova de Química Vestibular Verão PUCRS 2005 Prof. Emiliano Chemello www.quimica.net/emiliano
Propriedades Elétricas do Materiais
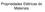 Propriedades Elétricas do Materiais Por que estudar propriedades elétricas dos materiais? Apreciação das propriedades elétricas de materiais é muitas vezes importante, quando na seleção de materiais e
Propriedades Elétricas do Materiais Por que estudar propriedades elétricas dos materiais? Apreciação das propriedades elétricas de materiais é muitas vezes importante, quando na seleção de materiais e
TEORIA DOS ORBITAIS MOLECULARES -TOM
 TEORIA DOS ORBITAIS MOLECULARES -TOM TOM - Importância - Elucidar alguns aspectos da ligação não explicados pelas estruturas de Lewis, pela teoria da RPENV e pela hibridização. - Exemplo: Por que o O 2
TEORIA DOS ORBITAIS MOLECULARES -TOM TOM - Importância - Elucidar alguns aspectos da ligação não explicados pelas estruturas de Lewis, pela teoria da RPENV e pela hibridização. - Exemplo: Por que o O 2
1ª série / EM. a) HSe e HS. d) H2Se e H2S. c) HSe e H2S. e) H3Se e H3S
 SECRETARIA DE SEGURANÇA PÚBLICA/SECRETARIA DE EDUCAÇÃO POLÍCIA MILITAR DO ESTADO DE GOIÁS COMANDO DE ENSINO POLICIAL MILITAR COLÉGIO DA POLÍCIA MILITAR NADER ALVES DOS SANTOS SÉRIE/ANO: 1ª TURMA(S): DISCIPLINA:
SECRETARIA DE SEGURANÇA PÚBLICA/SECRETARIA DE EDUCAÇÃO POLÍCIA MILITAR DO ESTADO DE GOIÁS COMANDO DE ENSINO POLICIAL MILITAR COLÉGIO DA POLÍCIA MILITAR NADER ALVES DOS SANTOS SÉRIE/ANO: 1ª TURMA(S): DISCIPLINA:
AULA 09 Tabela periódica e propriedades periódicas
 AULA 09 Tabela periódica e propriedades periódicas Em nossas aulas passadas aprendemos a respeito da composição dos átomos, suas subpartículas (prótons, elétrons e nêutrons) e como a distribuição dessas
AULA 09 Tabela periódica e propriedades periódicas Em nossas aulas passadas aprendemos a respeito da composição dos átomos, suas subpartículas (prótons, elétrons e nêutrons) e como a distribuição dessas
Np X U. 03) (ITA-SP) Considere as seguintes equações relativas a processos nucleares:
 01) (Uesb-BA) A radioatividade emitida por determinadas amostras de substâncias provém: a) da energia térmica liberada em sua combustão. b) de alterações em núcleos de átomos que as formam. c) de rupturas
01) (Uesb-BA) A radioatividade emitida por determinadas amostras de substâncias provém: a) da energia térmica liberada em sua combustão. b) de alterações em núcleos de átomos que as formam. c) de rupturas
Por que os átomos de diferentes elementos se combinam para formar compostos? Moléculas Formadas. Mais estáveis que elementos individuais
 LIGAÇÕES QUÍMICAS Por que os átomos de diferentes elementos se combinam para formar compostos? Moléculas Formadas Mais estáveis que elementos individuais Por que os átomos de diferentes elementos se combinam
LIGAÇÕES QUÍMICAS Por que os átomos de diferentes elementos se combinam para formar compostos? Moléculas Formadas Mais estáveis que elementos individuais Por que os átomos de diferentes elementos se combinam
EXERCÍCIOS. A 50ºC, encontram se no estado líquido: a) cloro e flúor. b) cloro e iodo. c) flúor e bromo. d) bromo e mercúrio. e) mercúrio e iodo.
 EXERCÍCIOS 1. (Cespe/UnB) Os diagramas representam modelos de substâncias simples, compostas e/ou misturas. As esferas claras, escuras, listradas, etc., ou de tamanhos variados representam átomos diferentes.
EXERCÍCIOS 1. (Cespe/UnB) Os diagramas representam modelos de substâncias simples, compostas e/ou misturas. As esferas claras, escuras, listradas, etc., ou de tamanhos variados representam átomos diferentes.
Átomos Moléculas Íons Biomoléculas. Matéria é formada por Átomos. Obs.: teoria confirmada apenas no início do século XX.
 Átomos Moléculas Íons Biomoléculas Estrutura da Matéria Matéria é formada por Átomos Obs.: teoria confirmada apenas no início do século XX. Os átomos dificilmente existem livres e possuem grande tendência
Átomos Moléculas Íons Biomoléculas Estrutura da Matéria Matéria é formada por Átomos Obs.: teoria confirmada apenas no início do século XX. Os átomos dificilmente existem livres e possuem grande tendência
FÍSICA APLICADA A RADIOLOGIA. Proº. Lillian Lemos E-mail: lillianlemos@yahoo.com.br
 FÍSICA APLICADA A RADIOLOGIA Proº. Lillian Lemos E-mail: lillianlemos@yahoo.com.br ESTADOS DA MATÉRIA Três tipos: -Estado Fundamental -Estado Excitado -Estado Ionizado ESTADOS DA MATÉRIA Estado Fundamental:
FÍSICA APLICADA A RADIOLOGIA Proº. Lillian Lemos E-mail: lillianlemos@yahoo.com.br ESTADOS DA MATÉRIA Três tipos: -Estado Fundamental -Estado Excitado -Estado Ionizado ESTADOS DA MATÉRIA Estado Fundamental:
A História da Tabela Periódica
 A História da Tabela Periódica Um pré-requisito necessário para construção da tabela periódica, foi a descoberta individual dos elementos químicos. Embora os elementos, tais como ouro (Au), prata (Ag),
A História da Tabela Periódica Um pré-requisito necessário para construção da tabela periódica, foi a descoberta individual dos elementos químicos. Embora os elementos, tais como ouro (Au), prata (Ag),
CONCEITOS DE BRÖNSTED-LOWRY CONCEITOS DE ÁCIDOS E BASES CONCEITOS DE ARRHENIUS. Ácido: Ácido: HCN + H O H O + - Base ou hidróxido: Base: + +
 Ácido: CONCEITOS DE ÁCIDOS E BASES CONCEITOS DE ARRENIUS Toda substância que em solução aquosa, sofre ionização, produzindo como cátion, apenas o íon CN O ( aq ) CN ( aq ) Na realidade, o íon, quando em
Ácido: CONCEITOS DE ÁCIDOS E BASES CONCEITOS DE ARRENIUS Toda substância que em solução aquosa, sofre ionização, produzindo como cátion, apenas o íon CN O ( aq ) CN ( aq ) Na realidade, o íon, quando em
Materiais cerâmicos Definições
 MATERIAIS CERÂMICOS Materiais cerâmicos Definições São compostos inorgânicos formados pela combinação de elementos metálicos e não metálicos. Do ponto de vista das ligações químicas, estas podem ser totalmente
MATERIAIS CERÂMICOS Materiais cerâmicos Definições São compostos inorgânicos formados pela combinação de elementos metálicos e não metálicos. Do ponto de vista das ligações químicas, estas podem ser totalmente
a) apenas I. b) apenas I e III. c) apenas II e III. d) apenas I e II. e) todas. Profa. Graça Porto
 www.agraçadaquímica.com.br BANCO DE QUESTÕES - FÍSICO-QUÍMICA ELETRÓLISE (12 questões) 1. (UFF) Quando uma solução aquosa de Li 2 SO 4 é eletrolizada, os produtos formados no ânodo e no cátodo são, respectivamente:
www.agraçadaquímica.com.br BANCO DE QUESTÕES - FÍSICO-QUÍMICA ELETRÓLISE (12 questões) 1. (UFF) Quando uma solução aquosa de Li 2 SO 4 é eletrolizada, os produtos formados no ânodo e no cátodo são, respectivamente:
~ 1 ~ IX Olimpíada de Química do Rio Grande do Sul 2010 PARTE 1 TESTES DE ESCOLHA SIMPLES
 Questão 2: Abaixo se encontra um esquema ilustrando dois frascos, um com água e outro com álcool. No quadro têm-se três diferentes materiais, A, B e C, todos sólidos e insolúveis em água e álcool. Considerando
Questão 2: Abaixo se encontra um esquema ilustrando dois frascos, um com água e outro com álcool. No quadro têm-se três diferentes materiais, A, B e C, todos sólidos e insolúveis em água e álcool. Considerando
APLICAÇÕES DOS METAIS
 APLICAÇÕES DOS METAIS Os metais aplicam-se nos três setores de atividades humanas. No setor primário têm diversas aplicações, tais como, embarcações, motores e alfaias agrícolas. No setor secundário podem-se
APLICAÇÕES DOS METAIS Os metais aplicam-se nos três setores de atividades humanas. No setor primário têm diversas aplicações, tais como, embarcações, motores e alfaias agrícolas. No setor secundário podem-se
QUÍMICA Aula 4. Leis Naturais da Química e Modelos Atômicos
 QUÍMICA Aula 4 Leis Naturais da Química e Modelos Atômicos No final do séc. XVIII, o cientista Antoine Lavoisier realizou uma série de experiências em recipientes fechados e efetuando pesagens com balanças
QUÍMICA Aula 4 Leis Naturais da Química e Modelos Atômicos No final do séc. XVIII, o cientista Antoine Lavoisier realizou uma série de experiências em recipientes fechados e efetuando pesagens com balanças
PERÍODO CAMADA NÚMERO DE ELEMENTOS
 I. INTRODUÇÃO No nosso dia-a-dia o ato de classificar as coisas é algo corriqueiro. Em um faqueiro colocamos em um mesmo espaço as facas, em outro os garfos, etc. Agrupar coisas semelhantes facilita a
I. INTRODUÇÃO No nosso dia-a-dia o ato de classificar as coisas é algo corriqueiro. Em um faqueiro colocamos em um mesmo espaço as facas, em outro os garfos, etc. Agrupar coisas semelhantes facilita a
Dicas de Química Tasso
 Dicas de Química Tasso Questão 01) Considere a reação química representada pela equação: 2Fe 2 S 3(s) + 6H 2 O (l) +3O 2(g) 4Fe(OH) 3(s) +6S (s) Calcule a quantidade de (em mols) de Fe(OH) 3 que pode ser
Dicas de Química Tasso Questão 01) Considere a reação química representada pela equação: 2Fe 2 S 3(s) + 6H 2 O (l) +3O 2(g) 4Fe(OH) 3(s) +6S (s) Calcule a quantidade de (em mols) de Fe(OH) 3 que pode ser
Estudo da Química. Profº André Montillo www.montillo.com.br
 Estudo da Química Profº André Montillo www.montillo.com.br Química Definição: Química - do egípcio kēme (chem) que significa "terra. É a ciência que estuda as substâncias da natureza, os elementos que
Estudo da Química Profº André Montillo www.montillo.com.br Química Definição: Química - do egípcio kēme (chem) que significa "terra. É a ciência que estuda as substâncias da natureza, os elementos que
Escola Secundária de Casquilhos Teste 1 de Física e Química A 10º ANO 22/10/2013 90 minutos
 Escola Secundária de Casquilhos Teste 1 de Física e Química A 10º ANO 22/10/2013 90 minutos NOME Nº Turma Informação Professor Enc. de Educação 1. Os átomos dos isótopos e do carbono têm (A) números atómicos
Escola Secundária de Casquilhos Teste 1 de Física e Química A 10º ANO 22/10/2013 90 minutos NOME Nº Turma Informação Professor Enc. de Educação 1. Os átomos dos isótopos e do carbono têm (A) números atómicos
Mg + 2 Cl MgCl2 E, como terceiro exemplo, a reação entre o alumínio e o. Al + 3 F AlF3 Como podemos observar, o número de íons que se.
 I. INTRODUÇÃO. Existe uma grande quantidade de substâncias na natureza e, isto se deve à capacidade de átomos iguais ou diferentes se combinarem entre si. Um grupo muito pequeno de átomos aparece na forma
I. INTRODUÇÃO. Existe uma grande quantidade de substâncias na natureza e, isto se deve à capacidade de átomos iguais ou diferentes se combinarem entre si. Um grupo muito pequeno de átomos aparece na forma
ferro bromo brometo de ferro 40g 120g 0g 12g 0g 148g 7g 40g 0g 0g x g 37g
 01) (FCMSC-SP) A frase: Do nada, nada; em nada, nada pode transformar-se relaciona-se com as idéias de: a) Dalton. b) Proust. c) Boyle. d) Lavoisier. e) Gay-Lussac. 02) Acerca de uma reação química, considere
01) (FCMSC-SP) A frase: Do nada, nada; em nada, nada pode transformar-se relaciona-se com as idéias de: a) Dalton. b) Proust. c) Boyle. d) Lavoisier. e) Gay-Lussac. 02) Acerca de uma reação química, considere
Analogia com a polarização elétrica
 Analogia com a polarização elétrica Polarização orientação de dipolos elétricos, devido à ação de um campo elétrico. Magnetização - orientação de dipolos magnéticos, devido à ação de um campo magnético.
Analogia com a polarização elétrica Polarização orientação de dipolos elétricos, devido à ação de um campo elétrico. Magnetização - orientação de dipolos magnéticos, devido à ação de um campo magnético.
2005 by Pearson Education. Capítulo 09
 QUÍMICA A Ciência Central 9ª Edição Capítulo 9: Geometria molecular e teorias de ligação David P. White Formas espaciais moleculares As estruturas de Lewis fornecem a conectividade atômica: elas nos mostram
QUÍMICA A Ciência Central 9ª Edição Capítulo 9: Geometria molecular e teorias de ligação David P. White Formas espaciais moleculares As estruturas de Lewis fornecem a conectividade atômica: elas nos mostram
