Ácidos e Bases. Os ácidos e bases fortes encontram-se completamente ionizados quando em solução aquosa. HCl H + + Cl - NaOH Na + + OH -
|
|
|
- Pietra Gil Chaves
- 7 Há anos
- Visualizações:
Transcrição
1 Ácidos e Bases Os ácidos e bases fortes encontram-se completamente ionizados quando em solução aquosa. HCl H + + Cl - NaOH Na + + OH -
2 Em sistemas biológicos os ácidos e bases fracas são bastante importantes Os ácidos e bases fracas não estão completamente ionizados quando dissolvidos na água
3 Par ácido-base conjugado Um doador de próton e seu receptor = par ácidobase conjugado (teoria de Bronsted-Lorry).
4
5 Cada ácido tem uma tendência para perder o seu próton em solução aquosa. Quanto mais forte é o ácido, maior a tendência para perder o próton. A tendência de qualquer ácido perder um próton e formar a sua base conjugada é definida pela constante de equilíbrio da reação reversível.
6 As constantes de equilíbrio para reações de ionização são chamadas de constante de dissociação São geralmente designadas por K a
7 Os valores de pka são análogos ao ph e são definidos pela equação: Quanto mais fortemente um ácido se dissocia, menor éo seu pka
8 Constantes de dissociação de alguns ácidos. Os ácidos mais fortes como o fórmico tem constante de dissociação maiores
9
10 A curva de titulação revela o pka dos ácidos fracos A curva de titulação é usada para determinar a concentração de um ácido em uma solução.
11
12 No início da titulação, antes que qualquer NaOH seja adicionado, o ácido acético já está ligeiramente ionizado, em uma extensão que pode ser calculada a partir da sua constante de ionização.
13
14 Ação tamponante contra variações de ph Quase todos os processos biológicos são dependentes de ph As enzimas que catalisam as reações celulares e muitas das biomoléculas possuem grupos ionizáveis com valores de pka característicos As células e os organismos mantêm um ph citosólico constante e específico, geralmente próximo de ph 7,0, que mantém as biomoléculas em seu iônico ótimo
15 Os tampões são misturas de ácidos fracos e suas bases conjugadas Os tampões são misturas que em solução aquosa dão a estas soluções a propriedade de resistir às variações de ph A região de tamponamento pode ser reconhecida na curva de titulação de um ácido fraco. No ponto médio da região tamponante, onde a concentração do doador se iguala a do receptor, o poder tamponante é máximo.
16
17
18 A equação de Henderson-Hasselbalch A relação quantitativa entre o valor do ph, a ação tamponante da mistura ácido-fraco/base conjugada e o pka do ácido graco é dada pela equação de Henderson- Hasselbalch. As curvas de titulação dos ácidos fracos têm formas quase idênticas sugerindo que todas elas refletem uma relação fundamental. As curvas são expressas pela equação de Henderson- Hasselbalch.
19 é apenas uma forma útil de redefinir a expressão para a constante de dissociação de um ácido fraco.
20 de uma forma mais genérica:
21 Com essa equação, fica fácil demonstrar que:
22
23
24
25 Os ácidos gracos e as bases fracas tamponam as células e os tecidos O citoplasma das células contém altas concentrações de proteínas, que possuem muitos aminoácidos com grupos funcionais que são ou ácidos ou bases fracas. A cadeia lateral do aminoácido histidina, por exemplo, tem um pka de 6,0 e proteínas contendo resíduos de histidina podem tamponar ao redor do ph neutro.
26
27 O fosfato e o bicarbonato são tampões biológicos importantes A primeira linha de defesa dos organismos contra variações do ph interno é fornecida pelos tampões. Dois dos tampões biológicos importantes são o sistema fosfato e bicarbonato. O sistema tampão fosfato, age no citoplasma de todas as células.
28 O tampão fosfato é tamponante efetivo dos fluidos intracelulares pka= 6,86 (resiste às variações entre ph 6,4-7,4) nos mamíferos, os fluidos extracelulares e a maioria dos compartimentos citoplasmáticos tem ph n aregião de 6,9-7,4
29 O plasma sanguíneo é tamponado em parte, pelo sistema tampão bicarbonato, que consiste de ácido carbônico como doador de prótons (H 2 CO 3 ) e do bicarbonato (HCO 3- ) como receptor.
30
31
32 o CO 2 éum gás em condições normais e a concentração de CO 2 dissolvido é:
33 o ph do sistema tampão bicarbonato O ph do sistema tampão bicarbonato depende da [H 2 CO 3 ] e [HCO 3- ] A [H 2 CO 3 ] depende do CO 2 (d) O CO 2 (d) depende da concentração ou da pressão parcial do CO 2 na fase gasosa.
34
35 Sangue, pulmões e tampões Nos animais com pulmões, o sistema tampão bicarbonato é um tampão fisiológico efetivo em ph próximo a 7,4 O pka do ácido carbônico (H 2 CO 3 ) = 3,77 Isso é possível porque o H 2 CO 3 do plasma sanguíneo está em equilíbrio com um grande reservatório de CO 2 localizado no espaço aéreo do pulmão. A concentração de CO 2 dissolvido pode ser ajustada rapidamente através da respiração pulmonar.
36 O controle do ph sanguíneo O tampão bicarbonato é um importante tampão dos fluidos corporais. A concentrações de bicarbonato e ácido carbônico são reguladas pelo sistema respiratório e pelos rins.
37 O controle respiratório do ph O mecanismo de controle respiratório do ph do sangue começa no cérebro com neurônios de controle do centro respiratório que são sensíveis aos níveis de CO 2 do sangue e ao ph. Um aumento do CO 2 arterial, ou um decréscimo do ph para 7.38 leva a uma hiperventilação que elimina o CO 2. Em oposição, um aumento no ph do sangue causa hipoventilação.
38 O controle urinário do ph Por sua capacidade de poder excretar quantidades diversas de ácidos e bases, o rim, como o pulmão, tem papel importante no controle do ph
39 Excreção de H + pelo rim CO 2 difunde dos capilares sanguíneos para o rim H 2 O e CO 2 reagem para dar ácido carbônico reação catalisada pela anidrase carbônica. O ácido carbônico se ioniza dando H+ e bicarbonato. O H + se difunde na urina Para cada H + que entra na urina, um íon sódio entra nos capilares da corrente sanguínea.
40
41 O resultado é a conversão de CO 2 em bicarbonato Tanto o decréscimo do CO 2, quanto o aumento do HCO 3 - elevam os níveis do ph sanguíneo para valores normais. A urina que estava se formando, ficou com os H + que reagem com tampões presentes na urina, como o fosfato H + + HPO > H 2 PO - 4 A presença do tampão fosfato previne a urina de ficar muito ácida (ph< 6)
42 O ph do sangue depende da concentração relativa de ácido carbônico e bicarbonato
43 Acidose e Alcalose Dois adjetivos descrevem a origem geral do desbalanço no ph dos fluidos do corpo. Acidose e alcalose respiratória resulta de padrões respiratórios anormais. Acidose e alcalose metabólica resulta de outros fatores metabólicos que não a respiração.
44 Alcalose Respiratória Causada por hiperventilação, respiração rápida e profunda. Muito CO 2 éexalado. Histeria, ansiedade, choro prolongado O tratamento consiste em re-respirar o próprio ar, administração de CO 2 ou eliminar as causas.
45 Acidose respiratória Causada por respiração lenta (hipoventilação) que pode ser resultante de overdose de narcóticos ou barbitúricos. Anestesistas tem que estar bastante atentos a esse problema. Doenças pulmonares como enfisema e pneumonia também provocam acidose. O tratamento consiste na administração intravenosa de solução de bicarbonato de sódio.
46 Acidose Metabólica Diversos processos metabólicos produzem substâncias ácidas que liberam H + A difusão dessas substâncias na corrente sanguínea causa um deslocamento no equilíbrio ácido carbônicobicarbonato Esse é um problema sério em diabete mellitus e também pode ocorrer temporariamente durante exercícios físicos pesados. Os sintomas são hiperventilação, aumento da formação de urina, sede, etc. O tratamento depende da causa e pode envolver terapia com insulina, bicarbonato intravenoso ou hemodiálise.
47
48 Ácido lático produzido durante a contração muscular HLac H + + Lac - H + + HCO 3 - H 2 CO 3 HLac + HCO 3- H 2 CO 3 + Lac - Ácido + forte Ácido + fraco
49 Alcalose Metabólica Neste caso, o corpo perdeu ácido de alguma forma. Pode ser por vômitos prolongados, ou a ingestão de substâncias alcalinas. Uso exessivo de bicarbonato de sódio para o estômago, etc. Neste caso, os centros respiratórios respondem com hipoventilação.
50
Sistema Tampão. Efeito de ph na Atividade Enzimática
 Sistema Tampão Efeito de ph na Atividade Enzimática Sistema Tampão - Ionização da Água - Definição de ácidos fortes e ácidos fracos - Equação de Henderson-Hasselbalch - Definição de sistema tampão - Curvas
Sistema Tampão Efeito de ph na Atividade Enzimática Sistema Tampão - Ionização da Água - Definição de ácidos fortes e ácidos fracos - Equação de Henderson-Hasselbalch - Definição de sistema tampão - Curvas
VOLUMETRIA DE NEUTRALIZAÇÃO
 VOLUMETRIA DE NEUTRALIZAÇÃO 1 semestre 2011 Profa. Maria Auxiliadora Costa Matos Volumetria de neutralização envolve a titulação de espécies químicas ácidas com uma solução padrão alcalina (ALCALIMETRIA)
VOLUMETRIA DE NEUTRALIZAÇÃO 1 semestre 2011 Profa. Maria Auxiliadora Costa Matos Volumetria de neutralização envolve a titulação de espécies químicas ácidas com uma solução padrão alcalina (ALCALIMETRIA)
Titulações Ácido-Base Titulações de Neutralização
 Titulações Ácido-Base Titulações de Neutralização Reacções de neutralização Métodos quantitativos Doseamentos Medição de ph e uso de indicadores Soluções tampão No ponto de meia titulação ph = pk a e consoante
Titulações Ácido-Base Titulações de Neutralização Reacções de neutralização Métodos quantitativos Doseamentos Medição de ph e uso de indicadores Soluções tampão No ponto de meia titulação ph = pk a e consoante
UNIVERSIDADE FEDERAL DE SERGIPE CENTRO DE CIÊNCIAS EXATAS E TECNOLOGIA DEPARTAMENTO DE QUÍMICA. Ácido e Base
 UNIVERSIDADE FEDERAL DE SERGIPE CENTRO DE CIÊNCIAS EXATAS E TECNOLOGIA DEPARTAMENTO DE QUÍMICA Ácido e Base Disciplina: Química l (106201) Professora: Elisangela Passos 22 de julho de 2011 1. Teorias Ácido-Base
UNIVERSIDADE FEDERAL DE SERGIPE CENTRO DE CIÊNCIAS EXATAS E TECNOLOGIA DEPARTAMENTO DE QUÍMICA Ácido e Base Disciplina: Química l (106201) Professora: Elisangela Passos 22 de julho de 2011 1. Teorias Ácido-Base
Auto-ionização da água
 ÁCIDOS E BASES Auto-ionização da água Os íons hidrônio e hidróxido A água possui uma propriedade de interesse particular no estudo de ácidos e bases: a auto-ionização. H 2 O + H 2 O H 3 O + + HO - - duas
ÁCIDOS E BASES Auto-ionização da água Os íons hidrônio e hidróxido A água possui uma propriedade de interesse particular no estudo de ácidos e bases: a auto-ionização. H 2 O + H 2 O H 3 O + + HO - - duas
CONCEITOS DE BRÖNSTED-LOWRY CONCEITOS DE ÁCIDOS E BASES CONCEITOS DE ARRHENIUS. Ácido: Ácido: HCN + H O H O + - Base ou hidróxido: Base: + +
 Ácido: CONCEITOS DE ÁCIDOS E BASES CONCEITOS DE ARRENIUS Toda substância que em solução aquosa, sofre ionização, produzindo como cátion, apenas o íon CN O ( aq ) CN ( aq ) Na realidade, o íon, quando em
Ácido: CONCEITOS DE ÁCIDOS E BASES CONCEITOS DE ARRENIUS Toda substância que em solução aquosa, sofre ionização, produzindo como cátion, apenas o íon CN O ( aq ) CN ( aq ) Na realidade, o íon, quando em
4- A pressão total de uma mistura de gases é igual à soma de suas. pressões parciais. Assim, a pressão atmosférica CONTROLE QUÍMICO DA RESPIRAÇÃO
 RESPIRAÇÃO A manutenção das funções celulares e da vida depende de um suprimento contínuo de quantidades adequadas de oxigênio aos tecidos. Grandes quantidades de CO2 precisando ser removida no organismo.
RESPIRAÇÃO A manutenção das funções celulares e da vida depende de um suprimento contínuo de quantidades adequadas de oxigênio aos tecidos. Grandes quantidades de CO2 precisando ser removida no organismo.
Ventilação Pulmonar. Vol. Ar Corrente (L) Pressão intrapleural (cm H 2 O) Fluxo de Ar (L/s) pleura parietal. pleura visceral.
 Difusão de O 2 e nos alvéolos e transporte de gases no sangue: dos pulmões aos tecidos e dos tecidos aos pulmões Efeitos do exercício Lisete Compagno Michelini Ventilação Pulmonar Pressão intrapleural
Difusão de O 2 e nos alvéolos e transporte de gases no sangue: dos pulmões aos tecidos e dos tecidos aos pulmões Efeitos do exercício Lisete Compagno Michelini Ventilação Pulmonar Pressão intrapleural
Ácidos e bases. Introdução. Objetivos. Pré-requisitos
 Objetivos Definir os conceitos de ácido e base, entender o que ocorre quando estas substâncias são dissolvidas em água e rever o conceito de constante de equilíbrio de uma reação química. Pré-requisitos
Objetivos Definir os conceitos de ácido e base, entender o que ocorre quando estas substâncias são dissolvidas em água e rever o conceito de constante de equilíbrio de uma reação química. Pré-requisitos
Equilíbrio Ácido-base. Controle de ph por meio de soluções tampão
 Equilíbrio Ácido-base Controle de ph por meio de soluções tampão Conceitos Soluções tampão = são sistemas aquosos que tendem a resistir a mudanças no seu ph quando pequenas quantidades de ácido ( H + )
Equilíbrio Ácido-base Controle de ph por meio de soluções tampão Conceitos Soluções tampão = são sistemas aquosos que tendem a resistir a mudanças no seu ph quando pequenas quantidades de ácido ( H + )
FISIOLOGIA ANIMAL - UERJ
 FISIOLOGIA ANIMAL - UERJ 1) Lipases são enzimas relacionadas à digestão dos lipídios, nutrientes que, em excesso, levam ao aumento da massa corporal. Certos medicamentos para combate à obesidade agem inibindo
FISIOLOGIA ANIMAL - UERJ 1) Lipases são enzimas relacionadas à digestão dos lipídios, nutrientes que, em excesso, levam ao aumento da massa corporal. Certos medicamentos para combate à obesidade agem inibindo
Sistema Urinário. 2º ano 2013 Profa. Rose Lopes
 Sistema Urinário 2º ano 2013 Profa. Rose Lopes Considerações iniciais Excretas Produto indesejável do metabolismo celular Excretas nitrogenadas Produtos indesejáveis do metabolismo de proteínas ou ácidos
Sistema Urinário 2º ano 2013 Profa. Rose Lopes Considerações iniciais Excretas Produto indesejável do metabolismo celular Excretas nitrogenadas Produtos indesejáveis do metabolismo de proteínas ou ácidos
Fisiologia do Sistema Respiratório. Prof. Camila Aragão Almeida
 Fisiologia do Sistema Respiratório Prof. Camila Aragão Almeida Funções do Sistema Respiratório Função principal: realizar as trocas gasosas entre O 2 e CO 2 Manutenção do equilíbrio ácido-básico Regulação
Fisiologia do Sistema Respiratório Prof. Camila Aragão Almeida Funções do Sistema Respiratório Função principal: realizar as trocas gasosas entre O 2 e CO 2 Manutenção do equilíbrio ácido-básico Regulação
AMINOÁCIDOS E PROTEÍNAS
 AMINOÁCIDOS E PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição
AMINOÁCIDOS E PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição
A Química da Vida. Anderson Dias Felipe Knak
 A Química da Vida Anderson Dias Felipe Knak A ÁGUA NAS CÉLULAS A água é imprescindível à vida dos indivíduos, independendo da espécie, idade, metabolismo e/ou grupo celular. A água exerce função de transporte
A Química da Vida Anderson Dias Felipe Knak A ÁGUA NAS CÉLULAS A água é imprescindível à vida dos indivíduos, independendo da espécie, idade, metabolismo e/ou grupo celular. A água exerce função de transporte
Estas aminas são bases de Lewis já que sobram elétrons no átomo de nitrogênio e como tal podem reagir com ácidos.
 01. Os compostos mostrados são respectivamente amina primária, amina secundária e amina terciária. O composto III, por não apresentar ligações (pontes) de hidrogênio, é o menos solúvel em água, tornando
01. Os compostos mostrados são respectivamente amina primária, amina secundária e amina terciária. O composto III, por não apresentar ligações (pontes) de hidrogênio, é o menos solúvel em água, tornando
t 1 t 2 Tempo t 1 t 2 Tempo
 Concentração 01)Uma reação química atinge o equilíbrio químico quando: a) ocorre simultaneamente nos sentidos direto e inverso. b) as velocidades das reações direta e inversa são iguais. c) os reatantes
Concentração 01)Uma reação química atinge o equilíbrio químico quando: a) ocorre simultaneamente nos sentidos direto e inverso. b) as velocidades das reações direta e inversa são iguais. c) os reatantes
METABOLISMO DE AMI OÁCIDOS
 METABOLISMO DE AMI OÁCIDOS As proteínas constituintes dos organismos estão continuamente sendo renovadas (turnover das proteínas). * Os aminoácidos presentes nas células animais originam-se das proteínas
METABOLISMO DE AMI OÁCIDOS As proteínas constituintes dos organismos estão continuamente sendo renovadas (turnover das proteínas). * Os aminoácidos presentes nas células animais originam-se das proteínas
A circulação de um fluido (sangue ou hemolinfa) acelera a distribuição dos gases respiratórios.
 A circulação de um fluido (sangue ou hemolinfa) acelera a distribuição dos gases respiratórios. Entretanto, os gases, especialmente oxigênio, são pouco solúveis em soluções aquosas. As proteínas respiratórias
A circulação de um fluido (sangue ou hemolinfa) acelera a distribuição dos gases respiratórios. Entretanto, os gases, especialmente oxigênio, são pouco solúveis em soluções aquosas. As proteínas respiratórias
Equilíbrio ácido-base
 Equilíbrio ácido-base Aula 2, QFL 1111 Química Analítica I Prof. Pedro H. C. Camargo, Ph.D. camargo@iq.usp.br São Paulo, 17/08/2015 Porque estudar equilíbrio ácido-base? Equilíbrio uma das espinhas dorsais
Equilíbrio ácido-base Aula 2, QFL 1111 Química Analítica I Prof. Pedro H. C. Camargo, Ph.D. camargo@iq.usp.br São Paulo, 17/08/2015 Porque estudar equilíbrio ácido-base? Equilíbrio uma das espinhas dorsais
Prof. Dr. Paulo Evora Ft. Luciana Garros Ferreira DISCIPLINA: PNEUMOLOGIA CLÍNICA E CIRÚRGICA
 Prof. Dr. Paulo Evora Ft. Luciana Garros Ferreira DISCIPLINA: PNEUMOLOGIA CLÍNICA E CIRÚRGICA Zonas de Condução e Respiração Mecânica respiratória Contração muscular; Elasticidade e distensibilidade
Prof. Dr. Paulo Evora Ft. Luciana Garros Ferreira DISCIPLINA: PNEUMOLOGIA CLÍNICA E CIRÚRGICA Zonas de Condução e Respiração Mecânica respiratória Contração muscular; Elasticidade e distensibilidade
Volumetria de Neutralização Ácido-Base
 Volumetria de Neutralização Ácido-Base 1 O que é um Processo de Titulação? A Titulação é uma operação analítica utilizada em análises volumétricas com o objetivo de determinar a Concentração de soluções.
Volumetria de Neutralização Ácido-Base 1 O que é um Processo de Titulação? A Titulação é uma operação analítica utilizada em análises volumétricas com o objetivo de determinar a Concentração de soluções.
UFJF CONCURSO VESTIBULAR 2012 GABARITO DA PROVA DE QUÍMICA
 Questão 1 O ácido carbônico é formado quando se borbulha o dióxido de carbono em água. Ele está presente em águas gaseificadas e refrigerantes. Em solução aquosa, ele pode sofrer duas dissociações conforme
Questão 1 O ácido carbônico é formado quando se borbulha o dióxido de carbono em água. Ele está presente em águas gaseificadas e refrigerantes. Em solução aquosa, ele pode sofrer duas dissociações conforme
INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO ARINOS MINAS GERAIS
 INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO ARINOS MINAS GERAIS 2016 INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO PROFESSOR:
INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO ARINOS MINAS GERAIS 2016 INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO PROFESSOR:
P1 - PROVA DE QUÍMICA GERAL 03/09/07
 1 - ROVA DE QUÍMICA GERAL 03/09/07 Nome: Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados R = 0,0821 atm L mol -1 K -1 T (K) = T ( C) + 273,15
1 - ROVA DE QUÍMICA GERAL 03/09/07 Nome: Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados R = 0,0821 atm L mol -1 K -1 T (K) = T ( C) + 273,15
DIVISÕES DA FISIOLOGIA
 INTRODUÇÃO À FISIOLOGIA HUMANA CMF-1 Professores: Clarissa, Lillian, Lucinda e Ricardo O QUE É FISIOLOGIA HUMANA? Estudo do funcionamento dos órgãos e sistemas que constituem o organismo humano. ANATOMIA
INTRODUÇÃO À FISIOLOGIA HUMANA CMF-1 Professores: Clarissa, Lillian, Lucinda e Ricardo O QUE É FISIOLOGIA HUMANA? Estudo do funcionamento dos órgãos e sistemas que constituem o organismo humano. ANATOMIA
Série: 2º ano. Assunto: Estequiometria
 Aluno: Série: 2º ano Assunto: Estequiometria 1) A massa de dióxido de carbono liberada na queima de 80 g de metano, quando utilizado como combustível, é: (Dados: massas molares, em g/mol: H = 1, C =12,
Aluno: Série: 2º ano Assunto: Estequiometria 1) A massa de dióxido de carbono liberada na queima de 80 g de metano, quando utilizado como combustível, é: (Dados: massas molares, em g/mol: H = 1, C =12,
UNIVERSIDADE DE CUIABÁ QUIMICA GERAL DOCENTE: ADRIANO LUIZ SANTANA AULAS PRÁTICAS DE QUÍMICA GERAL. Discente:
 UNIVERSIDADE DE CUIABÁ QUIMICA GERAL DOCENTE: ADRIANO LUIZ SANTANA AULAS PRÁTICAS DE QUÍMICA GERAL Discente: AULA PRÁTICA N º VI ASSUNTO: REAÇÕES QUIMICAS OBJETIVOS: Observar as reações químicas em soluções
UNIVERSIDADE DE CUIABÁ QUIMICA GERAL DOCENTE: ADRIANO LUIZ SANTANA AULAS PRÁTICAS DE QUÍMICA GERAL Discente: AULA PRÁTICA N º VI ASSUNTO: REAÇÕES QUIMICAS OBJETIVOS: Observar as reações químicas em soluções
QUÍMICA ANALÍTICA APLICADA - QUI 111 SOLUÇÃO TAMPÃO Natal/RN SOLUÇÃO TAMPÃO
 QUÍMICA ANALÍTICA APLICADA - QUI 111 SOLUÇÃO TAMPÃO Prof a. Nedja Suely Fernandes 2014.1 Natal/RN SOLUÇÃO TAMPÃO É uma solução que resiste a uma modificação da concentração de íon hidrogênio ou de ph,
QUÍMICA ANALÍTICA APLICADA - QUI 111 SOLUÇÃO TAMPÃO Prof a. Nedja Suely Fernandes 2014.1 Natal/RN SOLUÇÃO TAMPÃO É uma solução que resiste a uma modificação da concentração de íon hidrogênio ou de ph,
A ÁLISE TITRIMÉTRICA
 A ÁLISE TITRIMÉTRICA Análise titrimétrica - O termo análise titrimétrica refere-se à análise química quantitativa feita pela determinação do volume de uma solução, cuja concentração é conhecida com exatidão,
A ÁLISE TITRIMÉTRICA Análise titrimétrica - O termo análise titrimétrica refere-se à análise química quantitativa feita pela determinação do volume de uma solução, cuja concentração é conhecida com exatidão,
Ácido-base: objectivos principais
 Ácido-base: objectivos principais Definição de ph e poh Definição e interpretação de K a, K b, K w Relação entre K a e K b de pares ácido-base conjugados (a 25ºC pk a pk b =14) Calcular o ph de uma solução
Ácido-base: objectivos principais Definição de ph e poh Definição e interpretação de K a, K b, K w Relação entre K a e K b de pares ácido-base conjugados (a 25ºC pk a pk b =14) Calcular o ph de uma solução
Átomos Moléculas Íons Biomoléculas. Matéria é formada por Átomos. Obs.: teoria confirmada apenas no início do século XX.
 Átomos Moléculas Íons Biomoléculas Estrutura da Matéria Matéria é formada por Átomos Obs.: teoria confirmada apenas no início do século XX. Os átomos dificilmente existem livres e possuem grande tendência
Átomos Moléculas Íons Biomoléculas Estrutura da Matéria Matéria é formada por Átomos Obs.: teoria confirmada apenas no início do século XX. Os átomos dificilmente existem livres e possuem grande tendência
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012. Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 2ª AULA PRÁTICA 1. Noções
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 2ª AULA PRÁTICA 1. Noções
Equilíbrio. continuação. Prof a Alessandra Smaniotto. QMC 5325 - Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B
 Cap 3: Equilíbrio Químico Equilíbrio brioácido-base continuação Prof a Alessandra Smaniotto QMC 5325 - Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B Ácidosfortes Emumasolução,
Cap 3: Equilíbrio Químico Equilíbrio brioácido-base continuação Prof a Alessandra Smaniotto QMC 5325 - Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B Ácidosfortes Emumasolução,
BIOQUÍMICA PARA ODONTO
 BIOQUÍMICA PARA ODONTO Aula 1: ph, pk a e Sistemas tampão Aminoácidos Autoria: Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade Federal do Rio de Janeiro Reprodução
BIOQUÍMICA PARA ODONTO Aula 1: ph, pk a e Sistemas tampão Aminoácidos Autoria: Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade Federal do Rio de Janeiro Reprodução
Introdução ao Estudo da Fisiologia
 CURSO: FISIOTERAPIA DISCIPLINA: FISIOLOGIA HUMANA Introdução ao Estudo da Fisiologia Profª: Camila Aragão Almeida Campina Grande/PB Introdução Fisiologia = Phýsis (natureza) + Logos (estudo) Nasceu na
CURSO: FISIOTERAPIA DISCIPLINA: FISIOLOGIA HUMANA Introdução ao Estudo da Fisiologia Profª: Camila Aragão Almeida Campina Grande/PB Introdução Fisiologia = Phýsis (natureza) + Logos (estudo) Nasceu na
DISCIPLINA DE ANATOMIA E FISIOLOGIA ANIMAL SISTEMA URINÁRIO. Prof. Dra. Camila da Silva Frade
 DISCIPLINA DE ANATOMIA E FISIOLOGIA ANIMAL SISTEMA URINÁRIO Prof. Dra. Camila da Silva Frade Qual é a função do sistema urinário? Excreção de produtos e dejetos metabólicos Regulação do volume e composição
DISCIPLINA DE ANATOMIA E FISIOLOGIA ANIMAL SISTEMA URINÁRIO Prof. Dra. Camila da Silva Frade Qual é a função do sistema urinário? Excreção de produtos e dejetos metabólicos Regulação do volume e composição
CIÊNCIAS PROVA 3º BIMESTRE 8º ANO PROJETO CIENTISTAS DO AMANHÃ
 PREFEITURA DA CIDADE DO RIO DE JANEIRO SECRETARIA MUNICIPAL DE EDUCAÇÃO SUBSECRETARIA DE ENSINO COORDENADORIA DE EDUCAÇÃO CIÊNCIAS PROVA 3º BIMESTRE 8º ANO PROJETO CIENTISTAS DO AMANHÃ 2010 01. A organização
PREFEITURA DA CIDADE DO RIO DE JANEIRO SECRETARIA MUNICIPAL DE EDUCAÇÃO SUBSECRETARIA DE ENSINO COORDENADORIA DE EDUCAÇÃO CIÊNCIAS PROVA 3º BIMESTRE 8º ANO PROJETO CIENTISTAS DO AMANHÃ 2010 01. A organização
Potencial hidrogeniônico e hidroxiliônico - ph e poh
 Potencial hidrogeniônico e hidroxiliônico - ph e poh 01. (Fuvest) Coloca-se em um recipiente de vidro água destilada, gotas de solução de fenolftaleína e, em seguida, pedaços de sódio metálico: Observa-se,
Potencial hidrogeniônico e hidroxiliônico - ph e poh 01. (Fuvest) Coloca-se em um recipiente de vidro água destilada, gotas de solução de fenolftaleína e, em seguida, pedaços de sódio metálico: Observa-se,
As Bolhas Fatais do Mergulho
 Walter Ruggeri Waldman Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
Walter Ruggeri Waldman Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
Química Orgânica I. Ácidos e Bases, tipos de reações, intermediários de reações, termodinâmica e cinética de reações orgânicas.
 Química Orgânica I Ácidos e Bases, tipos de reações, intermediários de reações, termodinâmica e cinética de reações orgânicas Aula 4 (Parte I) Profa. Alceni Augusta Werle Profa Tânia Márcia Sacramento
Química Orgânica I Ácidos e Bases, tipos de reações, intermediários de reações, termodinâmica e cinética de reações orgânicas Aula 4 (Parte I) Profa. Alceni Augusta Werle Profa Tânia Márcia Sacramento
Texto de apoio ao professor
 Texto de apoio ao professor T1 Introdução: O sistema cárdio-respiratório, é composto pelos sistemas circulatório e respiratório. Este permite que todas as células do corpo recebam os elementos necessários
Texto de apoio ao professor T1 Introdução: O sistema cárdio-respiratório, é composto pelos sistemas circulatório e respiratório. Este permite que todas as células do corpo recebam os elementos necessários
COLÉGIO MONS. JOVINIANO BARRETO
 GABARITO 3ª ETAPA QUÍMICA II COLÉGIO MONS. JOVINIANO BARRETO 52 ANOS DE HISTÓRIA ENSINO E DISCIPLINA Rua Frei Vidal, 1621 São João do Tauape/Fone/Fax: 3272-1295 www.jovinianobarreto.com.br 2º ANO Nº TURNO:
GABARITO 3ª ETAPA QUÍMICA II COLÉGIO MONS. JOVINIANO BARRETO 52 ANOS DE HISTÓRIA ENSINO E DISCIPLINA Rua Frei Vidal, 1621 São João do Tauape/Fone/Fax: 3272-1295 www.jovinianobarreto.com.br 2º ANO Nº TURNO:
Exercícios de Respiração e Fermentação
 Exercícios de Respiração e Fermentação Material de apoio do Extensivo 1. (UFV) Enquanto os organismos superiores utilizam a respiração aeróbia para obter energia, algumas bactérias e fungos utilizam a
Exercícios de Respiração e Fermentação Material de apoio do Extensivo 1. (UFV) Enquanto os organismos superiores utilizam a respiração aeróbia para obter energia, algumas bactérias e fungos utilizam a
Introdução à Volumetria. Profa. Lilian Lúcia Rocha e Silva
 Introdução à Volumetria Profa. Lilian Lúcia Rocha e Silva INTRODUÇÃO À VOLUMETRIA TITULAÇÃO Processo no qual uma solução padrão ou solução de referência é adicionada a uma solução que contém um soluto
Introdução à Volumetria Profa. Lilian Lúcia Rocha e Silva INTRODUÇÃO À VOLUMETRIA TITULAÇÃO Processo no qual uma solução padrão ou solução de referência é adicionada a uma solução que contém um soluto
Metabolismo dos Carboidratos
 Metabolismo dos Carboidratos Disciplina: Nutrição Aplicada a Educação Física Prof ₐ Mda. Vanessa Ribeiro dos Santos Definição O que são carboidratos? Os carboidratos são compostos orgânicos que contêm:
Metabolismo dos Carboidratos Disciplina: Nutrição Aplicada a Educação Física Prof ₐ Mda. Vanessa Ribeiro dos Santos Definição O que são carboidratos? Os carboidratos são compostos orgânicos que contêm:
PlanetaBio Resolução de Vestibulares UNICAMP 2012 1ª fase www.planetabio.com
 1- Hemácias de um animal foram colocadas em meio de cultura em vários frascos com diferentes concentrações das substâncias A e B, marcadas com isótopo de hidrogênio. Dessa forma os pesquisadores puderam
1- Hemácias de um animal foram colocadas em meio de cultura em vários frascos com diferentes concentrações das substâncias A e B, marcadas com isótopo de hidrogênio. Dessa forma os pesquisadores puderam
ph SISTEMAS TAMPÕES Faculdade de Medicina PUC-Campinas Profa. Dra. Celene Fernandes Bernardes
 ph SISTEMAS TAMPÕES Faculdade de Medicina PUC-Campinas Profa. Dra. Celene Fernandes Bernardes ph = potencial hidrogeniônico ph = -log [H + ] Sorenson 1909 A escala de ph é logarítma; portanto, quando duas
ph SISTEMAS TAMPÕES Faculdade de Medicina PUC-Campinas Profa. Dra. Celene Fernandes Bernardes ph = potencial hidrogeniônico ph = -log [H + ] Sorenson 1909 A escala de ph é logarítma; portanto, quando duas
Experiência 07: Preparo de Solução a partir de Substâncias sólidas, Liquidas e de Solução Concentrada
 1 Experiência 07: Preparo de Solução a partir de Substâncias sólidas, Liquidas e de Solução Concentrada 1. Questões de estudo - Como preparar uma solução aquosa de NaOH 0,1 M? - Como preparar uma solução
1 Experiência 07: Preparo de Solução a partir de Substâncias sólidas, Liquidas e de Solução Concentrada 1. Questões de estudo - Como preparar uma solução aquosa de NaOH 0,1 M? - Como preparar uma solução
Química Analítica Avançada: Introdução. Profa. Lilian Silva 2011
 Química Analítica Avançada: Introdução Profa. Lilian Silva 2011 Introdução 1 Equilíbrio Químico -A posição de equilíbrio; -A constante de equilíbrio; -Efeito dos eletrólitos nos equilíbrios químicos (atividade);
Química Analítica Avançada: Introdução Profa. Lilian Silva 2011 Introdução 1 Equilíbrio Químico -A posição de equilíbrio; -A constante de equilíbrio; -Efeito dos eletrólitos nos equilíbrios químicos (atividade);
ph arterial entre 7,35 e 7,45 [H+] ~ 40 nanomoles/l (10-9) CO2 (Ácido volátil) O CO 2 não se acumula no organismo, é eliminado pelos pulmões
![ph arterial entre 7,35 e 7,45 [H+] ~ 40 nanomoles/l (10-9) CO2 (Ácido volátil) O CO 2 não se acumula no organismo, é eliminado pelos pulmões ph arterial entre 7,35 e 7,45 [H+] ~ 40 nanomoles/l (10-9) CO2 (Ácido volátil) O CO 2 não se acumula no organismo, é eliminado pelos pulmões](/thumbs/60/44575873.jpg) Regulação do ph dos líquidos Regulação do ph dos líquidos ph = log[ ] LEC =, ±, (, mm) ph , Alcalose Ojetivo: Manutenção do ph sistêmico na faixa de normalidade. ph arterial entre, e, [H]
Regulação do ph dos líquidos Regulação do ph dos líquidos ph = log[ ] LEC =, ±, (, mm) ph , Alcalose Ojetivo: Manutenção do ph sistêmico na faixa de normalidade. ph arterial entre, e, [H]
Sistema Circulatório: O Sangue
 Sistema Circulatório: O Sangue A composição do sangue Embora o sangue tenha uma aparência homogênea, se observado ao microscópio, logo se notará sua composição heterogênea. Isto significa que o sangue
Sistema Circulatório: O Sangue A composição do sangue Embora o sangue tenha uma aparência homogênea, se observado ao microscópio, logo se notará sua composição heterogênea. Isto significa que o sangue
26/03/2012. Componentes Químicos da Célula. Ligações Químicas. Ligações Químicas. Ligações Químicas. Componentes Químicos da Célula
 Componentes Químicos da Célula Componentes Químicos da Célula Células - estruturas incrivelmente complexas e diversas, capazes não somente de auto-replicação, mas também de realizarem uma ampla variedade
Componentes Químicos da Célula Componentes Químicos da Célula Células - estruturas incrivelmente complexas e diversas, capazes não somente de auto-replicação, mas também de realizarem uma ampla variedade
Homeostase do ph. Ácidos e Bases. HA H + + A - HCl H + + Cl - H 2 CO 3 H + + HCO H + + NH 3. Escala de ph
 Frederico Gueiros Filho Formação: Bacharelado em Biologia - UERJ Mestrado em Genética - UFRJ Doutorado - Harvard Medical School - EUA Pós-doutorado - Harvard, Depto. MCB - EUA Interesse de pesquisa: Mecanismo
Frederico Gueiros Filho Formação: Bacharelado em Biologia - UERJ Mestrado em Genética - UFRJ Doutorado - Harvard Medical School - EUA Pós-doutorado - Harvard, Depto. MCB - EUA Interesse de pesquisa: Mecanismo
Química analítica avançada
 Química analítica avançada Profa. Denise Lowinshon denise.lowinsohn@ufjf.edu.br http://www.ufjf.br/nupis Prof. Rafael Arromba de Sousa rafael.arromba@ufjf.edu.br http://www.ufjf.br/baccan 1º semestre 2014
Química analítica avançada Profa. Denise Lowinshon denise.lowinsohn@ufjf.edu.br http://www.ufjf.br/nupis Prof. Rafael Arromba de Sousa rafael.arromba@ufjf.edu.br http://www.ufjf.br/baccan 1º semestre 2014
Indicadores de ph naturais
 Instituto Federal de Educação, Ciência e Tecnologia da Bahia Indicadores de ph naturais Práticas de ensino 2014.1 Sheila Silva; Elton Rocha; Mayara Oliveira; Izabela Oliveira [Escolha a data] Introdução
Instituto Federal de Educação, Ciência e Tecnologia da Bahia Indicadores de ph naturais Práticas de ensino 2014.1 Sheila Silva; Elton Rocha; Mayara Oliveira; Izabela Oliveira [Escolha a data] Introdução
IMPORTANTE: Manter as vias aéreas desobstruídas. Divisão:
 SISTEMA RESPIRATÓRIO É uma característica dos seres vivos, pois o O² O é importante para energia celular. Obtemos o O² O do ar que respiramos. FUNÇÃO: Responsável pela respiração, isto é: Fornecimento
SISTEMA RESPIRATÓRIO É uma característica dos seres vivos, pois o O² O é importante para energia celular. Obtemos o O² O do ar que respiramos. FUNÇÃO: Responsável pela respiração, isto é: Fornecimento
ESCOLA SECUNDÁRIA DE CASQUILHOS
 ESCOLA SECUNDÁRIA DE CASQUILHOS 7º Teste sumativo de FQA 29. abril. 2015 Versão 1 11º Ano Turma A Professor: Maria do Anjo Albuquerque Duração da prova: 90 minutos. Este teste é constituído por 8 páginas
ESCOLA SECUNDÁRIA DE CASQUILHOS 7º Teste sumativo de FQA 29. abril. 2015 Versão 1 11º Ano Turma A Professor: Maria do Anjo Albuquerque Duração da prova: 90 minutos. Este teste é constituído por 8 páginas
Exercícios de Equílíbrio Químico ENEM Resolução Comentada Professora Simone
 Exercícios de Equílíbrio Químico ENEM Resolução Comentada Professora Simone 1. O equilíbrio químico se caracteriza por ser uma dinâmica em nível microscópico. Para se ter uma informação quantitativa da
Exercícios de Equílíbrio Químico ENEM Resolução Comentada Professora Simone 1. O equilíbrio químico se caracteriza por ser uma dinâmica em nível microscópico. Para se ter uma informação quantitativa da
CURSO APOIO QUÍMICA RESOLUÇÃO
 QUÍMICA CURSO APOIO 15. O sulfato de sódio é um composto utilizado na indústria de celulose e na fabricação de detergentes. Por apresentar grande afinidade por água, pode ser encontrado na forma de um
QUÍMICA CURSO APOIO 15. O sulfato de sódio é um composto utilizado na indústria de celulose e na fabricação de detergentes. Por apresentar grande afinidade por água, pode ser encontrado na forma de um
Sistema Circulatório
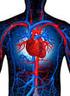 Anatomia Funcional do Sistema Cardio-respiratório dos Répteis Anatomia Funcional do Sistema Cardio-respiratório dos Répteis Especialização Anclivepa-SP Anclivepa-SP Cristina Fotin Sistema Circulatório
Anatomia Funcional do Sistema Cardio-respiratório dos Répteis Anatomia Funcional do Sistema Cardio-respiratório dos Répteis Especialização Anclivepa-SP Anclivepa-SP Cristina Fotin Sistema Circulatório
Prof. Giovani - Biologia
 Prof. Giovani - Biologia 1.(UFRS) Tanto em uma célula eucarionte quanto em uma procarionte podemos encontrar: a) membrana plasmática e retículo endoplasmático. b) ribossomos e aparelho de Golgi. c) mitocôndrias
Prof. Giovani - Biologia 1.(UFRS) Tanto em uma célula eucarionte quanto em uma procarionte podemos encontrar: a) membrana plasmática e retículo endoplasmático. b) ribossomos e aparelho de Golgi. c) mitocôndrias
7. EQUILÍBRIO QUÍMICO
 Departamento de Química Inorgânica IQ / UFRJ IQG 18 / IQG 1 7. EQUILÍBRIO QUÍMICO I. INTRODUÇÃO Quando a concentração de todos os reagentes e produtos, em um sistema fechado, não variam mais com o tempo
Departamento de Química Inorgânica IQ / UFRJ IQG 18 / IQG 1 7. EQUILÍBRIO QUÍMICO I. INTRODUÇÃO Quando a concentração de todos os reagentes e produtos, em um sistema fechado, não variam mais com o tempo
É o cálculo das quantidades de reagentes e/ou produtos das reações químicas.
 Estequiometria Introdução Estequiometria É derivada da palavra grega STOICHEON (elemento) e METRON (medida) significa medida dos elementos químicos", ou ainda medir algo que não pode ser dividido. É o
Estequiometria Introdução Estequiometria É derivada da palavra grega STOICHEON (elemento) e METRON (medida) significa medida dos elementos químicos", ou ainda medir algo que não pode ser dividido. É o
ph do sangue arterial = 7.4
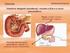 Regulação do Equilíbrio Ácido Base ph do sangue arterial = 7.4 < 6.9 ou > 7.7 = MORTE 1 Importância do ph nos processos biológicos Protonação ou desprotonação de radicais proteicos Variação da carga total
Regulação do Equilíbrio Ácido Base ph do sangue arterial = 7.4 < 6.9 ou > 7.7 = MORTE 1 Importância do ph nos processos biológicos Protonação ou desprotonação de radicais proteicos Variação da carga total
Membranas Biológicas. Profª Eleonora Slide de aula
 Membranas Biológicas Profª Eleonora Slide de aula Membranas Biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
Membranas Biológicas Profª Eleonora Slide de aula Membranas Biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
FCAV/ UNESP EQUILÍBRIO ÁCIDO-BASE
 FCAV/ UNESP EQUILÍBRIO ÁCIDO-BASE Prof a. Dr a. Luciana M. Saran 1 Tópicos da Aula: Substâncias que interferem no equilíbrio químico da água; Equilíbrio ácido-base; Soluções ácidas, neutras e alcalinas;
FCAV/ UNESP EQUILÍBRIO ÁCIDO-BASE Prof a. Dr a. Luciana M. Saran 1 Tópicos da Aula: Substâncias que interferem no equilíbrio químico da água; Equilíbrio ácido-base; Soluções ácidas, neutras e alcalinas;
Sistema Respiratório dos Vertebrados
 Sistema Respiratório dos Vertebrados Respiração: processo pelo qual o O 2 é transportado para a membrana de trocas gasosas a partir do meio externo e pelo qual o CO 2 é transportado para fora da membrana,
Sistema Respiratório dos Vertebrados Respiração: processo pelo qual o O 2 é transportado para a membrana de trocas gasosas a partir do meio externo e pelo qual o CO 2 é transportado para fora da membrana,
Organismos vivos compartilham as mesmas unidades básicas estruturais
 Organismos vivos compartilham as mesmas unidades básicas estruturais ATP- a remoção do terminal fosfato é altamente exergônica A energia varia durante uma reação química Uma via metabólica linear
Organismos vivos compartilham as mesmas unidades básicas estruturais ATP- a remoção do terminal fosfato é altamente exergônica A energia varia durante uma reação química Uma via metabólica linear
U R O L I T Í A S E UNESC - ENFERMAGEM 14/4/2015 CONCEITO. A urolitíase refere-se à presença de pedra (cálculo) no sistema urinário.
 CONCEITO UNESC - ENFERMAGEM SAÚDE DO ADULTO PROFª.: FLÁVIA NUNES A urolitíase refere-se à presença de pedra (cálculo) no sistema urinário. U R O L I T Í A S E COMO SÃO FORMADOS OS CÁLCULOS? São formados
CONCEITO UNESC - ENFERMAGEM SAÚDE DO ADULTO PROFª.: FLÁVIA NUNES A urolitíase refere-se à presença de pedra (cálculo) no sistema urinário. U R O L I T Í A S E COMO SÃO FORMADOS OS CÁLCULOS? São formados
Lista de Exercícios Química Geral Entropia e energia livre
 Lista de Exercícios Química Geral Entropia e energia livre 1. Se a reação A + B C tiver uma constante de equilíbrio maior do que 1, qual das seguintes indicações está correta? a) A reação não é espontânea.
Lista de Exercícios Química Geral Entropia e energia livre 1. Se a reação A + B C tiver uma constante de equilíbrio maior do que 1, qual das seguintes indicações está correta? a) A reação não é espontânea.
INTRODUÇÃO À CINETICA E TERMODINÂMICA QUÍMICA
 INTRODUÇÃO À CINETICA E TERMODINÂMICA QUÍMICA Principios de Termodinâmica Termodinamica determina se um processo fisicoquímico é possível (i.e. espontaneo) Termodinamica não providencia informação sobre
INTRODUÇÃO À CINETICA E TERMODINÂMICA QUÍMICA Principios de Termodinâmica Termodinamica determina se um processo fisicoquímico é possível (i.e. espontaneo) Termodinamica não providencia informação sobre
Glândulas. Paratireóides
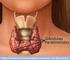 Glândulas Paratireóides Paratôrmonio (PTH) Essencial para a vida Regulação da [Ca +2 ] plasmática. Baixa [Ca 2+ ] no plasma Células da Paratireóide Retroalimentação Negativa Hormônio da Paratireóide Controle
Glândulas Paratireóides Paratôrmonio (PTH) Essencial para a vida Regulação da [Ca +2 ] plasmática. Baixa [Ca 2+ ] no plasma Células da Paratireóide Retroalimentação Negativa Hormônio da Paratireóide Controle
TEORIAS ÁCIDO- BASE DO SÉCULO XX
 UNIVERSIDADE CATÓLICA DE PETRÓPOLIS Tecnólogo em Processos de Sustentabilidade Ambiental TEORIAS ÁCIDO- BASE DO SÉCULO XX 22 de Abril de 2009 RESUMO RESUMO DE TEORIAS ÁCIDO-BASE DO SÉCULO XX, DO AUTOR
UNIVERSIDADE CATÓLICA DE PETRÓPOLIS Tecnólogo em Processos de Sustentabilidade Ambiental TEORIAS ÁCIDO- BASE DO SÉCULO XX 22 de Abril de 2009 RESUMO RESUMO DE TEORIAS ÁCIDO-BASE DO SÉCULO XX, DO AUTOR
Características gerais
 Citoplasma Citoplasma Características gerais Um vertebrado é formado por dezenas de tipos de células. Citoplasma Características gerais Um vertebrado é formado por dezenas de tipos de células. Neurônio
Citoplasma Citoplasma Características gerais Um vertebrado é formado por dezenas de tipos de células. Citoplasma Características gerais Um vertebrado é formado por dezenas de tipos de células. Neurônio
I Curso de Férias em Fisiologia - UECE
 I Curso de Férias em Fisiologia - UECE Realização: Instituto Superior de Ciências Biomédicas Mestrado Acadêmico em Ciências Biológicas Apoio: 1 FISIOLOGIA CELULAR Laboratório de Eletrofisiologia 1. POTENCIAL
I Curso de Férias em Fisiologia - UECE Realização: Instituto Superior de Ciências Biomédicas Mestrado Acadêmico em Ciências Biológicas Apoio: 1 FISIOLOGIA CELULAR Laboratório de Eletrofisiologia 1. POTENCIAL
Química Orgânica Ambiental
 Química Orgânica Ambiental Aula 4 Ácidos e bases em Química Orgânica Prof. Dr. Leandro Vinícius Alves Gurgel 1. Ácidos e bases - Teoria de Arrhenius De acordo com a teoria proposta por Svante Arrhenius,
Química Orgânica Ambiental Aula 4 Ácidos e bases em Química Orgânica Prof. Dr. Leandro Vinícius Alves Gurgel 1. Ácidos e bases - Teoria de Arrhenius De acordo com a teoria proposta por Svante Arrhenius,
Proteínas e aminoácidos
 Proteínas e aminoácidos Digestão Absorção Metabolismo Disciplina de Bioquímica Profa. Dra. Celene Fernandes Bernardes Proteínas da dieta Proteínas endógenas Proteínas endógenas Síntese de aminoácidos não
Proteínas e aminoácidos Digestão Absorção Metabolismo Disciplina de Bioquímica Profa. Dra. Celene Fernandes Bernardes Proteínas da dieta Proteínas endógenas Proteínas endógenas Síntese de aminoácidos não
11 Metabolismo Ácido-Básico
 Capítulo 11 Metabolismo Ácido-Básico Miguel Carlos Riella e Maria Aparecida Pachaly INTRODUÇÃO CONCEITOS E PRINCÍPIOS QUÍMICOS Ácido Base Sistema tampão ph Lei de ação das massas Equação de Henderson-Hasselbalch
Capítulo 11 Metabolismo Ácido-Básico Miguel Carlos Riella e Maria Aparecida Pachaly INTRODUÇÃO CONCEITOS E PRINCÍPIOS QUÍMICOS Ácido Base Sistema tampão ph Lei de ação das massas Equação de Henderson-Hasselbalch
Membranas Biológicas. Profª Eleonora Slide de aula
 Membranas Biológicas Profª Eleonora Slide de aula Membranas biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
Membranas Biológicas Profª Eleonora Slide de aula Membranas biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
Disciplina Química geral (MAF1293) Professora Cleonice Rocha Aluno - Estudo Dirigido Reações em solução aquosa (valor = 1,5 pt)
 Disciplina Química geral (MAF1293) Professora Cleonice Rocha Aluno - Estudo Dirigido Reações em solução aquosa (valor = 1,5 pt) Propriedades gerais das soluções aquosas Propriedades eletrolíticas As soluções
Disciplina Química geral (MAF1293) Professora Cleonice Rocha Aluno - Estudo Dirigido Reações em solução aquosa (valor = 1,5 pt) Propriedades gerais das soluções aquosas Propriedades eletrolíticas As soluções
1) (Fuvest-SP) 2) (Mackenzie-SP) 3) (UDESC-SC) 4) (ENEM) 5) (UNIOESTE-PR)
 1) (Fuvest-SP) As mitocôndrias são consideradas as casas de força das células vivas. Tal analogia refere-se ao fato de as mitocôndrias: a) estocarem moléculas de ATP produzidas na digestão de alimentos.
1) (Fuvest-SP) As mitocôndrias são consideradas as casas de força das células vivas. Tal analogia refere-se ao fato de as mitocôndrias: a) estocarem moléculas de ATP produzidas na digestão de alimentos.
P2 - PROVA DE QUÍMICA GERAL - 08/10/07
 P2 - PRVA DE QUÍMICA GERAL - 08/10/07 Nome: Nº de Matrícula: GABARIT Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 R = 8,314 J mol -1 K -1 = 0,0821 atm L mol
P2 - PRVA DE QUÍMICA GERAL - 08/10/07 Nome: Nº de Matrícula: GABARIT Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 R = 8,314 J mol -1 K -1 = 0,0821 atm L mol
Medição e cálculo do ph de algumas soluções
 Química Geral Medição e cálculo do ph de algumas soluções Docente: Dulce Gomes Engenharia do Ambiente (2º Ano) Turma EPQ Data de entrega do relatório: 17-02-2009. Relatório elaborado em 14-02-2009 pelo
Química Geral Medição e cálculo do ph de algumas soluções Docente: Dulce Gomes Engenharia do Ambiente (2º Ano) Turma EPQ Data de entrega do relatório: 17-02-2009. Relatório elaborado em 14-02-2009 pelo
Aula V 2013 Biologia Cursinho Ação Direta. Respiração:
 Aula V 2013 Biologia Cursinho Ação Direta Respiração: O processo de respiração tem como objetivo básico tornar possível extrair a energia química presente nos alimentos e utilizá-las nas diversas atividades
Aula V 2013 Biologia Cursinho Ação Direta Respiração: O processo de respiração tem como objetivo básico tornar possível extrair a energia química presente nos alimentos e utilizá-las nas diversas atividades
www.professormazzei.com FUNÇÕES INORGÂNICAS Folha 02 João Roberto Fortes Mazzei
 01. Durante um experimento, seu professor de química pediu que você identificasse as soluções aquosas presentes em cada um dos béqueres (A, B, C) apresentados na figura a seguir. Dois béqueres do experimento
01. Durante um experimento, seu professor de química pediu que você identificasse as soluções aquosas presentes em cada um dos béqueres (A, B, C) apresentados na figura a seguir. Dois béqueres do experimento
EQUILÍBRIO QUÍMICO: é o estado de um sistema reacional no qual não ocorrem variações na composição do mesmo ao longo do tempo.
 IV INTRODUÇÃO AO EQUILÍBRIO QUÍMICO IV.1 Definição EQUILÍBRIO QUÍMICO: é o estado de um sistema reacional no qual não ocorrem variações na composição do mesmo ao longo do tempo. Equilíbrio químico equilíbrio
IV INTRODUÇÃO AO EQUILÍBRIO QUÍMICO IV.1 Definição EQUILÍBRIO QUÍMICO: é o estado de um sistema reacional no qual não ocorrem variações na composição do mesmo ao longo do tempo. Equilíbrio químico equilíbrio
Conceito de ph ph = - Log [H + ] Aumento [H + ] => diminuição do ph => acidose Diminuição [H + ] => aumento do ph => alcalose Alterações são dependent
![Conceito de ph ph = - Log [H + ] Aumento [H + ] => diminuição do ph => acidose Diminuição [H + ] => aumento do ph => alcalose Alterações são dependent Conceito de ph ph = - Log [H + ] Aumento [H + ] => diminuição do ph => acidose Diminuição [H + ] => aumento do ph => alcalose Alterações são dependent](/thumbs/50/27125458.jpg) Equilíbrio ácido-básico A concentração de H no FEC é mantida dentro de um limite extremamente estreito: 40 nmol/l = 1.000.000 menor que a Concentração dos outros íons!! [H] tem profundo efeito nos eventos
Equilíbrio ácido-básico A concentração de H no FEC é mantida dentro de um limite extremamente estreito: 40 nmol/l = 1.000.000 menor que a Concentração dos outros íons!! [H] tem profundo efeito nos eventos
Biologia Professor Leandro Gurgel de Medeiros
 Biologia Professor Leandro Gurgel de Medeiros Aula 02: Biologia Celular (Membrana Plásmática) Biologia celular é o ramo da biologia que estuda as células no que diz respeito à sua estrutura, suas funções
Biologia Professor Leandro Gurgel de Medeiros Aula 02: Biologia Celular (Membrana Plásmática) Biologia celular é o ramo da biologia que estuda as células no que diz respeito à sua estrutura, suas funções
Ácidos e bases Auto-ionização da água
 Ácidos e bases Auto-ionização da água Composição química das águas Água da Chuva - a sua composição depende dos componentes do ar que atravessa; normalmente a chuva normal é ligeiramente ácida (ph= 5,6
Ácidos e bases Auto-ionização da água Composição química das águas Água da Chuva - a sua composição depende dos componentes do ar que atravessa; normalmente a chuva normal é ligeiramente ácida (ph= 5,6
I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2
 I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com 4
I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com 4
Sangue Professor: Fernando Stuchi
 Zoologia e Histologia Animal Sangue Professor: Fernando Stuchi Sangue Em animais invertebrados o líquido circulante no interior do sistema cardiovascular é a hemolinfa. Nos vertebrados esse liquido é o
Zoologia e Histologia Animal Sangue Professor: Fernando Stuchi Sangue Em animais invertebrados o líquido circulante no interior do sistema cardiovascular é a hemolinfa. Nos vertebrados esse liquido é o
Membrana celular: Transporte
 Membrana celular: Transporte Processos de Transporte Transporte em grande quantidade Transporte de íons e moléculas 1 Processos de Transporte: Transporte de íons e moléculas Qual a importância da manutenção
Membrana celular: Transporte Processos de Transporte Transporte em grande quantidade Transporte de íons e moléculas 1 Processos de Transporte: Transporte de íons e moléculas Qual a importância da manutenção
QUÍMICA PROFª MARCELA CARVALHO
 QUÍMICA 1 PROFª MARCELA CARVALHO EQUAÇÃO QUÍMICA É a representação química simbólica e abreviada de uma reação química. 2 H2 + O2 2 H2O 2, 1 e 2 = coeficientes estequiométricos ou simplesmente coeficiente,
QUÍMICA 1 PROFª MARCELA CARVALHO EQUAÇÃO QUÍMICA É a representação química simbólica e abreviada de uma reação química. 2 H2 + O2 2 H2O 2, 1 e 2 = coeficientes estequiométricos ou simplesmente coeficiente,
4/5/2010. Sistema Glicolítico. Intensidade. Sistema Glicolítico ATP CP. Sistema Oxidativo. Tempo de Duração. 10 2 Acima de 2
 Sistema Glicolítico Intensidade 100 80 % 60 ATP CP Sistema Glicolítico Sistema Oxidativo 40 20 0 10 2 Acima de 2 Tempo de Duração 1 Intensidade 100 80 % 60 40 Sistema Glicolítico 20 0 2 Tempo de Duração
Sistema Glicolítico Intensidade 100 80 % 60 ATP CP Sistema Glicolítico Sistema Oxidativo 40 20 0 10 2 Acima de 2 Tempo de Duração 1 Intensidade 100 80 % 60 40 Sistema Glicolítico 20 0 2 Tempo de Duração
Titulações de ácido- base
 QUÍMICA 11º ANO- TURMA A 201/2015 FICHA INFORMATIVA/FORMATIVA SOBRE TITULAÇÕES DE ÁCIDO-BASE E DE EFEITO TAMPÃO NOME: TURMA Nº: Titulações de ácido- base Nas titulações de ácido base, as reacções que ocorrem
QUÍMICA 11º ANO- TURMA A 201/2015 FICHA INFORMATIVA/FORMATIVA SOBRE TITULAÇÕES DE ÁCIDO-BASE E DE EFEITO TAMPÃO NOME: TURMA Nº: Titulações de ácido- base Nas titulações de ácido base, as reacções que ocorrem
MECANISMOS DE CORROSÃO DE MATERIAIS METÁLICOS. APOSTILA PARA A DISCIPLINA PMT 2507 2ª. Parte
 MECANISMOS DE CORROSÃO DE MATERIAIS METÁLICOS APOSTILA PARA A DISCIPLINA PMT 2507 2ª. Parte Neusa Alonso-Falleiros Mar/2008 2 Diagramas de Pourbaix A representação gráfica do potencial reversível em função
MECANISMOS DE CORROSÃO DE MATERIAIS METÁLICOS APOSTILA PARA A DISCIPLINA PMT 2507 2ª. Parte Neusa Alonso-Falleiros Mar/2008 2 Diagramas de Pourbaix A representação gráfica do potencial reversível em função
Tampão. O que é? MISTURA DE UM ÁCIDO FRACO COM SUA BASE CONJUGADA, QUE ESTABILIZA O P H DE UMA SOLUÇÃO
 Tampões biológicos Relembrar os conceitos de ácido e base (Brönsted-Lowry), ph, pka; Compreender a importância do ph na manutenção da estrutura tridimensional das biomoléculas; Conhecer os valores de ph
Tampões biológicos Relembrar os conceitos de ácido e base (Brönsted-Lowry), ph, pka; Compreender a importância do ph na manutenção da estrutura tridimensional das biomoléculas; Conhecer os valores de ph
Ácidos, bases e sistemas tampão
 Ácidos, bases e sistemas tampão Ionização da água A água pura tem uma baixa concentração de iões hidrónio (H 3 O + ) e uma igual concentração de iões hidróxido (OH - ) Os ácidos são dadores de protões
Ácidos, bases e sistemas tampão Ionização da água A água pura tem uma baixa concentração de iões hidrónio (H 3 O + ) e uma igual concentração de iões hidróxido (OH - ) Os ácidos são dadores de protões
Cat Ca ab a olismo Anab a ol o ismo
 A acção das enzimas Metabolismo celular É o conjunto de reacções químicas que ocorrem numa célula. Catabolismo moléculas complexas são convertidas em moléculas mais simples, com libertação de energia.
A acção das enzimas Metabolismo celular É o conjunto de reacções químicas que ocorrem numa célula. Catabolismo moléculas complexas são convertidas em moléculas mais simples, com libertação de energia.
