BIOQUÍMICA PARA ODONTO
|
|
|
- Maria Laura Paixão Farias
- 6 Há anos
- Visualizações:
Transcrição
1 BIOQUÍMICA PARA ODONTO Aula 1: ph, pk a e Sistemas tampão Aminoácidos Autoria: Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade Federal do Rio de Janeiro Reprodução Proibida ESCALA DE ph A escala de ph designa as concentrações de H + e OH - O ph de uma solução é uma medida de sua concentração de H +. O ph é definido como: Na água pura, a concentração de H + é 1.0 x 10 7 M, o ph pode ser calculado:
2 ESCALA DE ph A escala de ph é logarítmica! Quando uma solução difere de outra por 2 unidades de ph, significa que a solução tem 100 vezes mais H + que a outra EQUILÍBRIO ÁCIDO-BASE relevância biológica e fisiológica Manutenção da conformação e função das macromoléculas Ex: a atividade catalítica das enzimas é dependente de ph Mecanismos de ação e toxicidade dos fármacos Distúrbios do Equilíbrio Ácido-Base são relacionados a patologias Ex: pessoas com diabetes, ph do plasma < 7.4
3 EQUILÍBRIO ÁCIDO-BASE definição de ácidos e bases Ácidos doadores de prótons Bases aceptores de prótons Ácidos fortes são completamente ionizados em solução aquosas Ex: HCl + H 2 O H 3 O + + Cl - HCl H + + Cl - Bases fortes também são completamente ionizados em solução aquosas Ex: NaOH Na + + OH - EQUILÍBRIO ÁCIDO-BASE comportamento do ácidos fracos Os ácidos e bases fracos são ubíquos em sistemas biológicos e têm importante papel no metabolismo e na sua regulação. Quando um ácido fraco (HAc) como o ácido acético é adicionado em água, a equação para a dissociação do ácido pode ser descrita pela reação reversível: HAc + H 2 O Ac - + H + A tendência do ácido (HAc) de doar o próton e formar a base conjugada (Ac - ) é definida pela constante de ionização (K a ) K eq = [Ac - ] [H + ] [HAc] [H 2 O] K eq [H 2 O] = K a = [Ac - ] [H + ] [HAc] constante! Quanto maior a tendência de doar o próton, maior é a constante de dissociação K a
4 EQUILÍBRIO ÁCIDO-BASE comportamento do ácidos fracos K a = [Ac - ] [H + ] [HAc] [H + ] = K a [HAc] [Ac - ] Aplicando log negativo : -log [H + ] = - log K a - log [HAc] [Ac - ] -log [H + ] = - log K a + log [Ac - ] [HAc] ph = pk a + log [Ac - ] [HAc] EQUILÍBRIO ÁCIDO-BASE comportamento do ácidos fracos No equilíbrio, [Ac - ] = [HAc] ph = pk a + log [Ac - ] [HAc] ph = pk a + log 1 log 1 = 0 no equilíbrio!! ph = pk a O pk a do composto equivale ao ph do meio no qual a concentração das duas espécies é a mesma ph não é igual a pk a pk a = constante!
5 EQUILÍBRIO ÁCIDO-BASE comportamento do ácidos Quanto mais forte a tendência de doar o próton, maior é a constante de dissociação K a e menor o valor de pk a EQUILÍBRIO ÁCIDO-BASE curva de titulação ácido acético ânion acetato protonado desprotonado A titulação envolve a adição ou remoção gradual de prótons H + = ph protonada H + = ph desprotonada pk a = 4.7
6 EQUILÍBRIO ÁCIDO-BASE Titulação de ácidos fracos com base forte EQUILÍBRIO ÁCIDO-BASE Titulação do ácido acético ácido acético ânion acetato H + = ph protonada H + = ph desprotonada protonado desprotonado pk a = 4.76
7 EQUILÍBRIO ÁCIDO-BASE sistema tampão Quase todos os processos biológicos são dependentes do ph. As células e os fluidos extracelulares mantêm um ph constante e específico e altamente regulado. A constância do ph é conseguida primariamente pelos tampões biológicos: mistura de ácidos fracos e suas bases conjugadas. Dois tampões biologicamente importantes são os sistemas fosfato e bicarbonato. EQUILÍBRIO ÁCIDO-BASE sistema tampão O sistema-tampão fosfato, que age no citoplasma de todas as células consiste de H 2 PO 4- como doador de prótons e HPO 4 2- como aceptor de prótons: H 2 PO 4- HPO H + pk a = 6,86 Resiste às variações de ph na região de 5,9 e 7,9
8 EQUILÍBRIO ÁCIDO-BASE sistema tampão O plasma sanguíneo é tamponado em parte pelo sistema-tampão bicarbonato que consiste de ácido carbônico (H 2 CO 3 ) como doador de prótons e de bicarbonato (HCO 3- ) como aceptor de prótons. H 2 CO 3 HCO 3- + H + Por sua vez, o ácido carbônico (H 2 CO 3 ) é formado a partir de dióxido de carbono (CO 2 ) dissolvido (d) em água, por uma reação reversível catalisada pela enzima anidrase carbônica: CO 2 (d) + H 2 O H 2 CO 3 A concentração de dióxido de carbono (CO 2 ) dissolvido (d) é resultado do equilíbrio do CO 2 da fase gasosa: CO 2 (g) CO 2 (d) EQUILÍBRIO ÁCIDO-BASE sistema tampão em sistemas biológicos Resumindo:
9 DISTÚRBIOS DO EQUILÍBRIO ÁCIDO-BASE relevância fisiológica Acidose Alcalose Metabólica Respiratória DISTÚRBIOS DO EQUILÍBRIO ÁCIDO-BASE acidose respiratória Hipoventilação dos alvéolos Acúmulo de CO 2 CO 2 + H 2 O H 2 CO 3 H + + HCO 3 - Aguda Obstrução das vias respiratórias Desordens neuromusculares Doenças do SNC Inalação de [CO 2 ] Crônica Obstrução Alveolar (Enfisema Pulmonar)
10 DISTÚRBIOS DO EQUILÍBRIO ÁCIDO-BASE alcalose respiratória Hiperventilação dos alvéolos Diminuição da concentração de CO 2 CO 2 + H 2 O H 2 CO 3 H + + HCO 3 - ansiedade SNC envenenamento febre ventilação artificial altitude = Pressão Atmosférica = P alveolar DISTÚRBIOS DO EQUILÍBRIO ÁCIDO-BASE acidose e alcalose metabólica Acidose Metabólica ingestão de ácidos orgânicos não-voláteis eliminação excessiva de bases (diarréia severa) produção de ácidos metabólicos em excesso Alcalose Metabólica ingestão de excesso de bases (mais comum: bicarbonato de sódio) eliminação excessiva de ácidos (vômito prolongado; lavagem estomacal)
11 Aminoácidos AMINOÁCIDOS As proteínas são as macromoléculas biológicas mais abundantes. Estão presentes em todas as células e em todas as partes das células. As proteínas participam de todos os processos celulares, exibindo uma quase infinidade de funções As proteínas são constituídas por 20 aminoácidos naturais ESTRUTURA FUNÇÃO CATÁLISE ENZIMÁTICA SINALIZAÇÃO EXTRACELULAR PROTEÇÃO IMUNE TRANSPORTE DE SUBSTÂNCIAS PROTEÇÃO ELASTICIDADE MOTORES MOLECULARES RECEPTORES BOMBAS E CANAIS TRANSDUÇÃO DE SINAL (PAPEL NUTRICIONAL)
12 AMINOÁCIDOS aspectos estruturais Os aminoácidos são as unidades monoméricas que compõem as proteínas. Os aminoácidos são α-aminoácidos e compartilham aspectos estruturais: carbono α Cadeia lateral diferem na estrutura, tamanho, carga elétrica e influenciam a solubilidade dos aminoácidos em água AMINOÁCIDOS aspectos estruturais Por conta do arranjo tetraédrico do carbono, os aminoácidos podem existir em dois únicos arranjos espaciais (estereoisômeros): L - levorrotatório (desvia a rotação da luz para a esquerda) D - dextrorrotatório (desvia a rotação da luz para direita) Praticamente todos os compostos biológicos com centro quiral ocorrem naturalmente em apenas uma forma estereoisomérica. Os resíduos de aminoácidos nas proteínas são L-estereoisômeros!!
13 AMINOÁCIDOS classificação Os 20 aminoácidos comuns são classificados com base nas propriedades da cadeia lateral (grupo R) em particular a polaridade e a tendência de interagir com água no ph biológico. Apolares, alifáticos Apolares, aromáticos Polares, não carregados Polares, carregados positivamente Polares, carregados negativamente AMINOÁCIDOS grupos R apolares e alifáticos Conformação rígida Reduz a flexibilidade estruturas das regiões polipeptídicas contendo prolina As cadeias laterais desse aminoácidos tendem a se agrupar através de interações hidrofóbicas estabilizando a estrutura da proteína
14 AMINOÁCIDOS grupos R aromáticos Esses aminoácidos são relativamente apolares e participam de interações hidrofóbicas. AMINOÁCIDOS grupos R polares, não carregados Solúveis em água (hidrofílicos). Esses aminoácidos contém grupos funcionais que formam pontes de hidrogênio com a água
15 AMINOÁCIDOS grupos R carregados positivamente A histidna possui cadeia lateral ionizável com pka perto da neutralidade. No ph 7.0, a histidina pode estar protonada ou sem carga, e pode servir como doador ou aceptor de prótons! Solúveis em água Aminoácidos nos quais o grupo R tem carga positiva significativa em ph 7,0. AMINOÁCIDOS grupos R carregados negativamente
16 AMINOÁCIDOS ponte dissulfeto A cisteína é facilmente oxidada para formar um aminoácido dimérico, unido covalentemente, chamado cistina, no qual duas cisteínas estão ligadas por ponte dissulfeto Os resíduos ligados por pontes dissulfeto são fortemente hidrofóbicos As pontes dissulfeto têm importante papel na estabilização de estruturas de muitas proteínas, em virtude da formação de ligações covalentes entre diferentes partes de uma proteína ou entre duas cadeias protéicas distintas AMINOÁCIDOS incomuns Além dos 20 aminoácidos comuns, existem muitos outros mais raros. Alguns são modificados depois que a proteína é sintetizada. Outros 300 aminoácidos estão presentes em sistemas biológicos mas não são constituintes de proteínas.
17 AMINOÁCIDOS Comportamento ácido-base Os grupos carboxila e amino e os grupos R ionizáveis atuam como ácidos e bases fracas. Aminoácidos (sem cadeia lateral ionizável) são íons dipolares ou zwitterions AMINOÁCIDOS comportamento ácido-base Aminoácidos (sem cadeia lateral ionizável) podem atuar tanto como ácido como quanto base (anfóteros ou anfólitos) ácido (doador de prótons) base (aceptor de prótons)
18 AMINOÁCIDOS curva de titulação da glicina carga total: Todos os aminoácidos com apenas um grupo amino e um grupo carboxila têm curvas de titulação semelhante a da glicina AMINOÁCIDOS ponto isoelétrico carga total: ponto isoeletrico: pi ph no qual a carga total de uma molécula é igual a zero. Para a glicina, o pka pode ser calculado com:
19 AMINOÁCIDOS efeito do ambiente no pk a Repulsão entre o grupo amino e o próton liberado diminui o pka. As cargas opostas diminuem o pka, estabilizando o zwitterion Os átomos de oxigênio eletronegativos da carboxila atraem os elétrons para si, aumentando a tendência do grupo amino de doar o próton O pk a de qualquer grupo funcional é altamente afetado pelo ambiente químico AMINOÁCIDOS efeito do ambiente no pk a O pka normal para o grupo amino é 10,6 pk1 = 1.9 pk1 = 2.2 pk2 = 9.6 pk2 = 9.7 pkr = 3.65 ASPARTATO pkr = 4.3 GLUTAMATO O pka normal para grupo carboxila é 4,8 O pk a de qualquer grupo funcional é altamente afetado pelo ambiente químico
20 AMINOÁCIDOS efeito do ambiente no pk a As diferenças nos valores de pk a refletem os efeitos da cadeia lateral! AMINOÁCIDOS efeito do ambiente no pk a As diferenças nos valores de pk a refletem os efeitos da cadeia lateral!
13/08/2018. Escala de ph. Escala de ph. Crescimento básico. Crescimento ácido. Neutro. básico
 Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
 Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem do grego protos
Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem do grego protos
Origem grego (protos) primeira, mais importante
 PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
Macromolécula mais abundante nas células
 PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
Aminoácidos e peptídeos. Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I
 Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
Aminoácidos, Péptidos e Proteínas
 Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
Introdução à Bioquímica
 Introdução à Bioquímica Água Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. A água é fundamental para os seres vivos, atua como solvente
Introdução à Bioquímica Água Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. A água é fundamental para os seres vivos, atua como solvente
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA. Aminoácidos. Prof. Willame Bezerra
 CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
PROTEÍNAS. A palavra proteína derivada de proteos, (grego = primeira ou a mais importante)
 PROTEÍNAS A palavra proteína derivada de proteos, (grego = primeira ou a mais importante) Macromolécula mais abundante nas células Produto final da informação genética (DNA-RNA-Proteína) Diversidade funcional
PROTEÍNAS A palavra proteína derivada de proteos, (grego = primeira ou a mais importante) Macromolécula mais abundante nas células Produto final da informação genética (DNA-RNA-Proteína) Diversidade funcional
INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO ARINOS MINAS GERAIS
 INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO ARINOS MINAS GERAIS 2016 INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO PROFESSOR:
INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO ARINOS MINAS GERAIS 2016 INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO PROFESSOR:
Aula 1: Introdução à Bioquímica. A Água
 Aula 1: Introdução à Bioquímica A Água 1 A Célula Composição de uma célula PROTEÍNAS 15% LIPÍDIOS 2% CARBOIDRATOS 3% ÁC. NUCLEICOS 7% Sais Minerais 1% Água 70% 2 DISTRIBUIÇÃO CORPORAL DA ÁGUA EM ADULTOS
Aula 1: Introdução à Bioquímica A Água 1 A Célula Composição de uma célula PROTEÍNAS 15% LIPÍDIOS 2% CARBOIDRATOS 3% ÁC. NUCLEICOS 7% Sais Minerais 1% Água 70% 2 DISTRIBUIÇÃO CORPORAL DA ÁGUA EM ADULTOS
Água, ph e tampão. Profa. Alana Cecília
 Água, ph e tampão Profa. Alana Cecília Água: Estrutura e Propriedades Físico-químicas A água é o principal componente da maioria das células; Permeia todas as porções de todas as células; Importância em
Água, ph e tampão Profa. Alana Cecília Água: Estrutura e Propriedades Físico-químicas A água é o principal componente da maioria das células; Permeia todas as porções de todas as células; Importância em
Aminoácidos e Peptídeos
 Aminoácidos e Peptídeos 1 Qual a importância em conhecer os aminoácidos? 2 Aminoácidos Peptídeos Proteínas (polipeptídeos) Mas... O que são essas biomoléculas e onde estão localizadas? 3 Proteínas e peptídeos:
Aminoácidos e Peptídeos 1 Qual a importância em conhecer os aminoácidos? 2 Aminoácidos Peptídeos Proteínas (polipeptídeos) Mas... O que são essas biomoléculas e onde estão localizadas? 3 Proteínas e peptídeos:
Conceito de ph ph = - Log [H + ] Aumento [H + ] => diminuição do ph => acidose Diminuição [H + ] => aumento do ph => alcalose Alterações são dependent
![Conceito de ph ph = - Log [H + ] Aumento [H + ] => diminuição do ph => acidose Diminuição [H + ] => aumento do ph => alcalose Alterações são dependent Conceito de ph ph = - Log [H + ] Aumento [H + ] => diminuição do ph => acidose Diminuição [H + ] => aumento do ph => alcalose Alterações são dependent](/thumbs/50/27125458.jpg) Equilíbrio ácido-básico A concentração de H no FEC é mantida dentro de um limite extremamente estreito: 40 nmol/l = 1.000.000 menor que a Concentração dos outros íons!! [H] tem profundo efeito nos eventos
Equilíbrio ácido-básico A concentração de H no FEC é mantida dentro de um limite extremamente estreito: 40 nmol/l = 1.000.000 menor que a Concentração dos outros íons!! [H] tem profundo efeito nos eventos
Estrutura das Proteínas pode ser descrita em 4 níveis de organização
 PROTEÍNAS DNA Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem
PROTEÍNAS DNA Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem
Aminoácidos e Peptídeos. Profa. Alana Cecília
 Aminoácidos e Peptídeos Profa. Alana Cecília O que são aminoácidos? A estrutura geral dos aminoácidos inclui um grupo amina e um grupo carboxila, ambos ligados ao carbono α (aquele próximo ao grupo carboxila);
Aminoácidos e Peptídeos Profa. Alana Cecília O que são aminoácidos? A estrutura geral dos aminoácidos inclui um grupo amina e um grupo carboxila, ambos ligados ao carbono α (aquele próximo ao grupo carboxila);
ph arterial entre 7,35 e 7,45 [H+] ~ 40 nanomoles/l (10-9) CO2 (Ácido volátil) O CO 2 não se acumula no organismo, é eliminado pelos pulmões
![ph arterial entre 7,35 e 7,45 [H+] ~ 40 nanomoles/l (10-9) CO2 (Ácido volátil) O CO 2 não se acumula no organismo, é eliminado pelos pulmões ph arterial entre 7,35 e 7,45 [H+] ~ 40 nanomoles/l (10-9) CO2 (Ácido volátil) O CO 2 não se acumula no organismo, é eliminado pelos pulmões](/thumbs/60/44575873.jpg) Regulação do ph dos líquidos Regulação do ph dos líquidos ph = log[ ] LEC =, ±, (, mm) ph , Alcalose Ojetivo: Manutenção do ph sistêmico na faixa de normalidade. ph arterial entre, e, [H]
Regulação do ph dos líquidos Regulação do ph dos líquidos ph = log[ ] LEC =, ±, (, mm) ph , Alcalose Ojetivo: Manutenção do ph sistêmico na faixa de normalidade. ph arterial entre, e, [H]
O plasma sanguíneo contém uma reserva ("pool") total de carbonato (essencialmente HCO 3-
 Exercícios 1. Segel, Biochemical Calculations, Capítulo 1, Problema 1-19. O Ka do ácido fraco HA é 1,6 x 10-6. Calcular: a) O grau de ionização do ácido para uma solução 10-3 M. b) O ph 2. Segel, Biochemical
Exercícios 1. Segel, Biochemical Calculations, Capítulo 1, Problema 1-19. O Ka do ácido fraco HA é 1,6 x 10-6. Calcular: a) O grau de ionização do ácido para uma solução 10-3 M. b) O ph 2. Segel, Biochemical
LIPOFILIA LIPOFILIA COEFICIENTE DE PARTIÇÃO.
 LIPOFILIA A lipofilia de um composto é comumente estimada usando Log P a partir da partição de um sistema octanol/água aandrico@ifsc.usp.br A lipofilia é uma das propriedades mais importantes relacionadas
LIPOFILIA A lipofilia de um composto é comumente estimada usando Log P a partir da partição de um sistema octanol/água aandrico@ifsc.usp.br A lipofilia é uma das propriedades mais importantes relacionadas
ph SISTEMAS TAMPÕES Faculdade de Medicina PUC-Campinas Profa. Dra. Celene Fernandes Bernardes
 ph SISTEMAS TAMPÕES Faculdade de Medicina PUC-Campinas Profa. Dra. Celene Fernandes Bernardes ph = potencial hidrogeniônico ph = -log [H + ] Sorenson 1909 A escala de ph é logarítma; portanto, quando duas
ph SISTEMAS TAMPÕES Faculdade de Medicina PUC-Campinas Profa. Dra. Celene Fernandes Bernardes ph = potencial hidrogeniônico ph = -log [H + ] Sorenson 1909 A escala de ph é logarítma; portanto, quando duas
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas
 Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
4. Ácidos e Bases em Química Orgânica
 4. Ácidos e Bases em Química Orgânica Leitura Recomendada: Organic Chemistry, J. Clayden, N. Greeves, S. Warren, P. Wothers, Oxford, Oxford, 2001, cap. 8. Compreender aspectos de acidez e basicidade é
4. Ácidos e Bases em Química Orgânica Leitura Recomendada: Organic Chemistry, J. Clayden, N. Greeves, S. Warren, P. Wothers, Oxford, Oxford, 2001, cap. 8. Compreender aspectos de acidez e basicidade é
Lembrando. Ácidos são quaisquer substâncias capazes de ceder H+ Exemplos: ácido clorídrico, ácido lático, ácido úrico
 GASOMETRIA Lembrando Ácidos são quaisquer substâncias capazes de ceder H+ Exemplos: ácido clorídrico, ácido lático, ácido úrico Lembrando Bases são quaisquer substâncias capazes de captar H+ Exemplos:
GASOMETRIA Lembrando Ácidos são quaisquer substâncias capazes de ceder H+ Exemplos: ácido clorídrico, ácido lático, ácido úrico Lembrando Bases são quaisquer substâncias capazes de captar H+ Exemplos:
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA
 Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA CONCEITO DE SOLUÇÕES TAMPÃO, ph E pk 1. Conceito de soluções tampão (ph e pk) 2. Principais
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA CONCEITO DE SOLUÇÕES TAMPÃO, ph E pk 1. Conceito de soluções tampão (ph e pk) 2. Principais
BÁSICA EM IMAGENS. Aminoácidos, peptídeos e proteínas
 Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
ph do sangue arterial = 7.4
 Regulação do Equilíbrio Ácido Base ph do sangue arterial = 7.4 < 6.9 ou > 7.7 = MORTE 1 Importância do ph nos processos biológicos Protonação ou desprotonação de radicais proteicos Variação da carga total
Regulação do Equilíbrio Ácido Base ph do sangue arterial = 7.4 < 6.9 ou > 7.7 = MORTE 1 Importância do ph nos processos biológicos Protonação ou desprotonação de radicais proteicos Variação da carga total
Aminoácidos. Bioquímica Prof. Dr. Marcelo Soares
 Aminoácidos Aminoácidos Nutrição Século XIX: produtos contendo Nitrogênio eram essenciais para a sobrevivência dos animais G. J. Mulder (1839): termo Proteínas Gr Proteios (Primário) Teoria: Proteínas
Aminoácidos Aminoácidos Nutrição Século XIX: produtos contendo Nitrogênio eram essenciais para a sobrevivência dos animais G. J. Mulder (1839): termo Proteínas Gr Proteios (Primário) Teoria: Proteínas
A molécula de água A ÁGUA 2
 A água A maior parte da superfície do planeta terra está coberto com água. A água é também a substância mais abundante dos sistemas vivos, perfazendo cerca de 70% ou mais do peso dos mesmos. A água influência
A água A maior parte da superfície do planeta terra está coberto com água. A água é também a substância mais abundante dos sistemas vivos, perfazendo cerca de 70% ou mais do peso dos mesmos. A água influência
Homeostase do ph. Ácidos e Bases. HA H + + A - HCl H + + Cl - H 2 CO 3 H + + HCO H + + NH 3. Escala de ph
 Frederico Gueiros Filho Formação: Bacharelado em Biologia - UERJ Mestrado em Genética - UFRJ Doutorado - Harvard Medical School - EUA Pós-doutorado - Harvard, Depto. MCB - EUA Interesse de pesquisa: Mecanismo
Frederico Gueiros Filho Formação: Bacharelado em Biologia - UERJ Mestrado em Genética - UFRJ Doutorado - Harvard Medical School - EUA Pós-doutorado - Harvard, Depto. MCB - EUA Interesse de pesquisa: Mecanismo
Aminoácidos e Peptideos
 Aminoácidos e Peptideos O que são aminoácidos? Precursores de vários tipos de biomoléculas Compostos formados por : um grupo amina primário [ ] um grupo ácido carboxílico [ ] ambos ligados a um carbono
Aminoácidos e Peptideos O que são aminoácidos? Precursores de vários tipos de biomoléculas Compostos formados por : um grupo amina primário [ ] um grupo ácido carboxílico [ ] ambos ligados a um carbono
Ácidos, bases e sistemas tampão
 Ácidos, bases e sistemas tampão Ionização da água A água pura tem uma baixa concentração de iões hidrónio (H 3 O + ) e uma igual concentração de iões hidróxido (OH - ) Os ácidos são dadores de protões
Ácidos, bases e sistemas tampão Ionização da água A água pura tem uma baixa concentração de iões hidrónio (H 3 O + ) e uma igual concentração de iões hidróxido (OH - ) Os ácidos são dadores de protões
1. INTRODUÇÃO. Polímeros biológicos. Polissacarídeos Proteínas Ácidos Nucléicos. Reservas de energia. Armazenamento e Transmissão de informações
 AMINOÁIDOS 1. INTRODUÇÃO Polímeros biológicos Polissacarídeos Proteínas Ácidos Nucléicos Reservas de energia Materiais estruturais Marcadores bioquímicos Armazenamento e Transmissão de informações PROTEÍNAS
AMINOÁIDOS 1. INTRODUÇÃO Polímeros biológicos Polissacarídeos Proteínas Ácidos Nucléicos Reservas de energia Materiais estruturais Marcadores bioquímicos Armazenamento e Transmissão de informações PROTEÍNAS
Lista de Exercícios de Bioquímica
 Universidade Federal de Santa Catarina - UFSC Departamento de Bioquímica - CCB Disciplina: BQA5125 - Bioquímica para Engenharia Sanitária e Ambiental Bolsistas REUNI: Priscila G. A. Martins e Tiago Bortolotto
Universidade Federal de Santa Catarina - UFSC Departamento de Bioquímica - CCB Disciplina: BQA5125 - Bioquímica para Engenharia Sanitária e Ambiental Bolsistas REUNI: Priscila G. A. Martins e Tiago Bortolotto
Rafael Mesquita. Aminoácidos
 Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
Carla Bittar Bioquímica e Metabolismo Animal
 Carla Bittar Bioquímica e Metabolismo Animal Compostos orgânicos Unidades formadoras de PROTEÍNAS Ligações covalentes com perda de água Moléculas pequenas PM de aproximadamente 130 Estrutura da célula
Carla Bittar Bioquímica e Metabolismo Animal Compostos orgânicos Unidades formadoras de PROTEÍNAS Ligações covalentes com perda de água Moléculas pequenas PM de aproximadamente 130 Estrutura da célula
TEORIA DE ÁCIDOS E BASES
 TEORIA DE ÁCIDOS E BASES Proposição de S. Arrhenius (1887) Substâncias produtoras de íons hidrogênio em água fossem chamadas de ácidos Substâncias produtoras de íons hidroxila em água fossem chamadas de
TEORIA DE ÁCIDOS E BASES Proposição de S. Arrhenius (1887) Substâncias produtoras de íons hidrogênio em água fossem chamadas de ácidos Substâncias produtoras de íons hidroxila em água fossem chamadas de
QBQ 0204 Bioquímica. Carlos Hotta e Glaucia Souza. Introdução à disciplina 11/03/17
 QBQ 0204 Bioquímica Introdução à disciplina Carlos Hotta e Glaucia Souza 11/03/17 Organização do curso Os tópicos serão tratados em aulas expositivas e resolução de exercícios. Material disponível em http://carloshotta.com.br/qbq0304
QBQ 0204 Bioquímica Introdução à disciplina Carlos Hotta e Glaucia Souza 11/03/17 Organização do curso Os tópicos serão tratados em aulas expositivas e resolução de exercícios. Material disponível em http://carloshotta.com.br/qbq0304
TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO. Profa. Dra. Celene Fernandes Bernardes
 TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO Profa. Dra. Celene Fernandes Bernardes Plasma sanguíneo ph normal Acidose Alcalose Líquido extracelular Sangue arterial
TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO Profa. Dra. Celene Fernandes Bernardes Plasma sanguíneo ph normal Acidose Alcalose Líquido extracelular Sangue arterial
Regulação renal do equilíbrio ácido base
 Universidade de São Paulo Faculdade de Medicina de Ribeirão Preto Informática Biomédica Regulação renal do equilíbrio ácido base Gabriela Silva Borges O que é ácido e base? Função Química conjunto de compostos
Universidade de São Paulo Faculdade de Medicina de Ribeirão Preto Informática Biomédica Regulação renal do equilíbrio ácido base Gabriela Silva Borges O que é ácido e base? Função Química conjunto de compostos
Aminoácidos peptídeos e proteínas
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com Algumas funções de proteínas A luz produzida
Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com Algumas funções de proteínas A luz produzida
QUÍMICA ANALÍTICA APLICADA - QUI 111 SOLUÇÃO TAMPÃO Natal/RN SOLUÇÃO TAMPÃO
 QUÍMICA ANALÍTICA APLICADA - QUI 111 SOLUÇÃO TAMPÃO Prof a. Nedja Suely Fernandes 2014.1 Natal/RN SOLUÇÃO TAMPÃO É uma solução que resiste a uma modificação da concentração de íon hidrogênio ou de ph,
QUÍMICA ANALÍTICA APLICADA - QUI 111 SOLUÇÃO TAMPÃO Prof a. Nedja Suely Fernandes 2014.1 Natal/RN SOLUÇÃO TAMPÃO É uma solução que resiste a uma modificação da concentração de íon hidrogênio ou de ph,
SISTEMA TAMPÃO NOS ORGANISMOS ANIMAIS
 SISTEMA TAMPÃO NOS ORGANISMOS ANIMAIS Regulação do Equilíbrio Ácido-Básico ph = Potencial Hidrogeniônico Concentração de H + Quanto mais ácida uma solução maior sua concentração de H + e menor o seu ph
SISTEMA TAMPÃO NOS ORGANISMOS ANIMAIS Regulação do Equilíbrio Ácido-Básico ph = Potencial Hidrogeniônico Concentração de H + Quanto mais ácida uma solução maior sua concentração de H + e menor o seu ph
AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES
 UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS NOTURNO AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Cibele Rosalin Líria Domingues Luma Antonio
UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS NOTURNO AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Cibele Rosalin Líria Domingues Luma Antonio
1.5. Ácidos e Bases (Bibliografia Principal: Brown, 2nd) Primeira Definição: Arrhenius (1884)
 1.5. Ácidos e Bases (Bibliografia Principal: Brown, 2nd) i) Reações orgânicas são catalisadas por: a) ácidos doadores de prótons (Ex: H 3 O + ) b) ácidos de Lewis (Ex: AlCl 3 ) ii) Muitas reações em química
1.5. Ácidos e Bases (Bibliografia Principal: Brown, 2nd) i) Reações orgânicas são catalisadas por: a) ácidos doadores de prótons (Ex: H 3 O + ) b) ácidos de Lewis (Ex: AlCl 3 ) ii) Muitas reações em química
AMINOÁCIDOS. - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos;
 1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
Equilíbrio ácido-básico. Monitor: Tarcísio Alves Teixeira Professor: Guilherme Soares Fisiologia Veterinária / MFL / IB / UFF
 Equilíbrio ácido-básico Monitor: Tarcísio Alves Teixeira Professor: Guilherme Soares Fisiologia Veterinária / MFL / IB / UFF O que são Ácidos e Bases Ácido: substância que, em solução, é capaz de doar
Equilíbrio ácido-básico Monitor: Tarcísio Alves Teixeira Professor: Guilherme Soares Fisiologia Veterinária / MFL / IB / UFF O que são Ácidos e Bases Ácido: substância que, em solução, é capaz de doar
Prof. Luiz F. Silva Jr - IQ-USP
 ü Leitura Recomendada: Organic Chemistry, J. Clayden, N. Greeves, S. Warren, P. Wothers, Oxford, Oxford, 2001, cap. 8. ü Compreender aspectos de acidez e basicidade é essencial em Química Orgânica: i)
ü Leitura Recomendada: Organic Chemistry, J. Clayden, N. Greeves, S. Warren, P. Wothers, Oxford, Oxford, 2001, cap. 8. ü Compreender aspectos de acidez e basicidade é essencial em Química Orgânica: i)
1164 BIOLOGIA ESTRUTURAL Aula 1 Prof. Dr. Valmir Fadel
 H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
UFSC. Química (Amarela) Resposta: = 05
 Resposta: 01 + 04 = 05 01. Correto. Apresenta carboxila e grupamento amino no carbono alfa. 02. Incorreto. Com a elevação do ph ocorre a desprotonação da carboxila formando carga negativa. 04. Correto.
Resposta: 01 + 04 = 05 01. Correto. Apresenta carboxila e grupamento amino no carbono alfa. 02. Incorreto. Com a elevação do ph ocorre a desprotonação da carboxila formando carga negativa. 04. Correto.
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS. Bianca Zingales IQ-USP
 MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
Sistema Respiratório. Superior. Língua. Inferior
 Sistema Respiratório Língua Superior Inferior Funções 1. Troca de gases entre a atmosfera e o sangue. 2. Regulação homeostática do ph corporal 3. Proteção contra substâncias irritantes e patógenos 4. Vocalização
Sistema Respiratório Língua Superior Inferior Funções 1. Troca de gases entre a atmosfera e o sangue. 2. Regulação homeostática do ph corporal 3. Proteção contra substâncias irritantes e patógenos 4. Vocalização
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 5ª AULA PRÁTICA
 Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 5ª AULA PRÁTICA EQUILÍBRIO ÁCIDO-BASE NO ORGANISMO HUMANO REGULAÇÃO DA CONCENTRAÇÃO HIDROGENIÓNICA - IMPORTÂNCIA
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 5ª AULA PRÁTICA EQUILÍBRIO ÁCIDO-BASE NO ORGANISMO HUMANO REGULAÇÃO DA CONCENTRAÇÃO HIDROGENIÓNICA - IMPORTÂNCIA
Aula de Bioquímica I. Tema: Água. Prof. Dr. Júlio César Borges
 Aula de Bioquímica I Tema: Água Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Aula de Bioquímica I Tema: Água Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Ácidos e Bases, intermediários de reações orgânicas. Profa. Alceni Augusta Werle Profa. Tania Marcia do Sacramento Melo
 Ácidos e Bases, intermediários de reações orgânicas Parte I Profa. Alceni Augusta Werle Profa. Tania Marcia do Sacramento Melo 1-Introdução Revisão da teoria de ácidos de Arrhenius, Brönsted-Lowry e de
Ácidos e Bases, intermediários de reações orgânicas Parte I Profa. Alceni Augusta Werle Profa. Tania Marcia do Sacramento Melo 1-Introdução Revisão da teoria de ácidos de Arrhenius, Brönsted-Lowry e de
Tampão. O que é? MISTURA DE UM ÁCIDO FRACO COM SUA BASE CONJUGADA, QUE ESTABILIZA O P H DE UMA SOLUÇÃO
 Tampões biológicos Relembrar os conceitos de ácido e base (Brönsted-Lowry), ph, pka; Compreender a importância do ph na manutenção da estrutura tridimensional das biomoléculas; Conhecer os valores de ph
Tampões biológicos Relembrar os conceitos de ácido e base (Brönsted-Lowry), ph, pka; Compreender a importância do ph na manutenção da estrutura tridimensional das biomoléculas; Conhecer os valores de ph
3 LIGANTES. 3.1 Aspectos biológicos
 LIGANTES 38 3 LIGANTES Serão descritos os principais aspectos químicos e biológicos dos ligantes estudados neste trabalho. A importância desse capítulo fundamenta-se no fato de que os aminoácidos são as
LIGANTES 38 3 LIGANTES Serão descritos os principais aspectos químicos e biológicos dos ligantes estudados neste trabalho. A importância desse capítulo fundamenta-se no fato de que os aminoácidos são as
AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES
 Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
Universidade Federal Rural de Pernambuco
 Universidade Federal Rural de Pernambuco Departamento de Morfologia e Fisiologia Animal Área de Biofísica Medindo o potencial Hidrogeniônico Prof. Romildo Nogueira 1. Entendendo as bases A manutenção da
Universidade Federal Rural de Pernambuco Departamento de Morfologia e Fisiologia Animal Área de Biofísica Medindo o potencial Hidrogeniônico Prof. Romildo Nogueira 1. Entendendo as bases A manutenção da
Ciência que estuda a química da vida
 Ciência que estuda a química da vida Mostra como o conjunto de moléculas inanimadas que constituem os seres vivos interagem para manter e perpetuar a vida seguindo as leis da química e da física e conferindo
Ciência que estuda a química da vida Mostra como o conjunto de moléculas inanimadas que constituem os seres vivos interagem para manter e perpetuar a vida seguindo as leis da química e da física e conferindo
Manutenção do ph do sangue
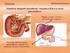 Manutenção do ph do sangue Muitos dos fluidos biológicos, quer no interior, quer no exterior das células, apresentam intervalos de ph muito apertados, ou seja um valor de ph praticamente constante, uma
Manutenção do ph do sangue Muitos dos fluidos biológicos, quer no interior, quer no exterior das células, apresentam intervalos de ph muito apertados, ou seja um valor de ph praticamente constante, uma
Estrutura e propriedade de aminoácidos Definição de ácidos fracos, fortes Ligação peptídica Peptídeos. Referência: Stryer ou Lehninger
 Estrutura e propriedade de aminoácidos Definição de ácidos fracos, fortes Ligação peptídica Peptídeos Referência: Stryer ou Lehninger Deoxi-hemoglobina Slide - Lehninger 5a edição Estrutura de proteínas
Estrutura e propriedade de aminoácidos Definição de ácidos fracos, fortes Ligação peptídica Peptídeos Referência: Stryer ou Lehninger Deoxi-hemoglobina Slide - Lehninger 5a edição Estrutura de proteínas
Aula 5 Estrutura e função de proteínas
 Aula 5 Estrutura e função de proteínas parte 1: aminoácidos Parte 2: estrutura Proteínas As proteínas são os principais constituinte da célula Importantes na manutenção da vida Desempenham diversas funções
Aula 5 Estrutura e função de proteínas parte 1: aminoácidos Parte 2: estrutura Proteínas As proteínas são os principais constituinte da célula Importantes na manutenção da vida Desempenham diversas funções
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos
 Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
REVISÃO: ENADE BIOQUÍMICA - 1
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
Aula Teórica 3 Cálculo de ph de Ácidos Fracos e Bases Fracas
 Aula Teórica 3 Cálculo de ph de Ácidos Fracos e Bases Fracas JRM Como calcular o ph de soluções de ácidos e bases fracas? Considere um ácido fraco (monoácido), HA H 2 O H OH - ------ Keq ~ 10-14 HA H A
Aula Teórica 3 Cálculo de ph de Ácidos Fracos e Bases Fracas JRM Como calcular o ph de soluções de ácidos e bases fracas? Considere um ácido fraco (monoácido), HA H 2 O H OH - ------ Keq ~ 10-14 HA H A
), a concentração interna na célula é relativamente elevada (da ordem de 10-3 mol/l).
 Íons metálicos em sistemas biológicos Shriver & Atikins, cap. 26 No interior de uma célula as concentrações de íons metálicos são significativamente diferentes daquelas observadas no meio externo aonde
Íons metálicos em sistemas biológicos Shriver & Atikins, cap. 26 No interior de uma célula as concentrações de íons metálicos são significativamente diferentes daquelas observadas no meio externo aonde
tampão Prof a Alessandra Smaniotto QMC Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B
 Cap 3: Equilíbrio Químico Soluções tampão Prof a Alessandra Smaniotto QMC 5325 - Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B Água:excepcional habilidade em dissolver grande
Cap 3: Equilíbrio Químico Soluções tampão Prof a Alessandra Smaniotto QMC 5325 - Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B Água:excepcional habilidade em dissolver grande
Ácidos e Bases. Funções Inorgânicas
 Ácidos e Bases Funções Inorgânicas Funções Inorgânicas As substâncias podem ser classificadas em duas classes: Substâncias orgânicas: aquelas que contém carbono. Substâncias inorgânicas: aquelas formadas
Ácidos e Bases Funções Inorgânicas Funções Inorgânicas As substâncias podem ser classificadas em duas classes: Substâncias orgânicas: aquelas que contém carbono. Substâncias inorgânicas: aquelas formadas
QB70C:// Química (Turmas S71/S72) Ácidos e Bases. Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 11 Atkins (5ed.
 QB70C:// Química (Turmas S71/S72) Ácidos e Bases Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 11 Atkins (5ed.) Pai, o que é chuva ácida? NaO idróxido de magnésio Mg(O)
QB70C:// Química (Turmas S71/S72) Ácidos e Bases Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 11 Atkins (5ed.) Pai, o que é chuva ácida? NaO idróxido de magnésio Mg(O)
21/07/14. Processos metabólicos. Conceitos Básicos. Respiração. Catabolismo de proteínas e ácidos nucleicos. Catabolismo de glicídios
 Prof. Dr. Adriano Bonfim Carregaro Medicina Veterinária FZEA USP www.anestesia.vet.br Processos metabólicos Respiração Catabolismo de proteínas e ácidos nucleicos Ácidos acético, sulfúrico, fosfórico e
Prof. Dr. Adriano Bonfim Carregaro Medicina Veterinária FZEA USP www.anestesia.vet.br Processos metabólicos Respiração Catabolismo de proteínas e ácidos nucleicos Ácidos acético, sulfúrico, fosfórico e
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012. Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICOPRÁTICO 5ª AULA TEÓRICOPRÁTICA RESOLUÇÃO
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICOPRÁTICO 5ª AULA TEÓRICOPRÁTICA RESOLUÇÃO
Equilíbrio Ácido Base. Definição de Brønsted-Lowry. O íon H + (aq) é simplesmente um próton sem elétrons. Em água, o H + (aq) forma aglomerados.
 Equilíbrio Ácido Base Definição de Brønsted-Lowry Ácidos têm gosto azedo e bases têm gosto amargo. Definição de Arrhenius: os ácidos aumentam a [H + ] e as bases aumentam a [OH ] em solução. Arrhenius:
Equilíbrio Ácido Base Definição de Brønsted-Lowry Ácidos têm gosto azedo e bases têm gosto amargo. Definição de Arrhenius: os ácidos aumentam a [H + ] e as bases aumentam a [OH ] em solução. Arrhenius:
Ciência que estuda a química da vida
 Ciência que estuda a química da vida Mostra como o conjunto de moléculas inanimadas que constituem os seres vivos interagem para manter e perpetuar a vida seguindo as leis da química e da física e conferindo
Ciência que estuda a química da vida Mostra como o conjunto de moléculas inanimadas que constituem os seres vivos interagem para manter e perpetuar a vida seguindo as leis da química e da física e conferindo
Acidez e Basicidade de Compostos Orgânicos
 Acidez e Basicidade de Compostos Orgânicos 1. Teorias sobre ácidos e bases Teoria de Arrhenius (1884) Substâncias neutras dissolvidas em água formam espécies carregadas ou íons através de dissociação iônica
Acidez e Basicidade de Compostos Orgânicos 1. Teorias sobre ácidos e bases Teoria de Arrhenius (1884) Substâncias neutras dissolvidas em água formam espécies carregadas ou íons através de dissociação iônica
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS. Bianca Zingales IQ-USP
 MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
Componentes Químicos das Células
 Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
- Molécula polar, devido à elevada electronegatividade do átomo de oxigénio e à própria estrutura da molécula.
 Água A água é a substância mais abundante dos organismos vivos, correspondendo a 70% ou mais da sua composição. Os primeiros organismos vivos surgiram certamente no meio aquoso, e o curso da evolução foi
Água A água é a substância mais abundante dos organismos vivos, correspondendo a 70% ou mais da sua composição. Os primeiros organismos vivos surgiram certamente no meio aquoso, e o curso da evolução foi
Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III
 Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III A maioria das cadeias polipeptídicas naturais contém entre 50 e 2.000 aminoácidos e são comumente referidas como proteínas. Peptídeos
Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III A maioria das cadeias polipeptídicas naturais contém entre 50 e 2.000 aminoácidos e são comumente referidas como proteínas. Peptídeos
UNIFESO - Engenharia Ambiental Prof. Edson Rodrigo Fernandes dos Santos. ÁGUA, ph E TAMPÕES
 UNIFES - Engenharia Ambiental Prof. Edson Rodrigo Fernandes dos Santos ÁGUA, p E TAMPÕES ÁGUA É uma substância essencial para o organismo. Todas as reações bioquímicas ocorrem em meio aquoso. É uma substância
UNIFES - Engenharia Ambiental Prof. Edson Rodrigo Fernandes dos Santos ÁGUA, p E TAMPÕES ÁGUA É uma substância essencial para o organismo. Todas as reações bioquímicas ocorrem em meio aquoso. É uma substância
Aminoácidos. Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP.
 Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
Ciência que estuda a química da vida
 Ciência que estuda a química da vida Mostra como o conjunto de moléculas inanimadas que constituem os seres vivos interagem para manter e perpetuar a vida seguindo as leis da química e da física que regem
Ciência que estuda a química da vida Mostra como o conjunto de moléculas inanimadas que constituem os seres vivos interagem para manter e perpetuar a vida seguindo as leis da química e da física que regem
 aandrico@if.sc.usp.br a molécula de água, a ligação existente é covalente, na qual dois átomos de hidrogênio compartilham elétrons com um átomo de oxigênio. A molécula de água possui dois dipolos, com
aandrico@if.sc.usp.br a molécula de água, a ligação existente é covalente, na qual dois átomos de hidrogênio compartilham elétrons com um átomo de oxigênio. A molécula de água possui dois dipolos, com
ÁGUA, SOLUBILIDADE E PH
 Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia ÁGUA, SOLUBILIDADE E PH ÁGUA: UM COMPONENTE E SOLVENTE UNIVERSAL A ÁGUA
Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia ÁGUA, SOLUBILIDADE E PH ÁGUA: UM COMPONENTE E SOLVENTE UNIVERSAL A ÁGUA
AMINOÁCIDOS. Dra. Flávia Cristina Goulart. Bioquímica
 AMINOÁCIDOS Dra. Flávia Cristina Goulart Bioquímica Os aminoácidos (aa). O que são? AMINOÁCIDOS São as unidades fundamentais das PROTEÍNAS. São ácidos orgânicos formados por átomos de carbono, hidrogênio,
AMINOÁCIDOS Dra. Flávia Cristina Goulart Bioquímica Os aminoácidos (aa). O que são? AMINOÁCIDOS São as unidades fundamentais das PROTEÍNAS. São ácidos orgânicos formados por átomos de carbono, hidrogênio,
Você deve desenhar o aminoácido com o grupo amino protonado (pka > 7) e o grupo carboxílico desprotonado (pka <7).
 QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011
 BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
Modelos Gerais de Ácidos, Bases e Reações Ácido-Base
 Modelos Gerais de Ácidos, Bases e Reações Ácido-Base Prof.: Willame Bezerra A Química dos Ácidos e Bases Os ácidos e as bases estão presentes em toda parte. Os vulcões e as fontes térmicas podem ser muito
Modelos Gerais de Ácidos, Bases e Reações Ácido-Base Prof.: Willame Bezerra A Química dos Ácidos e Bases Os ácidos e as bases estão presentes em toda parte. Os vulcões e as fontes térmicas podem ser muito
Programa de Pós-Graduação em Química
 1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
29/08/2015 QUÍMICA DE PROTEÍNAS. Medicina Veterinária IBGM - IBS. Medicina Veterinária IBGM - IBS
 QUÍMICA DE PROTEÍNAS D i s c i p l i n a : b i o q u í m i c a, p r o f. D r. Va g n e O l i v e i ra E-mail: vagne_melo_oliveira@outlook.com Medicina Veterinária IBGM - IBS Medicina Veterinária IBGM -
QUÍMICA DE PROTEÍNAS D i s c i p l i n a : b i o q u í m i c a, p r o f. D r. Va g n e O l i v e i ra E-mail: vagne_melo_oliveira@outlook.com Medicina Veterinária IBGM - IBS Medicina Veterinária IBGM -
Introdução. Estrutura dos Aminoácidos e Proteínas. Aminoácidos componentes de proteínas. Aminoácidos componentes de proteínas 10/02/2012.
 Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
Fundamentos de Química Profa. Janete Yariwake
 Soluções. Equilíbrio químico em solução aquosa Equilíbrio químico: ácidos e bases 1 ácidos e bases cf. Arrhenius Exemplo: Preparo de uma solução de HCl em água HCl (aq) + H 2 O H 3 O + (aq) + Cl (aq) íon
Soluções. Equilíbrio químico em solução aquosa Equilíbrio químico: ácidos e bases 1 ácidos e bases cf. Arrhenius Exemplo: Preparo de uma solução de HCl em água HCl (aq) + H 2 O H 3 O + (aq) + Cl (aq) íon
Ciência que estuda a química da vida (características dos seres vivos)
 Ciência que estuda a química da vida (características dos seres vivos) Características dos seres vivos Complexidade química e organização microscópica Elementos químicos comuns C, O, N, H e P Grande diversidade
Ciência que estuda a química da vida (características dos seres vivos) Características dos seres vivos Complexidade química e organização microscópica Elementos químicos comuns C, O, N, H e P Grande diversidade
- Apresentam uma fórmula básica: um átomo central de carbono onde se ligam:
 1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
Ciência que estuda a química da vida (características dos seres vivos)
 Ciência que estuda a química da vida (características dos seres vivos) Características dos seres vivos 1 - Complexidade química e organização microscópica Elementos químicos comuns C, O, N, H e P Grande
Ciência que estuda a química da vida (características dos seres vivos) Características dos seres vivos 1 - Complexidade química e organização microscópica Elementos químicos comuns C, O, N, H e P Grande
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Petr Soares de Alencar DISTÚRBIOS DO EQUILÍBRIO ÁCIDO BASE
 Petr Soares de Alencar DISTÚRBIOS DO EQUILÍBRIO ÁCIDO BASE GASOMETRIA ARTERIAL GASOMETRIA ARTERIAL Paciente com os seguintes valores na gasometria arterial: ph = 7,08; HCO - 3 = 10mEq/litro; PCO 2 = 35
Petr Soares de Alencar DISTÚRBIOS DO EQUILÍBRIO ÁCIDO BASE GASOMETRIA ARTERIAL GASOMETRIA ARTERIAL Paciente com os seguintes valores na gasometria arterial: ph = 7,08; HCO - 3 = 10mEq/litro; PCO 2 = 35
Cerca de 99% dos átomos no corpo humano são de H, O, C e N. Oxigenio 63% Hidrogenio 25.2% Carbono 9.5% Azoto 1.4%
 Cerca de 99% dos átomos no corpo humano são de H, O, C e N Oxigenio 63% Hidrogenio 25.2% Carbono 9.5% Azoto 1.4% Tipos de ligação covalente mais comuns em biomoleculas As reacções bioquímicas utilizam
Cerca de 99% dos átomos no corpo humano são de H, O, C e N Oxigenio 63% Hidrogenio 25.2% Carbono 9.5% Azoto 1.4% Tipos de ligação covalente mais comuns em biomoleculas As reacções bioquímicas utilizam
