PD-L1 IHC 28-8 pharmdx. SK testes para utilização no Autostainer Link 48
|
|
|
- Eugénio Conceição
- 5 Há anos
- Visualizações:
Transcrição
1 PD-L1 IHC 28-8 pharmdx SK testes para utilização no Autostainer Link 48 Índice 1. Finalidade Resumo e explicação NSCLC não escamoso Carcinoma das células escamosas da cabeça e pescoço (SCCHN) Carcinoma urotelial Melanoma Princípio do procedimento Materiais fornecidos Materiais necessários, mas não fornecidos Precauções Conservação Preparação das amostras Cortes impregnados em parafina Utilização de tecidos descalcificados Recomendação de conservação de secção cortada Preparação dos reagentes Procedimento de coloração no Autostainer Link Controlo de qualidade Verificação do ensaio Interpretação da coloração Interpretação da coloração: NSCLC não escamoso Interpretação da coloração: Carcinoma das células escamosas da cabeça e pescoço (SCCHN) Interpretação da coloração: Carcinoma urotelial Interpretação da coloração: Melanoma Avaliação das lâminas Limitações Limitações gerais Limitações específicas do produto Avaliação do desempenho não clínico Especificidade analítica para o PD-L1 IHC 28-8 pharmdx Tecidos normais e neoplásicos Avaliação do desempenho Avaliação do desempenho: NSCLC não escamoso Avaliação do desempenho: SCCHN Avaliação do desempenho: UC Avaliação do desempenho: Melanoma Resolução de problemas Referências...23 P03914PT_04/SK / p. 1/23
2 1. Finalidade Para utilização em diagnóstico in vitro. O PD-L1 IHC 28-8 pharmdx é um ensaio de imuno-histoquímica qualitativa que utiliza o anticorpo Monoclonal Rabbit Anti-PD-L1, Clone 28-8, para a deteção da proteína PD-L1 em tecidos de melanoma, carcinoma das células escamosas da cabeça e pescoço (SCCHN), cancro do pulmão de células não escamosas e não pequenas (NSCLC) e carcinoma urotelial (UC) fixados em formol e impregnados em parafina (FFPE), através do sistema de visualização EnVision FLEX no Autostainer Link 48. A expressão da proteína PD-L1 é definida como a percentagem de células tumorais avaliáveis que apresentam coloração da membrana parcial ou total em qualquer intensidade, conforme definido pelas diretrizes de interpretação da coloração de indicação do tumor específico. A expressão da PD-L1, conforme detetada pelo PD-L1 IHC 28-8 pharmdx no SCCHN e NSCLC não escamoso, pode estar associada a uma maior sobrevivência resultante do OPDIVO (nivolumab). A expressão da PD-L1 conforme detetada pelo PD-L1 IHC 28-8 pharmdx no carcinoma urotelial pode estar associada a uma maior taxa de resposta resultante do OPDIVO. A expressão da PD-L1, conforme detetada pelo PD-L1 IHC 28-8 pharmdx, no melanoma, pode ser utilizada como um auxiliar na avaliação de doentes para quem o tratamento com a combinação de OPDIVO (nivolumab) e YERVOY (ipilimumab) esteja a ser considerado. 2. Resumo e explicação A ligação dos ligandos da PD-1, PD-L1 e PD-L2 ao recetor da PD-1 encontrado nas células T inibe a proliferação de células T e a produção de citoquina. A regulação superior dos ligandos da PD-1 ocorre em alguns tumores e a sinalização através desta via pode contribuir para a inibição da vigilância a células T imunes ativas dos tumores (1). O OPDIVO (nivolumab) é um anticorpo monoclonal de imunoglobulina humana G4 (IgG4) que se liga ao recetor da PD-1 e bloqueia a interação deste com a PD-L1 e a PD-L2, promovendo a inibição mediada pela via da PD-1 da resposta imune, incluindo a resposta imune antitumoral (2). Em modelos tumorais de ratinhos singeneicos, o bloqueio da atividade da PD-1 resultou num menor crescimento do tumor (3). As vantagens clínicas do OPDIVO e a utilidade clínica do PD-L1 IHC 28-8 pharmdx têm sido investigadas no NSCLC, no SCCHN, no UC e no melanoma. 2.1 NSCLC não escamoso A deteção de células tumorais com expressão da PD-L1 numa amostra de um doente com cancro do pulmão de células não escamosas e não pequenas pode indicar uma vantagem em termos de maior sobrevivência para o doente com o tratamento com OPDIVO (nivolumab). As amostras de doentes em estudos clínicos do OPDIVO patrocinados pela Bristol-Myers Squibb foram testadas utilizando o PD-L1 IHC 28-8 pharmdx. Os estudos clínicos CA investigaram a validade clínica do PD-L1 IHC 28-8 pharmdx para a avaliação do estado da PD-L1 em doentes com NSCLC não escamoso tratados com o OPDIVO (5,11). 2.2 Carcinoma das células escamosas da cabeça e pescoço (SCCHN) A deteção de células tumorais com expressão da PD-L1 em amostras de um doente com SCCHN pode indicar uma vantagem em termos de maior sobrevivência para o doente com o tratamento com OPDIVO (nivolumab). As amostras de doentes em estudos clínicos do OPDIVO patrocinados pela Bristol-Myers Squibb foram testadas utilizando o PD-L1 IHC 28-8 pharmdx. Os estudos clínicos CA investigaram a validade clínica do PD-L1 IHC 28-8 pharmdx para a avaliação do estado da PD-L1 em doentes com SCCHN tratados com o OPDIVO (16). 2.3 Carcinoma urotelial A deteção de células tumorais com expressão da PD-L1 em amostras de doente com UC pode indicar uma vantagem em termos de maior taxa de resposta para o doente com o tratamento com OPDIVO (nivolumab). As amostras de doentes em estudos clínicos do OPDIVO patrocinados pela Bristol-Myers Squibb foram testadas utilizando o PD-L1 IHC 28-8 pharmdx. O estudo clínico CA investigou a validade clínica do PD-L1 IHC 28-8 pharmdx para a avaliação do estado da PD-L1 em doentes com UC tratados com o OPDIVO. 2.4 Melanoma O antigénio 4 associado aos linfócitos T citotóxicos (CTLA-4) é um regulador negativo da atividade das células T. YERVOY (ipilimumab) é um anticorpo monoclonal que se liga ao CTLA-4 e bloqueia a interação do CTLA-4 com os seus ligandos, CD80/CD86. O bloqueio do CTLA-4 tem demonstrado aumentar a ativação e proliferação de células T, o que contribui para um aumento geral da reação imune antitumoral (4). A PD-1 e o CTLA-4 inibem a imunidade antitumoral através de mecanismos complementares e não redundantes. A monoterapia com OPDIVO e a combinação de OPDIVO e YERVOY demonstraram uma melhoria significativamente maior da sobrevivência sem progressão em relação ao YERVOY de forma isolada em doentes com melanoma avançado que não tinham anteriormente recebido tratamento (8-10). As amostras de tecido de doentes com tumores de melanoma tratados com OPDIVO em estudos clínicos patrocinados pela Bristol- Myers Squibb foram testadas utilizando o PD-L1 IHC 28-8 pharmdx. O estudo clínico CA investigou a validade clínica do PD-L1 IHC 28-8 pharmdx para efeitos de avaliação da expressão da PD-L1 em doentes com melanoma tratados com OPDIVO, OPDIVO em combinação com YERVOY e YERVOY de forma isolada. OPDIVO e YERVOY são marcas comerciais registadas da Bristol-Myers Squibb. 3. Princípio do procedimento O PD-L1 IHC 28-8 pharmdx contém os reagentes otimizados e o protocolo necessário para concluir um procedimento de coloração por IHC de amostras FFPE utilizando o Autostainer Link 48 e o PT Link Pre-treatment Module (6). Após a incubação com o anticorpo monoclonal primário contra a PD-L1 ou com o Negative Control Reagent (NCR), as amostras são incubadas com um anticorpo de ligação específico às espécies hospedeiras do anticorpo primário, sendo depois incubadas com um reagente de visualização pronto a usar, que consiste em moléculas do anticorpo secundário e em moléculas de peroxidase de rábano associadas a uma estrutura base de polímero dextrano. A conversão enzimática do cromogénio adicionado posteriormente resulta na precipitação de um produto de reação visível no local do antigénio. A cor da reação cromogénica é modificada por um reagente de intensificação do cromogénio. Em seguida, é possível aplicar um contraste e uma lamela na amostra. Os resultados são interpretados utilizando um microscópio ótico. São fornecidas lâminas de controlo contendo duas linhas celulares humanas, fixadas em formol e impregnadas em parafina, para validar os processos de coloração. P03914PT_04/SK / p. 2/23
3 4. Materiais fornecidos PD-L1 IHC 28-8 pharmdx (Referência SK005) Os materiais enumerados abaixo são suficientes para 50 testes (50 lâminas incubadas com anticorpo primário contra a proteína PD-L1 e 50 lâminas incubadas com o Negative Control Reagent correspondente; 100 lâminas de teste no total). O anticorpo primário adicional da PD-L1 é fornecido no kit para corar 15 linhas celulares das lâminas de controlo. O número de testes baseia-se na utilização de 2 x 150 µl de cada reagente por lâmina, exceto para DAB+ e para a Target Retrieval Solution. O kit fornece materiais suficientes para, no máximo, 15 processos de coloração individuais. Quantidade Descrição 1 x 34,5 ml Peroxidase-Blocking Reagent PEROXIDASE-BLOCKING REAGENT Solução tamponada que contém peróxido de hidrogénio, detergente e 0,015 mol/l de azida de sódio. 1 x 19,5 ml Anticorpo primário: Monoclonal Rabbit Anti-PD-L1, Clone 28-8 MONOCLONAL RABBIT ANTI-PD-L1 CLONE 28-8 Anticorpo monoclonal de coelho anti PD-L1 numa solução tamponada que contém proteína estabilizadora e 0,015 mol/l de azida de sódio. 1 x 15 ml Negative Control Reagent* NEGATIVE CONTROL REAGENT Anticorpo IgG monoclonal de coelho de controlo numa solução tamponada que contém proteína estabilizadora e 0,015 mol/l de azida de sódio. *IgG de controlo Monoclonal Rabbit vendido ao abrigo da licença da Cell Signaling Technology. 1 x 34,5 ml LINKER, Anti-Rabbit LINKER, ANTI-RABBIT Anticorpo secundário de ratinho contra imunoglobulinas de coelho numa solução tamponada que contém proteína estabilizadora e 0,015 mol/l de azida de sódio. 1 x 34,5 ml Visualization Reagent-HRP VISUALIZATION REAGENT-HRP Dextrano associado a moléculas de peroxidase e moléculas de anticorpo secundário de caprino contra imunoglobulinas de coelho e ratinho numa solução tamponada, que contém proteína estabilizadora e um agente antimicrobiano. 15 x 7,2 ml DAB+ Substrate Buffer DAB+ SUBSTRATE BUFFER Solução tamponada que contém peróxido de hidrogénio e um agente antimicrobiano. 1 x 5 ml DAB+ Chromogen DAB+ CHROMOGEN 3,3'-diaminobenzidina tetrahidrocloreto num solvente orgânico. 1 x 34,5 ml DAB Enhancer DAB ENHANCER Sulfato cúprico em água. 6 x 30 ml EnVision FLEX Target Retrieval Solution, Low ph (50x) EnVision FLEX TARGET RETRIEVAL SOLUTION LOW ph (50X) Solução tamponada, ph 6,1, que contém detergente e um agente antimicrobiano. 15 lâminas PD-L1 IHC 28-8 pharmdx Control Slides CONTROL SLIDES Cada lâmina contém cortes de duas linhas celulares aglomeradas, fixadas em formol e impregnadas em parafina: NCI-H226** com expressão da proteína PD-L1 positiva (com origem em carcinoma das células escamosas do pulmão humano com expressão da proteína PD-L1 positiva) e MCF-7 com expressão da proteína PD-L1 negativa (com origem em adenocarcinoma da mama humano com expressão da proteína PD-L1 negativa). P03914PT_04/SK / p. 3/23
4 PD-L1, SK005 pharmdx XXXXX MCF-7: PD-L1 negativa NCI-H226: PD-L1 positiva **É reconhecido o contributo do Dr. AF Gazdar e do Dr. JD Minna nos Institutos Nacionais de Saúde (NIH) para o desenvolvimento da NCI-H226 (número ATCC: CRL-5826 ) (7) Nota: Todos os reagentes incluídos são especialmente formulados para a utilização com este kit. Para que o teste tenha o desempenho especificado, não podem ser feitas substituições, à exceção da EnVision FLEX Target Retrieval Solution, Low ph, 50x (Referência K8005). O PD-L1 IHC 28-8 pharmdx foi concebido para ser usado com o Autostainer Link 48. Consulte os manuais de utilizador do Autostainer Link 48 e do PT Link para obter mais informação. 5. Materiais necessários, mas não fornecidos PT Link Pre-treatment Module (Referências PT100/PT101/PT200) Autostainer Link 48 (Referência AS480) EnVision FLEX Wash Buffer, 20x (Referência K8007) EnVision FLEX Hematoxylin (Link) (Referência K8008) Água destilada ou desionizada (água de qualidade reagente) Cronómetro Tecidos positivos e negativos para utilizar como controlos do processo (consultar a secção Controlo de qualidade e a tabela 5) Lâminas de microscópio: lâminas de microscópio Dako FLEX IHC (Referência K8020) ou lâminas Fisherbrand Superfrost Plus carregadas Lamelas Meio de montagem permanente e reagentes acessórios necessários para a montagem de lamelas Microscópio ótico (ampliação de objetiva de 4x-40x) 6. Precauções 1. Para utilização em diagnóstico in vitro. 2. Para utilizadores profissionais. 3. Este produto contém azida de sódio (NaN 3 ), uma substância química altamente tóxica na forma pura. Em situações de concentrações do produto, embora não sendo classificada como perigosa, a NaN 3 pode reagir com as canalizações de chumbo e de cobre, formando acumulações de azidas metálicas altamente explosivas. Ao eliminar o produto, adicionar água abundante para evitar a acumulação de azida metálica na canalização (12). 4. O Anticorpo primário, o Negative Control Reagent, o Linker e o Visualization Reagent contêm material de origem animal. 5. As amostras, antes e depois da fixação, assim como todos os materiais expostos às amostras, deverão ser manuseados como sendo potencialmente infeciosos e eliminados com as precauções adequadas (13). 6. Os tempos e as temperaturas de incubação ou métodos diferentes dos especificados podem originar resultados erróneos. 7. Os reagentes apresentam uma diluição ideal. A diluição subsequente pode originar a perda de coloração do antigénio. 8. Caso sejam expostos a níveis de luz excessivos, o Visualization Reagent, o Liquid DAB+ Chromogen e a DAB+ Substrate- Chromogen Solution preparada podem ser afetados de forma adversa. Não conservar os componentes do sistema nem efetuar a coloração sob luz intensa como, por exemplo, luz solar direta. 9. Os resíduos de parafina podem dar origem a resultados falsos negativos. 10. Utilizar volumes de reagentes diferentes dos recomendados pode resultar na perda da imunorreatividade visível da PD-L Cortes de tecido de grandes dimensões presentes em 2/3 da lâmina podem necessitar de 3 x 150 µl de reagente. 12. Como regra geral, as pessoas com idade inferior a 18 anos não estão autorizadas a trabalhar com este produto. Os utilizadores devem ser cuidadosamente instruídos sobre os procedimentos de trabalho adequado, as propriedades perigosas do produto e as instruções de segurança necessárias. Consultar a Ficha de dados de segurança (FDS) para obter informações adicionais. 13. Usar equipamento de proteção pessoal adequado para evitar o contacto com a pele e os olhos. 14. A solução não utilizada deverá ser eliminada em conformidade com as regulamentações locais, regionais, nacionais e internacionais. 15. A ficha de dados de segurança encontra-se disponível para utilizadores profissionais mediante pedido. Perigo DAB+ Chromogen: Bifenil-3,3,4,4 -tetrailtetraamónio tetracloreto a 1-5% H350 Pode provocar cancro. H341 Suspeito de provocar anomalias genéticas. P201 Pedir instruções específicas antes da utilização. P202 Não manusear o produto antes de ter lido e percebido todas as precauções de segurança. P280 Usar luvas de proteção. Usar proteção ocular ou facial. Usar vestuário de proteção. P308 + P313 EM CASO DE exposição ou suspeita de exposição: consultar um médico. P405 Armazenar em local fechado à chave. P501 Eliminar o conteúdo/recipiente em conformidade com as regulamentações locais, regionais, nacionais e internacionais. P03914PT_04/SK / p. 4/23
5 Aviso EnVision FLEX Target Retrieval Solution, Low ph (50x): 1-5% de ácido cítrico H319 Provoca irritação ocular grave. H411 Tóxico para os organismos aquáticos com efeitos duradouros. P280 Usar proteção ocular ou facial. P273 Evitar a libertação para o ambiente. P264 Lavar cuidadosamente as mãos após manuseamento. P305 + P351 + P338 SE ENTRAR EM CONTACTO COM OS OLHOS: enxaguar cuidadosamente com água durante vários minutos. Se usar lentes de contacto, retire-as, se tal lhe for possível. Continuar a enxaguar. P337 + P313 Caso a irritação ocular persista: consultar um médico. P501 Eliminar o conteúdo/recipiente em conformidade com as regulamentações locais, regionais, nacionais e internacionais. 7. Conservação Conservar todos os componentes do PD-L1 IHC 28-8 pharmdx, incluindo as lâminas de controlo, no recipiente original e num local escuro a 2-8 C, quando não estiverem a ser utilizados no Autostainer Link 48. Não utilizar o kit após o fim da data de validade impressa no exterior da embalagem. Se os reagentes forem conservados sob outras condições que não as especificadas no folheto informativo, estas deverão ser validadas pelo utilizador. Não existem sinais óbvios que indiquem a instabilidade deste produto e, por isso, devem processar-se controlos positivos e negativos em simultâneo com as amostras do doente. 8. Preparação das amostras As amostras devem ser manuseadas de forma a preservar os tecidos para a coloração IHC. Devem ser utilizados para todas as amostras métodos padrão de processamento de tecidos. 8.1 Cortes impregnados em parafina Os tecidos fixados em formol e impregnados em parafina são adequados para utilização. As condições recomendadas de manuseamento e processamento são: < 30 minutos de tempo de isquemia antes da imersão num agente de fixação e horas de tempo de fixação em 10% de formol neutro tamponado. Agentes de fixação alternativos não foram validados e podem originar resultados erróneos. As amostras devem ser bloqueadas numa espessura de 3 mm ou 4 mm, fixadas em 10% de formol neutro tamponado e desidratadas e limpas numa série de álcoois e xilol, seguidas por uma infiltração com parafina derretida. A temperatura da parafina não deve exceder os 60 C. 8.2 Utilização de tecidos descalcificados A utilização do PD-L1 IHC 28-8 pharmdx em tecidos descalcificados não foi validada e não é recomendada. 8.3 Recomendação de conservação de secção cortada As amostras de tecido devem ser cortadas em secções de 4-5 µm. Após o seccionamento, os tecidos devem ser montados em lâminas carregadas Fisherbrand Superfrost Plus ou em lâminas de microscópio Dako FLEX IHC (Referência K8020) e, em seguida, colocadas num forno a 58 ± 2 C durante 1 hora. Para preservar a antigenicidade, os cortes de tecido, depois de montados nas lâminas, devem ser conservados em local escuro a 2-8 C ou a uma temperatura ambiente até 25 C e devem ser corados num prazo de 4 meses após o seccionamento. As condições de conservação e o manuseamento das lâminas não devem exceder os 25 C em qualquer momento posterior à montagem para garantir a integridade e a antigenicidade do tecido. 9. Preparação dos reagentes Antes da coloração devem ser preparados os seguintes reagentes: EnVision FLEX Target Retrieval Solution, Low ph (50x) Prepare uma quantidade suficiente de 1x Target Retrieval Solution, Low ph, diluindo a Target Retrieval Solution, Low ph (50x) 1:50 com água de qualidade reagente; o ph da 1x Target Retrieval Solution tem de ser 6,1 ± 0,2. Um frasco de 30 ml de Target Retrieval Solution, Low ph (50x) com uma diluição de 1:50 produz 1,5 L de 1x reagente, o suficiente para encher um depósito do PT Link para tratar até 24 lâminas por utilização. Eliminar a 1x Target Retrieval Solution após três utilizações e, no máximo, 5 dias após a diluição. Se for necessária mais EnVision FLEX Target Retrieval Solution, Low ph (50x), está disponível com a Referência K8005. EnVision FLEX Wash Buffer (20x) Prepare uma quantidade suficiente de tampão de lavagem, diluindo o tampão de lavagem (20x) 1:20 através da utilização de água de qualidade reagente para os passos de lavagem. Conservar a solução 1x não utilizada a 2-8 ºC durante não mais de um mês. Eliminar o tampão, caso este fique turvo. Consultar mais informações no Manual de Utilizador do seu Autostainer Link 48. O EnVision FLEX Wash Buffer (20x) está disponível com a Referência K8007. DAB+ Substrate-Chromogen Solution Antes de ser utilizada, esta solução deve ser completamente misturada. O desenvolvimento de precipitado na solução não afeta a qualidade da coloração. Para preparar a DAB+ Substrate-Chromogen Solution, adicionar 1 gota de Liquid DAB+ Chromogen por ml de DAB+ Substrate Buffer e misturar. O substrato-cromogénio preparado é estável durante 5 dias se conservado em local escuro a 2-8 C. Notas importantes: Se utilizar um frasco inteiro de DAB+ Substrate Buffer, adicionar 9 gotas de DAB+ Chromogen. Apesar de a etiqueta indicar 7,2 ml, este é o volume utilizável e não tem em conta o "volume morto" no frasco. A cor do Liquid DAB+ Chromogen no frasco pode variar de incolor a castanho-lavanda. Tal não afetará o desempenho deste produto. Diluir de acordo com as orientações acima fornecidas. A adição de Liquid DAB+ Chromogen em excesso ao DAB+ Substrate Buffer resultará na deterioração do sinal positivo. P03914PT_04/SK / p. 5/23
6 10. Procedimento de coloração no Autostainer Link 48 Notas do procedimento Antes da utilização, o utilizador deve ler estas instruções com cuidado e familiarizar-se com todos os componentes e instrumentação (consultar a secção Precauções). Todos os reagentes devem estar à temperatura ambiente (20-25 C) antes da imunocoloração. Do mesmo modo, todas as incubações devem ser realizadas à temperatura ambiente. Durante o procedimento de coloração, não permitir a secagem dos cortes de tecido. Os cortes de tecido secos poderão apresentar um aumento da coloração não específica. Todos os passos necessários e os tempos de incubação para a coloração são pré-programados no software Dako Link. Consultar os Manuais de Utilizador do Autostainer Link 48 e do PT Link para obter informações sobre os protocolos de programação e colocação das lâminas e dos reagentes. Nota: Os reagentes e instruções fornecidos com este sistema foram concebidos para se obter um desempenho ótimo quando utilizados com os reagentes e materiais recomendados. A diluição subsequente dos reagentes ou a alteração dos tempos ou temperaturas de incubação podem originar resultados erróneos ou discordantes. Protocolo de coloração Selecione o protocolo de coloração para o PD-L1 IHC 28-8 pharmdx a partir das opções do menu pendente do DakoLink. Todos os passos necessários e os tempos de incubação para a coloração estão pré-programados no DakoLink. Se os protocolos adequados para o PD-L1 IHC 28-8 pharmdx não estiverem presentes no servidor, contacte o seu representante local do serviço técnico. Passo 1: Procedimento de desparafinação, reidratação e recuperação do alvo (3 em 1) Procedimento recomendado: Para informações detalhadas, consultar o Manual de utilizador do PT Link. Definir Preheat (Pré-aquecimento) e Cool (Frio) do PT Link (Referências PT100/PT101/PT200) para 65 C. Definir Heat (Aquecimento) para 97 C durante 20 minutos. Encher os depósitos do PT Link com 1,5 L por depósito de solução de trabalho Target Retrieval Solution, Low ph, 1x para cobrir os cortes de tecido. Pré-aquecer a Target Retrieval Solution até 65 C. Mergulhar os suportes do Autostainer que contenham cortes de tecido FFPE montados na Target Retrieval Solution, Low ph, (1x solução de trabalho) pré-aquecida no depósito do PT Link. Incubar durante 20 minutos a 97 C. Quando a incubação de recuperação do alvo estiver concluída e a temperatura tiver arrefecido até 65 C, retirar todos os suportes de lâminas Autostainer com as respetivas lâminas do depósito do PT Link e colocar de imediato o suporte do Autostainer com as lâminas num depósito (ex., PT Link Rinse Station, Referência PT109) que contenha Wash Buffer (Referência K8007) diluído à temperatura ambiente. Deixe as lâminas no Wash Buffer, diluído e à temperatura ambiente, durante 5 minutos. Passo 2: Procedimento de coloração Após o procedimento de desparafinação, reidratação e recuperação do alvo (3 em 1), os suportes do Autostainer com as lâminas são colocados no Autostainer Link 48. Certificar-se de que as lâminas permanecem humedecidas com tampão durante a colocação no aparelho e antes de iniciar o processo. O instrumento realiza o procedimento de coloração aplicando o reagente apropriado, monitorizando o tempo de incubação e lavando as lâminas entre a colocação dos reagentes. Os tempos do reagente são préprogramados no software Dako Link. Passo 3: Contraste O contraste deve ser aplicado às lâminas durante 7 minutos com EnVision FLEX Hematoxylin (Link) (Referência K8008). O tempo de incubação da hematoxilina está pré-programado no protocolo. Passo 4: Montagem É necessário um meio de montagem permanente não aquoso. Nota: Ao longo do tempo, poderá ocorrer algum esbatimento das lâminas coradas mediante diversos fatores, incluindo, entre outros, contrastação, materiais e métodos de montagem e condições de conservação das lâminas. Para minimizar o esbatimento, conservar as lâminas num local escuro e à temperatura ambiente (20-25 C). 11. Controlo de qualidade O controlo de qualidade dos reagentes do PD-L1 IHC 28-8 pharmdx foi realizado por intermédio de imuno-histoquímica, utilizando os procedimentos de recuperação do alvo e coloração definidos anteriormente. Quaisquer desvios dos procedimentos recomendados para a fixação de tecidos, processamento e impregnação no laboratório do utilizador podem produzir uma variabilidade significativa nos resultados. Em cada processo de coloração, devem ser incluídos controlos de qualidade. Estes controlos de qualidade são especificados na tabela 5 e incluem: uma amostra de tecido do doente corada com H&E; tecidos de controlo positivo e negativo fornecidos pelo laboratório; e uma lâmina de controlo (15) fornecida pela Dako. Nos Estados Unidos, consultar as diretrizes de controlo de qualidade do College of American Pathologists (CAP) Certification Program for Immunohistochemistry; e consultar também CLSI Quality Assurance for Immunocytochemistry, Approved Guideline (14) para obter mais informação. 12. Verificação do ensaio Antes da utilização inicial de um sistema de coloração num procedimento de diagnóstico, o utilizador deve verificar o desempenho do ensaio, testando-o numa série de tecidos fornecidos pelo laboratório com características de desempenho IHC conhecidas, representando tecidos positivos e negativos conhecidos. Consultar os procedimentos de controlo de qualidade indicados previamente nesta secção do folheto informativo do produto. Estes procedimentos de controlo de qualidade devem ser repetidos para cada novo kit ou sempre que houver alterações nos parâmetros do ensaio. As opções de resolução de problemas para potenciais problemas, as suas causas e ações de correção sugeridas são indicadas na Tabela 22. P03914PT_04/SK / p. 6/23
7 13. Interpretação da coloração A avaliação da lâmina deve ser efetuada por um patologista, utilizando um microscópio ótico. Para a avaliação da coloração e classificação imuno-histoquímica da PD-L1, pode ser utilizada uma ampliação de objetiva de 4x para a avaliação inicial de toda a amostra, seguida por objetivas de 10-20x para a classificação (pode ser utilizada uma de 40x para confirmação, se necessário). A coloração da PD-L1 é indicada com um produto de reação castanho (3,3 -diaminobenzidina, DAB). A coloração positiva para PD-L1 é definida como uma coloração da membrana de plasma circunferencial completa e/ou linear parcial de células tumorais em qualquer intensidade. É necessário avaliar toda a amostra. Todas as células tumorais viáveis em toda a lâmina do doente corada com PD-L1 devem ser avaliadas e incluídas na avaliação dos resultados da PD-L1. Pelo menos 100 células tumorais viáveis devem estar presentes na lâmina do doente corada com PD-L1 para determinar a percentagem de células coradas. Consultar as secções de interpretação da coloração específicas neste documento para obter informações detalhadas sobre as diretrizes. A coloração citoplasmática, caso esteja presente, não é considerada para efeitos de classificação. Células não malignas e células imunes (como por ex., linfócitos infiltrantes ou macrófagos) podem também ser coradas com a PD-L1; no entanto, estas não devem ser incluídas na classificação para a determinação da positividade da PD-L1. Em cada processo de coloração, as lâminas devem ser examinadas na ordem apresentada na Tabela 5, para se determinar a validade do processo de coloração e permitir a avaliação da coloração da amostra de tecido. Para obter orientação adicional relacionada com a classificação da PD-L1, consultar as indicações das tabelas de interpretação da coloração específicas neste documento e o manual de interpretação relevante de PD-L1 IHC 28-8 pharmdx para cada indicação Interpretação da coloração: NSCLC não escamoso É necessário avaliar toda a amostra. Todas as células tumorais viáveis em toda a lâmina do doente corada com PD-L1 devem ser avaliadas e incluídas na avaliação dos resultados da PD-L1. Pelo menos 100 células tumorais viáveis devem estar presentes na lâmina do doente corada com PD-L1 para determinar a percentagem de células coradas. Para amostras de NSCLC não escamoso, registar a percentagem de células tumorais viáveis que apresentam coloração da PD-L1 da membrana de plasma circunferencial e/ou linear parcial em qualquer intensidade. Tabela 1: Interpretação da coloração: NSCLC não escamoso Indicação Mínimo de células tumorais viáveis necessário para classificação Células não malignas e células imunes Coloração citoplasmática, células necróticas, estromais e detritos celulares Outros elementos NSCLC não escamoso 100 Não incluídas na classificação Não considerados para efeitos de classificação NA 13.2 Interpretação da coloração: Carcinoma das células escamosas da cabeça e pescoço (SCCHN) Este ensaio foi validado para amostras de tecido com SCCHN invasivo e não para lesões com focos de displasia ou carcinoma in situ. As lâminas coradas com H&E devem ser processadas simultaneamente com cada amostra corada com PD-L1 para permitir a avaliação adequada de carcinoma invasivo, carcinoma in situ e epitélio normal adjacente. É necessário avaliar toda a amostra. Todas as células tumorais viáveis em toda a lâmina do doente corada com PD-L1 devem ser incluídas na avaliação dos resultados da PD-L1. Pelo menos 100 células tumorais viáveis devem estar presentes na lâmina do doente corada com PD-L1 para determinar a percentagem de células coradas. Para amostras de SCCHN, registar a percentagem de células tumorais viáveis que apresentam coloração da PD-L1 da membrana de plasma circunferencial e/ou linear parcial em qualquer intensidade. Tabela 2: Interpretação da coloração: SCCHN Mínimo de células Indicação tumorais viáveis necessário para classificação SCCHN 100 Células não malignas e células imunes Não incluídas na classificação Coloração citoplasmática, células necróticas, estromais e detritos celulares Não considerados para efeitos de classificação Outros elementos As células com focos de displasia e carcinoma in situ são excluídas da classificação. As lâminas com H&E correspondentes permitem a avaliação adequada de carcinoma invasivo, carcinoma in situ e epitélio normal adjacente Interpretação da coloração: Carcinoma urotelial Este ensaio foi validado para amostras de tecido com UC invasivo e não para lesões com focos de displasia ou carcinoma in situ. As lâminas coradas com H&E devem ser processadas simultaneamente com cada amostra corada com PD-L1 para permitir a avaliação adequada de carcinoma invasivo, carcinoma in situ e epitélio normal adjacente. É necessário avaliar toda a amostra. Todas as células tumorais viáveis em toda a lâmina do doente corada com PD-L1 devem ser incluídas na avaliação dos resultados da PD-L1. Pelo menos 100 células tumorais viáveis devem estar presentes na lâmina do doente corada com PD-L1 para determinar a percentagem de células coradas. Para amostras de UC, registar a percentagem de células tumorais viáveis que apresentam coloração da PD-L1 da membrana de plasma circunferencial e/ou linear parcial em qualquer intensidade. P03914PT_04/SK / p. 7/23
8 Tabela 3: Interpretação da coloração: UC Mínimo de células Indicação tumorais viáveis necessário para classificação UC 100 Células não malignas e células imunes Não incluídas na classificação Coloração citoplasmática, células necróticas, estromais e detritos celulares Não considerados para efeitos de classificação Outros elementos As células com focos de displasia e carcinoma in situ são excluídas da classificação. As lâminas com H&E correspondentes permitem a avaliação adequada de carcinoma invasivo, carcinoma in situ e epitélio normal adjacente Interpretação da coloração: Melanoma É necessário avaliar toda a amostra. Todas as células tumorais viáveis em toda a lâmina do doente corada com PD-L1 devem ser avaliadas e incluídas na avaliação dos resultados da PD-L1. Pelo menos 100 células tumorais viáveis devem estar presentes na lâmina do doente corada com PD-L1 para determinar a percentagem de células coradas. As amostras são consideradas positivas à PD-L1 caso 1% das células de melanoma apresente coloração da PD-L1 da membrana de plasma circunferencial e/ou linear parcial de células tumorais em qualquer intensidade. As amostras são consideradas negativas à PD-L1 caso < 1% das células de melanoma apresente coloração da PD-L1 da membrana de plasma circunferencial e/ou linear parcial de células tumorais em qualquer intensidade. NOTA: Ao interpretar as amostras de melanoma do doente, pode estar presente uma pigmentação castanha de melanina. A melanina deve ser excluída ao classificar a coloração da membrana plasmática; a comparação com uma lâmina corada sequencial com NCR pode ser útil para a identificação e exclusão do conteúdo de melanina. Se a melanina com níveis altamente elevados impedir a classificação da coloração da membrana plasmática de células tumorais, a amostra pode ser excluída da interpretação e considerada indeterminada. Tabela 4: Interpretação da coloração: Melanoma Mínimo de células Indicação tumorais viáveis necessário para classificação Melanoma 100 Células não malignas e células imunes Não incluídas na classificação Coloração citoplasmática, células necróticas, estromais e detritos celulares Não considerados para efeitos de classificação Outros elementos A melanina deve ser excluída durante a classificação da coloração da membrana de plasma. A comparação com uma lâmina corada sequencial com NCR pode ser útil para a identificação e exclusão do conteúdo de melanina. 14. Avaliação das lâminas Tabela 5: Ordem recomendada de avaliação das lâminas Amostras Racional Requisitos 1. H&E (Fornecidas pelo laboratório) Uma coloração da amostra de tecido com hematoxilina e eosina (H&E) é avaliada em primeiro lugar para avaliar a histologia do tecido e a qualidade da preservação. O PD-L1 IHC 28-8 pharmdx e a coloração H&E devem ser realizados em cortes em série do mesmo bloco de parafina da amostra. As amostras de tecido devem estar intactas, bem preservadas e devem confirmar a indicação de tumor. P03914PT_04/SK / p. 8/23
9 2. Lâmina de controlo (Fornecida pela Dako) 3. Positive Control Tissue Slides (Fornecidas pelo laboratório) 4. Negative Control Tissue Slides (Fornecidas pelo laboratório) A lâmina de controlo corada com o anticorpo primário da PD-L1 do PD-L1 IHC 28-8 pharmdx deve ser examinada para determinar se todos os reagentes estão a funcionar devidamente. A Control Slide contém o aglomerado da linha celular positiva a PD-L1 e o aglomerado da linha celular negativa a PD-L1. As Positive Control Tissue Slides coradas com o anticorpo primário da PD-L1 e com o Negative Control Reagent devem ser examinadas em seguida. Estas lâminas verificam se o método de fixação e o processo de recuperação do alvo são eficazes. Os controlos de tecidos positivos conhecidos devem ser utilizados apenas para monitorização do desempenho correto dos tecidos processados e dos reagentes de teste, NÃO para auxiliar na formulação de um diagnóstico específico das amostras dos doentes. As Negative Control Tissue Slides (conhecidas como sendo negativas para a PD-L1) coradas com o anticorpo primário da PD- L1 e com o Negative Control Reagent devem ser examinadas a seguir para verificar a especificidade da marcação do antigénio alvo pelo anticorpo primário. Em alternativa, as porções negativas do tecido de controlo positivo podem servir como tecido de controlo negativo, mas tal deverá ser validado pelo utilizador. Em cada procedimento de coloração, deve ser corada uma Control Slide com o anticorpo primário contra a PD-L1. Critérios de aceitação da NCI-H226 (linha celular de controlo positiva à PD-L1 proveniente de carcinoma das células escamosas do pulmão humano com expressão da proteína PD-L1 positiva): Coloração da membrana de plasma de 80% das células a 2+ da intensidade de coloração média. Intensidade de coloração não específica < 1+. Critérios de aceitação da MCF-7 (linha celular de controlo negativa à PD-L1 proveniente de adenocarcinoma da mama humano com expressão da proteína PD-L1 negativa): Sem coloração específica. Intensidade de coloração não específica < 1+. De notar que pode ser ocasionalmente observada a coloração de algumas células nos aglomerados de células de MCF-7. São aplicáveis os seguintes critérios de aceitação: a presença de 10 células totais com coloração distinta da membrana de plasma ou a coloração citoplasmática com 1+ de intensidade dentro dos limites do aglomerado de células de MCF-7 são aceitáveis. Se os resultados das linhas celulares de controlo não corresponderem a estes critérios, todos os resultados obtidos com as amostras do doente deverão ser considerados inválidos. Os controlos devem consistir em amostras de biopsia/cirúrgicas da mesma indicação de tumor da amostra do doente, fixadas, processadas e impregnadas logo que possível, da mesma forma que a(s) amostra(s) do doente. Utilizar amostras intactas para a interpretação dos resultados de coloração, já que as células necróticas ou degeneradas apresentam, normalmente, uma coloração não específica. Os tecidos selecionados para utilização como controlos de tecido positivo devem demonstrar uma coloração positiva fraca a moderada, quando corados com PD-L1, para ajudar na deteção de alterações subtis na sensibilidade do ensaio. Em cada processo de coloração, devem ser incluídas duas lâminas de controlo de tecido positivo. Lâmina corada com PD-L1: Deve ser observada presença de coloração castanha na membrana de plasma. A coloração não específica deve ser 1+. Lâmina corada com Negative Control Reagent: Sem coloração da membrana. A coloração não específica deve ser 1+. Caso os controlos de tecidos positivos não demonstrem uma coloração positiva apropriada, devem considerar-se inválidos os resultados obtidos com as amostras de teste. Os controlos devem consistir em amostras de biopsia/cirúrgicas da mesma indicação de tumor da amostra do doente, fixadas, processadas e impregnadas logo que possível, da mesma forma que a(s) amostra(s) do doente. Em cada processo de coloração, devem ser incluídas duas lâminas de controlo de tecido negativo. Lâmina corada com PD-L1: Sem coloração da membrana em células tumorais. A coloração não específica deve ser 1+. Lâmina corada com Negative Control Reagent: Sem coloração da membrana. A coloração não específica deve ser 1+. Caso ocorra coloração específica da membrana de plasma nas Negative Control Tissue Slides, os resultados obtidos com a amostra do doente devem ser considerados inválidos. P03914PT_04/SK / p. 9/23
10 5. Lâmina do tecido do doente corado com Negative Control Reagent 6. Lâmina do tecido do doente corado com o anticorpo primário da PD-L1 15. Limitações Examinar amostras de doentes coradas com o Negative Control Reagent do PD-L1 IHC 28-8 pharmdx. O reagente de controlo negativo é utilizado em vez do anticorpo primário e auxilia na interpretação da coloração específica do local do antigénio. Examinar por último toda a lâmina das amostras do doente coradas com o anticorpo primário da PD- L1 do PD-L1 IHC 28-8 pharmdx. Consultar as secções Resumo e explicação, Limitações e Avaliação do desempenho não clínico para obter informação específica sobre a imunorreatividade do PD-L1 IHC 28-8 pharmdx. A ausência da coloração da membrana de plasma verifica a marcação específica do antigénio alvo pelo anticorpo primário da PD-L1. A coloração não específica deve ser 1+. A intensidade da coloração positiva deve ser avaliada no contexto de qualquer coloração de fundo não específica observada na lâmina do Negative Control Reagent no mesmo processamento. À semelhança do que acontece com qualquer teste de imuno-histoquímica, um resultado negativo significa que o antigénio não foi detetado e não necessariamente que este estava ausente nas células/tecido analisado. Para obter as diretrizes sobre a interpretação da coloração, consultar a secção Limitações gerais 1. A imuno-histoquímica é um processo de diagnóstico com várias etapas que requer uma formação especializada na seleção dos reagentes apropriados; seleções de tecidos, fixação e processamento; preparação da lâmina de imuno-histoquímica e interpretação dos resultados da coloração. 2. A coloração de tecidos depende do manuseamento e processamento dos tecidos antes da coloração. A fixação, congelação, descongelação, lavagem, secagem, aquecimento e seccionamento incorretos ou a contaminação com outros tecidos ou fluidos poderá produzir artefactos, aprisionamento de anticorpos ou resultados falsos negativos. Os resultados inconsistentes podem dever-se a variações nos métodos de fixação e impregnação ou a irregularidades inerentes aos tecidos. 3. Uma contrastação excessiva ou incompleta poderá comprometer a interpretação adequada dos resultados. 4. A interpretação clínica de qualquer coloração positiva ou a sua ausência deve ser avaliada no contexto da apresentação clínica, morfologia e outros critérios histopatológicos. A interpretação clínica de qualquer coloração positiva ou a sua ausência deve ser complementada com estudos morfológicos e controlos adequados, bem como outros testes de diagnóstico. A interpretação da lâmina corada é da responsabilidade de um patologista qualificado que esteja familiarizado com os anticorpos, reagentes e métodos utilizados. A coloração deve ser efetuada por um laboratório licenciado certificado sob a supervisão de um patologista responsável pelo exame das lâminas coradas e garantia da adequação dos controlos positivos e negativos. 5. Os tecidos de pessoas infetadas pelo vírus da hepatite B que contenham o antigénio de superfície da hepatite B (HBsAg) podem exibir coloração não específica com a peroxidase (17). 6. A possibilidade de reações inesperadas em tipos de tecidos testados não pode ser completamente eliminada devido à variabilidade biológica da expressão de antígenos em neoplasmas ou noutros tecidos patológicos. Contactar a Assistência técnica Dako com reações inesperadas devidamente documentadas. 7. Podem observar-se resultados falsos positivos devido à ligação não imunológica de proteínas ou a produtos de reação do substrato. Poderão ser também causados pela atividade da pseudoperoxidase (eritrócitos) e pela atividade da peroxidase endógena (citocromo C) (14). 8. Os reagentes e instruções fornecidos neste sistema foram concebidos para se obter um desempenho ótimo. A diluição subsequente dos reagentes ou a alteração dos tempos ou temperaturas de incubação podem originar resultados erróneos ou discordantes Limitações específicas do produto 1. Os resultados falsos negativos poderão ser causados pela degradação do antigénio presente nos tecidos ao longo do tempo. Depois de montados nas lâminas, os cortes de tecido devem ser conservados em local escuro a 2-8 C ou a uma temperatura ambiente até 25 C e devem ser corados num prazo de 4 meses após o seccionamento. As condições de conservação e o manuseamento das lâminas não devem exceder os 25 C em qualquer momento posterior à montagem para garantir a integridade e a antigenicidade do tecido. 2. Para resultados ótimos e reprodutíveis, a proteína PD-L1 requer o pré-tratamento da recuperação do alvo quando os tecidos forem rotineiramente fixados (formol neutro tamponado) e impregnados em parafina. 3. Não substituir por reagentes de outros números de lote deste produto ou de kits de outros fabricantes. A única exceção é a EnVision FLEX Target Retrieval Solution, Low ph (50x), que, se necessário, está disponível com a Referência K As linhas celulares de controlo coradas apenas devem ser utilizadas para validação do processo de coloração e não para classificar a reação da coloração nos cortes de tecido. 5. A utilização do PD-L1 IHC 28-8 pharmdx em tecidos com agentes de fixação que não possuam 10% de formol neutro tamponado não foi validada. 6. As biopsias com agulha excisionais, incisionais, de punção ou internas foram consideradas tipos de amostras aceitáveis para os testes clínicos que utilizavam o PD-L1 IHC 28-8 pharmdx. Aspirações com agulha fina ou outras amostras citológicas eram insuficientes para análises de biomarcadores e foram excluídas dos testes clínicos que utilizavam o PD-L1 IHC 28-8 pharmdx. 16. Avaliação do desempenho não clínico 16.1 Especificidade analítica para o PD-L1 IHC 28-8 pharmdx O anticorpo primário para o PD-L1 IHC 28-8 pharmdx é um anticorpo monoclonal de coelho anti PD-L1 humana, clone O imunogénio utilizado para a geração de anticorpos é uma PD-L1 humana recombinante purificada, contendo o domínio extracelular (Phe19-Thr239) da PD-L1 humana. A coloração por IHC com o anticorpo primário da PD-L1 não mostrou qualquer reatividade cruzada para a PD-L2 expressa exogenamente em células de ovário de hamster chinês (CHO). O PD-L1 IHC 28-8 pharmdx deteta especificamente a proteína de membrana PD-L1 expressa em células tumorais em tecidos FFPE que podem ser completamente abolidas através da adição do antigénio da PD-L1. O PD-L1 IHC 28-8 pharmdx não deteta a proteína de membrana PD-L1 em células tumorais com a PD-L1 inativada quando o gene PD-L1 está geneticamente eliminado. P03914PT_04/SK / p. 10/23
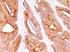
11 16.2 Tecidos normais e neoplásicos A tabela 6 resume a imunorreatividade do anticorpo Monoclonal Rabbit Anti-Human PD-L1 no painel recomendado de tecidos normais. A tabela 7 resume a imunorreatividade do anticorpo Monoclonal Rabbit Anti-Human PD-L1 em tecidos neoplásicos em micro-matrizes de tecido multitumoral. Todos os tecidos foram fixados com formol e impregnados em parafina e corados com PD-L1 IHC 28-8 pharmdx, de acordo com as instruções no folheto informativo. O PD-L1 IHC 28-8 pharmdx detetou a proteína PD-L1 localizada na membrana de plasma de tipos de células conhecidos por expressar o antígeno da PD-L1, como as células imunes e células de origem epitelial, sobretudo, células tumorais. Tabela 6: Resumo da reatividade do PD-L1 IHC 28-8 pharmdx em tecido normal Tipo de tecido (n.º testados) Coloração de membrana de plasma positiva: Elementos de tecido Coloração citoplasmática positiva: Elementos de tecido Amígdalas (3) 3/3 Epitélio da cripta 0/3 3/3 Centro germinativo (células imunes) Baço (3) 1/3 Macrófagos 0/3 3/3 Célula litorânea Células mesoteliais (3) 0/3 0/3 Cerebelo (3) 0/3 0/3 Cérebro (3) 0/3 0/3 Colo do útero (3) 1/3 Epitélio 1/3 Epitélio Cólon (3) 2/3 Macrófagos 0/3 Esófago (3) 0/3 0/3 Estômago (3) 0/3 0/3 Fígado (3) 2/3 Células imunes 2/3 Células imunes Glândula salivar (3) 0/3 0/3 Intestino delgado (2) 0/2 0/2 Mama (3) 0/3 0/3 Medula óssea (3) 3/3 Megacariócitos 3/3 Megacariócitos Músculo, cardíaco (3) 0/2 0/2 Músculo, esquelético (3) 0/2 0/2 Nervos, periféricos (3) 0/3 0/3 Ovário (3) 0/3 0/3 Pâncreas (3) 3/3 Epitélio (sobretudo células dos ilhéus) 3/3 Epitélio (sobretudo células dos ilhéus) Paratiroide (3) 3/3 Epitélio 0/3 Pele (3) 0/3 1/3 Epitélio Pituitária (3) 1/3 Adeno-hipófise anterior 1/3 Adeno-hipófise anterior 3/3 Neuro-hipófise posterior Próstata (2) 0/2 0/2 Pulmão (3) 3/3 Macrófagos alveolares 0/3 Rim (3) 3/3 Epitélio tubular 3/3 Epitélio tubular Suprarrenal (3) 3/3 Células medulares 3/3 Células medulares Testículos (3) 0/3 1/3 Células de Leydig Timo (3) 3/3 Epitélio medular 0/3 Tiroide (3) 0/3 0/3 Útero (3) 0/3 0/3 Tabela 7: Resumo da reatividade do PD-L1 IHC 28-8 pharmdx em tecidos neoplásicos Tipo de tumor Local/Órgão Positivo à PD-L1/total (N=162) Apêndice 1/1 Cabeça e pescoço, palato duro 0/1 Carcinoma bronco-alveolar, pulmão 0/1 Colo do útero, tipo endocervical 0/1 Cólon 2/5 Cólon, metastático para o fígado 1/1 Cólon, mucinoso 0/1 Esófago 1/1 Estômago 1/6 Estômago, mucinoso 0/1 Glândula salivar/parótida 0/2 Adenocarcinoma Intestino delgado 0/2 Mama, DCIS 0/2 Mama, ductal invasivo 3/7 Mama, metastático ductal invasivo para nódulo linfático 1/1 Ovário 0/1 Ovário, endometrioide 0/1 Ovário, mucinoso 0/1 Ovário, seroso 0/1 Pâncreas 1/2 Pâncreas, ductal 0/3 Próstata 2/4 Pulmão 2/5 Reto 2/4 P03914PT_04/SK / p. 11/23
12 Tipo de tumor Local/Órgão Positivo à PD-L1/total (N=162) Tiroide, folicular 0/1 Tiroide, folicular-papilar 0/1 Tiroide, papilar 0/3 Útero, célula clara 1/1 Útero, endométrio 1/3 Vesícula biliar 2/4 Vesícula biliar, metastático para o pulmão 0/1 Astrocitoma Cérebro 0/3 Carcinoma Nasofaríngeo, NPC 0/1 Carcinoma adrenocortical Suprarrenal 0/1 Carcinoma das células de transição Bexiga 3/6 Rim 0/1 Carcinoma das células em anel de sinete Carcinoma das células escamosas Carcinoma das células em anel de sinete metastático para o ovário 0/1 Cólon 0/1 Cabeça e pescoço 0/2 Carcinoma das células escamosas esofágicas metastático para o nódulo linfático Colo do útero 2/4 Esófago 4/7 Pele 1/2 Pulmão 1/3 Útero 1/1 Carcinoma das células renais Célula clara Rim 0/6 Papilar Rim 0/1 Carcinoma de célula basal Pele 0/1 Carcinoma de célula pequena Pulmão 1/2 Carcinoma de células grandes Pulmão 1/1 Carcinoma embrionário Testículos 0/1 Carcinoma hepatocelular Fígado 1/5 Carcinoma medular Tiroide 0/1 Cordoma Cavidade pélvica 0/1 Ependimoma Encéfalo 0/1 Espermatocitoma Testículos 0/2 Glioblastoma Encéfalo 0/1 Hepatoblastoma Fígado 0/1 Cólon 0/1 Intersticialoma Intestino delgado 0/1 Reto 0/1 Linfoma Célula B difusa Nódulo linfático 2/4 Célula grande anaplásica Nódulo linfático 1/1 Hodgkin Nódulo linfático 2/2 Não-Hodgkin Nódulo linfático 1/1 Lipossarcoma Cavidade abdominal, mucinoso 0/1 Meduloblastoma Encéfalo 0/1 Melanoma Cavidade nasal 0/1 Reto 0/1 Meningioma Encéfalo 0/2 Mesotelioma Peritoneu 0/1 Neuroblastoma Retroperitoneu 0/1 Neuroectodérmico primitivo Retroperitoneu 0/1 Neurofibroma Tecido mole, região lombar 0/1 Sarcoma Célula clara Parede abdominal 0/1 Condrossarcoma Osso 0/1 Bexiga 0/1 Leiomiossarcoma Tecido mole, parede torácica 0/1 Lipossarcoma Cavidade abdominal, mucinoso 0/1 Osteossarcoma Osso 0/2 Próstata 0/1 Rabdomiossarcoma Retroperitoneu 0/1 Tecido mole, embrionário 0/1 Sarcoma sinovial Cavidade pélvica 0/1 Seminoma Testículos 0/2 Timoma Mediastino 1/1 Tumor das células dos ilhéus Pâncreas 0/1 1/1 P03914PT_04/SK / p. 12/23
13 17. Avaliação do desempenho 17.1 Avaliação do desempenho: NSCLC não escamoso Sensibilidade analítica: NSCLC não escamoso A sensibilidade analítica do PD-L1 IHC 28-8 pharmdx foi testada em 112 casos únicos de amostras FFPE de carcinoma do pulmão de células não escamosas (NSCLC) de estádio I a IV, utilizando um lote de produção fabricado. A avaliação da expressão da PD-L1 demonstrou coloração num intervalo de células tumorais positivas de 0-100% e de intensidade de coloração de Repetibilidade/Reprodutibilidade externa: NSCLC não escamoso A repetibilidade e a reprodutibilidade externa do PD-L1 IHC 28-8 pharmdx foram avaliadas na Dako e em três locais de teste externos, respetivamente. Os dados de desempenho são fornecidos na Tabela 8 e na Tabela 9. A percentagem de concordância negativa (NPA), a percentagem de concordância positiva (PPA) e a percentagem de concordância global (OA) de uma comparação por pares independente dos testes foram determinadas para cada nível da expressão da PD-L1 avaliado. A observação que ocorreu com mais frequência foi aplicada como uma referência para calcular a NPA, a PPA e a OA, assim como os correspondentes intervalos de confiança de 95% da classificação de Wilson; portanto, um dos resultados com esta observação foi excluído das comparações por pares. Tabela 8: Repetibilidade do PD-L1 IHC 28-8 pharmdx - NSCLC não escamoso Repetibilidade Método 1% de nível de expressão Entre equipamentos Entre analistas Entre dias Entre lotes Entre processamentos Cada uma das 10 amostras de NSCLC não escamoso com um intervalo de expressão da PD-L1 por IHC foi testada com três réplicas em cada um dos três equipamentos Autostainer Link 48. Foram realizadas, no total, 60 comparações por pares independentes. Cada uma das 12 amostras de NSCLC não escamoso com um intervalo de expressão da PD-L1 por IHC foi testada com três réplicas por três analistas num equipamento Autostainer Link 48. Foram realizadas, no total, 72 comparações por pares independentes. Cada uma das 10 amostras de NSCLC não escamoso com um intervalo de expressão da PD-L1 por IHC foi testada com três réplicas ao longo de cinco dias não consecutivos no equipamento Autostainer Link 48. Foram realizadas, no total, 80 comparações por pares independentes. Cada uma das 20 amostras de NSCLC não escamoso com um intervalo de expressão da PD-L1 por IHC foi testada com duas réplicas com cada um dos cinco lotes de reagentes no equipamento Autostainer Link 48. Foram realizadas, no total, 160 comparações por pares independentes. Cada uma das 10 amostras de NSCLC não escamoso com um intervalo de expressão da PD-L1 por IHC foi testada com oito réplicas num processamento no equipamento Autostainer Link 48. Foram realizadas, no total, 70 comparações por pares independentes. NPA 100 (82,4, 100) PPA 100 (91,6, 100) OA 100 (94,0, 100) NPA 100 (86,2, 100) PPA 100 (92,6, 100) OA 100 (94,9, 100) NPA 100 (86,2, 100) PPA 100 (93,6, 100) OA 100 (95,4, 100) NPA 100 (94,3, 100) PPA 100 (96,2, 100) OA 100 (97,7, 100) NPA 100 (84,5, 100) PPA 100 (92,7, 100) OA 100 (94,8, 100) % de concordância (95% CI) 5% de nível de expressão NPA 100 (86,2, 100) PPA 100 (90,4, 100) OA 100 (94,0, 100) NPA 100 (91,6, 100) PPA 100 (88,6, 100) OA 100 (94,9, 100) NPA 100 (89,3, 100) PPA 100 (92,6, 100) OA 100 (95,4, 100) NPA 100 (95,4, 100) PPA 100 (95,4, 100) OA 100 (97,7, 100) NPA 100 (87,9, 100) PPA 100 (91,6, 100) OA 100 (94,8, 100) 10% de nível de expressão NPA 100 (91,6, 100) PPA 100 (82,4, 100) OA 100 (94,0, 100) NPA 100 (93,4, 100) PPA 100 (82,4, 100) OA 100 (94,9, 100) NPA 98,2 (90,6, 99,7) PPA 100 (86,2, 100) OA 98,8 (93,3, 99,8) NPA 100 (96,4, 100) PPA 100 (93,6, 100) OA 100 (97,7, 100) NPA 100 (92,7, 100) PPA 100 (84,5, 100) OA 100 (94,8, 100) P03914PT_04/SK / p. 13/23
14 Tabela 9: Reprodutibilidade do PD-L1 IHC 28-8 pharmdx - NSCLC não escamoso testado em três locais externos Reprodutibilidade Ensaio entre locais (três locais) Ensaio entre locais Intraobservador (um observador em cada um dos três locais) Intraobservador (um observador em cada um dos três locais) Método Cada uma das 10 amostras de NSCLC não escamoso com um intervalo de expressão da PD-L1 por IHC foi testada em cinco dias não consecutivos. A análise entre locais foi realizada entre três locais num total de 140 comparações por pares independentes. Cada uma das 10 amostras de NSCLC não escamoso com um intervalo de expressão da PD-L1 por IHC foi testada em cinco dias não consecutivos em cada um dos três locais de estudo. A análise intralocal foi realizada para três locais num total de 120 comparações por pares independentes. A classificação de 15 amostras de NSCLC não escamoso com um intervalo de expressão da PD-L1 por IHC, coradas com PD-L1 IHC 28-8 pharmdx, foi realizada por três patologistas, um em cada dos três locais do estudo, em três dias não consecutivos. A análise entre observadores foi realizada entre três locais num total de 120 comparações por pares independentes. A classificação de 15 amostras de NSCLC não escamoso com um intervalo de expressão da PD-L1 por IHC, coradas com PD-L1 IHC 28-8 pharmdx, foi realizada por três patologistas, um em cada dos três locais do estudo, em três dias não consecutivos. A análise intra-observador foi realizada para três locais num total de 90 comparações por pares independentes. % de concordância (95% CI) 1% de nível de expressão 5% de nível de expressão NPA 100 (93,6, 100) PPA 98,8 (93,6, 99,8) OA 99,3 (96,1, 99,9) NPA 100 (92,6, 100) PPA 98,6 (92,5, 99,8) OA 99,2 (95,4, 99,9) NPA 96,9 (89,3, 99,1) PPA 100 (93,6, 100) OA 98,3 (94,1, 99,5) NPA 95,8 (86,0, 98,8) PPA 100 (91,6, 100) OA 97,8 (92,3, 99,4) NPA 91,4 (82,5, 96,0) PPA 97,1 (90,2, 99,2) OA 94,3 (89,1, 97,1) NPA 96,4 (87,9, 99,0) PPA 95,3 (87,1, 98,4) OA 95,8 (90,6, 98,2) NPA 100 (94,3, 100) PPA 89,3 (78,5, 95,0) OA 95,0 (89,5, 97,7) NPA 100 (93,1, 100) PPA 100 (90,8, 100) OA 100 (95,9, 100) Avaliação do desempenho clínico: NSCLC não escamoso A utilidade clínica do PD-L1 IHC 28-8 pharmdx foi avaliada no CA209057, um estudo de fase 3, aleatorizado e sem dupla ocultação do nivolumab em comparação com docetaxel em indivíduos adultos ( 18 anos) com NSCLC de células não escamosas, avançado ou metastático, após falha do tratamento anterior de quimioterapia dupla baseada em platina. No total, 582 indivíduos foram aleatorizados em 112 locais em 22 países (Argentina, Austrália, Áustria, Brasil, Canadá, Chile, República Checa, França, Alemanha, Hong Kong, Hungria, Itália, México, Noruega, Peru, Polónia, Roménia, Federação Russa, Singapura, Espanha, Suíça e Estados Unidos). Os indivíduos foram aleatorizados 1:1 e estratificados de acordo com 1) a utilização anterior de terapia de manutenção vs. a não utilização de terapia de manutenção e 2) terapia de segunda vs. terceira linha. Amostras de tecido tumoral anteriores ao estudo (referência) foram recolhidas antes da aleatorização e antes do primeiro tratamento, para realizar análises pré-planeadas da eficácia, de acordo com níveis da expressão da PD-L1 predefinidos (objetivo secundário). O parâmetro de avaliação final primário era a sobrevivência global (OS). Outros parâmetros de avaliação final secundários consistiam na taxa de resposta objetiva (ORR), na sobrevivência sem progressão (PFS) e na melhoria dos sintomas relacionados com a doença ao fim de 12 semanas, medidos pela Lung Cancer Symptom Scale (LCSS). As características de referência em termos de população e doença foram normalmente equilibradas entre indivíduos aleatorizados nos grupos de nivolumab e docetaxel. A idade média era de 62 anos (intervalo: 21 a 85) com 34% com 65 anos e 7% com 75 anos. A maioria dos doentes era caucasiana (92%) e do sexo masculino (55%); o estado de desempenho ECOG de referência era 0 (31%) ou 1 (69%). Setenta e nove por cento dos doentes tinham sido/eram ainda fumadores. Foram recolhidas amostras tumorais de tumores NSCLC não escamosos, de acordo com os requisitos de inclusão do estudo. As frequências da expressão da PD-L1 em cada um dos níveis de expressão de referência predefinidos em todos os indivíduos aleatorizados no CA são apresentadas na tabela 10. Tabela 10: Frequência da expressão da PD-L1 anterior ao estudo em todos os indivíduos aleatorizados com NSCLC não escamoso - CA Categoria de expressão da PD-L1 da população Nivolumab 3 mg/kg Docetaxel Total Geral PD-L1 quantificável na referência, N (%) 231 (79,1) 224 (77,2) 455 (78,2) Expressão de referência da PD-L1 1% 123/231 (53,2) 123/224 (54,9) 246/455 (54,1) Expressão de referência da PD-L1 < 1% 108/231 (46,8) 101/224 (45,1) 209/455 (45,9) Expressão de referência da PD-L1 5% 95/231 (41,1) 86/224 (38,4) 181/455 (39,8) Expressão de referência da PD-L1 < 5% 136/231 (58,9) 138/224 (61,6) 274/455 (60,2) Expressão de referência da PD-L1 10% 86/231 (37,2) 79/224 (35,3) 165/455 (36,3) Expressão de referência da PD-L1 < 10% 145/231 (62,8) 145/224 (64,7) 290/455 (63,7) PD-L1 não quantificável, N (%) 61 (20,9) 66 (22,8) 127 (21,8) Os doentes com expressão da PD-L1 em todos os níveis de expressão predefinidos no grupo do OPDIVO foram associados a uma maior sobrevivência em comparação com o docetaxel, ao passo que a sobrevivência foi semelhante ao docetaxel em doentes sem expressão da PD-L1. Diferenças significativas na mediana de sobrevivência global foram observadas nos subgrupos do nivolumab em relação aos subgrupos do docetaxel, quando analisados pelo nível de expressão da PD-L1. A mediana de sobrevivência global foi de 17,1, 18,2 e 19,4 meses para indivíduos com o nivolumab, em comparação com 9,0, 8,1 e 8,0 meses para indivíduos com o docetaxel com níveis de expressão da PD-L1 de 1%, 5% e 10%, respetivamente. Não foi observada qualquer diferença na sobrevivência global entre os grupos de tratamento em indivíduos com < 1%, < 5% e < 10% de níveis de expressão, com intervalos de mediana de sobrevivência global de 9,7 a 10,4 meses para o nivolumab, e 10,1 a 10,3 meses para o docetaxel. As taxas de risco (HR) não estratificadas e a mediana de sobrevivência global (OS) são apresentadas na figura 1. O diagrama de Kaplan-Meier para subgrupos por nível de expressão da PD-L1 é mostrado nas figuras 2 e 3. P03914PT_04/SK / p. 14/23
15 Figura 1: Gráfico de floresta - Sobrevivência global baseada na expressão da PD-L1 em doentes com NSCLC não escamoso - CA Mediana de sobrevivência global (meses) Nível da expressão da PD-L1 Taxas de risco não estratificadas OPDIVO Docetaxel 1% (n = 246) 0,59 17,1 9,0 < 1% (n = 209) 0,90 10,4 10,1 5% (n = 181) 0,43 18,2 8,1 < 5% (n = 274) 1,01 9,7 10,1 10% (n = 165) 0,40 19,4 8,0 < 10% (n = 290) 1,00 9,9 10,3 0,25 0,5 1,0 2,0 Favorece o OPDIVO Nota: A taxa de risco não estratificada e os correspondentes intervalos de confiança de 95% foram estimados num modelo Cox de riscos proporcionais, utilizando o braço aleatorizado como uma covariável única. Figura 2: Sobrevivência global - Doentes com NSCLC não escamoso com expressão da PD-L1 1% - CA ,0 0,9 0,8 Probabilidade de sobrevivência 0,7 0,6 0,5 0,4 0,3 0,2 0,1 0,0 OPDIVO Docetaxel Sobrevivência global (meses) Número de risco OPDIVO Docetaxel P03914PT_04/SK / p. 15/23
16 Figura 3: Sobrevivência global - Doentes com NSCLC não escamoso com expressão da PD-L1 < 1% - CA ,0 0,9 Probabilidade de sobrevivência 0,8 0,7 0,6 0,5 0,4 0,3 0,2 0,1 OPDIVO Docetaxel 0, Sobrevivência global (meses) Número de risco OPDIVO Docetaxel Avaliação do desempenho: SCCHN Sensibilidade analítica: SCCHN A sensibilidade analítica do PD-L1 IHC 28-8 pharmdx foi testada em 236 casos únicos de amostras FFPE de SCCHN de estádio I a IV, utilizando um lote de produção fabricado. A avaliação da expressão da PD-L1 demonstrou coloração num intervalo de células tumorais positivas de 0-95% e de intensidade de coloração de Repetibilidade/Reprodutibilidade externa: SCCHN A repetibilidade e a reprodutibilidade externa do PD-L1 IHC 28-8 pharmdx foram avaliadas na Dako e em três locais de teste externos, respetivamente. Os dados de desempenho são fornecidos na Tabela 11 e na Tabela 12. Para a repetibilidade, a percentagem média de concordância negativa (ANA), a percentagem média de concordância positiva (APA) e a percentagem de concordância global (OA) de comparações por pares e dos correspondentes intervalos de confiança de 95% na classificação de Wilson foram determinadas para cada nível de expressão da PD-L1 avaliado. Para a reprodutibilidade, a percentagem de concordância negativa (NPA), a percentagem de concordância positiva (PPA) e a percentagem de concordância global (OA) de uma comparação por pares independente dos testes foram determinadas para cada nível da expressão da PD-L1 avaliado. A observação que ocorreu com mais frequência foi aplicada como uma referência para calcular a NPA, a PPA e a OA, assim como os correspondentes intervalos de confiança de 95% da classificação de Wilson. Tabela 11: Repetibilidade do PD-L1 IHC 28-8 pharmdx - SCCHN Repetibilidade Entre lotes Método Cada uma das 39 amostras de SCCHN com um intervalo de expressão da PD- L1 por IHC foi testada com cada um dos três lotes do ensaio no equipamento Autostainer Link 48. No total, foram realizadas 115 comparações por pares. % de concordância (95% CI) 1% de nível de expressão ANA 100 (96,9, 100) APA 100 (96,6, 100) OA 100 (98,4, 100) P03914PT_04/SK / p. 16/23
Monoclonal Mouse Anti-Human PD-L1 Clone 22C3. Referência M3653. Finalidade
 Monoclonal Mouse Anti-Human PD-L1 Clone 22C3 Referência M3653 Finalidade Sinónimos de antigénio Resumo e explicação Para utilização em diagnóstico in vitro. O Monoclonal Mouse Anti-Human PD-L1, Clone 22C3,
Monoclonal Mouse Anti-Human PD-L1 Clone 22C3 Referência M3653 Finalidade Sinónimos de antigénio Resumo e explicação Para utilização em diagnóstico in vitro. O Monoclonal Mouse Anti-Human PD-L1, Clone 22C3,
PD-L1 IHC 28-8 pharmdx. SK testes para utilização no Autostainer Link 48. Finalidade Para utilização em diagnóstico in vitro.
 PD-L1 IHC 28-8 pharmdx SK005 50 testes para utilização no Autostainer Link 48 Finalidade Para utilização em diagnóstico in vitro. O PD-L1 IHC 28-8 pharmdx é um ensaio de imunohistoquímica qualitativa que
PD-L1 IHC 28-8 pharmdx SK005 50 testes para utilização no Autostainer Link 48 Finalidade Para utilização em diagnóstico in vitro. O PD-L1 IHC 28-8 pharmdx é um ensaio de imunohistoquímica qualitativa que
O PD-L1 IHC 22C3 pharmdx está indicado como auxiliar na identificação de doentes com NSCLC para tratamento com KEYTRUDA (pembrolizumab).
 PD-L1 IHC 22C3 pharmdx SK006 50 testes para utilização no Autostainer Link 48 Finalidade Para utilização em diagnóstico in vitro. O PD-L1 IHC 22C3 pharmdx é um ensaio de imuno-histoquímica qualitativa
PD-L1 IHC 22C3 pharmdx SK006 50 testes para utilização no Autostainer Link 48 Finalidade Para utilização em diagnóstico in vitro. O PD-L1 IHC 22C3 pharmdx é um ensaio de imuno-histoquímica qualitativa
Solução tamponada que contém peróxido de hidrogénio, detergente e 0,015 mol/l de azida de sódio.
 PD-L1 IHC 22C3 pharmdx SK006 50 testes para utilização no Autostainer Link 48 Finalidade Para utilização em diagnóstico in vitro. O PD-L1 IHC 22C3 pharmdx é um ensaio de imuno-histoquímica qualitativa
PD-L1 IHC 22C3 pharmdx SK006 50 testes para utilização no Autostainer Link 48 Finalidade Para utilização em diagnóstico in vitro. O PD-L1 IHC 22C3 pharmdx é um ensaio de imuno-histoquímica qualitativa
Monoclonal Rabbit Anti-Human Cytokeratin 8/18 Clone EP17/EP30. Referência M3652. Finalidade
 Monoclonal Rabbit Anti-Human Cytokeratin 8/18 Clone EP17/EP30 Referência M3652 Finalidade Para utilização em diagnóstico in vitro. O Monoclonal Rabbit Anti-Human Cytokeratin 8/18, Clone EP17/EP30, destina-se
Monoclonal Rabbit Anti-Human Cytokeratin 8/18 Clone EP17/EP30 Referência M3652 Finalidade Para utilização em diagnóstico in vitro. O Monoclonal Rabbit Anti-Human Cytokeratin 8/18, Clone EP17/EP30, destina-se
EnVision FLEX+, Mouse, High ph, (Link)
 EnVision FLEX+, Mouse, High ph, (Link) Referência K8002 5ª edição O kit contém reagentes suficientes para 400 600 testes. Para os instrumentos Autostainer Link. Reagentes opcionais: Referência Nome do
EnVision FLEX+, Mouse, High ph, (Link) Referência K8002 5ª edição O kit contém reagentes suficientes para 400 600 testes. Para os instrumentos Autostainer Link. Reagentes opcionais: Referência Nome do
Dako REAL Detection System, Peroxidase/DAB+, Rabbit/Mouse
 Dako REAL Detection System, Peroxidase/DAB+, Rabbit/Mouse Referência K5001 6ª edição Para utilização com os instrumentos de imuno-coloração automatizados Dako. O kit contém reagentes suficientes para 500
Dako REAL Detection System, Peroxidase/DAB+, Rabbit/Mouse Referência K5001 6ª edição Para utilização com os instrumentos de imuno-coloração automatizados Dako. O kit contém reagentes suficientes para 500
FLEX Monoclonal Rabbit Anti-Human Cytokeratin 8/18 Clone EP17/EP30. Ready-to-Use (Link) Referência IR094. Finalidade
 FLEX Monoclonal Rabbit Anti-Human Cytokeratin 8/18 Clone EP17/EP30 Ready-to-Use (Link) Referência IR094 Finalidade Sinónimos de antigénio Resumo e explicação Para utilização em diagnóstico in vitro. O
FLEX Monoclonal Rabbit Anti-Human Cytokeratin 8/18 Clone EP17/EP30 Ready-to-Use (Link) Referência IR094 Finalidade Sinónimos de antigénio Resumo e explicação Para utilização em diagnóstico in vitro. O
EnVision FLEX, High ph, (Dako Autostainer/Autostainer Plus)
 EnVision FLEX, High ph, (Dako Autostainer/Autostainer Plus) Referência K8010 6ª edição O kit contém reagentes suficientes para 400 600 testes. Para Dako Autostainer/Autostainer Plus. Reagentes opcionais:
EnVision FLEX, High ph, (Dako Autostainer/Autostainer Plus) Referência K8010 6ª edição O kit contém reagentes suficientes para 400 600 testes. Para Dako Autostainer/Autostainer Plus. Reagentes opcionais:
EnVision DuoFLEX Doublestain System, (Link)
 EnVision DuoFLEX Doublestain System, (Link) Referência SK110 Edição 06/15 Este kit contém reagentes suficientes para 100 150 testes. Para instrumentos Autostainer Link. (127836-001) P04070PT_01/SK110/2015.06
EnVision DuoFLEX Doublestain System, (Link) Referência SK110 Edição 06/15 Este kit contém reagentes suficientes para 100 150 testes. Para instrumentos Autostainer Link. (127836-001) P04070PT_01/SK110/2015.06
PEROXIDASE-BLOCKING REAGENT Solução tamponada contendo peróxido de hidrogênio, detergente e 0,015 mol/l de azido de sódio.
 PD-L1 IHC 28-8 pharmdx SK005 Cinquenta testes para uso com Autostainer Link 48 Uso pretendido Para uso com diagnóstico in vitro. O PD-L1 IHC 28-8 pharmdx é um ensaio imuno-histoquímico qualitativo que
PD-L1 IHC 28-8 pharmdx SK005 Cinquenta testes para uso com Autostainer Link 48 Uso pretendido Para uso com diagnóstico in vitro. O PD-L1 IHC 28-8 pharmdx é um ensaio imuno-histoquímico qualitativo que
FLEX Monoclonal Rabbit Anti-Human Estrogen Receptor α Clone EP1 Ready-to-Use (Dako Autostainer/Autostainer Plus) Referência IS084.
 FLEX Monoclonal Rabbit Anti-Human Estrogen Receptor α Clone EP1 Ready-to-Use (Dako Autostainer/Autostainer Plus) Referência IS084 Finalidade Sinónimos de antigénio Resumo e explicação Reagente fornecido
FLEX Monoclonal Rabbit Anti-Human Estrogen Receptor α Clone EP1 Ready-to-Use (Dako Autostainer/Autostainer Plus) Referência IS084 Finalidade Sinónimos de antigénio Resumo e explicação Reagente fornecido
Solução tamponada contendo peróxido de hidrogênio, detergente e 0,015 mol/l de azido de sódio.
 PD-L1 IHC 22C3 pharmdx SK006 Cinquenta testes para uso com Autostainer Link 48 Uso pretendido Para uso com diagnóstico in vitro. O PD-L1 IHC 22C3 pharmdx é um ensaio imuno-histoquímico qualitativo que
PD-L1 IHC 22C3 pharmdx SK006 Cinquenta testes para uso com Autostainer Link 48 Uso pretendido Para uso com diagnóstico in vitro. O PD-L1 IHC 22C3 pharmdx é um ensaio imuno-histoquímico qualitativo que
Cytokeratin Cocktail (AE1 & AE3)
 Identificação de Produto N.º Cat. Descrição 44575 Cytokeratin Cocktail 0,1 M (AE1&AE3) 44576 Cytokeratin Cocktail 1 M (AE1&AE3) 44277 Cytokeratin Cocktail RTU M (AE1&AE3) Definições Dos Símbolos P C A
Identificação de Produto N.º Cat. Descrição 44575 Cytokeratin Cocktail 0,1 M (AE1&AE3) 44576 Cytokeratin Cocktail 1 M (AE1&AE3) 44277 Cytokeratin Cocktail RTU M (AE1&AE3) Definições Dos Símbolos P C A
Os produtos pré-diluídos são diluídos de forma ideal para utilizar com uma série de kits de detecção disponibilizados por outros fabricantes.
 Identificação de Produto N.º Cat. Descrição 45265 IMPATH TTF-1 RTU M (8G7G3/1) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
Identificação de Produto N.º Cat. Descrição 45265 IMPATH TTF-1 RTU M (8G7G3/1) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
Herpes Simplex Virus II (Polyclonal)
 Identificação de Produto N.º Cat. Descrição 45215 IMPATH Herpes Simplex Virus II RTU R (Poly) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído
Identificação de Produto N.º Cat. Descrição 45215 IMPATH Herpes Simplex Virus II RTU R (Poly) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 45153 IMPATH HMB-45 RTU M (HMB- 45) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
Identificação de Produto N.º Cat. Descrição 45153 IMPATH HMB-45 RTU M (HMB- 45) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
CD138/syndecan-1 (B-A38)
 Identificação de Produto N.º Cat. Descrição 44463 CD138 0,1 M (B-A38) 44464 CD138 1 M (B-A38) 44220 CD138 RTU M (B-A38) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
Identificação de Produto N.º Cat. Descrição 44463 CD138 0,1 M (B-A38) 44464 CD138 1 M (B-A38) 44220 CD138 RTU M (B-A38) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
HercepTest TM N.º de Referência K5204
 HercepTest TM N.º de Referência K5204 21ª edição Para coloração imunocitoquímica O kit é utilizado para 35 testes (70 lamelas). (129261-001) P04454PT_01/K520421-2/2016.05 p. 1/56 Índice Página Utilização
HercepTest TM N.º de Referência K5204 21ª edição Para coloração imunocitoquímica O kit é utilizado para 35 testes (70 lamelas). (129261-001) P04454PT_01/K520421-2/2016.05 p. 1/56 Índice Página Utilização
Estrogen Receptor (EP1)
 Identificação de Produto N.º Cat. Descrição 44592 Estrogen Receptor 0,1 R (EP1) 44593 Estrogen Receptor 1 R (EP1) 44285 Estrogen Receptor RTU R (EP1) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto
Identificação de Produto N.º Cat. Descrição 44592 Estrogen Receptor 0,1 R (EP1) 44593 Estrogen Receptor 1 R (EP1) 44285 Estrogen Receptor RTU R (EP1) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto
Adenovirus (20/11 & 2/6)
 Identificação de Produto N.º Cat. Descrição 45606 Adenovirus 0,1 M (20/11 & 2/6) 45607 Adenovirus 1 M (20/11 & 2/6) 45631 Adenovirus RTU M (20/11 & 2/6) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto
Identificação de Produto N.º Cat. Descrição 45606 Adenovirus 0,1 M (20/11 & 2/6) 45607 Adenovirus 1 M (20/11 & 2/6) 45631 Adenovirus RTU M (20/11 & 2/6) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 46928 c-myc 0,1 R (EP121) 46929 c-myc 1 R (EP121) 46927 c-myc RTU R (EP121) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
Identificação de Produto N.º Cat. Descrição 46928 c-myc 0,1 R (EP121) 46929 c-myc 1 R (EP121) 46927 c-myc RTU R (EP121) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
Epstein-Barr Virus (MRQ-47)
 Identificação de Produto N.º Cat. Descrição 45206 IMPATH Epstein-Barr Virus RTU R (MRQ-47) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído
Identificação de Produto N.º Cat. Descrição 45206 IMPATH Epstein-Barr Virus RTU R (MRQ-47) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44664 INI-1 0,1 M (MRQ-27) 44665 INI-1 1 M (MRQ-27) 44321 INI-1 RTU M (MRQ-27) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite
Identificação de Produto N.º Cat. Descrição 44664 INI-1 0,1 M (MRQ-27) 44665 INI-1 1 M (MRQ-27) 44321 INI-1 RTU M (MRQ-27) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44437 BCL6 0,1 M (GI191E/A8) 44438 BCL6 1 M (GI191E/A8) 44206 BCL6 RTU M (GI191E/A8) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado
Identificação de Produto N.º Cat. Descrição 44437 BCL6 0,1 M (GI191E/A8) 44438 BCL6 1 M (GI191E/A8) 44206 BCL6 RTU M (GI191E/A8) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado
Actin, Smooth Muscle (1A4)
 Identificação de Produto N.º Cat. Descrição 44419 Actin Smooth Muscle 0,1 M (1A4) 45040 Actin Smooth Muscle 1 M (1A4) 44196 Actin Smooth Muscle RTU M (1A4) Definições Dos Símbolos P C A E S DIL DOC# DIS
Identificação de Produto N.º Cat. Descrição 44419 Actin Smooth Muscle 0,1 M (1A4) 45040 Actin Smooth Muscle 1 M (1A4) 44196 Actin Smooth Muscle RTU M (1A4) Definições Dos Símbolos P C A E S DIL DOC# DIS
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 45629 SALL4 0,1 M (6E3) 45630 SALL4 1 M (6E3) 45643 SALL4 RTU M (6E3) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro sobrenadante
Identificação de Produto N.º Cat. Descrição 45629 SALL4 0,1 M (6E3) 45630 SALL4 1 M (6E3) 45643 SALL4 RTU M (6E3) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro sobrenadante
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 47346 IMPATH ALDH1A1 RTU M (44) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
Identificação de Produto N.º Cat. Descrição 47346 IMPATH ALDH1A1 RTU M (44) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44839 Wilms Tumor 0,1 M (6F-H2) 44840 Wilms Tumor 1 M (6F-H2) 44410 Wilms Tumor RTU M (6F-H2) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado
Identificação de Produto N.º Cat. Descrição 44839 Wilms Tumor 0,1 M (6F-H2) 44840 Wilms Tumor 1 M (6F-H2) 44410 Wilms Tumor RTU M (6F-H2) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 46934 EZH2 0,1 M (11) 46935 EZH2 1 M (11) 46933 EZH2 RTU M (11) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro sobrenadante
Identificação de Produto N.º Cat. Descrição 46934 EZH2 0,1 M (11) 46935 EZH2 1 M (11) 46933 EZH2 RTU M (11) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro sobrenadante
Cytokeratin 7 (OV-TL 12/30)
 Identificação de Produto N.º Cat. Descrição 44565 Cytokeratin 7 0,1 M (OV-TL 12/30) 44566 Cytokeratin 7 1 M (OV-TL 12/30) 44272 Cytokeratin 7 RTU M (OV-TL 12/30) Definições Dos Símbolos P C A E S DIL DOC#
Identificação de Produto N.º Cat. Descrição 44565 Cytokeratin 7 0,1 M (OV-TL 12/30) 44566 Cytokeratin 7 1 M (OV-TL 12/30) 44272 Cytokeratin 7 RTU M (OV-TL 12/30) Definições Dos Símbolos P C A E S DIL DOC#
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44644 HGAL 0,1 M (MRQ-49) 44645 HGAL 1 M (MRQ-49) 44311 HGAL RTU M (MRQ-49) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
Identificação de Produto N.º Cat. Descrição 44644 HGAL 0,1 M (MRQ-49) 44645 HGAL 1 M (MRQ-49) 44311 HGAL RTU M (MRQ-49) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
INSTRUÇÕES DE USO PARASITE SUSPENSIONS. n Parasite Suspensions em formalina UTILIZAÇÃO PREVISTA RESUMO E EXPLICAÇÃO PRINCÍPIOS COMPOSIÇÃO
 INSTRUÇÕES DE USO n Parasite Suspensions em formalina UTILIZAÇÃO PREVISTA As Parasite Suspensions da Microbiologics apoiam programas de garantia de qualidade servindo como amostras de controle de qualidade
INSTRUÇÕES DE USO n Parasite Suspensions em formalina UTILIZAÇÃO PREVISTA As Parasite Suspensions da Microbiologics apoiam programas de garantia de qualidade servindo como amostras de controle de qualidade
ZytoDot CEN 7 Probe. Para a deteção dos satélites alfa humanos do cromossoma 7 por meio de hibridação in situ cromogénica (CISH)
 ZytoDot CEN 7 Probe C-3008-400 40 (0,4 ml) Para a deteção dos satélites alfa humanos do cromossoma 7 por meio de hibridação in situ cromogénica (CISH).... Para utilização em diagnóstico in vitro em conformidade
ZytoDot CEN 7 Probe C-3008-400 40 (0,4 ml) Para a deteção dos satélites alfa humanos do cromossoma 7 por meio de hibridação in situ cromogénica (CISH).... Para utilização em diagnóstico in vitro em conformidade
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44662 Inhibin (Alpha) 0,1 M (R1) 44663 Inhibin (Alpha) 1 M (R1) 44320 Inhibin (Alpha) RTU M (R1) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar
Identificação de Produto N.º Cat. Descrição 44662 Inhibin (Alpha) 0,1 M (R1) 44663 Inhibin (Alpha) 1 M (R1) 44320 Inhibin (Alpha) RTU M (R1) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar
REGISTO ONCOLÓGICO 2009
 REGISTO ONCOLÓGICO 2009 2 Director do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Dra. Maria José Bento Registo Oncológico Dra. Ana Moreira Elsa
REGISTO ONCOLÓGICO 2009 2 Director do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Dra. Maria José Bento Registo Oncológico Dra. Ana Moreira Elsa
ZytoDot. Para a deteção dos satélites alfa humanos do cromossoma 17 por meio de hibridação in situ cromogénica (CISH)
 ZytoDot CEN 17 Probe C-3006-400 40 (0,4 ml) Para a deteção dos satélites alfa humanos do cromossoma 17 por meio de hibridação in situ cromogénica (CISH).... Para utilização em diagnóstico in vitro em conformidade
ZytoDot CEN 17 Probe C-3006-400 40 (0,4 ml) Para a deteção dos satélites alfa humanos do cromossoma 17 por meio de hibridação in situ cromogénica (CISH).... Para utilização em diagnóstico in vitro em conformidade
Androgen Receptor (SP107)
 Identificação de Produto N.º Cat. Descrição 44425 Androgen Receptor 0,1 M (SP107) 44426 Androgen Receptor 1 M (SP107) 44199 Androgen Receptor RTU M (SP107) Definições Dos Símbolos P C A E S DIL DOC# DIS
Identificação de Produto N.º Cat. Descrição 44425 Androgen Receptor 0,1 M (SP107) 44426 Androgen Receptor 1 M (SP107) 44199 Androgen Receptor RTU M (SP107) Definições Dos Símbolos P C A E S DIL DOC# DIS
Cytokeratin (34betaE12)
 Identificação de Produto N.º Cat. Descrição 45138 IMPATH Cytokeratin RTU M (34betaE12) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela
Identificação de Produto N.º Cat. Descrição 45138 IMPATH Cytokeratin RTU M (34betaE12) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44813 TFE3 0,1 R (MRQ-37) 44814 TFE3 1 R (MRQ-37) 44397 TFE3 RTU R (MRQ-37) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
Identificação de Produto N.º Cat. Descrição 44813 TFE3 0,1 R (MRQ-37) 44814 TFE3 1 R (MRQ-37) 44397 TFE3 RTU R (MRQ-37) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
Hemoglobin A (EPR3608)
 Identificação de Produto N.º Cat. Descrição 45286 IMPATH HEMOGLOBIN A RTU R (EPR3608) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela
Identificação de Produto N.º Cat. Descrição 45286 IMPATH HEMOGLOBIN A RTU R (EPR3608) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44744 p57 0,1 M (Kp10) 44745 p57 1 M (Kp10) 44362 p57 RTU M (Kp10) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro sobrenadante
Identificação de Produto N.º Cat. Descrição 44744 p57 0,1 M (Kp10) 44745 p57 1 M (Kp10) 44362 p57 RTU M (Kp10) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro sobrenadante
Ep-CAM/Epithelial Specific Antigen (Ber-EP4)
 Ep-CAM/Epithelial Specific Antigen (Ber- Identificação de Produto N.º Cat. Descrição 45614 Ep-CAM 0,1 M (Ber- 45615 Ep-CAM 1 M (Ber- 45635 Ep-CAM RTU M (Ber- Definições Dos Símbolos P C A E S DIL DOC#
Ep-CAM/Epithelial Specific Antigen (Ber- Identificação de Produto N.º Cat. Descrição 45614 Ep-CAM 0,1 M (Ber- 45615 Ep-CAM 1 M (Ber- 45635 Ep-CAM RTU M (Ber- Definições Dos Símbolos P C A E S DIL DOC#
GLUT1 (Polyclonal) Rabbit Polyclonal Antibody. Identificação de Produto. Definições Dos Símbolos. Utilização Pretendida. Resumo E Explicação
 Identificação de Produto N.º Cat. Descrição 44614 GLUT1 0,1 R (Poly) 44615 GLUT1 1 R (Poly) 44296 GLUT1 RTU R (Poly) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
Identificação de Produto N.º Cat. Descrição 44614 GLUT1 0,1 R (Poly) 44615 GLUT1 1 R (Poly) 44296 GLUT1 RTU R (Poly) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 45166 IMPATH BCL6 RTU M (GI191E/A8) Definições Dos Símbolos células grandes anaplásicos ALK+ (ALCL) e em 28% dos linfomas das células T/ALK- ALCL, NK (27%),
Identificação de Produto N.º Cat. Descrição 45166 IMPATH BCL6 RTU M (GI191E/A8) Definições Dos Símbolos células grandes anaplásicos ALK+ (ALCL) e em 28% dos linfomas das células T/ALK- ALCL, NK (27%),
REGISTO ONCOLÓGICO 2010
 REGISTO ONCOLÓGICO 2010 Director do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Dra. Maria José Bento Registo Oncológico Dra. Filipa Gonçalves
REGISTO ONCOLÓGICO 2010 Director do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Dra. Maria José Bento Registo Oncológico Dra. Filipa Gonçalves
Arjo Liquids. Flusher Rinse FICHA DE DADOS DE SEGURANÇA. Conforme: Regulamento (CE) N.º 1907/2006. Nome: Arjo Liquids Flusher Rinse
 FICHA DE DADOS DE SEGURANÇA Arjo Liquids Flusher Rinse Conforme: Regulamento (CE) N.º 1907/2006 Secção 1 1.1 Nome: Arjo Liquids Flusher Rinse 1.2 Flusher Rinse é uma solução alcalina suave para utilização
FICHA DE DADOS DE SEGURANÇA Arjo Liquids Flusher Rinse Conforme: Regulamento (CE) N.º 1907/2006 Secção 1 1.1 Nome: Arjo Liquids Flusher Rinse 1.2 Flusher Rinse é uma solução alcalina suave para utilização
A. 1-5 O adenocarcinoma pulmonar
 Identificação de Produto N.º Cat. Descrição 44723 Napsin A 1 M (MRQ-60) 44351 Napsin A RTU M (MRQ-60) 44722 Napsin A 0,1 M (MRQ-60) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado
Identificação de Produto N.º Cat. Descrição 44723 Napsin A 1 M (MRQ-60) 44351 Napsin A RTU M (MRQ-60) 44722 Napsin A 0,1 M (MRQ-60) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado
Anticorpo monoclonal de ratinho pronto a usar, fornecido na forma líquida num tampão com proteína estabilizadora e 0,015 mol/l de NaN 3.
 FLEX Monoclonal Mouse Anti-Human Progesterone Receptor Ready-to-Use (Link) Referência IR068 Finalidade Sinónimo do antigénio Resumo e explicação Reagente fornecido Para utilização em diagnóstico in vitro.
FLEX Monoclonal Mouse Anti-Human Progesterone Receptor Ready-to-Use (Link) Referência IR068 Finalidade Sinónimo do antigénio Resumo e explicação Reagente fornecido Para utilização em diagnóstico in vitro.
REGISTO ONCOLÓGICO 2013
 REGISTO ONCOLÓGICO 2013 Director do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Doutora Maria José Bento Registo Oncológico Doutora Ana Filipa
REGISTO ONCOLÓGICO 2013 Director do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Doutora Maria José Bento Registo Oncológico Doutora Ana Filipa
c-kit pharmdx Referência K testes para utilização manual Finalidade Para Utilização em Diagnóstico In Vitro.
 c-kit pharmdx Referência K1906 25 testes para utilização manual Finalidade Para Utilização em Diagnóstico In Vitro. O ensaio c-kit pharmdx consiste num sistema de kit de imuno-histoquímica (IHC) qualitativa
c-kit pharmdx Referência K1906 25 testes para utilização manual Finalidade Para Utilização em Diagnóstico In Vitro. O ensaio c-kit pharmdx consiste num sistema de kit de imuno-histoquímica (IHC) qualitativa
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI nivolumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM Frasco de
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI nivolumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM Frasco de
Registo Oncológico Nacional
 Registo Oncológico Nacional 2001 Instituto Português de Oncologia de Francisco Gentil Prefácio Com a publicação destes resultados, a Comissão Coordenadora do Instituto Português de Oncologia Francisco
Registo Oncológico Nacional 2001 Instituto Português de Oncologia de Francisco Gentil Prefácio Com a publicação destes resultados, a Comissão Coordenadora do Instituto Português de Oncologia Francisco
Factor XIIIa (EP3372)
 Identificação de Produto N.º Cat. Descrição 44596 Factor XIIIa 0,1 R (EP3372) 44597 Factor XIIIa 1 R (EP3372) 44287 Factor XIIIa RTU R (EP3372) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar
Identificação de Produto N.º Cat. Descrição 44596 Factor XIIIa 0,1 R (EP3372) 44597 Factor XIIIa 1 R (EP3372) 44287 Factor XIIIa RTU R (EP3372) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar
Hemoglobin A (EPR3608)
 Identificação de Produto N.º Cat. Descrição 44628 HEMOGLOBIN A 0,1 R (EPR3608) 44629 HEMOGLOBIN A 1 R (EPR3608) 44303 HEMOGLOBIN A RTU R (EPR3608) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto
Identificação de Produto N.º Cat. Descrição 44628 HEMOGLOBIN A 0,1 R (EPR3608) 44629 HEMOGLOBIN A 1 R (EPR3608) 44303 HEMOGLOBIN A RTU R (EPR3608) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto
Referência K testes para utilização no Dako Autostainer
 c-kit pharmdx Referência K1907 35 testes para utilização no Dako Autostainer Finalidade Para Utilização em Diagnóstico In Vitro. O ensaio c-kit pharmdx consiste num sistema de kit de imuno-histoquímica
c-kit pharmdx Referência K1907 35 testes para utilização no Dako Autostainer Finalidade Para Utilização em Diagnóstico In Vitro. O ensaio c-kit pharmdx consiste num sistema de kit de imuno-histoquímica
REGISTO ONCOLÓGICO INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL DE ONCOLOGIA DO PORTO, EPE
 INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL DE ONCOLOGIA DO PORTO, EPE REGISTO ONCOLÓGICO 2005 EDITADO PELO INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL
INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL DE ONCOLOGIA DO PORTO, EPE REGISTO ONCOLÓGICO 2005 EDITADO PELO INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 45265 IMPATH TTF-1 RTU M (8G7G3/1) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
Identificação de Produto N.º Cat. Descrição 45265 IMPATH TTF-1 RTU M (8G7G3/1) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI nivolumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM Frasco de
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI nivolumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM Frasco de
REGISTO ONCOLÓGICO 2011
 REGISTO ONCOLÓGICO 2011 Director do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Dra. Maria José Bento Registo Oncológico Dra. Filipa Gonçalves
REGISTO ONCOLÓGICO 2011 Director do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Dra. Maria José Bento Registo Oncológico Dra. Filipa Gonçalves
REGISTO ONCOLÓGICO INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL DE ONCOLOGIA DO PORTO, EPE
 INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL DE ONCOLOGIA DO PORTO, EPE REGISTO ONCOLÓGICO 2003 EDITADO PELO INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL
INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL DE ONCOLOGIA DO PORTO, EPE REGISTO ONCOLÓGICO 2003 EDITADO PELO INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL
REGISTO ONCOLÓGICO 2012
 REGISTO ONCOLÓGICO 2012 Director do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Dra. Maria José Bento Registo Oncológico Dra. Filipa Gonçalves
REGISTO ONCOLÓGICO 2012 Director do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Dra. Maria José Bento Registo Oncológico Dra. Filipa Gonçalves
REGISTO ONCOLÓGICO 2014
 REGISTO ONCOLÓGICO 2014 Diretor do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Doutora Maria José Bento Registo Oncológico Doutora Ana Filipa
REGISTO ONCOLÓGICO 2014 Diretor do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Doutora Maria José Bento Registo Oncológico Doutora Ana Filipa
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44523 CD71 0,1 M (MRQ-48) 44524 CD71 1 M (MRQ-48) 44251 CD71 RTU M (MRQ-48) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
Identificação de Produto N.º Cat. Descrição 44523 CD71 0,1 M (MRQ-48) 44524 CD71 1 M (MRQ-48) 44251 CD71 RTU M (MRQ-48) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
como o linfoma de células T gama-delta da mucosa e pele. 2-4 Referiu-se que 58% dos
 Identificação de Produto N.º Cat. Descrição 45612 CD16 0,1 R (SP175) 45613 CD16 1 R (SP175) 45634 CD16 RTU R (SP175) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
Identificação de Produto N.º Cat. Descrição 45612 CD16 0,1 R (SP175) 45613 CD16 1 R (SP175) 45634 CD16 RTU R (SP175) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
REGISTO ONCOLÓGICO INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL DE ONCOLOGIA DO PORTO, EPE
 INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL DE ONCOLOGIA DO PORTO, EPE REGISTO ONCOLÓGICO 2004 EDITADO PELO INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL
INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL DE ONCOLOGIA DO PORTO, EPE REGISTO ONCOLÓGICO 2004 EDITADO PELO INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL
Phosphohistone H3 (PHH3) (Polyclonal)
 Phosphohistone H3 (PHH3) (Polyclonal) Identificação de Produto N.º Cat. Descrição 44759 Phosphohistone H3 0,1 R (PHH3) 44760 Phosphohistone H3 1 R (PHH3) 44370 Phosphohistone H3 RTU R (PHH3) Definições
Phosphohistone H3 (PHH3) (Polyclonal) Identificação de Produto N.º Cat. Descrição 44759 Phosphohistone H3 0,1 R (PHH3) 44760 Phosphohistone H3 1 R (PHH3) 44370 Phosphohistone H3 RTU R (PHH3) Definições
REGISTO ONCOLÓGICO INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL DE ONCOLOGIA DO PORTO, EPE
 INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL DE ONCOLOGIA DO PORTO, EPE REGISTO ONCOLÓGICO 2006 EDITADO PELO INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL
INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL DE ONCOLOGIA DO PORTO, EPE REGISTO ONCOLÓGICO 2006 EDITADO PELO INSTITUTO PORTUGUÊS DE ONCOLOGIA DE FRANCISCO GENTIL CENTRO REGIONAL
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44781 PU.1 0,1 R (EPR3158Y) 44782 PU.1 1 R (EPR3158Y) 44381 PU.1RTU R (EPR3158Y) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite
Identificação de Produto N.º Cat. Descrição 44781 PU.1 0,1 R (EPR3158Y) 44782 PU.1 1 R (EPR3158Y) 44381 PU.1RTU R (EPR3158Y) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite
REGISTO ONCOLÓGICO 2016
 REGISTO ONCOLÓGICO 2016 Diretor do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Prof. Doutora Maria José Bento Registo Oncológico Doutora Ana
REGISTO ONCOLÓGICO 2016 Diretor do Registo Oncológico do IPO do Porto Dr. Laranja Pontes Compilação e Elaboração Serviço de Epidemiologia: Prof. Doutora Maria José Bento Registo Oncológico Doutora Ana
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44732 OCT-4 0,1 M (MRQ-10) 44733 OCT-4 1 M (MRQ-10) 44356 OCT-4 RTU M (MRQ-10) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite
Identificação de Produto N.º Cat. Descrição 44732 OCT-4 0,1 M (MRQ-10) 44733 OCT-4 1 M (MRQ-10) 44356 OCT-4 RTU M (MRQ-10) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite
incluindo carcinoma adrenal, seminomas, paraganglioma e hepatoma. Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 45205 IMPATH EMA RTU M (E29) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
Identificação de Produto N.º Cat. Descrição 45205 IMPATH EMA RTU M (E29) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
LABORATÓRIO ANÁLISE. PROCEDIMENTO OPERACIONAL PADRÃO. ANALITICO
 Edição Análise Crítica Aprovação Data / / Data: / / Data: / / ASS.: ASS.: ASS.: NOME: Rozileide Agostinho NOME:Rozileide Agostinho NOME: Marcelo Villar FUNÇÃO/CARGO: Controle de Documentos e Dados FUNÇÃO/CARGO:
Edição Análise Crítica Aprovação Data / / Data: / / Data: / / ASS.: ASS.: ASS.: NOME: Rozileide Agostinho NOME:Rozileide Agostinho NOME: Marcelo Villar FUNÇÃO/CARGO: Controle de Documentos e Dados FUNÇÃO/CARGO:
Métodos Cito-Histoquímicos
 Ciências Biomédicas Laboratoriais Métodos Cito-Histoquímicos Aula 4 2016/17 João Furtado jffurtado@ualg.pt Gab. 2.06 na ESSUAlg Sumário Hidratos Carbono Introdução Simples e Glicoconjugados Evidenciação
Ciências Biomédicas Laboratoriais Métodos Cito-Histoquímicos Aula 4 2016/17 João Furtado jffurtado@ualg.pt Gab. 2.06 na ESSUAlg Sumário Hidratos Carbono Introdução Simples e Glicoconjugados Evidenciação
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 45322 IMPATH PAX-8 RTU M (MRQ-50) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
Identificação de Produto N.º Cat. Descrição 45322 IMPATH PAX-8 RTU M (MRQ-50) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
CD11c (5D11) Mouse Monoclonal Antibody. Identificação de Produto. Definições Dos Símbolos. Utilização Pretendida. Resumo E Explicação
 Identificação de Produto N.º Cat. Descrição 44843 CD11c 0,1 M (5D11) 44462 CD11c 1 M (5D11) 44219 CD11c RTU M (5D11) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
Identificação de Produto N.º Cat. Descrição 44843 CD11c 0,1 M (5D11) 44462 CD11c 1 M (5D11) 44219 CD11c RTU M (5D11) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite soro
PROCESSOS PATOLÓGICOS GERAIS. Prof. Archangelo P. Fernandes
 PROCESSOS PATOLÓGICOS GERAIS Prof. Archangelo P. Fernandes www.profbio.com.br Aula 1: Conceitos gerais para o estudo de Patologia. Grego: pathos = sofrimento e logos = estudo Investigação das causas das
PROCESSOS PATOLÓGICOS GERAIS Prof. Archangelo P. Fernandes www.profbio.com.br Aula 1: Conceitos gerais para o estudo de Patologia. Grego: pathos = sofrimento e logos = estudo Investigação das causas das
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44684 Mammaglobin 0,1 R (31A5) 44685 Mammaglobin 1 R (31A5) 44331 Mammaglobin RTU R (31A5) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado
Identificação de Produto N.º Cat. Descrição 44684 Mammaglobin 0,1 R (31A5) 44685 Mammaglobin 1 R (31A5) 44331 Mammaglobin RTU R (31A5) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44753 PAX-8 0,1 M (MRQ-50) 44754 PAX-8 1 M (MRQ-50) 44367 PAX-8 RTU M (MRQ-50) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite
Identificação de Produto N.º Cat. Descrição 44753 PAX-8 0,1 M (MRQ-50) 44754 PAX-8 1 M (MRQ-50) 44367 PAX-8 RTU M (MRQ-50) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite
CD11c (5D11) Mouse Monoclonal Antibody. Identificação de Produto. Definições Dos Símbolos. Utilização Pretendida. Resumo E Explicação
 Identificação de Produto N.º Cat. Descrição 45126 IMPATH CD11c RTU M (5D11) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
Identificação de Produto N.º Cat. Descrição 45126 IMPATH CD11c RTU M (5D11) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
é um marcador de linfócitos T maduros e é expresso em níveis muito baixos nos linfócitos T h
 Identificação de Produto N.º Cat. Descrição 44807 T-Bet 0,1 R (MRQ-46) 44808 T-Bet 1 R (MRQ-46) 44394 T-Bet RTU R (MRQ-46) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite
Identificação de Produto N.º Cat. Descrição 44807 T-Bet 0,1 R (MRQ-46) 44808 T-Bet 1 R (MRQ-46) 44394 T-Bet RTU R (MRQ-46) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado ascite
Cytokeratin 5 (EP1601Y)
 Identificação de Produto N.º Cat. Descrição 44561 Cytokeratin 5 0,1 R (EP1601Y) 44562 Cytokeratin 5 1 R (EP1601Y) 44270 Cytokeratin 5 RTU R (EP1601Y) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto
Identificação de Produto N.º Cat. Descrição 44561 Cytokeratin 5 0,1 R (EP1601Y) 44562 Cytokeratin 5 1 R (EP1601Y) 44270 Cytokeratin 5 RTU R (EP1601Y) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44668 Kappa Light Chain 0,1 M (L1C1) 44669 Kappa Light Chain 1 M (L1C1) 44323 Kappa Light Chain RTU M (L1C1) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto
Identificação de Produto N.º Cat. Descrição 44668 Kappa Light Chain 0,1 M (L1C1) 44669 Kappa Light Chain 1 M (L1C1) 44323 Kappa Light Chain RTU M (L1C1) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto
R 2 Risco de explosão por choque, fricção, fogo ou outras fontes de ignição
 Texto de Apoio Data: 26 de Setembro 2010 Formador[a]: Mª Filipa Castanheira UC/UFCD: 3778 Agentes Químicos e Biológicos 1.Lista de frases de risco usadas com substâncias perigosas Códigos: Frases de Risco
Texto de Apoio Data: 26 de Setembro 2010 Formador[a]: Mª Filipa Castanheira UC/UFCD: 3778 Agentes Químicos e Biológicos 1.Lista de frases de risco usadas com substâncias perigosas Códigos: Frases de Risco
Introdução à Histologia e Técnicas Histológicas. Prof. Cristiane Oliveira
 Introdução à Histologia e Técnicas Histológicas Prof. Cristiane Oliveira Visão Geral Corpo humano organizado em 4 tecidos básicos: Epitelial Conjuntivo Muscular Nervoso Visão Geral - Tecidos consistem
Introdução à Histologia e Técnicas Histológicas Prof. Cristiane Oliveira Visão Geral Corpo humano organizado em 4 tecidos básicos: Epitelial Conjuntivo Muscular Nervoso Visão Geral - Tecidos consistem
Aptima Multitest Swab Specimen Collection Kit
 Multitest Swab Specimen Collection Kit Aptima Utilização prevista O Aptima Multitest Swab Specimen Collection Kit (Kit de colheita de espécimes de esfregaço multiteste Aptima) destina-se a ser utilizado
Multitest Swab Specimen Collection Kit Aptima Utilização prevista O Aptima Multitest Swab Specimen Collection Kit (Kit de colheita de espécimes de esfregaço multiteste Aptima) destina-se a ser utilizado
CD45 (LCA) (2B11 & PD7/26)
 Identificação de Produto N.º Cat. Descrição 44504 CD45 0,1 M (2B11 & PD7/26) 44577 CD45 1 M (2B11 & PD7/26) 44241 CD45 RTU M (2B11 & PD7/26) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar
Identificação de Produto N.º Cat. Descrição 44504 CD45 0,1 M (2B11 & PD7/26) 44577 CD45 1 M (2B11 & PD7/26) 44241 CD45 RTU M (2B11 & PD7/26) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar
Detecção de IL-1 por ELISA sanduíche. Andréa Calado
 Detecção de IL-1 por ELISA sanduíche Andréa Calado andreabelfort@hotmail.com ELISA O teste identifica e quantifica Ag ou Ac, utilizando um dos dois conjugados com enzimas; PRINCIPAIS TIPOS: INDIRETO:
Detecção de IL-1 por ELISA sanduíche Andréa Calado andreabelfort@hotmail.com ELISA O teste identifica e quantifica Ag ou Ac, utilizando um dos dois conjugados com enzimas; PRINCIPAIS TIPOS: INDIRETO:
Técnicas de Imuno-Citoquímica e Imuno-Histoquímica
 Técnicas de Imuno-Citoquímica e Imuno-Histoquímica Doutorando: Romeu Moreira dos Santos Prof. Hélio José Montassier Disciplina: Imunologia Veterinária Linfócitos T Seleção e maturação de células T TCR
Técnicas de Imuno-Citoquímica e Imuno-Histoquímica Doutorando: Romeu Moreira dos Santos Prof. Hélio José Montassier Disciplina: Imunologia Veterinária Linfócitos T Seleção e maturação de células T TCR
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 45285 IMPATH GCDFP-15 RTU R (EP1582Y) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
Identificação de Produto N.º Cat. Descrição 45285 IMPATH GCDFP-15 RTU R (EP1582Y) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela Utilização
ONDE OCORRE TRANSPORTE ACOPLADO? Exemplos
 ONDE OCORRE TRANSPORTE ACOPLADO? Exemplos Epitélio do estômago (Antiporte entre HCO 3 - e Cl- para formação do suco gástrico) Epitélio do intestino (Simporte entre glicose e Na + ) Dutos pancreáticos (Formação
ONDE OCORRE TRANSPORTE ACOPLADO? Exemplos Epitélio do estômago (Antiporte entre HCO 3 - e Cl- para formação do suco gástrico) Epitélio do intestino (Simporte entre glicose e Na + ) Dutos pancreáticos (Formação
CD45 (LCA) (2B11 & PD7/26)
 Identificação de Produto N.º Cat. Descrição 45185 IMPATH CD45 RTU M (2B11 & PD7/26) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela
Identificação de Produto N.º Cat. Descrição 45185 IMPATH CD45 RTU M (2B11 & PD7/26) Definições Dos Símbolos P A E S DOC# DIS pronto a usar ascite soro sobrenadante número do documento distribuído pela
Princípios E Procedimentos
 Identificação de Produto N.º Cat. Descrição 44622 GCDFP-15 0,1 R (EP1582Y) 44623 GCDFP-15 1 R (EP1582Y) 44300 GCDFP-15 RTU R (EP1582Y) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado
Identificação de Produto N.º Cat. Descrição 44622 GCDFP-15 0,1 R (EP1582Y) 44623 GCDFP-15 1 R (EP1582Y) 44300 GCDFP-15 RTU R (EP1582Y) Definições Dos Símbolos P C A E S DIL DOC# DIS pronto a usar concentrado
EGFR pharmdx. Referência K testes para utilização manual Edition 05/2015. Finalidade Para Utilização em Diagnóstico In Vitro.
 EGFR pharmdx Referência K1492 35 testes para utilização manual Edition 05/2015 Finalidade Para Utilização em Diagnóstico In Vitro. O ensaio EGFR pharmdx consiste num sistema de kit de imuno-histoquímica
EGFR pharmdx Referência K1492 35 testes para utilização manual Edition 05/2015 Finalidade Para Utilização em Diagnóstico In Vitro. O ensaio EGFR pharmdx consiste num sistema de kit de imuno-histoquímica
CONTROLE Rh Monoclonal
 CONTROLE Rh Monoclonal PROTHEMO Produtos Hemoterápicos Ltda. Controle negativo das classificações Rh - Hr PARA TESTES EM LÂMINA OU TUBO Somente para Uso Diagnóstico IN VITRO Conservar entre: 2-8 C Não
CONTROLE Rh Monoclonal PROTHEMO Produtos Hemoterápicos Ltda. Controle negativo das classificações Rh - Hr PARA TESTES EM LÂMINA OU TUBO Somente para Uso Diagnóstico IN VITRO Conservar entre: 2-8 C Não
2003 Editado pelo Instituto Português de Oncologia do Porto
 2003 Editado pelo Instituto Português de Oncologia do Porto > REGISTO ONCOLÓGICO REGIONAL DO NORTE Prefácio As alterações demográficas que afectam a nossa sociedade, provocam problemas graves de sustentabilidade
2003 Editado pelo Instituto Português de Oncologia do Porto > REGISTO ONCOLÓGICO REGIONAL DO NORTE Prefácio As alterações demográficas que afectam a nossa sociedade, provocam problemas graves de sustentabilidade
Hibridação in situ fluorescente em corte histológico (Câncer de Próstata)
 Hibridação in situ fluorescente em corte histológico (Câncer de Próstata) FISH em tecido incluído em parafina: Four Colour PTEN Deletion Probe O protocolo de FISH descrito abaixo é recomendado para cortes
Hibridação in situ fluorescente em corte histológico (Câncer de Próstata) FISH em tecido incluído em parafina: Four Colour PTEN Deletion Probe O protocolo de FISH descrito abaixo é recomendado para cortes
TÉCNICAS DE ESTUDO EM PATOLOGIA
 TÉCNICAS DE ESTUDO EM PATOLOGIA Augusto Schneider Carlos Castilho de Barros Faculdade de Nutrição Universidade Federal de Pelotas TÉCNICAS Citologia Histologia Imunohistoquímica/imunofluorescência Biologia
TÉCNICAS DE ESTUDO EM PATOLOGIA Augusto Schneider Carlos Castilho de Barros Faculdade de Nutrição Universidade Federal de Pelotas TÉCNICAS Citologia Histologia Imunohistoquímica/imunofluorescência Biologia
