Fosforilação oxidativa
|
|
|
- Luiz Fernando Aveiro
- 5 Há anos
- Visualizações:
Transcrição
1 Fosforilação oxidativa Índice 1- Aspetos da estrutura das mitocôndrias com relevância na compreensão do processo de fosforilação oxidativa O papel das oxiredútases da cadeia respiratória na regeneração do NAD + e do FAD Termodinâmica do processo de oxidação do NADH pelo O A atividade dos complexos I, III e IV é o transporte ativo primário de protões em que a componente exergónica são reações redox As atividades catalítica e de transporte do complexo I (desidrogénase do NADH) As atividades catalítica e de transporte do complexo III (redútase do citocromo c) As atividades catalítica e de transporte do complexo IV (oxídase do citocromo c) A transferência de um par de eletrões entre intermediários do metabolismo que são oxidados pelo NAD + e o O 2 está acoplado com o bombeamento de 10 protões As atividades catalíticas da desidrogénase do succinato e da desidrogénase do glicerol-3-fosfato da membrana mitocondrial interna A transferência de um par de eletrões entre o succinato (ou o glicerol-3-fosfato) e o O 2 está acoplado com o bombeamento de 6 protões As atividades catalítica e de transporte de protões da síntase de ATP Os processos de transporte transmembrar de ATP, ADP e Pi também envolvem gasto da energia associada ao gradiente eletroquímico A razão P:O O ADP como fator estimulador da síntase do ATP e da atividade da cadeia respiratória O ião Ca 2+ como fator estimulador da síntase do ATP e da atividade dos complexos I e IV O papel da cínase da creatina na manutenção da concentração de ATP nos músculos Inibidores dos complexos da cadeia respiratória Inibição da síntase do ATP e do trocador ATP/ADP Desacoplagem entre fosforilação e oxidação por ação do dinitrofenol A atividade das UCPs (proteínas de desacoplamento) As lançadeiras permitem transferir eletrões do NADH citoplasmático para a cadeia respiratória; a lançadeira do glicerol-3-fosfato A lançadeira do malato é muito mais complexa que a lançadeira do glicerol-3-fosfato O número de moléculas de ATP que se podem formar aquando da oxidação completa de uma molécula de glicose 9 1- Aspetos da estrutura das mitocôndrias com relevância na compreensão do processo de fosforilação oxidativa A maior parte do ATP formado durante a oxidação dos nutrientes ocorre nas mitocôndrias que contêm duas membranas: uma externa e outra interna. A membrana externa, porque contém uma proteína denominada porina, permite a passagem livre e inespecífica de moléculas com massa molecular relativamente elevada (5-10 kda). Este facto permite compreender que o espaço intermembranar seja, funcionalmente, considerado como pertencendo ao citoplasma. A membrana interna é mais seletiva e o transporte de muitas substâncias (como, por exemplo, o piruvato, o malato, o aspartato, o glutamato, o α- cetoglutarato, o citrato, o fosfato, os protões, o ATP e o ADP) depende da presença de transportadores específicos e ocorre a velocidades limitadas pela atividade destes transportadores. 2- O papel das oxiredútases da cadeia respiratória na regeneração do NAD + e do FAD A oxidação do piruvato (desidrogénase do piruvato), dos ácidos gordos (oxidação em β), da acetil-coa (ciclo de Krebs) e de muitos outros compostos dá-se à custa da redução do NAD + ou do FAD Página 1 de 11
2 (a NADH e FADH2) 1 e ocorre na matriz mitocondrial ou na face interna da membrana interna da mitocôndria. As concentrações fisiológicas de NAD + e de FAD são muito baixas e, na ausência de regeneração rápida das suas formas oxidadas, a oxidação dos nutrientes seria interrompida. A cadeia respiratória é formada por uma série de oxiredútases organizadas em complexos proteicos na membrana interna da mitocôndria e possibilita a regeneração do NAD + e do FAD. Esses complexos catalisam, no seu conjunto, a oxidação do NADH a NAD + e do FADH2 a FAD pelo O 2 que se reduz a H 2O. 3- Termodinâmica do processo de oxidação do NADH pelo O 2 O potencial de oxi-redução padrão (ou potencial de elétrodo padrão) de um determinado par oxidante/redutor é uma medida da estabilidade termodinâmica relativa das formas oxidada e reduzida: quanto maior o seu valor maior a estabilidade da forma reduzida relativamente à forma oxidada desse par. O seu valor é, em muitos casos, conhecido e pode ser obtido consultando tabelas. Dentre os compostos envolvidos na cadeia respiratória merecem especial destaque o O 2 e o NADH. O valor positivo e elevado do potencial redox padrão do par O 2/H 2O (Eº = +0,815 V) significa que o O 2 é um potente oxidante e tem tendência a aceitar eletrões de outros compostos reduzindo-se a H 2O. No outro extremo da escala está o par NAD + /NADH cujo baixo (muito negativo; Eº = -0,315 V) potencial redox padrão significa que o NADH tem uma grande tendência a ceder eletrões oxidando-se a NAD +. O valor da diferença entre o potencial de oxi-redução padrão do par O 2/H 2O e o do par NAD + /NADH é de +1,13 V o que permite calcular a Keq (Keq = e (nf Eº /RT) ; log Keq = n Eº /0,059) para a reação esquematizada na Equação 1 como sendo de cerca de 1, atm -1/2. O valor de Gº (energia de Gibbs padrão) associado à mesma reação é de -224 kj por mole de NADH oxidado. Estes dados permitem compreender que o processo de oxidação do NADH pelo O 2 tem tendência a ocorrer até ao esgotamento do reagente limitante. Equação 1 NADH + ½ O 2 NAD + + H 2O A velocidade a que o processo ocorre é uma questão diferente e depende da atividade de catalisadores; no caso, a atividade dos complexos proteicos I, III e IV da cadeia respiratória. 4- A atividade dos complexos I, III e IV é o transporte ativo primário de protões em que a componente exergónica são reações redox Catalisadas pelos complexos da cadeia respiratória ocorrem na membrana mitocondrial interna reações de oxi-redução seriadas através das quais o oxigénio oxida o NADH. Cada um destes complexos é formado por muitas subunidades proteicas, tem massa molecular muito elevada, tem mobilidade lateral e atravessa a membrana interna da mitocôndria no plano transversal mantendo uma orientação fixa nesse plano. Estes catalisadores não são apenas enzimas pois também catalisam o transporte de protões da matriz da mitocôndria para o citoplasma. Os dois processos (oxidação e transporte direcional de protões) estão acoplados: os complexos I, III e IV são bombas que fazem a acoplagem de processos de oxidação específicos (processo exergónico) com o transporte de protões da matriz da mitocôndria para o espaço intermembranar (contra gradiente eletroquímico; processo endergónico). O transporte de protões é ativo (contra gradiente eletroquímico) e diz-se primário porque a componente exergónica do processo é uma reação química. 1 Há uma diferença importante entre estes dois dinucleotídeos. Enquanto as moléculas de NAD + (e a sua forma reduzida, o NADH) estão maioritariamente desligadas das enzimas apenas se ligando no decurso do ciclo catalítico, o FAD (e a sua forma reduzida, o FADH2) faz parte intrínseca da estrutura das enzimas e, por isso, designa-se por grupo prostético. Tomando como exemplo a desidrogénase do piruvato (piruvato + NAD + + CoA acetil-coa + NADH + CO 2), enquanto o NAD + é, a par com o piruvato e o CoA, um verdadeiro substrato da enzima, o FAD é um intermediário no ciclo catalítico da enzima. Na intimidade da desidrogénase do piruvato existe uma minicadeia de transferência de eletrões em que os eletrões fluem sequencialmente do piruvato para o lipoato (outro grupo prostético), do dihidrolipoato formado para o FAD e do FADH2 formado para o NAD + que está transitoriamente presente no centro ativo. Apesar da tradição que persiste em apontar o FAD e o FMN como substratos de algumas enzimas, quer o FAD (dinucleotídeo de flavina e adenina) quer o FMN (mononucleotídeo de flavina) são sempre grupos prostéticos das enzimas onde existem. Se considerarmos a atividade global dessas enzimas (ver, por exemplo, a Equação 8 e Equação 9) é fácil reconhecer que o verdadeiro substrato aceitador de eletrões é sempre outra substância que não o FAD (ou o FMN). Página 2 de 11
3 O mecanismo de bombeamento de protões envolve alterações conformacionais cíclicas nos complexos que ocorrem aquando dos processos de oxidação e de redução dos seus grupos prostéticos. Estas alterações cíclicas decorrem com aumento da afinidade para os protões na face matricial dos complexos seguida de exposição desses protões na face citoplasmática e diminuição da afinidade para os protões neste passo do processo. O gradiente criado pelos complexos I, III e IV é elétrico porque existe uma diferença de potencial entre a matriz (carga negativa) e o espaço intermembranar (carga positiva), mas é também químico porque a concentração de protões é maior (o ph é menor) no espaço intermembranar que na matriz; daí a expressão gradiente eletroquímico. O valor da energia de Gibbs mínima necessária para bombear um protão da matriz para o espaço intermembranar pode ser calculado conhecendo o valor da diferença de potencial (cerca de -0,15 V) e as concentrações de protões dentro e fora da mitocôndria (cerca de 10-7,6 M e 10-7,0 M, respetivamente) e é cerca de 18 kj/mole de protões bombeados 2. Usando o Gº da reação representada pela Equação 1 (-224 kj/mole de NADH oxidado) como a estimativa possível para o valor da energia disponibilizada durante a oxidação de 1 mole de NADH nas condições das células vivas, pode calcular-se que, teoricamente, o máximo de protões que poderiam ser bombeados seria de 12 moles (224 kj / 18 kj; ver à frente, pontos nº 11, 12 e 13). 5- As atividades catalítica e de transporte do complexo I (desidrogénase do NADH) O complexo I (que também se designa por desidrogénase do NADH ou oxiredútase do NADH:ubiquinona) contém como grupos prostéticos FMN e complexos ferro-enxofre. O complexo I catalisa a transferência de dois eletrões do NADH para a ubiquinona (ou coenzima Q) formando-se NAD + e ubiquinol (ou coenzima QH2). A coenzima Q é uma substância hidrofóbica presente na membrana interna da mitocôndria que na forma oxidada (ubiquinona) tem dois grupos cetónicos e na forma reduzida (ubiquinol) dois hidroxilos 3. O local de ligação do complexo I com o NADH está voltado para a matriz enquanto que o local que se liga à ubiquinona está mergulhado na membrana mitocondrial interna. De forma acoplada com a reação de oxi-redução, o complexo I também catalisa o bombeamento de protões da matriz para o citoplasma. Embora não seja ainda consensual entre os investigadores que estudam esta problemática [1], o número de protões bombeados quando um par de eletrões reduz a coenzima Q poderá ser de 4; paralelamente dois protões (um cedido pelo NADH e outro com origem na matriz) ligamse à coenzima Q reduzida. Aceitando estes números, a Equação 2 descreveria as atividades acopladas de oxi-redução e de bombeamento do complexo I. Equação 2 NADH + Q + 5 H + (dentro) NAD + + QH2 + 4 H + (fora) 6- As atividades catalítica e de transporte do complexo III (redútase do citocromo c) O complexo III (que também se designa por complexo b-c1 ou redútase do citocromo c) contém como grupos prostéticos hemes de tipo c e de tipo idêntico ao existente na hemoglobina (tipo b) assim como complexos ferro-enxofre. O mecanismo reativo e de transporte do complexo III é muito complexo. Simplificando poderíamos escrever que, em termos líquidos, o complexo III catalisa a transferência de dois eletrões do ubiquinol (QH2) para o citocromo c e, de forma acoplada com o processo oxidativo, o bombeamento de 2 protões da matriz para o citoplasma; os 2 protões que se libertam do ubiquinol quando este se oxida também são vertidos na face citoplasmática da membrana interna da mitocôndria (ver Equação 3). 2 O G associado ao transporte de um mole de protões contra gradiente elétrico e contra gradiente químico é o que corresponde ao somatório dos dois componentes em causa. No caso do gradiente elétrico o valor pode ser calculado usando a fórmula: G = Z F Ψ; sendo Z a carga do ião (+1, no caso), F a constante de Faraday (96500 Coulomb/mole de eletrões) e Ψ a diferença de potencial em Volts. No caso do gradiente químico a fórmula adequada será G = - RT ln ([H + ](matriz)/ [H + ](fora); sendo R a constante dos gazes perfeitos (8,314 J /mol Kelvin) e T a temperatura em graus Kelvin. Assim, aceitando os valores apontados, o valor da energia mínima para transportar um mole de protões seria de +18,1 kj; ( Coulomb 0,15 V) + (-8,314 J mol -1 K K ln (10-7,6 /10-7,0 ). Obviamente que a energia de Gibbs associada à entrada de 1 mole de protões, nas mesmas condições, tem o mesmo valor absoluto e sinal negativo, correspondendo a libertação de energia. 3 Apesar de dois grupos cetónicos serem convertidos a dois hidroxilos, a redução da coenzima Q a coenzima QH2 só envolve dois eletrões porque esta última forma tem mais uma ligação dupla que a primeira. Página 3 de 11
4 O citocromo c é uma proteína hemínica (contém heme que é de tipo c) que está presente na face externa da membrana interna da mitocôndria. Na forma oxidada o ião de ferro presente no heme de cada uma das moléculas de citocromo c envolvidas na oxidação de uma molécula de ubiquinol tem carga 3+; quando o citocromo c é reduzido a carga do ião de ferro passa a 2+. Equação 3 QH2 + 2 Cyt c (Fe 3+ ) + 2H + (dentro) Q + 2 Cyt c (Fe 2+ ) + 4 H + (fora) 7- As atividades catalítica e de transporte do complexo IV (oxídase do citocromo c) Por último, o complexo IV (que também se designa por oxídase do citocromo c ou oxiredútase do ferrocitocromo c:oxigénio) contém como grupos prostéticos hemes de tipo a assim como iões de cobre. O complexo IV catalisa a transferência de dois eletrões da forma reduzida do citocromo c para o oxigénio e, de forma acoplada com o processo oxidativo, o bombeamento de 2 protões; outros 2 protões da matriz são consumidos na formação de água (ver Equação 4). Equação 4 2 Cyt c (Fe 2+ ) + ½ O H + (dentro) H 2O + 2 Cyt c (Fe 3+ ) + 2 H + (fora) 8- A transferência de um par de eletrões entre intermediários do metabolismo que são oxidados pelo NAD + e o O 2 está acoplado com o bombeamento de 10 protões O processo oxidativo catalisado pelos complexos envolvidos na oxidação do NADH pelo O 2 está acoplado com o transporte de protões da matriz mitocondrial para o citoplasma e o processo de bombeamento cria um gradiente eletroquímico: maior número de cargas positivas ( gradiente elétrico ) e maior concentração de protões ( gradiente químico ) no lado citoplasmático da membrana mitocondrial interna. As Equações 2, 3 e 4 descrevem os processos reativos e de transporte de protões catalisados pelos complexos I, III e IV e o somatório destas equações é a Equação 5: Equação 5 NADH + ½ O H + (dentro) NAD + + H 2O + 10 H + (fora) O NADH forma-se em reações de oxi-redução catalisadas por várias desidrogénases mitocondriais que podem ser esquematizadas pela Equação 6: Equação 6 XH2 4 + NAD + X + NADH + H + (dentro) O somatório da Equação 5 e da Equação 6 (Equação 7) mostra que a transferência de um par de eletrões entre os intermediários do metabolismo oxidativo dos nutrientes que são oxidados pelo NAD + e o oxigénio está acoplado com o bombeamento de 10 protões da matriz para o citoplasma: Equação 7 XH2 + ½ O H + (dentro) X + H 2O + 10 H + (fora) Tal como em muitos outros processos celulares (como o catalisado pela ATPase do Na + /K +, por exemplo) um processo com uma enorme tendência para ocorrer num determinado sentido (a oxidação do NADH pelo O 2) está acoplado com um processo que não ocorreria na ausência deste acoplamento (o transporte de protões contra gradiente). Ou dito de outro modo, a energia libertada no processo de oxidação do NADH pelo O 2 (processo exergónico) permite o bombeamento de protões contragradiente (processo endergónico). 9- As atividades catalíticas da desidrogénase do succinato e da desidrogénase do glicerol-3-fosfato da membrana mitocondrial interna A desidrogénase do succinato é a única enzima do ciclo de Krebs que não está situada na matriz, mas sim na face interna da membrana interna da mitocôndria. Esta enzima contém, como grupos prostéticos, FAD (que é o aceitador primário dos eletrões) e complexos ferro-enxofre e também é designada por complexo II. Dois eletrões do succinato são transferidos para a coenzima Q e não existe, neste caso, transporte acoplado de protões (ver Equação 8). Existem outras enzimas que, tal como o complexo II, também catalisam a redução da coenzima Q pelos respetivos substratos e que também não são bombas de protões. Uma delas é uma desidrogénase do 4 XH2 pode ser, por exemplo, o piruvato, o isocitrato, o α-cetoglutarato e o malato. Nestes casos X seria, respetivamente, o acetil-coa, o α-cetoglutarato, o succinil-coa e o oxalacetato. Página 4 de 11
5 glicerol-3-fosfato que também contém FAD (que é o aceitador primário dos eletrões) como grupo prostético e que se situa na face externa da membrana interna da mitocôndria (ver Equação 9) 5. Equação 8 Equação 9 succinato + Q fumarato + QH2 glicerol-3-fosfato + Q dihidroxiacetona-fosfato + QH2 10- A transferência de um par de eletrões entre o succinato (ou o glicerol-3-fosfato) e o O 2 está acoplado com o bombeamento de 6 protões A oxidação do QH2 (ubiquinol) pelo oxigénio envolve, como já referido, os complexos III e IV que, de forma acoplada, catalisam também o bombeamento de protões. O facto de a oxidação do succinato (e do glicerol-3-fosfato) pelo oxigénio não envolver o complexo I explica que, nestes casos, apenas 6 protões sejam bombeados para o citoplasma (ver Equação 3 e Equação 4 e a respetiva Equação soma, a Equação 10). Nas ações sequenciadas dos complexos III e IV há 6 protões que desaparecem da matriz enquanto 6 protões aparecem no citoplasma. Equação 10 QH2 + ½ O 2 + 6H + (dentro) Q + H 2O + 6 H + (fora) 11- As atividades catalítica e de transporte de protões da síntase de ATP Criado o gradiente eletroquímico acima referido, os protões têm tendência a passar do citoplasma para a matriz mitocondrial e esta tendência é às vezes designada de força protomotriz. No entanto, apesar da pequenez da partícula, o processo de entrada de protões para a matriz não ocorre por difusão simples: a carga positiva dos protões impede a sua dissolução nos lipídeos da membrana. Existem proteínas da membrana mitocondrial interna que permitem a entrada de protões acoplando este movimento (a favor de gradiente eletroquímico) com processos reativos que, tendo em conta a razão Keq/QR, não poderiam ocorrer na célula na ausência dessa acoplagem. O mais importante (mas não o único) destes processos é a síntese de ATP que é catalisada pela síntase do ATP (também designada de complexo V). No atual estádio do conhecimento, uma aproximação aceitável para a estequiometria do processo de acoplagem entre o transporte de protões (processo exergónico) e a síntese de ATP na síntase do ATP (processo endergónico) poderá ser 3 protões por ATP [1]; assim, a equação que descreve o processo pode ser escrita como mostra a Equação 11. É de notar que a síntase do ATP é uma hidrólase que opera em sentido inverso ao das outras hidrólases; isto é, na reação catalisada pela síntase do ATP há libertação de H 2O enquanto se unem dois compostos. Isto só é possível porque o processo reativo (que é endergónico) está acoplado com a entrada de protões a favor do gradiente eletroquímico (que é exergónico). Equação 11 ADP + Pi + 3 H + (fora) ATP + H 2O + 3 H + (dentro) Os processos de transporte transmembrar de ATP, ADP e Pi também envolvem gasto da energia associada ao gradiente eletroquímico O ATP gerado na matriz da mitocôndria é, na sua maior parte, hidrolisado no citoplasma da célula e é, portanto, também no citoplasma que se gera a maior parte do ADP e o do Pi. Por exemplo, é na face citoplasmática da membrana citoplasmática que ocorre a hidrólise do ATP catalisada pela bomba de Na + /K + e é também no citoplasma que ocorre a hidrólise do ATP aquando da contração muscular. O transporte de ADP (para dentro da mitocôndria) e de ATP (para fora da mitocôndria) ocorrem por ação de um transportador da membrana interna da mitocôndria que é um antiporter que é frequentemente designado por trocador ATP/ADP (ver Equação 12). O transporte de ADP 3- (para dentro) e de ATP 4- (para fora) 5 Para além desta, existe uma outra desidrogénase do glicerol-3-fosfato a que faremos referência neste texto (ver Equação 17). 6 Porque a troca ADP/ATP (ver ponto 10) é um processo que envolve gasto do gradiente elétrico a razão entre as concentrações de ADP e ATP é maior na mitocôndria que no citoplasma ([ADP] dentro/[atp] dentro > [ADP] fora/[atp] fora). Esta razão favorece a síntese de ATP na mitocôndria (ver Equação 11), ou seja, a energia de Gibbs necessária para a síntese de um mole de ATP na mitocôndria é menor que a que se liberta aquando da hidrólise de ATP no citoplasma. De qualquer forma, mesmo que usemos o valor de 50 kj/mole para a síntese de ATP (o habitualmente utilizado quando se pensa nas condições citoplasmáticas) a energia libertada aquando da entrada de 3 protões é superior à energia utilizada na síntese de 1 mole de ATP (3 18 kj /mole de protões que entra > 50 kj /mole de ATP sintetizado). Ou seja, entendido como um todo o processo global catalisado pela síntase de ATP tem, como não podia deixar de ser, G negativo; o processo exergónico (neste caso a entrada de 3 protões) é mais negativo (-54 kj) que a reação inversa à de hidrólise do ATP (+50 kj). Página 5 de 11
6 corresponde à saída de uma carga negativa e envolve, por isso, consumo de energia do gradiente elétrico criado pela cadeia respiratória (ver nota de rodapé nº 6). O transporte de Pi (para dentro da mitocôndria) é mediado por um simporter sendo o Pi cotransportado com um protão (a favor do gradiente químico; ver Equação 13) e, neste caso, o transporte envolve consumo de energia do gradiente químico criado pela cadeia respiratória. Equação 12 Equação 13 ADP 3- (fora) + ATP 4- (dentro) ADP 3- (dentro) + ATP 4- (fora) Pi + H + (fora) Pi + H + (dentro) Assim, o processo de transporte de 1 Pi e 1 ADP do citoplasma para a matriz da mitocôndria (e a saída de 1 ATP) implica a entrada de 1 protão e envolve gasto do gradiente eletroquímico formado pela atividade dos complexos I, III e IV. Aquando da síntese intramitocondrial de 1 molécula de ATP a nível do substrato (ação da sintétase de succinil-coa), o número de protões que tem de passar do citoplasma para a matriz é 1; na ação da sintétase de succinil-coa consome-se um Pi (ver Equação 14). Este Pi é indispensável para a síntese de ATP intramitocondrial e é cotransportado com um protão para dentro da mitocôndria por ação do transportador de Pi (ver Equação 13). Equação 14 succinil-coa + ADP (ou GDP) + Pi succinato + CoA + ATP (ou GTP) No entanto, no caso de a síntese de ATP envolver a síntase do ATP, o número de protões que entram para a mitocôndria para que 1 ATP possa ser sintetizados será de 4 (= 3+1; 3 que entram na atividade de transporte da síntase do ATP e 1 que entra com o Pi; ver Equação 11 e Equação 13). 13- A razão P:O A razão entre o número de ATPs formados e o número de átomos de oxigénio que são reduzidos na cadeia respiratória designa-se de razão P:O. Durante muitos anos admitiu-se que o valor desta razão era 3 quando o composto oxidado era o NADH e que era 2 quando o processo oxidativo não envolvia o complexo I. No entanto, com os dados que temos vindo a apresentar, podemos calcular valores diferentes para a razão P:O. Se, durante a oxidação de um NADH por um átomo de oxigénio, 10 protões são transportados para o citoplasma e têm de regressar 4 para que se forme 1 ATP, então a saída de 10 protões sustenta a síntese de 2,5 ATPs: quando o complexo I está envolvido a razão P:O seria, assim, 2,5. Um raciocínio semelhante leva-nos à conclusão que, no caso de não estar envolvido o complexo I, a razão P:O é de 1,5. Estes valores são semelhantes às médias obtidas experimentalmente com mitocôndrias isoladas e são também apontados em alguns livros de texto [2, 3]. 14- O ADP como fator estimulador da síntase do ATP e da atividade da cadeia respiratória Todos os processos atrás referidos tais como a hidrólise de ATP, o transporte transmembranar de ADP/ATP, a síntese de ATP e o transporte de protões para a matriz, o transporte de protões para o citoplasma e o conjunto de oxidações e reduções da cadeia respiratória assim como as vias metabólicas em que o NAD + ou o FAD se reduzem estão intimamente relacionados. Quando a velocidade de hidrólise de ATP aumenta (exercício físico, por exemplo) a sua velocidade de síntese também aumenta de tal modo que a sua concentração se mantém estacionária. Ou seja, quando a velocidade de hidrólise de ATP aumenta também aumenta a velocidade de oxidação de nutrientes e do consumo de oxigénio na cadeia respiratória. A ativação da cadeia respiratória quando há aumento da hidrólise de ATP é, em parte, uma consequência de uma cadeia de fenómenos originados pelo aumento da síntese de ADP e Pi no citoplasma. O aumento da concentração de ADP e Pi estimularia (i) a velocidade de troca ADP/ATP na membrana da mitocôndria (antiporter) e a entrada de Pi (simporter) que estimularia (ii) a velocidade de síntese de ATP e de entrada de protões para a matriz (síntase de ATP) que estimularia (iii) a velocidade de consumo de O 2 e a velocidade de saída dos protões para o citoplasma (cadeia respiratória). Ao ativar diretamente a síntase do ATP, o ADP esbate o gradiente eletroquímico da membrana (ver Equação 11) diminuindo o peso do componente endergónico na atividade dos complexos I, III e IV (ver Equação 5). O aumento da concentração de ADP (e o consequente aumento na concentração de AMP, via ação catalítica da cínase do adenilato; ver Equação 15) também estimula enzimas chave do ciclo de Krebs e da glicólise estimulando a oxidação dos nutrientes. Página 6 de 11
7 Equação 15 2 ADP ATP + AMP 15- O ião Ca 2+ como fator estimulador da síntase do ATP e da atividade dos complexos I e IV Um outro fator envolvido na regulação da atividade da cadeia respiratória poderá ser o ião Ca 2+ cuja concentração aumenta dentro da mitocôndria quando as células são estimuladas (por exemplo, estimulação do músculo pelo nervo motor). É o aumento da concentração de Ca 2+ que induz o músculo a contrair-se e a hidrolisar ATP, mas o Ca 2+ também ativa os complexos I e IV e a síntase do ATP, promovendo paralelamente a síntese de ATP [4-6]. 16- O papel da cínase da creatina na manutenção da concentração de ATP nos músculos Nos músculos a distância entre o espaço intermembranar das mitocôndrias (para onde, por ação do trocador ATP/ADP, o ATP é vertido e de onde o ADP é captado) e as miofibrilas (onde maioritariamente ocorre a hidrólise do ATP e a formação do ADP) é, tendo em conta a velocidade de difusão do ATP e do ADP, demasiado grande. Contudo, no caso da fosfocreatina e da creatina (que existem no músculo em concentrações muito mais elevadas que as de ATP e ADP) a velocidade de difusão é muito superior. No espaço intermembranar, a cínase da creatina catalisa a fosforilação da creatina sendo o ATP o dador do fosfato (ver Equação 16). À semelhança do ATP, a fosfocreatina também contém uma ligação rica em energia (no caso é uma ligação fosfamida) e a fosfocreatina formada difunde através da porina para o citoplasma. Junto das miofibrilas também existe cínase de creatina mas, neste local, a razão Keq/QR favorece a reação inversa: a fosforilação do ADP pela fosfocreatina (ver Equação 16). A creatina formada difunde da vizinhança das miofibrilas para o espaço intermembranar completando o ciclo. Para além deste papel no transporte de ligações ricas em energia a fosfocreatina também tem um papel na manutenção da concentração estacionária de ATP no músculo. Quando a velocidade de hidrólise do ATP acelera aquando do início da atividade contráctil, o mais rápido sistema de resposta na manutenção da concentração de ATP é o sistema fosfocreatina/creatina. Imediatamente após o início da contração, a atividade da cínase da creatina junto das miofibrilas aumenta fazendo com que a razão fosfocreatina/creatina baixe, mas a concentração de ATP mantém-se praticamente inalterada (ver Equação 16). Equação 16 creatina + ATP fosfocreatina + ADP 17- Inibidores dos complexos da cadeia respiratória É fácil de compreender que substâncias (como por exemplo a rotenona) capazes de bloquear a transferência de eletrões do NADH para a coenzima Q (inibidores do complexo I) impeçam a oxidação dos nutrientes e a síntese de ATP. Adicionada a uma preparação isolada de mitocôndrias a rotenona impede a oxidação do piruvato mas não a de succinato ou de glicerol-3-fosfato. Outras substâncias (como a antimicina A e o cianeto) que bloqueiam a cadeia respiratória num local a jusante da coenzima Q impedem a oxidação do piruvato, do succinato e do glicerol-3-fosfato. O cianeto é um veneno que provoca morte fulminante: ao ligar-se ao complexo IV impedindo a oxidação dos nutrientes (e a redução do O 2), impede a síntese de ATP. Em condições basais todo o ATP da célula se esgota em menos de 3 minutos e muito antes de se esgotar já pararam todos os processos que dependem do ATP como as atividades das bombas de Na + /K + e de Ca 2+ e a de contração muscular (como a do coração e diafragma). 18- Inibição da síntase do ATP e do trocador ATP/ADP A oligomicina e o atractilosídeo são substâncias usadas em trabalhos experimentais sobre fosforilação oxidativa. A oligomicina liga-se à subunidade Fo da síntase do ATP bloqueando a transferência de protões através da síntase. O atractilosídeo liga-se ao antiporter ADP/ATP impedindo a sua ação (ver Equação 12). Tendo um efeito direto nestes locais, a oligomicina e o atractilosídeo, quando adicionados a preparações de mitocôndrias isoladas, bloqueiam indiretamente a cadeia respiratória. A oligomicina ao impedir o regresso dos protões à matriz faz com que os processos de reação/transporte catalisados pela cadeia respiratória (ver Equação 5) atinjam um estado de equilíbrio parando os processos envolvidos. Ou dito de outra maneira, à medida que, por ação da oligomicina, os protões se vão acumulando no citoplasma mais difícil é a tarefa de bombear protões nos complexos I, III e IV. Porque os processos oxidativos estão acoplados com o de transporte de protões, também a oxidação dos nutrientes fica bloqueada. Página 7 de 11
8 Na presença de atractilosídeo o ATP acumula-se na matriz, o ADP não pode entrar e sem ADP dentro da mitocôndria não há síntese de ATP. Porque o processo de transporte de protões está acoplado com o da síntese de ATP (ver Equação 11), o efeito final do atractilosídeo acaba por ser idêntico ao da oligomicina. 19- Desacoplagem entre fosforilação e oxidação por ação do dinitrofenol O dinitrofenol é uma substância que, adicionada a uma preparação de mitocôndrias isoladas, permite a oxidação dos nutrientes adicionados ao sistema (piruvato ou succinato) na presença de oligomicina ou atractilosídeo porque permite a passagem de protões para a matriz (a favor do gradiente) através de um mecanismo independente da síntase do ATP. O dinitrofenol é um desacoplador da fosforilação oxidativa porque permite que a cadeia respiratória funcione e a oxidação dos nutrientes tenha lugar na ausência de fosforilação do ADP. A intoxicação com dinitrofenol provoca febre altíssima (podendo chegar aos 46ºC) e a morte [7]. A entrada de protões diminui (pelo menos transitoriamente) o gradiente eletroquímico da membrana da mitocôndria o que ativa os complexos da cadeia respiratória. Por outro lado, sem síntese de ATP são ativadas as enzimas que são inibidas pelo ATP e estimuladas pelo ADP (como a cínase da frutose-6-fosfato, a desidrogénase do piruvato, a síntase do citrato e as desidrogénases do isocitrato e do α-cetoglutarato) e ambos os processos contribuem para o aumento da velocidade de oxidação dos nutrientes. A febre é uma consequência do aumento da velocidade de oxidação dos nutrientes que é um processo exotérmico. A morte sobrevém porque deixa de haver síntese de ATP (ou/e porque a temperatura é demasiado elevada para que se mantenham funcionando de forma adequada os sistemas próprios de um organismo vivo). 20- A atividade das UCPs (proteínas de desacoplamento) Na membrana interna das mitocôndrias do tecido adiposo castanho dos bebés humanos existe uma proteína (termogenina ou Uncoupling Protein 1 UCP1) que têm um papel semelhante ao do dinitrofenol e permite dissociar a oxidação dos nutrientes do consumo (e da síntese) de ATP. A designação de termogenina tem origem no facto de a ativação da termogenina que ocorre como resposta ao frio (via hormonas tiroideias e sistema nervoso simpático) permitir a produção de calor de forma desproporcional ao gasto de ligações ricas em energia do ATP. Até há poucos anos pensava-se que, nos seres humanos adultos, o tecido adiposo castanho era praticamente inexistente, mas dados experimentais mais recentes têm desafiado esta ideia [8-11]. O aumento do metabolismo que ocorre como resposta ao frio ou nas situações em que as hormonas tiroideias estão aumentadas (quer situações patológicas, quer fisiológicas) implica ativação da UCP1 via ativação do sistema nervoso simpático [9-11]. Para além da UCP1 do tecido adiposo castanho, na membrana interna das mitocôndrias dos músculos e de outros órgãos existem proteínas que funcionam de forma semelhante à UCP1, mas cujo papel fisiológico é ainda controverso: são a UCP2 e a UCP3. À semelhança do que acontece com a UCP1 as atividades da UCP2 e da UCP3 são estimuladas pelas hormonas tiroideias e pelo sistema nervoso simpático, mas não parecem participar na resposta fisiológica ao frio [1, 12, 13]. A ativação das UCPs pelas hormonas tiroideias permite explicar porque é que no hipertiroidismo a temperatura corporal está cronicamente aumentada (e diminuída no hipotiroidismo). A temperatura corporal também aumenta quando há estimulação do sistema nervoso simpático; pensa-se que a febre (e a morte) que ocorre na intoxicação com ectasy (3,4-dimetilenedioximetanfetamina) resulta da hiperestimulação do sistema simpático e do consequente aumento de atividade da UCP3 [13]. Associada à atividade das UCPs está a palavra leak ( pingar ): as UCPs deixam pingar para dentro das mitocôndrias protões que, de outra forma, só poderiam entrar para a matriz via síntase do ATP As lançadeiras permitem transferir eletrões do NADH citoplasmático para a cadeia respiratória; a lançadeira do glicerol-3-fosfato O complexo I (ver Equação 2) tem o seu centro ativo voltado para a matriz da mitocôndria e não existe nenhum sistema de transporte para o NADH na membrana mitocondrial interna. A oxidação do NADH formado no citoplasma durante a glicólise é mediada por sistemas chamados lançadeiras (ou shuttles) que permitem oxidar o NADH citosólico e apresentar os equivalentes redutores ao sistema dos complexos proteicos da membrana interna da mitocôndria. 7 Esta frase não é completamente verdadeira pois sabe-se que existe leak de protões por outros mecanismos que não os descritos acima, mas o seu papel fisiológico e as proteínas que os medeiam são ainda desconhecidos. Página 8 de 11
9 Existem duas lançadeiras designadas de lançadeira do glicerol-3-fosfato e lançadeira do malato. A mais simples é a lançadeira do glicerol-3-fosfato. Esta lançadeira é mais importante no cérebro e tecido muscular esquelético, implica a redução pelo NADH da dihidroxiacetona-fosfato do citoplasma e a consequente formação de glicerol-3-fosfato; a enzima que catalisa esta reação é uma desidrogénase do glicerol-3-fosfato presente no citoplasma que usa o NADH como redutor (ver Equação 17). O glicerol-3- fosfato formado transfere os eletrões para a coenzima Q através da ação catalítica doutra desidrogénase do glicerol-3-fosfato presente na face externa da membrana interna da mitocôndria a que já fizemos referência (ver Equação 9). Equação 17 dihidroxiacetona-fosfato + NADH glicerol-3-fosfato + NAD + As desidrogénases do glicerol-3-fosfato do citoplasma (dependente do NADH) e a da face externa da membrana interna da mitocôndria (que tem como grupo prostético o FAD) são isoenzimas 8. O somatório da ação sequenciada destas duas desidrogénase é a Equação 18. Equação 18 NADH (citoplasma) + Q (membrana mitocondrial interna) NAD + (citoplasma) + QH2 (membrana mitocondrial interna) 22- A lançadeira do malato é muito mais complexa que a lançadeira do glicerol-3-fosfato A lançadeira do malato é mais importante no fígado, rim e coração e envolve atividades enzímicas intra e extramitocondriais assim como a ação de transportadores da membrana mitocondrial interna. Em última análise essas enzimas e transportadores vão permitir que uma molécula de NADH presente no citoplasma transfira dois eletrões para uma molécula de NAD + que está na matriz mitocondrial de forma a formar NADH que possa interagir com o centro ativo do complexo I. Num primeiro passo, por ação catalítica da desidrogénase do malato, o NADH citoplasmático reduz o oxalacetato a malato (ver Equação 19). De seguida, o malato entra para a matriz mitocondrial (trocando com α-cetoglutarato) e, por ação da mesma enzima, vai reduzir NAD + da matriz a NADH. Desta maneira os equivalentes redutores do NADH formado no citoplasma são transferidos (via malato) para a matriz e o NADH formado na matriz pode ser oxidado por ação sequenciada dos complexos I, III e IV. Equação 19 oxalacetato + NADH malato + NAD + Obviamente que um sistema como o descrito até aqui não poderia funcionar porque levaria ao consumo contínuo do oxalacetato citoplasmático e ao acumular de oxalacetato na mitocôndria. De facto, para compreender o processo, temos de fechar o ciclo e entender que o oxalacetato, de alguma forma, regressa ao citoplasma. Não existe transportador para o oxalacetato na membrana interna das mitocôndrias e o processo é complexo (ver Fig. 1). Dentro da matriz, o oxalacetato mitocondrial converte-se em aspartato por ação da transamínase do aspartato (Equação 20) e este aspartato regressa ao citoplasma onde, por ação da mesma transamínase (catalisando a reação inversa), volta a converter-se em oxalacetato. Nestas reações de transaminação o glutamato é consumido na matriz e forma-se no citoplasma acontecendo o contrário no caso do α- cetoglutarato. Um transportador da membrana (um antiporte que troca o aspartato que sai por glutamato que entra) catalisa a entrada do glutamato para a matriz impedindo que este se acumule no citoplasma e se esgote na matriz. O α-cetoglutarato também não se acumula na matriz porque um outro transportador da membrana (um antiporte que troca α-cetoglutarato que sai pelo malato que entra) catalisa a sua saída para o citoplasma. Equação 20 oxalacetato + glutamato aspartato + α-cetoglutarato 23- O número de moléculas de ATP que se podem formar aquando da oxidação completa de uma molécula de glicose Os valores de 2,5 e 1,5 (referidos acima como as razões P:O quando, respetivamente, estão envolvidas os complexos I, III e IV ou apenas os complexos III e IV) seriam os valores máximos para a razão P:O: obviamente que a atividade das UCPs (e de outros processos que não abordámos) fará baixar a 8 É de sublinhar que embora a desidrogénase do glicerol-3-p da membrana mitocondrial externa contenha FAD não é o complexo II: o complexo II é uma enzima da face interna da membrana interna da mitocôndria que também se pode designar por desidrogénase do succinato. Página 9 de 11
10 razão P:O para valores mais baixos [1, 12]. Se houver acoplamento perfeito entre oxidação e fosforilação, a razão P:O é 2,5 quando o redutor da ubiquinona é o NADH (via complexo I) e é 1,5 quando é o FADH2 (via desidrogénases do succinato ou do glicerol-3-fosfato). Admitindo estes números e o funcionamento predominante da lançadeira do glicerol-3-fosfato (como acontece, por exemplo, no músculo esquelético e no cérebro) a oxidação completa de uma molécula de glicose poderia render algo como 30 ligações ricas em energia do ATP 9 (ver Equação 21) Admitindo a ação predominante da lançadeira do malato, a oxidação completa de uma molécula de glicose poderia render 32 ligações ricas em energia do ATP (ver Equação 22). Equação 21 Equação 22 glicose + 6 O ADP + 30 Pi 6 CO ATP + 36 H 2O glicose + 6 O ADP + 32 Pi 6 CO ATP + 38 H 2O 1. Brand, M. D. (2005) The efficiency and plasticity of mitochondrial energy transduction, Biochem Soc Trans. 33, Hinkle, P. C., Kumar, M. A., Resetar, A. & Harris, D. L. (1991) Mechanistic stoichiometry of mitochondrial oxidative phosphorylation, Biochemistry. 30, Nelson, D. L. & Cox, M. M. (2013) Lehninger Principles of Biochemistry, sixth edition edn, W. H. Freeman and Company, New York. 4. Balaban, R. S. (2002) Cardiac energy metabolism homeostasis: role of cytosolic calcium, J Mol Cell Cardiol. 34, Kadenbach, B., Ramzan, R., Wen, L. & Vogt, S. (2010) New extension of the Mitchell Theory for oxidative phosphorylation in mitochondria of living organisms, Biochim Biophys Acta. 1800, Korzeniewski, B. (2006) Oxygen consumption and metabolite concentrations during transitions between different work intensities in heart, Am J Physiol Heart Circ Physiol. 291, H Mills, E. M., Rusyniak, D. E. & Sprague, J. E. (2004) The role of the sympathetic nervous system and uncoupling proteins in the thermogenesis induced by 3,4-methylenedioxymethamphetamine, J Mol Med. 82, Nedergaard, J., Bengtsson, T. & Cannon, B. (2007) Unexpected evidence for active brown adipose tissue in adult humans, Am J Physiol Endocrinol Metab. 293, E Cannon, B. & Nedergaard, J. (2010) Thyroid hormones: igniting brown fat via the brain, Nat Med. 16, Zingaretti, M. C., Crosta, F., Vitali, A., Guerrieri, M., Frontini, A., Cannon, B., Nedergaard, J. & Cinti, S. (2009) The presence of UCP1 demonstrates that metabolically active adipose tissue in the neck of adult humans truly represents brown adipose tissue, Faseb J. 23, Lopez, M., Varela, L., Vazquez, M. J., Rodriguez-Cuenca, S., Gonzalez, C. R., Velagapudi, V. R., Morgan, D. A., Schoenmakers, E., Agassandian, K., Lage, R., de Morentin, P. B., Tovar, S., Nogueiras, R., Carling, D., Lelliott, C., Gallego, R., Oresic, M., Chatterjee, K., Saha, A. K., Rahmouni, K., Dieguez, C. & Vidal-Puig, A. (2010) Hypothalamic AMPK and fatty acid metabolism mediate thyroid regulation of energy balance, Nat Med. 16, Kadenbach, B. (2003) Intrinsic and extrinsic uncoupling of oxidative phosphorylation, Biochim Biophys Acta. 1604, Sprague, J. E., Yang, X., Sommers, J., Gilman, T. L. & Mills, E. M. (2007) Roles of norepinephrine, free Fatty acids, thyroid status, and skeletal muscle uncoupling protein 3 expression in sympathomimetic-induced thermogenesis, J Pharmacol Exp Ther. 320, Este resultado resulta do seguinte cálculo: ATPs formados a nível do substrato (4; 2 na glicólise + 2 via sintétase do succinil-coa/cínase dos nucleosídeos difosfato) + ATPs formados via lançadeira do glicerol-3-p (1,5 2 = 3) + ATPs formados via oxidação do succinato (1,5 2 = 3) + ATPs formados via oxidação do NADH mitocondrial (4 2 2,5 = 20). As enzimas diretamente envolvidas na formação do NADH mitocondrial são as desidrogénases do piruvato, do isocitrato, do α-cetoglutarato e do malato. Página 10 de 11
11 Fig. 1: A lançadeira do malato envolve as atividades da desidrogénase do malato, da transamínase do aspartato e de dois transportadores, os antiportes malato/α-cetoglutarato e aspartato/glutamato. Fig 2: O papel das enzimas do ciclo de Krebs e da fosforilação oxidativa na oxidação completa do glutamato: glutamato + 4,5 O ,5 ADP + 22,5 Pi 5 CO 2 + NH ,5 ATP. Admitimos que à oxidação de uma molécula de NADH corresponde a formação de 2,5 ATP e que, à oxidação de uma molécula de succinato, 1,5 ATP. Também admitimos a ação da cínase de nucleosídeos difosfato e que, portanto, um GTP equivale um ATP Página 11 de 11
Fosforilação oxidativa
 Fosforilação oxidativa 1- A maior parte do ATP formado durante a oxidação dos nutrientes ocorre nas mitocôndrias que contém duas membranas: uma externa e outra interna. A membrana externa, porque contém
Fosforilação oxidativa 1- A maior parte do ATP formado durante a oxidação dos nutrientes ocorre nas mitocôndrias que contém duas membranas: uma externa e outra interna. A membrana externa, porque contém
Fosforilação oxidativa
 Fosforilação oxidativa 1- A maior parte do ATP formado durante a oxidação dos nutrientes ocorre nas mitocôndrias que contém duas membranas: uma externa e outra interna. A membrana externa, porque contém
Fosforilação oxidativa 1- A maior parte do ATP formado durante a oxidação dos nutrientes ocorre nas mitocôndrias que contém duas membranas: uma externa e outra interna. A membrana externa, porque contém
Fosforilação oxidativa
 Fosforilação oxidativa 1- A maior parte do ATP formado durante a oxidação dos nutrientes ocorre nas mitocôndrias que contêm duas membranas: uma externa e outra interna. A membrana externa, porque contém
Fosforilação oxidativa 1- A maior parte do ATP formado durante a oxidação dos nutrientes ocorre nas mitocôndrias que contêm duas membranas: uma externa e outra interna. A membrana externa, porque contém
Fosforilação oxidativa
 Fosforilação oxidativa Fosforilação oxidativa; Rui Fontes Índice 1- Aspetos da estrutura das mitocôndrias com relevância na compreensão do processo de fosforilação oxidativa... 1 2- O papel das oxiredútases
Fosforilação oxidativa Fosforilação oxidativa; Rui Fontes Índice 1- Aspetos da estrutura das mitocôndrias com relevância na compreensão do processo de fosforilação oxidativa... 1 2- O papel das oxiredútases
Fosforilação oxidativa
 Fosforilação oxidativa Fosforilação oxidativa; Rui Fontes 1- A maior parte do ATP formado durante a oxidação dos nutrientes ocorre nas mitocôndrias que contém duas membranas: uma externa e outra interna.
Fosforilação oxidativa Fosforilação oxidativa; Rui Fontes 1- A maior parte do ATP formado durante a oxidação dos nutrientes ocorre nas mitocôndrias que contém duas membranas: uma externa e outra interna.
Fosforilação oxidativa
 Fosforilação oxidativa Fosforilação oxidativa; Rui Fontes 1- A maior parte do ATP formado durante a oxidação dos nutrientes ocorre nas mitocôndrias que contém duas membranas: uma externa e outra interna.
Fosforilação oxidativa Fosforilação oxidativa; Rui Fontes 1- A maior parte do ATP formado durante a oxidação dos nutrientes ocorre nas mitocôndrias que contém duas membranas: uma externa e outra interna.
CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA COMO AS CÉLULAS SINTETIZAM ATP
 CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA OU COMO AS CÉLULAS SINTETIZAM ATP SINTETIZAM ATP ÀS CUSTAS DA OXIDAÇÃO DAS COENZIMAS NADH E FADH 2 PELO OXIGÊNIO AS COENZIMAS REDUZIDAS SÃO PRODUZIDAS
CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA OU COMO AS CÉLULAS SINTETIZAM ATP SINTETIZAM ATP ÀS CUSTAS DA OXIDAÇÃO DAS COENZIMAS NADH E FADH 2 PELO OXIGÊNIO AS COENZIMAS REDUZIDAS SÃO PRODUZIDAS
CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA COMO AS CÉLULAS SINTETIZAM ATP
 CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA OU COMO AS CÉLULAS SINTETIZAM ATP SINTETIZAM ATP ÀS CUSTAS DA OXIDAÇÃO DAS COENZIMAS NADH E FADH 2 PELO OXIGÊNIO AS COENZIMAS REDUZIDAS SÃO PRODUZIDAS
CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA OU COMO AS CÉLULAS SINTETIZAM ATP SINTETIZAM ATP ÀS CUSTAS DA OXIDAÇÃO DAS COENZIMAS NADH E FADH 2 PELO OXIGÊNIO AS COENZIMAS REDUZIDAS SÃO PRODUZIDAS
Rui Fontes. O sentido das reacções de oxi-redução e a fosforilação oxidativa
 Rui Fontes O sentido das reacções de oxi-redução e a fosforilação oxidativa Porto 2005 Índice 1. As tabelas de potencial redox dos bioquímicos não são iguais às dos químicos porque são diferentes as condições
Rui Fontes O sentido das reacções de oxi-redução e a fosforilação oxidativa Porto 2005 Índice 1. As tabelas de potencial redox dos bioquímicos não são iguais às dos químicos porque são diferentes as condições
C 6 H 12 O O 2 6 CO H 2 O
 O que os seres vivos sabem fazer melhor é comer ingerir substâncias no estado reduzido que vão ser oxidadas a e respirar inspirar O 2, o oxidante último dos nutrientes e expirar o produto da oxidação dos
O que os seres vivos sabem fazer melhor é comer ingerir substâncias no estado reduzido que vão ser oxidadas a e respirar inspirar O 2, o oxidante último dos nutrientes e expirar o produto da oxidação dos
A mitocôndria oxida combustíveis para gerar energia, em analogia ao processo pelo qual as usinas de força utilizam os combustíveis para gerar energia
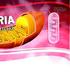 A mitocôndria oxida combustíveis para gerar energia, em analogia ao processo pelo qual as usinas de força utilizam os combustíveis para gerar energia elétrica Micrografia eletrônica de uma mitocôndria
A mitocôndria oxida combustíveis para gerar energia, em analogia ao processo pelo qual as usinas de força utilizam os combustíveis para gerar energia elétrica Micrografia eletrônica de uma mitocôndria
Cadeia de transporte de elétrons e fosforilação oxidativa
 Cadeia de transporte de elétrons e fosforilação oxidativa MAPA II POLISSACARÍDIOS PROTEÍNAS LIPÍDIOS GLICOSE AMINOÁCIDOS ÁCIDOS GRAXOS Fosfoenolpiruvato (3) Asp Gly Ala Ser Cys Leu Ile Lys Phe Glu Piruvato
Cadeia de transporte de elétrons e fosforilação oxidativa MAPA II POLISSACARÍDIOS PROTEÍNAS LIPÍDIOS GLICOSE AMINOÁCIDOS ÁCIDOS GRAXOS Fosfoenolpiruvato (3) Asp Gly Ala Ser Cys Leu Ile Lys Phe Glu Piruvato
CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA COMO AS CÉLULAS SINTETIZAM ATP
 CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA OU COMO AS CÉLULAS SINTETIZAM ATP SINTETIZAM ATP ÀS CUSTAS DA OXIDAÇÃO DAS COENZIMAS NADH E FADH 2 PELO OXIGÊNIO AS COENZIMAS REDUZIDAS SÃO PRODUZIDAS
CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA OU COMO AS CÉLULAS SINTETIZAM ATP SINTETIZAM ATP ÀS CUSTAS DA OXIDAÇÃO DAS COENZIMAS NADH E FADH 2 PELO OXIGÊNIO AS COENZIMAS REDUZIDAS SÃO PRODUZIDAS
Obtenção de Energia. Obtenção de Energia. Obtenção de Energia. Oxidação de Carboidratos. Obtenção de energia por oxidação 19/08/2014
 , Cadeia de Transporte de Elétrons e Fosforilação Oxidativa Prof. Dr. Bruno Lazzari de Lima Para que um organismo possa realizar suas funções básicas: Obtenção de nutrientes. Crescimento. Multiplicação.
, Cadeia de Transporte de Elétrons e Fosforilação Oxidativa Prof. Dr. Bruno Lazzari de Lima Para que um organismo possa realizar suas funções básicas: Obtenção de nutrientes. Crescimento. Multiplicação.
Anderson Guarise Cristina Haas Fernando Oliveira Leonardo M de Castro Sergio Vargas Júnior
 Anderson Guarise Cristina Haas Fernando Oliveira Leonardo M de Castro Sergio Vargas Júnior Respiração Celular Glicólise Ciclo do Ácido Cítrico (CAC) Fosforilação oxidativa (Fox) Respiração Celular Glicólise
Anderson Guarise Cristina Haas Fernando Oliveira Leonardo M de Castro Sergio Vargas Júnior Respiração Celular Glicólise Ciclo do Ácido Cítrico (CAC) Fosforilação oxidativa (Fox) Respiração Celular Glicólise
Universidade Federal do Pampa Campus Itaqui Bioquímica GLICÓLISE AERÓBICA. Ciclo de Krebs e Fosforilação Oxidativa. Profa.
 Universidade Federal do Pampa Campus Itaqui Bioquímica GLICÓLISE AERÓBICA Ciclo de Krebs e Fosforilação Oxidativa Profa. Marina Prigol 1 Glicólise Anaeróbica RESPIRAÇÃO CELULAR ou GLICÓLISE AERÓBICA:
Universidade Federal do Pampa Campus Itaqui Bioquímica GLICÓLISE AERÓBICA Ciclo de Krebs e Fosforilação Oxidativa Profa. Marina Prigol 1 Glicólise Anaeróbica RESPIRAÇÃO CELULAR ou GLICÓLISE AERÓBICA:
Acetil CoA e Ciclo de Krebs. Prof. Henning Ulrich
 Acetil CoA e Ciclo de Krebs Prof. Henning Ulrich Glicose + Consumo de 2 ATP 2 Ácidos Pirúvicos + 4H + + Produção de 4 ATP (2C 3 H 4 O 3 ) 2H + são Transportados pelo NAD passando Para o estado reduzido
Acetil CoA e Ciclo de Krebs Prof. Henning Ulrich Glicose + Consumo de 2 ATP 2 Ácidos Pirúvicos + 4H + + Produção de 4 ATP (2C 3 H 4 O 3 ) 2H + são Transportados pelo NAD passando Para o estado reduzido
Glicose / carboidratos Ácidos graxos Aminoácidos. Acetil-CoA. Ciclo de Krebs (NADH e FADH 2 )
 A fosforilação oxidativa (FO) é o estágio final do metabolismo produtor de energia nos organismos aeróbicos Nessa etapa toda a energia produzida (na forma de carreadores de elétrons) durante a oxidação
A fosforilação oxidativa (FO) é o estágio final do metabolismo produtor de energia nos organismos aeróbicos Nessa etapa toda a energia produzida (na forma de carreadores de elétrons) durante a oxidação
1. Produção de Acetil-CoA. 2. Oxidação de Acetil-CoA. 3. Transferência de elétrons e fosforilação oxidativa
 CICLO DE KREBS OU DO ÁCIDO CÍTRICO 1. Produção de Acetil-CoA 2. Oxidação de Acetil-CoA 3. Transferência de elétrons e fosforilação oxidativa CICLO DE KREBS OU DO ÁCIDO CÍTRICO 1. Produção de Acetil-CoA
CICLO DE KREBS OU DO ÁCIDO CÍTRICO 1. Produção de Acetil-CoA 2. Oxidação de Acetil-CoA 3. Transferência de elétrons e fosforilação oxidativa CICLO DE KREBS OU DO ÁCIDO CÍTRICO 1. Produção de Acetil-CoA
nutrientes Reacções de redox nos seres vivos n.o.= +1 n.o.= 0 n.o.= 0 n.o.= 0 n.o.= 0 n.o.= -1 n.o.= +3 n.o.= +2 n.o.= -3 n.o.
 Reacções de redox nos seres vivos O n.o. do carbono do formol (metanal) é zero: perde 2 electrões para o O mas ganha 2 dos H. Dizemos que a glicose se oxida quando se converte em na glicólise... nutrientes
Reacções de redox nos seres vivos O n.o. do carbono do formol (metanal) é zero: perde 2 electrões para o O mas ganha 2 dos H. Dizemos que a glicose se oxida quando se converte em na glicólise... nutrientes
A denominação das cínases não tem em linha de conta o sentido em que a reacção ocorre nos seres vivos
 A denominação das cínases não tem em linha de conta o sentido em que a reacção ocorre nos seres vivos mesmo quando (por razões de índole termodinâmica) apenas a reacção em que ocorre formação de ATP pode
A denominação das cínases não tem em linha de conta o sentido em que a reacção ocorre nos seres vivos mesmo quando (por razões de índole termodinâmica) apenas a reacção em que ocorre formação de ATP pode
Cadeia Transportadora de Elétrons. Profa. Alana Cecília
 Cadeia Transportadora de Elétrons Profa. Alana Cecília Transporte de Elétrons O metabolismo aeróbio é um modo altamente eficiente para um organismo extrair energia a partir dos nutrientes. Em células eucarióticas
Cadeia Transportadora de Elétrons Profa. Alana Cecília Transporte de Elétrons O metabolismo aeróbio é um modo altamente eficiente para um organismo extrair energia a partir dos nutrientes. Em células eucarióticas
Cadeia Respiratória (Fosforilação Oxidativa)
 Cadeia Respiratória (Fosforilação Oxidativa) Bioquímica Prof. Dr. Vagne Oliveira 1 Cadeia de Transporte de Elétrons Consiste em uma série de transportadores de elétrons que atuam sequencialmente, sendo
Cadeia Respiratória (Fosforilação Oxidativa) Bioquímica Prof. Dr. Vagne Oliveira 1 Cadeia de Transporte de Elétrons Consiste em uma série de transportadores de elétrons que atuam sequencialmente, sendo
Fosforilação oxidativa
 A fosforilação oxidativa (FO) é o estágio final do metabolismo produtor de energia nos organismos aeróbicos Nessa etapa toda a energia produzida (na forma de carreadores de elétrons) durante a oxidação
A fosforilação oxidativa (FO) é o estágio final do metabolismo produtor de energia nos organismos aeróbicos Nessa etapa toda a energia produzida (na forma de carreadores de elétrons) durante a oxidação
MAPA II POLISSACARÍDIOS PROTEÍNAS LIPÍDIOS GLICOSE AMINOÁCIDOS ÁCIDOS GRAXOS. Leu Ile Lys Phe. Gly Ala Ser Cys. Fosfoenolpiruvato (3) Piruvato (3)
 Ciclo de Krebs MAPA II POLISSACARÍDIOS PROTEÍNAS LIPÍDIOS GLICOSE AMINOÁCIDOS ÁCIDOS GRAXOS Fosfoenolpiruvato (3) Asp Gly Ala Ser Cys Leu Ile Lys Phe Glu Piruvato (3) CO 2 Acetil-CoA (2) CO 2 Oxaloacetato
Ciclo de Krebs MAPA II POLISSACARÍDIOS PROTEÍNAS LIPÍDIOS GLICOSE AMINOÁCIDOS ÁCIDOS GRAXOS Fosfoenolpiruvato (3) Asp Gly Ala Ser Cys Leu Ile Lys Phe Glu Piruvato (3) CO 2 Acetil-CoA (2) CO 2 Oxaloacetato
FISIOLOGIA VEGETAL 24/10/2012. Respiração. Respiração. Respiração. Substratos para a respiração. Mas o que é respiração?
 Respiração Mas o que é respiração? FISIOLOGIA VEGETAL Respiração É o processo pelo qual compostos orgânicos reduzidos são mobilizados e subsequentemente oxidados de maneira controlada É um processo de
Respiração Mas o que é respiração? FISIOLOGIA VEGETAL Respiração É o processo pelo qual compostos orgânicos reduzidos são mobilizados e subsequentemente oxidados de maneira controlada É um processo de
Profª Eleonora Slide de aula. Cadeia de Transporte de Elétrons e Fosforilação Oxidativa
 Cadeia de Transporte de Elétrons e Fosforilação Oxidativa Cadeia de Transporte de Elétrons ou Cadeia Respiratória Os transportadores de elétrons sempre funcionam em uma seqüência determinada Os potenciais
Cadeia de Transporte de Elétrons e Fosforilação Oxidativa Cadeia de Transporte de Elétrons ou Cadeia Respiratória Os transportadores de elétrons sempre funcionam em uma seqüência determinada Os potenciais
FOSFORILAÇÃO OXIDATIVA
 FOSFORILAÇÃO OXIDATIVA Fosforilação oxidativa Peter Mitchell (1961) O intermediário energético necessário para a formação ATP (ou fosforilação de ADP), é a diferença na concentração de prótons através
FOSFORILAÇÃO OXIDATIVA Fosforilação oxidativa Peter Mitchell (1961) O intermediário energético necessário para a formação ATP (ou fosforilação de ADP), é a diferença na concentração de prótons através
Profa Alessandra Barone.
 Profa Alessandra Barone www.profbio.com.br Bioenergética Parte da bioquímica que trata do estudo dos fenômenos energéticos nos seres vivos, bem como sua forma de obtenção, armazenamento, mobilização e
Profa Alessandra Barone www.profbio.com.br Bioenergética Parte da bioquímica que trata do estudo dos fenômenos energéticos nos seres vivos, bem como sua forma de obtenção, armazenamento, mobilização e
A partir de agora, o processo de respiração celular ocorre dentro da organela citoplasmática chamada mitocôndria.
 A partir de agora, o processo de respiração celular ocorre dentro da organela citoplasmática chamada mitocôndria. Espaço intermembranar Membrana externa CITOSOL Finalizado o processo de GLICÓLISE 2 moléculas
A partir de agora, o processo de respiração celular ocorre dentro da organela citoplasmática chamada mitocôndria. Espaço intermembranar Membrana externa CITOSOL Finalizado o processo de GLICÓLISE 2 moléculas
OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa
 OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa Metabolismo: integração entre catabolismo e anabolismo Assimilação ou processamento da mat. Orgânica Síntese de Substâncias Estágio 1
OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa Metabolismo: integração entre catabolismo e anabolismo Assimilação ou processamento da mat. Orgânica Síntese de Substâncias Estágio 1
Introdução e apresentação geral do metabolismo da glicose
 Introdução e apresentação geral do metabolismo da glicose Índice 1- O transporte transmembranar e a fosforilação da glicose...1 2- A glicólise e a oxidação da glicose a CO 2...1 3- A oxidação da glicose-6-fosfato
Introdução e apresentação geral do metabolismo da glicose Índice 1- O transporte transmembranar e a fosforilação da glicose...1 2- A glicólise e a oxidação da glicose a CO 2...1 3- A oxidação da glicose-6-fosfato
Membrana interna. Cristas. Matriz Membrana externa. P i P i P i. 7,3 kcal/mol 7,3 kcal/mol 3,4 kcal/mol
 BIEERGÉTIA a célula milhares de compostos estão a ser sintetizados e degradados em simultâneo. Metabolismo: é o conjunto de todas as reacções envolvidas na manutenção deste estado dinâmico. o geral as
BIEERGÉTIA a célula milhares de compostos estão a ser sintetizados e degradados em simultâneo. Metabolismo: é o conjunto de todas as reacções envolvidas na manutenção deste estado dinâmico. o geral as
nutrientes 1 Reacções de redox nos seres vivos As reacções de oxi-redução costumam definir-se como reacções em que há transferência de electrões.
 Reacções de redox nos seres vivos As reacções de oxi-redução costumam definir-se como reacções em que há transferência de electrões. nutrientes 1 Zn + Cu 2+ Zn 2+ + Cu...mas também se podem definir como
Reacções de redox nos seres vivos As reacções de oxi-redução costumam definir-se como reacções em que há transferência de electrões. nutrientes 1 Zn + Cu 2+ Zn 2+ + Cu...mas também se podem definir como
Visão geral do metabolismo glicídico
 Visão geral do metabolismo glicídico 1. Todas as células do organismo podem usar glicose oxidando-a (processo exergónico) de forma acoplada com a formação de (processo endergónico). a) O catabolismo da
Visão geral do metabolismo glicídico 1. Todas as células do organismo podem usar glicose oxidando-a (processo exergónico) de forma acoplada com a formação de (processo endergónico). a) O catabolismo da
26/05/2017. Destinos do Piruvato na Célula. Respiração Celular X Combustão. Respiração Celular
 Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Destinos do Piruvato na Célula Curso Engenharia Química Disciplina Bioquimica Metabolismo de Carboidratos Ciclo do
Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Destinos do Piruvato na Célula Curso Engenharia Química Disciplina Bioquimica Metabolismo de Carboidratos Ciclo do
Exemplos: Exemplos: Síntase da hidroxi-metil-glutaril-coa
 A palavra síntase (não confundir com sintétase) está popularmente associado a algumas enzimas e as síntases podem pertencer a diferentes classes. Algumas vezes o nome que foi originalmente atribuído a
A palavra síntase (não confundir com sintétase) está popularmente associado a algumas enzimas e as síntases podem pertencer a diferentes classes. Algumas vezes o nome que foi originalmente atribuído a
Quantas moléculas de acetil-coa uma molécula de glicose e uma molécula de ácido graxo com 16 carbonos podem produzir após sua oxidação?
 Quantas moléculas de acetil-coa uma molécula de glicose e uma molécula de ácido graxo com 16 carbonos podem produzir após sua oxidação? E de transportadores de elétrons são reduzidos durante a oxidação
Quantas moléculas de acetil-coa uma molécula de glicose e uma molécula de ácido graxo com 16 carbonos podem produzir após sua oxidação? E de transportadores de elétrons são reduzidos durante a oxidação
Regulação do metabolismo oxidativo e equilíbrio energético. Na + Na + K + Ca + Ca +
 Regulação do metabolismo oxidativo e equilíbrio energético Semelhanças Usam a oxidação de compostos orgânicos como fonte de energia. 2 A velocidade de oxidação dos compostos orgânicos aumenta com o exercício.
Regulação do metabolismo oxidativo e equilíbrio energético Semelhanças Usam a oxidação de compostos orgânicos como fonte de energia. 2 A velocidade de oxidação dos compostos orgânicos aumenta com o exercício.
Fosforilação Oxidativa. Como conseguimos acoplar a oxidação de NADH e FADH 2 à produção de ATP. Prof. Henning Ulrich
 Fosforilação Oxidativa ou Como conseguimos acoplar a oxidação de NADH e FADH 2 à produção de ATP Prof. Henning Ulrich A célula precisa trabalhar Portanto, precisa de energia Catabolismo Ganha enérgia com
Fosforilação Oxidativa ou Como conseguimos acoplar a oxidação de NADH e FADH 2 à produção de ATP Prof. Henning Ulrich A célula precisa trabalhar Portanto, precisa de energia Catabolismo Ganha enérgia com
Organelas Transdutoras de Energia: Mitocôndria - Respiração
 Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Organelas: Cloroplasto e Mitocôndria Obtenção de energia para a célula a partir diferentes fontes: Curso: Engenharia
Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Organelas: Cloroplasto e Mitocôndria Obtenção de energia para a célula a partir diferentes fontes: Curso: Engenharia
5/4/2011. Metabolismo. Vias Metabólicas. Séries de reações consecutivas catalisadas enzimaticamente, que produzem produtos específicos (metabólitos).
 Metabolismo Vias Metabólicas Séries de reações consecutivas catalisadas enzimaticamente, que produzem produtos específicos (metabólitos). 1 Endergônico Exergônico Catabolismo Durante o catabolismo de carboidratos,
Metabolismo Vias Metabólicas Séries de reações consecutivas catalisadas enzimaticamente, que produzem produtos específicos (metabólitos). 1 Endergônico Exergônico Catabolismo Durante o catabolismo de carboidratos,
O ciclo de Krebs ou do ácido cítrico
 O ciclo de Krebs ou do ácido cítrico 1- Por ação das enzimas da glicólise a glicose é, no citoplasma das células, parcialmente oxidada a piruvato. O piruvato entra para a mitocôndria e, através da ação
O ciclo de Krebs ou do ácido cítrico 1- Por ação das enzimas da glicólise a glicose é, no citoplasma das células, parcialmente oxidada a piruvato. O piruvato entra para a mitocôndria e, através da ação
MÓDULO 2 - METABOLISMO. Bianca Zingales IQ-USP
 MÓDULO 2 - METABOLISMO Bianca Zingales IQ-USP INTRODUÇÃO AO METABOLISMO CARACTERÍSTICAS DO SER VIVO 1- AUTO-REPLICAÇÃO Capacidade de perpetuação da espécie 2- TRANSFORMAÇÃO DE ENERGIA O ser vivo extrai
MÓDULO 2 - METABOLISMO Bianca Zingales IQ-USP INTRODUÇÃO AO METABOLISMO CARACTERÍSTICAS DO SER VIVO 1- AUTO-REPLICAÇÃO Capacidade de perpetuação da espécie 2- TRANSFORMAÇÃO DE ENERGIA O ser vivo extrai
Resumo esquemático da glicólise
 Resumo esquemático da glicólise Destino do piruvato em condições aeróbicas e anaeróbicas Glicólise Fermentação Oxidação completa Em condições aeróbicas o piruvato é oxidado a acetato que entra no ciclo
Resumo esquemático da glicólise Destino do piruvato em condições aeróbicas e anaeróbicas Glicólise Fermentação Oxidação completa Em condições aeróbicas o piruvato é oxidado a acetato que entra no ciclo
Reações de redox nos seres vivos. nutrientes
 Reações de redox nos seres vivos As reações de oxi-redução (ou redox) costumam definir-se como reações em que há transferência de eletrões. nutrientes ruifonte@med.up.pt Departamento de Bioquímica da Faculdade
Reações de redox nos seres vivos As reações de oxi-redução (ou redox) costumam definir-se como reações em que há transferência de eletrões. nutrientes ruifonte@med.up.pt Departamento de Bioquímica da Faculdade
O ciclo de Krebs ou do ácido cítrico
 O ciclo de Krebs ou do ácido cítrico O ciclo de Krebs ou do ácido cítrico; Rui Fontes Índice 1- O ciclo de Krebs é uma via metabólica central no metabolismo oxidativo de todos os nutrientes...1 2- As enzimas
O ciclo de Krebs ou do ácido cítrico O ciclo de Krebs ou do ácido cítrico; Rui Fontes Índice 1- O ciclo de Krebs é uma via metabólica central no metabolismo oxidativo de todos os nutrientes...1 2- As enzimas
nutrientes Reacções de redox nos seres vivos As reacções de oxi-redução costumam definir-se como reacções em que há transferência de electrões.
 Reacções de redox nos seres vivos As reacções de oxi-redução costumam definir-se como reacções em que há transferência de electrões. nutrientes Zn + Cu 2+ Zn 2+ + Cu...mas também se podem definir como
Reacções de redox nos seres vivos As reacções de oxi-redução costumam definir-se como reacções em que há transferência de electrões. nutrientes Zn + Cu 2+ Zn 2+ + Cu...mas também se podem definir como
Regulação metabólica e equilíbrio energético. Na + Na + K + Ca + Ca + Semelhanças
 Regulação metabólica e equilíbrio energético Semelhanças 1- Usam a oxidação de compostos orgânicos como fonte de energia. 2- A velocidade de oxidação dos compostos orgânicos aumenta com o exercício. Uma
Regulação metabólica e equilíbrio energético Semelhanças 1- Usam a oxidação de compostos orgânicos como fonte de energia. 2- A velocidade de oxidação dos compostos orgânicos aumenta com o exercício. Uma
2- No dia estavam classificadas 4046 enzimas que podem ser consultadas em
 A maioria das enzimas são de natureza proteica e, relativamente aos outros catalisadores, têm uma grande especificidade em relação aos substratos e produtos da reacção. 1- A palavra enzima (do Grego: en,
A maioria das enzimas são de natureza proteica e, relativamente aos outros catalisadores, têm uma grande especificidade em relação aos substratos e produtos da reacção. 1- A palavra enzima (do Grego: en,
12/11/2015. Disciplina: Bioquímica Prof. Dr. Vagne Oliveira
 Disciplina: Bioquímica Prof. Dr. Vagne Oliveira 2 1 ATP ADP Glicose (6C) C 6 H 12 O 6 ATP ADP P ~ 6 C ~ P 3 C ~ P 3 C ~ P Pi NAD NADH P ~ 3 C ~ P ADP P ~ 3 C ATP ADP ATP NAD Pi NADH P ~ 3 C ~ P ADP ATP
Disciplina: Bioquímica Prof. Dr. Vagne Oliveira 2 1 ATP ADP Glicose (6C) C 6 H 12 O 6 ATP ADP P ~ 6 C ~ P 3 C ~ P 3 C ~ P Pi NAD NADH P ~ 3 C ~ P ADP P ~ 3 C ATP ADP ATP NAD Pi NADH P ~ 3 C ~ P ADP ATP
LCB208 BIOQUÍMICA DEPARTAMENTO DE CIÊNCIAS BIOLÓGICAS BIOENERGÉTICA
 LCB208 BIOQUÍMICA DEPARTAMENTO DE CIÊNCIAS BIOLÓGICAS BIOENERGÉTICA + NH 4 + (CO 2, Esq. C, NH 4+, H 2 O) ATP A moeda Energética das Células INTRODUÇÃO Os organismos vivos, para manterem sua intrincada
LCB208 BIOQUÍMICA DEPARTAMENTO DE CIÊNCIAS BIOLÓGICAS BIOENERGÉTICA + NH 4 + (CO 2, Esq. C, NH 4+, H 2 O) ATP A moeda Energética das Células INTRODUÇÃO Os organismos vivos, para manterem sua intrincada
O ciclo de Krebs ou do ácido cítrico
 O ciclo de Krebs ou do ácido cítrico Ciclo de Krebs ou do ácido cítrico; Rui Fontes 1- Por acção das enzimas da glicólise a glicose é, no citoplasma das células, parcialmente oxidada a piruvato. O piruvato
O ciclo de Krebs ou do ácido cítrico Ciclo de Krebs ou do ácido cítrico; Rui Fontes 1- Por acção das enzimas da glicólise a glicose é, no citoplasma das células, parcialmente oxidada a piruvato. O piruvato
Metabolismo e Regulação
 Metabolismo e Regulação PRBLEMAS - Série 1 Soluções 2009/2010 idratos de Carbono (Revisão) e Metabolismo Central 1 R: (α 1 4) (lineares) Ο (α1 6) (pontos de ramificação) 2. R: Locais de glicosilação são
Metabolismo e Regulação PRBLEMAS - Série 1 Soluções 2009/2010 idratos de Carbono (Revisão) e Metabolismo Central 1 R: (α 1 4) (lineares) Ο (α1 6) (pontos de ramificação) 2. R: Locais de glicosilação são
O 2 CO 2 + H 2 O. Absorção da glicose, glicólise e desidrogénase do piruvato. ADP + Pi. nutrientes ATP
 Absorção da glicose, glicólise e desidrogénase do piruvato Em todas as células ocorre continuamente a hidrólise do ATP (formando ADP + a uma velocidade tal que, mesmo em repouso, todo o stock de ATP se
Absorção da glicose, glicólise e desidrogénase do piruvato Em todas as células ocorre continuamente a hidrólise do ATP (formando ADP + a uma velocidade tal que, mesmo em repouso, todo o stock de ATP se
Aulas Multimídias Santa Cecília Profª Renata Coelho Disciplina: Biologia Série: 9º ano EF
 Aulas Multimídias Santa Cecília Profª Renata Coelho Disciplina: Biologia Série: 9º ano EF QUAIS SÃO OS PROCESSOS METABÓLICOS QUE LIBERAM ENERGIA DO ALIMENTO DENTRO DAS CÉLULAS HUMANAS? ONDE, NAS CÉLULAS
Aulas Multimídias Santa Cecília Profª Renata Coelho Disciplina: Biologia Série: 9º ano EF QUAIS SÃO OS PROCESSOS METABÓLICOS QUE LIBERAM ENERGIA DO ALIMENTO DENTRO DAS CÉLULAS HUMANAS? ONDE, NAS CÉLULAS
Ciclo do Ácido Cítrico ou Ciclo de Krebs ou Ciclo dos Ácidos Tricarboxílicos
 Ciclo do Ácido Cítrico ou Ciclo de Krebs ou Ciclo dos Ácidos Tricarboxílicos Vias da Respiração Celular NADH Glicólise NADH 2 Ciclo de Krebs Mitocôndria Cadeia transp. elétrons Glicose Piruvato Citosol
Ciclo do Ácido Cítrico ou Ciclo de Krebs ou Ciclo dos Ácidos Tricarboxílicos Vias da Respiração Celular NADH Glicólise NADH 2 Ciclo de Krebs Mitocôndria Cadeia transp. elétrons Glicose Piruvato Citosol
21/11/2016. Destinos do Piruvato na Célula. Respiração Celular X Combustão. Respiração Celular
 Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Destinos do Piruvato na Célula Curso Engenharia Química Disciplina Bioquimica Metabolismo de Carboidratos Ciclo do
Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Destinos do Piruvato na Célula Curso Engenharia Química Disciplina Bioquimica Metabolismo de Carboidratos Ciclo do
Ciclo de Krebs ou Ciclo do ácido cítrico. Prof. Liza Felicori
 Ciclo de Krebs ou Ciclo do ácido cítrico Prof. Liza Felicori VISÃO GERAL Em circunstâncias aeróbicas piruvato é descarboxilado CO 2 C4 + C2 C6 C6 C6 C6 C5 CO 2 CO 2 C5 C4 C4 C4 C4 NAD+ & FAD 3 Íons H-
Ciclo de Krebs ou Ciclo do ácido cítrico Prof. Liza Felicori VISÃO GERAL Em circunstâncias aeróbicas piruvato é descarboxilado CO 2 C4 + C2 C6 C6 C6 C6 C5 CO 2 CO 2 C5 C4 C4 C4 C4 NAD+ & FAD 3 Íons H-
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Regulação do metabolismo oxidativo e equilíbrio energético
 Regulação do metabolismo oxidativo e equilíbrio energético Semelhanças Usam a oxidação de compostos orgânicos como fonte de energia. 2 A velocidade de oxidação dos compostos orgânicos aumenta com o exercício.
Regulação do metabolismo oxidativo e equilíbrio energético Semelhanças Usam a oxidação de compostos orgânicos como fonte de energia. 2 A velocidade de oxidação dos compostos orgânicos aumenta com o exercício.
Reacções de redox nos seres vivos. nutrientes
 Reacções de redox nos seres vivos As reacções de oxi-redução (ou redox) costumam definir-se como reacções em que há transferência de electrões. nutrientes rui.fontes@mail.telepac.pt Laboratório de Bioquímica
Reacções de redox nos seres vivos As reacções de oxi-redução (ou redox) costumam definir-se como reacções em que há transferência de electrões. nutrientes rui.fontes@mail.telepac.pt Laboratório de Bioquímica
Metabolismo de Lipídeos
 Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Curso Engenharia Química Disciplina Bioquimica Metabolismo Energético de Lipídeos Oxidação Completa: Combustível +
Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Curso Engenharia Química Disciplina Bioquimica Metabolismo Energético de Lipídeos Oxidação Completa: Combustível +
Hoje iremos conhecer o ciclo de Krebs e qual a sua importância no metabolismo aeróbio. Acompanhe!
 Aula: 13 Temática: Metabolismo aeróbio parte I Hoje iremos conhecer o ciclo de Krebs e qual a sua importância no metabolismo aeróbio. Acompanhe! O Ciclo de Krebs ou Ciclo do Ácido Cítrico A molécula de
Aula: 13 Temática: Metabolismo aeróbio parte I Hoje iremos conhecer o ciclo de Krebs e qual a sua importância no metabolismo aeróbio. Acompanhe! O Ciclo de Krebs ou Ciclo do Ácido Cítrico A molécula de
Introdução às reações enzímicas. Equilíbrio químico, catálise e classificação funcional.
 Introdução às reações enzímicas. Equilíbrio químico, catálise e classificação funcional. ulas a cargo de na Branco e Rui Fontes ruifonte@med.up.pt s vias metabólicas existem porque existem enzimas que
Introdução às reações enzímicas. Equilíbrio químico, catálise e classificação funcional. ulas a cargo de na Branco e Rui Fontes ruifonte@med.up.pt s vias metabólicas existem porque existem enzimas que
Conversão de energia Mitocôndria - Respiração
 Universidade de São Paulo (USP) Escola de Engenharia de Lorena (EEL) Engenharia Ambiental Organelas: Cloroplasto e Mitocôndria Obtenção de energia para a célula a partir diferentes fontes: Conversão de
Universidade de São Paulo (USP) Escola de Engenharia de Lorena (EEL) Engenharia Ambiental Organelas: Cloroplasto e Mitocôndria Obtenção de energia para a célula a partir diferentes fontes: Conversão de
Metabolismo CO 2 + H 2 O O 2 + CH 2 O
 Metabolismo CO 2 + H 2 O O 2 + CH 2 O Glicólise Glicólise A via de Embden-Meyerhof (Warburg) Essencialmente todas as células executam a glicólise Consiste em dez reacções iguais em todas as células
Metabolismo CO 2 + H 2 O O 2 + CH 2 O Glicólise Glicólise A via de Embden-Meyerhof (Warburg) Essencialmente todas as células executam a glicólise Consiste em dez reacções iguais em todas as células
Aula de Bioquímica Avançada. Fosforilação Oxidativa
 Aula de Bioquímica Avançada Tema: Fosforilação Oxidativa Cadeia transportadora de elétrons Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC
Aula de Bioquímica Avançada Tema: Fosforilação Oxidativa Cadeia transportadora de elétrons Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC
CICLO DE KREBS. Bianca Zingales IQ-USP
 CICLO DE KREBS https://www.youtube.com/watch?v=ubzwpqpqm Bianca Zingales IQ-USP G L IC O S E A M IN O Á C ID O S Á C ID O S G R A X O S A sp G ly L eu G lu A la Ile F o sfo e n o lp iru v a to ( ) S er
CICLO DE KREBS https://www.youtube.com/watch?v=ubzwpqpqm Bianca Zingales IQ-USP G L IC O S E A M IN O Á C ID O S Á C ID O S G R A X O S A sp G ly L eu G lu A la Ile F o sfo e n o lp iru v a to ( ) S er
BIOLOGIA. Moléculas, células e tecidos. Respiração celular e fermentação Parte 1. Professor: Alex Santos
 BIOLOGIA Moléculas, células e tecidos Parte 1 Professor: Alex Santos Tópicos em abordagem: Parte 1 Respiração celular I Conceitos fundamentais; II Etapas da respiração celular; Parte 2 Respiração celular
BIOLOGIA Moléculas, células e tecidos Parte 1 Professor: Alex Santos Tópicos em abordagem: Parte 1 Respiração celular I Conceitos fundamentais; II Etapas da respiração celular; Parte 2 Respiração celular
Corpos cetônicos. Quais são? A partir de qual composto se formam? Como se formam? Quando se formam? Efeitos de corpos cetônicos elevados?
 Corpos cetônicos Quais são? A partir de qual composto se formam? Como se formam? Quando se formam? Efeitos de corpos cetônicos elevados? Importante saber!!!!!!!!!!!! A partir de qual composto se formam?
Corpos cetônicos Quais são? A partir de qual composto se formam? Como se formam? Quando se formam? Efeitos de corpos cetônicos elevados? Importante saber!!!!!!!!!!!! A partir de qual composto se formam?
Oxidações Biológicas e Introdução ao Metabolismo
 Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica Oxidações Biológicas e Introdução ao Metabolismo Professora Ana Chaves Introdução nucleotídeos Transporte:
Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica Oxidações Biológicas e Introdução ao Metabolismo Professora Ana Chaves Introdução nucleotídeos Transporte:
Variam em: localização, abundancia, forma... Axonema flagelar
 Mitocôndrias Variam em: localização, abundancia, forma... Axonema flagelar Matriz Membrana interna (Impermeável a íons) Membrana externa Espaço Intermembranas ou intermembanoso A origem das mitocôndrias:
Mitocôndrias Variam em: localização, abundancia, forma... Axonema flagelar Matriz Membrana interna (Impermeável a íons) Membrana externa Espaço Intermembranas ou intermembanoso A origem das mitocôndrias:
BIOSSÍNTESE DE ÁCIDOS GRAXOS E TRIACILGLICERÓIS. Bianca Zingales IQ-USP
 BIOSSÍNTESE DE ÁCIDOS GRAXOS E TRIACILGLICERÓIS Bianca Zingales IQ-USP Importância dos Lipídios 1. A maior fonte de armazenamento de Energia dos mamíferos 2. Componente de todas as membranas biológicas
BIOSSÍNTESE DE ÁCIDOS GRAXOS E TRIACILGLICERÓIS Bianca Zingales IQ-USP Importância dos Lipídios 1. A maior fonte de armazenamento de Energia dos mamíferos 2. Componente de todas as membranas biológicas
Funções do Metabolismo
 Universidade Federal de Mato Grosso Disciplina de Bioquímica Conceito de Metabolismo METABOLISMO DOS CARBOIDRATOS Prof. Msc. Reginaldo Vicente Ribeiro Atividade celular altamente dirigida e coordenada,
Universidade Federal de Mato Grosso Disciplina de Bioquímica Conceito de Metabolismo METABOLISMO DOS CARBOIDRATOS Prof. Msc. Reginaldo Vicente Ribeiro Atividade celular altamente dirigida e coordenada,
7. OXIDAÇÕES BIOLÓGICAS
 7. OXIDAÇÕES BIOLÓGICAS 2 O que é a oxidação? É o processo pelo qual a matéria viva transforma em diferentes formas de energia atual a energia químico-potencial contida nas estruturas moleculares dos alimentos.
7. OXIDAÇÕES BIOLÓGICAS 2 O que é a oxidação? É o processo pelo qual a matéria viva transforma em diferentes formas de energia atual a energia químico-potencial contida nas estruturas moleculares dos alimentos.
aaa Bento Gonçalves/RS 1
 a FISIOLOGIA E NUTRIÇÃO DA VIDEIRA aaa Respiração Celular Prof. Leonardo Cury Bento Gonçalves/RS 1 Equação Geral (Respiração celular (Aeróbica)) ATP C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O G = + 2.880 kj -Compostos
a FISIOLOGIA E NUTRIÇÃO DA VIDEIRA aaa Respiração Celular Prof. Leonardo Cury Bento Gonçalves/RS 1 Equação Geral (Respiração celular (Aeróbica)) ATP C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O G = + 2.880 kj -Compostos
Acetil CoA e Ciclo de Krebs. Prof. Henning Ulrich
 Acetil CoA e Ciclo de Krebs Prof. Henning Ulrich No citossol Na mitocôndria Descarboxilação do piruvato: H 3 C- Piruvato Coenzima A Acetil CoA Redução de 1 NAD + Formação de acetil CoA (rica em energia)
Acetil CoA e Ciclo de Krebs Prof. Henning Ulrich No citossol Na mitocôndria Descarboxilação do piruvato: H 3 C- Piruvato Coenzima A Acetil CoA Redução de 1 NAD + Formação de acetil CoA (rica em energia)
Gliconeogénese e Metabolismo do Glicogénio
 Página 1 de 5 Aulas de grupo 2001-02; Rui Fontes Gliconeogénese e Metabolismo do Glicogénio 1- Gliconeogénese 1- A gliconeogénese é um termo usado para incluir o conjunto de processos pelos quais o organismo
Página 1 de 5 Aulas de grupo 2001-02; Rui Fontes Gliconeogénese e Metabolismo do Glicogénio 1- Gliconeogénese 1- A gliconeogénese é um termo usado para incluir o conjunto de processos pelos quais o organismo
MITOCÔNDRIAS MITOCÔNDRIAS. Respiração celular. Produção de moeda energética ATP. Fosforilação oxidativa
 MITOCÔNDRIAS MITOCÔNDRIAS Respiração celular Produção de moeda energética ATP Fosforilação oxidativa Mecanismo para obtenção de energia baseado em membrana 1 MITOCÔNDRIAS Mecanismo para obtenção de energia
MITOCÔNDRIAS MITOCÔNDRIAS Respiração celular Produção de moeda energética ATP Fosforilação oxidativa Mecanismo para obtenção de energia baseado em membrana 1 MITOCÔNDRIAS Mecanismo para obtenção de energia
MÓDULO 2 - METABOLISMO. Bianca Zingales IQ-USP
 MÓDULO 2 - METABOLISMO Bianca Zingales IQ-USP INTRODUÇÃO AO METABOLISMO CARACTERÍSTICAS DO SER VIVO 1- AUTO-REPLICAÇÃO Capacidade de perpetuação da espécie 2- TRANSFORMAÇÃO DE ENERGIA O ser vivo extrai
MÓDULO 2 - METABOLISMO Bianca Zingales IQ-USP INTRODUÇÃO AO METABOLISMO CARACTERÍSTICAS DO SER VIVO 1- AUTO-REPLICAÇÃO Capacidade de perpetuação da espécie 2- TRANSFORMAÇÃO DE ENERGIA O ser vivo extrai
Metabolismo de Lipídeos
 Outros Exemplos de Mecanismos de Regulação Glicose X Gliconeogênese Regulação da Frutose 6P pela Frutose 2,6 bifosfato FBPase: bifosfatofosfatase (Gliconeogênese) PFK : fosfofrutoquinase (Glicólise) Universidade
Outros Exemplos de Mecanismos de Regulação Glicose X Gliconeogênese Regulação da Frutose 6P pela Frutose 2,6 bifosfato FBPase: bifosfatofosfatase (Gliconeogênese) PFK : fosfofrutoquinase (Glicólise) Universidade
Profª Eleonora Slide de aula. Metabolismo de Carboidratos
 Metabolismo de Carboidratos Metabolismo de Carboidratos Profª Eleonora Slide de aula Condições de anaerobiose Glicose 2 Piruvato Ciclo do ácido cítrico Condições de anaerobiose 2 Etanol + 2 CO 2 Condições
Metabolismo de Carboidratos Metabolismo de Carboidratos Profª Eleonora Slide de aula Condições de anaerobiose Glicose 2 Piruvato Ciclo do ácido cítrico Condições de anaerobiose 2 Etanol + 2 CO 2 Condições
Metabolismo celular. É o conjunto de todas as reacções químicas que ocorrem numa célula.
 FERMENTAÇÃO Metabolismo celular 3 É o conjunto de todas as reacções químicas que ocorrem numa célula. Metabolismo celular 4 Anabolismo reacções de síntese de moléculas complexas a partir de moléculas simples.
FERMENTAÇÃO Metabolismo celular 3 É o conjunto de todas as reacções químicas que ocorrem numa célula. Metabolismo celular 4 Anabolismo reacções de síntese de moléculas complexas a partir de moléculas simples.
Oxidação parcial o que acontece com o piruvato?
 A glicólise ocorre no citosol das células transforma a glicose em duas moléculas de piruvato e é constituída por uma sequência de 10 reações (10 enzimas) divididas em duas fases. Fase preparatória (cinco
A glicólise ocorre no citosol das células transforma a glicose em duas moléculas de piruvato e é constituída por uma sequência de 10 reações (10 enzimas) divididas em duas fases. Fase preparatória (cinco
O ciclo de Krebs ou do ácido cítrico
 O ciclo de Krebs ou do ácido cítrico 1- Por ação das enzimas da glicólise a glicose é, no citoplasma das células, oxidada a piruvato. O piruvato entra para a mitocôndria e, através da ação catalítica da
O ciclo de Krebs ou do ácido cítrico 1- Por ação das enzimas da glicólise a glicose é, no citoplasma das células, oxidada a piruvato. O piruvato entra para a mitocôndria e, através da ação catalítica da
Respiração Celular. Ciclo de Krebs Ciclo do ácido Tricarboxílico Ciclo do ácido Cítrico. Prof. Ana Paula Jacobus
 Respiração Celular Ciclo de Krebs Ciclo do ácido Tricarboxílico Ciclo do ácido Cítrico Prof. Ana Paula Jacobus GLICOSE VIAS LINEARES (glicólise e gliconeogênese) PIRUVATO Ciclo do ácido cítrico ou
Respiração Celular Ciclo de Krebs Ciclo do ácido Tricarboxílico Ciclo do ácido Cítrico Prof. Ana Paula Jacobus GLICOSE VIAS LINEARES (glicólise e gliconeogênese) PIRUVATO Ciclo do ácido cítrico ou
Os organismos necessitam de um constante fornecimento de energia livre
 Os organismos necessitam de um constante fornecimento de energia livre Por que? - Biossíntese de moléculas complexas; - Transporte ativo de moléculas e íons c através de membranas; - Realização de Trabalho
Os organismos necessitam de um constante fornecimento de energia livre Por que? - Biossíntese de moléculas complexas; - Transporte ativo de moléculas e íons c através de membranas; - Realização de Trabalho
Prof André Montillo
 Prof André Montillo www.montillo.com.br Definição: É a soma de todas as reações químicas envolvidas na manutenção do estado dinâmico das células, onde milhares de reações ocorrem ao mesmo tempo, determinando
Prof André Montillo www.montillo.com.br Definição: É a soma de todas as reações químicas envolvidas na manutenção do estado dinâmico das células, onde milhares de reações ocorrem ao mesmo tempo, determinando
A mitocôndria oxida combustíveis para gerar energia, em analogia ao processo pelo qual as usinas de força utilizam os combustíveis para gerar energia
 A mitocôndria oxida combustíveis para gerar energia, em analogia ao processo pelo qual as usinas de força utilizam os combustíveis para gerar energia elétrica Micrografia eletrônica de uma mitocôndria
A mitocôndria oxida combustíveis para gerar energia, em analogia ao processo pelo qual as usinas de força utilizam os combustíveis para gerar energia elétrica Micrografia eletrônica de uma mitocôndria
Como é que as células extraem energia e poder redutor do ambiente? Como é que as células sintetizam as unidades das macromoléculas?
 Metabolismo Como é que as células extraem energia e poder redutor do ambiente? Como é que as células sintetizam as unidades das macromoléculas? Os seres vivos precisam de energia para: Realização de trabalho
Metabolismo Como é que as células extraem energia e poder redutor do ambiente? Como é que as células sintetizam as unidades das macromoléculas? Os seres vivos precisam de energia para: Realização de trabalho
Matéria: Biologia Assunto: Respiração celular Prof. Enrico blota
 Matéria: Biologia Assunto: Respiração celular Prof. Enrico blota Biologia 1. Moléculas, células e tecidos - Fotossíntese e respiração - Respiração celular Fermentação Organismos que só vivem na presença
Matéria: Biologia Assunto: Respiração celular Prof. Enrico blota Biologia 1. Moléculas, células e tecidos - Fotossíntese e respiração - Respiração celular Fermentação Organismos que só vivem na presença
Metabolismo de Lipídeos
 Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Curso Engenharia Química Disciplina Bioquimica Metabolismo Energético de Lipídeos Oxidação Completa: Combustível +
Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Curso Engenharia Química Disciplina Bioquimica Metabolismo Energético de Lipídeos Oxidação Completa: Combustível +
METABOLISMO ENERGÉTICO. BIOLOGIA 9º ano Profª Renata Coelho Rodrigues
 METABOLISMO ENERGÉTICO BIOLOGIA 9º ano Profª Renata Coelho Rodrigues METABOLISMO ENERGÉTICO PLASTOS: Organelas membranosas (células vegetais e algas eucarióticas). Tilacóides: CLOROPLASTOS Presente em
METABOLISMO ENERGÉTICO BIOLOGIA 9º ano Profª Renata Coelho Rodrigues METABOLISMO ENERGÉTICO PLASTOS: Organelas membranosas (células vegetais e algas eucarióticas). Tilacóides: CLOROPLASTOS Presente em
Fosforilação oxidativa
 Fosforilação oxidativa A fosforilação oxidativa é um processo metabólico em que as enzimas/transportadores envolvidos são proteínas da membrana interna da mitocôndria que, no seu conjunto, catalisam a
Fosforilação oxidativa A fosforilação oxidativa é um processo metabólico em que as enzimas/transportadores envolvidos são proteínas da membrana interna da mitocôndria que, no seu conjunto, catalisam a
Profª Eleonora Slide de aula. Revisão: Termodinâmica e Bioenergética
 Revisão: Termodinâmica e Bioenergética Revisão:Termodinâmica As leis da termodinâmica governam o comportamento de s bioquímicos As leis da termodinâmica são princípios gerais aplicados a todos os processos
Revisão: Termodinâmica e Bioenergética Revisão:Termodinâmica As leis da termodinâmica governam o comportamento de s bioquímicos As leis da termodinâmica são princípios gerais aplicados a todos os processos
Metabolismo energético das células
 Metabolismo energético das células Medicina Veterinária Bioquímica I 2º período Professora: Ms. Fernanda Cristina Ferrari Como a célula produz energia? Fotossíntese Quimiossíntese Respiração Adenosina
Metabolismo energético das células Medicina Veterinária Bioquímica I 2º período Professora: Ms. Fernanda Cristina Ferrari Como a célula produz energia? Fotossíntese Quimiossíntese Respiração Adenosina
A energética celular: o papel das mitocôndrias e cloroplastos
 A energética celular: o papel das mitocôndrias e cloroplastos A energética celular ATP: captura e transfere energia livre nos sistemas biológicos Hidrólise do ATP: libera energia para suprir processos
A energética celular: o papel das mitocôndrias e cloroplastos A energética celular ATP: captura e transfere energia livre nos sistemas biológicos Hidrólise do ATP: libera energia para suprir processos
A energética celular:
 A energética celular: o papel das mitocôndrias e cloroplastos Capitulo 13 (p 427 a 444) e Capitulo 14 Fundamentos da Biologia Celular- Alberts- 2ª edição A energética celular Como já vimos anteriormente
A energética celular: o papel das mitocôndrias e cloroplastos Capitulo 13 (p 427 a 444) e Capitulo 14 Fundamentos da Biologia Celular- Alberts- 2ª edição A energética celular Como já vimos anteriormente
