Dê aos seus doentes o tempo que precisam.
|
|
|
- Adriano Imperial Machado
- 5 Há anos
- Visualizações:
Transcrição
1 Dê aos seus doentes o tempo que precisam. Monografia do Produto FsstFsstFsst. Contra a ejaculação precoce. Novo tratamento em spray para a ejaculação precoce, clinicamente comprovado.
2 ÍNDICE 1. Contexto... Fundamentação clínica e social para o Fortacin Impacto das disfunções sexuais tais como a ejaculação precoce (EP) No paciente e na/o sua/seu parceira/o Na satisfação sexual mútua e no bem-estar Epidemiologia da EP - uma disfunção sexual frequente no homem Definindo a ejaculação precoce Fisiologia e fisiopatologia da ejaculação precoce Critérios de diagnóstico ensaios clínicos e prática clínica Uma necessidade não-atendida 2. Introdução ao Fortacin... Indicação licenciada Apresentação Posologia, administração e conservação Contraindicações Precauções especiais Efeitos indesejáveis 3. Propriedades do Fortacin... Composição química Modo de Administração Mecanismo de ação Farmacodinâmica e farmacocinética 4. Avaliação clínica... O Estudo ANAE O Estudo PSD502-PE-005 O Estudo PSD502-PE-001 Estudo de Fase III PSD502-PE-002 PSD503-PE-004 Indicadores principais dos dois estudos Seguimento em fase aberta Resumo da Tolerabilidade 5. Utilização na prática clínica... Linhas de orientação e recomendações Resumo da utilização potencial do Fortacin nos pacientes Informação de prescrição Pontos-Chave... Referências... IECRCM
3 RESUMO A ejaculação precoce (EP) é uma queixa sexual masculina frequente, complexa e multifatorial. O tempo de latência ejaculatória intravaginal (o tempo que decorre entre o momento de penetração vaginal e o momento da ejaculação intravaginal - TLEI) é uma medida objetiva da função ejaculatória para os ensaios clínicos. No entanto, o impacto negativo da EP estende-se para além da disfunção sexual. Vários estudos de observação têm demonstrado o impacto psicológico e na qualidade de vida que a EP tem no homem, na(o) sua(seu) parceira(o) e na relação entre ambos. Consequentemente, a definição da International Society for Sexual Medicine (ISSM), baseada na evidência, inclui não só o tempo para chegar à ejaculação, relatado pelo paciente, mas também a falta de controlo sobre a mesma e a presença de consequências pessoais negativas. Apesar da EP ser uma queixa sexual frequente, com uma prevalência estimada entre os 20-30%, muitos homens não procuram conselho nem tratamento. Um estudo observou que apenas 9% dos homens identificados com EP consultaram um médico para procurar tratamento. Os motivos dados são o constrangimento e a crença de que não existe nada que possa ser feito. Os médicos estão numa posição privilegiada para poderem ajudar os pacientes com dificuldades sexuais. Podem fazer com que o paciente se sinta à vontade e, desta feita, mais confortável para falar sobre as suas queixas. Com a EP a causar uma angústia significativa, tanto a nível pessoal como interpessoal, no homem, sua (seu) parceira(o) e no casal, a avaliação apropriada da queixa pode ajudar a quebrar o círculo vicioso, quando o diagnóstico for de EP crónica. Até há bem pouco tempo, não existiam tratamentos tópicos licenciados e havia apenas um tratamento sistémico que os médicos pudessem propor aos homens com EP. A relutância dos pacientes em falar sobre os seus problemas sexuais e o grau de insatisfação dos poucos que procuraram tratamento, traduz de forma clara, tanto a necessidade dos médicos em incentivar conversas sobre a saúde sexual, como a necessidade de uma oferta mais alargada de tratamentos aprovados, para os homens com diagnóstico de EP. O lançamento de Fortacin, um tratamento tópico de aplicação na hora, para homens adultos, proporciona aos médicos a oportunidade de poderem ajudar estes pacientes, acrescentando este medicamento licenciado ao seu repertório clínico. Enquanto fórmula de pulverização tópica que proporciona uma anestesia local, o Fortacin foi concebido para ser aplicado 5 minutos antes de uma relação sexual. Eficaz desde a primeira aplicação e com poucas restrições de utilização, a eficácia do Fortacin no aumento to TLEI tem sido demonstrada através de ensaios clínicos. Tem melhorado, ainda, de forma significativa, o grau de satisfação sexual de ambos os parceiros e, desta feita, ajudado a eliminar o efeito de exacerbação psicológica e a perpetuação do problema. Não há evidência de taquifilaxia com o uso repetido e o Fortacin é geralmente bem tolerado. 3
4 CONTEXTO 1. Contexto Fundamentação clínica e social para o Fortacin A ejaculação precoce (EP) é uma queixa sexual masculina frequente, complexa e multifatorial. 1 Caracteriza-se por uma ejaculação excessivamente rápida. No entanto, esta disfunção sexual, segundo o consenso profissional, não pode ser simplesmente definida nestes termos. 2,3 A utilização do tempo de latência ejaculatória intravaginal (TLEI), por si só, não é suficiente para definir a EP, uma vez que existe uma sobreposição significativa nos resultados dos homens com e sem EP. 4 A distribuição do TLEI na população geral demonstra uma variação significativa. Um estudo com 500 casais de cinco países e de diferentes grupos etários registou um TLEI médio de 5.4 minutos, mas um intervalo de minutos. 5 Comparando os homens com e sem EP, os resultados revelaram que 75% dos homens sem EP tinham um TLEI médio >4 min; no entanto, 25% tinham um TLEI médio 4 minutos e 12% um TLEI médio 2 minutos. Comparativamente aos homens com EP, 75% tinham um TLEI médio 4 minutos e 56% dos participantes tinham um TLEI médio 2 minutos. 4 Distribuição dos homens da UE pelos valores do TLEI, nos grupos com EP e sem EP EP (n=182) Non-EP (n=844) Percentagem (%) Figura 1 Adaptada de Giuliano * Média TLEI (min) *Os valores médios individuais do TLEI de 20.5 min foram colocados numa única categoria. O TLEI é uma medida objetiva da função ejaculatória. No entanto, o impacto negativo da EP estende-se para além da disfunção sexual. 6 Uma revisão de 11 estudos observacionais, não-intervencionais dos aspetos psicológicos e da qualidade de vida, da EP, no homem, na sua parceira e na relação, confirma de forma consistente a presença de um elevado nível de angústia pessoal nos homens e nas suas parceiras. 2 4
5 CONTEXTO De forma semelhante, a auto-estima e a autoconfiança diminuem nos homens com EP e cerca de um terço relataram ansiedade associada às relações sexuais. Isto pode tornar-se numa barreira para alguns, relativamente ao início de novos relacionamentos. 2 Os homens com EP sentem que estão a deixar ficar mal a sua parceira e que a qualidade do seu relacionamento seria melhor sem a EP. 2 O impacto qualitativo sobre o indivíduo foi avaliado como semelhante ao da disfunção erétil (DE). 7 A EP pode ter um efeito prejudicial sobre o relacionamento com a parceira e, por vezes, provocar sentimentos de angústia, ansiedade, vergonha e depressão. Como tal, pode ter graves consequências psicológicas e na qualidade de vida, tanto para o homem como para a sua parceira. 6 Adicionalmente, há evidência do impacto negativo da EP na função sexual feminina, e os homens e suas parceiras mostram sinais de dificuldades interpessoais e uma redução geral na qualidade de vida, provocadas pela EP. 2 Um estudo observacional europeu com 1,115 homens e suas parceiras estudou o TLEI e o Perfil de Ejaculação Precoce (PEP) de homens com e sem EP para validar a utilização de resultados relatados pelos pacientes na caracterização da EP e discernir a relação entre o PEP e o TLEI, nos homens da UE. 4 Este estudo foi semelhante a um estudo anterior feito pela Internet com 12,113 homens nos EUA, Alemanha e Itália. 8 As pontuações do Perfil de Ejaculação Precoce (PEP) (que medem a perceção de controlo, angústia pessoal, grau de satisfação com as relações sexuais e dificuldades interpessoais), revelaram-se significativamente mais baixas nos homens (e parceiras) com EP, comparativamente aos que não sofrem de EP (p<0,001). Os resultados do PEP diferenciaram os dois grupos e, logo, foram consideradas medidas úteis, de resultados relatados pelos pacientes. 4 Giuliano et al. concluíram que a perceção de controlo sobre a ejaculação tinha um efeito significativo sobre a satisfação com o ato sexual e no sentimento de angústia pessoal relacionada com a ejaculação. O TLEI, pelo contrário, não teve um efeito direto na satisfação e apenas um efeito direto reduzido no sentimento de angústia relacionado com a ejaculação. 4 Definindo a EP Tem sido reconhecido, de forma significativa, que a definição da EP precisa de incorporar todos esses fatores. A Sociedade Internacional de Medicina Sexual (International Society for Sexual Medicine - ISSM) inclui o tempo de ejaculação relatado pelo paciente, mas a EP também é definida como uma falta de controlo sobre a ejaculação, acompanhada pela presença de consequências pessoais negativas. Distingue, ainda, duas formas deste problema. 2,3 Existe, atualmente, uma ampla aceitação da existência de dois tipos distintos de ejaculação precoce: a EP crónica e a EP adquirida. 5
6 CONTEXTO A Ejaculação que ocorre sempre ou quase sempre num período inferior ou igual a 1 minuto de penetração vaginal desde a primeira experiência sexual (EP crónica); ou A Redução do tempo de latência, clinicamente significativa e incómoda, frequentemente até cerca de 3 minutos ou menos (EP adquirida); e B A incapacidade de retardar a ejaculação em todos ou quase todos os atos de penetração vaginal; e Figura 2 A definição da ejaculação precoce, da ISSM 2 C Consequências pessoais negativas, tais como angústia, incómodo, frustração e/ou evitamento da intimidade sexual. A ejaculação precoce é definida como uma ejaculação que ocorre num período inferior ou igual a 1 minuto (crónica) ou 3 minutos (adquirida) de penetração, acompanhada por uma falta de controlo sobre a ejaculação e consequências pessoais negativas. Esta tríade de dimensões interligadas da EP representa agora a definição baseada na evidência, da EP crónica e da EP adquirida. 3 TEMPO (TLEI) EP ANGÚSTIA CONTROLO Estudos apontam que 80-90% dos homens que procuram tratamento para a EP crónica chegam à ejaculação num tempo igual ou inferior a 1 minuto. No entanto, tal como observam Serefoglu et al., uma qualificação adicional deste critério de cerca de 1 minuto proporciona ao médico a flexibilidade de diagnóstico necessária para captar os restantes 10-20% dos homens que se queixam de EP, com um tempo para a ejaculação ligeiramente maior. 3 Estudos observacionais de grande dimensão concluem que a EP está subdiagnosticada. 4,8 6
7 CONTEXTO Sentimentos de constrangimento e a perceção de falta de opções de tratamento, ou de que nada pode ser feito, fazem com que poucos homens optem por consultar um médico. 4,6,8 A variação histórica na definição da EP tem confundido a avaliação da prevalência desta queixa. A maioria dos estudos foram realizados antes da definição baseada na evidência dada pela ISSM e, consequentemente, a prevalência de queixas de EP em homens adultos pode variar entre os 20-30%. 8 Althof et al. assinalam que a prevalência da EP crónica na população geral não irá, provavelmente, ultrapassar os 4%. Os estudos têm demonstrado que a EP é uma queixa sexual masculina frequente. Observou-se uma prevalência média de 22,7%, num estudo multinacional de grande escala feito pela Internet, no qual os homens foram classificados com EP com base em auto-relatos de falta (ou ausência) de controlo sobre a ejaculação, produzindo um sentimento de angústia nos próprios, nas suas parceiras, ou em ambos. 8 Neste inquérito de Atitudes e Prevalência da Ejaculação Precoce (Premature Ejaculation Prevalence and Attitudes Survey - PEPA), a prevalência foi indicada como independente da idade e do país dos participantes. 8 Estes resultados não diferem da taxa de prevalência média de 18% clinicamente diagnosticada no DSM-IV-TR, registada no estudo observacional europeu Percentagem de homens com EP % 23% 23% 24% 25% 20% Grupo de idades (anos) Figura 3 Prevalência da EP, por grupo etário n=12,113 Neste inquérito de APEP, foram incluídas perguntas para avaliar quantos homens tinham consultado um médico, assim como os motivos que tinham, ou teriam, influenciado a sua decisão de procurar conselho e tratamento. Apesar de conscientes da existência de tratamentos prescritos, apenas 9% dos homens identificados com EP relataram ter consultado um médico por causa da EP. Mais de dois terços destes homens recordam-se de terem ido falar com o médico, inicialmente, por outra razão. A maioria dos homens (81.9%) já tinha iniciado uma conversa sobre a EP; 91,5% dos homens que procuraram tratamento junto de um médico relataram poucas ou nenhuma melhoria. No entanto, não se sabe que tipo de gestão/tratamento(s) foram feitos e se foram devidamente aplicados. Apenas 12,9% dos homens com EP relataram ter usado tratamentos farmacológicos prescritos. 8 7
8 CONTEXTO Percentagem de homens com EP consultam médico Percentagem de homens com EP reportam melhoria depois de procurar tratamento 9% 8.5% 91% 91.5% Figura 4 Proporção dos homens com EP que consultou um médico e satisfação com os resultados Homens que consultam médico Homens que não consultam médico Homens com melhoria Homens com pouca ou nenhuma melhoria Os homens que participaram nesta pesquisa indicaram que os principais motivos para não terem procurado aconselhar-se sobre o assunto foram: o desconforto em falar sobre questões sensíveis, o constrangimento em falar sobre a EP, a dúvida de que existisse algo que pudesse ser feito para os ajudar e a preocupação de se poderem vir a tornar dependentes da medicação. 8 Curiosamente, vários homens com EP não viam o seu médico como a melhor fonte de informação relativamente à saúde. 8 Por outro lado, aproximadamente 60% dos homens disse que consultaria um médico caso a sua parceira o sugerisse, ou se soubessem da existência de uma solução para tratá-los. 75% dos homens que procuraram tratamento fizeram-no para aumentar a satisfação sexual da sua parceira. Os autores sugeriram o envolvimento das parceiras nas conversas sobre a saúde sexual, como uma abordagem útil para incentivar os homens a procurar orientação e tratamento médico. 8 Os homens com EP tiveram maior propensão para apresentarem comorbidades, incluindo outras disfunções sexuais e perturbações psicológicas (ex: depressão, ansiedade, excesso de stress), mas também uma série de outros problemas, como a artrite, a hipertensão arterial, os diabetes e as alergias, comparativamente aos homens sem EP (p<0,05 para todos). 8 Estas comorbidades proporcionam uma oportunidade ao médico para falar com os pacientes, mas também podem limitar as opções adequadas para a gestão da situação. Os autores observam que: Os médicos devem fazer perguntas sobre a saúde sexual dos seus pacientes do sexo masculino durante as suas consultas de rotina, de forma a criar um ambiente no qual os homens possam sentir-se mais à vontade para relatar a EP e outros problemas sexuais comuns. 8 8
9 CONTEXTO Os médicos estão numa posição privilegiada para poderem ajudar pacientes com dificuldades sexuais, muitas das quais são multifatoriais e podem exigir um acompanhamento a longo prazo. Os médicos podem fazer com que os pacientes se sintam mais à vontade e, logo, com maior capacidade de falar sobre as suas queixas. Tendo em conta a angústia pessoal e interpessoal significativa que a EP causa no homem, na sua parceira e no casal, uma avaliação adequada da queixa pode ajudar a quebrar o círculo vicioso, caso o diagnóstico seja de EP crónica. 1,2 Fisiologia e Fisiopatologia da EP A ejaculação é o resultado da atividade contrátil coordenada, envolvendo diferentes órgãos ejaculatórios, organizados pelo gerador ejaculatório espinhal (Spinal Ejaculatory Generator - SEG), localizado nos níveis T12-L1-L2 da medula espinhal. A informação aferente é recebida pelo SEG, que coordena as saídas simpáticas, parassimpáticas e motoras, para as duas fases de ejaculação: a emissão e a expulsão. O SEG integra estas influências inibitórias e excitatórias dos locais supra-espinhais, bem como as entradas que transportam informações bioquímicas ou mecânicas dos órgãos sexuais acessórios. 9 SSRIs Centro Secretor Emissão Anestésicos tópicos Nervo pudendo Aferentes sensoriais Centro Mecânico Expulsão Toxina Botulínica Ejaculação Figura 5 O reflexo ejaculatório e o controlo da ejaculação. Adaptado de Saitz A emissão do sémen envolve as fibras eferentes simpáticas do centro secretor (T10-L2), coordenando as contrações sequenciais do epidídimo, do canal deferente, das vesículas seminais e da próstata, com o fecho associado do pescoço da bexiga. A expulsão do sémen é, então, iniciada somaticamente pelo centro mecânico da medula espinhal sacral (S2-S4), através do 9
10 CONTEXTO nervo pudendo, que induz contrações nos músculos bulboesponjosos, bulbocavernosos e perineais, o que, por sua vez, força ritmicamente a ejaculação através da uretra distal. 9 Apesar da etiologia da EP ser largamente desconhecida, as reações psicológicas tanto do homem como da sua parceira podem levar a uma perpetuação e exacerbação do problema. Isto tem sido descrito como um círculo vicioso. 1 Exacerbação e perpetuação de fatores psicológicos Predisposição orgânica e/ou fatores psicológicos Figura 5 Círculo vicioso da exacerbação e da manutenção/ perpetuação dos fatores psicológicos da EP. Adaptado de Buvat 2011 Reações psicológicas do homem e parceiro/a Disfunção sexual Desencadeador de fatores orgânicos e/ou fatores psicológicos As causas subjacentes da ejaculação precoce são geralmente entendidas como psicológicas e/ou fisiológicas, apesar da falta de provas conclusivas relativamente aos fatores psicológicos que causam o problema. Apesar de existir evidência clara do envolvimento neurológico na regulação da ejaculação, nenhuma ligação foi estabelecida entre as anomalias neurológicas e a ejaculação precoce. As linhas de orientação da Associação Europeia de Urologia (European Association of Urology - EAU) assinalam que a EP não é afetada pelo estado civil ou pela situação económica, mas é mais comuns em homens negros, homens hispânicos e homens de meios islâmicos, e a sua incidência pode ser maior em homens com um nível educacional menor. Outros fatores de risco podem incluir uma predisposição genética, uma fraca condição de saúde geral e obesidade, inflamação da próstata, perturbações hormonais da tiroide, problemas emocionais, stress e experiências sexuais traumáticas. 6 A etiologia dos dois tipos principais de ejaculação precoce é claramente distinta. A ejaculação precoce crónica parece ter uma etiologia neurofisiológica, havendo um corpo de evidência crescente a apontar para o papel da serotonina e determinados subtipos de recetores de serotonina (5-HT), em alguns pacientes afetados com essa variante da doença. 10 Mas a evidência de um estudo de grande dimensão com gémeos sugere que 10
11 CONTEXTO este tipo de ejaculação precoce também seja significativamente influenciado por fatores ambientais. 11 Estes estudos apenas proporcionam uma compreensão parcial dos fatores causais envolvidos neste tipo de EP. É provável que outras hormonas e neurotransmissores também sejam fatores causais para a ejaculação precoce crónica. 12 No entanto, a evidência do papel de outras hormonas está atualmente limitada aos dados de estudos em animais. A hipersensibilidade da glande do pénis provavelmente também deverá estar envolvida, mas a causa biológica subjacente desta sensibilidade acrescida não é clara. 13 Diferentes subtipos de recetores da 5-HT podem ter ações opostas na ejaculação. Vários subtipos de recetores da 5-HT estruturalmente distintos foram identificados, mas apenas o envolvimento dos subtipos 5-HT1A, 5-HT1B, 5-HT2C e 5-HT7, no mecanismo da ejaculação, tem sido demonstrado. 14 O paciente com ejaculação precoce precisa de mais serotonina do que o normal na sua fenda sináptica para melhorar o sentimento de controlo sobre o reflexo da ejaculação. A EP não deveria ser considerada um problema caracterizado por níveis baixos de serotonina (5-HT), mas antes um problema em que, por vários motivos, existe uma maior necessidade de 5-HT para melhorar o sentimento de controlo, para diminuir a angústia no casal, relacionada com a doença e para melhorar o tempo de latência da ejaculação intravaginal (TLEI). 14 Os estudos relacionados com a genética têm-se focado no sistema serotonérgico e fornecido evidência de que alguns polimorfismos genéticos neste sistema estão associados à ejaculação precoce crónica. Esses estudos têm estabelecido uma correlação entre os polimorfismos ligados ao gene transportador 5-HT e os tempos de ejaculação intravaginal (TLEI) curtos, nos homens com ejaculação precoce crónica. 15 No entanto, uma revisão recente especulou que tais polimorfismos só podem estar presentes numa fração dos homens com esse tipo de ejaculação precoce. 10 Wyllie e Powell 16 observam que É agora aceite que tanto os fatores biológicos como os psicológicos são importantes na etiologia da ejaculação precoce (EP). É de particular interesse a correlação entre a latência ejaculatória e os limiares de sensibilidade do pénis. Os homens com EP parecem ter uma resposta de acentuada sensibilidade à estimulação peniana e manifestam, geralmente, outras vias de reflexo anormais durante o processo ejaculatório, o que aponta para uma ligação entre a hipersensibilidade peniana e a EP. Considerando estas diferenças sensoriais, os medicamentos que produzem algum grau de dessensibilização no pénis, de forma seletiva, ou que têm uma ação no reflexo aferente-eferente, podem retardar a latência ejaculatória sem afetar a sensação de ejaculação de forma adversa. Tem sido igualmente apontado que os anestésicos tópicos podem ser usados no tratamento sintomático da EP, com a lógica de que a redução do input sensorial da glande do pénis através de agentes de dessensibilização pode ser um meio de aumentar o TLEI. 7 11
12 CONTEXTO Em contrapartida, a ejaculação precoce adquirida aparece frequentemente associada a problemas comórbidos que, por mecanismos que não são claros, resultam em mudanças no desempenho ejaculatório. No entanto, o tratamento bem sucedido do problema subjacente resulta, geralmente, no restabelecimento da ejaculação normal. Os fatores causais considerados mais frequentes são a ansiedade de desempenho, problemas psicológicos ou de relacionamento, e a disfunção erétil. As causas menos frequentes incluem a prostatite, o hipertiroidismo e os sintomas de privação de substâncias. 3 Critérios de diagnóstico O diagnóstico deve ser feito com base na história clínica e sexual. Deve dar-se atenção à duração do tempo até a ejaculação, ao grau do estímulo sexual, ao impacto na atividade sexual e na qualidade de vida, e ao uso ou abuso de substâncias, tal como está assinalado nas Linhas de Orientação da EAU. 6 Os questionários de resultados relatados pelos pacientes, para complementar a medição do TLEI auto-estimado, o grau de satisfação sexual, o controlo e a angústia, são habitualmente usados nos ensaios clínicos para avaliar tratamentos, mas a sua utilização não é recomendada na prática clínica. 6 O diagnóstico de ejaculação precoce baseia-se em entrevistas, no uso de questionários e na avaliação do TLEI feita pelo paciente. Mas os homens sentem relutância em procurar aconselhamento. A utilização de questionários de resultados relatados pelos pacientes está descrita na atualização recente das linhas de orientação da EAU. Apenas existem dois questionários que podem distinguir entre os pacientes que têm, ou não, EP: a Ferramenta de Diagnóstico de Ejaculação Precoce (Premature Ejaculation Diagnostic Tool - PEDT) e o Índice Árabe de Ejaculação Precoce (Arabic Index of Premature Ejaculation - AIPE). 6 As linhas de orientação da ISSM de 2014 também sugerem perguntas para avaliar o impacto do problema sobre o relacionamento e a qualidade de vida do paciente, assim como a identificação do paciente sofrer ou não de disfunção erétil ou se já foi tratado para a ejaculação precoce. 2 Vários outros questionários foram desenvolvidos, devendo-se, contudo, indicar que todos esses instrumentos assumem que o paciente é heterossexual. Não foi validado nenhum instrumento para os homens que têm relações sexuais com homens, mas a linguagem utilizada na PEDT tem sido sugerida como a que se tornou mais indicada para o estudo do problema. 17 O papel de questionários tais como o Perfil de Ejaculação Precoce (Premature Ejaculation Profile - PEP), o Índice de Ejaculação Precoce (Index of Premature Ejaculation - IPE) e o Questionário de Saúde Sexual Masculina da Disfunção 12
13 CONTEXTO Ejaculatória (Male Sexual Health Questionnaire MSHQ-EjD) são utilizados em ensaios clínicos para avaliar o efeito dos tratamentos, mas o seu uso é apontado como opcional na prática clínica quotidiana. 6 Contrariamente a outros problemas da função sexual, não existe uma necessidade absoluta do médico examinar o paciente. No entanto, alguns pacientes podem achar o exame físico tranquilizador. Se o paciente for diagnosticado com ejaculação precoce adquirida, então será desejável o médico examinar o paciente de forma direcionada, para procurar comorbidades que possam ter dado origem ao problema. Em pacientes com outras disfunções sexuais, também é desejável que o médico examine o paciente, de forma a poder identificar quadros clínicos subjacentes associados à ejaculação precoce, tais como a endocrinopatia, a doença de Peyronie, a uretrite ou a prostatite. Se tais problemas estiverem presentes, recomenda-se que sejam tratados antes de se procurar tratar a ejaculação precoce. Tem-se verificado que esse tratamento resulta, muitas vezes, no alívio da ejaculação precoce (adquirida). Uma série de algoritmos complexos têm sido propostos para o diagnóstico de ejaculação precoce. As linhas de orientação da ISSM citam os algoritmos desenvolvidos por Rowland, ilustrados abaixo. 18 História doente-parceira/o Apresentar queixa TLEI Grau de controlo ejaculatório percebido Angústia doente-parceira/o Início e duração da ejaculação precoce NÃO Disfunção Ejaculatória como EP Variável natural Tratamento Tranquilizador Educação Psicoterapia Terapia comportamental SIM Ejaculação precoce SIM Secundário a: Disfunção erétil Disfunção sexual SIM Tratar a condição primária NÃO Ejaculação precoce crónica Ejaculação precoce adquirida Tratamento Tratamento Comportamental/Psicoterapia Farmacoterapia Tratamento combinado Preferência do doente Farmacoterapia Comportamental/Psicoterapia Tratamento combinado Figura 6 Algoritmo de diagnóstico Tentativa de privação gradual de medicação em doentes selecionados (depois 6-8 semanas) para a ejaculação precoce. Adaptado de Rowland et al,
14 CONTEXTO Uma necessidade não-atendida Até há bem pouco tempo, não existiam tratamentos tópicos licenciados e havia apenas um tratamento sistémico que os médicos pudessem propor aos homens com EP. A relutância dos pacientes em falar sobre os seus problemas sexuais e o grau de insatisfação dos poucos que procuraram tratamento, traduz de forma clara, tanto a necessidade dos médicos em incentivar conversas sobre a saúde sexual, como a necessidade de uma oferta mais alargada de tratamentos aprovados, para os homens com diagnóstico de EP. 6,8 O lançamento do Fortacin, um tratamento tópico de administração na hora, para homens adultos, avaliado num conjunto de ensaios clínicos e disponível sob receita médica, oferece aos médicos a oportunidade de poderem ajudar estes pacientes, acrescentando este medicamento licenciado ao seu repertório clínico. 14
15 INTRODUÇÃO AO FORTACIN 2. Introdução ao Fortacin Indicação licenciada O Fortacin está indicado para o tratamento da ejaculação precoce primária em homens adultos. Apresentação O Fortacin é disponibilizado num recipiente de pulverização em doses calibradas, contendo a solução de lidocaína (150 mg/ml) e de prilocaína (50 mg/ml), com norflurano. Cada pulverização fornece 50 microlitros da solução, contendo 7.5 mg de lidocaína e 2.5 mg de prilocaína. (1 dose equivale a 3 pulverizações). O Fortacin é fornecido num recipiente de pulverização, pequeno e discreto. Posologia, administração e conservação A dose recomendada é de 3 pulverizações, aplicadas de modo a cobrirem a glande do pénis, após puxar o prepúcio para trás. Cada dose consiste num total de 22,5 mg de lidocaína e 7,5 mg de prilocaína por aplicação. Pode-se aplicar um máximo de 3 doses num período de 24 horas, com pelo menos 4 horas de intervalo entre as doses. 19 Populações especiais Idosos Não são necessários ajustes de dosagem nos idosos. Os dados existentes relativamente à eficácia e segurança do Fortacin nos pacientes com idade igual ou superior a 65 anos, são limitados. Insuficiência renal ou hepática Não foram efetuados estudos clínicos em pacientes com função renal ou hepática comprometida. Contudo, devido ao modo de administração e à absorção sistémica extremamente baixa, não é necessário qualquer ajuste de dosagem. É aconselhada precaução no caso de insuficiência hepática grave. População pediátrica Não existe utilização relevante do Fortacin na população pediátrica. A indicação do medicamento é para o tratamento da ejaculação precoce primária em homens adultos. Os pacientes devem aplicar 3 pulverizações sucessivas, de forma a administrar a dose aprovada para o fármaco. A solução deve ser aplicada na glande do pénis após a retração do prepúcio (consultar o Modo de Administração da secção 3, para mais informação). O fármaco deve ser administrado 5 minutos antes do início da relação sexual
16 INTRODUÇÃO AO FORTACIN Contraindicações O Fortacin é contraindicado para os pacientes e parceiras/os com antecedentes conhecidos de sensibilidade a anestésicos locais do tipo amida. Também é contraindicado para os pacientes e parceiras/os com hipersensibilidade ao norflurano. 19 Advertências e precauções especiais de utilização Estados relacionados com a anemia Os pacientes ou parceiras/os com deficiência de glucose-6-fosfato desidrogenase ou metemoglobinemia congénita ou idiopática são mais suscetíveis à metemoglobinemia induzida por medicamentos. Apesar da disponibilidade sistémica da prilocaína por absorção cutânea do Fortacin ser baixa, é necessária precaução nos pacientes com anemia, metemoglobinemia congénita ou adquirida, ou pacientes sujeitos a terapêutica concomitante conhecida por produzir estes estados. Interações Os pacientes que estão a tomar medicamentos antiarrítmicos de classe III (a amiodarona, por exemplo), devem ser tratados com precaução. Hipersensibilidades Os pacientes alérgicos a derivados do ácido para-aminobenzóico (procaína, tetracaína, benzocaína, etc.) não exibiram qualquer sensibilidade cruzada à lidocaína e/ou prilocaína; contudo, o Fortacin deve ser utilizado com precaução nos pacientes, ou parceiras/os, com antecedentes de sensibilidade a medicamentos, sobretudo se o agente etiológico for desconhecido. Precauções de utilização Na medida em que pode causar irritação ocular, devem ser tomadas precauções de modo a não permitir que o Fortacin entre em contacto com os olhos. Do mesmo modo, a perda dos reflexos protetores pode permitir a ocorrência de irritação da córnea e potencial abrasão. Não foi determinada qualquer absorção do Fortacin em tecidos conjuntivos. Em caso de contacto com os olhos, lave-os de imediato com água ou uma solução de cloreto de sódio, e proteja-os até voltar a ter sensibilidade nos olhos. O Fortacin pulverizado nas membranas mucosas do paciente ou da/o parceira/o, como a boca, o nariz e a garganta, ou transferido para a genitália feminina ou revestimento anal, pode ser absorvido e possivelmente resultar numa sensação de dormência/anestesia local temporária. Esta hipoestesia pode ocultar as sensações dolorosas normais e, por conseguinte, aumentar os perigos de lesões localizadas. O Fortacin pulverizado numa membrana timpânica lesada pode causar ototoxicidade do ouvido médio. 16
17 INTRODUÇÃO AO FORTACIN Observou-se a ocorrência de deterioração quando o Fortacin foi utilizado com preservativos femininos e masculinos à base de poliuretano. Uma taxa mais elevada de disfunção erétil e hipoestesia genital masculina poderá ser observada quando o Fortacin for utilizado com preservativos masculinos. A fórmula utilizada Fortacin é compatível com a maioria dos métodos contracetivos do tipo barreira Devido ao risco de transferência para a parceira, os pacientes que pretendam alcançar a conceção devem evitar utilizar o Fortacin ou, caso este seja fundamental para a penetração, devem lavar a glande da forma mais meticulosa possível, 5 minutos após a pulverização, mas antes da relação sexual. Pacientes com insuficiência hepática grave Devido à incapacidade de metabolização normal dos anestésicos locais, os pacientes com doença hepática grave estão em maior risco de desenvolvimento de concentrações plasmáticas tóxicas de lidocaína e prilocaína. Efeitos indesejáveis Os efeitos secundários da utilização do Fortacin são leves tanto para os pacientes como para as suas parceiras e há uma baixa probabilidade de absorção sistémica para ambos os fármacos. 19,20 As reações adversas mais frequentes registadas com a utilização deste medicamento em pacientes do sexo masculino foram efeitos locais de hipoestesia genital (4,5 %) e disfunção erétil (4,4 %). Estas reações adversas levaram à descontinuação do tratamento em 0,2 % e 0,5 % dos pacientes, respetivamente. As reações adversas mais frequentes registadas com a utilização deste medicamento nas parceiras foram uma sensação de ardor vulvovaginal (3,9 %) e hipoestesia genital (1,0 %). O desconforto ou a sensação de ardor vulvovaginal levou à descontinuação do tratamento em 0,3 % dos participantes. O Fortacin proporciona um tratamento de aplicação na hora, para a ejaculação precoce, geralmente com muito poucos efeitos adversos e contraindicações 17
18 INTRODUÇÃO AO FORTACIN 3. Propriedades do Fortacin Composição química A lidocaína, 2-(dietilamino)-N-(2,6-dimetilfenil) acetamida, (Figura 7) é um fármaco sintético, preparado pela primeira em Também conhecida por lignocaína ou xilocaína, a lidocaína é um sólido cristalino com a fórmula molecular C 14 H 22 N 2 O e um peso molecular de g/mol. A prilocaína, N-(2-metilfenil)-2-(propilamino) propanamida, (Figura 7) é um fármaco sintético, preparado pela primeira em A prilocaína é um sólido cristalino com a fórmula molecular C 13 H 20 N 2 O e um peso molecular de g/mol. Figura 7 As estruturas químicas da lidocaína e da prilocaína A combinação da lidocaína e da prilocaína numa proporção de 3:1 produz uma mistura de tipo eutético, ligeiramente oleosa. O Fortacin é uma solução desta mistura, com norflurano (1,1,1,2-tetrafluoretano), dissolvida numa concentração de 150 mg/ml de lidocaína mais 50 mg/ml de prilocaína. O produto não contém excipientes. O norflurano é, simultaneamente, o solvente e o propelente do spray, evaporando-se a seguir à pulverização no local de aplicação, deixando uma camada fina dos ingredientes ativos. O norflurano é um hidrofluoralcano (HFA), usado habitualmente como um propelente de aerossol e é biologicamente inerte. Cada recipiente do Fortacin contém 5 ml de solução de norflurano, lidocaína e prilocaína. O spray emite doses calibradas de 50 microlitros por cada pulverização. Modo de administração O Fortacin só está indicado para aplicação no tecido mucocutâneo da glande do pénis. 18
19 INTRODUÇÃO AO FORTACIN Preparação do spray Antes da utilização inicial, o recipiente do spray deverá ser brevemente agitado e, de seguida, preparado, com três pulverizações para o ar. Antes de cada utilização posterior, o recipiente deverá ser novamente agitado e, de seguida, preparado com uma pulverização. Aplicação É necessário puxar-se o prepúcio para trás, deixando a glande a descoberto. Depois de colocar o recipiente na vertical (com a válvula para cima), deve aplicar-se 1 dose do Fortacin na totalidade da glande, pressionando a válvula três vezes. Cada pulverização deve cobrir um terço da glande do pénis. Figura 8 Administração do Fortacin na glande do pénis O propelente (solvente) utilizado na fórmula do Fortacin evapora-se prontamente, enquanto os ingredientes ativos são absorvidos de forma transdérmica. No entanto, recomenda-se aos pacientes a limpeza de qualquer excesso após 5 minutos, antes da penetração, minimizando, desta feita, qualquer transferência dos anestésicos locais para a/o parceira/o. Mecanismo de ação Spray Aerosol Creme/ Pomada Na + canal Membrana mucosa LA não-ionizadas LA ionizadas Protão Figura 9 Figura esquemática dos canais de bloqueio do sódio, o mecanismo de ação dos anestésicos locais Axónio 19
20 PROPRIEDADES DO FORTACIN O mecanismo de ação do Fortacin consiste na absorção dos ingredientes ativos através do tecido mucocutâneo, após a aplicação do spray na glande do pénis. Tanto a lidocaína como a prilocaína são bloqueadores das vias do sódio (Figura 9). O seu modo de ação ocorre através do bloqueio dos poros dessas vias, numa proporção estequiométrica (1:1), impedindo, desta feita, o fluxo dos iões de sódio e a despolarização das membranas celulares. 21 Esta despolarização das membranas celulares resulta numa perda de sensação (anestesia). A aplicação local dos agentes anestésicos assegura que os efeitos se limitem ao(s) tecido(s) nos quais são aplicados - daí a designação de anestésicos locais. A aplicação do Fortacin na glande do pénis produz, deste modo, a dessensibilização do pénis. O Fortacin contém apenas formas básicas (não-carregadas) dos anestésicos locais, enquanto os cremes anestésicos contêm, geralmente, uma mistura de formas básicas e ionizadas. Apenas as formas básicas não-ionizadas conseguem penetrar na pele ou nas membranas mucosas. O sistema de pulverização em doses calibradas permite que os agentes dessensibilizantes sejam depositados em dose controlada, numa camada fina concentrada na glande do pénis. A vaporização instantânea do propelente força a lidocaína e a prilocaína para fora da solução, numa mistura de tipo eutético, formando uma substância ligeiramente oleosa ideal para aplicação tópica, permitindo um depósito adequado no local de aplicação. Os anestésicos locais do Fortacin não conseguem penetrar na pele intacta, plenamente queratinizada. Isto representa uma vantagem no tratamento da EP, uma vez que uma sensação plena pode ser mantida na zona restante do pénis. 7 Os anestésicos locais produzem uma inibição reversível localizada da condução nervosa, ao reduzirem a permeabilidade das membranas neuronais aos iões de sódio, cujo movimento é necessário para a transmissão de impulsos nervosos. 7 O seu uso combinado produz um início rápido da anestesia. A aplicação dos anestésicos locais nas suas bases livres, tal como acontece no Fortacin, aumenta a sua taxa de absorção e logo, o início da anestesia local. (Melhora, igualmente, a solubilidade do fármaco no propelente). Farmacodinâmica e farmacocinética Nenhum estudo farmacodinâmico primário ou secundário foi realizado com a fórmula do Fortacin. As propriedades farmacodinâmicas, tanto da lidocaína como da prilocaína, e os seus metabolitos, estão bem documentadas. Absorção Após a aplicação tópica do Fortacin, os níveis plasmáticos de lidocaína e de prilocaína foram inferiores ao nível associado à toxicidade (5000 ng/ml), tanto nos participantes do sexo masculino como nas participantes do sexo feminino. 20
21 PROPRIEDADES DO FORTACIN Os voluntários do sexo masculino apresentaram concentrações plasmáticas máximas de lidocaína inferiores a 4% dos níveis tóxicos, e de prilocaína inferiores a 0,4% dos níveis tóxicos, após a administração repetida. As voluntárias receberam doses repetidas de 60 mg, diretamente no colo do útero e na vagina, durante 7 dias. 20 Estas doses, correspondendo a cinco vezes a dose recomendada para os parceiros do masculinos, produziram níveis plasmáticos máximos de lidocaína inferiores a 8% dos níveis tóxicos, e de prilocaína inferiores a 1% dos níveis tóxicos. 19 A exposição sistémica à lidocaína e à prilocaína e metabolitos (a 2,6-xilidina e a o-toluidina, respetivamente) é baixa após a aplicação na glande dos pacientes do sexo masculino e após a aplicação no colo do útero/vagina das participantes do sexo feminino, mesmo em doses superiores às recomendadas. 19 A aplicação do Fortacin deposita uma camada fina dos anestésicos locais, que penetram nas membranas epiteliais não-queratizinadas, tal como a glande, sem penetrar na pele queratinizada intacta, tal como a da zona restante do pénis. 7,22 A absorção pode ser reduzida nos homens circuncidados, nos quais a quantidade de pele queratinizada pode estar aumentada. 7,22 Em termos de melhoria do TLEI, apesar de ser 24% mais baixa do que nos homens não circuncidados, a eficácia do produto nos homens circuncidados continuou a ser estatisticamente e clinicamente significativa, nas avaliações clínica. 22 A natureza ligeiramente oleosa desta mistura eutética garante a permanência do fármaco no local de aplicação, até que seja absorvido ou limpo com uma toalha húmida. 7,22 Mistura eutética: uma mistura de substâncias com um ponto de fusão mais baixo do que o de qualquer um dos seus componentes. Farmacocinética Realizaram-se estudos farmacocinéticos em duas ocasiões, nos dias 7 e 14, com 16 voluntários, por um período de 21 dias durante os quais se aplicou a fórmula, diariamente. 20 O fármaco foi aplicado pelo menos uma vez por dia, e três vezes por dia em duas ocasiões, com intervalos de 4h entre aplicações. A anestesia foi observada num tempo igual ou inferior a 5 minutos após a aplicação. 17 Recolheram-se amostras de plasma nos dias 1 e 21, antes da administração da dose e novamente após 1h, 2h, 4h e 8h após a administraçãoda dose. Nos dias 7 e 14, recolheu-se uma amostra única, 1.5 horas após a administração da terceira dose do fármaco
22 PROPRIEDADES DO FORTACIN Dose única A lidocaína e a prilocaína foram quantificadas no plasma, 1 hora após a administração da dose. As concentrações máximas (C max ) para a lidocaína e para a prilocaína num indivíduo do sexo masculino foram de, respetivamente, 96 ng/ml e 13 ng/ml, ocorrendo 2h após a administração da dose. As concentrações plasmáticas de ambos os fármacos e seus metabolitos, foram muito baixas. 20,23 No dia 21, os valores médios para a C max foram de 56.1 ng/ml para a lidocaína e de 7.2 ng/ml para a prilocaína. 20 Parâmetro Lidocaína Prilocaína Dia 1 Dia 21 Dia 1 Dia 21 AUC (0 t) 164.2± ± ± ± 12.5 (h*ng/ml) (12) (12) (4) (8) Figura 10 Parâmetros farmacocinéticos após a administração de uma dose única do Fortacin. Os dados mostram os valores médios ± desvio padrão (DP) para (n) participantes 20 C max (ng/ml) 34.5± ± ± ± 2.5 (12) (12) (4) (8) t max (h) 2.58± ± ± ± 1.0 (12) (12) (4) (8) t ½ (h) 2.8± ± ± 0.1 (6) (3) (1) (3) Doses múltiplas As concentrações máximas de lidocaína e de prilocaína, medidas em qualquer um dos participantes, em qualquer um dos dias, foram de ng/ml para a lidocaína, no dia 14, e de ng/ml para a prilocaína, no dia 7. As concentrações máximas de lidocaína e de prilocaína, após de 3 aplicações do Fortacin, com 4 horas de intervalo entre doses, em voluntários saudáveis do sexo masculino, foram bem mais baixas do que as concentrações plasmáticas associadas à toxicidade sistémica (>5,000 ng/ml tanto para a lidocaína como para a prilocaína): um valor aproximadamente 29 vezes mais baixo para a lidocaína e quase 258 vezes mais baixo para a prilocaína. 20 Lidocaína Prilocaína Figura 10 Concentrações plasmáticas médias da lidocaína e da prilocaína, a seguir às 3 x 30 mg doses do Fortacin aplicado na glande do pénis, num intervalo de 4 horas. Todos os dados com base em n = 12 pacientes 20 Dia 7 Média ± DP 84.3 ± ± 5.4 (ng/ml) 1.5 h após 3ª dose intervalo Dia 21 Média ± DP 89.0 ± ± 4.1 (ng/ml) 1.5 h após 3ª dose intervalo
23 AVALIAÇÃO CLÍNICA 4. Avaliação clínica Cinco ensaios clínicos aleatorizados (ECAs) avaliaram a eficácia do Fortacin (conhecido formalmente como PSD-502) no tratamento da ejaculação precoce primária. Estes estudos contaram com um total de 596 pacientes do sexo masculino e 584 parceiras desses participantes. Os estudos incluem: l l l l 1 estudo de prova de conceito de fase II (ANAE ) 1 estudo confirmatório de fase II (PSD502-PE-001) 1 estudo de determinação da dose terapêutica (PSD502-PE-005) 2 estudos determinantes (PSD502-PE-002 e PSD502-PE-004) Estudos de Fase II Um resumo dos três estudos de fase II é apresentado na Figura 12. Estes estudos tinham indicadores principais semelhantes, mas diferiam nos indicadores secundários. Estudo Características do Estudo Tratamento e pacientes Indicador principal Indicador(es) secundário(s) ANAE Sem ocultação, estudo de braço único, controlo seguido por quatro doses 14 pacientes com ejaculação precoce primária dose de 30 mg Aumento do TLEI Satisfação do paciente e da parceira PSD502- PE-005 Dupla ocultação, controlado com placebo, estudo cruzado de 4 vias 35 pacientes com ejaculação precoce crónica doses de 3, 30 e 53 mg Aumento do TLEI Proporção de penetrações Proporção de ejaculações Dormência PSD502- PE-001 Dupla ocultação, controlado com placebo, estudo de grupo paralelo 554 pacientes enquadrados nos critérios da EP, do DSM-IV dose: 4 x 30 mg* 2 x TLEI 4 min TLEI QdVS Mudanças na pontuação do IEC Figura 12 Resumo dos três estudos de fase II * fórmula incluiu etanol (DSM = Manual de Diagnóstico e Estatística das Perturbações Mentais; ICE = Índice de Controlo Ejaculatório; QdVS = Qualidade de Vida Sexual) 23
24 AVALIAÇÃO CLÍNICA O Estudo ANAE O ANAE foi um estudo de prova de conceito, sem ocultação, de braço único, não controlado e conduzido pelo investigador. 24 Tinha como principal objetivo medir a mudança do TLEI dos homens com ejaculação precoce, antes e depois da aplicação do Fortacin no pénis. Os sujeitos elegíveis para participar foram homens de idade igual ou superior a 18 anos (intervalo de 23-70), com relato de insatisfação devido à ejaculação precoce, e a quem tinha sido sugerida uma consulta de urologia. Foi dada a indicação aos participantes para utilizarem o spray em cinco relações sexuais consecutivas e registarem, em cada ocasião, o número de pulverizações e duração da utilização. Os participantes foram instruídos em aplicar entre 3 a 5 pulverizações do Fortacin na glande do pénis (dependendo do tamanho da glande), aproximadamente 15 a 30 min antes do início da relação sexual. Selecionou-se uma amostra de 15 participantes, que iria proporcionar significância estatística caso o tempo de latência ejaculatória intravaginal (TLEI) aumentasse de 2 min para > 10 min. Foram tratados 14 participantes, dos quais 11 completaram o estudo. Pediu-se aos casais para medir, numa ocasião, o TLEI sem tratamento. Em cinco ocasiões subsequentes, foi-lhes pedido para aplicarem o spray, deixarem o seu conteúdo atuar durante 10 15min, e limparem-no cuidadosamente antes do início da relação sexual. O TLEI foi medido pelo cronómetro e pediu-se a ambos os parceiros para avaliarem o seu grau de satisfação individual, comparativamente à relação sexual inicial sem tratamento. Também lhes foi pedido para registarem qualquer efeito adverso ou comentário. O TLEI médio aumentou, neste estudo, até um valor 8 vezes mais elevado, de 1 min 24s para 11 min 21 s (p=0.008) Não se registaram diminuições do TLEI em qualquer participante. Tanto os participantes como as suas parceiras avaliaram o seu grau de satisfação sexual média como melhor. Apenas dois pacientes registaram uma sensação de dormência na glande, mas não a consideraram prejudicial. O Estudo PSD502-PE-005 O estudo PE-005 tinha como objetivo principal avaliar o efeito de 3 doses (3 mg, 30 mg, e 53 mg) do Fortacin no TLEI. 17 O desenho do estudo foi multicêntrico, com dupla ocultação, controlado com placebo, e cruzado com 4 vias (Figura 13). Após as avaliações de triagem, os participantes passaram por uma avaliação inicial de 2 semanas, durante a qual lhes foi pedido para registarem pelo menos uma relação sexual com um TLEI cronometrado 1 min. Os sujeitos elegíveis para continuar no estudo receberam um número aleatorizado, correspondente a sequências pré-determinadas do Fortacin ou do placebo. A duração do tratamento foi de 4 semanas (1 semana para o placebo e 1 semana para cada uma das 3 doses). 24
25 AVALIAÇÃO CLÍNICA Consulta 1 Avaliação Consulta 2 Aleatória Consulta 3 Consulta 4 Consulta 5 Acompanhamento Consulta 6 Fortacin 3mg, 30mg, 53mg OU Placebo Período 1 Transversal Períodos 2, 3 & 4 Transversal 2 Semanas Período de avaliação 1 Semana Período transversal e dupla-ocultação 1 Semana 1 Semana 1 Semana Figura 13 O desenho do Estudo PSD502-PE-005 As três doses escolhidas para serem testadas foram de 30 mg (3 pulverizações, cada uma contendo 7.5 mg de lidocaína e 2.5 mg de prilocaína); uma dose baixa de 3 mg (3 pulverizações, cada uma contendo 0.75 mg de lidocaína e 0.25 mg de prilocaína) e uma dose elevada de 53 mg (3 pulverizações, cada uma contendo mg de lidocaína e 4.45 mg de prilocaína). Os participantes deste estudo tinham uma idade 18 anos, enquadravam-se nos critérios da ISSM para a ejaculação precoce, então definida com um TLEI inicial 1 min. Os participantes, com ejaculação precoce crónica, encontravam-se num relacionamento estável, monogâmico, heterossexual. Os 35 participantes tratados não eram circuncidados. A variável principal da eficácia foi a mudança média do TLEI, a partir dos valores iniciais. As variáveis secundárias da eficácia foram a proporção de participantes com um TLEI médio de >1 min e de >2 min, e a proporção de participantes com um aumento do TLEI médio até um valor pelo menos 2 vezes mais elevado do que os valores iniciais. Todos os participantes que receberam o fármaco foram incluídos na População com Intenção de Tratamento (Intent-to-Treat - ITT). A população ITT foi utilizada para a análise de todas as características de base e para a análise principal da eficácia dos dados. A população por protocolo (per protocol) foi utilizada como um subconjunto da população ITT, sendo constituída após a exclusão dos participantes com grandes desvios protocolares, que poderiam afetar as avaliações de eficácia. Todos os participantes que receberam o fármaco do estudo foram incluídos na população de segurança. A população de segurança foi utilizada para a análise dos dados de segurança. 25
26 AVALIAÇÃO CLÍNICA Indicador principal Apenas o tratamento com a dose de 30 mg dose retardou a ejaculação de uma forma significativa, comparativamente ao placebo, (proporção da média geométrica para com o placebo foi de 1.7; mais baixo 95% CL 1.19; p=0.008). A proporção de participantes com um aumento do TLEI médio até um valor pelo menos 2 vezes mais elevado, foi de 32.4% para o placebo e de 57.1%, 65.7% e 47.1% para as respetivas doses do Fortacin de 3mg, 30mg, e 53mg. No entanto, uma percentagem significativa de participantes (12%; 4 de 34 participantes) teve hipoestesia com a dose de 53 mg, resultando na falha da ejaculação (os dados do TLEI inicial foram utilizados na ausência de dados do TLEI durante um período individual). Os dados estão ilustrados na Figura 14. Placebo Fortacin 3 mg Fortacin 30 mg* Fortacin 53 mg N TLEI inicial Média Geométrica Média ± DP 63 ± ± ± ± 65 TLEI médio Média Geométrica Média ± DP ± ± ± ± Figura 14 Médias do TLEI, da população com intenção de tratamento (ITT), do Estudo PSD Proporção Média Geométrica Média ± DP ± ± ± ± 2.1 Indicadores secundários A dose de 30 mg foi mais eficaz do que as outras doses, no que diz respeito aos indicadores secundários. Uma proporção maior deste grupo atingiu valores do TLEI 1 min, 2 min ou atingiu um valor do TLEI duas vezes mais elevado do que o valor inicial (Figura 15). Placebo (N=34) Fortacin 3mg (N=35) Fortacin 30mg* (N=35) Fortacin 53mg (N=34) TLEI médio > 1 min 24 (70.6%) 26 (74.3) 28 (80.0%) 21 (61.8%) TLEI médio > 2 mins 9 (26.5%) 18 (51.4%) 20 (57.1%) 17 (50%) Figura 15 Resultados dos indicadores secundários do PSD TLEI médio 2 vezes mais elevado do que o Valor Inicial 11 (32.4%) 20 (57.1%) 23 (65.7%) 16 (47.1%) *Esta é a versão licenciada e disponível do Fortacin 26
27 AVALIAÇÃO CLÍNICA O Estudo PSD502-PE-001 O PSD502-PE-001 foi um estudo multicêntrico, com dupla ocultação, controlado com placebo, de grupo paralelo, constituído por participantes que preenchiam os critérios do DSM-IV, no qual não havia um tempo limite para o TLEI. 25 O estudo foi feito com uma fórmula contendo uma mistura de etanol e norflurano, como solventes, com cada pulverização do spray a acrescentar 7.4 mg de etanol ao volume dos ingredientes ativos. Foi dada a indicação aos participantes para aplicarem 3 pulverizações na glande do pénis, aproximadamente 15 min antes da relação sexual, e de limparem qualquer excesso de spray antes da penetração. Os pacientes foram instruídos para utilizarem o spray num total de 4 ocasiões durante o tempo de tratamento de 1 mês, mas não mais do que uma vez por cada período de 24h. Estudo Mês 1 Estudo Mês 2 Consulta 1 Avaliação Consulta 2 Aleatória FORTACIN Consulta 2 Acompanhamento PLACEBO Linha de base Período transversal e dupla-ocultação *Consulta 3 Acompanhamento - realizada 2 semanas depois do fim do Estudo Mês 2 ou último registo TLEI, consoante o que ocorreu primeiro. Figura 16 O desenho do Estudo PSD502-PE-001 O estudo PSD502-PE-001 tinha como objetivo principal avaliar a eficácia do Fortacin, comparativamente ao placebo, no tratamento de pacientes com ejaculação precoce. O estudo teve um período inicial de 1 mês, no qual os pacientes registaram o TLEI inicial em três ocasiões separadas e completaram questionários iniciais. O indicador principal foi definido como a proporção de pacientes com um TLEI pós-tratamento 4 minutos, em pelo menos duas relações sexuais. A mudança dos valores iniciais do TLEI foi promovida a indicador co-principal numa alteração do protocolo. As variáveis secundárias de eficácia foram: a responsividade do TLEI (a responsividade foi definida como 2 registos do TLEI de 2 min ou 3 min no Mês 2) e a mudança nas pontuações do ICE e da QdVS. O estudo foi concebido para detetar uma diferença significativa entre grupos de tratamento, baseando-se nos resultados do estudo ANAE (desenhado com 70% possibilidade para mostrar uma diferença de resposta de 40% entre o Fortacin e o placebo). 27
28 AVALIAÇÃO CLÍNICA TLEI 2 min TLEI 3 min TLEI 4 min Figura 17 Resultados dos indicadores secundários do PSD Placebo 8/23 (35%) 3/23 (13%) 3/23 (13%) Fortacin TM 11/20 (55%) 8/20 (40%) 5/25 (20%) Um total de 54 participantes foram tratados neste estudo (26 participantes com Fortacin e 28 com placebo). As mudanças da média observada entre os valores iniciais e o final do período de tratamento foram de 3.8 min no grupo do Fortacin, comparado com 0.7 min no grupo de placebo. As médias geométricas estimadas para o TLEI durante o 2º mês, derivadas da análise dos dados transformados logaritmicamente, foram de 2.50 min para o Fortacin e 1.04 min para o placebo, representando um valor 2.4 vezes mais elevado (95% CI: 1.3 to 4.4; p<0.01) a favor do Fortacin. Vinte e cinco por cento dos participantes tratados com o Fortacin foram considerados responsivos (com um TLEI 4 min em pelo menos dois encontros) comparado com 13% dos participantes do grupo de placebo. Registaram-se tendências positivas, com melhorias do TLEI de 2, 3 ou 4 min (Figura 17), mas as diferenças não foram significativas. Também se verificaram tendências positivas nos ICEs preenchidos pelos participantes e nos questionários de QdVS preenchidos tanto pelos participantes como pelas suas parceiras. Ao todo, 35 dos 42 (83%) pacientes consideraram o spray de utilização fácil. Ocorreu uma sensação de dormência localizada, leve a moderada, em três (12%) dos pacientes tratados com o Fortacin ; mas tal não levou à descontinuação do tratamento. Estudos de Fase III Os estudos determinantes PSD502-PE-002 e PSD502-PE-004 foram estudos de fase III, multicêntricos, aleatorizados, com tratamento em dupla ocultação, controlados com placebo, com fase de seguimento aberta, em participantes com ejaculação precoce crónica e as suas parceiras sexuais. A figura 18 mostra um resumo dos dois estudos, que partilham o mesmo desenho, ainda que apenas se tenham avaliado os níveis de metabolitos do fármaco no primeiro estudo. Ambos os estudos avaliaram a eficácia e segurança de uma dose de 30 mg de Fortacin no tratamento da ejaculação precoce. 28
29 AVALIAÇÃO CLÍNICA Estudo Características do Estudo Tratamento e pacientes Indicador principal Indicador(es) secundário(s) PSD502- PE-002 Dupla ocultação, controlado com placebo. Eficácia, segurança e farmacocinética dos metabolitos 256 pacientes com ejaculação precoce crónica, tratamento de 12 semanas com uma dose de 30 mg TLEI e Índice de Ejaculação Precoce (IEP) Segurança e tolerabilidade nos pacientes e parceiras, Perfil de Ejaculação Precoce PSD502- PE-004 Dupla ocultação, controlado com placebo. Eficácia, segurança e tolerabilidade 300 pacientes com ejaculação precoce crónica, tratamento de 12 semanas com uma dose de 30 mg TLEI e Índice de Ejaculação Precoce (IEP) Relação entre o TLEI e o IEP, diferenças de importância mínima nos campos do IEP Segurança e tolerabilidade nos pacientes e parceiras, Perfil de Ejaculação Precoce Figura 18 Os estudos determinantes de fase III com o Fortacin Consulta 1 Avaliação Consulta 2 Aleatória Consulta 5 Fase estudo aberto Consulta 8 Fim do Estudo Linha de Base 3 relações sexuais Fortacin n=171 Placebo n=85 Fase estudo aberto sem uso mínimo Fase de tratamento de dupla ocultação 1 relação sexual por mês Barra de escala de tempo (não-linear): cada marca representa um mês Figura 19 Desenho do estudo PSD502-PE-002 O Estudo PSD502-PE-002 Este estudo tinha como objetivo determinar o efeito do Fortacin no Índice de Ejaculação Precoce (IEP) e no TLEI dos homens com ejaculação precoce crónica. 26 Homens com um TLEI registado de 1 min em pelo menos duas relações sexuais no decurso de um período inicial de 4 semanas, foram 29
30 AVALIAÇÃO CLÍNICA aleatorizados para receber tratamento com dupla ocultação com 30 mg do Fortacin (n= 171) ou placebo (n=85), durante 3 meses. O tratamento foi aplicado de forma tópica, 5 minutos antes do início de uma relação sexual. Os pacientes completaram os questionários do Índice de Ejaculação Precoce (IEP) e do Perfil de Ejaculação Precoce (PEP), à entrada e durante as visitas mensais, e registaram os valores do TLEI cronometrado, em cada relação sexual. A segurança foi avaliada através do registo de acontecimentos adversos e medidas elementares de segurança. Indicadores principais: registos do TLEI cronometrado e respostas dos resultados relatados pelos pacientes, no questionário IEP. Resultados: 256 homens com EP foram aleatorizados, a partir de 38 centros nos Estados Unidos, Canadá e Polónia. A média geométrica do TLEI aumentou dos valores iniciais de 0.56 min (grupo do Fortacin ) e 0.53 min (grupo de placebo) para, respetivamente, 2.60 min e 0.80 min, no decurso de 3 meses (Figura 20). Fortacin produziu um aumento elevado e estatisticamente significativo, entre o TLEI médio inicial e o TLEI médio, após 3 meses de tratamento, comparativamente ao placebo. A média geométrica do TLEI aumentou até um valor clinicamente significativo de 2.6 min, o que representa um aumento até um valor 4.7 vezes mais elevado do que o valor inicial, enquadrando-o no que geralmente se considera de intervalo normal, mais de três vezes maior do que o TLEI dos pacientes tratados com placebo. Figura 20 TLEI médio: valores iniciais e após 3 meses de tratamento; população com intenção de tratamento (ITT) Média geométrica do TLEI, min Fortacin Placebo Linha da Base Meses Período Tratamento 2.6 Registaram-se aumentos significativamente superiores nas pontuações dos campos do IEP correspondentes ao controlo ejaculatório, à satisfação sexual e à (redução da) angústia, no grupo do Fortacin, comparativamente ao grupo de placebo. A diferença de mudança média entre tratamentos, a partir dos valores iniciais, foi de 5.0 pontos no campo do IEP correspondente ao controlo ejaculatório, 4.6 pontos no campo do IEP correspondente à satisfação sexual, e 2.5 pontos no campo do IEP correspondente à angústia (Figura 21). 30
31 AVALIAÇÃO CLÍNICA Alteração na média ajustada de pontuação IPE Controlo Satisfação Angústia Fortacin Placebo Figura 21 Melhorias nas pontuações dos campos do IEP, após 3 meses Estes resultados foram apoiados pelas melhorias em todos os indicadores secundários, com 57.5% dos pacientes tratados com o Fortacin a registarem um TLEI 2 min (Figura 22). 90 % Indivíduos Fortacin Placebo TLEI > 1min TLEI > 2min Figura 22 Proporção de pacientes com valores médios registados do TLEI 1 min e 2 min, após 3 meses de tratamento. As mudanças ao fim dos 3 meses foram significativamente superiores com o Fortacin vs placebo (p<0.0001) O estudo PSD502-PE-004 Este estudo também teve como objetivo determinar os efeitos do Fortacin no IEP e no TLEI dos homens com ejaculação precoce crónica. 27 O desenho do estudo foi idêntico ao do estudo PSD502-PE-002, à exceção das duas visitas médicas adicionais incluídas na fase aberta, que teve uma duração de 9 meses, em vez de 5 meses (Figura 23). Os critérios de triagem e eficácia foram idênticos aos do estudo PSD502-PE-002. Foram aleatorizados 300 homens com ejaculação precoce, a partir de 31 centros da Europa. A média geométrica do TLEI (intervalo) aumentou de um valor inicial de 0.6 min em ambos os grupos, para 3.8 min ( ) no grupo do Fortacin e 1.1 (0 15.0) min no grupo do placebo, no decurso de 3 meses (Figura 24). Após ajustes de proporção entre os grupos de tratamento, estes valores representam aumentos de 6.3 e 1.7 vezes nas médias geométricas ajustadas. 31
32 AVALIAÇÃO CLÍNICA Consulta 1 Avaliação Consulta 2 Aleatória Consulta 5 Fase estudo aberto Consulta 10 Fim do Estudo Fortacin Linha de Base 3 relações sexuais Placebo sem uso mínimo Fase de tratamento de dupla ocultação 1 relação sexual por mês Figura 23 Desenho do estudo PSD Barra de escala de tempo (não-linear): cada marca representa um mês Verificaram-se aumentos significativamente superiores nas pontuações dos campos do IEP correspondentes ao controlo ejaculatório e à satisfação sexual, no grupo do Fortacin, comparativamente ao grupo de placebo. Os resultados indicaram uma diferença média de 7.0 ± 0.59 pontos entre tratamentos, a partir dos valores iniciais, no campo do IEP correspondente ao controlo ejaculatório e uma diferença média de 5.9 ± 0.57 pontos no campo do IEP correspondente à satisfação sexual (ambos com p<0.001) (Figura 25). Estes resultados foram apoiados pelas melhorias obtidas em todos os indicadores secundários. Verificou-se um aumento significativamente superior nas pontuações do campo da angústia (representando uma redução da angústia) no grupo do Fortacin, comparativamente ao grupo de placebo, após 3 meses de tratamento, com uma diferença pontual média de 2.8 (0.28) pontos, a partir dos valores iniciais registados neste campo (p<0.001). No final do período de tratamento, 66% dos pacientes classificaram o Fortacin como bom ou excelente. 4.5 Figura 24 Melhorias na média geométrica do TLEI após 3 meses. Aumentos até um valor 6.3 e 1.7 vezes mais elevado no grupo do Fortacin e no grupo de placebo, respetivamente (p< 0.001, 95% CI min) Média geométrica do TLEI, min Fortacin Placebo Linha de Base Meses Período Tratamento
33 AVALIAÇÃO CLÍNICA O Fortacin foi bem tolerado e nenhum efeito adverso sistémico foi relatado. Foram relatados efeitos adversos localizados, relacionados com o tratamento, por parte de 2.6% e 3.1% dos pacientes e das suas parceiras, respetivamente Alteração na média ajustada de pontuação IPE Controlo Satisfação Domínio IPE Angústia Fortacin Placebo Figura 25 Melhorias nas pontuações dos campos do IEP após 3 meses. P<0.001 para os campos do controlo ejaculatório, satisfação e angústia, na comparação do Fortacin com o placebo Resultados principais dos dois estudos 16 O Fortacin aumentou a média geométrica dos (TLEI)s até um valor 4.6 vezes e 6.3 vezes mais elevado, nos dois estudos de 0.56 min ( ) para 2.6 min ( ) e de 0.6 min (0-2.3) para 3.8 min ( ) as mudanças foram significativamente melhores do que as mudanças observadas com o placebo (p<0.0001) O Fortacin produziu melhorias superiores nos campos do IEP relativos ao controlo ejaculatório, satisfação sexual e (redução da) angústia, comparativamente ao placebo (p< e p<0.001). O tratamento com o Fortacin teve uma maior probabilidade de produzir um TLEI médio >2 min do que o tratamento com o placebo até um valor 7.9 vezes (p<0.0001) e 12.8 vezes mais elevado (p<0.001), nos dois estudos Comparativamente ao grupo de placebo, o tratamento com o Fortacin, registou o aumento de pelo menos um ponto em cada um dos 4 campos do PEP (p<0.0001, para ambos). A avaliação da satisfação dos pacientes favoreceu o Fortacin, 56.1% e 65.9% dos pacientes classificaram-no como bom ou excelente Apenas 8.9% e 14.6% dos pacientes tratados com o placebo classificaram o seu tratamento como bom ou excelente O Fortacin proporciona melhorias significativas no desempenho ejaculatório e na satisfação dos pacientes 33
34 AVALIAÇÃO CLÍNICA Seguimento em fase aberta No final da fase com dupla ocultação, os pacientes de ambos os estudos puderam optar por continuar com o tratamento com o Fortacin, em fase aberta. Este seguimento ocorreu durante um período de 5 e 9 meses, nos respetivos estudos. Um total de 497 participantes (98.4% dos que concluíram a fase com dupla ocultação) entrou na fase aberta dos estudos. A maioria (90.3%) dos participantes concluiu a fase aberta. As razões mais frequentes para a descontinuação numa fase inicial do tratamento foram por motivos de: pedido do participante/parceira e por desistência de participação na fase de seguimento (4.4% cada). Apenas 1 paciente (0.2%) descontinuou o tratamento devido a efeitos adversos. 20 Observaram-se melhorias acentuadas do TLEI durante a primeira avaliação após o início do tratamento com o Fortacin, nos participantes que receberam tratamento com o placebo durante a fase com dupla ocultação e que mudaram para o Fortacin durante a fase aberta (Figura 26). Os participantes tratados com o Fortacin durante a fase de tratamento com dupla ocultação obtiveram, em ambos os estudos, uma proporção ligeiramente maior entre os valores iniciais da média geométrica do TLEI e das visitas 6-8 na fase aberta de tratamento, comparativamente aos participantes que tinham recebido o placebo durante a fase de estudo com dupla ocultação. 20 Mudanças do TLEI no decurso de 3 meses (fase de estudo, com dupla ocultação) 3.5 Figura 26 TLEI médio com o passar do tempo, nos pacientes tratados com o Fortacin durante a fase de estudo com dupla ocultação 16 Média geométrica do TLEI, min Fortacin n=358 Placebo n= Linha de Base Mês 1 p<0.001 entre grupos de 1,2, e 3 meses Mês 2 Mês 3 34
35 AVALIAÇÃO CLÍNICA Também se observaram melhorias nas pontuações dos campos do IEP entre o final da fase de tratamento com dupla ocultação e o final da fase de tratamento aberta. As mudanças médias, a partir dos valores iniciais, nas pontuações do controlo ejaculatório, satisfação sexual e sentimento de angústia foram, respetivamente, de 12.3, 10.9, e 5.3 pontos, no final da fase de tratamento aberta. Estes resultados demonstram que o Fortacin foi eficaz no adiamento da ejaculação, na melhoria do controlo ejaculatório e do grau de satisfação sexual, e na redução da angústia, tanto no final da fase de tratamento aberta (12º mês) como no final do período de tratamento com dupla ocultação (3º mês). 20 O Fortacin é geralmente eficaz e parece proporcionar benefícios adicionais com o seu uso repetido Os resultados da fase aberta indicam melhorias consistentes nos valores do TLEI, no decurso do tratamento (Figura 27). Adicionalmente, houve uma melhoria observada no TLEI dos sujeitos que mudaram do placebo para o Fortacin. 16 Foram observadas melhorias no TLEI, de mês para mês, durante a fase com dupla ocultação, quando se combinaram os resultados dos dois estudos. 16 Estes resultados também indicaram a ausência de taquifilaxia com o Fortacin. Os autores observam que, de facto, Parece plausível que, à medida que o tratamento com [Fortacin ] prolonga o TLEI através da sua ação sobre os fatores neurogénicos, o sujeito se torne mais confiante na sua capacidade de controlar a ejaculação, e que isso tenha um efeito positivo nos fatores psicogénicos, resultando em melhorias acrescentadas nos sintomas e sinais da EP. Alteração geométrica do TLEI, min Fortacin Placebo n= n=358 Linha de Base * Todos os doentes usaram Fortacin n= n=358 3 Meses DB Tratamento n=75* n=144* 5 Meses OL Tratamento n=73* n=142* 9 Meses OL Tratamento Figura 27 Melhorias progressivas do TLEI ao longo dos estudos de fase III Adaptado de Wyllie & Powell 35
36 AVALIAÇÃO CLÍNICA Resumo da Tolerabilidade Resumo do perfil de segurança. 19 A tolerabilidade do Fortacin foi avaliada com base em 596 pacientes do sexo masculino que procederam à sua aplicação durante a realização de ensaios clínicos. A tolerabilidade foi igualmente avaliada em 584 parceiras desses participantes. Verificou-se a ocorrência de reações adversas em 9,6 % dos participantes e 6,0 % das parceiras. Os casos foram, na sua maioria, classificados como ligeiros ou moderados. As reações adversas mais frequentes, registadas com a utilização deste medicamento em pacientes do sexo masculino, foram efeitos locais de hipoestesia genital (4,5 %) e disfunção erétil (4,4 %). Estas reações adversas levaram à descontinuação do tratamento em 0,2 % e 0,5 % dos pacientes, respetivamente. As reações adversas mais frequentes registadas nas parceiras, com a utilização deste medicamento, foram sensação de ardor vulvovaginal (3,9%) e hipoestesia genital (1,0%). O desconforto ou a sensação de ardor vulvovaginal levou à descontinuação do tratamento em 0,3% dos participantes. A frequência das reações adversas é definida do modo seguinte: muito frequentes ( 1/10), frequentes ( 1/100 a < 1/10), pouco frequentes ( 1/1000 a < 1/100), raros ( 1/ a < 1/1000), muito raros (<1/10 000), desconhecida (não pode ser calculada a partir dos dados disponíveis). As reações adversas são apresentadas por ordem decrescente de incidência dentro de cada categoria de frequência. Reações Adversas Medicamentosas nos Participantes tratados à Glande do Pénis Classe de sistemas de órgãos Frequência Reações Adversas Perturbações do foro psiquiátrico Pouco frequentes Orgasmo anormal Doenças do sistema nervoso Pouco frequentes Dor de cabeça Doenças respiratórias, torácicas e do mediastino Pouco frequentes Irritação da garganta Afeções dos tecidos cutâneos e subcutâneos Pouco frequentes Irritação cutânea Figura 28 Efeitos indesejáveis observados nos homens tratados Doenças do sistema reprodutor e da mama Perturbações gerais e alterações no local de administração Frequentes Pouco frequentes Pouco frequentes Hipoestesia dos genitais masculinos, disfunção erétil, sensação de ardor genital Eritema genital, falha na ejaculação, parestesia dos genitais masculinos, dor peniana, distúrbio peniano, prurido genital Pirexia 36
37 AVALIAÇÃO CLÍNICA Reações Adversas Medicamentosas nas Parceiras Classe de sistemas de órgãos Frequência Reações Adversas Infeções e infestações Pouco frequentes Candidíase vaginal Doenças do sistema nervoso Pouco frequentes Dor de cabeça Doenças respiratórias, torácicas e do mediastino Pouco frequentes Irritação da garganta Doenças gastrointestinais Pouco frequentes Desconforto anorretal, parestesia oral Doenças renais e urinárias Pouco frequentes Disúria Doenças do sistema reprodutor e da mama Frequentes Pouco frequentes Sensação de ardor vulvovaginal, hipoestesia Desconforto vulvovaginal, dor vaginal, prurido vulvovaginal Figura 29 Efeitos indesejáveis observados nas parceiras Sobredosagem Tendo em conta que o Fortacin é aplicado de forma tópica na glande do pénis, o risco de sobredosagem é baixo. Em doses elevadas, a prilocaína pode causar um aumento do nível de metemoglobina, sobretudo em conjunção com agentes indutores de metemoglobina (as sulfonamidas, por exemplo). Qualquer situação de metemoglobinemia clinicamente significativa deve ser tratada com uma injeção intravenosa lenta de cloreto de metiltionínio. No caso da ocorrência de outros sintomas de toxicidade sistémica, prevê-se que os sinais tenham uma natureza semelhante aos observados após a administração de anestésicos locais por outras vias. A toxicidade anestésica local manifesta-se por meio de sintomas de excitação do sistema nervoso e, em casos graves, por sintomas de depressão nervosa central e cardiovascular. Os sintomas neurológicos graves (convulsões e depressão do SNC) têm de ser tratados de forma sintomática por suporte respiratório e administração de medicamentos anticonvulsivantes. 37
38 UTILIZAÇÃO NA PRÁTICA CLÍNICA 5. Utilização na prática clínica Linhas de orientação e recomendações O entendimento crescente da ejaculação precoce levou ao desenvolvimento de linhas de orientação baseadas na evidência, para a definição da doença, tanto por parte da European Association of Urology (EAU) como da International Society of Sexual Medicine (ISSM). 2,3,6 Os três elementos da EP o tempo, o controlo e a angústia, estão incluídos nas linhas de orientação de 2016 da EAU, para o diagnóstico da ejaculação precoce, como se poderá ver abaixo. 6 O diagnóstico deve ser feito com base na história clínica e sexual e no uso de questionários de resultados relatados pelos pacientes, assim como as medidas do TLEI auto-estimado, o grau de satisfação sexual, a perceção de controlo e o sentimento de angústia. Estas linhas de orientação não indicam explicitamente o questionário preferido, mas o texto indica uma preferência clara para o uso do PEDT. Recomendações NE QE Efetuar o diagnóstico e classificação da EP, com base na história clínica e sexual, que deve incluir a avaliação do TLEI (auto-estimado), a perceção de controlo, o grau de angústia e as dificuldades interpessoais que advêm da disfunção ejaculatória. 1a A Não utilizar o TLEI cronometrado na prática clínica.. Não utilizar resultados relatados pelos pacientes na prática clínica. 2a 3 B C O médico deve examinar o paciente durante a avaliação inicial da EP, para que possa identificar anomalias anatómicas que possam estar associadas à EP ou a outras disfunções sexuais sobretudo a DE. 3 C Figura 30 Recomendações da EAU para o diagnóstico de avaliação da ejaculação precoce Não realizar testes laboratoriais ou neurofisiológicos de rotina. Estes apenas devem ser feitos no caso de haverem indícios específicos obtidos a partir da história clínica ou do exame físico. 3 C EP = Ejaculação Precoce; TLEI = Tempo de Latência Ejaculatória Intravaginal; DE = Disfunção Erétil; NE = Nível de Evidência; QE = Qualidade da Evidência. 38
39 UTILIZAÇÃO NA PRÁTICA CLÍNICA Estas linhas de orientação europeias fornecem uma base mais clara para as abordagens de tratamento da ejaculação precoce. Apesar de alguns fármacos estarem, atualmente, aprovados para o tratamento da ejaculação precoce, existe uma aceitação difundida do uso de certos fármacos sem indicação especificamente aprovada para a EP. A utilização destas linhas de orientação forneceu os alicerces para o desenvolvimento de um algoritmo para o tratamento da ejaculação precoce. 6 Diagnóstico clínico da ejaculação precoce baseada na história do paciente +/- parceira/o t Tratamento da ejaculação precoce l Aconselhamento do paciente/educação l Discussão das opções de tratamento l Se a EP for secundária à DE, tratar a DE primeiro ou de forma concomitante t Opções de tratamento 1. Farmacoterapia a. Dapoxetina de administração na hora b. Tratamentos sem indicação específica aprovada ISRSs diários Anestésicos tópicos Tramadol de administração na hora 2. Terapia comportamental 3. Tratamento combinado Figura 31 Linhas de orientação para tratar a ejaculação precoce Adaptadas de Hatzimouratidis et al DE = Disfunção Erétil; EP = Ejaculação Precoce; ISRS = Inibidor Seletivo de Serotonina (5-T) As orientações mais recentes estão indicadas acima e realçam o ponto de vista de que a farmacoterapia oral deve ser a opção de tratamento de primeira linha, antes de se recorrer a fármacos de anestesia local tópica. 6 Estas linhas de orientação referem-se a estes últimos como sem indicação específica aprovada (off-label), talvez porque, apesar de aprovado para esta situação clínica, o Fortacin ainda não tem estado disponível para os pacientes em vários países e está apontado nas linhas de orientação como experimental, com resultados positivos. 6 A maioria dos tratamentos atuais recomendados para a ejaculação precoce, pela EAU, são tratamentos sem indicação específica aprovada. Fortacin : uma opção adicional licenciada disponível. 39
40 UTILIZAÇÃO NA PRÁTICA CLÍNICA Resumo da potencial utilização do Fortacin nos pacientes Fortacin proporciona uma solução de aplicação na hora, para os homens adultos que sofrem de ejaculação precoce primária. 19 Proporciona um tratamento de aplicação simples, que pode ser administrado pouco tempo antes do início de uma relação sexual. 19 Os pacientes com ejaculação precoce têm, atualmente, poucas opções de tratamento que possam ser prescritas pelos médicos, após o diagnóstico. 6,19,28-30 A outra opção de tratamento na hora (a dapoxetina), requer a administração da dose muito mais cedo do que 5 minutos, a fim de se obter o início dos efeitos desejados. 28 Com base nos estudos realizados até à data, o Fortacin tem apresentado eficácia na maioria dos pacientes, quando utilizado como monoterapia, sendo eficaz desde a primeira aplicação. 16,19,25-27 O Fortacin tem muito poucas contraindicações, tornando o seu uso indicado para a grande maioria dos pacientes com ejaculação precoce, independentemente das comorbidades, ou medicamentos concomitantes, ou do consumo de substâncias e/ou de álcool. 19 Tendo em conta que a integridade do preservativo masculino, do capuz cervical, e do diafragma (todos fabricados com látex) não foi afetada pela exposição ao Fortacin no decurso dos estudos efetuados, estes métodos do tipo barreira podem continuar a ser utilizados por motivos contracetivos. No entanto, o preservativo feminino (feito com poliuretano) não deve ser utilizado. 19 Deve-se, contudo, assinalar um aumento de incidência de hipoestesia masculina e de DE nos pacientes que utilizaram o Fortacin com preservativos masculinos. 19 Adicionalmente, parece não haver qualquer necessidade de usar o preservativo para impedir a transferência dos ingredientes ativos do Fortacin à/ao parceira/o, apesar de ser recomendável limpar qualquer excesso do produto antes da penetração. 19 A fórmula utilizada no Fortacin permite a absorção do produto através da pele da glande, mas não da pele mais queratinizada da restante zona do pénis, o que torna a administração do fármaco localizada. 7,22 Esta fórmula também facilita a limpeza de alguma quantidade residual do produto que tenha permanecido na superfície do pénis, reduzindo ainda mais a possibilidade de provocar uma sensação de anestesia na/o parceira/o. 7,16,19,26 40
41 UTILIZAÇÃO NA PRÁTICA CLÍNICA Fortacin é geralmente bem tolerado, com poucos efeitos adversos. 16,19,25-27 A ausência de excipientes também ajuda a minimizar as reações adversas. 7,19 Os benefícios do tratamento com o Fortacin também são sentidos pelas parceiras dos pacientes com ejaculação precoce. As parceiras avaliaram o produto de forma muito positiva. O aumento da satisfação sexual de ambos os parceiros sexuais pode eliminar o efeito de exacerbação psicológica e a perpetuação do problema. O Fortacin pode, desta feita, ajudar a quebrar o círculo vicioso que resulta da EP. 16,27 Os resultados a longo prazo também indicaram melhorias adicionais ao longo do tempo, com a utilização do Fortacin, proporcionando, desta feita, benefícios de uma forma contínua, sem evidência de taquifilaxia
42 PONTOS-CHAVE Pontos-Chave Fortacin : o primeiro produto tópico aprovado e prescrito para a EP 19 Fortacin : o sistema de pulverização em doses calibradas permite que os agentes dessensibilizantes a lidocaína e a prilocaína sejam depositados em dose controlada, numa camada fina concentrada na glande do pénis 7 Fortacin : uma fórmula inovadora de tipo eutético que contém apenas formas básicas dos dois anestésicos locais 7 Fortacin : uma fórmula única que otimiza a penetração rápida dos produtos através da mucosa da glande, minimizando a absorção através da pele normal (mantendo uma sensação plena na zona restante do pénis) 7 Fortacin : o fármaco pode ser facilmente limpo com uma toalha húmida antes do ato sexual de forma a minimizar a transferência para a/o parceira/o sexual 7,19 Fortacin tem um efeito tópico rápido observado em 5 min 19 Fortacin aumenta o TLEI até um valor 6.3 vezes mais elevado no decurso de 3 meses 27 Fortacin aumenta o TLEI de um valor inicial de 0.6 min para 3.8 min após 3 meses 27 Fortacin aumenta o TLEI ao longo do tempo: observaram-se melhorias de mês para mês no decurso do tratamento, em estudos de longo prazo 16 Fortacin aumenta a satisfação sexual: 5.9 pontos de diferença comparativamente ao placebo no respetivo campo do IEP 27 Fortacin diminui a angústia: 2.8 pontos de diferença comparativamente ao placebo no respetivo campo do IEP 27 Fortacin melhora o controlo da ejaculação: 7.0 pontos de diferença comparativamente ao placebo no respetivo campo do IEP 27 Fortacin melhora a qualidade do desempenho sexual com um bom perfil de segurança 42
43 REFERÊNCIAS Referências 1. Buvat J Pathophysiology of Premature Ejaculation J Sex Med 2011;8 (suppl 4): Althof SE, McMahon CG, et al. An Update of the International Society of Sexual Medicine s Guidelines for the Diagnosis and Treatment of Premature Ejaculation (PE). Sex Med Jun;2(2): Serefoglu EC, McMahon CG, et all. An evidence-based unified definition of lifelong and acquired premature ejaculation: report of the second International Society for Sexual Medicine Ad Hoc Committee for the Definition of Premature Ejaculation. J Sex Med Jun;11(6): Giuliano F., et al Premature Ejaculation: Results from a Five-Country European Observational Study European Urology, Volume 53 Issue 5, May 2008, Pages Waldinger MD et al. A Multinational Population Survey of Intravaginal Ejaculation Latency Time 2005 J Sex Med Volume 2, Issue 4, Hatzimouratidis K, Giuliano F, Moncada I, Muneer G, Salonia A, Verze P EAU Guidelines on Erectile Dysfunction, Premature Ejaculation, Penile Curvature and Priapism European Association of Urology March 2016 update 7. Henry R, Morales A & Wyllie MG TEMPE: Topical Eutectic-Like Mixture for Premature Ejaculation, Expert Opinion on Drug Delivery, :2, , DOI: / Porst H, Montorsi F, et al. The Premature Ejaculation Prevalence and Attitudes (PEPA) survey: prevalence, comorbidities, and professional help-seeking. Eur Urol Mar;51(3): Saitz, T. R. & Serefoglu, E. C. Advances in understanding and treating of premature ejaculation. Nat. Rev. Urol. 12, (2015); published online 27 October 2015; doi: /nrurol Waldinger MD. Toward evidence-based genetic research on lifelong premature ejaculation: a critical evaluation of methodology. Korean J Urol Jan;52(1): Jern P, Santtila P, et al. Genetic and environmental effects on the continuity of ejaculatory dysfunction. BJU Int Jun;105(12): Giuliano F, Clèment P. Pharmacology for the treatment of premature ejaculation. Pharmacol Rev Jul;64(3): Xin ZC, Choi YD, et al. Somatosensory evoked potentials in patients with primary premature ejaculation. J Urol 1997;158: Jannini EA, Giacomo C et al. Premature ejaculation; old story, new insights Fertility and Sterility Vol 104 No 5; Janssen PK, Bakker SC, et al. Serotonin transporter promoter region (5-HTTLPR) polymorphism is associated with the intravaginal ejaculation latency time in Dutch men with lifelong premature ejaculation. J Sex Med Jan;6(1):
44 REFERÊNCIAS 16. Wyllie MG, Powell JA The role of local anaesthetics in premature ejaculation. BJU Int Dec;110(11 Pt C):E Shindel AW, Vittinghof E, et al. Erectile dysfunction and premature ejaculation in men who have sex with men. J Sex Med Feb; 9(2): Rowland D, McMahon CG, et al. Disorders of orgasm and ejaculation in men. J Sex Med Apr;7(4 Pt 2): Fortacin Summary of Product Characteristics 20. European Medicines Agency CHMP assessment report Lidocaine/Prilocaine Plethora EMEA/H/C/002693/ Cummins TR Setting up for the block: the mechanism underlying lidocaine s use-dependent inhibition of sodium channels. J Physiol Jul 1;582(Pt 1): Hellstrom WJG Update on treatments for premature ejaculation Int J Clin Pract 2011; 65: Plethora Solutions Holdings PLC Clinical Update - PSD502: First-line Therapy for Premature Ejaculation Press Release 12 July Henry R and Morales A. Topical lidocaine prilocaine spray for the treatment of premature ejaculation: a proof of concept study. Int J Impotence Research (2003) 15, Dinsmore WW, Hackett G, et al. Topical eutectic mixture for premature ejaculation (TEMPE): a novel aerosol-delivery form of lidocaine-prilocaine for treating premature ejaculation. BJU Int Feb;99(2): Carson C, and Wyllie M. Improved ejaculatory latency, control and sexual satisfaction when PSD502 is applied topically in men with premature ejaculation: Results of a phase III, double-blind, placebo-controlled study. J Sex Med 2010;7: Dinsmore WW, Wyllie MG. PSD502 improves ejaculatory latency, control and sexual satisfaction when applied topically 5 min before intercourse in men with premature ejaculation: results of a phase III, multicentre, double-blind, placebo-controlled study. BJU Int Apr;103(7): Priligy Summary of Product Characteristics 29. Gur S, Kadowitz PJ, Sikka SC. Current therapies for premature ejaculation. Drug Discov Today Jul;21(7): Morales A. Evolving therapeutic strategies for premature ejaculation: The search for on-demand treatment topical versus systemic Can Urol Assoc J 2012;6(5): org/ /cuaj
45 IECRCM Informações compatíveis com o RCM - 1. NOME DO MEDICAMENTO: Fortacin 150 mg/ml + 50 mg/ml solução. 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA: Cada ml da solução contém 150 mg de lidocaína e 50 mg de prilocaína. Cada recipiente fornece pelo menos 20 doses (6,5 ml) ou 12 doses (5 ml). Cada pulverização fornece 50 microlitros, contendo 7,5 mg de lidocaína e 2,5 mg de prilocaína. 3. FORMA FARMACÊUTICA: Solução para pulverização cutânea. Solução incolor a amarela clara. 4. INDICAÇÕES TERAPÊUTICAS: Tratamento da ejaculação precoce primária em homens adultos. 5. POSOLOGIA E MODO DE ADMINISTRAÇÃO: Uso cutâneo. A dose recomendada é de 3 pulverizações, aplicadas de modo a cobrirem a glande do pénis. É possível aplicar um máximo de 3 doses num período de 24 horas, com pelo menos 4 horas de intervalo entre as doses. O Fortacin só está indicado para aplicação na glande do pénis. Antes da utilização inicial, o recipiente pulverizador deve ser brevemente agitado e, de seguida, expurgado, com três vezes pulverizações para o ar. Antes de cada utilização subsequente, deve ser brevemente agitado e, de seguida, o recipiente pulverizador deve ser novamente expurgado, com uma pulverização. É necessário puxar o prepúcio para trás, deixando a glande a descoberto. Depois de a lata ser colocada na vertical (com a válvula para cima), aplica-se uma dose de Fortacin na glande inteira, pressionando a válvula três vezes. Cada pulverização deve cobrir um terço da glande do pénis. Ao fim de cinco minutos, é necessário eliminar qualquer solução pulverizada em excesso, antes de uma relação sexual. Não são necessários ajustes de dosagem nos idosos e nos insuficientes renais e hepáticos. É aconselhada precaução no caso de insuficiência hepática grave. 6. CONTRAINDICAÇÕES: Hipersensibilidade do doente ou do(a) parceiro(a) às substâncias ativas ou a qualquer um dos excipientes. Doentes ou parceiros(as) com antecedentes conhecidos de sensibilidade a anestésicos locais do tipo amida. 7. ADVERTÊNCIAS E PRECAUÇÕES ESPECIAIS DE UTILIZAÇÃO: Estados relacionados com a anemia: Os doentes ou parceiros(as) com deficiência de glucose-6-fosfato desidrogenase ou metemoglobinemia congénita ou idiopática são mais suscetíveis à metemoglobinemia induzida por medicamentos. Interações: Os doentes a tomarem medicamentos antiarrítmicos de classe III (por exemplo, amiodarona) devem ser tratados com precaução. Hipersensibilidades: Doentes alérgicos a derivados do ácido para-aminobenzoico (procaína, tetracaína, benzocaína, etc.) não exibiram qualquer sensibilidade cruzada à lidocaína e/ou prilocaína; contudo, o Fortacin deve ser utilizado com precaução nos doentes com antecedentes (ou parceiros(as) com antecedentes) de sensibilidade a medicamentos, sobretudo se o agente etiológico for desconhecido. Precauções de utilização: Na medida em que pode causar irritação ocular, devem ser tomadas precauções de modo a não permitir que o Fortacin entre em contacto com os olhos. Em caso de contacto com os olhos, lave-os de imediato com água ou uma solução de cloreto de sódio, e proteja-os até voltar a ter sensibilidade nos olhos. O Fortacin pulverizado nas membranas mucosas do doente ou parceiro(a), como boca, nariz e garganta, ou transferido para a genitália feminina ou revestimento anal, pode ser absorvido e possivelmente resultar em sensação de dormência/anestesia local temporária. 45
46 IECRCM Esta hipoestesia pode ocultar as sensações dolorosas normais e, por conseguinte, aumentar os perigos de lesões localizadas. Observou-se a ocorrência de deterioração quando o Fortacin foi utilizado com preservativos femininos e masculinos à base de poliuretano. Quando o Fortacin é utilizado com preservativos masculinos, é possível observar-se uma taxa mais elevada de disfunção erétil e hipoestesia genital masculina. Devido ao risco de transferência para a parceira, os doentes que pretendam alcançar a conceção devem evitar utilizar o Fortacin ou, caso este seja fundamental para a penetração, devem lavar a glande da forma mais meticulosa possível, 5 minutos após a pulverização, mas antes da relação sexual. Doentes com insuficiência hepática grave: Devido à incapacidade de metabolização normal dos anestésicos locais, os doentes com doença hepática grave estão em maior risco de desenvolvimento de concentrações plasmáticas tóxicas de lidocaína e prilocaína. 8. INTERACÇÕES MEDICAMENTOSAS E OUTRAS FORMAS DE INTERACÇÃO: A metemoglobinemia pode ser mais marcada nos doentes que já se encontram a tomar medicamentos conhecidos por induzirem este estado, como, por exemplo, sulfonamidas, acetanilida, corantes à base de anilina, benzocaína, cloroquina, dapsona, metoclopramida, naftaleno, nitratos e nitritos, nitrofurantoína, nitroglicerina, nitroprussiato, pamaquina, ácido paraaminosalicílico, fenobarbital, fenitoína, primaquina e quinina. O risco de toxicidade sistémica adicional deve ser tido em conta quando se aplicam doses elevadas de Fortacin a doentes que já se encontram a utilizar outros anestésicos locais ou medicamentos estruturalmente aparentados como, por exemplo, os antiarrítmicos de classe I, como a mexiletina. Não foram realizados estudos específicos de interação com a lidocaína/prilocaína e antiarrítmicos de classe III (por exemplo, amiodarona), mas aconselha-se precaução. 9. EFEITOS INDESEJÁVEIS: Resumo do perfil de segurança: A segurança do Fortacin foi avaliada com base em 596 doentes do sexo masculino que procederam à sua aplicação durante a realização de ensaios clínicos. A segurança foi igualmente avaliada em 584 parceiras desses participantes. Verificou-se a ocorrência de reações adversas em 9,6 % dos participantes e 6,0 % das parceiras. Os casos foram, na sua maioria, classificados como ligeiros ou moderados. Reações adversas medicamentosas nos participantes tratados à glande do pénis: Frequentes ( 1/100 a < 1/10) Hipoestesia dos genitais masculinos, disfunção erétil, sensação de ardor genital. Pouco frequentes ( 1/1000 a < 1/100) - Orgasmo anormal, dor de cabeça, irritação da garganta, irritação cutânea, eritema genital, falha na ejaculação, parestesia dos genitais masculinos, dor peniana, distúrbio peniano, prurido genital, pirexia. Reações adversas medicamentosas nas parceiras: Frequentes ( 1/100 a < 1/10) - Sensação de ardor vulvovaginal, hipoestesia. Pouco frequentes ( 1/1000 a < 1/100) - Candidíase vaginal, dor de cabeça, irritação da garganta, desconforto anorretal, parestesia oral, disúria, desconforto vulvovaginal, dor vaginal, prurido vulvovaginal. 10. DATA DA REVISÃO DO TEXTO DO RCM: Outubro de Medicamento sujeito a receita médica não comparticipado. Para mais informações deverá contactar o Titular da Autorização de Introdução no Mercado. 46
47 NOTAS 47
48 FsstFsstFsst. Contra a ejaculação precoce. Novo tratamento em spray para a ejaculação precoce, clinicamente comprovado. Lagoas Park, Edf.5, Torre C, Piso Porto Salvo, Portugal Tel.: Fax: Capital Social de ,00 Euros Contribuinte nº matriculada na Conservatória do Registo Comercial de Cascais sob o mesmo número. Ref.: 045/2018 MP02/2018
Caso clínico de ejaculação prematura. Edgar Tavares da Silva, Hugo Antunes
 Caso clínico de ejaculação prematura Edgar Tavares da Silva, Hugo Antunes Caso clínico Doente de 30 anos Saudável Parceira nova Dra, eu ejaculo cedo demais Caso clínico Definição de EP Tempo Controlo Perturbação
Caso clínico de ejaculação prematura Edgar Tavares da Silva, Hugo Antunes Caso clínico Doente de 30 anos Saudável Parceira nova Dra, eu ejaculo cedo demais Caso clínico Definição de EP Tempo Controlo Perturbação
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Fortacin 150 mg/ml + 50 mg/ml solução para pulverização cutânea 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada ml da solução contém
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Fortacin 150 mg/ml + 50 mg/ml solução para pulverização cutânea 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada ml da solução contém
Cloridrato de Mepivacaína Cloreto de sódio. Água para injectáveis q.b.p.
 1. DENOMINAÇÃO DO MEDICAMENTO SCANDINIBSA 3% 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cloridrato de Mepivacaína Cloreto de sódio Metilparabeno Água para injectáveis q.b.p. 3,00 g 0,60 g 0,06 g 100,00 ml
1. DENOMINAÇÃO DO MEDICAMENTO SCANDINIBSA 3% 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cloridrato de Mepivacaína Cloreto de sódio Metilparabeno Água para injectáveis q.b.p. 3,00 g 0,60 g 0,06 g 100,00 ml
APROVADO EM INFARMED
 FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR Xylocaína 5% 50 mg/g Pomada (lidocaína) Leia atentamente este folheto antes de utilizar o medicamento. Conserve este folheto. Pode ter necessidade de o
FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR Xylocaína 5% 50 mg/g Pomada (lidocaína) Leia atentamente este folheto antes de utilizar o medicamento. Conserve este folheto. Pode ter necessidade de o
Resposta Sexual Masculina Normal
 Resposta Sexual Masculina Normal Interesse sexual/ estimulação Orgasmo Ejaculação acompanhada por orgasmo Tumescência peniana Penetração Detumescênci a peniana Excitação/ erecção peniana elevada Planalto
Resposta Sexual Masculina Normal Interesse sexual/ estimulação Orgasmo Ejaculação acompanhada por orgasmo Tumescência peniana Penetração Detumescênci a peniana Excitação/ erecção peniana elevada Planalto
Colírio, solução. Solução oleosa, amarelo claro com aspeto límpido e cheiro característico.
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Diomicete 10 mg/ml colírio, solução 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Um ml de solução contém 10 mg de clotrimazol. Excipientes com
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Diomicete 10 mg/ml colírio, solução 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Um ml de solução contém 10 mg de clotrimazol. Excipientes com
FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR
 FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR CICLOVIRAL 50 mg/g Creme Aciclovir Este folheto contém informações importantes para si. Leia-o atentamente. Este medicamento pode ser adquirido sem receita
FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR CICLOVIRAL 50 mg/g Creme Aciclovir Este folheto contém informações importantes para si. Leia-o atentamente. Este medicamento pode ser adquirido sem receita
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. DENOMINAÇÃO DO MEDICAMENTO BETADINE 100mg/g pomada 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Princípio activo: Iodopovidona 10g Lista completa de excipientes,
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. DENOMINAÇÃO DO MEDICAMENTO BETADINE 100mg/g pomada 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Princípio activo: Iodopovidona 10g Lista completa de excipientes,
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. DENOMINAÇÂO DO MEDICAMENTO Procto-Glyvenol 50 mg/g + 20 mg/g Creme rectal 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada grama de Procto-Glyvenol creme rectal
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. DENOMINAÇÂO DO MEDICAMENTO Procto-Glyvenol 50 mg/g + 20 mg/g Creme rectal 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada grama de Procto-Glyvenol creme rectal
Cada grama de Quinodermil As Pomada contém 30 mg de Clioquinol e 30 mg de Ácido salicílico como substâncias activas.
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. DENOMINAÇÃO DO MEDICAMENTO Quinodermil As 30 mg/g + 30 mg/g Pomada 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada grama de Quinodermil As Pomada contém 30 mg
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. DENOMINAÇÃO DO MEDICAMENTO Quinodermil As 30 mg/g + 30 mg/g Pomada 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada grama de Quinodermil As Pomada contém 30 mg
Dermomax. Biosintética Farmacêutica Ltda. Creme dermatológico 40 mg/g. Dermomax_BU 02_VP 1
 Dermomax Biosintética Farmacêutica Ltda. Creme dermatológico 40 mg/g Dermomax_BU 02_VP 1 BULA PARA PACIENTE Bula de acordo com a Resolução-RDC nº 47/2009 I- IDENTIFICAÇÃO DO MEDICAMENTO Dermomax lidocaína
Dermomax Biosintética Farmacêutica Ltda. Creme dermatológico 40 mg/g Dermomax_BU 02_VP 1 BULA PARA PACIENTE Bula de acordo com a Resolução-RDC nº 47/2009 I- IDENTIFICAÇÃO DO MEDICAMENTO Dermomax lidocaína
XYLOCAÍNA Geleia 2% cloridrato de lidocaína
 XYLOCAÍNA Geleia 2% cloridrato de lidocaína I) IDENTIFICAÇÃO DO MEDICAMENTO XYLOCAÍNA Geleia 2% cloridrato de lidocaína APRESENTAÇÕES Geleia 20 mg/ml em embalagem com uma bisnaga contendo 30 g. VIA URETRAL
XYLOCAÍNA Geleia 2% cloridrato de lidocaína I) IDENTIFICAÇÃO DO MEDICAMENTO XYLOCAÍNA Geleia 2% cloridrato de lidocaína APRESENTAÇÕES Geleia 20 mg/ml em embalagem com uma bisnaga contendo 30 g. VIA URETRAL
1. O QUE É SILVESPRAY E PARA QUE É UTILIZADO?
 FOLHETO INFORMATIVO Leia atentamente este folheto antes de tomar o medicamento - Conserve este folheto: Pode ter necessidade de o reler. - Caso tenha dúvidas, consulte o seu médico ou farmacêutico. - Este
FOLHETO INFORMATIVO Leia atentamente este folheto antes de tomar o medicamento - Conserve este folheto: Pode ter necessidade de o reler. - Caso tenha dúvidas, consulte o seu médico ou farmacêutico. - Este
Terramicina com sulfato de polimixina B. cloridrato de oxitetraciclina, sulfato de polimixina B. Pomada Tópica
 Terramicina com sulfato de polimixina B cloridrato de oxitetraciclina, sulfato de polimixina B Pomada Tópica PARTE I IDENTIFICAÇÃO DO PRODUTO Nome: Terramicina com sulfato de polimixina B - pomada tópica.
Terramicina com sulfato de polimixina B cloridrato de oxitetraciclina, sulfato de polimixina B Pomada Tópica PARTE I IDENTIFICAÇÃO DO PRODUTO Nome: Terramicina com sulfato de polimixina B - pomada tópica.
Aproximadamente 60% dos doentes começou o tratamento numa fase inicial (prodroma ou eritema) e 40% numa fase tardia (pápula ou vesícula).
 Folheto informativo: Informação para o utilizador Aciclosina 50 mg/g Creme Aciclovir Leia com atenção todo este folheto antes de começar a utilizar este medicamento pois contém informação importante para
Folheto informativo: Informação para o utilizador Aciclosina 50 mg/g Creme Aciclovir Leia com atenção todo este folheto antes de começar a utilizar este medicamento pois contém informação importante para
Fabricado por: Sofarimex Industria Química e Farmacêutica L.da,
 FOLHETO INFORMATIVO Leia atentamente este folheto informativo antes de tomar o medicamento - Conserve este folheto. Pode ter necessidade de o ler novamente. - Caso tenha dúvidas, consulte o seu médico
FOLHETO INFORMATIVO Leia atentamente este folheto informativo antes de tomar o medicamento - Conserve este folheto. Pode ter necessidade de o ler novamente. - Caso tenha dúvidas, consulte o seu médico
RESODERMIL CREME. COMPOSIÇÃO: O RESODERMIL possui na sua composição: Enxofre a 75 mg/g e Resorcina a 10 mg/g.
 RESODERMIL CREME Leia atentamente este folheto antes de utilizar o medicamento. - Conserve este folheto. Pode ter necessidade de o reler. - Caso tenha dúvidas, contacte o seu Médico ou Farmacêutico. -
RESODERMIL CREME Leia atentamente este folheto antes de utilizar o medicamento. - Conserve este folheto. Pode ter necessidade de o reler. - Caso tenha dúvidas, contacte o seu Médico ou Farmacêutico. -
HYPOTEARS Plus HYPOTEARS Plus DU
 HYPOTEARS Plus HYPOTEARS Plus DU povidona 50 mg/ ml Lágrima artificial estéril Forma farmacêutica e apresentação HYPOTEARS Plus: colírio. Embalagem com frasco conta-gotas contendo 10 ml. HYPOTEARS Plus
HYPOTEARS Plus HYPOTEARS Plus DU povidona 50 mg/ ml Lágrima artificial estéril Forma farmacêutica e apresentação HYPOTEARS Plus: colírio. Embalagem com frasco conta-gotas contendo 10 ml. HYPOTEARS Plus
PROCTO-GLYVENOL tribenosídeo + lidocaína
 MODELO DE TEXTO DE BULA PROCTO-GLYVENOL tribenosídeo + lidocaína TRATAMENTO LOCAL DAS HEMORRÓIDAS Formas farmacêuticas, via de administração e apresentações: Supositórios. Embalagens com 5 ou 10 supositórios.
MODELO DE TEXTO DE BULA PROCTO-GLYVENOL tribenosídeo + lidocaína TRATAMENTO LOCAL DAS HEMORRÓIDAS Formas farmacêuticas, via de administração e apresentações: Supositórios. Embalagens com 5 ou 10 supositórios.
NEOSORO. (cloridrato de nafazolina)
 NEOSORO (cloridrato de nafazolina) Brainfarma Indústria Química e Farmacêutica S.A. 0,5mg/mL I - IDENTIFICAÇÃO DO MEDICAMENTO: NEOSORO cloridrato de nafazolina MEDICAMENTO SIMILAR EQUIVALENTE AO MEDICAMENTO
NEOSORO (cloridrato de nafazolina) Brainfarma Indústria Química e Farmacêutica S.A. 0,5mg/mL I - IDENTIFICAÇÃO DO MEDICAMENTO: NEOSORO cloridrato de nafazolina MEDICAMENTO SIMILAR EQUIVALENTE AO MEDICAMENTO
MAIOR CONTRO. Informação De Segurança Importante Sobre PRILIGY. 1 Informação para o médico
 MAIOR CONTRO Informação De Segurança Importante Sobre PRILIGY 1 Informação para o médico 2 A Ejaculação Precoce e PRILIGY PRILIGY é um medicamento oral aprovado para o tratamento da Ejaculação Precoce
MAIOR CONTRO Informação De Segurança Importante Sobre PRILIGY 1 Informação para o médico 2 A Ejaculação Precoce e PRILIGY PRILIGY é um medicamento oral aprovado para o tratamento da Ejaculação Precoce
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO. Bisolspray Nebulicina Adulto 0,5 mg/ml solução para pulverização nasal
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1.NOME DO MEDICAMENTO Bisolspray Nebulicina Adulto 0,5 mg/ml solução para pulverização nasal 2. COMPOSIÇÃO QUANTITATIVA E QUALITATIVA Cada ml de solução para pulverização
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1.NOME DO MEDICAMENTO Bisolspray Nebulicina Adulto 0,5 mg/ml solução para pulverização nasal 2. COMPOSIÇÃO QUANTITATIVA E QUALITATIVA Cada ml de solução para pulverização
Mifepriston Linepharma. Mifepristone Linepharma. Mifepristone Linepharma 200 mg comprimé. Mifepristone Linepharma 200 mg Tafla
 Anexo I Lista dos nomes (de fantasia), forma farmacêutica, dosagem dos medicamentos, modo de administração, requerentes/titulares da autorização de introdução no mercado nos Estados-Membros 1 Estado-Membro
Anexo I Lista dos nomes (de fantasia), forma farmacêutica, dosagem dos medicamentos, modo de administração, requerentes/titulares da autorização de introdução no mercado nos Estados-Membros 1 Estado-Membro
Sorine Adulto. Aché Laboratórios Farmacêuticos S.A. Solução nasal 0,5 mg/ml
 Sorine Adulto Aché Laboratórios Farmacêuticos S.A. Solução nasal 0,5 mg/ml BULA PARA PACIENTE Bula de acordo com a Resolução-RDC nº 47/2009 I- IDENTIFICAÇÃO DO MEDICAMENTO Sorine cloridrato de nafazolina
Sorine Adulto Aché Laboratórios Farmacêuticos S.A. Solução nasal 0,5 mg/ml BULA PARA PACIENTE Bula de acordo com a Resolução-RDC nº 47/2009 I- IDENTIFICAÇÃO DO MEDICAMENTO Sorine cloridrato de nafazolina
Lidocaína. EMS S/A Creme dermatológico 40 mg/g
 Lidocaína EMS S/A Creme dermatológico 40 mg/g IDENTIFICAÇÃO DO MEDICAMENTO LIDOCAÍNA Medicamento Genérico, Lei nº. 9.787, de 1999. APRESENTAÇÕES Creme dermatológico 40 mg/g: bisnaga com 5g, 15g ou 30g.
Lidocaína EMS S/A Creme dermatológico 40 mg/g IDENTIFICAÇÃO DO MEDICAMENTO LIDOCAÍNA Medicamento Genérico, Lei nº. 9.787, de 1999. APRESENTAÇÕES Creme dermatológico 40 mg/g: bisnaga com 5g, 15g ou 30g.
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO. Excipientes: cada comprimido contém 268,36 mg de sacarose e 102,99 mg de glucose.
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Xonkor 450 mg Comprimidos revestidos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada comprimido revestido contém 450 mg de extracto (sob a
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Xonkor 450 mg Comprimidos revestidos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada comprimido revestido contém 450 mg de extracto (sob a
cloridrato de lidocaína Medicamento genérico Lei nº de 1999 Cristália Prod. Quím. Farm. Ltda. Geleia 20 mg/g (2%) MODELO DE BULA PARA O PACIENTE
 cloridrato de lidocaína Medicamento genérico Lei nº 9.787 de 1999 Cristália Prod. Quím. Farm. Ltda. Geleia 20 mg/g (2%) MODELO DE BULA PARA O PACIENTE I- IDENTIFICAÇÃO DO MEDICAMENTO cloridrato de lidocaína
cloridrato de lidocaína Medicamento genérico Lei nº 9.787 de 1999 Cristália Prod. Quím. Farm. Ltda. Geleia 20 mg/g (2%) MODELO DE BULA PARA O PACIENTE I- IDENTIFICAÇÃO DO MEDICAMENTO cloridrato de lidocaína
lidina 0,125 mg/0,5 ml, colírio, solução Cetotifeno
 FOLHETO INFORMATIVO FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR lidina 0,125 mg/0,5 ml, colírio, solução Cetotifeno Leia atentamente este folheto antes de utilizar este medicamento. - Conserve este
FOLHETO INFORMATIVO FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR lidina 0,125 mg/0,5 ml, colírio, solução Cetotifeno Leia atentamente este folheto antes de utilizar este medicamento. - Conserve este
ANESTÉSICOS LOCAIS: utilização clínica
 ANESTÉSICOS LOCAIS: utilização clínica Luís Vicente Garcia Faculdade de Medicina de Ribeirão Preto Disciplina de Anestesiologia Conceito 1. substâncias que quando aplicadas localmente no tecido nervoso,
ANESTÉSICOS LOCAIS: utilização clínica Luís Vicente Garcia Faculdade de Medicina de Ribeirão Preto Disciplina de Anestesiologia Conceito 1. substâncias que quando aplicadas localmente no tecido nervoso,
Substância activa: Um mililitro de solução vaginal contém 1 mg de Cloridrato de benzidamina.
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Rosalgin 1 mg/ml solução vaginal 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Substância activa: Um mililitro de solução vaginal contém 1 mg
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Rosalgin 1 mg/ml solução vaginal 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Substância activa: Um mililitro de solução vaginal contém 1 mg
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. DENOMINAÇÃO DO MEDICAMENTO BETADINE 100mg/ml solução cutânea 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Princípio activo: Iodopovidona 10g Lista completa de excipientes,
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. DENOMINAÇÃO DO MEDICAMENTO BETADINE 100mg/ml solução cutânea 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Princípio activo: Iodopovidona 10g Lista completa de excipientes,
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO VETERINÁRIO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO VETERINÁRIO Página 1 de 9 1. NOME DO MEDICAMENTO VETERINÁRIO Zuritol 50 mg/ml suspensão oral para suínos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA 1 ml contém:
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO VETERINÁRIO Página 1 de 9 1. NOME DO MEDICAMENTO VETERINÁRIO Zuritol 50 mg/ml suspensão oral para suínos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA 1 ml contém:
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. DENOMINAÇÃO DO MEDICAMENTO BETADINE 100mg/ml solução vaginal 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Princípio activo: Iodopovidona 10,0g Lista completa de
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. DENOMINAÇÃO DO MEDICAMENTO BETADINE 100mg/ml solução vaginal 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Princípio activo: Iodopovidona 10,0g Lista completa de
Ultraproct Creme Rectal é utilizado para o alívio sintomático da dor, edema ou prurido associado a doença hemorroidária.
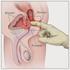 FOLHETO INFORMATIVO Leia atentamente este folheto antes de tomar o medicamento. - Conserve este folheto. Pode ter necessidade de o reler. - Caso tenha dúvidas, consulte o seu médico ou farmacêutico. -
FOLHETO INFORMATIVO Leia atentamente este folheto antes de tomar o medicamento. - Conserve este folheto. Pode ter necessidade de o reler. - Caso tenha dúvidas, consulte o seu médico ou farmacêutico. -
Folheto informativo: Informação para o utilizador. alerjon 0,25 mg/ml colírio, solução Cloridrato de oximetazolina
 FOLHETO INFORMATIVO Folheto informativo: Informação para o utilizador alerjon 0,25 mg/ml colírio, solução Cloridrato de oximetazolina Leia com atenção todo este folheto antes de começar a utilizar este
FOLHETO INFORMATIVO Folheto informativo: Informação para o utilizador alerjon 0,25 mg/ml colírio, solução Cloridrato de oximetazolina Leia com atenção todo este folheto antes de começar a utilizar este
FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR
 FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR Supofen 125 mg supositórios Supofen 250 mg supositórios Supofen 500 mg supositórios Paracetamol APROVADO EM Este folheto contém informações importantes
FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR Supofen 125 mg supositórios Supofen 250 mg supositórios Supofen 500 mg supositórios Paracetamol APROVADO EM Este folheto contém informações importantes
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO. Cada mililitro contém 0,345 mg de fumarato de cetotifeno, correspondente a 0,25 mg de cetotifeno.
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO ZADITEN 0,25 mg/ml, colírio, solução 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada mililitro contém 0,345 mg de fumarato de cetotifeno,
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO ZADITEN 0,25 mg/ml, colírio, solução 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada mililitro contém 0,345 mg de fumarato de cetotifeno,
ALLERGAN PRODUTOS FARMACÊUTICOS LTDA
 STILL ALLERGAN PRODUTOS FARMACÊUTICOS LTDA Solução Oftálmica Estéril diclofenaco sódico 0,1% BULA PARA O PROFISSIONAL DE SAÚDE Bula para o Profissional de Saúde APRESENTAÇÃO Solução Oftálmica Estéril Frasco
STILL ALLERGAN PRODUTOS FARMACÊUTICOS LTDA Solução Oftálmica Estéril diclofenaco sódico 0,1% BULA PARA O PROFISSIONAL DE SAÚDE Bula para o Profissional de Saúde APRESENTAÇÃO Solução Oftálmica Estéril Frasco
RESUMO DAS CARATERÍSTICAS DO MEDICAMENTO. Zuritol 25 mg/ml solução para administração na água de bebida para galinhas.
 RESUMO DAS CARATERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO VETERINÁRIO Zuritol 25 mg/ml solução para administração na água de bebida para galinhas. 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada ml
RESUMO DAS CARATERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO VETERINÁRIO Zuritol 25 mg/ml solução para administração na água de bebida para galinhas. 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada ml
Posologia: A posologia habitual corresponde à ingestão de uma cápsula, três vezes por dia, no momento das principais refeições.
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Venosmil 200 mg cápsula 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Composição por cápsula: Substância ativa: Cada cápsula contém 200 mg de
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Venosmil 200 mg cápsula 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Composição por cápsula: Substância ativa: Cada cápsula contém 200 mg de
APROVADO EM INFARMED FOLHETO INFORMATIVO
 FOLHETO INFORMATIVO Leia atentamente este folheto antes de tomar o medicamento. Conserve este folheto. Pode ter necessidade de o voltar a ler. Caso tenha dúvidas, consulte o seu médico ou farmacêutico.
FOLHETO INFORMATIVO Leia atentamente este folheto antes de tomar o medicamento. Conserve este folheto. Pode ter necessidade de o voltar a ler. Caso tenha dúvidas, consulte o seu médico ou farmacêutico.
NOVO RINO Solução Nasal. CLORIDRATO DE NAFAZOLINA - 0,5 mg/ml
 NOVO RINO Solução Nasal CLORIDRATO DE NAFAZOLINA - 0,5 mg/ml Novo Rino cloridrato de nafazolina FORMA FARMACÊUTICA E APRESENTAÇÃO Solução nasal 0,5 mg/ml: embalagem contendo um frasco com 15 ml. USO NASAL
NOVO RINO Solução Nasal CLORIDRATO DE NAFAZOLINA - 0,5 mg/ml Novo Rino cloridrato de nafazolina FORMA FARMACÊUTICA E APRESENTAÇÃO Solução nasal 0,5 mg/ml: embalagem contendo um frasco com 15 ml. USO NASAL
APROVADO EM INFARMED. Folheto informativo: Informação para o utilizador. COLTRAMYL 4 mg/2 ml solução injetável Tiocolquicosido
 Folheto informativo: Informação para o utilizador COLTRAMYL 4 mg/2 ml solução injetável Tiocolquicosido Este medicamento está sujeito a monitorização adicional. Isto irá permitir a rápida identificação
Folheto informativo: Informação para o utilizador COLTRAMYL 4 mg/2 ml solução injetável Tiocolquicosido Este medicamento está sujeito a monitorização adicional. Isto irá permitir a rápida identificação
Produto: cotovelol Protocolo: XYZ123 Data: 10 de agosto de 2015 Página 1 de 5
 Data: 10 de agosto de 2015 Página 1 de 5 Sinopse do Protocolo Título: Estudo Randomizado, Duplo-cego, Controlado por Placebo para Avaliar a Eficácia e Segurança do Uso de Cotovelol no Tratamento da Dor
Data: 10 de agosto de 2015 Página 1 de 5 Sinopse do Protocolo Título: Estudo Randomizado, Duplo-cego, Controlado por Placebo para Avaliar a Eficácia e Segurança do Uso de Cotovelol no Tratamento da Dor
FORMA FARMACÊUTICA E APRESENTAÇÃO Solução otológica - Frasco com 10 ml, provido de conta-gotas.
 Lidosporin lidocaína 43,4 mg/ml sulfato de polimixina B 10.000 UI/ml Solução otológica FORMA FARMACÊUTICA E APRESENTAÇÃO Solução otológica - Frasco com 10 ml, provido de conta-gotas. USO ADULTO E PEDIÁTRICO
Lidosporin lidocaína 43,4 mg/ml sulfato de polimixina B 10.000 UI/ml Solução otológica FORMA FARMACÊUTICA E APRESENTAÇÃO Solução otológica - Frasco com 10 ml, provido de conta-gotas. USO ADULTO E PEDIÁTRICO
Dimensão Segurança do Doente Check-list Procedimentos de Segurança
 Check-list Procedimentos de Segurança 1. 1.1 1.2 Cultura de Segurança Existe um elemento(s) definido(s) com responsabilidade atribuída para a segurança do doente Promove o trabalho em equipa multidisciplinar
Check-list Procedimentos de Segurança 1. 1.1 1.2 Cultura de Segurança Existe um elemento(s) definido(s) com responsabilidade atribuída para a segurança do doente Promove o trabalho em equipa multidisciplinar
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 9 1. NOME DO MEDICAMENTO VETERINÁRIO Colivet 2 000 000 UI/ml, concentrado para solução oral para suínos e aves de capoeira 2. COMPOSIÇÃO QUALITATIVA
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 9 1. NOME DO MEDICAMENTO VETERINÁRIO Colivet 2 000 000 UI/ml, concentrado para solução oral para suínos e aves de capoeira 2. COMPOSIÇÃO QUALITATIVA
Cada mililitro de gotas nasais, solução contém 2,5 mg de Cloridrato de fenilefrina, como substância ativa.
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Neo-Sinefrina 2,5 mg/ml Gotas nasais, solução 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada mililitro de gotas nasais, solução contém 2,5
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Neo-Sinefrina 2,5 mg/ml Gotas nasais, solução 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada mililitro de gotas nasais, solução contém 2,5
Sinustrat Vasoconstrictor. Avert Laboratórios Ltda. Solução nasal. Cloridrato de nafazolina. 0,5mg/mL
 Sinustrat Vasoconstrictor Avert Laboratórios Ltda. Solução nasal Cloridrato de nafazolina 0,5mg/mL Avert Sinustrat Vasoconstrictor (Paciente) 04/2015 1 IDENTIFICAÇÃO DO MEDICAMENTO Sinustrat Vasoconstrictor
Sinustrat Vasoconstrictor Avert Laboratórios Ltda. Solução nasal Cloridrato de nafazolina 0,5mg/mL Avert Sinustrat Vasoconstrictor (Paciente) 04/2015 1 IDENTIFICAÇÃO DO MEDICAMENTO Sinustrat Vasoconstrictor
SEMINÁRIO: IDOSOS... UM OLHAR PARA O FUTURO! PAINEL 4: CUIDAR E PROTEGER - CUIDADOS DE SAÚDE DIÁRIOS - VANESSA MATEUS FAÍSCA
 SEMINÁRIO: IDOSOS... UM OLHAR PARA O FUTURO! PAINEL 4: CUIDAR E PROTEGER - CUIDADOS DE SAÚDE DIÁRIOS - USO RACIONAL DO MEDICAMENTO VANESSA MATEUS FAÍSCA Área Científica de Farmácia ESTeSL vanessa.mateus@estesl.ipl.pt
SEMINÁRIO: IDOSOS... UM OLHAR PARA O FUTURO! PAINEL 4: CUIDAR E PROTEGER - CUIDADOS DE SAÚDE DIÁRIOS - USO RACIONAL DO MEDICAMENTO VANESSA MATEUS FAÍSCA Área Científica de Farmácia ESTeSL vanessa.mateus@estesl.ipl.pt
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO TONSILOTREN 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA 1 comprimido (250 mg) contém: Substâncias activas: Atropinum sulfuricum trit. D5 Hepar
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO TONSILOTREN 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA 1 comprimido (250 mg) contém: Substâncias activas: Atropinum sulfuricum trit. D5 Hepar
Anexo III Alterações às secções relevantes do resumo das características do medicamento e do folheto informativo
 Anexo III Alterações às secções relevantes do resumo das características do medicamento e do folheto informativo Nota: Estas alterações às secções relevantes do resumo das características do medicamento
Anexo III Alterações às secções relevantes do resumo das características do medicamento e do folheto informativo Nota: Estas alterações às secções relevantes do resumo das características do medicamento
Os outros ingredientes são: álcool, propilenoglicol, água purificada, carbómero e diisopropanolamina.
 MINOCALVE 2% Folheto Informativo Proposto FOLHETO INFORMATIVO Leia atentamente este folheto antes de tomar o medicamento. Conserve este folheto. Pode ter necessidade de o reler. Caso tenha dúvidas, consulte
MINOCALVE 2% Folheto Informativo Proposto FOLHETO INFORMATIVO Leia atentamente este folheto antes de tomar o medicamento. Conserve este folheto. Pode ter necessidade de o reler. Caso tenha dúvidas, consulte
Xylestesin geleia 2% cloridrato de lidocaína. 2% (20mg/g) geleia. Cristália Prod. Quím. Farm. Ltda. MODELO DE BULA PARA O PACIENTE
 Xylestesin geleia 2% cloridrato de lidocaína 2% (20mg/g) geleia Cristália Prod. Quím. Farm. Ltda. MODELO DE BULA PARA O PACIENTE I - IDENTIFICAÇÃO DO MEDICAMENTO Xylestesin Geleia 2% (20mg/g) cloridrato
Xylestesin geleia 2% cloridrato de lidocaína 2% (20mg/g) geleia Cristália Prod. Quím. Farm. Ltda. MODELO DE BULA PARA O PACIENTE I - IDENTIFICAÇÃO DO MEDICAMENTO Xylestesin Geleia 2% (20mg/g) cloridrato
Este medicamento foi receitado para si. Não deve dá-lo a outros; o medicamento pode ser-lhes prejudicial mesmo que apresentem os mesmos sintomas
 FOLHETO INFORMATIVO LEIA ATENTAMENTE ESTE FOLHETO ANTES DE TOMAR O MEDICAMENTO. Conserve este folheto. Pode ter necessidade de o voltar a ler. Caso tenha dúvidas, consulte o seu médico ou farmacêutico.
FOLHETO INFORMATIVO LEIA ATENTAMENTE ESTE FOLHETO ANTES DE TOMAR O MEDICAMENTO. Conserve este folheto. Pode ter necessidade de o voltar a ler. Caso tenha dúvidas, consulte o seu médico ou farmacêutico.
Informação importante para os profissionais de saúde acerca dos riscos graves associados a CAPRELSA
 CAPRELSA (vandetanib) Informação importante para os profissionais de saúde acerca dos riscos graves associados a CAPRELSA Estes materiais educacionais estão focados no risco de prolongamento do intervalo
CAPRELSA (vandetanib) Informação importante para os profissionais de saúde acerca dos riscos graves associados a CAPRELSA Estes materiais educacionais estão focados no risco de prolongamento do intervalo
CLORIDRATO DE NAFAZOLINA EMS S/A. Solução Nasal. 0,5 mg/ml
 CLORIDRATO DE NAFAZOLINA EMS S/A Solução Nasal 0,5 mg/ml IDENTIFICAÇÃO DO MEDICAMENTO cloridrato de nafazolina Medicamento Genérico, Lei n 9.787, de 1999 APRESENTAÇÕES Solução nasal 0,5 mg/ml: embalagem
CLORIDRATO DE NAFAZOLINA EMS S/A Solução Nasal 0,5 mg/ml IDENTIFICAÇÃO DO MEDICAMENTO cloridrato de nafazolina Medicamento Genérico, Lei n 9.787, de 1999 APRESENTAÇÕES Solução nasal 0,5 mg/ml: embalagem
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO VETERINÁRIO Metricure 500 mg suspensão intrauterina 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada seringa contém: Substância ativa: Cefapirina
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO VETERINÁRIO Metricure 500 mg suspensão intrauterina 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada seringa contém: Substância ativa: Cefapirina
Curso Técnico em Zootecnia
 Curso Técnico em Zootecnia Aula: 01/01 SUB TEMA: INTRODUÇÃO À Professor: Vitor Hugo SUB TEMA: HISTÓRIA DA HÁ MUITO TEMPO MAIS DE 5 MIL ANOS PROCURAM-SE SUBSTÂNCIAS QUÍMICAS COM O OBJETIVO DE CURAR AS MAIS
Curso Técnico em Zootecnia Aula: 01/01 SUB TEMA: INTRODUÇÃO À Professor: Vitor Hugo SUB TEMA: HISTÓRIA DA HÁ MUITO TEMPO MAIS DE 5 MIL ANOS PROCURAM-SE SUBSTÂNCIAS QUÍMICAS COM O OBJETIVO DE CURAR AS MAIS
Cloridrato de Lidocaína
 Cloridrato de Lidocaína Hipolabor Farmacêutica Ltda. Geleia Tópica 2% 20mg/g 1 cloridrato de lidocaína Medicamento Genérico Lei n 9.787, de 1999 NOME GENÉRICO: cloridrato de lidocaína FORMA FARMACÊUTICA:
Cloridrato de Lidocaína Hipolabor Farmacêutica Ltda. Geleia Tópica 2% 20mg/g 1 cloridrato de lidocaína Medicamento Genérico Lei n 9.787, de 1999 NOME GENÉRICO: cloridrato de lidocaína FORMA FARMACÊUTICA:
Folheto informativo: Informação para o utilizador. Dolban 0,75 mg/g creme. Capsaícina, óleo-resina (expressa em capsaícina)
 Folheto informativo: Informação para o utilizador Dolban 0,75 mg/g creme Capsaícina, óleo-resina (expressa em capsaícina) Leia com atenção todo este folheto antes de começar a utilizar este medicamento
Folheto informativo: Informação para o utilizador Dolban 0,75 mg/g creme Capsaícina, óleo-resina (expressa em capsaícina) Leia com atenção todo este folheto antes de começar a utilizar este medicamento
Laboratório Janssen cilag Farmacêutica Ltda. Referência Tylenol
 Laboratório Janssen cilag Farmacêutica Ltda. Referência Tylenol Apresentação de Tylenol Gotas (paracetamol) Solução oral 200 mg/ml em frasco plástico com 15 ml. USO ADULTO E PEDIÁTRICO USO ORAL COMPOSIÇÃO
Laboratório Janssen cilag Farmacêutica Ltda. Referência Tylenol Apresentação de Tylenol Gotas (paracetamol) Solução oral 200 mg/ml em frasco plástico com 15 ml. USO ADULTO E PEDIÁTRICO USO ORAL COMPOSIÇÃO
cloridrato de nafazolina
 cloridrato de nafazolina Medley Farmacêutica Ltda. solução nasal 0,5 mg/ml cloridrato de nafazolina Medicamento Genérico, Lei nº 9.787, de 1999 APRESENTAÇÃO Solução nasal 0,5 mg/ml: embalagem contendo
cloridrato de nafazolina Medley Farmacêutica Ltda. solução nasal 0,5 mg/ml cloridrato de nafazolina Medicamento Genérico, Lei nº 9.787, de 1999 APRESENTAÇÃO Solução nasal 0,5 mg/ml: embalagem contendo
APROVADO EM INFARMED
 FOLHETO INFORMATIVO Tirocular, colírio, solução Leia atentamente este folheto antes de tomar o medicamento Conserve este Folheto Informativo. Pode ter necessidade de o reler. Caso tenha dúvidas, consulte
FOLHETO INFORMATIVO Tirocular, colírio, solução Leia atentamente este folheto antes de tomar o medicamento Conserve este Folheto Informativo. Pode ter necessidade de o reler. Caso tenha dúvidas, consulte
Dimensão Segurança do Doente Check-list Procedimentos de Segurança
 1. 1.1 1.2 Cultura de Segurança Existe um elemento(s) definido(s) com responsabilidade atribuída para a segurança do doente Promove o trabalho em equipa multidisciplinar na implementação de processos relativos
1. 1.1 1.2 Cultura de Segurança Existe um elemento(s) definido(s) com responsabilidade atribuída para a segurança do doente Promove o trabalho em equipa multidisciplinar na implementação de processos relativos
Anexo II. Conclusões científicas
 Anexo II Conclusões científicas 15 Conclusões científicas Haldol, que contém a substância ativa haloperidol, é um antipsicótico do grupo das butirofenonas. É um potente antagonista dos recetores de dopamina
Anexo II Conclusões científicas 15 Conclusões científicas Haldol, que contém a substância ativa haloperidol, é um antipsicótico do grupo das butirofenonas. É um potente antagonista dos recetores de dopamina
0,4 mililitros contêm 0,138 mg de fumarato de cetotifeno, correspondente a 0,1 mg de cetotifeno.
 1. NOME DO MEDICAMENTO ZADITEN 0,25 mg/ml, colírio, solução em recipiente unidose 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA 0,4 mililitros contêm 0,138 mg de fumarato de cetotifeno, correspondente a 0,1
1. NOME DO MEDICAMENTO ZADITEN 0,25 mg/ml, colírio, solução em recipiente unidose 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA 0,4 mililitros contêm 0,138 mg de fumarato de cetotifeno, correspondente a 0,1
Brochura Educacional para os Médicos Prescritores sobre a PrEP
 Brochura Educacional para os Médicos Prescritores sobre a PrEP Informação de segurança importante para os médicos prescritores sobre a profilaxia pré-exposição (PrEP) com Emtricitabina/Tenofovir disoproxil
Brochura Educacional para os Médicos Prescritores sobre a PrEP Informação de segurança importante para os médicos prescritores sobre a profilaxia pré-exposição (PrEP) com Emtricitabina/Tenofovir disoproxil
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO VETERINÁRIO
 ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO VETERINÁRIO 1. NOME DO MEDICAMENTO VETERINÁRIO Zuritol 50 mg/ml suspensão oral para suínos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada ml contém: Substância
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO VETERINÁRIO 1. NOME DO MEDICAMENTO VETERINÁRIO Zuritol 50 mg/ml suspensão oral para suínos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada ml contém: Substância
APROVADO EM INFARMED
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Fucidine H 20 mg/g + 10 mg/g Creme 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Ácido fusídico 20 mg/g e Acetato de hidrocortisona 10 mg/g.
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Fucidine H 20 mg/g + 10 mg/g Creme 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Ácido fusídico 20 mg/g e Acetato de hidrocortisona 10 mg/g.
Utilize este medicamento exatamente como está descrito neste folheto, ou de acordo com as indicações do seu médico ou farmacêutico.
 Folheto informativo: Informação para o utilizador Lidina 0,125 mg/0,5 ml, colírio, solução Cetotifeno Leia com atenção todo este folheto antes de começar a utilizar este medicamento, pois contém informação
Folheto informativo: Informação para o utilizador Lidina 0,125 mg/0,5 ml, colírio, solução Cetotifeno Leia com atenção todo este folheto antes de começar a utilizar este medicamento, pois contém informação
Guia do Prescritor. Versão 1 (novembro 2017)
 Versão (novembro 7) CONTEÚDO Introdução sobre MAVENCLAD Regimes de tratamento Monitorização durante o tratamento Contagens de linfócitos Infeções graves Leucoencefalopatia multifocal progressiva Neoplasias
Versão (novembro 7) CONTEÚDO Introdução sobre MAVENCLAD Regimes de tratamento Monitorização durante o tratamento Contagens de linfócitos Infeções graves Leucoencefalopatia multifocal progressiva Neoplasias
tedol Folheto informativo: Informação para o utilizador
 Folheto informativo: Informação para o utilizador tedol 20 mg/ml champô Cetoconazol Leia com atenção todo este folheto antes de começar a utilizar este medicamento pois contém informação importante para
Folheto informativo: Informação para o utilizador tedol 20 mg/ml champô Cetoconazol Leia com atenção todo este folheto antes de começar a utilizar este medicamento pois contém informação importante para
Anexo III. Alterações nas secções relevantes do resumo das caraterísticas do medicamento e do folheto informativo
 Anexo III Alterações nas secções relevantes do resumo das caraterísticas do medicamento e do folheto informativo Nota: As alterações ao Resumo das Características do Medicamento e ao Folheto Informativo
Anexo III Alterações nas secções relevantes do resumo das caraterísticas do medicamento e do folheto informativo Nota: As alterações ao Resumo das Características do Medicamento e ao Folheto Informativo
BULA. Terramicina com sulfato de polimixina B. (cloridrato de oxitetraciclina e sulfato de polimixina B) Pomada Oftálmica
 BULA Terramicina com sulfato de polimixina B (cloridrato de oxitetraciclina e sulfato de polimixina B) Pomada Oftálmica PARTE I IDENTIFICAÇÃO DO PRODUTO Nome: Terramicina com sulfato de polimixina B -
BULA Terramicina com sulfato de polimixina B (cloridrato de oxitetraciclina e sulfato de polimixina B) Pomada Oftálmica PARTE I IDENTIFICAÇÃO DO PRODUTO Nome: Terramicina com sulfato de polimixina B -
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 9 1. NOME DO MEDICAMENTO VETERINÁRIO COLIVET 2 000 000 UI/ml, concentrado para solução oral para suínos e aves. 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 9 1. NOME DO MEDICAMENTO VETERINÁRIO COLIVET 2 000 000 UI/ml, concentrado para solução oral para suínos e aves. 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
Classificando as crises epilépticas para a programação terapêutica Farmacocinética dos fármacos antiepilépticos... 35
 Índice Parte 1 - Bases para a terapêutica com fármacos antiepilépticos Classificando as crises epilépticas para a programação terapêutica... 19 Classificação das Crises Epilépticas (1981)... 20 Classificação
Índice Parte 1 - Bases para a terapêutica com fármacos antiepilépticos Classificando as crises epilépticas para a programação terapêutica... 19 Classificação das Crises Epilépticas (1981)... 20 Classificação
Andolba. Bula para paciente. Aerossol. 45 mg + 5 mg + 5 mg
 Andolba Bula para paciente Aerossol 45 mg + 5 mg + 5 mg ANDOLBA benzocaína, triclosana e mentol AEROSSOL FORMAS FARMACÊUTICAS E APRESENTAÇÕES: AEROSSOL Embalagens contendo 1 tubo de 43g. USO TÓPICO USO
Andolba Bula para paciente Aerossol 45 mg + 5 mg + 5 mg ANDOLBA benzocaína, triclosana e mentol AEROSSOL FORMAS FARMACÊUTICAS E APRESENTAÇÕES: AEROSSOL Embalagens contendo 1 tubo de 43g. USO TÓPICO USO
Conclusões científicas
 Anexo II Conclusões científicas e fundamentos para a revogação ou alteração dos termos das Autorizações de Introdução no Mercado e explicação detalhada para as diferenças relativamente à recomendação do
Anexo II Conclusões científicas e fundamentos para a revogação ou alteração dos termos das Autorizações de Introdução no Mercado e explicação detalhada para as diferenças relativamente à recomendação do
Ensaios clínicos. Definições. Estudos de intervenção. Conceitos e desenhos
 Ensaios clínicos Conceitos e desenhos Definições Basicamente, os estudos médicos são classificados em dois grandes grupos: Estudos observacionais Edson Zangiacomi Martinez Depto. de Medicina Social Faculdade
Ensaios clínicos Conceitos e desenhos Definições Basicamente, os estudos médicos são classificados em dois grandes grupos: Estudos observacionais Edson Zangiacomi Martinez Depto. de Medicina Social Faculdade
RESUMO DAS CARATERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARATERÍSTICAS DO MEDICAMENTO Página 1 de 19 1. NOME DO MEDICAMENTO VETERINÁRIO NOSEDORM 5 mg/ml Solução injetável para cães e gatos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada ml de solução
RESUMO DAS CARATERÍSTICAS DO MEDICAMENTO Página 1 de 19 1. NOME DO MEDICAMENTO VETERINÁRIO NOSEDORM 5 mg/ml Solução injetável para cães e gatos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada ml de solução
TYLEMAX paracetamol. APRESENTAÇÃO Linha Farma: Solução oral em frasco plástico opaco gotejador com 10 ml, contendo 200mg/mL de paracetamol.
 TYLEMAX paracetamol APRESENTAÇÃO Linha Farma: Solução oral em frasco plástico opaco gotejador com 10 ml, contendo 200mg/mL de paracetamol. USO ADULTO E PEDIÁTRICO USO ORAL COMPOSIÇÃO Cada ml da solução
TYLEMAX paracetamol APRESENTAÇÃO Linha Farma: Solução oral em frasco plástico opaco gotejador com 10 ml, contendo 200mg/mL de paracetamol. USO ADULTO E PEDIÁTRICO USO ORAL COMPOSIÇÃO Cada ml da solução
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 14 1. NOME DO MEDICAMENTO VETERINÁRIO Metricure 500 mg suspensão intrauterina para vacas 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada seringa de 19g
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 14 1. NOME DO MEDICAMENTO VETERINÁRIO Metricure 500 mg suspensão intrauterina para vacas 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada seringa de 19g
Cada mililitro de gotas nasais, solução contém 5 mg de Cloridrato de fenilefrina, como substância ativa.
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Neo-Sinefrina 5 mg/ml Gotas nasais, solução 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada mililitro de gotas nasais, solução contém 5 mg
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Neo-Sinefrina 5 mg/ml Gotas nasais, solução 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada mililitro de gotas nasais, solução contém 5 mg
Nosso objetivo: Exposição de casos clínicos, compartilhar conhecimentos e ampliar as possibilidades de atendimentos no seu dia a dia profissional.
 GEN IV Grupo de Estudos em Neurometria Discussão de Casos Clínicos Nosso objetivo: Exposição de casos clínicos, compartilhar conhecimentos e ampliar as possibilidades de atendimentos no seu dia a dia profissional.
GEN IV Grupo de Estudos em Neurometria Discussão de Casos Clínicos Nosso objetivo: Exposição de casos clínicos, compartilhar conhecimentos e ampliar as possibilidades de atendimentos no seu dia a dia profissional.
Anexo II. Conclusões científicas
 Anexo II Conclusões científicas 7 Conclusões científicas O pó e solvente Solu-Medrol 40 mg para solução para injeção (a seguir designado «Solu-Medrol») contém metilprednisolona e, tratando-se de um excipiente,
Anexo II Conclusões científicas 7 Conclusões científicas O pó e solvente Solu-Medrol 40 mg para solução para injeção (a seguir designado «Solu-Medrol») contém metilprednisolona e, tratando-se de um excipiente,
AVALIAÇÃO DA SATISFAÇÃO E DA QUALIDADE APERCEBIDA PELOS UTENTES DO CHMA 2016 RELATÓRIO DETALHADO
 AVALIAÇÃO DA SATISFAÇÃO E DA QUALIDADE APERCEBIDA PELOS UTENTES DO CHMA 2016 RELATÓRIO DETALHADO 1 INDICE Aspetos Metodológicos 3 Consulta Externa 9 Consulta Externa Caracterização dos Respondentes 10
AVALIAÇÃO DA SATISFAÇÃO E DA QUALIDADE APERCEBIDA PELOS UTENTES DO CHMA 2016 RELATÓRIO DETALHADO 1 INDICE Aspetos Metodológicos 3 Consulta Externa 9 Consulta Externa Caracterização dos Respondentes 10
QUÍMICA MEDICINAL. Em temos etimológicos pode considerar-se um ramo da farmacologia (de pharmakon + logos = estudo dos fármacos).
 QUÍMICA MEDICINAL Sentido prospectivo envolve o planeamento e produção de compostos que podem ser usados em medicina para a prevenção, tratamento e/ou cura de doenças humanas ou de animais. Em temos etimológicos
QUÍMICA MEDICINAL Sentido prospectivo envolve o planeamento e produção de compostos que podem ser usados em medicina para a prevenção, tratamento e/ou cura de doenças humanas ou de animais. Em temos etimológicos
Se não se sentir melhor ou se piorar, tem de consultar um médico.
 Folheto Informativo: Informação para o doente Aciclovir Axone 50 mg/g Creme Aciclovir Leia com atenção todo este folheto antes de começar a utilizar este medicamento pois contém informação importante para
Folheto Informativo: Informação para o doente Aciclovir Axone 50 mg/g Creme Aciclovir Leia com atenção todo este folheto antes de começar a utilizar este medicamento pois contém informação importante para
MEDICAMENTO SIMILAR EQUIVALENTE AO MEDICAMENTO DE REFERÊNCIA. Creme dermatológico 1 mg/g Embalagens contendo 01 ou 50 bisnagas de 10 g.
 Cortitop acetato de dexametasona MEDICAMENTO SIMILAR EQUIVALENTE AO MEDICAMENTO DE REFERÊNCIA FORMA FARMACÊUTICA E APRESENTAÇÕES Creme dermatológico 1 mg/g Embalagens contendo 01 ou 50 bisnagas de 10 g.
Cortitop acetato de dexametasona MEDICAMENTO SIMILAR EQUIVALENTE AO MEDICAMENTO DE REFERÊNCIA FORMA FARMACÊUTICA E APRESENTAÇÕES Creme dermatológico 1 mg/g Embalagens contendo 01 ou 50 bisnagas de 10 g.
IDENTIFICAÇÃO DO MEDICAMENTO Abcd. Cardizem CD cloridrato de diltiazem
 IDENTIFICAÇÃO DO MEDICAMENTO Abcd Cardizem CD cloridrato de diltiazem FORMAS FARMACÊUTICAS E APRESENTAÇÕES Cápsula de liberação prolongada de 180 mg: embalagem com 16 cápsulas. Cápsula de liberação prolongada
IDENTIFICAÇÃO DO MEDICAMENTO Abcd Cardizem CD cloridrato de diltiazem FORMAS FARMACÊUTICAS E APRESENTAÇÕES Cápsula de liberação prolongada de 180 mg: embalagem com 16 cápsulas. Cápsula de liberação prolongada
ANEXO III SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO E FOLHETO INFORMATIVO
 ANEXO III SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO E FOLHETO INFORMATIVO Nota: Estas alterações ao Resumo das Características do Medicamento e ao Folheto Informativo são válidas
ANEXO III SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO E FOLHETO INFORMATIVO Nota: Estas alterações ao Resumo das Características do Medicamento e ao Folheto Informativo são válidas
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO. Zuritol 25 mg/ml solução oral para administração na água de bebida para galinhas
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO VETERINÁRIO Zuritol 25 mg/ml solução oral para administração na água de bebida para galinhas 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO VETERINÁRIO Zuritol 25 mg/ml solução oral para administração na água de bebida para galinhas 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO. Cada cápsula contém 300 mg de diosmina como substância ativa.
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Venex 300 mg Cápsulas 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada cápsula contém 300 mg de diosmina como substância ativa. Excipiente(s)
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Venex 300 mg Cápsulas 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada cápsula contém 300 mg de diosmina como substância ativa. Excipiente(s)
