Eliane Ferreira Rodrigues
|
|
|
- Rafael Arruda Salgado
- 8 Há anos
- Visualizações:
Transcrição
1 Eliane Ferreira Rodrigues Estudo das Alterações Cromossômicas e Análise de Metilação nos Genes p15 INK4B e p16 INK4A em Síndrome Mielodisplásica Primária na Infância no Estado do Rio de Janeiro DISSERTAÇÃO DE MESTRADO SUBMETIDA À UNIVERSIDADE FEDERAL DO RIO DE JANEIRO VISANDO A OBTENÇÃO DO GRAU DE MESTRE EM CIÊNCIAS BIOLÓGICAS (BIOFÍSICA) Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Biofísica Carlos Chagas Filho 2007
2 Livros Grátis Milhares de livros grátis para download.
3 ELIANE FERREIRA RODRIGUES Estudo das Alterações Cromossômicas e Análise de Metilação nos Genes p15 INK4B e p16 INK4A em Síndrome Mielodisplásica Primária na Infância no Estado do Rio de Janeiro Dissertação de Mestrado apresentada ao programa de Pós-graduação em Biofísica, Instituto de Biofísica Carlos Chagas Filho, da Universidade Federal do Rio de Janeiro, como parte dos requisitos necessários à obtenção do título de Mestre em Ciências. Orientadoras: Teresa de Souza Fernandez Eliana Saul Furquim Werneck Abdelhay 2007
4 ii RODRIGUES, Eliane Ferreira Estudo das Alterações Cromossômicas e Análise de Metilação nos Genes p15 INK4B e p16 INK4A em Síndrome Mielodisplásica Primária na Infância no Estado do Rio de Janeiro / Eliane Ferreira Rodrigues. Rio de Janeiro: UFRJ, IBCCF, XVIII, 119 p. Orientadoras: Teresa de Souza Fernandez e Eliana Saul Furquim Werneck Abdelhay Dissertação (Mestrado em Ciências) UFRJ/ IBCCF/ Programa de Pósgraduação em Biofísica - Biologia Molecular, Referências Bibliográficas: f Síndrome Mielodisplásica Primária na Infância. 2. Alterações Cromossômicas. 3. Metilação 4. p15 INK4B e p16 INK4A. I Fernandez, Teresa de Souza; Abdellhay, Eliana Saul Furquim Werneck II. Universidade Federal do Rio de Janeiro, Instituto de Biofísica Carlos Chagas Filho, Programa de Pós-graduação em Biofísica. III. Título
5 iii Este trabalho foi desenvolvido no Laboratório de Citogenética, no Centro de Transplante de Medula Óssea do Instituto Nacional do Câncer (CEMO-INCA), em colaboração com o Serviço de Genética Humana da Universidade do Estado do Rio de Janeiro (SERVGEN-UERJ). Durante o desenvolvimento deste projeto de pesquisa fomos beneficiados por auxílios do Ministério da Saúde- INCA e da FAPERJ.
6 iv
7 v A minha amada família.
8 vi AGRADECIMENTOS - À Deus por ter me protegido e acompanhado em toda a minha caminhada; - Aos meus pais pelo amor incondicional, incentivo, apoio, compreensão e paciência ao longo de toda a minha vida; - Ao meu irmão por se fazer presente na minha vida e pelo apoio e incentivo; - Ao meu namorado Leonardo, por tornar meus dias mais felizes e me incentivar a cada dia a seguir sempre em frente, por toda a sua ajuda na confecção desta tese, compreensão, carinho e paciência; - Ao Dr. Luis Fernando Bouzas diretor do CEMO-INCA, pela oportunidade e todo o apoio que recebemos para realização deste projeto de pesquisa; - À Dra. Teresa de Souza Fernandez, minha orientadora, por acreditar no meu potencial incentivando-me a sempre conseguir o melhor, por todo conhecimento transmitido e principalmente pela amizade; - À Dra. Eliana Abdelhay pelo seus ensinamentos, experiência, apoio e auxílio durante a elaboração desta tese; - Às Professoras Dra. Cíntia Barros Santos-Rebouças e Dra. Márcia Mattos Gonçalves Pimentel do Laboratório de Serviço de Genética Humana da Universidade do Estado do Rio de Janeiro (SERVGEN-UERJ), pela valiosa colaboração e enorme ajuda em toda a parte de biologia molecular; - À Dra. Gilda Alves Brown do Laboratório de Genética Aplicada Serviço de Hematologia do INCA pelo auxílio na obtenção e no cultivo da linhagem celular DLD-1; - Aos pesquisadores Dr. André Vettore e Dra. Andréa Seixas e ao técnico Fabrício de Carvalho do Instituto de Ludwig São Paulo por cederem a linhagem DLD-1 para a nossa pesquisa;
9 vii - À Dra. Hilda do Laboratório de Imunologia do Centro de Transpalnte de Medula Óssea INCA por ter cedido a linhagem Raji para a nossa pesquisa; - À Beatriz e Lílian do Programa de Biologia Molecular do Instituto de Biofísica -UFRJ, pelo auxílio no sequenciamento das amostras; - Ás minhas amigas Daiane e Michelle por todo o carinho e companherismo durante toda a minha vida acadêmica, e pelo enorme laço de amizade que nos une; - Às minhas amigas Adriana e Luize por toda a ajuda prática, pelos conselhos e pelas demonstrações de carinho e amizade ao longo destes anos; - Aos amigos de trabalho Aline, Moises, Amanda e Luciano por todos os momentos de descontração; - Aos mais recentes amigos Eleonidas e Elenice por suas preciosas dicas e experiência; - À todas as pessoas do laboratório SERVGEN-UERJ, Claúdia, Mário, Jussara, Juliana, Karla, Natália, Adriana, Cristiane e Mariana por terem me recebido com carinho e amizade no laboratório; - À toda equipe do CEMO, médicos, enfermeiros e técnicos que de certa forma contribuíram para a realização deste projeto; - Aos meus professores da Faculdade de Formação de Professores da UERJ que contribuíram para minha formação;
10 viii RESUMO A Síndrome Mielodisplásica (SMD) primária é rara na infância representando cerca de 4% de todas as malignidades hematológicas desta faixa etária. Devido a sua raridade muitas vezes torna-se difícil o seu diagnóstico. Alterações citogenéticas envolvendo o cromossomo 7 (-7/7q-) representam as principais alterações neste grupo de pacientes e estão associadas com mau prognóstico. Entretanto, existem controvérsias em relação ao valor prognóstico de algumas alterações cromossômicas como +8 e del(11)(q23). Mudanças no padrão de metilação do DNA são freqüentemente observadas em adultos e parecem estar associadas com a transformação leucêmica. No entanto, poucos estudos mostraram o papel de mudanças no padrão de metilação em genes importantes que controlam o ciclo celular, como p15 INK4B e p16 INK4A em SMD na infância. Este trabalho apresentou como objetivos caracterizar as alterações cromossômicas em SMD primária na infância e analisar a presença de metilação na região promotora dos genes p15 INK4B e p16 INK4A, no sentido de identificar marcadores biológicos que auxiliem o diagnóstico e a definição de fatores prognósticos, contribiundo na escolha de protocolos de tratamento. Foram analisados citogeneticamente, no período de 1991 a 2006, 64 pacientes, com idades entre 5 meses a 18 anos. A análise citogenética foi realizada através da técnica de bandeamento G e através da citogenética molecular (FISH). A frequência de cariótipos anormais foi 72% dos 61 pacientes analisados. Em três casos o índice mitótico foi nulo. De acordo com a classificação para SMD da infância, 35 pacientes apresentaram CR, 14 AREB, 10 AREB-t e 5 LMMJ. Nos subtipos mais avançados da doença a freqüência de casos com alterações cromossômicas foi maior. As anomalias cromossômicas mais freqüentes foram: -7/7q -, del(11)(q23), cariótipos complexos e del(17)(p12). Não foi verificada uma alteração cromossômica específica por subtipo. Nossos resultados sugerem que o padrão cromossômico em SMD primária na infância é caraterizado principalmente por perdas parcias e completas de cromossomos (deleções e monossomias), assim como ganhos cromossômicos (trissomias). A análise citogenética auxiliou no diagnóstico dos casos com suspeita de SMD primária pediátrica e foi uma importante ferramenta para a escolha do tratamento. O estudo da presença de metilação na região promotora dos genes p15 INK4B e p16 INK4A em 45 pacientes foi realizado pela técnica reação em cadeia da polimerase específica para a metilação (MSP). Todas as amostras positivas para a metilação de ambos os genes foram sequenciadas, como metodologia confirmatória. A análise molecular revelou que 16 pacientes (35,5%) apresentaram metilação para o gene p15 INK4B e apenas 4 (8,8%) para o gene p16 INK4A. As maiores freqüências de metilação para os genes p15 INK4B e p16 INK4A foram observadas nos subtipos mais agressivos de SMD. Evolução da doença foi verificada em 22 pacientes (36%). A correlação entre a presença de uma alteração cromossômica específica com metilação nos genes p15 INK4B e p16 INK4A mostrou uma forte associação entre a metilação em p15 INK4B e alterações envolvendo o cromossomo 7, sugerindo uma provável via de evolução da doença. Nossos resultados sugerem que as alterações cromossômicas, -7/7q-; +8 e del(11)(q23), e a presença de metilação em p15 INK4B e p16 INK4A estão associadas com mau prognóstico, sendo prováveis marcadores biológicos de evolução da doença.
11 ix ABSTRACT Primary Myelodysplastic Syndrome (MDS) is rare in children representing around 4% of all hematologic malignancies in childhood. Because of its rarity the diagnosis is usually difficult. Chromosomal alterations involving chromosome 7 (-7/7q-) represent the main alteration in this group of patients and are associated with poor prognosis. However, there is controversy in relation of prognosis value of some chromosomal alterations as +8 and del(11)(q23). Changes on the DNA methylation pattern are frequently observed in adults and seem to be associated with leukemic transformation. Nevertheless, few studies investigated the role of changes on methylation pattern in important genes that regulate cell cycle, as p15 INK4B and p16 INK4A in primary MDS in childhood. The aim of this study was to characterize chromosomal alterations in childhood MDS and analyze the presence of methylation in promoter regions of p15 INK4B and p16 INK4A genes, to identify biologic markers that would aid the diagnosis and the definition of prognostic factors, contributing on treatment choice. In this study 64 patients with age between 5 months to 18 years old were analyzed cytogenetically, between 1991 and Cytogentic analysis was performed by G banding and by molecular cytogenetic (FISH). The frequency of abnormal karyotypes was 72% in 61 patients analyzed. In three cases the mitotic index was null. Acording to the classification of primary MDS in childhood, 35 patients presented CR, 14 RAEB, 10 RAEB-t and 5 JMML. In more advanced subtypes of disease the frequency of cases with chromosomal alterations was higher. The most frequent chromosomal abnormalities were: -7/7q -, del(11)(q23), complex karyotypes and del(17)(p12). No specific chromosomal alteration could be related to subtype. Our results suggest that the chromossomal pattern in primary MDS childhood is characterized mainly by partial and complete lose of chromosomes (deletion and monosomy), as well as chromosomal gain (trisomy). The cytogenetic analysis aided in diagnosis of cases with suspicion of pediatric primary MDS and it was an important tool for treatment choose. The study of methylation in the promoter region of p15 INK4B and p16 INK4A genes in 45 patients was performed by methyl specific polymerase chain reaction (MSP). All samples positive for methylation in both genes were sequenced as a confirmatory methodology. The molecular analysis revealed that 16 patients (35,5%) presented methylation on p15 INK4B gene and 4 (8,8%) on p16 INK4A gene. The higher frequency of methylation in p15 INK4B and p16 INK4A genes was observed in more aggressive subtypes of MDS. Evolution of disease was verified in 22 cases (36%). The correlation between karyotype and methylation in the p15 INK4B and p16 INK4A genes showed a strong association between methylation in p15 INK4B gene and alterations involving chromosome 7, suggesting a pathway of disease evolution. Our results suggest that chromosomal alterations 7/7q-, +8, del(11)(q23) and the presence of methylation in p15 INK4B and p16 INK4A were associated with poor prognosis, being possibe biologic markers of disease evolution.
12 x LISTA DE ABREVIATURAS E SIGLAS A ALIP AR ARDM ARDM-SA AREB AREB-t ARSA ARA-C ATG C CDK CDKI CpG CR adenina localização anormal de precurssores imaturos anemia refratária anemia refratária com displasias multilinhagem anemia refratária com displasias multilinhagem com sideroblastos em anel anemia refratária com excesso de blastos anemia refratária com excesso de blastos em transformação anemia refratária com sideroblastos em anel arabinosídeo citosina anti-linfócito globulina citosina quinases dependentes de ciclinas inibidores de quinases dependentes de ciclinas região de alta densidade de dinucleotídeos citosina-guanina citopenia refratária CSF-1 fator estimulador de colônia 1 CTH DAPI datp dctp del dgtp DNA células tronco hematopoéticas 4,6-diamidino-2-fenilindol 2 desoxiadenosina 5 trifosfato 2 desoxicitidina 5 trifosfato deleção 2 desoxiguanosina 5 trifosfato ácido desoxirribonucléico
13 xi DNMT dntps dttp EDTA FAB FISH FITC G DNA metiltransferase desoxirribonucleotídeos trifosfatos 2 desoxitimidina 5 trifosfato ácido etilenodiaminotetrácético Grupo Franco-Americano-Britânico hibridização in situ por fluorescência isotiocianato de fluoresceína guanina GCB-MDS-PED Grupo Cooperativo Brasileiro em SMD Pediátrica GDP GM-CSF GTP GTPase G6PD HDACs HLA HPRT IMT inv IPSS Kb LA LLA LMA guanosina 5 difosfato fator de estimulação de colônias granulócito-macrófago guanosina 5 trifosfato guanosina trifosfatase glicose 6 fosfato desidrogenase histonas desacetilases antígeno de histocompatibilidade hipoxantina fosforibosil transferase inibidores da metiltransferase inversão Sistema Internacional de Escala Prognóstica Kilobases leucemia aguda leucemia linfoblástica aguda leucemia mielóide aguda
14 xii LMMC LMMJ M MO ml MPBs MSP leucemia mielomonocítica crônica leucemia mielomonocítica juvenil metilado medula óssea mili litro proteínas ligadoras de CpGs metilados reação em cadeia da polimerase específica para a metilação NF1 neurofibromatose do tipo 1 OMS p Ph prb q RFLP RNA rpm RPMI SAM SD SMD T t TCTCU TCTH Organização Mundial de Saúde braço curto do cromossomo cromossomo Philadelphia proteína de retinoblastoma braço longo do cromossomo polimorfismo de comprimento de fragmentos de restrição ácido ribonucléico rotações por minuto Roswell Park Memorial Institute - meio de cultivo de células S-adenosil-L-metionina Síndrome de Down Síndrome Mielodisplásica timina translocação transplante de células tronco de cordão umbilical transplante de células tronco hematopoéticas
15 xiii TMO TNF-α TNFR-α U transplante de medula óssea fator de necrose tumoral- α receptor de fator de necrose tumoral- α não metilado + ganho de cromossomo - perda de cromossomo ºC graus Celsius
16 xiv ISTA DE FIGURAS Figuras p. 1 Modelo de Múltiplas Etapas no Desenvolvimento da SMD Região de metilação na seqüência do DNA e adição do grupamento metila pelas enzimas DNMT Atividade transcricional do gene de acordo com o padrão de metilação Modelo para o silenciamento transcricional dependente de metilação Classificação da Síndrome Mielodisplásica e Doenças Mieloproliferativas na Infância Efeito do tratamento com bissulfito em uma amostra de DNA com seqüências ricas em dinucleotídeos CpG Freqüência das alterações cromossômicas em SMD primária na infância Análise por hibridização in situ por fluorescência utilizando a sonda de dupla marcação do cromossomo 7 e a sonda da região 11q23 (MLL) Análise por citogenética clássica e citogenética molecular (FISH) utilizando a sonda da região p13.1 do cromossomo 17 (p53) e a sonda da região 11q23 (MLL) Análise por citogenética clássica e citogenética molecular (FISH) utilizando a sonda de dupla marcação do cromossomo Análise por citogenética clássica e citogenética molecular (FISH) utilizando a sonda da região p13.1 do cromossomo 17 (p53) Análise por hibridização in situ por fluorescência utilizando a sonda de dupla 12 marcação do cromossomo Fotografia de gel de poliacrilamida 5% utilizado para verificar a amplificação dos produtos de PCR referente a análise de metilação do gene p15 INK4B após a modificação do DNA com bisulfito... 55
17 xv 14 Análise do sequenciamento do gene p15 INK4B (5 3 ) através do programa BioEdit Sequence Alignment Editor Fotografia de gel de poliacrilamida 5% utilizado para verificar a amplificação dos produtos de PCR referente à análise de metilação da região promotora do gene p16 após a modificação do DNA com bisulfito Análise do sequenciamento do gene p16 INK4A (5 3 ) através do programa BioEdit Sequence Alignment Editor Correlação entre a presença de metilação nos genes p15 INK4B e 16 INK4A e o cariótipo em crianças portadoras de SMD primária... 66
18 xvi LISTA DE TABELAS Tabelas p. 1 Classificação das Síndromes Mielodisplásicas segundo os critérios propostos pelo Grupo FAB em Classificação das Síndromes Mielodisplásicas segundo a proposta OMS em Pontuação segundo os Parâmetros Críticos do IPSS (1997) em Síndromes Mielodisplásicas Diferenças entre SMD em Crianças e em Adultos Oligonucleotídeos utilizados na técnica MSP para análise dos genes p15 INK4B e p16 INK4A Análise Citogenética em Síndrome Mielodisplásica Primária na Infância Freqüência de Casos com Cariótipos Anormais em SMD Primária na Infância Distribuição do Padrão Cromossômico por Subtipo de SMD Primária na Infância Freqüência de Pacientes com SMD Primária na Infância de acordo com o IPSS (1997) que mostraram evolução da doença Identificação de Metilação no Gene p15 INK4B em SMD Primária na Infância Freqüência de Metilação no Gene p15 INK4B nos Subtipos da SMD Primária na Infância Identificação de Metilação no Gene p16 INK4A em SMD primária na infância Freqüência de Metilação no Gene p16 INK4A nos Subtipos da SMD Primária na Infância Correlação entre a Presença de Metilação nos Genes p15 INK4B e p16 INK4A com o Padrão Cromossômico em SMD Primária da Infância... 64
19 xvii SUMÁRIO Resumo... viii Abstract... ix Lista de abreviaturas e siglas x Lista de figuras... xiv Lista de tabelas... xvi 1. Introdução Síndrome Mielodisplásica Classificação e Escala Prognóstica em SMD Primária Teoria de Múltiplas Etapas no Desenvolvimento da SMD Primária Alterações Cromossômicas em SMD Primária Oncogengenes e Genes Supressores de Tumor Envolvidos no Desenvolvimento da SMD Primária Alterações Epigenéticas em SMD Primária: Metilação dos Membros da Família InK4 p15 e p SMD Primária na Infância Objetivos Materiais e Métodos Pacientes Análise Citogenética Cultura de Células de Medula Óssea Término das Culturas e Preparação das Lâminas Bandeamento G Análise Cromossômica Citogenética Molecular: Análise por Hibridização in situ por Fluorescência (FISH) Análise Molecular Cultura de Células da Linhagem DLD-1 e Raji Extração de DNA Análise de Metilação dos Genes p15 INK4B e p16 INK4A pelo Método MSP Tratamento do DNA com Bisulfito Reação em Cadeia da Polimerase Específica para a Metilação (MSP) Avaliação dos Produtos Gerados pela PCR nos Genes p15 INK4B e p16 INK4A... 39
20 xviii Sequenciamento de DNA Resultados Análise Citogenética em Síndrome Mielodisplásica Primária na Infância Freqüência de Casos com Alterações Cromossômicas por Subtipos de SMD Primária na Infância Citogenéica Molecular: Aplicação do FISH em SMD Primária na Infância Distribuição dos Pacientes com SMD Primária na Infância segundo os Grupos de Risco (IPSS) Análise Molecular Análise da Freqüência de Metilação na Região Promotora do Gene p15 INK4 em Pacientes com SMD Primária na Infância Confirmação por Sequenciamento das Amostras Positivas para a Metilação do Gene p15 INK4B Freqüência de Metilação em p15 INK4B nos Subtipos de SMD Primária na Infância Análise da Freqüência de Metilação no Gene p16 INK4A em Pacientes com SMD Primária na Infância Confirmação por Sequenciamento das Amostras Positivas para a Metilação do Gene p16 INK4A Freqüência de Metilação na Região Promotora do Gene p16 INK4A nos Subtipos de SMD Primária na Infância Correlação entre a Presença de Metilação nos Genes p15 INK4B e p16 INK4A e o Padrão Cromossômico em SMD Primária na Infância Discussão Conclusões Referências Bibliográficas Anexos Anexo Aprovação pelo Comitê de Ética do Projeto de Pesquisa Termo Informado e Esclarecido Anexo Cariótipos... 99
21 1 1. INTRODUÇÃO 1.1 Síndrome Mielodisplásica A síndrome mielodisplásica (SMD) compreende um grupo de doenças hematopoéticas de natureza clonal de célula tronco pluripotente, que se caracteriza por uma hematopoese ineficaz, apoptose intramedular aumentada, presença de displasias na medula óssea e citopenias em uma ou mais linhagens (DELFORGE, 2003). Uma grande variedade de agentes genotóxicos têm sido implicada na sua etiologia, sendo os mais conhecidos e estudados as drogas citotóxicas, especialmente os agentes alquilantes e os inibidores da topoisomerase II, nestes casos a SMD é denominada secundária (NISSE et al., 2001). As SMDs primárias, ou de novo, ocorrem quando o paciente não foi submetido a nenhum tratamento prévio com medicamentos citotóxicos nem esteve em contato com agentes mutagênicos, não havendo portanto causa conhecida para o aparecimento da doença. Entretanto, há um consenso de que fatores hereditários, ambientais e a senescência da hematopoese podem influenciar no surgimento da SMD (LORAND-METZE, 2005). A SMD primária afeta preferencialmente pessoas acima dos 50 anos de idade, sendo rara na infância. A incidência anual desta síndrome é de aproximadamente a cada indivíduos da população geral e de a cada indivíduos da população idosa. O aumento da freqüência e da incidência da SMD podem ser atribuídos ao crescimento da expectativa de vida e ao reconhecimento e diagnóstico desta doença (NISHINO & CHANG, 2005). A história natural da SMD é altamente variável, podendo apresentar formas brandas, com sobrevivência alta e baixa taxa de transformação leucêmica ou formas mais agressivas que podem evoluir rapidamente para leucemia mielóide aguda (LMA). Pacientes com SMD raramente transformam para leucemia linfóide aguda (LLA) (DELFORGE, 2003).
22 2 Uma das características da SMD é a presença de citopenias periféricas, isoladas ou em associação. As citopenias mais comuns em SMD são anemia, neutropenia e a trombocitopenia. Uma outra característica é a presença de alterações morfológicas decorrentes de defeitos de diferenciação celular chamadas de displasias. Estas alterações ocorrem principalmente nas linhagens eritróide, granulocítica e megacariocítica (OGATA, 2006). A renovação celular é aumentada na maioria dos pacientes com mielodisplasia, sendo a medula óssea geralmente, hipercelular ou normocelular. O aparente paradoxo entre medula óssea hipercelular e sangue periférico com citopenias foi esclarecido quando se mostrou que pacientes com SMD apresentam taxas de apoptose intra-medular aumentada, causando assim as citopenias no sangue periférico. Nos estágios mais avançados da doença a taxa apoptótica diminui, permitindo a proliferação de células imaturas (blastos) e contribuindo para a transformação leucêmica (PARKER et al., 2000; HELLSTRÖM-LINDBERG et al., 2000). Em alguns casos raros, pacientes podem apresentar a medula óssea hipocelular, podendo levar a um diagnóstico duvidoso com anemia aplástica (WONG & SO, 2002). A SMD é considerada hipocelular se tiver menos de 30% de celularidade em indivíduos jovens, e menos de 20% em indivíduos idosos (TOMONAGA & NAGAI, 2002). O diagnóstico da SMD é feito inicialmente através de um hemograma (que indica a presença de uma ou mais citopenias no sangue periférico e ausência de resposta para vitamina B12 e ácido fólico), seguido da análise de biópsia e de mielograma de medula óssea para identificar as displasias presentes, a possível presença de blastos caracterizando estágios mais avançados da doença e a presença de precursores imaturos com localização anormal (ALIP). Estudos adicionais auxiliam no estabelecimento do diagnóstico, incluindo a análise citogenética e a imunofenotipagem (LIST et al., 2004). Grande variedade de tratamentos vem sendo utilizada em pacientes adultos e crianças com SMD primária, com o objetivo de eliminar as citopenias, assim como de recuperar a
23 3 hematopoese. Uma das terapias utilizadas é a de suporte que envolve as transfusões sanguíneas, antibióticos, fatores de crescimento isolados ou em combinação, ciclosporina ou anti-linfócito globulina (ATG) que são também utilizados em pacientes que apresentam medula óssea hipocelular. Nos subtipos mais avançados da SMD (AREB, AREB-t, LMMC) é utilizada a quimioterapia com agente único: hidroxiurea, etoposídeo, mercaptopurina, baixa dose de arabinosídeo citosina (ARA-C). Em alguns casos é utilizada a quimioterapia intensiva similar àquela dada a pacientes com LMA, como a combinação de fludarabina e alta dose de ARA-C, induzindo a remissão nesses doentes (HELLSTRÖM-LINDBERG et al., 2000). O transplante de células tronco hematopoéticas (TCTH) alogenêico é a única opção terapêutica curativa para pacientes com SMD, no entanto, o seu uso é limitado a pacientes até 55 anos de idade e que possuam doadores histocompatíveis (GIRALT, 2005; WONG et al., 2005). Para pacientes jovens com SMD ou LMA secundária a SMD, o TCTH alogenêico é apontado como a melhor opção de tratamento (YUSUF et al., 2004; ESPIGADO et al., 2005). Atualmente, o sangue de cordão umbilical tem sido utilizado como uma satisfatória fonte de células tronco para diversos grupos de pacientes adultos e pediátricos. Estudos demonstraram que após o transplante de sangue de cordão umbilical a taxa de recaída, de sobrevida livre da doença e a sobrevida total dos pacientes com malignidades mielóides é similar a de outras fontes de células tronco hematopoéticas (BALLEN et al., 2006; BRUNSTEIN et al., 2007). Desta forma, o sangue de cordão umbilical é uma fonte alternativa de células tronco hematopoéticas para pacientes que necessitam de um transplante alogenêico, mas não apresentam doadores histocompatíveis. Com a delineação das características biológicas que norteiam o fenótipo da SMD, novas drogas introduzidas no tratamento desta doença têm mostrado um grande potencial terapêutico. Como por exemplo, agentes imunossupressores, anti-angiogênicos (principalmente a talidommida) (MUSTO, 2004), citoprotetores (amifostina), inibidores do
24 4 receptor da tirosina quinase (mesilato de imatinibe) (GILES et al., 2003) e inibidor de farnesil transferase (inibidor da via Ras) (KURZROCK et al., 2004). Além disso, uma nova classe terapêutica chamada inibidores da metiltransferase (IMT) vem sendo utilizada no tratamento da SMD. Os representantes desta classe incluem a azacitidina (5-azacitidina) e decitabina (5- aza 2 deoxicitidina). Ambos são agentes hipometilantes que se incorporam no DNA e então irreversivelmente ligam-se e inibem a ação da DNA metiltransferase. Esta interação resulta inicialmente em um DNA semi-metilado, no entanto, após outros ciclos celulares, este, tornase totalmente não metilado. A ação destes fármacos leva à reativação de genes epigeneticamente reprimidos, como genes supressores de tumor. Resultados iniciais demonstraram que pacientes com SMD de alto risco têm um aumento no tempo de transformação para LMA e sobrevida (SILVERMAN & MUFTI, 2005; ATALLAH et al., 2007). Devido à introdução de novas formas de tratamento torna-se importante o estudo da correlação das características citogenéticas, celulares e moleculares com as características clínicas da doença e a resposta ao tratamento, auxiliando desta forma no desenvolvimento de esquemas de classificação e de escalas prognósticas Classificação e Escala Prognóstica em SMD Primária Até 1976 as mielodisplasias incluíam uma variedade de anormalidades hematológicas classificadas como síndromes ou estados pré-leucêmicos. Entretanto, essa classificação era insatisfatória, uma vez que não havia um termo definido para designar as citopenias geralmente associadas com a medula hiperplásica, com displasias e progressão variável para leucemia aguda. Em 1982, um grupo internacional de hematologistas franceses, americanos e britânicos (grupo FAB) aplicou o nome síndrome mielodisplásica e classificou esta doença em 5
25 5 subtipos (tabela 1), usando como critérios a porcentagem de blastos na medula óssea e no sangue periférico e características morfológicas (a presença ou ausência de sideroblastos em anel e de bastões de Auer) (BENNETT et al., 1982). Tabela 1: Classificação das Síndromes Mielodisplásicas segundo os Critérios propostos pelo Grupo FAB em 1982 Subtipo Monócitos (µl) Sangue Periférico Sideroblastos em anel (%) Medula óssea Células Blásticas (%) Sangue Medula Periférico óssea Bastões de Auer Medula óssea AR Não < 15 < 1 < 5 Não ARSA Não > 15 < 1 < 5 Não AREB Não Não < Não AREB-t Não Não > Sim ou Não LMMC > 1000 Não < 5 < 20 Não AR- anemia refratária; ARSA- anemia refratária com sideroblastos em anel; AREB- anemia refratária com excesso de blastos; AREB-t- anemia refratária com excesso de blastos em transformação; LMMC- leucemia mielomonocítica crônica (BENNETT et al., 1982). Desde que foi introduzida, vários estudos comprovaram a utilidade da classificação FAB, tanto para o monitoramento de estudos envolvendo um grande número de pacientes com SMD, permitindo comparações entre os diversos trabalhos, quanto para o tratamento de pacientes. No entanto, para a determinação de um prognóstico preciso, esta classificação apresentava alguns problemas: distinguia somente duas categorias de risco, baixo (AR e ARSA) e alto risco (AREB, AREB-t e LMMC) e dentro de um mesmo subgrupo FAB os pacientes mostravam grandes variações na evolução da doença e na sobrevivência, especialmente dentro dos subgrupos AR e ARSA. A denominação anemia refratária nem sempre é adequada, sendo a anemia apenas uma de três possíveis citopenias em SMD; a expressão citopenia refratária foi sugerida por alguns autores (GARANDEAU et al., 2000). A LMMC apresenta em alguns casos características de síndrome mielodisplásica e em outros de
26 6 síndrome mieloproliferativa, desta forma sua inclusão na SMD vem sendo discutida nas classificações mais recentes, como a classificação da Organização Mundial da Saúde (OMS) (tabela 2) (HARRIS et al., 2000). Tabela 2: Classificação das Síndromes Mielodisplásicas segundo a proposta OMS em Subtipo Sangue periférico Medula óssea AR ARSA ARDM ARDM - SA anemia / ausência de blastos anemia ausência de blastos monócitos <1% citopenias sem ou raros blastos citopenias sem ou raros blastos AREB-1 blastos <5% pancitopenia AREB-2 blastos <5% Síndrome 5q- SMD não classificada pancitopenia anemia / blastos < 5% plaquetas normais ou aumentadas neutropenia e/ou plaquetopenia mas não anemia blastos <5% celularidade variável atipias discretas blastos <5% sideroblastos em anel >15% atipias discretas displasia em : 10% das células de 2 ou 3 linhagens blastos <5% sem bastonetes de Auer displasia em 2 ou 3 linhagens blastos <5% sem bastonetes de Auer sideroblastos em anel >15% blastos 5-9% hipercelular com atipias nas 3 séries blastos 10-19% hipercelular com atipias nas 3 séries micromegacariócitos blastos < 5% citogenética : del(5q) blastos <5% atipias discretas AR: Anemia Refratária; ARSA: Anemia Refratária com Sideroblastos em Anel; AREB: Anemia Refratária com Excesso de Blastos; ARDM: Anemia Refratária com Displasia Multilinhagem; ARDM-SA: Anemia Refratária com Displasia Multilinhagem com Sideroblastos em Anel; SMD: Síndrome Mielodisplásica (Harris et al, 2000).
27 7 A Organização Mundial da Saúde sugeriu novos critérios de classificação para SMD, sendo incorporado muitos conceitos e definições do sistema FAB. Esta classificação acrescentou dados para melhorar a definição dos subgrupos, assim como a sua relevância clínica. A maior diferença entre as duas classificações é o desaparecimento do subtipo AREBt, sendo considerada a transformação para LMA a partir de 20% de blastos na medula óssea (HARRIS et al., 2000). As citopenias refratárias, com ou sem sideroblastos, são divididas em AR e ARSA, quando a medula óssea apresenta somente uma displasia, e em citopenia refratária com displasia em multilinhagem (CRDM) e CRDM com sideroblastos em anel (CRDM-SA), quando a medula óssea apresenta várias displasias. Foram criados dois subtipos para AREB: AREB-1 (5 a 10% de blastos na medula óssea) e AREB-2 (11 a 20% de blastos na medula óssea). O subtipo LMMC foi retirado da categoria de SMD para um novo grupo de doenças mielodisplásicas /mieloproliferativas. Dados citogenéticos foram incorporados à classificação OMS, como a adição do subtipo síndrome do 5q-, como uma entidade separada. Esta síndrome é bem estabelecida entre os pacientes com SMD, estando associada com características clínicas específicas como anemia macrocítica, hiperplasia micromegacariocítica, menos de 5% de mieloblastos medulares com um diagnóstico de AR. A faixa etária alvo é constituída principalmente por pacientes acima dos 50 anos de idade e do sexo feminino (MHAWECH P & SALEEM, 2001). Apesar de ter como objetivos melhorar o valor prognóstico e clínico da classificação FAB, esta classificação levantou algumas críticas (HEAD, 2002; HELLSTRÖM-LINDBERG et al., 2000). As principais falhas apontadas foram a criação de categorias imprecisas e sem bases biológicas ou genéticas (citopenias refratárias com displasias de várias linhagens e SMD inclassificável) e a falta de precisão prognóstica. Estudos recentes comparando ambas
28 8 classificações sugerem que a classificação da OMS estabelece subgrupos mais homogêneos de pacientes e apresenta um grande valor prognóstico quando comparada com o sistema FAB, entretanto, controvérsias ainda permanecem (BENNETT, 2005). Vários estudos têm sido realizados com o objetivo de determinar quais os fatores que mais influenciam a sobrevivência e a freqüência de evolução para LMA nos pacientes com SMD, de modo a permitir a elaboração de escalas prognósticas. A porcentagem de blastos na medula óssea, as alterações citogenéticas e o número de citopenias são atualmente utilizados como os parâmetros mais importantes para as escalas prognósticas; outros fatores de menor importância incluem sexo, idade, contagem de plaquetas e de hemoglobina no sangue periférico e presença de ALIP (GREENBERG et al., 1997). A classificação de grupos de risco em SMD mais recente corresponde ao Sistema Internacional de Escala Prognóstica (IPSS) (GREENBERG et al., 1997). Após estudarem retrospectivamente os dados citogenéticos, morfológicos e clínicos de 816 pacientes, um número maior do que o número usado para a elaboração de qualquer outra classificação, foi concluído que a porcentagem de blastos na medula óssea, o número de citopenias no sangue periférico e a citogenética eram os fatores prognósticos de maior importância, tanto em relação ao tempo de sobrevivência, como quanto à taxa de transformação leucêmica. A maneira como a pontuação foi atribuída a cada parâmetro está descrita na tabela 3. O IPSS dividiu então a SMD em 4 grupos: baixo, intermediário 1, intermediário 2 e alto risco. A aplicação do IPSS tem gerado discussão em relação aos grupos separados por cariótipo. Em alguns estudos, a trissomia do cromossomo 8 e a del(11)(q23), por exemplo, estão freqüentemente associadas com a evolução da doença (FERNANDEZ et al., 2000; SOLÉ et al., 2000). Entretanto, o IPSS classifica estas alterações cromossômicas como prognóstico intermediário, sendo, portanto, necessária uma análise mais refinada em relação aos grupos de risco segundo o cariótipo.
29 9 TABELA 3: Pontuação segundo os Parâmetros Críticos do IPSS (1997) em Síndromes Mielodisplásicas Variáveis Prognósticas Pontuação 0 0,5 1 1,5 2,0 Blastos M.O. < 5% 5-10% % 21-30% Cariótipo * Bom Intermediário Mau Citopenias Pontuação para os grupos de risco: Baixo risco (0 pontos); Intermediário 1 (0,5-1,0 pontos); Intermediário 2 (1,5-2,0); Alto risco (> ou = 2,5). Cariótipos*: bom prognóstico: cariótipos normais, -Y, del(5q), del(20q), mau prognóstico: cariótipos complexos, anomalias envolvendo o cromossomo 7; prognóstico intermediário: outras anomalias cromossômicas (GREENBERG et al., 1997). Apesar de vários estudos na área de citogenética e de biologia molecular ainda não foi identificado o preciso mecanismo que leva ao aparecimento da SMD e quais são os eventos envolvidos na via de evolução da doença para leucemia aguda (DELFORGE, 2003; NISHINO E CHANG, 2005; PANANI & ROUSSOS, 2005). No entanto, todos os modelos sugeridos referem-se a um processo de múltiplas etapas (RASKIND et al, 1984; ROSENFELD & LIST, 2000; MUTFI, 2004; OGATA, 2006) Teoria de Múltiplas Etapas no Desenvolvimento da SMD Primária As investigações sobre a patofisiologia da SMD têm confirmado a heterogeneidade e a complexidade biológica desta doença. Avanços na tecnologia têm promovido observações que levam a sugerir hipóteses sobre o desenvolvimento da SMD. A hipótese mais aceita é que uma mutação inicial na célula tronco hematopoética pluripotente (a qual pode ser herdada ou adquirida), resulte na sua expansão limitada. Numa segunda etapa, uma dessas células adquire uma nova mutação, que leva a alterações na função celular e conseqüentemente evolução do clone pré-maligno. Este clone, o qual tem vantagens no crescimento, é associado com displasias, disfunção celular (como excesso de secreção local de citocinas inibitórias), alta
30 10 taxa de morte celular programada (apoptose), hematopoese ineficiente, defeitos de diferenciação e instabilidade genômica. Aquisições de novas mutações, como perda da função de genes supressores de tumor ou mutações em oncogenes, dentro de uma célula neste clone anormal levam a um aumento no número de células blásticas ocorrendo a evolução para leucemia (transformação leucêmica) (fig. 1) (AUL et al., 1998; ROSENFELD & LIST, 2000; MUFTI, 2004). Fig. 1: Modelo de Múltiplas Etapas no Desenvolvimento da SMD. Evento 1- mutação inicial na célula tronco hematopética. Evento 2- aquisições de novas mutações que levam à alterações na função celular. Evento 3- aparecimento de novas mutações levando à perda de função de genes supressores de tumor e mutações em oncogenes (AUL et al., 1998). Três linhas de evidências suportam este modelo e a existência de pré-disposição genética para SMD: (1) a ocorrência de LMA e SMD em famílias com um defeito de reparo no DNA herdado ou neurofibromatose tipo 1; (2) estudos de mapeamento genético em raras
31 11 famílias com histórico familiar de SMD e LMA; e (3) estudos da associação de vários polimorfismos genéticos em LMA e SMD (HELLSTRÖM-LINDBERG et al., 2000). Embora muitas alterações cromossômicas tenham sido detectadas em SMD, os genes envolvidos estão sendo ainda identificados, este desconhecimento leva ao questionamento se estas alterações genéticas são um evento inicial levando ao desenvolvimento da SMD ou se são eventos secundários contribuindo para a transformação leucêmica (LOOK, 2005) Alterações Cromossômicas em SMD Primária A concepção de SMD como uma doença de célula tronco hematopoética de natureza clonal, foi inicialmente demostrada por estudos envolvendo a inativação do cromossomo X (JANSSEN et al., 1989), assim como estudos isoenzimáticos da glicose 6 fosfato desidrogenase (G6PD) (RASKIND et al., 1984). A descoberta de alterações cromossômicas não randômicas em SMD primária confirmou esta clonalidade, oferecendo um meio de identificar o clone maligno e de apontar alguns oncogenes e genes supressores de tumor possivelmente envolvidos com o desenvolvimento e a evolução da doença. As alterações citogenéticas clonais podem ser detectadas em 30 50% dos pacientes adultos com SMD primária, no entanto, nenhuma alteração citogenética específica foi ainda definida para este grupo de pacientes (PANANI & ROUSSOS, 2005). Essas alterações variam de uma simples mudança estrutural ou numérica a complexas lesões genômicas envolvendo três ou mais cromossomos distintos. Aberrações citogenéticas simples ocorrem freqüentemente nos estágios iniciais da doença, entretanto, em estágios de transformação leucêmica e/ou durante a progressão da doença são comuns mudanças genômicas mais complexas (FERNANDEZ et al., 2000). As alterações cromossômicas mais freqüentes em SMD são a deleção do braço longo dos cromossomos 5 (del5q), 7 (del7q), 11 (del11q) e 20 (del20q), a monossomia do 7 (-7), a
32 12 deleção do braço curto dos cromossomos 17 (del 17p) e 12 (del 12p), a trissomia do cromossomo 8 (+8) e inversão do cromossomo 3 (inv 3). Translocações recíprocas são raras e incluem: t(1;7)(q10;p10), t(1;3)(p36;q21), t(3;3)(q21;q26); t(6;9)(p23;q34), t(5;12)(q33;p13), e t(5;7)(q33;p11.2) (DELFORGE, 2003; PANANI & ROUSSSOS, 2005, BORGONOVO et al., 2005). Anormalidades citogenéticas envolvendo o cromossomo 5 incluem a del(5q), -5 e as translocações não balanceadas. A deleção do braço longo do cromossomo 5 pode ser terminal, ou na maioria dos casos intersticial, com o ponto de quebra na região 5q13q33 ou 5q31q33. Neste caso, não se observa uma freqüência aumentada de evolução para leucemia, a menos que exista uma combinação com outros defeitos cromossômicos (PANANI & ROUSSOS, 2005). Monossomia do 7 é a alteração cromossômica de maior freqüência em SMD primária da infância. Esta alteração está associada com mau prognóstico, sendo a sobrevivência dos pacientes baixa devido a complicações causadas pelas citopenias, disfunção medular ou transformação para LMA (KARDOS et al., 2003). Deleção 7q é também freqüentemente encontrada em SMD, sendo geralmente acompanhada de outras alterações cromossômicas predizendo mau prognóstico (MHAWECH & SALEEM, 2001). A incidência do ganho do cromossomo 8 em SMD primária é de aproximadamente 10%, sendo observada em todos os subtipos FAB (PANANI & ROUSSOS, 2005). Anormalidades do braço longo do cromossomo 11 são comuns em malignidades mielóides, sendo observadas em 5% dos casos de SMD primária. Geralmente esta alteração está acompanhada de cariótipos complexos e tem um prognóstico não favorável (PANANI & ROUSSOS, 2005). A deleção do braço curto do cromossomo 17, del(17p), tem sido descrita em 4% dos pacientes com SMD, estando freqüentemente associada com alterações adicionais envolvendo
33 13 principalmente os cromossomos 5 e 7. Pacientes com esta alteração geralmente apresentam as seguintes características morfológicas: disgranulopoese com hipolobulação pseudo-pelger- Hüet, hipo-granulação e vacúolos observados em pequenos neutrófilos (VALLESPI et al., 1998). Clinicamente a doença é agressiva com resistência ao tratamento e curta sobrevida. O gene p53 localizado na região 17p13 é tipicamente perdido nestes casos e inativação do segundo alelo no cromossomo homólogo ocorre em aproximadamente 70% dos casos (LAI et al., 1995). Deleção do braço longo do cromossomo 20 como anomalia única ou em associação com outras alterações, ocorre com uma incidência de aproximadamente 5%. A deleção 20q é usualmente intersticial, afetando em geral a região 20q11 e 20q13 (PANANI & ROUSSOS, 2005). De acordo com o IPSS e um estudo recente, pacientes que apresentam esta alteração de forma isolada apresentam um prognóstico favorável (LIU et al., 2006), entretanto, alguns estudos demonstram que esta anomalia está associada com um pior prognóstico (CAMPBELL & GARSON, 1994). A incidência destas alterações citogenéticas pode refletir em uma instabilidade genômica clonal, levando a uma pré-disposição para aquisições adicionais de lesões genéticas. Estudos citogenéticos de acompanhamento da evolução de SMD para LMA puderam demonstrar que anomalias cromossômicas simples ocorrendo em subtipos de SMD são acrescidas de outras anomalias durante a progressão da doença (FERNANDEZ et al., 2000), estando envolvidas alterações em oncogenes e genes supressores de tumor (MORI et al., 2000; MHAWECH & SALEEM, 2001).
34 Oncogengenes e Genes Supressores de Tumor Envolvidos no Desenvolvimento da SMD Primária Múltiplas vias genéticas estão envolvidas na patogênese da SMD. Estudos têm demonstrado que a ativação de certos oncogenes, assim como a inativação de genes supressores de tumor exercem um papel importante no desenvolvimento desta doença. Alterações em oncogenes como N-ras (FERNANDEZ et al., 1998) e, genes supressores de tumor como NF1e p53 foram descritas em SMD (KIKUKAWA et al., 1999; SIDE et al., 1998). A função da proteína RAS é transduzir sinais a nível da membrana plasmática para o interior da célula, associados a divisão e diferenciação celular. As proteínas ras se ligam a nucleotídeos de guanina GDP e GTP com alta afinidade e possuem uma atividade GTPase intrínsica. Essas proteínas funcionam como switches moleculares que são ativas quando GTP é ligado a elas e inativas quando GDP está ligado. Mutação no proto-oncogene N-ras sinaliza de forma constitutiva sinais para a proliferação celular. Estudos demonstraram mutação pontual no oncogene N-ras em 10% a 40% das SMD, sendo esta alteração associada com diminuição na sobrevida e alta incidência de progressão leucêmica (NIIMI et al., 2006). Entretanto, alguns estudos sugerem que a mutação N-ras ocorre em estágios iniciais da SMD, uma vez que pacientes com cariótipos normais dos subtipos menos agressivos da doença AR e ARSA podem apresentar N-ras mutado (FERNANDEZ et al., 1998). Os achados de mutação N-ras em SMD ainda são controversos e têm sido sugerido que a mutação no oncogene N-ras pode ocorrer em estágios inicias ou avançados da doença podendo contribuir para a patogênese da SMD por estimular inicialmente a expansão clonal ou tardiamente a transformação leucêmica (NISHINO & CHANG, 2005).
35 15 Outro gene alterado descrito em pacientes com SMD é o fms. O gene fms codifica o receptor de superficíe celular CSF-1 ou CSF de macrófagos, sendo sua atividade dependente da ligação à tirosina quinase. CSF-1 quando ativo promove a proliferação e diferenciação de células hematopoéticas da série monócito-macrófago. Mutações no gene c-fms resulta em uma proteína com mudanças conformacionais, levando à ativação constitutiva do receptor. Mapeado na região q33 do cromossomo 5, o gene fms tem sido implicado na patogênese de doenças hematológicas da linhagem mielóide. Uma mutação pontual no codon 969 tem sido reportada com aumentada incidência em subtipos mais avançados de SMD (NISHINO & CHANG, 2005). O gene MLL, mapeado na região q23 do cromossomo 11, age como fator de transcrição envolvido na diferenciação celular e foi descrito como associado com a transformação para LMA em pacientes com SMD (IBRAHIM et al., 2000). Os produtos dos genes descritos participam como fatores fundamentais nos programas de proliferação e diferenciação celular. Já as proteínas derivadas dos proto-oncogenes bcl-2, c-myc e do gene supressor de tumor p53 têm sido descritas como elementos regulatórios chave da via apoptótica. Bcl-2 representa uma classe de reguladores negativos da apoptose. Realiza sua função através da dimerização com membros de sua família e com outros reguladores, como p53 e RAS. Aumento da expressão de bcl-2 tem sido correlacionado com a progressão da SMD, sendo observada uma super expressão dessa proteína em subtipos de maior risco (AREB e AREB-t) (BOUDARD, 2002). Além destes oncogenes diversos genes supressores de tumor parecem ter papéis de destaque no estabelecimento e evolução de neoplasias, como o p53. O gene p53 se localiza no braço curto do cromossomo 17 na posição 17p13, em humanos e o seu produto é uma fosfoproteína nuclear. A proteína p53 atua como um "guarda molecular" monitorando a integridade do genoma, tendo um papel de pivô na mediação da resposta celular ao dano do
36 16 DNA, induzindo a parada de crescimento em G1 e a apoptose (CHANG et al., 1993; PERRY & LEVINE, 1993). Mutação no gene p53 têm sido correlacionada com estágios mais avançados da doença, sugerindo que seja um evento relacionado ao processo de transformação leucemica (ADAMSON et al., 1995; KIKUKAWA et al., 1999). Recentemente alterações epigenéticas, como metilação aberrante da ilha CpG na região promotora de genes envolvidos no controle do ciclo celular, têm sido descritas inativando genes supressores de tumor e contribuindo para o desenvolvimento de neoplasias (GALM et al., 2006) Alterações Epigenéticas em SMD Primária: Metilação dos Membros da Família InK4 p15 e p16 O termo epigenética refere-se a modificações covalentes reversíveis e herdadas da molécula de DNA, sem que haja alteração na seqüência de bases (GALM et al., 2006). O principal mecanismo epigenético conhecido é o controle da atividade transcricional através da alteração da estrutura da cromatina, sinalizada pela metilação do DNA (WEINHOLD, 2006). Essa modificação endógena desempenha um papel essencial no silenciamento transcricional em muitos processos, tais como a inativação do cromossomo X, a impressão parental, o controle da expressão gênica tecido-específica e a manutenção da integridade cromossômica, agindo também na defesa do genoma contra elementos genéticos móveis (LAIRD & JAENISCH, 1996). A metilação do DNA é um processo epigenético natural que constitui a modificação endógena mais comum no genoma de mamíferos, sendo essencial para o desenvolvimento do organismo (GALM et al, 2006). A metilação ocorre somente nas bases citosina que estão localizadas próximas das bases guanina de um dinucleotídeo simétrico, CpG (fig. 2A).
37 17 Citosinas metiladas representam 0,75-1% do total de bases do DNA (WORM & GULDBERG, 2002). O padrão de metilação da célula é precisamente reproduzido após a síntese do DNA e estavelmente transmitido para as células filhas. A adição de um grupamento metila (CH 3 ) na posição 5 da citosina é um evento catalisado por um grupo de enzimas chamadas DNA metiltransferases (DNMT). A S-adenosil-metionina (SAM) serve como doadora de radicais metila nas reações de transmetilação (fig. 2B). A transmetilação é inibida, através de competição, pela S-adenosil-homocisteína (WORM & GULDBERG, 2002). Fig. 2: Região de metilação na seqüência do DNA e adição do grupamento metila pelas enzimas DNMT. (A) O genoma humano apresenta grupos metil, os quais ocorrem exclusivamente em resíduos de citosina dentro de um dinucleotídeo simétrico CpG. (B) A adição do grupo metil a citosina é catalizada pela DNA metiltransferase (DNMT), usando a S-adenosil-L-metionina (SAM) como um substrato (WORM & GULDBERG, 2002). As ilhas CpGs são encontradas em pequenas regiões de 1-2 Kb, representando, aproximadamente, 2% do genoma, e possuem propriedades distintas quando comparadas com
38 18 o restante do DNA genômico. Com relação a sua distribuição, as ilhas CpGs são comumente encontradas dentro ou próximas a promotores de genes de manutenção (RAKYAN et al, 2001). Aproximadamente 70% dos dinucleotídeos CpGs estão metilados, no entanto, muitas ilhas CpGs apresentam-se livres de metilação, estando associadas com a atividade transcricional do gene. Genes que são ativamente transcritos tendem a ter baixos níveis de metilação das suas regiões promotoras, enquanto que genes silenciosos, isto é, que não se expressam em determinados tecidos ou circunstâncias, têm sua região promotora altamente metilada (fig. 3) (WORM & GULDBERG, 2002). Fig. 3: Atividade transcricional do gene de acordo com o padrão de metilação. Citosinas não metiladas são amplamente encontradas em ilhas CpGs, as quais usualmente mapeiam no promotor e nas regiões do primeiro exon de genes housekeeping. (A) O estado completamente desmetilado de uma ilha CpG na região promotora esta relacionado com a atividade transcricional, entretanto (B) metilação completa causa o silenciamento transcricional (WORM & GULDBERG, 2002). A metilação do DNA promove mudanças na estrutura da cromatina, modificando as interações entre o DNA e os fatores de transcrição. Tais mudanças podem, reversível ou irreversivelmente, regular as funções do genoma atuando na repressão transcricional e na organização da cromatina. Estudos iniciais sobre o efeito inibitório da metilação sugeriram uma interferência direta dos grupamentos metila na ligação de fatores de transcrição a seus sítios de reconhecimento na cromatina. Sendo assim, os fatores de transcrição que se associam a
39 19 seqüências que contêm dinucleotídeos CpG não conseguem se ligar a essas seqüências quando os resíduos CpG estão metilados. No entanto, modelos alternativos referem-se a mudanças na arquitetura do nucleossomo como um elemento de repressão. Este modelo foi reforçado pela identificação de uma família de proteínas que preferencialmente ligam-se a CpGs metilados (MBPs - proteínas ligadoras de CpG metilados) (WADE, 2001). Algumas destas proteínas têm sido diretamente implicadas no silenciamento de genes dependentes de metilação, por recr9utar histonas desacetilases (HDACs) para o local da metilação. HDACs catalizam a remoção dos grupos acetil dos nucleossomos, convertendo a estrutura da cromatina aberta para transcrição para uma estrutura fechada, a qual torna-se inacessível à maquinaria transcricional basal (fig. 4) (WORM & GULDBERG, 2002; GALM et al.,2006). Fig. 4: Modelo para o silenciamento transcricional dependente de metilação. Citosinas metiladas são reconhecidas por proteínas ligadoras de metil CpG (MBPs), as quais recrutam histonas desacetilases (HDACs) para o local da metilação, convertendo a cromatina em uma estrutura fechada que se torna inacessível à maquinária de transcrição (WORM & GULDBERG, 2002).
40 20 A metilação do DNA foi observada pela primeira vez em câncer humano em 1983 (FREINBERG & VOLGELSTEIN, 1983). No câncer, a hipermetilação de regiões promotoras de genes supressores de tumor é uma importante alteração epigenética que está despertando um grande interesse para o de desenvolvimento de novas terapias. Estudos em malignidades hematológicas têm mostrado uma forte relação entre metilação e fenótipo neoplásico, estando envolvidos principalmente os membros da família INK 4, p15 e p16, que desempenham um importante papel no controle do ciclo celular (LEHMANN et al., 2004). Os genes p15 INK4B e p16 INK4A estão localizados na região p21 do cromossomo 9. As proteínas codificadas por esses genes induzem a parada do ciclo celular na fase G1-S através da inibição da atividade do complexo ciclina D e CDK4 e CDK6. A transição da fase G1 para S, representa um ponto extremamente importante no relógio do ciclo celular. A metilação em regiões promotoras dos genes p15 INK4B e p16 INK4A induz a repressão transcricional desses dois genes, contribuindo para a passagem direta da célula para a fase S (COTRAN et al., 2000). Dessa forma, a inibição da expressão deses genes está associada com alta taxa de proliferação celular (LEES, 1995). Em neoplasias hematológicas, através de estudos cromossômicos, têm sido verificado que os genes p15 INK4B e p16 INK4A estão freqüentemente deletados em leucemia linfóide aguda em crianças e adultos (STREFFORD et al., 2007). No entanto, em SMD estes dois genes são raramente mutados ou deletados (NAKAMAKI et al., 1997). Estudos mostraram que p15 INK4B atua como um importante regulador da proliferação e diferenciação das linhagens mielóides, monocítica e megacariocítica, inibindo esses processos (TEOFILI et al., 2001). Posteriormente, foi demonstrado através do emprego de técnicas de biologia molecular (MSP- PCR) que o silenciamento transcricional dos genes p15 INK4B e p16 INK4A via metilação aberrante é um evento crítico na leucemogênese, e a metilação no gene p15 INK4B têm sido
41 21 freqüentemente associada a leucemias agudas, tanto linfóide quanto mielóide, em crianças e adultos (HERMAN et al., 1996, AU et al., 2003; GARCIA-MANERO et al., 2002). No sentido de verificar o papel desses dois genes no processo de desenvolvimento e evolução da SMD para LMA foram realizados alguns estudos correlacionando alterações nos genes com os subtipos da doença segundo a classificação FAB. Alguns grupos demonstraram que a metilação aberrante de p15 INK4B ocorre com maior incidência nos casos de expansão blástica como AREB, AREB-t e LMA resultante de transformação de SMD e mais raramente nos subtipos iniciais da doença (UCHIDA et al., 1997; QUESNEL et al., 1998). No entanto, outros estudos mostraram que alterações nos padrões de metilação em p15 INK4B podem ocorrer em todos os subtipos da doença (TIEN et al., 2001; AGGERHOLM et al., 2006; HOFMANN et al., 2006). Dessa forma, não é claro se esta alteração epigenética ocorre em fases iniciais do diagnóstico ou se é um evento associado à transformação leucêmica e qual o seu impacto prognóstico. A maioria desses trabalhos foi realizada em pacientes adultos com SMD primária, existindo poucos estudos de investigação da incidência e do papel da metilação dos genes p15 INK4B e p16 INK4A no prognóstico em SMD primária na infância SMD Primária na Infância A SMD primária na infância representa cerca de 4% de todas as malignidades hematológicas da faixa pediátrica (HASLE et al., 2003). Em alguns casos, ela pode estar presente em crianças com doenças genéticas como a Síndrome de Down ou a Anemia de Fanconi. Nestes casos existe uma predisposição genética para o desenvolvimento da SMD. Em outros casos ela apenas se manifesta idiopaticamente. Crianças que apresentam essa doença hematológica estão associadas a um pior prognóstico quando comparadas com os adultos. No Brasil, de acordo com o Grupo Cooperativo Brasileiro em SMD Pediátrica (GCB-
42 22 MDS-PED), a taxa de sobrevida total para pacientes com SMD na infância que não foram tratados com transplante de medula óssea é de 20-25% (VALERA et al., 2004). Embora a SMD na infância seja considerada uma doença com características displásicas e hematopoese ineficaz, como a SMD do adulto, as características clínicas, a presença de anormalidades associadas e a caracterização das alterações cromossômicas têm indicado que a SMD durante a infância represente uma diferente questão biológica (POLYCHRONOPOULOU et al., 2004). As principais diferenças entre a SMD na infância e no adulto são: incidência extremamente rara de ARSA na infância ao passo que em adultos consiste em cerca de 25% dos casos; a monossomia do 7 é a alteração cromossômica mais freqüente na infância e nos adultos é a deleção do braço longo do cromossomo 5; as possibilidades terapêuticas em adultos com SMD são limitadas devido à idade avançada, sendo indicada geralmente uma terapia paliativa, enquanto que nas crianças com SMD a principal terapia é a curativa, através do transplante de medula óssea (HASLE & NIEMEYER, 2002). Na tabela 4 podemos observar as principais diferenças entre a SMD em crianças e em adultos. Tabela 4: Diferenças entre SMD em Crianças e em Adultos Parâmetros Crianças Adultos Incidência/milhão 3.6 >35 ARSA <2% 25% Alterações Citogenéticas 60% 40% -7/7q- 30% 10% -5/5q- 1-2% 20% Anormalidades clínicas associadas 30% <5% Objetivo principal do tratamento Curativo Paliativo (HASLE & NIEMEYER, 2002) A SMD na infância pode apresentar características específicas que dificultam a sua inclusão nos sistemas de classificação tradicionais, tendo sido propostos subgrupos específicos da SMD para a infância. Por exemplo, pacientes de menos de 4 anos que apresentavam monossomia do cromossomo 7 foram inicialmente classificados em uma
43 23 síndrome distinta, a síndrome de monossomia do 7 (GYGER et al., 1982; HUTTER et al., 1984; PASSMORE et al., 1995). Esta estava tipicamente associada a uma doença mieloproliferativa crônica rara na infância, com mau prognóstico (EVANS et al., 1988). No entanto, outros estudos mostraram que pacientes com monossomia do 7 podiam por vezes ser classificados nos outros subgrupos FAB, descartando conseqüentemente a síndrome de monossomia do 7 (BRANDWEIN et al., 1990; HASLE et al., 1999). Para diferenciar os pacientes que apresentavam SMD com características mieloproliferativas, foi adotado um novo subgrupo, a leucemia mielomonocítica juvenil (LMMJ). A LMMJ diferencia-se da LMMC do tipo adulto, tanto biologicamente (a contagem de leucócitos é mais alta, sendo superior a 13000/µL e a faixa etária atingida é de menos de 4 anos de idade, ao contrário do que acontece geralmente na LMMC) como citogeneticamente (as translocações encontradas em LMMC, como t(5;12), ainda não foram descritas em LMMJ) (NIEMEYER et al., 1997; SIDE et al, 1998; LUNA-FINEMAN et al, 1999). A LMMJ, assim como a LMMC do tipo adulto, é diferenciada citogeneticamente das doenças mieloproliferativas pela ausência do cromossomo Philadelphia (Ph). O prognóstico dos pacientes com LMMJ é significativamente pior do que de LMMC (EMANUEL, 1999; ARICO et al., 1997). A SMD infantil tem sido portanto classificada em SMD do tipo adulto, à qual se aplica a classificação FAB, acrescentando a LMMJ (SASAKI et al., 2001). Entretanto, a utilização dos sistemas de classificação tradicionais FAB (BENNETT et al., 1982) e OMS (HARRIS et al., 2000) baseados em SMD do adulto, têm sido tema de muita discussão em SMD na infância. Hasle et al. em 2003 sugeriram novos critérios para classificação da SMD da infância, sendo os critérios mínimos: citopenias sem uma causa esclarecida (anemia, neutropenia e trombocitopenia); pelo menos duas linhagens apresentando displasias, alteração citogenética clonal adquirida e número de blastos igual ou maior que 5% na medula óssea. Nesta classificação da SMD na infância são reconhecidos três grupos: o
44 24 grupo das doenças mieloproliferativas e mielodisplásicas (LMMJ), o qual apresenta características mieloproliferativa e mielodisplásica; o grupo da síndrome de Down associada com a SMD, uma vez que esses pacientes apresentam características clínicas e prognósticas distintas; e o grupo da SMD primária propriamente dita, o qual foi subdividido em: citopenia refratária (CR), anemia refratária com excesso de blastos (AREB) e anemia refratária com excesso de blastos em transformação (AREB-t) (fig. 5). Doenças Mieloproliferativas/ Síndrome Mielodisplásica Mielodisplásicas LMMJ Síndrome de Down Células Blásticas(%) S.P. M.O. CR 2% 5% AREB <2 19% 5 19% AREB-t >20-29% 20 29% Fig. 5: Classificação da Síndrome Mielodisplásica na Infância. LMMJ- leucemia mielomonocítica juvenil; CR - Citopenia Refratária; AREB - Anemia Refratária com excesso de blastos; AREB-t - Anemia Refratária com excesso de blastos em transformação; SMD- síndrome mielodisplásica; LMAleucemia mielóide aguda SP- sangue periférico; MO- medula óssea (modificado de HASLE et al., 2003). A LMMJ ocorre principalmente em meninos com menos de 2 anos de idade, que apresentam hepatoesplenomegalia, febre, infecção, sangramento, alta contagem leucocitária com monocitose absoluta, anemia, trombocitopenia e hemoglobina fetal aumentada. Pacientes que apresentam neurofibromatose do tipo 1 (NF1) possuem risco aumentado de desenvolverem LMMJ. Citogeneticamente a LMMJ é caracterizada em 25-30% dos casos
45 25 pela monossomia do cromossomo 7, 10% apresentam outras alterações cromossômicas e em cerca de 60% dos casos os cariótipos são normais. Em nível molecular é freqüentemente caracterizada por mutações em NF1 e N-ras, apresentando a via de sinalização para proliferação celular ativada de forma permanente (EMANUEL, 1999). As crianças com LMMJ apresentam mau prognóstico e resistência à quimioterapia convencional (WOODS et al., 2002), sendo o transplante de células tronco alogenêico o único tratamento curativo. Com este tratamento, aproximadamente 30% dos pacientes alcançam a cura, entretanto, a taxa de recaída é alta (em torno de 40-50% dos casos) (YUSUF et al., 2004). A Síndrome de Down (SD) é a condição de predisposição genética mais freqüente observada em crianças com o diagnóstico de SMD, estando presente em 25% dos casos diagnosticados com AR, AREB ou AREB-t. A LMMJ ocorre com uma menor freqüência. A alteração cromossômica clonal mais comum em crianças com SMD associada com a SD é a trissomia do cromossomo 8 e o ganho de um cromossomo 21, dessa forma a criança apresenta uma tetrassomia (sendo um cromossomo 21 constitucional associado com a SD e o outro adquirido associado com a SMD). Estudos moleculares relataram a presença de mutações no gene GATA-1 associado com o desenvolvimento de LMA em pacientes portadores de SD (MUNDSCHAU et al, 2003). No entanto, até o momento não existem relatos de alterações moleculares relacionadas com SMD em crianças com SD. Em relação ao prognóstico, crianças com SD e SMD apresentam prognóstico bom ou intermediário, evoluindo freqüentemente para LMA-M7. Essas crianças são tratadas com protocolos de LMA, tendo uma boa evolução clínica com baixo risco de recaída. O transplante de células tronco alogenêico está associado com excesso de toxicidade sem ganho terapêutico (BEVERLY et al, 1998).
46 26 Como podemos notar, essa classificação exclui o subgrupo anemia refratária com sideroblastos em anel (ARSA) devido a sua freqüência ser muito baixa na infância, aproximadamente 2% dos casos (CHAN et al., 1997; HASLE et al., 2003). Em relação à distribuição de casos segundo os subtipos, AR tem sido apontada por alguns estudos como relativamente comum, acometendo em torno de 40-60% dos pacientes (POLYCHRONOPOULOU et al., 2004), enquanto os subtipos AREB e AREB-t aparecem em cerca de 15-20% da SMD na infância (WEBB et al., 2001; PASSMORE et al., 2003). No entanto, outros estudos mostraram que a maior freqüência de casos de SMD na infância ocorre nos subtipos mais avançados da doença (AREB e AREB-t) (VIDAL et al., 2006). Grandes diferenças vêm sendo demonstradas entre crianças e adultos com SMD. As características clínicas são diferentes e os fatores que predizem a sobrevida ou a progressão em adultos são de pouco valor para crianças. Hasle et al. em 2004, avaliando o sistema de escala prognóstica, o IPSS, em um grupo de 308 crianças com SMD primária e LMMJ, verificaram que esta escala apresenta valor limitado, tanto para SMD pediátrica quanto para LMMJ. Crianças com SMD freqüentemente apresentam citopenias em duas ou três linhagens, sendo poucas crianças classificadas como de baixo risco, segundo esse sistema. Estudos sobre as características morfológicas do sangue periférico e medula óssea demonstraram presença de displasias nas linhagens eritróide, mielóide e megacariocítica. Tem sido descrita a presença de medula óssea hiper e normocelular em SMD na infância (POLYCHRONOPOULOU et al., 2004). Estudos de biópsia de medula óssea revelaram a presença de hipocelularidade nos pacientes do subtipo AR em cerca de 60% dos casos, sendo que este achado é atribuído ao fato de que a avaliação da celularidade da medula óssea em crianças não é adequadamente descrita (POLYCHRONOPOULOU et al., 2004). Ainda não existem estudos relatando se a hipocelularidade da medula óssea está relacionada com um prognóstico diferencial em comparação com a medula normocelular ou hipercelular.
47 27 Em relação aos estudos citogenéticos, estes mostraram um papel fundamental no diagnóstico de todos os casos de suspeita de SMD pediátrica, sendo utilizados para a confirmação da natureza clonal desta doença (SASAKI et al., 2001; PASSMORE et al., 2003). Alterações citogenéticas podem ser detectadas em % dos pacientes com SMD primária da infância (WEBB et al., 2001; KARDOS et al, 2003; YSUSUF et al., 2004). A monossomia do 7 é a anormalidade cromossômica mais freqüente nestes pacientes, sendo encontrada em aproximadamente 19 a 23% dos casos. Esta alteração está associada com mau prognóstico e uma rápida progressão para LMA (SASAKI et al., 2001; PASSMORE et al., 2003; AKTAS & TUNCBILEK, 2006). O transplante de células tronco hematopoéticas alogenêico, na fase inicial da doença, tem sido apontado como a terapia mais indicada para essas crianças (YSUSUF et al., 2004). Outras alterações descritas em SMD primária na infância foram: del(5q), +8, del(17p), del (11q) e hiperdiploidia (FERNANDEZ et al., 2003; PITMAN et al., 2006; KARDOS et al., 2003). Os mecanismos moleculares envolvidos em SMD na infância ainda não estão bem definidos. Um recente estudo com os genes p53 e fms demonstrou a inexistência de mutação nas seqüências analisadas, sugerindo que os mecanismos moleculares de evolução da SMD em crianças são diferentes daqueles observados em adultos (JEKIC et al, 2006). A presença de mutações no onocogene N-ras e K-ras ocorre em uma freqüência muito baixa em SMD da infância. Em um estudo de 35 pacientes, apenas três mostraram a presença de mutação em N-ras, estando esse grupo associado com cariótipos normais (JEKIC et al., 2004). A metilação aberrante do DNA é freqüentemente observada em adultos com SMD e tem sido reconhecida como uma importante alteração epigenética em sua patogênese. Hasegawa et al. em 2005 realizaram o primeiro estudo mostrando a presença de metilação envolvendo os genes p15 INK4B e p16 INK4A em crianças com SMD. Neste estudo foi verificado que a freqüência de metilação em p15 INK4B foi alta estando presente em 78% dos casos, entretanto, foi um
48 28 achado raro em LMMJ. Não foi detectada neste estudo presença de metilação em p16 INK4A (HASEGAWA et al., 2005). O estudo de metilação do DNA é importante uma vez que um dos tratamentos mais recentes para SMD utiliza inibidores da metilação do DNA como decitabina e azacitidina que têm promovido resposta citogenética para os pacientes de alto risco. Entretanto, não é conhecida nenhuma correlação entre uma alteração epigenética envolvendo um gene específico e a resposta a um agente inibidor de metilação (ATALLAH et al., 2007). Devido à raridade da SMD na infância, estudos sobre a sua patogênese não têm sido adequados e a via que leva a uma hematopoese anormal e a associação com alterações genéticas e epigenéticas precisam ser estudadas, existindo poucos dados na literatura que correlacionem estas alterações com o diagnóstico, prognóstico e evolução da doença. Dessa forma, torna-se fundamental a caracterização de marcadores citogenéticos e moleculares que auxiliem o diagnóstico e a definição de fatores prognósticos em SMD primária na infância, principalmente em relação a definição de grupos de risco de acordo com a presença de uma alteração cromossômica específica ou uma alteração molecular, sendo importante esse esclarecimento para auxiliar na escolha de protocolos de tratamento.
49 29 2. OBJETIVOS A síndrome mielodisplásica primária é um grupo de doenças altamente heterogêneo do ponto de vista clínico, morfológico e biológico, tanto em pacientes adultos quanto em crianças. No sentido de definir os fatores prognósticos em SMD primária na infância relacionados com o desenvolvimento desta doença e com a evolução para leucemia mielóide aguda, o presente trabalho apresentou como objetivos: 1) Realizar uma análise citogenética retrospectiva e prospectiva em pacientes portadores de SMD primária na infância e acompanhar citogeneticamente e clinicamente estes pacientes para observar as principais anomalias numéricas e estruturais envolvidas no processo de transformação leucêmica; 2) Caracterizar o padrão cromossômico de pacientes com SMD primária na infância; 3) Aplicar a técnica de FISH para confirmar as alterações cromossômicas nos seguintes casos: quando os cromossomos apresentassem baixa resolução pela técnica de bandeamento G, quando o número de metáfases analisadas para caracterizar um clone fosse pequeno e para o monitoramento do tratamento quando a preparação citogenética fosse sem mitose; 4) Analisar o padrão de metilação na região promotora do gene p15 INK4B em células de medula óssea de pacientes com SMD primária na infância e comparar com o padrão obtido em doadores para o TMO; 5) Analisar o padrão de metilação na região promotora do gene p16 INK4A em células de medula óssea de pacientes com SMD primária na infância e comparar com o padrão obtido em doadores para o TMO; 6) Correlacionar o padrão de metilação dos genes p15 INK4B e p16 INK4A com os subtipos da classificação de SMD primária na infância;
50 7) Correlacionar o padrão de metilação na região promotora dos genes p15 INK4B e p16 INK4A com o cariótipo dos pacientes, na tentativa de sugerir vias de evolução da SMD para LMA; 30
51 31 3. MATERIAIS E MÉTODOS 3.1 Pacientes Foram estudadas retrospectivamente e prospectivamente no período de 1991 a 2006, 64 amostras de medula óssea de pacientes com síndrome mielodisplásica primária na infância provenientes das seguintes Instituições: Centro de Transplante de Medula Óssea (CEMO- INCA), Serviço de Hematologia (INCA), Instituto Estadual de Hematologia Arthur Siqueira Cavalcanti (HEMORIO), Hospital Universitário Pedro Ernesto (HUPE-UERJ) e Instituto de Puericultura e Pediatria Martagão Gesteira (IPPMG -UFRJ). A idade dos pacientes variou de 5 meses a 18 anos, sendo 40 do sexo masculino e 24 do sexo feminino. Os estudos hematológicos e clínicos foram realizados pelos próprios hematologistas nas instituições de origem, como parte da investigação de rotina e os diagnósticos seguiram os critérios propostos pela classificação de SMD primária da infância segundo HASLE et al (2003). Foram excluídos deste estudo os pacientes acima de 18 anos de idade e portadores de SMD secundária. Para as análises moleculares foram utilizados como grupo controle células de medula óssea de doadores provenientes do CEMO-INCA. Este projeto foi aprovado pelo Comitê de Ética em Pesquisa do Instituto Nacional de Câncer (Anexo 1). Todos os procedimentos realizados seguiram as normas de bioética segundo a resolução 196/96 do Conselho Nacional de Saúde. 3.2 Análise Citogenética Cultura de Células de Medula Óssea Para este procedimento, utilizamos a técnica de TESTA et al(1985) com algumas modificações. As células da medula óssea foram lavadas com meio RPMI 1640 (Sigma), em seguida, foi feita uma diluição de 1:20 da suspensão celular em líquido de Thomas (1mL de ácido acético glacial, uma gota de violeta genciana, 100mL de água destilada) e as células
52 32 foram contadas na câmara de Newbauer em microscópio ótico Olympus (contraste de fase). Foram incubadas de 5 x 10 6 a 10 x 10 6 células/ml em 80% de RPMI e 20% de soro fetal bovino GIBCO, a 37 o C, numa atmosfera de 5% de CO 2, por 24 horas. Duas horas antes do término da cultura, foram adicionados 0.05µg/mL de colchicina e a cultura foi incubada novamente por mais 1 hora nas mesmas condições Término das Culturas e Preparação das Lâminas Neste procedimento o método utilizado foi o de HUNGERFORD (1965) com modificações. Ao final da incubação, o material foi centrifugado a 1500 rpm (centrifuga EPPENDORF- modelo 5804) por 6 minutos. O sobrenadante foi desprezado e o precipitado ressuspenso em 5mL de uma solução hipotônica (KCl 0,075M). O material foi incubado a 37 o C por 15 minutos, sendo em seguida centrifugado a 1500 rpm (centrifuga EPPENDORFmodelo 5804) por 6 minutos. O precipitado foi fixado com Solução Carnoy 3:1 (metanol : ácido acético), sendo na primeira fixação adicionado lentamente um volume de 5mL. Após 20 minutos à temperatura ambiente, o material foi centrifugado a 1500 rpm (centrifuga EPPENDORF- modelo 5804) durante 6 minutos e o sobrenadante desprezado. O procedimento foi repetido mais 2 vezes e o precipitado da última fixação foi ressuspenso em um pequeno volume de fixador, que variou de acordo com a quantidade de material. As lâminas foram preparadas pingando-se uma gota de suspensão celular em uma lâmina limpa e umedecida e o material foi fixado sobre a lâmina na chama. A primeira lâmina obtida foi corada com corante Giemsa 2% em tampão fosfato (0,102M de NaH 2 PO 4 ; 0,098M de Na 2 HPO 4, ph 6,8) e observada no microscópio ótico para verificar o índice mitótico e a qualidade das metáfases. As demais lâminas foram envelhecidas de 1 dia a 1 semana à temperatura ambiente para o bandeamento G.
53 Bandeamento G Para obtenção de padrões de bandeamento G foi utilizada a técnica de SEABRIGHT (1971), com o seguinte procedimento: as lâminas foram incubadas em uma solução de tripsina 0.1% em solução Dulbeco (0,137M NaCl; 0,0027M KCl; 0,0015M KH 2 PO 4 ; 0,011M NaH 2 PO 4 ; ph 7.8), em tempos que variaram de 1 segundo a 1 minuto. Em seguida, as lâminas foram lavadas com solução de soro fisiológico (NaCl 9%) e coradas em uma solução de Giemsa (Merck) a 2% em tampão fosfato durante 15 minutos Análise Cromossômica Os cromossomos foram identificados e classificados de acordo com o Sistema Internacional de Nomenclatura de Citogenética Humana de 1995 (ISCN, 1995). A análise cromossômica foi realizada em microscopia ótica utilizando no mínimo 20 metáfases por paciente. Um caso foi considerado anormal quando três ou mais células apresentaram a mesma anomalia cromossômica estrutural e/ou numérica. Foram adquiridas através do Sistema de Cariotipagem Cytovision Applied Image de 5 a 10 metáfases para a montagem dos cariótipos de cada paciente. 3.3 Citogenética Molecular: Análise por Hibridização in situ por Fluorescência (FISH) Para a técnica de FISH foi utilizado o material da preparação citogenética (metáfases e núcleos interfásicos em fixador). Foram utilizadas as sondas para a investigação das regiões q33-q34 do cromossomo 5 (LSI CSF1R SO/ LSID5S23:D5S721 SG) e da região q31 do cromossomo 7 (LSI D7S486 spectrum orange/cep 7 spectrum green), do gene MLL mapeado no cromossomo 11 na região q23 (LSI MLL dual color break apart rearrangement probe) e do gene p53 mapeado no cromossomo 17 na região p13 ( LSI p53, spectrum orange). Todas as sondas utilizadas foram da Vysis, Abbott Laboratories, USA.
54 34 As lâminas foram preparadas em lençol d água e envelhecidas durante 24 horas. Após este período, as lâminas foram colocadas em uma solução 2x SSC (a partir de diluição de uma solução 20x SSC: 3,0M NaCl e 0,3M Citrato de Sódio, ph 7,0) a 37º C por 30 minutos; desidratadas em série com etanol 70%, 80% e 95% à temperatura ambiente por 2 minutos. Em seguida, o material foi desnaturado em uma solução de 70% formamida / 2x SSC, a 73 o C por 5 minutos. Foi dimensionado 10µl de sonda previamente desnaturada a uma temperatura de 73ºC por 5 minutos, em uma área de 25mm x 25mm e aplicada lamínula de vidro. As lâminas foram seladas com cola de isopor e incubadas por 16 horas em câmara úmida a 37ºC. Após o período de hibridização, as lâminas foram transferidas para solução de 0,4x SSC e 0,3% IGEPAL (SIGMA) a 73 o C durante 2 minutos. Os cromossomos e os núcleos interfásicos foram corados em uma solução de DAPI/Antiphade (125ng/mL) e a área foi coberta com uma lamínula de vidro e selada com esmalte incolor. A análise foi realizada em microscópio de fluorescência (OLYMPUS BX51) com filtros apropriados e o resultado obtido foi adquirido pelo Sistema de FISH da Cytovision Applied Image. 3.4 Análise Molecular Cultura de Células da linhagem DLD-1 e Raji Para a análise da presença de metilação na região promotora dos genes p15 INK4B e p16 INK4A em células da medula óssea dos pacientes com SMD primária na infância foram utilizados como controles negativos, DNA de células de medula óssea de doadores para o TMO e como controles positivos DNA de células das linhagens Raji (derivada de Linfoma de Burkitt), que apresenta metilação para o gene p15 INK4B (HERMAN et al., 1996) e DLD-1 (derivada de adenocarcinoma de coloretal), que apresenta metilação para o gene p16 INK4A (comunicação pessoal com o grupo de pesquisa do Dr. André Vettore e Dra. Andréa Seixas do Instituto Ludwig). As células em cultura das linhagens DLD-1 e Raji foram cedidas
55 35 gentilmente pelo Instituto Ludwig - São Paulo e pelo Laboratório de Imunologia do CEMO- INCA, respectivamente. As células da linhagem DLD-1 foram cultivadas em 90% de meio de cultura RPMI 1640 (Sigma) e 10% de soro fetal bovino (HYCLONE) em garrafas de cultura (50mL) a 37 o C, numa atmosfera de 5% de CO 2. As culturas foram observadas diariamente em microscópio invertido (Leitz). Após dois dias de cultura, quando as células encontravam-se em uma monocamada homogênea, foi adicionanda uma solução de 0,25% de tripsina e 0,53mM de EDTA à temperatura ambiente para o repique das células (em uma razão de 1:3 células) e estas foram novamente incubadas nas mesmas condições, para amplificação celular e posterior extração de DNA. As células da linhagem Raji foram cultivadas nas mesmas condições da linhagem DLD-1, no entanto, devido este tipo celular crescer em suspensão, não foi adicionada solução de tripsina antes de realizar o repique. Para o repique, as células foram centrifugadas a 1500 rpm (centrifuga EPPENDORF- modelo 5804) por 5 minutos, em seguida foi feita uma diluição de 1:20 da suspensão celular em líquido de Thomas e as células foram contadas na câmara de Newbauer em microscópio óptico (OLYMPUS BX50). Foram incubadas 4x10 5 /ml células em garrafas de cultura (50mL) em 90% de meio RPMI 1640 (Sigma) e 10% de soro fetal bovino (GIBCO) a 37 o C, numa atmosfera de 5% de CO 2. Para a obtenção de DNA das amostras dos controles positivos, negativos e dos pacientes foi realizado o procedimento descrito a seguir Extração de DNA O DNA das células de medula óssea de 45 crianças (17 amostras prospectivas e 28 amostras retrospectivas) com SMD primária, 10 doadores de medula óssea (controles negativos), e das linhagens Raji (controle positivo para metilação no gene p15 INK4B ) e DLD-1
56 36 (controle positivo para metilação no gene p16 INK4A ) foi extraído pelo método de Dnazol (INVITROGEN), segundo o protocolo do fabricante. As células mononucleares foram separadas por centrifugação a 1500 rpm por 20 minutos (centrifuga EPPENDORF- modelo 5804) utilizando gradiente de densidade Ficoll-Paque (AMERSHAM BIOSCIENCES) e lavadas com solução de soro fisiológico (9% NaCl). Após a lavagem foi adicionado 1mL do reagente Dnazol (INVITROGEN). O material foi homogeneizado lentamente, em seguida o DNA foi precipitado. A precipitação do DNA foi feita em etanol 100% e o material foi lavado em etanol 75%. A amostra de DNA foi seca à temperatura ambiente, ressuspensa em solução de Tris-EDTA (10mM de Tris e 1mM de EDTA, ph 7,4) e armazenada a uma temperatura de aproximadamente 15ºC. Um gel de agarose de 0,8% corado com brometo de etídeo (0,5µg/mL) foi feito para a verificação da integridade do DNA e presença de RNA. A concentração de DNA nas amostras foi verificada no espectrofotômetro através de leitura em comprimento de onda 260nm (Biophotometer 8,5mm- EPPENDORF) Análise de Metilação dos genes p15 INK4B e p16 INK4A pelo Método MSP Tratamento do DNA com Bisulfito Cada amostra de DNA (pacientes, controles negativos e controles positivos) foi tratada com bisulfito de acordo com o método descrito por Herman et al. (1996) com algumas modificações. O tratamento com bisulfito induz a desaminação das bases citosinas não metiladas, convertendo-as em uracil, as quais após a reação de PCR são amplificadas como timina, no entanto, citosinas metiladas permanecem inalteradas (fig. 6).
57 37 Fig. 6: Efeito do tratamento com bisulfito em uma amostra de DNA com seqüências ricas em dinucleotídeo CpG. Todas as citosinas fora do dinucleotídeo CpG são desaminadas e convertidas em uracil. As citosinas não metiladas que se encontram dentro do dinucleotídeo CpG sofrem a ação do bisulfito e são convertidas em uracil, no entanto, as citosinas metiladas permanecem inalteradas (*) (GALM, 2006). Amostras de DNA (2µg) em 50µL de água destilada foram previamente desnaturadas em uma solução de NaOH 0.2mol/L por 10 minutos a 37 C. Após este período foram adicionados 30µL de hidroquinona (10mM, SIGMA) e 520µL de sulfito de sódio hidrogenado, ph 5,0 (3M, SIGMA). Foi adicionado óleo mineral sobre as amostras, sendo estas então mantidas em banho-maria a 50 C durante 16 horas. Após este período, o óleo mineral foi retirado das amostras e o DNA foi purificado utilizando o kit Wizard DNA Clean-Up System (PROMEGA). Foi adicionado 1mL de resina no material, homogenizado lentamente e filtrado em uma coluna. As colunas foram lavadas utilizando 2mL de isopropanol 80%. Para eluir o DNA da coluna foi utilizado 50µL de água MILIQ a 70 C. A modificação do DNA foi finalizada com o tratamento em uma solução de NaOH 0.3mol/L por 5 minutos a temperatura ambiente. Em seguida, para a precipitação do DNA foi adicionada 5.5µL de acetato de sódio (3M, ph 5,2) e 200µL etanol 100%. As amostras foram mantidas a uma temperatura de 3 C durante 16 horas. Após este periodo, as amostras foram centrifugadas a 7000 rpm (centrifuga EPPENDORF- modelo 5804) por 30 minutos e o sobrenadante desprezado. O DNA foi lavado em etanol 70%, seco à temperatura ambiente e ressuspenso em 20µL de água destilada.
58 Reação em Cadeia da Polimerase específica para a Metilação (técnica MSP) Para verificar a presença de metilação na região promotora dos genes p15 INK4B e p16 INK4A utilizamos a técnica MSP (reação da polimerase específica para a metilação). Nesta análise, usamos os oligonucleotídeos descritos na tabela 5 segundo Herman et al. (1996). Tabela 5: Oligonucleotídeos* utilizados na técnica MSP para análise do gene p15 INK4B e p16 INK4A Genes Seqüencia dos Oligonucleotídeos (5 3 ) p15-mf p15-mr p15-uf p15-ur p16-mf p16-mr p16-uf p16-ur GCGTTCGTATTTTGCGGTT CGTACAATAACCGAACGACCGA TGTGATGTGTTTGTATTTTGTGGTT CCATACAATAACCAAACAACCAA TTATTAGAGGGTGGGGCGGATCGC GACCCCGAACCGCGACCGTAA TTATTAGAGGGTGGGGTGGATTGT CAACCCCAAACCACAACCATAA M- oligonucleotídeo específico para o alelo metilado; U- oligonucleotídeo específico para alelo não metilado; f- forward = senso; r- reverse = anti-senso (*HERMAN et al.,1996). As condições finais, nas quais as reações de PCR foram conduzidas, consistiram de 3µL do DNA modificado por bisulfito, MgCl 2 6.7mM (INVITROGEN), 5µL de tampão de reação (200mM tris-hcl ph 8.4, 500mM KCl) (INVITROGEN), datp 1.25mM, dttp 1.25mM, dctp 1.25mM e dgtp 1.25mM (INVITROGEN), 1nmol de cada oligonucleotídeo e 1U de Taq polimerase (INVITROGEN) para um volume final de 50µL. A reação foi realizada utilizando-se o termociclador PTC-150 (MJ Research) e as condições de ciclagem para ambos os genes incluíram: desnaturação inicial a 95ºC por 10 minutos, hot-started a 72ºC por 5 minutos, 35 ciclos de desnaturação a 95ºC por 1 minuto, pareamento a 60ºC por 30 segundos, extensão a 72 C por 30 segundos; e extensão final a 72 C por 10 minutos. Após a amplificação, os produtos foram visualizados em gel de poliacrilamida.
59 Avaliação dos Produtos gerados pela PCR nos Genes p15 INK4B e p16 INK4A Após a amplificação, os produtos da PCR foram submetidos à eletroforese em gel de poliacrilamida 5%. O preparo do gel foi realizado com 1,5mL de solução de acrilamida (AMERSHAM BIOSCIENCES): bis-acrilamida (AMERSHAM BIOSCIENCES) 20% (19:1), 0,3 ml de tampão TBE 10X [tris 0,89M (AMERSHAM BIOSCIENCES); ácido bórico 0,89M (ISOFAR); EDTA 0,02M (AMERSHAM BIOSCIENCES)], 42µL de persulfato de amônio 10% (AMERSHAM BIOSCIENCES), 6µL de TEMED (INVITROGEN) e água destilada para volume final de 6mL. Em um volume de 5µL do produto de PCR foram acrescentados 2µL do corante de corrida [azul de bromofenol 0,25% (AMERSHAM BIOSCIENCES); xileno cianol 0,25% (AMERSHAM BIOSCIENCES); glicerol 30% (ISOFAR)]. A eletroforese foi realizada em cuba vertical (Cuba Mini-Protean BIO-RAD) a 110V por 50 minutos e o TBE 0,5X foi utilizado como tampão de corrida. Em seguida, o gel foi corado com nitrato de prata (MERCK) (Santos, 2002). Para fins comparativos, foi utilizado o padrão de peso molecular Low DNA Mass Ladder (INVITROGEN) Sequenciamento de DNA Em todas as amostras positivas para a presença de metilação na região promotora dos genes p15 INK4B e p16 INK4A foi realizado o sequenciamento automático do DNA, como uma metodologia adicional confirmatória. As amostras positivas derivadas do produto de PCR foram purificadas utilizando o kit GFX TM PCR (DNA and Gel Band purification Kit- AMERSHAM BIOSCIENCES), segundo recomendações do fabricante. Um volume de 30µL do produto de PCR foram acrescentados em 500µL de tampão de captura e colocadas em um tubo contendo uma coluna. A amostra foi centrifugada a 6000 rpm por 30 segundos e o precipitado descartado. Foi adicionado 500µL de tampão de lavagem (10mM TE; etanol 80%)
60 40 na coluna e centrifugado novamente a 6000 rpm por 30 segundos. A coluna foi lavada com 20µL de água destilada e centrifugada a 6000 rpm por 1 minuto para eluir o DNA. O DNA purificado foi quantificado através do espectrofotômetro em leitura em comprimento de onda de 260nm(Biophotometer 8,5mm- EPPENDORF). O sequenciamento foi realizado utilizando a Plataforma ABI PRISM 3100 Genetic Analyser (Applied Biossistems). Para cada amostra de produto de PCR foram realizados dois sequenciamentos, um utilizando oligonucleotídeos senso (f) e outro oligonucleotídeos antisenso (r). Para a reação de sequenciamento foi utilizado 100ng do DNA purificado e 3,2pmol do oligonucleotídeo (tabela 7), em um volume total de 7µL, 1 µl de tampão 5x (Tris HCl 400mM; MgCl 2 10mM, ph 9,0), 1µL de H 2 O ultra pura e 1µL do Mix Big Dye (Taq + fluoróforos + MgCl 2 ). As condições de ciclagem foram 25 ciclos de desnaturação a 96ºC por 10 segundos, pareamento a 50ºC por 5 segundos e extensão a 60ºC por 4 minutos. Após a PCR, o material foi precipitado com 40µL de isopropanol 75%, deixado a temperatura ambiente por 15 minutos e centrifugado a 4000 rpm (centrifuga EPPENDORFmodelo 5804) por 45 minutos. O sobrenadante foi desprezado e o precipitado lavado com 50µL de etanol 70% e centrifugado por 15 minutos a 4000 rpm (centrifuga EPPENDORFmodelo 5804). Após secar por 15 minutos a 37 C foram acrescentados 10µL de formamida ultrapura (MERCK). O material foi então desnaturado por 10 min a 96 C em máquina de PCR e mantido no gelo. A placa foi então colocada na Plataforma 3100 para a leitura da seqüência. A análise do resultado do sequenciamento foi feita através do programa BioEdit Sequence Alignment Editor
61 41 Resultados 4.1 Análise Citogenética em Síndrome Mielodisplásica Primária na Infância No presente estudo foi feita a análise citogenética em 64 pacientes com síndrome mielodisplásica primária na infância com idades que variaram de 5 meses a 18 anos, sendo 40 do sexo masculino e 24 do sexo feminino. Do total de pacientes analisados de acordo com a classificação para SMD da infância (HASLE et al., 2003), 35 apresentaram CR, 14 AREB, 10 AREB-t e 5 LMMJ. Neste estudo não foram caracterizados pacientes com ARSA. Duas crianças eram portadoras da Síndrome de Down (pacientes nº36 e nº58, tabela 6). Em três casos (pacientes nº7, nº11 e nº37, tabela 6) não foi possível a obtenção de mitoses para a análise citogenética. Nos demais casos, o índice mitótico variou de regular para bom, com uma boa qualidade de cromossomos metafásicos para definição do padrão cromossômico. Alterações cromossômicas foram detectadas em 44 pacientes (72%) dos 61 casos analisados (tabela 6). A análise citogenética auxiliou no diagnóstico dos casos com suspeita de SMD primária pediátrica e foi uma importante ferramenta para a escolha do tratamento. Tabela 6: Análise Citogenética em Síndrome Mielodisplásica Primária na Infância Nº Idade/ Sexo Subtipo Cariótipo Evolução da doença Grupos de Risco (IPSS) 1 8a /F CR 46,XX,del(9)(p21)[3]/46,XX[19] não/tmo/óbito int a /M CR 46,XY,del(17)(p12)[9]/46,XY,del(17)(p12), não /TCTCU int-1 del(12)(p13)[5]/46,xy,del(11)(q23)[3]/46,xy[34] 3 9a /M CR 46,XY,del(3)(p23)[5]/46,XY[38] sim/ Epo/AREB int-1 3a 10a /M AREB 46,XY,del(3)(p23)[11]/46,XY[21] Epo/óbito int-2 4 1a /M CR 46,XY[32] não/transfusão int-1 5 3a /M CR 46,XY,+der(3)del(3)(q21),-7,-9,+mar[2]/46,XY[27] sim/areb/ int-2 QT 6 13a /F CR 46,XX,del(5)(q15q35)[15]/46,XX[38] não/tmo int-1
62 42 7 5m /M CR sem mitose não/transfusão a /M CR 46,XY,del(11)(q23)[5]/46,XY[27] não/ transfusão int-1 9 7a /F CR 46,XX,del(12)(p13)[10]/46,XX[28] não/tmo int a /M CR 46,XY[26] não/ transfusão int a /M CR sem mitose não transfusão a /F CR 46,XX[22] não/ transfusão int a /M CR 46,XY[35] não/ transfusão/ int-1 óbito 14 8a /M CR 46,XY[33] não/ transfusão/ int-1 óbito 15 7a /M CR 46,XY[20] não/ transfusão int a /M CR 46,XY[41] não/ transfusão int m/F CR 46,XX[40] sim/gm-csf int-1 /AREB 17a 2a /F AREB 46,XX,del(11)(q23)[15]/46,XX[18] óbito int a /M CR 46,XY,-7,+20[13]/46,XY[17] não/tmo int a /M CR 46,XY,del(12)(p12)[6]/46,XY[37] não/tmo int a /F CR 46,XX[30] não/ transfusão int a/F CR 46,XX,del(6)(q21)[13]/46,XX[25] sim /AREB int-1 21a 18a/F AREB 46,XX,del(6)(q21)[10]/46,XX[12] TMO int a /M CR 46,XY[32] não/ transfusão int a /F CR 46,XX[36] não/ transfusão int a /F CR 47,XX,+mar[2]/46,XX[27] não/tmo/óbito int a /F CR 46,XX[30] não/ transfusão int a /F CR 46,XX[32] não/ transfusão int a /M CR 46,XY,del(17)(p12)[15]/46,XY[28] não/tmo int a /M CR 46,XY,del(17)(p12)[4]/ 46,XY[25] não/tmo int a /M CR 46,XY[20] não/tmo int a /M CR 46,XY,del(17)(p12)[12]/46,XY[8] não/tmo int a /F CR 46,XX[20] não/tmo int a /F CR 51,XX,+4,+6,+8,+14,+20[3]/46,XX[41] não/tmo int a /M CR 46,XY,csb[6]/46,XY[20] não/tmo int a /M CR 46,XY,del(17)(p12)[5]/46,XY[16] não/tmo int-1
63 a /F CR 46,XX,csb[8]/46,XX[31] não/tmo int m /F AREB 47,XX,der(17)t(1?;17)(q32?,p13),+21c[15]/ 47,XX,+21c[6] sim/lma/ QT/óbito alto-risco 37 7a/M AREB sem mitose não/ transfusão a /M AREB 45,XY,-19[4]/46,XY[25] não/ transfusão int m /M AREB 46,XY,del(6)(q23)[5]/46,XY[15] não/ transfusão int a /M AREB 47,XY,+8[11]/46,XY[34] sim/ LMA/ QT /óbito int a /M AREB 47,XY,+8[30]/46,XY[21] sim /LMA/ QT/óbito int a /F AREB 46,XX,i(9)(q10)[15]/46,XX[7] sim/lma/ TMO/ óbito int a /F AREB 46,XX,del(11)(q23)[14]/46,XX[23] sim/lma/ int-2 TMO/óbito 44 13a /F AREB 46,XX,del(7)(q22)[10]/46,XX[12] não/tmo alto risco 45 12a /M AREB 46,XY,del(11)(q23)[12]/46,XY[8] sim/lma/ QT/ óbito int a /F AREB 58,XX,+X,+3,+5,+6,+8,+10,+11,+12,+13,+18,+20, +21[5]/58,XX,idem,dup(1)(q21q31)[14]/46,XX[21] sim /LMA/ QT/óbito alto risco 47 14a /M AREB 46,XY,del(7)(q22)[10]/46,XY,del(7)(q22), sim /LMA/ alto risco del(12)(p12)[3]/46,xy[7] QT/óbito 48 18a /M AREB 46,XY[20] não/tmo int a /M AREB 46,XY[20] não/tmo int a /F AREB-t 46,XX,t(4;7)(p16;p15)[16]/46,XX[23] sim/lma/ QT/óbito alto risco 51 4a /F AREB-t 49,XX,dup(1)(q21q32),+6,+8,+mar[4]/46,XX[16] sim /LMA/ QT/óbito alto risco 52 1a /M AREB-t 46,XY,add(9)(q34)[5]/46,XY,inv(1)(q21), add(9)(q34)[4]/46,xy[22] sim /LMA/ QT/óbito alto risco 53 10a /M AREB-t 45,XY,-7[26]/46,XY[4] sim /LMA/ alto risco QT/óbito 54 21m/M AREB-t 45,XY,-7[24]/46,XY[6] sim /LMA/ QT/óbito alto risco 55 12a /M AREB-t 45,XY,-7[18]/46,XY[2] não/ TMO/ óbito alto risco
64 56 5a /M AREB-t 46,XY,t(5;8)(q32;q22)[23]/46,XY[8] sim/lma/ QT/ óbito 57 22m/M AREB-t 45,XY,-7[14]/46,XY[6] sim /LMA/ 58 12a /M AREB-t 58,XY,+8,+13,+13,+14,+15,+20,+21c,+21,+21, +21,+22,+22[20]/47,XY,+21c[2] QT/óbito sim /LMA/ QT/óbito 59 17a /M AREB-t 47,XY,+8[22]/46,XY[4] sim /LMA/ TMO/óbito 44 alto risco alto risco alto risco alto risco 60 21m /F LMMJ 46,XX,inv(5)(q11q21),-9,+mar[2]/46,XX[38] não/qt/óbito alto risco 61 2a /M LMMJ 47,XY,+16[6]/46,XY[17] não/qt int a /M LMMJ 46,XY,del(11)(q23)[10]/46,XY[10] sim /LMA/ QT/óbito 63 1a /F LMMJ 46,XX,del(11)(q23)[5]/46,XX[24] não/qt/óbito int a /M LMMJ 45,XY,-7[20]/46,XY[2] não/ TMO/ óbito alto risco CR - citopenia refratária; AREB - anemia refratária com excesso de blastos; AREB-t - anemia refratária com excesso de blastos em transformação; LMMJ- leucemia mielomonocítica juvenil; LMA- leucemia mielóide aguda; a - ano(s), m- meses, F- feminino, M- masculino, TMO- transplante de medula óssea alogenêico, TCTCU- transplante de células tronco de cordão umbilical, QTquimioterapia; GM-CSF - fator de estimulação de colônias granulócito-macrófago, Epoeritropoetina; int-1- intermediário 1; int-2- intermediário 2; números 3a, 17a e 21a- acompanhamento dos paciente 3, 17 e 21 respectivamente. int Freqüência de Casos com Alterações Cromossômicas por Subtipos de SMD Primária na Infância Para o cálculo da freqüência de casos com anomalias cromossômicas nos subtipos foi considerado como 100% o total de casos analisados por subtipo. Dos 33 pacientes com CR, 18 (54,5%) apresentaram cariótipo anormal. Nos subtipos mais avançados da doença a freqüência de casos com alterações cromossômicas foi maior, sendo verificada em 11 (85%) dos 13 pacientes com AREB, em 10 (100%) dos casos com AREB-t e em 5 (100%) dos casos de LMMJ (tabela 7). Portanto, podemos perceber que conforme o subtipo da SMD se torna mais avançado o número de casos com cariótipos anormais aumenta.
65 45 Tabela 7: Freqüência de Casos com Cariótipos Anormais em SMD Primária na Infância Classificação Total de Pacientes Analisados Nº de casos com cariótipos anormais CR (54,5%) AREB (85%) AREB-t (100%) LMMJ 5 5 (100%) Total (72%) Verificamos que diferente das leucemias, o padrão cromossômico em pacientes portadores de SMD primária na infância é caracterizado principalmente por perdas parciais e completas de cromossomos (as deleções e as monossomias), assim como o ganho cromossômico (trissomias). Neste estudo foram encontrados poucos casos de translocações cromossômicas. Como podemos observar na figura 7, as anomalias cromossômicas mais freqüentes foram: alterações envolvendo o cromossomo 7 (-7/7q - ), sendo verificadas em 8 pacientes (18%), cariótipos complexos em 6 pacientes (14%), del(11)(q23) em 5 pacientes (11%), e a del(17)(p12) em 4 pacientes (9%). Outras alterações encontradas com menor freqüência foram: +8, alterações envolvendo o cromossomo 9 [add(9)(q34), del(9)(p21) e i(9)(q10)] e translocações cromossômicas, sendo observados em 3 pacientes (7%) cada alteração cromossômica; del(6)(q21), del(12)(p13) e quebras cromatídicas em 2 pacientes (4,5%) e del(3)(p23), del(5)(q15q35),+16, alteração cromossômica biclonal, -19 e +mar em 1 paciente (2%). Os cariótipos mostrando as principais alterações cromossômicas detectadas neste estudo podem ser visualizados no anexo 2.
66 46 18% 16% 14% 12% Freqüência de casos 10% 8% 6% 4% 2% 0% del(7q)/-7 del(11)(q23) del(17p) +8 add(9q)/ del(9p)/ i(9q) del(6q) del(12p) del(3p) del(5q) +16 biclonal -19 +mar Fig. 7: Freqüência das alterações cromossômicas em SMD primária na infância. Estudando a distribuição das alterações cromossômicas por subtipo, foi verificado que aparentemente não há uma especificidade de uma alteração cromossômica por subtipo. No subtipo CR, os pacientes apresentaram cariótipos normais, del(3p), del(5q), del(6q), -7 associado com +20, del(9p), del(11q), del(12p), del(17p), +mar e cariótipo complexo, sendo a alteração mais freqüente a del(17p). No subtipo AREB a incidência de cariótipos normais foi baixa predominando as seguintes alterações cromossômicas: del(6q), del(7q), +8, i(9q), del(11q), der(17), -19 e cariótipos complexos, no entanto, a del(7q), +8 e del(11)(q23) foram as alterações mais freqüentes; em AREB-t todos os pacientes apresentaram alterações cromossômicas, como: -7, add(9q) associado com inv(1q), +8, t(5;8) e cariótipos complexos, sendo a alteração mais freqüente a -7. Os pacientes classificados como LMMJ não
67 47 apresentaram cariótipos normais, tendo como alterações cromossômicas a -7, del(11)(q23), +16 e cariótipos complexos, no entanto, a del(11)(q23) foi a alteração mais freqüente. Podemos observar que a monossomia do cromossomo 7 esteve presente principalmente nos subtipos mais avançados da doença (tabela 8). Tabela 8: Distribuição do Padrão Cromossômico por Subtipo de SMD Primária na Infância Subtipo Cariótipo N de pacientes cariótipo normal 15 del(3p) 1 del(5q) 1 del(6q) 1-7 e del(9p) 1 del(11)(q23) 1 del(12p) 2 del(17p) 4 +mar 1 alteração biclonal 1 quebras cromatídicas 2 cariótipos complexos 2 CR (33 pacientes) AREB (13 pacientes) AREB-t (10 pacientes) LMMJ (5 pacientes) cariótipos normais del(6q) del(7q) +8 i(9q) del(11)(q23) -19 translocações cromossômicas cariótipos complexos cariótipos normais add(9q) e inv(1q) translocações cromossômicas cariótipos complexos cariótipos normais -7 del(11)(q23) +16 cariótipos complexos %/ subtipo 46% 3% 3% 3% 3% 3% 3% 6% 12% 3% 3% 6% 6% 15% 8% 15% 15% 8% 15% 8% 8% 8% 0% 40% 10% 10% 20% 20% 0% 20% 40% 20% 20%
68 Citogenéica Molecular: Aplicação do FISH em SMD Primária na Infância (B A metodologia da citogenética molecular (FISH) foi utlizada em sete pacientes com SMD primária na infância. Em três pacientes, que não apresentaram mitose para análise através da citogenética clássica, para afastarmos alterações cromossômicas de mau prognóstico foram utilizadas as sondas do cromossomo 7 e da região q23 do cromossomo 11. Os três pacientes mostraram os sinais normais, respectivos de cada cromossomo (fig. 8). (A) (A) (B) Fig 8: Análise por hibridização in situ por fluorescência. (A) FISH utilizando a sonda do cromossomo 7 (LSI D7S486 spectrum orange/cep 7 spectrum green, Vysis, Inc. Downers Grove, USA). Podemos observar quatro marcações nos núcleos interfásicos, caracterizando uma célula normal para o cromossomo 7. O segmento da sonda de cor verde marca a região centromérica do cromossomo 7 e o de cor vermelha, a região q31. (B) FISH utlizando a sonda da região 11q23 (LSI MLL Dual Color, Vysis, Inc. Downers Grove, USA). Podemos observar que ocorreu a marcação normal do gene nos dois cromossomos na metáfase, mostrando a presença dos dois alelos. O mesmo podemos observar no núcleo interfásico. Utilizamos a técnica de FISH para confirmação da presença da deleção do braço curto do cromossomo 17 e a deleção do braço longo do cromossomo 11 na região q23, em uma criança com SMD hipocelular, CR, que apresentou dois clones caracterizados citogeneticamente:46,xy,del(17)(p12)[9]/46,xy,del(17)(p12),del(12)(p13)[5]/46,xy,del(11) (q23)[3]/ 46,XY[34] (fig.9a). Neste caso foram realizadas duas preparações, uma utilizando a sonda do gene p53 mapeado na região p13.1 do cromossomo 17 e a outra utilizando a sonda do gene MLL mapeado no braço longo do cromossomo 11, na região q23. A análise por FISH
69 detectou a ausência dos alelos dos genes p53 e MLL (fig. 9B e 9C, respectivamente). Este 49 caso é o primeiro relato da literatura, mostrando uma alteração citogenética biclonal envolvendo os cromossomos 11 e 17 em SMD hipocelular na infância. A análise citogenética exerceu um papel fundamental para a confirmação da doença, uma vez que esta criança não apresentava diagnóstico concluído. Este paciente foi indicado para o transplante de medula óssea alogenêico (TMO), entretanto, não possuía doador HLA compatível, sendo submetido ao transplante de células tronco de cordão umbilical (TCTCU) (doador feminino) e hoje, 15 meses após o transplante ele se encontra em remissão citogenética completa (100% de células femininas). (A) 17p(12) 17p(12) 12p(13) 11q(23) (B) (C) Fig. 9: Análise por citogenética clássica e citogenética molecular (FISH). (A) Cariótipo parcial, bandeamento G, mostrando a alteração cromossômica biclonal: del(17)(p12)/ del(17)(p12),del(12)(p13) e del(11)(q23); FISH utilizando as sondas dos genes p53 (B) e MLL (C). Podemos observar que tanto em B quanto em C ocorreu a marcação do gene em apenas um cromossomo na metáfase, mostrando a ausência de seu respectivo alelo (setas). O mesmo podemos observar no núcleo interfásico (setas). Na figura C podemos observar um núcleo interfásico com duas marcações, caracterizando uma célula normal.
70 50 A técnica de FISH também foi aplicada em um caso de SMD hipocelular classificada como CR que apresentou o seguinte padrão cromossômico: 46,XX,del(5)(q15q35)[15]/ 46,XX[38] (fig. 10A). A del(5q) corresponde a uma alteração cromossômica muito rara na infância, desta forma, para caracterizarmos melhor esta alteração e verificarmos se houve a perda do gene c-fms (localizado na região q33), utilizamos a sonda que marca o braço curto do cromossomo 5 (cor verde) e a região 5q33-q34 (cor vermelha) (LSI CSF1R SO/ LSID5S23:D5S721 SG Vysis, Inc. Downers Grove, USA). Nosso resultado mostrou a perda da região q33-q34 do cromossomo 5 neste paciente (fig. 10B), confirmando nosso achado prévio da citogenética clássica. (B) (A) Fig. 10: Análise por citogenética clássica e citogenética molecular (FISH). (A) Cariótipo parcial, bandeamento G, mostrando a alteração cromossômica: del(5)(q15q35). (B) FISH utilizando a sonda de dupla marcação do cromossomo 5. O segmento da sonda de cor verde marca o braço curto do cromossomo 5 e o de cor vermelha, a região 5q33-q34. Podemos observar a marcação em dois núcleos interfásicos, um núcleo apresentando quatro sinais caracterizando os dois cromossomos 5 normais e outro núcleo apresentando três sinais(seta), confirmando a perda da região q33-q34. Para investigarmos o envolvimento do gene supressor de tumor p53, em um cromossomo derivativo, resultante da translocação não balanceada envolvendo provavelmente o braço longo do cromossomo 1 e o braço curto do cromossomo 17, utilizamos a técnica de FISH. Este paciente era portador da SD e a análise por citogenética clássica mostrou o
71 51 seguinte padrão cromossômico: 47,XX,der(17)t(1?;17)(q32?;p13),+21c[15]/47,XX,+21c[6] (fig. 11A). Através da análise por FISH foi confirmado o derivativo do cromossomo 17, sem o envolvimento do gene supressor de tumor p53 (fig. 11B). Esta paciente foi tratada com quimioterapia, evoluindo para LMA e logo após foi a óbito. (B) (A) Fig. 11: Análise por citogenética clássica e citogenética molecular (FISH). (A) Cariótipo parcial, bandeamento G, mostrando a alteração cromossômica: der(17)t(1?;17)(q32?;p13). (B) Análise por FISH utilizando a sonda do gene p53 localizado na região p13.1 do cromossomo 17, mostrando a presença do gene p53 nos dois cromossomos. Para realizar o acompanhamento de evolução da doença e monitoramento terapêutico (pós QT) de um paciente apresentando AREB-t e monossomia do cromossomo 7 ao diagnóstico (fig. 12A), aplicamos a técnica de FISH. Para esta análise foi utilizada a sonda com dupla marcação do cromossomo 7 (fig. 12B). Esta metodologia foi aplicada, pois para definição do padrão cromossômico no acompanhamento de evolução da doença, o número de metáfases analisadas foi pequeno, apenas 12, entretanto, não observamos a presença de alterações cromossômicas adicionais. O FISH mostrou através de 300 células analisadas (metáfases e núcleos interfásicos) um aumento do clone apresentando a monossomia do cromossomo 7 (95%). Esta criança evoluiu para LMA e foi tratada com QT. No monitoramento da terapia observamos células com monossomia do cromossomo 7, indicando a recaída da doença.
72 52 (B) (A) Fig. 12: Análise por citogenética clássica e citogenética molecular (FISH). (A) Cariótipo parcial, bandeamento G, mostrando a alteração cromossômica: -7. (B) FISH: sonda do cromossomo 7 (LSI D7S486 spectrum orange/ CEP 7 spectrum green, Vysis, Inc. Downers Grove, USA). O segmento da sonda de cor verde marca a região centromérica do cromossomo 7 e o de cor vermelha, a região q31. Podemos observar quatro marcações nos núcleos interfásicos, caracterizando uma célula normal para o cromossomo 7. Observamos a presença de alguns núcleos com apenas dois sinais, caracterizando a monossomia de 7 (setas). Na metáfase, observamos também a marcação em apenas um cromossomo, confirmando a monossomia de 7 (seta). 4.3 Distribuição dos Pacientes com SMD Primária na Infância segundo os Grupos de Risco (IPSS) Utilizamos os critérios adotados pelo IPSS (tabela 3) para classificar os pacientes com SMD primária na infância de acordo com os grupos de risco. O IPSS tem por objetivo prever o tempo de sobrevivência e a taxa de transformação leucêmica. Verificamos que nenhum dos nossos pacientes foi classificado como de baixo risco, sendo o grupo de risco mais freqüente o intermediário 1 (tabela 9). Dos 61 pacientes 33 (54%) foram classificados como intermediário 1, 12 (20%) intermediário 2 e 16 (26%) alto risco. Evolução da doença foi verificada em 34,4% (22) do total dos 64 pacientes estudados. Correlacionando os grupos de risco com a taxa de evolução da doença, verificamos que os pacientes classificados com alto risco, apresentaram a maior taxa de evolução da doença. Dos
73 53 pacientes classificados como intermediário 1 (33) e intermediário 2 (12), apenas 3 (9%) e 5 (42%) apresentaram evolução da doença e 18% e 58,3% foram à óbito respectivamente. No entanto, 12 (75%) dos 16 pacientes classificados como alto risco apresentaram evolução da doença, revelando um pior prognóstico e alta taxa de mortalidade (94%). Tabela 9: Freqüência de Pacientes com SMD Primária na Infância de acordo com o IPSS (1997) que mostraram evolução da doença Classificação IPSS Grupos de Risco Total de Pacientes Pacientes que mostraram evolução da doença (%) N de óbitos Baixo Intermediário (9%) 6 (18%) Intermediário (58,3%) 7 (58,3%) Alto (75%) 15 (94%) Total (36%) 28 (46%) OBS: três pacientes não apresentaram mitose, dessa forma não foi possível aplicar o IPSS. Diferentes tratamentos foram utilizados em nossos pacientes como transfusão sanguínea que foi aplicada em 18 pacientes (28%), fatores de crescimento em 2 pacientes (3%), quimioterapia em 19 pacientes (30%) e TMO em 25 pacientes (39%). A quimioterapia revelou-se como sendo o pior tratamento para estes pacientes com uma taxa de mortalidade de 84%. O transplante de medula óssea alogenêico demonstrou ser eficaz para este grupo de pacientes, apresentado uma taxa de mortalidade de 28%. 4.4 Análise Molecular A análise do padrão de metilação na região promotora dos genes p15 INK4B e p16 INK4A em 45 pacientes com SMD primária na infância foi realizada pela técnica MSP. Os pacientes foram distribuídos segundo a classificação em: 26 casos com CR, 9 com AREB, 8 com AREB-t e 2 com LMMJ. A metilação em p15 INK4B foi detectada em 35,5% dos pacientes e em p16 INK4A em 8,8% do total de casos analisados.
74 4.4.1 Análise da Freqüência de Metilação na Região Promotora do Gene p15 INK4B em Pacientes com SMD Primária na Infância 54 Para a análise da presença de metilação no gene p15 INK4B em pacientes com SMD primária na infância, nós utilizamos como controle negativo o DNA de células mononucleares de doadores de medula óssea e como controle positivo o DNA das células da linhagem Raji. Em todas as amostras foram amplificadas as regiões promotoras do gene p15 INK4B através da reação em cadeia da polimerase específica para a metilação (MSP) com 100% de sucesso após otimização das concentrações dos reagentes e das condições de ciclagem. Não foi detectada a presença de metilação no gene p15 INK4B nas 10 amostras de DNA dos doadores de medula óssea. As células da linhagem Raji não apresentaram 100% de metilação para este gene, sendo detectada também a presença de células não metiladas para este gene, como observado por Herman et al., 1996 (fig. 13A). Das 45 amostras de DNA de pacientes com SMD primária analisadas 16 (35,5%) apresentaram metilação na região promotora deste gene (tabela 10). No entanto, nenhum destes pacientes apresentou metilação em 100% das células analisadas, como podemos verificar na fig.13b, a qual mostra a presença do gene tanto nas reações que foram utilizados oligonucleotídeos específicos para metilação (M), quanto nas reações com oligonucleotídeos específicos para o gene não metilado (U), sugerindo desta forma que o gene apresenta-se metilado em apenas uma porcentagem de células.
75 55 (A) (B) Fig. 13: Fotografia de gel de poliacrilamida 5% utilizado para verificar a amplificação dos produtos de PCR referente à análise de metilação do gene p15 INK4B após a modificação do DNA com bisulfito. (A) Linha L: marcador de peso molecular Low DNA Mass Ladder (INVITROGEN); linhas U: fragmentos relativos ao produto de PCR de 154pb realizado com oligonucleotídeos específicos para o gene não metilado; linha M: fragmentos relativos ao produto de PCR de 148pb realizado com oligonucleotídeos específicos para o gene metilado. Água: controle da reação; doador: controle negativo para metilação; linhagem celular Raji: controle positivo para metilação e paciente nº1 (tabela 10). (B) 1-4: pacientes positivos para a metilação na região promotora do gene p15 INK4B (pacientes nº. 9, 18, 42, 53 da tabela 10) Tabela 10: Identificação de Metilação no Gene p15 INK4B em SMD Primária na Infância Paciente Subtipo Idade / Sexo Metilação no gene p15 1 CR 8a / F - 2 CR 13a / M - 4 CR 1a / M - 5 CR 3a / M - 6 CR 13a / F - 7 CR 5m /M - 8 CR 14a / M - 9 CR 7a / F + 10 CR 11a / M - 11 CR 8a / M - 12 CR 15a / F + 13 CR 5a / M - 14 CR 8a / M - 15 CR 7a / M - 16 CR 16a / M - 17a AREB 18m / F + 18 CR 7a / M + 19 CR 7a / M - 20 CR 8a / F - 21 CR 18a/F + 22 CR 7a / M - 23 CR 15a / F -
76 56 24 CR 16a / F + 25 CR 7a / F - 26 CR 6a / F - 27 CR 14a / M - 29 CR 7a/M - 36 AREB 17m / F - 40 AREB 5a / M - 41 AREB 16a / M - 42 AREB 7a / F + 43 AREB 15a / F - 44 AREB 13a / F + 45 AREB 12a / M + 47 AREB 14a / M + 50 AREB-t 2a/F + 53 AREB-t 10a / M + 54 AREB-t 21m / M + 55 AREB-t 12a / M + 56 AREB-t 5a / M - 57 AREB-t 22m / M + 58 AREB-t 12a / M - 59 AREB-t 17a / M - 60 LMMJ 21m / F - 63 LMMJ 1a /F Confirmação por Sequenciamento das Amostras Positivas para a Metilação na Região Promotora do Gene p15 INK4B Todas as 16 amostras de produto da MSP positivas para metilação (M) na região promotora do gene p15 INK4B dos pacientes com SMD primária, uma amostra da linhagem celular Raji (controle positivo) e uma amostra para ausência de metilação (U) (controle negativo, doador de medula óssea) foram seqüenciadas com o objetivo de confirmar a presença de metilação e demonstrar a modificação do DNA pelo tratamento com bisulfito, comprovando a eficiência desta técnica. Para cada paciente foram realizadas duas reações de sequenciamento, uma utilizando oligonucleotídeo F ( forward = senso) e a outra utilizando o oligonucleotídeo R (reverse = anti-senso). A análise do sequenciamento demonstrou que os DNAs foram modificados pelo tratamento com bisulfito. Como podemos verificar na fig. 14, quando comparamos a seqüência selvagem (S) com a seqüência não metilada (U) percebemos, que todas as citosinas
77 57 não metiladas foram convertidas em timinas após a técnica MSP em ambos os genes. Além disso, quando comparamos a seqüência não metilada (U) com a seqüência metilada (M), verificamos os sítios de metilação (*), confirmando dessa forma, a presença de metilação nestes pacientes. (A) S U M * * * * * * * (B) Fig. 14: Análise do sequenciamento do gene p15 INK4B (5 3 ) através do programa BioEdit Sequence Alignment Editor. (A) Comparação da seqüência da região promotora do gene p15 INK4B selvagem (S) com amostra de DNA tratada com bisulfito de um doador- seqüência não metilada (U) e um paciente com SMD positivo para a metilação (M), mostrando que houve a conversão de todas as citosinas não metiladas em timinas após a amplificação e os sítios específicos de metilação na sequência metilada (*); (B) Gráfico mostrando o resultado do sequenciamento do gene p15 INK4B de um paciente positivo para metilação Freqüência de Metilação em p15 INK4B nos Subtipos de SMD Primária na Infância A correlação entre a freqüência de metilação no gene p15 INK4B e os diferentes subtipos foi calculada e pode ser vista na tabela 11. Como podemos notar as maiores freqüências de metilação para o gene p15 INK4B estiveram presentes nos subtipos mais agressivos de SMD como AREB, AREB-t e LMMJ, com as freqüências de 55,5% e 62,5% e 50% respectivamente. No subtipo menos agressivo da doença como, CR, a freqüência foi mais baixa sendo 19% do total de pacientes analisados para este grupo. Dos 16 pacientes positivos para metilação, 9 apresentaram evolução da doença (56%) e 11 pacientes faleceram (69%).
78 58 Nossos resultados sugerem que a metilação na região promotora do gene p15 INK4B está associada com maior risco de evolução da doença e confere mau prognóstico. Tabela 11: Freqüência de Metilação no Gene p15 INK4B nos Subtipos de SMD Primária na Infância Classificação N de pacientes N de pacientes com metilação em p15 INK4B CR 26 5 (19%) AREB 9 5 (55,5%) AREB-t 8 5 (62,5%) LMMJ 2 1 (50%) Total (35,5%) Análise da Freqüência de Metilação na Região Promotora do Gene p16 INK4A em Pacientes com SMD Primária na Infância No estudo do padrão de metilação no gene p16 INK4A em pacientes com SMD primária na infância, foram utilizados como controle negativo DNA de células mononucleares de doadores de medula óssea e como controle positivo DNA de células da linhagem DLD-1. A análise do padrão de metilação nos DNAs dos 10 doadores de medula óssea revelou ausência de metilação em todas as amostras. A amostra de DNA das células da linhagem DLD-1 apresentou 100% de metilação. A metilação na região promotora do gene p16 INK4A foi detectada em apenas quatro (8,8%) dos 45 pacientes portadores de SMD primária na infância (tabela 12). No entanto, nenhum dos pacientes apresentou este gene totalmente metilado, sendo positivos também para a MSP com oligonucleotídeos específicos para o gene não metilado (fig. 15).
79 59 Tabela 12: Identificação de Metilação no Gene p16 INK4A em SMD Primária na Infância Paciente Subtipo Idade / Sexo Metilação no gene p16 INK4A 1 CR 8a / F - 2 CR 13a / M - 4 CR 1a / M - 5 CR 3a / M - 6 CR 13a / F - 7 CR 5m /M - 8 CR 14a / M - 9 CR 7a / F - 10 CR 11a / M - 11 CR 8a / M - 12 CR 15a / F - 13 CR 5a / M - 14 CR 8a / M - 15 CR 7a / M - 16 CR 16a / M - 17a AREB 18m / F + 18 CR 7a / M - 19 CR 7a / M - 20 CR 8a / F - 21 CR 18a/F - 22 CR 7a / M - 23 CR 15a / F - 24 CR 16a / F - 25 CR 7a / F - 26 CR 6a / F - 27 CR 14a / M - 29 CR 7a/M - 36 AREB 17m / F - 40 AREB 5a / M - 41 AREB 16a / M - 42 AREB 7a / F - 43 AREB 15a / F + 44 AREB 13a / F - 45 AREB 12a / M - 47 AREB 14a / M - 50 AREB-t 2a/F - 53 AREB-t 10a / M - 54 AREB-t 21m / M - 55 AREB-t 12a / M - 56 AREB-t 5a / M + 57 AREB-t 22m / M + 58 AREB-t 12a / M - 59 AREB-t 17a / M - 60 LMMJ 21m / F - 63 LMMJ 1a /F -
80 60 (A) (B) Fig. 15 Fotografia de gel de poliacrilamida 5% utilizado para verificar a amplificação dos produtos de PCR referente à análise de metilação da região promotora do gene p16 INK4A após a modificação do DNA com bisulfito. (A) Linha L: marcador de peso molecular Low DNA Mass Ladder (INVITROGEN); linhas U: fragmentos relativos ao produto de PCR de 151pb, realizado com oligonucleotídeos específicos para o gene não metilado; linha M: fragmentos relativos ao produto de PCR de 150pb realizado com oligonucleotídeos específicos para o gene metilado. Água: controle da reação; doador: controle negativo para metilação; linhagem celular DLD-1: controle positivo para metilação e paciente nº1 (tabela 12). (B) 1-4: pacientes positivos para a metilação na região promotora do gene p16 INK4A (pacientes nº 56, 17a, 57 da tabela 12) Confirmação por Sequenciamento das Amostras Positivas para a Metilação na Região Promotora do Gene p16 INK4A As quatro amostras do produto da MSP positivas para metilação (M) no gene p16 INK4A de pacientes com SMD primária, uma amostra da linhagem DLD-1 (controle positivo) e uma amostra para ausência de metilação (U) (controle negativo - doador de medula óssea) do gene p16 INK4A foram seqüenciadas. A análise do sequenciamento foi realizado pelo programa BioEdit Sequence Alignment Editor demonstrando que os DNAs foram modificados pelo tratamento com bisulfito, comprovando a eficiência do método. Podemos verificar através da comparação da seqüência selvagem (S) que todas as citosinas não metiladas foram convertidas em timinas após a técnica MSP. O resultado do sequenciamento dos pacientes selecionados confirmou a presença de metilação nesta região do gene p16 INK4A, sendo este dado verificado quando
81 61 comparamos a seqüência não metilada (U) com a seqüência metilada (M), na qual podemos perceber os sítios de metilação (*) (fig. 16). (A) S- U M- (B) * * * * * * * Fig. 16: Análise do sequenciamento do gene p16 INK4A (5 3 ) através do programa BioEdit Sequence Alignment Editor. (A) Comparação da seqüência da região promotora do gene p16 INK4A selvagem (S) com a amostra de DNA tratada com bisulfito de um doador - seqüência não metilada (U) e um paciente com SMD positivo para a metilação (M), mostrando que houve a conversão de todas as citosinas não metiladas em timinas após a amplificação e os sítios específicos de metilação na sequência metilada (*); (B) Gráfico mostrando o resultado do sequenciamento do gene p16 INK4A de um paciente positivo para metilação Freqüência de Metilação na Região Promotora do Gene p16 INK4A nos Subtipos de SMD Primária na Infância A freqüência de metilação no gene p16 INK4A em nossos pacientes com SMD primária na infância foi baixa, sendo obervada apenas em 8,8% dos pacientes. No entanto, aqueles que apresentaram esta alteração estavam classificados dentro dos subtipos mais agressivos da doença, como AREB e AREB-t, ocorrendo como uma freqüência de 22,2% e 25%, respectivamente. Não foram observados casos de metilação deste gene em pacientes classificados com CR e LMMJ (tabela 13). Dos 4 pacientes que apresentaram metilação para região promotora do gene p16 INK4A, todos apresentaram evolução da doença (100%) e
82 faleceram. Nossos resultados sugerem que a presença de metilação está associada com evolução da doença e mau prognóstico. 62 Tabela 13: Freqüência de Metilação no Gene p16 INK4A nos Subtipos de SMD Primária na Infância Classificação N de pacientes N de pacientes com metilação em p16 INK4A CR 26 0 AREB 9 2 (22,2%) AREB-t 8 2 (25%) LMMJ 2 0 Total 45 4 (8,8%) 4.5 Correlação entre a Presença de Metilação na Região Promotora dos Genes p15 INK4B e p16 INK4A com o Padrão Cromossômico em SMD Primária na Infância Na tabela 14 é possível observar que a metilação no gene p15 INK4B esteve presente em todos os subtipos de SMD primária na infância. No subtipo CR foi verificada metilação em células apresentando cariótipo normal e com as alterações cromossômicas del(6q), -7 e +20, del(12p) e +mar. Estes pacientes não apresentaram evolução da doença. No subtipo AREB foi observada metilação nos pacientes com as alterações cromossômicas: del(7q) (2 pacientes), i(9q) (1 paciente) e del(11)(q23) (2 pacientes). Os pacientes com estas alterações apresentaram evolução para LMA, exceto o paciente apresentando del(7q) (paciente nº 44, tabela 14), que foi submetido ao TMO. No subtipo AREB-t, a metilação na região promotora do gene p15 INK4B esteve presente nos pacientes com - 7 (4 pacientes) e t(4;7) (1 paciente). Destes 5 pacientes, 4 apresentaram evolução para LMA, o paciente (nº 55, tabela 14) apresentando -7 foi submetido ao TMO e não mostrou evolução da doença.
83 63 Foi detectada metilação no gene p15 INK4B em um dos dois pacientes com LMMJ. Este paciente apresentava a del(11)(q23) e não apresentou evolução da doença. A presença de metilação em p15 INK4B não foi observada nos pacientes apresentando trissomia do cromossomo 8, hiperdiploidia, t(5;8), no entanto, estes pacientes apresentaram evolução da doença. Desta forma, provavelmente, existem diferentes vias que levam à transformação leucêmica. A metilação na região promotora do gene p16 INK4A foi observada apenas nos subtipos mais agressivos AREB e AREB-t, estando presente em pacientes com as alterações cromossômicas -7 (1 paciente), del(11q) (2 pacientes) e t(5;8) (1 paciente). Todos os quatro pacientes evoluiram da doença e faleceram. Apenas os pacientes 17a e 57 mostraram metilação em ambos os genes. O paciente 17a foi inicialmente diagnosticado com CR e cariótipo normal. No entanto, apresentou evolução da doença para um subtipo mais agressivo AREB, adquirindo alteração cariotípica, a del(11)(q23). A análise do DNA para presença de metilação após a evolução detectou positividade para ambos os genes. Já o paciente 57 classificado como AREB-t apresentou como alteração citogenética a monossomia do 7. A análise molecular revelou a presença de metilação nos dois genes estudados. Este paciente também apresentou evolução da doença. Ambos os pacientes foram a óbito.
84 64 Tabela 14: Correlação entre a Presença de Metilação nos genes p15 INK4B e p16 INK4A com o padrão cromossômico em SMD primária da infância N Idade/ Subtipo Cariótipo Metilação Evolução Sexo nos genes da p15 p16 doença 1 8a /F CR 46,XX,del(9)(p21)[3]/46,XX[19] - - não 2 13a /M CR 46,XY,del(17)(p12)[9]/46,XY,del(17)(p12), - - não del(12)(p13)[5]/ 46,XY,del(11)(q23)[3]/46,XY[34] 4 1a /M CR 46,XY[32] - - não 5 3a /M CR 46,XY,+der(3)del(3)(q21),-7,-9,+mar[2]/46,XY[27] - - sim 6 13a /F CR 46,XX,del(5)(q15q35)[15]/46,XX[38] - - não 7 5m /M CR sem mitose - - não 8 14a /M CR 46,XY,del(11)(q23)[5]/46,XY[27] - - não 9 7a /F CR 46,XX,del(12)(p13)[10]/46,XX[28] + - não 10 11a /M CR 46,XY[26] - - não 11 8a /M CR sem mitose - - não 12 15a /F CR 46,XX[22] + - não 13 5a /M CR 46,XY[35] - - não 14 8a /M CR 46,XY[33] - - não 15 7a /M CR 46,XY[20] - - não 16 16a /M CR 46,XY[41] - - não 17a 2a /F AREB 46,XX,del(11)(q23)[5]/46,XX[18] + + sim 18 7a /M CR 46,XY,-7,+20[13]/46,XY[17] + - não 19 7a /M CR 46,XY,del(12)(p12)[6]/46,XY[37] - - não 20 8a /F CR 46,XX[30] - - não 21 18a/F CR 46,XX,del(6)(q21)[13]/46,XX[25] + - sim 22 7a /M CR 46,XY[32] - - não 23 15a /F CR 46,XX[36] - - não 24 16a /F CR 47,XX,+mar[2]/46,XX[27] + - não 25 7a /F CR 46,XX[30] - - não 26 6a /F CR 46,XX[32] - - não 27 14a /M CR 46,XY,del(17)(p12)[15]/ 46,XY[28] - - não 29 7a/M CR 46,XY[20] - - não 36 17m /F AREB 47,XX,der(17)t(1?;17)(q32?,p13),+21c[15]/ 47,XX,+21c[6] - - sim
85 a /M AREB 47,XY,+8[11]/46,XY[34] - - sim 41 16a /M AREB 47,XY,+8[30]/46,XY[21] - - sim 42 7a /F AREB 46,XX,i(9)(q10)[15]/46,XX[7] + - sim 43 15a /F AREB 46,XX,del(11)(q23)[14]/46,XX[23] - + sim 44 13a /F AREB 46,XX,del(7)(q22)[10]/46,XX[12] + - não 45 12a /M AREB 46,XY,del(11)(q23)[12]/46,XY[8] + - sim 47 14a /M AREB 46,XY,del(7)(q22)[10]/46,XY,del(7)(q22), + - sim del(12)(p12)[3]/46,xy[7] 50 2a/F AREB-t 46,XX,t(4;7)(p16;p15)[16]/46,XX[23] + - sim 53 10a /M AREB-t 45,XY,-7[24]/46,XY[6] + - sim 54 21m/M AREB-t 45,XY,-7[14]/46,XY[8] + - sim 55 12a /M AREB-t 45,XY,-7[18]/46,XY[2] + - não 56 5a /M AREB-t 46,XY,t(5;8)(q32;q22)[23]/46,XY[8] - + sim 57 22m/M AREB-t 45,XY,-7[14]/46,XY[6] + + sim 58 12a /M AREB-t 58,XY,+8,+13,+13,+14,+15,+20,+21c,+21,+21,+21, - - sim +22,+22[20]/ 47,XY,+21c[2] 59 17a /M AREB-t 47,XY,+8[22]/46,XY[4] - - sim 60 21m /F LMMJ 46,XX,inv(5)(q11q21),-9,+mar[2]/46,XX[38] - - não 63 1a /F LMMJ 46,XX,del(11)(q23)[5]/46,XX[24] + - não A correlação entre a presença de metilação na região promotora dos genes p15 INK4B e p16 INK4A com o padrão cromossômico em crianças portadoras de SMD primária com pode ser observada na fig. 17. Nossos resultados sugerem uma forte correlação entre a metilação do gene supressor de tumor p15 INK4B e alterações envolvendo o cromossomo 7 (del(7q)/-7). Dos 16 pacientes positivos para a metilação no gene p15 INK4B, 7 (44%) apresentaram alterações envolvendo o cromossomo 7 e 3 (19%) apresentaram a del(11)(q23). Com uma menor freqüência (6,2%), a metilação no gene p15 INK4B foi observada em pacientes com cariótipo normal, del(6q), i(9q), del(12p), t(4;7) e +mar. Em relação ao estudo de correlação entre o cariótipo e a metilação em p16 INK4A, nossos resultados sugerem que a metilação neste gene é um evento raro em SMD da infância, entretanto parece estar associado com a transformação leucêmica.
86 66 30% 25% p15u p15m p16u p16m Freqüência de casos 20% 15% 10% 5% 0% del(5q) del(6q) -7 / del(7q) +8 i(9q)/del(9p) del(11q) del(12p) del(17p) +mar Fig. 17: Correlação entre o padrão cromossômico em crianças portadoras de SMD primária e presença de metilação na região promotora dos genes p15 INK4B e 16 INK4A. U- não metilado, M- metilado.
87 67 5. DISCUSSÃO A síndrome mielodisplásica primária (SMD) é uma doença clonal de célula tronco hematopoética, a qual ocorre predominantemente em idosos, sendo rara na infância. Embora os aspectos clínicos, morfológicos e laboratoriais da SMD durante a infância não estejam ainda completamente definidos, alguns estudos sugerem distintas características entre a SMD no adulto e na criança (SASAKI et al., 2001; HASLE et al., 2003). No sentido de entender melhor os mecanismos envolvidos nesta patogênese diversos estudos têm sido realizados. Estudos iniciais em SMD na infância, utilizando a classificação FAB, mostraram que a freqüência de pacientes apresentando o subtipo menos agressivo AR era baixa, ocorrendo com maior incidência casos de AREB, AREB-t e LMMJ (NOWELL, 1992; LOCATELLI et al., 1995; MARTINEZ-CLIMENT, 1997). No entanto, estudos mais recentes têm revelado uma predominância do subtipo AR (KARDOS et al., 2003; POLYCHRONOPOULOU et al., 2004). Provavelmente estas diferenças aconteceram devido à dificuldade do diagnóstico de SMD primária na infância, principalmente nos casos com menos de 5% de blastos na medula óssea, onde na prática clínica em pediatria, temos as anemias carenciais por deficiência de vitamina B12 e folato, patologias mitocondriais e infecções virais que podem levar a achados com dispoese de células hematopoéticas. Nestes casos tornam-se importantes diagnósticos diferenciais para a SMD em pediatria, sendo de extrema importância a análise do mielograma, biópsia de medula óssea e a análise citogenética. O estudo das alterações cromossômicas nesse contexto auxilia não só no diagnóstico, mas evidencia aspectos importantes da biologia da doença que se refletem no prognóstico e na evolução do paciente. A classificação FAB para SMD primária, muito utilizada em adultos, vem sendo substituída pela classificação proposta por Hasle et al. em 2003, por este grupo de pacientes apresentar características particulares, como por exemplo a associação de doenças genéticas, como a Síndrome de Down. Portanto, já existindo uma pré-disposição para o
88 68 desenvolvimento de neoplasias. Em nosso estudo foi utilizada a classificação proposta por Hasle et al. (2003) em 64 pacientes sendo identificados os seguintes subtipos: 35 casos de CR, 14 casos de AREB, 10 casos de AREB-t e 5 casos de LMMJ, sendo dois pacientes portadores de Síndrome de Down (1 AREB, 1 AREB-t). As idades dos pacientes variaram de 5 meses a 18 anos. Existem poucos estudos com um grande número de pacientes com SMD primária na infância devido a sua raridade. Entretanto, estudos multicêntricos ou de um longo período de acompanhamento demonstraram que a incidência de alterações cromossômicas é de 40 a 80%. Estes estudos revelaram uma alta freqüência de anormalidades citogenéticas, principalmente nos subtipos mais agressivos da doença como AREB e AREB-t (LUNA-FINEMAN et al, 1999; SASAKI et al, 2001; POLYCHRONOPOULOU et al, 2004; LOPES et al, 2006). Em três pacientes do nosso estudo não foi possível a obtenção de mitoses para o estudo do padrão cromossômico. Anormalidades cromossômicas foram detectadas em 72% dos 61 casos estudados. Com relação à distribuição da freqüência de alterações cromossômicas por subtipo foi verificado que dos 33 pacientes com CR, 18 pacientes (54,5%) apresentaram cariótipos anormais, nos subtipos mais avançados da doença a freqüência de casos com alterações cromossômicas foi maior, sendo verificada em 11 (85%) dos 13 pacientes com AREB, em 10 pacientes com AREB-t (100%) e em 5 pacientes com LMMJ (100%). Nossos resultados são semelhantes aos descritos na literatura, entretanto, tem sido descrita a presença de cariótipos normais em pacientes portadores de LMMJ, fato não encontrado no presente estudo. A variação na porcentagem de casos com alterações cromossômicas pode ser creditada a diversos fatores como variações no número de mitoses analisadas ou amostragem com tendências para subtipos específicos. Assim, em estudos contendo um maior número de casos de AREB e AREB-t, o índice de anormalidades cromossômicas é elevado. Em nosso estudo, procuramos analisar um grande número de metáfases por paciente, uma vez que no subtipo
89 69 inicial da SMD na infância, CR, o clone citogeneticamente anormal pode ser muito pequeno, ao contrário do que acontece nos subtipos mais avançados da doença (AREB, AREB-t e LMMJ). Nossos resultados mostraram no subtipo CR a presença de células com cariótipos normais e células com cariótipos anormais. Dente as células com cariótipos anormais observamos as seguintes alterações: del(3p), del(5q), del(6q), -7, del(9p), del(11q), del(12p), del(17p), +mar e cariótipos complexos. Nos subtipos AREB e AREB-t e LMMJ a incidência de cariótipos normais foi baixa, sendo encontradas diversas anomalias citogenéticas como: inv(1q), t(5;8), inv(5q), del(6q),-7, del(7q), +8, i(9q), add(9q), del(11q), +16, der(17), -19 e cariótipos complexos. Ao contrário do que é encontrado em outras neoplasias hematológicas (leucemias e linfomas), não tem sido possível estabelecer uma correlação entre anomalias citogenéticas e subtipos de SMD. Dessa forma, assim como em outros estudos (LUNA- FINEMAN et al., 1999; HARBOTT et al., 2000), nossos resultados sugerem a ausência de uma alteração específica correlacionada com um subtipo da doença. Neste estudo as anomalias cromossômicas mais freqüentes foram: as alterações envolvendo o cromossomo 7 (18%); cariótipos complexos (14%), a del(11)(q23) (11%), e a del(17)(p12) (9%). Portanto, assim como na SMD do adulto, as alterações cromossômicas em SMD primária na infância são caracterizadas principalmente por perdas parciais ou totais de cromossomos, com uma incidência relativamente alta também de ganho cromossômico e ocorrendo em menor incidência as translocações cromossômicas. O padrão citogenético em SMD primária sugere a inativação de genes supressores tumorais (ou sua haploinsuficiência) necessária para o desenvolvimento de células hematopoéticas normais, principalmente as da linhagem mielóide. As alterações cromossômicas mais freqüentes em SMD primária na infância são: a monossomia de 7 e a deleção 7q (AKTAS & TUNCBILEK, 2006). Estas alterações estão
90 70 associadas com mau prognóstico e elevado risco de transformação leucêmica. Nestes casos têm sido sugerido o transplante de medula óssea alogenêico, principalmente em estágios iniciais da doença (KARDOS et al, 2003). Vale a pena ressaltar, a importância da citogenética selecionando pacientes com baixa contagem de blastos na medula óssea, para tratamentos mais agressivos como o TMO. Esse fato aconteceu durante a realização deste estudo em dois pacientes, um apresentando CR com a alteração cromossômica 7, +20, e o outro apresentando AREB (com 7% de blastos na medula óssea) com a alteração cromossômica 7q- Hoje, ambos pacientes estão vivos desempenhando suas funções normais e apresentando uma boa qualidade de vida. Nossos resultados mostraram que dos 8 pacientes que apresentaram alterações cromossômicas envolvendo o cromossomo 7, 4 (50%) evoluíram da doença e 6 (75%) foram a óbito. Cariótipos complexos corresponderam ao segundo tipo de alteração cromossômica de maior incidência em nosso estudo. Esta alteração esteve associada com todos os subtipos. Um cariótipo complexo envolve três ou mais alterações cromossômicas, estruturais e/ou numéricas e está associado com mau prognóstico. A hiperdiploidia é considerada um cariótipo complexo. A hiperdiploidia I (número cromossômico modal maior que 46) é observada em várias crianças com diferentes neoplasias como a LLA e sua presença confere um prognóstico favorável (PUI, 1995). Já hiperdiploidia II (mais de 70 cromossomos), uma marca nos tumores anaplásicos, em combinação com translocações pode identificar pacientes com alto risco de apresentarem falha ao tratamento (DOUGLAS et al., 1986). Em nosso estudo tivemos quatro casos de hiperdiploidia, dois associados com alteração cromossômica estrutural, a duplicação do braço longo do cromossomo 1. Somente um paciente era do subtipo inicial da doença CR, os outros três eram portadores de AREB e AREB-t. Poucos estudos em SMD na infância correlacionaram o valor prognóstico da hiperdiploidia em SMD na infância. Acar et al. (2001) descreveram uma criança com SMD hipocelular apresentando
91 71 hiperdiploidia associada com mau prognóstico, no entanto, esta criança apresentava alterações congênitas. Portanto, em SMD da infância é necessário que um maior número de pacientes com hiperdiploidia sejam estudados para definição do seu valor prognóstico. A deleção do braço longo do cromossomo 11 na região q23 foi a terceira alteração mais freqüente em nosso estudo. Nesta região cromossômica está mapeado o gene MLL, frequentemente envolvido em leucemias agudas da infância (LLA e LMA). Geralmente, esse gene está associado a alterações cromossômicas do tipo translocação, conferindo mau prognóstico (MATHEW et al., 1999). De acordo com o IPSS alterações envolvendo o cromossomo 11 são consideradas de prognóstico intermediário, no entanto, nossos resultados sugerem que esta alteração está envolvida em casos de evolução da SMD (CR para AREB), sendo necessário o estudo de um maior número de casos que confirmem esse achado. A deleção do braço curto do cromossomo de 17 também apresentou uma significativa incidência (10%) na nossa amostra, esta alteração é apontada segundo o IPSS como prognóstico intermediário. Em nossos pacientes, a del(17p) esteve presente nos subtipos iniciais CR e em casos com medula óssea hipocelular. Nestes casos vale a pena ressaltar o valor da citogenética como um diagnóstico diferencial entre SMD hipocelular e anemia aplástica, onde a presença de uma alteração cromossômica clonal carateriza a SMD. Esse dado é muito importante, pois ambas as doenças são indicadas para o TMO alogenêico, no entanto, o condicionamento pré-tmo é específico para cada doença (YOUNG et al., 2006; DONEY et al., 1997). A nivel morfológico a del(17p) esteve associada com uma dispoese significativa no setor granulocítio, ocorrendo a presença de células Pelguer-Hüet e assência de granulações. Essas crianças apresentaram sérias infecções e foram indicadas para o transplante de medula óssea apresentando uma boa resposta ao tratamento. Na literatura não existem relatos da del(17p) na SMD na infãncia e seu valor prognóstico.
92 72 A trissomia do cromossomo 8 foi observada em 8% do total de casos analisados, esta alteração cromossômica esteve presente em casos de AREB e AREB-t, estes pacientes apresentaram evolução para LMA e faleceram. A trissomia do cromossomo 8 é a alteração numérica mais comum em SMD primária nos adultos e parece ser predominante no sexo masculino. Não se associa a um subtipo específico, mas geralmente se apresenta com citopenia de uma ou três linhagens (CHAUFFAILLE, 2006). Pacientes com trissomia de 8 como anomalia isolada têm risco significativamente maior de transformação leucêmica e pior comportamento do que esperado para o grupo intermediário de prognóstico segundo o IPSS, fato que lança dúvidas quanto a definição prognóstica. Solé et al. (2000) e Fernandez et al. (2000) sugerem que alterações envolvendo o cromossomo 8 estão associadas com mau prognóstico e risco aumentado de transformação leucêmica. A deleção do braço longo do cromossomo 5 foi observada em apenas um dos nossos pacientes. Esta alteração cromossômica é extremamente rara em crianças. Uma revisão da literatura descrita por Pitman et al. (2006) mostraram apenas 7 casos. Em SMD primária nos adultos a del(5q) apresenta características morfológicas e clínicas específicas sendo reconhecida como a Síndrome 5q-, entidade adotada pela classificação OMS. A clássica síndrome 5q- foi descrita pela primeira vez em 1974 por Van den Berghe e colaboradores. Esta alteração ocorre predominantemente em indivíduos do sexo feminino e idades avançadas, estando relacionada com bom prognóstico e baixo risco de transformação leucêmica. Entretanto, os poucos casos descritos na literatura apresentando del(5q) na infância estiveram associados com mau prognóstico (PITMAN et al., 2006). Em nosso estudo, um paciente do sexo feminino, de 13 anos de idade apresentou a del(5q) como única alteração citogenética. Através da análise por FISH foi detectada a perda em um dos alelos do gene c-fms localizado na região q33q34. Este gene codifica o receptor de crescimento de macrófago e apresenta uma função importante para a proliferação e diferenciação de células
93 73 mielóides (KRYSINSKA et al., 2007). Um grande número de genes codificando fatores de crescimento e receptores de fatores de crescimento tem sido localizados no braço longo do cromossomo 5 na região 5q23q33. Isso inclui IL-3, IL-5, IL-9 e GM-CSF. Análises moleculares detalhadas da anomalia 5q- têm demonstrado inversões submicroscópicas e duplicações adjacentes nesta região, assim como deleções ou mutações de c-fms (BARTRAM, 1996; CRESCENZI et al., 2004). Dessa forma, é provável que a perda desta região esteja diretamente envolvida com com desenvolvimento da doença. Devido à presença de citopenias graves, nossa paciente foi indicada para o TMO alogenêico. Atualmente 15 meses pós TMO, se encontra com 100% de quimerismo. Clones citogeneticamente não relacionados (alteração cromossômica biclonal) correspondem a um achado extremamente raro em doenças hemotólogicas. Em SMD, esta alteração tem sido descrita com uma freqüência de % (HAN et al, 2006). Em nosso estudo, foi observado um paciente com SMD hipocelular com a alteração cromossômica biclonal, envolvendo os cromossomos 17 e 11. A freqüência da alteração citogenética biclonal foi de 1,6%. Ainda não é claro, se clones citogeneticamente não relacionados indicam uma verdadeira biclonalidade da doença hematológica ou se é um resultado de uma evolução clonal de um precursor em comum. Nós acreditamos na hipótese de que clones não relacionados cariotipicamente se originam de um clone maligno comum através de mudanças moleculares submicroscópicas e processos de evolução. O clone com del(17p) adquiriu uma segunda alteração del(12p) sugerindo evolução da doença. Neste caso, a análise por FISH detectou a ausência dos alelos dos genes p53 e MLL, confirmado a deleção do braço curto do cromossomo 17 e a deleção do braço longo do cromossomo 11, respectivamente. O clone contendo a del(11q) estava presente em pequeno número, sendo visto em apenas 3 das 51 células analisadas, dessa forma a técnica de FISH foi fundamental para a confirmação desta alteração. As alterações mais freqüentes descritas envolvendo clones não relacionados foram:
94 74 del(5q), +8, del(20q), del(7q),+11, +21 e 22 (HAN et al, 2006). De acordo com uma revisão da literatura, este representa o primeiro caso de SMD pediátrica mostrando o envolvimento destas alterações cromossômicas em SMD hipocelular- CR. As alterações cromossômicas associadas à SMD são, na imensa maioria das vezes, detectadas pela citogenética clássica, mas há casos, em particular aqueles em que ocorre ausência de metáfases ou com clones pequenos, nos quais a anormalidade cromossômica não é identificada pela técnica de bandeamento G, mas diagnosticada por FISH. Já foi demonstrado que clones pequenos são mais bem detectados por citogenética molecular (FISH) (CHAUFFAILLE et al., 2006). Além disso, a análise por FISH auxilia na confirmação de alterações cromossômicas e estabelecimento de pontos de quebra. Pela técnica de FISH um grande número de células podem ser examinadas e alterações cromossômicas específicas podem ser detectadas, tanto em interfase quanto em metáfases. No entanto, esta técnica apresenta algumas limitações, uma dessas limitações envolve a incapacidade de detecção de anormalidades envolvendo regiões que não estejam na região da sonda (PANANI & ROUSSOS, 2005). Estudos estabelecendo vantagens e desvantagens da análise cariotípica clássica e FISH, sugerem que a combinação das duas metologias pode levar a um diagnóstico mais acurado (ROMEO et al, 2002). Aplicamos a metodologia da citogenética molecular-fish para afastar alterações cromossômicas de mau prognóstico, nos casos sem mitose ou quando o índice mitótico foi muito baixo, e para confirmação de alterações cromossômicas previamente identificadas pela citogenética clássica. Devido à importância da citogenética esta foi incorporada em escalas prognósticas. O Sistema Internacional de Escala Prognostica (IPSS) utiliza como variáveis prognósticas a porcentagem de blastos na medula óssea, as alterações citogenéticas e o número de citopenias para separar os pacientes em quatro grupos de risco. O IPSS tem mostrado grande valor
95 75 prognóstico para adultos com SMD. No entanto, alguns estudos sugerem que os fatores prognósticos que predizem a sobrevida ou progressão em adultos são de pouco valor para crianças (HASLE et al, 2004). Nós verificamos que dos 61 pacientes 33 (54%), foram classificados como intermediário 1, 12 (19,6%) intermediário 2 e 16 (26%) alto risco. Em um estudo japonês com crianças com SMD, a sobrevida diferiu entre os grupos de risco citogenético adotado pelo IPSS (SASAKI et al, 2001). Estudos encontraram uma tendência para uma sobrevida maior no grupo citogenético de risco intermediário (HASLE et al, 2004; PASSMORE et al., 2003). Nossos dados revelaram que pacientes classificados como intermediário 1, tiveram uma menor taxa de óbito. Não foram identificados pacientes de baixo risco. Este fato aconteceu devido a todos os nossos pacientes com CR apresentarem 2 citopenias (anemia e neutroponia; anemia e trombocitopenia; neutropenia e trombocitopenia), recebendo pontuação 0,5. Esta escala revelou que pacientes de alto risco apresentaram uma alta probabilidade de transformação leucêmica e alta taxa de óbito. Mesmo quando protocolos mais agressivos de tratamento foram utilizados, como TMO alogenêico, a resposta foi muito baixa. Várias estratégias terapêuticas vêm sendo utilizadas no tratamento para SMD da infância e LMMJ. Um estudo brasileiro revisando os tipos de tratamentos aplicados em crianças com SMD, verificou que as modalidades de tratamentos são muito heterogêneas não havendo um grupo cooperativo com protocolo específico (VALERA et al, 2004). Devido a SMD ser uma doença de célula tronco imatura, é considerada uma doença incurável quando terapias convencionais são utilizadas. Atualmente o TMO permanece como a única opção curativa para este grupo de pacientes, no entanto, para aquelas crianças que o TMO não é possível, outras modalidades terapêuticas como quimioterapia, fatores de crescimento e diversos outros agentes terapêuticos, são utilizados objetivando diminuir o número de citopenias.
96 76 Nosso estudo mostrou que a melhor opção de tratamento para crianças com SMD primária foi o TMO alogenêico. Entretanto, alguns pacientes apresentaram doença enxerto versus hospedeiro, comprometendo a qualidade de vida dessas crianças. Apesar do TMO alogênico ser o único tratamento atual que proporciona a cura, ele apresenta uma série de complicações. Dentre essas complicações podemos citar aquelas relacionadas com a recuperação da função medular, como um longo período de aplasia e o mais grave, a doença enxerto versus hospedeiro, que dependendo do grau de severidade pode levar à morte. Dessa forma é de extrema importância o conhecimento da biologia da SMD primária, na tentativa de elaborar novas formas de tratamento. Neste sentido, a identificação de alterações no padrão de metilação em genes supressores de tumor em SMD em adultos tornou possível o desenvolvimento e a utilização de protocolos de tratamento que utilizam agentes desmetilantes. Alguns grupos já demonstraram a freqüência e a importância da hipermetilação na região promotora de alguns genes como p15 INK4B e p16 INK4A, que estão envolvidos no controle do ciclo celular, e no gene CALCA (calcitonina) que está envolvido com a regulação dos níveis de cálcio no sangue em pacientes adultos com SMD. A freqüência de metilação do gene p15 INK4B em adultos com SMD ou leucemia aguda (LA) variou de 38% a 69% (UCHIDA et al., 1997; QUESNEL et al, 1998; HOFMANN et al, 2006), podendo ser verificada no diagnóstico ou durante a progressão da doença (TIEN et al, 2001). Entretanto, apenas dois estudos mostraram a presença de metilação em SMD primária na infância (HASEGAWA et al, 2005; VIDAL et al, 2006). Isso nos levou a investigar a presença de metilação na região promotora dos genes p15 INK4B e p16 INK4A em 45 crianças com SMD primária da infância, incluindo 25 do subtipo AR, 11 AREB, 7 AREB-t e 2 LMMJ pelo método MSP. Metilação em pelo menos um destes genes foi verificada em 40% (18/45) dos pacientes.
97 77 A freqüência de metilação no gene p15 INK4B nos nossos pacientes com SMD da infância foi de 35,5% (16/45). Hasegawa et al. (2005), em um estudo similar, apresentou uma freqüência superior de metilação neste gene (78%), esta diferença pode estar relacionada ao fato da maioria dos seus pacientes terem sido classificados dentro dos subtipos mais agressivos AREB e LMMC ou em um subtipo duvidoso entre SMD e LMA-M6, o qual ele denominou de AREB/M6. Outro estudo demonstrou uma freqüência de metilação em p15 INK4B de 50%, sendo também todos os pacientes classificados dentro dos subtipos AREB e AREB-t (VIDAL et al, 2006). Em nosso estudo as maiores freqüências de metilação para o gene p15 INK4B estiveram presentes nos subtipos mais agressivos de SMD como AREB, AREB-t e LMMJ, com as freqüências de 54,5% e 71,5% e 50% respectivamente. No subtipo menos agressivo da doença como CR, a freqüência de metilação foi mais baixa sendo observada em 16% dos pacientes. Hasegawa et al., em uma população de 18 pacientes classificados com LMMJ detectou metilação em apenas 17% dos casos. A metilação de vários genes tem sido associada a um pior prognóstico em pacientes com leucemia aguda (LA), como por exemplo, o gene da calcitonina em LLA (GARCIA- MANERO et al., 2002) e o gene MDR1 em LMA (GUARCIA-MANERO, 2003). No entanto, metilação no gene ER foi associada com um bom prognóstico em pacientes com LMA (TOYOTA et al., 2001). Em adultos com SMD, a metilação do gene p15 INK4B esteve associada com estágio agressivo da doença (AREB e AREB-t), sugerindo exercer um papel na progressão e evolução para LMA (UCHIDA et al., 1997; QUESNEL et al., 1998). Em SMD pediátrica tem sido verificada uma alta freqüência de metilação do gene p15 INK4B, no entanto, estes estudos não indicam se esta alteração está associada a bom ou mau prognóstico (HASEGAWA et al., 2005). Dos 45 pacientes estudados para o padrão de metilação 17 mostraram evolução da doença e 9 (53%) desses pacientes tiveram metilação em p15 INK4B. Os nossos dados mostraram que metilação do gene p15 INK4B provavelmente está envolvida no
98 78 processo de evolução da doença em direção à LMA, sugerindo que a proliferação de células leucêmicas pode requerer um escape da regulação da fase G1 do ciclo celular. A proteína codificada pelo gene p16 INK4A age também como um regulador negativo do ciclo celular, inibindo a ação das proteínas CDK4/6. Além disso, está associada ao processo de diferenciação celular e manutenção da homeostase durante a diferenciação da linhagens eritróides (MINAMI et al, 2003). Estudos têm demonstrado silenciamento deste gene por metilação em tumores sólidos, como carcinoma hepatocelular (FUKAI et al, 2005). No entanto, em malignidades hematológicas a freqüência de metilação neste gene é baixa ou nula (TOYOTA et al., 2001; GARCIA-MANERO et al., 2002; HASEGAWA et al., 2005; HOFMANN et al., 2006). Vidal et al. (2006) analisando o padrão de metilação de vários genes em SMD da infância, não detectou metilação no gene p16 em nenhum dos pacientes analisados. O mesmo resultado foi obtido por Hasegawa et al. (2005). Dos nossos 45 pacientes, apenas 4 (8,8%) apresentaram metilação neste gene. Todos os pacientes positivos para metilação no gene p16 INK4A estavam classificados dentro dos subtipos mais agressivos AREB e AREB-t. Dessa forma, concordando com os dados da literatura, nossos resultados mostraram uma baixa freqüência de metilação no gene p16 INK4A, sugerindo que provavelmente este não seja o principal evento envolvido na patogênese da SMD, tanto em adultos quanto em crianças. Metilação aberrante em ambos os genes foi vista em apenas 2 (4,4%) dos 45 pacientes analisados. Embora o número de pacientes seja pequeno, a metilação em ambos os genes p15 INK4B e p16 INK4A revelou ser um pior prognóstico para pacientes com SMD da infância, visto que os pacientes evoluíram da doença e foram a óbito. Em nosso trabalho estudamos a correlação entre a presença de uma alteração cromossômica específica com a metilação na região promotora dos genes p15 INK4B e p16 INK4A. Nossos resultados sugerem um forte associação envolvendo alterações no cromossomo 7
99 79 (-7/del7q) e metilação do gene p15 INK4B, levando à evolução da doença. Além disso, observamos associação entre a del(11)(q23) e alteração no padrão de metilação nos genes p15 INK4B e p16 INK4A, relacionados também com a evolução da doença. Não foi encontrada correlação entre alterações citogenéticas e presença de metilação em vários genes em pacientes adultos e crianças com malignidades hematológicas primárias (LLA, LMA e SMD) (GARCIA-MANERO et al., 2002). No entanto, Au et al.(2003) verificaram uma forte correlação entre metilação do gene p15 INK4B e alterações cromossômicas envolvendo o cromossomo 7 (-7/7q-) em pacientes adultos com SMD secundária. Dos nossos 16 pacientes positivos para a metilação no gene p15 INK4B, 7 (44%) possuíam alterações envolvendo o cromossomo 7, sugerindo que a metilação pode ser uma outra característica que confere a este grupo de pacientes um pior prognóstico. No entanto, um estudo com maior número de pacientes, é necessário para confirmar o nosso achado. Embora algumas das alterações citogenéticas estejam associadas a um pior prognóstico, as alterações moleculares envolvidas na iniciação e evolução desta doença permanecem desconhecidas. Alguns estudos levantam a seguinte questão: se alterações cromossômicas detectadas em SMD primária são eventos iniciais que levam ao desenvolvimento da doença (causa) ou se são apenas fenômenos secundários (conseqüencia) (CHAUFFAILLE, 2006). De acordo com a teoria de multíplas etapas, nossos resultados sugerem que as alterações cromossômicas são eventos intermediários, desencadeando uma grande instabilidade genética. A aquisição de alteração no padrão de metilação da região promotora dos genes p15 INK4B e p16 INK4A seria um evento mais tardio, associado com a transformação leucêmica. Seguindo este modelo uma provável via de evolução em SMD primária na infância seria a associação -7/del(7q) e metilação em p15 INK4B. Nossos resultados apresentam implicações potenciais para a classificação e prognóstico da SMD primária na infância. A detecção de metilação anormal em genes de pacientes com
100 80 SMD da infância pode ter um grande potencial como um fator prognóstico, podendo também ser utilizado na identificação de pacientes que podem ser beneficiados pelo tratamento com inibidores da metilação.
101 81 6. CONCLUSÕES A SMD primária na infância apresenta uma alta freqüência de alterações cromossômicas (72%); O estudo citogenético mostrou que o padrão cariotípico da SMD primária na infância é caracterizado principalmente por perdas parciais ou completas de cromossomos (deleções e monossomias) e ganhos cromossômicos (trissomias); As translocações cromossômicas são encontradas com uma menor freqüência; A análise citogenética mostrou ser essencial no processo de diagnóstico de todos os casos de suspeita de SMD pediátrica e foi uma importante ferramenta para a escolha do tratamento; As anomalias cromossômicas de maior freqüência neste estudo foram as alterações envolvendo o cromossomo 7 (-7/ 7q-), cariótipos complexos, del(11)(q23) e del(17)(p12); A metilação da região promotora do gene p15ink4b é um evento frequente em subtipos mais avançados da SMD primária na infância e está associada com a transformação leucêmica. A metilação na região promotora do gene p16ink4a é um evento raro em SMD primária na infância, estando possivelmente associada com a evolução da doença; A correlação entre o padrão de metilação em p15 INK4B e p16 INK4A e alterações cromossômicas específicas mostrou uma forte associação entre -7/7q- e metilação em p15 INK4B, sugerindo uma provável via de evolução da doença; As alterações cromossômicas, -7/7q-; +8 e del(11)(q23), e a presença de metilação em p15 INK4B e p16 INK4A estão associadas com mau prognóstico, sendo prováveis marcadores biológicos de evolução da doença.
102 82 7. REFERÊNCIAS BIBLIOGRÁFICAS Acar H, Çaliskan U, Kaynak M, Yildirim, Selman M., Largaespada David A. Hyperdiploid Karyotype in a childhood MDS patient. Clin. Lab. Haematol. 2001; 23: Adamson DJ, Dawson AA, Bennett B, King DJ, Haites NE. p53 mutation in the myelodysplastic syndromes. Br. J. Haematol. 1995; 89: Aggerholm A, Holm MS, Guldberg P, Olesen LH, Hokland P. Promoter hypermethylation of p15 INK4B, HIC1, CDH1, and ER is frequent in myelodysplastic syndrome and predicts poor prognosis in early-stage patients. Eur. J. Haematol. 2006; 76: Aktas D & Tuncbilek E. Myelodysplastic syndrom associated with monosomy 7 in childhood: a retrospective study. Cancer Genet. Cytogenet. 2006; 171: Arico M, Biondi A, Pui CH. Juvenile myelomonocytic leukemia. Blood.1997; 90: Atallah E, Kantarjian H, Garcia-Manero G. The role of decitabine in the treatment of myelodysplastic syndromes. Exp. O. Pharmac. 2007; 8: Au WY, Fung A, Man C, Ma SK, Wan TS, Liang R, Kwong YL. Aberrant p15 gene promoter methylation in therapy-related myelodysplastic syndrome and acute myeloide leukaemia: clinicophatological and karyotypic associations. Br. J. Haematol. 2003; 120: Aul C, Bowen DT, Yoshida Y. Pathogenesis, etiology and epidemiology of myelodysplastic syndromes. Haematologica, 1998; 83: Ballen KK, Haley NR, Kurtzberg J, Lane TA, Lindgren BR, Miller JP, Newman B, McCullough. Outcomes of 122 diverse adult and pediatric cord blood transplant recipients from a large cord blood bank. Transfusion. 2006; 46: Bartram CR. Molecular genetic aspect of myelodysplastic syndromes. Semin Hematol. 1996; 33: Bennett JM, Catovsky, D, Daniel, MT, Flandrin, G, Galton, DA, Gralnick, HR, Sultan, C. Proposals for the classification of the myelodysplastic syndromes. Br J Haematol 1982; 51:
103 Bennett JM. A comparative review of classification systems in myelodysplastic syndromes (MDS). Semin Oncol. 2005; 32: S Beverly JL, Kobrinsky N, Barnard DR, Arthur DC, Buckley JD, Howells WB, Gold S, Sanders J, Neudorf S, Smith FO, Woods WG. Distinctive Demography, Biology, and Outcome of Acute Myeloid Leukemia and Myelodysplastic Syndrome in children with Down Syndrome: children s cancer group studies 2861 and Blood. 1998; 2: Borgonovo T, Ribeiro EMSF, Cornélio DA, Schimid-Braz AT, Jamur VR, Wuicik L, Veiga LBA, Ehmke NAM, Pasquini R, Cavalli IJ. Cytogenetic study of Brazilian patients with myelodysplastic syndrome (MDS). Genetics and Molecular Biology. 2005; 28: Boudard D, Vasselon C, Bertheas MF, Jaubert J, Mounier C, Reynaud J, Viallet A, Chautard S, Guyotat D, Campos L. Expression and prognostic significance of Bcl-2 family proteins in myelodysplastic syndromes. Am J Hematol, 2002; 70: Brandwein JM, Horsman DE, Eaves AC, Eaves CJ, Massing BG, Wadsworth LD, Rogers PC, Kalousek DK. Childhood myelodysplasia: suggested classification as myelodysplastic syndrome based on laboratory and clinical findings. Am J Pediatr Oncol. 1990; 12: Brunstein CG, Baker KS, Wagner JE. Umbilical cord blood transplatation for myeloid malignancies. Curr Opin Hematol. 2007; 14: Campbell LJ & Garson OM. The prognostic significance of deletion of the long arm of chromosome 20 in myeloid disorders. Leukemia. 1994; 8: Chan GC, Wang WC, Raimondi SC, Behm FG, Krance RA, Chen G, Freiberg A, Ingram L, Butler D, Head DR. Myelodysplastic syndrome in children: differentiation from acute myeloid leukemia with a low blast count. Leukemia. 1997; 11: Chang F, Syrjanen CS, Tervahauta A, Syrjanen K. Tumorigenesis associated with the p53 tumor suppressor gene. Br. J. Cancer. 1993; 68: Chauffaille, MLLF. Alterações moleculares em síndrome mielodisplásica. Rev. Bras. Hematol. Hemoter. 2006; 28: Crescenzi B, La Starza R, Romoli S, Beacci D, Matteucci C, Barba G, Aventi A, Marynen P, Ciolli S, Nozzoli C, Martelli MF, Mecucci C. Submicroscopic deletions in 5q- associated malignancies. Haematologica. 2004; 89:
104 Delforge M. Understanding the pathogenesis of myelodysplastic syndromes. The Hematol. J., 2003; 4: Douglas EC, Look AT, Webber B, Parham D, Wilimas JA, Green AA, Roberson PK. Hyperdiploidy and chromosomal rearrangements define the aplastic variant of Wilm s tumor. J Clin Oncol. 1986; 4: Doney K, Leisenring W, Storb R, Appelbaum FR. Primary treatment of acquired aplastic anemia: Outcomes with bone marrow transplantation and immunosuppressive therapy. Annals Internal. Med. 1997; 126: Emanuel PD. Myelodysplastic and myeloproliferative disorders in childhood: an update. Br. J. Haematol. 1999; 105: Espigado I, Marín-Niebla A, Pérez-Hurtado JM, Ríos E, Carmona, Plaza E, Vaquero A, Campo T, Soto IP, Martino ML, Parody R, Rodríguez-Fernandez JM. Hemopoietic Stem Cell transplantation in Childhood: Reduction in Mortality and Improvement of Survival Over the Years. Transpl. Proceed. 2005; 37: Evans JP, Czepulkowski B, Gibbons B, Swansburry GJ, Chessells JM. Childhood monosomy 7 revisited. Br J Haematol. 1988; 69: Fernandez TS, Menezes, ds, Macedo Silva, ML, Tabak, D, Abdelhay, E. Correlation of N-ras point mutations with specific chromosomal abnormalities in primary myelodysplastic syndrome. Leuk Res 1998; 22: Fernandez TS, Abdelhay E, de Souza FT, Ornellas MH, Otero L, Tabak D. Chromosomal alterations associated with evolution from myelodysplastic syndrome to acute myeloid leukemia. Leuk. Res. 2000; 24: Fernandez TS, Ornellas MH, Tavares RC, Otero L, Diamond HR, Bouzas LF, Tabak D, Abdelhay. Hyperdiploid karyotype in a child with hypocelular primary myelodysplastic syndrome. Europ. J. Haematol. 2003; 71: Freinberg AP, Vogelstein B. Hypomethylation distinguishes gene of some human cancers from their normal counterparts. Nature, 1983; 301: Fukai K, Yokosuka O, Imazeki F, Tada M, Mikata R, Miyazaki M, Ochiai T, Saisho H. Methylation status of p14 ARF, p15 INK4B and p16 INK4A genes in human hepatocellular carcinoma. Liver Internat. 2005; 25:
105 Galm O, Herman JG, Baylin SB. The fundamental role of epigenetics in hematopoietic malignancies. Blood Reviews. 2006; 20: Garandeau C, Pautas, E, Andreux, M, Andreux, J, Gaussem, P, Siguret, V. Myelodysplastic syndromes. Ann. Biol. Clin. 2000; 58: Garcia-Manero G, Ramos-Bueso C, Daniel J, Williamson J, Kantarjian HM, Issa J J-P. DNA methylation patterns at relapse in adult acute lymphocytic leukemia. Clin. Cancer Res. 2002; 8: Garcia-Manero G. Methylation, aging, and pediatric acute lymphocytic leukemia. Leukemia. 2003; 17: Giles FJ, Stopeck, AT, Silverman, LR, Lancet, JE, Cooper, MA, Hannah, AL, Cherrington, JM, O'Farrell, AM, Yuen, HA, Louie, SG, Hong, W, Cortes, JE, Verstovsek, S, Albitar, M, O'Brien, SM, Kantarjian, HM, Karp, JE. SU5416, a small molecule tyrosine kinase receptor inhibitor, has biologic activity in patients with refractory acute myeloid leukemia or myelodysplastic syndromes. Blood. 2003; 102: Giralt S. Bone marrow transplant in myelodysplastic syndromes: new technologies, same questions. Curr Hematol Rep. 2005; 4: Greenberg P, Cox, C, LeBeau, MM, Fenaux, P, Morel, P, Sanz, G, Sanz, M, Vallespi, T, Hamblin, T, Oscier, D, Ohyashiki, K, Toyama, K, Aul, C, Mufti, G, Bennett, J. International scoring system for evaluating prognosis in myelodysplastic syndromes. Blood. 1997; 89: Gyger M, Bonny Y, Forest L. Childhood monosomy 7 syndrome. Am J Hematol. 1982; 13: Han JY, Theil KS, Hoeltge G. Frequencies and characterization of cytogenetically unrelated clones in various hematologic malignancies: seven years of experiences in a single institution. Cancer Genet. Cytogenet. 2006; 164: Harbott J, Haas OA, Kerndrup G, Michalová K, Sainati L, Slater R, Biondi A, Fenu S, Hasle H, Kühne T, Mann G, Stary J, Van Wering ER, Baumann I, Nöllke P, Rogge T, Zimmermann M, Niemeyer C. Cytogenetic evaluation of children with MDS and JMML. Results of the European working group of childhood MDS (EWOG-MDS). Leukemia. 2000;
106 Harris NL, Jaffe, ES, Diebold, J, Flandrin, G, Muller-Hermelink, HK, Vardiman, J, Lister, TA, Bloomfield, CD. The World Health Organization classification of hematological malignancies report of the Clinical Advisory Committee Meeting, Airlie House, Virginia, November Mod Pathol. 2000; 13: Hasegawa Dmanabe A, Kubota T, Kawasaki H, Hirose I, Ohtsuka Y, Tsuruta T, Ebihara Y, Goto Y, Zhao XY, Sakashita K, Koike K, Isomura M, Kojima S, Hoshika A, Tsuji K, Nakahata T. Methylation status of the p15 and p16 genes in paedriatric myelodysplastic syndrome and juvenile myelomonocytic leukaemia. Br. J. Haematol. 2005; 128: Hasle, Arico M, Basso G, Biondi A, Rajnoldi AC, Creutzig U, Fenu S, Fonotsch C, Haas OA, Harbott J, Kardos G, Kerndrup G, Mann G, Niemeyer CM et al. Myelodysplastic syndrome, Juvenile myelomonocytic leukemia, and acute myeloid leukemia associated with complete or partial monosomy 7. Leukemia. 1999; 13: Hasle H and Niemeyer. Myelodysplastic syndrome and juvenile myelomonocytic leukemia in children Hasle, H., Niemeyer, C. M., Chessels, j.m., Baumann, I., Bennett J.M, Kerndrup, G., Head, D.R. A pediatric approach to the WHO classification of myelodysplastic and myeloproliferative diseases. Leukemia. 2003; 17: Hasle H., Baumann I., Bergsträsser E., Fenu S., Fischer ª, Kardos G., Kerndrup G., Locatelli F., Rogge T., Schultz K.R., Stary J., Trebo M., Heuvel-Eibrink M.M.V.D., Harbott J., Nöllke P., Niemeyer C.M. The international prognostic scoring sytem (IPSS) for childhoold myelodysplastic syndrome (MDS) and juvenile myelomonocytic leukemia (JMML). Leukemia. 2004; 18: Head DR. Proposed changes in the definitions of acute myeloid leukemia and myelodysplastic syndrome: are they helpful? Curr Opin Oncol. 2002; 14: Hellström-Lindberg E., Willman C., Barrett A.J., Saunthararajah Y. Achievements in understanding and treatment of myelodysplastic syndromes. Hematology. 2000; Herman J, Graff JR, Myöhänen S, Nelkin BD, Baylin SB. Methylation-specific PCR: A novel PCR assay for methylation status of CpG islands. Proc. Natl. Acad. Sci. Medical Sciences. 1996; 93: Hutter JJJr, Hecht F, Kaiser-McCawB, Hays T, Barank P, Cohin J, Rurie B. Bone marrow monosomy 7: hematologic and clinical manifestations in childhood and adolescense. Hematol. Oncol. 1984; 2: 2-12
107 Hofmann W-K, Takeuchi S, Takeuchi N, Thiel E, Hoelzer D, Koeffler HP. Comparative analysis of hypermethylation of cell cycle control and DNA-mismatch repair genes in lowdensity and CD34+ bone marrow cells from patients with myelodysplastic syndrome. Leuk. Res. 2006; 30: Hungerford DA. Leukocytes cultured from small inocula of whole blood and the preparation of metaphase chromosomes by treatment with hypotonic KCl. Stain Technol 1965; 40: Ibrahim S, Estey EH, Pierce S, Glassman A, Keating M, O Brien S, Kantarjian HM, Albitar M. 11q23 abnormalities in patients with acute myelodysplastic syndrome as detected by molecular and cytogenetic analyses. Am J Clin. Pathol. 2000; 114: ISCN. An International System for Human Cytogenetic Nomeclature. Mitelman F, ed. Basel: S Karger, Janssen JW, Buschle, M, Layton, M, Drexler, HG, Lyons, J, van den, BH, Heimpel, H, Kubanek, B, Kleihauer, E, Mufti, GJ,. Clonal analysis of myelodysplastic syndromes: evidence of multipotent stem cell origin. Blood 1989; 73: Jekic B, Novakovic I, Lukovic L, Kuzmanovic M, Popovic B, Pastar I, Milasin J, Bunjevacki G, Bunjevacki V. Low frequency of N-ras and K-ras gene mutation in childhood myelodysplastic syndromes. Cancer Genet. Cytogenet. 2004; 154: Jekic B, Novakovic I, Lukovic L, Kuzmanovic M, Popovic B, Milasin J, Bunjevacki G, Damnjanovic T, Cvjeticanin S, Bunjevacki V. Lack of Tp53 and FMS gene mutations in children with myelodysplastic syndrome. Cancer Genet. Cytogenet. 2006; 166: Kardos G, Baumann I, Passmore J., Locatelli F., Hasle H., Schultz K.R., Stary J., Schmitt- Graeff A., Fischer A., Harbott J., Chessells J.M., Hann I., Fenu S., Rajnoldi A.C., Kerndrup G., Wering E.V.W, Rogge T., Nölke P., Niemeyer C.M. Refratory anemia in childhoold: a retrospective analysis of 67 patients with particular reference to monosomy 7. Blood. 2003; 102: Kikukawa M, Aoki N, Sakamoto Y, Mori M. Study of p53 in elderly patients with myelodysplastic syndromes by immunohistochemistry and DNA analisys. A. J. Pathol. 1999; 155: Krysinska H, Hoogenkamp M, Ingram R, Wilson N, Tagoh H, Laslo P, Singh H, Bonifer C. A two-step, PU.1-dependent mechanism for developmentally regulated chromatin remodeling and transcription of the c-fms gene. Mol Cell Biol. 2007; 27:
108 Kurzrock R, Albitar, M, Cortes, JE, Estey, EH, Faderl, SH, Garcia-Manero, G, Thomas, DA, Giles, FJ, Ryback, ME, Thibault, A, De Porre, P, Kantarjian, HM. Phase II study of R115777, a farnesyl transferase inhibitor, in myelodysplastic syndrome. J Clin Oncol. 2004; 22: Lai J-L, Preudhomme C, Zandecki M, Flactif M, Varumbeke M, Lepelley P. Myelodysplastic syndromes and acute myeloid leukemia with 17p deletion. An entity characterized by specific dysgranulopoiesis and high incidence of p53 mutations. Leukemia. 1995: Laird PW and Jaenisch R. The role of DNA methylation in cancer genetic and epigenetics. Annu Rev Genet. 1996; 30: Lees E. Cyclin dependent kinase regulation. Curr. Opin. Cell. Biol. 1995; 7: Lehmann U, Brakensiek K, Kreipe H. Role of epigenetic change in hematological malignancies. Ann Hematol. 2004: 83: List AF, Vardiman J, Issa J-PJ, Dewitte TM. Myelodysplastic syndromes. American Society of Hematology. 2004: Liu YC, Ito Y, Hsiao HH, Sashida G, Kodama A, Ohyashiki JH, Ohyshiki K. Risk factor analysis in myelodysplastic syndrome patients with del(20q): prognosis revisited. Cancer Genet. Cytogenet. 2006; 171: 9-16 Locatelli F, Zecca M, Pession A, Maserati E, De Stefano P, Severi F. Myelodysplastic Syndromes: the pediatric point view. Haematologica. 1995; 80: Look AT. Molecular Pathogenesis of MDS. Amer. Society Hematol. 2005; Lopes LF, Lorand-Metze I, Mendes WL, Seber A, Melo LN. Síndrome mielodisplásica na infância. Rev. Brasil. Hematol. Hemoterap. 2006; 28: Lorand-Metze I. Síndromes Mielodisplásicas. Conceito e Classificação. Diagnóstico. Evolução e Complicações. In: Hematologia: Fundamentos e Práticas. Editora Atheneu. Zago MA, 2005; Luna-Fineman S, Shanno KM, Atwater SK, Davis J, Masterson M, Ortega J, Sanders J, Steinherz P, Weinberg V, Lange BJ. Myelodysplastic and myeloproliferative disorders of childhood: a study of 167 patients. Blood.1999; 93:
109 Martinez-Climent JA. Molecular Cytogenetics of Childhoold hematolological malignancies. Leukemia. 1997; 11: Mathew S, Behm FG, Dalton J, Raimondi SC. Comparison of cytogenetics, southern blotting, and fluorescence in situ hybridization as methods for detecting MLL gene rearrangements in children with acute leukemia and with 11q23 abnormalities. Leukemia. 1999;13: Mhawech P& Saleem A. Myelodysplastic syndrome: review of the cytogenetic and molecular data. Clin. Rev. Oncology/Hematol. 2001; 40: Minami R, Muta K, Umemura T, Motomura S, Abe Y, Nishimura J, Nawata H. p16 INK4A induces differentiation and apoptosis in erythroid linage cells. Exp Hematol. 2003; 31: Mori N, Morosetti R, Hoflehner E, Lubbert M, Mizogichi H, Koeffler HP. Allelic Loss in the progression of myelodysplastic syndrome. Cancer Res. 2000; 60: Mundschau G, Gurbuxani S, Gamis AS, Greene ME, Arceci RJ, Crispino JD. Mutagenesis of GATA 1 is an initiating event in Down syndrome leukemogenesis. Blood. 2003; 101: Musto P. Thalidomide therapy for myelodysplastic syndromes: current status and future perspectives. Leuk Res. 2004; 28: Mufti GJ. Pathobiology, classification, and diagnosis of myelodysplastic syndrome. Best Practice & Research Clinical Haematology. 2004; 17: Nakamaki T, Bartram C, Seriu T, Kahan J, Fukuchi K, Tsuruoka N, et al. Molecular analysis of the cyclin-dependent kinase inhibitor genes, p15, p16, p18 and p19 in the myelodysplastic syndromes. Lek Res. 1997; 21: Niemeyer CM, Aricò M, Basso G, Cantù Rajnoldi A, Creutzig U, Haas OA, Harbott J, Hasle H, Kerndrup G, Locatelli F, Mann G, Stollmann-Gibbels B, van t Veer Korthof ET, van Wering ER, Zimmermann M. Chronic myelomonocytic leukemia in childhood: a retrospective analysis of 110 cases. European Working Group on Myelodysplastic Syndromes in Childhood (EWOG-MDS). Blood. 1997; 89: Niimi H, Harada LH, Harada Y, Ding Y, Imagawa J, Inaba T, Kyo T and Kimura A. Hyperactivation of the RAS signaling pathway in myelodysplastic syndrome with AML1/RUNX1 point mutations. Leukemia. 2006; 20:
110 Nishino HT & Chang C-C. Myelodysplastic Syndromes: Clinicophathologic features, phatobiology, and molecular pathogenesis. Arch Pathol Lab Med. 2005; 129: Nisse C, Haguenoer Jm, Grandbastien B, Preudhomme C,Fontaine B, Brillet JM. Occupational and enviromental risk factors of the myelodysplastic syndromes in the North of France. Br J Haematol 2001; 112: Nowell PC. Chromosome abnormalities in myelodysplastic syndromes. Semin Oncol. 1992; 19: Ogata K. Myelodysplastic Syndromes: Recent progress in diagnosis and understanding of their pathophysiology. J. Nippon Med Sch. 2006; 73: Panani AD & Roussos C. Cytogenetic aspects of adult primary myelodysplastic syndromes: Clinical implications. Cancer Letters. 2005; 235: Parker JE, Mufti, GJ, Rasool, F, Mijovic, A, Devereux, S, Pagliuca, A. The role of apoptosis, proliferation, and the Bcl-2-related proteins in the myelodysplastic syndromes and acute myeloid leukemia secondary to MDS. Blood. 2000; 96: Passmore SJ, Hann IM, Stiller CA, Ramani P, Swanbury GS, Gibbsons B, Reeves BR, Chessells JM. Peadiatric myelodysplastic: a study of 68 children and a new prognostic scoring system. Blood. 1995; 85: Passmore SJ, Cheessells JM, Kempski H, Hann JM, Brownbill PA, Stiller CA. Paediatric myelodysplastic syndromes and juvenila myelomonocytic leukemia in UK: a populationbased study of incidence and survival. Br J Haematol. 2003; 121: Perry ME & Levine, AJ. Tumor-suppressor p53 and the cell cycle. Curr Opin Genet Dev. 1993; 3: Pitman SD, Victorio A, Rowsell E, Morris J, Wang J. 5q- Syndrome in a child with slowly progressive pancytopenia. A case report and review of the literature. J Pediatrr Hematol Oncol. 2006; 28: Polychronopoulou S, Panagiotou JP, Kossiva L, Mavrou A, Anagnostou D, Haidas S. Clinical and morphological features of paediatric myelodysplastic syndromes: a review of 34 cases. Acta Paediatric. 2004; 93:
111 91 Pui CH. Childhood leukemias. N Engl J Med. 1995; 332: Quesnel B, Guillerm G, Vereecque R, Wattel E, Preudhomme, Bauters F, Vanrumbeke M, Fenaux P. methylation of the p15 INK4 gene in myelodysplastic syndromes is frequent and adquired during disease progression. Blood. 1998; 8: Rakyan VK, Preis J, Morgan HD, Whitelaw E. The marks, mechanisms and memory of epigenetics states in mammalian. Biochem J. 2001; 356: Raskind WH, Tirumali, N, Jacobson, R, Singer, J, Fialkow, PJ. Evidence for a multistep pathogenesis of a myelodysplastic syndrome. Blood. 1984; 63: Cotran RS, Kumar V, Collins T. Neoplasias. In: Robbins, Patologia Estrutural e Funcional. Guanabara Koogan. 6ª ed., p , Romeo M, Chauffaille ML, Silva MRR, Bahia DMM. Comparison of cytogenetics with FISH in 40 myelodysplastic syndrome patients. Leuk Res. 2002; 26: Rosenfeld C & List A. A hypothesis for the pathogenesis of myelodysplastic syndromes: implications for new therapies. Leukemia. 2000; 14. Santos, Cíntia Barros. Síndrome do X frágil e retardo mental Fraxe: distribuição dos alelos FRAXA e FRAXE em indivíduos portadores de retardo mental idiopático no Estado do Rio de Janeiro f. Tese (doutorado) Centro biomédico, Instituto de biologia Roberto Alcântara Gomes, Universidade do Estado do Rio de Janeiro, Rio de Janeiro, Sasaki H, Manabe A, Kojima S, Tsuchida M, Hayashi Y, Ikuta K, Okamura J, Koike K, Ohara A, Ishii E, Komada Y, Hibi S, Nakahata T. Myelodysplastic syndrome in childhood: a retrospective study of 189 patients in Japan. Leukemia. 2001; 15: Seabright M. A rapid banding technique for human chromosomes. Lancet 1971; 2: Side LE, Emanuel PD, Taylor B, Franklin J, Thompson P, Castleberry RP, Shannon KM. Mutations of the NF1 gene in children with juvenile myelomonocytic leukemia without clinical evidence of neurofibromatosis type 1. Blood. 1998; 92: Silverman LR & Mufti G. Methylation inhibitor therapy in the treatment of myelodysplastic syndrome. Nat Clin Pract Oncol. 2005; 2:
112 Sole F, Espinet, B, Sanz, GF, Cervera, J, Calasanz, MJ, Luno, E, Prieto, F, Granada, I, Hernandez, JM, Cigudosa, JC, Diez, JL, Bureo, E, Marques, ML, Arranz, E, Rios, R, Martinez Climent, JA, Vallespi, T, Florensa, L, Woessner, S. Incidence, characterization and prognostic significance of chromosomal abnormalities in 640 patients with primary myelodysplastic syndromes. Grupo Cooperativo Espanol de Citogenetica Hematologica. Br J Haematol 2000; 108: Strefford JC, Worley H, Barber K, Wright S, Stewart AR, et al. Genome complexity in acute lymphoblastic leukemia is revealed by array-based comparative genomic hybridization. Oncogene Teofili L, Martini M, Di Mario A, Rutella S, Urbano R, Luongo M, Leone G, Larocca LM. Expression of p15 INK4b gene during megakaryocytic differentiation of normal and myelodysplastic hemetopoietic progenitors. Blood. 2001; 98: Testa JR, Misawa, S, Oguma, N, Van Sloten, K, Wiernik, PH. Chromosomal alterations in acute leukemia patients studied with improved culture methods. Cancer Res. 1985; 45: Tien H-F, Tang J-L, Tsay W, Liu M-C, Lee F-Y, Wang C-H, Chen Y-C, Shen M-C. Methylation of the p15ink4b gene in myelodisplastic syndrome: it can be detected early or during disease progression and is highly associated with leukaemic transformation. Brit. J. Haematol. 2001; 112: Tomonaga M & Nagai K. Hypocellular Myelodysplastic Syndromes and Hypocellular Acute Myeloid Leukemia: Relationship to Aplastic Anemia. In: The Myelodysplastic Syndromes: Pathobiol. Clin Management ed. John M Bennett. 2002; Toyota M, Kopecky KJ, Toyota M-O Jair K-W, Willman CL, Issa J-P. Methylation profiling in acute myeloid leukemia. Blood. 2001; 97: Uchida T, Kinoshita T, Nagai H, Nakahara Y, Saito H, Hotta T, Murate T. Hypermethylation of the p15ink4b gene in myelodysplastic syndromes. Blood. 1997; Valera ET, Latorre MRD, Mandes WL, Seber A, Lee MLM, Paula MJA, Loggetto AR, Velloso E, Niero-Melo L, Lopes LF. Treatment of pediatric myelodysplastic syndromes and juvenile myelomonocytic leukemia: the Brazilian experience in the past decade. Leuk Res. 2004; 28: Vallespi T, Imbert M, Mecucci C, Preudhomme C, Fenaux, P. Diagnosis, classification, and cytogenetics of myelodysplastic syndromes. Haematologica. 1998; 83:
113 93 Van den Berghe H, Vernaelen K, Mecucci C, et al. The 5q- anomaly. Cancer Cytogenet. 1974; 17: Vidal OD, Paixão VA, Brait M, Souto EX, Caballero OL, Lopes LF, Vettore AL. Aberrant methylation in pediatric myelodysplastic syndrome. Leuk Res Wade PA. Methyl CpG binding proteins: coupling chromatin architecture to gene regulation. Oncogene. 2001; 20: Webb D.K.H., Passmore S.J., Hann I.M., Harrison G., Wheatley K., Chessells J.M. Results of treatment of children with refrectory anaemia with excess blasts (RAEB) and RAEB in transformation (RABE-t) in Great Britain Br J Haematol. 2001; 117: Weinhold B. Epigenetics: the science of change. Environ Health Perspect. 2006; 114:160-7 Wong KF & So CC. Hypoplastic Myelodysplastic Syndrome a Clinical, Morphologic, or Genetic Diagnosis? Cancer Genet Cytogenet. 2002; 138: Woods WG, Barnard DR, Alonzo TA, Buckley JD, Kobrinsky N, Arthur DC, Sanders J, Neudorf S, Gold S, Lange BJ. Prospective study of 90 children requiring treatment for juvenile myelomonocytic leukemia or myelodysplastic syndrome: a report from the children s cancer group. J Clin Oncol. 2002; 20: Wong R, Shahjahan, M, Wang, X, Thall, PF, De Lima, M, Khouri, I, Gajewski, J, Alamo, J, Couriel, D, Andersson, BS, Donato, M, Hosing, C, Komanduri, K, Anderlini, P, Molldrem, J, Ueno, NT, Estey, E, Ippoliti, C, Champlin, R, Giralt, S. Prognostic factors for outcomes of patients with refractory or relapsed acute myelogenous leukemia or myelodysplastic syndromes undergoing allogeneic progenitor cell transplantation. Biol Blood Marrow Transplant. 2005; 11: Worm J and Guldberg P. DNA methylation: an epigenetic pathway to cancer and a promising target for anticancer therapy. J Oral Pathol Med. 2002; 31: Young NS, Calado RT, Scheinberg P. Current concepts in the pathophysiology and treatment of aplastic anemia. Blood. 2006; 108: Yusuf U., Frangoul H.A., Gooley T.A., Woolfrey A.E., Carpenter P.A., Andrews R.G., Deeg H.J., Appelbaum F.R., Anasetti C., Storb R., Sanders J.E. Allogeneic bone marrow transplantation in children with myelodysplastic syndrome or juvenile myelomonocytic leukemia: the Seattle experience. Bone Marrow Transplant. 2004; 33:
114 94 8. ANEXOS 8.1 Anexo 1
115 95
116 96
117 97 TERMO DE CONSENTIMENTO INFORMADO E ESCLARECIDO A JUSTIFICATIVA A síndrome mielodisplásica (SMD) é considerada um estado pré-leucêmico, cerca de 10 a 40% dos casos evoluem para leucemia mielóide aguda (LMA). As causas principais de óbito estão associadas com infecções de repetição, devido à queda de glóbulos brancos; sangramentos, devido à queda de plaquetas; além da presença de cansaço, devido a anemia refratária (que não responde ao tratamento). Para estes pacientes é necessário transfusões sanguíneas periódicas. Atualmente é o transplante de medula óssea (TMO) que pode proporcionar a cura para um grupo de pacientes com faixa etária até 55 anos. Para o grupo de pacientes com idade superior aos 55 anos é oferecido tratamento com outros métodos (por exemplo: transfusões sanguíneas, uso de fatores de crescimento entre outros). Para os pacientes com SMD independente da idade é necessário a investigação diagnóstica, pois em alguns casos esta doença pode ser semelhante a anemia aplástica grave ou uma doença mieloproliferativa. Este diagnóstico é possível através de testes realizados no sangue e em amostras de medula óssea, utilizando modernas técnicas de citogenética e de biologia molecular. O emprego destas técnicas é fundamental no diagnóstico diferencial e é importante quanto à decisão do regime preparatório (quimioterapia e ou radioterapia) para o TMO. Além disso, alguns estudos relatam que os pacientes com SMD devem ser transplantados no início da doença, antes do aparecimento de células leucêmicas na medula óssea (diagnóstico precoce). Desta forma, a detecção de um pequeno número de células anormais caracterizado a nível citogenético e/ou molecular está relacionado a um curso clínico pós-transplante favorável. Estamos realizando este estudo para definir quais são os testes mais eficientes na identificação de marcadores citogenéticos e moleculares para um diagnóstico inicial e para a caracterização de estágios de transformação leucêmica. B DESCRIÇÃO DO PROGRAMA Este estudo propõe a análise das características citogenéticas e moleculares de amostras de medula óssea de pacientes e de doadores. Serão colhidas amostras de sangue e de medula óssea (mielograma) para realização dos testes. Ressaltamos que estas amostras são necessárias para todos os pacientes para auxiliar o diagnóstico. Não estaremos realizando nenhum procedimento adicional aos da rotina. Os pacientes serão submetidos a biópsia, sendo o material enviado para estudo no serviço de Patologia. As técnicas de coleta de material são as mesmas aplicadas na rotina do serviço. Os resultados obtidos serão relacionados com quadro clínico dos pacientes, afim de contribuir o para o diagnóstico e prognóstico do mesmo. C INFORMAÇÕES GERAIS As informações obtidas serão tratadas de forma confidencial e utilizadas para avaliação proposta bem como para o estabelecimento de um programa de melhoria na rotina de diagnóstico e definição do estágio da doença. Este é um benefício real para você e outros pacientes participantes do programa. Você não será identificado em nenhuma apresentação ou publicação. Não haverá qualquer ressarcimento pela participação no estudo. A qualquer momento o paciente e doador poderá desistir da participação, sem contudo apresentar prejuízo quanto ao seguimento do tratamento a ser realizado nesta instituição. Nos casos de necessidade de atendimento este será prestado, como habitualmente, na unidade de pacientes externos e internos das instituições Em caso de dúvidas quanto ao protocolo, o contato no Comitê de Ética em Pesquisa
118 98 Divisão de Assistência Médica TERMO DE CONSENTIMENTO INFORMADO Nome: Data de nascimento: Idade: Endereço: Bairro: Cidade: Estado: CEP: Telefone: Membro da equipe: Carimbo: Declaro que: - Entendo que estarei participando deste estudo conforme informações obtidas acima e com esclarecimento do médico. - Entendo que as amostras de sangue e medula óssea estarão sendo colhidas conforme o protocolo de rotina do serviço e que nenhum procedimento adicional será necessário para o estudo. - Entendo que não serei ressarcido por participar deste estudo. - Entendo que as informações obtidas serão confidenciais e em nenhuma publicação serei identificado. - Consinto que as informações sejam utilizadas para publicações e apresentações. - Consinto que as informações sejam utilizadas para um programa que beneficiará pacientes prè e pós-transplante de medula óssea com diagnóstico de Síndrome Mielodisplásica Primária. Em conseqüência aceito, nos termos acima, participar deste estudo: Data: Assinatura do Médico: Assinatura do Paciente: Em caso de Paciente menor de idade: Assinatura do responsável (legal): Testemunhas: 1) 2)
119 Anexo Cariótipos
120 Paciente 2, 13 anos, masculino, CR. Cariótipo:46,XY,del(17)(p12)/46,XY,del(17)(p12),del(12)(p13)/46,XY,del(11)(q23). 100
121 Paciente 3, 9 anos, masculino, CR. Cariótipo: 46,XY,del(3)(p23). 101
122 Paciente 5, 3 anos, masculino, CR. Cariótipo: 46,XY,+der(3)del(3)(q21),-7,-9,+mar. 102
123 Paciente 6, 13 anos, feminino, CR. Cariótipo: 46,XX,del(5)(q15q35). 103
124 Paciente 8, 14 anos, masculino, CR, Cariótipo: 46,XY,del(11)(q23). 104
125 Paciente 9, 7 anos, feminino, CR. Cariótipo: 46,XX,del(12)(p13). 105
126 Paciente 27, 14 anos, masculino, CR. Cariótipo: 46,XY,del(17)(p12). 106
127 Paciente 36, 17 meses, feminino, AREB. Cariótipo: 47,XX,der(17)t(1?;17)(q32?,p13),+21c. 107
128 Paciente 38, 2 anos, masculino, AREB. Cariótipo: 45,XY,
129 Paciente 39, 9 meses,masculino, AREB. Cariótipo: 46,XY,del(6)(q23). 109
130 Paciente 40, 5 anos, masculino, AREB. Cariótipo: 47,XY,
131 Paciente 42, 7 anos, feminino, AREB. Cariótipo: 46,XX,i(9)(q10). 111
132 Paciente 50, 2 anos, feminino, AREB-t. Cariótipo: 46,XX,t(4;7)(p16;p15). 112
133 Paciente 51, 4 anos, feminino, AREB-t. Cariotipo: 49,XX,dup(1)(q21q32),+6,+8,+mar. 113
134 Paciente 52, 1 anos, masculino, AREB-t. Cariótipo: 46,XY,inv(1)(q21),add(9)(q34). 114
135 Paciente 53, 10 anos, masculino, AREB-t. Cariótipo: 45,XY,
136 Paciente 56, 5 anos, masculino, AREB-t. Cariótipo: 46,XY,t(5;8)(q32;q22). 116
137 Paciente 58, 12 anos, masculino, AREB-t. Cariótipo: 58,XY,+8,+13,+13,+14,+15,+20,+21c,+21,+21,+21,+22,
138 Paciente 60, 21 meses, feminino, LMMJ. Cariótipo: 46,XX,inv(5)(q11q21),-9,+mar. 118
139 Paciente 61, 2 anos, masculino, LMMJ. Cariótipo: 47,XY,
140 Milhares de Livros para Download: Livros Grátis ( ) Baixar livros de Administração Baixar livros de Agronomia Baixar livros de Arquitetura Baixar livros de Artes Baixar livros de Astronomia Baixar livros de Biologia Geral Baixar livros de Ciência da Computação Baixar livros de Ciência da Informação Baixar livros de Ciência Política Baixar livros de Ciências da Saúde Baixar livros de Comunicação Baixar livros do Conselho Nacional de Educação - CNE Baixar livros de Defesa civil Baixar livros de Direito Baixar livros de Direitos humanos Baixar livros de Economia Baixar livros de Economia Doméstica Baixar livros de Educação Baixar livros de Educação - Trânsito Baixar livros de Educação Física Baixar livros de Engenharia Aeroespacial Baixar livros de Farmácia Baixar livros de Filosofia Baixar livros de Física Baixar livros de Geociências Baixar livros de Geografia Baixar livros de História Baixar livros de Línguas
141 Baixar livros de Literatura Baixar livros de Literatura de Cordel Baixar livros de Literatura Infantil Baixar livros de Matemática Baixar livros de Medicina Baixar livros de Medicina Veterinária Baixar livros de Meio Ambiente Baixar livros de Meteorologia Baixar Monografias e TCC Baixar livros Multidisciplinar Baixar livros de Música Baixar livros de Psicologia Baixar livros de Química Baixar livros de Saúde Coletiva Baixar livros de Serviço Social Baixar livros de Sociologia Baixar livros de Teologia Baixar livros de Trabalho Baixar livros de Turismo
- Condição adquirida caracterizada por alterações do crescimento e da diferenciação celular
 DISPLASIA: - Condição adquirida caracterizada por alterações do crescimento e da diferenciação celular Lesão celular reversível desencadeada por irritantes crônicos. Sua alteração pode acontecer na forma,
DISPLASIA: - Condição adquirida caracterizada por alterações do crescimento e da diferenciação celular Lesão celular reversível desencadeada por irritantes crônicos. Sua alteração pode acontecer na forma,
PROTOCOLOS DE TRATAMENTO DE DOENÇAS HEMATOLÓGICAS
 Fundação de Hematologia e Hemoterapia de Pernambuco - HEMOPE PROTOCOLOS DE TRATAMENTO DE DOENÇAS HEMATOLÓGICAS MIELODISPLASIA Versão 00/2015 EQUIPE DE ELABORAÇÃO Dra. Alessandra Ferraz de Sá Dra. Bruna
Fundação de Hematologia e Hemoterapia de Pernambuco - HEMOPE PROTOCOLOS DE TRATAMENTO DE DOENÇAS HEMATOLÓGICAS MIELODISPLASIA Versão 00/2015 EQUIPE DE ELABORAÇÃO Dra. Alessandra Ferraz de Sá Dra. Bruna
Alessandra Comparotto de Menezes IHOC-2013
 Alessandra Comparotto de Menezes IHOC-2013 DEFINIÇÃO: - Proliferação neoplásica clonal de uma linhagem de células do sistema hematopoético Representam um grupo heterogêneo de desordens hematopoéticas malignas
Alessandra Comparotto de Menezes IHOC-2013 DEFINIÇÃO: - Proliferação neoplásica clonal de uma linhagem de células do sistema hematopoético Representam um grupo heterogêneo de desordens hematopoéticas malignas
O Cancro - Aspectos gerais O termo Cancro é aplicado e utilizado genericamente para identificar um vasto conjunto de doenças que são os tumores malign
 presentes na Leucemia Daniela Bessa O Cancro - Aspectos gerais O termo Cancro é aplicado e utilizado genericamente para identificar um vasto conjunto de doenças que são os tumores malignos, também designamos
presentes na Leucemia Daniela Bessa O Cancro - Aspectos gerais O termo Cancro é aplicado e utilizado genericamente para identificar um vasto conjunto de doenças que são os tumores malignos, também designamos
BIOLOGIA MOLECULAR EM ENDOCRINOLOGIA
 BIOLOGIA MOLECULAR EM ENDOCRINOLOGIA Curso de Atualização em Endocrinologia 2017 Denise Pires de Carvalho Instituto de Biofísica Carlos Chagas Filho / UFRJ DNA Sequência de Nucleotídeos RNA Sequência de
BIOLOGIA MOLECULAR EM ENDOCRINOLOGIA Curso de Atualização em Endocrinologia 2017 Denise Pires de Carvalho Instituto de Biofísica Carlos Chagas Filho / UFRJ DNA Sequência de Nucleotídeos RNA Sequência de
Análises moleculares - DNA
 Análises moleculares - DNA Como o mapeamento genético contribui para a genética médica? A caracterização de um gene e suas mutações aumenta a compreensão da doença Aplicações: -Desenvolvimento de diagnóstico
Análises moleculares - DNA Como o mapeamento genético contribui para a genética médica? A caracterização de um gene e suas mutações aumenta a compreensão da doença Aplicações: -Desenvolvimento de diagnóstico
Eliane Ferreira Rodrigues
 Eliane Ferreira Rodrigues Estudo das Alterações Cromossômicas e Análise de Metilação nos Genes p15 INK4B e p16 INK4A em Síndrome Mielodisplásica Primária na Infância no Estado do Rio de Janeiro DISSERTAÇÃO
Eliane Ferreira Rodrigues Estudo das Alterações Cromossômicas e Análise de Metilação nos Genes p15 INK4B e p16 INK4A em Síndrome Mielodisplásica Primária na Infância no Estado do Rio de Janeiro DISSERTAÇÃO
PATOLOGIA DO SISTEMA HEMATOPOIÉTICO
 PATOLOGIA DO SISTEMA HEMATOPOIÉTICO Rafael Fighera Laboratório de Patologia Veterinária Hospital Veterinário Universitário Universidade Federal de Santa Maria INTRODUÇÃO AOS TUMORES HEMATOPOIÉTICOS Rafael
PATOLOGIA DO SISTEMA HEMATOPOIÉTICO Rafael Fighera Laboratório de Patologia Veterinária Hospital Veterinário Universitário Universidade Federal de Santa Maria INTRODUÇÃO AOS TUMORES HEMATOPOIÉTICOS Rafael
Investigação Laboratorial de LLA
 Investigação Laboratorial de LLA Ana Paula Fadel RESUMO A leucemia linfóide aguda (LLA) é a doença que ocorre principalmente na infância em crianças de 2 e 10 anos correspondendo a 70% dos casos; em adultos
Investigação Laboratorial de LLA Ana Paula Fadel RESUMO A leucemia linfóide aguda (LLA) é a doença que ocorre principalmente na infância em crianças de 2 e 10 anos correspondendo a 70% dos casos; em adultos
Leucemias Agudas: 2. Anemia: na leucemia há sempre anemia, então esperamos encontrar valores diminuídos de hemoglobina, hematócrito e eritrócitos.
 Leucemias Agudas: Leucemias são disfunções graves da hematopoese, consideradas neoplasias hematológicas, que resultam em grandes alterações na composição do sangue. Na maioria das leucemias, todo o hemograma
Leucemias Agudas: Leucemias são disfunções graves da hematopoese, consideradas neoplasias hematológicas, que resultam em grandes alterações na composição do sangue. Na maioria das leucemias, todo o hemograma
Obs. fase crônica (FC), fase acelerada (FA) e crise blástica (CB)
 P2 2018.1 Genética Médica Prof Isabela Arruda Gabarito: 1. A, 2A, 3.A, 4B, 5 D, 6.E, 7. C, 8A, 9A, 10 C 1. A leucemia mieloide crônica (LMC) é uma doença caracterizada pela perda progressiva da diferenciação
P2 2018.1 Genética Médica Prof Isabela Arruda Gabarito: 1. A, 2A, 3.A, 4B, 5 D, 6.E, 7. C, 8A, 9A, 10 C 1. A leucemia mieloide crônica (LMC) é uma doença caracterizada pela perda progressiva da diferenciação
BIOLOGIA MOLECULAR EM ENDOCRINOLOGIA. Denise Pires de Carvalho Instituto de Biofísica Carlos Chagas Filho / UFRJ
 BIOLOGIA MOLECULAR EM ENDOCRINOLOGIA Denise Pires de Carvalho Instituto de Biofísica Carlos Chagas Filho / UFRJ DNA Sequência de Nucleotídeos RNA Sequência de Nucleotídeos PROTEÍNA Sequência de Aminoácidos
BIOLOGIA MOLECULAR EM ENDOCRINOLOGIA Denise Pires de Carvalho Instituto de Biofísica Carlos Chagas Filho / UFRJ DNA Sequência de Nucleotídeos RNA Sequência de Nucleotídeos PROTEÍNA Sequência de Aminoácidos
Alterações cromossômicas em síndrome mielodisplásica Chromosomal abnormalities in myelodysplastic syndrome
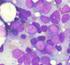 Rev. bras. hematol. hemoter. 2006;28(3):182-187 Chauffaille MLLF Artigo / Article Alterações cromossômicas em síndrome mielodisplásica Chromosomal abnormalities in myelodysplastic syndrome Maria de Lourdes
Rev. bras. hematol. hemoter. 2006;28(3):182-187 Chauffaille MLLF Artigo / Article Alterações cromossômicas em síndrome mielodisplásica Chromosomal abnormalities in myelodysplastic syndrome Maria de Lourdes
mielodisplasia doenças mieloproliferativas m i e l o f i b r o s e Crônicas : Policitemia Vera Agudas: LMC grânulo-megacariocítica
 Hemocentro Botucatu & Hospital Amaral Carvalho - Jaú Grupo Brasileiro -iatria UNESP Profª Drª Lígia Niero-Melo GB doenças mieloproliferativas Agudas: LMAs crise blástica de LMC mielodisplasia Crônicas
Hemocentro Botucatu & Hospital Amaral Carvalho - Jaú Grupo Brasileiro -iatria UNESP Profª Drª Lígia Niero-Melo GB doenças mieloproliferativas Agudas: LMAs crise blástica de LMC mielodisplasia Crônicas
2. METODOLOGIA 3. DIAGNÓSTICO LABORATORIAL
 4 1. INTRODUÇÃO A Leucemia Mielóide Crônica (LMC) possui uma incidência de 15% a 20% de todas as leucemias no adulto, equivalendo a 1,6 casos por 100 mil habitantes. Esta doença apresenta uma maior predominância
4 1. INTRODUÇÃO A Leucemia Mielóide Crônica (LMC) possui uma incidência de 15% a 20% de todas as leucemias no adulto, equivalendo a 1,6 casos por 100 mil habitantes. Esta doença apresenta uma maior predominância
ALTERAÇÕES MOLECULARES COMO CAUSA DE DOENÇAS GENÉTICAS. Profa. Dra. Vanessa Silveira
 ALTERAÇÕES MOLECULARES COMO CAUSA DE DOENÇAS GENÉTICAS Profa. Dra. Vanessa Silveira Genoma Humano - DNA Variações genéticas Alterações Erros de replicação do DNA Erros durante a divisão celular Agentes
ALTERAÇÕES MOLECULARES COMO CAUSA DE DOENÇAS GENÉTICAS Profa. Dra. Vanessa Silveira Genoma Humano - DNA Variações genéticas Alterações Erros de replicação do DNA Erros durante a divisão celular Agentes
SELEÇÃO DE MÉDICOS RESIDENTES PARA 2017 ÁREA DE ATUAÇÃO COM PRÉ-REQUISITO GABARITO
 SELEÇÃO DE MÉDICOS RESIDENTES PARA 2017 ÁREA DE ATUAÇÃO COM PRÉ-REQUISITO PROGRAMA:. PRÉ-REQUISITO: Hematologia e Hemoterapia. GABARITO QUESTÃO A B C D 1 2 3 4 5 6 7 8 9 10 Comissão de Residência Médica
SELEÇÃO DE MÉDICOS RESIDENTES PARA 2017 ÁREA DE ATUAÇÃO COM PRÉ-REQUISITO PROGRAMA:. PRÉ-REQUISITO: Hematologia e Hemoterapia. GABARITO QUESTÃO A B C D 1 2 3 4 5 6 7 8 9 10 Comissão de Residência Médica
13/08/2010. Marcos Fleury Laboratório de Hemoglobinas Faculdade de Farmácia UFRJ
 Diagnóstico Laboratorial das Neoplasias Hematológicas. Marcos Fleury Laboratório de Hemoglobinas Faculdade de Farmácia UFRJ Neoplasias Hematológicas. São doenças causadas pela proliferação descontrolada
Diagnóstico Laboratorial das Neoplasias Hematológicas. Marcos Fleury Laboratório de Hemoglobinas Faculdade de Farmácia UFRJ Neoplasias Hematológicas. São doenças causadas pela proliferação descontrolada
Curso de atualização à distância em SMD - organizado pelo GLAM
 Grupo Latino-Americano De SMD GLAM Curso de atualização à distância em SMD - organizado pelo GLAM O Grupo Latino-Americano em SMD (GLAM), como Associação Científica Sem Fins Lucrativos, desenvolveu um
Grupo Latino-Americano De SMD GLAM Curso de atualização à distância em SMD - organizado pelo GLAM O Grupo Latino-Americano em SMD (GLAM), como Associação Científica Sem Fins Lucrativos, desenvolveu um
Algoritmo para o tratamento das SMD de baixo risco. Teresa Cristina Bortolheiro Disciplina de Hematologia e Oncologia FCM Santa Casa de São Paulo
 Algoritmo para o tratamento das SMD de baixo risco ì Teresa Cristina Bortolheiro Disciplina de Hematologia e Oncologia FCM Santa Casa de São Paulo Antes de decidir o tratamento.. ì Diagnós)co adequado
Algoritmo para o tratamento das SMD de baixo risco ì Teresa Cristina Bortolheiro Disciplina de Hematologia e Oncologia FCM Santa Casa de São Paulo Antes de decidir o tratamento.. ì Diagnós)co adequado
φ Fleury Stem cell Mastócitos Mieloblastos Linfócito pequeno Natural Killer (Grande linfócito granular) Hemácias Linfócito T Linfócito B Megacariócito
 Hemopoese Marcos Fleury [email protected] Hematopoese É o processo de formação, maturação e liberação das células sanguíneas Eritropoese Leucopoese Trombopoese - Hemácias - Leucócitos - Plaquetas Tem como
Hemopoese Marcos Fleury [email protected] Hematopoese É o processo de formação, maturação e liberação das células sanguíneas Eritropoese Leucopoese Trombopoese - Hemácias - Leucócitos - Plaquetas Tem como
APLICAÇÕES ATUAIS DA CITOMETRIA DE FLUXO NA ROTINA LABORATORIAL
 APLICAÇÕES ATUAIS DA CITOMETRIA DE FLUXO NA ROTINA LABORATORIAL Citometria de fluxo uma ferramenta multidisciplinar guiada por hipótese Janossy G - Cytometry 2004 Profa Dra Irene Lorand-Metze Universidade
APLICAÇÕES ATUAIS DA CITOMETRIA DE FLUXO NA ROTINA LABORATORIAL Citometria de fluxo uma ferramenta multidisciplinar guiada por hipótese Janossy G - Cytometry 2004 Profa Dra Irene Lorand-Metze Universidade
Sibele Borsuk
 Mutações Sibele Borsuk [email protected] Mutações São alterações hereditárias do material genético de um organismo decorrente de erros de replicação antes da divisão celular e não causadas por recombinação.
Mutações Sibele Borsuk [email protected] Mutações São alterações hereditárias do material genético de um organismo decorrente de erros de replicação antes da divisão celular e não causadas por recombinação.
Transplante de medula óssea nas síndromes mielodisplásicas
 Tabak D.G. Artigo Especial / Special Article Transplante de medula óssea nas síndromes mielodisplásicas Daniel G. Tabak Cerca de 40% dos pacientes portadores de síndromes mielodisplásicas podem ser curados
Tabak D.G. Artigo Especial / Special Article Transplante de medula óssea nas síndromes mielodisplásicas Daniel G. Tabak Cerca de 40% dos pacientes portadores de síndromes mielodisplásicas podem ser curados
Resposta imune adquirida do tipo celular
 Universidade Federal do Pampa Campus Itaqui Curso de Nutrição Imunologia Resposta imune adquirida do tipo celular Profa. Dra. Silvana Boeira Imunidade adquirida Imunidade adaptativa = específica = adquirida
Universidade Federal do Pampa Campus Itaqui Curso de Nutrição Imunologia Resposta imune adquirida do tipo celular Profa. Dra. Silvana Boeira Imunidade adquirida Imunidade adaptativa = específica = adquirida
Fundamentos da Citometria de Fluxo. Elizabeth Xisto Souto
 Fundamentos da Citometria de Fluxo Elizabeth Xisto Souto A Citometria de Fluxo consiste de tecnologia laser que analisa partículas suspensas em meio líquido e fluxo contínuo. Estas partículas podem ser
Fundamentos da Citometria de Fluxo Elizabeth Xisto Souto A Citometria de Fluxo consiste de tecnologia laser que analisa partículas suspensas em meio líquido e fluxo contínuo. Estas partículas podem ser
Responda às perguntas seguintes usando exclusivamente o glossário.
 Responda às perguntas seguintes usando exclusivamente o glossário. 1 - Um homem de 50 anos com queixas de fadiga muito acentuada fez um exame médico completo que incluiu RX do tórax. Identificaram-se lesões
Responda às perguntas seguintes usando exclusivamente o glossário. 1 - Um homem de 50 anos com queixas de fadiga muito acentuada fez um exame médico completo que incluiu RX do tórax. Identificaram-se lesões
Carcinogêse e Neoplasia. Profº Ary da Silveira Mendes Jr.
 Carcinogêse e Neoplasia Profº Ary da Silveira Mendes Jr. Epidemiologia Principal causa de morte entre 45-60 anos Incidência no Brasil em 2003 (INCA) 126.290 mortes 402.190 casos novos DOENÇA GENÉTICA Padrão
Carcinogêse e Neoplasia Profº Ary da Silveira Mendes Jr. Epidemiologia Principal causa de morte entre 45-60 anos Incidência no Brasil em 2003 (INCA) 126.290 mortes 402.190 casos novos DOENÇA GENÉTICA Padrão
Requisitos básicos. Nas regiões hematopoéticas, 50% do tecido medular é representado por gordura. O tecido hematopoético pode ocupar áreas de gordura.
 Hematopoese Requisitos básicos. 1. Stem cells (células tronco hematopoéticas). 2. Meio ambiente medular (fibroblastos, macrófagos e células endoteliais). 3. Fatores de crescimento (GM-CSF, Eritropoietina...)
Hematopoese Requisitos básicos. 1. Stem cells (células tronco hematopoéticas). 2. Meio ambiente medular (fibroblastos, macrófagos e células endoteliais). 3. Fatores de crescimento (GM-CSF, Eritropoietina...)
CYNTHIA DE ASSUMPÇÃO LUCIDI 1 ; FLÁVIA FERNANDES DE MENDONÇA UCHÔA 2
 Trabalho apresentado na 8ª Conferência Sul-Americana de Medicina Veterinária SÍNDROME MIELODISPLÁSICA ERITRÓIDE PREDOMINANTE COMO DIAGNÓSTICO DIFERENCIAL DE CITOPENIAS PERSISTENTES EM QUATRO CÃES CYNTHIA
Trabalho apresentado na 8ª Conferência Sul-Americana de Medicina Veterinária SÍNDROME MIELODISPLÁSICA ERITRÓIDE PREDOMINANTE COMO DIAGNÓSTICO DIFERENCIAL DE CITOPENIAS PERSISTENTES EM QUATRO CÃES CYNTHIA
Introdução à Bioquímica
 Introdução à Bioquímica Nucleotídeos e Ácidos Nucléicos Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física.. UNESP São José do Rio Preto - SP. Genoma! O genoma de um organismo
Introdução à Bioquímica Nucleotídeos e Ácidos Nucléicos Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física.. UNESP São José do Rio Preto - SP. Genoma! O genoma de um organismo
CLASSIFICAÇÃO DAS LEUCEMIAS
 CLASSIFICAÇÃO DAS LEUCEMIAS Prof. Rafael Fighera Laboratório de Patologia Veterinária Hospital Veterinário Universitário Universidade Federal de Santa Maria Classificação das leucemias Por que classificar
CLASSIFICAÇÃO DAS LEUCEMIAS Prof. Rafael Fighera Laboratório de Patologia Veterinária Hospital Veterinário Universitário Universidade Federal de Santa Maria Classificação das leucemias Por que classificar
Imunidade adaptativa celular
 Universidade de São Paulo Faculdade de Medicina de Ribeirão Preto Pós-graduação em Imunologia Básica e Aplicada Disciplina RIM 5757 Integração Imunologia Básica-Clínica Imunidade adaptativa celular Cássia
Universidade de São Paulo Faculdade de Medicina de Ribeirão Preto Pós-graduação em Imunologia Básica e Aplicada Disciplina RIM 5757 Integração Imunologia Básica-Clínica Imunidade adaptativa celular Cássia
MicroRNAs: nova classe de reguladores gênicos envolvidos na função endócrina e câncer
 FACULDADE DE MEDICINA DE SÃO JOSÉ DO RIO PRETO Novas tecnologias de biologia molecular no câncer MicroRNAs: nova classe de reguladores gênicos envolvidos na função endócrina e câncer Filho J.C.M Ricarte,
FACULDADE DE MEDICINA DE SÃO JOSÉ DO RIO PRETO Novas tecnologias de biologia molecular no câncer MicroRNAs: nova classe de reguladores gênicos envolvidos na função endócrina e câncer Filho J.C.M Ricarte,
BIOLOGIA. Hereditariedade e Diversidade da Vida Mutações e alterações cromossômicas. Prof. Daniele Duó
 BIOLOGIA Hereditariedade e Diversidade da Vida Mutações e alterações cromossômicas Prof. Daniele Duó - As mutações são espontâneas e podem ser silenciosas, em alguns casos, podem ainda ser letais, ou ainda
BIOLOGIA Hereditariedade e Diversidade da Vida Mutações e alterações cromossômicas Prof. Daniele Duó - As mutações são espontâneas e podem ser silenciosas, em alguns casos, podem ainda ser letais, ou ainda
Técnicas utilizadas para estudo citogenético clínico. Prof. Dr. Bruno Lazzari de Lima
 Técnicas utilizadas para estudo citogenético clínico Prof. Dr. Bruno Lazzari de Lima Citogenética Clínica Estudo do cromossomo aplicado à prática da genética médica. 40 anos atrás Distúrbios cromossômicos
Técnicas utilizadas para estudo citogenético clínico Prof. Dr. Bruno Lazzari de Lima Citogenética Clínica Estudo do cromossomo aplicado à prática da genética médica. 40 anos atrás Distúrbios cromossômicos
CARACTERÍSTICAS DA LEUCEMIA MIELOIDE CRÔNICA, COM ENFASE NO DIAGNÓSTICO E TRATAMENTO
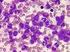 CARACTERÍSTICAS DA LEUCEMIA MIELOIDE CRÔNICA, COM ENFASE NO DIAGNÓSTICO E TRATAMENTO Danilo Alves da Silva¹; Clarice Silva Sales¹; Zacarias Guilherme dos Santos Junior¹; Bartolomeu Garcia de Souza Medeiros
CARACTERÍSTICAS DA LEUCEMIA MIELOIDE CRÔNICA, COM ENFASE NO DIAGNÓSTICO E TRATAMENTO Danilo Alves da Silva¹; Clarice Silva Sales¹; Zacarias Guilherme dos Santos Junior¹; Bartolomeu Garcia de Souza Medeiros
SÍNDROMES MIELODISPLÁSICAS. Hye, 2014
 SÍNDROMES MIELODISPLÁSICAS Hye, 2014 DEFINIÇÃO Trata se de um grupo de diversas desordens da medula óssea que leva o indivíduo não produzir células sanguíneas saudáveis em número suficiente. SINTOMATOLOGIA
SÍNDROMES MIELODISPLÁSICAS Hye, 2014 DEFINIÇÃO Trata se de um grupo de diversas desordens da medula óssea que leva o indivíduo não produzir células sanguíneas saudáveis em número suficiente. SINTOMATOLOGIA
Fases do Ciclo Celular
 Ciclo Celular Fases do Ciclo Celular Todas as células passam por um ciclo de vida que, assim como a vida de um organismo complexo, apresenta diferentes fases e é irreversível. Duração do ciclo celular
Ciclo Celular Fases do Ciclo Celular Todas as células passam por um ciclo de vida que, assim como a vida de um organismo complexo, apresenta diferentes fases e é irreversível. Duração do ciclo celular
PCR Reação de Polimerase em Cadeia. Termociclador
 PCR Reação de Polimerase em Cadeia Termociclador REAÇÃO EM CADEIA DA POLIMERASE (PCR) Técnica que permite a amplificação da quantidade de DNA específico utilizando a enzima Taq DNA polimerase, sequências
PCR Reação de Polimerase em Cadeia Termociclador REAÇÃO EM CADEIA DA POLIMERASE (PCR) Técnica que permite a amplificação da quantidade de DNA específico utilizando a enzima Taq DNA polimerase, sequências
Análises de DNA. O DNA e sua história. DNA nos remete a Hereditariedade. -Hipócrates ( a.c.): pangênese
 Análises de DNA O DNA e sua história DNA nos remete a Hereditariedade -Hipócrates (460-377 a.c.): pangênese -Aristóteles (384-322 a.c.): transmissão das características pelo sêmen 1 O genoma e sua história
Análises de DNA O DNA e sua história DNA nos remete a Hereditariedade -Hipócrates (460-377 a.c.): pangênese -Aristóteles (384-322 a.c.): transmissão das características pelo sêmen 1 O genoma e sua história
O CONTROLE DO CICLO CELULAR / PROLIFERAÇÃO EM CÂNCER: CONCEITOS E POTENCIAIS APLICAÇÕES TERAPÊUTICAS
 Universidade Federal do Rio Grande do Sul Laboratório de Sinalização e Plasticidade Celular O CONTROLE DO CICLO CELULAR / PROLIFERAÇÃO EM CÂNCER: CONCEITOS E POTENCIAIS APLICAÇÕES TERAPÊUTICAS Msc. Eduardo
Universidade Federal do Rio Grande do Sul Laboratório de Sinalização e Plasticidade Celular O CONTROLE DO CICLO CELULAR / PROLIFERAÇÃO EM CÂNCER: CONCEITOS E POTENCIAIS APLICAÇÕES TERAPÊUTICAS Msc. Eduardo
IMPORTÂNCIA DA GENÉTICA PARA ÁREA DA SAÚDE: Diagnóstico clínico: alteração no número ou estrutura dos cromossomos (síndrome de Down)
 Aplicações: IMPORTÂNCIA DA GENÉTICA PARA ÁREA DA SAÚDE: Diagnóstico clínico: alteração no número ou estrutura dos cromossomos (síndrome de Down) Mapeamento genético e identificação: mapeamento de genes
Aplicações: IMPORTÂNCIA DA GENÉTICA PARA ÁREA DA SAÚDE: Diagnóstico clínico: alteração no número ou estrutura dos cromossomos (síndrome de Down) Mapeamento genético e identificação: mapeamento de genes
Prof. Dr. Bruno Lazzari de Lima. Genes e Câncer
 Prof. Dr. Bruno Lazzari de Lima Genes e Câncer O que é câncer? Diferente de doenças cromossômicas, monogênicas e multifatoriais. Presente em todas as células do organismo inclusive gametas. Doenças genéticas
Prof. Dr. Bruno Lazzari de Lima Genes e Câncer O que é câncer? Diferente de doenças cromossômicas, monogênicas e multifatoriais. Presente em todas as células do organismo inclusive gametas. Doenças genéticas
GABARITO RESIDÊNCIA MÉDICA R1-2017
 RESIDÊNCIA MÉDICA R1-2017 1 D 21 D 41 C 61 A 81 B 2 A 22 A 42 A 62 A 82 C 3 B 23 B 43 C 63 C 83 A 4 B 24 C 44 D 64 D 84 B 5 C 25 A 45 B 65 A 85 C 6 C 26 D 46 C 66 A 86 D 7 B 27 C 47 A 67 C 87 D 8 C 28
RESIDÊNCIA MÉDICA R1-2017 1 D 21 D 41 C 61 A 81 B 2 A 22 A 42 A 62 A 82 C 3 B 23 B 43 C 63 C 83 A 4 B 24 C 44 D 64 D 84 B 5 C 25 A 45 B 65 A 85 C 6 C 26 D 46 C 66 A 86 D 7 B 27 C 47 A 67 C 87 D 8 C 28
INSTABILIDADE DO GENOMA HUMANO INSTABILIDADE CROMOSSÔMICA
 INSTABILIDADE DO GENOMA HUMANO INSTABILIDADE CROMOSSÔMICA Genética Molecular - IBM1027 Profa. Dra. Vanessa Silveira 1. Definição Fenótipo celular onde vários processos responsáveis pela manutenção e replicação
INSTABILIDADE DO GENOMA HUMANO INSTABILIDADE CROMOSSÔMICA Genética Molecular - IBM1027 Profa. Dra. Vanessa Silveira 1. Definição Fenótipo celular onde vários processos responsáveis pela manutenção e replicação
Universidade Estadual de Maringá. Curso de Especialização em Biotecnologia e Bioprocessos Ementa e Programa das disciplinas
 Ementa e Programa das disciplinas Iniciação à Pesquisa Fundamentos teóricos da produção do conhecimento científico como instrumento para a análise e desenvolvimento de estudos na área de biotecnologia.
Ementa e Programa das disciplinas Iniciação à Pesquisa Fundamentos teóricos da produção do conhecimento científico como instrumento para a análise e desenvolvimento de estudos na área de biotecnologia.
Módulo 1: Citogenética, Genética Molecular e Epigenética: atualização de conceitos básicos
 O I Curso de Pós-Graduação e Actualização em Genética Laboratorial" organizado pela Secção Regional do Norte da Ordem dos Farmacêuticos é composto por 3 módulo, o primeiro dos quais iniciar-se-á no mês
O I Curso de Pós-Graduação e Actualização em Genética Laboratorial" organizado pela Secção Regional do Norte da Ordem dos Farmacêuticos é composto por 3 módulo, o primeiro dos quais iniciar-se-á no mês
DNA recombinante. Nilce M. Martinez Rossi Depto de Genética
 DNA recombinante Nilce M. Martinez Rossi Depto de Genética Descobertas marcantes 1962 Arber, Nathans e Smith Enzimas de restrição 1966 Niremberg, Ochoa e Khorana Elucidaram o código genético 1961 Marmur
DNA recombinante Nilce M. Martinez Rossi Depto de Genética Descobertas marcantes 1962 Arber, Nathans e Smith Enzimas de restrição 1966 Niremberg, Ochoa e Khorana Elucidaram o código genético 1961 Marmur
TÍTULO: MONITORAMENTO DE DOENÇA RESIDUAL MÍNIMA PÓS TRANSPLANTE DE MEDULA ÓSSEA EM PACIENTES COM LEUCEMIA LINFOIDE AGUDA
 16 TÍTULO: MONITORAMENTO DE DOENÇA RESIDUAL MÍNIMA PÓS TRANSPLANTE DE MEDULA ÓSSEA EM PACIENTES COM LEUCEMIA LINFOIDE AGUDA CATEGORIA: CONCLUÍDO ÁREA: CIÊNCIAS BIOLÓGICAS E SAÚDE SUBÁREA: BIOMEDICINA INSTITUIÇÃO:
16 TÍTULO: MONITORAMENTO DE DOENÇA RESIDUAL MÍNIMA PÓS TRANSPLANTE DE MEDULA ÓSSEA EM PACIENTES COM LEUCEMIA LINFOIDE AGUDA CATEGORIA: CONCLUÍDO ÁREA: CIÊNCIAS BIOLÓGICAS E SAÚDE SUBÁREA: BIOMEDICINA INSTITUIÇÃO:
RELATÓRIO DE AVALIAÇÃO PRÉVIA DE MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DE MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI AZACITIDINA Medicamento PVH PVH com IVA Titular de AIM VIDAZA Embalagem de 1 frasco para injectáveis, de pó para suspensão
RELATÓRIO DE AVALIAÇÃO PRÉVIA DE MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI AZACITIDINA Medicamento PVH PVH com IVA Titular de AIM VIDAZA Embalagem de 1 frasco para injectáveis, de pó para suspensão
BIBLIOTECAS DE DNA E HIBRIDIZAÇÃO. FABIANA SEIXAS
 BIBLIOTECAS DE DNA E HIBRIDIZAÇÃO FABIANA SEIXAS email: [email protected] ABORDAGENS... BIBLIOTECAS DE DNA -Bibliotecas de DNA Genômico -Bibliotecas de cdna TÉCNICAS DE HIBIDIZAÇÃO -Hibidização em
BIBLIOTECAS DE DNA E HIBRIDIZAÇÃO FABIANA SEIXAS email: [email protected] ABORDAGENS... BIBLIOTECAS DE DNA -Bibliotecas de DNA Genômico -Bibliotecas de cdna TÉCNICAS DE HIBIDIZAÇÃO -Hibidização em
Aspectos gerais da estrutura celular
 Ciclo celular Aspectos gerais da estrutura celular A célula é a unidade básica da vida Altamente organizada, dividida em compartimentos As células surgem de outras células préexistentes As células são
Ciclo celular Aspectos gerais da estrutura celular A célula é a unidade básica da vida Altamente organizada, dividida em compartimentos As células surgem de outras células préexistentes As células são
1.3 Explique a razão pela qual, na ausência de lactose, as enzimas necessárias à degradação desta molécula não se produzem.
 A g r u p a m e n t o d e E s c o l a s A n t ó n i o S é r g i o - V. N. Gaia E S C O L A S E C U N D Á R I A / 3 A N T Ó N I O S É R G I O BIOLOGIA Módulo 2 12º CTec CURSO CIENTÍFICO-HUMANÍSTICO DE CIÊNCIAS
A g r u p a m e n t o d e E s c o l a s A n t ó n i o S é r g i o - V. N. Gaia E S C O L A S E C U N D Á R I A / 3 A N T Ó N I O S É R G I O BIOLOGIA Módulo 2 12º CTec CURSO CIENTÍFICO-HUMANÍSTICO DE CIÊNCIAS
ENFERMAGEM. DOENÇAS HEMATOLÓGICAS Parte 2. Profª. Tatiane da Silva Campos
 ENFERMAGEM DOENÇAS HEMATOLÓGICAS Parte 2 Profª. Tatiane da Silva Campos ALTERAÇÕES DA COAGULAÇÃO Púrpuras (Trombocitopênica Imunológica): doença adquirida; os anticorpos destroem as plaquetas. Sintomas:
ENFERMAGEM DOENÇAS HEMATOLÓGICAS Parte 2 Profª. Tatiane da Silva Campos ALTERAÇÕES DA COAGULAÇÃO Púrpuras (Trombocitopênica Imunológica): doença adquirida; os anticorpos destroem as plaquetas. Sintomas:
Paula Curi de Freitas
 Paula Curi de Freitas Análise de Alterações Cromossômicas, Mutações no Éxon 1 e do Padrão de Metilação da Região Promotora do Gene FOXO3 em Síndrome Mielodisplásica São José do Rio Preto 2015 Paula Curi
Paula Curi de Freitas Análise de Alterações Cromossômicas, Mutações no Éxon 1 e do Padrão de Metilação da Região Promotora do Gene FOXO3 em Síndrome Mielodisplásica São José do Rio Preto 2015 Paula Curi
PROTOCOLOS DE TRATAMENTO DE DOENÇAS HEMATOLÓGICAS
 Fundação de Hematologia e Hemoterapia de Pernambuco - HEMOPE PROTOCOLOS DE TRATAMENTO DE DOENÇAS HEMATOLÓGICAS LEUCEMIA LINFOCÍTICA CRÔNICA Versão 00/2015 ELABORAÇÃO Dra. Renata Lygia Vieira Vasconcelos
Fundação de Hematologia e Hemoterapia de Pernambuco - HEMOPE PROTOCOLOS DE TRATAMENTO DE DOENÇAS HEMATOLÓGICAS LEUCEMIA LINFOCÍTICA CRÔNICA Versão 00/2015 ELABORAÇÃO Dra. Renata Lygia Vieira Vasconcelos
TERAPIAS MOLECULARES CONTRA O CÂNCER
 TERAPIAS MOLECULARES CONTRA O CÂNCER Paulo Cesar Naoum Pós-Doutorado pela Cambridge University, Inglaterra, e Professor Titular pela Unesp. Diretor da Academia de Ciência e Tecnologia de São José do Rio
TERAPIAS MOLECULARES CONTRA O CÂNCER Paulo Cesar Naoum Pós-Doutorado pela Cambridge University, Inglaterra, e Professor Titular pela Unesp. Diretor da Academia de Ciência e Tecnologia de São José do Rio
LOCAL: CENTRO DE EDUCAÇÃO EM SAÚDE ABRAM SZAJMAN (CESAS) BLOCO A 1ºSS 26 DE JUNHO DE 2018, TERÇA-FEIRA
 Programação Preliminar LOCAL: CENTRO DE EDUCAÇÃO EM SAÚDE ABRAM SZAJMAN (CESAS) BLOCO A 1ºSS 26 DE JUNHO DE 2018, TERÇA-FEIRA I SIMPÓSIO MULTIDISCIPLINAR EM ONCOLOGIA PEDIÁTRICA *Atividade simultânea ao
Programação Preliminar LOCAL: CENTRO DE EDUCAÇÃO EM SAÚDE ABRAM SZAJMAN (CESAS) BLOCO A 1ºSS 26 DE JUNHO DE 2018, TERÇA-FEIRA I SIMPÓSIO MULTIDISCIPLINAR EM ONCOLOGIA PEDIÁTRICA *Atividade simultânea ao
Diagnóstico Laboratorial em Hematologia. Marcos K. Fleury Laboratório de Hemoglobinas Faculdade de Farmácia - UFRJ
 Diagnóstico Laboratorial em Hematologia Marcos K. Fleury Laboratório de Hemoglobinas Faculdade de Farmácia - UFRJ [email protected] Anemia É definida como uma diminuição de hemoglobina e ou hemácias no
Diagnóstico Laboratorial em Hematologia Marcos K. Fleury Laboratório de Hemoglobinas Faculdade de Farmácia - UFRJ [email protected] Anemia É definida como uma diminuição de hemoglobina e ou hemácias no
Proliferação. Diferenciação. Apoptose. Maturação. Ativação funcional. SCF PSC TPO CFU GEMM. BFU EMeg CFU GMEo BFU E IL-3. CFU EMeg CFU GM EPO.
 Hematopoese Requisitos básicos. 1. Stem cells (células tronco hematopoéticas). 2. Meio ambiente medular (fibroblastos, macrófagos e células endoteliais). 3. Fatores de crescimento (GM-CSF, Eritropoietina...)
Hematopoese Requisitos básicos. 1. Stem cells (células tronco hematopoéticas). 2. Meio ambiente medular (fibroblastos, macrófagos e células endoteliais). 3. Fatores de crescimento (GM-CSF, Eritropoietina...)
Unidade 2 PATRIMÓNIO GENÉTICO
 Unidade 2 PATRIMÓNIO GENÉTICO Como explicar a transmissão das características à descendência? Carácter cor da semente; Característica semente lisa ou rugosa. F 1 100% sementes lisas;logo, esta característica
Unidade 2 PATRIMÓNIO GENÉTICO Como explicar a transmissão das características à descendência? Carácter cor da semente; Característica semente lisa ou rugosa. F 1 100% sementes lisas;logo, esta característica
Protocolo. Síndromes mielodisplásicas- Propostas para diagnóstico e tratamento (incluindo TCTH)
 Protocolo Síndromes mielodisplásicas- Propostas para diagnóstico e tratamento (incluindo TCTH) Versão eletrônica atualizada em Abril 2012 Conceito As síndromes mielodisplásicas constituem um grupo heterogêneo
Protocolo Síndromes mielodisplásicas- Propostas para diagnóstico e tratamento (incluindo TCTH) Versão eletrônica atualizada em Abril 2012 Conceito As síndromes mielodisplásicas constituem um grupo heterogêneo
SOBRE MIM... Graduação em nutrição em 2010 pela UNIVERSIDADE ESTADUAL DO CENTRO OESTE UNICENTRO
 SOBRE MIM... Graduação em nutrição em 2010 pela UNIVERSIDADE ESTADUAL DO CENTRO OESTE UNICENTRO Pós graduada em Nutrição Clínica Funcional Unicsul/VP em 2014 Aluna de Mestrado na Universidade Federal de
SOBRE MIM... Graduação em nutrição em 2010 pela UNIVERSIDADE ESTADUAL DO CENTRO OESTE UNICENTRO Pós graduada em Nutrição Clínica Funcional Unicsul/VP em 2014 Aluna de Mestrado na Universidade Federal de
ANOMALIAS CROMOSSÔMICAS
 ANOMALIAS CROMOSSÔMICAS Profa. Dra. Vanessa Silveira RFM0009 Citogenética q 1882 Walther Flemming q Kroma: cor Soma: corpo q 1956 Citogenética humana q Número de cromossomos humanos q 1959 Síndrome de
ANOMALIAS CROMOSSÔMICAS Profa. Dra. Vanessa Silveira RFM0009 Citogenética q 1882 Walther Flemming q Kroma: cor Soma: corpo q 1956 Citogenética humana q Número de cromossomos humanos q 1959 Síndrome de
LEUCEMIAS E LINFOMAS CITOLOGIA HEMATOLÓGICA AVANÇADA Professor: Márcio Melo
 Curso S E LINFOMAS CITOLOGIA HEMATOLÓGICA AVANÇADA Professor: Márcio Melo EMENTA DO CURSO: Este curso tem como objetivo estudar de forma prática e dinâmica a citologia das Leucemias e dos Linfomas... apresentando
Curso S E LINFOMAS CITOLOGIA HEMATOLÓGICA AVANÇADA Professor: Márcio Melo EMENTA DO CURSO: Este curso tem como objetivo estudar de forma prática e dinâmica a citologia das Leucemias e dos Linfomas... apresentando
Sumário ANEXO I COMUNICADO HERMES PARDINI
 Sumário ANEXO I COMUNICADO HERMES PARDINI Conteúdo ANÁLISE DE CARIÓTIPO COM BANDA G CONSTITUCIONAL ALTERAÇÃO DE INFORMAÇÕES DO HELP... 2 ÁCIDO METIL MALÔNICO NOVO EXAME... 4 ROTAVÍRUS ANTICORPOS IGM ALTERAÇÃO
Sumário ANEXO I COMUNICADO HERMES PARDINI Conteúdo ANÁLISE DE CARIÓTIPO COM BANDA G CONSTITUCIONAL ALTERAÇÃO DE INFORMAÇÕES DO HELP... 2 ÁCIDO METIL MALÔNICO NOVO EXAME... 4 ROTAVÍRUS ANTICORPOS IGM ALTERAÇÃO
EPIGENÉTICA. Fernanda Molognoni Laboratório de Ontogenia e Epigenética Departamento de Farmacologia - UNIFESP
 EPIGENÉTICA Fernanda Molognoni [email protected] Laboratório de Ontogenia e Epigenética Departamento de Farmacologia - UNIFESP Especial Genética não é espelho Definição de Epigenética Epigenética
EPIGENÉTICA Fernanda Molognoni [email protected] Laboratório de Ontogenia e Epigenética Departamento de Farmacologia - UNIFESP Especial Genética não é espelho Definição de Epigenética Epigenética
AULA 1: Introdução à Quimioterapia Antineoplásica
 FARMACOLOGIA DOS QUIMIOTERÁPICOS AULA 1: Introdução à Quimioterapia Antineoplásica Profª. MsC Daniele Cavalheiro Oliveira Zampar Farmacêutica Especialista em Oncologia - Sobrafo Campo Grande, 29/09/2012
FARMACOLOGIA DOS QUIMIOTERÁPICOS AULA 1: Introdução à Quimioterapia Antineoplásica Profª. MsC Daniele Cavalheiro Oliveira Zampar Farmacêutica Especialista em Oncologia - Sobrafo Campo Grande, 29/09/2012
Mecanismos Genéticos e Epigenéticos do Câncer
 Mecanismos Genéticos e Epigenéticos do Câncer IBM1027 Genética Molecular Wilson Araújo Silva Jr O câncer é uma doença genética? Hereditário Esporádico Eventos genéticos! genômicos Eventos epigenético!
Mecanismos Genéticos e Epigenéticos do Câncer IBM1027 Genética Molecular Wilson Araújo Silva Jr O câncer é uma doença genética? Hereditário Esporádico Eventos genéticos! genômicos Eventos epigenético!
TÉCNICAS DE ESTUDO EM PATOLOGIA
 TÉCNICAS DE ESTUDO EM PATOLOGIA Augusto Schneider Carlos Castilho de Barros Faculdade de Nutrição Universidade Federal de Pelotas TÉCNICAS Citologia Histologia Imunohistoquímica/imunofluorescência Biologia
TÉCNICAS DE ESTUDO EM PATOLOGIA Augusto Schneider Carlos Castilho de Barros Faculdade de Nutrição Universidade Federal de Pelotas TÉCNICAS Citologia Histologia Imunohistoquímica/imunofluorescência Biologia
Livros Grátis. Milhares de livros grátis para download.
 1 Livros Grátis http://www.livrosgratis.com.br Milhares de livros grátis para download. 2 3 4 5 6 7 8 9 10 11 12 1. INTRODUÇÃO 1.1 - Hematopoese A hematopoese é o processo responsável pela formação do
1 Livros Grátis http://www.livrosgratis.com.br Milhares de livros grátis para download. 2 3 4 5 6 7 8 9 10 11 12 1. INTRODUÇÃO 1.1 - Hematopoese A hematopoese é o processo responsável pela formação do
Declaração de Conflito de Interesse
 Declaração de Conflito de Interesse Declaro que não possuo conflitos de interesse na (s) categoria (s) abaixo: Consultoria: não Financiamento de Pesquisa: não Honorário: não Patentes e Royalties: não Afiliação
Declaração de Conflito de Interesse Declaro que não possuo conflitos de interesse na (s) categoria (s) abaixo: Consultoria: não Financiamento de Pesquisa: não Honorário: não Patentes e Royalties: não Afiliação
Tratamentos do Câncer. Prof. Enf.º Diógenes Trevizan
 Tratamentos do Câncer Prof. Enf.º Diógenes Trevizan As opções de tratamento oferecidas para os pacientes com câncer devem basear-se em metas realistas e alcançáveis para cada tipo de câncer específico.
Tratamentos do Câncer Prof. Enf.º Diógenes Trevizan As opções de tratamento oferecidas para os pacientes com câncer devem basear-se em metas realistas e alcançáveis para cada tipo de câncer específico.
CARIÓTIPO & MUTAÇÕES CROMOSSÔMICAS
 Ensino Médio Biologia Professor João CARIÓTIPO & MUTAÇÕES CROMOSSÔMICAS O que são mutações? Qualquer alteração permanente no DNA é chamada de mutação; Podem ocorrer em qualquer célula, tanto nas somáticas
Ensino Médio Biologia Professor João CARIÓTIPO & MUTAÇÕES CROMOSSÔMICAS O que são mutações? Qualquer alteração permanente no DNA é chamada de mutação; Podem ocorrer em qualquer célula, tanto nas somáticas
REGULAÇÃO DA EXPRESSÃO GÊNICA. RCB105 Biomoléculas, biologia celular e moléculas
 REGULAÇÃO DA EXPRESSÃO GÊNICA RCB105 Biomoléculas, biologia celular e moléculas Conceito Processo pelo qual a expressão de genes é controlada em resposta a estímulos intra ou extracelulares Regulação da
REGULAÇÃO DA EXPRESSÃO GÊNICA RCB105 Biomoléculas, biologia celular e moléculas Conceito Processo pelo qual a expressão de genes é controlada em resposta a estímulos intra ou extracelulares Regulação da
CÉLULAS SANGUÍNEAS. Professora Janaina Serra Azul Monteiro Evangelista
 CÉLULAS SANGUÍNEAS Professora Janaina Serra Azul Monteiro Evangelista No nosso sangue circulam vários tipos de células Glóbulos vermelhos Que também podem ser chamados hemácias ou eritrócitos. Glóbulos
CÉLULAS SANGUÍNEAS Professora Janaina Serra Azul Monteiro Evangelista No nosso sangue circulam vários tipos de células Glóbulos vermelhos Que também podem ser chamados hemácias ou eritrócitos. Glóbulos
Biologia. Mutações e Aconselhamento Genético. Professor Enrico Blota.
 Biologia Mutações e Aconselhamento Genético Professor Enrico Blota www.acasadoconcurseiro.com.br Biologia MUTAÇÕES Mutação é uma mudança ou alteração no conteúdo genético de uma célula ou de um ser vivo.
Biologia Mutações e Aconselhamento Genético Professor Enrico Blota www.acasadoconcurseiro.com.br Biologia MUTAÇÕES Mutação é uma mudança ou alteração no conteúdo genético de uma célula ou de um ser vivo.
Aula teórica: Hematopoese
 Aula teórica: Hematopoese MED, 2017 Elementos figurados do sangue periférico Glóbulos vermelhos, eritrócitos ou hemácias 4-5 milhões/ml Glóbulos brancos ou leucócitos 6-9 mil/ml Polimorfonucleares (granulócitos)
Aula teórica: Hematopoese MED, 2017 Elementos figurados do sangue periférico Glóbulos vermelhos, eritrócitos ou hemácias 4-5 milhões/ml Glóbulos brancos ou leucócitos 6-9 mil/ml Polimorfonucleares (granulócitos)
ÁCIDOS NUCLÉICOS ESTRUTURA E FUNÇÕES
 DNA ÁCIDOS NUCLÉICOS ESTRUTURA E FUNÇÕES Prof. Edimar Campos Antes de 1950 sabia-se apenas que qualquer que fosse a natureza do material genético, ele deveria possuir 3 características importantes: O MATERIAL
DNA ÁCIDOS NUCLÉICOS ESTRUTURA E FUNÇÕES Prof. Edimar Campos Antes de 1950 sabia-se apenas que qualquer que fosse a natureza do material genético, ele deveria possuir 3 características importantes: O MATERIAL
CITOGENÉTICA CROMOSSOMOS
 CITOGENÉTICA CROMOSSOMOS 1 CROMOSSOMOS Os cromossomos são estruturas filamentosas localizadas no interior do núcleo das células. Os cromossomos contém os genes que são os transmissores das caracterís2cas
CITOGENÉTICA CROMOSSOMOS 1 CROMOSSOMOS Os cromossomos são estruturas filamentosas localizadas no interior do núcleo das células. Os cromossomos contém os genes que são os transmissores das caracterís2cas
Nutrigenômica x Nutrigenética - doenças relacionadas
 Nutrigenômica x Nutrigenética - doenças relacionadas Início Projeto Genoma Humano 20.000 genes (120.000 inicialmente estimados) Diversidade nucleotídica: 0,1 a 0,4% pares de base correspondente a aproximadamente
Nutrigenômica x Nutrigenética - doenças relacionadas Início Projeto Genoma Humano 20.000 genes (120.000 inicialmente estimados) Diversidade nucleotídica: 0,1 a 0,4% pares de base correspondente a aproximadamente
