Propriedades Absorventes dos Produtos da Carbóxi- Metilação de Polpa Etanol/Água de Medula de Bagaço de Cana-de-Açucar
|
|
|
- Vanessa Valgueiro di Azevedo
- 6 Há anos
- Visualizações:
Transcrição
1 A R T I G O T É C N I C O C I E N T Í F I C O Propriedades Absorventes dos Produtos da Carbóxi- Metilação de Polpa Etanol/Água de Medula de Bagaço de Cana-de-Açucar Cibele M. F. Martinez, Elisabete Frollini e Sérgio P. Campana Filho Resumo: Polpas etanol/água de medula de bagaço de cana de açúcar foram empregadas para a obtenção de carbóxi-metil-celulose insolúvel, aplicável como material absorvente. Tipicamente, a reação de carbóximetilação da polpa branqueada foi realizada em suspensão de isopropanol/água (1:8 / m:m) a 80 ºC por 4 horas, empregando-se relação molar 1 / 5,4 / 8,8 de celulose / NaOH / ClAcOH. O material com melhores características corresponde a um produto muito pouco solúvel (S W < 2%), com propriedades absorventes superiores às da polpa de partida. Palavras-chave: Carbóxi-metil-celulose insolúvel; polpa etanol/água; medula de bagaço de cana de açúcar Introdução O bagaço de cana de açúcar representa a quarta produção mundial de fibras celulósicas para fins industriais, estimada em aproximadamente 4,1 trilhões de toneladas métricas anuais 1. A moagem de cana para a produção de açúcar e álcool nas usinas brasileiras durante a safra 95 / 96 deve gerar cerca de 40 milhões de toneladas métricas de bagaço 2, o que representa mais da metade da produção mundial. O bagaço é intensivamente usado como combustível de caldeiras e, em menor escala, para a composição de ração animal e a preparação de polpas para manufatura de papel 3. Alguns estudos sugerem também outras utilizações potenciais tais como a produção de polpas químicas para a preparação de derivados de celulose 4, a obtenção de termoplásticos 5 e a preparação de compósitos 6. Entretanto, as principais limitações ao emprego de polpas de bagaço se devem ao custo do transporte e à necessidade de se desenvolver e/ou adaptar as tecnologias apropriadas. Quando o interesse focaliza a produção de polpas, a necessidade de etapas adicionais para a eliminação de impurezas e exclusão da medula, fração não-fibrosa correspondente a cerca de % do bagaço integral, se constitui em mais um fator limitador do seu emprego. Os teores de celulose, lignina e polioses presentes na medula e nas fibras são muito próximos entre si e àqueles de madeiras duras 3. Entretanto, medula e fibras verdadeiras são diferentes do ponto de vista morfológico, quanto às suas funções fisiológicas e ao que diz respeito às respectivas capacidades de absorção de líquidos. Em relação a essa última característica, uma aplicação potencial da medula pode ser antecipada na preparação de materiais absorventes. De fato, a Cibele M. F. Martinez, Elisabete Frollini e Sérgio P. Campana Filho, Instituto de Química de São Carlos - Universidade de São Paulo, Caixa Postal 780, , São Carlos, São Paulo. 48 Polímeros: Ciência e Tecnologia - Jan/Mar - 97
2 demanda por materiais com elevada capacidade de retenção de água tem resultado no rápido crescimento da produção industrial de hidrogéis desde os meados da década de A maioria dos absorventes, e principalmente dos superabsorventes, disponíveis no mercado é preparada a partir de polímeros sintéticos, essencialmente poliacrílicos 7. Entretanto, estudos sobre a obtenção e caracterização de hidrogéis preparados a partir de polissacarídeos naturais vêm ganhando importância em vista das crescentes preocupações relacionadas com questões ambientais e também devido à abundância, disponibilidade e elevado grau de hidrofilicidade desses polímeros naturais 8. Outra possível vantagem dos hidrogéis baseados em polissacarídeos reside na elevada rigidez intrínseca de suas cadeias poliméricas quando comparadas a polímeros vinílicos 9, disso resultando seu comportamento não-gaussiano 10 e melhores propriedades mecânicas 8. Além disso, a presença de muitos grupos hidroxila oferece possibilidades de derivatização visando à melhoria das propriedades absorventes. Isso pode ser conseguido através da preparação de polissacarídeos polieletrólitos. Polieletrólitos possuem elevada capacidade de inchamento em sistemas aquosos devido à presença, nesse tipo de gel, de cargas sobre a cadeia polimérica e dos respectivos contra-íons H + no meio líquido aprisionado no interior da rede. As interações eletrostáticas repulsivas entre as cargas sobre a cadeia e a pressão osmótica devido aos contra-íons H + se somam para aumentar o inchamento da rede 11. A carbóxi-metilação de celulose nas condições adequadas 12 ou a aplicação de procedimentos de purificação, tais como lavagens com misturas apropriadas solvente / não-solvente 13, resultam em carbóxi-metil-celuloses substancialmente insolúveis dotadas de características absorventes muitas vezes superiores às das polpas empregadas como matériaprima. No sentido de avaliar o potencial do bagaço de cana de açúcar para a preparação de materiais absorventes, o presente estudo relata o emprego de medula como matéria-prima para a preparação de carbóxi-metil-celulose insolúvel com propriedades absorventes. Nele são apresentados e discutidos os resultados dos experimentos em que polpas branqueadas etanol/água são empregadas para, numa etapa, preparar o produto com as características citadas através de sua carbóxi-metilação na presença de excesso de ácido mono-cloro-acético. Experimental Matéria-prima : A fração correspondente à medula foi separada do bagaço, fornecido pela Usina Ipiranga de São Carlos, por peneiramento via úmida de suspensão de 200g de matéria-prima em 4 litros de água. Nesta etapa, a suspensão contendo o bagaço integral foi inicialmente agitada por 1 hora a 70 C (o que permitiu a extração de substâncias hidrossolúveis), resfriada à temperatura ambiente e então forçada através do conjunto de peneiras com o auxílio de ducha de água. Polpação etanol/água: Após secagem a 70 C por 24 horas a medula foi submetida a um processo de polpação com mistura etanol/água (1:1 / v:v) em reator de 2 litros observando a relação 1:30 (m/v) entre medula e etanol/água. Após a polpação por 1 hora a 190 C, a medula foi filtrada, extraída com etanol e depois com água quente (90 C), lavada com água fria até a neutralidade e seca ao ar. A polpa obtida foi branqueada pelo processo clorito de sódio 14, seguido de extração com solução aquosa de NaOH 0,1M durante 90 minutos. Carbóxi-metilação das polpas 12 Em um experimento típico, a polpa branqueada moída, cerca de 8,5g, foi suspensa em 270 ml de isopropanol e vigorosamente agitada em reator de vidro. Foram adicionados 6,6g de NaOH dissolvidos em 25mL de água e a suspensão foi mantida sob agitação mecânica à temperatura ambiente durante 30 minutos. Em seguida, foram adicionados 10,21g de ácido mono-cloro-acético, a temperatura elevada para 80 C e a reação foi deixada nessas condições durante 5 horas. Ao final desse período, o produto foi filtrado, abundantemente lavado com metanol e seco ao ar (amostra A). Mais sete amostras foram preparadas, variando-se o tempo de reação entre 3 e 6 horas e a concentração de ácido mono-cloro-acético entre 0,54M e 1,0M. Caracterizações: Polpas branqueadas foram caracterizadas quanto ao grau de umidade e teores de cinzas, lignina e holocelulose através de metodologia padrão 14,15. O Polímeros: Ciência e Tecnologia - Jan/Mar
3 grau de polimerização foi determinado por medidas de viscosidade de soluções de polpa branqueada em cupra-etileno-diamina segundo norma padrão 16. Solubilidade e Propriedades Absorventes Solubilidades em água e em solução aquosa 2,5 x 10-4 M de NaOH foram determinadas após embebição por 12 horas, filtração, lavagem com metanol e pesagem do material insolúvel. Capacidades de retenção de água (CRA) e de solução aquosa de NaCl 1% (CRS) foram determinadas através de metodologia semelhante àquela empregada para a caracterização de produtos absorventes obtidos a partir da carbóxi-metilação de polpas de madeira 12. Após a embebição da amostra, cerca de 0,3g, em 100mL de água (ou solução salina) durante 16 horas, filtração e centrifugação a 2500 rpm durante 20 minutos, as massas do material úmido (m u ) e seco em estufa a 100 C (m s ) foram determinadas. Os valores de capacidades de retenção de solução aquosa de NaCl 1% (CRS) foram corrigidos devido à contribuição do sal à massa de material seco (m s ). As expressões abaixo foram empregadas para os cálculos de CRA e CRS em termos percentuais. (%) CRA = (m u - m s / m s ) 100 (%) CRS = [(m u - 0,99m s ) / 0,99m s ] 100 Grau de Substituição Graus de substituição (DS) dos produtos carbóximetilados foram determinados por espectroscopia de ressonância magnética nuclear do próton (espectrômetro Bruker 200) de amostras hidrolisadas em meio D 2 SO 4 / D 2 O 17 e por dosagem de sódio via titulação das cinzas de amostras incineradas 18. Nas determinações de DS através de espectroscopia de ressonância magnética nuclear, a amostra de carbóxi-metil-celulose, cerca de 50mg, foi suspensa em 1mL de mistura D 2 O / D 2 SO 4 (1:1/v:v) e a suspensão aquecida a 90 C por minutos. A obtenção de solução límpida, ligeiramente amarelada, foi tomada como evidência de que a hidrólise procedeu sem ocorrência de degradação da amostra através de reações colaterais. Ácido acético foi adicionado como padrão de referência interna, e uma alíquota, cerca de 0,4mL da solução, foi transferida para o tubo de ressonância para a varredura do espectro. As atribuições dos sinais observados nos espectros foram feitas segundo descrito na literatura 17 e os valores de graus de substituição (DS) calculados através da expressão abaixo. DS = (a / 2) / (c / 6) Nessa expressão, a e c correspondem às áreas dos sinais atribuídos aos 2 átomos de hidrogênio dos metilenos dos grupos carbóxi-metila e aos 6 átomos de hidrogênio ligados aos átomos de carbono 2, 3, 4, 5 e 6 das unidades anidroglicopiranose, respectivamente. Nas dosagens de sódio empregadas para a determinação de DS, a amostra seca, cerca de 0,5g, foi incinerada em cadinho de porcelana na chama do bico de bunsen e, em seguida, calcinada em mufla durante 4 horas a 600 C. As cinzas secas foram dissolvidas em água e a solução resultante titulada com solução aquosa padronizada de ácido sulfúrico 0,1M. Atingido o ponto de equivalência, detectado pela presença de vermelho de metila como indicador, a solução foi aquecida para a eliminação de CO 2 e mais ácido foi adicionado até que um novo ponto final fosse observado. Os valores de DS foram calculados a partir da expressão DS = (0,162B) / (1-0,08B) sendo B o número de miliequivalentes de sódio por grama da amostra de carbóxi-metil-celulose dosada. Análises Térmicas e Microscopia Eletrônica de Varredura Análises calorimétricas diferenciais de varredura foram realizadas com cerca de 10mg de amostra em equipamento Netzsch DSC 200, operando entre -20 C e 100 C e taxa de aquecimento de 10 C/min. Micrografias foram obtidas em Digital Scanning Microscope após secagem das amostras por 24 horas em estufa a vácuo, a cerca de 50 C, e após recobrimento com ouro em Sputter Coater por 7 minutos. Resultados e Discussão Obtenção e Caracterização de Polpas Etanol/Água de Medula O processo etanol / água de polpação foi aplicado à medula nas condições descritas como sendo as melhores, em termos de rendimento e eficiência de 50 Polímeros: Ciência e Tecnologia - Jan/Mar - 97
4 deslignificação, por um estudo cinético realizado com fibras de bagaço 19. Em vista da maior capacidade de absorção de líquidos da medula, foi introduzida uma única modificação no procedimento de polpação descrito para as fibras verdadeiras e que consistiu na utilização de maior volume de etanol/ água. A aplicação da polpação etanol / água à medula resultou em rendimento da ordem de 45%, o que está de acordo com resultados da literatura relativos à polpação de fibras de bagaço 20. Em ambos os casos, os rendimentos são inferiores aos obtidos quando processos industriais, como o Soda / Antraquinona, são aplicados provavelmente devido à maior ocorrência de degradação da fração de polissacarídeos, inclusive celulose, na polpação etanol / água. De fato, no processo etanol/água, bem como em outros processos organossolve em que não são utilizados catalisadores, o meio reacional torna-se ácido devido à liberação de ácido acético proveniente da hidrólise de grupos acetila de polioses presentes na fibra vegetal. Em vista da susceptibilidade de polissacarídeos à hidrólise em meio ácido, parece razoável supor que, na polpação etanol/água, esse processo seja o responsável pela queda de rendimento. A polpa não-branqueada apresentou teor de lignina em torno de 3,5% e o rendimento da etapa de branqueamento com clorito de sódio foi de cerca de 75%. Rendimentos dos processos de polpação e de branqueamento e características das polpas etanol / água de medula são apresentados na Tabela 1. Tabela 1. Rendimentos de polpação e branqueamento e características das polpas etanol/água de medula de bagaço de cana de açúcar. Teores Percentuais Polpa nãobranqueada Polpa branqueada Rendimento O grau de polimerização da polpa branqueada foi calculado através da expressão proposta por Immerget, Shurtz e Mark, a partir da determinação de viscosidade intrínseca em solução de cupra-etilenodiamina 16. O valor da viscosidade intrínseca de solução 0,004g/cm 3 de polpa foi de 412,5 cm 3 /g e o correspondente grau de polimerização, igual a 565. Este valor é inferior ao de polpas etanol/água de fibras de bagaço, o que resulta do fato de as cadeias de celulose na medula apresentarem menor grau de polimerização. Características de Carbóxi-metil-celulose Absorvente Preparada de Polpa de Medula Na Tabela 2 são apresentados os dados relativos a solubilidade em água (S W ), capacidades de retenção de água (CRA) e de solução aquosa salina (CRS) e graus de substituição (DS) de polpas carbóximetiladas obtidas empregando diferentes concentrações de ácido mono-cloro-acético. Como pode ser constatado dos dados da Tabela 2, os produtos obtidos pela carbóxi-metilação das polpas etanol/água de medula nas condições descritas são pouco solúveis em água. Isso se deve ao fato de a reação proceder por tempo suficiente em presença de excesso do agente eterificante neutralizado, monocloro-acetato de sódio, frente à concentração restante Tabela 2. Solubilidade, grau de substituição e propriedades absorventes de polpas carbóxi-metiladas em função da concentração de ácido monocloro-acético, ClAcOH, empregado em sua obtenção. D b) ( a) S A mostra [ ClAcOH] W) S (% CRA ( D S ( c) (%) CRS (%) A 0,37 8, 5 0,76 0,11 220, 4 153, 7 B 0,54 37, 8 0,82 0,17 249, 6 174, 4 Lignina Klason Insolúvel 3,4 - C 0,74 15, 0 0,84 0,14 640, 4 196, 2 D 0,90 11, 6 0,96 0,12 662, 6 202, 9 a) N úmero Kappa ( 15 < - E 1,00 19, 7-0,15 321, 6 168, 3 Holocelulose - >80 (a) Teor de lignina expresso como o número de mililitros de solução padrão de tiossulfato de sódio necessários à oxidação da macromolécula 14. a) Concentração (mol/l) de ácido mono-cloro-acético presente no início da reação; b) valores determinados através de espectroscopia de ressonância magnética nuclear do próton 17 ; c) valores determinados através da dosagem de sódio nas cinzas das amostras 18. Polímeros: Ciência e Tecnologia - Jan/Mar
5 de hidróxido de sódio 12. Em todos os casos aqui relatados, a relação molar ClAcO (-) Na (+) / NaOH foi igual ou superior a 2, pois quando foi empregada uma relação menor, o produto obtido apresentou baixa capacidade de absorção de água e solubilidade superior a 75% 21. É necessário ressaltar, entretanto, que todas as amostras apresentaram valores de grau de substitutição (DS), determinados através de espectroscopia de ressonância magnética nuclear, comparáveis àqueles normalmente apresentados por produtos solúveis. Com o objetivo de tentar esclarecer a relação entre o conteúdo de grupos carbóxi-metila e a solubilidade das amostras, dois procedimentos distintos foram adotados para as determinações de graus de substituição: i) através de espectroscopia de ressonância magnética nuclear do próton 17 e ii) pela dosagem de sódio 18 modificada pela exclusão da etapa de conversão das amostras à forma salina. Nas determinações de DS de carbóxi-metilcelulose através de espectroscopia de ressonância magnética nuclear do próton, as amostras são completamente hidrolisadas em meio D 2 SO 4 / D 2 O a fim de evitar que a viscosidade do polímero provoque o alargamento dos sinais e dificulte a obtenção de espectros interpretáveis. A ocorrência de hidrólise completa é verificada através da relação entre as áreas dos sinais devidos ao próton ligado ao carbono 1 e aos seis prótons ligados aos carbonos 2, 3, 4, 5 e 6 da unidade de anidroglicopiranose. O grau de substituição é determinado a partir da área dos sinais devidos aos prótons metilênicos dos grupos carbóximetila presentes nas unidades de anidroglicopiranose e os valores de DS determinados através desse procedimento são, na faixa de DS < 3,0, sempre superiores àqueles obtidos pelo emprego de procedimentos de titulação 18. Isso é atribuído ao fato de, no caso da determinação via espectroscopia de ressonância magnética nuclear, todas as unidades monoméricas serem levadas em consideração, enquanto que, no caso dos procedimentos de titulação, a conversão incompleta à forma ácida e a ocorrência de agregação levam à subestimação do valor de DS. Assim, os valores de DS determinados através de espectroscopia de ressonância magnética nuclear correspondem, de fato, à melhor aproximação do número médio de grupos carbóxi-metila presentes por unidade de anidroglicose nas amostras de carbóximetil-celulose. Entretanto, os valores de graus de substituição determinados através da dosagem de sódio presente nas cinzas das amostras incineradas foram entre 5 e 8 vezes menores (Tabela 2), o que pode ser melhor compreendido na discussão a seguir. Nas determinações de DS de carbóxi-metilcelulose através da dosagem de sódio nas cinzas da amostra incinerada o pressuposto básico é que exista uma relação estequiométrica equimolar entre grupos carboximetila negativamente carregados e contra-íons sódio. Para assegurar a observância dessa condição a amostra é convertida à forma salina por tratamento em suspensão aquosa alcalina, seca e então incinerada. Através desse procedimento, o Na 2 O formado na incineração da amostra é decomposto a NaOH em solução aquosa e este último é titulado com solução padronizada de ácido sulfúrico diluído. Os erros de pesagem, a presença de impurezas, a conversão incompleta da amostra à forma salina e perdas de massa por solubilização parcial são as principais fontes de imprecisão nas determinações de DS por dosagem de sódio. Neste trabalho, a dosagem de sódio após incineração dos produtos não foi precedida de tratamento alcalino para conversão à forma salina. Desta forma, a dosagem realizada de fato reflete o número médio de grupos carbóxi-metila que possuem contra-íons sódio. Portanto, os baixos valores de DS determinados através deste procedimento devem ser atribuídos ao fato de poucos grupos carbóxi-metila se encontrarem presentes na forma de sal de sódio. Por outro lado, o procedimento que emprega ressonância magnética nuclear para adeterminação de DS não faz distinção entre grupos carbóxi-metila nas formas salina e protonada mas fornece valores mais precisos, independentemente do grau de pureza da amostra analisada, e permite avaliar, por comparação com os resultados obtidos através da técnica de cinzas, a fração correspondente a grupos carbóxi-metila na forma ácida. Em vista desses resultados deve ser concluído que as amostras de carbóxi-metil-celulose obtidas nas condições descritas têm entre 80% e 90% dos grupos carbóxi-metila sob a forma protonada, e este é um dos fatores responsáveis pela baixa solubilidade apresentada pelos produtos. A amostra D apresentou solubilidade em meio aquoso alcalino cerca de três vezes superior àquela exibida em água pura, o que também deve ser tomado como uma forte evidência do cárater ácido do produto 21. Entretanto, a estrutura da rede polimérica não foi totalmente destruída pois a completa solubilização da amostra não foi 52 Polímeros: Ciência e Tecnologia - Jan/Mar - 97
6 conseguida mesmo com o prolongamento do tempo de embebição no meio alcalino. Quanto aos valores de DS, pode ser verificado na Tabela 2 que, como esperado, o conteúdo de grupos carbóxi-metila é maior nas amostras obtidas em presença de maior excesso de ácido mono-cloroacético. No caso da amostra E, não foi possível determinar o valor de DS através de espectroscopia de ressonância magnética nuclear devido à ocorrência de severa degradação da amostra durante a hidrólise, o que foi evidenciado pela obtenção de uma suspensão viscosa e escura. O comportamento absorvente das amostras de carbóxi-metil-celulose em função da concentração de ácido mono-cloro-acético empregado em sua obtenção é melhor avaliado através das curvas na Figura 1. Pela Figura 1, pode ser constatado que os produtos de carbóxi-metilação das polpas etano/água de bagaço possuem capacidade de retenção de água superior àquela apresentada pela matéria-prima empregada em sua obtenção, e que essa superioridade é mais acentuada à medida que aumenta a concentração de ácido mono-cloro-acético empregado na reação de carbóxi-metilação. Portanto, o aumento observado da capacidade de retenção de água também acompanha o aumento dos respectivos valores de grau de substituição (DS) e deve ser atribuído à presença de grupos ionizáveis no interior da rede polimérica. Assim, apesar de substancialmente insolúveis, os produtos obtidos contêm grupos que se caracterizam por apresentarem grande afinidade por água. Capacidade Absorvente (%) CRA (%) CRS (%) 0,0 0,2 0,4 0,6 0,8 1,0 [ClAcOH] (mol/l) Figura 1. Capacidades de retenção de água (CRA) e de solução aquosa salina (CRS) de carbóxi-metil-celulose em função da concentração de ácido mono-cloro-acético empregado em sua obtenção. De fato, a presença de grupos carbóxi-metila na forma ácida é, em grande parte, responsável pela pouca solubilidade dos produtos, e é sua ionização parcial que confere propriedades absorventes superiores às da polpa de partida. Isso se deve à pressão osmótica que se desenvolve no interior da rede polimérica pela dissociação de íons H +. Tal conclusão é respaldada pela ocorrência do efeito polieletrolítico, constatável pela redução das capacidades absorventes dos produtos quando NaCl está presente na água de embebição (Figura 1). No caso de polieletrólitos solúveis, a blindagem das interações repulsivas entre as cargas sobre as cadeias, devida aos íons Na + adicionados à solução, se manifesta pela diminuição da viscosidade com o aumento da concentração de sal 22. Nos produtos deste trabalho, o efeito polieletrolítico se expressa pela contração da rede polimérica e, conseqüentemente, pela menor capacidade de retenção da solução aquosa. A diminuição da capacidade de retenção de líquido pelas polpas carbóxi-metiladas, observada em solução aquosa de NaCl a 1%, deve portanto ser atribuída ao efeito polieletrolítico. Tal efeito não se manifesta quando a polpa não-carbóxi-metilada é embebida na solução salina já que esta não contém grupos iônicos ao longo das cadeias de celulose. Quanto à intensidade do efeito de redução da capacidade absorvente manifestado pelas amostras carbóxi-metiladas, dois grupos de comportamentos distintos podem ser identificados. Ao serem embebidas em solução aquosa salina, as amostras A e B apresentaram uma redução de cerca de 30% em suas capacidades absorventes enquanto que as amostras C e D exibiram uma diminuição mais acentuada, cerca de 70%, quando submetidas ao mesmo tratamento. A amostra E manifestou um efeito intermediário, quase 50% de redução na capacidade absorvente, nas mesmas condições. Caso o efeito observado fosse atribuível tão somente ao conteúdo de grupos carbóxi-metila sobre as cadeias celulósicas, seria esperado que as amostras possuidoras dos maiores valores de grau de substituição (DS) apresentassem reduções mais drásticas nas capacidades de retenção de solução aquosa salina. Essa tendência foi, de fato, observada (Tabela 2). Porém, diferenças muito pequenas nos valores de grau de substituição (DS) resultaram em variações muito grandes nas respectivas reduções das capacidades de retenção de solução aquosa salina. Considerando a capacidade de retenção de água, Polímeros: Ciência e Tecnologia - Jan/Mar
7 Tabela 3. Solubilidade, grau de substituição e propriedades absorventes de polpas carboxi-metiladas em função do tempo de reação empregado em sua obtenção (a). Amostra Tempo (h) S W) S (% D b) CRA ( D S ( c) (%) CRS (%) F 3 25, 4 0,69 0,16 393, 2 163, 0 G 4 1, 7 0,76 0,10 841, 5 239, 4 D 5 11, 6 0,96 0,12 662, 6 202, 9 Capacidade Absorvente (%) CRA (%) CRS (%) H 6 10, 9 0,72 0,11 442, 4 172, 0 a) As condições empregadas nas reações de obtenção desse produtos são aquelas descritas para a amostra D; b) Valores determinados através de espectroscopia de ressonância magnética nuclear do próton 17 ; c) Valores determinados através da dosagem de sódio nas cinzas das amostras 18. a amostra D (Tabela 2) foi aquela que apresentou as melhores propriedades. Com o objetivo de avaliar o efeito do tempo de reação sobre as características da carbóxi-metil-celulose obtida, foram realizadas mais três preparações em condições idênticas àquelas empregadas para obtenção da amostra D, a menos do tempo, que variou no intervalo de 3 a 6 horas. As características dos produtos obtidos nessas condições são apresentadas na Tabela 3. Por esses dados pode-se constatar que um mínimo de solubilidade é atingido quando a reação é interrompida após 4 horas a 80 C, em presença de 0,90 mol/l de ácido mono-cloro-acético no meio reacional. Esse produto e também aqueles obtidos a diferentes tempos de reação apresentam valores de DS comparáveis àqueles de produtos solúveis. Também nesses casos se aplicam as observações relativas às técnicas de determinação de DS e a constatação de que se trata de amostras de carboxi-metilcelulose predominantemente obtidas em forma ácida. Quanto às características absorventes, o perfil de sua variação em função do tempo de reação é melhor avaliado na Figura 2. Também com relação ao parâmetro tempo de reação, pode ser observada na Figura 2 a ocorrência de um valor máximo para a capacidade de retenção de água (CRA), como já havia sido constatado com relação à concentração de ácido mono-cloro-acético Tempo [ClAcOH] de Reação (mol/l) (h) Figura 2. Capacidades de retenção de água (CRA) e de solução aquosa salina (CRS) de carbóxi-metil-celulose em função do tempo de reação empregado em sua obtenção. empregado na carbóxi-metilação das polpas. Tempos de reação maiores ou menores resultaram em produtos mais solúveis e com características absorventes inferiores àquelas da amostra obtida através de carbóxi-metilação durante quatro horas. Quanto às variações nas capacidades de retenção de água e de solução aquosa salina, pode ser verificado que todos os produtos apresentam o efeito polieletrolítico, mas novamente pode ser constatado que não há uma relação direta entre o valor de DS e a redução na capacidade absorvente em solução aquosa salina. Por outro lado, diferentemente do que foi observado quando a concentração de ácido monocloro-acético foi variada, no caso das amostras obtidas em diferentes tempos de carbóxi-metilação pode ser observado um comportamento mais uniforme. Assim, essas amostras apresentam redução da capacidade absorvente em torno de 60% a 70% quando a água de embebição contém NaCl enquanto os respectivos graus de substituição (DS) variam no intervalo 0,69 < DS < 0,96. Deve ser ressaltado que não foi constatada uma relação biunívoca entre os valores de DS e as propriedades absorventes de água e de solução salina pelos produtos deste trabalho. Assim, por exemplo, as amostras A e F apresentam valores de DS = 0,76, porém diferem muito quanto às respectivas capacidades de retenção de água e de solução salina. Além disso, essas amostras apresentam comportamentos quantitativamente distintos quanto às reduções nas suas capacidades absorventes devido à presença de NaCl na água de embebição. Por outro 54 Polímeros: Ciência e Tecnologia - Jan/Mar - 97
8 lado, as amostras C e D apresentam características semelhantes quanto a comportamentos absorventes e sensibilidades à presença de sal na água de embebição mas exibem valores bem distintos de DS. Esses resultados sugerem que outros fatores devem ser também considerados para compreeender os comportamentos observados, dentre eles a resposta elástica da rede e o grau de afinidade entre as cadeias poliméricas. O primeiro fator está associado ao grau de intercruzamento da rede polimérica, e o segundo depende das interações polímero / polímero e polímero / solvente 23. A avaliação da importância relativa de ambos os fatores deve ser feita através da caracterização mais detalhada da estrutura dos produtos e de seus comportamentos em relação à solubilidade em função do ph e à absorção de soluções aquosas de diferentes forças iônicas. Características morfológicas As características morfológicas da polpa etanol/água de medula e de um dos produtos de carbóxi-metilação com boas propriedades absorventes, a amostra D, foram determinadas através de microscopia eletrônica de varredura (Figura 3). Para a realização dessas análises, ambos os materiais foram primeiramente condicionados em água durante 16 horas, de modo que as fotomicrografias apresentadas correspondem a amostras completamente expandidas. Pela comparação dessas fotomicrografias pode ser observado que a amostra carbóxi-metilada apresenta muito menos regiões vazias e que corresponde, aparentemente, a um material de natureza mais homogênea que a polpa não-carbóxi-metilada. O fato de a amostra D apresentar menos espaços vazios é indicativo que este material se encontra mais expandido e, portanto, pode conter mais água aprisionada em sua estrutura. A aparência heterogênea da polpa nãocarbóxi-metilada deve ser atribuída ao fato de este material conter algumas estruturas celulares parcialmente preservadas, o que certamente não ocorre no caso da amostra D devido à modificação química que sofreu através da reação de carbóxi-metilação. De fato, a estrutura da polpa não-branqueada, examinada com aumento de vezes, revela a existência de regiões que preservam a natureza fibrosa do material e a ocorrência de empacotamento com formação de fibrilas altamente cristalinas 21. Nos casos da polpa branqueada e da amostra D, essas estruturas não foram observadas mas constatou-se a natureza amorfa deste último material bem como alguma heterogeneidade, observada pela presença de estruturas granulares aparentes já no aumento de 200 vezes. Calorimetria Diferencial de Varredura Materiais absorventes contêm dois tipos distintos de água que interagem com o hidrogel 24 : i) água associada à rede macromolecular e ii) água que envolve a rede polimérica. O primeiro tipo pode ser subdividido a partir da consideração de que parte do líquido se associa fortemente à rede e faz parte da (a) (b) Figura 3. Fotomicrografias dos materiais expandidos em água: a) polpa branqueada etanol / água de medula de bagaço de cana de açúcar; b) amostra carbóxi-metilada D. (Aumento de 200 vezes). Polímeros: Ciência e Tecnologia - Jan/Mar
9 estrutura do hidrogel enquanto a outra fração interage mais fracamente com as cadeias poliméricas. A água estrutural do hidrogel é denominada água ligada e se associa às cadeias poliméricas através de pontes de hidrogênio e/ou interações dipolo-dipolo. A fração de moléculas de água que interage mais fracamente com o polímero, localizada nas proximidades de grupos hidrofóbicos da macromolécula, é denominada água intersticial. A denominação água livre é empregada para designar a água que não participa da estrutura do hidrogel mas que envolve a rede polimérica que o constitui. Em função dos diferentes graus de associação que mantêm com as cadeias poliméricas, esses diferentes tipos de água são distintos do ponto de vista de suas propriedades físicas, tais como ponto de fusão e viscosidade. Se o hidrogel é resfriado abaixo de 0 C, a fração correspondente à água livre, a exemplo do que acontece com a água pura, passa para o estado sólido. Em decorrência do grau de interações que estabelecem com a rede polimérica, as frações correspondentes à água ligada e à água intersticial apresentam comportamento diferente daquele da água livre. No primeiro caso, não ocorre mudança de estado enquanto que, no segundo, a solidificação ocorre abaixo de 0 C. A distinção entre os diferentes tipos de água acima definidos pode ser realizada através de calorimetria diferencial de varredura 25. Na Figura 4 são mostrados o termograma resultante da análise por calorimetria diferencial de varredura da amostra de polpa branqueada etanol/água de medula e o de um de seus produtos carbóximetilados (amostra G). - 0,2 DSC (mw/mg) - 0,4-0,6-0,8 exo -6,4ºC Polpa Branqueada Amostra G -1,8ºC - 1,0-1,8 C Temperatura (ºC) Figura 4. Termogramas resultantes da análise por calorimetria diferencial de varredura de: a) polpa branqueada etanol/água de medula e b) amostra carbóxi-metilada G. Ambos os materiais se encontram no estado expandido de hidrogel pois foram inicialmente embebidos em água por 16 horas e o excesso de água foi excluído por filtração. Portanto, as transições endotérmicas observadas em -6,4 C e -1,8 C para a polpa e a amostra G, respectivamente, devem ser atribuídas à fusão da água. Embora a resolução dos termogramas não permita a identificação dos diferentes tipos de água definidos acima, a comparação do sistema estudado com outros géis hidrofílicos indica que as transições observadas estão relacionadas ao processo de fusão de a água intersticial 26. Neste caso, os diferentes pontos de fusão podem ser atribuídos ao fato de a água intersticial estar confinada em volumes diferentes quando as redes poliméricas da polpa e da amostra G são consideradas. Assim, a rede polimérica do hidrogel formado pela interação da amostra G com água encontra-se mais expandida devido à presença de cargas originadas da ionização dos grupos carbóxi-metila. No caso da polpa, a inexistência de repulsões eletrostáticas resulta em menor capacidade de retenção de água, menor volume no estado expandido e, consequentemente, a água intersticial se encontra mais constrita, o que provoca um abaixamento mais importante no seu ponto de fusão. Conclusões Considerando o conjunto de resultados apresentados, o produto com melhores características, visando a aplicação como material absorvente, foi obtido quando a polpa branqueada etanol/água de medula foi submetida à reação de carbóxi-metilação a 80 C, durante 4 horas, na presença de ácido mono-cloroacético na concentração 0,90M. Este produto, correspondente à amostra G, apresentou solubilidade muita baixa (S W = 1,7%) e capacidade de retenção de água quase oito vezes superior à da medula não-carbóximetilada. Em vista de se tratar de um polieletrólito, sua capacidade absorvente é bastante reduzida, quando embebido em soluções aquosas salinas. Sua aplicação na confecção de papel absorvente é sugerida, pois, além de apresentar boa capacidade de absorção de água, exibe alvura compatível com essa finalidade em função de ser obtido a partir de polpa branqueada e de não ser submetido a processamento térmico, o que costuma resultar em produtos mais ou menos escurecidos em função da severidade do tratamento. Entretanto, as propriedades mecânicas do papel resultante devem 56 Polímeros: Ciência e Tecnologia - Jan/Mar - 97
10 ser avaliadas, pois é conhecido que a medula empobrece suas características de resistência ao rasgo e à ruptura. No caso das polpas carbóxi-metiladas deste trabalho, tal efeito deletério pode não ocorrer dado que a morfologia da medula deve ser modificada em razão das alterações químicas introduzidas em sua estrutura. A microscopia eletrônica de varredura da polpa etanol/água de medula e a de um dos produtos obtidos após carbóxi-metilação indicam que, de fato, parte da estrutura morfológica da medula é destruída pela reação de carbóxi-metilação. Os resultados obtidos sugerem ainda que produtos com características superiores de retenção de líquidos podem ser preparados a partir de medula submetida a processos de polpação que resultem na maior preservação das cadeias celulósicas no que diz respeito ao grau de polimerização. Trabalho nesse sentido, empregando polpas Soda / Antraquinona de medula, se encontra em andamento em nossos laboratórios. Agradecimentos Os autores agradecem à CAPES a bolsa de Mestrado concedida a Cibele M.F.Martinez durante a realização deste trabalho. Referências Bibliográficas 1. Rowell,R.; Workshop Internacional Aplicação de fibras vegetais na indústria automobilística ; CNPDIA / EMBRAPA (1996). 2. Avaliação da evolução da safra 94/95. Posição em 28/02/95. AIAA - SIAESP - SIFAESP. São Paulo (1995). 3. Paturau, J.M. - By-Products of Sugar Cane Bagasse ; Elsevier Publ. Comp.- Amsterdam/ London/New York, Part II (1969). 4. Campana Filho,S.P.; Curvelo,A.A.S.; Caraschi - J. Braz.Assoc.Advanc. Sci., 45(1), (1993). 5. Curvelo A.A.S.; Pereira, R.E.; Campana Filho,S.P.; Gandini,A.- submetido a Cellulose. 6. Mattoso, L.H.C.; Zucolloto,V.; Paterno,L.G.; Griethuijsen,R.; Ferreira,M.; Oliveira Jr.,O.N.; Campana Filho,S.P. - Synthetic Metals 71, (1995). 7. Engelhardt,F.; Ebert,G.; Funk,R. - Advanced Materials 4(3), (1992). 8. Anberger,U.; Oppermann,W. - Polymer 31, (1990). 9. Nissan,A.H.; Hunger,G.K.; Sternstein,S.S. - Encyclopedia of Polymer Science and Technology ; vol.3,190; Ed.H.F.Mark, Interscience, New York (1965). 10. Oppermann,W.; Rose,S.; Rehage,G. - Br.Polym.J. 17, 175 (1985). 11.Flory,P.J. - Principles of Polymer Chemistry, Cornell University Press, Ithaca, New york (1953). 12. U.S..Patent (1974). 13. U.S.Patent (1987). 14. ABTCP - Normas da Associação Brasileira Técnica de Papel e Celulose. São Paulo - Brasil. 15. TAPPI STANDARDS - Testing Procedures of Technical Association of the Pulp and Paper Industry. Atlanta / Estados Unidos da América do Norte. 16. SCAN - C15:62 - Scandinavian Pulp, Paper and Board - Viscosity of Cellulose in Cupric - ethylenediamine solution (CED) (1962). 17. Ho,F.F.; Klosiewicz,D.W. - Anal.Chem. 52, (1980). 18. Wilson,K - Svensk Papper. 20, (1960). 19. Curvelo,A.A.S.; Pereira,R. - The 8 th International Symposium on Wood and Pulping Chemistry, Proceedings Vol.II, 473; Finland (1995). 20. Curvelo,A.A.S.; Caraschi,J.C.; Campana Filho, Polímeros, Ciência e Tecnologia jul/set, (1996). 21. Martinez,C.M.F., Obtenção e Caracterização de Materiais Absorventes através de Carboximetilação de Polpa de Etanol/Água de Medula de Bagaço de Cana-de-Acúcar, Dissertação de Mestrado apresentada ao IQSC/USP (1996). 22. Rice,S.A.; Nagasawa,M. - Polyelectrolyte Solutions ; Academic Press, London/New York (1961). 23. Tanaka,T. - Scientific American 244, (1981). 24. Khare,A.R.; Peppas,N.A. - Polymer 34, (1993). 25. Bershtein,V.A.; Egorov,V.M. - Diferential Scanning Calorimetry of Polymers, p Ed. by Ellis Horwood Limited (1994). 26. Seo,T.; Iijima,T. - Biotechnology and Polymers p Ed. by C.G.Gebelein - Plenum Press (1991). Polímeros: Ciência e Tecnologia - Jan/Mar
Preparação e Caracterização de Polpas para Dissolução Obtidas a Partir de Bagaço de Cana-de-Açúcar
 Preparação e Caracterização de Polpas para Dissolução Obtidas a Partir de Bagaço de Cana-de-Açúcar José Claudio Caraschi, Sergio P. Campana Filho e Antonio Aprígio S. Curvelo Resumo: Este trabalho descreve
Preparação e Caracterização de Polpas para Dissolução Obtidas a Partir de Bagaço de Cana-de-Açúcar José Claudio Caraschi, Sergio P. Campana Filho e Antonio Aprígio S. Curvelo Resumo: Este trabalho descreve
ESTUDO DO PROCESSO DE RECUPERAÇÃO E FRACIONAMENTO DA LIGNINA PROVENIENTE DE RESÍDUOS LIGNOCELULÓSICOS
 ESTUDO DO PROCESSO DE RECUPERAÇÃO E FRACIONAMENTO DA LIGNINA PROVENIENTE DE RESÍDUOS LIGNOCELULÓSICOS A.A. MORANDIM-GIANNETTI 1, J.M. SILVA 1, I.A. PEREIRA 1 1 Centro Universitário do FEI - Departamento
ESTUDO DO PROCESSO DE RECUPERAÇÃO E FRACIONAMENTO DA LIGNINA PROVENIENTE DE RESÍDUOS LIGNOCELULÓSICOS A.A. MORANDIM-GIANNETTI 1, J.M. SILVA 1, I.A. PEREIRA 1 1 Centro Universitário do FEI - Departamento
Característica principal: tratamento químico seguido de desfibramento/refino em um refinador de disco
 POLPAÇÃO SEMI-QUÍMICA (ou quimiomecânica) Característica principal: tratamento químico seguido de desfibramento/refino em um refinador de disco >> O processo semiquímico mais desenvolvido é o NSSC (Neutral
POLPAÇÃO SEMI-QUÍMICA (ou quimiomecânica) Característica principal: tratamento químico seguido de desfibramento/refino em um refinador de disco >> O processo semiquímico mais desenvolvido é o NSSC (Neutral
Sumário do tópico Breve revisão sobre celulose e matéria prima para produção de derivados de celulose
 Derivados de Celulose Sumário do tópico Breve revisão sobre celulose e matéria prima para produção de derivados de celulose Processos de preparação de derivados com aplicação comercial - celulosato de
Derivados de Celulose Sumário do tópico Breve revisão sobre celulose e matéria prima para produção de derivados de celulose Processos de preparação de derivados com aplicação comercial - celulosato de
Reações em meio ácido Sumário e objetivo das aulas (2 aulas)
 Reações em meio ácido Sumário e objetivo das aulas (2 aulas) 1. que ocorre com um lignocelulósico exposto ao meio ácido? - Quais grupos funcionais podem reagir? 2. Reações dos polissacarídeos - ligação
Reações em meio ácido Sumário e objetivo das aulas (2 aulas) 1. que ocorre com um lignocelulósico exposto ao meio ácido? - Quais grupos funcionais podem reagir? 2. Reações dos polissacarídeos - ligação
3033 Síntese do ácido acetilenodicarboxílico a partir de ácido meso dibromosuccínico
 3033 Síntese do ácido acetilenodicarboxílico a partir de ácido meso dibromosuccínico HOOC H Br Br H COOH KOH HOOC COOH C 4 H 4 Br 2 O 4 C 4 H 2 O 4 (275.9) (56.1) (114.1) Classificação Tipos de reação
3033 Síntese do ácido acetilenodicarboxílico a partir de ácido meso dibromosuccínico HOOC H Br Br H COOH KOH HOOC COOH C 4 H 4 Br 2 O 4 C 4 H 2 O 4 (275.9) (56.1) (114.1) Classificação Tipos de reação
POLPAÇÃO ALCALINA Principais processos: Soda e Sulfato (ou kraft)
 POLPAÇÃO ALCALINA Principais processos: Soda e Sulfato (ou kraft) O processo kraft é o mais importante processo alcalino de polpação Nos dois processos, o agente principal é o hidróxido de sódio, porém
POLPAÇÃO ALCALINA Principais processos: Soda e Sulfato (ou kraft) O processo kraft é o mais importante processo alcalino de polpação Nos dois processos, o agente principal é o hidróxido de sódio, porém
Produção de monossacarídeos por hidrólise
 Produção de monossacarídeos por hidrólise Referências Fengel D e Wegener, G, 1989. cap. 10 ação de ácidos Tuula Teeri e Gunnar Henriksson, 2009. Enzymes degrading wood components, In: Wood Chemistry and
Produção de monossacarídeos por hidrólise Referências Fengel D e Wegener, G, 1989. cap. 10 ação de ácidos Tuula Teeri e Gunnar Henriksson, 2009. Enzymes degrading wood components, In: Wood Chemistry and
POLPAÇÃO SEMI-QUÍMICA e QUÍMICA
 POLPAÇÃO SEMI-QUÍMICA e QUÍMICA Ref. básica para estudo: Capítulos 5 (revisão) e 6: Ek M, Gellerstedt G, Henriksson G. Pulping Chemistry and Technology (Volume 2). Berlin, Walter de Gruyter, 2009 Polpação
POLPAÇÃO SEMI-QUÍMICA e QUÍMICA Ref. básica para estudo: Capítulos 5 (revisão) e 6: Ek M, Gellerstedt G, Henriksson G. Pulping Chemistry and Technology (Volume 2). Berlin, Walter de Gruyter, 2009 Polpação
Calcule o ph de uma solução de HCl 1x10-7 mol L-1
 Calcule o ph de uma solução de HCl 1x10-7 mol L-1 TITULAÇÃO EM QUÍMICA ANALÍTICA Titulação Procedimento analítico, no qual a quantidade desconhecida de um composto é determinada através da reação deste
Calcule o ph de uma solução de HCl 1x10-7 mol L-1 TITULAÇÃO EM QUÍMICA ANALÍTICA Titulação Procedimento analítico, no qual a quantidade desconhecida de um composto é determinada através da reação deste
TITULAÇÃO EM QUÍMICA ANALÍTICA
 TITULAÇÃO EM QUÍMICA ANALÍTICA Titulação Procedimento analítico, no qual a quantidade desconhecida de um composto é determinada através da reação deste com um reagente padrão ou padronizado. Titulante
TITULAÇÃO EM QUÍMICA ANALÍTICA Titulação Procedimento analítico, no qual a quantidade desconhecida de um composto é determinada através da reação deste com um reagente padrão ou padronizado. Titulante
Aspectos da conversão de biomassas vegetais em Etanol 2G. Prof. Dr. Bruno Chaboli Gambarato
 Aspectos da conversão de biomassas vegetais em Etanol 2G Prof. Dr. Bruno Chaboli Gambarato Lorena 2016 Oferta Interna de Energia no Brasil (2014-2015) Fonte: Ministério de Minas e Energia (2016) Uso de
Aspectos da conversão de biomassas vegetais em Etanol 2G Prof. Dr. Bruno Chaboli Gambarato Lorena 2016 Oferta Interna de Energia no Brasil (2014-2015) Fonte: Ministério de Minas e Energia (2016) Uso de
POLPAÇÃO SEMI-QUÍMICA e QUÍMICA
 POLPAÇÃO SEMI-QUÍMICA e QUÍMICA Ref. básica para estudo: Capítulos 5 (revisão) e 6: Ek M, Gellerstedt G, Henriksson G. Pulping Chemistry and Technology (Volume 2). Berlin, Walter de Gruyter, 2009 Polpação
POLPAÇÃO SEMI-QUÍMICA e QUÍMICA Ref. básica para estudo: Capítulos 5 (revisão) e 6: Ek M, Gellerstedt G, Henriksson G. Pulping Chemistry and Technology (Volume 2). Berlin, Walter de Gruyter, 2009 Polpação
5007 Reação do anidrido ftálico com resorcinol para obtenção de fluoresceína
 57 Reação do anidrido ftálico com resorcinol para obtenção de fluoresceína CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Classificação Tipos de reações e classes das substâncias
57 Reação do anidrido ftálico com resorcinol para obtenção de fluoresceína CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Classificação Tipos de reações e classes das substâncias
INTRODUÇÃO À OBTENÇÃO DE CELULOSE E PAPEL UFPR - SCA - DETF. Polpa e Papel Tecnologia de produção de polpa celulósica e papel. Prof.
 INTRODUÇÃO À OBTENÇÃO DE CELULOSE E PAPEL UFPR - SCA - DETF Polpa e Papel Tecnologia de produção de polpa celulósica e papel Prof. Umberto Klock Objetivo Informar as energias utilizadas para os processos
INTRODUÇÃO À OBTENÇÃO DE CELULOSE E PAPEL UFPR - SCA - DETF Polpa e Papel Tecnologia de produção de polpa celulósica e papel Prof. Umberto Klock Objetivo Informar as energias utilizadas para os processos
SOLUÇÕES. 1. Concentração (C) 2. Concentração molar (M) C = massa de soluto / volume da solução. M = mol de soluto / volume de solução
 SOLUÇÕES Em Química, solução é o nome dado a dispersões cujo tamanho das moléculas dispersas é menor que 1 nanômetro. A solução ainda pode ser caracterizada por formar um sistema homogêneo (a olho nu e
SOLUÇÕES Em Química, solução é o nome dado a dispersões cujo tamanho das moléculas dispersas é menor que 1 nanômetro. A solução ainda pode ser caracterizada por formar um sistema homogêneo (a olho nu e
UNIVERSIDADE ESTADUAL PAULISTA CAMPUS DE BOTUCATU FACULDADE DE CIÊNCIAS AGRONÔMICAS PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIA FLORESTAL PLANO DE ENSINO
 PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIA FLORESTAL PLANO DE ENSINO IDENTIFICAÇÃO DA DISCIPLINA DISCIPLINA: Propriedades Físicas e Químicas da Madeira CÓDIGO: ÁREA: Domínio Específico ( x ) NÍVEL: Mestrado
PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIA FLORESTAL PLANO DE ENSINO IDENTIFICAÇÃO DA DISCIPLINA DISCIPLINA: Propriedades Físicas e Químicas da Madeira CÓDIGO: ÁREA: Domínio Específico ( x ) NÍVEL: Mestrado
4 Resultados Experimentais
 77 4 Resultados Experimentais As amostras soldadas de acordo com os parâmetros da tabela 3-2 do capítulo 3 foram submetidas aos ensaios mecânicos de tração e rigidez, análises térmicas (calorimetria diferencial
77 4 Resultados Experimentais As amostras soldadas de acordo com os parâmetros da tabela 3-2 do capítulo 3 foram submetidas aos ensaios mecânicos de tração e rigidez, análises térmicas (calorimetria diferencial
Capítulo 3 Celulose Propriedades da Celulose Conceito da Celulose Grau de Polimerização da Celulose (GP)...
 Sumário Capítulo 1 Estereoquímica... 1 1.1 Isomeria Óptica... 1 1.2 Estereoisômeros... 2 1.2.1 Misturas de Enantiômeros e Misturas Racêmicas... 2 1.2.2 Isomeria Óptica em Compostos Cíclicos... 5 1.3 Rotação
Sumário Capítulo 1 Estereoquímica... 1 1.1 Isomeria Óptica... 1 1.2 Estereoisômeros... 2 1.2.1 Misturas de Enantiômeros e Misturas Racêmicas... 2 1.2.2 Isomeria Óptica em Compostos Cíclicos... 5 1.3 Rotação
APLICAÇÃO DE QUITOSANA MODIFICADA COMO CATALISADOR HETEROGÊNEO NA PRODUÇÃO DE BIODIESEL POR ESTERIFICAÇÃO
 APLICAÇÃO DE QUITOSANA MODIFICADA COMO CATALISADOR HETEROGÊNEO NA PRODUÇÃO DE BIODIESEL POR ESTERIFICAÇÃO D. GURGEL 1, A. L. FREIRE 1, B. J. P. COSTA 1, I. L. LUCENA 1 e Z. M. dos SANTOS 1 1 Universidade
APLICAÇÃO DE QUITOSANA MODIFICADA COMO CATALISADOR HETEROGÊNEO NA PRODUÇÃO DE BIODIESEL POR ESTERIFICAÇÃO D. GURGEL 1, A. L. FREIRE 1, B. J. P. COSTA 1, I. L. LUCENA 1 e Z. M. dos SANTOS 1 1 Universidade
QUÍMICA PRIMEIRA ETAPA
 QUÍMICA PRIMEIRA ETAPA - 1999 QUESTÃO 46 Um limão foi espremido num copo contendo água e as sementes ficaram no fundo do recipiente. A seguir, foi adicionado ao sistema um pouco de açúcar, que se dissolveu
QUÍMICA PRIMEIRA ETAPA - 1999 QUESTÃO 46 Um limão foi espremido num copo contendo água e as sementes ficaram no fundo do recipiente. A seguir, foi adicionado ao sistema um pouco de açúcar, que se dissolveu
Reações em meio ácido Sumário e objetivo da aula (2 aulas)
 Reações em meio ácido Sumário e objetivo da aula (2 aulas) 1. que ocorre com um lignocelulósico exposto ao meio ácido? - Quais grupos funcionais podem reagir? 2. Reações dos polissacarídeos - ligação glicosídica
Reações em meio ácido Sumário e objetivo da aula (2 aulas) 1. que ocorre com um lignocelulósico exposto ao meio ácido? - Quais grupos funcionais podem reagir? 2. Reações dos polissacarídeos - ligação glicosídica
3016 Oxidação do ácido ricinoléico a ácido azeláico (a partir de óleo de rícino) com KMnO 4
 6 Oxidação do ácido ricinoléico a ácido azeláico (a partir de óleo de rícino) com KMnO 4 CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Classificação
6 Oxidação do ácido ricinoléico a ácido azeláico (a partir de óleo de rícino) com KMnO 4 CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Classificação
3003 Síntese de 2-cloro-ciclohexanol a partir de ciclohexeno
 3003 Síntese de 2-cloro-ciclohexanol a partir de ciclohexeno _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7
3003 Síntese de 2-cloro-ciclohexanol a partir de ciclohexeno _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7
4023 Síntese do éster etílico do ácido 2-cicclopentanona carboxílico a partir do éster dietílico do ácido adípico
 NP 4023 Síntese do éster etílico do ácido 2-cicclopentanona carboxílico a partir do éster dietílico do ácido adípico NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202,2) (23,0) (46,1) (156,2) Classificação Tipos
NP 4023 Síntese do éster etílico do ácido 2-cicclopentanona carboxílico a partir do éster dietílico do ácido adípico NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202,2) (23,0) (46,1) (156,2) Classificação Tipos
UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO
 UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO 08/11/2010 PROVA ESCRITA Assinatura do candidato: Área de concentração:
UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO 08/11/2010 PROVA ESCRITA Assinatura do candidato: Área de concentração:
Estudo Estudo da Química
 Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 16 CONCENTRAÇÃO DE SOLUÇÕES 1.
Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 16 CONCENTRAÇÃO DE SOLUÇÕES 1.
SOLUÇÕES Folha 01 João Roberto Mazzei
 01. (PUC SP 2009) O gráfico a seguir representa a curva de solubilidade do nitrato de potássio (KNO 3) em água. A 70 C, foram preparadas duas soluções, cada uma contendo 70 g de nitrato de potássio (KNO
01. (PUC SP 2009) O gráfico a seguir representa a curva de solubilidade do nitrato de potássio (KNO 3) em água. A 70 C, foram preparadas duas soluções, cada uma contendo 70 g de nitrato de potássio (KNO
3005 Síntese de 7,7-diclorobiciclo [4.1.0] heptano (7,7- dicloronorcarano) a partir de ciclohexeno
![3005 Síntese de 7,7-diclorobiciclo [4.1.0] heptano (7,7- dicloronorcarano) a partir de ciclohexeno 3005 Síntese de 7,7-diclorobiciclo [4.1.0] heptano (7,7- dicloronorcarano) a partir de ciclohexeno](/thumbs/61/45682965.jpg) 00 Síntese de,-diclorobiciclo [..0] heptano (,- dicloronorcarano) a partir de ciclohexeno + CHCl NaOH tri-n-propylamine CCl + HCl C H 0 (8.) (9.) NaOH C 9 H N C H 0 Cl (0.0) (.) (.) (.) Classificação Tipos
00 Síntese de,-diclorobiciclo [..0] heptano (,- dicloronorcarano) a partir de ciclohexeno + CHCl NaOH tri-n-propylamine CCl + HCl C H 0 (8.) (9.) NaOH C 9 H N C H 0 Cl (0.0) (.) (.) (.) Classificação Tipos
Química Analítica I Tratamento dos dados analíticos Soluções analíticas
 Química Analítica I Tratamento dos dados analíticos Soluções analíticas Profª Simone Noremberg Kunz 2 Mol Medidas em química analítica É a quantidade de uma espécie química que contém 6,02x10 23 partículas
Química Analítica I Tratamento dos dados analíticos Soluções analíticas Profª Simone Noremberg Kunz 2 Mol Medidas em química analítica É a quantidade de uma espécie química que contém 6,02x10 23 partículas
3001 Hidroboração/oxidação de 1-octeno a 1-octanol
 3001 Hidroboração/oxidação de 1-octeno a 1-octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Referência Bibliográfica A.S. Bhanu
3001 Hidroboração/oxidação de 1-octeno a 1-octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Referência Bibliográfica A.S. Bhanu
TÍTULO: ANÁLISE TITRIMÉTRICA (Volumétrica)
 Componente Curricular: Química dos Alimentos Prof. Barbosa e Prof. Daniel 4º Módulo de Química Procedimento de Prática Experimental Competências: Identificar as propriedades dos alimentos. Identificar
Componente Curricular: Química dos Alimentos Prof. Barbosa e Prof. Daniel 4º Módulo de Química Procedimento de Prática Experimental Competências: Identificar as propriedades dos alimentos. Identificar
SOLUÇÕES. C = massa de soluto / volume da solução. A unidade usual para concentração é gramas por litro (g/l). M = mol de soluto / volume de solução
 SOLUÇÕES 1. Concentração (C) C = massa de soluto / volume da solução A unidade usual para concentração é gramas por litro (g/l). 2. Concentração molar (M) M = mol de soluto / volume de solução A unidade
SOLUÇÕES 1. Concentração (C) C = massa de soluto / volume da solução A unidade usual para concentração é gramas por litro (g/l). 2. Concentração molar (M) M = mol de soluto / volume de solução A unidade
SOLUÇÕES PREPARO DE SOLUÇÕES. 1. Concentração (C) 3. Percentagem em massa ou em volume. 2. Concentração molar (M)
 PREPARO DE SOLUÇÕES SOLUÇÕES (a) (b) (c) 1. Concentração (C) C = massa de soluto / volume da solução A unidade usual para concentração é gramas por litro (g/l). 2. Concentração molar (M) M = mol de soluto
PREPARO DE SOLUÇÕES SOLUÇÕES (a) (b) (c) 1. Concentração (C) C = massa de soluto / volume da solução A unidade usual para concentração é gramas por litro (g/l). 2. Concentração molar (M) M = mol de soluto
QUÍMICA Tipos de soluções Edson Mesquita
 QUÍMICA Tipos de soluções Edson Mesquita 1 Soluções Uma solução é uma mistura homogênea de substâncias puras (átomos, moléculas ou íons) na qual não há precipitação. Substância pura: substância com composição
QUÍMICA Tipos de soluções Edson Mesquita 1 Soluções Uma solução é uma mistura homogênea de substâncias puras (átomos, moléculas ou íons) na qual não há precipitação. Substância pura: substância com composição
Diagrama simplificado do processo kraft. Branqueamento
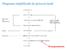 Diagrama simplificado do processo kraft Branqueamento Branqueamento de polpas celulósicas Dois tipos básicos: a) eliminação de material responsável pela cor - usado em polpas químicas b) transformação
Diagrama simplificado do processo kraft Branqueamento Branqueamento de polpas celulósicas Dois tipos básicos: a) eliminação de material responsável pela cor - usado em polpas químicas b) transformação
TITULAÇÃO EM QUÍMICA ANALÍTICA
 TITULAÇÃO EM QUÍMICA ANALÍTICA Titulação Procedimento analítico, no qual a quantidade desconhecida de um composto é determinada através da reação deste com um reagente padrão ou padronizado. Titulante
TITULAÇÃO EM QUÍMICA ANALÍTICA Titulação Procedimento analítico, no qual a quantidade desconhecida de um composto é determinada através da reação deste com um reagente padrão ou padronizado. Titulante
LISTA DE EXERCÍCIOS # 05 QUÍMICA ANALÍTICA PROF. Wendell
 LISTA DE EXERCÍCIOS # 05 QUÍMICA ANALÍTICA PROF. Wendell 1. Considere uma solução aquosa de NH 3, preparada na concentração de 0,100 mol L -1. Calcule o ph desta solução. Use K b = 1,8 10-5. 2. Uma alíquota
LISTA DE EXERCÍCIOS # 05 QUÍMICA ANALÍTICA PROF. Wendell 1. Considere uma solução aquosa de NH 3, preparada na concentração de 0,100 mol L -1. Calcule o ph desta solução. Use K b = 1,8 10-5. 2. Uma alíquota
1011 Síntese do 1,4-di-terc-butil benzeno a partir do terc-butil benzeno e cloreto de terc-butila.
 1011 Síntese do 1,4-di-terc-butil benzeno a partir do terc-butil benzeno e cloreto de terc-butila. + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Classificação Tipos de Reações e
1011 Síntese do 1,4-di-terc-butil benzeno a partir do terc-butil benzeno e cloreto de terc-butila. + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Classificação Tipos de Reações e
PROCESSOS QUÍMICOS INDUSTRIAIS I
 PROCESSOS QUÍMICOS INDUSTRIAIS I INDÚSTRIAS DE CLORO-ÁLCALIS INTRODUÇÃO INDÚSTRIAS DE CLORO-ÁLCALIS: Na 2 CO 3 SODA CÁUSTICA NaOH CLORO Essas substâncias estão entre as mais importantes das indústrias
PROCESSOS QUÍMICOS INDUSTRIAIS I INDÚSTRIAS DE CLORO-ÁLCALIS INTRODUÇÃO INDÚSTRIAS DE CLORO-ÁLCALIS: Na 2 CO 3 SODA CÁUSTICA NaOH CLORO Essas substâncias estão entre as mais importantes das indústrias
1017 Acoplamento Azo do cloreto de benzenodiazônio com 2- naftol, originando 1-fenilazo-2-naftol
 OP 1017 Acoplamento Azo do cloreto de benzenodiazônio com 2- naftol, originando 1-fenilazo-2-naftol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl
OP 1017 Acoplamento Azo do cloreto de benzenodiazônio com 2- naftol, originando 1-fenilazo-2-naftol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl
Professor: Fábio Silva SOLUÇÕES
 Professor: Fábio Silva SOLUÇÕES Solvente: Substância que apresenta o mesmo estado de agregação da solução; Substância encontrada em maior quantidade. SOLUÇÃO É uma mistura homogênea de dois ou mais componentes.
Professor: Fábio Silva SOLUÇÕES Solvente: Substância que apresenta o mesmo estado de agregação da solução; Substância encontrada em maior quantidade. SOLUÇÃO É uma mistura homogênea de dois ou mais componentes.
1004 Nitração do N-óxido de piridina para N-óxido de 4- nitropiridina
 1004 Nitração do N-óxido de piridina para N-óxido de 4- nitropiridina O N HNO 3 /H 2 SO 4 O N NO 2 C 5 H 5 NO (95,1) (63,0) (98,1) C 5 H 4 N 2 O 3 (140,1) Classificação Tipos de reações e classes de substâncias
1004 Nitração do N-óxido de piridina para N-óxido de 4- nitropiridina O N HNO 3 /H 2 SO 4 O N NO 2 C 5 H 5 NO (95,1) (63,0) (98,1) C 5 H 4 N 2 O 3 (140,1) Classificação Tipos de reações e classes de substâncias
Diagrama simplificado do processo kraft. Branqueamento
 Diagrama simplificado do processo kraft Branqueamento A figura abaixo mostra como o rendimento é afetado no final do processo de polpação kraft. Se você necessitasse preparar polpas com número kappa =
Diagrama simplificado do processo kraft Branqueamento A figura abaixo mostra como o rendimento é afetado no final do processo de polpação kraft. Se você necessitasse preparar polpas com número kappa =
Curva de titulação efeito da concentração
 Exercício 1) Considere a titulação de 100 ml de solução HCl 0,0100 mol L -1 com solução padrão de NaOH 0,0500 mol L -1. Calcule o ph da solução do titulado após a adição das seguintes quantidades de titulante:
Exercício 1) Considere a titulação de 100 ml de solução HCl 0,0100 mol L -1 com solução padrão de NaOH 0,0500 mol L -1. Calcule o ph da solução do titulado após a adição das seguintes quantidades de titulante:
TITULAÇÃO EM QUÍMICA ANALÍTICA
 TITULAÇÃO EM QUÍMICA ANALÍTICA Titulação Procedimento analítico, no qual a quantidade desconhecida de um composto é determinada através da reação deste com um reagente padrão ou padronizado. Titulante
TITULAÇÃO EM QUÍMICA ANALÍTICA Titulação Procedimento analítico, no qual a quantidade desconhecida de um composto é determinada através da reação deste com um reagente padrão ou padronizado. Titulante
QUÍMICA - 2 o ANO MÓDULO 03 SOLUÇÕES: INTRODUÇÃO - PARTE 3
 QUÍMICA - 2 o ANO MÓDULO 03 SOLUÇÕES: INTRODUÇÃO - PARTE 3 Fixação 1) (PUC) No preparo de solução alvejante de tinturaria, 521,5g de hipoclorito de sódio são dissolvidos em água suficiente para 10,0 litros
QUÍMICA - 2 o ANO MÓDULO 03 SOLUÇÕES: INTRODUÇÃO - PARTE 3 Fixação 1) (PUC) No preparo de solução alvejante de tinturaria, 521,5g de hipoclorito de sódio são dissolvidos em água suficiente para 10,0 litros
4009 Síntese de ácido adípico a partir do ciclohexeno
 4009 Síntese de ácido adípico a partir do ciclohexeno C 6 H 10 (82,2) + tungstato de sódio dihidratado 4 H 2 H + 2 H + 4 H 2 + Aliquat 336. Na 2 W 4 2 H 2 (329,9) C 6 H 10 4 (34,0) C 25 H 54 ClN (404,2)
4009 Síntese de ácido adípico a partir do ciclohexeno C 6 H 10 (82,2) + tungstato de sódio dihidratado 4 H 2 H + 2 H + 4 H 2 + Aliquat 336. Na 2 W 4 2 H 2 (329,9) C 6 H 10 4 (34,0) C 25 H 54 ClN (404,2)
SOLUÇÕES. C = massa de soluto / volume da solução. A unidade usual para concentração é gramas por litro (g/l). M = mol de soluto / volume de solução
 SOLUÇÕES 1. Concentração (C) C = massa de soluto / volume da solução A unidade usual para concentração é gramas por litro (g/l). 2. Concentração molar (M) M = mol de soluto / volume de solução A unidade
SOLUÇÕES 1. Concentração (C) C = massa de soluto / volume da solução A unidade usual para concentração é gramas por litro (g/l). 2. Concentração molar (M) M = mol de soluto / volume de solução A unidade
Produção de Açúcar. Processos Químicos Industriais II
 Produção de Açúcar Processos Químicos Industriais II Energia Brasil Moagem de cana de açúcar da safra 2013/2014 acumulada até 01/06/2013 somou aproximadamente 105 milhões de toneladas. Ainda de acordo
Produção de Açúcar Processos Químicos Industriais II Energia Brasil Moagem de cana de açúcar da safra 2013/2014 acumulada até 01/06/2013 somou aproximadamente 105 milhões de toneladas. Ainda de acordo
CPV seu pé direito também na Medicina
 seu pé direito também na Medicina UNIFESP 17/dezembro/2010 QUÍMICA 06. Ligas metálicas são comuns no cotidiano e muito utilizadas nas indústrias automobilística, aeronáutica, eletrônica e na construção
seu pé direito também na Medicina UNIFESP 17/dezembro/2010 QUÍMICA 06. Ligas metálicas são comuns no cotidiano e muito utilizadas nas indústrias automobilística, aeronáutica, eletrônica e na construção
4005 Síntese do éster metílico do ácido 9-(5-oxotetra-hidrofuran- 2-ila) nonanóico
 4005 Síntese do éster metílico do ácido 9-(5-oxotetra-hidrofuran- 2-ila) nonanóico H (CH I 2 ) 8 C + 3 C CH 2 CH 3 H 3 C (CH 2 ) 8 CH 3 CH 2 I C 12 H 22 2 C 4 H 7 I 2 C 14 H 24 4 C 2 H 5 I (198,3) (214,0)
4005 Síntese do éster metílico do ácido 9-(5-oxotetra-hidrofuran- 2-ila) nonanóico H (CH I 2 ) 8 C + 3 C CH 2 CH 3 H 3 C (CH 2 ) 8 CH 3 CH 2 I C 12 H 22 2 C 4 H 7 I 2 C 14 H 24 4 C 2 H 5 I (198,3) (214,0)
4028 Síntese de 1-bromodecano a partir de 1-dodecanol
 4028 Síntese de 1-bromodecano a partir de 1-dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Classificação Tipos de reações e classes das substâncias
4028 Síntese de 1-bromodecano a partir de 1-dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Classificação Tipos de reações e classes das substâncias
Aprender a preparar soluções aquosas, realizar diluições e determinar suas concentrações.
 EXPERIMENTO 2 Preparação e Padronização de Soluções OBJETIVOS Rever os conceitos de concentração de soluções. Aprender a preparar soluções aquosas, realizar diluições e determinar suas concentrações. Exercitar
EXPERIMENTO 2 Preparação e Padronização de Soluções OBJETIVOS Rever os conceitos de concentração de soluções. Aprender a preparar soluções aquosas, realizar diluições e determinar suas concentrações. Exercitar
Soluções, concentrações e diluições
 Soluções, concentrações e diluições Mistura homogênea constituída: soluto (presente em menor quantidade) solvente (presente em maior quantidade). MASSA MOLECULAR: soma das massas atômicas de cada átomo
Soluções, concentrações e diluições Mistura homogênea constituída: soluto (presente em menor quantidade) solvente (presente em maior quantidade). MASSA MOLECULAR: soma das massas atômicas de cada átomo
4002 Síntese de benzil a partir da benzoína
 4002 Síntese de benzil a partir da benzoína H + 1 / 2 2 VCl 3 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212,3) 173,3 (210,2) Classificação Tipos de reações e classes de substâncias oxidação álcool, cetona,
4002 Síntese de benzil a partir da benzoína H + 1 / 2 2 VCl 3 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212,3) 173,3 (210,2) Classificação Tipos de reações e classes de substâncias oxidação álcool, cetona,
4001 Transesterificação do óleo de mamona em ricinoleato de metila
 4001 Transesterificação do óleo de mamona em ricinoleato de metila Classificação Tipos de reações e classes de substâncias. Reação do grupo carbonila de derivados do ácido carboxílico, trans-esterificação,
4001 Transesterificação do óleo de mamona em ricinoleato de metila Classificação Tipos de reações e classes de substâncias. Reação do grupo carbonila de derivados do ácido carboxílico, trans-esterificação,
Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente.
 SOLUÇÕES Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente. Fase: numa mistura, é cada uma das porções que apresenta aspecto homogéneo ou uniforme. CLASSIFICAÇÃO
SOLUÇÕES Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente. Fase: numa mistura, é cada uma das porções que apresenta aspecto homogéneo ou uniforme. CLASSIFICAÇÃO
CONHEÇA AS PRINCIPAIS ETAPAS QUÍMICAS NA INDÚSTRIA DE CELULOSE. Processos Químicos Industriais II
 CONHEÇA AS PRINCIPAIS ETAPAS QUÍMICAS NA INDÚSTRIA DE CELULOSE E PAPEL Processos Químicos Industriais II POLPAÇÃO QUÍMICA Os cavacos são cozidos em licores ou lixívias, isto é, em soluções aquosas contendo
CONHEÇA AS PRINCIPAIS ETAPAS QUÍMICAS NA INDÚSTRIA DE CELULOSE E PAPEL Processos Químicos Industriais II POLPAÇÃO QUÍMICA Os cavacos são cozidos em licores ou lixívias, isto é, em soluções aquosas contendo
a) 20 d) 100 b) 40 e) 160 c) 80
 01) (Unifesp-SP) Uma solução contendo 14 g de cloreto de sódio dissolvidos em 200 ml de água foi deixada em um frasco aberto, a 30 C. Após algum tempo, começou a cristalizar o soluto. Qual volume mínimo
01) (Unifesp-SP) Uma solução contendo 14 g de cloreto de sódio dissolvidos em 200 ml de água foi deixada em um frasco aberto, a 30 C. Após algum tempo, começou a cristalizar o soluto. Qual volume mínimo
4 PROCEDIMENTO EXPERIMENTAL
 34 4 PROCEDIMENTO EXPERIMENTAL 4.1. Metodologia Experimental Figura 7 - Fluxograma geral do processo experimental com o uso de NaOH na ustulação 35 A figura 7 mostra o fluxograma geral do processo. Ele
34 4 PROCEDIMENTO EXPERIMENTAL 4.1. Metodologia Experimental Figura 7 - Fluxograma geral do processo experimental com o uso de NaOH na ustulação 35 A figura 7 mostra o fluxograma geral do processo. Ele
4 Materiais e Métodos
 62 4 Materiais e Métodos Neste capítulo serão apresentados os materiais, reagentes e equipamentos, assim como as metodologias experimentais utilizadas na realização deste trabalho. 4.1. Obtenção e preparo
62 4 Materiais e Métodos Neste capítulo serão apresentados os materiais, reagentes e equipamentos, assim como as metodologias experimentais utilizadas na realização deste trabalho. 4.1. Obtenção e preparo
INTRODUÇÃO À QUÍMICA
 INTRODUÇÃO À QUÍMICA O QUE É QUÍMICA? É a ciência que estuda a matéria, suas propriedades, transformações e interações, bem como a energia envolvida nestes processos. QUAL A IMPORTÂNCIA DA QUÍMICA? Entender
INTRODUÇÃO À QUÍMICA O QUE É QUÍMICA? É a ciência que estuda a matéria, suas propriedades, transformações e interações, bem como a energia envolvida nestes processos. QUAL A IMPORTÂNCIA DA QUÍMICA? Entender
Química Orgânica Experimental I BAC CRITÉRIOS PARA CORREÇÃO DOS PRÉ-RELATÓRIOS E RELATÓRIOS
 Química Orgânica Experimental I BAC - 2009 CRITÉRIOS PARA CORREÇÃO DOS PRÉ-RELATÓRIOS E RELATÓRIOS Além do aqui solicitado para os Pré-Relatórios, devem ser apresentados os itens correspondentes a cada
Química Orgânica Experimental I BAC - 2009 CRITÉRIOS PARA CORREÇÃO DOS PRÉ-RELATÓRIOS E RELATÓRIOS Além do aqui solicitado para os Pré-Relatórios, devem ser apresentados os itens correspondentes a cada
PAG Química Estequiometria
 1. 2. 3. Em países de clima desfavorável ao cultivo de cana-de-açúcar, o etanol (C 2 H 6 O) é sintetizado através da reação de eteno (C 2 H 4 ) com vapor de água, a alta temperatura e alta pressão, segundo
1. 2. 3. Em países de clima desfavorável ao cultivo de cana-de-açúcar, o etanol (C 2 H 6 O) é sintetizado através da reação de eteno (C 2 H 4 ) com vapor de água, a alta temperatura e alta pressão, segundo
4014 Separação enantiomérica de (R)- e (S)-2,2'-dihidroxi-1,1'- binaftil ((R)- e (S)-1,1-bi-2-naftol)
 4014 Separação enantiomérica de (R)- e (S)-2,2'-dihidroxi-1,1'- binaftil ((R)- e (S)-1,1-bi-2-naftol) NBCC CH 3 CN + C 20 H 14 O 2 C 26 H 29 ClN 2 O (286,3) (421,0) R-enantiômero S-enantiômero Classificação
4014 Separação enantiomérica de (R)- e (S)-2,2'-dihidroxi-1,1'- binaftil ((R)- e (S)-1,1-bi-2-naftol) NBCC CH 3 CN + C 20 H 14 O 2 C 26 H 29 ClN 2 O (286,3) (421,0) R-enantiômero S-enantiômero Classificação
4024 Síntese enantioseletiva do éster etílico do ácido (1R,2S)-cishidroxiciclopentano-carboxílico
 4024 Síntese enantioseletiva do éster etílico do ácido (1R,2S)-cishidroxiciclopentano-carboxílico H levedura C 8 H 12 3 C 8 H 14 3 (156,2) (158,2) Classificação Tipos de reação e classes de substâncias
4024 Síntese enantioseletiva do éster etílico do ácido (1R,2S)-cishidroxiciclopentano-carboxílico H levedura C 8 H 12 3 C 8 H 14 3 (156,2) (158,2) Classificação Tipos de reação e classes de substâncias
aplicável aos estudos de fraccionamento detalhado das paredes celulares. No entanto, o material das
 7 - Conclusões 190 O resíduo insolúvel em álcool obtido a partir da polpa da azeitona tinha uma quantidade bastante grande de proteína e compostos fenólicos co-precipitados e, por tal motivo, não se tornou
7 - Conclusões 190 O resíduo insolúvel em álcool obtido a partir da polpa da azeitona tinha uma quantidade bastante grande de proteína e compostos fenólicos co-precipitados e, por tal motivo, não se tornou
POLIOSES (Hemiceluloses)
 UFPR/DETF Disciplina QUÍMICA DA MADEIRA POLIOSES (emiceluloses) Prof. Dr. Umberto Klock MADEIRA Polioses 2 CAMADAS DA PAREDE CELULAR Camada Espessura, µm LM 0,2-1,0 lignina, pectinas Composição P 0,1-0,2
UFPR/DETF Disciplina QUÍMICA DA MADEIRA POLIOSES (emiceluloses) Prof. Dr. Umberto Klock MADEIRA Polioses 2 CAMADAS DA PAREDE CELULAR Camada Espessura, µm LM 0,2-1,0 lignina, pectinas Composição P 0,1-0,2
Prova de conhecimento em Química Analítica DQ/UFMG
 CÓDIGO DO(A) CANDIDATO(A): Questão 1A. Considere os seguintes reagentes: I) KF sólido com teor de pureza de 95,0% m/m II) HF 28,0% m/m, d = 1,02 kg L -1, pk a = 3,17 III) KOH 0,400 mol L -1 a) Calcule
CÓDIGO DO(A) CANDIDATO(A): Questão 1A. Considere os seguintes reagentes: I) KF sólido com teor de pureza de 95,0% m/m II) HF 28,0% m/m, d = 1,02 kg L -1, pk a = 3,17 III) KOH 0,400 mol L -1 a) Calcule
Definição: As dispersões são misturas nas quais uma substância está disseminada na forma de partículas no interior de uma outra substância.
 Definição: As dispersões são misturas nas quais uma substância está disseminada na forma de partículas no interior de uma outra substância. Vejamos alguns exemplos: Ao agitar a mistura, a sacarose (disperso)
Definição: As dispersões são misturas nas quais uma substância está disseminada na forma de partículas no interior de uma outra substância. Vejamos alguns exemplos: Ao agitar a mistura, a sacarose (disperso)
Química FUVEST ETAPA. Resposta QUESTÃO 1 QUESTÃO 2
 Química FUVEST QUESTÃO 1 Em uma aula de laboratório de Química, a professora propôs a realização da eletrólise da água. Após a montagem de uma aparelhagem como a da figura a seguir, e antes de iniciar
Química FUVEST QUESTÃO 1 Em uma aula de laboratório de Química, a professora propôs a realização da eletrólise da água. Após a montagem de uma aparelhagem como a da figura a seguir, e antes de iniciar
Keliene M. Amaral, Adilson R. Gonçalves, Júlio C. Santos. Universidade de São Paulo/Escola de Engenharia de Lorena.
 Obtenção de membranas filtrantes de acetato de celulose a partir de bagaço de cana-de-açúcar: avaliação de diferentes opções de branqueamento da polpa celulósica Keliene M. Amaral, Adilson R. Gonçalves,
Obtenção de membranas filtrantes de acetato de celulose a partir de bagaço de cana-de-açúcar: avaliação de diferentes opções de branqueamento da polpa celulósica Keliene M. Amaral, Adilson R. Gonçalves,
Relatório 7 Determinação do produto de solubilidade do AgBrO3
 UNIVERSIDADE DE SÃO PAULO QUÍMICA GERAL Prof. Maria Regina Alcântara Relatório 7 Determinação do produto de solubilidade do AgBrO3 Mayara Moretti Vieira Palmieri 7159862 Rodrigo Tonon 7993766 Outubro,
UNIVERSIDADE DE SÃO PAULO QUÍMICA GERAL Prof. Maria Regina Alcântara Relatório 7 Determinação do produto de solubilidade do AgBrO3 Mayara Moretti Vieira Palmieri 7159862 Rodrigo Tonon 7993766 Outubro,
a) Escreva os nomes das substâncias presentes nos frascos A, B e C. A B C
 PROVA DE QUÍMICA 2ª ETAPA do VESTIBULAR 2006 (cada questão desta prova vale até cinco pontos) Questão 01 Foram encontrados, em um laboratório, três frascos A, B e C, contendo soluções incolores e sem rótulos.
PROVA DE QUÍMICA 2ª ETAPA do VESTIBULAR 2006 (cada questão desta prova vale até cinco pontos) Questão 01 Foram encontrados, em um laboratório, três frascos A, B e C, contendo soluções incolores e sem rótulos.
PROCESSOS QUÍMICOS INDUSTRIAIS I
 PROCESSOS QUÍMICOS INDUSTRIAIS I INDÚSTRIAS DE CLORO-ÁLCALIS LCALIS INTRODUÇÃO INDÚSTRIAS DE CLORO-ÁLCALIS: LCALIS: Na 2 CO 3 SODA CÁUSTICA C NaOH CLORO Essas substâncias estão entre as mais importantes
PROCESSOS QUÍMICOS INDUSTRIAIS I INDÚSTRIAS DE CLORO-ÁLCALIS LCALIS INTRODUÇÃO INDÚSTRIAS DE CLORO-ÁLCALIS: LCALIS: Na 2 CO 3 SODA CÁUSTICA C NaOH CLORO Essas substâncias estão entre as mais importantes
Equipe de Química QUÍMICA
 Aluno (a): Série: 3ª Turma: TUTORIAL 12R Ensino Médio Equipe de Química Data: QUÍMICA Mistura de soluções que não reagem entre si: Misturas de soluções de mesmo soluto quando misturamos soluções de mesmo
Aluno (a): Série: 3ª Turma: TUTORIAL 12R Ensino Médio Equipe de Química Data: QUÍMICA Mistura de soluções que não reagem entre si: Misturas de soluções de mesmo soluto quando misturamos soluções de mesmo
Diagrama simplificado do processo kraft
 Diagrama simplificado do processo kraft Ref. básica para estudo: Capítulos 6: Ek M, Gellerstedt G, Henriksson G. Pulping Chemistry and Technology (Volume 2). Berlin, Walter de Gruyter, 2009 https://www.youtube.com/watch?v=2uh3xiadm1a
Diagrama simplificado do processo kraft Ref. básica para estudo: Capítulos 6: Ek M, Gellerstedt G, Henriksson G. Pulping Chemistry and Technology (Volume 2). Berlin, Walter de Gruyter, 2009 https://www.youtube.com/watch?v=2uh3xiadm1a
4006 Síntese do éster etílico do ácido 2-(3-oxobutil) ciclopentanona-2-carboxílico
 4006 Síntese do éster etílico do ácido 2-(3-oxobutil) ciclopentanona-2-carboxílico CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156,2) (70,2) (270,3) (226,3) Classificação Tipos de reações
4006 Síntese do éster etílico do ácido 2-(3-oxobutil) ciclopentanona-2-carboxílico CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156,2) (70,2) (270,3) (226,3) Classificação Tipos de reações
Produção de etanol a partir de resíduos celulósicos. II GERA - Workshop de Gestão de Energia e Resíduos na Agroindústria Sucroalcooleira 13/06/2007
 Produção de etanol a partir de resíduos celulósicos II GERA - Workshop de Gestão de Energia e Resíduos na Agroindústria Sucroalcooleira 13/06/2007 Fermentação Energia (ATP) Etanol Açucares Glicose Frutose
Produção de etanol a partir de resíduos celulósicos II GERA - Workshop de Gestão de Energia e Resíduos na Agroindústria Sucroalcooleira 13/06/2007 Fermentação Energia (ATP) Etanol Açucares Glicose Frutose
COVEST/UFPE ª ETAPA
 COVEST/UFPE 2000 2ª ETAPA. A partir das entalpias padrão das reações de oxidação do ferro dadas abaixo: determine a quantidade de calor liberada a 298K e 1 atm na reação:. Iguais volumes de amônia e cloreto
COVEST/UFPE 2000 2ª ETAPA. A partir das entalpias padrão das reações de oxidação do ferro dadas abaixo: determine a quantidade de calor liberada a 298K e 1 atm na reação:. Iguais volumes de amônia e cloreto
Soluções usadas em escala industrial ou escala ampliada
 Soluções usadas em escala industrial ou escala ampliada Produção de açúcar e álcool (e eletricidade) (produz açúcar estocado nas células de parênquima da planta, além de etanol por fermentação de sacarose.
Soluções usadas em escala industrial ou escala ampliada Produção de açúcar e álcool (e eletricidade) (produz açúcar estocado nas células de parênquima da planta, além de etanol por fermentação de sacarose.
4025 Síntese de 2-iodopropano a partir do 2-propanol
 4025 Síntese de 2-iodopropano a partir do 2-propanol OH I + 1/2 I 2 + 1/3 P x + 1/3 P(OH) 3 C 3 H 8 O (60,1) (253,8) (31,0) C 3 H 7 I (170,0) (82,0) Classificação Tipos de reação e classes de substâncias
4025 Síntese de 2-iodopropano a partir do 2-propanol OH I + 1/2 I 2 + 1/3 P x + 1/3 P(OH) 3 C 3 H 8 O (60,1) (253,8) (31,0) C 3 H 7 I (170,0) (82,0) Classificação Tipos de reação e classes de substâncias
Carboximetilação de Polpas de Bagaço de Cana-de-Açúcar e Caracterização dos Materiais Absorventes Obtidos
 A R T G O T É N O E N T Í F O arboximetilação de Polpas de Bagaço de ana-de-açúcar e aracterização dos Materiais Absorventes Obtidos Luís. Morais e Sérgio P. ampana Filho Resumo: Os processos soda/antraquinona
A R T G O T É N O E N T Í F O arboximetilação de Polpas de Bagaço de ana-de-açúcar e aracterização dos Materiais Absorventes Obtidos Luís. Morais e Sérgio P. ampana Filho Resumo: Os processos soda/antraquinona
AVALIAÇÃO DA POLPAÇÃO SODA DE PINUS TAEDA COM ADIÇÃO DE ANTRAQUINONA
 AVALIAÇÃO DA POLPAÇÃO SODA DE PINUS TAEDA COM ADIÇÃO DE ANTRAQUINONA Débora Goelzer Fraga 1, Francides Gomes da Silva Júnior 2, Joaquim Carlos Gonçalez 3 1 Brasil. Universidade de Brasília. Tel (61) 326-0706
AVALIAÇÃO DA POLPAÇÃO SODA DE PINUS TAEDA COM ADIÇÃO DE ANTRAQUINONA Débora Goelzer Fraga 1, Francides Gomes da Silva Júnior 2, Joaquim Carlos Gonçalez 3 1 Brasil. Universidade de Brasília. Tel (61) 326-0706
4010 Síntese de p-metoxiacetofenona a partir do anisol
 4010 Síntese de p-metoxiacetofenona a partir do anisol O C 3 + O O C 3 O C 3 Zeolith O C 3 + C 3 COO O C 3 C 7 8 O (108,1) C 4 6 O 3 (102,1) C 9 10 O 2 (150,2) C 2 4 O 2 (60,1) Classificação Tipos de reação
4010 Síntese de p-metoxiacetofenona a partir do anisol O C 3 + O O C 3 O C 3 Zeolith O C 3 + C 3 COO O C 3 C 7 8 O (108,1) C 4 6 O 3 (102,1) C 9 10 O 2 (150,2) C 2 4 O 2 (60,1) Classificação Tipos de reação
SIMULADO de QUÍMICA 2 os anos 2008 TODOS COLÉGIOS
 SIMULADO de QUÍMICA 2 os anos 2008 TODOS COLÉGIOS ) Foram misturados 400 mililitros de solução 0,25 molar de ácido sulfúrico com 600 mililitros,5 molar do mesmo ácido. A molaridade da solução final é:
SIMULADO de QUÍMICA 2 os anos 2008 TODOS COLÉGIOS ) Foram misturados 400 mililitros de solução 0,25 molar de ácido sulfúrico com 600 mililitros,5 molar do mesmo ácido. A molaridade da solução final é:
LABORATÓRIO DE QUÍMICA QUI126 1ª LISTA DE EXERCÍCIOS
 1. Soluções básicas servem para a dissolução de gorduras sólidas que obstruem tubulações das cozinhas. O hidróxido de sódio é um exemplo, pois reage com gorduras e gera produtos solúveis. Qual a massa
1. Soluções básicas servem para a dissolução de gorduras sólidas que obstruem tubulações das cozinhas. O hidróxido de sódio é um exemplo, pois reage com gorduras e gera produtos solúveis. Qual a massa
5009 Síntese de ftalocianina de cobre
 P 59 Síntese de ftalocianina de cobre 4 H 2 + 8 H 2 + CuCl (H 4 ) 6 Mo 7 24. 4 H 2-8 H 3-8 C 2-4 H 2 - HCl Cu C 8 H 4 3 CH 4 2 CuCl H 24 Mo 7 6 24. 4 H2 C 32 H 16 8 Cu (148,1) (6,1) (99,) (1235,9) (576,1)
P 59 Síntese de ftalocianina de cobre 4 H 2 + 8 H 2 + CuCl (H 4 ) 6 Mo 7 24. 4 H 2-8 H 3-8 C 2-4 H 2 - HCl Cu C 8 H 4 3 CH 4 2 CuCl H 24 Mo 7 6 24. 4 H2 C 32 H 16 8 Cu (148,1) (6,1) (99,) (1235,9) (576,1)
Química. Xandão (Renan Micha) Soluções
 Soluções Soluções 1. (FUVEST) Sabe-se que os metais ferro (Fe 0 ), magnésio (Mg 0 ) e estanho (Sn 0 ) reagem com soluções de ácidos minerais, liberando gás hidrogênio e formando íons divalentes em solução.
Soluções Soluções 1. (FUVEST) Sabe-se que os metais ferro (Fe 0 ), magnésio (Mg 0 ) e estanho (Sn 0 ) reagem com soluções de ácidos minerais, liberando gás hidrogênio e formando íons divalentes em solução.
Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio.
 ATIVIDADE 2 - CÁLCULO DE CONCENTRAÇÃO Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio. Exercício 2. Calcule
ATIVIDADE 2 - CÁLCULO DE CONCENTRAÇÃO Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio. Exercício 2. Calcule
2017 Obtenção da amida do ácido cinâmico através da reação do cloreto do ácido cinâmico com amônia
 217 Obtenção da amida do ácido cinâmico através da reação do cloreto do ácido cinâmico com amônia O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Classificação Tipos de reação e classes de
217 Obtenção da amida do ácido cinâmico através da reação do cloreto do ácido cinâmico com amônia O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Classificação Tipos de reação e classes de
QUÍMICA RECUPERAÇÃO PARALELA. Prof. ALEXANDRE D. MARQUIORETO
 QUÍMICA RECUPERAÇÃO PARALELA Prof. ALEXANDRE D. MARQUIORETO SOLUÇÕES são misturas homogêneas de duas ou mais substâncias. SOLUÇÃO = SOLUTO + SOLVENTE Que se dissolve Que dissolverá Como se forma uma solução?
QUÍMICA RECUPERAÇÃO PARALELA Prof. ALEXANDRE D. MARQUIORETO SOLUÇÕES são misturas homogêneas de duas ou mais substâncias. SOLUÇÃO = SOLUTO + SOLVENTE Que se dissolve Que dissolverá Como se forma uma solução?
Experiência 7. PREPARO DE SOLUÇÃO A PARTIR DE SUBSTÂNCIAS SÓLIDAS, LIQUIDAS E DE SOLUÇÃO CONCENTRADA
 Experiência 7. PREPARO DE SOLUÇÃO A PARTIR DE SUBSTÂNCIAS SÓLIDAS, LIQUIDAS E DE SOLUÇÃO CONCENTRADA 1. Objetivos Após a realização desta aula experimental, espera-se que o graduando do curso de Química
Experiência 7. PREPARO DE SOLUÇÃO A PARTIR DE SUBSTÂNCIAS SÓLIDAS, LIQUIDAS E DE SOLUÇÃO CONCENTRADA 1. Objetivos Após a realização desta aula experimental, espera-se que o graduando do curso de Química
Moacir Cardoso Elias
 Moacir Cardoso Elias eliasmc@ufpel.tche.br PREPARO E DILUIÇÃO DE SOLUÇÕES 1 Características das soluções 2 Classificação das soluções 3 Expressão da concentração de soluções 4 Cálculos de preparo de soluções
Moacir Cardoso Elias eliasmc@ufpel.tche.br PREPARO E DILUIÇÃO DE SOLUÇÕES 1 Características das soluções 2 Classificação das soluções 3 Expressão da concentração de soluções 4 Cálculos de preparo de soluções
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. DISCIPLINA:Química SÉRIE: 3º. ALUNO(a): Lista de Exercícios P1 I Bimestre
 GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 3º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 3º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
2029 Reação do trifenilfosfano com o éster metílico do ácido bromoacético originando brometo de (carbometoximetil) trifenilfosfônio
 229 Reação do trifenilfosfano com o éster metílico do ácido bromoacético originando brometo de (carbometoximetil) trifenilfosfônio CH 3 Br + P P Br C 3 H 5 Br 2 C 18 H 15 P (153,) (262,3) CH 3 C 21 H 2
229 Reação do trifenilfosfano com o éster metílico do ácido bromoacético originando brometo de (carbometoximetil) trifenilfosfônio CH 3 Br + P P Br C 3 H 5 Br 2 C 18 H 15 P (153,) (262,3) CH 3 C 21 H 2
