Procedimentos Simplificados para Registro de Medicamentos CLONES
|
|
|
- Maria das Graças Bastos Leão
- 8 Há anos
- Visualizações:
Transcrição
1 SUMED Procedimentos Simplificados para Registro de Medicamentos CLONES IV Symposium Sindusfarma IPS/FIP-Anvisa Novas Fronteiras Farmacêuticas nas ciências, tecnologia, regulamentação e sistema de qualidade Brasília, 23/06/2015
2 Definições XXII - Medicamento de Referência Produto inovador registrado no órgão federal responsável pela vigilância sanitária e comercializado no País, cuja eficácia, segurança e qualidade foram comprovadas cientificamente junto ao órgão federal competente, por ocasião do registro; (Inciso incluído pela LEI Nº 9.787, DE 10 DE FEVEREIRO DE 1999)
3 Definições XXI - Medicamento Genérico Medicamento similar a um produto de referência ou inovador, que se pretende ser com este intercambiável, geralmente produzido após a expiração ou renúncia da proteção patentária ou de outros direitos de exclusividade, comprovada a sua eficácia, segurança e qualidade, e designado pela DCB ou, na sua ausência, pela DCI; (Inciso incluído pela LEI Nº 9.787, DE 10 DE FEVEREIRO DE 1999)
4 Definições XX - Medicamento Similar Aquele que contém o mesmo ou os mesmos princípios ativos, apresenta a mesma concentração, forma farmacêutica, via de administração, posologia e indicação terapêutica, e que é equivalente ao medicamento registrado no órgão federal responsável pela vigilância sanitária, podendo diferir somente em características relativas ao tamanho e forma do produto, prazo de validade, embalagem, rotulagem, excipientes e veículos, devendo sempre ser identificado por nome comercial ou marca (Redação dada pela MEDIDA PROVISÓRIA Nº , DE 23 DE AGOSTO DE 2001
5 Registro de Medicamentos Sintéticos 1976 até 1999 Registro de medicamentos novos e similares Utilização de dados clínicos da molécula para o registro de similares 1999 em diante Registro de medicamentos novos, similares e genéricos Apresentação de estudos de comparabilidade entre as cópias e medicamento de referência
6 Histórico Marco regulatório para o Registro de Medicamentos RDC 133/2003 Registro de Similares RDC 134/2003 Adequação de medicamento já registrado RDC 135/2003 Registro de Genéricos RDC 136/2003 Registro de Novos Atualização RDC 16/ Registro de Genéricos RDC 17/ Registro de Similares
7 Considerações Gerais Uma empresa pode obter registro de um produto com marca e o registro de um produto genérico; Não há vedação para que empresas de um mesmo grupo econômico tenham registros de um mesmo produto; Não há vedação para que uma empresa compartilhe seu dossiê técnico e clínico com outra empresa, sendo mesma de um mesmo grupo econômico ou não.
8 Desvantagens inerentes à análise de processos idênticos Retrabalho; Decisões divergentes para um mesmo dossiê; Falta de previsibilidade.
9 Processo de racionalização da análise 2005 RESOLUÇÃO - RE Nº 1.315, DE 31 DE MAIO DE 2005 Visava realização de análise concomitante nos processos de registro genéricos e similares; À época uma gerência era responsável pelo registro de medicamentos genéricos e outra pelo registro de medicamentos similares;
10 Processo de racionalização da análise 2008 INSTRUÇÃO NORMATIVA Nº 06, DE 23 DE DEZEMBRO DE 2008 Estabeleceu o envio de declaração de igualdade; Não havia vinculação entre os produtos, apenas vinculação entre as solicitações de Registro ou para as asolicitações de Alteração Pós-Registro
11 Processo de racionalização da análise 2014 RESOLUÇÃO RDC Nº 31, DE 29 DE MAIO DE 2014 Documentação simplificada; Estabeleceu a vinculação entre produtos; Impossibilidade de produtos clones se diferenciarem do produto matriz ; Possibilidade de migração de registros já concedidos para o sistema simplificado.
12 Resultados esperados Racionalização da análise Existiam diversos grupos econômicos ou parcerias comerciais Em alguns casos um mesmo registro matriz dava origem a 9 clones ; Análise feita se restringiria a bula, rotulagem e nome comercial; Redução do Volume de peticionamento Estimava-se que 1/3 das solicitações de registro eram de medicamentos clones; Racionalização das atividades de pós-registro;
13 Resultados esperados Melhor acompanhamento dos produtos no mercado A vinculação dos produtos permitiria maior rastreabilidade de produtos No caso de desvios de qualidade todos os clones poderiam ser identificados rapidamente; A identificação de clones permitiria ampliar o volume de dados para o acompanhamento de farmacovigilância de um determinado produto;
14 Principais dificuldades durante a implementação da norma Incongruências entre as informações presentes no registro de clones e as informações aprovadas para o medicamento matriz; Volume de solicitações muito superior a demanda inicialmente prevista; Concessão de um novo registro, com consequente perda do material de embalagem e novo registro de preço reduziu a migração de registros antigos para o registro simplificado
15 Panorama após 1 ano da norma No primeiro ano da RDC 31/2014 foram solicitados 958 registros de medicamentos clones; Durante o 1º semestre de 2015 foram concedidos 7 registros/semana ; Tempo médio para a concessão do registro de 424 dias Estabelecimento de procedimento específico para a migração de processos já registrados para o registro simplificado;
16 Obrigado! Ricardo Borges Gerência Geral de Medicamentos (61)
Prescrição e Dispensação de Medicamentos Genéricos e Similares Destaques da Legislação Vigente
 Prescrição e Dispensação de Medicamentos Genéricos e Similares Destaques da Legislação Vigente Brasília, 21 de outubro de 2013. Processo nº: 25351.584974/2013-59 Tema da Agenda Regulatória 2013/2014 nº:
Prescrição e Dispensação de Medicamentos Genéricos e Similares Destaques da Legislação Vigente Brasília, 21 de outubro de 2013. Processo nº: 25351.584974/2013-59 Tema da Agenda Regulatória 2013/2014 nº:
MEDICAMENTOS SIMILARES
 MEDICAMENTOS SIMILARES Fica assegurado o direito de registro de medicamentos similares a outros já registrados, desde que satisfaçam as exigências estabelecidas nesta Lei. (Art. 21 da Lei 6360/76) MEDICAMENTOS
MEDICAMENTOS SIMILARES Fica assegurado o direito de registro de medicamentos similares a outros já registrados, desde que satisfaçam as exigências estabelecidas nesta Lei. (Art. 21 da Lei 6360/76) MEDICAMENTOS
Genéricos - Guia Básico. Autor: Cesar Roberto CRF-RJ: 7461
 Autor: Cesar Roberto CRF-RJ: 7461 Versão 3.00 2001 Introdução: Este guia visa a orientar o profissional farmacêutico sobre os genéricos, e como este deve proceder na hora de aviar uma receita nesta nova
Autor: Cesar Roberto CRF-RJ: 7461 Versão 3.00 2001 Introdução: Este guia visa a orientar o profissional farmacêutico sobre os genéricos, e como este deve proceder na hora de aviar uma receita nesta nova
BIBLIOTECA ARTIGO Nº 48
 BIBLIOTECA ARTIGO Nº 48 MUITO BARULHO POR NADA - COMO COMPLICAR A EXPLICAÇÃO Autores - Marcos Lobo De Freitas Levy e Silvia V. Fridman A ANVISA prevê a elaboração de uma nova resolução para permitir a
BIBLIOTECA ARTIGO Nº 48 MUITO BARULHO POR NADA - COMO COMPLICAR A EXPLICAÇÃO Autores - Marcos Lobo De Freitas Levy e Silvia V. Fridman A ANVISA prevê a elaboração de uma nova resolução para permitir a
Agência Nacional de Vigilância Sanitária REGISTRO DE MEDICAMENTOS
 REGISTRO DE MEDICAMENTOS GERÊNCIA GERAL DE MEDICAMENTOS - SETORES A Gerência Geral de Medicamentos está em fase de reestruturação, portanto as divisões setoriais são provisórias; Gerência de Pesquisas,
REGISTRO DE MEDICAMENTOS GERÊNCIA GERAL DE MEDICAMENTOS - SETORES A Gerência Geral de Medicamentos está em fase de reestruturação, portanto as divisões setoriais são provisórias; Gerência de Pesquisas,
DÚVIDAS MAIS FREQUENTES NO BALCÃO DA FARMÁCIA
 DÚVIDAS MAIS FREQUENTES NO BALCÃO DA FARMÁCIA Neste módulo vamos tratar de situações que envolvem dúvidas quanto à melhor maneira de agir e as práticas permitidas ou não pela legislação, mas que, comumente,
DÚVIDAS MAIS FREQUENTES NO BALCÃO DA FARMÁCIA Neste módulo vamos tratar de situações que envolvem dúvidas quanto à melhor maneira de agir e as práticas permitidas ou não pela legislação, mas que, comumente,
PORTARIA Nº 219/SUMED/ANVISA, DE 23 DE FEVEREIRO DE 2015
 PORTARIA Nº 219/SUMED/ANVISA, DE 23 DE FEVEREIRO DE 2015 A Superintendente de Medicamentos e Produtos Biológicos da Agência Nacional de Vigilância Sanitária no uso das atribuições que lhe confere Portaria
PORTARIA Nº 219/SUMED/ANVISA, DE 23 DE FEVEREIRO DE 2015 A Superintendente de Medicamentos e Produtos Biológicos da Agência Nacional de Vigilância Sanitária no uso das atribuições que lhe confere Portaria
Novas Medidas de Regulação do Mercado de Medicamentos Câmara de Regulação do Mercado de Medicamentos (CMED)
 Novas Medidas de Regulação do Mercado de Medicamentos Câmara de Regulação do Mercado de Medicamentos (CMED) Ministério da Saúde e Agência de Vigilância Sanitária Brasília, 27 de fevereiro Contexto Lei
Novas Medidas de Regulação do Mercado de Medicamentos Câmara de Regulação do Mercado de Medicamentos (CMED) Ministério da Saúde e Agência de Vigilância Sanitária Brasília, 27 de fevereiro Contexto Lei
RESOLUÇÃO RDC Nº 59, DE 10 DE OUTUBRO DE 2014. Dispõe sobre os nomes dos medicamentos, seus complementos e a formação de famílias de medicamentos.
 RESOLUÇÃO RDC Nº 59, DE 10 DE OUTUBRO DE 2014 Dispõe sobre os nomes dos medicamentos, seus complementos e a formação de famílias de medicamentos. A Diretoria Colegiada da Agência Nacional de Vigilância
RESOLUÇÃO RDC Nº 59, DE 10 DE OUTUBRO DE 2014 Dispõe sobre os nomes dos medicamentos, seus complementos e a formação de famílias de medicamentos. A Diretoria Colegiada da Agência Nacional de Vigilância
Políticas de Regulação de Produtos Biotecnológicos
 Diretoria Dirceu Raposo de Melo Gerência Geral de Medicamentos Gerência de Avaliação de Segurança e Eficácia Políticas de Regulação de Produtos Biotecnológicos Daniela Marreco Cerqueira CPBIH/GESEF/GGMED/ANVISA
Diretoria Dirceu Raposo de Melo Gerência Geral de Medicamentos Gerência de Avaliação de Segurança e Eficácia Políticas de Regulação de Produtos Biotecnológicos Daniela Marreco Cerqueira CPBIH/GESEF/GGMED/ANVISA
Novas Regras para Rotulagem Medicamentos
 XV ENCONTRO TÉCNICO E XI ENCONTRO EMPRESARIAL - ABRASP Novas Regras para Rotulagem Medicamentos RESOLUÇÃO-RDC Nº 71/2009 Carolina K. Rodrigues 21/09/2010 RESOLUÇÃO-RDC Nº 71/2009 DOU de 23/12/2009 Estabelece
XV ENCONTRO TÉCNICO E XI ENCONTRO EMPRESARIAL - ABRASP Novas Regras para Rotulagem Medicamentos RESOLUÇÃO-RDC Nº 71/2009 Carolina K. Rodrigues 21/09/2010 RESOLUÇÃO-RDC Nº 71/2009 DOU de 23/12/2009 Estabelece
REGULAÇÃO SANITÁRIA DE MEDICAMENTOS
 REGULAÇÃO SANITÁRIA DE MEDICAMENTOS Fabrício Carneiro de Oliveira Especialista em regulação e Vigilância Sanitária Gerência Geral de Medicamentos Curso de Regulação e Defesa do Consumidor Brasília, 23
REGULAÇÃO SANITÁRIA DE MEDICAMENTOS Fabrício Carneiro de Oliveira Especialista em regulação e Vigilância Sanitária Gerência Geral de Medicamentos Curso de Regulação e Defesa do Consumidor Brasília, 23
RDC 60. Perguntas e Respostas. RDC nº 60, RDC 60 - PERGUNTAS E RESPOSTAS
 Regulamentação SOBRE AMOSTRAS GRÁTIS DE MEDICAMENTOS RDC 60 Perguntas e Respostas RDC nº 60, de 26 de NOVEmbro de 2009 1 Regulamentação SOBRE AMOSTRAS GRÁTIS RDC 60 Perguntas e Respostas RDC nº 60, de
Regulamentação SOBRE AMOSTRAS GRÁTIS DE MEDICAMENTOS RDC 60 Perguntas e Respostas RDC nº 60, de 26 de NOVEmbro de 2009 1 Regulamentação SOBRE AMOSTRAS GRÁTIS RDC 60 Perguntas e Respostas RDC nº 60, de
O Papel da ANVISA na Regulamentação da Inovação Farmacêutica
 O Papel da ANVISA na Regulamentação da Inovação Farmacêutica Renato Alencar Porto Diretor 22 de junho de 2015 Bases legais para o estabelecimento do sistema de regulação Competências na Legislação Federal
O Papel da ANVISA na Regulamentação da Inovação Farmacêutica Renato Alencar Porto Diretor 22 de junho de 2015 Bases legais para o estabelecimento do sistema de regulação Competências na Legislação Federal
Legislação e normatização dos medicamentos biológicos no Brasil
 Gerência Geral de Medicamentos Gerência de Avaliação de Segurança e Eficácia Coordenação de Produtos Biológicos Legislação e normatização dos medicamentos biológicos no Brasil Brenda Gomes Valente agosto/2011
Gerência Geral de Medicamentos Gerência de Avaliação de Segurança e Eficácia Coordenação de Produtos Biológicos Legislação e normatização dos medicamentos biológicos no Brasil Brenda Gomes Valente agosto/2011
WORKSHOP PANORAMA MUNDIAL SOBRE PROBIÓTICOS. Regulamentação atual Medicamentos contendo probióticos
 WORKSHOP PANORAMA MUNDIAL SOBRE PROBIÓTICOS Regulamentação atual Medicamentos contendo probióticos Neemias Silva de Andrade Gerência de Produtos Biológicos / GPBIO Gerência-Geral de Produtos Biológicos,
WORKSHOP PANORAMA MUNDIAL SOBRE PROBIÓTICOS Regulamentação atual Medicamentos contendo probióticos Neemias Silva de Andrade Gerência de Produtos Biológicos / GPBIO Gerência-Geral de Produtos Biológicos,
RESOLUÇÃO - RDC Nº 40, DE 26 DE AGOSTO DE 2015
 RESOLUÇÃO - RDC Nº 40, DE 26 DE AGOSTO DE 2015 Define os requisitos do cadastro de produtos médicos. A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da atribuição que lhe conferem
RESOLUÇÃO - RDC Nº 40, DE 26 DE AGOSTO DE 2015 Define os requisitos do cadastro de produtos médicos. A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da atribuição que lhe conferem
Registro Eletrônico de Medicamentos
 Registro Eletrônico de Medicamentos Emanuela Vieira Gerência Geral de Medicamentos ANVISA - MS Histórico Registro Eletrônico 2008 Contratação da empresa responsável pelo desenho do processo 11/2008 Início
Registro Eletrônico de Medicamentos Emanuela Vieira Gerência Geral de Medicamentos ANVISA - MS Histórico Registro Eletrônico 2008 Contratação da empresa responsável pelo desenho do processo 11/2008 Início
REGISTRO DE MEDICAMENTOS
 REGISTRO DE MEDICAMENTOS Deborah Masano Cavaloti Manira Georges Soufia 1 Como a Anvisa avalia o registro de medicamentos novos no Brasil Brasília, 20 de janeiro de 2005 No Brasil, os medicamentos são registrados
REGISTRO DE MEDICAMENTOS Deborah Masano Cavaloti Manira Georges Soufia 1 Como a Anvisa avalia o registro de medicamentos novos no Brasil Brasília, 20 de janeiro de 2005 No Brasil, os medicamentos são registrados
Instrução Normativa PROEX/IFRS nº 13, de 17 de dezembro de 2013.
 Instrução Normativa PROEX/IFRS nº 13, de 17 de dezembro de 2013. Estabelece o fluxo e os procedimentos para o registro, a análise e o acompanhamento das ações de extensão do IFRS e dá outras providências.
Instrução Normativa PROEX/IFRS nº 13, de 17 de dezembro de 2013. Estabelece o fluxo e os procedimentos para o registro, a análise e o acompanhamento das ações de extensão do IFRS e dá outras providências.
JAIME CÉSAR DE MOURA OLIVEIRA
 Agência Nacional de Vigilância Sanitária www.anvisa.gov.br Consulta Pública n 27, de 06 de abril de 2015 D.O.U de 08/04/2015 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso das
Agência Nacional de Vigilância Sanitária www.anvisa.gov.br Consulta Pública n 27, de 06 de abril de 2015 D.O.U de 08/04/2015 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso das
Consulta Pública n. 72, de 14 de julho de 2010. Estabelece os critérios de aceitabilidade de nomes comerciais de medicamentos.
 Consulta Pública n. 72, de 14 de julho de 2010. Estabelece os critérios de aceitabilidade de nomes comerciais de medicamentos. Versão Consolidada n. 07, de 27 de maio de 2013. Para Audiência Pública Resolução
Consulta Pública n. 72, de 14 de julho de 2010. Estabelece os critérios de aceitabilidade de nomes comerciais de medicamentos. Versão Consolidada n. 07, de 27 de maio de 2013. Para Audiência Pública Resolução
Os 1 Item(ns) da lista de documentos que não foram cumprido(s):
 Agência Nacional de Vigilância Sanitária Unidade de Atendimento e Protocolo - UNIAP Listagem de Encaminhamento de Documentação em Caráter Precário Data: 14.11.05 EMPRESA: ANCHIETA INDÚSTRIA E COMÉRCIO
Agência Nacional de Vigilância Sanitária Unidade de Atendimento e Protocolo - UNIAP Listagem de Encaminhamento de Documentação em Caráter Precário Data: 14.11.05 EMPRESA: ANCHIETA INDÚSTRIA E COMÉRCIO
Adota a seguinte Consulta Pública e eu, Diretora-Presidente Substituta, determino a sua publicação:
 Agência Nacional de Vigilância Sanitária www.anvisa.gov.br Consulta Pública nº 14, de 16 de março de 2011. D.O.U de 21/03/2011 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso
Agência Nacional de Vigilância Sanitária www.anvisa.gov.br Consulta Pública nº 14, de 16 de março de 2011. D.O.U de 21/03/2011 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso
Medicamento O que é? Para que serve?
 Medicamento O que é? Para que serve? Os Medicamentos são produtos farmacêuticos, tecnicamente obtidos ou elaborados, com finalidade profilática, curativa, paliativa ou para fins de diagnóstico (Lei nº
Medicamento O que é? Para que serve? Os Medicamentos são produtos farmacêuticos, tecnicamente obtidos ou elaborados, com finalidade profilática, curativa, paliativa ou para fins de diagnóstico (Lei nº
RESOLUÇÃO - RDC Nº 60, DE 10 DE OUTUBRO DE 2014
 *Este texto não substitui o publicado do Diário Oficial da União* DIÁRIO OFICIAL DA UNIÃO MINISTÉRIO DA SAÚDE AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA DIRETORIA COLEGIADA RESOLUÇÃO - RDC Nº 60, DE 10 DE
*Este texto não substitui o publicado do Diário Oficial da União* DIÁRIO OFICIAL DA UNIÃO MINISTÉRIO DA SAÚDE AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA DIRETORIA COLEGIADA RESOLUÇÃO - RDC Nº 60, DE 10 DE
AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA RESOLUÇÃO RDC Nº 2, DE 17 DE JANEIRO DE 2012
 AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA RESOLUÇÃO RDC Nº 2, DE 17 DE JANEIRO DE 2012 Institui o protocolo eletrônico para emissão de Certificado de Registro de Medicamento e Certidão de Registro para
AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA RESOLUÇÃO RDC Nº 2, DE 17 DE JANEIRO DE 2012 Institui o protocolo eletrônico para emissão de Certificado de Registro de Medicamento e Certidão de Registro para
Guia de Submissão Eletrônica de Rótulos
 Agência Nacional de Vigilância Sanitária Guia de Submissão Eletrônica de Rótulos Superintendência de Medicamentos e Produtos Biológicos SUMED www.anvisa.gov.br Brasília, 31 de outubro de 2014. Agência
Agência Nacional de Vigilância Sanitária Guia de Submissão Eletrônica de Rótulos Superintendência de Medicamentos e Produtos Biológicos SUMED www.anvisa.gov.br Brasília, 31 de outubro de 2014. Agência
SELO ABRAIDI Programa de BPADPS
 SELO ABRAIDI Programa de BPADPS Reuniões: Julho a Agosto de 2010 Associação Brasileira de Importadores e Distribuidores de Implantes PAUTA * OBJETIVOS * ASPECTOS FUNDAMENTAIS * HISTÓRICO * SITUAÇÃO ATUAL
SELO ABRAIDI Programa de BPADPS Reuniões: Julho a Agosto de 2010 Associação Brasileira de Importadores e Distribuidores de Implantes PAUTA * OBJETIVOS * ASPECTOS FUNDAMENTAIS * HISTÓRICO * SITUAÇÃO ATUAL
adota a seguinte Consulta Pública e eu, Diretor-Presidente Substituto, determino a sua publicação:
 Agência Nacional de Vigilância Sanitária www.anvisa.gov.br Consulta Pública nº 48, de 13 de julho de 2012. D.O.U de 23/07/12 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da
Agência Nacional de Vigilância Sanitária www.anvisa.gov.br Consulta Pública nº 48, de 13 de julho de 2012. D.O.U de 23/07/12 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da
Guia de Submissão Eletrônica de Texto de Bula
 Agência Nacional de Vigilância Sanitária Guia de Submissão Eletrônica de Texto de Bula Gerência-geral de Medicamentos - GGMED www.anvisa.gov.br Brasília, 13 de janeiro de 2014 Agência Nacional de Vigilância
Agência Nacional de Vigilância Sanitária Guia de Submissão Eletrônica de Texto de Bula Gerência-geral de Medicamentos - GGMED www.anvisa.gov.br Brasília, 13 de janeiro de 2014 Agência Nacional de Vigilância
Importação de Produtos para Saúde
 Importação de Produtos para Saúde Gerência de Inspeção de Produtos e Autorização de Empresas em Portos, Aeroportos Fronteiras e Recintos Alfandegados GIPAF Mônica Cristina A. F. Duarte Organograma - ANVISA
Importação de Produtos para Saúde Gerência de Inspeção de Produtos e Autorização de Empresas em Portos, Aeroportos Fronteiras e Recintos Alfandegados GIPAF Mônica Cristina A. F. Duarte Organograma - ANVISA
RESOLUÇÃO RDC Nº 133, DE 29 DE MAIO DE 2003
 RESOLUÇÃO RDC Nº 133, DE 29 DE MAIO DE 2003 Dispõe sobre o registro de Medicamento Similar e dá outras providências. A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da atribuição
RESOLUÇÃO RDC Nº 133, DE 29 DE MAIO DE 2003 Dispõe sobre o registro de Medicamento Similar e dá outras providências. A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da atribuição
adota a seguinte Consulta Pública e eu, Diretor Presidente, determino a sua publicação:
 Agência Nacional de Vigilância Sanitária www.anvisa.gov.br Consulta Pública nº 19, de 6 de maio de 2009. D.O.U de 11/05/09 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso das
Agência Nacional de Vigilância Sanitária www.anvisa.gov.br Consulta Pública nº 19, de 6 de maio de 2009. D.O.U de 11/05/09 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso das
adota a seguinte Consulta Pública e eu, Diretor Presidente, determino a sua publicação:
 Consulta Pública nº 34, de 28 de junho de 2011. A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso das atribuições que lhe confere o inciso IV do art. 11 e o art. 35 do Regulamento
Consulta Pública nº 34, de 28 de junho de 2011. A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso das atribuições que lhe confere o inciso IV do art. 11 e o art. 35 do Regulamento
Ivo Bucaresky CONBRAFARMA. Diretor ANVISA. Agosto de 2015
 Ivo Bucaresky Diretor ANVISA CONBRAFARMA Agosto de 2015 1 PROGRAMA DE MELHORIA DO PROCESSO DE REGULAMENTAÇÃO Diretrizes: Fortalecimento da capacidade institucional para gestão em regulação Melhoria da
Ivo Bucaresky Diretor ANVISA CONBRAFARMA Agosto de 2015 1 PROGRAMA DE MELHORIA DO PROCESSO DE REGULAMENTAÇÃO Diretrizes: Fortalecimento da capacidade institucional para gestão em regulação Melhoria da
Ministério da Saúde Agência Nacional de Vigilância Sanitária RESOLUÇÃO DA DIRETORIA COLEGIADA - RDC Nº 60, DE 10 DE OUTUBRO DE 2014.
 ADVERTÊNCIA Este texto não substitui o publicado no Diário Oficial da União Ministério da Saúde Agência Nacional de Vigilância Sanitária RESOLUÇÃO DA DIRETORIA COLEGIADA - RDC Nº 60, DE 10 DE OUTUBRO DE
ADVERTÊNCIA Este texto não substitui o publicado no Diário Oficial da União Ministério da Saúde Agência Nacional de Vigilância Sanitária RESOLUÇÃO DA DIRETORIA COLEGIADA - RDC Nº 60, DE 10 DE OUTUBRO DE
RESOLUÇÃO-RDC Nº 17, DE 02 DE MARÇO DE 2007 DOU DE 05/03/2007
 RESOLUÇÃO-RDC Nº 17, DE 02 DE MARÇO DE 2007 DOU DE 05/03/2007 Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da atribuição que lhe confere o inciso IV do art. 11 do Regulamento
RESOLUÇÃO-RDC Nº 17, DE 02 DE MARÇO DE 2007 DOU DE 05/03/2007 Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da atribuição que lhe confere o inciso IV do art. 11 do Regulamento
1.5. Dados pessoais que devem constar na receita médica. 1.6. Validade das receitas de medicamentos antimicrobianos
 Atualizado: 10 / 05 / 2013 FAQ AI 1. Controle de medicamentos antimicrobianos (antibióticos) 1.1. Informações gerais 1.2. Uso contínuo (tratamento prolongado) 1.3. Retenção da segunda via da receita médica
Atualizado: 10 / 05 / 2013 FAQ AI 1. Controle de medicamentos antimicrobianos (antibióticos) 1.1. Informações gerais 1.2. Uso contínuo (tratamento prolongado) 1.3. Retenção da segunda via da receita médica
Informe Técnico n. 67, de 1º de setembro de 2015.
 Informe Técnico n. 67, de 1º de setembro de 2015. Assunto: Orientações sobre os procedimentos para solicitação de alterações na lista de alimentos alergênicos. I. Introdução. A Resolução de Diretoria Colegiada
Informe Técnico n. 67, de 1º de setembro de 2015. Assunto: Orientações sobre os procedimentos para solicitação de alterações na lista de alimentos alergênicos. I. Introdução. A Resolução de Diretoria Colegiada
RESOLUÇÃO - RDC Nº 40, DE 26 DE AGOSTO DE 2015. (DOU Seção 1, nº 164, pag. 47, 27.08.2015) (Retificação DOU Seção 1, nº 165, pag. 69, 28.08.
 RESOLUÇÃO - RDC Nº 40, DE 26 DE AGOSTO DE 2015 (DOU Seção 1, nº 164, pag. 47, 27.08.2015) (Retificação DOU Seção 1, nº 165, pag. 69, 28.08.2015) Define os requisitos do cadastro de produtos médicos. A
RESOLUÇÃO - RDC Nº 40, DE 26 DE AGOSTO DE 2015 (DOU Seção 1, nº 164, pag. 47, 27.08.2015) (Retificação DOU Seção 1, nº 165, pag. 69, 28.08.2015) Define os requisitos do cadastro de produtos médicos. A
Guia do Professor. Esta atividade poderá ser realizada, satisfatoriamente, em uma aula de 50 minutos.
 Caro Professor, O principal objetivo do projeto RIVED é oferecer aos professores do Ensino Médio novos recursos didáticos, em forma de módulos, para a melhoria da aprendizagem dos alunos em sala de aula.
Caro Professor, O principal objetivo do projeto RIVED é oferecer aos professores do Ensino Médio novos recursos didáticos, em forma de módulos, para a melhoria da aprendizagem dos alunos em sala de aula.
INSTRUÇÃO NORMATIVA CONJUNTA SDA/SDC/ANVISA/IBAMA Nº 1, DE 24 DE MAIO DE 2011.
 INSTRUÇÃO NORMATIVA CONJUNTA SDA/SDC/ANVISA/IBAMA Nº 1, DE 24 DE MAIO DE 2011. O SECRETÁRIO DE DEFESA AGROPECUÁRIA DO MINISTÉRIO DA AGRICULTURA, PECUÁRIA E ABASTECIMENTO - MAPA, o SECRETÁRIO DE DESENVOLVIMENTO
INSTRUÇÃO NORMATIVA CONJUNTA SDA/SDC/ANVISA/IBAMA Nº 1, DE 24 DE MAIO DE 2011. O SECRETÁRIO DE DEFESA AGROPECUÁRIA DO MINISTÉRIO DA AGRICULTURA, PECUÁRIA E ABASTECIMENTO - MAPA, o SECRETÁRIO DE DESENVOLVIMENTO
REGISTRO, TRATAMENTO E APURAÇÃO DE INDISPONIBILIDADES DE USINAS HIDRÁULICAS NÃO DESPACHADAS CENTRALIZADAMENTE E PARTICIPANTES DO MRE
 Procedimento de Comercialização REGISTRO, TRATAMENTO E APURAÇÃO DE INDISPONIBILIDADES DE USINAS HIDRÁULICAS NÃO DESPACHADAS CENTRALIZADAMENTE E PARTICIPANTES DO MRE Versão: 1 Início de Vigência: REGISTRO,
Procedimento de Comercialização REGISTRO, TRATAMENTO E APURAÇÃO DE INDISPONIBILIDADES DE USINAS HIDRÁULICAS NÃO DESPACHADAS CENTRALIZADAMENTE E PARTICIPANTES DO MRE Versão: 1 Início de Vigência: REGISTRO,
Versão: 2 Início de Vigência: XX. XX.2006 Instrumento de Aprovação:
 Procedimento de Comercialização MANUTENÇÃO DE CADASTRO DE AGENTES DA CCEE E USUÁRIOS DO SCL Versão: 2 Início de Vigência: XX. XX.2006 Instrumento de Aprovação: ÍNDICE 1. APROVAÇÃO...3 2. HISTÓRICO DE REVISÕES...3
Procedimento de Comercialização MANUTENÇÃO DE CADASTRO DE AGENTES DA CCEE E USUÁRIOS DO SCL Versão: 2 Início de Vigência: XX. XX.2006 Instrumento de Aprovação: ÍNDICE 1. APROVAÇÃO...3 2. HISTÓRICO DE REVISÕES...3
Ministério da Educação Universidade Tecnológica Federal do Paraná Pró-Reitoria de Graduação e Educação Profissional
 Ministério da Educação Instrução Normativa 04 /13 OGRAD Estabelece os procedimentos a serem adotados quando do afastamento de alunos para a realização de estudos no exterior. O Pró-Reitor de Graduação
Ministério da Educação Instrução Normativa 04 /13 OGRAD Estabelece os procedimentos a serem adotados quando do afastamento de alunos para a realização de estudos no exterior. O Pró-Reitor de Graduação
Programa UNIBRAL Edital CGCI n. 014 /2007
 Programa UNIBRAL Edital CGCI n. 014 /2007 1 Do programa e objetivo 1.1 O Programa UNIBRAL, apoiado no acordo de cooperação assinado entre Brasil e Alemanha em 31 de outubro de 2000, tem como objetivo estimular
Programa UNIBRAL Edital CGCI n. 014 /2007 1 Do programa e objetivo 1.1 O Programa UNIBRAL, apoiado no acordo de cooperação assinado entre Brasil e Alemanha em 31 de outubro de 2000, tem como objetivo estimular
Secretaria-Executiva da Câmara de Regulação do Mercado de Medicamentos - CMED. São Paulo 17 de março de 2015
 Secretaria-Executiva da Câmara de Regulação do Mercado de Medicamentos - CMED São Paulo 17 de março de 2015 Procedimentos para submissão de documentos à SCMED Ato legal: Comunicado nº 7, de 31 de julho
Secretaria-Executiva da Câmara de Regulação do Mercado de Medicamentos - CMED São Paulo 17 de março de 2015 Procedimentos para submissão de documentos à SCMED Ato legal: Comunicado nº 7, de 31 de julho
Portaria n.º 510, de 13 de outubro de 2015.
 Serviço Público Federal MINISTÉRIO DO DESENVOLVIMENTO, INDÚSTRIA E COMÉRCIO EXTERIOR INSTITUTO NACIONAL DE METROLOGIA, QUALIDADE E TECNOLOGIA-INMETRO Portaria n.º 510, de 13 de outubro de 2015. O PRESIDENTE
Serviço Público Federal MINISTÉRIO DO DESENVOLVIMENTO, INDÚSTRIA E COMÉRCIO EXTERIOR INSTITUTO NACIONAL DE METROLOGIA, QUALIDADE E TECNOLOGIA-INMETRO Portaria n.º 510, de 13 de outubro de 2015. O PRESIDENTE
RESOLUÇÃO - RDC Nº 120, DE 25 DE ABRIL DE 2002
 RESOLUÇÃO - RDC Nº 120, DE 25 DE ABRIL DE 2002 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da atribuição que lhe confere o inciso IV do art. 11 do Regulamento da ANVISA, aprovado
RESOLUÇÃO - RDC Nº 120, DE 25 DE ABRIL DE 2002 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da atribuição que lhe confere o inciso IV do art. 11 do Regulamento da ANVISA, aprovado
adota a seguinte Consulta Pública e eu, Diretor-Presidente, determino a sua publicação:
 Agência Nacional de Vigilância Sanitária www.anvisa.gov.br Consulta Pública nº 56 de 13 de setembro de 2006. D.O.U de 14/09/2006. A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso
Agência Nacional de Vigilância Sanitária www.anvisa.gov.br Consulta Pública nº 56 de 13 de setembro de 2006. D.O.U de 14/09/2006. A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso
Agência Nacional de Vigilância Sanitária ANVISA Gerência-Geral de Tecnologia de Produtos para a Saúde - GGTPS
 Agência Nacional de Vigilância Sanitária ANVISA Gerência-Geral de Tecnologia de Produtos para a Saúde - GGTPS NOTA TÉCNICA N 002/2009/GGTPS/ANVISA 1. Objeto: Orientações para o Peticionamento de Certificado
Agência Nacional de Vigilância Sanitária ANVISA Gerência-Geral de Tecnologia de Produtos para a Saúde - GGTPS NOTA TÉCNICA N 002/2009/GGTPS/ANVISA 1. Objeto: Orientações para o Peticionamento de Certificado
RESOLUÇÃO - RDC Nº 124, DE 13 DE MAIO DE 2004.
 RESOLUÇÃO - RDC Nº 124, DE 13 DE MAIO DE 2004. Dispõe sobre os procedimentos gerais para utilização dos serviços de protocolo de correspondências e documentos técnicos no âmbito da Anvisa e sobre as formas
RESOLUÇÃO - RDC Nº 124, DE 13 DE MAIO DE 2004. Dispõe sobre os procedimentos gerais para utilização dos serviços de protocolo de correspondências e documentos técnicos no âmbito da Anvisa e sobre as formas
Seminário Valor Econômico Complexo Industrial da Saúde Agência Nacional de Vigilância Sanitária Regulação em Saúde
 Seminário Valor Econômico Complexo Industrial da Saúde Agência Nacional de Vigilância Sanitária Regulação em Saúde Dirceu Raposo de Mello Diretor-Presidente São Paulo, 1º de março de 2010 Vigilância Sanitária
Seminário Valor Econômico Complexo Industrial da Saúde Agência Nacional de Vigilância Sanitária Regulação em Saúde Dirceu Raposo de Mello Diretor-Presidente São Paulo, 1º de março de 2010 Vigilância Sanitária
Experiência: Revisão dos Procedimentos de Pós-Registro de Medicamentos
 Experiência: Revisão dos Procedimentos de Pós-Registro de Medicamentos Agência Nacional de Vigilância Sanitária (Anvisa) Unidade Técnica da Anvisa (Untec) Responsável: Mônica da Luz Carvalho Soares Equipe:
Experiência: Revisão dos Procedimentos de Pós-Registro de Medicamentos Agência Nacional de Vigilância Sanitária (Anvisa) Unidade Técnica da Anvisa (Untec) Responsável: Mônica da Luz Carvalho Soares Equipe:
Diário Oficial Imprensa Nacional
 INSTRUÇÃO NORMATIVA Nº 13, DE 22 DE OUTUBRO DE 2009 Dispõe sobre a documentação para regularização de equipamentos médicos das Classes de Risco I e II. A Diretoria Colegiada da Agência Nacional de Vigilância
INSTRUÇÃO NORMATIVA Nº 13, DE 22 DE OUTUBRO DE 2009 Dispõe sobre a documentação para regularização de equipamentos médicos das Classes de Risco I e II. A Diretoria Colegiada da Agência Nacional de Vigilância
INFORME DO PROGRAMA CIÊNCIA SEM FRONTEIRAS
 INFORME DO PROGRAMA CIÊNCIA SEM FRONTEIRAS FACULDADE INDEPENDENTE DO NORDESTE A Direção Geral da Faculdade Independente do Nordeste, com vistas à chamada para seleção de alunos para o Programa Ciência
INFORME DO PROGRAMA CIÊNCIA SEM FRONTEIRAS FACULDADE INDEPENDENTE DO NORDESTE A Direção Geral da Faculdade Independente do Nordeste, com vistas à chamada para seleção de alunos para o Programa Ciência
RESOLUÇÃO NORMATIVA - RN No- 187, DE 9 DE MARÇO DE 2009
 AGÊNCIA NACIONAL DE SAÚDE SUPLEMENTAR DIRETORIA COLEGIADA RESOLUÇÃO NORMATIVA - RN No- 187, DE 9 DE MARÇO DE 2009 Estabelece normas para a geração, transmissão e controle de dados cadastrais de beneficiários
AGÊNCIA NACIONAL DE SAÚDE SUPLEMENTAR DIRETORIA COLEGIADA RESOLUÇÃO NORMATIVA - RN No- 187, DE 9 DE MARÇO DE 2009 Estabelece normas para a geração, transmissão e controle de dados cadastrais de beneficiários
Norma para Registro de Projetos de Pesquisa - UNIFEI-
 Norma para Registro de Projetos de Pesquisa - UNIFEI- Página 1 / 8 TÍTULO I Das definições Art. 1º - Projeto de Pesquisa constitui-se em um conjunto de ações que geram conhecimento científico e/ou tecnológico,
Norma para Registro de Projetos de Pesquisa - UNIFEI- Página 1 / 8 TÍTULO I Das definições Art. 1º - Projeto de Pesquisa constitui-se em um conjunto de ações que geram conhecimento científico e/ou tecnológico,
Regulamentação de Bulas de Medicamentos no Brasil RDC n 47/2009n
 Regulamentação de Bulas de Medicamentos no Brasil RDC n 47/2009n Janeiro de 2011 Motivação para a nova regra para as bulas Necessidade de definir novo marco regulatório para: traçar regra única para as
Regulamentação de Bulas de Medicamentos no Brasil RDC n 47/2009n Janeiro de 2011 Motivação para a nova regra para as bulas Necessidade de definir novo marco regulatório para: traçar regra única para as
ANEXO 3 da Ata 3/ 2000 da XXIII Reunião Especializada de Ciência e Tecnologia do MERCOSUL
 ANEXO 3 da Ata 3/ 2000 da XXIII Reunião Especializada de Ciência e Tecnologia do MERCOSUL Ata da 3 a Reunião da Comissão Temática de Capacitação de Recursos Humanos e Projetos de Pesquisa e Desenvolvimento
ANEXO 3 da Ata 3/ 2000 da XXIII Reunião Especializada de Ciência e Tecnologia do MERCOSUL Ata da 3 a Reunião da Comissão Temática de Capacitação de Recursos Humanos e Projetos de Pesquisa e Desenvolvimento
REGISTRO, TRATAMENTO E APURAÇÃO DE INDISPONIBILIDADES DE USINAS HIDRÁULICAS NÃO DESPACHADAS CENTRALIZADAMENTE E PARTICIPANTES DO MRE
 Procedimento de Comercialização REGISTRO, TRATAMENTO E APURAÇÃO DE INDISPONIBILIDADES DE USINAS HIDRÁULICAS NÃO DESPACHADAS CENTRALIZADAMENTE E PARTICIPANTES DO MRE Versão: 1 Início de Vigência: XX/XX/200X
Procedimento de Comercialização REGISTRO, TRATAMENTO E APURAÇÃO DE INDISPONIBILIDADES DE USINAS HIDRÁULICAS NÃO DESPACHADAS CENTRALIZADAMENTE E PARTICIPANTES DO MRE Versão: 1 Início de Vigência: XX/XX/200X
Instrução Normativa xx de... 2014.
 REGULAMENTO PARA AFASTAMENTO DE SERVIDORES DOCENTES DO INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO SUL PARA CAPACITAÇÃO EM PROGRAMAS DE PÓS-GRADUAÇÃO STRICTO SENSU E PÓS-DOUTORADO
REGULAMENTO PARA AFASTAMENTO DE SERVIDORES DOCENTES DO INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO SUL PARA CAPACITAÇÃO EM PROGRAMAS DE PÓS-GRADUAÇÃO STRICTO SENSU E PÓS-DOUTORADO
WORKSHOP Registro e Manutenção dos Produtos RN 356 IN-DIPRO 45 IN-DIPRO 46
 WORKSHOP Registro e Manutenção dos Produtos RN 356 IN-DIPRO 45 IN-DIPRO 46 NORMATIVOS Resolução Normativa nº 356, de 2014 Altera a RN nº 85, de 2004. Altera a RN nº 89, de 2003. Altera a RN nº 309, de
WORKSHOP Registro e Manutenção dos Produtos RN 356 IN-DIPRO 45 IN-DIPRO 46 NORMATIVOS Resolução Normativa nº 356, de 2014 Altera a RN nº 85, de 2004. Altera a RN nº 89, de 2003. Altera a RN nº 309, de
CÓPIA NÃO CONTROLADA. DOCUMENTO CONTROLADO APENAS EM FORMATO ELETRÔNICO. PSQ PROCEDIMENTO DO SISTEMA DA QUALIDADE
 PSQ PROCEDIMENTO DO SISTEMA DA QUALIDADE PSQ 290.0339 - PROCEDIMENTO DO SISTEMA DA QUALIDADE APROVAÇÃO CARLOS ROBERTO KNIPPSCHILD Gerente da Qualidade e Assuntos Regulatórios Data: / / ELABORAÇÃO REVISÃO
PSQ PROCEDIMENTO DO SISTEMA DA QUALIDADE PSQ 290.0339 - PROCEDIMENTO DO SISTEMA DA QUALIDADE APROVAÇÃO CARLOS ROBERTO KNIPPSCHILD Gerente da Qualidade e Assuntos Regulatórios Data: / / ELABORAÇÃO REVISÃO
MANDAMENTOS DO USO CORRETO DOS MEDICAMENTOS
 ELIEZER J. BARREIRO NATALIA MEDEIROS DE LIMA MANDAMENTOS DO USO CORRETO DOS MEDICAMENTOS ISBN 978-85-910137-1-5 INCT INOFAR/ Portal dos Fármacos 2009 DOS MEDICAMENTOS INCT INOFAR/ Portal dos Fármacos 2009
ELIEZER J. BARREIRO NATALIA MEDEIROS DE LIMA MANDAMENTOS DO USO CORRETO DOS MEDICAMENTOS ISBN 978-85-910137-1-5 INCT INOFAR/ Portal dos Fármacos 2009 DOS MEDICAMENTOS INCT INOFAR/ Portal dos Fármacos 2009
Versão: 2 Início de Vigência: 27.11.2006 Instrumento de Aprovação: Despacho ANEEL nº 2.773, de 27 de novembro de 2006
 Procedimento de Comercialização Versão: 2 Início de Vigência: Instrumento de Aprovação: Despacho ANEEL nº 2.773, de 27 de novembro de 2006 ÍNDICE 1. APROVAÇÃO... 3 2. HISTÓRICO DE REVISÕES... 3 3. PROCESSO
Procedimento de Comercialização Versão: 2 Início de Vigência: Instrumento de Aprovação: Despacho ANEEL nº 2.773, de 27 de novembro de 2006 ÍNDICE 1. APROVAÇÃO... 3 2. HISTÓRICO DE REVISÕES... 3 3. PROCESSO
REFERÊNCIA SIM SIM NÃO. Inovando para o seu bem-estar.
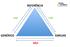 REFERÊNCIA SIM SIM GENÉRICO SIMILAR NÃO SIM SIM NÃO RDC 58 de 13/10/14 Intercambialidade entre medicamento similar e referência O que muda? A intercambialidade entre o similar e o referência já pode ser
REFERÊNCIA SIM SIM GENÉRICO SIMILAR NÃO SIM SIM NÃO RDC 58 de 13/10/14 Intercambialidade entre medicamento similar e referência O que muda? A intercambialidade entre o similar e o referência já pode ser
Agência Nacional de Vigilância Sanitária ANVISA
 Agência Nacional de Vigilância Sanitária ANVISA Coordenação do Comitê Gestor da Implantação do Sistema Nacional de Controle de Medicamentos SNCM Portaria nº 176, de 10/02/2014 NOTA TÉCNICA Nº 01/2015 Considerando
Agência Nacional de Vigilância Sanitária ANVISA Coordenação do Comitê Gestor da Implantação do Sistema Nacional de Controle de Medicamentos SNCM Portaria nº 176, de 10/02/2014 NOTA TÉCNICA Nº 01/2015 Considerando
Instruções gerais para o preenchimento do formulário
 Instruções gerais para o preenchimento do formulário Cada tipo de tecnologia (medicamento, produto para saúde ou procedimento) possui um formulário específico. Alguns campos poderão não aparecer dependendo
Instruções gerais para o preenchimento do formulário Cada tipo de tecnologia (medicamento, produto para saúde ou procedimento) possui um formulário específico. Alguns campos poderão não aparecer dependendo
RESOLUÇÃO Nº 74/2011
 Conselho de Ensino, Pesquisa e Extensão RESOLUÇÃO Nº 74/2011 DÁ NOVA REDAÇÃO À RESOLUÇÃO Nº 81/04 QUE TRATA DAS ATIVIDADES COMPLEMENTARES COMO COMPONENTE CURRICULAR DOS CURSOS DE GRADUAÇÃO DA UNIVERSIDADE
Conselho de Ensino, Pesquisa e Extensão RESOLUÇÃO Nº 74/2011 DÁ NOVA REDAÇÃO À RESOLUÇÃO Nº 81/04 QUE TRATA DAS ATIVIDADES COMPLEMENTARES COMO COMPONENTE CURRICULAR DOS CURSOS DE GRADUAÇÃO DA UNIVERSIDADE
Amostra grátis de remédios: ANVISA regula a produção e dispensação
 Amostra grátis de remédios: ANVISA regula a produção e dispensação Profª Dra Roseli Calil / DEC Enfº Adilton D. Leite / SADP A ANVISA, através da RDC (RESOLUÇÃO DA DIRETORIA COLEGIADA da Agência Nacional
Amostra grátis de remédios: ANVISA regula a produção e dispensação Profª Dra Roseli Calil / DEC Enfº Adilton D. Leite / SADP A ANVISA, através da RDC (RESOLUÇÃO DA DIRETORIA COLEGIADA da Agência Nacional
A política do medicamento: passado, presente e futuro
 A política do medicamento: passado, presente e futuro Barcelos, 27 de março de 2015 Ricardo Ramos (Direção de Avaliação Económica e Observação do Mercado) INFARMED - Autoridade Nacional do Medicamento
A política do medicamento: passado, presente e futuro Barcelos, 27 de março de 2015 Ricardo Ramos (Direção de Avaliação Económica e Observação do Mercado) INFARMED - Autoridade Nacional do Medicamento
Tecnologia da Informação
 Tecnologia da Informação Os sistemas ERP são divididos em módulos, tanto comercial quanto didaticamente, dentre os quais os mais clássicos são: financeiro, materiais, vendas, controladoria, qualidade,
Tecnologia da Informação Os sistemas ERP são divididos em módulos, tanto comercial quanto didaticamente, dentre os quais os mais clássicos são: financeiro, materiais, vendas, controladoria, qualidade,
DIRETRIZES DE CONTROLE EXTERNO Projeto Qualidade e Agilidade dos TCs QATC2
 DE CONTROLE EXTERNO Projeto Qualidade e Agilidade dos TCs QATC2 Resolução Atricon 02/2014 Controle Externo Concomitante Coordenador: Cons. Valter Albano da Silva TCE/MT Resolução Atricon 09/2014 LC123/2006
DE CONTROLE EXTERNO Projeto Qualidade e Agilidade dos TCs QATC2 Resolução Atricon 02/2014 Controle Externo Concomitante Coordenador: Cons. Valter Albano da Silva TCE/MT Resolução Atricon 09/2014 LC123/2006
EDITAL nº 04, de 06 de janeiro de 2015
 EDITAL nº 04, de 06 de janeiro de 2015 EDITAL PARA SELEÇÃO DE PROJETOS RELATIVOS A NÚCLEOS DE ESTUDOS AFRO-BRASILEIROS E INDÍGENAS E CONCESSÃO DE BOLSAS DE EXTENSÃO E INICIAÇÃO CIENTÍFICA PARA NEABI -
EDITAL nº 04, de 06 de janeiro de 2015 EDITAL PARA SELEÇÃO DE PROJETOS RELATIVOS A NÚCLEOS DE ESTUDOS AFRO-BRASILEIROS E INDÍGENAS E CONCESSÃO DE BOLSAS DE EXTENSÃO E INICIAÇÃO CIENTÍFICA PARA NEABI -
Nova RDC 09/15 para a realização de ensaios clínicos com medicamentos no Brasil
 Nova RDC 09/15 para a realização de ensaios clínicos com medicamentos no Brasil Flávia Regina Souza Sobral COPEC/ANVISA 10/04/2015 Proposta de RDC - Objetivos da Atuação Regulatória: Harmonizar o marco
Nova RDC 09/15 para a realização de ensaios clínicos com medicamentos no Brasil Flávia Regina Souza Sobral COPEC/ANVISA 10/04/2015 Proposta de RDC - Objetivos da Atuação Regulatória: Harmonizar o marco
Inspeção dos Centros de PesquisapelaANVISA
 Inspeção dos Centros de PesquisapelaANVISA ALESSANDRO FERREIRA DO NASCIMENTO Coordenação de Pesquisas e Ensaios Clínicos e Medicamentos Novos COPEM GERÊNCIA-GERAL DE MEDICAMENTOS GGMED Definição PESQUISAS
Inspeção dos Centros de PesquisapelaANVISA ALESSANDRO FERREIRA DO NASCIMENTO Coordenação de Pesquisas e Ensaios Clínicos e Medicamentos Novos COPEM GERÊNCIA-GERAL DE MEDICAMENTOS GGMED Definição PESQUISAS
Questões Frequentes sobre Medicamentos de dispensa exclusiva em farmácia
 Questões Frequentes sobre Medicamentos de dispensa exclusiva em farmácia 1- O que são Medicamentos sujeitos a receita médica de dispensa exclusiva em farmácia (MSRM-EF)? É uma sub-categoria dos Medicamentos
Questões Frequentes sobre Medicamentos de dispensa exclusiva em farmácia 1- O que são Medicamentos sujeitos a receita médica de dispensa exclusiva em farmácia (MSRM-EF)? É uma sub-categoria dos Medicamentos
Reavaliação: a adoção do valor de mercado ou de consenso entre as partes para bens do ativo, quando esse for superior ao valor líquido contábil.
 Avaliação e Mensuração de Bens Patrimoniais em Entidades do Setor Público 1. DEFINIÇÕES Reavaliação: a adoção do valor de mercado ou de consenso entre as partes para bens do ativo, quando esse for superior
Avaliação e Mensuração de Bens Patrimoniais em Entidades do Setor Público 1. DEFINIÇÕES Reavaliação: a adoção do valor de mercado ou de consenso entre as partes para bens do ativo, quando esse for superior
DECLARAÇÕES EUROPEIAS DA FARMÁCIA HOSPITALAR
 DECLARAÇÕES EUROPEIAS DA FARMÁCIA HOSPITALAR As páginas que se seguem constituem as Declarações Europeias da Farmácia Hospitalar. As declarações expressam os objetivos comuns definidos para cada sistema
DECLARAÇÕES EUROPEIAS DA FARMÁCIA HOSPITALAR As páginas que se seguem constituem as Declarações Europeias da Farmácia Hospitalar. As declarações expressam os objetivos comuns definidos para cada sistema
CARTILHA INSCRIÇÃO MUNICIPAL E REDESIM
 CARTILHA INSCRIÇÃO MUNICIPAL E REDESIM 1- ATRAVÉS DA REDESIM PORTAL REGIN 1.1 -SOLICITAÇÃO DE INSCRIÇÃO MUNICIPAL ( EMPRESA SEM REGISTRO NA JUCEB) PASSO 1: PEDIDO DE VIABILIDADE DE INSCRIÇÃO A empresa
CARTILHA INSCRIÇÃO MUNICIPAL E REDESIM 1- ATRAVÉS DA REDESIM PORTAL REGIN 1.1 -SOLICITAÇÃO DE INSCRIÇÃO MUNICIPAL ( EMPRESA SEM REGISTRO NA JUCEB) PASSO 1: PEDIDO DE VIABILIDADE DE INSCRIÇÃO A empresa
A Avaliação Ética da Investigação Científica de Novas Drogas:
 Unidade de Pesquisa Clínica A Avaliação Ética da Investigação Científica de Novas Drogas: A importância da caracterização adequada das Fases da Pesquisa Rev. HCPA, 2007 José Roberto Goldim Apresentado
Unidade de Pesquisa Clínica A Avaliação Ética da Investigação Científica de Novas Drogas: A importância da caracterização adequada das Fases da Pesquisa Rev. HCPA, 2007 José Roberto Goldim Apresentado
VESTIBULAR 2013 PERGUNTAS FREQUENTES COM RESPOSTAS. (2013.2). Ambos utilizarão as notas do ENEM 2012.
 VESTIBULAR 2013 PERGUNTAS FREQUENTES COM RESPOSTAS 1) Como será o processo vestibular da UFCG em 2013? Serão realizando dois (2) processos seletivos. O primeiro, para os cursos com entrada para o primeiro
VESTIBULAR 2013 PERGUNTAS FREQUENTES COM RESPOSTAS 1) Como será o processo vestibular da UFCG em 2013? Serão realizando dois (2) processos seletivos. O primeiro, para os cursos com entrada para o primeiro
Regulamento dos Cursos da Diretoria de Educação Continuada
 Regulamento dos Cursos da Diretoria de Educação Continuada Art. 1º Os Cursos ofertados pela Diretoria de Educação Continuada da Universidade Nove de Julho UNINOVE regem-se pela legislação vigente, pelo
Regulamento dos Cursos da Diretoria de Educação Continuada Art. 1º Os Cursos ofertados pela Diretoria de Educação Continuada da Universidade Nove de Julho UNINOVE regem-se pela legislação vigente, pelo
Parágrafo único. O prazo de validade do CA objeto de pedido de alteração será o mesmo do CA anteriormente concedido.
 MINISTÉRIO DO TRABALHO E EMPREGO SECRETARIA DE INSPEÇÃO DO TRABALHO PORTARIA N.º 162, DE 12 DE MAIO DE 2006 (DOU de 16/05/06 Seção 1) Estabelece procedimentos para o cadastro de empresas e para a emissão
MINISTÉRIO DO TRABALHO E EMPREGO SECRETARIA DE INSPEÇÃO DO TRABALHO PORTARIA N.º 162, DE 12 DE MAIO DE 2006 (DOU de 16/05/06 Seção 1) Estabelece procedimentos para o cadastro de empresas e para a emissão
SUPRIMENTOS - FORNECEDORES
 SUMÁRIO 1. OBJETIVO... 2 2. ÂMBITO... 2 3. CONCEITOS... 2 4. NORMAS E LEGISLAÇÕES APLICÁVEIS... 3 5. INSTRUÇÕES GERAIS... 3 6. PROCEDIMENTOS... 4 7. NATUREZA DAS ALTERAÇÕES... 7 8. ANEXOS... 7 Elaboração:
SUMÁRIO 1. OBJETIVO... 2 2. ÂMBITO... 2 3. CONCEITOS... 2 4. NORMAS E LEGISLAÇÕES APLICÁVEIS... 3 5. INSTRUÇÕES GERAIS... 3 6. PROCEDIMENTOS... 4 7. NATUREZA DAS ALTERAÇÕES... 7 8. ANEXOS... 7 Elaboração:
RESOLUÇÃO Nº 20/2012, DE 14 DE AGOSTO DE 2012
 SERVIÇO PÚBLICO FEDERAL MEC - INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO TRIÂNGULO MINEIRO RESOLUÇÃO Nº 20/2012, DE 14 DE AGOSTO DE 2012 Aprova a regulamentação do Programa de Incentivo à Pesquisa,
SERVIÇO PÚBLICO FEDERAL MEC - INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO TRIÂNGULO MINEIRO RESOLUÇÃO Nº 20/2012, DE 14 DE AGOSTO DE 2012 Aprova a regulamentação do Programa de Incentivo à Pesquisa,
A solução do BANCO i para aprovação de crédito
 A solução do BANCO i para aprovação de crédito Autoria: Profª Sheila Madrid Saad Mestre em Administração de Empresas Universidade Presbiteriana Mackenzie Gislaine Stangalin Avelar Graduando em Administração
A solução do BANCO i para aprovação de crédito Autoria: Profª Sheila Madrid Saad Mestre em Administração de Empresas Universidade Presbiteriana Mackenzie Gislaine Stangalin Avelar Graduando em Administração
CIRCULAR SUSEP N o 265, de 16 de agosto de 2004.
 CIRCULAR SUSEP N o 265, de 16 de agosto de 2004. Disciplina os procedimentos relativos à adoção, pelas sociedades seguradoras, das condições contratuais e das respectivas disposições tarifárias e notas
CIRCULAR SUSEP N o 265, de 16 de agosto de 2004. Disciplina os procedimentos relativos à adoção, pelas sociedades seguradoras, das condições contratuais e das respectivas disposições tarifárias e notas
Tabela de Composição de Fenilalanina em Alimentos
 Reunião da Câmara Setorial de Alimentos - 2011 Tabela de Composição de Fenilalanina em Alimentos Gerência de Produtos Especiais Gerência-Geral de Alimentos FENILCETONÚRIA Erro inato do metabolismo que
Reunião da Câmara Setorial de Alimentos - 2011 Tabela de Composição de Fenilalanina em Alimentos Gerência de Produtos Especiais Gerência-Geral de Alimentos FENILCETONÚRIA Erro inato do metabolismo que
QUADRO PADRONIZADO PARA APRESENTAÇÃO DE SUGESTÕES E COMENTÁRIOS
 QUADRO PADRONIZADO PARA APRESENTAÇÃO DE SUGESTÕES E COMENTÁRIOS Remetente: Signatário: CIRCULAR PROPOSTA SUGESTÃO DE ALTERAÇÃO JUSTIFICATIVA OU COMENTÁRIO CIRCULAR SUSEP N.º de 2004., de Disciplina os
QUADRO PADRONIZADO PARA APRESENTAÇÃO DE SUGESTÕES E COMENTÁRIOS Remetente: Signatário: CIRCULAR PROPOSTA SUGESTÃO DE ALTERAÇÃO JUSTIFICATIVA OU COMENTÁRIO CIRCULAR SUSEP N.º de 2004., de Disciplina os
FACITEC - Faculdade de Ciências Sociais e Tecnológicas IESST Instituto de Ensino Superior Social e Tecnológico
 RESOLUÇÃO CONSU Nº. 07/2012 DE 28/08/2012. Aprova o Regulamento Atividades complementares dos cursos de graduação da Faculdade de Ciências Sociais e Tecnológicas - Facitec. O DIRETOR DA FACULDADE DE CIÊNCIAS
RESOLUÇÃO CONSU Nº. 07/2012 DE 28/08/2012. Aprova o Regulamento Atividades complementares dos cursos de graduação da Faculdade de Ciências Sociais e Tecnológicas - Facitec. O DIRETOR DA FACULDADE DE CIÊNCIAS
Perguntas e Respostas sobre Portabilidade de Carência em Planos de Saúde
 Perguntas e Respostas sobre Portabilidade de Carência em Planos de Saúde Atos Normativos ANS Agência Nacional de Saúde Suplementar Resolução Normativa 186, de 14 de janeiro de 2009 - ANS Instrução Normativa
Perguntas e Respostas sobre Portabilidade de Carência em Planos de Saúde Atos Normativos ANS Agência Nacional de Saúde Suplementar Resolução Normativa 186, de 14 de janeiro de 2009 - ANS Instrução Normativa
PRESIDÊNCIA DA REPÚBLICA
 PRESIDÊNCIA DA REPÚBLICA DECRETO Nº 8.448, DE 6 DE MAIO DE 2015 Altera o Regulamento de Fiscalização de Produtos de Uso Veterinário e dos Estabelecimentos que os Fabriquem ou Comerciem, aprovado pelo Decreto
PRESIDÊNCIA DA REPÚBLICA DECRETO Nº 8.448, DE 6 DE MAIO DE 2015 Altera o Regulamento de Fiscalização de Produtos de Uso Veterinário e dos Estabelecimentos que os Fabriquem ou Comerciem, aprovado pelo Decreto
Resolução - RDC nº 135, de 29 de maio de 2003(*)
 1 de 10 24/11/2008 17:14 Resolução - RDC nº 135, de 29 de maio de 2003(*) Republicada no D.O.U de 12/08/2003 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da atribuição que
1 de 10 24/11/2008 17:14 Resolução - RDC nº 135, de 29 de maio de 2003(*) Republicada no D.O.U de 12/08/2003 A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da atribuição que
RESOLUÇÃO - RDC Nº 23, DE 4 DE ABRIL DE 2012
 RESOLUÇÃO - RDC Nº 23, DE 4 DE ABRIL DE 2012 Dispõe sobre a obrigatoriedade de execução e notificação de ações de campo por detentores de registro de produtos para a saúde no Brasil. A Diretoria Colegiada
RESOLUÇÃO - RDC Nº 23, DE 4 DE ABRIL DE 2012 Dispõe sobre a obrigatoriedade de execução e notificação de ações de campo por detentores de registro de produtos para a saúde no Brasil. A Diretoria Colegiada
Resumo das Interpretações Oficiais do TC 176 / ISO
 Resumo das Interpretações Oficiais do TC 176 / ISO Referência RFI 011 Pergunta NBR ISO 9001:2000 cláusula: 2 Apenas os termos e definições da NBR ISO 9000:2000 constituem prescrições da NBR ISO 9001:2000,
Resumo das Interpretações Oficiais do TC 176 / ISO Referência RFI 011 Pergunta NBR ISO 9001:2000 cláusula: 2 Apenas os termos e definições da NBR ISO 9000:2000 constituem prescrições da NBR ISO 9001:2000,
