Professor Orientador: Nestor Cezar Heck
|
|
|
- Marcela Filipe Avelar
- 9 Há anos
- Visualizações:
Transcrição
1 UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL ESCOLA DE ENGENHARIA ENGENHARIA DE MATERIAIS ENG TRABALHO DE DIPLOMAÇÃO ESTUDO DA INTERAÇÃO AÇO/ATMOSFERA EM FORNOS DE TRATAMENTO TÉRMICO Aluno: Rafael Wagner Florêncio dos Santos Matrícula: 2801/97-5 Professor Orientador: Nestor Cezar Heck Setembro de 2002
2 sumário 1. Introdução REVISÃO BIBLIOGRÁFICA FUNDAMENTOS DO COMPORTAMENTO DOS GASES Pressão gasosa Difusão Densidade Viscosidade Efeito da temperatura no estado dos gases PRINCIPAIS GASES E VAPORES Oxigênio Nitrogênio Dióxido de carbono e monóxido de carbono Hidrogênio Hidrocarbonetos REAÇÕES ENTRE OS GASES NAS ATMOSFERAS DE FORNOS Dióxido de carbono mais hidrogênio Reação do gás d água CLASSIFICAÇÃO DAS ATMOSFERAS PREPARADAS PERIGO DAS ATMOSFERAS DOS FORNOS Risco de fogo Risco de explosão Toxidade ATMOSFERAS DE BASE EXOTÉRMICA Atmosferas exotérmicas ricas Produção do gás Atmosferas exotérmicas pobres Produção do gás ATMOSFERAS DE BASE ENDOTÉRMICA Aplicações Geração de atmosferas endotérmicas ATMOSFERAS EM BASE DE NITROGÊNIO PREPARADO Classificação Vantagens e desvantagens Aplicações ATMOSFERAS EM BASE DE NITROGÊNIO COMERCIAL Tipos de atmosferas em base de nitrogênio comercial Atmosferas protetivas Atmosferas reativas Atmosferas com carbono controlado Vantagens Componentes Aplicações PROCEDIMENTO EXPERIMENTAL Trabalho prático Dados gerais Material Atmosfera Fornos Medidor de gases Metodologia empregada Esferoidização Coleta dos gases Análise metalográfica Trabalho teórico Programa de simulação Simulações Sistema de equilíbrio Fe-O Decomposição do vapor d água Interação aço/atmosfera do forno
3 4. RESULTADOS E DISCUSSÃO Trabalho prático Coleta dos gases Análise metalográfica trabalho teórico Sistemas de equilíbrio Fe-O e decomposição do vapor d água Interação aço/atmosfera do forno CONCLUSÕES SUGESTÕES PARA OUTROS TRABALHOS BIBLIOGRAFIAS
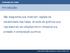
4 LISTA DE FIGURAS Figura 1 Curvas de equilíbrio para formação dos óxidos FeO/Fe 3 O 4 quando o ferro é aquecido em uma atmosfera CO/CO Figura 2 - Curvas de equilíbrio para formação dos óxidos FeO/Fe 3 O 4 quando o ferro é aquecido em uma atmosfera H 2 /H 2 O...16 Figura 3 Composição da atmosfera exotérmica em função da relação ar-metano22 Figura 4 Fotografia de um dos fornos utilizados no tratamento térmico...37 Figura 5 Fotografia do medidor de gases instalado para coleta...38 Figura 6 Imagem mostrando os valores inseridos no programa de simulação...45 Figura 7- Micrografia obtida na região superficial do aço. Observa-se uma descarbonetação nesta região Figura 8 Gráfico Temperatura x Log p(o 2 )...50 Figura 9 Resultados obtidos na simulação do sistema teórico
5 LISTA DE TABELAS Tabela 1: Propriedades de gases e vapores comuns...11 Tabela 2 Composição química do aço SAE 10B Tabela 3 Características do nitrogênio empregado...36 Tabela 4 Resultados obtidos no forno com fios-máquina com carepa...46 Tabela 5 Resultados obtidos no forno vazio...46 Tabela 6 Resultados obtidos no forno com fios-máquina sem carepa
6 RESUMO O presente trabalho mostra as atmosferas mais importantes que são utilizadas em fornos de tratamento térmico. Além do mais, dados práticos foram obtidos na esferoidização de um aço SAE 10B22, que utilizou uma atmosfera em base de nitrogênio comercial. Para a verificação destes dados, foi realizado um trabalho teórico, onde foram feitos cálculos para obtenção de um sistema teórico semelhante ao sistema real. Os dados teóricos obtidos foram simulados em um programa de simulações termodinâmicas. 6
7 ABSTRACT The present work shows the most important atmospheres that are used in heat treating furnaces. Besides, pratical data was obtained from a spheroidizing heat treatment of a SAE 10B22 steel, that used a prepared nitrogen-based atmosphere. For the verification of these data, a theoretical work was accomplished where was made calculations for obtaining of a theoretical system similar to the real system. The obtained theoretical data were simulated in a program of thermodynamic simulations. 7
8 1. INTRODUÇÃO O controle da atmosfera dos fornos é de extrema importância para se conseguir um tratamento térmico bem sucedido com uma boa precisão na obtenção das especificações metalúrgicas requeridas. A prevenção da oxidação da superfície quando os metais são expostos a temperaturas elevadas é uma das atribuições da atmosfera do forno. Quando propriamente aplicada e controlada esta atmosfera é a fonte de elementos em alguns tratamentos térmicos, como a nitretação; provoca a limpeza superficial de peças que sofreram outros processos e é um ambiente protetor contra efeitos adversos do ar quando metais são expostos à alta temperatura. O estudo da interação entre a carga e a atmosfera do forno é de extrema importância, pois através deste estudo poderá haver uma previsão se as propriedades mecânicas do material submetido ao tratamento térmico será afetada de acordo com os componentes presentes na atmosfera do forno. O objetivo deste trabalho é a verificação dos dados práticos que serão obtidos em uma esferoidização de um aço SAE 10B22, utilizando uma atmosfera em base de nitrogênio comercial, através da termodinâmica computacional. A verificação destes dados será realizada através de cálculos e de simulações feitas em um programa de simulação termodinâmica, onde o sistema teórico encontrado deverá ser o mais semelhante possível com o sistema real. 8
9 2. REVISÃO BIBLIOGRÁFICA 2.1 FUNDAMENTOS DO COMPORTAMENTO DOS GASES As moléculas gasosas estão na maioria das vezes bem separadas e se movem incessantemente no espaço em que elas estão confinadas. Os gases se diferem dos líquidos em dois aspectos; gases são altamente compressíveis e preenchem qualquer recipiente fechado no qual estejam presentes. Entretanto, gases se assemelham a líquidos no sentido de que ambos são capazes de escoar, exercer pressão em superfícies que estão em contato e exibir uma velocidade de escoamento que pode ser medida através de um orifício [1]. Embora não exista uma distinção clara entre gases e vapores, o termo vapor é usualmente aplicado para o gás que está próximo da sua temperatura de liquefação. O dióxido de carbono é usualmente referido como vapor, pois é fácil de liqüefazer. Ar, hidrogênio e nitrogênio ordinariamente são chamados de gases [1] Pressão gasosa A característica da compressibilidade dos gases leva a uma relação muito simples entre a pressão de um gás e seu volume. Essa relação é conhecida como lei de Boyle, que define que o volume de um gás confinado varia inversamente com a pressão absoluta, sendo que a temperatura esteja constante. A pressão do gás confinado pode ser medida por um manômetro com tubo em forma de U contendo mercúrio ou outros líquidos. O gás cuja pressão quer ser medida é conectado a um dos lados do manômetro, enquanto o outro lado permanece aberto. A pressão exercida pelo gás irá forçar o líquido a sair pelo lado aberto. A diferença de altura do líquido nas duas colunas multiplicada pela densidade do líquido irá indicar quanto que a pressão gasosa excede a pressão atmosférica [1]. 9
10 2.1.2 Difusão Quando dois ou mais recipientes fechados, originalmente contendo gases diferentes, são juntados para que cada gás tenha acesso a todos os recipientes, e assumindo que não haja reação química, o movimento molecular provoca que cada gás penetre em todos os recipientes postos em contato. Por esta difusão, a mistura, conseqüentemente, se torna homogênea. De acordo com a lei de Boyle, a pressão absoluta de cada gás é reduzida a um valor menor chamado de pressão parcial. A pressão da mistura gasosa resultante será igual a soma das pressões parciais dos constituintes gasosos [1]. A lei de Avogrado estabelece que, em uma mesma temperatura e pressão, volumes iguais de diferentes gases contem número igual de moléculas. Quando esta lei é aplicada para uma quantidade particular de um gás, esta quantidade é conhecida como mol. O número de moléculas em um mol de gás é conhecido como número de Avogrado. Um mol de qualquer gás contem 6 x moléculas, sendo que a 0 C e pressão atmosférica padrão de 760 mmhg ocupa 22,4 l de espaço [1] Densidade A densidade de um gás é a quantidade de massa contida por unidade de volume, e a densidade é influenciada pela pressão e pela temperatura. A densidade e a pressão crescem na mesma proporção, e os gases expandem quando aquecidos e contraem quando resfriados. A densidade do ar foi determinada com muito cuidado, sendo que 1 litro de ar em temperatura e pressão padrões pesa 1,293g e sua densidade é de 1,293 Kg/m 3. A densidade relativa de um gás é a densidade do gás comparada com a densidade do ar [1] (Tabela 1). 10
11 Tabela 1: Propriedades de gases e vapores comuns [1] PESO SÍMBOLO DENSIDADE DENSIDADE GÁS MOLECULAR QUÍMICO (Kg/m 3 ) RELATIVA APROXIMADO Ar ,97 (a) 1,293 1,000 Dióxido de carbono CO 2 44,02 1,965 1,520 Monóxido de carbono CO 28,01 1,250 0,967 Hidrogênio H 2 2,02 0,090 0,070 Metano CH 4 16,04 0,716 0,552 Nitrogênio N 2 28,01 1,250 0,968 Oxigênio O 2 32,00 1,429 1,105 Propano C 3 H 8 44,09 1,968 1,522 (a)devido ao ar ser uma mistura, não possui um peso molecular verdadeiro. Este valor é um peso molecular médio dos constituintes Viscosidade Viscosidade está presente nos gases, assim como nos líquidos, entretanto devido ao espaçamento maior entre as moléculas gasosas, a viscosidade dos gases é bem menor do que a dos líquidos. Esta fricção entre as moléculas retarda o movimento dos gases através de canais como tubos ou dutos. O coeficiente de viscosidade aumenta com a temperatura para os gases e diminue para os líquidos [1] Efeito da temperatura no estado dos gases A lei de Charles estabelece que o volume de uma massa fixa de gás e sua pressão variam diretamente com sua temperatura absoluta. Usando o efeito da temperatura uma lei geral dos gases pode ser escrita na forma de uma equação matemática, como a que segue: P 1 V 1 = P 2 V 2 T 1 T 2 11
12 Onde P é a pressão absoluta, V é o volume da massa fixa, T é a temperatura absoluta e 1 e 2 duas condições diferentes de pressão, volume e temperatura [1]. Quando a atmosfera de um forno é requerida para contribuir com elementos durante o tratamento térmico, essas leis fundamentais dos gases se tornam importantes. Muitas formas de controle são usadas para desenvolver um potencial de carbono, ou potencial de um elemento, com a atmosfera [1]. Uma medida quantitativa de um elemento pode ser obtida através da pressão parcial dos gases da fórmula usados para produzir o elemento. 2.2 PRINCIPAIS GASES E VAPORES Ar é um gás importante na atmosfera dos fornos porque está presente em fornos que não utilizam atmosferas protetoras e porque é constituinte majoritário em muitas atmosferas preparadas. O ar é constituído quimicamente de 79% de nitrogênio e 21% de oxigênio, com traços de dióxido de carbono [1]. Entretanto, sabe-se que o ar se comporta como uma atmosfera de oxigênio, pois este é o constituinte mais reativo do ar Oxigênio O oxigênio reage com a maioria dos metais para formar óxidos. Além disso, o oxigênio reage com o carbono dissolvido no aço reduzindo assim a quantidade de carbono superficial (descarbonetação) [1] Nitrogênio Nitrogênio molecular é passivo para ferrita e inteiramente satisfatório para uso como atmosfera no recozimento/esferoidização de aços baixo carbono; entretanto, deve estar completamente seco para ser utilizado como atmosfera protetiva para aços alto carbono, 12
13 porque mesmo pequenas quantidades de vapor d água no nitrogênio podem provocar descarbonetação. Nitrogênio molecular é reativo com vários aços inoxidáveis e não pode ser utilizado no tratamento térmico destes [1] Dióxido de carbono e monóxido de carbono Estes dois gases são muito importantes na atmosfera utilizada para processamento dos aços. Em temperaturas de austenitização, dióxido de carbono reage com o carbono da superfície dos aços para produzir monóxido de carbono: (C) + CO 2 2CO Onde (C) representa o carbono dissolvido na austenita. Esta reação continua até que não haja mais dióxido de carbono disponível ou até que a superfície do aço esteja completamente sem carbono - neste ponto, se existir um fornecimento contínuo de dióxido de carbono, ferro e óxido de ferro irão oxidar segundo as seguintes reações: Fe + CO 2 FeO + CO 3 FeO + CO 2 Fe 3 O 4 + CO Óxido ferroso (FeO) é o óxido estável formado acima de 555 C, enquanto o óxido magnético (Fe 3 O 4 ) é formado abaixo de 555 C, como mostra a Figura 1 [1]. 13
14 Figura 1 Curvas de equilíbrio para formação dos óxidos FeO/Fe 3 O 4 quando o ferro é aquecido em uma atmosfera CO/CO 2 [1] As reações acima irão continuar até o equilíbrio for estabelecido, sendo que estas evoluem em uma taxa que depende do tempo, temperatura e pressão do sistema [1] Hidrogênio O hidrogênio reduz o óxido de ferro para ferro. Sob certas condições, hidrogênio pode agir como agente descarbonetante do aço. O efeito descarbonetante do hidrogênio no aço depende da temperatura do forno, quantidade de umidade (do gás e do forno), tempo em temperatura e quantidade de carbono do aço. O efeito descarbonetante do hidrogênio em 705 C ou abaixo é desprezível, mas aumenta significadamente acima desta temperatura. Vapor d água aumenta o efeito descarbonetante, porque esta dissocia e passa a ser uma fonte de hidrogênio nascente e oxigênio. O hidrogênio reage com o carbono do aço para formar metano [1]: (C) + 4H CH 4 Oxigênio reage com o carbono do aço para formar monóxido de carbono [1]: 14
15 (C) + O CO Mesmo uma atmosfera de hidrogênio com ponto de orvalho baixo possui algum efeito descarbonetante, particularmente em aços alto carbono devido à habilidade do gás, mesmo quando não está na condição de nascente, em reagir com o carbono [1]: (C) + 2H 2 CH 4 Obviamente, o potencial descarbonetante do hidrogênio em ambas as condições é marcadamente influenciada pela quantidade de carbono do aço e é esperado que aumente diretamente com o aumento da quantidade de carbono. Vapor d água é oxidante para o ferro [1]: Fe + H 2 O FeO + H 2 E combina com o carbono do aço para formar monóxido de carbono e hidrogênio [1]: (C) + H 2 O CO + H 2 É reativo com a superfície do aço em temperaturas baixas e com pressões parciais baixas. É a principal causa do azulamento durante o ciclo de resfriamento. O efeito do vapor d água na oxidação do ferro em várias temperaturas está indicado pelas curvas de equilíbrio mostradas na Figura 2 [1]. 15
16 Figura 2 - Curvas de equilíbrio para formação dos óxidos FeO/Fe 3 O 4 quando o ferro é aquecido em uma atmosfera H 2 /H 2 O [1] Hidrocarbonetos Os gases hidrocarbonetos que são normalmente adicionados ou encontrados em atmosferas de fornos são metano (CH 4 ), etano (C 2 H 6 ), propano (C 3 H 8 ) e butano (C 4 H 10 ). Estes gases conferem uma tendência cementante para a atmosfera do forno. A atividade química em reagir com a superfície quente do aço depende da decomposição térmica de cada um e da tendência de formar carbono nascente na superfície do aço, além da temperatura do forno e da carga utilizada. A decomposição térmica resulta na formação de fuligem em quantidades proporcionais ao número de átomos de carbono nos hidrocarbonetos; portanto, propano e butano são mais suscetíveis a formação de fuligem na câmara dos fornos do que etano e metano [1]. 2.3 REAÇÕES ENTRE OS GASES NAS ATMOSFERAS DE FORNOS Os gases presentes em fornos de queima direta são os gases criados na combustão de um combustível hidrocarboneto. A 16
17 composição destes gases dentro do forno é uma mistura de alguns, ou todos, os gases citados a seguir: dióxido de carbono, monóxido de carbono, hidrogênio, oxigênio, nitrogênio e vapor d água [1]. Quando os queimadores são ajustados para operar com um excesso de ar, os produtos de combustão incompleta como monóxido de carbono e hidrogênio são minimizados, mas existem quantidades residuais de oxigênio. Inversamente, em queimadores operando com uma deficiência de ar de combustão, consomem todo o oxigênio disponível antes da combustão completa do combustível. Nesse caso, oxigênio residual é minimizado e produz-se monóxido de carbono e hidrogênio em maior quantidade. Sob todas as circunstancias, quantidades substanciais de vapor d água são produzidas pela combustão [1]. Outros fatores que podem afetar os gases constituintes da atmosfera do forno são a eficiência do queimador, a selagem do forno e o tamanho da porta de abertura. As aberturas influenciam em uma possível infiltração de ar e por seguinte um aumento do teor de oxigênio dentro do forno. Não obstante, fornos equipados com múltiplos queimadores podem operar com taxas ar-combustível variadas produzindo uma atmosfera de composição imprevisível [1]. Quando a atmosfera possui oxigênio em excesso, além de vapor d água e dióxido de carbono, o potencial de oxidação promove uma formação de carepa no aço. Operação de queimadores com deficiência de ar de combustão produzem muito menos oxigênio e grandes quantidades de monóxido de carbono e hidrogênio, que são redutores e podem causar a descarbonetação da superfície do aço. O óxido formado pelo dióxido de carbono e pelo vapor d água é aderente e não é removido com facilidade. A quantidade de carepa formada é função da temperatura do forno e do tempo que o material é mantido em temperatura [1]. 17
18 2.3.1 Dióxido de carbono mais hidrogênio O hidrogênio irá reagir, ou com o dióxido de carbono, ou com o oxigênio para formar vapor d água [1]. O vapor d água possui um alto potencial oxidante ou descarbonetante do aço, portanto deve ser bem controlado na atmosfera Reação do gás d água As reações listadas abaixo, nas quais aço ou ferro são oxidados em elevadas temperaturas, são irreversíveis e não podem ser controladas [1]: 2 Fe + O 2 2FeO 4 Fe + 3 O 2 2 Fe 2 O 3 3 Fe + 2 O 2 Fe 3 O 4 Outras reações de oxidação gás-metal, entretanto, são reversíveis e podem ser controladas [1], além de poderem ser empregadas vantajosamente. São elas: Fe + H 2 O FeO + H 2 Fe + CO 2 FeO + CO Vapor d água e dióxido de carbono são gases oxidantes, e hidrogênio e monóxido de carbono são gases redutores. As quantidades de gases redutores ou gases oxidantes podem ser grandes o suficiente para uma anular o efeito do outra. Através de um controle apropriado destas reações, pode ser produzido um efeito neutro, oxidante ou redutor [1]. Estas reações opostas podem ser controladas através da reação do gás d água [1], que é a seguinte: 18
19 CO + H 2 O CO 2 + H 2 Os gases presentes na reação do gás d água reagem com a superfície do aço para causar oxidação ou redução, dependendo da condição de equilíbrio correspondente a temperatura e composição do sistema [1]. A 830 C, o potencial oxidante do dióxido de carbono e do vapor d água são iguais, e o potencial redutor do monóxido de carbono e do hidrogênio também. Nesta temperatura, portanto, a constante de equilíbrio da reação do gás de água tem valor unitário. Acima de 830 C, o dióxido de carbono é um agente oxidante mais forte que o vapor d água, e o hidrogênio é um agente redutor mais forte que o monóxido de carbono. Abaixo de 830 C o inverso é verdadeiro [1]. Considerando as reações: C + CO 2 2CO CO + H 2 O CO 2 + H 2 C + H 2 O CO + H 2 Suas constantes de equilíbrio são respectivamente: K 1 = [CO 2 ] [CO] 2 K 2 = [CO][H 2 O] [CO 2 ][H 2 ] K 3 = [H 2 O] [CO][H 2 ] 19
20 2.4 CLASSIFICAÇÃO DAS ATMOSFERAS PREPARADAS Grande parte das atmosferas preparadas são normalmente referidas por seu nome genérico. A American Gas Association (AGA) classificou estas atmosferas comerciais em seis grupos [1], mas neste trabalho serão descritas as três mais importantes. Classe 100, base exotérmica: formada por uma combustão parcial ou completa de uma mistura ar-gás; o vapor d água deve ser removido para a obtenção de um ponto de orvalho desejável. Classe 200, base de nitrogênio preparado: Uma atmosfera de base exotérmica com o dióxido de carbono e o vapor d água removidos. Classe 300, base endotérmica: Formada pela reação parcial de uma mistura de ar e gás combustível em uma câmara externa catalisadora aquecida. 2.5 PERIGO DAS ATMOSFERAS DOS FORNOS As atmosferas dos fornos constituem uns dos pontos mais perigosos em um tratamento térmico [1]. Em geral, são considerados três grandes riscos: risco de fogo, risco de explosão e toxidade Risco de fogo Quando as atmosferas contem mais de 4% de gases combustíveis são classificadas como flamáveis. Incluída nesta porcentagem está uma margem de segurança que não deve ser 20
21 ignorada. Os gases combustíveis H2, CO, CH4 e outros hidrocarbonetos nunca devem ser inseridos nas câmaras dos fornos em temperaturas inferiores a 760 C sem ter ocorrido uma purga apropriada com gás inerte [1] Risco de explosão Em algum ponto, misturas de ar e gás combustível irão explodir se sofrerem ignição. Quando uma câmara de forno é propriamente gaseificada com temperaturas da câmara em 760 C ou maior, os gases combustíveis irão queimar antes de criar um perigo de explosão [1] Toxidade Muitos dos gases constituintes das atmosferas dos fornos são tóxicos. Os produtos devem ser ventilados para fora do local de trabalho para evitar uma diluição do oxigênio local disponível [1]. 2.6 ATMOSFERAS DE BASE EXOTÉRMICA Gases exotérmicos (classe 100) tem sido utilizado por muitos anos como atmosferas preparadas de baixo custo. Atmosferas exotérmicas são divididas em duas classes básicas: rica e pobre. Atmosferas exotérmicas ricas (classe 102) possuem uma capacidade de redução moderada com uma combinação de 10 a 21% de monóxido de carbono e hidrogênio, enquanto que atmosferas exotérmicas pobres (classe 101), usualmente com uma combinação de 1 a 4% de monóxido de carbono e hidrogênio, possuem uma capacidade redutora mínima [1]. 21
22 Figura 3 Composição da atmosfera exotérmica em função da relação ar-metano [1] Atmosferas exotérmicas ricas As propriedades redutoras das atmosferas exotérmicas ricas podem ser variadas para a adequação desta para processos específicos, como recozimento de aço ou sinterização de pós metálicos [1]. A Figura 3 indica o range usual de operação do gerador de gás e as mudanças ocorridas, pela medição do volume seco, dos seguintes constituintes gasosos em diferentes ajustes da relação argás: dióxido de carbono, monóxido de carbono, hidrogênio e metano não queimado. O restante da mistura é nitrogênio. Devido a essas atmosferas possuírem um potencial de carbono abaixo de 0,1%, o tratamento térmico dos aços geralmente é limitado para processos de aços baixo carbono para minimizar a descarbonetação. Vapor d água está presente em quantidades substanciais e deve ser removido parcialmente por um resfriamento inicial e por uma secagem refrigerante até um ponto de orvalho equivalente de 5 C. Este procedimento deve ser seguido por uma 22
23 desidratação com um dessecante adsorvente para pontos de orvalho finais de 40 a 50 C, segundo as aplicações requeridas [1] Produção do gás Um gás exotérmico rico é produzido pela combustão de um hidrocarboneto combustível, como metano e propano, com uma relação ar-gás bem controlada. Essa mistura ar-gás é queimada em um espaço confinado para manter uma temperatura de reação de pelo menos 980 C em tempo suficiente para permitir que a reação de combustão alcance o equilíbrio. Calor é obtido diretamente da combustão. O gás resultante é então resfriado para remover parte do vapor d água formado pela combustão [1]. Neste processo, a reação teórica simplificada do metano com o ar é: CH 4 + 1,25 O 2 + 4,75 N 2 0,375 CO 2 + 0,625 CO + 0,88 H 2 + 4,75 N 2 + 1,12 H 2 O + calor Onde 1 volume de combustível e 6 volumes de ar produzem 6,63 volumes de produto de mistura gasosa, com o vapor d água removido. Na prática, geradores de gás exotérmico são raramente operados com uma relação ar-gás inferior a 6,6 para 1, para prevenir a formação de fuligem como resultado da reação incompleta. Porcentagens traço de metano que não reagiu também existem no produto gasoso [1] Atmosferas exotérmicas pobres Atmosferas exotérmicas pobres geralmente possuem uso limitado na maioria dos processos de tratamento térmico, particularmente para materiais ferrosos, exceto quando estas 23
24 atmosferas são usadas intencionalmente como agentes oxidantes superficiais ou em operações especializadas em baixa temperatura [1]. Pode-se observar na Figura 3 o range usual de operação do gerador de gás e as mudanças ocorridas nos produtos gasosos constituídos de dióxido de carbono, monóxido de carbono e hidrogênio. O balanço da mistura é nitrogênio. A capacidade redutora da atmosfera é limitada e o processo de retirada do vapor d água, presente em grandes quantidades, é o mesmo utilizado nas atmosferas exotérmicas ricas [1] Produção do gás Um gás exotérmico pobre é produzido pela combustão de um hidrocarboneto combustível, como metano e propano, com uma relação ar-gás bem controlada. A mistura ar-gás é queimada em um espaço confinado por tempo suficiente para permitir que a reação alcance o equilíbrio. O gás resultante é então resfriado para condensar parcialmente o vapor d água formado pela combustão [1]. A reação teórica simplificada do metano com o ar é: CH 4 + 1,9 O 2 + 7,6 N 2 0,9 CO 2 + 0,1 CO + 0,1 H 2 + 7,6 N 2 + 1,9 H 2 O + calor Onde 1 volume de combustível e 9,5 volumes de ar produzem 8,7 volumes de produto de mistura gasosa, com o vapor d água removido. Na prática, geradores de gás exotérmico são raramente operados com uma relação ar-gás maior que a requerida para produzir um mínimo de 1% total de monóxido de carbono e hidrogênio, a fim de se evitar quantidades residuais de oxigênio. Uma exceção envolve certas aplicações de purga onde pequenas quantidades de oxigênio podem ser toleradas e a presença de combustíveis não é desejada. Neste caso, a relação ar-gás é 24
25 aumentada para operar com uma pequena quantidade de excesso de ar, mantendo 1 a 2% de oxigênio no produto gasoso [1]. 2.7 ATMOSFERAS DE BASE ENDOTÉRMICA Atmosferas de base endotérmica são produzidas em geradores que utilizam ar e um gás hidrocarboneto como combustível. Esses gases são misturados com uma proporção controlada, sendo levemente comprimidos e depois passam por uma câmara que contem um catalisador. Esta câmara é aquecida externamente a aproximadamente 1040 C. Os gases reagem na câmara para formar um gás endotérmico. A atmosfera endotérmica produzida deve ser resfriada rapidamente para assegurar a integridade da composição química [1]. Gases endotérmicos produzidos pela queima do metano possuem a típica análise seguinte: 40,4% hidrogênio, 39% nitrogênio, 19,8% monóxido de carbono, 0,5% metano, 0,2% vapor d água e 0,1% dióxido de carbono [1] Aplicações Atmosferas endotérmicas podem ser usadas em praticamente em todos os processos de forno que requerem uma alta condição redutora. Outra aplicação é sendo utilizado como gás portante na cementação gasosa [1] Geração de atmosferas endotérmicas Na geração de atmosferas endotérmicas, o gás hidrocarboneto e o ar são medidos em proporções que assegurem um oxigênio suficiente para formar monóxido de carbono e hidrogênio, sem estar em excesso para formação de dióxido de carbono e vapor d água [1]. 25
26 Para uma reação completa do gás de análise consistente, a temperatura dentro do catalisador deve estar de 980 C a 1040 C. Após a passagem pelo catalisador, os gases são resfriados para uma temperatura inferior a 315 C, prevenindo assim uma reação reversa que forme carbono e dióxido de carbono a partir do monóxido de carbono [1]: 2 CO C + CO 2 A reação na direção indicada predomina em temperaturas entre 705 C e 480 C [1]. Devido o gás natural ser composto praticamente só de metano, a reação química geral ocorrida no gerador de gás endotérmico que utiliza gás natural como combustível pode ser expressa como: 2 CH 4 + O 2 2 CO + 4 H 2 Negligenciando 3,8 volumes de nitrogênio (antes e depois) para cada 2 volumes de metano [1]. A reação é processada em dois estágios. No primeiro, parte do metano queima com ar gerando calor. No segundo, o metano restante reage com o dióxido de carbono e com o vapor d água produzidos no primeiro estágio, provocando uma reação endotérmica. Alta temperatura e uma câmara catalítica limpa são requeridas para a obtenção de uma reação completa do gás, minimizando dióxido de carbono, excesso de metano e de vapor d água. Na prática, uma reação completa é aquela na qual a quantidade de metano no produto não excede 0,4 a 0,8% [1]. 26
27 2.8 ATMOSFERAS EM BASE DE NITROGÊNIO PREPARADO Atmosferas em base de nitrogênio preparado são atmosferas exotérmicas, produzidas pela combustão de ar e gás hidrocarboneto, nas quais quase todo o dióxido de carbono e o vapor d água são removidos. A combinação de um ponto de orvalho baixo (aproximadamente 40 C) com a ausência virtual de dióxido de carbono provoca a diferença entre as propriedades e aplicações da atmosfera preparada de base de nitrogênio e a atmosfera de base exotérmica [1]. A definição acima descrita está conforme o sistema de classificação da Associação de Gás Americana (AGA). Ainda, o termo atmosfera preparada de base de nitrogênio não é apropriado para atmosferas de fornos consistentes de uma mistura de nitrogênio comercial e outros gases, nem para atmosferas de base de amônia, embora estas possuam uma base de nitrogênio. As altas concentrações de dióxido de carbono e de vapor d água no produto da combustão podem ser reduzidas aos baixos níveis desejados por duas maneiras diferentes [1] Classificação Indiferente ao método de geração, as atmosferas em base de nitrogênio preparado são de duas grandes classes, pobre e rica. Importantes subclasses envolvem a remoção de praticamente todo o monóxido de carbono, sendo que a atmosfera gerada consiste quase exclusivamente de nitrogênio e hidrogênio [1] Vantagens e desvantagens A principal vantagem das atmosferas em base de nitrogênio preparado é a sua aplicabilidade a uma variedade de operações de 27
28 tratamento térmico para aços baixo, médio e alto carbono, além de alguns outros metais. Devido ao baixo ponto de orvalho e a ausência virtual de dióxido de carbono estas atmosferas, na ausência de oxigênio contaminante introduzido como resultado de operações no forno, não são oxidantes nem descarbonetantes, contrastando com a atmosfera de base exotérmica. Adicionalmente, o custo nominal por unidade de volume de atmosfera produzida é mais baixo que para a maioria das outras atmosferas protetivas [1]. As desvantagens deste tipo de atmosfera devem-se ao alto custo inicial dos equipamentos, o espaço requerido e a necessidade de uma manutenção e de um controle maior dos geradores [1] Aplicações Estas atmosferas podem ser usadas em praticamente todas as aplicações de fornos que não necessitem altas condições redutoras. Como a atmosfera não é descarbonetante, pode ser utilizada em recozimento/esferoidização, normalização e têmpera de aços alto e médio carbono. Entretanto, sua utilidade no tratamento térmico do aço está relacionada com o baixo ponto de orvalho, que pode ser mantido se o design do forno e sua operação prevenirem uma contaminação da atmosfera do forno com ar ou qualquer outra fonte de oxigênio. Conseqüentemente, na prática atual são usados fornos sino (bell-type) para recozimento/esferoidização de bobinas de aço. Para esta aplicação relações de 9 partes e ar para 1 parte de gás natural são empregadas para produção de uma atmosfera seca, não descarbonetante e não explosiva contendo 4% de combustíveis [1]. 28
29 2.9 ATMOSFERAS EM BASE DE NITROGÊNIO COMERCIAL As atmosferas industriais em base de nitrogênio comercial são tecnicamente aceitas para a maioria dos processamentos metálicos. A troca de muitas operações de tratamento térmico para atmosferas em base de nitrogênio comercial acelerou no fim dos anos 70 devido às mudanças ocorridas nos valores dos combustíveis hidrocarbonetos [1]. Os sistemas de atmosferas em base de nitrogênio comercial empregados na indústria de tratamento térmico utilizam gases e equipamentos que são comuns entre a maioria das aplicações. Em muitas ocasiões o componente majoritário da atmosfera é nitrogênio gasoso industrial, que é fornecido para o forno através de um sistema que consiste de um tanque de armazenamento, de um vaporizador e de uma estação de controle de pressão e vazão. O nitrogênio serve como um gás puro, seco e inerte que promove uma purga eficiente no interior do forno de tratamento térmico. O fluxo de nitrogênio pode ser enriquecido com um componente reativo, sendo que a composição resultante e a vazão são determinadas pelo design do forno, temperatura e material que sofrerá o tratamento térmico Tipos de atmosferas em base de nitrogênio comercial A classificação dos sistemas de atmosferas em base de nitrogênio comercial é feita de acordo com as três maiores categorias de função da atmosfera proteção, reatividade e controle de carbono. 29
30 Atmosferas protetivas Os sistemas de atmosferas requeridos para estas aplicações devem prevenir a oxidação ou descarbonetação da superfície metálica durante o tratamento térmico. Essas reações ocorrem se houver a presença de oxigênio residual ou vapor d água dentro do forno como resultado de uma infiltração de ar ou purga inadequada. Sabe-se que mesmo os nitrogênios comerciais mais puros possuem oxigênio livre (até 10ppm), suficiente para oxidar o ferro [2]. Assim, a atmosfera empregada pode ser de nitrogênio puro ou de nitrogênio com pequenas quantidades de um gás reativo como hidrogênio. O hidrogênio reagiria com o oxigênio livre formando vapor d água em todas as temperaturas normalmente encontradas nos processos de tratamento térmico. Em um forno típico de recozimento/esferoidização, uma atmosfera de nitrogênio comercial com aproximadamente 3% de hidrogênio evitaria a oxidação do aço, mas, por não haver uma fonte de carbono e pelo hidrogênio ser redutor, ocorreria uma descarbonetação. No entanto, se a relação hidrogênio-vapor d água for alta e a adição de hidrogênio pequena, a descarbonetação será menor [2] Atmosferas reativas Estes sistemas de atmosferas requerem uma concentração de gases reativos maior que 5% para reduzir os óxidos metálicos ou para transferir pequenas quantidades de carbono para materiais ferrosos. Os componentes reativos são geralmente hidrogênio e monóxido de carbono. As concentrações dependem da quantidade de óxido a ser removida e do nível de produtos de reação, vapor d água e dióxido de carbono que são formados na atmosfera do forno. Aplicações típicas são em sinterização e redução de pós metálicos [1]. 30
31 Atmosferas com carbono controlado A principal função deste sistema de atmosfera é de reagir com o aço de uma maneira controlada para que quantidades significantes de carbono possam ser adicionadas ou removidas da superfície do aço. Estas atmosferas são caracterizadas pelas altas concentrações de gases reativos no nitrogênio e pelo requerimento que a taxa e a quantidade de carbono transferida deve ser controlada pela composição da atmosfera. Podem ser citados componentes típicos da atmosfera como 10 a 50% H 2, 5 a 20% CO e traços (acima de 3%) de CO 2 e vapor d água. As aplicações mais comuns de atmosferas de carbono controlado incluem cementação, têmpera neutra, sinterização de pós metálicos e recuperação de carbono em materiais trabalhados à quente ou forjados [1] Vantagens Os sistemas de atmosfera de base de nitrogênio promovem uma substituição tecnicamente viável para as atmosferas geradas na maioria das aplicações de tratamento térmico. Embora os resultados desejados são praticamente os mesmos tanto para atmosferas comerciais de base de nitrogênio, quanto para atmosferas geradas, existem diferenças significativas em relação ao equipamento, operação e função entre estes sistemas [1]. As atmosferas geradas promovem uma composição de saída fixa, que é determinada pela relação ar-gás de entrada, dos equipamentos de purificação do gerador e a condição dos equipamentos e do catalisador. Os sistemas de atmosferas comerciais de base de nitrogênio geralmente iniciam com componentes elementares guardados em recipientes separados, depois formam uma blenda com uma composição de atmosfera desejada, sendo esta introduzida no forno. A composição resultante pode ser variada em tempos diferentes durante o ciclo [1,2]. 31
32 A maioria dos componentes das atmosferas em base de nitrogênio comercial é produzido ou por processos criogênicos ou por refino químico. Como resultado, os níveis de impureza são baixos, normalmente menores que 20 ppm de impureza total para o nitrogênio líquido. Adicionalmente, como não há produtos de queima de misturas ar-gás, a atmosfera resultante geralmente possui um ponto de orvalho menor que 60 C e níveis de impureza e dióxido de carbono menores que 10 ppm [1,2]. O potencial redutor ou cementante de uma atmosfera é determinado por várias reações, que estão associadas com constantes de equilíbrio [1]. Entre estas estão inclusas: FeO + H 2 Fe + H 2 O Fe + 2CO FeC + CO 2 Fe + CO + H 2 FeC + H 2 O Devido as blendas em base de nitrogênio comercial reduzirem significativamente as quantidades de vapor d'água e dióxido de carbono na atmosfera do forno, o nível de gases reativos também pode ser reduzido para manutenção de potenciais termodinâmicos aceitáveis. O resultado é que atmosferas geradas que contem aproximadamente 60% de produtos combustíveis estão sendo trocadas para atmosferas em base de nitrogênio comercial contendo menos que 10% de hidrogênio e monóxido de carbono [1]. A possibilidade de controle da composição também permite uma flexibilidade das taxas de vazão durante o ciclo do tratamento térmico. Uma das vantagens mais comuns desta característica é o uso de uma alta taxa de vazão durante o carregamento dos fornos equipados com portas. Quando a porta é aberta, existe uma mudança da vazão de nitrogênio para redução da infiltração de ar para dentro do forno. Após a porta ser fechada a vazão retorna ao nível requerido 32
33 para manutenção da pressão adequada ao forno fechado e continuar as reações superficiais gás-metal requeridas [1,2] Componentes Nitrogênio é o componente principal da maioria dos sistemas comerciais de base de nitrogênio. Como o nitrogênio é um não corrosivo, materiais especiais para construção não são requeridos, exceto que estes devem ser adequados à temperatura do nitrogênio líquido [1]. Hidrogênio é usado como gás redutor reativo na maioria das atmosferas de tratamento térmico. Em atmosferas em base de nitrogênio comercial normalmente forma uma blenda com nitrogênio para formar uma atmosfera com composição de 90% nitrogênio e 10% hidrogênio [1]. Em atmosferas em base de nitrogênio comercial, metanol é utilizado como fonte de hidrogênio e monóxido de carbono para sistemas de atmosfera reativos e de controle de carbono. Metanol é adicionado ao forno como líquido ou vapor. Quando exposto a temperaturas de forno maiores que 760 C, o metanol dissocia de acordo com a seguinte reação [1,2]: CH 3 OH 2 H 2 + CO Atmosferas em base de nitrogênio comercial contendo 20 a 40 % de metanol podem ser utilizadas em recozimento/esferoidização com temperaturas entre 690 a 810 C [2] Aplicações Atmosferas reativas são requeridas para aplicações de tratamento térmico como sinterização de pós metálicos. A atmosfera 33
34 reage com a superfície do metal para remover todos os óxidos metálicos. Na sinterização de pós metálicos, a redução dos óxidos na superfície do pó é necessária para promover uma difusão e ligação efetiva do pó compactado. A natureza reativa dessas atmosferas também pode ser aplicada para transferência de carbono. Na sinterização de pós metálicos de aço, lubrificantes podem ser removidos em uma seção do forno e o carbono se tornar disponível para o aço em outra seção [1]. Atmosferas de carbono controlado transferem carbono da atmosfera para a superfície da peça metálica (C) através de reações controladas gás-metal [1]: 2 CO C + CO 2 CO + H 2 C + H 2 O Como a transferência de carbono é requisitada para muitas destas aplicações, é comum encontrar concentrações mais altas de monóxido de carbono e de hidrogênio nestas atmosferas do que em atmosferas protetivas e reativas [1]. Os sistemas de atmosferas de carbono controlado são usados, por exemplo, na cementação superficial de peças de aço e em têmpera neutra. O essencial na aplicação destas atmosferas é o controle. Na têmpera neutra, o potencial de carbono da atmosfera deve estar similar ao da superfície do aço para evitar descarbonetação ou cementação [1]. 34
35 3. PROCEDIMENTO EXPERIMENTAL O procedimento experimental pode ser dividido em duas partes. Na primeira parte foi efetuado um trabalho prático, onde um material foi submetido a um processo de esferoidização, sendo então feitas as aquisições dos dados da atmosfera. Posteriormente, foram realizadas análises metalográficas em uma amostra do material que foi submetida ao processo de tratamento térmico citado anteriormente. Na segunda parte foi efetuado um trabalho teórico, onde foi tentada a verificação dos resultados práticos através de cálculos e de simulações realizadas em um programa de computador. 3.1 TRABALHO PRÁTICO Dados gerais Material O material utilizado foi um aço baixo carbono SAE 10B22. Este material estava em forma de fios-máquina com diâmetro de 1,31cm. A composição química típica deste aço está expressa na Tabela 2. Este aço está classificado na classe de aços construção mecânica ligados para deformação a frio [3]. Tabela 2 Composição química do aço SAE 10B22 %C %Si %Mn %P %S %Cr %Ni %Mo %Ti %Al %Cu %B 0,18 0,21 0,15 0,25 0,70 0,85 0,04 0,025 0,015 0,20 0,25 0,06 0,06 0,025 0,040 0,35 0,002 0, Atmosfera A atmosfera utilizada no ciclo da esferoidização foi uma atmosfera em base de nitrogênio comercial. O nitrogênio é de alta pureza proveniente da White Martins. Algumas características do gás estão descritas na Tabela 3 [4]. 35
36 Tabela 3 Características do nitrogênio empregado Produto NITROGÊNIO Nome Químico Grupo Químico NITROGÊNIO Considerado como gás inerte Fórmula N 2 Peso Molecular 28,01 Ponto de Ebulição (760 mmhg) -195,8 ºC Ponto de Congelamento -209,9 ºC Massa específica (kg/m 3 ) 1,153 Densidade do Vapor (ar=1) 0,967 Percentagem de Matéria Volátil em Volume Aparência e Odor Impurezas 100 Gás incolor e inodoro a pressão e temperatura normais; sem gosto. <5ppm O 2, <5ppm H 2 O Fornos Os fornos onde foram realizados o tratamento térmico de esferoidização são fornos tipo sino da Brasimet. Estes fornos são operados através de pontes rolantes. A câmara interna destes fornos possui um diâmetro de 4,05 m e uma altura de 5,9 m. Na Figura 4 observa-se um dos fornos utilizados para a realização do tratamento térmico. Estes fornos são capazes de tratar de 20 a 22t por carga. 36
37 Figura 4 Fotografia de um dos fornos utilizados no tratamento térmico Medidor de gases O equipamento que foi utilizado para a aquisição dos dados da atmosfera foi um medidor de gases BACHARACH ECA-450. Este equipamento mede diretamente os teores de CO (ppm), HC (%), NO (ppm), SO2(ppm), O2(%), variação de pressão, temperatura do ar primário ou de referência e temperatura do gás de saída. O equipamento também calcula, para o caso de combustão, outros parâmetros a partir dos dados medidos Metodologia empregada Esferoidização Primeiramente foram colocadas dentro do forno sino bobinas de fio-máquina do material a ser tratado. Foi iniciada então uma purga da atmosfera interna através da vazão de nitrogênio para dentro do forno. Após a purga inicial, a vazão de nitrogênio para dentro do forno é diminuída, sendo efetuada somente para manter pressão de nitrogênio dentro do forno levemente positiva durante o ciclo para evitar a infiltração de ar. A temperatura foi elevada lentamente, da temperatura ambiente até a temperatura de trabalho, que é normalmente de 37
38 725 ºC [5]. A carga permaneceu nesta temperatura por algumas horas, sendo posteriormente resfriada em uma taxa lenta até a temperatura ambiente. Durante o ciclo foi observado o ponto de orvalho da atmosfera Coleta dos gases Os gases foram coletados através da sonda do aparelho que foi colocada na tubulação dos gases de saída, sendo que o local de coleta se situava em um corredor subterrâneo embaixo da base dos fornos, conforme pode ser visto na Figura 5. Figura 5 Fotografia do medidor de gases instalado para coleta Com o objetivo de se avaliar as diferentes interações entre carga e atmosfera do forno, primeiramente foram realizadas coletas da atmosfera onde foi utilizada carga de fios-máquina com carepa, sendo posteriormente coletados os dados em um forno vazio, e por último, em um forno com carga de fios-máquina sem carepa Análise metalográfica Para a execução da análise metalográfica foram cortadas amostras dos fios-máquina submetidos ao processo de 38
39 esferoidização. Estas amostras então foram embutidas com baquelite, lixadas nas lixas 100, 200, 400, 600 e 1000, sendo posteriormente polidas em panos de 4 e 1 µm com pastas de diamante. Após polidas, as amostras foram atacadas com Nital 2%, sendo levadas a um microscópio ótico para a identificação e obtenção de micrografias da microestrutura das amostras. 3.2 TRABALHO TEÓRICO Programa de simulação O programa utilizado para a realização das simulações dos possíveis gases que seriam formados através da interação da carga com a atmosfera do forno foi o ChemSage v. 4.1 [6]. O criador do programa foi o sueco Gunnar Erikson e o programa foi desenvolvido dentro da RWTH-Aachen (Alemanha). Entretanto, a versão comercial do programa foi feita pela GTT-Technologies. A lógica utilizada pelo programa é a de calcular o equilíbrio químico entre as fases por meio da técnica de minimização da energia livre de Gibbs. Os dados termodinâmicos necessários para a realização dos cálculos são provenientes de um consórcio de laboratórios de 7 países (SGTE) Simulações Sistema de equilíbrio Fe-O Esta simulação foi realizada para verificar as pressões parciais de oxigênio em um sistema Fe-O nas quais o ferro estaria na forma oxidada ou na forma reduzida. Foram feitas então duas simulações: 1 Sistema composto por Fe O 2 FeO 2 Sistema composto por Fe O 2 Fe 3 O 4 39
40 As temperaturas utilizadas nas simulações estavam entre 400 e 800 ºC utilizando um intervalo de 50 ºC. Após a obtenção dos dados fornecidos pelo programa, estes foram plotados em um gráfico Temperatura x Log p(o 2 ) Decomposição do vapor d água Devido a existência de quantidades traço de vapor d água mesmo nos nitrogênios mais purificados, foram realizadas simulações para verificar se estas quantidades são suficientes para oxidar o ferro. As simulações foram realizadas em um sistema Fe N 2 H 2 O, sendo utilizadas quantidades de H 2 O no nitrogênio de 5, 50 e 500 ppm. As temperaturas utilizadas nas simulações estavam entre 400 e 800 ºC utilizando um intervalo de 50 ºC. Após a obtenção dos dados fornecidos pelo programa, foram observadas as pressões parciais de oxigênio em equilíbrio, formadas pela decomposição do vapor d água. Estes dados foram plotados no gráfico Temperatura x Log p(o2) obtido anteriormente Interação aço/atmosfera do forno Para a realização das simulações da interação do aço com a atmosfera do forno, primeiramente foram realizados cálculos para a obtenção de dados que tornasse o sistema teórico adequado e coerente com sistema encontrado na prática. Para a adequação dos sistemas foram realizados os seguintes cálculos: 1) Determinação da área superficial total da carga dentro do forno. Para a determinação da área superficial total da carga dentro do forno foram consideradas a massa total de carga (M AÇO ) e a densidade do aço ( ). Isto foi necessário, pois não foi possível determinar a quantidade de fios-máquina por bobina inserida no 40
41 forno, nem o comprimento de cada um deles. Os cálculos realizados para a determinação da área superficial total estão descritos a seguir. M AÇO = kg (carga utilizada) = 7800 kg/m 3 = M AÇO / V AÇO V AÇO = M AÇO / V AÇO = (kg) / 7800 (kg/m 3 ) V AÇO = 2,564 m 3 Volume de um fio = r 2 h, onde h é o comprimento e r o raio do fio. Sabendo-se que o diâmetro do fio é de 0,0131m, o seu raio é de 0,00655m. Portanto: V AÇO = r 2 h h = V AÇO / r 2 h = 2,564 m 3 / (6,55 x 10-3 m) 2 h = 19024,06 m Área superficial de um fio = 2 r h: A T = 2 r h A T = 782,93 m 2 2) Determinação da relação volume de gás por área superficial de material. Para a determinação desta relação primeiramente foi calculado o volume da câmara interna do forno V F : V F = R 2 H, onde R é o raio e H a altura da câmara interna do forno. Sabendo se que R = 2,025 m e D = 5,9 m: V F = R 2 H 41
42 V F = (2,025 m) 2 (5,9 m) V F = 76,0066 m 3 Em seguida, para determinar o volume disponível de gás (V GÁS ) dentro da câmara do forno contendo a carga de kg de aço, foi determinado que: V GÁS = V F V AÇO V GÁS = 76,0066 m 3-2,564 m 3 V GÁS = 73,4426 m 3 A relação volume de gás por área superficial de material pode agora ser determinada por V GÁS / A T : V GÁS / A T = 73,4426 m 3 / 782,93 m 2 V GÁS / A T = 0,0938 m 3 /m 2 Entretanto, para uma melhor quantificação do número de móis de gás presentes na atmosfera, transformou-se o volume encontrado em normal metro cúbico (Nm 3 ). Sabe-se que para condições normais de temperatura e pressão (CNTP), isto é, para uma temperatura de 273 K (0ºC) e uma pressão de 1 atm, o volume de 1m 3 de gás possui 44,615 móis. Pela Lei de Charles temos que para uma pressão constante, o volume de uma determinada massa gasosa é diretamente proporcional a temperatura absoluta [7]. Portanto transformando para Nm 3 : 0,0938 m 3 /m K x = 0,025 Nm 3 /m 2 x K 3) Determinação da quantidade de vapor d água em equilíbrio na atmosfera. Para determinação da quantidade de vapor d água na 42
43 atmosfera foi utilizada uma fórmula que relaciona o ponto de orvalho com a porcentagem de água presente. A fórmula é [8]: %H 2 O = (e 14,7316 (5422,18/T+273,16) ) x 100 Onde T é o ponto de orvalho da atmosfera. O analisador de ponto de orvalho, no dia em que foi feita a coleta dos gases, indicava um ponto de orvalho de 20ºC. Aplicando a fórmula para T = -20ºC, temos: %H 2 O = 0,1248% = 1248 ppm 4) Determinação da quantidade de Fe-C inserida no sistema teórico. Para a determinação da quantidade de Fe-C inserida no sistema teórico foi considerado um cubo de 1m 3 de aço contendo 0,2% de carbono. Os cálculos realizados para a obtenção destas quantidades foram: = 7800 kg/m 3 = g/m 3 V CUBO = 1m 3 = M CUBO / V CUBO M CUBO = X V CUBO M CUBO = g Sendo a quantidade de carbono em gramas G C, e a quantidade de ferro em gramas G Fe, temos: G C = M CUBO x 0,002 G Fe = M CUBO x 0,998 G C = g G Fe = g 5) Determinação da quantidade de móis de nitrogênio inseridos no sistema teórico. Para a determinação da quantidade de móis de 43
44 nitrogênio inseridos no sistema, primeiramente se calculou quantos móis de gás por m 2 de área superficial estariam presentes no sistema. Assim: V GÁS / A T = 0,025 Nm 3 /m 2 n GÁS = (0,025 Nm 3 /m 2 ) X (44,615 móis/nm 3 ) n GÁS = 1, móis/m 2 Posteriormente, foi calculada a pressão parcial de nitrogênio na atmosfera. Se haviam 1248 ppm de vapor d água em equilíbrio na atmosfera ou 0,1248%, a pressão parcial do vapor d água é 0,1248/100 ou 0, atm. Portanto: p(n 2 ) = 1 p(h 2 O) p(n2) = 0, atm Assim, o número de móis de nitrogênio na atmosfera é: n N2 = 1, x p(n 2 ) n N2 = 1, móis 6) Inserção dos dados no programa. Para o início da simulação do sistema teórico, foram inseridos os dados das massas de ferro (Fe) e de carbono (C) em gramas, o número de móis de nitrogênio (n N2 ) e a pressão parcial do vapor d água em equilíbrio. A Figura 6 mostra os valores na tela de inserção dos dados do programa. 44
45 Figura 6 Imagem mostrando os valores inseridos no programa de simulação 45
46 4. RESULTADOS E DISCUSSÃO 4.1 TRABALHO PRÁTICO Coleta dos gases Os resultados obtidos durante a coleta dos gases na temperatura de trabalho (725ºC) estão mostrados nas Tabelas 4, 5 e 6. Os dados das Tabelas 4, 5 e 6 foram obtidos em fornos com fiosmáquina com carepa, em forno vazio, e, com fios-máquina sem carepa, respectivamente. Tabela 4 Resultados obtidos no forno com fios-máquina com carepa T (ºC) O2 CO NO NO2 SO2 HC 725 0, ,00 0,00 35 xxx 725 0, ,00 0,00 36 xxx 725 0, ,00 0,00 39 xxx 725 0, ,00 0,00 42 xxx 725 0, ,00 0,00 48 xxx 725 0, ,00 0,00 50 xxx 725 0, ,00 0,00 51 xxx 725 0, ,00 0,00 52 xxx Tabela 5 Resultados obtidos no forno vazio T (ºC) O2 CO NO NO2 SO2 HC 790 0, ,00 0,00 0,20 0, , ,00 0,00 0,40 0, , ,00 0,00 0,50 0, , ,00 0,00 0,90 0, , ,00 0,00 1,09 0,00 46
47 Tabela 6 Resultados obtidos no forno com fios-máquina sem carepa T (ºC) O2 CO NO NO2 SO2 HC 725 0, ,49 0,00 37,41 xxxx 725 0, ,32 0,00 39,80 xxxx 725 0, ,64 0,00 137,40 xxxx 725 6, ,51 0,00 139,79 1, , ,99 0,00 147,65 1, , ,00 0,00 212,91 xxxx 725 0, ,00 0,00 239,38 xxxx Os sinais xxxx presentes na coluna dos hidrocarbonetos (HC) indicam que a concentração de hidrocarbonetos na atmosfera excedeu a capacidade de leitura do equipamento. É importante ressaltar que esta capacidade está correlacionada com a quantidade de oxigênio presente, isto é, para um determinado teor de oxigênio na atmosfera, existe um teor máximo de hidrocarbonetos que o equipamento consegue medir. Observa-se que a atmosfera apresenta teores significantes de monóxido de carbono para os fornos que foram monitorados contendo carga de material. Estes teores não estão condizentes com os encontrados em uma atmosfera em base de nitrogênio comercial Análise metalográfica A microestrutura das amostras analisadas pode ser observada nas Figuras 6 e 7, que estão apresentadas a seguir. 47
48 Figura 6 Micrografia obtida na região de núcleo do aço. Observa-se uma microestrutura típica de um aço baixo carbono esferoidizado. Figura 7- Micrografia obtida na região superficial do aço. Observa-se uma descarbonetação nesta região. A micrografia obtida na região de núcleo da amostra analisada apresenta uma microestrutura típica de um aço baixo carbono esferoidizado, com cementita esferoidizada em uma matriz ferrítica. Entretanto, na região superficial é notada uma certa descarbonetação do aço. 48
49 Analisando os resultados apresentados nas Tabelas 4, 5 e 6, observa-se que a atmosfera presente dentro da câmara do forno não está correspondente a uma atmosfera em base de nitrogênio comercial, haja visto o teor do gás de monóxido de carbono (CO) encontrado. A hipótese inicial de que o monóxido de carbono seria formado devido à degradação das graxas utilizadas para lubrificação de componentes internos do forno foi descartada com a verificação dos resultados obtidos na coleta da atmosfera realizada com o forno vazio. Portanto, pôde ser considerado que o carbono presente no monóxido de carbono foi proveniente do aço. Este fato está mostrado na Figura 7, onde pode se observar uma descarbonetação na região superficial da amostra analisada, entretanto a profundidade da camada não pôde ser medida pois não está bem resolvida. Segundo a literatura, os óxidos presentes na superfície do aço (carepa) poderiam reagir com o carbono presente na superfície do aço e formar monóxido de carbono. Entretanto, foi verificado que o aço que estava com carepa formou uma quantidade de monóxido de carbono menor que o aço sem carepa. Assim, foi considerado que na atmosfera do forno estavam presentes elementos oxidantes ao aço, como o vapor d água, e a carepa presente no aço serviu como um filme protetor, evitando o contato do hidrogênio e do oxigênio, provenientes da dissociação da água, com a superfície do aço. 4.2 TRABALHO TEÓRICO Sistemas de equilíbrio Fe-O e decomposição do vapor d água A Figura 8 apresenta as curvas resultantes dos processos de simulação dos sistemas de equilíbrio Fe-O e da decomposição do vapor d água em um gráfico Temperatura x Log p(o 2 ). 49
50 Fe T [ C] Óxidos ,00-30,00-25,00-20,00-15,00-10,00-5,00 0,00 Log(pO2) [Log(atm)] Figura 8 Gráfico Temperatura x Log p(o 2 ) O gráfico Temperatura x Log p(o 2 ) da Figura 8 mostra que as três curvas assimétricas paralelas, que representam uma atmosfera de nitrogênio contendo, da esquerda para direita, 5, 50 e 500 ppm de água, estão na região de oxidação do ferro. Portanto, nas temperaturas utilizadas para esferoidização, o ferro, termodinamicamente, tenderia a se oxidar mesmo com quantidades mínimas de vapor d água na atmosfera Interação aço/atmosfera do forno Os resultados obtidos na simulação do sistema teórico N2 H2O Fe C estão apresentados na Figura 9. 50
51 T = C P = E+00 atm V = E-02 m3 STREAM CONSTITUENTS Fe C N2/GAS/ H2O/GAS/ AMOUNT/mol E E E E-02 EQUIL AMOUNT MOLE FRACTION FUGACITY PHASE: GAS mol atm N E E E-01 H E E E-02 CO E E E-02 CO E E E-03 H2O E E E-03 CH E E E-04 O E E E-23 TOTAL: E E E+00 Figura 9 Resultados obtidos na simulação do sistema teórico Os resultados apresentados na Figura 9 mostram que a quantidade de monóxido de carbono formada até o equilíbrio termodinâmico está bem próxima dos valores obtidos no sistema real. Uma fração molar de 0,05751 é igual a 5,751% ou ppm. A diferença encontrada entre os valores do sistema real e do sistema teórico pode estar associada à ação de alguns efeitos cinéticos e também a situação de adição, quando foi necessária, de nitrogênio para dentro do forno para manter a pressão levemente positiva. Através dos resultados apresentados na simulação também se estimou a profundidade de camada descarbonetada provocada pela ação da atmosfera. Para isso, primeiramente, foram somadas as quantidades de móis do monóxido de carbono (CO), do dióxido de carbono (CO 2 ) e do metano (CH 4 ). Posteriormente, para sabermos a quantidade de carbono presente nos gases, esta soma foi multiplicada por 12, pois 1 mol de carbono pesa 12 gramas. Assim: G C = (0, , , ) mol X 12 g/mol G C = 0,8415 g 51
52 Para determinar a camada descarbonetada, calculou-se a quantidade de carbono que um aço com 0,2 %carbono possuiria em um volume com 1 m 2 de área superficial e 1 m de profundidade: 1 m m 2 x 1 m x = 10-6 m 3 x m 2 x 10-6 m Como 1 m 3 de aço possui g de carbono, 10-6 m 3 possui 0,0156 g. Assim, a profundidade de camada descarbonetada P D é: P D = (0,8415 g) / (0,0156 g/ m) P D = 53,9 m É importante ressaltar que a camada descarbonetada obtida foi considerando uma descarbonetação total. Os valores encontrados normalmente na empresa não foram liberados. 52
53 5. CONCLUSÕES A partir dos resultados experimentais obtidos neste trabalho, conclui-se que: A descarbonetação do aço submetido ao processo de esferoidização foi conseqüência da presença de uma alta concentração de vapor d água no interior da câmara do forno. Esta concentração não foi derivada do nitrogênio, mas pode ter entrado adsorvida na superfície da carga metálica ou por problemas na tubulação de entrada de nitrogênio; É possível, através de cálculos, a utilização da termodinâmica computacional como auxílio na simulação das interações aço/atmosfera existentes nos fornos para tratamento térmico; As atmosferas em base de nitrogênio comercial protetivas, mesmo sendo as mais puras na sua função, ainda podem promover uma descarbonetação do aço. Este efeito descarbonetante pode ser diminuído através de um controle do ponto de orvalho da atmosfera, evitando-se ao máximo a infiltração de vapor d água para dentro do forno. 53
54 6. SUGESTÕES PARA OUTROS TRABALHOS Realização de trabalhos práticos e simulações para diferentes pontos de orvalho de uma atmosfera em base de nitrogênio comercial para avaliação do efeito do vapor d água na descarbonetação dos aços; 54
55 7. BIBLIOGRAFIAS 1 Johnson, P. Furnace Atmospheres, ASM Handbook, vol.4, 1991, p Disponível em: < Acesso em: 2 de setembro Disponível em: < Acesso em: 28 de agosto Disponível em: < Acesso em: 30 de agosto Bramfitt, B. L. Annealing of Steel, ASM Handbook, vol.4, 1991 p.48 6 ERIKSSON, G.; HACK, K.: ChemSage a computer program for the calculation of complex chemical equilibria, Met. Transactions B, vol.21b, 1990, p Disponível em: < Acessado em: 2 de setembro Stickels, C. A. Gas Carburizing, ASM Handbook, vol.4, 1991, p
Ar de combustão. Água condensada. Balanço da energia. Câmara de mistura. Convecção. Combustível. Curva de aquecimento
 Ar de combustão O ar de combustão contém 21% de oxigênio, que é necessário para qualquer combustão. Além disso, 78% de nitrogênio está incorporado no ar. São requeridos aproximadamente 10 metros cúbicos
Ar de combustão O ar de combustão contém 21% de oxigênio, que é necessário para qualquer combustão. Além disso, 78% de nitrogênio está incorporado no ar. São requeridos aproximadamente 10 metros cúbicos
UNIVERSIDADE FEDERAL DO PARANÁ SETOR DE TECNOLOGIA DEPARTAMENTO DE ENGENHARIA MECÂNICA TM-364 MÁQUINAS TÉRMICAS I. Máquinas Térmicas I
 Eu tenho três filhos e nenhum dinheiro... Porque eu não posso ter nenhum filho e três dinheiros? - Homer J. Simpson UNIVERSIDADE FEDERAL DO PARANÁ SETOR DE TECNOLOGIA DEPARTAMENTO DE ENGENHARIA MECÂNICA
Eu tenho três filhos e nenhum dinheiro... Porque eu não posso ter nenhum filho e três dinheiros? - Homer J. Simpson UNIVERSIDADE FEDERAL DO PARANÁ SETOR DE TECNOLOGIA DEPARTAMENTO DE ENGENHARIA MECÂNICA
OXICORTE SENAI CETEMP OUTROS PROCESSOS TOBIAS ROBERTO MUGGE
 OXICORTE SENAI CETEMP OUTROS PROCESSOS TOBIAS ROBERTO MUGGE TIPOS DE CORTE MECÂNICO: Cisalhamento ou remoção de cavacos (guilhotinas e tesouras, serra) FUSÃO: Fusão do material pela transferência de calor
OXICORTE SENAI CETEMP OUTROS PROCESSOS TOBIAS ROBERTO MUGGE TIPOS DE CORTE MECÂNICO: Cisalhamento ou remoção de cavacos (guilhotinas e tesouras, serra) FUSÃO: Fusão do material pela transferência de calor
EQUILÍBRIO QUÍMICO: é o estado de um sistema reacional no qual não ocorrem variações na composição do mesmo ao longo do tempo.
 IV INTRODUÇÃO AO EQUILÍBRIO QUÍMICO IV.1 Definição EQUILÍBRIO QUÍMICO: é o estado de um sistema reacional no qual não ocorrem variações na composição do mesmo ao longo do tempo. Equilíbrio químico equilíbrio
IV INTRODUÇÃO AO EQUILÍBRIO QUÍMICO IV.1 Definição EQUILÍBRIO QUÍMICO: é o estado de um sistema reacional no qual não ocorrem variações na composição do mesmo ao longo do tempo. Equilíbrio químico equilíbrio
LISTA DE EXERCÍCIOS Trabalho, Calor e Primeira Lei da Termodinâmica para Sistemas
 - 1 - LISTA DE EXERCÍCIOS Trabalho, Calor e Primeira Lei da Termodinâmica para Sistemas 1. Um aquecedor de ambientes a vapor, localizado em um quarto, é alimentado com vapor saturado de água a 115 kpa.
- 1 - LISTA DE EXERCÍCIOS Trabalho, Calor e Primeira Lei da Termodinâmica para Sistemas 1. Um aquecedor de ambientes a vapor, localizado em um quarto, é alimentado com vapor saturado de água a 115 kpa.
www.professormazzei.com Estequiometria Folha 03 Prof.: João Roberto Mazzei
 01. (CFTCE 2007) Dada a reação de neutralização: HCl + NaOH NaCl + H 2O, a massa de NaCl, produzida a partir de 80 g de hidróxido de sódio (NaOH), é: a) 58,5 g b) 40 g c) 117 g d) 80 g e) 120 g 02. (CFTCE
01. (CFTCE 2007) Dada a reação de neutralização: HCl + NaOH NaCl + H 2O, a massa de NaCl, produzida a partir de 80 g de hidróxido de sódio (NaOH), é: a) 58,5 g b) 40 g c) 117 g d) 80 g e) 120 g 02. (CFTCE
É o cálculo das quantidades de reagentes e/ou produtos das reações químicas.
 Estequiometria Introdução Estequiometria É derivada da palavra grega STOICHEON (elemento) e METRON (medida) significa medida dos elementos químicos", ou ainda medir algo que não pode ser dividido. É o
Estequiometria Introdução Estequiometria É derivada da palavra grega STOICHEON (elemento) e METRON (medida) significa medida dos elementos químicos", ou ainda medir algo que não pode ser dividido. É o
A forma geral de uma equação de estado é: p = f ( T,
 Aula: 01 Temática: O Gás Ideal Em nossa primeira aula, estudaremos o estado mais simples da matéria, o gás, que é capaz de encher qualquer recipiente que o contenha. Iniciaremos por uma descrição idealizada
Aula: 01 Temática: O Gás Ideal Em nossa primeira aula, estudaremos o estado mais simples da matéria, o gás, que é capaz de encher qualquer recipiente que o contenha. Iniciaremos por uma descrição idealizada
Concurso de Seleção 2004 NÚMERO DE INSCRIÇÃO - QUÍMICA
 QUÍMICA QUESTÃO 21 Muitas pessoas já ouviram falar de gás hilariante. Mas será que ele é realmente capaz de provocar o riso? Na verdade, essa substância, o óxido nitroso (N 2 O), descoberta há quase 230
QUÍMICA QUESTÃO 21 Muitas pessoas já ouviram falar de gás hilariante. Mas será que ele é realmente capaz de provocar o riso? Na verdade, essa substância, o óxido nitroso (N 2 O), descoberta há quase 230
FÍSICO-QUÍMICA TERMOQUÍMICA Aula 1
 FÍSICO-QUÍMICA TERMOQUÍMICA Aula 1 A termoquímica é parte da termodinâmica e corresponde ao segmento da química que compreende as trocas de calor e seus efeitos nas substâncias e reações químicas. Os primeiros
FÍSICO-QUÍMICA TERMOQUÍMICA Aula 1 A termoquímica é parte da termodinâmica e corresponde ao segmento da química que compreende as trocas de calor e seus efeitos nas substâncias e reações químicas. Os primeiros
Lista de Exercícios Estequiometria
 Lista de Exercícios Estequiometria Átomos e Mols de Átomos Fonte: Química Geral, Vol. 1 John B. Russel 1. Calcule a massa atômica do elemento X, dado que 2,02 x l0 6 átomos de X têm uma massa de 1,70 x
Lista de Exercícios Estequiometria Átomos e Mols de Átomos Fonte: Química Geral, Vol. 1 John B. Russel 1. Calcule a massa atômica do elemento X, dado que 2,02 x l0 6 átomos de X têm uma massa de 1,70 x
P1 - PROVA DE QUÍMICA GERAL 03/09/07
 1 - ROVA DE QUÍMICA GERAL 03/09/07 Nome: Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados R = 0,0821 atm L mol -1 K -1 T (K) = T ( C) + 273,15
1 - ROVA DE QUÍMICA GERAL 03/09/07 Nome: Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados R = 0,0821 atm L mol -1 K -1 T (K) = T ( C) + 273,15
Recozimento recuperação) Tratamento Térmico (Amolecimento, Normalização (Resfriamento ao ar) Tempera (Endurecimento) homogeneização, Revenido (alívio
 É o conjunto de operações de aquecimento e resfriamento que são submetidos os aços sob condições controladas de temperatura, tempo, atmosfera e velocidade de esfriamento. Objetivos dos tratamentos térmicos.
É o conjunto de operações de aquecimento e resfriamento que são submetidos os aços sob condições controladas de temperatura, tempo, atmosfera e velocidade de esfriamento. Objetivos dos tratamentos térmicos.
SUBSTÂNCIAS, MISTURAS E SEPARAÇÃO DE MISTURAS
 NOTAS DE AULA (QUÍMICA) SUBSTÂNCIAS, MISTURAS E SEPARAÇÃO DE MISTURAS PROFESSOR: ITALLO CEZAR 1 INTRODUÇÃO A química é a ciência da matéria e suas transformações, isto é, estuda a matéria. O conceito da
NOTAS DE AULA (QUÍMICA) SUBSTÂNCIAS, MISTURAS E SEPARAÇÃO DE MISTURAS PROFESSOR: ITALLO CEZAR 1 INTRODUÇÃO A química é a ciência da matéria e suas transformações, isto é, estuda a matéria. O conceito da
ferro bromo brometo de ferro 40g 120g 0g 12g 0g 148g 7g 40g 0g 0g x g 37g
 01) (FCMSC-SP) A frase: Do nada, nada; em nada, nada pode transformar-se relaciona-se com as idéias de: a) Dalton. b) Proust. c) Boyle. d) Lavoisier. e) Gay-Lussac. 02) Acerca de uma reação química, considere
01) (FCMSC-SP) A frase: Do nada, nada; em nada, nada pode transformar-se relaciona-se com as idéias de: a) Dalton. b) Proust. c) Boyle. d) Lavoisier. e) Gay-Lussac. 02) Acerca de uma reação química, considere
EXPERIMENTAÇÃO NO ENSINO DE QUÍMICA COM TRANSFERÊNCIA DE ELÉTRONS
 EXPERIMENTAÇÃO NO ENSINO DE QUÍMICA COM TRANSFERÊNCIA DE ELÉTRONS José Celson Braga Fernandes¹ - [email protected] Emanuele Montenegro Sales² Flaviana Vieira da Costa³ Apoliana Braga Fernandes 4
EXPERIMENTAÇÃO NO ENSINO DE QUÍMICA COM TRANSFERÊNCIA DE ELÉTRONS José Celson Braga Fernandes¹ - [email protected] Emanuele Montenegro Sales² Flaviana Vieira da Costa³ Apoliana Braga Fernandes 4
Cálculo Químico ESTEQUIOMETRIA
 Cálculo Químico ESTEQUIOMETRIA Profº André Montillo www.montillo.com.br Definição: É o estudo da quantidade de reagentes e produtos em uma reação química, portanto é uma análise quantitativa de um fenômeno
Cálculo Químico ESTEQUIOMETRIA Profº André Montillo www.montillo.com.br Definição: É o estudo da quantidade de reagentes e produtos em uma reação química, portanto é uma análise quantitativa de um fenômeno
UFJF CONCURSO VESTIBULAR 2012 GABARITO DA PROVA DE QUÍMICA
 Questão 1 O ácido carbônico é formado quando se borbulha o dióxido de carbono em água. Ele está presente em águas gaseificadas e refrigerantes. Em solução aquosa, ele pode sofrer duas dissociações conforme
Questão 1 O ácido carbônico é formado quando se borbulha o dióxido de carbono em água. Ele está presente em águas gaseificadas e refrigerantes. Em solução aquosa, ele pode sofrer duas dissociações conforme
ATIVIDADE DE ÁGUA (Aw) E REAÇÕES DE DETERIORAÇÃO
 ATIVIDADE DE ÁGUA (Aw) E REAÇÕES DE DETERIORAÇÃO Água A molécula de água é triatômica e possui estrutura tetraédrica. Tem baixo peso molecular, pequeno volume e é diamagnética. Apresentaria um ângulo de
ATIVIDADE DE ÁGUA (Aw) E REAÇÕES DE DETERIORAÇÃO Água A molécula de água é triatômica e possui estrutura tetraédrica. Tem baixo peso molecular, pequeno volume e é diamagnética. Apresentaria um ângulo de
Capítulo 10. 2005 by Pearson Education
 QUÍMICA A Ciência Central 9ª Edição Gases David P. White Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão,
QUÍMICA A Ciência Central 9ª Edição Gases David P. White Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão,
MÁQUINAS HIDRÁULICAS AULA 15 TURBINAS A VAPOR PROF.: KAIO DUTRA
 MÁQUINAS HIDRÁULICAS AULA 15 TURBINAS A VAPOR PROF.: KAIO DUTRA Usinas Termoelétricas As turbinas a vapor são máquinas que utilizam a elevada energia cinética da massa de vapor expandido em trabalho de
MÁQUINAS HIDRÁULICAS AULA 15 TURBINAS A VAPOR PROF.: KAIO DUTRA Usinas Termoelétricas As turbinas a vapor são máquinas que utilizam a elevada energia cinética da massa de vapor expandido em trabalho de
Lista de Exercícios Química Geral Entropia e energia livre
 Lista de Exercícios Química Geral Entropia e energia livre 1. Se a reação A + B C tiver uma constante de equilíbrio maior do que 1, qual das seguintes indicações está correta? a) A reação não é espontânea.
Lista de Exercícios Química Geral Entropia e energia livre 1. Se a reação A + B C tiver uma constante de equilíbrio maior do que 1, qual das seguintes indicações está correta? a) A reação não é espontânea.
Átomos & Moléculas. Definição: é uma porção de matéria que tem propriedades bem definidas e que lhe são característica.
 Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Definição: é uma porção de matéria que tem propriedades bem definidas e que lhe são característica. SUBSTÂNCIA (Material Puro): material formado
Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Definição: é uma porção de matéria que tem propriedades bem definidas e que lhe são característica. SUBSTÂNCIA (Material Puro): material formado
Tecnologia em Automação Industrial Mecânica dos Fluidos Lista 03 página 1/5
 Curso de Tecnologia em utomação Industrial Disciplina de Mecânica dos Fluidos prof. Lin Lista de exercícios nº 3 (Estática/manometria) 1. Determine a pressão exercida sobre um mergulhador a 30 m abaixo
Curso de Tecnologia em utomação Industrial Disciplina de Mecânica dos Fluidos prof. Lin Lista de exercícios nº 3 (Estática/manometria) 1. Determine a pressão exercida sobre um mergulhador a 30 m abaixo
Aula 16 A Regra das Fases
 Aula 16 A Regra das Fases 1. Introdução Poderíamos especular se quatro fases de uma única substância poderiam estar em equilíbrio (como, por exemplo, as duas formas sólidas do estanho, o estanho líquido
Aula 16 A Regra das Fases 1. Introdução Poderíamos especular se quatro fases de uma única substância poderiam estar em equilíbrio (como, por exemplo, as duas formas sólidas do estanho, o estanho líquido
P4 - PROVA DE QUÍMICA GERAL - 29/06/06
 P4 - PROVA DE QUÍMICA GERAL - 9/06/06 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 a,5 4 a,5 Total 10,0 Constantes e equações: R 0,08 atm L -1 K -1 8,14 J -1
P4 - PROVA DE QUÍMICA GERAL - 9/06/06 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 a,5 4 a,5 Total 10,0 Constantes e equações: R 0,08 atm L -1 K -1 8,14 J -1
b) Qual é a confusão cometida pelo estudante em sua reflexão?
 1º B EM Química A Lailson Aval. Trimestral 28/03/11 1. Qual o estado físico (sólido, líquido ou gasoso) das substâncias da tabela a seguir, quando as mesmas se encontram no Deserto da Arábia, à temperatura
1º B EM Química A Lailson Aval. Trimestral 28/03/11 1. Qual o estado físico (sólido, líquido ou gasoso) das substâncias da tabela a seguir, quando as mesmas se encontram no Deserto da Arábia, à temperatura
Resolução da Prova de Química Vestibular Inverno UPF 2003 Prof. Emiliano Chemello
 Resolução da Prova de Química Vestibular Inverno UPF 2003 Professor Emiliano Chemello www.quimica.net/emiliano [email protected] Questões Resoluções Os óxidos básicos (Oxigênio ligado a um metal de
Resolução da Prova de Química Vestibular Inverno UPF 2003 Professor Emiliano Chemello www.quimica.net/emiliano [email protected] Questões Resoluções Os óxidos básicos (Oxigênio ligado a um metal de
Calor Específico. 1. Introdução
 Calor Específico 1. Introdução Nesta experiência, serão estudados os efeitos do calor sobre os corpos, e a relação entre quantidade de calor, variação da temperatura e calor específico. Vamos supor que
Calor Específico 1. Introdução Nesta experiência, serão estudados os efeitos do calor sobre os corpos, e a relação entre quantidade de calor, variação da temperatura e calor específico. Vamos supor que
As Bolhas Fatais do Mergulho
 Walter Ruggeri Waldman Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
Walter Ruggeri Waldman Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
Aula 6: Lista de Exercícios. Laminação Extrusão e Trefilação Forjamento e Estampagem Fundição
 Aula 6: Lista de Exercícios Materiais Laminação Extrusão e Trefilação Forjamento e Estampagem Fundição Podemos definir como aço: a) LigadeFeeCcomteorentre0,1e6%deC. b) LigadeFeeMgcomteorentre0,1e6%deMg.
Aula 6: Lista de Exercícios Materiais Laminação Extrusão e Trefilação Forjamento e Estampagem Fundição Podemos definir como aço: a) LigadeFeeCcomteorentre0,1e6%deC. b) LigadeFeeMgcomteorentre0,1e6%deMg.
MASSA ATÔMICA, MOLECULAR, MOLAR, NÚMERO DE AVOGADRO E VOLUME MOLAR.
 MASSA ATÔMICA, MOLECULAR, MOLAR, NÚMERO DE AVOGADRO E VOLUME MOLAR. UNIDADE DE MASSA ATÔMICA Em 1961, na Conferência da União Internacional de Química Pura e Aplicada estabeleceu-se: DEFINIÇÃO DE MASSA
MASSA ATÔMICA, MOLECULAR, MOLAR, NÚMERO DE AVOGADRO E VOLUME MOLAR. UNIDADE DE MASSA ATÔMICA Em 1961, na Conferência da União Internacional de Química Pura e Aplicada estabeleceu-se: DEFINIÇÃO DE MASSA
1
 Níveis de dificuldade das Questões Fácil Pontifícia Universidade Católica do Rio Grande do Sul Médio Difícil Resolução da Prova de Química Vestibular Verão PUCRS 2005 Prof. Emiliano Chemello www.quimica.net/emiliano
Níveis de dificuldade das Questões Fácil Pontifícia Universidade Católica do Rio Grande do Sul Médio Difícil Resolução da Prova de Química Vestibular Verão PUCRS 2005 Prof. Emiliano Chemello www.quimica.net/emiliano
DIAGRAMA DE FASES Clique para editar o estilo do título mestre
 Introdução São diagramas que mostram regiões de estabilidade das fases, através de gráficos que representam as relações entre temperatura, pressão e composição química. Para que serve: Investigar reações
Introdução São diagramas que mostram regiões de estabilidade das fases, através de gráficos que representam as relações entre temperatura, pressão e composição química. Para que serve: Investigar reações
ROTEIRO DE ORIENTAÇÃO DE ESTUDOS Ensino Médio
 ROTEIRO DE ORIENTAÇÃO DE ESTUDOS Ensino Médio Professora: Renata Disciplina: Física Série: 1ª Aluno(a): Turma: 1ª Nº.: Caro(a) aluno(a), Os objetivos listados para esta atividade de recuperação são parte
ROTEIRO DE ORIENTAÇÃO DE ESTUDOS Ensino Médio Professora: Renata Disciplina: Física Série: 1ª Aluno(a): Turma: 1ª Nº.: Caro(a) aluno(a), Os objetivos listados para esta atividade de recuperação são parte
Universidade Federal do Acre Coordenação de Ciências Agrárias PET-Agronomia
 Universidade Federal do Acre Coordenação de Ciências Agrárias PET-Agronomia Renato Bolsistas: Renato Renato(7ºPeríodo-Florestal) Tutor: Prof. Dr. José Ribamar Rio Branco, Acre 2006 1 As leis ponderais
Universidade Federal do Acre Coordenação de Ciências Agrárias PET-Agronomia Renato Bolsistas: Renato Renato(7ºPeríodo-Florestal) Tutor: Prof. Dr. José Ribamar Rio Branco, Acre 2006 1 As leis ponderais
EXTRUSÃO E TREFILAÇÃO
 EXTRUSÃO E TREFILAÇÃO 1 Se a necessidade é de perfis de formatos complicados ou, então, de tubos, o processo de fabricação será a extrusão. Se o que se quer fabricar, são rolos de arame, cabos ou fios
EXTRUSÃO E TREFILAÇÃO 1 Se a necessidade é de perfis de formatos complicados ou, então, de tubos, o processo de fabricação será a extrusão. Se o que se quer fabricar, são rolos de arame, cabos ou fios
ESTRUTURA E PROPRIEDADES DOS MATERIAIS DIFUSÃO ATÔMICA
 ESTRUTURA E PROPRIEDADES DOS MATERIAIS DIFUSÃO ATÔMICA Prof. Rubens Caram 1 DIFUSÃO ATÔMICA DIFUSÃO ATÔMICA É O MOVIMENTO DE MATÉRIA ATRAVÉS DA MATÉRIA EM GASES, LÍQUIDOS E SÓLIDOS, OS ÁTOMOS ESTÃO EM
ESTRUTURA E PROPRIEDADES DOS MATERIAIS DIFUSÃO ATÔMICA Prof. Rubens Caram 1 DIFUSÃO ATÔMICA DIFUSÃO ATÔMICA É O MOVIMENTO DE MATÉRIA ATRAVÉS DA MATÉRIA EM GASES, LÍQUIDOS E SÓLIDOS, OS ÁTOMOS ESTÃO EM
Características dos gases
 Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão, seu volume diminui. Os gases sempre formam misturas homogêneas
Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão, seu volume diminui. Os gases sempre formam misturas homogêneas
CAPÍTULO 3 TRATAMENTOS TÉRMICOS EM LIGAS DE ALUMÍNIO. Os tratamentos térmicos têm como finalidade causar modificações nas
 CAPÍTULO 3 TRATAMENTOS TÉRMICOS EM LIGAS DE ALUMÍNIO Os tratamentos térmicos têm como finalidade causar modificações nas propriedades dos materiais pela alteração do tipo e proporção das fases presentes,
CAPÍTULO 3 TRATAMENTOS TÉRMICOS EM LIGAS DE ALUMÍNIO Os tratamentos térmicos têm como finalidade causar modificações nas propriedades dos materiais pela alteração do tipo e proporção das fases presentes,
O que é Cinética Química?
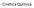 Cinética Química O que é Cinética Química? Ramo da físico-química que estuda a velocidade das reações; Velocidade na química: variação de uma grandeza no tempo: x v t Velocidade Considere a reação aa bb
Cinética Química O que é Cinética Química? Ramo da físico-química que estuda a velocidade das reações; Velocidade na química: variação de uma grandeza no tempo: x v t Velocidade Considere a reação aa bb
SIMULAÇÃO DE UMA COLUNA DE ABSORÇÃO DE PRATOS COMO EQUIPAMENTO DE CONTROLE DA POLUIÇÃO DO AR EM UM INCINERADOR DE RESÍDUOS PERIGOSOS
 SIMULAÇÃO DE UMA COLUNA DE ABSORÇÃO DE PRATOS COMO EQUIPAMENTO DE CONTROLE DA POLUIÇÃO DO AR EM UM INCINERADOR DE RESÍDUOS PERIGOSOS Carlos Alberto Ferreira Rino (1) Engenheiro Químico (UNICAMP, 1989);
SIMULAÇÃO DE UMA COLUNA DE ABSORÇÃO DE PRATOS COMO EQUIPAMENTO DE CONTROLE DA POLUIÇÃO DO AR EM UM INCINERADOR DE RESÍDUOS PERIGOSOS Carlos Alberto Ferreira Rino (1) Engenheiro Químico (UNICAMP, 1989);
Introdução à Eletroquímica. 1. Gentil V. Corrosão. 3 edição. 2. Cotton F. A. e Wilkinson G. Basic Inorganic Chemistry, John Wiley & Son, USA, 1976.
 Introdução à Eletroquímica 1. Gentil V. Corrosão. 3 edição. 2. Cotton F. A. e Wilkinson G. Basic Inorganic Chemistry, John Wiley & Son, USA, 1976. INTRODUÇÃO Eletroquímica: estuda as relações entre efeitos
Introdução à Eletroquímica 1. Gentil V. Corrosão. 3 edição. 2. Cotton F. A. e Wilkinson G. Basic Inorganic Chemistry, John Wiley & Son, USA, 1976. INTRODUÇÃO Eletroquímica: estuda as relações entre efeitos
Unidade 2 Substâncias e átomos
 Unidade 2 Substâncias e átomos Substâncias Puras pág. 51 A matéria é composta por uma ou mais substâncias químicas. Porém, é difícil saber se um corpo é composto por uma única substância ou por uma mistura
Unidade 2 Substâncias e átomos Substâncias Puras pág. 51 A matéria é composta por uma ou mais substâncias químicas. Porém, é difícil saber se um corpo é composto por uma única substância ou por uma mistura
Introdução à Volumetria. Profa. Lilian Lúcia Rocha e Silva
 Introdução à Volumetria Profa. Lilian Lúcia Rocha e Silva INTRODUÇÃO À VOLUMETRIA TITULAÇÃO Processo no qual uma solução padrão ou solução de referência é adicionada a uma solução que contém um soluto
Introdução à Volumetria Profa. Lilian Lúcia Rocha e Silva INTRODUÇÃO À VOLUMETRIA TITULAÇÃO Processo no qual uma solução padrão ou solução de referência é adicionada a uma solução que contém um soluto
COMPORTAMENTO DOS GASES - EXERCÍCIOS DE FIXAÇÃO E TESTES DE VESTIBULARES
 www.agraçadaquímica.com.br COMPORTAMENTO DOS GASES - EXERCÍCIOS DE FIXAÇÃO E TESTES DE VESTIBULARES 1. (UNIPAC-96) Um mol de gás Ideal, sob pressão de 2 atm, e temperatura de 27ºC, é aquecido até que a
www.agraçadaquímica.com.br COMPORTAMENTO DOS GASES - EXERCÍCIOS DE FIXAÇÃO E TESTES DE VESTIBULARES 1. (UNIPAC-96) Um mol de gás Ideal, sob pressão de 2 atm, e temperatura de 27ºC, é aquecido até que a
TERMOQUÍMICA EXERCÍCIOS ESSENCIAIS 1. O CALOR E OS PROCESSOS QUÍMICOS
 TERMOQUÍMICA EXERCÍCIOS ESSENCIAIS 1. O CALOR E OS PROCESSOS QUÍMICOS Termoquímica: Estudo das quantidades de energia, na forma de calor, liberada ou absorvida durante os processos de interesse da Química,
TERMOQUÍMICA EXERCÍCIOS ESSENCIAIS 1. O CALOR E OS PROCESSOS QUÍMICOS Termoquímica: Estudo das quantidades de energia, na forma de calor, liberada ou absorvida durante os processos de interesse da Química,
P1 - PROVA DE QUÍMICA GERAL 17/04/10
 P1 - PROVA DE QUÍMICA GERAL 17/04/10 Nome: GABARITO Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Dados R 0,081 atm L mol -1 K -1 T (K) T ( C) + 73,15
P1 - PROVA DE QUÍMICA GERAL 17/04/10 Nome: GABARITO Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Dados R 0,081 atm L mol -1 K -1 T (K) T ( C) + 73,15
Principais elementos de liga. Cr Ni V Mo W Co B Cu Mn, Si, P e S (residuais)
 Aços Ligas Aços ligas A introdução de outros elementos de liga nos aços-carbono é feita quando se deseja um ou diversos dos seguintes efeitos: Aumentar a resistência mecânica e dureza. Conferir resistência
Aços Ligas Aços ligas A introdução de outros elementos de liga nos aços-carbono é feita quando se deseja um ou diversos dos seguintes efeitos: Aumentar a resistência mecânica e dureza. Conferir resistência
PILHAS - TEORIA. a) Oxidação: A oxidação envolve o aumento do número de oxidação (NOX) de um determinado elemento a partir da perda de elétrons.
 PILHAS TEORIA Introdução A Eletroquímica é o ramo da Química que estuda a relação existente entre a corrente elétrica e as reações. Ela pode ser dividida em dois tipos de processos: pilhas e eletrólise.
PILHAS TEORIA Introdução A Eletroquímica é o ramo da Química que estuda a relação existente entre a corrente elétrica e as reações. Ela pode ser dividida em dois tipos de processos: pilhas e eletrólise.
TECNOLOGIA HIDRÁULICA. Fagner Ferraz
 TECNOLOGIA HIDRÁULICA Fagner Ferraz Potência x Eficiência 2 Cavitação 3 Causas da cavitação Tecnologia Hidráulica Filtro da linha de sucção saturado Linha de sucção muito longa Muitas curvas na linha de
TECNOLOGIA HIDRÁULICA Fagner Ferraz Potência x Eficiência 2 Cavitação 3 Causas da cavitação Tecnologia Hidráulica Filtro da linha de sucção saturado Linha de sucção muito longa Muitas curvas na linha de
QUÍMICA REVISÃO 1 INTERATIVIDADE. Unidade IV. Reações químicas e cálculo estequiométrico.
 Unidade IV Reações químicas e cálculo estequiométrico. 2 Aula 16.1 Conteúdo: Revisão e avaliação da unidade IV. 3 O que é uma reação química? É uma transformação em que novas substâncias são formados a
Unidade IV Reações químicas e cálculo estequiométrico. 2 Aula 16.1 Conteúdo: Revisão e avaliação da unidade IV. 3 O que é uma reação química? É uma transformação em que novas substâncias são formados a
AVALIAÇÃO DA INTERFERÊNCIA DO FATOR DE COMPRESSIBILIDADE Z NO CÁLCULO DO FATOR DE COREÇÃO DE VOLUME DE GÁS NATURAL
 AVALIAÇÃO DA INTERFERÊNCIA DO FATOR DE COMPRESSIBILIDADE Z NO CÁLCULO DO FATOR DE COREÇÃO DE VOLUME DE GÁS NATURAL IOLANDO MENESES SANTOS Professor Especialista em Didática do Ensino Superior e em Automação
AVALIAÇÃO DA INTERFERÊNCIA DO FATOR DE COMPRESSIBILIDADE Z NO CÁLCULO DO FATOR DE COREÇÃO DE VOLUME DE GÁS NATURAL IOLANDO MENESES SANTOS Professor Especialista em Didática do Ensino Superior e em Automação
C o l é g i o R i c a r d o R o d r i g u e s A l v e s
 C o l é g i o R i c a r d o R o d r i g u e s A l v e s Educação Infantil - Ensino Fundamental I - Ensino Médio 1 TRIMESTRE Química 1ª Série do Ensino Médio Conteúdo Introdução a Química Átomo Molécula
C o l é g i o R i c a r d o R o d r i g u e s A l v e s Educação Infantil - Ensino Fundamental I - Ensino Médio 1 TRIMESTRE Química 1ª Série do Ensino Médio Conteúdo Introdução a Química Átomo Molécula
Substâncias Puras e Misturas
 MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES Substâncias Puras e Misturas Elementos Químicos
MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES Substâncias Puras e Misturas Elementos Químicos
Estrutura física e química da Terra
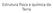 Estrutura física e química da Terra Os elementos químicos que estão globalmente presentes são os mesmos que constituem os minerais mais comuns. Existem atualmente cerca de 116 elementos químicos, incluindo
Estrutura física e química da Terra Os elementos químicos que estão globalmente presentes são os mesmos que constituem os minerais mais comuns. Existem atualmente cerca de 116 elementos químicos, incluindo
Segunda Lei da Termodinâmica
 Segunda Lei da Termodinâmica (Análise restrita a um ciclo) Da observação experimental, sabe-se que se um dado ciclo termodinâmico proposto não viola a primeira lei, não está assegurado que este ciclo possa
Segunda Lei da Termodinâmica (Análise restrita a um ciclo) Da observação experimental, sabe-se que se um dado ciclo termodinâmico proposto não viola a primeira lei, não está assegurado que este ciclo possa
INTRODUÇÃO À CINETICA E TERMODINÂMICA QUÍMICA
 INTRODUÇÃO À CINETICA E TERMODINÂMICA QUÍMICA Principios de Termodinâmica Termodinamica determina se um processo fisicoquímico é possível (i.e. espontaneo) Termodinamica não providencia informação sobre
INTRODUÇÃO À CINETICA E TERMODINÂMICA QUÍMICA Principios de Termodinâmica Termodinamica determina se um processo fisicoquímico é possível (i.e. espontaneo) Termodinamica não providencia informação sobre
Série: 2º ano. Assunto: Estequiometria
 Aluno: Série: 2º ano Assunto: Estequiometria 1) A massa de dióxido de carbono liberada na queima de 80 g de metano, quando utilizado como combustível, é: (Dados: massas molares, em g/mol: H = 1, C =12,
Aluno: Série: 2º ano Assunto: Estequiometria 1) A massa de dióxido de carbono liberada na queima de 80 g de metano, quando utilizado como combustível, é: (Dados: massas molares, em g/mol: H = 1, C =12,
CURSO APOIO QUÍMICA RESOLUÇÃO
 QUÍMICA CURSO APOIO 15. O sulfato de sódio é um composto utilizado na indústria de celulose e na fabricação de detergentes. Por apresentar grande afinidade por água, pode ser encontrado na forma de um
QUÍMICA CURSO APOIO 15. O sulfato de sódio é um composto utilizado na indústria de celulose e na fabricação de detergentes. Por apresentar grande afinidade por água, pode ser encontrado na forma de um
Exercícios Gases e Termodinâmica
 Exercícios Gases e Termodinâmica 1-O gás carbônico produzido na reação de um comprimido efervescente com água foi seco e recolhido àpressão de 1 atm e temperatura de 300K, ocupando um volume de 4 L. Se
Exercícios Gases e Termodinâmica 1-O gás carbônico produzido na reação de um comprimido efervescente com água foi seco e recolhido àpressão de 1 atm e temperatura de 300K, ocupando um volume de 4 L. Se
Centro Universitário Padre Anchieta Ciência dos Materiais AÇOS-LIGA
 AÇOS-LIGA 5.1 INTRODUÇÃO Todos os aços-liga são mais caros do que os aços carbonos, sendo seu preço em geral tanto mais caro quanto maior a porcentagem de elementos de liga no aço. Por essa razão, só se
AÇOS-LIGA 5.1 INTRODUÇÃO Todos os aços-liga são mais caros do que os aços carbonos, sendo seu preço em geral tanto mais caro quanto maior a porcentagem de elementos de liga no aço. Por essa razão, só se
DUTOS E CHAMINÉS DE FONTES ESTACIONÁRIAS DETERMINAÇÃO DA MASSA MOLECULAR SECA E DO EXCESSO DE AR DO FLUXO GASOSO Método de ensaio
 CETESB DUTOS E CHAMINÉS DE FONTES ESTACIONÁRIAS DETERMINAÇÃO DA MASSA MOLECULAR SECA E DO EXCESSO DE AR DO FLUXO GASOSO Método de ensaio L9.223 JUN/92 SUMÁRIO Pág. 1 Objetivo...1 2 Normas complementares...1
CETESB DUTOS E CHAMINÉS DE FONTES ESTACIONÁRIAS DETERMINAÇÃO DA MASSA MOLECULAR SECA E DO EXCESSO DE AR DO FLUXO GASOSO Método de ensaio L9.223 JUN/92 SUMÁRIO Pág. 1 Objetivo...1 2 Normas complementares...1
QUÍMICA PROFª MARCELA CARVALHO
 QUÍMICA 1 PROFª MARCELA CARVALHO EQUAÇÃO QUÍMICA É a representação química simbólica e abreviada de uma reação química. 2 H2 + O2 2 H2O 2, 1 e 2 = coeficientes estequiométricos ou simplesmente coeficiente,
QUÍMICA 1 PROFª MARCELA CARVALHO EQUAÇÃO QUÍMICA É a representação química simbólica e abreviada de uma reação química. 2 H2 + O2 2 H2O 2, 1 e 2 = coeficientes estequiométricos ou simplesmente coeficiente,
O EFEITO DO ELETROPOLIMENTO EM SOLDAS DE AÇO INOX E ZONAS AFETADAS PELO CALOR
 O EFEITO DO ELETROPOLIMENTO EM SOLDAS DE AÇO INOX E ZONAS AFETADAS PELO CALOR por Ryszard Rokicki Electrobright, Macungie, PA INTRODUÇÃO Os aços inoxidáveis austeníticos (série 300) são largamente utilizados
O EFEITO DO ELETROPOLIMENTO EM SOLDAS DE AÇO INOX E ZONAS AFETADAS PELO CALOR por Ryszard Rokicki Electrobright, Macungie, PA INTRODUÇÃO Os aços inoxidáveis austeníticos (série 300) são largamente utilizados
EFEITO DOS ELEMENTOS DE LIGA NOS AÇOS
 EFEITO DOS ELEMENTOS DE LIGA NOS AÇOS Seleção do processo de fundição Metal a ser fundido [C. Q.]; Qualidade requerida da superfície do fundido; Tolerância dimensional requerida para o fundido; Quantidade
EFEITO DOS ELEMENTOS DE LIGA NOS AÇOS Seleção do processo de fundição Metal a ser fundido [C. Q.]; Qualidade requerida da superfície do fundido; Tolerância dimensional requerida para o fundido; Quantidade
Na natureza nada se cria, nada se perde, tudo se transforma
 CEEJA QUÍMICA CONTEÚDO PARA U. E. 05 Na natureza nada se cria, nada se perde, tudo se transforma O QUE VAMOS APRENDER? Conservação da matéria na reação química Proporção das substâncias que reagem Os símbolos
CEEJA QUÍMICA CONTEÚDO PARA U. E. 05 Na natureza nada se cria, nada se perde, tudo se transforma O QUE VAMOS APRENDER? Conservação da matéria na reação química Proporção das substâncias que reagem Os símbolos
BALANÇO ENERGÉTICO NUM SISTEMA TERMODINÂMICO
 BALANÇO ENERGÉTICO NUM SISTEMA TERMODINÂMICO O que se pretende Determinar experimentalmente qual dos seguintes processos é o mais eficaz para arrefecer água à temperatura ambiente: Processo A com água
BALANÇO ENERGÉTICO NUM SISTEMA TERMODINÂMICO O que se pretende Determinar experimentalmente qual dos seguintes processos é o mais eficaz para arrefecer água à temperatura ambiente: Processo A com água
Unidade 10 Estudo dos Gases. Introdução Equação dos gases Transformação Isotérmica Transformação Isobárica Transformação Isocórica Diagrama de Fases
 Unidade 0 Estudo dos Gases Introdução Equação dos gases ransformação Isotérmica ransformação Isobárica ransformação Isocórica Diagrama de Fases Introdução Equação Geral dos Gases Na Química, aprendemos
Unidade 0 Estudo dos Gases Introdução Equação dos gases ransformação Isotérmica ransformação Isobárica ransformação Isocórica Diagrama de Fases Introdução Equação Geral dos Gases Na Química, aprendemos
7 COMPORTAMENTO DOS GASES, VAPORES E MISTURAS NÃO IDEAIS
 7 COMPORTAMENTO DOS GASES, VAPORES E MISTURAS NÃO IDEAIS 7.1 PROPRIEDADE Qualquer característica mensurável de uma substância ou mistura, tal como pressão, volume, temperatura, ou característica que possa
7 COMPORTAMENTO DOS GASES, VAPORES E MISTURAS NÃO IDEAIS 7.1 PROPRIEDADE Qualquer característica mensurável de uma substância ou mistura, tal como pressão, volume, temperatura, ou característica que possa
EXERCÍCIOS PARA ESTUDOS DILATAÇÃO TÉRMICA
 1. (Unesp 89) O coeficiente de dilatação linear médio de um certo material é = 5,0.10 ( C) e a sua massa específica a 0 C é ³. Calcule de quantos por cento varia (cresce ou decresce) a massa específica
1. (Unesp 89) O coeficiente de dilatação linear médio de um certo material é = 5,0.10 ( C) e a sua massa específica a 0 C é ³. Calcule de quantos por cento varia (cresce ou decresce) a massa específica
Água na atmosfera. Capítulo 5 - Ahrens
 Água na atmosfera Capítulo 5 - Ahrens Propriedades da água Estados Físicos Única substântica natural que ocorre naturalmente nos três estados sobre a superfície da terra Capacidade Térmica Mais alta se
Água na atmosfera Capítulo 5 - Ahrens Propriedades da água Estados Físicos Única substântica natural que ocorre naturalmente nos três estados sobre a superfície da terra Capacidade Térmica Mais alta se
t 1 t 2 Tempo t 1 t 2 Tempo
 Concentração 01)Uma reação química atinge o equilíbrio químico quando: a) ocorre simultaneamente nos sentidos direto e inverso. b) as velocidades das reações direta e inversa são iguais. c) os reatantes
Concentração 01)Uma reação química atinge o equilíbrio químico quando: a) ocorre simultaneamente nos sentidos direto e inverso. b) as velocidades das reações direta e inversa são iguais. c) os reatantes
M A S S A S E M E D I D A S
 M A S S A S E M E D I D A S PROF. AGAMENON ROBERTO < 2010 > Prof. Agamenon Roberto ATOMÍSTICA www.agamenonquimica.com 2 MASSAS E MEDIDAS UNIDADE DE MASSA ATÔMICA (u.m.a.) Para pesar ou medir algo se torna
M A S S A S E M E D I D A S PROF. AGAMENON ROBERTO < 2010 > Prof. Agamenon Roberto ATOMÍSTICA www.agamenonquimica.com 2 MASSAS E MEDIDAS UNIDADE DE MASSA ATÔMICA (u.m.a.) Para pesar ou medir algo se torna
COLÉGIO XIX DE MARÇO excelência em educação 2ª PROVA PARCIAL DE CIÊNCIAS
 COLÉGIO XIX DE MARÇO excelência em educação 2012 2ª PROVA PARCIAL DE CIÊNCIAS Aluno(a): Nº Ano: 6º Turma: Data: 11/08/2012 Nota: Professor(a): Karina Valor da Prova: 40 pontos Orientações gerais: 1) Número
COLÉGIO XIX DE MARÇO excelência em educação 2012 2ª PROVA PARCIAL DE CIÊNCIAS Aluno(a): Nº Ano: 6º Turma: Data: 11/08/2012 Nota: Professor(a): Karina Valor da Prova: 40 pontos Orientações gerais: 1) Número
PROF. DÊNIS ALUNO(A) FUNDAMENTOS TEÓRICOS CÁLCULOS ESTEQUIOMÉTRICOS. A seguir devemos igualar o número de elétrons: 1) DEFINIÇÃO
 31/1/2011 PROF. DÊNIS ALUNO(A) FUNDAMENTOS TEÓRICOS CÁLCULOS ESTEQUIOMÉTRICOS 1) DEFINIÇÃO Pra que o cálculo proporcional esteja devidamente acertado se faz necessário o balanceamento da reação química
31/1/2011 PROF. DÊNIS ALUNO(A) FUNDAMENTOS TEÓRICOS CÁLCULOS ESTEQUIOMÉTRICOS 1) DEFINIÇÃO Pra que o cálculo proporcional esteja devidamente acertado se faz necessário o balanceamento da reação química
PROBLEMAS DE TERMOLOGIA
 PROBLEMAS DE TERMOLOGIA 1 - Numa estação meteorológica, foi registrada uma temperatura máxima de 25ºC. Qual é a indicação da máxima na escala Fahrenheit? 2 - Numa escala termométrica X, marca-se -10ºX
PROBLEMAS DE TERMOLOGIA 1 - Numa estação meteorológica, foi registrada uma temperatura máxima de 25ºC. Qual é a indicação da máxima na escala Fahrenheit? 2 - Numa escala termométrica X, marca-se -10ºX
Tecnol. Mecânica: Produção do Aço
 Mesmo quando os métodos de fabricação eram bastante rudimentares os artesãos da Antiguidade, na Ásia e, mais tarde, na Europa medieval, conseguiam fabricar o aço. O aço daquela época chamava-se aço de
Mesmo quando os métodos de fabricação eram bastante rudimentares os artesãos da Antiguidade, na Ásia e, mais tarde, na Europa medieval, conseguiam fabricar o aço. O aço daquela época chamava-se aço de
Física Térmica Exercícios. Dilatação.
 Física Térmica Exercícios. Dilatação. Dilatação linear 1- Uma bobina contendo 2000 m de fio de cobre medido num dia em que a temperatura era de 35 C. Se o fio for medido de novo em um dia que a temperatura
Física Térmica Exercícios. Dilatação. Dilatação linear 1- Uma bobina contendo 2000 m de fio de cobre medido num dia em que a temperatura era de 35 C. Se o fio for medido de novo em um dia que a temperatura
Distância entre o eléctrodo de medida e a parede do tanque ( eléctrodos ). Área da superfície dos eléctrodos. Constante dieléctrica da substância.
 O nível de líquidos, interfaces e sólidos granulares pode ser medido usando o efeito de capacitância eléctrica.. A capacitância do condensador é principalmente influenciada por três elementos: Distância
O nível de líquidos, interfaces e sólidos granulares pode ser medido usando o efeito de capacitância eléctrica.. A capacitância do condensador é principalmente influenciada por três elementos: Distância
www.professormazzei.com Assunto: Eletroquímica Folha 4.2 Prof.: João Roberto Mazzei
 www.professormazzei.com Assunto: Eletroquímica Folha 4.2 Prof.: João Roberto Mazzei 01. (UDESC 2009) O hidrogênio tem sido proposto como o combustível "ecológico", já que a sua reação de combustão com
www.professormazzei.com Assunto: Eletroquímica Folha 4.2 Prof.: João Roberto Mazzei 01. (UDESC 2009) O hidrogênio tem sido proposto como o combustível "ecológico", já que a sua reação de combustão com
Termodinâmica Aplicada I Lista de exercícios 1ª Lei para Volume de Controle
 Termodinâmica Aplicada I Lista de exercícios 1ª Lei para Volume de Controle 1. Água evapora no interior do tubo de uma caldeira que opera a 100 kpa. A velocidade do escoamento de líquido saturado que alimenta
Termodinâmica Aplicada I Lista de exercícios 1ª Lei para Volume de Controle 1. Água evapora no interior do tubo de uma caldeira que opera a 100 kpa. A velocidade do escoamento de líquido saturado que alimenta
VI Olimpíada Norte - Nordeste de Química e
 VI Olimpíada Norte - Nordeste de Química e Seletiva para a Olimpíada Ibero-americana de Química - 2000 Exame aplicado em 27.05.2000 Somente as questões de números 1 a 6 serão consideradas na composição
VI Olimpíada Norte - Nordeste de Química e Seletiva para a Olimpíada Ibero-americana de Química - 2000 Exame aplicado em 27.05.2000 Somente as questões de números 1 a 6 serão consideradas na composição
CONSERVAÇÃO DE ALIMENTOS PELO FRIO PRODUÇÃO ARTIFICIAL DO FRIO
 1 CONSERVAÇÃO DE ALIMENTOS PELO FRIO PRODUÇÃO ARTIFICIAL DO FRIO O frio industrial é produzido pela expansão de um gás, que tenha um baixo ponto de ebulição. Tabela 6.1. O gás escolhido é mantido sob pressão,
1 CONSERVAÇÃO DE ALIMENTOS PELO FRIO PRODUÇÃO ARTIFICIAL DO FRIO O frio industrial é produzido pela expansão de um gás, que tenha um baixo ponto de ebulição. Tabela 6.1. O gás escolhido é mantido sob pressão,
ENTENDA OS PRINCÍPIOS DA ALTIMETRIA
 ENTENDA OS PRINCÍPIOS DA ALTIMETRIA Altura, Altitude, Nível de Voo. Para muitos de nós, isto pode parecer muito semelhante, talvez até a mesma coisa. Mas em aeronáutica, cada uma destas palavras tem um
ENTENDA OS PRINCÍPIOS DA ALTIMETRIA Altura, Altitude, Nível de Voo. Para muitos de nós, isto pode parecer muito semelhante, talvez até a mesma coisa. Mas em aeronáutica, cada uma destas palavras tem um
A ÁLISE TITRIMÉTRICA
 A ÁLISE TITRIMÉTRICA Análise titrimétrica - O termo análise titrimétrica refere-se à análise química quantitativa feita pela determinação do volume de uma solução, cuja concentração é conhecida com exatidão,
A ÁLISE TITRIMÉTRICA Análise titrimétrica - O termo análise titrimétrica refere-se à análise química quantitativa feita pela determinação do volume de uma solução, cuja concentração é conhecida com exatidão,
PROPRIEDADES COLIGATIVAS PARTE 2
 PROPRIEDADES COLIGATIVAS PARTE 2 1. (Adaptado) Tendo em vista o momento em que um líquido se encontra em equilíbrio com seu vapor, leia atentamente as afirmativas abaixo: I. A evaporação e a condensação
PROPRIEDADES COLIGATIVAS PARTE 2 1. (Adaptado) Tendo em vista o momento em que um líquido se encontra em equilíbrio com seu vapor, leia atentamente as afirmativas abaixo: I. A evaporação e a condensação
2. MEDIDORES DE TEMPERATURA POR DILATAÇÃO/EXPANSÃO
 2. MEDIDORES DE TEMPERATURA POR DILATAÇÃO/EXPANSÃO 2.1 TERMÔMETRO A DILATAÇÃO DE LÍQUIDO 2.1.1 Características Os termômetros de dilatação de líquidos, baseiam-se na lei de expansão volumétrica de um líquido
2. MEDIDORES DE TEMPERATURA POR DILATAÇÃO/EXPANSÃO 2.1 TERMÔMETRO A DILATAÇÃO DE LÍQUIDO 2.1.1 Características Os termômetros de dilatação de líquidos, baseiam-se na lei de expansão volumétrica de um líquido
MF.513.R-2 - DETERMINAÇÃO DA CONCENTRAÇÃO DE CO2, DO EXCESSO DE AR E DO PESO MOLECULAR DO GÁS SECO, EM CHAMINÉS
 MF.513.R-2 - DETERMINAÇÃO DA CONCENTRAÇÃO DE CO2, DO EXCESSO DE AR E DO PESO MOLECULAR DO GÁS SECO, EM CHAMINÉS Notas: Aprovada pela Deliberação CECA n. 168, de 02 de abril de 1981 Publicada no DOERJ de
MF.513.R-2 - DETERMINAÇÃO DA CONCENTRAÇÃO DE CO2, DO EXCESSO DE AR E DO PESO MOLECULAR DO GÁS SECO, EM CHAMINÉS Notas: Aprovada pela Deliberação CECA n. 168, de 02 de abril de 1981 Publicada no DOERJ de
P1 - PROVA DE QUÍMICA GERAL 10/09/08
 P1 - PROVA DE QUÍMICA GERAL 10/09/08 Nome: GABARITO Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Dados R 0,081 atm L mol -1 K -1 T (K) T ( C) + 73,15
P1 - PROVA DE QUÍMICA GERAL 10/09/08 Nome: GABARITO Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Dados R 0,081 atm L mol -1 K -1 T (K) T ( C) + 73,15
Lista de Exercícios. Estudo da Matéria
 FACULDADE PITÁGORAS DE BETIM Credenciada pela portaria 792, de 27 de março de 2006. Curso: Engenharia Química Lista de Exercícios Disciplina: Química Geral Semestre: 2º / 2013 Docente: Carla Soares Souza
FACULDADE PITÁGORAS DE BETIM Credenciada pela portaria 792, de 27 de março de 2006. Curso: Engenharia Química Lista de Exercícios Disciplina: Química Geral Semestre: 2º / 2013 Docente: Carla Soares Souza
Massa é a grandeza física que mede quanto de matéria possui um corpo ou objeto. Ocupar lugar no espaço significa ter volume.
 Matéria é tudo que tem massa e ocupa lugar no espaço Massa é a grandeza física que mede quanto de matéria possui um corpo ou objeto. Ocupar lugar no espaço significa ter volume. Como exemplos de matéria
Matéria é tudo que tem massa e ocupa lugar no espaço Massa é a grandeza física que mede quanto de matéria possui um corpo ou objeto. Ocupar lugar no espaço significa ter volume. Como exemplos de matéria
Fenômenos de Transporte I Lista de Exercícios Conservação de Massa e Energia
 Fenômenos de Transporte I Lista de Exercícios Conservação de Massa e Energia Exercícios Teóricos Formulário: Equação de Conservação: Acúmulo = Entrada - Saída + Geração - Perdas Vazão Volumétrica: Q v.
Fenômenos de Transporte I Lista de Exercícios Conservação de Massa e Energia Exercícios Teóricos Formulário: Equação de Conservação: Acúmulo = Entrada - Saída + Geração - Perdas Vazão Volumétrica: Q v.
RESULTADO DO LEVANTAMENTO DE DADOS DE MONITORAMENTO DA EMISSÃO ATMOSFÉRICA EM PROCESSOS DE QUEIMA DE DERIVADOS DE MADEIRA
 CONAMA - Grupo de Trabalho Fontes Fixas Existentes Subgrupo Derivados de Madeira abril-2009 RESULTADO DO LEVANTAMENTO DE DADOS DE MONITORAMENTO DA EMISSÃO ATMOSFÉRICA EM PROCESSOS DE QUEIMA DE DERIVADOS
CONAMA - Grupo de Trabalho Fontes Fixas Existentes Subgrupo Derivados de Madeira abril-2009 RESULTADO DO LEVANTAMENTO DE DADOS DE MONITORAMENTO DA EMISSÃO ATMOSFÉRICA EM PROCESSOS DE QUEIMA DE DERIVADOS
Colégio Santa Dorotéia
 Colégio Santa Dorotéia Área de Ciências da Natureza Disciplina: Física Série: 2ª Ensino Médio Professor: Marcelo Chaves Física Atividades para Estudos Autônomos Data: 25 / 4 / 2016 Valor: xxx pontos Aluno(a):
Colégio Santa Dorotéia Área de Ciências da Natureza Disciplina: Física Série: 2ª Ensino Médio Professor: Marcelo Chaves Física Atividades para Estudos Autônomos Data: 25 / 4 / 2016 Valor: xxx pontos Aluno(a):
MOQ-14 PROJETO E ANÁLISE DE EXPERIMENTOS LISTA DE EXERCÍCIOS 3
 MOQ-14 PROJETO E ANÁLISE DE EXPERIMENTOS LISTA DE EXERCÍCIOS 3 1. Chapas de uma liga metálica de mesma procedência foram submetidas, de forma aleatória, a três diferentes tratamentos térmicos: A, B e C.
MOQ-14 PROJETO E ANÁLISE DE EXPERIMENTOS LISTA DE EXERCÍCIOS 3 1. Chapas de uma liga metálica de mesma procedência foram submetidas, de forma aleatória, a três diferentes tratamentos térmicos: A, B e C.
P2 - PROVA DE QUÍMICA GERAL - 08/10/07
 P2 - PRVA DE QUÍMICA GERAL - 08/10/07 Nome: Nº de Matrícula: GABARIT Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 R = 8,314 J mol -1 K -1 = 0,0821 atm L mol
P2 - PRVA DE QUÍMICA GERAL - 08/10/07 Nome: Nº de Matrícula: GABARIT Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 R = 8,314 J mol -1 K -1 = 0,0821 atm L mol
Colégio Saint Exupéry
 Colégio Saint Exupéry Apostila QUÍMICA No nosso dia-a-dia o ato de classificar as coisas é algo corriqueiro. Em um faqueiro colocamos em um mesmo espaço as facas, em outro os garfos, etc. Agrupar coisas
Colégio Saint Exupéry Apostila QUÍMICA No nosso dia-a-dia o ato de classificar as coisas é algo corriqueiro. Em um faqueiro colocamos em um mesmo espaço as facas, em outro os garfos, etc. Agrupar coisas
Aço Inoxidável Ferrítico ACE P410D
 ArcelorMittal Inox Brasil Aço Inoxidável Ferrítico ACE P410D transformando o amanhã 2 3 ACE P410D O aço inoxidável ACE P410D é um material que apresenta, por sua resistência a problemas de corrosão e abrasão
ArcelorMittal Inox Brasil Aço Inoxidável Ferrítico ACE P410D transformando o amanhã 2 3 ACE P410D O aço inoxidável ACE P410D é um material que apresenta, por sua resistência a problemas de corrosão e abrasão
Propriedades de Misturas. Parte 2
 Propriedades de Misturas Parte 2 Exemplo: cálculo de M do ar seco M = y i M i 0,78M N2 + 0,21M O2 + 0,0093M Ar + 0,0003M CO2 0,78.28 + 0,21.32 + 0,0093.40 + 0,0003.44 = 28,97kg/kmol Exemplo A análise
Propriedades de Misturas Parte 2 Exemplo: cálculo de M do ar seco M = y i M i 0,78M N2 + 0,21M O2 + 0,0093M Ar + 0,0003M CO2 0,78.28 + 0,21.32 + 0,0093.40 + 0,0003.44 = 28,97kg/kmol Exemplo A análise
