Substâncias Puras e Misturas
|
|
|
- Lucas Gabriel Soares Bernardes
- 9 Há anos
- Visualizações:
Transcrição
1 MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES Substâncias Puras e Misturas
2 Elementos Químicos Átomos Nome (Português-Latim) Ferro (Ferrum) Cálcio (Calcium) Prata (Argentum) Oxigênio (Oxygenium) Símbolo Fe Ca Ag O Natureza Fe 3 O 4 CaCO 3 Ag O 2
3 Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas
4 Substância Química Definição: é uma porção de matéria que tem propriedades bem definidas e que lhe são característica. Fósforo Sódio Chumbo Cloro
5 ESTUDO DAS SUBSTÂNCIAS E MISTURAS SUBSTÂNCIA: material formado por moléculas quimicamente iguais. Substância pura simples : é constituída de uma molécula formada por átomos do mesmo elemento químico (mesmo tipo de átomo).
6 Substância Pura Substância pura é todo material com as seguintes características: Unidades estruturais (moléculas, conjuntos iônicos) quimicamente iguais entre si. Composição fixa, do que decorrem propriedades fixas, como densidade, ponto de fusão e de ebulição, etc. A temperatura se mantém inalterada desde o início até o fim de todas as suas mudanças de estado físico (fusão, ebulição, solidificação, etc.).
7 Substância Pura Simples Substâncias puras simples: que são formadas pela combinação de átomos de um único elemento químico, como por exemplo o gás hidrogênio (H 2 ) formado por dois átomos de hidrogênio ligados entre si; o ozônio (O 3 ) formado por três átomos de oxigênio.
8 Substância pura simples Substância Fórmula Representação Gás hidrogênio H 2 Gás oxigênio O 2 Gás ozônio O 3
9 Substância Pura Composta Substâncias puras compostas: formadas pela combinação de átomos de dois ou mais elementos químicos diferentes Ex.: água formada por dois átomos de hidrogênio e um átomo de oxigênio; ácido clorídrico (HCl)formado por um átomo de hidrogênio e um átomo de cloro.
10 Substância pura composta: é constituída por uma molécula formada por mais de um elemento químico. Substância Fórmula Representação Água Sal de cozinha H 2 O NaCl Açúcar C 12 H 22 O 11
11 Substâncias Puras SIMPLES COMPOSTA
12 Misturas Homogêneas e Heterogêneas
13 Mistura: é formada por duas, ou mais, substâncias, sendo cada uma destas denominada componente. CLASSIFICAÇÃO DAS MISTURAS Fase: em uma mistura, é cada uma das porções que apresenta aspecto homogêneo ou uniforme. Mistura homogênea: toda mistura que apresenta uma única fase. Mistura heterogênea: toda mistura que apresenta pelo menos duas fases.
14 EXEMPLO: Água (H 2 O) + açúcar dissolvido (C 12 H 22 O 11 ) Aspecto visual contínuo: uma única fase Óleo(C x H y ) + água (H 2 O) Aspecto visual descontínuo: duas fases Água gaseificada Aspecto visual descontínuo: duas fases
15 Nome Amálgama Componentes principais Mercúrio (Hg) + outros metais Vinagre Água (H 2 O) + ácido acético (CH 3 COOH) Latão Cobre (Cu) + zinco (Zn) Bronze Aço Álcool hidratado Cobre (Cu) + estanho (Sn) Ferro (Fe) + carbono (C) Etanol (CH 3 OH) + água (H 2 O)
16 Misturas Homogêneas e Heterogêneas Por exemplo, uma garrafa de álcool (etanol) tem sempre uma certa porção de água misturada; estas duas substâncias estão tão bem misturadas uma com a outra que não se pode dizer que a água está num lado e o álcool de outro, ou seja, a composição da mistura é a mesma em qualquer zona da garrafa - mistura homogênea. Já o mesmo não acontece com uma mistura de água e areia; a areia fica em baixo separada da água. A composição desta mistura não é uniforme - mistura heterogênea.
17 Misturas Homogêneas e Heterogêneas Misturas Homogêneas - não é possível distinguir os componentes da mistura, mesmo observando ao microscópio. Misturas Heterogêneas - é possível distinguir, à vista desarmada os diferentes componentes que a constituem.
18 MISTURAS AR ÁGUA + AREIA HOMOGÊNEA solução HETEROGÊNEA
19 O leite é... Aspecto homogêneo a olho nu Aspecto heterogêneo ao microscópio Copo de leite Líquido branco com gotículas de gordura O leite é, então, considerado uma mistura heterogênea.
20 Sistema: tudo o que é objeto da observação humana. Sistemas homogêneos Sistemas heterogêneos Substância pura Mistura Substância pura Mistura Água Álcool hidratado Gelo: H 2 O (sól) + Água: H 2 O (líq) Água + óleo
21 SUBSTÂNCIA PURA SUBSTÂNCIA PURA X MISTURA temperatura (graus Celsius) 100 água vapor d'água 0 gelo gelo + água água + vapor d'água estado sólido fusão solidificação estado líquido ebulição condensação estado gasoso
22 Água Pura + Sal de cozinha Misturas Água Pura Definição: é a união de duas ou mais substâncias químicas. Uma das formas de diferenciação das substâncias puras e das misturas é através da temperatura, durante as mudanças de estado físico. Essas observações podem ser traduzidas em um gráfico, a linha horizontal que aparece no gráfico é chamada de patamar e indica a temperatura de fusão e a de vaporização da substância pura. Para um mistura de água e sal, por exemplo, não se verifica o aparecimento do patamar, tanto na fusão como na ebulição, porque a temperatura não se mantém constante.
23 MISTURA
24 MISTURAS EUTÉTICAS É uma mistura de elementos ou compostos sólidos e distintos que se comportam como se fossem uma substância pura e onde o ponto de fusão ocorre em temperatura constante até que o componente mais volátil seja totalmente descristalizado.
25
26 MISTURA AZEOTRÓPICA No caso de misturas azeotrópicas, a composição da fase líquida da mistura e da fase gasosa é a mesma numa temperatura denominada temperatura azeotrópica ou ponto azeotrópico. Na prática, isto inviabiliza a separação da mistura por destilação, pois, quando a temperatura atinge a temperatura azeotrópica, a composição da fase líquida é a mesma da fase gasosa.
27
28 EXEMPLOS DE MISTURAS Mistura eutética Ponto de fusão Chumbo (38%) + estanho (62%) 183 C Chumbo (87%) + antimônio (13%) 246 C Bismuto (58%) + estanho (42%) 133 C Mistura azeotrópica Ponto de ebulição Acetona (86,5%) + metanol (13,5%) 56 C Álcool etílico (7%) + clorofórmio (93%) 60 C Álcool fórmico (77,5%) + água (22,5%) 107,3 C
29 Sistemas Materiais Substância Pura Mistura Simples Composta Homogênea Heterogênea
30 SISTEMAS HOMOGÊNEOS SISTEMAS HETEROGÊNEOS SUBSTÂNCIAS PURAS MISTURAS DE UMA FASE MISTURAS DE MAIS DE UMA FASE SUBSTÂNCIAS EM MUDANÇA DE ESTADO
31 EXERCÍCIOS DE FIXAÇÃO Considere os sistemas a seguir, em que os átomos são representados por esferas: I II III IV Determine onde encontramos: a) Substância pura; b) Mistura; c) Duas substâncias simples; d) Somente substância composta. Considere apenas o sistema III, determine: a) O número de átomos presentes; b) O número de elementos químicos; c) O número de moléculas; d) O número de substâncias;
32 2. Os diferentes tipos de matéria podem ser classificados em dois grupos: Substâncias puras e misturas. As substâncias puras podem ser simples e compostas. Considerando esse modo de classificação, julgue as afirmativas: I. O ar atmosférico é uma substância pura. II. A água é uma substância simples. III.O oxigênio e o ozônio são substâncias distintas, embora constituídas por átomos de um mesmo elemento. IV.A matéria que contém três tipos de moléculas é uma substância composta. V. A matéria que contém apenas um tipo de molécula é uma substância simples, mesmo que cada molécula seja formada por dois átomos diferentes.
33 3. Observe os seguintes fatos: I Uma pedra de naftalina deixada no armário. II Uma vasilha com água deixada no freezer. III Uma vasilha com água deixada no fogo. IV O derretimento de um pedaço de chumbo quando aquecido. Nestes fatos estão relacionados corretamente os seguintes fenômenos: a) I sublimação, II solidificação, III vaporização, IV fusão. b) I sublimação, II solidificação, III fusão, IV vaporização. c) I fusão, II sublimação, III vaporização, IV solidificação. d) I vaporização, II solidificação, III fusão, IV sublimação. e) I vaporização, II sublimação, II fusão, IV solidificação.
34 5. Qual dos fenômenos a seguir não envolve reações químicas? Fusão de gelo. Digestão de alimentos. Combustão. Queima de vela. Explosão de dinamite.
35 6) Das alternativas abaixo, a que constitui exemplo de substâncias simples é: a) H 2 O, O 2, H 2 b) N 2, O 3, O 2 c) CH 4, H 2 O, H 2 d) H 2 O 2, CH 4, N 2 e) P 4, S 8, H 2 S 7) A menor quantidade de clorofórmio (CHCl 3 ) onde podem ser reconhecidas suas propriedades é: a) um átomo de clorofórmio b) um mol de clorofórmio c) um átomo de carbono d) uma molécula de clorofórmio e) uma molécula de cloro
36 8) Na natureza, as três classes gerais em que todas as formas de matéria podem ser divididas são: elementos, compostos e misturas. Dados os materiais: I. Ouro II. Leite III. Cloreto de sódio quais deles constituem, respectivamente, uma mistura, um composto e um elemento? 9) O oxigênio, fundamental à respiração dos animais, e o ozônio, gás que protege a Terra dos efeitos dos raios ultravioletas da luz solar, diferem quanto: a) ao número atômico dos elementos químicos que os formam. b) à configuração eletrônica dos átomos que os compõem. c) ao número de prótons dos átomos que entram em suas composições. d) ao número de átomos que compõem suas moléculas. e) à natureza dos elementos químicos que os originam.
37 10) Durante a fusão de um sistema homogêneo A, verifica-se que a temperatura se mantém constante do início ao fim da fusão. O sistema A: a) certamente é uma substância pura b) certamente é uma mistura eutética c) certamente é uma mistura azeotrópica d) pode ser uma substância pura ou uma mistura eutética e) pode ser uma substância pura ou uma mistura azeotrópica. 11) Durante a ebulição de um sistema A, verifica-se que a temperatura se mantém constante até o fim da ebulição (vaporização). O sistema A: a) certamente é uma substância pura b) certamente é uma mistura eutética c) certamente é uma mistura azeotrópica d) pode ser uma substância pura ou uma mistura eutética e) pode ser uma substância pura ou uma mistura azeotrópica.
38 12) Durante a fusão e a ebulição de um sistema A, a temperatura se mantém constante até o fim de cada mudança de estado. O sistema A: a) certamente é uma substância pura b) certamente é uma mistura eutética c) certamente é uma mistura azeotrópica d) pode ser uma substância pura ou uma mistura eutética e) pode ser uma substância pura ou uma mistura azeotrópica. 13) Dados os materiais: I - água (l) + álcool (l) II - O 2 (g) + CO 2 (g) III - água(l) + NaCl(s) IV - água(l) + gasolina (l) constituem sempre um sistema homogêneo qualquer que seja a quantidade: a) somente I, II e III. b) somente I, II. c) somente II e III. d) somente I e III. e) todos.
39 MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES Soluções
40 Algumas Definições Uma solução é uma mistura HOMOGÊNEA de 2 ou mais substâncias em uma única fase. Um dos constituintes é o SOLVENTE os outros são os SOLUTOS.
41 Definições Soluções pode ser classificadas como saturadas ou insaturadas. Uma solução saturada contém a maior quantidade de soluto capaz de ser dissolvida em uma determinada temperatura.
42 Processo de Separação de Misturas
43 Fracionamento de Misturas São as técnicas usadas para separar misturas, e que se fundamentam nas diferentes propriedades físicas das substâncias que constituem as misturas. Para separar uma mistura devemos seguir os seguintes passos: 1) Verificar se HOMO ou HETERO; 2) Verificar ESTADO FÍSICO; 3) Escolher o método
44 Separação de Mistura
Átomos & Moléculas. Definição: é uma porção de matéria que tem propriedades bem definidas e que lhe são característica.
 Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Definição: é uma porção de matéria que tem propriedades bem definidas e que lhe são característica. SUBSTÂNCIA (Material Puro): material formado
Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Definição: é uma porção de matéria que tem propriedades bem definidas e que lhe são característica. SUBSTÂNCIA (Material Puro): material formado
Química Prof. Rogério 2016. Química. Professor Rogério. Imagens meramente ilustrativas, domínio público sites diversos/internet
 Química Prof. Rogério 2016 Química Professor Rogério Imagens meramente ilustrativas, domínio público sites diversos/internet 1º MOMENTO - Propriedades básicas da matéria - Tabela periódica - Estrutura
Química Prof. Rogério 2016 Química Professor Rogério Imagens meramente ilustrativas, domínio público sites diversos/internet 1º MOMENTO - Propriedades básicas da matéria - Tabela periódica - Estrutura
Unidade 2 Substâncias e átomos
 Unidade 2 Substâncias e átomos Substâncias Puras pág. 51 A matéria é composta por uma ou mais substâncias químicas. Porém, é difícil saber se um corpo é composto por uma única substância ou por uma mistura
Unidade 2 Substâncias e átomos Substâncias Puras pág. 51 A matéria é composta por uma ou mais substâncias químicas. Porém, é difícil saber se um corpo é composto por uma única substância ou por uma mistura
Lista de Exercícios. Estudo da Matéria
 FACULDADE PITÁGORAS DE BETIM Credenciada pela portaria 792, de 27 de março de 2006. Curso: Engenharia Química Lista de Exercícios Disciplina: Química Geral Semestre: 2º / 2013 Docente: Carla Soares Souza
FACULDADE PITÁGORAS DE BETIM Credenciada pela portaria 792, de 27 de março de 2006. Curso: Engenharia Química Lista de Exercícios Disciplina: Química Geral Semestre: 2º / 2013 Docente: Carla Soares Souza
HOMOGÊNEO HETEROGÊNEO
 Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico f que contenha ou não matéria,
Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico f que contenha ou não matéria,
AS TRANSFORMAÇÕES DA MATÉRIA.
 AS TRANSFORMAÇÕES DA MATÉRIA. Toda e qualquer alteração que a matéria venha a sofrer é denominada de transformação ou fenômeno. Algumas transformações (fenômenos) são reversíveis, isto é, podem ser desfeitas
AS TRANSFORMAÇÕES DA MATÉRIA. Toda e qualquer alteração que a matéria venha a sofrer é denominada de transformação ou fenômeno. Algumas transformações (fenômenos) são reversíveis, isto é, podem ser desfeitas
C o l é g i o R i c a r d o R o d r i g u e s A l v e s
 C o l é g i o R i c a r d o R o d r i g u e s A l v e s Educação Infantil - Ensino Fundamental I - Ensino Médio 1 TRIMESTRE Química 1ª Série do Ensino Médio Conteúdo Introdução a Química Átomo Molécula
C o l é g i o R i c a r d o R o d r i g u e s A l v e s Educação Infantil - Ensino Fundamental I - Ensino Médio 1 TRIMESTRE Química 1ª Série do Ensino Médio Conteúdo Introdução a Química Átomo Molécula
Aluno(a): Nº. Professor: Série: 1 Disciplina: Data da prova:
 Lista de Exercícios Aluno(a): Nº. Professor: Série: 1 Disciplina: Data da prova: 1. (UFAC) O gráfico abaixo mostra a curva de aquecimento para o clorofórmio, usualmente utilizado como solvente para lipídeos.
Lista de Exercícios Aluno(a): Nº. Professor: Série: 1 Disciplina: Data da prova: 1. (UFAC) O gráfico abaixo mostra a curva de aquecimento para o clorofórmio, usualmente utilizado como solvente para lipídeos.
ORIENTAÇÃO DE ESTUDOS
 ORIENTAÇÃO DE ESTUDOS RECUPERAÇÃO SEMESTRAL 1º Ano do Ensino Médio Disciplina: Química 1. Considere a tabela a seguir, onde estão relacionados os pontos de fusão e de ebulição de algumas substâncias sob
ORIENTAÇÃO DE ESTUDOS RECUPERAÇÃO SEMESTRAL 1º Ano do Ensino Médio Disciplina: Química 1. Considere a tabela a seguir, onde estão relacionados os pontos de fusão e de ebulição de algumas substâncias sob
Massa é a grandeza física que mede quanto de matéria possui um corpo ou objeto. Ocupar lugar no espaço significa ter volume.
 Matéria é tudo que tem massa e ocupa lugar no espaço Massa é a grandeza física que mede quanto de matéria possui um corpo ou objeto. Ocupar lugar no espaço significa ter volume. Como exemplos de matéria
Matéria é tudo que tem massa e ocupa lugar no espaço Massa é a grandeza física que mede quanto de matéria possui um corpo ou objeto. Ocupar lugar no espaço significa ter volume. Como exemplos de matéria
INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA EXPERIMENTAL
 INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA EXPERIMENTAL ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os
INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA EXPERIMENTAL ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os
COLÉGIO RESSURREIÇÃO NOSSA SENHORA Disciplina:
 CONTEÚDO A SER EXIGIDO COLÉGIO RESSURREIÇÃO NOSSA SENHORA Disciplina: Professor(a): Data: Química Natan 30/10/2014 Roteiro e Período: Exercícios 4 o Prova final e Recuperação final. Bimestre Aluno: Nº
CONTEÚDO A SER EXIGIDO COLÉGIO RESSURREIÇÃO NOSSA SENHORA Disciplina: Professor(a): Data: Química Natan 30/10/2014 Roteiro e Período: Exercícios 4 o Prova final e Recuperação final. Bimestre Aluno: Nº
www.professormazzei.com Propriedades da Matéria Folha 05- Prof.: João Roberto Mazzei
 Questão 01 Em uma cena de um filme, um indivíduo corre carregando uma maleta tipo 007 (volume 20 dm³) cheia de barras de um certo metal. Considerando que um adulto de peso médio (70 kg) pode deslocar,
Questão 01 Em uma cena de um filme, um indivíduo corre carregando uma maleta tipo 007 (volume 20 dm³) cheia de barras de um certo metal. Considerando que um adulto de peso médio (70 kg) pode deslocar,
É o cálculo das quantidades de reagentes e/ou produtos das reações químicas.
 Estequiometria Introdução Estequiometria É derivada da palavra grega STOICHEON (elemento) e METRON (medida) significa medida dos elementos químicos", ou ainda medir algo que não pode ser dividido. É o
Estequiometria Introdução Estequiometria É derivada da palavra grega STOICHEON (elemento) e METRON (medida) significa medida dos elementos químicos", ou ainda medir algo que não pode ser dividido. É o
Aula 01 QUÍMICA GERAL
 Aula 01 QUÍMICA GERAL 1 Natureza da matéria Tales de Mileto (624-548 a. C.) Tudo é água Anaxímenes de Mileto (585-528 a. C.) Tudo provém do ar e retorna ao ar Empédocle (484-424 a. C.) As quatro raízes,
Aula 01 QUÍMICA GERAL 1 Natureza da matéria Tales de Mileto (624-548 a. C.) Tudo é água Anaxímenes de Mileto (585-528 a. C.) Tudo provém do ar e retorna ao ar Empédocle (484-424 a. C.) As quatro raízes,
CIÊNCIAS PROVA 1º BIMESTRE 9º ANO PROJETO CIENTISTAS DO AMANHÃ
 PREFEITURA DA CIDADE DO RIO DE JANEIRO SECRETARIA MUNICIPAL DE EDUCAÇÃO SUBSECRETARIA DE ENSINO COORDENADORIA DE EDUCAÇÃO CIÊNCIAS PROVA 1º BIMESTRE 9º ANO PROJETO CIENTISTAS DO AMANHÃ Prova elaborada
PREFEITURA DA CIDADE DO RIO DE JANEIRO SECRETARIA MUNICIPAL DE EDUCAÇÃO SUBSECRETARIA DE ENSINO COORDENADORIA DE EDUCAÇÃO CIÊNCIAS PROVA 1º BIMESTRE 9º ANO PROJETO CIENTISTAS DO AMANHÃ Prova elaborada
Aulas: 1, 2 e 3. 4. Qual será a massa de uma amostra de 150 ml de urina, sabendo-se que sua densidade é 1,085 g.ml -1?
 Lista de Exercícios Professor: Igor Saburo Suga Serie: Nome: Aulas: 1, 2 e 3 Ano: n⁰ 1. Transforme as massas em gramas: a) 0,20 kg; b) 200 mg; c) 1x10-3 kg; d)5,0 x 10 2 mg 2. Transforme os volumes em
Lista de Exercícios Professor: Igor Saburo Suga Serie: Nome: Aulas: 1, 2 e 3 Ano: n⁰ 1. Transforme as massas em gramas: a) 0,20 kg; b) 200 mg; c) 1x10-3 kg; d)5,0 x 10 2 mg 2. Transforme os volumes em
Aula 5_ Cursinho TRIU - 08_04_2013-Profa: Luciana Assis Terra. Tópicos: MÉTODOS DE SEPARAÇÃO DE MISTURAS_2
 Aula 5_ Cursinho TRIU - 08_04_2013-Profa: Luciana Assis Terra Tópicos: MÉTODOS DE SEPARAÇÃO DE MISTURAS_2 Continuação de Métodos de Separação de Misturas Heterogênea Sedimentação ou decantação é o processo
Aula 5_ Cursinho TRIU - 08_04_2013-Profa: Luciana Assis Terra Tópicos: MÉTODOS DE SEPARAÇÃO DE MISTURAS_2 Continuação de Métodos de Separação de Misturas Heterogênea Sedimentação ou decantação é o processo
mais vapores do vinho. É, portanto, uma mistura homogênea.
 Resolução das atividades complementares Química p. I. Falsa. As amostras A e B contêm a mesma substância (naftalina). Essas amostras se fundem, portanto, na mesma temperatura. II. Falsa. A temperatura
Resolução das atividades complementares Química p. I. Falsa. As amostras A e B contêm a mesma substância (naftalina). Essas amostras se fundem, portanto, na mesma temperatura. II. Falsa. A temperatura
SUBSTÂNCIAS, MISTURAS E SEPARAÇÃO DE MISTURAS
 NOTAS DE AULA (QUÍMICA) SUBSTÂNCIAS, MISTURAS E SEPARAÇÃO DE MISTURAS PROFESSOR: ITALLO CEZAR 1 INTRODUÇÃO A química é a ciência da matéria e suas transformações, isto é, estuda a matéria. O conceito da
NOTAS DE AULA (QUÍMICA) SUBSTÂNCIAS, MISTURAS E SEPARAÇÃO DE MISTURAS PROFESSOR: ITALLO CEZAR 1 INTRODUÇÃO A química é a ciência da matéria e suas transformações, isto é, estuda a matéria. O conceito da
Aos materiais que a Química usa como matéria-prima podemos classificá-los como:
 Sumário Módulo inicial Unidade temática 0 A sua origem, a sua constituição e a sua composição. Classificação de misturas e classificação de substâncias. Processos físicos de separação de misturas. Unidades
Sumário Módulo inicial Unidade temática 0 A sua origem, a sua constituição e a sua composição. Classificação de misturas e classificação de substâncias. Processos físicos de separação de misturas. Unidades
Escola Básica e Secundária da Calheta. Físico-Química 7.º Ano de escolaridade
 Escola Básica e Secundária da Calheta Físico-Química 7.º Ano de escolaridade Ano letivo 2015/2016 FICHA INFORMATIVA 1 Classificação dos materiais NOME: N.º TURMA DATA DA REALIZAÇÃO: / / CLASSIFICAÇÃO DOS
Escola Básica e Secundária da Calheta Físico-Química 7.º Ano de escolaridade Ano letivo 2015/2016 FICHA INFORMATIVA 1 Classificação dos materiais NOME: N.º TURMA DATA DA REALIZAÇÃO: / / CLASSIFICAÇÃO DOS
ferro bromo brometo de ferro 40g 120g 0g 12g 0g 148g 7g 40g 0g 0g x g 37g
 01) (FCMSC-SP) A frase: Do nada, nada; em nada, nada pode transformar-se relaciona-se com as idéias de: a) Dalton. b) Proust. c) Boyle. d) Lavoisier. e) Gay-Lussac. 02) Acerca de uma reação química, considere
01) (FCMSC-SP) A frase: Do nada, nada; em nada, nada pode transformar-se relaciona-se com as idéias de: a) Dalton. b) Proust. c) Boyle. d) Lavoisier. e) Gay-Lussac. 02) Acerca de uma reação química, considere
PROPRIEDADES COLIGATIVAS PARTE 2
 PROPRIEDADES COLIGATIVAS PARTE 2 1. (Adaptado) Tendo em vista o momento em que um líquido se encontra em equilíbrio com seu vapor, leia atentamente as afirmativas abaixo: I. A evaporação e a condensação
PROPRIEDADES COLIGATIVAS PARTE 2 1. (Adaptado) Tendo em vista o momento em que um líquido se encontra em equilíbrio com seu vapor, leia atentamente as afirmativas abaixo: I. A evaporação e a condensação
PROCESSOS DE SEPARAÇÃO. Prof FERENC
 PROCESSOS DE SEPARAÇÃO Prof FERENC SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido nas quais um
PROCESSOS DE SEPARAÇÃO Prof FERENC SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido nas quais um
HIPÓTESE ATÔMICA. SENHA: emat BC0102: ESTRUTURA DA MATÉRIA. André Sarto Polo.
 BC0102: ESTRUTURA DA MATÉRIA HIPÓTESE ATÔMICA Crédito: Sprace André Sarto Polo [email protected] http://sqbf.ufabc.edu.br/disciplinas/bc0102.php SENHA: emat Estados da matéria 2 http://www.cave.com.br/cave2009/images/conteudo/quintoestado.gif
BC0102: ESTRUTURA DA MATÉRIA HIPÓTESE ATÔMICA Crédito: Sprace André Sarto Polo [email protected] http://sqbf.ufabc.edu.br/disciplinas/bc0102.php SENHA: emat Estados da matéria 2 http://www.cave.com.br/cave2009/images/conteudo/quintoestado.gif
QUÍMICA TAISSA LUKJANENKO
 QUÍMICA TAISSA LUKJANENKO SUBSTÂNCIA PURA MISTURA ESTUDO DAS SUBSTÂNCIAS E MISTURAS SUBSTÂNCIA: material formado por moléculas quimicamente iguais. Substância simples: é constituída de uma molécula formada
QUÍMICA TAISSA LUKJANENKO SUBSTÂNCIA PURA MISTURA ESTUDO DAS SUBSTÂNCIAS E MISTURAS SUBSTÂNCIA: material formado por moléculas quimicamente iguais. Substância simples: é constituída de uma molécula formada
Faculdade Pitágoras de Londrina Disciplina: Química Geral Prof. Me. Thiago Orcelli. Aluno:
 1 Faculdade Pitágoras de Londrina Disciplina:. Aluno: Turma: Exercícios de Fixação englobando conteúdos das Aulas 1-4. Orientação: Escolha um livro de Química Geral disponível na biblioteca e resolva os
1 Faculdade Pitágoras de Londrina Disciplina:. Aluno: Turma: Exercícios de Fixação englobando conteúdos das Aulas 1-4. Orientação: Escolha um livro de Química Geral disponível na biblioteca e resolva os
1ª série / EM. a) HSe e HS. d) H2Se e H2S. c) HSe e H2S. e) H3Se e H3S
 SECRETARIA DE SEGURANÇA PÚBLICA/SECRETARIA DE EDUCAÇÃO POLÍCIA MILITAR DO ESTADO DE GOIÁS COMANDO DE ENSINO POLICIAL MILITAR COLÉGIO DA POLÍCIA MILITAR NADER ALVES DOS SANTOS SÉRIE/ANO: 1ª TURMA(S): DISCIPLINA:
SECRETARIA DE SEGURANÇA PÚBLICA/SECRETARIA DE EDUCAÇÃO POLÍCIA MILITAR DO ESTADO DE GOIÁS COMANDO DE ENSINO POLICIAL MILITAR COLÉGIO DA POLÍCIA MILITAR NADER ALVES DOS SANTOS SÉRIE/ANO: 1ª TURMA(S): DISCIPLINA:
b) Qual é a confusão cometida pelo estudante em sua reflexão?
 1º B EM Química A Lailson Aval. Trimestral 28/03/11 1. Qual o estado físico (sólido, líquido ou gasoso) das substâncias da tabela a seguir, quando as mesmas se encontram no Deserto da Arábia, à temperatura
1º B EM Química A Lailson Aval. Trimestral 28/03/11 1. Qual o estado físico (sólido, líquido ou gasoso) das substâncias da tabela a seguir, quando as mesmas se encontram no Deserto da Arábia, à temperatura
8ª série / 9º ano U. E. 13
 8ª série / 9º ano U. E. 13 Introdução ao estudo da química A ciência é formada por um conjunto de disciplinas que se relacionam entre si. A química faz parte desse conjunto e é responsável por estudar
8ª série / 9º ano U. E. 13 Introdução ao estudo da química A ciência é formada por um conjunto de disciplinas que se relacionam entre si. A química faz parte desse conjunto e é responsável por estudar
INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA II
 INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA II ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os materiais
INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA II ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os materiais
Concurso de Seleção 2004 NÚMERO DE INSCRIÇÃO - QUÍMICA
 QUÍMICA QUESTÃO 21 Muitas pessoas já ouviram falar de gás hilariante. Mas será que ele é realmente capaz de provocar o riso? Na verdade, essa substância, o óxido nitroso (N 2 O), descoberta há quase 230
QUÍMICA QUESTÃO 21 Muitas pessoas já ouviram falar de gás hilariante. Mas será que ele é realmente capaz de provocar o riso? Na verdade, essa substância, o óxido nitroso (N 2 O), descoberta há quase 230
ROTEIRO DE ESTUDOS 2015 Disciplina: Ciências Ano: 9º ano Ensino: FII Nome: Atividade Regulação do 3º Bimestre Ciências
 ROTEIRO DE ESTUDOS 2015 Disciplina: Ciências Ano: 9º ano Ensino: FII Nome: Refazer as avaliações; Refazer as listas de exercícios; Refazer exercícios do caderno. Entregar a atividade abaixo no dia da avaliação
ROTEIRO DE ESTUDOS 2015 Disciplina: Ciências Ano: 9º ano Ensino: FII Nome: Refazer as avaliações; Refazer as listas de exercícios; Refazer exercícios do caderno. Entregar a atividade abaixo no dia da avaliação
MASSA ATÔMICA, MOLECULAR, MOLAR, NÚMERO DE AVOGADRO E VOLUME MOLAR.
 MASSA ATÔMICA, MOLECULAR, MOLAR, NÚMERO DE AVOGADRO E VOLUME MOLAR. UNIDADE DE MASSA ATÔMICA Em 1961, na Conferência da União Internacional de Química Pura e Aplicada estabeleceu-se: DEFINIÇÃO DE MASSA
MASSA ATÔMICA, MOLECULAR, MOLAR, NÚMERO DE AVOGADRO E VOLUME MOLAR. UNIDADE DE MASSA ATÔMICA Em 1961, na Conferência da União Internacional de Química Pura e Aplicada estabeleceu-se: DEFINIÇÃO DE MASSA
DIAGRAMA DE FASES Clique para editar o estilo do título mestre
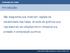 Introdução São diagramas que mostram regiões de estabilidade das fases, através de gráficos que representam as relações entre temperatura, pressão e composição química. Para que serve: Investigar reações
Introdução São diagramas que mostram regiões de estabilidade das fases, através de gráficos que representam as relações entre temperatura, pressão e composição química. Para que serve: Investigar reações
Experiência 07: Preparo de Solução a partir de Substâncias sólidas, Liquidas e de Solução Concentrada
 1 Experiência 07: Preparo de Solução a partir de Substâncias sólidas, Liquidas e de Solução Concentrada 1. Questões de estudo - Como preparar uma solução aquosa de NaOH 0,1 M? - Como preparar uma solução
1 Experiência 07: Preparo de Solução a partir de Substâncias sólidas, Liquidas e de Solução Concentrada 1. Questões de estudo - Como preparar uma solução aquosa de NaOH 0,1 M? - Como preparar uma solução
GERAL I. Fonte de consultas: http://dequi.eel.usp.br/domingos. Email: [email protected]. Telefone: 3159-5142
 QUÍMICA GERAL I Fonte de consultas: http://dequi.eel.usp.br/domingos Email: [email protected] Telefone: 3159-5142 QUÍMICA GERAL I Unidade 1 Princípios Elementares em Química O estudo da química
QUÍMICA GERAL I Fonte de consultas: http://dequi.eel.usp.br/domingos Email: [email protected] Telefone: 3159-5142 QUÍMICA GERAL I Unidade 1 Princípios Elementares em Química O estudo da química
c B = 25 g/l m soluto = 200 g V solução = 2,5 L ; V esfera = πr 3 F I C H A N. o 2 T E R R A E M T R A N S F O R M A Ç Ã O
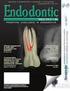 F I C H A N. o 2 T E R R A E M T R A N S F O R M A Ç Ã O Nome N. o Turma Data / / Prof. Enc. de educação 01. Considera duas soluções aquosas de sulfato de cobre, ambas de cor azul. Solução A m soluto =
F I C H A N. o 2 T E R R A E M T R A N S F O R M A Ç Ã O Nome N. o Turma Data / / Prof. Enc. de educação 01. Considera duas soluções aquosas de sulfato de cobre, ambas de cor azul. Solução A m soluto =
Lista de Exercícios Estequiometria
 Lista de Exercícios Estequiometria Átomos e Mols de Átomos Fonte: Química Geral, Vol. 1 John B. Russel 1. Calcule a massa atômica do elemento X, dado que 2,02 x l0 6 átomos de X têm uma massa de 1,70 x
Lista de Exercícios Estequiometria Átomos e Mols de Átomos Fonte: Química Geral, Vol. 1 John B. Russel 1. Calcule a massa atômica do elemento X, dado que 2,02 x l0 6 átomos de X têm uma massa de 1,70 x
Colégio Saint Exupéry
 Colégio Saint Exupéry Apostila QUÍMICA No nosso dia-a-dia o ato de classificar as coisas é algo corriqueiro. Em um faqueiro colocamos em um mesmo espaço as facas, em outro os garfos, etc. Agrupar coisas
Colégio Saint Exupéry Apostila QUÍMICA No nosso dia-a-dia o ato de classificar as coisas é algo corriqueiro. Em um faqueiro colocamos em um mesmo espaço as facas, em outro os garfos, etc. Agrupar coisas
ESCOLA SECUNDÁRIA DE CASQUILHOS
 ESCOLA SECUNDÁRIA DE CASQUILHOS.º teste sumativo de FQA 7. OUTUBRO. 204 Versão 0.º Ano Turma A Professor: Maria do Anjo Albuquerque Duração da prova: 90 minutos. Este teste é constituído por 7 páginas
ESCOLA SECUNDÁRIA DE CASQUILHOS.º teste sumativo de FQA 7. OUTUBRO. 204 Versão 0.º Ano Turma A Professor: Maria do Anjo Albuquerque Duração da prova: 90 minutos. Este teste é constituído por 7 páginas
Química Inorgânica Aula 3
 Química Inorgânica Aula 3 Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira LIGAÇÕES QUÍMICAS O que são Ligações Químicas? São as ligações que se estabelecem entre a união de dois átomos.
Química Inorgânica Aula 3 Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira LIGAÇÕES QUÍMICAS O que são Ligações Químicas? São as ligações que se estabelecem entre a união de dois átomos.
LIGAÇÕES QUÍMICAS Folha 04 João Roberto Mazzei
 01. Assinale a fórmula de Lewis da molécula HCN. a) H x C xn b) H x C x N c) H x C x N x d) H x C x x N e) Hx C x xn 0. Assinale a alternativa que apresenta, ao mesmo tempo, ligações covalentes e iônicas.
01. Assinale a fórmula de Lewis da molécula HCN. a) H x C xn b) H x C x N c) H x C x N x d) H x C x x N e) Hx C x xn 0. Assinale a alternativa que apresenta, ao mesmo tempo, ligações covalentes e iônicas.
Educação para toda a vida
 LIGAÇÕES IÔNICAS E COVALENTES Noções sobre Ligações Químicas Regra do Octeto Ligação Iônica ou Eletrovalente Ligação Covalente ou Molecular Ligação Metálica Teoria do Octeto Todos os elementos buscam formas
LIGAÇÕES IÔNICAS E COVALENTES Noções sobre Ligações Químicas Regra do Octeto Ligação Iônica ou Eletrovalente Ligação Covalente ou Molecular Ligação Metálica Teoria do Octeto Todos os elementos buscam formas
VIII OSEQUIM Olimpíada Sergipana de Química 1ª. Etapa Modalidade A
 Bom dia aluno! Está é a prova da primeira etapa da OSEQUIM, Olimpíada Sergipana de Química 2014, modalidade A, para alunos que se encontram cursando o 1º. Ano do ensino médio em 2014. Confira se a sua
Bom dia aluno! Está é a prova da primeira etapa da OSEQUIM, Olimpíada Sergipana de Química 2014, modalidade A, para alunos que se encontram cursando o 1º. Ano do ensino médio em 2014. Confira se a sua
QUÍMICA REVISÃO 1 INTERATIVIDADE. Unidade IV. Reações químicas e cálculo estequiométrico.
 Unidade IV Reações químicas e cálculo estequiométrico. 2 Aula 16.1 Conteúdo: Revisão e avaliação da unidade IV. 3 O que é uma reação química? É uma transformação em que novas substâncias são formados a
Unidade IV Reações químicas e cálculo estequiométrico. 2 Aula 16.1 Conteúdo: Revisão e avaliação da unidade IV. 3 O que é uma reação química? É uma transformação em que novas substâncias são formados a
www.professormazzei.com PROPREDADES COLIGATIVAS Folha 03 João Roberto Mazzei
 01. (UNESP 1989) Considerar duas soluções de ácido clorídrico e outra de ácido acético (ácido etanóico), ambas 10 2 M. Pergunta-se: a) Qual das duas soluções apresenta menor temperatura de congelação?
01. (UNESP 1989) Considerar duas soluções de ácido clorídrico e outra de ácido acético (ácido etanóico), ambas 10 2 M. Pergunta-se: a) Qual das duas soluções apresenta menor temperatura de congelação?
M A S S A S E M E D I D A S
 M A S S A S E M E D I D A S PROF. AGAMENON ROBERTO < 2010 > Prof. Agamenon Roberto ATOMÍSTICA www.agamenonquimica.com 2 MASSAS E MEDIDAS UNIDADE DE MASSA ATÔMICA (u.m.a.) Para pesar ou medir algo se torna
M A S S A S E M E D I D A S PROF. AGAMENON ROBERTO < 2010 > Prof. Agamenon Roberto ATOMÍSTICA www.agamenonquimica.com 2 MASSAS E MEDIDAS UNIDADE DE MASSA ATÔMICA (u.m.a.) Para pesar ou medir algo se torna
I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2
 I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com 4
I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com 4
Aula 16 A Regra das Fases
 Aula 16 A Regra das Fases 1. Introdução Poderíamos especular se quatro fases de uma única substância poderiam estar em equilíbrio (como, por exemplo, as duas formas sólidas do estanho, o estanho líquido
Aula 16 A Regra das Fases 1. Introdução Poderíamos especular se quatro fases de uma única substância poderiam estar em equilíbrio (como, por exemplo, as duas formas sólidas do estanho, o estanho líquido
Apresentação. Química TRIU Apostila 1. Caro Aluno,
 Apresentação Caro Aluno, Nossos materiais didáticos são preparados, especialmente para você, visando o seu aprendizado e desenvolvimento na disciplina de Química, e sua aprovação nos vestibulares que irá
Apresentação Caro Aluno, Nossos materiais didáticos são preparados, especialmente para você, visando o seu aprendizado e desenvolvimento na disciplina de Química, e sua aprovação nos vestibulares que irá
Lista de Exercícios Química Geral Entropia e energia livre
 Lista de Exercícios Química Geral Entropia e energia livre 1. Se a reação A + B C tiver uma constante de equilíbrio maior do que 1, qual das seguintes indicações está correta? a) A reação não é espontânea.
Lista de Exercícios Química Geral Entropia e energia livre 1. Se a reação A + B C tiver uma constante de equilíbrio maior do que 1, qual das seguintes indicações está correta? a) A reação não é espontânea.
1
 Níveis de dificuldade das Questões Fácil Pontifícia Universidade Católica do Rio Grande do Sul Médio Difícil Resolução da Prova de Química Vestibular Verão PUCRS 2005 Prof. Emiliano Chemello www.quimica.net/emiliano
Níveis de dificuldade das Questões Fácil Pontifícia Universidade Católica do Rio Grande do Sul Médio Difícil Resolução da Prova de Química Vestibular Verão PUCRS 2005 Prof. Emiliano Chemello www.quimica.net/emiliano
CONDIÇÃO: Sólidos que facilmente são separados à mão ou com a ajuda de um. CONDIÇÃO: Sólidos com densidades diferentes, em que um deles facilmente é
 TEMA B TERRA EM TRANSFORMAÇÃO B1 MATERIAIS 1.1 Constituição do mundo material 1.2 Substâncias e misturas de substâncias 1.3 Soluções 1.4 Transformações dos materiais 1.5 Propriedades físicas e químicas
TEMA B TERRA EM TRANSFORMAÇÃO B1 MATERIAIS 1.1 Constituição do mundo material 1.2 Substâncias e misturas de substâncias 1.3 Soluções 1.4 Transformações dos materiais 1.5 Propriedades físicas e químicas
TERMOQUÍMICA EXERCÍCIOS ESSENCIAIS 1. O CALOR E OS PROCESSOS QUÍMICOS
 TERMOQUÍMICA EXERCÍCIOS ESSENCIAIS 1. O CALOR E OS PROCESSOS QUÍMICOS Termoquímica: Estudo das quantidades de energia, na forma de calor, liberada ou absorvida durante os processos de interesse da Química,
TERMOQUÍMICA EXERCÍCIOS ESSENCIAIS 1. O CALOR E OS PROCESSOS QUÍMICOS Termoquímica: Estudo das quantidades de energia, na forma de calor, liberada ou absorvida durante os processos de interesse da Química,
II OLimpíada Brasileira de Química Júnior - Fase II
 II OLimpíada Brasileira de Química Júnior - Fase II 17/10/2009 - II OBQjr 2009 INSTRUÇÕES: II Olimpíada Brasileira de Química Júnior Exames - Fase II 1. A prova consta de 25 questões, cada uma contém quatro
II OLimpíada Brasileira de Química Júnior - Fase II 17/10/2009 - II OBQjr 2009 INSTRUÇÕES: II Olimpíada Brasileira de Química Júnior Exames - Fase II 1. A prova consta de 25 questões, cada uma contém quatro
www.professormazzei.com Estequiometria Folha 03 Prof.: João Roberto Mazzei
 01. (CFTCE 2007) Dada a reação de neutralização: HCl + NaOH NaCl + H 2O, a massa de NaCl, produzida a partir de 80 g de hidróxido de sódio (NaOH), é: a) 58,5 g b) 40 g c) 117 g d) 80 g e) 120 g 02. (CFTCE
01. (CFTCE 2007) Dada a reação de neutralização: HCl + NaOH NaCl + H 2O, a massa de NaCl, produzida a partir de 80 g de hidróxido de sódio (NaOH), é: a) 58,5 g b) 40 g c) 117 g d) 80 g e) 120 g 02. (CFTCE
Química B Extensivo V. 2
 Química B Extensivo V. 2 Exercícios Sistema Componentes Fases Classificação Água + gelo 1 2 Heterogêneo Água + 3 cubos de gelo 1 2 Heterogêneo Açúcar + sal 2 2 Heterogêneo Areia + enxofre + sal 3 3 Heterogêneo
Química B Extensivo V. 2 Exercícios Sistema Componentes Fases Classificação Água + gelo 1 2 Heterogêneo Água + 3 cubos de gelo 1 2 Heterogêneo Açúcar + sal 2 2 Heterogêneo Areia + enxofre + sal 3 3 Heterogêneo
DETERMINAÇÃO DA MASSA VOLÚMICA DE UM SÓLIDO
 Escola Básica dos 2º e 3º Ciclos de Santo António Ciências Físico-Químicas 2009/2010 DETERMINAÇÃO DA MASSA VOLÚMICA DE UM SÓLIDO Trabalho realizado por: Ano: Nº T: Índice Introdução 3 Objectivos.4 Material/
Escola Básica dos 2º e 3º Ciclos de Santo António Ciências Físico-Químicas 2009/2010 DETERMINAÇÃO DA MASSA VOLÚMICA DE UM SÓLIDO Trabalho realizado por: Ano: Nº T: Índice Introdução 3 Objectivos.4 Material/
DIAGRAMAS DE EQUILÍBRIO
 DIAGRAMAS DE EQUILÍBRIO Diagramas de equilíbrio 1 DIAGRAMA EUTÉTICO Exemplo 1: Cobre - Prata (Cu-Ag) Principais características: 3 regiões monofásicas (α, β e L) 3 regiões bifásicas (α+l, α+β, L+β) Fase
DIAGRAMAS DE EQUILÍBRIO Diagramas de equilíbrio 1 DIAGRAMA EUTÉTICO Exemplo 1: Cobre - Prata (Cu-Ag) Principais características: 3 regiões monofásicas (α, β e L) 3 regiões bifásicas (α+l, α+β, L+β) Fase
Universidade Federal do Acre Coordenação de Ciências Agrárias PET-Agronomia
 Universidade Federal do Acre Coordenação de Ciências Agrárias PET-Agronomia Renato Bolsistas: Renato Renato(7ºPeríodo-Florestal) Tutor: Prof. Dr. José Ribamar Rio Branco, Acre 2006 1 As leis ponderais
Universidade Federal do Acre Coordenação de Ciências Agrárias PET-Agronomia Renato Bolsistas: Renato Renato(7ºPeríodo-Florestal) Tutor: Prof. Dr. José Ribamar Rio Branco, Acre 2006 1 As leis ponderais
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 01 TURMA ANUAL. 05. Item A
 RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS 01. Item B AULA 01 TURMA ANUAL I Correto. Ao passar para um nível mais interno o elétron emite energia na forma de luz. II Falso. Rutherford não propôs um átomo maciço,
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS 01. Item B AULA 01 TURMA ANUAL I Correto. Ao passar para um nível mais interno o elétron emite energia na forma de luz. II Falso. Rutherford não propôs um átomo maciço,
INTRODUÇÃO. Na antiguidade, as substâncias encontradas na natureza eram divididas em três grandes reinos: O vegetal, o animal e o mineral.
 A QUÍMICA ORGÂNICA INTRODUÇÃO Na antiguidade, as substâncias encontradas na natureza eram divididas em três grandes reinos: O vegetal, o animal e o mineral. INTRODUÇÃO A química orgânica começou estudando
A QUÍMICA ORGÂNICA INTRODUÇÃO Na antiguidade, as substâncias encontradas na natureza eram divididas em três grandes reinos: O vegetal, o animal e o mineral. INTRODUÇÃO A química orgânica começou estudando
Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente.
 SOLUÇÕES Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente. Fase: numa mistura, é cada uma das porções que apresenta aspecto homogéneo ou uniforme. CLASSIFICAÇÃO
SOLUÇÕES Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente. Fase: numa mistura, é cada uma das porções que apresenta aspecto homogéneo ou uniforme. CLASSIFICAÇÃO
ENERGIA TÉRMICA: A Energia Térmica de um corpo é a energia cinética de suas moléculas e corresponde à sua temperatura.
 CALOR 1 ENERGIA: É a capacidade de se realizar um trabalho. Ela se apresenta sob várias formas: cinética (de movimento), gravitacional, elástica (de molas), elétrica, térmica, radiante e outras. Mede-se
CALOR 1 ENERGIA: É a capacidade de se realizar um trabalho. Ela se apresenta sob várias formas: cinética (de movimento), gravitacional, elástica (de molas), elétrica, térmica, radiante e outras. Mede-se
POTENCIAL DE PRODUÇÃO DE PLANTAS FORRAGEIRAS. Maria Aparecida Salles Franco Curso de Veterinária Disciplina: Forragicultura e Plantas Tóxicas
 POTENCIAL DE PRODUÇÃO DE PLANTAS FORRAGEIRAS Maria Aparecida Salles Franco Curso de Veterinária Disciplina: Forragicultura e Plantas Tóxicas Um pouco sobre nutrientes nos alimentos Do ano de 1917 para
POTENCIAL DE PRODUÇÃO DE PLANTAS FORRAGEIRAS Maria Aparecida Salles Franco Curso de Veterinária Disciplina: Forragicultura e Plantas Tóxicas Um pouco sobre nutrientes nos alimentos Do ano de 1917 para
II Correto. Quanto maior a distância entre as cargas, mais fraca é a ligação e menos energia é empregada na sua quebra.
 01. Item B I Correto. A energia para quebrar a ligação H (568 kj/mol) é a maior da tabela. Isto torna mais difícil a sua quebra, portanto ionizando menos o ácido que passa a ser o mais fraco entre os listados.
01. Item B I Correto. A energia para quebrar a ligação H (568 kj/mol) é a maior da tabela. Isto torna mais difícil a sua quebra, portanto ionizando menos o ácido que passa a ser o mais fraco entre os listados.
Propriedades térmicas em Materiais
 FACULDADE SUDOESTE PAULISTA Ciência e Tecnologia de Materiais Prof. Msc. Patrícia Correa Propriedades térmicas em Materiais Noções importantes para entendermos os mecanismos de transporte através dos materiais
FACULDADE SUDOESTE PAULISTA Ciência e Tecnologia de Materiais Prof. Msc. Patrícia Correa Propriedades térmicas em Materiais Noções importantes para entendermos os mecanismos de transporte através dos materiais
Concentrações. Flavia de Almeida Vieira Tatiana Dillenburg Saint Pierre
 Flavia de Almeida Vieira Tatiana Dillenburg Saint Pierre Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
Flavia de Almeida Vieira Tatiana Dillenburg Saint Pierre Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
SUBSTÂNCIA PURA & MISTURAS
 SUBSTÂNCIA PURA & MISTURAS Química Professora: Danielle Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Sistemas Materiais Substância Pura Mistura Simples Composta Homogênea Heterogênea
SUBSTÂNCIA PURA & MISTURAS Química Professora: Danielle Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Sistemas Materiais Substância Pura Mistura Simples Composta Homogênea Heterogênea
Curso Técnico em Manutenção em Educação de Jovens e Adultos. Aprendiz: Química Geral. Prof. Maurício Façanha
 Curso Técnico em Manutenção em Educação de Jovens e Adultos. Aprendiz: Química Geral. Prof. Maurício Façanha PROPRIEDADES DA MATÉRIA, SUBSTÂNCIA E MISTURAS Eu li em algum lugar que o amor é uma questão
Curso Técnico em Manutenção em Educação de Jovens e Adultos. Aprendiz: Química Geral. Prof. Maurício Façanha PROPRIEDADES DA MATÉRIA, SUBSTÂNCIA E MISTURAS Eu li em algum lugar que o amor é uma questão
www.professormazzei.com FUNÇÕES INORGÂNICAS Folha 02 João Roberto Fortes Mazzei
 01. Durante um experimento, seu professor de química pediu que você identificasse as soluções aquosas presentes em cada um dos béqueres (A, B, C) apresentados na figura a seguir. Dois béqueres do experimento
01. Durante um experimento, seu professor de química pediu que você identificasse as soluções aquosas presentes em cada um dos béqueres (A, B, C) apresentados na figura a seguir. Dois béqueres do experimento
www.professormazzei.com Assunto: Eletroquímica Folha 4.2 Prof.: João Roberto Mazzei
 www.professormazzei.com Assunto: Eletroquímica Folha 4.2 Prof.: João Roberto Mazzei 01. (UDESC 2009) O hidrogênio tem sido proposto como o combustível "ecológico", já que a sua reação de combustão com
www.professormazzei.com Assunto: Eletroquímica Folha 4.2 Prof.: João Roberto Mazzei 01. (UDESC 2009) O hidrogênio tem sido proposto como o combustível "ecológico", já que a sua reação de combustão com
OLIMPÍADA PIAUIENSE DE QUÍMICA - 2014 Modalidade EF
 OLIMPÍADA PIAUIENSE DE QUÍMICA - 2014 Modalidade EF INSTRUÇÕES 1 Esta prova contém oito questões no total, sendo duas questões abertas e seis questões de múltipla escolha. 2 Antes de iniciar a prova, confira
OLIMPÍADA PIAUIENSE DE QUÍMICA - 2014 Modalidade EF INSTRUÇÕES 1 Esta prova contém oito questões no total, sendo duas questões abertas e seis questões de múltipla escolha. 2 Antes de iniciar a prova, confira
Cálculo Químico ESTEQUIOMETRIA
 Cálculo Químico ESTEQUIOMETRIA Profº André Montillo www.montillo.com.br Definição: É o estudo da quantidade de reagentes e produtos em uma reação química, portanto é uma análise quantitativa de um fenômeno
Cálculo Químico ESTEQUIOMETRIA Profº André Montillo www.montillo.com.br Definição: É o estudo da quantidade de reagentes e produtos em uma reação química, portanto é uma análise quantitativa de um fenômeno
www.professormazzei.com LIGAÇÕES QUÍMICAS Folha 03 João Roberto Mazzei
 01. (UNICAMP 1994) Considere três substâncias CH 4, NH 3 e H 2O e três temperaturas de ebulição: 373K, 112K e 240K. Levando-se em conta a estrutura e a polaridade das moléculas destas substâncias, pede-se:
01. (UNICAMP 1994) Considere três substâncias CH 4, NH 3 e H 2O e três temperaturas de ebulição: 373K, 112K e 240K. Levando-se em conta a estrutura e a polaridade das moléculas destas substâncias, pede-se:
Escola Secundária de Casquilhos Teste 1 de Física e Química A 10º ANO 22/10/2013 90 minutos
 Escola Secundária de Casquilhos Teste 1 de Física e Química A 10º ANO 22/10/2013 90 minutos NOME Nº Turma Informação Professor Enc. de Educação 1. Os átomos dos isótopos e do carbono têm (A) números atómicos
Escola Secundária de Casquilhos Teste 1 de Física e Química A 10º ANO 22/10/2013 90 minutos NOME Nº Turma Informação Professor Enc. de Educação 1. Os átomos dos isótopos e do carbono têm (A) números atómicos
1. (G1 - ifsul 2016) Para o processo de purificação da água, são adicionadas substâncias como sulfato de alumínio, A 2(SO 4) 3,
 1. (G1 - ifsul 2016) Para o processo de purificação da água, são adicionadas substâncias como sulfato de alumínio, A 2(SO 4) 3, para formação de flocos com a sujeira da água; cloro, C 2, para desinfecção;
1. (G1 - ifsul 2016) Para o processo de purificação da água, são adicionadas substâncias como sulfato de alumínio, A 2(SO 4) 3, para formação de flocos com a sujeira da água; cloro, C 2, para desinfecção;
1 2 3 4 5 6 Total. Nota: Apresente todos os cálculos que efectuar
 12 de Março 2011 (Semifinal) Pergunta 1 2 3 4 5 6 Total Classificação Escola:. Nome:. Nome:. Nome:. Nota: Apresente todos os cálculos que efectuar Dados: Questão 1 Constante de Avogadro: N A = 6,022 x
12 de Março 2011 (Semifinal) Pergunta 1 2 3 4 5 6 Total Classificação Escola:. Nome:. Nome:. Nome:. Nota: Apresente todos os cálculos que efectuar Dados: Questão 1 Constante de Avogadro: N A = 6,022 x
CURSO APOIO QUÍMICA RESOLUÇÃO
 QUÍMICA CURSO APOIO 15. O sulfato de sódio é um composto utilizado na indústria de celulose e na fabricação de detergentes. Por apresentar grande afinidade por água, pode ser encontrado na forma de um
QUÍMICA CURSO APOIO 15. O sulfato de sódio é um composto utilizado na indústria de celulose e na fabricação de detergentes. Por apresentar grande afinidade por água, pode ser encontrado na forma de um
A transferência de calor ocorre até o instante em que os corpos atingem a mesma temperatura (equilíbrio térmico).
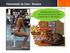 REVISÃO ENEM Calorimetria CONCEITO FÍSICO DE CALOR Calor é a energia transferida de um corpo a outro, devido à desigualdade de temperaturas existente entre eles. Essa transferência sempre ocorre do corpo
REVISÃO ENEM Calorimetria CONCEITO FÍSICO DE CALOR Calor é a energia transferida de um corpo a outro, devido à desigualdade de temperaturas existente entre eles. Essa transferência sempre ocorre do corpo
FÍSICO-QUÍMICA TERMOQUÍMICA Aula 1
 FÍSICO-QUÍMICA TERMOQUÍMICA Aula 1 A termoquímica é parte da termodinâmica e corresponde ao segmento da química que compreende as trocas de calor e seus efeitos nas substâncias e reações químicas. Os primeiros
FÍSICO-QUÍMICA TERMOQUÍMICA Aula 1 A termoquímica é parte da termodinâmica e corresponde ao segmento da química que compreende as trocas de calor e seus efeitos nas substâncias e reações químicas. Os primeiros
QUÍMICA. Quantos átomos de carbono e quantos átomos de hidrogênio existem em uma molécula desse composto? a) 10 e 13 b) 10 e 14 c) 9 e 12 d) 8 e 4
 QUÍMICA 1. O benzopireno é um composto aromático formado na combustão da hulha e do fumo. Pode ser encontrado em carnes grelhadas, em carvão ou peças defumadas. Experiências em animais comprovaram sua
QUÍMICA 1. O benzopireno é um composto aromático formado na combustão da hulha e do fumo. Pode ser encontrado em carnes grelhadas, em carvão ou peças defumadas. Experiências em animais comprovaram sua
Átomos. Nome Símbolo Natureza Ferro Fe Fe 3 O 4 Cálcio Ca CaCO 3 Prata Ag (Argentum) Ag Oxigênio O O 2
 SOLUÇÕES ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os materiais ou coisas que compõem o universo. A matéria é formada por moléculas, que por sua vez são formadas por partículas minúsculas
SOLUÇÕES ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os materiais ou coisas que compõem o universo. A matéria é formada por moléculas, que por sua vez são formadas por partículas minúsculas
Aula II - Tabela Periódica
 Aula II - Tabela Periódica Tutora: Marcia Mattos Pintos Rio Grande, 16 agosto de 2014. Revisão Átomo: Unidade fundamental da matéria; Partes do átomo: núcleo e eletrosfera. Carga Elétrica das partículas
Aula II - Tabela Periódica Tutora: Marcia Mattos Pintos Rio Grande, 16 agosto de 2014. Revisão Átomo: Unidade fundamental da matéria; Partes do átomo: núcleo e eletrosfera. Carga Elétrica das partículas
Do que é feita a matéria?
 Acesse: http://fuvestibuar.com.br/ Do que é feita a matéria? COMO SERÁ QUE VAMOS DIVIDIR O ÁTOMO?! O que você vai aprender O que são átomos O que são moécuas A reação entre as propriedades das substâncias
Acesse: http://fuvestibuar.com.br/ Do que é feita a matéria? COMO SERÁ QUE VAMOS DIVIDIR O ÁTOMO?! O que você vai aprender O que são átomos O que são moécuas A reação entre as propriedades das substâncias
Escola Secundária de Lagoa. Ficha de Trabalho 4. Física e Química A 11º Ano Turma A Paula Melo Silva. Revisão 10º Ano: As três miudinhas
 Escola Secundária de Lagoa Física e Química A 11º Ano Turma A Paula Melo Silva Ficha de Trabalho 4 Cálculos estequiométricos Parte Um Revisão 10º Ano: As três miudinhas Quantidade em química corresponde
Escola Secundária de Lagoa Física e Química A 11º Ano Turma A Paula Melo Silva Ficha de Trabalho 4 Cálculos estequiométricos Parte Um Revisão 10º Ano: As três miudinhas Quantidade em química corresponde
www.professormazzei.com Estrutura da Matéria Folha 03 Prof.: João Roberto Mazzei
 01- (PUCAMP 2004) O elemento carbono se apresenta em muitas formas alotrópicas. Três dessas são...x... : diamante, grafita e fulereno; outras, em maior número são...y.... Diamante, a mais rara e a mais
01- (PUCAMP 2004) O elemento carbono se apresenta em muitas formas alotrópicas. Três dessas são...x... : diamante, grafita e fulereno; outras, em maior número são...y.... Diamante, a mais rara e a mais
CURSINHO TRIU QUÍMICA FRENTE B
 CURSINHO TRIU QUÍMICA FRENTE B AULA 3 EXPRESSÕES DE CONCENTRAÇÃO (CONT.) E PROPRIEDADES COLIGATIVAS DATA: 01/09/2014 1) EXPRESSÕES DE CONCENTRAÇÃO (CONTINUAÇÃO) a. FRAÇÃO EM MOL Fração em mols ou fração
CURSINHO TRIU QUÍMICA FRENTE B AULA 3 EXPRESSÕES DE CONCENTRAÇÃO (CONT.) E PROPRIEDADES COLIGATIVAS DATA: 01/09/2014 1) EXPRESSÕES DE CONCENTRAÇÃO (CONTINUAÇÃO) a. FRAÇÃO EM MOL Fração em mols ou fração
Pode-se dizer que na molécula H Cl as eletrosferas dos átomos H e Cl são, respectivamente, iguais às eletrosferas dos átomos dos gases nobres:
 Questão 01) Um elemento químico A, de número atômico 11, um elemento químico B, de número atômico 8, e um elemento químico C, de número atômico 1, combinam-se formando o composto ABC. As ligações entre
Questão 01) Um elemento químico A, de número atômico 11, um elemento químico B, de número atômico 8, e um elemento químico C, de número atômico 1, combinam-se formando o composto ABC. As ligações entre
Verdadeiro dado que a massa dos protões e dos neutrões é muito superior à dos eletrões!
 Escola Secundária de Lagoa Física e Química A 10º Ano Turma A Paula Melo Silva Correção da Ficha de Trabalho 1 Unidade Zero Materiais: diversidade e constituição 2014/2015 1. Atualmente conhecem-se mais
Escola Secundária de Lagoa Física e Química A 10º Ano Turma A Paula Melo Silva Correção da Ficha de Trabalho 1 Unidade Zero Materiais: diversidade e constituição 2014/2015 1. Atualmente conhecem-se mais
Como os químicos se comunicam?
 Como os químicos se comunicam? A UU L AL A Símboos de eementos Fórmuas de compostos O que você vai aprender O que é átomo O que é moécua A matéria é formada de átomos Eemento químico Substância simpes
Como os químicos se comunicam? A UU L AL A Símboos de eementos Fórmuas de compostos O que você vai aprender O que é átomo O que é moécua A matéria é formada de átomos Eemento químico Substância simpes
A) 11,7 gramas B) 23,4 gramas C) 58,5 gramas D) 68,4 gramas E) 136,8 gramas
 Questão 1 Sejam dadas as seguintes soluções aquosas: I) 0,2 mol/l de cloreto de potássio (KCl) II) 0,3 mol/l de glicose (C 6 H 12 O 6 ) III) 0,1 mol/l de sacarose (C 12 H 22 O 11 ) IV) 0,2 mol/l de sulfato
Questão 1 Sejam dadas as seguintes soluções aquosas: I) 0,2 mol/l de cloreto de potássio (KCl) II) 0,3 mol/l de glicose (C 6 H 12 O 6 ) III) 0,1 mol/l de sacarose (C 12 H 22 O 11 ) IV) 0,2 mol/l de sulfato
1 Seleccionar material adequado à separação dos componentes de uma mistura heterogénea.
 ACTIVIDADE LABORATORIAL Ciências Físico-Químicas 7ºANO VOU SEPARAR OS COMPONENTES DE UMA MISTURA O que se pretende 1 Seleccionar material adequado à separação dos componentes de uma mistura heterogénea.
ACTIVIDADE LABORATORIAL Ciências Físico-Químicas 7ºANO VOU SEPARAR OS COMPONENTES DE UMA MISTURA O que se pretende 1 Seleccionar material adequado à separação dos componentes de uma mistura heterogénea.
9º ANO ENSINO FUNDAMENTAL -2015
 COLÉGIO NOSSA SENHORA DE LOURDES trimestral Disciplina: Professor (a): QUÍMICA LUIS FERNANDO Roteiro de estudos para recuperação 9º ANO ENSINO FUNDAMENTAL -2015 Conteúdo: Referência para estudo: Sites
COLÉGIO NOSSA SENHORA DE LOURDES trimestral Disciplina: Professor (a): QUÍMICA LUIS FERNANDO Roteiro de estudos para recuperação 9º ANO ENSINO FUNDAMENTAL -2015 Conteúdo: Referência para estudo: Sites
Química 1 Cecília e Regina 2ºEM/TI 2º. Química 1-2ºTI
 2º anos - 2012 Matéria Professor(a) Ano/Série Turma Data Trimestre Química 1 Cecília e Regina 2ºEM/TI 2º Aluno(a) Número Observação Química 1-2ºTI Projeto de Recuperação Paralela Atividades podem ser feitas
2º anos - 2012 Matéria Professor(a) Ano/Série Turma Data Trimestre Química 1 Cecília e Regina 2ºEM/TI 2º Aluno(a) Número Observação Química 1-2ºTI Projeto de Recuperação Paralela Atividades podem ser feitas
Maria do Anjo Albuquerque
 ispersões na atmosfera Maria do Anjo Albuquerque Atmosfera A atmosfera é uma solução gasosa de vários gases (sobretudo oxigénio, dióxido de carbono e vapor de água) dispersos em azoto (componente maioritário);
ispersões na atmosfera Maria do Anjo Albuquerque Atmosfera A atmosfera é uma solução gasosa de vários gases (sobretudo oxigénio, dióxido de carbono e vapor de água) dispersos em azoto (componente maioritário);
10- (UNESP) Nesta tabela periódica, os algarismos romanos substituem os símbolos dos elementos.
 TABELA PERIÓDICA 1- (UNITAU) Considere as seguintes afirmações: I - Quanto menor o raio do íon, maior será sua quantidade de elétrons quando comparado com seu átomo. II - O potencial de ionização aumenta
TABELA PERIÓDICA 1- (UNITAU) Considere as seguintes afirmações: I - Quanto menor o raio do íon, maior será sua quantidade de elétrons quando comparado com seu átomo. II - O potencial de ionização aumenta
QUÍMICA PARA CEFET-MG - APOSTILA DE EXERCÍCIOS
 QUÍMICA PARA CEFET-MG - APOSTILA DE EXERCÍCIOS Organização: Prof. Eduardo Chaves (Engenheiro Cívil e Matemático formado pela UFMG) Prof. Thiago Silva (Biologo Formado no Centro Universitário Metodista
QUÍMICA PARA CEFET-MG - APOSTILA DE EXERCÍCIOS Organização: Prof. Eduardo Chaves (Engenheiro Cívil e Matemático formado pela UFMG) Prof. Thiago Silva (Biologo Formado no Centro Universitário Metodista
