Aula Teórico-Prática Nº1
|
|
|
- João Lucas Pinto Pacheco
- 10 Há anos
- Visualizações:
Transcrição
1 Aula Teórico-Prática Nº1 Sumário Introdução aos sistemas de unidades: SI e cgs. (1) Exloração de videos e exeriências simles sobre o fenómeno de difusão. (2) Discussão orientada sobre a 1ª lei de Fick e resolução de exercícios sobre o tema. (3) 1- Sistemas de unidades: SI e cgs o nosso conhecimento só é satisfatório quando odemos exressá-lo or meio de números (Lord Kevin ) Sistema MRS Metro, Kilo, Segundo Sistema Internacional Sistema cgs centímetro, grama, segundo Sistema cgs Dimensão Unidades S.I. Unidades cgs Comrimento metro Centímetro Massa kilograma Grama Força newton Dine Pressão N/m 2 dine/cm 2 Energia Joule Erg Quantidade de matéria mol mol Conversões F = m x a 1N = 1Kg x 1m/s g x 100cm/s 2 1N = 10 5 dyn Múltilos Quilo K Mega M Giga G Submúltilos mili m micro µ nano n
2 2 - Exloração de videos e exeriências simles sobre o fenómeno de difusão 3 - Transorte de Massa Diferentes rocessos biológicos vitais deendem de trocas de matéria Ex. Alvéolos ulmonares Trocas de fluidos e moléculas ocorrem constantemente através de membranas celulares, aredes vasculares e das fronteiras dos órgãos. Processos de transferência de matéria (dentro de um sistema ou entre sistemas) Quando temos uma única fase os rinciais mecanismos associados ao transorte são: convecção e difusão Solvente em contacto com um soluto, sendo este, or exemlo constituído or moléculas neutras Convecção Transorte de moléculas or uma corrente de arrastamento Ex. Transorte de nutrientes ela corrente sanguínea (moléculas de um soluto arrastadas ela corrente de água através de uma membrana. Difusão Movimento de moléculas de um local ara o outro or movimento estatístico de agitação térmica, or movimentos moleculares ao acaso Desaarecimento dos gradientes de concentração Este movimento a que as moléculas estão sujeitas deende da temeratura Quanto maior a temeratura mais intenso é o deslocamento molecular As moléculas colidem altera a direcção do movimento molecular Estes movimentos devidos à difusão são normalmente idênticos à roagação do calor num condutor Leis de Fick da Difusão 2
3 Regime Estacionário Movimentos de soluto só devidos à difusão Não há movimentos de solvente Densidade de Corrente de Moléculas - Quantidade de moléculas que atravessa uma unidade de área de um lado ara o outro or unidade de temo, considerada erendicular à velocidade de deslocamento das moléculas (Js) mol cm -2 s -1 Conservação da massa A densidade de corrente do soluto à entrada da membrana é igual à saída Constante Constante 3
4 Membranas Homogéneas A concentração do soluto no interior da membrana é graficamente uma recta y = ax + b mol cm -4 Concentrações desconhecidas É ossível saberem-se as concentrações a artir das concentrações conhecidas dos reciientes I e II através dos coeficientes de artição (K) C s (0) = K C s I C s ( x) = K C s II Permeabilidade (P) As constantes que caracterizam uma membrana relativamente ao soluto definem a maior ou menor facilidade com que o soluto a atravessa. cm s -1 Js = Is A Intensidade de Corrente (Is) Quantidade de moléculas que atravessam de um lado ara outro 4 or unidade de temo. mol s -1
5 Aula Teórico-Prática Nº2 Sumário Transorte de massa através de membranas homogéneas e orosas. Resolução de exercícios. Membranas Porosas Os oros têm eixos normais à arede da membrana oro é um cilindro cuja geratriz é a esessura da membrana Os movimentos das moléculas só se fazem através dos oros Difusão Livre através dos oros As concentrações do soluto na interface da membrana são iguais às concentrações das soluções dos reciientes I e II I M II x No entanto o que se retende é a densidade de corrente de soluto através da membrana orosa, e não através dos oros. Assim tem que ser considerada a fracção de área ermeável - Φ w Área média ermeável or cm 2 de membrana 5
6 Adimensional STP - Suerfície Total de Poros STM - Suerfície Total de Membrana VTP - Volume Total de Poros VTM - Volume Total de Membrana Assim, a Densidade de corrente ara uma membrana orosa é igual a: Sendo que a ermeabilidade (w) é dada or: Aula Teórico-Prática Nº3 Sumário Sistemas de membranas. Resolução de exercícios. 6
7 Aula Teórico-Prática Nº4 Sumário Corrente de soluto devido ao arrastamento (1). Definição de ressão osmótica. Resolução de exercícios (2). 1 Corrente de Arrastamento de Soluto na Corrente de Água Movimentos de solutos Difusão Convecção Js = Js (difusão) + Js (arrastamento) Jw Densidade de corrente de água (moles cm -2 s -1 ) Não é a densidade de corrente de solvente que interessa mas sim o número de moléculas de soluto que são arrastadas elo solvente deduzida à custa do volume de solvente Jw x Vw volume arcial molar da água (vol em cm 3 / mol de água) Número de cm 3 que existem numa mole de água Jv Densidade de corrente de solvente exressa em volume ou seja volume total de solvente que atravessa a membrana e que arrasta artículas (cm s -1 ) Densidade de corrente de convecção No entanto ainda não é ossível ter a densidade de corrente de arrastamento deende - Concentração de soluto existente - Corrente de solvente 7
8 Js (arrastamento) = Cs x Jv Concentração média de soluto no interior da membrana Membrana Homogénea Cs = K (CsI + Cs II) 2 Membrana Porosa Cs = (CsI + Cs II) 2 No entanto nem todas as moléculas de soluto que são arrastadas atravessam a membrana odem ser reflectidas Coeficiente de reflexão de Staverman (σ) Js (arrastamento) = Cs (1-σ) Jv Reresenta a unidade menos as moléculas reflectidas Js (arrastamento) = Cs Jv - Cs Jv σ Moléculas que assam Total de moléculas arrastadas or convecção Moléculas reflectidas 8
9 Equações Gerais ara a Densidade de Corrente de Soluto Membrana Homogénea Js = P Cs + Cs Jv (1-σ) Membrana Heterogénea Js = W Cs + Cs Jv (1-σ) 2 - Definição de ressão osmótica Na densidade de corrente de difusão or vezes é mais conveniente utilizar ressões em vez de concentrações. Pela Lei de Van T Hoff (temeratura constante) Correntes de Água (consequência das ressões) - Osmótica - Hidrostática 9
10 Equilíbrio Altura da coluna líquida - A ressão hidrostática que se está a exercer sobre a solução equilibra a ressão osmótica É a ressão que é necessário exercer sobre um asolução, ara imedir a entrada de solvente Membrana semi-ermeável Membrana ermeáveis somente às moléculas de solvente Ideal absolutamente imermeável às moléculas de soluto Reais algumas moléculas de soluto (as mais equenas) conseguem atravessá-la Membrana semi-ermeável ideal 2 reciientes searados or uma membrana semiermeável ideal Cs II > Cs I Condições a imor - Membrana semi-ermeável ideal - Pressões hidrostáticas iguais nos dois reciientes 10
11 Como a concentração do soluto é maior no reciiente II do que no I e a membrana semi-ermeáveal é ideal a assagem de água é realizada do reciiente I ara o II Existe uma corrente osmótica ororcional à diferença de concentrações (CsI Cs II) A corrente de água é ositiva e ocorre do reciiente I ara o II Uma forma alternativa de criar transorte de água consiste em criar diferenças de ressão hidrostática Suondo que um êmbolo em II maniulado de forma a que PII>PI então haverá corrente de água de II ara I. Jw H = L (PI-PII) Coeficiente de Filtração Jw total = Jw o + Jw H = - K Cs + L P 11
12 Jw total = Jw o + Jw H = - L π - L P = L ( P π) Membrana semi-ermeável real No caso da membrana semi-ermeável real a corrente de água é menor, tendo em conta que uma fracção de moléculas de soluto também se move reduz as diferenças de otencial químico da água É necessário introduzir um factor de correcção relacionado com o coeficiente de reflexão (σ) ara as moléculas de soluto Jw total = L ( σ π) Membranas semi-ermeáveis ideais σ = 1 Em condições de equilíbrio as diferenças de ressão osmótica e hidrostática estão comensadas - Jw = 0 = π 12
13 Dimensões Densidade de corrente de água mol cm -2 s -1 Pressões (Osmótica e Hidrostática) dine cm -2 Coeficiente de Filtração mol dine - 1 s -1 Aula Teórico-Prática Nº5 Sumário Membrana de Donnan. Resolução de exercícios. Membrana de Donnan 13
14 Quando NaCl se dissocia a concentração de cada um dos iões nos reciientes fica igual (concentração = n) - equilíbrio Equação de Nernst Potencial de membrana ara cada ião 14
15 Assim - A ressão e a temeratura são constantes - A diferença de otencial ara cada ião é igual no equilíbrio - RT/F constante Os quocientes entre as concentrações têm que ser iguais 15
16 16
17 o entanto, aós a adição da roteína e devido à electroneutralidade que tem de ser mantida nos 2 reciientes as concentrações são: 17
18 Sal Monovalente Variação ocorrida na concentração dum microião A diferença entre equenos iões será: Se d>0 Concentração de microiões maior no comartimento I Existe um número de equenos iões contidos no reciiente I que corresondem a artículas não difusíveis sendo deste modo caazes de gerar ressão osmótica. 18
19 19 Diferença de Pressão Osmótica Concentração Diferença de Pressão Osmótica Sal Bivalente nd Z n Z d C + + = + = = = = nd II I Z n Z T R C T R π π π
20 A diferença entre equenos iões será: Aula Teórico-Prática Nº6 Sumário Primeira avaliação teórico-rática 20
BIOMEMBRANAS. M Filomena Botelho
 BIOMEMBRANAS M Filomena Botelho Transporte de massa Transporte de moléculas neutras Transporte de iões Noções de bioelectricidade Biomembranas Transporte de massa Transporte de massa ou transferência de
BIOMEMBRANAS M Filomena Botelho Transporte de massa Transporte de moléculas neutras Transporte de iões Noções de bioelectricidade Biomembranas Transporte de massa Transporte de massa ou transferência de
CORRENTE DE ARRASTAMENTO
 Objectivos Compreender as correntes de arrastamento Apreender a noção de concentração média de uma membrana homogénea e de uma membrana porosa Apreender a noção de densidade de corrente total Compreender
Objectivos Compreender as correntes de arrastamento Apreender a noção de concentração média de uma membrana homogénea e de uma membrana porosa Apreender a noção de densidade de corrente total Compreender
Segunda aula de mecânica dos fluidos básica. Estática dos Fluidos capítulo 2 do livro do professor Franco Brunetti
 Segunda aula de mecânica dos fluidos básica Estática dos Fluidos caítulo 2 do livro do rofessor Franco Brunetti NO DESENVOLVIMENTO DESTA SEGUNDA AULA NÃO IREI ME REPORTAR DIRETAMENTE AO LIVRO MENCIONADO
Segunda aula de mecânica dos fluidos básica Estática dos Fluidos caítulo 2 do livro do rofessor Franco Brunetti NO DESENVOLVIMENTO DESTA SEGUNDA AULA NÃO IREI ME REPORTAR DIRETAMENTE AO LIVRO MENCIONADO
CAPÍTULO 1 INTODUÇÃO. O DESENVOLVIMENTO DE BIOPROCESSOS. INTRODUÇÃO AOS CÁLCULOS DE ENGENHARIA
 CAPÍTULO 1 INTODUÇÃO. O DESENVOLVIMENTO DE BIOPROCESSOS. INTRODUÇÃO AOS CÁLCULOS DE ENGENHARIA OBJECTIVO: Interpretação e desenvolvimento de processos biológicos. Análise quantitativa de sistemas e processos
CAPÍTULO 1 INTODUÇÃO. O DESENVOLVIMENTO DE BIOPROCESSOS. INTRODUÇÃO AOS CÁLCULOS DE ENGENHARIA OBJECTIVO: Interpretação e desenvolvimento de processos biológicos. Análise quantitativa de sistemas e processos
Capítulo 1 Química-Física das Interfaces
 Problemas de Química-Física 2017/2018 Caítulo 1 Química-Física das Interfaces 1. Calcule o trabalho necessário ara aumentar de 1.5 cm 2 a área de um filme de sabão suortado or uma armação de arame (ver
Problemas de Química-Física 2017/2018 Caítulo 1 Química-Física das Interfaces 1. Calcule o trabalho necessário ara aumentar de 1.5 cm 2 a área de um filme de sabão suortado or uma armação de arame (ver
Unidade VII - Teoria Cinética dos Gases
 Unidade VII - eoria Cinética dos Gases fig. VII.. Nesse rocesso, a ressão em um gás aumenta e o olume diminui. Isto é, a colisão de suas moléculas dee aumentar, sua energia cinética aumenta e diminui a
Unidade VII - eoria Cinética dos Gases fig. VII.. Nesse rocesso, a ressão em um gás aumenta e o olume diminui. Isto é, a colisão de suas moléculas dee aumentar, sua energia cinética aumenta e diminui a
O calor específico desse material no estado sólido e seu calor latente de fusão valem, respectivamente:
 4 GRITO 3 1 o DI PSES 2 a ETP TRIÊNIO 25-27 FÍSIC QUESTÕES DE 11 2 11. Um bloco de um material sólido, de massa 1 g, é aquecido e sofre uma transição de fase ara o estado líquido. O gráfico abaixo mostra
4 GRITO 3 1 o DI PSES 2 a ETP TRIÊNIO 25-27 FÍSIC QUESTÕES DE 11 2 11. Um bloco de um material sólido, de massa 1 g, é aquecido e sofre uma transição de fase ara o estado líquido. O gráfico abaixo mostra
Inspeção de Sistemas de. Módulo 4 Medição de Vazão
 C u r s o Inspeção de Sistemas de Medição de Gás NATURAL Módulo 4 Medição de Vazão C u r s o Inspeção de Sistemas de Medição de Gás NATURAL Módulo 4 Medição de Vazão desafio 1 Quantidades Físicas Módulo
C u r s o Inspeção de Sistemas de Medição de Gás NATURAL Módulo 4 Medição de Vazão C u r s o Inspeção de Sistemas de Medição de Gás NATURAL Módulo 4 Medição de Vazão desafio 1 Quantidades Físicas Módulo
Mecânica Técnica. Aula 1 Conceitos Fundamentais. Prof. MSc. Luiz Eduardo Miranda J. Rodrigues
 Aula 1 Conceitos Fundamentais Tópicos Abordados Nesta Aula Apresentação do Curso. Apresentação da Bibliografia Definição da. Sistema Internacional de Unidades. Apresentação do Curso Aula 1 - Definição
Aula 1 Conceitos Fundamentais Tópicos Abordados Nesta Aula Apresentação do Curso. Apresentação da Bibliografia Definição da. Sistema Internacional de Unidades. Apresentação do Curso Aula 1 - Definição
Estudo dos gases. Antes de estudar o capítulo PARTE I
 PARTE I Unidade D 8 Caítulo Estudo dos gases Seções: 81 As transformações gasosas 82 Conceito de mol Número de Avogadro 83 Equação de Claeyron 84 Teoria cinética dos gases Antes de estudar o caítulo eja
PARTE I Unidade D 8 Caítulo Estudo dos gases Seções: 81 As transformações gasosas 82 Conceito de mol Número de Avogadro 83 Equação de Claeyron 84 Teoria cinética dos gases Antes de estudar o caítulo eja
Fundamentos de Física. Vitor Sencadas
 Fundamentos de Física Vitor Sencadas [email protected] Grandezas físicas e sistemas de unidades 1.1. Introdução A observação de um fenómeno é incompleta quando dela não resultar uma informação quantitativa.
Fundamentos de Física Vitor Sencadas [email protected] Grandezas físicas e sistemas de unidades 1.1. Introdução A observação de um fenómeno é incompleta quando dela não resultar uma informação quantitativa.
Aula 15 Introdução à Convecção
 ula 15 Introdução à Convecção luna: Renata Ladeia Data: 14.5.21 1) Ojetivos Os ojetivos desta aula serão aresentar as roriedades físicas envolvidas na transferência de calor or convecção assim como exor
ula 15 Introdução à Convecção luna: Renata Ladeia Data: 14.5.21 1) Ojetivos Os ojetivos desta aula serão aresentar as roriedades físicas envolvidas na transferência de calor or convecção assim como exor
Ismael Rodrigues Silva Física-Matemática - UFSC. cel: (48)
 Ismael Rodrigues Silva Física-Matemática - UFSC cel: (48)9668 3767 Ramos da Mecânica... Grandezas... Sistema Internacional... Unidades Derivadas... Cálculo com Unidades... Potências de 10... Prefixos do
Ismael Rodrigues Silva Física-Matemática - UFSC cel: (48)9668 3767 Ramos da Mecânica... Grandezas... Sistema Internacional... Unidades Derivadas... Cálculo com Unidades... Potências de 10... Prefixos do
Começando por misturas binárias de substâncias que não reagem entre si, a composição da mistura é caracterizada por: x A + x B = 1
 Começando or misturas binárias de substâncias que não reagem entre si, a comosição da mistura é caracterizada or: x + x = 1 termodinâmica das soluções é formulada em termos de roriedades arciais molares
Começando or misturas binárias de substâncias que não reagem entre si, a comosição da mistura é caracterizada or: x + x = 1 termodinâmica das soluções é formulada em termos de roriedades arciais molares
Unidades e Dimensões
 Universidade Tecnológica Federal do Paraná Câmpus Londrina Departamento Acadêmico de Alimentos Introdução às Operações Unitárias na Indústria de Alimentos Unidades e Dimensões Profa. Marianne Ayumi Shirai
Universidade Tecnológica Federal do Paraná Câmpus Londrina Departamento Acadêmico de Alimentos Introdução às Operações Unitárias na Indústria de Alimentos Unidades e Dimensões Profa. Marianne Ayumi Shirai
1. ENTALPIA. (a) A definição de entalpia. A entalpia, H, é definida como:
 1 Data: 31/05/2007 Curso de Processos Químicos Reerência: AKINS, Peter. Físico- Química. Sétima edição. Editora, LC, 2003. Resumo: Proas. Bárbara Winiarski Diesel Novaes 1. ENALPIA A variação da energia
1 Data: 31/05/2007 Curso de Processos Químicos Reerência: AKINS, Peter. Físico- Química. Sétima edição. Editora, LC, 2003. Resumo: Proas. Bárbara Winiarski Diesel Novaes 1. ENALPIA A variação da energia
FENÔMENOS DE TRANSPORTE Estática dos Fluidos
 FENÔMENOS DE TRANSPORTE Estática dos Fluidos CAPÍTULO. 1 HIDROSTÁTICA HIDRODINÂMICA reouso ou equilíbrio (1ª e 3ª leis de Newton) movimento (comlexo e será tratado suerficialmente) OU HIDROSTÁTICA 1 Densidade
FENÔMENOS DE TRANSPORTE Estática dos Fluidos CAPÍTULO. 1 HIDROSTÁTICA HIDRODINÂMICA reouso ou equilíbrio (1ª e 3ª leis de Newton) movimento (comlexo e será tratado suerficialmente) OU HIDROSTÁTICA 1 Densidade
2.1.1. Sistemas simples a uma dimensão
 2. CONVERSÃO DE UNIDADES Velocidade do carro (S.I.): m/s ; mais compreensível em km/h. 2.1. Conversão de unidades simples: comprimento (m), área (m 2 ),... 2.2. Conversão de unidades compostas: velocidade
2. CONVERSÃO DE UNIDADES Velocidade do carro (S.I.): m/s ; mais compreensível em km/h. 2.1. Conversão de unidades simples: comprimento (m), área (m 2 ),... 2.2. Conversão de unidades compostas: velocidade
Comprimento metro m Massa quilograma kg Tempo segundo s. Temperatura termodinâmica Kelvin K
 INTRODUÇÃO O Sistema Internacional e s ( S.I.) O SI é dividido em três grupos, a seguir: Sete s de Base Duas s Suplementares s derivadas Tabela 1 - s de Base do SI Comprimento metro m Massa quilograma
INTRODUÇÃO O Sistema Internacional e s ( S.I.) O SI é dividido em três grupos, a seguir: Sete s de Base Duas s Suplementares s derivadas Tabela 1 - s de Base do SI Comprimento metro m Massa quilograma
MEDIÇÃO DE GRANDEZAS. Para medir uma grandeza precisamos de: -Uma unidade - Um instrumento que utilize essa unidade
 Para medir uma grandeza precisamos de: -Uma unidade - Um instrumento que utilize essa unidade Medição e medida Medição: conjunto de operações que têm por objetivo determinar o valor de uma grandeza. Medida:
Para medir uma grandeza precisamos de: -Uma unidade - Um instrumento que utilize essa unidade Medição e medida Medição: conjunto de operações que têm por objetivo determinar o valor de uma grandeza. Medida:
Formulário. Física. Constante
 Física Formulário Factores Multiplicativos Factores Multiplicativos Prefixo Símbolo 1 000 000 000 000 = 10 12 tera T 1 000 000 000 = 10 9 giga G 1 000 000 = 10 6 mega M 1 000 = 10 3 quilo k 100 = 10 2
Física Formulário Factores Multiplicativos Factores Multiplicativos Prefixo Símbolo 1 000 000 000 000 = 10 12 tera T 1 000 000 000 = 10 9 giga G 1 000 000 = 10 6 mega M 1 000 = 10 3 quilo k 100 = 10 2
FENÔMENOS DE TRANSPORTE
 FENÔMENOS DE TRANSPORTE Sistemas de Unidades Prof. Miguel Toledo del Pino, Dr. DEFINIÇÕES Os sistemas habitualmente utilizados são do tipo: F L T : F: força L: comprimento T: tempo M L T : M: massa 1 DEFINIÇÕES
FENÔMENOS DE TRANSPORTE Sistemas de Unidades Prof. Miguel Toledo del Pino, Dr. DEFINIÇÕES Os sistemas habitualmente utilizados são do tipo: F L T : F: força L: comprimento T: tempo M L T : M: massa 1 DEFINIÇÕES
Engenharia Mecânica Método de avaliação. Física Geral e Experimental I Prof. Me. Eder Baroni da Silveira
 Método de avaliação Física Geral e Experimental I Prof. Me. Eder Baroni da Silveira [email protected] Método de avaliação Nota M1 20% Conceito do laboratório; 10% Nota de participação; 10% Trabalho individual;
Método de avaliação Física Geral e Experimental I Prof. Me. Eder Baroni da Silveira [email protected] Método de avaliação Nota M1 20% Conceito do laboratório; 10% Nota de participação; 10% Trabalho individual;
Escoamentos Compressíveis. Aula 03 Escoamento unidimensional
 Escoamentos Comressíveis Aula 03 Escoamento unidimensional 3. Introdução 4 de outubro de 947: Chuck Yeager a bordo do Bell XS- torna-se o rimeiro homem a voar a velocidade suerior à do som. 6 de março
Escoamentos Comressíveis Aula 03 Escoamento unidimensional 3. Introdução 4 de outubro de 947: Chuck Yeager a bordo do Bell XS- torna-se o rimeiro homem a voar a velocidade suerior à do som. 6 de março
8/3/18. Unidades e Dimensões. Objetivos desta aula. Dimensões e Unidades. Dimensões e Unidades CONTROLE DE PROCESSOS NA INDÚSTRIA
 8/3/8 Unidades e Dimensões Profa. Juliana Ract Profa. Marina Ishii Objetivos desta aula Discutir as dimensões e unidades de grandezas físicas e termofísicas empregadas em cálculos industriais Apresentar
8/3/8 Unidades e Dimensões Profa. Juliana Ract Profa. Marina Ishii Objetivos desta aula Discutir as dimensões e unidades de grandezas físicas e termofísicas empregadas em cálculos industriais Apresentar
1) Unidades de Medida
 CURSO DE INSTRUMENTAÇÃO Conceitos Fundamentais Cedtec 2007/2 Sem equivalente na Apostila 1 Pressão e NívelN 1) Unidades de Medida É necessário saber trabalhar com unidades de medida no Sistema Internacional
CURSO DE INSTRUMENTAÇÃO Conceitos Fundamentais Cedtec 2007/2 Sem equivalente na Apostila 1 Pressão e NívelN 1) Unidades de Medida É necessário saber trabalhar com unidades de medida no Sistema Internacional
Avaliação da cadeira
 Avaliação da cadeira Trabalho de síntese 20% Trabalhos práticos (4/5) 40% Exame final 40% Metrologia Ciência da medição - desenvolvimento de métodos e procedimentos de medição; - desenho de equipamento
Avaliação da cadeira Trabalho de síntese 20% Trabalhos práticos (4/5) 40% Exame final 40% Metrologia Ciência da medição - desenvolvimento de métodos e procedimentos de medição; - desenho de equipamento
Capítulo 4: Equação da energia para um escoamento em regime permanente
 Caítulo 4: Equação da energia ara um escoamento em regime ermanente 4.. Introdução Eocando o conceito de escoamento incomressíel e em regime ermanente ara a instalação (ide figura), odemos afirmar que
Caítulo 4: Equação da energia ara um escoamento em regime ermanente 4.. Introdução Eocando o conceito de escoamento incomressíel e em regime ermanente ara a instalação (ide figura), odemos afirmar que
Universidade Federal do Maranhão - Campus Imperatriz Centro de Ciências Sociais, Saúde e Tecnologia Licenciatura em Ciências Naturais - LCN
 Universidade Federal do Maranhão - Campus Imperatriz Centro de Ciências Sociais, Saúde e Tecnologia Licenciatura em Ciências Naturais - LCN Física Módulo 1 No encontro de hoje... Medição Grandezas Físicas,
Universidade Federal do Maranhão - Campus Imperatriz Centro de Ciências Sociais, Saúde e Tecnologia Licenciatura em Ciências Naturais - LCN Física Módulo 1 No encontro de hoje... Medição Grandezas Físicas,
INOVAÇÕES NA CONSTRUÇÃO E NO CONTROLO DE ATERROS DE ESTRADAS E DE CAMINHOS DE FERRO DE ALTA VELOCIDADE PARTE 2
 INOVAÇÕES NA CONSTRUÇÃO E NO CONTROLO DE ATERROS DE ESTRADAS E DE CAMINHOS DE FERRO DE ALTA VELOCIDADE PARTE 2 A. Gomes Correia Universidade do Minho Eduardo Fortunato - LNEC Universidade do Minho ESTRUTURA
INOVAÇÕES NA CONSTRUÇÃO E NO CONTROLO DE ATERROS DE ESTRADAS E DE CAMINHOS DE FERRO DE ALTA VELOCIDADE PARTE 2 A. Gomes Correia Universidade do Minho Eduardo Fortunato - LNEC Universidade do Minho ESTRUTURA
CURSINHO TRIU QUÍMICA FRENTE B
 CURSINHO TRIU QUÍMICA FRENTE B AULA 3 EXPRESSÕES DE CONCENTRAÇÃO (CONT.) E PROPRIEDADES COLIGATIVAS DATA: 01/09/2014 1) EXPRESSÕES DE CONCENTRAÇÃO (CONTINUAÇÃO) a. FRAÇÃO EM MOL Fração em mols ou fração
CURSINHO TRIU QUÍMICA FRENTE B AULA 3 EXPRESSÕES DE CONCENTRAÇÃO (CONT.) E PROPRIEDADES COLIGATIVAS DATA: 01/09/2014 1) EXPRESSÕES DE CONCENTRAÇÃO (CONTINUAÇÃO) a. FRAÇÃO EM MOL Fração em mols ou fração
Estudo dos Gases. Equação de estado de um gás f(m, p, V, T) Estado de um gás m (p, V, T) estado inicial: p 1, V 1, T 1. estado final: p 2, V 2, T 2
 Estudo dos Gases Introdução Na fase gasosa as forças de atração entre as artículas são raticamente desrezíveis quando comaradas com as das fases sólida e líquida; or isso elas se movimentam desordenadamente
Estudo dos Gases Introdução Na fase gasosa as forças de atração entre as artículas são raticamente desrezíveis quando comaradas com as das fases sólida e líquida; or isso elas se movimentam desordenadamente
Termodinâmica. Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Deartamento de Química ermodinâmica Aula 3 Professora: Melissa Soares Caetano Discilina QUI 702 Mudanças de estado a ressão
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Deartamento de Química ermodinâmica Aula 3 Professora: Melissa Soares Caetano Discilina QUI 702 Mudanças de estado a ressão
AULA 15 GASES PERFEITOS 1- INTRODUÇÃO
 AULA 5 GASES PERFEIOS - INRODUÇÃO Neste caítulo, vamos estudar as transformações gasosas e as leis elaboradas or Boyle e ariotte, Claeyron, Gay-Lussac e Charles, que regem estas transformações. Vamos considerar
AULA 5 GASES PERFEIOS - INRODUÇÃO Neste caítulo, vamos estudar as transformações gasosas e as leis elaboradas or Boyle e ariotte, Claeyron, Gay-Lussac e Charles, que regem estas transformações. Vamos considerar
Resoluções dos testes propostos
 da física Caítulo 8 Estudo dos gases Resoluções dos testes roostos.49 Resosta: c Dados: A ; A ; B ; B Alicando a lei geral dos gases erfeitos, obtemos: A A A B B A B B A B B A.5 Resosta: d A transformação
da física Caítulo 8 Estudo dos gases Resoluções dos testes roostos.49 Resosta: c Dados: A ; A ; B ; B Alicando a lei geral dos gases erfeitos, obtemos: A A A B B A B B A B B A.5 Resosta: d A transformação
Figuras: ALVARENGA, Beatriz, MÁXIMO, Antônio. Curso de Física-Vol. 1, Editora Scipione, 6a Ed. São Paulo (2005) Comprimento metro m
 FÍSICA I AULA 01: GRANDEZAS FÍSICAS; SISTEMAS DE UNIDADES; VETORES TÓPICO 02: SISTEMAS DE UNIDADES Para efetuar medidas é necessário fazer uma padronização, escolhendo unidades para cada grandeza. Antes
FÍSICA I AULA 01: GRANDEZAS FÍSICAS; SISTEMAS DE UNIDADES; VETORES TÓPICO 02: SISTEMAS DE UNIDADES Para efetuar medidas é necessário fazer uma padronização, escolhendo unidades para cada grandeza. Antes
Estruturas de Betão Armado II 17 Pré-Esforço Perdas
 struturas de Betão rmado II 17 ré-sforço erdas 1 Força Máxima de Tensionamento (Força de uxe) força alicada à armadura de ré-esforço, max (ou seja, a força na extremidade activa durante a alicação do ré-esforço),
struturas de Betão rmado II 17 ré-sforço erdas 1 Força Máxima de Tensionamento (Força de uxe) força alicada à armadura de ré-esforço, max (ou seja, a força na extremidade activa durante a alicação do ré-esforço),
GUIA DO ESTUDANTE PARA A ELABORAÇÃO DE RELATÓRIOS PRÁTICOS II (Avançado)
 GUIA DO ESTUDANTE PARA A ELABORAÇÃO DE RELATÓRIOS PRÁTICOS II (Avançado) Traduzido e adaptado * por M. J. Matos de Walker, J. R. L. (1991). A student s guide to practical write-ups. Biochemical Education
GUIA DO ESTUDANTE PARA A ELABORAÇÃO DE RELATÓRIOS PRÁTICOS II (Avançado) Traduzido e adaptado * por M. J. Matos de Walker, J. R. L. (1991). A student s guide to practical write-ups. Biochemical Education
UFJF MÓDULO III DO PISM TRIÊNIO 2009-2011 GABARITO DA PROVA DE FÍSICA
 UFJF MÓDULO III DO PISM TRIÊNIO 9- GABARITO DA PROVA DE FÍSICA Na solução da rova, use uando necessário: 8 Velocidade da luz no vácuo c = 3, m/s 7 Permeabilidade magnética do vácuo =4π T m / A 9 Constante
UFJF MÓDULO III DO PISM TRIÊNIO 9- GABARITO DA PROVA DE FÍSICA Na solução da rova, use uando necessário: 8 Velocidade da luz no vácuo c = 3, m/s 7 Permeabilidade magnética do vácuo =4π T m / A 9 Constante
1. Em cada caso, obtenha a equação e esboce o grá co da circunferência.
 3.1 A Circunferência EXERCÍCIOS & COMPLEMENTOS 3.1 1. Em cada caso, obtenha a equação e esboce o grá co da circunferência. (a) Centro C ( 2; 1) e raio r = 5: (b) Passa elos ontos A (5; 1) ; B (4; 2) e
3.1 A Circunferência EXERCÍCIOS & COMPLEMENTOS 3.1 1. Em cada caso, obtenha a equação e esboce o grá co da circunferência. (a) Centro C ( 2; 1) e raio r = 5: (b) Passa elos ontos A (5; 1) ; B (4; 2) e
Escoamentos Compressíveis. Capítulo 03 Escoamento unidimensional
 Escoamentos Comressíveis Caítulo 03 Escoamento unidimensional 3. Introdução 4 de outubro de 947: Chuck Yeager a bordo do Bell XS- torna-se o rimeiro homem a voar a velocidade suerior à do som. 6 de março
Escoamentos Comressíveis Caítulo 03 Escoamento unidimensional 3. Introdução 4 de outubro de 947: Chuck Yeager a bordo do Bell XS- torna-se o rimeiro homem a voar a velocidade suerior à do som. 6 de março
PROPRIEDADES DAS SOLUÇÕES
 PROPRIEDADES DAS SOLUÇÕES M Filomena Botelho Objectivos Identificar e aplicar as propriedades das soluções Compreender a importância das propriedades coligativas Aplicar os conceito de pressão osmótica
PROPRIEDADES DAS SOLUÇÕES M Filomena Botelho Objectivos Identificar e aplicar as propriedades das soluções Compreender a importância das propriedades coligativas Aplicar os conceito de pressão osmótica
Aula # 8 Vibrações em Sistemas Contínuos Modelo de Segunda Ordem
 UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE SÃO CARLOS DEPARTAMENTO DE ENGENHARIA MECÂNICA Laboratório de Dinâmica SEM 504 DINÂMICA ESTRUTURAL Aula # 8 Vibrações em Sistemas Contínuos Modelo de Segunda
UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE SÃO CARLOS DEPARTAMENTO DE ENGENHARIA MECÂNICA Laboratório de Dinâmica SEM 504 DINÂMICA ESTRUTURAL Aula # 8 Vibrações em Sistemas Contínuos Modelo de Segunda
Termodinâmica. Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Deartamento de Química ermodinâmica Aula 2 Professora: Melissa Soares Caetano Físico Química Avançada H = U + V dh = du + dv
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Deartamento de Química ermodinâmica Aula 2 Professora: Melissa Soares Caetano Físico Química Avançada H = U + V dh = du + dv
Um catalisador heterogêneo é aquele que está em uma fase diferente da do sistema reacional. Focaremos nossa aula em sistemas de gás e sólido.
 ula: 32 Temática: Catálise Heterogênea Um catalisador heterogêneo é aquele que está em uma fase diferente da do sistema reacional. Focaremos nossa aula em sistemas de gás e sólido. catálise heterogênea
ula: 32 Temática: Catálise Heterogênea Um catalisador heterogêneo é aquele que está em uma fase diferente da do sistema reacional. Focaremos nossa aula em sistemas de gás e sólido. catálise heterogênea
AA-220 AERODINÂMICA NÃO ESTACIONÁRIA
 AA- AERODINÂMICA NÃO ESTACIONÁRIA Introdução e conceitos básicos da teoria Prof. Roberto GIL Email: [email protected] Ramal: 648 1 AERODINÂMICA NÃO ESTACIONÁRIA Objetivo: Partir das equações de Navier-Stokes
AA- AERODINÂMICA NÃO ESTACIONÁRIA Introdução e conceitos básicos da teoria Prof. Roberto GIL Email: [email protected] Ramal: 648 1 AERODINÂMICA NÃO ESTACIONÁRIA Objetivo: Partir das equações de Navier-Stokes
Unidades de Medidas e as Unidades do Sistema Internacional
 Unidades de Medidas e as Unidades do Sistema Internacional Metrologia é a ciência da medição, abrangendo todas as medições realizadas num nível conhecido de incerteza, em qualquer dominio da atividade
Unidades de Medidas e as Unidades do Sistema Internacional Metrologia é a ciência da medição, abrangendo todas as medições realizadas num nível conhecido de incerteza, em qualquer dominio da atividade
Física. Introdução. Professor Alexei Muller.
 Física Introdução Professor Alexei Muller www.acasadoconcurseiro.com.br Física INTRODUÇÃO Grandezas Físicas Grandeza Física é tudo que pode ser medido. Medir uma grandeza é compará-la com outra grandeza
Física Introdução Professor Alexei Muller www.acasadoconcurseiro.com.br Física INTRODUÇÃO Grandezas Físicas Grandeza Física é tudo que pode ser medido. Medir uma grandeza é compará-la com outra grandeza
SOLUÇÕES SOLUÇÕES MISTURAS
 MISTURAS SOLUÇÕES Quando juntamos duas espécies químicas diferentes e, não houver reação química entre elas, isto é, não houver formação de nova(s) espécie(s), teremos uma mistura. Exemplos: Mistura de
MISTURAS SOLUÇÕES Quando juntamos duas espécies químicas diferentes e, não houver reação química entre elas, isto é, não houver formação de nova(s) espécie(s), teremos uma mistura. Exemplos: Mistura de
Transporte Iônico e o Potencial de Membrana
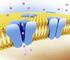 Transporte Iônico e o Potencial de Membrana Até o momento, consideramos apenas o transporte de solutos neutros (sem carga elétrica) através da membrana celular. A partir de agora, vamos passar a estudar
Transporte Iônico e o Potencial de Membrana Até o momento, consideramos apenas o transporte de solutos neutros (sem carga elétrica) através da membrana celular. A partir de agora, vamos passar a estudar
UFRPE: Física 11 Márcio Cabral de Moura 1. 2 aulas, 5 horas Capítulos 1 e 3 do Fundamentos de Física 1, de D. Halliday e R. Resnick, 3ª edição.
 UFRPE: Física 11 Márcio Cabral de Moura 1 1. Introdução 1 e 3 do Fundamentos de Física 1, de D. Halliday e R. Resnick, 3ª edição. 1.1 O objeto da Física O objeto da física é a natureza 1.2 O método físico.
UFRPE: Física 11 Márcio Cabral de Moura 1 1. Introdução 1 e 3 do Fundamentos de Física 1, de D. Halliday e R. Resnick, 3ª edição. 1.1 O objeto da Física O objeto da física é a natureza 1.2 O método físico.
1.1.2 PROPRIEDADES FUNDAMENTAIS DOS FLUIDOS
 UNIVERSIDADE FEDERAL DE GOIÁS ESCOLA DE AGRONOMIA E ENGENHARIA DE ALIMENTOS SETOR DE ENGENHARIA RURAL Prof. Adão Wagner Pêgo Evangelista 1.1.2 PROPRIEDADES FUNDAMENTAIS DOS FLUIDOS A) MASSA ESPECÍFICA
UNIVERSIDADE FEDERAL DE GOIÁS ESCOLA DE AGRONOMIA E ENGENHARIA DE ALIMENTOS SETOR DE ENGENHARIA RURAL Prof. Adão Wagner Pêgo Evangelista 1.1.2 PROPRIEDADES FUNDAMENTAIS DOS FLUIDOS A) MASSA ESPECÍFICA
Osmose, osmolaridade e tonicidade: transporte de água e regulação do volume celular
 Osmose, osmolaridade e tonicidade: transporte de água e regulação do volume celular Fisiologia I RCG0214 Medicina RP Prof. Ricardo Leão Departamento de Fisiologia FMRP-USP Era uma vez uma hemácia feliz
Osmose, osmolaridade e tonicidade: transporte de água e regulação do volume celular Fisiologia I RCG0214 Medicina RP Prof. Ricardo Leão Departamento de Fisiologia FMRP-USP Era uma vez uma hemácia feliz
Regulação da tonicidade do FEC
 Regulação da tonicidade do FEC Jackson de Souza Menezes Laboratório Integrado de Bioquímica Hatisaburo Masuda Núcleo de Pesquisas em Ecologia e Desenvolvimento Sócio-Ambiental Universidade Federal do Rio
Regulação da tonicidade do FEC Jackson de Souza Menezes Laboratório Integrado de Bioquímica Hatisaburo Masuda Núcleo de Pesquisas em Ecologia e Desenvolvimento Sócio-Ambiental Universidade Federal do Rio
UFSC Universidade Federal de Santa Catarina Depto De Eng. Química e de Eng. De Alimentos EQA 5313 Turma 645 Op. Unit. de Quantidade de Movimento
 UFSC Universidade Federal de Santa Catarina eto e Eng. Química e de Eng. e Alimentos EQA 51 Turma 645 O. Unit. de Quantidade de Movimento ESCOAMENTO EM MEIOS POROSOS LEITO FIXO O escoamento de fluidos
UFSC Universidade Federal de Santa Catarina eto e Eng. Química e de Eng. e Alimentos EQA 51 Turma 645 O. Unit. de Quantidade de Movimento ESCOAMENTO EM MEIOS POROSOS LEITO FIXO O escoamento de fluidos
Prof. Renato. EME Prof. Vicente Bastos. Física 1ª. Série Aula 1. Movimentos. - Deslocamento (translação) Ir de um ponto a outro.
 Aula 1 Movimentos 1. Tipos de movimentos - Deslocamento (translação) Ir de um ponto a outro. - Giro (rotação) Girar ao redor de um ponto fixo. 2. O Espaço (estimativas) a) altura da sala de aula (3,5m)
Aula 1 Movimentos 1. Tipos de movimentos - Deslocamento (translação) Ir de um ponto a outro. - Giro (rotação) Girar ao redor de um ponto fixo. 2. O Espaço (estimativas) a) altura da sala de aula (3,5m)
Capítulo II. Fenómenos de Transporte
 Capítulo II Fenómenos de Transporte Fenómenos de transporte: aspectos gerais Movimento molecular De que depende o movimento aleatório das moléculas? TEMPERATURA Física Aplicada 2013/14 MICF FFUP 2 Fenómenos
Capítulo II Fenómenos de Transporte Fenómenos de transporte: aspectos gerais Movimento molecular De que depende o movimento aleatório das moléculas? TEMPERATURA Física Aplicada 2013/14 MICF FFUP 2 Fenómenos
Classificação Solução Colóide Suspensão Exemplo: açúcar na água, sal de cozinha na água, álcool hidratado.
 Química - Unidade 5 de 12: GOVERNO DO ESTADO DE MATO GROSSO DO SUL Conteúdo 10: Dispersões (definição,classificação, e características) Habilidade e competência: Identificar a diferença entre dispersões,
Química - Unidade 5 de 12: GOVERNO DO ESTADO DE MATO GROSSO DO SUL Conteúdo 10: Dispersões (definição,classificação, e características) Habilidade e competência: Identificar a diferença entre dispersões,
Capítulo 7: Escoamento Interno
 Caítulo 7: Escoamento Interno Transferência de calor Escoamento interno O fluido está comletamente confinado or uma suerfície sólida: reresenta o escoamento de um fluido em um duto ou tubulação. Assim
Caítulo 7: Escoamento Interno Transferência de calor Escoamento interno O fluido está comletamente confinado or uma suerfície sólida: reresenta o escoamento de um fluido em um duto ou tubulação. Assim
DIAGRAMA DE FASES. Ex.: diagrama de fases da água (H 2 O)
 óico.5 DIAGRAMA DE FASES Diagrama de Fases Ex.: diagrama de fases da água (H O) Denomina-se diagrama de fases de uma substância o gráfico x que define o estado de agregação dessa substância em função dessas
óico.5 DIAGRAMA DE FASES Diagrama de Fases Ex.: diagrama de fases da água (H O) Denomina-se diagrama de fases de uma substância o gráfico x que define o estado de agregação dessa substância em função dessas
Aula 6 EQUILÍBRIO QUÍMICO. Kleber Bergamaski
 Aula 6 EQUILÍBRIO QUÍMICO META Aresentar os rinciais conceitos desenvolvidos no equilíbrio químico e suas relações termodinâmicas com a constante e comosição de equilíbrio OBJETIVOS Ao final desta aula,
Aula 6 EQUILÍBRIO QUÍMICO META Aresentar os rinciais conceitos desenvolvidos no equilíbrio químico e suas relações termodinâmicas com a constante e comosição de equilíbrio OBJETIVOS Ao final desta aula,
O Universo e Composição Fundamental
 1 O Universo e Composição Fundamental I) Componentes Fundamentais do Universo São aqueles que não podem ser substituídos por outros. Matéria (M): representada pela massa, são os objetos, corpos, alimentos.
1 O Universo e Composição Fundamental I) Componentes Fundamentais do Universo São aqueles que não podem ser substituídos por outros. Matéria (M): representada pela massa, são os objetos, corpos, alimentos.
F S F S F S HIDROSTÁTICA. A hidrostática analisa os fluidos em repouso. PRESSÃO. De acordo com a figura:
 HIDROTÁTIC hidrostática analisa os fluidos em reouso. De acordo com a figura: PREÃO ressão,, exercida ela força de intensidade, que atua erendicularmente numa suerfície de área, é dada ela exressão: unidade
HIDROTÁTIC hidrostática analisa os fluidos em reouso. De acordo com a figura: PREÃO ressão,, exercida ela força de intensidade, que atua erendicularmente numa suerfície de área, é dada ela exressão: unidade
Exercícios Práticos de Biofísica
 Exercícios Práticos de Biofísica Faculdade de Medicina da Universidade de Coimbra Membranas 2 Convenções Nos exercícios desta secção, e salvo indicação em contrário, utilizaremos as seguintes convenções:
Exercícios Práticos de Biofísica Faculdade de Medicina da Universidade de Coimbra Membranas 2 Convenções Nos exercícios desta secção, e salvo indicação em contrário, utilizaremos as seguintes convenções:
A Estrutura Metrológica Nacional e Internacional. O Sistema Internacional de Unidades (SI) Definições e Terminologia
 A Estrutura Metrológica Nacional e Internacional O Sistema Internacional de Unidades (SI) Definições e Terminologia 1 Estrutura Metrológica Nacional e Internacional A metrologia não sobrevive no mercado
A Estrutura Metrológica Nacional e Internacional O Sistema Internacional de Unidades (SI) Definições e Terminologia 1 Estrutura Metrológica Nacional e Internacional A metrologia não sobrevive no mercado
UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO DEPARTAMENTO DE CIÊNCIAS AMBIENTAIS FENÔMENOS DE TRANSPORTE MECÂNICA DOS FLUIDOS
 Universidade Federal Rural do Semiárido UNIVERSIDADE FEDERAL RURAL DO SEMIÁRIDO DEPARTAMENTO DE CIÊNCIAS AMBIENTAIS FENÔMENOS DE TRANSPORTE MECÂNICA DOS FLUIDOS EQUAÇÃO DA CONTINUIDADE EQUAÇÃO DE BERNOULLI
Universidade Federal Rural do Semiárido UNIVERSIDADE FEDERAL RURAL DO SEMIÁRIDO DEPARTAMENTO DE CIÊNCIAS AMBIENTAIS FENÔMENOS DE TRANSPORTE MECÂNICA DOS FLUIDOS EQUAÇÃO DA CONTINUIDADE EQUAÇÃO DE BERNOULLI
LISTA 3 - Prof. Jason Gallas, DF UFPB 10 de Junho de 2013, às 14:28. Jason Alfredo Carlson Gallas, professor titular de física teórica,
 Exercícios Resolvidos de Física Básica Jason Alfredo Carlson Gallas, rofessor titular de física teórica, Doutor em Física ela Universidade Ludwig Maximilian de Munique, Alemanha Universidade Federal da
Exercícios Resolvidos de Física Básica Jason Alfredo Carlson Gallas, rofessor titular de física teórica, Doutor em Física ela Universidade Ludwig Maximilian de Munique, Alemanha Universidade Federal da
