Introdução. Introdução. Eletroquímico. Mecanismo. Tipos. patináveis. Aços. Prevenção. Light Steel Frame. Introdução. Introdução.
|
|
|
- Gonçalo Araújo Bergmann
- 5 Há anos
- Visualizações:
Transcrição
1 UNIVERSIDADE FEDERAL DO PARANÁ DEPARTAMENTO DE CONSTRUÇÃO CIVIL CONSTRUÇÃO CIVIL III (TC-038) ESTRUTURAS METÁLICAS CORROSÃO Os metais raramente são encontrados no estado puro. Eles quase sempre são encontrados em combinação com um ou mais elementos nãometálicos presentes no ambiente Minérios são, de modo geral, formas oxidadas do metal Com raras exceções, quantidades significativas de energia devem ser fornecidas aos minérios para reduzi-los aos metais puros. A fundição e conformação posterior do metal envolvem processos onde mais energia é gasta De uma perspectiva puramente termodinâmica, a tendência de decréscimo energético é a principal força encorajadora da corrosão metálica 1
2 pode ser definida Como sendo a tendência espontânea do metal produzido e conformado de reverter ao seu estado original, de mais baixa energia livre É a deterioração de propriedades que ocorre quando um material reage com o ambiente Solos Atmosfera Produtos químicos Meios corrosivos Águas naturais (rios, lagos e subsolo) Água do mar Os meios corrosivos em corrosão eletroquímica são responsáveis pela formação do eletrólito que é uma solução eletricamente condutora constituída de água contendo sais, ácidos ou Profª bases M.Sc. Thaísa Rocha O ar contém umidade, sais em suspensão, gases industriais, poeira, etc Atmosfera Os produtos químicos, desde que em contato com água ou com umidade e formem um eletrólito, podem provocar corrosão eletroquímica Solos Produtos químicos Os solos contêm umidade, sais minerais e bactérias. Alguns solos apresentam também características ácidas ou básicas Meios corrosivos Estas águas contêm grande quantidade de sais Águas naturais (rios, lagos e subsolo) Água do mar Estas águas podem conter sais minerais, eventualmente ácidos ou bases, resíduos industriais, bactérias, poluentes diversos e gases dissolvidos 2
3 Uma reação é considerada eletroquímica se ela estiver associada à passagem de corrente elétrica através de uma distância finita, maior do que a distância interatômica Esta passagem de corrente envolve o movimento de partículas carregadas - íons, elétrons ou ambos Dessa forma, na maioria das reações que se manifestam na presença de uma superfície metálica, ocorre a passagem de corrente através do metal, e a reação é eletroquímica em sua natureza A distância que a corrente elétrica percorre numa reação de corrosão eletroquímica pode variar bastante Na maioria das reações eletroquímicas os íons se movimentam através de eletrólito líquido Como no caso da dissolução de um metal em uma solução ácida Normalmente aquoso Desde uma dimensão da ordem de um tamanho de grão (micrometros) Até quilômetros de distância Como no caso da corrosão por correntes de fuga de tubulações enterradas nas vizinhanças de uma estrada de ferro eletrificada No entanto, em reações de oxidação não se tem eletrólito líquido e o movimento de íons ocorre através da película de óxido metálico que se forma na superfície do metal Este óxido funciona como um eletrólito sólido e garante a natureza eletroquímica Profª da M.Sc. reação Thaísa Rocha Experiências clássica que ilustra de forma bem clara as reações eletroquímicas envolvidas no processo de corrosão do aço-carbono Uma gota de uma solução NaCl 3% é vertida sobre uma superfície finamente lixada de aço carbono, contém uma pequena quantidade Olhando a gota por cima, observa-se, no início, o aparecimento de pequenas áreas tanto de coloração azul como rosa, distribuídas ao acaso sobre a superfície do aço (distribuição primária) Experiência da gota salina Do indicador ferricianeto de potássio, que se torna azul em presença de íons ferrosos (azul da Prússia) E do indicador fenolftaleína, que se torna rosa na presença de hidroxilas (OH-) 3
4 Após certo tempo, a distribuição dessas áreas altera-se A área rosa na periferia da gota A área azul no centro E, aparecendo entre as duas áreas, um precipitado de coloração marrom (distribuição secundária) A ferrugem A área azul no centro A área rosa Deve-se à formação de íons ferrosos Devido à formação do íon hidroxila a partir do oxigênio dissolvido na solução Fe Fe e- Trata-se de uma reação de oxidação, também chamada de reação anódica, visto que os elétrons são produtos da reação O 2 + 2H 2 O + 4e - 4OH - Reação de oxidação Reação de redução Ocorrem juntas graças à passagem de corrente elétrica pelo metal, da região de dissolução do metal (anódica), para a região de redução do oxigênio (catódica) Estas reações de natureza eletroquímica Redução do oxigênio Trata-se de uma reação de redução, ou reação catódica, uma vez que os elétrons são reagentes na reação São as reações básicas do processo corrosivo que ocorre dentro da gota salina Os elétrons que são gerados pela reação anódica se deslocam através do metal da região azul para a região rosa, isto é, da região anódica para a região catódica 4
5 Reação global que descreve o processo de enferrujamento do aço carbono ao ar é 4Fe + 3O 2 + 2H 2 O 2Fe 2 O 3.H 2 O AÇO OXIGÊNIO ÁGUA FERRUGEM O processo de corrosão atmosférica do aço carbono consiste Em elétrons fluindo dentro do metal Em íons fluindo no eletrólito superficial A velocidade de corrosão é muito influenciada pela condutividade elétrica do eletrólito Vários são os fatores que determinam a criação e a distribuição de regiões anódicas e catódicas na superfície do metal A existência de diferenças de composição química, de microestrutura, de concentração e velocidade de eletrólitos, de tensões residuais, dentre outras Determinam a formação de regiões catódicas ou anódicas É menor para meio pouco condutores É maior para meios condutores Para que a corrosão atmosférica do aço carbono aconteça, é necessária a presença simultânea de água e oxigênio Água muito pura Água do mar ou soluções ácidas Na ausência de um deles, a corrosão não acontecerá 5
6 Uniforme Por de corrosão Galvânica Por Uniforme O ataque mente distribuído por grandes regiões da superfície metálica é certamente a forma mais comum de corrosão A velocidade com que progride, por ser, pode ser estimada Pode ocorrer quando dois metais diferentes, em contato elétrico (ou conectados por um condutor elétrico) são expostos a uma solução condutora de eletricidade Galvânica Uma diferença de potencial elétrico existente entre diferentes metais ou ligas acaba por fornecer o potencial termodinâmico necessário à manutenção do processo de corrosão 6
7 As condições ambientais dentro de uma fresta podem, com o tempo, tornar-se muito diferentes daquelas encontradas em uma superfície próxima, limpa e exposta ao ambiente externo Um ambiente muito mais agressivo pode se desenvolver e causar a corrosão localizada no interior da fresta Por Frestas acontecem, por exemplo, em parafusos, pontos de solda descontínua e rebites, mas também podem ser criadas por depósitos de sujeira, produtos de corrosão, riscos em pintura A corrosão por é uma forma de corrosão localizada que consiste na formação de cavidades de pequena extensão e razoável profundidade Ocorre em determinados pontos da superfície enquanto que o restante pode permanecer praticamente sem ataque Por Grande parte das ocorrências de corrosão envolvem reações eletroquímicas 7
8 Alveolar: fundo arredondado e profundidade geralmente menor que o diâmetro A corrosão é o fenômeno de corrosão mais importante, comum, simples e conhecido por por por por Acontece em metais e ligas relativamente homogêneas expostas a ambientes também homogêneos Esta homogeneidade de comportamento pode ser, de fato, tanto reflexo da homogeneidade intrínseca do material (ausência de defeitos estruturais, por exemplo) quanto a não seletividade do ambiente com respeito a estes defeitos -carbono expostos à atmosfera e ligas de cobre expostos às águas naturais são bons exemplos de materiais que podem sofrer este tipo de ataque 8
9 por por Velocidade de corrosão é expressa Pela perda de massa por unidade de superfície e por unidade de tempo Pela perda de espessura do metal corroído em função do tempo Em certos casos particulares, a corrosão pode ser muito acelerada pela ação de agentes externos É o caso de um fenômeno conhecido por corrosão por correntes de fuga por por Influência da umidade relativa do ar A presença de sais depositados exerce uma dupla ação A figura mostra a evolução da corrosão de um aço carbono em função da umidade relativa, para uma atmosfera poluída com 0,01% de SO 2 e por um período de exposição de 55 dias Fica evidenciado que a corrosão é acelerada quando a umidade relativa supera os 60% Reduz o valor da pressão de saturação Cria uma situação desfavorável, pois estes sais, dissolvidos na água condensada, podem levar à formação de um eletrólito particularmente agressivo Caracterização Definem os critérios relativos à caracterização de uma atmosfera e o grau de corrosividade Caracterização Definem os critérios relativos à caracterização de uma atmosfera e o grau de corrosividade Definida pelas normas ISO 9223 e ISO 9226 A duração da exposição à uma dada umidade (tempo de umedecimento) t Determinado a partir da velocidade de corrosão de metais expostos Três são os parâmetros utilizados na classificação de uma atmosfera Definida pelas normas ISO 9223 e ISO 9226 A duração da exposição à uma dada umidade (tempo de umedecimento) t Determinado a partir da velocidade de corrosão de metais expostos Três são os parâmetros utilizados na classificação de uma atmosfera por A concentração de SO atmosférico, dado em mg/m 3 A concentração de íons cloreto, dada como velocidade de deposição, em mg/(m².dia) por Período de tempo no qual a umidade relativa é superior a 80% e a temperatura é superior a 0 C por por São descritas cinco categorias, indo de t (< 10 h/ano) a t (> h/ano) 9
10 Caracterização Definem os critérios relativos à caracterização de uma atmosfera e o grau de corrosividade Caracterização Definem os critérios relativos à caracterização de uma atmosfera e o grau de corrosividade Definida pelas normas ISO 9223 e ISO 9226 São descritas quatro categorias, indo de P (< 12 mg/m³) a P (90 < P < 250 mg/m³) Determinado a partir da velocidade de corrosão de metais expostos Três são os parâmetros utilizados na classificação de uma atmosfera Definida pelas normas ISO 9223 e ISO 9226 Determinado a partir da velocidade de corrosão de metais expostos Três são os parâmetros utilizados na classificação de uma atmosfera por por A concentração de SO atmosférico, dado em mg/m 3 Uma atmosfera rural não poluída como a de Sorocaba - SP, apresenta um valor médio anual de 5 mg/m³, enquanto que uma atmosfera industrial como a encontrada em Cubatão - SP, possui um valor médio anual de 27 mg/m³ por por São descritas 4 categorias, indo de S (< 3 mg/(m².dia)) a S (300 < S < mg/(m².dia) Fortaleza/CE apresenta uma taxa de deposição de cloretos de cerca de 300 mg/(m².dia) A concentração de íons cloreto, dada como velocidade de deposição, em mg/(m².dia) Caracterização Este fenômeno ocorre quando o metal é colocado em presença de um ambiente não homogêneo A corrosão galvânica é uma das formas mais comuns de ataque em meio aquoso Estas diferenças podem advir de múltiplas origens, tanto ao nível do material (ligas multifásicas, defeitos localizados em revestimentos protetores, pares bimetálicos, etc.) quanto ao ambiental (variação local de composição química, de ph ou da temperatura) Como o próprio nome indica, ela resulta da formação de uma pilha, promovendo um ataque localizado em um dos componentes do par por A tabela descrita a seguir ilustra a corrosividade de uma atmosfera segundo a Norma ISO 9226 em função das velocidades de corrosão do aço carbono por por por 10
11 Cada metal ou liga pode ser caracterizada pelo seu potencial de corrosão Torna-se possível, deste modo, estabelecer o que se chama de série galvânica por por Material heterogêneo A partir destas indicações, torna-se possível estimar a pilha que será criada pelo acoplamento elétrico dos dois metais diferentes Observa-se num dado meio Consiste em fornecer, para um meio considerado, uma classificação de diferentes metais e ligas segundo seu potencial de corrosão medido experimentalmente O aumento da velocidade de corrosão do metal menos nobre (aquele que possui o menor potencial de corrosão) A diminuição da velocidade de corrosão do metal mais nobre (o que apresenta o maior potencial de corrosão) por por Material heterogêneo Este efeito pode ser utilizado com vantagens na proteção de um metal ou liga frente à corrosão É conhecido como proteção catódica É a quantidade do revestimento (isto é, espessura) que acaba sendo o fator primordial de proteção por por Material heterogêneo Este fenômeno está na origem do procedimento conhecido como galvanização, que objetiva proteger o aço pelo zinco O material que tem predominância da reação anódica (o anodo de sacrifício) acaba protegendo o resto da estrutura, que passa a ser, preponderantemente, cátodo por por É necessário distinguir Material heterogêneo Composição das ligas Proteção catódica onde o revestimento faz o papel de anodo de sacrifício Dos casos onde o revestimento é mais nobre que o material a proteger (como exemplo, temos a niquelação ou cobreação do aço) É a qualidade do revestimento que se revela primordial (ausência de defeitos que podem levar ao ataque localizado do substrato) A corrosão devida ao acoplamento galvânico de dois materiais dependerá de muitos parâmetros Presença de produtos de corrosão ph e agitação do eletrólito Razão de áreas ânodo/cátodo 11
12 por A série galvânica para metais e ligas imersas em água do mar Material heterogêneo por Quando o aço carbono é colocado em um eletrólito neutro (p.ex.: NaCl), pode-se observar o ataque intenso nas regiões pouco aeradas e a redução catódica nas regiões aeradas Meio heterogêneo Se o material é passivável O ph das regiões aeradas (áreas catódicas) se torna mais alto devido à redução do oxigênio Envolvendo a formação de íons hidroxila (o que contribui para a passivação local do material) A corrosão da região menos ventilada pode se tornar muito maior do que aquela da região ventilada por por A corrosão por aeração diferencial É a responsável pelo ataque abaixo da linha d'água de navios e em estruturas enterradas em solos onde a permeabilidade do oxigênio é desigual Exemplos de aeração diferencial Caracteriza-se por um ataque localizado que está geralmente associado à ruptura local de uma película passiva E que acontece muitas vezes na presença de cloretos ou de passivação incompleta por por Meio heterogêneo por por A quantidade de metal perdido por esta forma de ataque é muito pequena, mas pode levar à perfuração rápida das peças afetadas Podemos distinguir duas etapas distintas no processo de geração e crescimento de A corrosão por é um fenômeno bastante frequente, que afeta os aços carbono, aços inoxidáveis, ligas de níquel, de titânio, de alumínio ou cobre A iniciação, onde ocorre a quebra localizada da camada passiva O desenvolvimento do pite 12
13 por por Que permitem o acesso à superfície dos ânions agressivos (em particular os halogenetos) que tem tendência a formar complexos com os íons metálicos Existem vários mecanismos que tratam de explicar a iniciação de um pite Este processo pode ser concebido na presença de películas passivas muito desordenadas e na presença de um campo elétrico elevado O mecanismo da ruptura da película O mecanismo da penetração Este mecanismo pressupõe a existência de fissuras de origem mecânica na camada passiva (p.ex.: riscos) Supõe a transferência dos íons agressivos através da película passiva, até a interface metalóxido por por A ação simultânea do baixo ph e dos ânions que migraram para dentro da fresta cria um ambiente restrito muito agressivo, que impede a repassivação localizada As taxas de corrosão expressam a velocidade do desgaste verificado na superfície metálica A avaliação correta das taxas de corrosão é, de modo geral, de grande importância para a determinação da vida útil provável de equipamentos e instalações industriais Em mm/ano Taxas de corrosão Os valores das taxas de corrosão podem ser expressos por meio Da redução de espessura do material por unidades de tempo Em perda de massa por unidade de área, por unidade de tempo Em mg/dm 2 /dia (mdd). Pode ser expressa ainda em milésimos de polegada por ano (mpy) 13
14 Sabe-se há mais de 80 anos que a adição de pequenas quantidades de cobre, fósforo e outros elementos têm um efeito benéfico sobre os aços, reduzindo a velocidade de corrosão quando expostos ao ar O aço Cor-Ten foi desenvolvido originalmente para a indústria ferroviária, e sua grande virtude aparente era permitir a construção de vagões mais leves Mas o grande estímulo ao emprego de aços enriquecidos com esses elementos - chamados de aços de baixa liga e alta resistência resistentes à corrosão atmosférica - foi dado pela companhia norte americana United States Steel Corporation Na década de 1930, desenvolveu um aço chamado Cor-Ten A propriedade de resistir à corrosão foi alcançada por casualidade, embora desde o fim do século XIX já se conhecessem as influências benéficas do Cobre e do Fósforo Em 1958, o arquiteto Eero Saarinen utilizou-o na construção de um edifício em Moline, no estado de Illinois Desde o lançamento do Cor-Ten até os nossos dias, desenvolveram-se outros aços com comportamentos semelhantes, formando a família de aços O aço foi deixado aparente nessa obra, tendo o arquiteto considerado que a ferrugem que sobre ele se formava constituía por si mesma um revestimento não só aceitável, como atraente O pleno esclarecimento do mecanismo responsável pela formação da pátina protetora só veio a ser alcançado já nos anos 70 Enquadrados em diversas normas, como NBR 5008, 5920, 5921 e 7007 e as norteamericanas ASTM A 242, A 588 e A 709, que especificam limites de composição química e propriedades mecânicas, estes aços tem sido utilizados no mundo todo na construção de pontes, viadutos, edifícios, silos, torres de transmissão de energia, etc Sua grande vantagem, além de dispensarem a pintura em certos ambientes É possuírem uma resistência maior que a dos aços comuns Em ambientes extremamente agressivos, como regiões que apresentam grande poluição por dióxido de enxofre ou aquelas próximas da orla marítima A pintura lhes confere uma proteção superior àquela conferida aos aços comuns 14
15 Composição química do aço A formação da pátina é função de alguns fatores Geometria da peça Composição química do aço A formação da pátina é função de alguns fatores Geometria da peça Do que depende a formação da pátina Fatores ambientais Os principais elementos de liga que aumentam a resistência frente à corrosão atmosférica, favorecendo a formação da pátina Entretanto, o fósforo deve ser mantido em baixos teores (menores que 0,1%), sob pena de prejudicar propriedades mecânicas do aço e sua soldabilidade São o cobre e o fósforo (o cromo, o níquel, e o silício também exercem efeitos secundários) Do que depende a formação da pátina Como a presença de SO 2 e NaCl na atmosfera, a temperatura, a força dos ventos (direção, velocidade e frequência), os ciclos de umedecimento e secagem, etc Fatores ambientais Enquanto o SO 2, até certos limites, favorece o desenvolvimento da pátina, o NaCl das atmosferas marítimas prejudica suas propriedades protetoras Não se recomenda o uso de aços não protegidos em atmosferas marinhas onde a taxa de deposição de cloretos exceda 300 μg/m 2 /dia Composição química do aço A formação da pátina é função de alguns fatores Geometria da peça Do que depende a formação da pátina Do que depende a formação da pátina Fatores ambientais Os ventos, que carreiam agentes agressivos até o local onde está o metal, tem importante efeito sobre os ciclos de umedecimento e secagem: tais ciclos são essenciais no desenvolvimento de películas protetoras O efeito da temperatura, embora provável, ainda não foi claramente caracterizado 15
16 Composição química do aço A formação da pátina é função de alguns fatores Geometria da peça Jamais utilizar parafusos galvanizados em estruturas de aço sem pintura Pois o zinco (e o aço do parafuso) servirá de ânodo de sacrifício para a estrutura Do que depende a formação da pátina Assim, por exemplo, sob condições de contínuo molhamento, determinadas por secagem insatisfatória, a formação da pátina fica gravemente prejudicada Fatores ambientais Esse fenômeno é atribuído à influência de seções abertas/fechadas, drenagem correta da água e outros fatores que atuam diretamente sobre os ciclos de umedecimento e secagem Condições para a formação da pátina protetora De modo geral, a velocidade de corrosão dos aços é estabilizada na maior parte das atmosferas após três ou quatro anos de exposição Uma condição importante para a formação da pátina protetora é a existência de períodos de umedecimento e secagem alternados Em áreas abrigadas da chuva, a pátina marrom escura avermelhada não é normalmente obtida Explicam por quê diferentes estruturas do mesmo aço dispostas lado a lado podem ser atacadas de maneira distinta E a superfície metálica fica recoberta por uma camada de ferrugem de coloração marrom amarela que é menos protetora do que a pátina bem formada, mas mais compacta e aderente do que aquela formada sobre o aço carbono comum na mesma condição Em exposições internas, nenhuma diferença sistemática tem sido observada entre os aços e os aços carbono estruturais comuns O desempenho do aço patinável pintado com certo sistema de pintura costuma ser superior quando o mesmo sistema é aplicado sobre os aços carbono estruturais, desde que o meio promova a formação da pátina Condições para a formação da pátina protetora Em áreas rurais a velocidade de corrosão também é normalmente pequena tanto para os aços carbono estruturais quanto para os aços As baixas velocidades de corrosão observadas em ensaios comparativos entre aços e aços estruturais comuns são devidas primordialmente à baixa corrosividade do meio e não devido à composição química diferenciada do aço E o período de tempo necessário para o desenvolvimento de uma pátina protetora e de boa aparência pode ser muito longo Condições para a formação da pátina protetora Uma eventual falha no revestimento levará à formação de produtos de corrosão bem menos volumosos do que aqueles formados sobre os aços comuns Nestas condições, a durabilidade do sistema costuma ser superior à soma das durabilidades propiciadas isoladamente pela proteção do revestimento e pela natureza do material, isto é, há sinergia dos mecanismos Aumentando a durabilidade do revestimento 16
17 Condições para a formação da pátina protetora Comportamento de um aço patinável e de um aço carbono estrutural expostos à atmosfera industrial, após entalhe na pintura Condições para a formação da pátina protetora Atmosferas contendo gases ou particulados corrosivos necessitam de pintura (ou outra forma de proteção) em ambientes onde a pátina protetora não pode ser formada totalmente Locais sujeitos à névoa salina Aplicações onde o aço permanece continuamente submerso em água ou enterrado no solo Aplicações onde o aço está em contato direto com madeiras ou materiais porosos Condições para a formação da pátina protetora Atmosferas contendo gases ou particulados corrosivos necessitam de pintura (ou outra forma de proteção) em ambientes onde a pátina protetora não pode ser formada totalmente Locais sujeitos à névoa salina Como em áreas industriais com alto teor de óxidos de enxofre (> 100μg/m 3 ), cloreto de amônia, ácido clorídrico, etc Aplicações onde o aço permanece continuamente submerso em água ou enterrado no solo Aplicações onde o aço está em contato direto com madeiras ou materiais porosos Condições para a formação da pátina protetora Atmosferas contendo gases ou particulados corrosivos Nestes casos, o preparo de superfície e o esquema de pintura escolhido deverá ser o mesmo especificado para o aço carbono estrutural, visto que a pátina protetora não pode ser plenamente desenvolvida nestas condições necessitam de pintura (ou outra forma de proteção) em ambientes onde a pátina protetora não pode ser formada totalmente Locais sujeitos à névoa salina Aplicações onde o aço permanece continuamente submerso em água ou enterrado no solo Em atmosferas altamente contaminadas com cloretos, em especial regiões muito próximas da arrebentação, ou ainda regiões cobertas, nas quais o efeito da lavagem propiciada pelas chuvas não é sentida (com o consequente acúmulo de cloretos) Aplicações onde o aço está em contato direto com madeiras ou materiais porosos A pátina formada não tem características protetoras Recomenda-se a pintura de toda estrutura confeccionada em aço patinável desde que esta esteja a menos de 1 km da orla marinha 17
18 Condições para a formação da pátina protetora Atmosferas contendo gases ou particulados corrosivos necessitam de pintura (ou outra forma de proteção) em ambientes onde a pátina protetora não pode ser formada totalmente Locais sujeitos à névoa salina Tais como adutoras de água Aplicações onde o aço permanece continuamente submerso em água ou enterrado no solo Aplicações onde o aço está em contato direto com madeiras ou materiais porosos Condições para a formação da pátina protetora Atmosferas contendo gases ou particulados corrosivos necessitam de pintura (ou outra forma de proteção) em ambientes onde a pátina protetora não pode ser formada totalmente Locais sujeitos à névoa salina Aplicações onde o aço permanece continuamente submerso em água ou enterrado no solo Que podem reter a umidade permanentemente em contato com o metal Em resumo, podemos afirmar que em situações onde a formação da pátina não é adequada, exigindo o uso de sistemas de proteção (p. ex.: a pintura) Aplicações onde o aço está em contato direto com madeiras ou materiais porosos Os aços e os aços carbono tornam-se praticamente equivalentes na sua aplicação de corrosão atmosférica do aço patinável de corrosão dos aços : objeto de pesquisas no mundo Teoria Quando o aço patinável é exposto a uma atmosfera sulfurosa, a ciclos de umedecimento/secagem alternados e a temperaturas relativamente altas (35-60 C), o cobre e os outros elementos de liga constituintes do aço patinável inibirão o desenvolvimento de magnetita (não protetora) e estimularão Por outro lado, o desenvolvimento de um óxido amorfo, protetor, na interface metal/ferrugem Essa camada, a pátina, é muito pouco porosa e isola eficientemente o metal dos constituintes agressivos existentes na atmosfera, como a água, o oxigênio e outros íons 18
19 Simplifique as formas Quanto mais simples a forma dada à construção, maiores as chances de que uma boa proteção frente à corrosão seja alcançada Evitar umidade residual Como já visto, a corrosão não ocorre na ausência de umidade Um dos fatores mais importantes no projeto para o controle da corrosão é o de evitar Uma tarefas importantes do engenheiro é garantir que a construção esteja protegida da umidade tanto quanto possível Onde depósitos de compostos solúveis em água e umidade possam se acumular, e não se tornem visíveis ou acessíveis à manutenção Qualquer região onde duas superfícies estejam muito próximas também se qualifica como uma fresta Várias situações deste tipo devem ser analisadas: parafusos, rebites, cantoneiras perfiladas, soldas irregulares, respingos de solda, cantos vivos, descontinuidades e soldas intermitentes Os perfis devem ser dispostos de modo que a umidade não fique retida e que a construção possa ser devidamente pintada e mantida Evitar umidade residual por Pode se estabelecer sempre quando existir uma fresta que possa coletar água (outro líquido) ou depósitos sólidos tais como lama e pós diversos Evite a criação de cavidades; juntas parafusadas são preferíveis às soldadas em campo, que necessitam de controle e testes Devem-se criar condições para que, uma vez que a umidade tenha se depositado, possa secar O lixamento de cantos vivos, soldas e respingos ajudarão a prevenir as, assim como a proteção adicional da tinta de fundo, feita nestas regiões As juntas devem ser dispostas de modo a propiciar linhas limpas, contínuas. Juntas soldadas são preferíveis às parafusadas ou rebitadas Esta aplicação deverá ser feita cuidadosamente, com pincel (ou spray) e fornecerá uma barreira adicional contra a corrosão 19
20 galvânica Evite todos os pares bimetálicos possíveis galvânica Um meio comum de se prevenir da corrosão galvânica é intercalar, entre os dois metais ou ligas, um isolante elétrico Não é verdadeiro dizer que a junção de metais distantes na série galvânica provocará problemas de corrosão O material isolante não deve ser poroso, pois ele poderia absorver água e propiciar a formação da corrosão por Existem inúmeros exemplos de metais ou ligas conectados eletricamente que nunca apresentaram problemas A corrosão só acontecerá se uma cela galvânica for formada, isto é, se houver dois metais ou ligas situados distantes na série galvânica conectados eletricamente e imersos em um mesmo eletrólito A utilização de juntas coladas auxilia em muito a prevenção da corrosão galvânica, impedindo o ingresso de eletrólitos Algumas vezes é conveniente introduzir uma peça intermediária, que pode ser facilmente substituída ou então que tenha um potencial intermediário Os efeitos galvânicos acontecem quando a diferença de potencial medida (p. ex.: com um multímetro) entre os dois metais ou ligas imersos no mesmo eletrólito particular supera os 0,05 V Um exemplo desta última situação é o do uso de arruelas de zinco entre parafusos de aço conectando chapas de alumínio galvânica Outra solução possível é a utilização de pintura galvânica Os parafusos e os aços a serem unidos devem, obrigatoriamente, possuir composições químicas parecidas, sob o risco do aparecimento da corrosão galvânica Recomenda-se pintar os componentes mais nobres e o menos nobres Parafusos de aço galvanizado unindo estruturas de aços Entretanto, parafusos de aço carbono galvanizados tem sido utilizados algumas vezes em substituição aos de aço patinável Caso não se possa pintar todo o conjunto, recomenda-se pintar o membro mais nobre do par galvânico (membro catódico) A pintura do membro menos nobre (anódico) pode agravar a situação, pois ela poderá levar ao intenso ataque por nos poros do revestimento O zinco, sendo muito mais anódico do que os aços carbono, protegerá a estrutura (e os próprios parafusos) enquanto estiver presente Entretanto, aços utilizados em estruturas, sendo mais catódicos do que os aços carbono comuns, costumam promover a rápida deterioração da camada de zinco do parafuso Quando todo o zinco estiver oxidado, restará o parafuso que, não tendo composição química comparável aos aços, sofrerá rápida degradação, pela própria característica anódica dos aços comuns quando comparados aos aços 20
21 galvânica A velocidade de corrosão resultante da ação galvânica dependerá, frequentemente, das áreas relativas expostas dos dois metais galvânica Diferenças de composição, ou de condições superficiais de metais similares podem resultar, frequentemente, em celas galvânicas Razão de áreas desfavorável Pequenas áreas anódicas, em combinação com grandes áreas catódicas devem ser evitadas tanto quanto possível Conexão de materiais novos e antigos Por exemplo, o aço carbono de superfície limpa é tipicamente anódico com relação ao aço carbono enferrujado Uma pequena área de zinco corroerá rapidamente quando acoplado à uma grande área de aço carbono, embora o aço receba pouca proteção O ataque galvânico pode ser prevenido através da utilização, quando possível, de isolantes elétricos, de modo a prevenir o contato elétrico entre ambas as partes É comum observar em reparos de tubulações enterradas que a linha nova corrói muito mais rapidamente que o trecho de linha velha A tubulação mais velha causa a corrosão acelerada da nova tubulação devido à ação galvânica O metal mais nobre pode ser isolado do menos nobre pelo uso de arruelas plásticas, fitas adesivas especiais, cerâmicas, etc A instalação de anodos de sacrifício locais ou a aplicação de um isolante elétrico resolverá o problema galvânica Tubulações de aço enterradas no solo ou na água, conectados eletricamente a vergalhões de aço existentes no concreto reforçado é outro problema relacionado à formação de celas galvânicas galvânica Em temperaturas normais, os tubos de aço galvanizado são anódicos com relação ao aço não protegido Aterramento elétrico A tubulação de aço deve sempre ser protegida do contato com o vergalhão imerso no concreto, pois o vergalhão está em uma situação passiva, causando um ataque intenso na tubulação A reversão do zinco à 60 C Entretanto, em aplicações de água quente (de 60 C a 77 C), o potencial do zinco decresce, isto é, se torna mais catódico, podendo causar a reversão entre catodos e anodos A ação de sacrifício do zinco é causada pela diferença de potencial relativa existente entre o zinco e o aço à temperatura ambiente O aço então se torna anódico face ao zinco Desse modo, tubulações de aço galvanizado não devem ser usados quando a água transportada estiver na temperatura compreendida entre 60 C a 77 C, pois o aço será ânodo de sacrifício nesta condição peculiar 21
22 por aeração diferencial Uma cela de aeração diferencial pode ser desenvolvida em qualquer situação onde a água estiver em contato com uma superfície por aeração diferencial Assim, todo cuidado deve ser tomado para se prevenir do ingresso da água em áreas onde ela possa ficar retida por longos períodos Sujeiras depositadas Exemplos de criação de pilhas de aeração diferencial Uso de materiais absorventes em contato com superfícies metálicas Drenagem e ventilação Frestas potenciais devem ser preenchidas com selantes (epoxídicos, poliuretânicos ou à base de silicone); os componentes devem, costumeiramente, possuir furos de drenagem Permita a ventilação de todo conjunto, para que a água possa evaporar por aeração diferencial por aeração diferencial Sujeiras depositadas Exemplos de criação de pilhas de aeração diferencial Uso de materiais absorventes em contato com superfícies metálicas Drenagem e ventilação Sujeiras depositadas Exemplos de criação de pilhas de aeração diferencial Uso de materiais absorventes em contato com superfícies metálicas Drenagem e ventilação Sujeiras que absorvem ou mantém água (ou lama), produtos de corrosão, folhas, tecidos e papel Em contato com a estrutura promovem a formação de pilhas de aeração diferencial Estes materiais podem absorver água como uma esponja, possibilitando a ocorrência de celas de aeração diferencial na interface material absorvente/metal Materiais porosos e absorventes (p. ex.: lã de rocha, não-tecidos, feltro, etc) tem sido muito utilizados como isolantes térmicos, isolantes acústicos, etc. Os materiais absorventes devem ser evitados em todas as situações em que a umidade relativa do ambiente exceda (costumeiramente) os 60% 22
23 por aeração diferencial por aeração diferencial Sujeiras depositadas Exemplos de criação de pilhas de aeração diferencial Uso de materiais absorventes em contato com superfícies metálicas Drenagem e ventilação Sujeiras depositadas Exemplos de criação de pilhas de aeração diferencial Uso de materiais absorventes em contato com superfícies metálicas Drenagem e ventilação Não minimize o potencial da corrosão! Cada gota age como uma cela de aeração diferencial, mas, se a superfície tiver a oportunidade de secar, a corrosão será limitada Quando a chuva ou o orvalho umedece uma estrutura metálica, pontos de ferrugem serão observados após a evaporação da água Problemas sérios podem ser observados nas partes inferiores das estruturas, onde a ventilação é menos eficiente 23
24 Referências bibliográficas Aulas Profº Leonardo Miranda Aulas Profº Marco Argenta 24
CORROSÃO PATOLOGIA E RECUPERAÇÃO DAS CONSTRUÇÕES. Prof. Mazer AULA 05
 AULA 05 Prof. Mazer PATOLOGIA E RECUPERAÇÃO DAS CONSTRUÇÕES 2 FUNDAMENTOS GERAIS: O concreto protege a armadura de duas formas: - Confere uma barreira física separando o aço do meio-ambiente - A água no
AULA 05 Prof. Mazer PATOLOGIA E RECUPERAÇÃO DAS CONSTRUÇÕES 2 FUNDAMENTOS GERAIS: O concreto protege a armadura de duas formas: - Confere uma barreira física separando o aço do meio-ambiente - A água no
1 Introdução Princípios Básicos da Corrosão Eletroquímica... 5
 Sumário 1 Introdução................................ 1 2 Princípios Básicos da Corrosão Eletroquímica........ 5 2.1 POTENCIAIS ELETROQUÍMICOS............................ 5 2.2 PILHAS DE CORROSÃO...................................17
Sumário 1 Introdução................................ 1 2 Princípios Básicos da Corrosão Eletroquímica........ 5 2.1 POTENCIAIS ELETROQUÍMICOS............................ 5 2.2 PILHAS DE CORROSÃO...................................17
Corrosão: Definições e implicações práticas Aspectos termodinâmicos Formas de controle
 Curso Técnico Integrado em Química Físico-química III VÍDEO AULA Corrosão: Definições e implicações práticas Aspectos termodinâmicos Formas de controle 1 Professor: Me. Sebastião Junior T. Vasconcelos
Curso Técnico Integrado em Química Físico-química III VÍDEO AULA Corrosão: Definições e implicações práticas Aspectos termodinâmicos Formas de controle 1 Professor: Me. Sebastião Junior T. Vasconcelos
CORROSÃO ATMOSFÉRICA. É extremamente dependente das condições no local de exposição.
 CORROSÃO ATMOSFÉRICA Ocorre sob um filme fino de eletrólito adsorvido à superfície do metal É extremamente dependente das condições no local de exposição. CORROSÃO ATMOSFÉRICA Classificação das atmosferas:
CORROSÃO ATMOSFÉRICA Ocorre sob um filme fino de eletrólito adsorvido à superfície do metal É extremamente dependente das condições no local de exposição. CORROSÃO ATMOSFÉRICA Classificação das atmosferas:
Corrosão Metálica. Introdução. O que é corrosão? Classificação dos processos de corrosão. Principais tipos de corrosão
 Corrosão Metálica Introdução O estudo da corrosão de superfícies é importante para a solução de problemas de peças e equipamentos. Ter o conhecimento dos tipos de corrosão existentes, compreender os seus
Corrosão Metálica Introdução O estudo da corrosão de superfícies é importante para a solução de problemas de peças e equipamentos. Ter o conhecimento dos tipos de corrosão existentes, compreender os seus
Corrosão das Armaduras das Estruturas de Concreto
 Corrosão das Armaduras das Estruturas de Concreto FELIPE KOBUS, FRANCINE FERNANDES, GIOVANNI GUIDELLI, JAQUELINE F. SOARES, JULYANA ROCHA E MARINA D. TRENTIN Passivação da Armadura no Concreto Passivação
Corrosão das Armaduras das Estruturas de Concreto FELIPE KOBUS, FRANCINE FERNANDES, GIOVANNI GUIDELLI, JAQUELINE F. SOARES, JULYANA ROCHA E MARINA D. TRENTIN Passivação da Armadura no Concreto Passivação
COLETÂNEA DE INFORMAÇÕES TÉCNICAS AÇO INOXIDÁVEL. Seleção dos aços inoxidáveis para aplicações externas em construção civil
 COLETÂNEA DE INFORMAÇÕES TÉCNICAS AÇO INOXIDÁVEL Seleção dos aços inoxidáveis para aplicações externas em construção civil Introdução Os aços inoxidáveis são selecionados para aplicações arquiteturais,
COLETÂNEA DE INFORMAÇÕES TÉCNICAS AÇO INOXIDÁVEL Seleção dos aços inoxidáveis para aplicações externas em construção civil Introdução Os aços inoxidáveis são selecionados para aplicações arquiteturais,
Corrosão e degradação de materiais. Modificação aparência. Interação Comprometimento pp mecânicas
 Corrosão e degradação de materiais Modificação aparência Interação Comprometimento pp mecânicas Deterioração é diferente para os diversos tipos de materiais: M Dissolução (corrosão) Formação de crosta
Corrosão e degradação de materiais Modificação aparência Interação Comprometimento pp mecânicas Deterioração é diferente para os diversos tipos de materiais: M Dissolução (corrosão) Formação de crosta
Índice. Agradecimentos... Prefácio da Edição Revisada... Prefácio...
 Índice Agradecimentos... Prefácio da Edição Revisada... Prefácio... VII IX XI CAPÍTULO 1 INTRODUÇÃO... 1 1.1 Definição da Corrosão... 1 1.2 Importância Econômica da Corrosão... 3 1.3 Análise Econômica
Índice Agradecimentos... Prefácio da Edição Revisada... Prefácio... VII IX XI CAPÍTULO 1 INTRODUÇÃO... 1 1.1 Definição da Corrosão... 1 1.2 Importância Econômica da Corrosão... 3 1.3 Análise Econômica
ELECTROQUÍMICA E CORROSÃO
 Valentim M B Nunes, 2003 ELECTROQUÍMICA E CORROSÃO CORROSÃO 1. Corrosão Podemos definir como corrosão a interacção físico-química de um metal com o meio do qual resultam alterações das propriedades do
Valentim M B Nunes, 2003 ELECTROQUÍMICA E CORROSÃO CORROSÃO 1. Corrosão Podemos definir como corrosão a interacção físico-química de um metal com o meio do qual resultam alterações das propriedades do
PMT 2507 Corrosão e Proteção dos Materiais Segunda Lista de Exercício Prof. Dr. Hercílio Gomes de Melo
 PMT 2507 Corrosão e Proteção dos Materiais Segunda Lista de Exercício 2015 Prof. Dr. Hercílio Gomes de Melo 1 Esquematize um sistema de proteção catódica por anodo de sacrifício. Indique claramente o fluxo
PMT 2507 Corrosão e Proteção dos Materiais Segunda Lista de Exercício 2015 Prof. Dr. Hercílio Gomes de Melo 1 Esquematize um sistema de proteção catódica por anodo de sacrifício. Indique claramente o fluxo
CORROSÃO EM FRESTAS ("crevice corrosion")
 CORROSÃO EM FRESTAS ("crevice corrosion") Corrosão relativamente localizada em frestas de uma peça metálica, ou formadas pela sobreposição de outro metal ou de materiais inertes sobre o metal. Exemplos
CORROSÃO EM FRESTAS ("crevice corrosion") Corrosão relativamente localizada em frestas de uma peça metálica, ou formadas pela sobreposição de outro metal ou de materiais inertes sobre o metal. Exemplos
FORMAÇÃO DE CORROSÃO GALVÂNICA
 FORMAÇÃO DE CORROSÃO GALVÂNICA EJC ENGENHARIA DE UTILIDADES WWW.EJCENGENHARIA.COM.BR CORROSÃO GALVÂNICA O aço inox ou o alumínio, quando utilizados em placas de identificação para vasos de pressão, através
FORMAÇÃO DE CORROSÃO GALVÂNICA EJC ENGENHARIA DE UTILIDADES WWW.EJCENGENHARIA.COM.BR CORROSÃO GALVÂNICA O aço inox ou o alumínio, quando utilizados em placas de identificação para vasos de pressão, através
Parafusos estruturais de aço ASTM A325 tipo 3 na construção em aço
 ArtigoTécnico Fabio Domingos Pannoni, Ph.D. Consultor Técnico - Gerdau Aços Brasil fabio.pannoni@gerdau.com.br Parafusos estruturais de aço ASTM A325 tipo 3 na construção em aço INTRODUÇÃO A construção
ArtigoTécnico Fabio Domingos Pannoni, Ph.D. Consultor Técnico - Gerdau Aços Brasil fabio.pannoni@gerdau.com.br Parafusos estruturais de aço ASTM A325 tipo 3 na construção em aço INTRODUÇÃO A construção
Disciplina: Química Professor: Lourival Neto Cidade: Uberlândia
 Disciplina: Química Professor: Lourival Neto Cidade: Uberlândia Introdução Corrosão Tipos de corrosão Corrosão Eletroquímica Exemplos e reações Corrosão Química Exemplos e reações Corrosão Eletrolítica
Disciplina: Química Professor: Lourival Neto Cidade: Uberlândia Introdução Corrosão Tipos de corrosão Corrosão Eletroquímica Exemplos e reações Corrosão Química Exemplos e reações Corrosão Eletrolítica
PRINCÍPIOS DA PROTEÇÃO DE ESTRUTURAS METÁLICAS EM SITUAÇÃO DE CORROSÃO E INCÊNDIO
 COLETÂNEA DO USO DO AÇO PRINCÍPIOS DA PROTEÇÃO DE ESTRUTURAS METÁLICAS EM SITUAÇÃO DE CORROSÃO E INCÊNDIO ª Edição 004 Volume Fábio Domingos Pannoni, M.Sc., Ph.D. Colaboração: Carlos Gaspar - Revisão Andréa
COLETÂNEA DO USO DO AÇO PRINCÍPIOS DA PROTEÇÃO DE ESTRUTURAS METÁLICAS EM SITUAÇÃO DE CORROSÃO E INCÊNDIO ª Edição 004 Volume Fábio Domingos Pannoni, M.Sc., Ph.D. Colaboração: Carlos Gaspar - Revisão Andréa
OXIDAÇÃO DE METAIS INTRODUÇÃO
 OXIDAÇÃO DE METAIS INTRODUÇÃO Oxidação é uma palavra do âmbito da química que significa a perda de elétrons, mesmo que não seja causada pelo oxigênio. Indica também o processo de oxidar, ou seja, de combinar
OXIDAÇÃO DE METAIS INTRODUÇÃO Oxidação é uma palavra do âmbito da química que significa a perda de elétrons, mesmo que não seja causada pelo oxigênio. Indica também o processo de oxidar, ou seja, de combinar
Corrosão por frestas em um sistema de tubulação de aço inox 304L causa: soldagem sem penetração completa
 CORROSÃO EM FRESTAS CARACTERÍSTICAS Tipo de corrosão localizada; Frequentemente associada a líquidos estagnados no interior de furos, superfícies de gaxetas, juntas sobrepostas, depósitos superficiais,
CORROSÃO EM FRESTAS CARACTERÍSTICAS Tipo de corrosão localizada; Frequentemente associada a líquidos estagnados no interior de furos, superfícies de gaxetas, juntas sobrepostas, depósitos superficiais,
Carbonatação do concreto (despassiva a armadura porque reduz o ph do concreto)
 CAUSAS DA CORROSÃO, FATORES DESENCADEADORES E FATORES ACELERANTES Profa. Eliana Barreto Monteiro CAUSAS DA CORROSÃO, FATORES DESENCADEADORES E FATORES ACELERANTES CAUSAS DA CORROSÃO A perda da passivação
CAUSAS DA CORROSÃO, FATORES DESENCADEADORES E FATORES ACELERANTES Profa. Eliana Barreto Monteiro CAUSAS DA CORROSÃO, FATORES DESENCADEADORES E FATORES ACELERANTES CAUSAS DA CORROSÃO A perda da passivação
15. Trabalho Experimental - Proteção Catódica
 15. Trabalho Experimental - Proteção Catódica 15.1 - Introdução A proteção catódica é um método de controle de corrosão que consiste em transformar a estrutura à proteger no cátodo de um célula eletroquímica
15. Trabalho Experimental - Proteção Catódica 15.1 - Introdução A proteção catódica é um método de controle de corrosão que consiste em transformar a estrutura à proteger no cátodo de um célula eletroquímica
ELETROQUÍMICA. paginapessoal.utfpr.edu.br/lorainejacobs. Profª Loraine Jacobs DAQBI
 lorainejacobs@utfpr.edu.br paginapessoal.utfpr.edu.br/lorainejacobs Profª Loraine Jacobs DAQBI CORROSÃO Corrosão Processo espontâneo Contato do metal com um eletrólito Reações Anódicas e Catódicas Frequente
lorainejacobs@utfpr.edu.br paginapessoal.utfpr.edu.br/lorainejacobs Profª Loraine Jacobs DAQBI CORROSÃO Corrosão Processo espontâneo Contato do metal com um eletrólito Reações Anódicas e Catódicas Frequente
CORROSÃO. Processo de destruição superficial de um metal, dando origem a sais iónicos (óxidos hidróxidos) do referido metal
 CORROSÃO Processo de destruição superficial de um metal, dando origem a sais iónicos (óxidos hidróxidos) do referido metal Corrosão Química: reacção superficial de transferência de carga em ambiente seco
CORROSÃO Processo de destruição superficial de um metal, dando origem a sais iónicos (óxidos hidróxidos) do referido metal Corrosão Química: reacção superficial de transferência de carga em ambiente seco
NOVOS AÇOS ESTRUTURAIS DE ELEVADA RESISTÊNCIA À CORROSÃO MARINHA
 Contribuição técnica nº 21 NOVOS AÇOS ESTRUTURAIS DE ELEVADA RESISTÊNCIA À CORROSÃO MARINHA Autores: Rogério Augusto Carneiro Evandro de Azevedo Alvarenga NOVOS AÇOS ESTRUTURAIS DE ELEVADA RESISTÊNCIA
Contribuição técnica nº 21 NOVOS AÇOS ESTRUTURAIS DE ELEVADA RESISTÊNCIA À CORROSÃO MARINHA Autores: Rogério Augusto Carneiro Evandro de Azevedo Alvarenga NOVOS AÇOS ESTRUTURAIS DE ELEVADA RESISTÊNCIA
Catálogo de produtos
 Catálogo de produtos Galvanização a fogo (zincagem por imersão a quente) - Conforme NBR 6323 O processo de zincagem por imersão a quente é o mesmo que qualquer produto, podendo variar na espessura da camada
Catálogo de produtos Galvanização a fogo (zincagem por imersão a quente) - Conforme NBR 6323 O processo de zincagem por imersão a quente é o mesmo que qualquer produto, podendo variar na espessura da camada
Painel: Corrosão em Ativos de Geração
 Painel: Corrosão em Ativos de Geração A Corrosão em Linhas de Transmissão e Subestações Alberto P. Ordine, Cristina C. Amorim, Elber V. Bendinelli, Marcos M. Sá Centro de Pesquisas de Energia Elétrica
Painel: Corrosão em Ativos de Geração A Corrosão em Linhas de Transmissão e Subestações Alberto P. Ordine, Cristina C. Amorim, Elber V. Bendinelli, Marcos M. Sá Centro de Pesquisas de Energia Elétrica
A UTILIZAÇÃO DO AÇO PATINÁVEL EM ESTRUTURAS ARQUITETÔNICAS
 1 A UTILIZAÇÃO DO AÇO PATINÁVEL EM ESTRUTURAS ARQUITETÔNICAS FARIA,Marianna Ribeiro (Unitri) naninha_282@hotmail.com PEIXOTO, Sergio Augusto Pedroso (Unitri) sappeixoto@hotmail.com RESUMO A utilização
1 A UTILIZAÇÃO DO AÇO PATINÁVEL EM ESTRUTURAS ARQUITETÔNICAS FARIA,Marianna Ribeiro (Unitri) naninha_282@hotmail.com PEIXOTO, Sergio Augusto Pedroso (Unitri) sappeixoto@hotmail.com RESUMO A utilização
Estudo das reações químicas para geração de energia.
 Estudo das reações químicas para geração de energia. Células Galvânicas (Pilhas e Baterias): Conversão de Energia Química em Energia Elétrica (Reações Espontâneas) Células Eletrolíticas: Conversão de Energia
Estudo das reações químicas para geração de energia. Células Galvânicas (Pilhas e Baterias): Conversão de Energia Química em Energia Elétrica (Reações Espontâneas) Células Eletrolíticas: Conversão de Energia
Aluno (a): Data: / / Obs: Data de entrega: 12/11 (Todas as respostas devem apresentar justificativa) Resposta à caneta, organizada e completa.
 Disciplina: Química Turma: 2 série Escola SESI Jundiaí Professor: Rosilene Paulino da Silva Aluno (a): Data: / / 2018. Obs: Data de entrega: 12/11 (Todas as respostas devem apresentar justificativa) Resposta
Disciplina: Química Turma: 2 série Escola SESI Jundiaí Professor: Rosilene Paulino da Silva Aluno (a): Data: / / 2018. Obs: Data de entrega: 12/11 (Todas as respostas devem apresentar justificativa) Resposta
Metais não ferrosos Prof. Dr. Julio Cesar Sabadini de Souza
 Ligas não ferrosas Metais não ferrosos Prof. Dr. Julio Cesar Sabadini de Souza Dentre as mais importantes na construção civil estão incluídas as ligas de Alumínio Cobre Zinco Alumínio É o terceiro elemento
Ligas não ferrosas Metais não ferrosos Prof. Dr. Julio Cesar Sabadini de Souza Dentre as mais importantes na construção civil estão incluídas as ligas de Alumínio Cobre Zinco Alumínio É o terceiro elemento
Aula 20 Eletrodeposição
 Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula 20 Eletrodeposição Dr. Tiago P. Camargo Eletrólise Eletroquímica Processo inverso das pilhas. Células galvânicas
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula 20 Eletrodeposição Dr. Tiago P. Camargo Eletrólise Eletroquímica Processo inverso das pilhas. Células galvânicas
Catálise e Inibição de Reação Eletroquímica
 Catálise e Inibição de Reação Eletroquímica - Se o material do eletrodo não se transforma em produto; - em principio, é apenas para transferir elétrons; - mas, podendo também participar adsorvendo reagentes
Catálise e Inibição de Reação Eletroquímica - Se o material do eletrodo não se transforma em produto; - em principio, é apenas para transferir elétrons; - mas, podendo também participar adsorvendo reagentes
Corrosão em Juntas Soldadas
 "Corrosão é um assunto bastante complexo e a compreensão dos mecanismos atuantes em diferentes condições de meio agressivo exige muitos conceitos com os quais nós (da soldagem) normalmente não estamos
"Corrosão é um assunto bastante complexo e a compreensão dos mecanismos atuantes em diferentes condições de meio agressivo exige muitos conceitos com os quais nós (da soldagem) normalmente não estamos
Soldagem por Alta Frequência. Maire Portella Garcia -
 Soldagem por Alta Frequência Maire Portella Garcia - E-mail: mairegarcia@bol.com.br Freqüência: 450KHZ Profundidade por aquecimento: Somente poucos centésimos de milímetros condutividade térmica provoca
Soldagem por Alta Frequência Maire Portella Garcia - E-mail: mairegarcia@bol.com.br Freqüência: 450KHZ Profundidade por aquecimento: Somente poucos centésimos de milímetros condutividade térmica provoca
Cobertura Quadra Poliesportiva Escola Batista Timóteo - MG Foto: Edmar Silva. Inox é a solução para coberturas e fachadas
 Inox é a solução para coberturas e fachadas Cobertura Quadra Poliesportiva Escola Batista Timóteo - MG Foto: Edmar Silva Cobertura Quadra Poliesportiva Sesi Timóteo - MG Foto: Edmar Silva Beleza e durabilidade
Inox é a solução para coberturas e fachadas Cobertura Quadra Poliesportiva Escola Batista Timóteo - MG Foto: Edmar Silva Cobertura Quadra Poliesportiva Sesi Timóteo - MG Foto: Edmar Silva Beleza e durabilidade
Fotografia 29 - Microestrutura destacada em vermelho na Fotografia 28
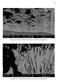 60 Fotografia 29 - Microestrutura destacada em vermelho na Fotografia 28 Fotografia 30 - Microestrutura destacada em amarelo na Fotografia 28 61 Tabela 11- Composição química do revestimento da chapa L
60 Fotografia 29 - Microestrutura destacada em vermelho na Fotografia 28 Fotografia 30 - Microestrutura destacada em amarelo na Fotografia 28 61 Tabela 11- Composição química do revestimento da chapa L
Autor: Celso Gnecco...Gerente de Treinamento Técnico... Sherwin-Williams do Brasil - Divisão Sumaré
 Autor: Celso Gnecco...Gerente de Treinamento Técnico... Sherwin-Williams do Brasil - Divisão Sumaré Se a galvanização a quente já é, por si mesma, uma grande proteção anticorrosiva, então por que pintá-la?
Autor: Celso Gnecco...Gerente de Treinamento Técnico... Sherwin-Williams do Brasil - Divisão Sumaré Se a galvanização a quente já é, por si mesma, uma grande proteção anticorrosiva, então por que pintá-la?
Processo de alteração prejudicial e indesejável de um determinado material
 CORROSÃO PRINCÍPIOS BÁSICOS O termo corrosão é originário da palavra latina corredere que significa consumir rapidamente como o rato. Nas traduções das línguas portuguesas a palavra ficou como corrosão
CORROSÃO PRINCÍPIOS BÁSICOS O termo corrosão é originário da palavra latina corredere que significa consumir rapidamente como o rato. Nas traduções das línguas portuguesas a palavra ficou como corrosão
Factores Influentes na Corrosão e Protecção de Metais. Química 12º Ano
 Factores Influentes na Corrosão e Protecção de Metais Química 12º Ano Unidade 1 Metais e ligas metálicas Actividades de Projecto Laboratorial Outubro 2005 Jorge R. Frade, Ana Teresa Paiva Dep. Eng. Cerâmica
Factores Influentes na Corrosão e Protecção de Metais Química 12º Ano Unidade 1 Metais e ligas metálicas Actividades de Projecto Laboratorial Outubro 2005 Jorge R. Frade, Ana Teresa Paiva Dep. Eng. Cerâmica
Materiais e Corrosão - Cap 3 FORMAS DE CORROSÃO. Fontana, cap. 3. Formas de Corrosão- A.Simões_2006 3a.1
 Materiais e Corrosão - Cap 3 FORMAS DE CORROSÃO Fontana, cap. 3 Formas de Corrosão- A.Simões_2006 3a.1 FORMAS DE CORROSÃO No aspecto morfológico, a corrosão pode ser classificada em duas grandes categorias:
Materiais e Corrosão - Cap 3 FORMAS DE CORROSÃO Fontana, cap. 3 Formas de Corrosão- A.Simões_2006 3a.1 FORMAS DE CORROSÃO No aspecto morfológico, a corrosão pode ser classificada em duas grandes categorias:
UNIVERSIDADE DE SÃO PAULO FACULDADE DE ODONTOLOGIA. Roteiro de estudos Corrosão Data: 17/04/2013. Ambiente bucal favorece a degradação dos materiais
 UNIVERSIDADE DE SÃO PAULO FACULDADE DE ODONTOLOGIA DEPARTAMENTO DE BIOMATERIAIS E BIOLOGIA ORAL Roteiro de estudos Corrosão Data: 17/04/2013 Corrosão de ligas metálicas e suas implicações clínicas 1 Introdução
UNIVERSIDADE DE SÃO PAULO FACULDADE DE ODONTOLOGIA DEPARTAMENTO DE BIOMATERIAIS E BIOLOGIA ORAL Roteiro de estudos Corrosão Data: 17/04/2013 Corrosão de ligas metálicas e suas implicações clínicas 1 Introdução
Corrosão e Eletroquímica
 Química Aplicada Corrosão e Eletroquímica O corrosionista tem por objetivo estudar a deterioração dos materiais pela ação do meio em que são usados. Existe um grande interesse prático neste estudo uma
Química Aplicada Corrosão e Eletroquímica O corrosionista tem por objetivo estudar a deterioração dos materiais pela ação do meio em que são usados. Existe um grande interesse prático neste estudo uma
PROTECÇÃO DOS METAIS
 PROTECÇÃO DOS METAIS FORMAÇÃO DE LIGAS Neste caso associase o metal a proteger a outro, originando uma liga altamente resistente à corrosão. Exemplo: aço inox PROTECÇÃO CATÓDICA A protecção catódica é
PROTECÇÃO DOS METAIS FORMAÇÃO DE LIGAS Neste caso associase o metal a proteger a outro, originando uma liga altamente resistente à corrosão. Exemplo: aço inox PROTECÇÃO CATÓDICA A protecção catódica é
TECNOLOGIA EPD-H A TECNOLOGIA
 A TECNOLOGIA Tecnologia de decapagem e passivação feita através de reação eletrolítica, desenvolvida pelo GRUPO HUMMA para aplicação em aços inoxidáveis e ligas especiais para limpeza de peças, componentes
A TECNOLOGIA Tecnologia de decapagem e passivação feita através de reação eletrolítica, desenvolvida pelo GRUPO HUMMA para aplicação em aços inoxidáveis e ligas especiais para limpeza de peças, componentes
Centro de Pesquisas de Energia Elétrica. Corrosão e Proteção Anticorrosiva. Cristina Amorim. Laboratório de Corrosão do Cepel
 Centro de Pesquisas de Energia Elétrica Corrosão e Proteção Anticorrosiva Cristina Amorim Laboratório de Corrosão do Cepel Departamento de Laboratórios do Fundão (DLF) Departamento de Materiais, Eficiência
Centro de Pesquisas de Energia Elétrica Corrosão e Proteção Anticorrosiva Cristina Amorim Laboratório de Corrosão do Cepel Departamento de Laboratórios do Fundão (DLF) Departamento de Materiais, Eficiência
Parte 2. Química Aplicada. Professor Willyan Machado Giufrida
 Tópicos especiais Corrosão na construção civil Parte 2 Propriedades de alguns elementos metálicos Química Aplicada 1 Professor Willyan Machado Giufrida Propriedades Físicas dos Metais São, geralmente,
Tópicos especiais Corrosão na construção civil Parte 2 Propriedades de alguns elementos metálicos Química Aplicada 1 Professor Willyan Machado Giufrida Propriedades Físicas dos Metais São, geralmente,
02/10/2017 ELETRÓLISE AQUOSA
 ELETRÓLISE AQUOSA Ocorre quando um eletrólito é dissolvido em água (havendo ionização ou dissociação do mesmo), além dos seus íons, devemos considerar a ionização da própria água. 1 Experimentalmente,
ELETRÓLISE AQUOSA Ocorre quando um eletrólito é dissolvido em água (havendo ionização ou dissociação do mesmo), além dos seus íons, devemos considerar a ionização da própria água. 1 Experimentalmente,
Química Aplicada. Professor Willyan Machado Giufrida
 Tópicos especiais Corrosão na construção civil Corrosão no Concreto e no Aço Química Aplicada 1 Professor Willyan Machado Giufrida Introdução Desde o início da utilização do concreto armado, nos meados
Tópicos especiais Corrosão na construção civil Corrosão no Concreto e no Aço Química Aplicada 1 Professor Willyan Machado Giufrida Introdução Desde o início da utilização do concreto armado, nos meados
LIMPEZA QUÍMICA E PASSIVAÇÃO. Em Sistemas Críticos de Alta Pureza
 LIMPEZA QUÍMICA E PASSIVAÇÃO Em Sistemas Críticos de Alta Pureza TIPOS DE CONTAMINAÇÃO (FONTES) Contaminação Orgânica Sujidade oriunda de resíduos dos produtos, gorduras, proteínas, óleos, etc. Contaminação
LIMPEZA QUÍMICA E PASSIVAÇÃO Em Sistemas Críticos de Alta Pureza TIPOS DE CONTAMINAÇÃO (FONTES) Contaminação Orgânica Sujidade oriunda de resíduos dos produtos, gorduras, proteínas, óleos, etc. Contaminação
Processo de Soldagem MIG/MAG. Processo MIG / MAG Prof. Vilmar Senger
 Processo de Soldagem MIG/MAG Gases de proteção O ar atmosférico é expulso da região de soldagem por um gás de proteção com o objetivo de evitar a contaminação da poça de fusão. A contaminação é causada
Processo de Soldagem MIG/MAG Gases de proteção O ar atmosférico é expulso da região de soldagem por um gás de proteção com o objetivo de evitar a contaminação da poça de fusão. A contaminação é causada
Robustez e agilidade de montagem comprovada por situações reais de emergência.
 Precisão, segurança, facilidade de montagem e manutenção, fazem da TET a ferramenta perfeita para suas equipes de emergência e manutenção de linhas de transmissão de até 500 kv. Estrutura projetada pela
Precisão, segurança, facilidade de montagem e manutenção, fazem da TET a ferramenta perfeita para suas equipes de emergência e manutenção de linhas de transmissão de até 500 kv. Estrutura projetada pela
SOLDAGEM. Engenharia Mecânica Prof. Luis Fernando Maffeis Martins
 07 SOLDAGEM Engenharia Mecânica Prof. Luis Fernando Maffeis Martins Processo de soldagem por arco elétrico Este é mais um processo de soldagem que utiliza como fonte de calor a formação de um arco elétrico
07 SOLDAGEM Engenharia Mecânica Prof. Luis Fernando Maffeis Martins Processo de soldagem por arco elétrico Este é mais um processo de soldagem que utiliza como fonte de calor a formação de um arco elétrico
Quí. Quí. Monitor: Rodrigo Pova
 Quí. Professor: Allan Rodrigues Monitor: Rodrigo Pova Eletroquímica 07 nov EXERCÍCIOS DE AULA 1. Texto I Biocélulas combustíveis são uma alternativa tecnológica para substituição das baterias convencionais.
Quí. Professor: Allan Rodrigues Monitor: Rodrigo Pova Eletroquímica 07 nov EXERCÍCIOS DE AULA 1. Texto I Biocélulas combustíveis são uma alternativa tecnológica para substituição das baterias convencionais.
CORROSÃO E DEGRADAÇÃO DE MATERIAIS. Proteção e Combate à Corrosão CARLA SOARES SOUZA
 CORROSÃO E DEGRADAÇÃO DE MATERIAIS Proteção e Combate à Corrosão CARLA SOARES SOUZA O controle da corrosão inclui as medidas tomadas em cada etapa desde o projeto até a fabricação, instalação e utilização
CORROSÃO E DEGRADAÇÃO DE MATERIAIS Proteção e Combate à Corrosão CARLA SOARES SOUZA O controle da corrosão inclui as medidas tomadas em cada etapa desde o projeto até a fabricação, instalação e utilização
Revestimento Níquel Químico
 Revestimento Níquel Químico O que é Níquel Químico Propriedades do Níquel Químico É um tipo especial de revestimento que aumenta a resistência à abrasão e corrosão e que não requer corrente elétrica, retificadores
Revestimento Níquel Químico O que é Níquel Químico Propriedades do Níquel Químico É um tipo especial de revestimento que aumenta a resistência à abrasão e corrosão e que não requer corrente elétrica, retificadores
TECNOLOGIA DOS MATERIAIS
 TECNOLOGIA DOS MATERIAIS Aula 5: Aços e Ferros Fundidos Produção Feito de Elementos de Liga Ferros Fundidos CEPEP - Escola Técnica Prof.: Aços e Ferros Fundidos O Ferro é o metal mais utilizado pelo homem.
TECNOLOGIA DOS MATERIAIS Aula 5: Aços e Ferros Fundidos Produção Feito de Elementos de Liga Ferros Fundidos CEPEP - Escola Técnica Prof.: Aços e Ferros Fundidos O Ferro é o metal mais utilizado pelo homem.
Sistemas Estruturais em Aço MÓDULO. Proteção Anticorrosiva de Estruturas Metálicas
 Sistemas Estruturais em Aço MÓDULO Proteção Anticorrosiva de Estruturas Metálicas 1 Porque é necessário o tratamento anti-corrosivo das estruturas de aço? Apesar de este curso ter como foco os sistemas
Sistemas Estruturais em Aço MÓDULO Proteção Anticorrosiva de Estruturas Metálicas 1 Porque é necessário o tratamento anti-corrosivo das estruturas de aço? Apesar de este curso ter como foco os sistemas
TRATAMENTO DA ÁGUA PARA GERADORES DE VAPOR
 Universidade Federal do Paraná Curso de Engenharia Industrial Madeireira MÁQUINAS TÉRMICAS AT-056 M.Sc. Alan Sulato de Andrade alansulato@ufpr.br 1 INTRODUÇÃO: A água nunca está em estado puro, livre de
Universidade Federal do Paraná Curso de Engenharia Industrial Madeireira MÁQUINAS TÉRMICAS AT-056 M.Sc. Alan Sulato de Andrade alansulato@ufpr.br 1 INTRODUÇÃO: A água nunca está em estado puro, livre de
AULA DE RECUPERAÇÃO PROF. NEIF NAGIB
 AULA DE RECUPERAÇÃO PROF. NEIF NAGIB ELETROQUÍMICA Estuda os fenômenos envolvidos na produção de corrente elétrica a partir da transferência de elétrons em reações de óxido-redução, e a utilização de corrente
AULA DE RECUPERAÇÃO PROF. NEIF NAGIB ELETROQUÍMICA Estuda os fenômenos envolvidos na produção de corrente elétrica a partir da transferência de elétrons em reações de óxido-redução, e a utilização de corrente
HISTÓRIA, COMPORTAMENTO E USOS DOS AÇOS PATINÁVEIS NA ENGENHARIA ESTRUTURAL BRASILEIRA
 HISTÓRIA, COMPORTAMENTO E USOS DOS AÇOS PATINÁVEIS NA ENGENHARIA ESTRUTURAL BRASILEIRA Fabio Domingos Pannoni, M.Sc., Ph.D. 1 INTRODUÇÃO Todos os aços contêm pequenas quantidades de elementos de liga,
HISTÓRIA, COMPORTAMENTO E USOS DOS AÇOS PATINÁVEIS NA ENGENHARIA ESTRUTURAL BRASILEIRA Fabio Domingos Pannoni, M.Sc., Ph.D. 1 INTRODUÇÃO Todos os aços contêm pequenas quantidades de elementos de liga,
FÍSICO QUÍMICA AULA 5 - ELETRÓLISE
 FÍSICO QUÍMICA AULA 5 - ELETRÓLISE Em nossas aulas anteriores aprendemos como reações de óxidoredução podem ser utilizadas para se obter energia. Nas pilhas ocorrem reações químicas capazes de produzir
FÍSICO QUÍMICA AULA 5 - ELETRÓLISE Em nossas aulas anteriores aprendemos como reações de óxidoredução podem ser utilizadas para se obter energia. Nas pilhas ocorrem reações químicas capazes de produzir
PROMILITARES 20/09/2018 QUÍMICA. Professora Caroline Azevedo ELETROQUÍMICA. Eletroquímica. Você precisa saber o que é oxidação e redução!
 QUÍMICA Professora Caroline Azevedo ELETROQUÍMICA Eletroquímica Você precisa saber o que é oxidação e redução! Pilha É o nome dado ao dispositivo que aproveita a transferência de elétrons em uma reação
QUÍMICA Professora Caroline Azevedo ELETROQUÍMICA Eletroquímica Você precisa saber o que é oxidação e redução! Pilha É o nome dado ao dispositivo que aproveita a transferência de elétrons em uma reação
PMT CORROSÃO E PROTEÇÃO DOS MATERIAIS
 Corrosão em Fresta Abertura estreita junções: gaxetas, parafusos depósitos; produtos aderidos Materiais passivos Al; Ti Exemplo: liga 825 (44Ni-22Cr- 3Mo-2Cu) - água do mar 6 meses Trocador de calor com
Corrosão em Fresta Abertura estreita junções: gaxetas, parafusos depósitos; produtos aderidos Materiais passivos Al; Ti Exemplo: liga 825 (44Ni-22Cr- 3Mo-2Cu) - água do mar 6 meses Trocador de calor com
EFEITO DOS ELEMENTOS DE LIGA NOS AÇOS RSCP/ LABATS/DEMEC/UFPR
 EFEITO DOS ELEMENTOS DE LIGA NOS AÇOS RSCP/ LABATS/DEMEC/UFPR Seleção do processo de fundição Metal a ser fundido [C. Q.]; Qualidade requerida da superfície do fundido; Tolerância dimensional requerida
EFEITO DOS ELEMENTOS DE LIGA NOS AÇOS RSCP/ LABATS/DEMEC/UFPR Seleção do processo de fundição Metal a ser fundido [C. Q.]; Qualidade requerida da superfície do fundido; Tolerância dimensional requerida
PMT AULAS 1 E 2 Augusto Camara Neiva. PMT Augusto Neiva
 PMT3130 2017 - AULAS 1 E 2 Augusto Camara Neiva 1 2 3 4 AS AULAS NÃO SEGUIRÃO LINEARMENTE A APOSTILA HOJE: ELETROQUÍMICA 5 MOLÉCULA DE ÁGUA A molécula de água é polar e, portanto, a água pode alojar íons
PMT3130 2017 - AULAS 1 E 2 Augusto Camara Neiva 1 2 3 4 AS AULAS NÃO SEGUIRÃO LINEARMENTE A APOSTILA HOJE: ELETROQUÍMICA 5 MOLÉCULA DE ÁGUA A molécula de água é polar e, portanto, a água pode alojar íons
WCSE2018_17 PINTURA DE ESTRUTURAS METÁLICAS EM ÁREA DE MANGUE E POLUIÇÃO INDUSTRIAL DE ALTA AGRESSIVIDADE
 WCSE2018_17 PINTURA DE ESTRUTURAS METÁLICAS EM ÁREA DE MANGUE E POLUIÇÃO INDUSTRIAL DE ALTA AGRESSIVIDADE Bartolomeu Neves Cordeiro, Cristina da Costa Amorim Eletrobras Chesf Centro de Pesquisas de Energia
WCSE2018_17 PINTURA DE ESTRUTURAS METÁLICAS EM ÁREA DE MANGUE E POLUIÇÃO INDUSTRIAL DE ALTA AGRESSIVIDADE Bartolomeu Neves Cordeiro, Cristina da Costa Amorim Eletrobras Chesf Centro de Pesquisas de Energia
INTRODUÇÃO À ELETROQUÍMICA Prof. Dr. Patricio R. Impinnisi Departamento de engenharia elétrica UFPR
 INTRODUÇÃO À ELETROQUÍMICA Prof. Dr. Patricio R. Impinnisi Departamento de engenharia elétrica UFPR REAÇÕES ELETROQUÍMICAS Uma reação eletroquímica é um processo químico heterogêneo (que envolve uma interface
INTRODUÇÃO À ELETROQUÍMICA Prof. Dr. Patricio R. Impinnisi Departamento de engenharia elétrica UFPR REAÇÕES ELETROQUÍMICAS Uma reação eletroquímica é um processo químico heterogêneo (que envolve uma interface
Proteção anódica e catódica
 6/2/17 PROTEÇÃO CONTRA A CORROSÃO Proteção catódica e anódica Inibidores - Revestimentos - - Proteção anódica e catódica Como prevenir ou minimizar os efeitos da corrosão de um metal? 4-1823, Sri Humplrray
6/2/17 PROTEÇÃO CONTRA A CORROSÃO Proteção catódica e anódica Inibidores - Revestimentos - - Proteção anódica e catódica Como prevenir ou minimizar os efeitos da corrosão de um metal? 4-1823, Sri Humplrray
Atividade prática - Como se forma a ferrugem? Parte 3
 Atividade prática - Como se forma a ferrugem? Parte 3 1º e 2º ANOS DO ENSINO MÉDIO Objetivo Vivenciar alguns testes para a determinação das causas do surgimento da ferrugem, ou seja, da oxidação dos objetos
Atividade prática - Como se forma a ferrugem? Parte 3 1º e 2º ANOS DO ENSINO MÉDIO Objetivo Vivenciar alguns testes para a determinação das causas do surgimento da ferrugem, ou seja, da oxidação dos objetos
01) O elemento X reage com o elemento Z, conforme o processo: Nesse processo: Z 3 + X Z 1 + X 2. b) X ganha elétrons de Z. d) X e Z perdem elétrons.
 SECRETARIA DE SEGURANÇA PÚBLICA/SECRETARIA DE EDUCAÇÃO POLÍCIA MILITAR DO ESTADO DE GOIÁS COMANDO DE ENSINO POLICIAL MILITAR COLÉGIO DA POLÍCIA MILITAR NADER ALVES DOS SANTOS SÉRIE/ANO: TURMA(S): 2º anos
SECRETARIA DE SEGURANÇA PÚBLICA/SECRETARIA DE EDUCAÇÃO POLÍCIA MILITAR DO ESTADO DE GOIÁS COMANDO DE ENSINO POLICIAL MILITAR COLÉGIO DA POLÍCIA MILITAR NADER ALVES DOS SANTOS SÉRIE/ANO: TURMA(S): 2º anos
SUMÁRIO. 1 Introdução Obtenção dos Metais Apresentação do IBP... xiii. Apresentação da ABENDI... Apresentação da ABRACO...
 SUMÁRIO Apresentação do IBP... xiii Apresentação da ABENDI... xv Apresentação da ABRACO... xvii Prefácio... xix 1 Introdução... 1 1.1 Exercícios... 3 2 Obtenção dos Metais... 5 2.1 Minérios... 5 2.1.1
SUMÁRIO Apresentação do IBP... xiii Apresentação da ABENDI... xv Apresentação da ABRACO... xvii Prefácio... xix 1 Introdução... 1 1.1 Exercícios... 3 2 Obtenção dos Metais... 5 2.1 Minérios... 5 2.1.1
IMPORTANTE: Nunca Pintar Sobre Superfícies Anodizadas ou Pintadas Sem Fazer a Correta Decapagem, a Nova Camada de Tinta NÃO Irá Aderir Corretamente.
 1/108 CUIDADOS NA FABRICAÇÃO DE ESQUADRIAS EM AMBIENTES DE ELEVADA MARESIA Principalmente em atmosferas altamente contaminadas por maresia recomenda-se a utilização de portas e janelas produzidas com materiais
1/108 CUIDADOS NA FABRICAÇÃO DE ESQUADRIAS EM AMBIENTES DE ELEVADA MARESIA Principalmente em atmosferas altamente contaminadas por maresia recomenda-se a utilização de portas e janelas produzidas com materiais
TÍTULO: ESTUDO DA PASSIVAÇÃO DO AISI 316-L COM ÁCIDO NÍTRICO EM PRESENÇA DE MEIO CORROSIVO DE ÁCIDO CLORÍDRICO ATÉ 0,50 MOL. L-1
 Anais do Conic-Semesp. Volume 1, 2013 - Faculdade Anhanguera de Campinas - Unidade 3. ISSN 2357-8904 TÍTULO: ESTUDO DA PASSIVAÇÃO DO AISI 316-L COM ÁCIDO NÍTRICO EM PRESENÇA DE MEIO CORROSIVO DE ÁCIDO
Anais do Conic-Semesp. Volume 1, 2013 - Faculdade Anhanguera de Campinas - Unidade 3. ISSN 2357-8904 TÍTULO: ESTUDO DA PASSIVAÇÃO DO AISI 316-L COM ÁCIDO NÍTRICO EM PRESENÇA DE MEIO CORROSIVO DE ÁCIDO
Prof André Montillo
 Prof André Montillo www.montillo.com.br Reações de Oxido-Redução Definição: São as reações químicas onde ocorre a variação dos números de oxidação (Nox) das substâncias envolvidas. Portanto haverá transferência
Prof André Montillo www.montillo.com.br Reações de Oxido-Redução Definição: São as reações químicas onde ocorre a variação dos números de oxidação (Nox) das substâncias envolvidas. Portanto haverá transferência
Falhas prematuras de esquemas de pintura aplicados em aço galvanizado novo - Principais causas - Fábio Kränkel
 Falhas prematuras de esquemas de pintura aplicados em aço galvanizado novo - Principais causas - Fábio Kränkel EXPECTATIVA DE DURABILIDADE Aço galvanizado x Intempéries A durabilidade das estruturas galvanizadas
Falhas prematuras de esquemas de pintura aplicados em aço galvanizado novo - Principais causas - Fábio Kränkel EXPECTATIVA DE DURABILIDADE Aço galvanizado x Intempéries A durabilidade das estruturas galvanizadas
Organização: REVESTIMENTOS MONOCAMADA VpCI ALUMÍNIO DE LONGA DURABILIDADE NANO TECNOLOGIA DE INIBIDOES DE CORROSÃO POR VAPOR
 Organização: REVESTIMENTOS MONOCAMADA VpCI ALUMÍNIO DE LONGA DURABILIDADE NANO TECNOLOGIA DE INIBIDOES DE CORROSÃO POR VAPOR REVESTIMENTOS MONOCAMADA VpCI ALUMÍNIO DE LONGA DURABILIDADE NANO TECNOLOGIA
Organização: REVESTIMENTOS MONOCAMADA VpCI ALUMÍNIO DE LONGA DURABILIDADE NANO TECNOLOGIA DE INIBIDOES DE CORROSÃO POR VAPOR REVESTIMENTOS MONOCAMADA VpCI ALUMÍNIO DE LONGA DURABILIDADE NANO TECNOLOGIA
XV COBREAP - CONGRESSO BRASILEIRO DE ENGENHARIA DE AVALIAÇÕES E PERÍCIAS - IBAPE/SP
 XV COBREAP - CONGRESSO BRASILEIRO DE ENGENHARIA DE AVALIAÇÕES E PERÍCIAS - IBAPE/SP - 2009 NATUREZA DO TRABALHO: TRABALHO DE PERÍCIA Resumo: Este trabalho teve por objetivo avaliar o potencial de corrosão
XV COBREAP - CONGRESSO BRASILEIRO DE ENGENHARIA DE AVALIAÇÕES E PERÍCIAS - IBAPE/SP - 2009 NATUREZA DO TRABALHO: TRABALHO DE PERÍCIA Resumo: Este trabalho teve por objetivo avaliar o potencial de corrosão
CORROSÃO GALVÂNICA OU BIMETÁLICA
 CORROSÃO GALVÂNICA OU BIMETÁLICA Corrosão Galvânica - Características Acoplamento de metais com diferentes potenciais de corrosão (nobrezas diferentes) em contato elétrico em um mesmo eletrólito METAL
CORROSÃO GALVÂNICA OU BIMETÁLICA Corrosão Galvânica - Características Acoplamento de metais com diferentes potenciais de corrosão (nobrezas diferentes) em contato elétrico em um mesmo eletrólito METAL
Construção dos Navios. Seção B LIGAÇÃO DAS PEÇAS DE CONSTRUÇÃO
 Construção dos Navios Seção B LIGAÇÃO DAS PEÇAS DE CONSTRUÇÃO Juntas permanentes Solda Pressão JUNTAS Exemplo: ligação de uma camisa em um cilindro Contração Quando se aquece uma peça antes de forçar a
Construção dos Navios Seção B LIGAÇÃO DAS PEÇAS DE CONSTRUÇÃO Juntas permanentes Solda Pressão JUNTAS Exemplo: ligação de uma camisa em um cilindro Contração Quando se aquece uma peça antes de forçar a
A Importância das Tintas Ricas em Zinco no Desempenho dos Esquemas de Pintura
 A Importância das Tintas Ricas em Zinco no Desempenho dos Esquemas de Pintura Cristina Amorim Marcos Sá Fernando Fragata Participação Especial Eng. Sebastião Alves Gerente de Pesquisa e Desenvolvimento
A Importância das Tintas Ricas em Zinco no Desempenho dos Esquemas de Pintura Cristina Amorim Marcos Sá Fernando Fragata Participação Especial Eng. Sebastião Alves Gerente de Pesquisa e Desenvolvimento
e - Zinco ZnSO 4 Zn(s) Zn 2 Zn(s) Zn 2+ (aq) + 2 e - + 0,76 V Cu(s) Cu 2+ (aq) + 2 e - - 0,34 V
 Capítulo 7 Introdução teórica Pilhas e baterias são células eletroquímicas ou células galvânicas que produzem energia elétrica por meio de reações de oxirredução. A diferença básica é que a bateria é formada
Capítulo 7 Introdução teórica Pilhas e baterias são células eletroquímicas ou células galvânicas que produzem energia elétrica por meio de reações de oxirredução. A diferença básica é que a bateria é formada
ELETROQUÍMICA REAÇÃO ENERGIA QUÍMICA ELÉTRICA. Pilha. Eletrólise. espontânea. não espontânea
 ELETROQUÍMICA REAÇÃO Pilha espontânea ENERGIA QUÍMICA Eletrólise não espontânea ELÉTRICA SEMI REAÇÕES DE OXIDAÇÃO E REDUÇÃO Zn 0 Zn +2 + 2e - semi-reação de oxidação Cu +2 + 2e - Cu 0 semi-reação de redução
ELETROQUÍMICA REAÇÃO Pilha espontânea ENERGIA QUÍMICA Eletrólise não espontânea ELÉTRICA SEMI REAÇÕES DE OXIDAÇÃO E REDUÇÃO Zn 0 Zn +2 + 2e - semi-reação de oxidação Cu +2 + 2e - Cu 0 semi-reação de redução
Durabilidade do concreto versus Agressividade do meio
 Durabilidade do concreto versus Agressividade do meio CONCEITUAÇÃO Vida útil É o período de tempo após a instalação de um material ou componente da edificação, durante o qual todas as propriedades excedem
Durabilidade do concreto versus Agressividade do meio CONCEITUAÇÃO Vida útil É o período de tempo após a instalação de um material ou componente da edificação, durante o qual todas as propriedades excedem
PROCESSOS DE FABRICAÇÃO III SOLDAGEM METALURGIA DA SOLDAGEM
 PROCESSOS DE FABRICAÇÃO III SOLDAGEM METALURGIA DA SOLDAGEM Professor: Moisés Luiz Lagares Júnior 1 METALURGIA DA SOLDAGEM A JUNTA SOLDADA Consiste: Metal de Solda, Zona Afetada pelo Calor (ZAC), Metal
PROCESSOS DE FABRICAÇÃO III SOLDAGEM METALURGIA DA SOLDAGEM Professor: Moisés Luiz Lagares Júnior 1 METALURGIA DA SOLDAGEM A JUNTA SOLDADA Consiste: Metal de Solda, Zona Afetada pelo Calor (ZAC), Metal
Centro Universitário Padre Anchieta Controle de Processos Químicos Ciência dos Materiais Prof Ailton. Metais Não Ferrosos
 Metais Não Ferrosos 8.1 - Introdução Denominam-se metais não ferrosos, os metais em que não haja ferro ou em que o ferro está presente em pequenas quantidades, como elemento de liga Os metais não ferrosos
Metais Não Ferrosos 8.1 - Introdução Denominam-se metais não ferrosos, os metais em que não haja ferro ou em que o ferro está presente em pequenas quantidades, como elemento de liga Os metais não ferrosos
GOVERNO DO ESTADO DO RIO DE JANEIRO SECRETARIA DE ESTADO DE CIÊNCIA E TECNOLOGIA FUNDAÇÃO DE APOIO À ESCOLA TÉCNICA ESCOLA TÉCNICA ESTADUAL REPÚBLICA
 GOVERNO DO ESTADO DO RIO DE JANEIRO SECRETARIA DE ESTADO DE CIÊNCIA E TECNOLOGIA FUNDAÇÃO DE APOIO À ESCOLA TÉCNICA ESCOLA TÉCNICA ESTADUAL REPÚBLICA Aulas de Apoio Química 3ª Série Eletroquímica II 1.
GOVERNO DO ESTADO DO RIO DE JANEIRO SECRETARIA DE ESTADO DE CIÊNCIA E TECNOLOGIA FUNDAÇÃO DE APOIO À ESCOLA TÉCNICA ESCOLA TÉCNICA ESTADUAL REPÚBLICA Aulas de Apoio Química 3ª Série Eletroquímica II 1.
Aço Inoxidável Ferrítico com 11% de Cromo para Construção Soldada. Columbus Stainless. Nome X2CrNil2. Elementos C Mn Si Cr Ni N P S
 Aço Inoxidável Ferrítico com 11% de Cromo para Construção Soldada ArcelorMittal Inox Brasil S.A. Ugine S.A. Columbus Stainless P410D F12N 3CR12 * equivalência aproximada Designação Européia NF EN 10088-2
Aço Inoxidável Ferrítico com 11% de Cromo para Construção Soldada ArcelorMittal Inox Brasil S.A. Ugine S.A. Columbus Stainless P410D F12N 3CR12 * equivalência aproximada Designação Européia NF EN 10088-2
SOLDAGEM. Engenharia Mecânica Prof. Luis Fernando Maffeis Martins
 09 SOLDAGEM Engenharia Mecânica Prof. Luis Fernando Maffeis Martins Soldagem por resistência Soldagem por resistência Soldagem através da geração de calor devida à passagem de corrente elétrica e da aplicação
09 SOLDAGEM Engenharia Mecânica Prof. Luis Fernando Maffeis Martins Soldagem por resistência Soldagem por resistência Soldagem através da geração de calor devida à passagem de corrente elétrica e da aplicação
Exercícios Sobre Potenciais elétricos e Pilhas - Eletroquímica
 Exercícios Sobre Potenciais elétricos e Pilhas - Eletroquímica 01. (U. F. Uberlândia MG) São dadas as seguintes semi-reações, com respectivos potenciais de eletrodos: Mg Mg 2+ + 2e - Ni Ni 2+ + 2e - Cu
Exercícios Sobre Potenciais elétricos e Pilhas - Eletroquímica 01. (U. F. Uberlândia MG) São dadas as seguintes semi-reações, com respectivos potenciais de eletrodos: Mg Mg 2+ + 2e - Ni Ni 2+ + 2e - Cu
ESTUDO DA CORROSÃO DO Al RECICLADO DA INDÚSTRIA DE BEBIDAS
 ESTUDO DA CORROSÃO DO Al RECICLADO DA INDÚSTRIA DE BEBIDAS T. SILVA 1, D. MIRANDA 1, G. ALVES 3, O.L ROCHA 2, J.C. CARDOSO FILHO 1 1 Universidade Federal do Pará/ Laboratório de Corrosão 2 Instituto Federal
ESTUDO DA CORROSÃO DO Al RECICLADO DA INDÚSTRIA DE BEBIDAS T. SILVA 1, D. MIRANDA 1, G. ALVES 3, O.L ROCHA 2, J.C. CARDOSO FILHO 1 1 Universidade Federal do Pará/ Laboratório de Corrosão 2 Instituto Federal
Exercício de Revisão III Unidade. Eletroquímica
 1 Exercício de Revisão III Unidade Eletroquímica 1) O que difere uma célula galvânica e uma célula eletrolítica? 2) Considere a pilha: Zn(s)/Zn 2+ // Ag + /Ag(s) a) Proponha um esquema de funcionamento
1 Exercício de Revisão III Unidade Eletroquímica 1) O que difere uma célula galvânica e uma célula eletrolítica? 2) Considere a pilha: Zn(s)/Zn 2+ // Ag + /Ag(s) a) Proponha um esquema de funcionamento
Revestimento especial Corrotect. Proteção anticorrosiva para rolamentos
 Revestimento especial Corrotect Proteção anticorrosiva para rolamentos Revestimento especial Corrotect A corrosão é o inimigo número 1 dos metais e o Grupo Schaeffler está sempre buscando soluções para
Revestimento especial Corrotect Proteção anticorrosiva para rolamentos Revestimento especial Corrotect A corrosão é o inimigo número 1 dos metais e o Grupo Schaeffler está sempre buscando soluções para
CURSO DE INSPETOR ICZ - INSTITUTO DE METAIS NÃO FERROSOS LANÇAMENTO
 LANÇAMENTO - 2015 O ICZ tem o prazer de comunicar que está lançando nos meses de fevereiro e março os seguintes cursos: 1. Curso de Inspetor de Galvanização Dias 03 e 04 de fevereiro ou 17 e 18 de março;
LANÇAMENTO - 2015 O ICZ tem o prazer de comunicar que está lançando nos meses de fevereiro e março os seguintes cursos: 1. Curso de Inspetor de Galvanização Dias 03 e 04 de fevereiro ou 17 e 18 de março;
Introdução ao estudo das Estruturas Metálicas
 Introdução ao estudo das Estruturas Metálicas Processos de produção Propriedades físicas e mecânicas do aço estrutural FTC-116 Estruturas Metálicas Eng. Wagner Queiroz Silva UFAM Composição do aço O elemento
Introdução ao estudo das Estruturas Metálicas Processos de produção Propriedades físicas e mecânicas do aço estrutural FTC-116 Estruturas Metálicas Eng. Wagner Queiroz Silva UFAM Composição do aço O elemento
Aços estruturais e materiais de ligação
 Aços estruturais e materiais de ligação Introdução O aço é um material de construção utilizado em diversas estruturas fixas, como as edificações, e em estruturas móveis, como máquinas e equipamentos. Para
Aços estruturais e materiais de ligação Introdução O aço é um material de construção utilizado em diversas estruturas fixas, como as edificações, e em estruturas móveis, como máquinas e equipamentos. Para
METALURGIA EXTRATIVA DOS NÃO FERROSOS
 METALURGIA EXTRATIVA DOS NÃO FERROSOS PMT 2509 PMT 3409 Flávio Beneduce PRODUÇÃO DE Ni USOS DO NÍQUEL Aços inoxidáveis e aços ligados: 70% Ligas não ferrosas Superligas: ligas resistentes à oxidação e
METALURGIA EXTRATIVA DOS NÃO FERROSOS PMT 2509 PMT 3409 Flávio Beneduce PRODUÇÃO DE Ni USOS DO NÍQUEL Aços inoxidáveis e aços ligados: 70% Ligas não ferrosas Superligas: ligas resistentes à oxidação e
METAIS, AÇOS E PROCESSOS SIDERÚRGICOS
 METAIS, AÇOS E PROCESSOS SIDERÚRGICOS METAIS Podem ser moldados; São dúcteis (deformam antes de romper); Bons condutores de energia elétrica e calor. OBTENÇÃO DOS METAIS OBTENÇÃO DOS METAIS OBTENÇÃO DOS
METAIS, AÇOS E PROCESSOS SIDERÚRGICOS METAIS Podem ser moldados; São dúcteis (deformam antes de romper); Bons condutores de energia elétrica e calor. OBTENÇÃO DOS METAIS OBTENÇÃO DOS METAIS OBTENÇÃO DOS
HIDROMETALURGIA E ELETROMETALURGIA. Prof. Carlos Falcão Jr.
 HIDROMETALURGIA E ELETROMETALURGIA Prof. Carlos Falcão Jr. de um sólido em fase aquosa natureza do sólido (iônico, covalente ou metálico) processo: físico químico eletroquímico de redução eletrolítico
HIDROMETALURGIA E ELETROMETALURGIA Prof. Carlos Falcão Jr. de um sólido em fase aquosa natureza do sólido (iônico, covalente ou metálico) processo: físico químico eletroquímico de redução eletrolítico
Corrosão galvânica (bimetálica)
 Corrosão galvânica (bimetálica) A corrosão galvânica (bimetálica) pode ocorrer quando metais diferentes estão em contato num eletrólito comum (p. ex.: chuva, condensação, etc.). Se a corrente elétrica
Corrosão galvânica (bimetálica) A corrosão galvânica (bimetálica) pode ocorrer quando metais diferentes estão em contato num eletrólito comum (p. ex.: chuva, condensação, etc.). Se a corrente elétrica
Construindo sobre bases sólidas PROTEÇÃO CATÓDICA ÁREA PORTUÁRIA. (21)
 Construindo sobre bases sólidas PROTEÇÃO CATÓDICA ANODO DE SACRIFÍCIO A proteção catódica é um método de controle de corrosão que consiste em transformar a estrutura à proteger no cátodo de um célula eletroquímica
Construindo sobre bases sólidas PROTEÇÃO CATÓDICA ANODO DE SACRIFÍCIO A proteção catódica é um método de controle de corrosão que consiste em transformar a estrutura à proteger no cátodo de um célula eletroquímica
