7. Chamas Pré Misturadas
|
|
|
- Luca Ferrão Sanches
- 9 Há anos
- Visualizações:
Transcrição
1 7. Chamas Pré Misturadas 7.1 Introdução Uma chama é pré misturada quando o oxidante e o combustível já estão misturados antes da queima. O outro tipo é denominada chama de difusão, na qual o oxidante e o combustível estão inicialmente separados e a combustão ocorre em uma interface entre eles. Um bico de Bunsen, cujo esquema é mostrado na Figura 7.1, pode ser usado como exemplo para os dois tipos de chama. O jato de gás carreia o ar pela abertura da base do tubo, pelo efeito Venturi, e os dois se misturam durante o trajeto até a saída. O cone interno do bico de Bunsen é a chama pré misturada de uma mistura rica e o produto de combustão ainda contém componentes que podem reagir. O cone externo é o local de uma segunda reação de combustão devido à formação de uma chama de difusão entre os gases parcialmente queimados e o ar atmosférico. Figura 7.1 Bico de Bunsen. As duas chamas coincidem apenas na borda do tubo. No entanto, elas podem ser separadas no chamado separador de Smithells, mostrado na Figura
2 Figura 7.2 Separador de Smithells (Griffiths e Barnard, 1995). 7.2 Algumas Definições Velocidade de Chama A velocidade de chama, chamada também de velocidade de queima, velocidade normal de combustão, ou velocidade de chama laminar, é a velocidade na qual os gases reagentes entram na superfície da onda de combustão. Como veremos, trata-se de uma propriedade da mistura combustível/oxidante. Para um queimador laminar, a velocidade do gás é baixa próximo à parede, mas aumenta conforme se aproxima do centro, em um perfil aproximadamente parabólico. Em todos os pontos no interior da borda do tubo, a velocidade de escoamento excede a velocidade de queima. A chama toma o formato cônico de tal maneira que, na frente de chama, a componente normal da velocidade de escoamento seja igual à velocidade de chama Estabilização de Chamas A chama é estabilizada apenas entre certos limites de velocidade de escoamento dentro do tubo. Se a velocidade for muito baixa, a chama entra dentro do tubo e percorre a mistura até se apagar, ocorrendo o que chamamos de flash back. Por outro lado, se a velocidade for muito alta, não é possível estabilizar a chama na borda do tubo e ela tende a escapar e apagar, no que chamamos blow off. 135
3 Em geral, os valores dos limites da velocidade do gás para flash back e blow off dependem das dimensões do queimador e da composição do gás. Para misturas ricas e velocidades altas de escoamento, acima do limite de blow off, um outro fenômeno pode ocorrer. Devido ao carreamento do ar atmosférico, a mistura tornar-se-á progressivamente pobre acima da borda do queimador e, por causa da velocidade de escoamento, uma chama suspensa (lifted flame) pode se formar em uma certa posição acima da borda. A chama suspensa também terá dois limites. Quando a velocidade do gás é reduzida, ocorre o que chamamos de drop back, isto é, a chama volta a se ancorar na borda do tubo. De outra maneira, quando a velocidade do gás é aumentada ainda mais, a chama tende a escapar e apaga, no que chamamos de blow out. de Bunsen. Voltaremos adiante com uma discussão detalhada sobre flash back e blow off em um bico A Zona Luminosa A zona luminosa de uma chama é bastante estreita (< 1 mm), correspondendo ao local onde a temperatura é máxima e onde a reação efetivamente está ocorrendo. A taxa de reação varia exponencialmente com a temperatura, o que justifica o fato de termos a zona luminosa bastante estreita. A cor da zona luminosa muda com a razão ar/combustível. Para misturas pobres, a cor é violeta, por causa dos radicais CH. Para misturas rica, a cor é verde, por causa da molécula C2. Para misturas muito ricas, a cor é amarelada, por causa de partículas de carbono sólido. 7.3 eoria de Mallard e Le Chatelier para a Velocidade de Chama Mallard e Le Chatelier dividiram a chama em duas zonas: uma correspondente ao pré aquecimento da mistura combustível (zona I) e a outra à queima (zona II) (Glassman, 1996; Kuo, 1986), conforme mostrado na Figura 7.3. Conceitualmente, eles afirmaram que a quantidade de calor conduzida na zona II é igual à quantidade de calor necessária para que os gases não queimados atinjam a temperatura de ignição. Assim: f i m Cp i 0 (balanço de entalpia), (7.1) 136
4 onde o termo do lado esquerdo corresponde ao fluxo de calor para a esquerda para aumentar a temperatura de um valor inicial 0 até a temperatura de ignição i e o termo do lado direito corresponde ao fluxo de calor, também para a esquerda, devido ao gradiente de temperatura. Na equação, m, Cp e são a vazão mássica, o calor específico a pressão constante e a condutividade térmica da mistura, respectivamente, é a espessura da zona de reação e f é a temperatura final após a passagem da onda de combustão. Figura 7.3 Esquema de Mallard e Le Chatelier (Glassman, 1996; Kuo, 1986). O modelo assume Cp constante, aumento linear de temperatura entre i e f na distância, e que há uma região onde não há liberação de calor terminando em i. Sendo o problema unidimensional, temos: m AS L (balanço de massa), (7.2) onde A é a área da seção (assumida como unitária) e SL é a velocidade de chama laminar. Assim: 137
5 138 i f 0 i p L C S, (7.3) 1 C S 0 i i f p L (resultado de Mallard e Le Chatelier). (7.4) Esta expressão não é suficientemente representativa porque não é conhecido e i define um ponto hipotético onde começa uma região de reação com incremento linear de temperatura. Contudo, o problema real é que não há informação sobre a razão de reação no modelo. Assim, vamos investigar um modelo simplificado considerando a razão de reação. É possível relacionar com SL, uma vez que é a espessura da zona de reação. Portanto: L S, (7.5) onde é um tempo de reação que corresponde a uma razão de reação média d/dt tal que 1 dt d, (7.6) onde é a fração de massa de um reagente que é totalmente consumido na reação. Assim: dt d S 1 1 L. (7.7) Substituindo esta equação no resultado de Mallard e Le Chatelier, temos: 2 1 p i i f p L RR C dt d C S, (7.8) onde RR é a razão de reação. Investigaremos a seguir a dependência com a pressão da velocidade de chama. Sabemos que
6 dc n kc, (7.9) dt onde k é a constante de reação, tal que k = Ae -E/R, A é o fator de freqüência, C a concentração do reagente consumido e n a ordem de reação. Para o reagente, C =. Se a pressão e a temperatura variarem pouco com o tempo, temos: d k n dt d dt n k n1. (7.10) Como p, temos d/dt p n-1. Voltando à expressão para a velocidade de chama, obtemos (n2) 2 S L p. (7.11) A maior parte de chamas de hidrocarbonetos tem ordem de reação igual a 2 e, assim, conclui-se que as velocidades de chama para hidrocarbonetos devem ser independentes da pressão. Isto tem sido verificado experimentalmente. Investigaremos a seguir a dependência da velocidade de chama com a temperatura. A dependência com a temperatura da velocidade de chama é dominada pela exponencial. Assim, pode-se assumir que L -E R e 1 2 S. (7.12) Uma vez que a maior parte da reação ocorre perto da temperatura mais alta, a temperatura a ser usada na expressão é f, e L -E R e 1 2 f S. (7.13) Assim, o efeito de variar a temperatura inicial pode ser conhecido se conhecermos como esta variação altera a temperatura de chama. Sabemos que um aumento de 100 o C na temperatura inicial resulta em um aumento de temperatura bem menor na temperatura de chama. A dependência de SL com dada pela equação acima tem sido observada experimentalmente. 139
7 Nota: f é apropriada aqui porque estamos considerando uma reação de um único passo. Em reações mais complexas, as reações finais produzindo f podem ter contribuição mínima em SL. 7.4 Métodos de Medida da Velocidade de Chama São os seguintes os processos fotográficos para observar a chama (Kuo, 1986): a) A parte luminosa da chama é observada e o lado dessa região na direção dos gases não queimados é usado para medidas (fotografia direta). b) Fotografia tipo shadowgraph (mede 2 / x 2 ). Mede uma frente variacional e não uma superfície definida. São duas superfícies, uma no lado queimado e outra no lado não queimado. c) Fotografia tipo Schlieren (mede / x, que tem o maior valor perto do ponto de inflexão da temperatura e que corresponde à temperatura de ignição). d) Interferometria (mede massa específica ou temperatura diretamente e pode ser usada apenas em chamas bidimensionais). Descrições desses processos fotográficos podem ser encontrados em Liepmann e Rosko (1957). Os métodos para medir velocidade de chama são descritos a seguir (Kuo, 1986) Método do Bico de Bunsen A Figura 7.4 mostra o cone de um bico de Bunsen com as configurações da velocidade de aproximação, u, e da velocidade de chama, SL, esta perpendicular à frente de chama. emos: V S L, A onde V é a vazão volumétrica e A é a área do cone. 140
8 Figura 7.4 Esquema para o método do bico de Bunsen (Glassman, 1996). Este método tem as desvantagens: a) O cone escolhido pode ser um problema porque a área varia (pesquisadores preferem shadowgraph). b) A queima não é constante em todo o cone. A velocidade perto da parede do tubo é menor por causa do resfriamento pelas paredes. c) Precisa-se de uma fonte estável de gás, o que para gases raros ou puros pode ser um problema Método do ubo Cilíndrico A Figura 7.5 mostra um esquema do método do tubo cilíndrico. Uma mistura em um tubo horizontal aberto em uma das extremidades é ignitada no lado aberto. A velocidade com a qual a chama progride nos gases não queimados é a velocidade de chama. A principal dificuldade do método é: a frente de chama é curvada devido a efeitos de flutuação (SLAf = umr 2, onde Af é a área da chama, um é a velocidade média de progressão da onda e R é o raio do tubo). Figura 7.5 Esquema do método do tubo cilíndrico (Kuo, 1986). 141
9 Outras dificuldades do método são: a) O gás na frente de chama é afetado pela chama porque uma onda de pressão é estabelecida pela queima. Essa onda de pressão causa uma velocidade nos gases não queimados e é necessário levar em conta esse movimento. Essa velocidade deve ser subtraída do valor medido, uma vez que a chama está se propagando em um gás em movimento. b) Efeitos de fricção causam uma onda de pressão mais forte e o comprimento do tubo pode afetar a medida Método da Bolha de Sabão Este método, cujo esquema é mostrado na Figura 7.6, é uma tentativa de eliminar efeitos de fricção. O crescimento da frente de chama ao longo de um diâmetro é seguido por algum meio fotográfico. Uma vez que o gás é mantido em uma bolha de sabão, a pressão é constante. emos: S L b A u u rab SL u r, (7.14) u onde ur é a velocidade observada, e b e u são as massas específicas dos gases queimados e não queimados, respectivamente. Figura 7.6 Esquema do método da bolha de sabão (Kuo, 1986). 142
10 A maior dificuldade do método é a grande incerteza na razão entre a temperatura dos gases não queimados e a temperatura dos gases queimados, u/b, necessária para determinar b/u. Outras dificuldades são: a) O método pode apenas ser usado para chamas rápidas para evitar efeito convectivo dos gases quentes. b) O método só pode funcionar em misturas secas Método da Bomba Esférica Este método é muito similar ao da bolha de sabão. A diferença é que o volume é constante (pressão varia). O gás no qual a chama está se movendo está sempre mudando. É adequado apenas para chamas rápidas. A expressão para a velocidade de chama é: S L 3 3 R r dp dr 1, (7.15) 2 3p r dr dt u onde R é o raio do vaso, r o raio da frente de chama, p a pressão, t o tempo, e u a razão dos calores específicos dos gases não queimados Método do Queimador de Chama Plana Este é provavelmente o meio mais preciso para medir a velocidade de chama porque trabalha com uma frente de chama plana, para a qual as áreas correspondentes do shadowgraph, Schlieren e visível são as mesmas. O equipamento para aplicação do método é mostrado na Figura
11 Figura 7.7 Esquema do método do queimador de chama plana (Kuo, 1986). O método é aplicável apenas a misturas tendo razões de queima baixas. Botha e Spalding (1954) ampliaram o uso para velocidades de chama mais altas usando o artifício de refrigerar o plug de entrada. O valor desejado da velocidade de chama é encontrado por extrapolação da reta obtida experimentalmente, conforme mostra a Figura 7.8. Figura 7.8 Gráfico explicativo do artifício de Botha e Spalding. 7.5 Resultados Experimentais e Efeitos Físico Químicos A variação da velocidade de chama com a razão oxidante/combustível segue a variação da temperatura de chama adiabática com a razão de mistura. Assim, a velocidade de chama será máxima quando a mistura for aproximadamente estequiométrica. A maioria dos hidrocarbonetos 144
12 têm temperaturas de chama não muito diferentes para mistura estequiométrica com ar. Assim, a maioria dos hidrocarbonetos têm máximas velocidades de chama aproximadamente iguais para misturas com ar. A velocidade de propagação de uma chama laminar depende do tipo de combustível e da concentração de combustível na mistura. A Figura 7.9 apresenta a velocidade de chama laminar para acetileno, metano, etileno, monóxido de carbono e hidrogênio em ar. O metano tem uma velocidade máxima de propagação de cerca de 0,4 m/s. Velocidades máximas de chama da ordem de 0,4 a 0,5 m/s são típicas para hidrocarbonetos. Acetileno, etileno e hidrogênio possuem velocidades de chama mais elevadas devido à rápida cinética de reação e à alta difusividade molecular. Figura 7.9 Velocidades de chama para acetileno, metano, etileno, monóxido de carbono e hidrogênio em misturas com ar (Bjerketvedt et al., 1992). alvez os experimentos mais interessantes para elucidar os fatores dominantes na velocidade de chama foram aqueles realizados por Clingman et al. (1953). Os resultados mostram os efeitos da difusividade térmica e do calor específico. Foram medidas as velocidades de chama de misturas oxidante/metano com o oxidante contendo as mesmas proporções oxigênio/inerte do ar, isto é, 21/79 em base volumétrica. Os inertes escolhidos foram o hélio (He) e o argônio (Ar), além do nitrogênio (N2). Os resultados são mostrados na Figura Argônio e nitrogênio têm difusividades térmicas aproximadamente iguais. Contudo, o argônio é monoatômico e, portanto, tem calor específico menor que o do nitrogênio, que é 145
13 diatômico. Como o calor liberado na reação é o mesmo, a temperatura de chama será maior para a mistura com argônio e, em consequência, a sua velocidade de chama será maior. Figura 7.10 Velocidade de chama de metano em vários ares (Clingman et al., 1953). Argônio e hélio são ambos monoatômicos e as temperaturas finais de ambas as misturas serão as mesmas. Contudo, a difusividade térmica do hélio é muito maior que aquela do argônio. O hélio tem uma maior condutividade térmica e uma muito menor massa específica que o argônio. Em conseqüência, a velocidade de chama para a mistura contendo hélio é maior. 7.6 Estabilização de Chamas Consideremos uma chama plana de orientação arbitrária no escoamento de um gás pré misturado, conforme esquematizado na Figura Assumimos inicialmente que um escoamento uniforme exista. Sobre o movimento desta chama cabem as seguintes considerações: a. Se o gás não estivesse escoando, a chama na posição 1 mudaria de posição para 2 ou 3 (por exemplo) em uma unidade de tempo, sendo que a posição 3 corresponderia a uma velocidade de chama mais alta. A chama se propaga perpendicularmente à frente de chama. 146
14 Figura 7.11 Posição de uma chama pré misturada em um escoamento uniforme (Price, 1979). b. Se o gás está escoando, o meio no qual a chama está se propagando se move com o tempo, resultando em um movimento adicional da chama que não tem relação alguma com a sua propagação nos reagentes. Assim, se um observador estiver se movendo com o gás, a onda de combustão ainda mover-se-ia perpendicularmente à sua frente, com velocidade característica SL. c. Se os valores de SL e da velocidade do gás u forem os adequados, durante o tempo em que a chama progride a distância AO, o gás terá escoado a distância AA, até um ponto na linha da frente de onda original e a chama parecerá ser estacionária. Isto ocorrerá se S L usen. d. Notas: 1. u SL, exceto quando o 90 ; 2. Se S L usen, a chama permanecerá estacionária; se usen, a chama avançará; se S L S L usen, a chama retardará. 147
15 3. O ponto O se propaga em uma unidade de tempo para um elemento de massa que estará em A depois de uma unidade de tempo (quando usen ). Assim, a chama estacionária na S L realidade desliza sobre si mesma com uma velocidade S L u cos. 4. A chama estacionária precisa de um local de ignição em sua extremidade a montante. 5. Se houver um local de ignição, o valor de ajustar-se-á para satisfazer S L usen. 6. Da mesma maneira, se houver uma não uniformidade de escoamento, o valor local de ajustar-se-á para haver uma chama estacionária, sendo mostra a Figura S L usen localmente, conforme Figura 7.12 Esquema do ajuste local de para satisfazer S L usen (Price, 1979) 7. Da mesma maneira, qualquer não uniformidade do gás reagente (porcentagem de combustível, temperatura, etc.) causará uma acomodação em devido ao efeito local da velocidade de chama. Uma condição na extremidade a montante que esteja abaixo do limite de flamabilidade terá como conseqüência que a chama desprender-se-á por falta de um local de ignição. 7.7 Estabilização da Chama em um Bico de Bunsen A Figura 7.13 ilustra o fenômeno que ocorre com a chama do bico de Bunsen nas vizinhanças da borda do queimador. 148
16 Figura 7.13 Chama nas vizinhanças da borda de um bico de Bunsen (Lewis e von Elbe, 1961). Ao longo da onda de combustão, a velocidade de chama decresce devido a perdas de calor para as paredes e destruição de radicais. Para a esquerda, a velocidade de chama atinge seu valor máximo 0 S L. Se a onda de combustão estiver muito perto da saída do tubo (posição 1), a velocidade de queima é menor que a velocidade do escoamento em qualquer ponto da onda, e a chama é empurrada pelo escoamento. Quando a distância da borda aumenta, a perda de calor e a destruição de radicais diminui e a velocidade de queima aumenta. Uma posição é alcançada em algum ponto no perfil da onda no qual a velocidade de queima é igual à velocidade do gás (posição 2). A onda ficará em equilíbrio com respeito à borda sólida. Se a onda é movida a uma distância maior (posição 3), a velocidade de queima no ponto indicado fica maior que a velocidade do escoamento. A chama volta para a posição de equilíbrio. 149
17 7.7.1 Flash Back e Blow Off Quando o diâmetro do tubo é suficientemente grande de maneira que o perfil de velocidades possa ser considerado linear, pode-se escrever para a velocidade do gás: u gy, (7.16) onde y é a distância até a borda e g é uma constante chamada gradiente de velocidade. Se u é diminuída, g diminui e a posição 2 se move para mais perto da borda. Com uma diminuição posterior de u, uma condição é atingida para a qual a velocidade do gás torna-se menor que a velocidade de queima e a onda de combustão se propaga para dentro do tubo. Isto é chamado de flash back e o valor crítico de g para o qual esta condição começa a ocorrer é chamada gf. Outro valor crítico do gradiente de velocidade se refere à condição de blow off e é chamada gb. Quando u é aumentada, a posição de equilíbrio se distancia da borda do tubo. Ocorre, também, que conforme a distância da borda aumenta, a mistura é diluída por interdifusão com a atmosfera adjacente e a velocidade de queima na parte direita da onda torna-se progressivamente menor. Assim, há uma posição de equilíbrio crítica a partir da qual a velocidade do gás excede a velocidade de queima em todas linhas de corrente e a onda de combustão se desprende (blow off). Os gráficos da velocidade do escoamento e da velocidade de chama no queimador são mostrados na Figura emos: curvas A, B, C: velocidades de queima nas alturas A, B, C; curva 1: flash back; curva 2: limite de flash back; curva 3: chama estável; curva 4: limite de blow off; curva 5: blow off. 150
18 Figura 7.14 Velocidades do escoamento e de queima; (a) velocidade de queima e do gás dentro do tubo, (b) velocidade de queima e do gás acima da borda do tubo (Lewis e von Elbe, 1961). Referências Bjerketvedt, D.; Bakke, J.R.; van Wingerden, K., Gas Explosion Handbook, Christian Michelsen Research, Botha, J.P.; Spalding, D.B., he Laminar Flame Speed of Propane/air Mixtures with Heat Extraction from the Flame. Proc. of the Royal Society of London A, 225A(1160):71-96, Clingman, W.H.; Brokaw, R.S.; Pease, R.N. Burning Velocities of Methane with Nitrogenoxygen, Argon-oxygen, and Helium-oxygen Mixtures, Proc. of the Fourth International Symposium on Combustion, pp , Glassman, I., Combustion, Academic Press, Griffiths, J.F.; Barnard, J.A., Flame and Combustion, hird Edition, Blackie Academic & Professional, Kuo, K.K., Principles of Combustion, John Wiley & Sons, Lewis, B.; von Elbe, G., Combustion, Flames and Explosion of Gases, Academic Press, Liepmann, H.W.; Rosko, A., Elements of Gasdynamics, John Wiley and Sons, Price, E., Notas de Aula do Curso Combustion II, Georgia Institute of echnology,
COMBUSTÍVEIS E COMBUSTÃO
 COMBUSTÍVEIS E COMBUSTÃO PROF. RAMÓN SILVA Engenharia de Energia Dourados MS - 2013 CHAMAS PRÉ MISTURADAS 2 DEFINIÇÃO Uma chama é pré misturada quando o oxidante e o combustível já estão misturados antes
COMBUSTÍVEIS E COMBUSTÃO PROF. RAMÓN SILVA Engenharia de Energia Dourados MS - 2013 CHAMAS PRÉ MISTURADAS 2 DEFINIÇÃO Uma chama é pré misturada quando o oxidante e o combustível já estão misturados antes
Apêndice E Alguns outros conceitos interessantes: temperatura adiabática da chama; velocidade de chama; estabilização de chamas; a zona luminosa;
 Apêndice E Alguns outros conceitos interessantes: temperatura adiabática da chama; velocidade de chama; estabilização de chamas; a zona luminosa; teoria de Mallard e Lê Chatelier para a velocidade de chama.
Apêndice E Alguns outros conceitos interessantes: temperatura adiabática da chama; velocidade de chama; estabilização de chamas; a zona luminosa; teoria de Mallard e Lê Chatelier para a velocidade de chama.
Velocidade de propagação Notas sobre estabilização de chamas e velocidade de propagação.
 Notas sobre estabilização de chamas e velocidade de propagação. Estabilização de chamas de pré-mistura em diversas situações: A estabilização da chama pode ser efectuada quer pela variação da velocidade
Notas sobre estabilização de chamas e velocidade de propagação. Estabilização de chamas de pré-mistura em diversas situações: A estabilização da chama pode ser efectuada quer pela variação da velocidade
COMBUSTÍVEIS E COMBUSTÃO
 COMBUSTÍVEIS E COMBUSTÃO PROF. RAMÓN SILVA Engenharia de Energia Dourados MS - 2013 INFLAMABILIDADE DEFINIÇÃO O significado de limite de inflamabilidade é o seguinte: se um dado conjunto de condições permite
COMBUSTÍVEIS E COMBUSTÃO PROF. RAMÓN SILVA Engenharia de Energia Dourados MS - 2013 INFLAMABILIDADE DEFINIÇÃO O significado de limite de inflamabilidade é o seguinte: se um dado conjunto de condições permite
Estabilização de chama
 Estabilização de chama ( 7.8-9 do livro Combustão ) É possível estabilizar uma chama num escoamento (ver bico de Busen) A sua posição e geometria são determinados pela condição de equilíbrio: em cada ponto
Estabilização de chama ( 7.8-9 do livro Combustão ) É possível estabilizar uma chama num escoamento (ver bico de Busen) A sua posição e geometria são determinados pela condição de equilíbrio: em cada ponto
2. Os Reagentes: Limites de Inflamabilidade
 2. Os Reagentes: Limites de Inflamabilidade 2.1 Introdução O significado de limite de inflamabilidade é o seguinte: se um dado conjunto de condições permite a propagação de uma chama estável e se as condições
2. Os Reagentes: Limites de Inflamabilidade 2.1 Introdução O significado de limite de inflamabilidade é o seguinte: se um dado conjunto de condições permite a propagação de uma chama estável e se as condições
MOTORES TÉRMICOS AULA MISTURAS REAGENTES E COMBUSTÃO
 MOTORES TÉRMICOS AULA 13-17 MISTURAS REAGENTES E COMBUSTÃO PROF.: KAIO DUTRA Nas reações de combustão, a rápida oxidação dos elementos combustíveis do combustível resulta em uma liberação de energia à
MOTORES TÉRMICOS AULA 13-17 MISTURAS REAGENTES E COMBUSTÃO PROF.: KAIO DUTRA Nas reações de combustão, a rápida oxidação dos elementos combustíveis do combustível resulta em uma liberação de energia à
Caldeiras Flamotubulares. Não apropriadas para combustíveis sólidos
 Reações Químicas Caldeiras Flamotubulares Não apropriadas para combustíveis sólidos Caldeiras Aquatubulares Ciclo Termodinâmico de Geração de Eletricidade Combustíveis Todo material que pode ser queimado
Reações Químicas Caldeiras Flamotubulares Não apropriadas para combustíveis sólidos Caldeiras Aquatubulares Ciclo Termodinâmico de Geração de Eletricidade Combustíveis Todo material que pode ser queimado
Caracterização das Chamas:
 Caracterização das Chamas: A combustão da mistura ar/combustível dentro do cilindro é um dos processos que controlam a potência, eficiência e emissões dos motores. Os processos de combustão são diferentes
Caracterização das Chamas: A combustão da mistura ar/combustível dentro do cilindro é um dos processos que controlam a potência, eficiência e emissões dos motores. Os processos de combustão são diferentes
Combustão. Problemas para as aulas práticas
 Combustão Problemas para as aulas práticas ª aula - sexta-feira 5 e terça-feira 9 de Março Problema Escreva a fórmula química e represente esquematicamente a molécula dos seguintes combustíveis: metano,
Combustão Problemas para as aulas práticas ª aula - sexta-feira 5 e terça-feira 9 de Março Problema Escreva a fórmula química e represente esquematicamente a molécula dos seguintes combustíveis: metano,
FENÔMENOS DE TRANSPORTES AULA 12 E 13 INTRODUÇÃO À CONVECÇÃO E CONDUÇÃO
 FENÔMENOS DE TRANSPORTES AULA 12 E 13 INTRODUÇÃO À CONVECÇÃO E CONDUÇÃO PROF.: KAIO DUTRA Convecção Térmica O modo de transferência de calor por convecção é composto por dois mecanismos. Além da transferência
FENÔMENOS DE TRANSPORTES AULA 12 E 13 INTRODUÇÃO À CONVECÇÃO E CONDUÇÃO PROF.: KAIO DUTRA Convecção Térmica O modo de transferência de calor por convecção é composto por dois mecanismos. Além da transferência
Combustão Industrial
 Combustão Industrial JOSÉ EDUARDO MAUTONE BARROS Professor Adjunto da Universidade Federal de Minas Gerais Coordenador do Laboratório de Combustíveis e Combustão Doutor em Engenharia Mecânica - Térmica
Combustão Industrial JOSÉ EDUARDO MAUTONE BARROS Professor Adjunto da Universidade Federal de Minas Gerais Coordenador do Laboratório de Combustíveis e Combustão Doutor em Engenharia Mecânica - Térmica
Escoamento completamente desenvolvido
 Escoamento completamente desenvolvido A figura mostra um escoamento laminar na região de entrada de um tubo circular. Uma camada limite desenvolve-se ao longo das paredes do duto. A superfície do tubo
Escoamento completamente desenvolvido A figura mostra um escoamento laminar na região de entrada de um tubo circular. Uma camada limite desenvolve-se ao longo das paredes do duto. A superfície do tubo
Combustão. Objetivos. O Professor Responsável. J M C Mendes Lopes
 Combustão Objetivos Objetivo de ordem geral: Integrar num assunto específico os conhecimentos adquiridos em disciplinas a montante (termodinâmica, química, mecânica de fluidos, transmissão de calor e de
Combustão Objetivos Objetivo de ordem geral: Integrar num assunto específico os conhecimentos adquiridos em disciplinas a montante (termodinâmica, química, mecânica de fluidos, transmissão de calor e de
OTIMIZAÇÃO DE PROCESSOS DE COMBUSTÃO DE CALDEIRAS A GÁS
 OTIMIZAÇÃO DE PROCESSOS DE COMBUSTÃO DE CALDEIRAS A GÁS Aluno: William Schindhelm Georg Orientador: Marcos Sebastião de Paula Gomes Introdução O modelo de caldeira a gás inicialmente utilizado foi o mesmo
OTIMIZAÇÃO DE PROCESSOS DE COMBUSTÃO DE CALDEIRAS A GÁS Aluno: William Schindhelm Georg Orientador: Marcos Sebastião de Paula Gomes Introdução O modelo de caldeira a gás inicialmente utilizado foi o mesmo
Combustão Industrial
 Combustão Industrial JOSÉ EDUARDO MAUTONE BARROS Professor Adjunto da Universidade Federal de Minas Gerais Coordenador do Laboratório de Combustíveis e Combustão Doutor em Engenharia Mecânica - Térmica
Combustão Industrial JOSÉ EDUARDO MAUTONE BARROS Professor Adjunto da Universidade Federal de Minas Gerais Coordenador do Laboratório de Combustíveis e Combustão Doutor em Engenharia Mecânica - Térmica
Química Aplicada. QAP0001 Licenciatura em Química Prof a. Dr a. Carla Dalmolin
 Química Aplicada QAP0001 Licenciatura em Química Prof a. Dr a. Carla Dalmolin [email protected] [email protected] Combustíveis Reações de Combustão Reação química entre uma substância (combustível)
Química Aplicada QAP0001 Licenciatura em Química Prof a. Dr a. Carla Dalmolin [email protected] [email protected] Combustíveis Reações de Combustão Reação química entre uma substância (combustível)
BALANÇOS DE MASSA EM PROCESSOS COM REAÇÃO
 BALANÇOS DE MASSA EM PROCESSOS COM REAÇÃO PROF. MARCELO HENRIQUE 2 BALANÇOS COM REAÇÃO QUÍMICA A diferença agora é que aparecerão na equação do balanço, além dos termos ENTRA e SAÍDA, os termos GERAÇÃO
BALANÇOS DE MASSA EM PROCESSOS COM REAÇÃO PROF. MARCELO HENRIQUE 2 BALANÇOS COM REAÇÃO QUÍMICA A diferença agora é que aparecerão na equação do balanço, além dos termos ENTRA e SAÍDA, os termos GERAÇÃO
JOSÉ EDUARDO MAUTONE BARROS
 Combustão JOSÉ EDUARDO MAUTONE BARROS Professor Adjunto da Universidade Federal de Minas Gerais Coordenador do Laboratório de Combustíveis e Combustão Doutor em Engenharia Mecânica - Térmica (UFMG) Doutor
Combustão JOSÉ EDUARDO MAUTONE BARROS Professor Adjunto da Universidade Federal de Minas Gerais Coordenador do Laboratório de Combustíveis e Combustão Doutor em Engenharia Mecânica - Térmica (UFMG) Doutor
LOQ Fenômenos de Transporte I
 LOQ 4083 - Fenômenos de Transporte I FT I 07 Equações básicas na forma integral para o volume de controle Prof. Lucrécio Fábio dos Santos Departamento de Engenharia Química LOQ/EEL Atenção: Estas notas
LOQ 4083 - Fenômenos de Transporte I FT I 07 Equações básicas na forma integral para o volume de controle Prof. Lucrécio Fábio dos Santos Departamento de Engenharia Química LOQ/EEL Atenção: Estas notas
EN 2411 Aula 13 Trocadores de calor Método MLDT
 Universidade Federal do ABC EN 24 Aula 3 Trocadores de calor Método MLDT Trocadores de calor São equipamentos utilizados para promover a transferência de calor entre dois fluidos que se encontram sob temperaturas
Universidade Federal do ABC EN 24 Aula 3 Trocadores de calor Método MLDT Trocadores de calor São equipamentos utilizados para promover a transferência de calor entre dois fluidos que se encontram sob temperaturas
COMBUSTÍVEIS E COMBUSTÃO
 COMBUSTÍVEIS E COMBUSTÃO PROF. RAMÓN SILVA Engenharia de Energia Dourados MS - 2013 COMBUSTÃO DE LÍQUIDOS 2 INTRODUÇÃO A Queima de uma Gota de Combustível em um Ambiente Estacionário Na queima de uma gota
COMBUSTÍVEIS E COMBUSTÃO PROF. RAMÓN SILVA Engenharia de Energia Dourados MS - 2013 COMBUSTÃO DE LÍQUIDOS 2 INTRODUÇÃO A Queima de uma Gota de Combustível em um Ambiente Estacionário Na queima de uma gota
CONSTANTE DE EQUILÍBRIO
 EQUILÍBRIO QUÍMICO CONSTANTE DE EQUILÍBRIO A maneira de descrever a posição de equilíbrio de uma reação química é dar as concentrações de equilíbrio dos reagentes e produtos. A expressão da constante de
EQUILÍBRIO QUÍMICO CONSTANTE DE EQUILÍBRIO A maneira de descrever a posição de equilíbrio de uma reação química é dar as concentrações de equilíbrio dos reagentes e produtos. A expressão da constante de
Tabela 5.1- Características e condições operacionais para a coluna de absorção. Altura, L Concentração de entrada de CO 2, C AG
 5 Resultados Neste capítulo, são apresentados sob forma de tabelas os dados operacionais e as propriedades físico-químicas utilizados no processo de absorção CO 2 -MEA. Em seguida são apresentados a comparação
5 Resultados Neste capítulo, são apresentados sob forma de tabelas os dados operacionais e as propriedades físico-químicas utilizados no processo de absorção CO 2 -MEA. Em seguida são apresentados a comparação
Aula 6 de FT II. Prof. Gerônimo
 Aula 6 de FT II Prof. Gerônimo Transferência de calor em superfícies estendidas Superfície estendida é comumente usado para descrever um caso especial importante envolvendo a transferência de calor por
Aula 6 de FT II Prof. Gerônimo Transferência de calor em superfícies estendidas Superfície estendida é comumente usado para descrever um caso especial importante envolvendo a transferência de calor por
7ª Ficha de Avaliação de Conhecimentos Turma: 11ºA
 Página1 7ª Ficha de Avaliação de Conhecimentos Turma: 11ºA Física e Química A - 11ºAno (Versão 1) Professora Paula Melo Silva Data: 20 de março Ano Letivo: 2018/2019 90 min + 15 min 1. O ácido acético,
Página1 7ª Ficha de Avaliação de Conhecimentos Turma: 11ºA Física e Química A - 11ºAno (Versão 1) Professora Paula Melo Silva Data: 20 de março Ano Letivo: 2018/2019 90 min + 15 min 1. O ácido acético,
CONDUÇÃO DE CALOR UNIDIMENSIONAL EXERCÍCIOS EM SALA
 CONDUÇÃO DE CALOR UNIDIMENSIONAL EXERCÍCIOS EM SALA 1) Uma casa possui uma parede composta com camadas de madeira, isolamento à base de fibra de vidro e gesso, conforme indicado na figura. Em um dia frio
CONDUÇÃO DE CALOR UNIDIMENSIONAL EXERCÍCIOS EM SALA 1) Uma casa possui uma parede composta com camadas de madeira, isolamento à base de fibra de vidro e gesso, conforme indicado na figura. Em um dia frio
ESTE Aula 1- Introdução à convecção. A camada limite da convecção
 Universidade Federal do ABC ESTE013-13 Aula 1- Introdução à convecção. A camada limite da convecção Convecção Definição: Processo de transferência de calor entre uma superfície e um fluido adjacente, quando
Universidade Federal do ABC ESTE013-13 Aula 1- Introdução à convecção. A camada limite da convecção Convecção Definição: Processo de transferência de calor entre uma superfície e um fluido adjacente, quando
Mas Da figura, temos:
 1. Na tubulação da figura 1, óleo cru escoa com velocidade de 2,4 m/s no ponto A; calcule até onde o nível de óleo chegará no tubo aberto C. (Fig.1). Calcule também a vazão mássica e volumétrica do óleo.
1. Na tubulação da figura 1, óleo cru escoa com velocidade de 2,4 m/s no ponto A; calcule até onde o nível de óleo chegará no tubo aberto C. (Fig.1). Calcule também a vazão mássica e volumétrica do óleo.
Curso Engenharia de Energia
 UNIVERSIDADE FEDERAL DA GRANDE DOURADOS - UFGD FACULDADE DE ENGENHARIA Curso Engenharia de Energia Prof. Dr. Omar Seye [email protected] Disciplina: COMBUSTÃO E COMBUSTÍVEIS A queima direta, ou combustão,
UNIVERSIDADE FEDERAL DA GRANDE DOURADOS - UFGD FACULDADE DE ENGENHARIA Curso Engenharia de Energia Prof. Dr. Omar Seye [email protected] Disciplina: COMBUSTÃO E COMBUSTÍVEIS A queima direta, ou combustão,
Atrito na Camada Limite atrito interno
 Circulações Locais e Turbulência Atmosférica Atrito na Camada Limite atrito interno Atrito interno está relacionado a viscosidade molecular Viscosidade é o freiamento de um fluido devido ao movimento molecular.
Circulações Locais e Turbulência Atmosférica Atrito na Camada Limite atrito interno Atrito interno está relacionado a viscosidade molecular Viscosidade é o freiamento de um fluido devido ao movimento molecular.
Reações químicas aplicas ao processamento de materiais cerâmicos
 Reações químicas aplicas ao processamento de materiais cerâmicos Em vários casos, no processo de fabricação de peças cerâmicas, as reações entre os diferentes constituintes dos corpos cerâmicos são interrompidas
Reações químicas aplicas ao processamento de materiais cerâmicos Em vários casos, no processo de fabricação de peças cerâmicas, as reações entre os diferentes constituintes dos corpos cerâmicos são interrompidas
Universidade Federal do ABC. EN 2411 Aula 10 Convecção Livre
 Universidade Federal do ABC EN 2411 Aula 10 Convecção ivre Convecção ivre Convecção natural (ou livre): transferência de calor que ocorre devido às correntes de convecção que são induzidas por forças de
Universidade Federal do ABC EN 2411 Aula 10 Convecção ivre Convecção ivre Convecção natural (ou livre): transferência de calor que ocorre devido às correntes de convecção que são induzidas por forças de
FÍSICA E QUÍMICA A 10º ANO
 DEPARTAMENTO DE MATEMÁTICA E CIÊNCIAS EXPERIMENTAIS Planificação Anual FÍSICA E QUÍMICA A 10º ANO 2017 / 2018 1º Período - QUÍMICA Apresentação e divulgação de critérios 2 1. ELEMENTOS QUÍMICOS E SUA ORGANIZAÇÃO
DEPARTAMENTO DE MATEMÁTICA E CIÊNCIAS EXPERIMENTAIS Planificação Anual FÍSICA E QUÍMICA A 10º ANO 2017 / 2018 1º Período - QUÍMICA Apresentação e divulgação de critérios 2 1. ELEMENTOS QUÍMICOS E SUA ORGANIZAÇÃO
UNIVERSIDADE ZAMBEZE. Fundamentos de Combustão Aula 2-Prática Prof. Jorge Nhambiu
 UNIVERSIDADE ZAMBEZE Fundamentos de Combustão Aula 2-Prática Aula 2. Tópicos Termodinâmica da combustão: Revisão dos conceitos da primeira lei; Propriedades das misturas; Estequiometria da combustão; Energia
UNIVERSIDADE ZAMBEZE Fundamentos de Combustão Aula 2-Prática Aula 2. Tópicos Termodinâmica da combustão: Revisão dos conceitos da primeira lei; Propriedades das misturas; Estequiometria da combustão; Energia
Objetivos. Escoamento de um fluido. O aluno deverá ser capaz de: Introduzir noções acerca do movimento dos fluidos.
 Introdução à hidrodinâmica MÓDULO 1 - AULA 3 Aula 3 Introdução à hidrodinâmica Objetivos O aluno deverá ser capaz de: Introduzir noções acerca do movimento dos fluidos. Estabelecer critérios para o estudo
Introdução à hidrodinâmica MÓDULO 1 - AULA 3 Aula 3 Introdução à hidrodinâmica Objetivos O aluno deverá ser capaz de: Introduzir noções acerca do movimento dos fluidos. Estabelecer critérios para o estudo
Aula 4 de FT II. Prof. Gerônimo
 Aula 4 de FT II Prof. Gerônimo Equação diferencial de Condução Vamos considerar a taxa de geração interna de calor q = E g. Coordenada x, y e z. Regime transiente. Considerando: q = q Volume de controle
Aula 4 de FT II Prof. Gerônimo Equação diferencial de Condução Vamos considerar a taxa de geração interna de calor q = E g. Coordenada x, y e z. Regime transiente. Considerando: q = q Volume de controle
ESTE Aula 2- Introdução à convecção. As equações de camada limite
 Universidade Federal do ABC ESTE013-13 Aula - Introdução à convecção. As equações de camada limite EN 41: Aula As equações de camada limite Análise das equações que descrevem o escoamento em camada limite:
Universidade Federal do ABC ESTE013-13 Aula - Introdução à convecção. As equações de camada limite EN 41: Aula As equações de camada limite Análise das equações que descrevem o escoamento em camada limite:
OPERAÇÕES UNITÁRIAS II AULA 1: REVISÃO TRANSFERÊNCIA DE CALOR. Profa. Dra. Milena Martelli Tosi
 OPERAÇÕES UNITÁRIAS II AULA 1: REVISÃO TRANSFERÊNCIA DE CALOR Profa. Dra. Milena Martelli Tosi A IMPORTÂNCIA DA TRANSFERÊNCIA DE CALOR NA INDÚSTRIA DE ALIMENTOS Introdução Revisão: Mecanismos de transferência
OPERAÇÕES UNITÁRIAS II AULA 1: REVISÃO TRANSFERÊNCIA DE CALOR Profa. Dra. Milena Martelli Tosi A IMPORTÂNCIA DA TRANSFERÊNCIA DE CALOR NA INDÚSTRIA DE ALIMENTOS Introdução Revisão: Mecanismos de transferência
Lista de Exercícios Solução em Sala
 Lista de Exercícios Solução em Sala 1) Um conjunto pistão-cilindro área de seção transversal igual a 0,01 m². A massa do pistão é 101 kg e ele está apoiado nos batentes mostrado na figura. Se a pressão
Lista de Exercícios Solução em Sala 1) Um conjunto pistão-cilindro área de seção transversal igual a 0,01 m². A massa do pistão é 101 kg e ele está apoiado nos batentes mostrado na figura. Se a pressão
Transferência de Calor
 Transferência de Calor Trocadores de Calor Filipe Fernandes de Paula [email protected] Departamento de Engenharia de Produção e Mecânica Faculdade de Engenharia Universidade Federal de Juiz
Transferência de Calor Trocadores de Calor Filipe Fernandes de Paula [email protected] Departamento de Engenharia de Produção e Mecânica Faculdade de Engenharia Universidade Federal de Juiz
RESUMO MECFLU P2. 1. EQUAÇÃO DE BERNOULLI Estudo das propriedades de um escoamento ao longo de uma linha de corrente.
 RESUMO MECFLU P2 1. EQUAÇÃO DE BERNOULLI Estudo das propriedades de um escoamento ao longo de uma linha de corrente. Hipóteses Fluido invíscido (viscosidade nula) não ocorre perda de energia. Fluido incompressível
RESUMO MECFLU P2 1. EQUAÇÃO DE BERNOULLI Estudo das propriedades de um escoamento ao longo de uma linha de corrente. Hipóteses Fluido invíscido (viscosidade nula) não ocorre perda de energia. Fluido incompressível
Transferência de Calor
 Transferência de Calor Introdução à Convecção Filipe Fernandes de Paula [email protected] Departamento de Engenharia de Produção e Mecânica Faculdade de Engenharia Universidade Federal de
Transferência de Calor Introdução à Convecção Filipe Fernandes de Paula [email protected] Departamento de Engenharia de Produção e Mecânica Faculdade de Engenharia Universidade Federal de
O combustível e a Combustão
 CAPITULO 3 O combustível e a Combustão Motores a GASOLINA / ÁLCOOL com ignição por centelha Volvo Powertrain Julio Lodetti Revisão sobre as características gerais A COMBUSTÃO consiste na etapa essencial
CAPITULO 3 O combustível e a Combustão Motores a GASOLINA / ÁLCOOL com ignição por centelha Volvo Powertrain Julio Lodetti Revisão sobre as características gerais A COMBUSTÃO consiste na etapa essencial
REVISIONAL DE QUÍMICA 1º ANO PROF. RICARDO
 REVISIONAL DE QUÍMICA 1º ANO PROF. RICARDO 1- Um aluno de química, ao investigar as propriedades de gases, colocou uma garrafa plástica (PET), contendo ar e devidamente fechada, em um freezer e observou
REVISIONAL DE QUÍMICA 1º ANO PROF. RICARDO 1- Um aluno de química, ao investigar as propriedades de gases, colocou uma garrafa plástica (PET), contendo ar e devidamente fechada, em um freezer e observou
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação
 Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
Transferência de Calor
 Transferência de Calor Escoamento Interno - Parte 1 Filipe Fernandes de Paula [email protected] Departamento de Engenharia de Produção e Mecânica Faculdade de Engenharia Universidade Federal
Transferência de Calor Escoamento Interno - Parte 1 Filipe Fernandes de Paula [email protected] Departamento de Engenharia de Produção e Mecânica Faculdade de Engenharia Universidade Federal
PARTE III Balanço de massa
 PARTE III Balanço de massa 1. Procedimentos para cálculo de Balanço de Massa i. Escolha como base de cálculo uma quantidade ou vazão de uma das correntes do processo. ii. Desenhe o fluxograma e rotule
PARTE III Balanço de massa 1. Procedimentos para cálculo de Balanço de Massa i. Escolha como base de cálculo uma quantidade ou vazão de uma das correntes do processo. ii. Desenhe o fluxograma e rotule
Lista de exercícios LOB1019 Física 2
 Lista de exercícios 02 1. Tão rapidamente a Terra foi formada, o calor liberado pelo decaimento de elementos radioativos elevaram a sua temperatura média interna de 300 para 3000K (valor atual). Supondo
Lista de exercícios 02 1. Tão rapidamente a Terra foi formada, o calor liberado pelo decaimento de elementos radioativos elevaram a sua temperatura média interna de 300 para 3000K (valor atual). Supondo
Aula 25 Radiação. UFJF/Departamento de Engenharia de Produção e Mecânica. Prof. Dr. Washington Orlando Irrazabal Bohorquez
 Aula 25 Radiação UFJF/Departamento de Engenharia de Produção e Mecânica Prof. Dr. Washington Orlando Irrazabal Bohorquez REVISÃO: Representa a transferência de calor devido à energia emitida pela matéria
Aula 25 Radiação UFJF/Departamento de Engenharia de Produção e Mecânica Prof. Dr. Washington Orlando Irrazabal Bohorquez REVISÃO: Representa a transferência de calor devido à energia emitida pela matéria
a = 2, Física Questão 53 - Alternativa D Devido ao tempo de reação, o carro percorre uma distância , antes de
 Física 53. No instante t =, o motorista de um carro que percorre uma estrada retilínea, com velocidade constante de m/s, avista um obstáculo m a sua frente. O motorista tem um tempo de reação t = s, após
Física 53. No instante t =, o motorista de um carro que percorre uma estrada retilínea, com velocidade constante de m/s, avista um obstáculo m a sua frente. O motorista tem um tempo de reação t = s, após
Exame de Admissão 2016/1 Prova da área de termo fluidos Conhecimentos específicos
 Exame de Admissão 2016/1 Prova da área de termo fluidos Conhecimentos específicos 1ª. Questão (1 ponto) Considere uma bomba centrífuga de 20 kw de potência nominal, instalalada em uma determinada planta
Exame de Admissão 2016/1 Prova da área de termo fluidos Conhecimentos específicos 1ª. Questão (1 ponto) Considere uma bomba centrífuga de 20 kw de potência nominal, instalalada em uma determinada planta
Lista de Exercícios - Máquinas Térmicas
 DISCIPLINA: MÁQUINAS TÉRMICAS - 2017/02 PROF.: MARCELO COLAÇO PREPARADO POR GABRIEL ROMERO ([email protected]) 4. Motores de combustão interna: Os calores específicos são constantes para todos os exercícios
DISCIPLINA: MÁQUINAS TÉRMICAS - 2017/02 PROF.: MARCELO COLAÇO PREPARADO POR GABRIEL ROMERO ([email protected]) 4. Motores de combustão interna: Os calores específicos são constantes para todos os exercícios
Fenômenos de Transferência FEN/MECAN/UERJ Prof Gustavo Rabello 2 período 2014 lista de exercícios 06/11/2014. Conservação de Quantidade de Movimento
 Fenômenos de Transferência FEN/MECAN/UERJ Prof Gustavo Rabello 2 período 2014 lista de exercícios 06/11/2014 Conservação de Quantidade de Movimento 1. A componente de velocidade v y de um escoamento bi-dimensional,
Fenômenos de Transferência FEN/MECAN/UERJ Prof Gustavo Rabello 2 período 2014 lista de exercícios 06/11/2014 Conservação de Quantidade de Movimento 1. A componente de velocidade v y de um escoamento bi-dimensional,
ESCOAMENTOS UNIFORMES EM CANAIS
 ESCOAMENTOS UNIFORMES EM CANAIS Nome: nº turma INTRODUÇÃO Um escoamento em canal aberto é caracterizado pela existência de uma superfície livre. Esta superfície é na realidade uma interface entre dois
ESCOAMENTOS UNIFORMES EM CANAIS Nome: nº turma INTRODUÇÃO Um escoamento em canal aberto é caracterizado pela existência de uma superfície livre. Esta superfície é na realidade uma interface entre dois
ENGENHARIA DE MATERIAIS. Fenômenos de Transporte em Engenharia de Materiais (Transferência de Calor e Massa)
 ENGENHARIA DE MATERIAIS Fenômenos de Transporte em Engenharia de Materiais (Transferência de Calor e Massa) Prof. Dr. Sérgio R. Montoro [email protected] [email protected] TRANSFERÊNCIA DE
ENGENHARIA DE MATERIAIS Fenômenos de Transporte em Engenharia de Materiais (Transferência de Calor e Massa) Prof. Dr. Sérgio R. Montoro [email protected] [email protected] TRANSFERÊNCIA DE
5. Conclusões e Perspectivas
 5. Conclusões e Perspectivas Neste estudo experimental foram apresentados resultados da caracterização de chamas turbulentas não pré-misturadas de spray de etanol e ar. Para realização deste estudo foi
5. Conclusões e Perspectivas Neste estudo experimental foram apresentados resultados da caracterização de chamas turbulentas não pré-misturadas de spray de etanol e ar. Para realização deste estudo foi
Universidade Federal do Rio de Janeiro Instituto de Física Lista 1 Física 2. prof. Daniela Szilard 23 de maio de 2016
 Universidade Federal do Rio de Janeiro Instituto de Física Lista 1 Física 2 prof. Daniela Szilard 23 de maio de 2016 1. Julgue os itens: verdadeiro ou falso. ( ) A lei de Stevin é válida para qualquer
Universidade Federal do Rio de Janeiro Instituto de Física Lista 1 Física 2 prof. Daniela Szilard 23 de maio de 2016 1. Julgue os itens: verdadeiro ou falso. ( ) A lei de Stevin é válida para qualquer
Halliday & Resnick Fundamentos de Física
 Halliday & Resnick Fundamentos de Física Mecânica Volume 1 www.grupogen.com.br http://gen-io.grupogen.com.br O GEN Grupo Editorial Nacional reúne as editoras Guanabara Koogan, Santos, Roca, AC Farmacêutica,
Halliday & Resnick Fundamentos de Física Mecânica Volume 1 www.grupogen.com.br http://gen-io.grupogen.com.br O GEN Grupo Editorial Nacional reúne as editoras Guanabara Koogan, Santos, Roca, AC Farmacêutica,
SUMÁRIO. Parte I. Agradecimentos Resumo Abstract. Página. Capítulo 1 Introdução e objetivos Introdução 1.2. Objetivos
 SUMÁRIO Parte I Agradecimentos Resumo Abstract Página Capítulo 1 Introdução e objetivos 1.1. Introdução 1.2. Objetivos 1 4 Capítulo 2 Revisão bibliográfica 2.1. Introdução 2.2. Aspectos históricos 2.2.1.
SUMÁRIO Parte I Agradecimentos Resumo Abstract Página Capítulo 1 Introdução e objetivos 1.1. Introdução 1.2. Objetivos 1 4 Capítulo 2 Revisão bibliográfica 2.1. Introdução 2.2. Aspectos históricos 2.2.1.
ESZO Fenômenos de Transporte
 Universidade Federal do ABC ESZO 001-15 Fenômenos de Transporte Profa. Dra. Ana Maria Pereira Neto [email protected] Bloco A, torre 1, sala 637 Mecanismos de Transferência de Calor Calor Calor pode
Universidade Federal do ABC ESZO 001-15 Fenômenos de Transporte Profa. Dra. Ana Maria Pereira Neto [email protected] Bloco A, torre 1, sala 637 Mecanismos de Transferência de Calor Calor Calor pode
Operações Unitárias II Lista de Exercícios 1 Profa. Dra. Milena Martelli Tosi
 1. Vapor d água condensado sobre a superfície externa de um tubo circular de parede fina, com diâmetro interno igual a 50 mm e comprimento igual a 6 m, mantém uma temperatura na superfície externa uniforme
1. Vapor d água condensado sobre a superfície externa de um tubo circular de parede fina, com diâmetro interno igual a 50 mm e comprimento igual a 6 m, mantém uma temperatura na superfície externa uniforme
Convecção (natural e forçada) Prof. Dr. Edval Rodrigues de Viveiros
 Convecção (natural e forçada) Prof. Dr. Edval Rodrigues de Viveiros Convecção natural Convecção forçada Convecção natural A transmissão de calor por convecção natural ocorre sempre quando um corpo é
Convecção (natural e forçada) Prof. Dr. Edval Rodrigues de Viveiros Convecção natural Convecção forçada Convecção natural A transmissão de calor por convecção natural ocorre sempre quando um corpo é
Ciências dos Materiais
 ASSOCIAÇÃO TERESINENSE DE ENSINO ATE FACULDADE SANTO AGOSTINHO FSA DIREÇÃO DE ENSINO NÚCLEO DE APOIO PEDAGÓGICO NUAPE Ciências dos Materiais Profª Esp. Priscylla Mesquita Por que Estudar a Difusão? Materiais
ASSOCIAÇÃO TERESINENSE DE ENSINO ATE FACULDADE SANTO AGOSTINHO FSA DIREÇÃO DE ENSINO NÚCLEO DE APOIO PEDAGÓGICO NUAPE Ciências dos Materiais Profª Esp. Priscylla Mesquita Por que Estudar a Difusão? Materiais
SISTEMAS TÉRMICOS DE POTÊNCIA
 SISTEMAS TÉRMICOS DE POTÊNCIA PROF. RAMÓN SILVA Engenharia de Energia Dourados MS - 2013 GERADOR DE GASES 2 GERADOR DE GASES O conjunto gerador de gases é composto basicamente de três componentes: compressor,
SISTEMAS TÉRMICOS DE POTÊNCIA PROF. RAMÓN SILVA Engenharia de Energia Dourados MS - 2013 GERADOR DE GASES 2 GERADOR DE GASES O conjunto gerador de gases é composto basicamente de três componentes: compressor,
FÍSICA 2 PROVA 2 TEMA 1 HIDROSTÁTICA E HIDRODINÂMICA PROF. LEANDRO NECKEL
 FÍSICA 2 PROVA 2 TEMA 1 HIDROSTÁTICA E HIDRODINÂMICA PROF. LEANDRO NECKEL HIDROSTÁTICA PARTE I CONSIDERAÇÕES INICIAIS Características gerais de fluidos para este capítulo É uma substância que pode fluir,
FÍSICA 2 PROVA 2 TEMA 1 HIDROSTÁTICA E HIDRODINÂMICA PROF. LEANDRO NECKEL HIDROSTÁTICA PARTE I CONSIDERAÇÕES INICIAIS Características gerais de fluidos para este capítulo É uma substância que pode fluir,
ESTUDO DA TRANSIÇÃO ENTRE ESCOAMENTO LAMINAR E TURBULENTO EM TUBO CAPILAR
 ESTUDO DA TRANSIÇÃO ENTRE ESCOAMENTO LAMINAR E TURBULENTO EM TUBO CAPILAR M. H. MARTINS 1, A. KNESEBECK 1 1 Universidade Federal do Paraná, Departamento de Engenharia Química E-mail para contato: [email protected]
ESTUDO DA TRANSIÇÃO ENTRE ESCOAMENTO LAMINAR E TURBULENTO EM TUBO CAPILAR M. H. MARTINS 1, A. KNESEBECK 1 1 Universidade Federal do Paraná, Departamento de Engenharia Química E-mail para contato: [email protected]
Quí. Monitor: Marcos Melo
 Professor: Xandão Monitor: Marcos Melo Específicas: Cinética Química 27 nov EXERCÍCIOS DE AULA 1. A água oxigenada H 2O 2 (aq) se decompõe, produzindo água e gás oxigênio, de acordo com a equação: H 2O
Professor: Xandão Monitor: Marcos Melo Específicas: Cinética Química 27 nov EXERCÍCIOS DE AULA 1. A água oxigenada H 2O 2 (aq) se decompõe, produzindo água e gás oxigênio, de acordo com a equação: H 2O
Departamento de Engenharia Mecânica. ENG 1011: Fenômenos de Transporte I
 Departamento de Engenharia Mecânica ENG 1011: Fenômenos de Transporte I Aula 9: Formulação diferencial Exercícios 3 sobre instalações hidráulicas; Classificação dos escoamentos (Formulação integral e diferencial,
Departamento de Engenharia Mecânica ENG 1011: Fenômenos de Transporte I Aula 9: Formulação diferencial Exercícios 3 sobre instalações hidráulicas; Classificação dos escoamentos (Formulação integral e diferencial,
EM34B Transferência de Calor 2
 EM34B Transferência de Calor 2 Prof. Dr. André Damiani Rocha [email protected] Convecção Forçada Escoamento Interno Parte I 2 Convecção Forçada: Escoamento Interno Definição Escoamento Interno: é um
EM34B Transferência de Calor 2 Prof. Dr. André Damiani Rocha [email protected] Convecção Forçada Escoamento Interno Parte I 2 Convecção Forçada: Escoamento Interno Definição Escoamento Interno: é um
PROCESSO SELETIVO TURMA DE 2015 FASE 1 PROVA DE FÍSICA E SEU ENSINO
 PROCESSO SELETIVO TURMA DE 2015 FASE 1 PROVA DE FÍSICA E SEU ENSINO Caro professor, cara professora esta prova tem 2 partes; a primeira parte é objetiva, constituída por 14 questões de múltipla escolha,
PROCESSO SELETIVO TURMA DE 2015 FASE 1 PROVA DE FÍSICA E SEU ENSINO Caro professor, cara professora esta prova tem 2 partes; a primeira parte é objetiva, constituída por 14 questões de múltipla escolha,
3 Modelagem Física e Matemática
 3 Modelagem Física e Matemática omo mencionado no capítulo introdução, o objetivo do presente trabalho consiste em identificar a importância dos mecanismos de absorção química para previsão da absorção
3 Modelagem Física e Matemática omo mencionado no capítulo introdução, o objetivo do presente trabalho consiste em identificar a importância dos mecanismos de absorção química para previsão da absorção
Lei de Fourier. Considerações sobre a lei de Fourier. A lei de Fourier é fenomenológica, isto é, desenvolvida de fenômenos observados.
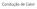 Condução de Calor Lei de Fourier A lei de Fourier é fenomenológica, isto é, desenvolvida de fenômenos observados Considerações sobre a lei de Fourier q x = ka T x Fazendo Δx 0 q taxa de calor [J/s] ou
Condução de Calor Lei de Fourier A lei de Fourier é fenomenológica, isto é, desenvolvida de fenômenos observados Considerações sobre a lei de Fourier q x = ka T x Fazendo Δx 0 q taxa de calor [J/s] ou
a) Qual deverá ser o volume do PFR para converter 80% de A em fase líquida? Considerar alimentação a 44 L min -1 e C A0 = C B0 = 1 mol L -1
 501) Um dado composto A se decompõe conforme a cinética enzimática de Michaelis-Menten,. Determine os parâmetros V máx e K M, considerando os dados experimentais a seguir. C A (kmol m -3 ) 0,1 0,01 0,005
501) Um dado composto A se decompõe conforme a cinética enzimática de Michaelis-Menten,. Determine os parâmetros V máx e K M, considerando os dados experimentais a seguir. C A (kmol m -3 ) 0,1 0,01 0,005
8 Resultados das velocidades de propagação de chama turbulentas no interior do cilindro do motor
 8 Resultados das velocidades de propagação de chama turbulentas no interior do cilindro do motor Neste capítulo, primeiramente serão apresentadas de forma consolidada as curvas típicas obtidas para a evolução
8 Resultados das velocidades de propagação de chama turbulentas no interior do cilindro do motor Neste capítulo, primeiramente serão apresentadas de forma consolidada as curvas típicas obtidas para a evolução
Para o desenvolvimento do projeto de uma caldeira flamotubular os requisitos de projeto deverão estar definidos conforme a Tabela 1.
 1. Dimensionamento Caldeiras 1.1. Requisitos de Projeto Para o desenvolvimento do projeto de uma caldeira flamotubular os requisitos de projeto deverão estar definidos conforme a Tabela 1.1 Tabela 1.1
1. Dimensionamento Caldeiras 1.1. Requisitos de Projeto Para o desenvolvimento do projeto de uma caldeira flamotubular os requisitos de projeto deverão estar definidos conforme a Tabela 1.1 Tabela 1.1
Capitulo IX RELAÇOES ENTRE RIQUEZA, TEMPÉRATURA E COMPOSIÇOES DOS GASES DE COMBUSTAO
 Capitulo IX RELAÇOES ENTRE RIQUEZA, TEMPÉRATURA E COMPOSIÇOES DOS GASES DE COMBUSTAO No Caso mais geral, a mistura reativa num motor é composta por:.1- O carburante presente na câmara de combustão.2- O
Capitulo IX RELAÇOES ENTRE RIQUEZA, TEMPÉRATURA E COMPOSIÇOES DOS GASES DE COMBUSTAO No Caso mais geral, a mistura reativa num motor é composta por:.1- O carburante presente na câmara de combustão.2- O
BC 0303: Fenômenos Térmicos 2 a Lista de Exercícios
 BC 33: Fenômenos Térmicos a Lista de Exercícios ** Onde for necessário adote a constante universal dos gases R = 8,3 J/mol K e o número de Avogadro N A = 6,. 3 ** Caminho Livre Médio. Em um dado experimento,
BC 33: Fenômenos Térmicos a Lista de Exercícios ** Onde for necessário adote a constante universal dos gases R = 8,3 J/mol K e o número de Avogadro N A = 6,. 3 ** Caminho Livre Médio. Em um dado experimento,
EM34B Transferência de Calor 2
 EM34B Transferência de Calor 2 Prof. Dr. André Damiani Rocha [email protected] Convecção Forçada Escoamento Externo Parte II 2 Convecção Forçada: Escoamento Externo Cilindro em escoamento cruzado Um
EM34B Transferência de Calor 2 Prof. Dr. André Damiani Rocha [email protected] Convecção Forçada Escoamento Externo Parte II 2 Convecção Forçada: Escoamento Externo Cilindro em escoamento cruzado Um
Aços de alta liga resistentes a corrosão II
 Aços de alta liga resistentes a corrosão II Aços de alta liga ao cromo ferríticos normalmente contêm 13% ou 17% de cromo e nenhum ou somente baixo teor de níquel. A figura da esquerda apresenta uma parte
Aços de alta liga resistentes a corrosão II Aços de alta liga ao cromo ferríticos normalmente contêm 13% ou 17% de cromo e nenhum ou somente baixo teor de níquel. A figura da esquerda apresenta uma parte
FENÔMENOS DE TRANSPORTES
 FENÔMENOS DE TRANSPORTES AULA 11 FUNDAMENTOS DE TRANSFERÊNCIA DE CALOR PROF.: KAIO DUTRA Transferência de Calor Transferência de calor (ou calor) é a energia em trânsito devido a uma diferença de temperatura.
FENÔMENOS DE TRANSPORTES AULA 11 FUNDAMENTOS DE TRANSFERÊNCIA DE CALOR PROF.: KAIO DUTRA Transferência de Calor Transferência de calor (ou calor) é a energia em trânsito devido a uma diferença de temperatura.
2a LISTA DE EXERCÍCIOS
 IPH 01107 a LISTA DE EXERCÍCIOS 1) Para o escoamento de 15 N/s de ar [R = 87 m /(s.k)] a 30 o C e 100 kpa (absoluta), através de um conduto de seção transversal retangular com 15 X 30 cm, calcule (a) a
IPH 01107 a LISTA DE EXERCÍCIOS 1) Para o escoamento de 15 N/s de ar [R = 87 m /(s.k)] a 30 o C e 100 kpa (absoluta), através de um conduto de seção transversal retangular com 15 X 30 cm, calcule (a) a
EXERCÍCIOS FÍSICA 10. e problemas Exames Testes intermédios Professor Luís Gonçalves
 FÍSICA 10 EXERCÍCIOS e problemas Exames 2006 2007 2008 2009 2010 2011 Testes intermédios 2008 2009 2010 2011 Escola Técnica Liceal Salesiana do Estoril Professor Luís Gonçalves 2 3 Unidade 1 Do Sol ao
FÍSICA 10 EXERCÍCIOS e problemas Exames 2006 2007 2008 2009 2010 2011 Testes intermédios 2008 2009 2010 2011 Escola Técnica Liceal Salesiana do Estoril Professor Luís Gonçalves 2 3 Unidade 1 Do Sol ao
Transferência de Calor
 Transferência de Calor Condução em Superfícies Estendidas Filipe Fernandes de Paula [email protected] Departamento de Engenharia de Produção e Mecânica Faculdade de Engenharia Universidade
Transferência de Calor Condução em Superfícies Estendidas Filipe Fernandes de Paula [email protected] Departamento de Engenharia de Produção e Mecânica Faculdade de Engenharia Universidade
UNIVERSIDADE EDUARDO MONDLANE Faculdade de Engenharia. Transmissão de calor. 3º ano
 UNIVERSIDADE EDUARDO MONDLANE Faculdade de Engenharia Transmissão de calor 3º ano Aula 3 Equação diferencial de condução de calor Condições iniciais e condições de fronteira; Geração de Calor num Sólido;
UNIVERSIDADE EDUARDO MONDLANE Faculdade de Engenharia Transmissão de calor 3º ano Aula 3 Equação diferencial de condução de calor Condições iniciais e condições de fronteira; Geração de Calor num Sólido;
1º BIMESTRE. Série Turma (s) Turno 3º A B C D E F G H MATUTINO Disciplina: QUÍMICA Professor: CHARLYS FERNANDES Data: / / 2017 Aluno (a): Nº
 1º BIMESTRE Visto do Professor Nota (Fuvest) A uma determinada temperatura, as substâncias HI, H2 e I2 estão no estado gasoso. A essa temperatura, o equilíbrio entre as três substâncias foi estudado, em
1º BIMESTRE Visto do Professor Nota (Fuvest) A uma determinada temperatura, as substâncias HI, H2 e I2 estão no estado gasoso. A essa temperatura, o equilíbrio entre as três substâncias foi estudado, em
Aprsentar os principais conceitos envolvidos no equilíbrio químico e suas relações termodinâmicas com a constante e composições de equilíbrio.
 EQUILÍBRIO QUÍMICO Metas Aprsentar os principais conceitos envolvidos no equilíbrio químico e suas relações termodinâmicas com a constante e composições de equilíbrio. Objetivos Ao final desta aula, o
EQUILÍBRIO QUÍMICO Metas Aprsentar os principais conceitos envolvidos no equilíbrio químico e suas relações termodinâmicas com a constante e composições de equilíbrio. Objetivos Ao final desta aula, o
