Ministério da Saúde Secretaria de Ciência, Tecnologia e Insumos Estratégicos. CONITEC 5 ANOS Avanços e desafios
|
|
|
- Antônio Felgueiras Benke
- 7 Há anos
- Visualizações:
Transcrição
1 Ministério da Saúde Secretaria de Ciência, Tecnologia e Insumos Estratégicos CONITEC 5 ANOS Avanços e desafios
2 LEI 8080/90 SISTEMA ÚNICO DE SAÚDE - SUS Universalidade Garantia de acesso de toda e qualquer pessoa a todo e qualquer serviço de saúde, seja ele público ou contratado pelo poder público. Equidade Garantia de acesso de toda e qualquer pessoa em igualdade de condições aos diferentes níveis de complexidade do sistema e ações coletivas dirigidas por prioridades amplas e reconhecidas.
3 LEI 8080/90 SISTEMA ÚNICO DE SAÚDE - SUS Integralidade Reconhece o homem e o sistema de saúde, cada qual com uma totalidade: cada pessoa num todo indivisível e membro de uma comunidade e as ações de saúde como sistema indivisível, capaz de prestar atenção integral à saúde. Controle social Participação e co-responsabilização da sociedade na gestão integrada das ações e serviços de saúde com democratização do processo decisório, cujo núcleo central é a participação popular na perspectiva de descentralização do poder e gerenciamento dos serviços e ações de saúde.
4 NOVO MARCO LEI N /2011 Altera a lei n e dispõe sobre assistência terapêutica e incorporação de tecnologia em saúde no SUS Cria a Comissão Nacional de Incorporação de Tecnologias no SUS
5 NOVO MARCO LEI N /2011 Incorporação baseada em evidências (eficácia e segurança) e estudos de avaliação econômicas (custo-efetividade) Consulta Pública para todas as avaliações Prazo para avaliação: 180 dias, prorrogáveis por mais 90 dias Veda o uso de tecnologias sem registro na Anvisa e de procedimentos experimentais Define o que é Protocolo Clínico e Diretrizes Terapêuticas
6 A CONITEC É um órgão colegiado de caráter permanente, integrante da estrutura regimental do Ministério da Saúde, tem por objetivo assessorar o Ministério da Saúde nas atribuições relativas à incorporação, exclusão ou alteração pelo SUS de tecnologias em saúde, bem como na constituição ou alteração de protocolos clínicos e diretrizes terapêuticas.
7 CONITEC NA ESTRUTURA DO MS
8 ESTRUTURA
9 O DEPARTAMENTO DE GESTÃO E INCOPORAÇÃO DE TECNOLOGIAS EM SAÚDE - DGITS
10 Equipe de Trabalho: 34 profissionais 15 Humanas_ 7 Exatas_ 2 Saúde _ Orçamento Anual do DGITS: R$ 16,2 milhões
11 OBJETIVOS ESTRATÉGICOS MISSÃO E VISÃO DO DGITS Qualificar o processo decisório na avaliação de tecnologias em saúde, buscando a promoção e a proteção da saúde da população brasileira, a melhor alocação dos recursos disponíveis e a redução das desigualdades regionais Ser reconhecido pela excelência na gestão e incorporação de tecnologias em saúde considerando o desenvolvimento tecnológico e as transformações sociais para um Brasil saudável 1. Contribuir para a qualificação das decisões judiciais e para a redução da judicialização do direito à saúde no país 2. Aprimorar o processo brasileiro de ATS em conformidade com o marco legal e o avanço da ciência 3. Ampliar e qualificar a participação social no processo de incorporação tecnológica 4. Dar visibilidade ao processo de gestão e incorporação de tecnologias em saúde 5. Gerir o processo de elaboração e revisão de PCDTs
12 DGITS DAS Diretor DAS Assistente Protocolos Clínicos e Diretrizes Terapêuticas Avaliação e Monitoramento de Tecnologias Gestão Administrativa e Participação Social DAS Coordenador Geral DAS Assessor DAS Coordenador Geral DAS Assessor DAS Coordenador Geral DAS Assessor
13 PLANEJAMENTO_MS Resultado % das demandas em análise na CONITEC avaliadas dentro do prazo legal (REM, PNS) Resultado 02 Pelo menos 12 protocolos clínicos e diretrizes terapêuticas ( PCDT) elaboradas e/ou revisadas no ano de Resultado 03 Pelo menos 60 sínteses de evidências sobre tecnologias disponibilizadas para subsidiar tecnicamente os operadores de direito e os gestores de saúde em relação a demandas judiciais no ano de 2015.
14 INDICADOR_MS Percentual de demandas em análise na CONITEC avaliadas dentro do prazo legal no ano. Meta 100% _ Indicador anual 86% das demandas em análise na CONITEC avaliadas dentro do prazo legal _ apurado em 03/2016
15 SUBCOMISSÕES Subcomissão de Avaliação de Protocolos Clínicos e Diretrizes Terapêuticas PCDT s SCTIE/DGITS Subcomissão de Atualização da Relação Nacional de Medicamentos Essenciais RENAME e do Formulário Terapêutico Nacional FTN SCTIE/DAF Subcomissão de Atualização da Relação Nacional de Ações e Serviços de Saúde RENASES SAS
16 REQUISITOS PARA AVALIAÇÃO I Formulário integralmente preenchido, de acordo com o modelo estabelecido pela CONITEC II Número e validade do registro da tecnologia em saúde ANVISA III Evidência científica que demostre que a tecnologia pautada é, no mínimo tão eficaz e segura quanto aquelas disponíveis no SUS para determinada indicação
17 REQUISITOS PARA AVALIAÇÃO IV Estudo de avaliação econômica comparando a tecnologia pautada com as tecnologias em saúde disponibilizadas no SUS V Amostras de produtos, se cabível para o atendimento do disposto no 2º do art. 19-Q, nos termos do regimento interno VI O preço fixado pela CMED, no caso de medicamentos
18 FLUXO
19
20 RELATÓRIO - ATS Doença Tecnologia Análise das evidências apresentadas pelo Demandante - Evidência Clínica - Avaliação Econômica - Impacto Orçamentário Busca e Análise de Evidências Científicas complementares (AvE, C.Ind.) Experiências internacionais Recomendação da Conitec Consulta Pública Deliberação Final Decisão Everolimo para imunossupressão em transplante hepático em adultos Nº 174 Agosto/2015
21 INCORPORAÇÃO BASEADA EM
22 DEMANDAS TIPO DE TECNOLOGIA 294 medicamento 99 procedimento 68 produto TOTAL 461
23 DEMANDAS ÁREA DA SAÚDE demais temas
24 RESULTADOS Janeiro/2012 a março/2016 Número de reuniões mensais 45 (42 ordinárias e 3 extraordinárias) Número de demandas por incorporação 461 Externas 201 Internas (MS) 260 Demandas externas não conformes 78(39%) Demandas em avaliação 22
25 PERCENTUAL DE DEMANDAS NÃO CONFORMES 43 % 35 % 31 % 14 %
26 RESULTADOS Janeiro/2012 a março/2016 Consultas públicas 145 Nº de Contribuições Tecnologias incorporadas 168 Não incorporadas 73 Impacto Estimado Total com as incorporações R$ 2,5 bilhões
27 CONSULTAS PÚBLICAS evolução de contribuições por ano ,8% ,6 % ,9 % ,7 %
28 EVOLUÇÃO DA INCORPORAÇÃO DE TECNOLOGIAS
29 INCORPORAÇÃO TECNOLÓGICA SUSTENTÁVEL
30 MEDICAMENTOS EFICÁCIA (RVS12) EFETIVIDADE (RVS12) Hepatite C POSOLOGIA CONTRAINDICAÇÕES ABRANGÊNCIA GENOTÍPICA CUSTO DO TRATAMENTO (R$) GENÓTIPO 1 (PREVALÊNCIA BRASIL 65%) TRATAMENTOS DESINCORPORADOS TELAPREVIR + INTERFERON PEGUILADO E RIBAVIRINA (ORAL E INJETÁVEL) 40 a 80% 65% 12 semanas telaprevir (6 comp./dia) + 48 semanas pegintf. injetável e ribavirina Transplantados, cirrose descompensada, doenças autoimunes e transtornos mentais ,20 BOCEPREVIR + INTERFERON PEGUILADO E RIBAVIRINA (ORAL E INJETÁVEL) 34 a 79% 58% 44 semanas boceprevir (12 comp./dia) + 48 semanas pegintf. injetável e ribavirina Transplantados, cirrose descompensada, doenças autoimunes e transtornos mentais ,72 TRATAMENTOS INCORPORADOS SOFOSBUVIR + SIMEPREVIR (TOTALMENTE ORAL) 88 a 95% 83 a 91% 12 semanas sofosbuvir + simeprevir (2 comp./dia) - SOFOSBUVIR 1,2,3,4. SIMEPREVIR ,65 (BRA) > ,00 (EUA) SOFOSBUVIR + DACLATASVIR (TOTALMENTE ORAL) 95 a 100% 93% 12 semanas sofosbuvir + daclatasvir (2 comp./dia) - SOFOSBUVIR 1,2,3,4. DACLATASVIR 1,3, ,29 (BRA) > ,00 (EUA)
31 Tecnologias de alto custo incorporadas Tecnologia/Ano de avaliação Sofosbuvir, daclatasvir e simeprevir (2015) Vacina contra HPV (2013) Clozapina, Lamotrigina, Olanzapina, Quetiapina e Risperidona (2015) Trastuzumabe (2012) Palivizumabe (2013) PET-CT (2014) Fingolimode (2014) Indicação Hepatite C crônica Prevenção do câncer de colo de útero Transtorno Afetivo Bipolar Câncer de mama inicial e localmente avançado Infecção pelo Vírus Sincicial Respiratório Câncer de pulmão, colorretal e linfoma Esclerose Múltipla (falhados) Gasto anual estimado (R$) 500 milhões 361 milhões 177 milhões 132 milhões 127 milhões 41 milhões 6 milhões (R$ / paciente/ano)
32 Tecnologias de alto custo não incorporadas Tecnologia/Ano da avaliação Insulinas análogas (2014) Ranibizumabe (2014) Indicação Justificativa Gasto anual estimado (R$) Diabetes Tipo I e II Degeneração Macular Relacionada à Idade Não demonstrou eficácia superior em relação ao controle glicêmico nem redução da hipoglicemia grave. Ensaios clínicos* de comparação direta entre ranibizumabe e bevacizumabe demonstraram que não há diferença de eficácia e segurança. A dose do ranibizumabe é 5 mais cara que a do bevacizumabe. 3,4 bilhões 250 milhões *CATT - USA, IVAN-UK, VIBERA-Germany, MANTA-Austria, LUCAS-Norway, GEFAL-France, BRAMD - Netherlands
33 Tecnologias de alto custo não incorporadas Tecnologia/Ano da avaliação Indicação Justificativa Gasto anual estimado (R$) Everolimo (2013) Câncer de mama avançado na pósmenopausa I ensaio clínico fase III: a adição de everolimo não aumentou a sobrevida global e qualidade de vida 102 milhões Cetuximabe (2015) Câncer de cabeça e pescoço metastático 2 Ensaios clínicos: um mostra que a adição de cetuximabe não aumenta a sobrevida global e o outro estudo apresenta aumento de 2,7 meses na sobrevida 52 milhões
34 NOVO SITE Site no modelo E-gov Em 2016 : - Versão em inglês e espanhol (PROADI) - Resumos dos Relatórios em inglês e espanhol (UNB)
35 RENAME 2016 DGITS: Evidências Científicas - HC USP; HC Ribeirão Preto; HCPA; HC Botucatu; INC; UNB e UFPE DAF: Formulário Terapêutico Nacional - ABRACIT
36 - Cerca de 100 PCDTs publicados em 5 anos
37 PCDTs para doenças Doenças Raras Painel de Especialistas para a priorização (maio/2014) Apresentação para o Plenário dos resultados (jun/2014) Elaboração de relatório (jul a set/2014) Consulta Pública (out/2014) 834 contribuições Recomendação final da Conitec (dez/2014) Oficina com os Especialistas para a Elaboração do PCDTs (maio/2015) 12 PCDTs em elaboração
38 PROTOCOLOS E DIRETRIZES Nova Portaria SCTIE (estabelece fluxo para elaboração de PCDTs) Guia metodológico (diretriz) Iniciativas para implementação (aplicativo, envolvimento dos pacientes e prescritores, versão para pacientes, etc) Priorização para elaboração e atualização (memo às Secretarias do MS) PROADI HAOC (Triênio: ): 27 PCDTs novos e 57 revisão FNS e OPAS: Protocolos de Uso de OPME INC(5) e INTO (3) FNS: Edital (40 temas)
39 DIREITO E SAÚDE 51 Fichas Técnicas de Tecnologias disponível para o Judiciário (Parceria com CNJ) Participação em audiências sobre ACP
40 DIREITO E SAÚDE Síntese de Evidências (Em breve) - Parceiros: NATS HC UFMG CCATES UFMG UNB
41 SÍNTESE DE EVIDÊNCIAS PARA POLÍTICAS DE SAÚDE: qualificando o uso de evidências científicas nas decisões judiciais POLICY BRIEF Problema: Deficiente uso de evidências científicas nas decisões judiciais sobre tecnologias em saúde. Opções para enfrentar o problema Opção 1 Construção de um banco de dados em linguagem acessível para os magistrados com sínteses de evidências científicas relacionadas às tecnologias em saúde. Opção 2 Curso para operadores do direito sobre como são elaboradas e como interpretar as avaliações de tecnologias em saúde. Opção 3 Sistema de apoio ao judiciário com consultores em saúde.
42 SÍNTESE DE EVIDÊNCIAS PARA POLÍTICAS DE SAÚDE: qualificando o uso de evidências científicas nas decisões judiciais ESTRUTURA DO POLICY BRIEF Contexto e descrição do problema Opções e achados relevantes para a opção segundo as revisões sistemáticas (benefícios, danos, custos, incertezas, principais elementos da opção, percepção dos sujeitos quanto à efetividade) Considerações adicionais sobre equidade das opções Considerações sobre a implementação das opções Diálogo deliberativo
43 Produtos mais judicializados no MS e PRODUTOS MAIS DEMANDADOS EM 2014 REAGENTE PARA DIAGNÓSTICO CLÍNICO, QUANTITATIVO DE GLICOSE, CAPILAR, TIRA VALOR TOTAL ,00 2 INSULINA, ASPART ,55 3 INSULINA, LISPRO ,45 4 ECULIZUMABE* ,08 5 LANCETA, AÇO INOXIDÁVEL,PONTA AFIADA,TRIFACETADA, DESCARTÁVEL, ESTÉRIL, EMBALAGEM INDIVIDUAL, ULTRA FINA ,08 6 INSULINA, GLARGINA ,87 7 INSULINA, GLULISINA ,79 8 RITUXIMABE ,50 9 ELOSULFASE ALFA* ,23 10 ALFAGALSIDASE ,01 11 ICATIBANTO ,98 12 OMEPRAZOL 8.094,00 13 LOMITAPIDA, 5 MG* ,87 INIBIDOR DE ESTERASE, INIBIDOR DE ESTERASE 14 C1 HUMANA, 500 UI, PÓ LIÓFILO PARA INJETÁVEL ,60 15 LOMITAPIDA, 10 MG* ,62 16 TEMOZOLOMIDA ,65 17 ABIRATERONA ,40 18 TRAVOPROSTA ,26 19 SINVASTATINA 4.866,00 20 LOSARTANA 5.173,20 PRODUTOS MAIS DEMANDADOS EM 2013 VALOR TOTAL 1 ECULIZUMABE* ,66 2 REAGENTE PARA DIAGNÓSTICO CLÍNICO, QUANTITATIVO DE GLICOSE, CAPILAR, TIRA ,27 3 ALFAGALSIDASE ,40 4 INSULINA, ASPART ,18 5 INSULINA, LISPRO ,95 6 OMEPRAZOL ,24 7 ICATIBANTO ,96 8 TIOTRÓPIO ,93 9 ÁCIDO ACETILSALICÍLICO, 100 MG 1.870,40 10 CINACALCETE ,00 11 SUNITINIBE ,36 12 BEVACIZUMABE ,51 13 ÁCIDO URSODESOXICÓLICO ,20 14 SORAFENIBE ,80 15 SINVASTATINA 9.487,20 ALFA-1 ANTITRIPSINA (AAT), 20 MG/ML, SOLUÇÃO P/ 16 INFUSÃO INJETÁVEL ,62 17 TEMOZOLOMIDA ,70 18 IDURSULFASE ,50 19 ABIRATERONA ,40 20 CLONAZEPAM 2.424,00 * Sem comercialização no Brasil (Fonte: CMED 20/08/2015)
44 PARTICIPAÇÃO SOCIAL Diálogo com a sociedade Relatório para a Sociedade Formulário para opinião/experiência Formulário técnico-científico Mala direta Cadastro para assinatura no site Boletim informativo mensal
45 RELATÓRIO PARA SOCIEDADE
46 MONITORAMENTO DO HORIZONTE TECNOLÓGICO Informes e alertas de MHT Informe N 1: Stent Bioabsorvível Alerta N 1: Harvoni para Hepatite C Oficina Internacional - dez 2015
47 MONITORAMENTO DA INCORPORAÇÃO Elaboração de metodologia para medicamentos e de alguns relatórios; Projeto com UnB: modelo de monitoramento (medicamento, produto, procedimento e equipamento); Construção do banco de dados.
48 DIRETRIZES Parceria com o CCATES/UFMG Desinvestimento - Próximos passos: Oficina Internacional em novembro e Revisão final do texto para publicação Detalhamento Acadêmico - Piloto: PCDT de Alzheimer - Próximos passos: PCDT de Esclerose Múltipla e disponibilização de materiais
49 REGULAÇÃO DE PREÇOS GT de OPME - Perspectiva de Regulação de Preço de Dispositivos Médicos Implantáveis alteração da Lei da CMED CMED - Coordenação do Secretário da SCTIE - Participação do DGITS no Comitê Técnico-Executivo (CTE) - Atividades no CTE: Casos Omissos, Recursos de Preços, Processos de Multas e Agenda regulatória
50 PARCEIROS CONITEC
51 COOPERAÇÃO INTERNACIONAL Disseminação da experiência em eventos internacionais Visitas técnicas (Noruega) Participação em redes internacionais - REDETSA - INAHTA - EUROSCAN - POLICY FORUM / HTAi -GIN
52
53 REVISTA ELETRÔNICA GESTÃO E SAÚDE - UNB Editorial CONITEC 11 artigos originais 06 relatos de experiência 01 artigo de revisão gestaoesaude.bce.unb.br
54
AVALIAÇÃO DE TECNOLOGIAS EM SAÚDE (ATS)
 AVALIAÇÃO DE TECNOLOGIAS EM SAÚDE (ATS) TECNOLOGIAS EM SAÚDE Medicamentos, equipamentos e procedimentos técnicos, sistemas organizacionais, informacionais, educacionais e de suporte, e programas e protocolos
AVALIAÇÃO DE TECNOLOGIAS EM SAÚDE (ATS) TECNOLOGIAS EM SAÚDE Medicamentos, equipamentos e procedimentos técnicos, sistemas organizacionais, informacionais, educacionais e de suporte, e programas e protocolos
Comitê Executivo da Saúde
 Comitê Executivo da Saúde - Histórico - Audiência Pública - Recomendação 31/2010 CNJ - Aos Tribunais: adoção de medidas para subsidiar os magistrados e demais operadores com informações técnicas; criação
Comitê Executivo da Saúde - Histórico - Audiência Pública - Recomendação 31/2010 CNJ - Aos Tribunais: adoção de medidas para subsidiar os magistrados e demais operadores com informações técnicas; criação
RELATÓRIO PARA A. SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS
 RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS RELATÓRIO PARA A SOCIEDADE Este relatório é uma versão resumida do relatório técnico
RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS RELATÓRIO PARA A SOCIEDADE Este relatório é uma versão resumida do relatório técnico
CONSELHO REGIONAL DE MEDICINA DO ESTADO DE SÃO PAULO
 CONSELHO REGIONAL DE MEDICINA DO ESTADO DE SÃO PAULO JUDICIALIZAÇÃO DA SAÚDE PANORAMA ESTADUAL PÚBLICO PROPOSTAS RENATA GOMES DOS SANTOS SECRETARIA DE ESTADO DA SAÚDE-SP Maio de 2018 Quantidade de novas
CONSELHO REGIONAL DE MEDICINA DO ESTADO DE SÃO PAULO JUDICIALIZAÇÃO DA SAÚDE PANORAMA ESTADUAL PÚBLICO PROPOSTAS RENATA GOMES DOS SANTOS SECRETARIA DE ESTADO DA SAÚDE-SP Maio de 2018 Quantidade de novas
Antirretroviral etravirina 200mg para o tratamento da infecção pelo HIV
 Antirretroviral etravirina 200mg para o tratamento da infecção pelo HIV N o 255 Março/2017 1 2017 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que
Antirretroviral etravirina 200mg para o tratamento da infecção pelo HIV N o 255 Março/2017 1 2017 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que
Ampliação de concentrações de somatropina para o tratamento de pacientes com síndrome de Turner e de pacientes com deficiência de hormônio de
 Ampliação de concentrações de somatropina para o tratamento de pacientes com síndrome de Turner e de pacientes com deficiência de hormônio de crescimento Hipopituitarismo Nº 297 Outubro/2017 1 2017 Ministério
Ampliação de concentrações de somatropina para o tratamento de pacientes com síndrome de Turner e de pacientes com deficiência de hormônio de crescimento Hipopituitarismo Nº 297 Outubro/2017 1 2017 Ministério
III Fórum Nacional de Produtos para Saúde Brasília, setembro Inovação é acesso. Fabiana Raynal Floriano DGITS/SCTIE/MS
 III Fórum Nacional de Produtos para Saúde Brasília, setembro 2016 Inovação é acesso Fabiana Raynal Floriano DGITS/SCTIE/MS INOVAÇÃO Definição: introdução de novidade ou aperfeiçoamento no ambiente produtivo
III Fórum Nacional de Produtos para Saúde Brasília, setembro 2016 Inovação é acesso Fabiana Raynal Floriano DGITS/SCTIE/MS INOVAÇÃO Definição: introdução de novidade ou aperfeiçoamento no ambiente produtivo
Análise Crítica da Incorporação Tecnológica no SUS: Lei /11
 Análise Crítica da Incorporação Tecnológica no SUS: Lei 12.401/11 LENIR SANTOS 16 DE AGOSTO DE 2011 SALVADOR-BA Lenir Santos 25/8/2011 1 LEI 12.401/2011 ALTERA A LEI 8080/90 Objeto da Lei: explicitar o
Análise Crítica da Incorporação Tecnológica no SUS: Lei 12.401/11 LENIR SANTOS 16 DE AGOSTO DE 2011 SALVADOR-BA Lenir Santos 25/8/2011 1 LEI 12.401/2011 ALTERA A LEI 8080/90 Objeto da Lei: explicitar o
BRASIL Contexto Nacional
 UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO Ins9tuto Nacional de Ciência e Tecnologia para Avaliação de Tecnologias em Saúde (IATS) BRASIL Contexto Nacional Denizar Vianna 1. Sistema de Saúde Brasileiro 2.
UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO Ins9tuto Nacional de Ciência e Tecnologia para Avaliação de Tecnologias em Saúde (IATS) BRASIL Contexto Nacional Denizar Vianna 1. Sistema de Saúde Brasileiro 2.
SEMINÁRIO: " O SETOR DE SAÚDE COMO MODELO
 SEMINÁRIO: " O SETOR DE SAÚDE COMO MODELO PRODUTIVO E DE DESENVOLVIMENTO ECONÔMICO " Painel 2: Alternativas para reduzir a judicialização e garantir uma assistência à saúde justa e equânime aos brasileiros
SEMINÁRIO: " O SETOR DE SAÚDE COMO MODELO PRODUTIVO E DE DESENVOLVIMENTO ECONÔMICO " Painel 2: Alternativas para reduzir a judicialização e garantir uma assistência à saúde justa e equânime aos brasileiros
Redes de Atenção à Saúde e o Cuidado às Pessoas com TEA no SUS
 Redes de Atenção à Saúde e o Cuidado às Pessoas com TEA no SUS Viver Sem Limite - Marco Legal Nacional e Internacional Convenção sobre os Direitos da Pessoa com Deficiência (NY, 2007) Decreto Presidencial
Redes de Atenção à Saúde e o Cuidado às Pessoas com TEA no SUS Viver Sem Limite - Marco Legal Nacional e Internacional Convenção sobre os Direitos da Pessoa com Deficiência (NY, 2007) Decreto Presidencial
Comitê de Avaliação de Tecnologias (ATS) ) do Hospital Israelita Albert Einstein
 Comitê de Avaliação de Tecnologias (ATS) ) do Hospital Israelita Albert Einstein Luiz Vicente Rizzo Diretor Superintendente Instituto Israelita de Ensino e Pesquisa Albert Einstein Avaliação de Tecnologia
Comitê de Avaliação de Tecnologias (ATS) ) do Hospital Israelita Albert Einstein Luiz Vicente Rizzo Diretor Superintendente Instituto Israelita de Ensino e Pesquisa Albert Einstein Avaliação de Tecnologia
Avaliação de Tecnologia em Saúde na Qualificação dos Gastos
 IV Jornada de Economia da Saúde Agosto 2008 Avaliação de Tecnologia em Saúde na Qualificação dos Gastos Rosimary Almeida Gerência de Avaliação de Tecnologia - GEATS Diretoria de Desenvolvimento Setorial
IV Jornada de Economia da Saúde Agosto 2008 Avaliação de Tecnologia em Saúde na Qualificação dos Gastos Rosimary Almeida Gerência de Avaliação de Tecnologia - GEATS Diretoria de Desenvolvimento Setorial
Judicialização da Saúde no Brasil
 Judicialização da Saúde no Brasil Judicialização no contexto do SUS Assistência Farmacêutica Desenvolvimento tecnológico Incorporação de Novas Tecnologias Ações realizadas pelo Ministério da Saúde O Brasil
Judicialização da Saúde no Brasil Judicialização no contexto do SUS Assistência Farmacêutica Desenvolvimento tecnológico Incorporação de Novas Tecnologias Ações realizadas pelo Ministério da Saúde O Brasil
Antoine Daher Presidente da Casa Hunter
 Antoine Daher Presidente da Casa Hunter ESTUDOS NO MUNDO SOBRE MEDICAMENTOS PARA DOENÇAS RARAS 1155 estudos Fonte: www.clinicaltrials.gov ESTUDOS NA AMÉRICA LATINA SOBRE DOENÇAS RARAS 36 estudos Fonte:
Antoine Daher Presidente da Casa Hunter ESTUDOS NO MUNDO SOBRE MEDICAMENTOS PARA DOENÇAS RARAS 1155 estudos Fonte: www.clinicaltrials.gov ESTUDOS NA AMÉRICA LATINA SOBRE DOENÇAS RARAS 36 estudos Fonte:
Doxiciclina para tratamento da Donovanose
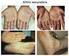 Doxiciclina para tratamento da Donovanose N o 156 Outubro/2015 1 2015 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que não seja para venda ou qualquer
Doxiciclina para tratamento da Donovanose N o 156 Outubro/2015 1 2015 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que não seja para venda ou qualquer
Acesso aos medicamentos e globalização: questões éticas e sociais.
 Acesso aos medicamentos e globalização: questões éticas e sociais. Atelier 1 As Políticas Públicas de acesso aos medicamentos. O contexto e os principais determinantes da política brasileira de. Montreal
Acesso aos medicamentos e globalização: questões éticas e sociais. Atelier 1 As Políticas Públicas de acesso aos medicamentos. O contexto e os principais determinantes da política brasileira de. Montreal
Saúde Pública de qualidade para cuidar bem das pessoas: direito do povo brasileiro
 Saúde Pública de qualidade para cuidar bem das pessoas: direito do povo brasileiro Prof. Marcos Alex Mendes da Silva PhD, MsC, Especialista em Gestão em Saúde Prof. Adjunto FOUFF Nova Friburgo Ciência,
Saúde Pública de qualidade para cuidar bem das pessoas: direito do povo brasileiro Prof. Marcos Alex Mendes da Silva PhD, MsC, Especialista em Gestão em Saúde Prof. Adjunto FOUFF Nova Friburgo Ciência,
Coordenadoria de Gestão do Trabalho e da Educação em Saúde. Núcleo de Ciência e Tecnologias em Saúde
 Coordenadoria de Gestão do Trabalho e da Educação em Saúde Núcleo de Ciência e Tecnologias em Saúde Comissão de Avaliação de Tecnologias em Saúde do Estado do Ceará 2012 COMISSÃO DE AVALIAÇÃO DE TECNOLOGIAS
Coordenadoria de Gestão do Trabalho e da Educação em Saúde Núcleo de Ciência e Tecnologias em Saúde Comissão de Avaliação de Tecnologias em Saúde do Estado do Ceará 2012 COMISSÃO DE AVALIAÇÃO DE TECNOLOGIAS
Rio de Janeiro, 08 de dezembro de 2009
 IX Encontro Nacional de Economia da Saúde Rio de Janeiro, 08 de dezembro de 2009 O Estado da Arte da Avaliação de Tecnologias no Brasil Gabrielle Troncoso Gerência de Avaliação Econômica de Novas Tecnologias
IX Encontro Nacional de Economia da Saúde Rio de Janeiro, 08 de dezembro de 2009 O Estado da Arte da Avaliação de Tecnologias no Brasil Gabrielle Troncoso Gerência de Avaliação Econômica de Novas Tecnologias
AÇÕES PARA SAÚDE. Saúde Suplementar: Desafios e Perspectivas
 AÇÕES PARA SAÚDE Saúde Suplementar: Desafios e Perspectivas Muito imposto X baixa qualidade 90% dos brasileiros avaliam que pagam muitos impostos e têm serviços públicos de baixa qualidade Os serviços
AÇÕES PARA SAÚDE Saúde Suplementar: Desafios e Perspectivas Muito imposto X baixa qualidade 90% dos brasileiros avaliam que pagam muitos impostos e têm serviços públicos de baixa qualidade Os serviços
BRAZIL The New Hepatitis C Treatment Protocol
 BRAZIL The New Hepatitis C Treatment Protocol Paulo Roberto Lerias de Almeida Hospital Nossa Senhora da Conceição - Pôrto Alegre Secretaria Estadual da Saúde do Rio Grande do Sul Ministério da Saúde DISCLOSURE
BRAZIL The New Hepatitis C Treatment Protocol Paulo Roberto Lerias de Almeida Hospital Nossa Senhora da Conceição - Pôrto Alegre Secretaria Estadual da Saúde do Rio Grande do Sul Ministério da Saúde DISCLOSURE
SUS SINDUSFARMA. Clarice Petramale
 Seminário Incorporação de Novas Tecnologias no SUS SINDUSFARMA Clarice Petramale Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde Diretora do Departamento de Gestão e Incorporação
Seminário Incorporação de Novas Tecnologias no SUS SINDUSFARMA Clarice Petramale Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde Diretora do Departamento de Gestão e Incorporação
número 29 - setembro/2016 RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS
 número 29 - setembro/2016 RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS INSULINAS ANÁLOGAS RÁPIDAS NO TRATAMENTO DO DIABETES MELLITUS
número 29 - setembro/2016 RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS INSULINAS ANÁLOGAS RÁPIDAS NO TRATAMENTO DO DIABETES MELLITUS
COMPONENTES DA ASSISTÊNCIA FARMACÊUTICA NO SUS
 TEXTOS DIDÁTICOS DO CEMED Nº 2.c Compreendendo o SUS e a Assistência Farmacêutica Módulo 2 Tema 7 Aula Expositiva 4 COMPONENTES DA ASSISTÊNCIA FARMACÊUTICA NO SUS Verlanda Lima Bontempo Secretaria de Estado
TEXTOS DIDÁTICOS DO CEMED Nº 2.c Compreendendo o SUS e a Assistência Farmacêutica Módulo 2 Tema 7 Aula Expositiva 4 COMPONENTES DA ASSISTÊNCIA FARMACÊUTICA NO SUS Verlanda Lima Bontempo Secretaria de Estado
SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS RELATÓRIO PARA A
 número 08 - agosto/2015 DECISÃO FINAL RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS RELATÓRIO PARA A SOCIEDADE Este relatório é
número 08 - agosto/2015 DECISÃO FINAL RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS RELATÓRIO PARA A SOCIEDADE Este relatório é
A ASSISTÊNCIA FARMACÊUTICA NA REDE DE ATENÇÃO A SAÚDE. Salvador 2017
 A ASSISTÊNCIA FARMACÊUTICA NA REDE DE ATENÇÃO A SAÚDE Salvador 2017 Assistência Farmacêutica no SUS Lei nº. 8080/ 1990: Art. 6, 1, Al. d Reconhece a assistência terapêutica integral, inclusive farmacêutica,
A ASSISTÊNCIA FARMACÊUTICA NA REDE DE ATENÇÃO A SAÚDE Salvador 2017 Assistência Farmacêutica no SUS Lei nº. 8080/ 1990: Art. 6, 1, Al. d Reconhece a assistência terapêutica integral, inclusive farmacêutica,
Estudos de avaliação de tecnologias em saúde e a incorporação de novas tecnologias no sistema de saúde
 ABRES 2014 - XI Encontro Nacional de Economia da Saúde & VI Encontro Latino Americano de Economia da Saúde Estudos de avaliação de tecnologias em saúde e a incorporação de novas tecnologias no sistema
ABRES 2014 - XI Encontro Nacional de Economia da Saúde & VI Encontro Latino Americano de Economia da Saúde Estudos de avaliação de tecnologias em saúde e a incorporação de novas tecnologias no sistema
Custo Benefício Tratar F0-F1
 Custo Benefício Tratar F0-F1 Maria Cássia Mendes-Correa Faculdade de Medicina da USP Departamento de Vigilância, Prevenção e Controle das IST, do HIV/Aids e das Hepatites Virais - SVS Ano Prevalência
Custo Benefício Tratar F0-F1 Maria Cássia Mendes-Correa Faculdade de Medicina da USP Departamento de Vigilância, Prevenção e Controle das IST, do HIV/Aids e das Hepatites Virais - SVS Ano Prevalência
Desafios Atuais do Ministério da Saúde para o Tratamento da Hepatite C no Brasil
 Desafios Atuais do Ministério da Saúde para o Tratamento da Hepatite C no Brasil Elisa Cattapan Ministério da Saúde Secretaria de Vigilância em Saúde Departamento de DST, AIDS e Hepatites Virais Coordenação
Desafios Atuais do Ministério da Saúde para o Tratamento da Hepatite C no Brasil Elisa Cattapan Ministério da Saúde Secretaria de Vigilância em Saúde Departamento de DST, AIDS e Hepatites Virais Coordenação
SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS
 n. 62 publicado em agosto/2017 RELATÓRIO PARA SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS SECUQUINUMABE PARA O TRATAMENTO DA ESPONDILITE ANQUILOSANTE
n. 62 publicado em agosto/2017 RELATÓRIO PARA SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS SECUQUINUMABE PARA O TRATAMENTO DA ESPONDILITE ANQUILOSANTE
Cipionato de Hidrocortisona, comprimidos de 10 mg e 20 mg, para tratamento de hiperplasia adrenal congênita de recém-nascidos diagnosticados no
 Cipionato de Hidrocortisona, comprimidos de 10 mg e 20 mg, para tratamento de hiperplasia adrenal congênita de recém-nascidos diagnosticados no programa nacional de triagem neonatal- PNTN. N o 146 Março/2015
Cipionato de Hidrocortisona, comprimidos de 10 mg e 20 mg, para tratamento de hiperplasia adrenal congênita de recém-nascidos diagnosticados no programa nacional de triagem neonatal- PNTN. N o 146 Março/2015
Comissão Nacional de Incorporação de Tecnologias em Saúde no SUS CONITEC
 Comissão Nacional de Incorporação de Tecnologias em Saúde no SUS CONITEC Brasília, abril de 2013 MS CONITEC Histórico Legislação: Portaria GM/MS 152 19 de janeiro de 2006 - Fluxo para incorporação de tecnologias
Comissão Nacional de Incorporação de Tecnologias em Saúde no SUS CONITEC Brasília, abril de 2013 MS CONITEC Histórico Legislação: Portaria GM/MS 152 19 de janeiro de 2006 - Fluxo para incorporação de tecnologias
RIPSA: uma iniciativa brasileira
 Rede Interagencial de Informação para a Saúde Ministério da Saúde OPS/OMS RIPSA: uma iniciativa brasileira CRICS-8 Rio de Janeiro, 18 setembro 2008 João B. Risi Jr. Informação para decisão: uma questão
Rede Interagencial de Informação para a Saúde Ministério da Saúde OPS/OMS RIPSA: uma iniciativa brasileira CRICS-8 Rio de Janeiro, 18 setembro 2008 João B. Risi Jr. Informação para decisão: uma questão
Consenso Brasileiro em Doença de Chagas e Protocolo Clínico e Diretrizes Terapêuticas - PCDT
 REUNIÃO ANUAL DA PLATAFORMA DE PESQUISA CLÍNICA PARA A DOENÇA DE CHAGAS DNDi 2016 Consenso Brasileiro em Doença de Chagas e Protocolo Clínico e Diretrizes Terapêuticas - PCDT Renato Vieira Alves Ministério
REUNIÃO ANUAL DA PLATAFORMA DE PESQUISA CLÍNICA PARA A DOENÇA DE CHAGAS DNDi 2016 Consenso Brasileiro em Doença de Chagas e Protocolo Clínico e Diretrizes Terapêuticas - PCDT Renato Vieira Alves Ministério
10º Encontro Nacional de Inovação em Fármacos e Medicamentos (ENIFarMed)
 10º Encontro Nacional de Inovação em Fármacos e Medicamentos (ENIFarMed) DIAGNÓSTICO MEDICAMENTO TRATAMENTO ACOMPANHAMENTO MULTIDISCIPLINAR ESTUDOS NO MUNDO SOBRE MEDICAMENTOS PARA DOENÇAS RARAS 1155
10º Encontro Nacional de Inovação em Fármacos e Medicamentos (ENIFarMed) DIAGNÓSTICO MEDICAMENTO TRATAMENTO ACOMPANHAMENTO MULTIDISCIPLINAR ESTUDOS NO MUNDO SOBRE MEDICAMENTOS PARA DOENÇAS RARAS 1155
O papel dos laboratórios oficiais no acesso a medicamentos no SUS
 O papel dos laboratórios oficiais no acesso a medicamentos no SUS Os desafios da expansão de produção de fármacos para os componentes as Assistência Farmacêutica No Brasil, o desabastecimento de medicamentos
O papel dos laboratórios oficiais no acesso a medicamentos no SUS Os desafios da expansão de produção de fármacos para os componentes as Assistência Farmacêutica No Brasil, o desabastecimento de medicamentos
Impacto das Novas Tecnologias em Saúde. Prof. Dr. Alex Itria IPTSP-UFG/IATS
 Impacto das Novas Tecnologias em Saúde Prof. Dr. Alex Itria IPTSP-UFG/IATS 1 Instituto Nacional de Ciência e Tecnologia para Avaliação de Tecnologia em Saúde (IATS) Universidade Federal de Goiânia Instituto
Impacto das Novas Tecnologias em Saúde Prof. Dr. Alex Itria IPTSP-UFG/IATS 1 Instituto Nacional de Ciência e Tecnologia para Avaliação de Tecnologia em Saúde (IATS) Universidade Federal de Goiânia Instituto
PORTARIAS DE DIRETRIZES PARA REGULAÇÃO e INCENTIVO DE CUSTEIO PARA COMPLEXOS REGULADORES
 Secretaria de Atenção à Saúde Departamento de Regulação, Avaliação e Controle de Sistemas Coordenação-Geral de Regulação e Avaliação PORTARIAS DE DIRETRIZES PARA REGULAÇÃO e INCENTIVO DE CUSTEIO PARA COMPLEXOS
Secretaria de Atenção à Saúde Departamento de Regulação, Avaliação e Controle de Sistemas Coordenação-Geral de Regulação e Avaliação PORTARIAS DE DIRETRIZES PARA REGULAÇÃO e INCENTIVO DE CUSTEIO PARA COMPLEXOS
Como evitar ou racionalizar a judicialização. Desembargador Renato Dresch
 Como evitar ou racionalizar a judicialização Desembargador Renato Dresch A AS CAUSAS DAS JUDICIALIZAÇÃO Princípio da inafastabilidade da jurisdição Constituição Federal de 1988 Art. 5º Todos são iguais
Como evitar ou racionalizar a judicialização Desembargador Renato Dresch A AS CAUSAS DAS JUDICIALIZAÇÃO Princípio da inafastabilidade da jurisdição Constituição Federal de 1988 Art. 5º Todos são iguais
PORTARIA CONJUNTA Nº 19, DE 3 DE JULHO DE Aprova as Diretrizes Diagnósticas e Terapêuticas do Carcinoma de Mama.
 PORTARIA CONJUNTA Nº 19, DE 3 DE JULHO DE 2018 Aprova as Diretrizes Diagnósticas e Terapêuticas do Carcinoma de Mama. O SECRETÁRIO DE ATENÇÃO À SAÚDE e o SECRETÁRIO DE CIÊNCIA, TECNOLOGIA E INSUMOS ESTRATÉGICOS,
PORTARIA CONJUNTA Nº 19, DE 3 DE JULHO DE 2018 Aprova as Diretrizes Diagnósticas e Terapêuticas do Carcinoma de Mama. O SECRETÁRIO DE ATENÇÃO À SAÚDE e o SECRETÁRIO DE CIÊNCIA, TECNOLOGIA E INSUMOS ESTRATÉGICOS,
COMISSÃO NACIONAL DE INCORPORAÇÃO DE TECNOLOGIAS NO SISTEMA ÚNICO DE SAÚDE (CONITEC)
 Relatório COMISSÃO NACIONAL DE INCORPORAÇÃO DE TECNOLOGIAS NO SISTEMA ÚNICO DE SAÚDE (CONITEC) 74ª Reunião Ordinária Item 15. Informe: Antiangiogênicos (bevacizumabe e ranibizumabe) para o tratamento do
Relatório COMISSÃO NACIONAL DE INCORPORAÇÃO DE TECNOLOGIAS NO SISTEMA ÚNICO DE SAÚDE (CONITEC) 74ª Reunião Ordinária Item 15. Informe: Antiangiogênicos (bevacizumabe e ranibizumabe) para o tratamento do
2016 RELATÓRIO TÉCNICO
 ORGANIZAÇÃO MUNDIAL DA SAÚDE ORGANIZAÇÃO PAN-AMERICANA DA SAÚDE REPRESENTAÇÃO NO BRASIL Medicamentos e Tecnologias em Saúde MINISTÉRIO DA SAÚDE Secretaria de Ciência, Tecnologia e Insumos Estratégicos
ORGANIZAÇÃO MUNDIAL DA SAÚDE ORGANIZAÇÃO PAN-AMERICANA DA SAÚDE REPRESENTAÇÃO NO BRASIL Medicamentos e Tecnologias em Saúde MINISTÉRIO DA SAÚDE Secretaria de Ciência, Tecnologia e Insumos Estratégicos
Políticas de expansão do atendimento oncológico
 Rede de atenção à saúde das pessoas com doenças crônicas Políticas de expansão do atendimento oncológico Atenção Básica: Reforço da prevenção (câncer de colo de útero e câncer de mama): Atualização das
Rede de atenção à saúde das pessoas com doenças crônicas Políticas de expansão do atendimento oncológico Atenção Básica: Reforço da prevenção (câncer de colo de útero e câncer de mama): Atualização das
Implementação do Núcleo de Segurança do Paciente e elaboração do Plano de Segurança do Paciente. Helaine Carneiro Capucho, DSc.
 Implementação do Núcleo de Segurança do Paciente e elaboração do Plano de Segurança do Paciente Helaine Carneiro Capucho, DSc. 21 de março de 2016 2007 Implantação do Comitê de Segurança do Paciente
Implementação do Núcleo de Segurança do Paciente e elaboração do Plano de Segurança do Paciente Helaine Carneiro Capucho, DSc. 21 de março de 2016 2007 Implantação do Comitê de Segurança do Paciente
PAINEL - ALTERNATIVAS
 PORTO ALEGRE, RS PAINEL - ALTERNATIVAS 06/10/2017 Flavio Badaró Núcleo de Assessoria Técnica em Ações de Saúde Secretaria de Estado de Saúde do Rio de Janeiro PODER JUDICIÁRIO JUSTIÇA FEDERAL Seção Judiciária
PORTO ALEGRE, RS PAINEL - ALTERNATIVAS 06/10/2017 Flavio Badaró Núcleo de Assessoria Técnica em Ações de Saúde Secretaria de Estado de Saúde do Rio de Janeiro PODER JUDICIÁRIO JUSTIÇA FEDERAL Seção Judiciária
Componente Especializado da Assistência Farmacêutica. Revisão da 2ª Edição: Carolina Rodrigues Gomes e Vera Lúcia Edais Pepe
 Componente Especializado da Assistência Farmacêutica Autora: Tatiana Aragão Figueiredo Revisão da 2ª Edição: Carolina Rodrigues Gomes e Vera Lúcia Edais Pepe Revisoras da 1ª Edição: Ana Márcia Messeder
Componente Especializado da Assistência Farmacêutica Autora: Tatiana Aragão Figueiredo Revisão da 2ª Edição: Carolina Rodrigues Gomes e Vera Lúcia Edais Pepe Revisoras da 1ª Edição: Ana Márcia Messeder
Consulta Pública nº 03/2017
 Resolução nº, de de de 20 Ementa: Regulamenta a atuação do farmacêutico na prestação de serviços e assessoramento técnico sobre informação de medicamentos e produtos para a saúde. O Conselho Federal de
Resolução nº, de de de 20 Ementa: Regulamenta a atuação do farmacêutico na prestação de serviços e assessoramento técnico sobre informação de medicamentos e produtos para a saúde. O Conselho Federal de
Diretrizes Nacionais de Assitência ao Parto Normal
 Diretrizes Nacionais de Assitência ao Parto Normal N o 211 Março/2017 2017 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que não seja para venda
Diretrizes Nacionais de Assitência ao Parto Normal N o 211 Março/2017 2017 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que não seja para venda
ENCOMENDA TECNOLÓGICA NA SAÚDE
 ENCOMENDA TECNOLÓGICA NA SAÚDE Ministério da Saúde Secretaria de Ciência, Tecnologia e Insumos Estratégicos Departamento do Complexo Industrial e Inovação em Saúde O PODER DE COMPRA DA SAÚDE EM PROL DO
ENCOMENDA TECNOLÓGICA NA SAÚDE Ministério da Saúde Secretaria de Ciência, Tecnologia e Insumos Estratégicos Departamento do Complexo Industrial e Inovação em Saúde O PODER DE COMPRA DA SAÚDE EM PROL DO
Secretaria de Vigilância em Saúde Ministério da Saúde
 Programa Nacional para a Prevenção e o Controle das Hepatites Virais Secretaria de Vigilância em Saúde Ministério da Saúde Ministério da Saúde Secretaria de Atenção à Saúde Secretaria de Vigilância em
Programa Nacional para a Prevenção e o Controle das Hepatites Virais Secretaria de Vigilância em Saúde Ministério da Saúde Ministério da Saúde Secretaria de Atenção à Saúde Secretaria de Vigilância em
Ministério da Saúde Gabinete do Ministro PORTARIA Nº 2.915, DE 12 DE DEZEMBRO DE 2011
 Ministério da Saúde Gabinete do Ministro PORTARIA Nº 2.915, DE 12 DE DEZEMBRO DE 2011 Institui a Rede Brasileira de Avaliação de Tecnologias em Saúde (REBRATS). O MINISTRO DE ESTADO DA SAÚDE, no uso das
Ministério da Saúde Gabinete do Ministro PORTARIA Nº 2.915, DE 12 DE DEZEMBRO DE 2011 Institui a Rede Brasileira de Avaliação de Tecnologias em Saúde (REBRATS). O MINISTRO DE ESTADO DA SAÚDE, no uso das
Rede Nacional de Pesquisa Clínica em Hospitais de Ensino RNPC
 Rede Nacional de Pesquisa Clínica em Hospitais de Ensino RNPC XXXIV Congresso da Sociedade Brasileira de Medicina Farmacêutica SBMF São Paulo, 27 de novembro de 2008. Sandra Ceciliano de Souza Veloso Departamento
Rede Nacional de Pesquisa Clínica em Hospitais de Ensino RNPC XXXIV Congresso da Sociedade Brasileira de Medicina Farmacêutica SBMF São Paulo, 27 de novembro de 2008. Sandra Ceciliano de Souza Veloso Departamento
Desdobrando o Mapa Estratégico da Justiça Federal do Rio Grande do Sul
 Desdobrando o Mapa Estratégico da Justiça Federal do Rio Grande do Sul Marcelo De Nardi Porto Alegre, 04 de julho de 2011. CONTEXTUALIZAÇÃO Poder Judiciário no Contexto da Gestão Pública Nacional Processos
Desdobrando o Mapa Estratégico da Justiça Federal do Rio Grande do Sul Marcelo De Nardi Porto Alegre, 04 de julho de 2011. CONTEXTUALIZAÇÃO Poder Judiciário no Contexto da Gestão Pública Nacional Processos
número 32 - outubro/2016 RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS
 número 32 - outubro/2016 RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS RELATÓRIO PARA A SOCIEDADE Este relatório é uma versão resumida
número 32 - outubro/2016 RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS RELATÓRIO PARA A SOCIEDADE Este relatório é uma versão resumida
DECRETO Nº 8.389, DE 04 DE JULHO DE 2016.
 DECRETO Nº 8.389, DE 04 DE JULHO DE 2016. Define os critérios para o fornecimento de insumos destinados ao monitoramento da glicemia capilar aos portadores de diabetes cadastrados em Programa de Hipertensão
DECRETO Nº 8.389, DE 04 DE JULHO DE 2016. Define os critérios para o fornecimento de insumos destinados ao monitoramento da glicemia capilar aos portadores de diabetes cadastrados em Programa de Hipertensão
DOCUMENTOS E EXAMES PARA SOLICITAÇÃO INICIAL DE MEDICAMENTOS PARA HEPATITE C (Segundo Portaria MS/SCTIE nº 37 de 24 de julho de 2015)
 ESTADO DO RIO GRANDE DO SUL SECRETARIA DA SAÚDE DO ESTADO COORDENAÇÃO DA POLÍTICA DE ASSISTÊNCIA FARMACÊUTICA DOCUMENTOS E EXAMES PARA SOLICITAÇÃO INICIAL DE MEDICAMENTOS PARA HEPATITE C (Segundo Portaria
ESTADO DO RIO GRANDE DO SUL SECRETARIA DA SAÚDE DO ESTADO COORDENAÇÃO DA POLÍTICA DE ASSISTÊNCIA FARMACÊUTICA DOCUMENTOS E EXAMES PARA SOLICITAÇÃO INICIAL DE MEDICAMENTOS PARA HEPATITE C (Segundo Portaria
MODALIDADES DE ACESSO A MEDICAMENTOS NO BRASIL: DESAFIOS E PERSPECTIVAS PARA AGENDA ATUAL DO SUS. Cleonice Gama DAF/SCTIE/MS
 MODALIDADES DE ACESSO A MEDICAMENTOS NO BRASIL: DESAFIOS E PERSPECTIVAS PARA AGENDA ATUAL DO SUS Cleonice Gama DAF/SCTIE/MS A ASSISTÊNCIA FARMACÊUTICA NO SUS OBJETIVOS A garantia necessária da segurança,
MODALIDADES DE ACESSO A MEDICAMENTOS NO BRASIL: DESAFIOS E PERSPECTIVAS PARA AGENDA ATUAL DO SUS Cleonice Gama DAF/SCTIE/MS A ASSISTÊNCIA FARMACÊUTICA NO SUS OBJETIVOS A garantia necessária da segurança,
Ampliação de uso do naproxeno para osteoartrite de joelho e quadril
 Ampliação de uso do naproxeno para osteoartrite de joelho e quadril N o 298 Agosto/2017 1 2017 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que
Ampliação de uso do naproxeno para osteoartrite de joelho e quadril N o 298 Agosto/2017 1 2017 Ministério da Saúde. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que
Uso Racional de Medicamentos. Felipe Dias Carvalho Consultor Nacional de Desenvolvimento e Inovação Tecnológica em Saúde OPAS/OMS
 Uso Racional de Medicamentos Felipe Dias Carvalho Consultor Nacional de Desenvolvimento e Inovação Tecnológica em Saúde OPAS/OMS Conceito URM - OMS Existe uso racional quando os pacientes recebem medicamentos
Uso Racional de Medicamentos Felipe Dias Carvalho Consultor Nacional de Desenvolvimento e Inovação Tecnológica em Saúde OPAS/OMS Conceito URM - OMS Existe uso racional quando os pacientes recebem medicamentos
REGULAÇÃO NO SISTEMA ÚNICO DE SAÚDE SUS. Setembro/2010
 MINISTÉRIO DA SAÚDE Secretaria de Atenção à Saúde Departamento de Regulação, Avaliação e Controle de Sistemas Coordenação Geral de Regulação e Avaliação REGULAÇÃO NO SISTEMA ÚNICO DE SAÚDE SUS Setembro/2010
MINISTÉRIO DA SAÚDE Secretaria de Atenção à Saúde Departamento de Regulação, Avaliação e Controle de Sistemas Coordenação Geral de Regulação e Avaliação REGULAÇÃO NO SISTEMA ÚNICO DE SAÚDE SUS Setembro/2010
Comissão Nacional de Incorporação de Tecnologias no SUS (CONITEC) - Relatório n 69
 INCORPORAÇÃO DE NOVOS PROCEDIMENTOS RELATIVOS AO PROCESSO TRANSEXUALIZADOR NO ÂMBITO DO SUS Demandante: Departamento de Atenção Especializada/Secretaria de Atenção à Saúde DAE/SAS/MS 1. APRESENTAÇÃO Algumas
INCORPORAÇÃO DE NOVOS PROCEDIMENTOS RELATIVOS AO PROCESSO TRANSEXUALIZADOR NO ÂMBITO DO SUS Demandante: Departamento de Atenção Especializada/Secretaria de Atenção à Saúde DAE/SAS/MS 1. APRESENTAÇÃO Algumas
REGULAÇÃO: acesso equânime, racional e oportuno
 REGULAÇÃO: acesso equânime, racional e oportuno As Políticas de Regulação vêm se desenvolvendo em consonância com osregulação princípios e as diretrizes DE ACESSO do SUS, para viabilizar o acesso equânime
REGULAÇÃO: acesso equânime, racional e oportuno As Políticas de Regulação vêm se desenvolvendo em consonância com osregulação princípios e as diretrizes DE ACESSO do SUS, para viabilizar o acesso equânime
MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DO PARANÁ PRÓ-REITORIA DE EXTENSÃO E CULTURA CHAMADA INTERNA N.º 22/2018 PROEC/UFPR
 CHAMADA INTERNA N.º 22/2018 PROEC/UFPR A Pró-Reitora de Extensão e Cultura (PROEC) da Universidade Federal do Paraná (UFPR), no uso de suas atribuições torna pública a Chamada para apresentação de propostas
CHAMADA INTERNA N.º 22/2018 PROEC/UFPR A Pró-Reitora de Extensão e Cultura (PROEC) da Universidade Federal do Paraná (UFPR), no uso de suas atribuições torna pública a Chamada para apresentação de propostas
ANEXO 2 TEMÁTICAS E CATEGORIAS DAS EXPERIÊNCIAS
 ANEXO 2 TEMÁTICAS E CATEGORIAS DAS EXPERIÊNCIAS TEMÁTICA CATEGORIA ESPECIFICAÇÃO DE RELATO Inclui relatos sobre práticas na elaboração e acompanhamento dos Instrumentos: 1.A FERRAMENTAS DO PLANEJAMENTO
ANEXO 2 TEMÁTICAS E CATEGORIAS DAS EXPERIÊNCIAS TEMÁTICA CATEGORIA ESPECIFICAÇÃO DE RELATO Inclui relatos sobre práticas na elaboração e acompanhamento dos Instrumentos: 1.A FERRAMENTAS DO PLANEJAMENTO
GESTÃO DA MÉDIA E ALTA COMPLEXIDADE NO SUS PARA ALÉM DOS REGISTROS DE ALTA INCORPORAÇÃO DE TECNOLOGIA MÉDICA
 GESTÃO DA MÉDIA E ALTA COMPLEXIDADE NO SUS PARA ALÉM DOS REGISTROS DE ALTA INCORPORAÇÃO DE TECNOLOGIA MÉDICA Marília C. P. Louvison Faculdade de Saúde Pública da USP 2016 mariliacpl@gmail.com Princípios
GESTÃO DA MÉDIA E ALTA COMPLEXIDADE NO SUS PARA ALÉM DOS REGISTROS DE ALTA INCORPORAÇÃO DE TECNOLOGIA MÉDICA Marília C. P. Louvison Faculdade de Saúde Pública da USP 2016 mariliacpl@gmail.com Princípios
III Fórum Nacional de Produtos para a Saúde no Brasil 1º
 III Fórum Nacional de Produtos para a Saúde no Brasil 1º.9.2016 Um pouco da nossa história Foi fundada e esse ano completou 83 anos de existência Laboratórios farmacêuticos nacionais e internacionais e
III Fórum Nacional de Produtos para a Saúde no Brasil 1º.9.2016 Um pouco da nossa história Foi fundada e esse ano completou 83 anos de existência Laboratórios farmacêuticos nacionais e internacionais e
Exemplos de Padrões de Prescrição Influenciados pela Indústria Farmacêutica no Sistema Público Brasileiro
 Exemplos de Padrões de Prescrição Influenciados pela Indústria Farmacêutica no Sistema Público Brasileiro Prof. Paulo D. Picon, MD PhD Declaração de Conflitos de Interesses Nenhum conflito de interesses
Exemplos de Padrões de Prescrição Influenciados pela Indústria Farmacêutica no Sistema Público Brasileiro Prof. Paulo D. Picon, MD PhD Declaração de Conflitos de Interesses Nenhum conflito de interesses
PROGRAMA SEMINÁRIO DE SAÚDE VIGILÂNCIA SANITÁRIA
 PROGRAMA SEMINÁRIO DE SAÚDE VIGILÂNCIA SANITÁRIA Q UA LIDA DE REG ULATÓ R I A R E G U L A Ç Ã O E V I G I L Â N C I A S A N I TÁ R I A : O P R O G R A M A D E M E L H O R I A D O P R O C E S S O D E R
PROGRAMA SEMINÁRIO DE SAÚDE VIGILÂNCIA SANITÁRIA Q UA LIDA DE REG ULATÓ R I A R E G U L A Ç Ã O E V I G I L Â N C I A S A N I TÁ R I A : O P R O G R A M A D E M E L H O R I A D O P R O C E S S O D E R
Tatiana Accioly Fayad Gerente Jurídica
 Tatiana Accioly Fayad Gerente Jurídica UNIMED GOIÂNIA COOPERATIVA MÉDICA (Lei 5.764/71) e OPERADORA DE PLANOS DE SAÚDE (Lei 9.656/98) Lei 9656/98 Lei dos Planos de Saúde Lei relativamente nova (20 anos)
Tatiana Accioly Fayad Gerente Jurídica UNIMED GOIÂNIA COOPERATIVA MÉDICA (Lei 5.764/71) e OPERADORA DE PLANOS DE SAÚDE (Lei 9.656/98) Lei 9656/98 Lei dos Planos de Saúde Lei relativamente nova (20 anos)
RETIFICAÇÃO/ LEGISLAÇÃO COMPLEMENTAR
 RETIFICAÇÃO/ LEGISLAÇÃO COMPLEMENTAR RESOLUÇÃO N. 198 DO CONSELHO NACIONAL DE JUSTIÇA. RESOLUÇÃO Nº 198, DE 1º DE JULHO DE 2014 COMUNICADO O Secretário-Geral Adjunto do Conselho Nacional de Justiça, com
RETIFICAÇÃO/ LEGISLAÇÃO COMPLEMENTAR RESOLUÇÃO N. 198 DO CONSELHO NACIONAL DE JUSTIÇA. RESOLUÇÃO Nº 198, DE 1º DE JULHO DE 2014 COMUNICADO O Secretário-Geral Adjunto do Conselho Nacional de Justiça, com
RESPOSTA RÁPIDA 387/2013
 RESPOSTA RÁPIDA 387/2013 SOLICITANTE NÚMERO DO PROCESSO Juíza de Direito em Substituição Comarca de Cláudio MG 0022220-88-2013 (0166.13.002222-0) DATA 27/11/2013 SOLICITAÇÃO Solicitação de: Insulina Glargina
RESPOSTA RÁPIDA 387/2013 SOLICITANTE NÚMERO DO PROCESSO Juíza de Direito em Substituição Comarca de Cláudio MG 0022220-88-2013 (0166.13.002222-0) DATA 27/11/2013 SOLICITAÇÃO Solicitação de: Insulina Glargina
MODELO DE GESTÃO E DE ORGANIZAÇÃO DO CUIDADO HOSPITALAR "Acesso e Regulação"
 MODELO DE GESTÃO E DE ORGANIZAÇÃO DO CUIDADO HOSPITALAR "Acesso e Regulação" 31º Congresso de Secretários Municipais de Saúde do Estado de São Paulo Renata Martello Gestora Hospitalar CONTEXTO TRANSIÇÃO
MODELO DE GESTÃO E DE ORGANIZAÇÃO DO CUIDADO HOSPITALAR "Acesso e Regulação" 31º Congresso de Secretários Municipais de Saúde do Estado de São Paulo Renata Martello Gestora Hospitalar CONTEXTO TRANSIÇÃO
PORTARIA No- 252, DE 26 DE JANEIRO DE 2017
 PORTARIA No- 252, DE 26 DE JANEIRO DE 2017 Define a lista de produtos estratégicos para o Sistema Único de Saúde (SUS), nos termos dos anexos a esta Portaria. O MINISTRO DE ESTADO DA SAÚDE, no uso das
PORTARIA No- 252, DE 26 DE JANEIRO DE 2017 Define a lista de produtos estratégicos para o Sistema Único de Saúde (SUS), nos termos dos anexos a esta Portaria. O MINISTRO DE ESTADO DA SAÚDE, no uso das
CONGRESSO DE SECRETÁRIOS MUNICIPAIS DE SAÚDE DE SÃO PAULO. Implicações na prática da Assistência à Saúde no SUS. Mar/2012
 CONGRESSO DE SECRETÁRIOS MUNICIPAIS DE SAÚDE DE SÃO PAULO Implicações na prática da Assistência à Saúde no SUS Mar/2012 O SUS HOJE IDSUS aponta problemas de acesso e de qualidade do sistema na maioria
CONGRESSO DE SECRETÁRIOS MUNICIPAIS DE SAÚDE DE SÃO PAULO Implicações na prática da Assistência à Saúde no SUS Mar/2012 O SUS HOJE IDSUS aponta problemas de acesso e de qualidade do sistema na maioria
O que o Estado Brasileiro Necessita Fazer para Ativar o Desenvolvimento Tecnológico de Biológicos no Brasil?
 III Seminário Anual Científico e Tecnológico de Bio-Manguinhos Rio de Janeiro, 04 de maio de 2015. O que o Estado Brasileiro Necessita Fazer para Ativar o Desenvolvimento Tecnológico de Biológicos no Brasil?
III Seminário Anual Científico e Tecnológico de Bio-Manguinhos Rio de Janeiro, 04 de maio de 2015. O que o Estado Brasileiro Necessita Fazer para Ativar o Desenvolvimento Tecnológico de Biológicos no Brasil?
Avaliação Econômica de Tecnologias em Saúde
 Palestra 3: Avaliação Econômica de Tecnologias em Saúde Everton Nunes da Silva everton@ppge.ufrgs.br Maio/2008 CONTEXTO MUNDIAL: GASTO EM SAÚDE Total Health Expenditure % of GDP Public Expenditure % of
Palestra 3: Avaliação Econômica de Tecnologias em Saúde Everton Nunes da Silva everton@ppge.ufrgs.br Maio/2008 CONTEXTO MUNDIAL: GASTO EM SAÚDE Total Health Expenditure % of GDP Public Expenditure % of
JUDICIALIZAÇÃO DA SAÚDE NO ESTADO DE SÃO PAULO
 AVALIAÇÃO DE ATS PARA TOMADA DE DECISÃO NO SUS JUDICIALIZAÇÃO DA SAÚDE NO ESTADO DE SÃO PAULO PAULA SUE FACUNDO DE SIQUEIRA INSTITUTO DE SAÚDE Junho - 2016 RELATÓRIO DE DEMANDAS CADASTRADAS AÇÕES JUDICIAIS
AVALIAÇÃO DE ATS PARA TOMADA DE DECISÃO NO SUS JUDICIALIZAÇÃO DA SAÚDE NO ESTADO DE SÃO PAULO PAULA SUE FACUNDO DE SIQUEIRA INSTITUTO DE SAÚDE Junho - 2016 RELATÓRIO DE DEMANDAS CADASTRADAS AÇÕES JUDICIAIS
Ministério da Saúde Consultoria Jurídica/Advocacia Geral da União
 Nota Técnica N 265/2013 Brasília, agosto de 2013. Princípio Ativo: cabergolina Nome Comercial 1 : Dostinex. Sumário 1. O que é a cabergolina?... 1 2. O medicamento possui registro na Agência Nacional de
Nota Técnica N 265/2013 Brasília, agosto de 2013. Princípio Ativo: cabergolina Nome Comercial 1 : Dostinex. Sumário 1. O que é a cabergolina?... 1 2. O medicamento possui registro na Agência Nacional de
SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS RELATÓRIO PARA A
 número 15 - dezembro/2015 DECISÃO FINAL RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS RELATÓRIO PARA A SOCIEDADE Este relatório
número 15 - dezembro/2015 DECISÃO FINAL RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS RELATÓRIO PARA A SOCIEDADE Este relatório
HOSPITAL UNIMED NOROESTE RS SERVIÇO DE QUIMIOTERAPIA
 HOSPITAL UNIMED NOROESTE RS SERVIÇO DE QUIMIOTERAPIA Serviço de Quimioterapia inaugurado em agosto de 2005 FATORES QUE LEVARAM A ABERTURA DO SERVIÇO Custo elevado dos medicamentos quimioterápicos; Aumento
HOSPITAL UNIMED NOROESTE RS SERVIÇO DE QUIMIOTERAPIA Serviço de Quimioterapia inaugurado em agosto de 2005 FATORES QUE LEVARAM A ABERTURA DO SERVIÇO Custo elevado dos medicamentos quimioterápicos; Aumento
FÓRUM NACIONAL DE JUDICIALIZAÇÃO EM SAÚDE SOMAERGS AMRIGS PORTO ALEGRE 05 e 06 de outubro de 2017
 FÓRUM NACIONAL DE JUDICIALIZAÇÃO EM SAÚDE SOMAERGS AMRIGS PORTO ALEGRE 05 e 06 de outubro de 2017 MARTIN SCHULZE DESEMBARGADOR, ATUA NA 23ª CÂMARA CÍVEL DO TRIBUNAL DE JUSTIÇA DO RS, COORDENADOR DO COMITÊ
FÓRUM NACIONAL DE JUDICIALIZAÇÃO EM SAÚDE SOMAERGS AMRIGS PORTO ALEGRE 05 e 06 de outubro de 2017 MARTIN SCHULZE DESEMBARGADOR, ATUA NA 23ª CÂMARA CÍVEL DO TRIBUNAL DE JUSTIÇA DO RS, COORDENADOR DO COMITÊ
Programa de Hepatites Virais do Ministério da Saúde
 Programa de Hepatites Virais do Ministério da Saúde Ministério da Saúde Secretaria de Vigilância em Saúde Departamento de Vigilância, Prevenção e Controle das Infecções Sexualmente Transmissíveis, do HIV/Aids
Programa de Hepatites Virais do Ministério da Saúde Ministério da Saúde Secretaria de Vigilância em Saúde Departamento de Vigilância, Prevenção e Controle das Infecções Sexualmente Transmissíveis, do HIV/Aids
O trabalho médico em cooperativa
 O trabalho médico em cooperativa Sistema Unimed 38 Prestadoras 293 Operadoras 17 Federações Institucionais 348 Cooperativas 1 Confederação Nacional 1 Confederação Regional 1 Central Nacional 33 Federações
O trabalho médico em cooperativa Sistema Unimed 38 Prestadoras 293 Operadoras 17 Federações Institucionais 348 Cooperativas 1 Confederação Nacional 1 Confederação Regional 1 Central Nacional 33 Federações
Seminário EEUSP - 05 de maio de Experiências da tradução do conhecimento: visão do Brasil a partir do Instituto de Saúde
 Seminário EEUSP - 05 de maio de 2017 Experiências da tradução do conhecimento: visão do Brasil a partir do Instituto de Saúde Instituto de Saúde Instituto de ensino e pesquisa da Secretaria de Estado da
Seminário EEUSP - 05 de maio de 2017 Experiências da tradução do conhecimento: visão do Brasil a partir do Instituto de Saúde Instituto de Saúde Instituto de ensino e pesquisa da Secretaria de Estado da
n. 63 publicado em setembro/2017
 n. 63 publicado em setembro/2017 RELATÓRIO PARA SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS SECUQUINUMABE PARA O TRATAMENTO DE ARTRITE PSORIÁSICA
n. 63 publicado em setembro/2017 RELATÓRIO PARA SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS SECUQUINUMABE PARA O TRATAMENTO DE ARTRITE PSORIÁSICA
Panorama das Redes de Atenção à Saúde.
 Panorama das Redes de Atenção à Saúde. Saúde Direito de todos e dever do Estado CONSTITUIÇÃO FEDERAL Lei 8.080 Lei 8.142 DECRETO 7.508 Lei 12.401 Lei 12.466 Lei complementar 141 1986 1988 1990 1991 1993
Panorama das Redes de Atenção à Saúde. Saúde Direito de todos e dever do Estado CONSTITUIÇÃO FEDERAL Lei 8.080 Lei 8.142 DECRETO 7.508 Lei 12.401 Lei 12.466 Lei complementar 141 1986 1988 1990 1991 1993
Dra Karen Sarmento Costa. Coordenadora Geral de Assistência Farmacêutica Básica/DAF/SCTIE/MS
 Dra Karen Sarmento Costa Coordenadora Geral de Assistência Farmacêutica Básica/DAF/SCTIE/MS Belo Horizonte, 11 de novembro de 2014 O Brasil é o único país com mais de 100 milhões de habitantes que assumiu
Dra Karen Sarmento Costa Coordenadora Geral de Assistência Farmacêutica Básica/DAF/SCTIE/MS Belo Horizonte, 11 de novembro de 2014 O Brasil é o único país com mais de 100 milhões de habitantes que assumiu
Qualificação da Gestão
 Qualificação da Gestão O que é o SUS Instituído pela Constituição de 1988, o Sistema Único de Saúde SUS é formado pelo conjunto das ações e serviços de saúde sob gestão pública Com direção única em cada
Qualificação da Gestão O que é o SUS Instituído pela Constituição de 1988, o Sistema Único de Saúde SUS é formado pelo conjunto das ações e serviços de saúde sob gestão pública Com direção única em cada
Região de abrangência do HC FMRP USP HOSPITAL DAS CLÍNICAS DE RIBEIRÃO AVALIAÇÃO DOS FORNECEDORES NO. PRETO - Parceria lado a lado
 AVALIAÇÃO DOS FORNECEDORES NO HOSPITAL DAS CLÍNICAS DE RIBEIRÃO PRETO - Parceria lado a lado Edna Aparecida Garcia Tonioli Defendi Departamento de Apoio Administrativo Região de abrangência do HC FMRP
AVALIAÇÃO DOS FORNECEDORES NO HOSPITAL DAS CLÍNICAS DE RIBEIRÃO PRETO - Parceria lado a lado Edna Aparecida Garcia Tonioli Defendi Departamento de Apoio Administrativo Região de abrangência do HC FMRP
Resolução nº 198/2014 do Conselho Nacional de Justiça
 126 126 = Legislação Tribunal de Justiça / Rio de Janeiro Resolução nº 198/2014 do Conselho Nacional de Justiça Dispõe sobre o Planejamento e a Gestão Estratégica no âmbito do Poder Judiciário e dá outras
126 126 = Legislação Tribunal de Justiça / Rio de Janeiro Resolução nº 198/2014 do Conselho Nacional de Justiça Dispõe sobre o Planejamento e a Gestão Estratégica no âmbito do Poder Judiciário e dá outras
Fiocruz Informação em Ciência, Tecnologia e Inovação na área da Saúde
 Fiocruz Informação em Ciência, Tecnologia e Inovação na área da Saúde Ana Maranhão Coordenadora do Arca Repositório Institucional Instituto de Comunicação e Informação Científica e Tecnológica em Saúde
Fiocruz Informação em Ciência, Tecnologia e Inovação na área da Saúde Ana Maranhão Coordenadora do Arca Repositório Institucional Instituto de Comunicação e Informação Científica e Tecnológica em Saúde
Dispõe sobre processo de atualização periódica do Rol de Procedimentos e Eventos em Saúde, no âmbito da Agência Nacional de Saúde Suplementar.
 CONTEÚDO CAPÍTULO I - DISPOSIÇÕES GERAIS CAPÍTULO II - DO INICIO DO CICLO DE ATUALIZAÇÃO CAPÍTULO III - DA ANÁLISE E DA PARTICIPAÇÃO SOCIAL CAPÍTULO IV - DISPOSIÇÕES FINAIS RESOLUÇÃO NORMATIVA - RN Nº
CONTEÚDO CAPÍTULO I - DISPOSIÇÕES GERAIS CAPÍTULO II - DO INICIO DO CICLO DE ATUALIZAÇÃO CAPÍTULO III - DA ANÁLISE E DA PARTICIPAÇÃO SOCIAL CAPÍTULO IV - DISPOSIÇÕES FINAIS RESOLUÇÃO NORMATIVA - RN Nº
A integração dos Núcleos de Segurança do Paciente com os Setores e Comissões Hospitalares. Antonio da Silva Bastos Neto
 A integração dos Núcleos de Segurança do Paciente com os Setores e Comissões Hospitalares Antonio da Silva Bastos Neto Nossa História Missão, Visão e Valores Estrutura Organizacional Programa de Qualidade
A integração dos Núcleos de Segurança do Paciente com os Setores e Comissões Hospitalares Antonio da Silva Bastos Neto Nossa História Missão, Visão e Valores Estrutura Organizacional Programa de Qualidade
Limiar de custo-efetividade para novas tecnologias: reflexões do GRUDA-RJ. Marisa Santos, médica, esp ATS Coordenadora NATS-INC MS Junho 2018
 Limiar de custo-efetividade para novas tecnologias: reflexões do GRUDA-RJ Marisa Santos, médica, esp ATS Coordenadora NATS-INC MS Junho 2018 1 Tópicos O que é limiar de custo-efetividade Processo de incorporação
Limiar de custo-efetividade para novas tecnologias: reflexões do GRUDA-RJ Marisa Santos, médica, esp ATS Coordenadora NATS-INC MS Junho 2018 1 Tópicos O que é limiar de custo-efetividade Processo de incorporação
DELIBERAÇÃO CIB-SUS/MG Nº 2.512, DE 19 DE JULHO DE 2017.
 DELIBERAÇÃO CIB-SUS/MG Nº 2.512, DE 19 DE JULHO DE 2017. Aprova o Protocolo Estadual para Dispensação de Insumos para Monitoramento de Diabetes no âmbito do SUS-MG. A Comissão Intergestores Bipartite do
DELIBERAÇÃO CIB-SUS/MG Nº 2.512, DE 19 DE JULHO DE 2017. Aprova o Protocolo Estadual para Dispensação de Insumos para Monitoramento de Diabetes no âmbito do SUS-MG. A Comissão Intergestores Bipartite do
número 23- maio/2016 RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS
 número 23- maio/2016 RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS TOCILIZUMABE PARA O TRATAMENTO DA ARTRITE REUMATOIDE RELATÓRIO
número 23- maio/2016 RELATÓRIO PARA A SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS TOCILIZUMABE PARA O TRATAMENTO DA ARTRITE REUMATOIDE RELATÓRIO
MINISTÉRIO DA SAÚDE. O MINISTRO DE ESTADO DA SAÚDE, no uso de suas atribuições legais, e
 MINISTÉRIO DA SAÚDE PORTARIA nº 2.583 de 10 de outubro de 2007 Define elenco de medicamentos e insumos disponibilizados pelo Sistema Único de Saúde, nos termos da Lei nº 11.347/2006, aos usuários portadores
MINISTÉRIO DA SAÚDE PORTARIA nº 2.583 de 10 de outubro de 2007 Define elenco de medicamentos e insumos disponibilizados pelo Sistema Único de Saúde, nos termos da Lei nº 11.347/2006, aos usuários portadores
