Termodinâmica II - FMT 259
|
|
|
- Marco Bayer
- 7 Há anos
- Visualizações:
Transcrição
1 Termodinâmica II - FMT 59 Diurno e Noturno, primeiro semestre de 1 Gabarito da lista 6 1. Considere um gás hipotético para o qual a função de distribuição de velocidades tivesse a forma indicada na gura abaixo. Calcule, em função de : (a) A constante de normalização C (ver gura). (b) Os valores de < v >, v p e v qm. Observe que o gráco acima pode ser representado pela função C v para < v <, C v + C para < v <. Assim, usando a condição de normalização da distribuição n(v), teremos que n(v)dv = C = 1 C = 1 Vamos reescrever n(v) substituindo o valor de C 1 v para < v < v v, (v ) para < v <. 1 v Agora podemos obter as velocidades características, item (b) do problema, < v >= v v v v v dv + v dv = = v ( ) v 3 + v3 3v = < v >=. Obtemos v qm através do cálculo de < v > tal que v < v >= v v 3 v v v dv + v3 v dv = ( ) = v v v4 ( 1 3 4v = v ) = 7v 6, 1
2 sendo assim v qm = 7 6. Finalmente, podemos observar no gráco que o valor mais provável é v p =.. Calcule a velocidade quadrática média, no ar, de partículas de fumaça, cuja massa é de 5, 1 14 g, a o C e à pressão de 1 atmosfera. Assumindo que distribuição de velocidades das partículas seque uma distribuição de Maxwell então, v qm = 3 m substituindo os valores dados de temperatura e massa temos v qm 1, 5 cm/s 3. (a) Calcule a distribuição de energia n(e), tal que n(e) de é a fração de moléculas com energia entre E e E + de, para um gás ideal em equilí brio térmico à temperatura T. Adimitindo que a fração de moléculas com energia entre E e E + de é igual a fração de moléculas com velocidade entre v e v + dv. Então n E (E)dE = n v (v)dv. As partículas que compõem o gás ideal possuem apenas energia cinética de translação, portanto, E = mv de = mvdv, logo Sabemos que n E (E)mv = n v (v). ( m ) 3/ n v (v) = 4π v e mv. π Portanto, simplicando os termos teremos n E (E) = 4π m ( m ) ( ) 3/ E 1/ e E, π m E n E (E) = πk 3 T 3 e E. (b) A partir da distribuição calculada no item (a), calcule a energia média < E >, comparando o resultado com 1 m v qm. Partindo da denição de média temos < E >= E n E (E) de, < E >= E 3 πk 3 T 3 e E de.
3 Fazendo a mudança de variável E/ = x, dx = < E >= de E logo 4 π x 4 e x dx < E >= 3 = mv qm (c) Calcule a energia mais provável E p, comparando o resultado com 1 m v p. Para obter o valor de E que maximiza a distribuição n E (E) faremos obtendo n E(E p ) = 1 E p =, E p = = 1 ( mv p ). 4. Ao nível do mar, a composição volumétrica da atmosfera é 1% de oxigênio e 78% de nitrogênio (há 1% de outros gases, principalmente argônio). Suponha (embora não seja uma boa aproximação!) que a temperatura do ar não variasse com a altitude, e que seu valor fosse 1 o C. Nesse caso, qual seria a composição volumétrica da atmosfera a 1 km de altitude? (considere 1 unidade de massa atômica = 1, kg). Ao nível do mar, o número total de moléculas na atmosfera é n(). Além disso, n O () é o número de moleculas de oxigênio, n N () é o número de moleculas de nitrogênio, n Ar () é o número de moleculas de Argônio. Sabendo disso, é válida a relação n() = n O () + n N () + n Ar (), ou seja, Do enunciado sabemos que n O () n() 1 = n O () n() =.1, n N () n() + n N () n() + n Ar() n(). =.78 e n Ar() n() =.1. No entanto, o número total de moléculas na atmosfera a 1 km de altitude n(z = 1 km) é certamente menor do que na superfície da terra, isto é n(z = 1 km) < n(z = ). Para z = 1 km é válida a relação Pela lei de Halley, a expressão acima pode ser reescrita como = n O () exp m O gz = n O (z) + n N (z) + n Ar (z). (1) + n N () exp m N gz + n Ar () exp m Argz Observe que m O = 3 u, m N = 8 u e m Ar = 18 u (onde 1 u=1 unidade de massa atômica = 1, kg), substituindo esses valores na expressão acima e dividindo ambos os membros por n() teremos n() = n O () n() 3 ugz + n N () n() 3 8 ugz + n Ar() n(). 18 ugz,
4 chamando λ = exp ugz/ e usando os dados do enunciado teremos que λ = ugz, 9595 (obs.: Vamos aproximar os valores apenas no nal das contas!) então e obtemos que n() = n O () n() λ3, n N () n() λ8, n Ar() n() λ18,, = r =, , corroborando a hipotese de que n(z = 1 km) < n(z = ). n() Finalmente, podemos calcular a composição volumétrica da atmosfera em z = 1 km de altitude para cada tipo de molécula constituinte da atmosfera: n O (z) n N (z) n Ar (z) n O () n() λ3 =, , 3%, n N () n() λ8 =, 8 8, %, n Ar () n() λ18 =, 15 1, 5%. 5. Suponha um gás ideal em um mundo imaginário bidimensional. (a) Modique, onde necessário, os argumentos empregados na dedução da distribuição de Maxwell- Boltzmann, obtendo a distribuição de velocidades n(v) para esse gás ideal bidimensional. A forma geral da distribuição de Maxwell-Boltzmann é n(v x,y ) = Ae mv x,y. Como v x e v y são independentes, a distribuição conjunta é o produto das duas: n(v x, v y ) = A e m(v x +v y ). Fazendo a mudança de coordenadas para o sistema polar obtemos n(v x, v y )dv x dv y = n(v, θ v ) vdvdθ v, onde o jacobiano da transformação é v, logo n(v, θ v ) = n(v x, v y )v. Assim, a distribuição em coordenadas polares é n(v, θ v ) = A ve mv. Integrando em θ v obtemos a distribuição marginal, apenas para v, π A ve mv dθv = πa ve mv = Bve mv Para obter a constante B usamos o critério de normalização. O Calculo dessa integral pode ser feita por partes e é mais simples do que a que aparece no caso tridimensional, 4
5 n(v)dv = B ve mv dv = B m = 1. Logo mv mv e. (b) Determine a velocidade mais provável, a velocidade média e a velocidade quadrática média. Chamando λ = m, então λ v e λv. Recordando a integral para normalizar a distribuição de Maxwell (3 dimensões) teremos < v >= λ < v >= λ v e λv dv = 1 π λ = π m, v 3 e λv dv = 1 λ = m v qm = m, n (v) = 1 λv = v = 1 λ = m v p = m. 5
Termodinâmica II - FMT 259
 Termodinâmica II - FMT 259 Diurno e Noturno, primeiro semestre de 2009 Lista 3 GABARITO (revisado em 22/04/0). Se as moléculas contidas em,0 g de água fossem distribuídas uniformemente sobre a superfície
Termodinâmica II - FMT 259 Diurno e Noturno, primeiro semestre de 2009 Lista 3 GABARITO (revisado em 22/04/0). Se as moléculas contidas em,0 g de água fossem distribuídas uniformemente sobre a superfície
AULA 8 Teoria Cinética dos Gases II
 UFABC - BC0205 Prof. Germán Lugones AULA 8 Teoria Cinética dos Gases II James Clerk Maxwell 1831-1879 A Distribuição de Velocidades Moleculares A velocidade média quadrática V rms nos fornece uma ideia
UFABC - BC0205 Prof. Germán Lugones AULA 8 Teoria Cinética dos Gases II James Clerk Maxwell 1831-1879 A Distribuição de Velocidades Moleculares A velocidade média quadrática V rms nos fornece uma ideia
Formalismo microcanônico ( ensemble microcanônico) Formalismo canônico ( ensemble canônico)
 Formalismo microcanônico ( ensemble microcanônico) sist(j) estado j f j = Ω j Ω Formalismo canônico ( ensemble canônico) reservatório de temperatura tot res sistema f j = Ω res+sist(j) Ω tot sist(j) Física
Formalismo microcanônico ( ensemble microcanônico) sist(j) estado j f j = Ω j Ω Formalismo canônico ( ensemble canônico) reservatório de temperatura tot res sistema f j = Ω res+sist(j) Ω tot sist(j) Física
Teoria Cinética dos Gases
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II Teoria Cinética dos Gases Prof. Bruno Farias Introdução Termodinâmica é o estudo das transformações
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II Teoria Cinética dos Gases Prof. Bruno Farias Introdução Termodinâmica é o estudo das transformações
A teoria Cinética dos Gases
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II A teoria Cinética dos Gases Prof. Bruno Farias Gases Um gás é formado de átomos (isolados
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II A teoria Cinética dos Gases Prof. Bruno Farias Gases Um gás é formado de átomos (isolados
Termodinâmica II - FMT 259
 Termodinâmica II - FMT 259 Diurno e Noturno, primeiro semestre de 2009 Lista 2 (Entregar até dia 19 de março) Leia o capítulos 1.2 e 1.3 do livro-texto e resolva os exercícios abaixo: 1. Que hipóteses
Termodinâmica II - FMT 259 Diurno e Noturno, primeiro semestre de 2009 Lista 2 (Entregar até dia 19 de março) Leia o capítulos 1.2 e 1.3 do livro-texto e resolva os exercícios abaixo: 1. Que hipóteses
19.2 Número de Avogadro mol número de átomos em uma amostra de 12g do carbono-12. Num mol de qualquer substância existem
 Cap. 19 Um gás consiste em átomos que preenchem o volume de seu recipiente. As variáveis volume, pressão e temperatura, são conseqüências do movimento dos átomos. Volume resultado da liberdade dos átomos;
Cap. 19 Um gás consiste em átomos que preenchem o volume de seu recipiente. As variáveis volume, pressão e temperatura, são conseqüências do movimento dos átomos. Volume resultado da liberdade dos átomos;
FIS-14 Mecânica I. Ronaldo Rodrigues Pela
 FIS-14 Mecânica I Ronaldo Rodrigues Pela Objetivos Visão geral: Termodinâmica e Mecânica Velocidade rms Equipartição da Energia e calor específico Origem microscópica da distribuição de Maxwell-Boltzmann
FIS-14 Mecânica I Ronaldo Rodrigues Pela Objetivos Visão geral: Termodinâmica e Mecânica Velocidade rms Equipartição da Energia e calor específico Origem microscópica da distribuição de Maxwell-Boltzmann
Lista de Exercícios 9 Teoria cinética dos gases, Primeira e Segunda leis da Termodinâmica
 Lista de Exercícios 9 Teoria cinética dos gases, Primeira e Segunda leis da Termodinâmica Exercícios Sugeridos (14 de novembro de 2008) A numeração corresponde ao Livro Texto. 16.19 Um balão de ar quente
Lista de Exercícios 9 Teoria cinética dos gases, Primeira e Segunda leis da Termodinâmica Exercícios Sugeridos (14 de novembro de 2008) A numeração corresponde ao Livro Texto. 16.19 Um balão de ar quente
Física Geral II. Aula 1 - Teoria cinética dos gases. D. Valin 1. Universidade do Estado de Mato Grosso. Sinop-MT, April 25, 2017
 Física Geral II Aula 1 - Teoria cinética dos gases D. Valin 1 1 Faculdade de Ciências Exatas - FACET Universidade do Estado de Mato Grosso Sinop-MT, April 25, 2017 D. Valin (Universidade do Estado de Mato
Física Geral II Aula 1 - Teoria cinética dos gases D. Valin 1 1 Faculdade de Ciências Exatas - FACET Universidade do Estado de Mato Grosso Sinop-MT, April 25, 2017 D. Valin (Universidade do Estado de Mato
03/Mar/2017 Aula 3. 01/Mar/2017 Aula 2
 01/Mar/2017 Aula 2 Teoria Cinética dos Gases Teoria Cinética e Equação dos Gases Ideais Gás Ideal num Campo Gravitacional Distribuição de Boltzmann; distribuição de velocidades de Maxwell e Boltzmann Velocidades
01/Mar/2017 Aula 2 Teoria Cinética dos Gases Teoria Cinética e Equação dos Gases Ideais Gás Ideal num Campo Gravitacional Distribuição de Boltzmann; distribuição de velocidades de Maxwell e Boltzmann Velocidades
25/Fev/2015 Aula 2. 20/Fev/2015 Aula 1
 /Fe/15 Aula 1 Temperatura e a Lei Zero da Termodinâmica Sistema Termodinâmico Termómetros e Escalas de Temperatura Descrição macroscópica dos gases ideais Equação dos gases ideais 5/Fe/15 Aula Teoria Cinética
/Fe/15 Aula 1 Temperatura e a Lei Zero da Termodinâmica Sistema Termodinâmico Termómetros e Escalas de Temperatura Descrição macroscópica dos gases ideais Equação dos gases ideais 5/Fe/15 Aula Teoria Cinética
Universidade Federal do Pampa UNIPAMPA. Teoria Cinética do Gases
 Universidade Federal do Pampa UNIPAMPA Teoria Cinética do Gases Introdução A descrição de um gás por inteiro (descrição macroscópica) pode ser feito estabelecendo as grandezas macroscópicas que caracterizam
Universidade Federal do Pampa UNIPAMPA Teoria Cinética do Gases Introdução A descrição de um gás por inteiro (descrição macroscópica) pode ser feito estabelecendo as grandezas macroscópicas que caracterizam
Problemas Capítulo 4: Solução e Dicas
 Problemas Capítulo 4: Solução e Dicas José Fernando de Jesus & Rodrigo Fernandes Lira de Holanda 6 de junho de 2007 4. - Se estamos nos movimentando na direção do grande atrator, podemos dizer que nossa
Problemas Capítulo 4: Solução e Dicas José Fernando de Jesus & Rodrigo Fernandes Lira de Holanda 6 de junho de 2007 4. - Se estamos nos movimentando na direção do grande atrator, podemos dizer que nossa
Problemas de Física Estatística e Termodinâmica
 1 Problemas de Física Estatística e Termodinâmica Todas as grandezas físicas se supõem expressas no Sistema Internacional de Unidades. 1. Uma variável aleatória y pode tomar valores no conjunto {1,2,3,4,5}
1 Problemas de Física Estatística e Termodinâmica Todas as grandezas físicas se supõem expressas no Sistema Internacional de Unidades. 1. Uma variável aleatória y pode tomar valores no conjunto {1,2,3,4,5}
Mecânica I (FIS-14) Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785
 Mecânica I (FIS-14) Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 [email protected] www.ief.ita.br/~rrpela Mecânica Mecânica: estuda o estado de movimento (ou repouso) de corpos sujeitos à ação
Mecânica I (FIS-14) Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 [email protected] www.ief.ita.br/~rrpela Mecânica Mecânica: estuda o estado de movimento (ou repouso) de corpos sujeitos à ação
Exercícios de Mínimos Quadrados
 INSTITUTO DE CIÊNCIAS MATEMÁTICAS E DE COMPUTAÇÃO DEPARTAMENTO DE MATEMÁTICA APLICADA E ESTATÍSTICA Exercícios de Mínimos Quadrados 1 Provar que a matriz de mínimos quadrados é denida positiva, isto é,
INSTITUTO DE CIÊNCIAS MATEMÁTICAS E DE COMPUTAÇÃO DEPARTAMENTO DE MATEMÁTICA APLICADA E ESTATÍSTICA Exercícios de Mínimos Quadrados 1 Provar que a matriz de mínimos quadrados é denida positiva, isto é,
Resposta: (A) o traço é positivo (B) o determinante é negativo (C) o determinante é nulo (D) o traço é negativo (E) o traço é nulo.
 MESTRADO INTEGRADO EM ENG. INFORMÁTICA E COMPUTAÇÃO 201/2018 EIC0010 FÍSICA I 1º ANO, 2º SEMESTRE 12 de junho de 2018 Nome: Duração 2 horas. Prova com consulta de formulário e uso de computador. O formulário
MESTRADO INTEGRADO EM ENG. INFORMÁTICA E COMPUTAÇÃO 201/2018 EIC0010 FÍSICA I 1º ANO, 2º SEMESTRE 12 de junho de 2018 Nome: Duração 2 horas. Prova com consulta de formulário e uso de computador. O formulário
Física Moderna I Aula 03. Marcelo G Munhoz Pelletron, sala 245, ramal 6940
 Física Moderna I Aula 03 Marcelo G Munhoz Pelletron, sala 245, ramal 6940 [email protected] 1 Radiação Térmica Ondas eletromagnéticas emitidas por todos os objetos com temperatura acima do zero absoluto
Física Moderna I Aula 03 Marcelo G Munhoz Pelletron, sala 245, ramal 6940 [email protected] 1 Radiação Térmica Ondas eletromagnéticas emitidas por todos os objetos com temperatura acima do zero absoluto
Mecânica Estatística - Exercícios do EUF Professor: Gabriel T. Landi
 Mecânica Estatística - Exercícios do EUF Professor: Gabriel T. Landi (2016-2) Sólido cristalino Num modelo para um sólido cristalino podemos supor que os N átomos sejam equivalentes a 3N osciladores harmônicos
Mecânica Estatística - Exercícios do EUF Professor: Gabriel T. Landi (2016-2) Sólido cristalino Num modelo para um sólido cristalino podemos supor que os N átomos sejam equivalentes a 3N osciladores harmônicos
Gases reais. ρ(γ) = ρ(q 1,q 2,...,q 3N,p 1,p 2,...,p 3N ) (1)
 Capítulo 7 Gases reais 1 Distribuição canônica Diferentemente do que foi feito nos capítulos anteriores vamos considerar agora sistemas de partículas interagentes. Por exemplo, um gás composto de N moléculas
Capítulo 7 Gases reais 1 Distribuição canônica Diferentemente do que foi feito nos capítulos anteriores vamos considerar agora sistemas de partículas interagentes. Por exemplo, um gás composto de N moléculas
2 bt2 20 o C. O calor trocado pelo sistema é, fazendo a = 5,4 cal/g.k, b = 0,0024 cal/g.k 2, c = 0, cal.k/g, dt, T 2. = 230,2kcal.
 FÍSICA BÁSICA II - LISTA 3 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância
FÍSICA BÁSICA II - LISTA 3 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância
2 bt2 20 o C. O calor trocado pelo sistema é, fazendo a = 5,4 cal/g.k, b = 0,0024 cal/g.k 2, c = 0, cal.k/g, dt, T 2. = 230,2kcal.
 FÍSICA - LISTA 4 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância se a temperatura
FÍSICA - LISTA 4 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância se a temperatura
UFABC - BC Prof. Germán Lugones. AULA 7 Teoria Cinética dos Gases I
 UFABC - BC0205 - Prof. Germán Lugones AULA 7 Teoria Cinética dos Gases I Teoria cinética dos gases o Um gás consiste em partículas (e.g. átomos ou moléculas) que preenchem o volume de seu recipiente e
UFABC - BC0205 - Prof. Germán Lugones AULA 7 Teoria Cinética dos Gases I Teoria cinética dos gases o Um gás consiste em partículas (e.g. átomos ou moléculas) que preenchem o volume de seu recipiente e
Instituto de Física USP. Física Moderna I. Aula 4. Professora: Mazé Bechara
 Instituto de Física USP Física Moderna I Aula 4 Professora: Mazé Bechara Aula 04 Modelos de estrutura da matéria e a mecânica estatística clássica 1. Uma teoria para a dinâmica de um sistema de muitas
Instituto de Física USP Física Moderna I Aula 4 Professora: Mazé Bechara Aula 04 Modelos de estrutura da matéria e a mecânica estatística clássica 1. Uma teoria para a dinâmica de um sistema de muitas
Capítulo 4 Condução Bidimensional em Regime Estacionário. Prof. Dr. Santiago del Rio Oliveira
 Capítulo 4 Condução Bidimensional em Regime Estacionário Prof. Dr. Santiago del Rio Oliveira 4. Considerações Gerais A distribuição de temperaturas é caracterizada por duas coordenadas espaciais, ou seja:
Capítulo 4 Condução Bidimensional em Regime Estacionário Prof. Dr. Santiago del Rio Oliveira 4. Considerações Gerais A distribuição de temperaturas é caracterizada por duas coordenadas espaciais, ou seja:
FIS-26 Resolução Lista-11 Lucas Galembeck
 FIS-6 Resolução Lista-11 Lucas Galembeck 1. Dentro de uma esfera de raio R e de densidade ρ existe uma cavidade esférica de raio a a < R. A distncia entre os centros O e O da esfera e da cavidade é d,
FIS-6 Resolução Lista-11 Lucas Galembeck 1. Dentro de uma esfera de raio R e de densidade ρ existe uma cavidade esférica de raio a a < R. A distncia entre os centros O e O da esfera e da cavidade é d,
Universidade Federal de Mato Grosso do Sul - UFMS VGA - 2 a Prova - Engenharia Civil + Física 03 de Julho de Prof o. E.T.
 Universidade Federal de Mato Grosso do Sul - UFMS VGA - 2 a Prova - Engenharia Civil + Física 0 de Julho de 2014 - Prof o ETGalante 1 (2,0 pontos) Na gura acima ABCDEF GH é um paralelepípedo O ponto M
Universidade Federal de Mato Grosso do Sul - UFMS VGA - 2 a Prova - Engenharia Civil + Física 0 de Julho de 2014 - Prof o ETGalante 1 (2,0 pontos) Na gura acima ABCDEF GH é um paralelepípedo O ponto M
Dedução da termodinâmica no conjunto microcanónico MEFT, IST. Areyoureallysurethatafloorcan talsobeaceiling? M. C. Escher
 Física estatística Dedução da termodinâmica no conjunto microcanónico MEFT, IST Areyoureallysurethatafloorcan talsobeaceiling? M. C. Escher Dedução da termodinâmica Definimos a entropia no conjunto microcanónico
Física estatística Dedução da termodinâmica no conjunto microcanónico MEFT, IST Areyoureallysurethatafloorcan talsobeaceiling? M. C. Escher Dedução da termodinâmica Definimos a entropia no conjunto microcanónico
Universidade Estadual do Sudoeste da Bahia
 Universidade Estadual do Sudoeste da Bahia Departamento de Estudos Básicos e Instrumentais 4 Termodinâmica Física II Ferreira 1 ÍNDICE 1. Conceitos Fundamentais; 2. Sistemas Termodinâmicos; 3. Leis da
Universidade Estadual do Sudoeste da Bahia Departamento de Estudos Básicos e Instrumentais 4 Termodinâmica Física II Ferreira 1 ÍNDICE 1. Conceitos Fundamentais; 2. Sistemas Termodinâmicos; 3. Leis da
Física II FEP 112 ( ) 1º Semestre de Instituto de Física - Universidade de São Paulo. Professor: Valdir Guimarães
 Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: [email protected] Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: [email protected] Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
MAP CÁLCULO NUMÉRICO (POLI) Lista de Exercícios sobre Interpolação e Integração. φ(x k ) ψ(x k ).
 MAP 22 - CÁLCULO NUMÉRICO (POLI) Lista de Exercícios sobre Interpolação e Integração : Sejam x =, x =, x 2 = 2 e x 3 = 3. (a) Determine os polinômios de Lagrange L i (x) correspondentes a estes pontos
MAP 22 - CÁLCULO NUMÉRICO (POLI) Lista de Exercícios sobre Interpolação e Integração : Sejam x =, x =, x 2 = 2 e x 3 = 3. (a) Determine os polinômios de Lagrange L i (x) correspondentes a estes pontos
INTEGRAIS IMPRÓPRIAS
 Teoria INTEGRAIS IMPRÓPRIAS Intervalos Infinitos: Seja f integrável em [a, t], para todo t > a. Definimos + a f(x)dx = lim t + t a f(x)dx. Tal limite denomina-se integral imprópria de f estendida ao intervalo
Teoria INTEGRAIS IMPRÓPRIAS Intervalos Infinitos: Seja f integrável em [a, t], para todo t > a. Definimos + a f(x)dx = lim t + t a f(x)dx. Tal limite denomina-se integral imprópria de f estendida ao intervalo
Física Moderna I Período: noturno
 UNIVERSIDADE DE SÃO PAULO INSTITUTO DE FÍSICA Física Moderna I - 4300375 Período: noturno 1o Semestre de 01 --------------------------------------------------------------------------------------- Guia
UNIVERSIDADE DE SÃO PAULO INSTITUTO DE FÍSICA Física Moderna I - 4300375 Período: noturno 1o Semestre de 01 --------------------------------------------------------------------------------------- Guia
Universidade Tecnológica Federal do Paraná. APS Cálculo 2
 Ministério da Educação Universidade Tecnológica Federal do Paraná Campus Campo Mourão Wellington José Corrêa Nome: APS Cálculo 2 1. As dimensões de uma caixa retangular fechada foram medidas com 80 cm,
Ministério da Educação Universidade Tecnológica Federal do Paraná Campus Campo Mourão Wellington José Corrêa Nome: APS Cálculo 2 1. As dimensões de uma caixa retangular fechada foram medidas com 80 cm,
A natureza corpuscular da matéria
 A natureza corpuscular da matéria Vimos as evidências da natureza corpuscular da radiação: quantização dos osciladores Planck quantização da luz Einstein fótons como partículas Compton Evidências da natureza
A natureza corpuscular da matéria Vimos as evidências da natureza corpuscular da radiação: quantização dos osciladores Planck quantização da luz Einstein fótons como partículas Compton Evidências da natureza
UFABC - BC Prof. Germán Lugones. AULA 9 Teoria Cinética dos Gases III
 UFABC - BC0205 - Prof. Germán Lugones AULA 9 Teoria Cinética dos Gases III Graus de liberdade e Calores Específicos Molares A previsão de que c v = 3/2 R concorda com o experimento para gases monoatômicos,
UFABC - BC0205 - Prof. Germán Lugones AULA 9 Teoria Cinética dos Gases III Graus de liberdade e Calores Específicos Molares A previsão de que c v = 3/2 R concorda com o experimento para gases monoatômicos,
Energia cinética de rotação:
 2 comenta a) Energia cinética de translação: Energia cinética de rotação: Todos os pontos que constituem o aro têm a mesma velocidade tangencial em relação ao seu centro. Por isso, sua energia cinética
2 comenta a) Energia cinética de translação: Energia cinética de rotação: Todos os pontos que constituem o aro têm a mesma velocidade tangencial em relação ao seu centro. Por isso, sua energia cinética
4. Propriedades dos gases experimentos e modelo microscópico simples para a temperatura
 PV T = nr, onde R é um número (a constante dos gases). Repare que esta é uma lei universal para qualquer gás em pressão e temperatura próxima da atmosférica: não aparece nenhuma dependência de características
PV T = nr, onde R é um número (a constante dos gases). Repare que esta é uma lei universal para qualquer gás em pressão e temperatura próxima da atmosférica: não aparece nenhuma dependência de características
Instituto de Física USP Física V - Aula 04
 Instituto de Física USP Física V - Aula 04 Professora: Mazé Bechara Aula 04 Mecânica estatística clássica. Estimativa dos do calor específico molar a volume constante em gases mono e poliatômicos e nos
Instituto de Física USP Física V - Aula 04 Professora: Mazé Bechara Aula 04 Mecânica estatística clássica. Estimativa dos do calor específico molar a volume constante em gases mono e poliatômicos e nos
Universidade Federal do Rio de Janeiro Instituto de Física Primeira Prova (Diurno) Disciplina: Física III-A /2 Data: 17/09/2018
 Universidade Federal do Rio de Janeiro Instituto de Física Primeira Prova (Diurno) Disciplina: Física III-A - 2018/2 Data: 17/09/2018 Seção 1: Múltipla Escolha (7 0,8 = 5,6 pontos) 3. O campo elétrico
Universidade Federal do Rio de Janeiro Instituto de Física Primeira Prova (Diurno) Disciplina: Física III-A - 2018/2 Data: 17/09/2018 Seção 1: Múltipla Escolha (7 0,8 = 5,6 pontos) 3. O campo elétrico
UFABC Fenômenos Térmicos Prof. Germán Lugones. Aula 7: Capacidades caloríficas de gases ideais, processos adiabáticos, equipartição da energia.
 UFABC Fenômenos Térmicos Prof. Germán Lugones Aula 7: Capacidades caloríficas de gases ideais, processos adiabáticos, equipartição da energia. Energia interna de um gás ideal Energia interna: Do ponto
UFABC Fenômenos Térmicos Prof. Germán Lugones Aula 7: Capacidades caloríficas de gases ideais, processos adiabáticos, equipartição da energia. Energia interna de um gás ideal Energia interna: Do ponto
Integrais Duplos e Triplos.
 Capítulo 4 Integrais uplos e Triplos. 4.1 Integrais uplos xercício 4.1.1 Calcule os seguintes integrais. a. e. 1 1 e 1 2x+2 15xy + 1y 2 dy dx b. y x dx dy 4 x 2y) dy dx f. 4 1 π 6 2 π 2 x 1 6xy 3 + x )
Capítulo 4 Integrais uplos e Triplos. 4.1 Integrais uplos xercício 4.1.1 Calcule os seguintes integrais. a. e. 1 1 e 1 2x+2 15xy + 1y 2 dy dx b. y x dx dy 4 x 2y) dy dx f. 4 1 π 6 2 π 2 x 1 6xy 3 + x )
O degrau de potencial. Caso I: energia menor que o degrau
 O degrau de potencial. Caso I: energia menor que o degrau A U L A 8 Meta da aula Aplicar o formalismo quântico ao caso de uma partícula quântica que incide sobre um potencial V(x) que tem a forma de um
O degrau de potencial. Caso I: energia menor que o degrau A U L A 8 Meta da aula Aplicar o formalismo quântico ao caso de uma partícula quântica que incide sobre um potencial V(x) que tem a forma de um
EUF. Exame Unificado
 EUF Exame Unificado das Pós-graduações em Física Para o segundo semestre de 016 Respostas esperadas Parte 1 Estas são sugestões de possíveis respostas Outras possibilidades também podem ser consideradas
EUF Exame Unificado das Pós-graduações em Física Para o segundo semestre de 016 Respostas esperadas Parte 1 Estas são sugestões de possíveis respostas Outras possibilidades também podem ser consideradas
2. Em um sistema massa-mola temos k = 300 N/m, m = 2 kg, A = 5 cm. Calcule ω, T, f, E (12,25 rad/s; 0,51 s; 1,95 Hz; 0,38 J).
 FÍSICA BÁSICA II - LISTA 1 - OSCILAÇÕES - 2019/1 1. Em um sistema massa-mola temos k = 200 N/m, m = 1 kg, x(0) = A = 10 cm. Calcule ω, T, f, v m, a m, E (14,14 rad/s; 0,44 s; 2,25 Hz; 1,41 m/s; 20 m/s
FÍSICA BÁSICA II - LISTA 1 - OSCILAÇÕES - 2019/1 1. Em um sistema massa-mola temos k = 200 N/m, m = 1 kg, x(0) = A = 10 cm. Calcule ω, T, f, v m, a m, E (14,14 rad/s; 0,44 s; 2,25 Hz; 1,41 m/s; 20 m/s
(d) F < P a, F = P b, F < P c, P a < P c. (e) F = P a, F > P b, F < P c, P a < P c. Não é possível determinar com os dados do enunciado.
 Seção 1. Universidade Federal do io de Janeiro Instituto de Física Física II 017.1 Prova 1: 4/04/017 Versão: A 5. A gura abaixo mostra três recipientes com a mesma área da base e contendo o mesmo uido
Seção 1. Universidade Federal do io de Janeiro Instituto de Física Física II 017.1 Prova 1: 4/04/017 Versão: A 5. A gura abaixo mostra três recipientes com a mesma área da base e contendo o mesmo uido
= 6, mol de moléculas de um gás possui aproximadamente 6, moléculas deste gás, ou seja, seiscentos e dois sextilhões de moléculas;
 TEORIA CINÉTICA DOS GASES PROF. LEANDRO NECKEL NÚMERO DE AVOGADRO Mol é a quantidade de substância de um sistema que contém tantas entidades elementares quanto são os átomos contidos em 0,012 quilograma
TEORIA CINÉTICA DOS GASES PROF. LEANDRO NECKEL NÚMERO DE AVOGADRO Mol é a quantidade de substância de um sistema que contém tantas entidades elementares quanto são os átomos contidos em 0,012 quilograma
Sétima Lista. MAT0216 Cálculo Diferencial e Integral III Prof. Daniel Victor Tausk 14/04/2019
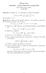 Sétima Lista MAT216 Cálculo iferencial e Integral III Prof. aniel Victor Tausk 14/4/219 Exercício 1. ados a, b, c >, determine o volume do elipsóide {(x, y, z) R 3 : x2 a 2 + y2 b 2 + z2 } c 2 1 de semi-eixos
Sétima Lista MAT216 Cálculo iferencial e Integral III Prof. aniel Victor Tausk 14/4/219 Exercício 1. ados a, b, c >, determine o volume do elipsóide {(x, y, z) R 3 : x2 a 2 + y2 b 2 + z2 } c 2 1 de semi-eixos
Física Geral. Trabalho, Energia e Momentum Linear.
 Física Geral Trabalho, Energia e Momentum Linear. l Energia e Momentum Há muitas formas de energia como por exemplo, energia nuclear, energia elétrica, energia sonora, energia luminosa. Quando você levanta
Física Geral Trabalho, Energia e Momentum Linear. l Energia e Momentum Há muitas formas de energia como por exemplo, energia nuclear, energia elétrica, energia sonora, energia luminosa. Quando você levanta
QUESTÕES DE MÚLTIPLA-ESCOLHA (1-4)
 Física I para a Escola Politécnica 4323101) - P2 26/05/2017) [0000]-p1/?? QUESTÕES DE ÚLTIPLA-ESCOLHA 1-4) ando necessário, use π = 3, 14, g=10 m/s 2. 1) [1,0] Um bloco de massa encontra-se em repouso
Física I para a Escola Politécnica 4323101) - P2 26/05/2017) [0000]-p1/?? QUESTÕES DE ÚLTIPLA-ESCOLHA 1-4) ando necessário, use π = 3, 14, g=10 m/s 2. 1) [1,0] Um bloco de massa encontra-se em repouso
Programa da cadeira Termodinâmica e Teoria Cinética
 Programa da cadeira Termodinâmica e Teoria Cinética Cursos: Engenharia Civil, Engenharia de Instrumentação e Electrónica Ano lectivo 2004-05, 2º semestre Docentes: Prof. Dr. Mikhail Benilov (aulas teóricas,
Programa da cadeira Termodinâmica e Teoria Cinética Cursos: Engenharia Civil, Engenharia de Instrumentação e Electrónica Ano lectivo 2004-05, 2º semestre Docentes: Prof. Dr. Mikhail Benilov (aulas teóricas,
Conjunto canónico MEFT, IST. Reality is merely an illusion, albeit a very persistent one Albert Einstein
 Física estatística Conjunto canónico MEFT, IST Reality is merely an illusion, albeit a very persistent one Albert Einstein Necessidade do conjunto canónico Fizémos o conjunto microcanónico, que descreve
Física estatística Conjunto canónico MEFT, IST Reality is merely an illusion, albeit a very persistent one Albert Einstein Necessidade do conjunto canónico Fizémos o conjunto microcanónico, que descreve
Instituto de Física USP. Física V - Aula 18. Professora: Mazé Bechara
 Instituto de Física USP Física V - Aula 18 Professora: Mazé Bechara Aula 28 Discussão da 1ª prova e Apresentação do Tópico III 1. Soluções das questões da prova com comentários. Critérios de correção.
Instituto de Física USP Física V - Aula 18 Professora: Mazé Bechara Aula 28 Discussão da 1ª prova e Apresentação do Tópico III 1. Soluções das questões da prova com comentários. Critérios de correção.
Capítulo 11 - Teoria Cinética dos Gases. O número de Avogrado é número de moléculas contido em 1 mol de qualquer substãncia
 Capítulo 11 - Teoria Cinética dos Gases Em 1811, o italiano Amedeo Avogrado enunciou 2 hipóteses: 1) As moléculas de um gás podem ser compostas por mais de um único átomo. 2) Nas mesmas condições de temperatura
Capítulo 11 - Teoria Cinética dos Gases Em 1811, o italiano Amedeo Avogrado enunciou 2 hipóteses: 1) As moléculas de um gás podem ser compostas por mais de um único átomo. 2) Nas mesmas condições de temperatura
CENTRO DE MASSA E MOMENTO LINEAR
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA I CENTRO DE MASSA E MOMENTO LINEAR Prof. Bruno Farias Introdução Neste módulo vamos discutir
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA I CENTRO DE MASSA E MOMENTO LINEAR Prof. Bruno Farias Introdução Neste módulo vamos discutir
Nota: Turma: MA 327 Álgebra Linear. Terceira Prova. Boa Prova! Primeiro Semestre de T o t a l
 Turma: Nota: MA 327 Álgebra Linear Primeiro Semestre de 26 Terceira Prova Nome: RA: Questões Pontos Questão 1 Questão 2 Questão 3 Questão 4 Questão 5 T o t a l Boa Prova! Questão 1. 2. Pontos) Seja U um
Turma: Nota: MA 327 Álgebra Linear Primeiro Semestre de 26 Terceira Prova Nome: RA: Questões Pontos Questão 1 Questão 2 Questão 3 Questão 4 Questão 5 T o t a l Boa Prova! Questão 1. 2. Pontos) Seja U um
CÁLCUL O INTEGRAI S DUPLAS ENGENHARIA
 CÁLCUL O INTEGRAI S DUPLAS ENGENHARIA 1 INTERPRETAÇÃO GEOMÉTRICA DE Nas integrais simples, nós somamos os valores de uma função f(x) em comprimentos dx. Agora, nas integrais duplas fazemos o mesmo, mas
CÁLCUL O INTEGRAI S DUPLAS ENGENHARIA 1 INTERPRETAÇÃO GEOMÉTRICA DE Nas integrais simples, nós somamos os valores de uma função f(x) em comprimentos dx. Agora, nas integrais duplas fazemos o mesmo, mas
GAAL - Terceira Prova - 15/junho/2013. Questão 1: Analise se a afirmação abaixo é falsa ou verdadeira:
 GAAL - Terceira Prova - /junho/3 SOLUÇÕES Questão : Analise se a afirmação abaio é falsa ou verdadeira: [ A matriz A é diagonalizável SOLUÇÃO: Sabemos que uma matriz n n é diagonalizável se ela possuir
GAAL - Terceira Prova - /junho/3 SOLUÇÕES Questão : Analise se a afirmação abaio é falsa ou verdadeira: [ A matriz A é diagonalizável SOLUÇÃO: Sabemos que uma matriz n n é diagonalizável se ela possuir
1 Transformada de Legendre
 1 Transformada de Legendre No caso da parede porosa a pressão constante a quantidade se conserva. Além disso H = U + P V dh = du + P dv + V dp du = dq + dw = dq dh = dq + V dp P dv escrevendo H = H (P;
1 Transformada de Legendre No caso da parede porosa a pressão constante a quantidade se conserva. Além disso H = U + P V dh = du + P dv + V dp du = dq + dw = dq dh = dq + V dp P dv escrevendo H = H (P;
CÁLCULO I. 1 Concavidade. Objetivos da Aula. Aula n o 16: Máximos e Mínimos - 2 a Parte
 CÁLCULO I Prof. Edilson Neri Júnior Prof. André Almeida Aula n o 16: Máximos e Mínimos - 2 a Parte Objetivos da Aula Denir e discutir a concavidade de uma função em um intervalo do domínio; Denir e calcular
CÁLCULO I Prof. Edilson Neri Júnior Prof. André Almeida Aula n o 16: Máximos e Mínimos - 2 a Parte Objetivos da Aula Denir e discutir a concavidade de uma função em um intervalo do domínio; Denir e calcular
Desenvolvimento. Em coordenadas esféricas:
 Desenvolvimento Para que possamos resolver a equação da onda em coordenadas esféricas, antes é necessária a dedução do operador Laplaciano nessas coordenadas, portanto temos: Em coordenadas esféricas:
Desenvolvimento Para que possamos resolver a equação da onda em coordenadas esféricas, antes é necessária a dedução do operador Laplaciano nessas coordenadas, portanto temos: Em coordenadas esféricas:
PROFESSOR: RICARDO SÁ EARP
 LISTA DE EXERCÍCIOS SOBRE TRABALHO, CAMPOS CONSERVATIVOS, TEOREMA DE GREEN, FLUXO DE UM CAMPO AO LONGO DE UMA CURVA, DIVERGÊNCIA E ROTACIONAL DE UM CAMPO NO PLANO, FUNÇÕES HARMÔNICAS PROFESSOR: RICARDO
LISTA DE EXERCÍCIOS SOBRE TRABALHO, CAMPOS CONSERVATIVOS, TEOREMA DE GREEN, FLUXO DE UM CAMPO AO LONGO DE UMA CURVA, DIVERGÊNCIA E ROTACIONAL DE UM CAMPO NO PLANO, FUNÇÕES HARMÔNICAS PROFESSOR: RICARDO
Biologia Estrutural. Cálculo da Densidade Eletrônica. Prof. Dr. Walter Filgueira de Azevedo Jr. wfdaj.sites.uol.com.br
 Biologia Estrutural Cálculo da Densidade Eletrônica Prof. Dr. Walter Filgueira de Azevedo Jr. Resumo Introdução Cálculo da densidade eletrônica Densidade eletrônica de um cristal unidimensional Densidade
Biologia Estrutural Cálculo da Densidade Eletrônica Prof. Dr. Walter Filgueira de Azevedo Jr. Resumo Introdução Cálculo da densidade eletrônica Densidade eletrônica de um cristal unidimensional Densidade
Física estatística. Sistemas de Fermi ideais MEFT, IST
 Física estatística Sistemas de Fermi ideais MEFT, IST Before I came here I was confused about this subject. Having listened to your lecture I am still confused. But on a higher level. Enrico Fermi (1901
Física estatística Sistemas de Fermi ideais MEFT, IST Before I came here I was confused about this subject. Having listened to your lecture I am still confused. But on a higher level. Enrico Fermi (1901
Capítulo Equações da reta no espaço. Sejam A e B dois pontos distintos no espaço e seja r a reta que os contém. Então, P r existe t R tal que
 Capítulo 11 1. Equações da reta no espaço Sejam A e B dois pontos distintos no espaço e seja r a reta que os contém. Então, P r existe t R tal que AP = t AB Fig. 1: Reta r passando por A e B. Como o ponto
Capítulo 11 1. Equações da reta no espaço Sejam A e B dois pontos distintos no espaço e seja r a reta que os contém. Então, P r existe t R tal que AP = t AB Fig. 1: Reta r passando por A e B. Como o ponto
Física estatística. Teoria cinética dos gases MEFT, IST
 Física estatística Teoria cinética dos gases MEFT, IST Life is a series of collisions with the future; it is not the sum of what we have been, but what we yearn to be. Jose Ortega y Gasset (1883-1955)
Física estatística Teoria cinética dos gases MEFT, IST Life is a series of collisions with the future; it is not the sum of what we have been, but what we yearn to be. Jose Ortega y Gasset (1883-1955)
Gabarito da Prova Final Unificada de Cálculo IV Dezembro de 2010
 Gabarito da Prova Final Unificada de Cálculo IV Dezembro de a Questão: (5 pts) Dentre as três séries alternadas abaixo, diga se convergem absolutamente, se convergem condicionalmente ou se divergem Justifique
Gabarito da Prova Final Unificada de Cálculo IV Dezembro de a Questão: (5 pts) Dentre as três séries alternadas abaixo, diga se convergem absolutamente, se convergem condicionalmente ou se divergem Justifique
Resolução das questões objetivas* da 1ª e da 2ª Prova de Física II Unificada do Período UFRJ
 Resolução das questões objetivas* da ª e da ª Prova de Física II Unificada do Período 0.-UFRJ *Assuntos: Termodinâmica, Hidrodinâmica e Hidrostática. Resolução: João Batista F. Sousa Filho (Graduando Engenharia
Resolução das questões objetivas* da ª e da ª Prova de Física II Unificada do Período 0.-UFRJ *Assuntos: Termodinâmica, Hidrodinâmica e Hidrostática. Resolução: João Batista F. Sousa Filho (Graduando Engenharia
Física estatística MEFT, IST. Statistical thinking will one day be as necessary for efficient citizenship as the ability to read and write.
 Física estatística Gases ideais nas estatísticas quânticas: conjunto microcanónico MEFT, IST Statistical thinking will one day be as necessary for efficient citizenship as the ability to read and write.
Física estatística Gases ideais nas estatísticas quânticas: conjunto microcanónico MEFT, IST Statistical thinking will one day be as necessary for efficient citizenship as the ability to read and write.
Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a. o resultado do movimento dos átomos e moléculas.
 TEORIA CINÉTICA Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a energia interna são interpretadas como o resultado do movimento dos átomos e moléculas. Pressão
TEORIA CINÉTICA Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a energia interna são interpretadas como o resultado do movimento dos átomos e moléculas. Pressão
Universidade Estadual de Santa Cruz
 Universidade Estadual de Santa Cruz PROFÍSICA Programa de Pós-graduação em Física Seleção 2009. Prova Escrita 2/0/2009 Candidato (nome legível): - Esta prova consta de oito questões distribuídas da seguinte
Universidade Estadual de Santa Cruz PROFÍSICA Programa de Pós-graduação em Física Seleção 2009. Prova Escrita 2/0/2009 Candidato (nome legível): - Esta prova consta de oito questões distribuídas da seguinte
Física II-P1 INTRODUÇÃO 1 ENTROPIA
 Física II-P1 INTRODUÇÃO Fala, galera!! Fizemos aqui um resumão com o que mais tem caído nas P1s de Física II, abordando os temas de entropia, reversibilidade, cinética dos gases e distribuição de Maxwell.
Física II-P1 INTRODUÇÃO Fala, galera!! Fizemos aqui um resumão com o que mais tem caído nas P1s de Física II, abordando os temas de entropia, reversibilidade, cinética dos gases e distribuição de Maxwell.
Universidade Federal de Mato Grosso do Sul - UFMS VGA - 2 a Prova - Engenharia de Computação 03 de Julho de Prof o. E.T.
 Universidade Federal de Mato Grosso do Sul - UFMS VGA - 2 a Prova - Engenharia de Computação 0 de Julho de 2014 - Prof o ETGalante 1 (2,0 pontos) Na gura acima ABCDEF GH é um paralelepípedo O ponto M é
Universidade Federal de Mato Grosso do Sul - UFMS VGA - 2 a Prova - Engenharia de Computação 0 de Julho de 2014 - Prof o ETGalante 1 (2,0 pontos) Na gura acima ABCDEF GH é um paralelepípedo O ponto M é
CÁLCULO I. 1 Taxa de Variação. Objetivos da Aula. Aula n o 15: Taxa de Variação. Taxas Relacionadas. Denir taxa de variação;
 CÁLCULO I Prof. Marcos Diniz Prof. Edilson Neri Prof. André Almeida Aula n o 15: Taxa de Variação. Taxas Relacionadas Objetivos da Aula Denir taxa de variação; Usar as regras de derivação no cálculo de
CÁLCULO I Prof. Marcos Diniz Prof. Edilson Neri Prof. André Almeida Aula n o 15: Taxa de Variação. Taxas Relacionadas Objetivos da Aula Denir taxa de variação; Usar as regras de derivação no cálculo de
