TRANSPORTADORES DE OXIGENIO NiAl 2 O 4 /θ-al 2 O 3 APLICÁVEIS A PROCESSOS COM RECIRCULAÇÃO QUÍMICA.
|
|
|
- Elza Anjos Bacelar
- 7 Há anos
- Visualizações:
Transcrição
1 TRANSPORTADORES DE OXIGENIO NiAl 2 O 4 /θ-al 2 O 3 APLICÁVEIS A PROCESSOS COM RECIRCULAÇÃO QUÍMICA. R. D. Barbosa 1,2, G. M. da Cruz. 1, P. H. L. N. A. Santos 1,2, G. G. Cortez 2, J. A. J. Rodrigues 1 1 Instituto Nacional de Pesquisas, Laboratório Associado de Combustão e Propulsão 2 Universidade de São Paulo, Escola de Engenharia de Lorena, Dep. de Engenharia Química para contato: renatodiasbarbosa@gmail.com RESUMO As tecnologias em desenvolvimento, Combustão com Recirculação Química (CLC) e Reforma com Recirculação Química (CLR) mostram-se promissoras para produção de energia limpa. O processo CLC é capaz de produzir calor com intrínseca separação de CO 2. O processo CLR pode ser usado para produzir H 2 a partir do gás de síntese gerado. Os sistemas CLC e CLR consistem de dois reatores de leito fluidizado interconectados, um de combustível e outro de ar, pelos quais circula um fluxo contínuo de transportadores de oxigênio (TO). O TO, constituído por óxido metálico, é responsável por transferir oxigênio do ar ao combustível, evitando o contato direto entre os dois gases. Tais processos permitem a oxidação completa e/ou parcial de combustíveis gasosos sem que os produtos estejam misturados a N 2, O 2 ou NO x. Neste trabalho foi realizada a síntese de TOs constituídos de diferentes teores NiAl 2 O 4 /θ-al 2 O 3, caracterizações por diferentes técnicas e testes reacionais por TGA e em reator de leito fixo. Os TOs foram avaliados com diferentes tempos de redução, utilizando metano como combustível modelo, com e sem adição de CO 2 e/ou H 2 O à mistura reacional. Os TOs mostraram-se seletivos à reforma do combustível produzindo preferencialmente CO e H INTRODUÇÃO Nas ultimas décadas, avanços significativos foram alcançados no entendimento relativo às mudanças climáticas provocadas pelo aquecimento global. Sabe-se que as emissões dos gases estufa, entre eles, CO 2, CO, NO x, SO x e CH 4 são os principais causadores do aquecimento global. O dióxido de carbono figura entre os mais nocivos, devido à enorme quantidade em que é liberado para a atmosfera a partir da utilização de combustíveis de origem fóssil. Segundo estimativas, a concentração de CO 2 na atmosfera terrestre passou de 280 ppm, no período anterior à industrialização, para 390 ppm em 2010, significando um acréscimo de 39% (Adanez et al, 2012). A indiscriminada emissão de gases estufa tem sido foco de grandes discussões e tentativas de acordos de redução em conferências internacionais tais como: a conferência da ONU sobre o meio ambiente em Estocolmo em 1972, Suécia; ECO-92 em 1992, Brasil; Protocolo de Kyoto em 1997, Japão; e Rio+20 em 2012, Brasil. Por outro lado a sociedade moderna enfrenta grandes problemas relacionados à questão energética, tendo em vista que o consumo de energia é crescente, devido ao crescimento da Área temática: Engenharia Ambiental e Tecnologias Limpas 1
2 produção industrial, necessidades de transporte, iluminação, aquecimento, refrigeração, além do uso de diversos equipamentos eletrônicos considerados indispensáveis ao estilo de vida moderno. Através de cálculos baseados no atual ritmo de crescimento mundial, o Departamento de Energia Americano estima que a demanda mundial de energia cresça de 462 quatrilhões de BTU em 2005 para 690 quatrilhões de BTU em 2030 (Fan e Li, 2010). Enquanto isso, a maior parte da matriz energética primária mundial continua a ser de origem fóssil, não renovável e consequentemente limitada, segundo dados da BP, sendo composta principalmente por 33% petróleo, 29% carvão mineral e 23% gás natural. No Brasil, a matriz energética se diferencia da mundial, tendo como índices: 44% petróleo, 35% hidroelétricas, 9% gás natural e 5% carvão mineral (British Petroleum, 2013). O gás natural é um produto abundante em todo o planeta, sua composição varia em cada região, consistindo em grande parte de metano, juntamente a etano e propano, observando-se também a presença de CO 2 e H 2 S em algumas regiões. Outra importante fonte de metano é o biogás, gerado pela decomposição de matéria orgânica, o qual é composto majoritariamente por CH 4 (55-65%) e CO 2 (30-45%). Dentro deste contexto, destacam-se os processos de combustão com recirculação química e reforma com recirculação química, que visam a oxidação de hidrocarbonetos gasosos, para produção de energia ou gás de síntese (CO e H 2 ), através da ação de um transportador de oxigênio sólido, sem a emissão de gases estufa para a atmosfera. Combustão e Reforma com Recirculação Química O processo de combustão com recirculação química (CLC, do inglês Chemical-Looping Combustion ), tem por objetivo a produção de energia (calor) a partir da oxidação completa de hidrocarbonetos gasosos, permitindo a separação do CO 2. O processo de reforma com recirculação química (CLR, do inglês Chemical-Looping Reforming ) realiza a oxidação parcial do combustível, neste caso priorizando a produção de gás de síntese. CLC e CLR funcionam a partir de um sistema composto por dois reatores de leito fluidizado interconectados, reator de ar (RA) e reator de combustível (RC), por onde circulam transportadores de oxigênio sólidos. A seletividade de cada transportador de oxigênio (TO) é um dos principais fatores que diferenciam CLC de CLR, tendo em vista que ambos operam com configurações de processo semelhantes. O TO, composto por óxido metálico na forma de pó fino, é responsável por transferir oxigênio do ar ao combustível, evitando o contato direto entre combustível e ar por diferentes propósitos. Uma circulação constante de TOs ocorre entre os dois reatores de leito fluidizado (RA e RC), sofrendo sucessivos ciclos de redução e oxidação (Santos et. al., 2013). No processo CLC, CO 2 puro pode ser facilmente separado de H 2 O através do resfriamento do efluente do sistema reacional, podendo ser armazenado geologicamente ou ainda ser usado como reagente em outros processos industriais. Esta é a principal vantagem da combustão CLC em relação às demais tecnologias para captura de CO 2, possibilitando a captura e armazenamento geológico de CO 2 de maneira eficiente e a baixo custo, pois não existe a necessidade de unidades Área temática: Engenharia Ambiental e Tecnologias Limpas 2
3 secundárias para separação, principalmente de NO x e N 2, evitando perdas de energia e aumentos de custos de produção. Estudos preliminares de viabilidade sugerem que o CLC é um processo de combustão promissor, entretanto, a aplicação deste processo em escala industrial depende, efetivamente, do desenvolvimento de TOs com alto desempenho e estabilidade (Fan e Li, 2010). Mais de 700 combinações de materiais já foram testadas como TOs em processos CLC e CLR (Adanez et al, 2012). As pesquisas investigaram o uso de metais de transição, com destaque para Fe, Cu e Ni. O Fe, seletivo a CLC, apesar de ter baixo custo apresenta baixa reatividade. O cobre apresenta-se vantajoso, pelo fato de liberar energia, reação exotérmica durante a redução e também durante a oxidação, operando em CLC; entretanto, por apresentar baixo ponto de fusão e os processos operarem em temperaturas elevadas, este metal apresenta limitações. O níquel mostra-se vantajoso, apresentando alta reatividade com conversões próximas a 100%, resistência a alta temperatura e elevada capacidade de transporte de oxigênio, podendo operar em regime CLC ou CLR. Apesar de não figurar entre os óxidos mais baratos, pode-se empregá-lo na forma suportada, reduzindo significativamente o custo de matérias primas (Fan e Li, 2010; Adanez et al, 2012). Os processos CLC e CLR podem ser representados esquematicamente segundo o diagrama apresentado a seguir: Figura 1 Esquema de funcionamento dos processos CLC e CLR As equações a seguir representam as principais reações envolvidas no processo de Combustão CLC: H r (1) H o (2) A equação seguinte representa a reação de oxidação completa do metano, ou combustão, equivalente à soma das reações de CLC, sem levar em consideração o transportador de oxigênio: H c = H r + H o (3) Levando-se em consideração os produtos das reações, entalpias de combustão e calor gerados nas duas etapas da combustão CLC, pode-se dizer que o processo é semelhante aos convencionais processos de combustão, onde o combustível é queimado em contato direto com ar (Adanez et al, 2012). Observa-se também como vantagem deste processo de combustão, a minimização da formação de NO x, tendo em vista que o combustível é oxidado em atmosfera isenta de nitrogênio, e a reoxidação no reator de ar ocorre sem a presença de metano. Área temática: Engenharia Ambiental e Tecnologias Limpas 3
4 As equações abaixo representam as principais reações envolvidas no processo de reforma CLR: O processo CLR pode ser comparado ao tradicional processo de oxidação parcial de hidrocarbonetos. No CLR o TO é o responsável pelo fornecimento de oxigênio, evitando-se custos adicionais associados à obtenção de oxigênio puro, necessário no processo de oxidação parcial. Os produtos do processo CLR podem ser usados como reagentes em processos para síntese de hidrocarbonetos, através de reações de Fischer-Tropsch. O gás de síntese é também o principal intermediário na produção de hidrogênio molecular; neste caso a mistura produto do CLR pode ser enviada a um reator de deslocamento gás-água SHIFT (CO + H 2 O H 2 + CO 2 ), aumentando assim a concentração de H 2. A mistura final segue para processos de purificação por adsorção a pressão modulada (PSA, do inglês Pressure Swing Adsorption ), destilação fracionada ou criogênica, ou ainda separação por membranas permeáveis a hidrogênio, como a membrana de paládio. 2. MATERIAIS E MÉTODOS Para a obtenção dos TOs, compostos por 2, 4 e 8% m/m de NiO suportado sobre uma alumina ativa, utilizou-se o método de impregnação incipiente por etapas sucessivas. Neste processo, uma gama alumina comercial (SASOL, PURALOX NWa-155), calcinada a 600ºC pelo fabricante, foi impregnada com solução aquosa de nitrato de níquel hexahidratado (VETEC), de concentração suficiente para adicionar 2% m/m NiO. Após cada etapa de impregnação, o material foi secado a 130ºC por 30 min e calcinado a 550ºC, também por 30 min, a fim de decompor o sal precursor. Ao final das etapas de impregnação e decomposição do sal, o material foi submetido a uma calcinação final a 1000ºC por 3h. Os TOs obtidos foram caracterizados por diferentes técnicas, entre elas difratometria de raios X (DRX) e redução a temperatura programada (RTP). Os difratogramas foram obtidos utilizando um difratômetro de raios X modelo PW1830, marca PHILIPS, com radiação Cu kα, tensão de 45 kv, corrente de 40mA, filtro monocromador de níquel, passo angular de 0,02º no intervalo de medição de 10º 2θ 80º. As RTPs foram efetuadas em equipamento modelo ChemBET-3000 da marca QUANTACHROME INSTRUMENTS, utilizando 160 mg de amostra, atenuação 16, corrente 150 A e fluxo de 130 ml/min de mistura redutora composta por 5% H 2 /N 2. Os TOs foram submetidos a avaliações reacionais em microbalança termogravimétrica (TGA), modelo SDT Q600 da marca TA instruments, e em reator de leito fixo (RLF). Nos testes reacionais os TOs foram submetidos a sucessivos ciclos de redução e oxidação, constituídos por uma etapa de redução e outra de oxidação, separadas por um período em presença de gás inerte. Os produtos da reação foram analisados por espectrometria de massas (EM) e cromatografia gasosa (CG). As misturas reacionais utilizadas nos ensaios foram dosadas por controladores de fluxo mássico da marca MKS, tendo as vazões medidas por bolhômetro e composições aferidas (4) (5) Área temática: Engenharia Ambiental e Tecnologias Limpas 4
5 por CG. Durante os ciclos redox realizados em TGA, objetivou-se analisar o transporte de oxigênio, equivalente à variação da massa e a estabilidade dos TOs. Para tanto, utilizou-se um fluxo de 300 ml/min de mistura redutora composta por 10% v/v CH 4 (redução do TO) e mistura oxidante composta por 20% v/v O 2 (oxidação do TO), ambas com balanço em argônio. No RLF objetivou-se analisar a seletividade dos TOs e capacidade de conversão do combustível entre outros parâmetros; para tal, utilizou-se fluxo de 50 ml/min de misturas redutoras compostas de: 10% CH 4 ; 5% H 2 O adicionado a 10% CH 4 ou 5% CO 2 adicionado a 10% CH 4, sendo a mistura oxidante composta de 20% O 2, todas com balanço em argônio. Na Figura 2 é apresentado um diagrama do sistema utilizado para a avaliação em RLF. Figura 2 Diagrama esquemático do sistema de avaliação RLF 3. RESULTADOS E DISCUSSÃO A seguir são apresentados os resultados de DRX: Figura 3 DRX Suporte (γ-al 2 O 3 ) e transportadores de oxigênio No DRX da alumina PURALOX NWa-155, calcinada a 600ºC, observou-se a predominância da fase gama alumina (γ-al 2 O 3 ), apresentando estrutura cúbica de face centrada. Nos TOs 2, 4 e 8% NiO/γ-Al 2 O 3, calcinados a 1000 C, observou-se a presença de duas fases cristalinas, fase teta alumina (θ-al 2 O 3 ) e fase aluminato de níquel (NiAl 2 O 4 ). A formação do aluminato de níquel estava prevista, tendo em vista a temperatura empregada e a reatividade da gama alumina. Observa-se em literatura que γ-al 2 O 3 é caracterizada pela estrutura cristalina de espinélio com déficit de cátions, facilitando a difusão dos íons de níquel nas camadas superficiais do suporte durante a calcinação (Li e Chen, 1995). Área temática: Engenharia Ambiental e Tecnologias Limpas 5
6 A seguir são apresentados os resultados de RTP para os TOs sintetizados e para um óxido de níquel mássico obtido pela calcinação de nitrato de níquel a 1000 ºC: Figura 4 Temperatura de redução programada transportadores de oxigênio e NiO mássico Observa-se que as reduções dos TOs da série níquel ocorrem em temperaturas elevadas e com menor intensidade de sinal (~8 vezes menor) quando em comparação ao NiO mássico. Quanto maior o teor de níquel no TO, menor a temperatura em que se inicia a redução, mais intenso o sinal do detector e maior a largura do pico. O óxido de níquel mássico apresentou redução na faixa de temperatura de 260 a 560 C, com máximo em 400 C. Constatou-se em estudos publicados de RTP com NiO, NiAl 2 O 4 e NiO/Al 2 O 3, que NiO mássico apresenta redução próxima à temperatura de 220 C e que NiAl 2 O 4 mássico se reduz próximo à 790 C e, mesmo quando suportados sobre alumina, diferentes teores de NiO apresentam reduções em temperaturas inferiores a 700 C (Li e Chen, 1995). A diferença entre a temperatura de redução do NiO, observada na literatura e a constatada no ensaio realizado, pode ser atribuída às diferenças de temperatura de calcinação entre os materiais, quantidade de amostra e vazão de reagentes, entre outras. Comparando-se os resultados é razoável afirmar que, para todos os TOs da série níquel existe a presença da fase NiAl 2 O 4 superficial, indicando também não possuírem a fase NiO segregada. Quanto menor o teor de NiAl 2 O 4 sobre a alumina, menor a sua redutibilidade, mais dispersos os cristais de NiAl 2 O 4 e mais forte a interação destes com o suporte. Resultados semelhantes foram observados por Santos et. al. (2013). A seguir são apresentadas ampliações de ciclos redox representativos para os TOs 2, 4 e 8% NiO/Al 2 O 3, obtidos por TGA a 950ºC, utilizando-se período de 1,5 min de mistura redutora (etapa 1) e 3 min de mistura oxidante (etapa 2), separados por um período de inerte (Argônio). Figura 5 Ciclos redox em TGA/DSC 2, 4 e 8% NiO/Al 2 O 3, respectivamente Área temática: Engenharia Ambiental e Tecnologias Limpas 6
7 Durante os testes reacionais em TGA, foram realizadas várias sequências de ciclos redox (mínimo de 25 ciclos), onde pôde ser observada estabilidade entre os ciclos com relação à variação de massa e fluxo de calor. É possível observar, para as três amostras, que na etapa 1 ocorre diminuição da massa referente à redução dos TOs, ou seja, transporte de oxigênio. O TO 8% NiO/Al 2 O 3 apresentou variação de 1,20% da massa, cerca de 77% do oxigênio teoricamente disponível, considerando um átomo de oxigênio por átomo de níquel, conforme resultados obtidos por espectrometria de emissão atômica (ICP-AES). Os TOs 2 e 4% NiO/Al 2 O 3 apresentaram, respectivamente, variações de 0,29 e 0,59% da massa, cerca de 71 e 73% do oxigênio teoricamente disponível. Para o TO 2% NiO/Al 2 O 3 foi observado um ganho de massa ao final do período de redução, relativo à formação de depósito de carbono proveniente da decomposição catalítica de CH 4 sobre Ni 0 formado pela redução do óxido. Para os três TOs foram observadas reações endotérmicas com CH 4, comprovadas pelo fluxo de calor negativo e seletividade para produção de CO e H 2 (processo CLR), observada por EM. Durante a oxidação (etapa 2), observou-se que os TOs recuperam a massa inicial e apresentam reações exotérmicas, bem como produção de CO 2 e/ou CO provenientes da combustão do carbono depositado durante a etapa de redução. A seguir, são apresentados os resultados de ciclos redox representativos obtidos para o TO 8% NiO/Al 2 O 3 em RLF a 950ºC, utilizando metano como combustível, com e sem a adição de H 2 O ou CO 2 (6 min de redução e 4 min de oxidação), analisados por EM e CG: Figura 6 Ciclos redox em RLF TO 8% NiO/Al 2 O 3 influência da adição de H 2 O e CO 2 É possível observar, durante as etapas de redução (Figura 6), que o TO 8% NiO/Al 2 O 3 apresenta alta conversão do combustível e seletividade para produção de CO e H 2 (processo CLR) para qualquer das três misturas reacionais. No entanto, foi observada pequena produção de CO 2 e H 2 O (processo CLC), principalmente no início da etapa de redução. Por DRX, após a sequencia de ciclos reacionais em RLF (não apresentado neste trabalho), foi observado o surgimento da fase cristalina NiO segregada, evidenciando instabilidade estrutural. Observa-se na literatura que a fase NiO é mais reativa do que NiAl 2 O 4, o que leva a crer ser a fase NiO a responsável pela oxidação completa do combustível, ou seja, processo CLC (Adanez et al, 2012). Foi observado também, quando da realização de ciclos redox com tempos de redução menores (3; 1,5 e 0,75 min, não apresentados neste trabalho) que a diminuição do tempo na etapa de redução reduz a formação do depósito de carbono, por decomposição catalítica do metano sobre Ni 0 Área temática: Engenharia Ambiental e Tecnologias Limpas 7
8 durante a redução do TO (CH 4 C (s) + 2H 2 ). Esta deposição de carbono foi evidenciada pela liberação de CO e CO 2 no início da etapa seguinte de oxidação (C (s) + 1/2O 2 CO ou C (s) + O 2 CO 2 ). Pôde ser constatado também que as adições de H 2 O ou CO 2 ao CH 4 favorecem uma alta seletividade a CLR, diminuindo significativamente a formação de depósito de carbono, por favorecerem as seguintes reações: reforma a vapor, catalisada por Ni 0 (CH 4 + H 2 O CO + 3H 2 ); reforma seca, catalisada por Ni 0 (CH 4 + CO 2 2CO + 2H 2 ); gaseificações do carbono por água (C (S) + H 2 O CO + H 2 ) e por dióxido de carbono (C (S) + CO 2 2CO) (Santos et. al., 2013). A razão H 2 /CO estequiométrica para o processo CLR é igual a dois (equação 4), podendo-se observar nos resultados da Figura 6 que esta razão H 2 /CO é deslocada para valores maiores com a adição de H 2 O e para valores menores com a adição de CO CONCLUSÕES Os materiais sintetizados neste trabalho, compostos por NiAl 2 O 4 /θ-al 2 O 3, são seletivos à reforma do metano, quando empregados no processo modelo (CLR). Ocorreram evoluções estruturais após prolongadas sequências de ciclos redox, pela segregação de NiO cristalino, mas estas não prejudicaram sensivelmente a seletividade a CLR. As adições de H 2 O ou CO 2 ao combustível reduzem significativamente a formação de depósitos de carbono, sem alterar a seletividade à produção de gás de síntese. REFERÊNCIAS ADANEZ, J.; ABAD, A.; GARCIA-LABIANO, F.; GAYAN, P.; DE DIEGO, L. F. Review Progress in Chemical-Looping Combustion and Reforming Technologies. Prog. in Energy and Comb. Science, v. 38, p , BRITISH PETROLEUM. BP Statistical Review of World Energy. p Disponível em < Acesso em: 24 de abril de FAN, L.-S.; LI, F. Chemical Looping Technology and Its Fossil Energy Conversion Applications. Industrial Engineering Chemistry Research. v. 49, p , LI, C.; CHEN, Y.W. Temperature-programmed-reduction studies of nickel oxide/alumina catalysts: effects of the preparation method. Thermochimica Acta. v. 256, p , SANTOS, P. H. L. N. A.; CRUZ, G. M.; CARNEIRO, L. M.; MOURE, G. T.; FERREIRA, M. A.; RODRIGUES, J. A. J. Effect od adding steam to CH 4 during chemical-looping processes with Ni-based oxygen carriers. II Congresso Brasileiro de CO 2 na Indústria de Petróleo, Gás e Biocombustíveis, Rio de Janeiro, AGRADECIMENTOS LCP-INPE, INCT, PETROBRAS, CNPQ e CAPES. Área temática: Engenharia Ambiental e Tecnologias Limpas 8
NOVOS TRANSPORTADORES DE OXIGÊNIO AlNbO 4 /θ-al 2 O 3 SELETIVOS A H 2 NA GERAÇÃO DE ENERGIA LIMPA
 NOVOS TRANSPORTADORES DE OXIGÊNIO AlNbO 4 /θ-al 2 O 3 SELETIVOS A H 2 NA GERAÇÃO DE ENERGIA LIMPA R. D. Barbosa 1,2, G. M. da Cruz. 1, G. G. Cortez 2, P. H. L. N. A. Santos 1,2, J. A. J. Rodrigues 1 1
NOVOS TRANSPORTADORES DE OXIGÊNIO AlNbO 4 /θ-al 2 O 3 SELETIVOS A H 2 NA GERAÇÃO DE ENERGIA LIMPA R. D. Barbosa 1,2, G. M. da Cruz. 1, G. G. Cortez 2, P. H. L. N. A. Santos 1,2, J. A. J. Rodrigues 1 1
Produção de hidrogênio a partir do biogás
 Produção de hidrogênio a partir do biogás Líderes: Emerson Léo Schultz (2013-2015) Itânia Pinheiro Soares (2015-2016) Equipe: Fábio Bellot Noronha (INT) Introdução Processos de reforma de metano são usados
Produção de hidrogênio a partir do biogás Líderes: Emerson Léo Schultz (2013-2015) Itânia Pinheiro Soares (2015-2016) Equipe: Fábio Bellot Noronha (INT) Introdução Processos de reforma de metano são usados
ÓXIDOS APLICADOS A PROCESSOS DE COMBUSTÃO COM CAPTURA DE DIÓXIDO DE CARBONO PARA MITIGAÇÃO DO EFEITO ESTUFA
 ÓXIDOS APLICADOS A PROCESSOS DE COMBUSTÃO COM CAPTURA DE DIÓXIDO DE CARBONO PARA MITIGAÇÃO DO EFEITO ESTUFA RELATÓRIO PARCIAL DE PROJETO DE INICIAÇÃO CIENTÍFICA (PIBIC/CNPq/INPE) Marcelo Leme do Prado
ÓXIDOS APLICADOS A PROCESSOS DE COMBUSTÃO COM CAPTURA DE DIÓXIDO DE CARBONO PARA MITIGAÇÃO DO EFEITO ESTUFA RELATÓRIO PARCIAL DE PROJETO DE INICIAÇÃO CIENTÍFICA (PIBIC/CNPq/INPE) Marcelo Leme do Prado
Centro de Tecnologias do Gás e Energias Renováveis - 2
 ESTUDO DO EFEITO DA ADIÇÃO DE CÉRIO AO SUPORTE E DO TEOR DE COBRE NA REATIVIDADE DE MATERIAIS PARA RECIRCULAÇÃO QUIMICA Fabíola Correia de Carvalho 1 ; Adolfo Lopes de Figueredo 2 ; José Carlos do Nascimento
ESTUDO DO EFEITO DA ADIÇÃO DE CÉRIO AO SUPORTE E DO TEOR DE COBRE NA REATIVIDADE DE MATERIAIS PARA RECIRCULAÇÃO QUIMICA Fabíola Correia de Carvalho 1 ; Adolfo Lopes de Figueredo 2 ; José Carlos do Nascimento
Quí. Monitor: Rodrigo Pova
 Quí. Professor: Allan Rodrigues Monitor: Rodrigo Pova Exercícios de estudo de calor nas reações químicas????? EXERCÍCIOS DE AULA 1. (Ufg 2014) Leia as informações a seguir. Uma árvore, em um ambiente natural
Quí. Professor: Allan Rodrigues Monitor: Rodrigo Pova Exercícios de estudo de calor nas reações químicas????? EXERCÍCIOS DE AULA 1. (Ufg 2014) Leia as informações a seguir. Uma árvore, em um ambiente natural
ESTUDO DO DESEMPENHO DE CATALISADORES DESTINADOS À PRODUÇÃO DE HIDROGÊNIO A PARTIR DA REFORMA A VAPOR DE METANOL E DIMETIL ÉTER
 ESTUDO DO DESEMPENHO DE CATALISADORES DESTINADOS À PRODUÇÃO DE HIDROGÊNIO A PARTIR DA REFORMA A VAPOR DE METANOL E DIMETIL ÉTER J. L. C. W. Pimenta 1, H. O. Correia 1, R. Menechini Neto, O. A. A. Santos
ESTUDO DO DESEMPENHO DE CATALISADORES DESTINADOS À PRODUÇÃO DE HIDROGÊNIO A PARTIR DA REFORMA A VAPOR DE METANOL E DIMETIL ÉTER J. L. C. W. Pimenta 1, H. O. Correia 1, R. Menechini Neto, O. A. A. Santos
Combustíveis e Redutores ENERGIA PARA METALURGIA
 Combustíveis e Redutores ENERGIA PARA METALURGIA Energia para Metalurgia Principal fonte energética: Carbono Carvão mineral e carvão vegetal C + O 2 >> CO 2 + energia Portanto, carbono é redutor, usado
Combustíveis e Redutores ENERGIA PARA METALURGIA Energia para Metalurgia Principal fonte energética: Carbono Carvão mineral e carvão vegetal C + O 2 >> CO 2 + energia Portanto, carbono é redutor, usado
4 Resultados e Discussão 78. Figura 4.8 DRS-UV-vis para os catalisadores bimetálicos suportados, calcinados a 400 o C por 4 horas.
 4 Resultados e Discussão 78 Figura 4.8 DRS-UV-vis para os catalisadores bimetálicos suportados, calcinados a 400 o C por 4 horas. Pode-se observar, para o catalisador Ni/Al 2 O 3, uma banda próxima a 250
4 Resultados e Discussão 78 Figura 4.8 DRS-UV-vis para os catalisadores bimetálicos suportados, calcinados a 400 o C por 4 horas. Pode-se observar, para o catalisador Ni/Al 2 O 3, uma banda próxima a 250
5 Metodologia e planejamento experimental
 Metodologia experimental 5 Metodologia e planejamento experimental Neste capítulo serão descritos a metodologia e o planejamento experimental utilizados no presente estudo, além da descrição do equipamento
Metodologia experimental 5 Metodologia e planejamento experimental Neste capítulo serão descritos a metodologia e o planejamento experimental utilizados no presente estudo, além da descrição do equipamento
Energia para Metalurgia
 Energia para Metalurgia Energia para Metalurgia Principal fonte energética: Carbono Carvão mineral e carvão vegetal C + O 2 CO 2 + energia Carbono é combustível, usado para gerar energia reagindo com oxigênio
Energia para Metalurgia Energia para Metalurgia Principal fonte energética: Carbono Carvão mineral e carvão vegetal C + O 2 CO 2 + energia Carbono é combustível, usado para gerar energia reagindo com oxigênio
TEMA PARA DOUTORADO 1º SEMESTRE DE 2019
 1 ÁREA DE PESQUISA: Controle Ambiental PROFESSOR: Edson Luiz Silva TÍTULO: Produção de H 2 e CH 4 a partir da co-digestão de vinhaça e caldo de cana em sistema de único e duplo estágio usando reatores
1 ÁREA DE PESQUISA: Controle Ambiental PROFESSOR: Edson Luiz Silva TÍTULO: Produção de H 2 e CH 4 a partir da co-digestão de vinhaça e caldo de cana em sistema de único e duplo estágio usando reatores
ESTUDO DA INFLUÊNCIA DA TEMPERATURA NA OBTENÇÃO DE HIDROXIAPATITA PARA FINS BIOMÉDICOS
 ESTUDO DA INFLUÊNCIA DA TEMPERATURA NA OBTENÇÃO DE HIDROXIAPATITA PARA FINS BIOMÉDICOS T. C. S. PEREIRA 1, G. A. FERNANDES 1 1 Universidade Federal de Itajubá, Instituto de Engenharia Mecânica E-mail para
ESTUDO DA INFLUÊNCIA DA TEMPERATURA NA OBTENÇÃO DE HIDROXIAPATITA PARA FINS BIOMÉDICOS T. C. S. PEREIRA 1, G. A. FERNANDES 1 1 Universidade Federal de Itajubá, Instituto de Engenharia Mecânica E-mail para
SÍNTESE E CARACTERIZAÇÃO DE CATALISADORES V/Cr SUPORTADO EM Nb/Al E AVALIAÇÃO CATALÍTICA NA DECOMPOSIÇÃO DO ISOPROPANOL
 SÍNTESE E CARACTERIZAÇÃO DE CATALISADORES V/Cr SUPORTADO EM E AVALIAÇÃO CATALÍTICA NA DECOMPOSIÇÃO DO ISOPROPANOL M. C. de ALMEIDA MONTEIRO 1, J. A. J. RODRIGUES 2, G. G. CORTEZ 1 1 Departamento de Engenharia
SÍNTESE E CARACTERIZAÇÃO DE CATALISADORES V/Cr SUPORTADO EM E AVALIAÇÃO CATALÍTICA NA DECOMPOSIÇÃO DO ISOPROPANOL M. C. de ALMEIDA MONTEIRO 1, J. A. J. RODRIGUES 2, G. G. CORTEZ 1 1 Departamento de Engenharia
ÓXIDOS APLICADOS A PROCESSOS DE COMBUSTÃO COM CAPTURA DE DIÓXIDO DE CARBONO PARA MITIGAÇÃO DO EFEITO ESTUFA
 1 ÓXIDOS APLICADOS A PROCESSOS DE COMBUSTÃO COM CAPTURA DE DIÓXIDO DE CARBONO PARA MITIGAÇÃO DO EFEITO ESTUFA RELATÓRIO FINAL DE PROJETO DE INICIAÇÃO CIENTÍFICA (PIBIC/CNPq/INPE) Fernanda Galhardo (EEL-USP,
1 ÓXIDOS APLICADOS A PROCESSOS DE COMBUSTÃO COM CAPTURA DE DIÓXIDO DE CARBONO PARA MITIGAÇÃO DO EFEITO ESTUFA RELATÓRIO FINAL DE PROJETO DE INICIAÇÃO CIENTÍFICA (PIBIC/CNPq/INPE) Fernanda Galhardo (EEL-USP,
COMBUSTÍVEIS E REDUTORES
 COMBUSTÍVEIS E REDUTORES Combustíveis e redutores usados em metalugia são as matérias primas responsáveis pelo fornecimento de energia, e pela redução dos minérios oxidados a metal A origem destas matéria
COMBUSTÍVEIS E REDUTORES Combustíveis e redutores usados em metalugia são as matérias primas responsáveis pelo fornecimento de energia, e pela redução dos minérios oxidados a metal A origem destas matéria
SÍNTESE DE BIODIESEL UTILIZANDO ARGILA BENTONÍTICA NATURAL E IMPREGNADA COMO CATALISADOR
 SÍNTESE DE BIODIESEL UTILIZANDO ARGILA BENTONÍTICA NATURAL E IMPREGNADA COMO CATALISADOR J. C. MARINHO 1, P. H. D. FELIX 1, E. G. LIMA, M. W. N. C. CARVALHO e A. A. CUTRIM 1 Universidade Federal de Campina
SÍNTESE DE BIODIESEL UTILIZANDO ARGILA BENTONÍTICA NATURAL E IMPREGNADA COMO CATALISADOR J. C. MARINHO 1, P. H. D. FELIX 1, E. G. LIMA, M. W. N. C. CARVALHO e A. A. CUTRIM 1 Universidade Federal de Campina
SÍNTESE E CARACTERIZAÇÃO DE SÍLICAS MESOPOROSAS COM FERRO E COBALTO ASSOCIADOS
 SÍNTESE E CARACTERIZAÇÃO DE SÍLICAS MESOPOROSAS COM FERRO E COBALTO ASSOCIADOS Aluno: Renan Vieira Bela Orientadora: Maria Isabel Pais Introdução Desde o seu desenvolvimento, em 1998, a sílica mesoporosa
SÍNTESE E CARACTERIZAÇÃO DE SÍLICAS MESOPOROSAS COM FERRO E COBALTO ASSOCIADOS Aluno: Renan Vieira Bela Orientadora: Maria Isabel Pais Introdução Desde o seu desenvolvimento, em 1998, a sílica mesoporosa
PRODUÇÃO DE ETILENO A PARTIR DO ETANOL COM USO DE DIFERENTES ALUMINAS COMERCIAIS COMO CATALISADORES
 PRODUÇÃO DE ETILENO A PARTIR DO ETANOL COM USO DE DIFERENTES ALUMINAS COMERCIAIS COMO CATALISADORES L. T. SILVA 1, T. F. BRAGA 1, F. S. FERRATO 1, K. A. RESENDE 2 e S. C. DANTAS 1 1 Universidade Federal
PRODUÇÃO DE ETILENO A PARTIR DO ETANOL COM USO DE DIFERENTES ALUMINAS COMERCIAIS COMO CATALISADORES L. T. SILVA 1, T. F. BRAGA 1, F. S. FERRATO 1, K. A. RESENDE 2 e S. C. DANTAS 1 1 Universidade Federal
Síntese e caracterização de um complexo de níquel suportado em Vulcan X 72R para utilização em pilhas a combustível
 Química Inorgânica Síntese e caracterização de um complexo de níquel suportado em Vulcan X 72R para utilização em pilhas a combustível ISBN 978-85-85905-10-1 Área Química Inorgânica Autores Santos, R.D.
Química Inorgânica Síntese e caracterização de um complexo de níquel suportado em Vulcan X 72R para utilização em pilhas a combustível ISBN 978-85-85905-10-1 Área Química Inorgânica Autores Santos, R.D.
2 Considerações teóricas
 2 Considerações teóricas Uma breve abordagem termodinâmica e cinética do sistema reacional Cu- Ni/Al 2 O 3, será apresentada neste capitulo. As previsões teóricas do comportamento reacional do sistema
2 Considerações teóricas Uma breve abordagem termodinâmica e cinética do sistema reacional Cu- Ni/Al 2 O 3, será apresentada neste capitulo. As previsões teóricas do comportamento reacional do sistema
5º CONGRESSO BRASILEIRO DE PESQUISA E DESENVOLVIMENTO EM PETRÓLEO E GÁS
 5º CONGRESSO BRASILEIRO DE PESQUISA E DESENVOLVIMENTO EM PETRÓLEO E GÁS TÍTULO DO TRABALHO: Produção de hidrogênio, gás de síntese pelo processo de reforma seca do metano desenvolvido em reator de leito
5º CONGRESSO BRASILEIRO DE PESQUISA E DESENVOLVIMENTO EM PETRÓLEO E GÁS TÍTULO DO TRABALHO: Produção de hidrogênio, gás de síntese pelo processo de reforma seca do metano desenvolvido em reator de leito
NANOESTRUTURAS DE MgO+Cu E ZrO2+Cu PARA O CICLO DA COMBUSTÃO
 NANOESTRUTURAS DE MgO+Cu E ZrO2+Cu PARA O CICLO DA COMBUSTÃO Aluno: Pedro Macena Correia Orientador: Roberto Ribeiro de Avillez Introdução Com o intuito de solucionar o problema de emissão de alguns gases
NANOESTRUTURAS DE MgO+Cu E ZrO2+Cu PARA O CICLO DA COMBUSTÃO Aluno: Pedro Macena Correia Orientador: Roberto Ribeiro de Avillez Introdução Com o intuito de solucionar o problema de emissão de alguns gases
CARACTERIZAÇÃO E ANÁLISE DE CATALISADORES INDUSTRIAIS DE REFORMA A VAPOR DE METANOL E SHIFT
 CARACTERIZAÇÃO E ANÁLISE DE CATALISADORES INDUSTRIAIS DE REFORMA A VAPOR DE METANOL E SHIFT Cláudio Vilas Boas Fávero, Mauricio Pereira Cantão, Luiz Mario de Matos Jorge, Regina Maria Matos Jorge Bolsista
CARACTERIZAÇÃO E ANÁLISE DE CATALISADORES INDUSTRIAIS DE REFORMA A VAPOR DE METANOL E SHIFT Cláudio Vilas Boas Fávero, Mauricio Pereira Cantão, Luiz Mario de Matos Jorge, Regina Maria Matos Jorge Bolsista
6º CONGRESSO BRASILEIRO DE PESQUISA E DESENVOLVIMENTO EM PETRÓLEO E GÁS
 6º CONGRESSO BRASILEIRO DE PESQUISA E DESENVOLVIMENTO EM PETRÓLEO E GÁS TÍTULO DO TRABALHO: Otimização da Reforma a Seco do Gás Natural direcionado a Produção de Nanotubos de Carbono e Consumo de CO 2.
6º CONGRESSO BRASILEIRO DE PESQUISA E DESENVOLVIMENTO EM PETRÓLEO E GÁS TÍTULO DO TRABALHO: Otimização da Reforma a Seco do Gás Natural direcionado a Produção de Nanotubos de Carbono e Consumo de CO 2.
C (grafite) + 2 H 2(g) + ½ O 2(g) CH 3 OH (l) + 238,6 kj. CO 2(g) C (grafite) + O 2(g) 393,5 kj. H 2(g) + ½ O 2(g) H 2 O (l) + 285,8 kj
 Questão 1 (PUC SP) Num calorímetro de gelo, fizeram-se reagir 5,400 g de alumínio (Al) e 16,000 g de óxido férrico, Fe 2 O 3. O calorímetro continha, inicialmente, 8,000 Kg de gelo e 8,000 Kg de água.
Questão 1 (PUC SP) Num calorímetro de gelo, fizeram-se reagir 5,400 g de alumínio (Al) e 16,000 g de óxido férrico, Fe 2 O 3. O calorímetro continha, inicialmente, 8,000 Kg de gelo e 8,000 Kg de água.
Caldeiras Flamotubulares. Não apropriadas para combustíveis sólidos
 Reações Químicas Caldeiras Flamotubulares Não apropriadas para combustíveis sólidos Caldeiras Aquatubulares Ciclo Termodinâmico de Geração de Eletricidade Combustíveis Todo material que pode ser queimado
Reações Químicas Caldeiras Flamotubulares Não apropriadas para combustíveis sólidos Caldeiras Aquatubulares Ciclo Termodinâmico de Geração de Eletricidade Combustíveis Todo material que pode ser queimado
ESTUDO DE REGENERAÇÃO DE CATALISADOR Cu-Co-Al PARA A PRODUÇÃO DE HIDROGÊNIO A PARTIR DO GÁS NATURAL
 ESTUDO DE REGENERAÇÃO DE CATALISADOR Cu-Co-Al PARA A PRODUÇÃO DE HIDROGÊNIO A PARTIR DO GÁS NATURAL F.M. BERNDT 1, O.W. PEREZ LOPEZ 1 1 Universidade Federal do Rio Grande do Sul, Departamento de Engenharia
ESTUDO DE REGENERAÇÃO DE CATALISADOR Cu-Co-Al PARA A PRODUÇÃO DE HIDROGÊNIO A PARTIR DO GÁS NATURAL F.M. BERNDT 1, O.W. PEREZ LOPEZ 1 1 Universidade Federal do Rio Grande do Sul, Departamento de Engenharia
PROMOVE PROCESSOS DE CONVERSÃO
 1.1.Definição: 1. ALQUILAÇÃO CATALÍTICA Molécula Leve Energia Térmica ou catalisadores Molécula com massa molar pesada Catalisadores HF, H 2 SO 4 e AlCl 3. Catalisador HF: usado como referência no processo.
1.1.Definição: 1. ALQUILAÇÃO CATALÍTICA Molécula Leve Energia Térmica ou catalisadores Molécula com massa molar pesada Catalisadores HF, H 2 SO 4 e AlCl 3. Catalisador HF: usado como referência no processo.
6 RESULTADOS E DISCUSSÃO
 6 RESULTADOS E DISCUSSÃO Nesta seção serão apresentados e discutidos os resultados em relação à influência da temperatura e do tempo espacial sobre as características dos pósproduzidos. Os pós de nitreto
6 RESULTADOS E DISCUSSÃO Nesta seção serão apresentados e discutidos os resultados em relação à influência da temperatura e do tempo espacial sobre as características dos pósproduzidos. Os pós de nitreto
Energia para metalurgia
 Energia para metalurgia Consumo energético brasileiro Consumo Energético Brasileiro 2006: 190.000.000 tep/ano Outros 19% Transporte 28% Industrial 41% Residencial 12% Metalurgia 35% da industria e 14,7
Energia para metalurgia Consumo energético brasileiro Consumo Energético Brasileiro 2006: 190.000.000 tep/ano Outros 19% Transporte 28% Industrial 41% Residencial 12% Metalurgia 35% da industria e 14,7
DETERMINAÇÃO DAS CONDIÇÕES IDEAIS DE ATIVAÇÃO DO ÓXIDO DE CÉRIO VISANDO A SUA UTILIZAÇÃO COMO PROMOTOR EM CATALISADORES DE FISCHER-TROPSCH
 DETERMINAÇÃO DAS CONDIÇÕES IDEAIS DE ATIVAÇÃO DO ÓXIDO DE CÉRIO VISANDO A SUA UTILIZAÇÃO COMO PROMOTOR EM CATALISADORES DE FISCHER-TROPSCH Franciele Oliveira Costa (1) ; Bianca Viana de Sousa (2) 1 Universidade
DETERMINAÇÃO DAS CONDIÇÕES IDEAIS DE ATIVAÇÃO DO ÓXIDO DE CÉRIO VISANDO A SUA UTILIZAÇÃO COMO PROMOTOR EM CATALISADORES DE FISCHER-TROPSCH Franciele Oliveira Costa (1) ; Bianca Viana de Sousa (2) 1 Universidade
PARTE III Balanço de massa
 PARTE III Balanço de massa 1. Procedimentos para cálculo de Balanço de Massa i. Escolha como base de cálculo uma quantidade ou vazão de uma das correntes do processo. ii. Desenhe o fluxograma e rotule
PARTE III Balanço de massa 1. Procedimentos para cálculo de Balanço de Massa i. Escolha como base de cálculo uma quantidade ou vazão de uma das correntes do processo. ii. Desenhe o fluxograma e rotule
1/14 PROCESSO DE REFORMA A VAPOR PARA A REDUÇÃO DO TEOR DE ALCATRÃO EM CORRENTES DE GÁS DE SÍNTESE
 1/14 PROCESSO DE REFORMA A VAPOR PARA A REDUÇÃO DO TEOR DE ALCATRÃO EM CORRENTES DE GÁS DE SÍNTESE 1 2 CAMPO DA INVENÇÃO A presente invenção se insere no campo de processos para a redução do teor de alcatrão
1/14 PROCESSO DE REFORMA A VAPOR PARA A REDUÇÃO DO TEOR DE ALCATRÃO EM CORRENTES DE GÁS DE SÍNTESE 1 2 CAMPO DA INVENÇÃO A presente invenção se insere no campo de processos para a redução do teor de alcatrão
Produção de combustíveis sintéticos renováveis a partir de eletricidade, utilizando o conceito ELECTROFUEL
 27 de novembro de 2014 Produção de combustíveis sintéticos renováveis a partir de eletricidade, utilizando o conceito ELECTROFUEL Luís Guerra ; João Gomes ; Jaime Puna ; José Rodrigues Conteúdos Conceito
27 de novembro de 2014 Produção de combustíveis sintéticos renováveis a partir de eletricidade, utilizando o conceito ELECTROFUEL Luís Guerra ; João Gomes ; Jaime Puna ; José Rodrigues Conteúdos Conceito
Cinética e Eq. Químico Folha 10 João Roberto Fortes Mazzei
 01. Em um recipiente de 500 ml, encontram-se, em condições de equilíbrio, 10 mol/l de H 2 (g) e 0,01 mol/l de I 2 (g). Qual é a concentração do HI(g), sabendo-se que, nas condições do experimento, a constante
01. Em um recipiente de 500 ml, encontram-se, em condições de equilíbrio, 10 mol/l de H 2 (g) e 0,01 mol/l de I 2 (g). Qual é a concentração do HI(g), sabendo-se que, nas condições do experimento, a constante
Síntese e Caracterização dos espinéliosal 2 CuO 4 e Al 2 MnO 4
 Síntese e Caracterização dos espinéliosal 2 CuO 4 e Al 2 MnO 4 Aluna: Pâmela Fernandes de Oliveira Orientador: Eduardo Brocchi Co-orientador: Rogério Navarro Correia de Siqueira 1. Introdução Materiais
Síntese e Caracterização dos espinéliosal 2 CuO 4 e Al 2 MnO 4 Aluna: Pâmela Fernandes de Oliveira Orientador: Eduardo Brocchi Co-orientador: Rogério Navarro Correia de Siqueira 1. Introdução Materiais
COMPARAÇÃO DA ESTRUTURA E REATIVIDADE DE CHARS OBTIDOS EM FORNO DTF E SIMULADOR DA ZONA DE COMBUSTÃO DO ALTO-FORNO
 COMPARAÇÃO DA ESTRUTURA E REATIVIDADE DE CHARS OBTIDOS EM FORNO DTF E SIMULADOR DA ZONA DE COMBUSTÃO DO ALTO-FORNO André da S. Machado, Juliana G. Pohlmann Antônio C. F. Vilela & Eduardo Osório Sumário
COMPARAÇÃO DA ESTRUTURA E REATIVIDADE DE CHARS OBTIDOS EM FORNO DTF E SIMULADOR DA ZONA DE COMBUSTÃO DO ALTO-FORNO André da S. Machado, Juliana G. Pohlmann Antônio C. F. Vilela & Eduardo Osório Sumário
PRODUÇÃO DE HIDROGÊNIO A PARTIR DA REFORMA DO ETANOL
 PROCEL PRODUÇÃO DE HIDROGÊNIO A PARTIR DA REFORMA DO ETANOL VANDERLEI SÉRGIO BERGAMASCHI E-mail: vsberga@ipen ipen.br PROCEL / IPEN-SP OUTUBRO / 2003 COMBUSTÍVEL PETRÓLEO: VANTAGENS: -LÍQUIDO DE FÁCIL
PROCEL PRODUÇÃO DE HIDROGÊNIO A PARTIR DA REFORMA DO ETANOL VANDERLEI SÉRGIO BERGAMASCHI E-mail: vsberga@ipen ipen.br PROCEL / IPEN-SP OUTUBRO / 2003 COMBUSTÍVEL PETRÓLEO: VANTAGENS: -LÍQUIDO DE FÁCIL
Reforma a vapor de biogás usando catalisadores de óxidos mistos Ni-Mg-Al obtidos a partir de hidrotalcitas
 Processos Químicos Reforma a vapor de biogás usando catalisadores de óxidos mistos Ni-Mg-Al obtidos a partir de hidrotalcitas Itânia Pinheiro Soares 1, Felippe Heimer Correia 2, Isabela C. Curado 3, Emerson
Processos Químicos Reforma a vapor de biogás usando catalisadores de óxidos mistos Ni-Mg-Al obtidos a partir de hidrotalcitas Itânia Pinheiro Soares 1, Felippe Heimer Correia 2, Isabela C. Curado 3, Emerson
Curso Engenharia de Energia
 UNIVERSIDADE FEDERAL DA GRANDE DOURADOS - UFGD FACULDADE DE ENGENHARIA Curso Engenharia de Energia Prof. Dr. Omar Seye omarseye@ufgd.edu.br Disciplina: COMBUSTÃO E COMBUSTÍVEIS A queima direta, ou combustão,
UNIVERSIDADE FEDERAL DA GRANDE DOURADOS - UFGD FACULDADE DE ENGENHARIA Curso Engenharia de Energia Prof. Dr. Omar Seye omarseye@ufgd.edu.br Disciplina: COMBUSTÃO E COMBUSTÍVEIS A queima direta, ou combustão,
EXERCÍCIOS DE REVISÃO P/ Avaliação 01/06
 Tema do Ano: Eu e o outro construindo um mundo mais solidário Projeto Interdisciplinar da 2 a Série do Ensino Médio: Segunda metade do século XX e início do século XXI: movimentos, conflitos e desenvolvimento.
Tema do Ano: Eu e o outro construindo um mundo mais solidário Projeto Interdisciplinar da 2 a Série do Ensino Médio: Segunda metade do século XX e início do século XXI: movimentos, conflitos e desenvolvimento.
Estudo do potencial catalítico do espinélio CoFe2O4 na oxidação de matéria orgânica oriunda da pirólise da madeira
 Estudo do potencial catalítico do espinélio CoFe2O4 na oxidação de matéria orgânica oriunda da pirólise da madeira 1. Introdução Aluno: Felipe Rozenberg Orientador: Rogério N. C. de Siqueira A biomassa
Estudo do potencial catalítico do espinélio CoFe2O4 na oxidação de matéria orgânica oriunda da pirólise da madeira 1. Introdução Aluno: Felipe Rozenberg Orientador: Rogério N. C. de Siqueira A biomassa
QUÍMICA PRIMEIRA ETAPA
 QUÍMICA PRIMEIRA ETAPA - 1998 QUESTÃO 01 Uma mistura de hidrogênio, H 2 (g), e oxigênio, O 2 (g), reage, num recipiente hermeticamente fechado, em alta temperatura e em presença de um catalisador, produzindo
QUÍMICA PRIMEIRA ETAPA - 1998 QUESTÃO 01 Uma mistura de hidrogênio, H 2 (g), e oxigênio, O 2 (g), reage, num recipiente hermeticamente fechado, em alta temperatura e em presença de um catalisador, produzindo
COLÉGIO DA POLÍCIA MILITAR
 COLÉGIO DA POLÍCIA MILITAR ASSESSORIA TÉCNICA Processo Avaliativo Recuperação - 3º Bimestre/2015 Disciplina: QUÍMICA 3ª série EM A/B Nome do aluno Nº Turma A Recuperação deve ser entregue no dia 08/09/2015.
COLÉGIO DA POLÍCIA MILITAR ASSESSORIA TÉCNICA Processo Avaliativo Recuperação - 3º Bimestre/2015 Disciplina: QUÍMICA 3ª série EM A/B Nome do aluno Nº Turma A Recuperação deve ser entregue no dia 08/09/2015.
Exercícios de Revisão - 2
 Exercícios de Revisão - 2 1. Na tentativa de explicar a origem dos seres vivos, Müller reproduziu, em seu experimento, as condições atmosféricas primitivas, que continham os gases metano (CH4); amônia
Exercícios de Revisão - 2 1. Na tentativa de explicar a origem dos seres vivos, Müller reproduziu, em seu experimento, as condições atmosféricas primitivas, que continham os gases metano (CH4); amônia
SOLDAGEM. Engenharia Mecânica Prof. Luis Fernando Maffeis Martins
 08 SOLDAGEM Engenharia Mecânica Prof. Luis Fernando Maffeis Martins Solda oxi-acetileno Solda oxi-acetileno Combustão: É a reação exotérmica entre uma substância (combustível) e um gás (corburente), geralmente
08 SOLDAGEM Engenharia Mecânica Prof. Luis Fernando Maffeis Martins Solda oxi-acetileno Solda oxi-acetileno Combustão: É a reação exotérmica entre uma substância (combustível) e um gás (corburente), geralmente
Estudos de Calor Nas Reações Químicas
 studos de Calor Nas Reações s 1. Leia as informações a seguir: Uma árvore, em um ambiente natural a 0 C, apresentando 10 5 folhas com área média de 0,5 dm por folha, está perdendo água para a atmosfera
studos de Calor Nas Reações s 1. Leia as informações a seguir: Uma árvore, em um ambiente natural a 0 C, apresentando 10 5 folhas com área média de 0,5 dm por folha, está perdendo água para a atmosfera
X X. Calor ou Luz. Calor R O O R. Exemplo 1: Peróxidos. Exemplo 2: Halogênios. Universidade Federal Rural do Semi Árido UFERSA. 1. Reações de Alcanos
 1. Reações de Alcanos Os alcanos são caracterizados por apresentar pouca reatividade a muitos reagentes químicos. As ligações carbono carbono e hidrogênio hidrogênio são bastante fortes; elas não quebram,
1. Reações de Alcanos Os alcanos são caracterizados por apresentar pouca reatividade a muitos reagentes químicos. As ligações carbono carbono e hidrogênio hidrogênio são bastante fortes; elas não quebram,
Programa de Retomada de Conteúdo 2º bimestre 2º ano Química
 Educação Infantil, Ensino Fundamental e Ensino Médio Regular, Rua Cantagalo, 339 Tatuapé Fones: 2293-9393 e 2293-9166 Diretoria de Ensino Região LESTE 5 Programa de Retomada de Conteúdo 2º bimestre 2º
Educação Infantil, Ensino Fundamental e Ensino Médio Regular, Rua Cantagalo, 339 Tatuapé Fones: 2293-9393 e 2293-9166 Diretoria de Ensino Região LESTE 5 Programa de Retomada de Conteúdo 2º bimestre 2º
Temas de Dissertação. Programa de Pós-graduação em Engenharia Química da Universidade Federal Fluminense. Lisiane Veiga Mattos
 Temas de Dissertação Programa de Pós-graduação em Engenharia Química da Universidade Federal Fluminense Lisiane Veiga Mattos Temas de Dissertação 1) Produção de hidrogênio para células a combustível do
Temas de Dissertação Programa de Pós-graduação em Engenharia Química da Universidade Federal Fluminense Lisiane Veiga Mattos Temas de Dissertação 1) Produção de hidrogênio para células a combustível do
PEROVSKITAS A BASE DE NÍQUEL E NIÓBIO COMO CATALISADORES PARA REFORMA A VAPOR DE METANO
 PEROVSKITAS A BASE DE NÍQUEL E NIÓBIO COMO CATALISADORES PARA REFORMA A VAPOR DE METANO JULIANA F. GONÇALVES 1, MARIANA M.V.M. SOUZA 1 1 Escola de Química, Universidade Federal do Rio de Janeiro E-mail
PEROVSKITAS A BASE DE NÍQUEL E NIÓBIO COMO CATALISADORES PARA REFORMA A VAPOR DE METANO JULIANA F. GONÇALVES 1, MARIANA M.V.M. SOUZA 1 1 Escola de Química, Universidade Federal do Rio de Janeiro E-mail
Energia para Siderurgia
 Energia para Siderurgia Principal fonte energética: Carbono Carvão mineral e carvão vegetal C + O 2 >> CO 2 + energia Portanto, carbono é redutor, usado para reagir com o oxigênio do minério de ferro Carbono
Energia para Siderurgia Principal fonte energética: Carbono Carvão mineral e carvão vegetal C + O 2 >> CO 2 + energia Portanto, carbono é redutor, usado para reagir com o oxigênio do minério de ferro Carbono
AVALIAÇÃO DA TÉCNICA DO USO DO ÓXIDO DE FERRO PARA REMOÇÃO DE SULFETO DE HIDROGÊNIO DO BIOGAS
 Universidade Federal de Santa Catarina Departamento de Engenharia Sanitária e Ambiental Programa de Pós-Graduação em Engenharia Ambiental AVALIAÇÃO DA TÉCNICA DO USO DO ÓXIDO DE FERRO PARA REMOÇÃO DE SULFETO
Universidade Federal de Santa Catarina Departamento de Engenharia Sanitária e Ambiental Programa de Pós-Graduação em Engenharia Ambiental AVALIAÇÃO DA TÉCNICA DO USO DO ÓXIDO DE FERRO PARA REMOÇÃO DE SULFETO
SÍNTESE E CARACTERIZAÇÃO DO COBALTATO DE CÉRIO ATRAVÉS DO MÉTODO DE COMBUSTÃO
 1 SÍNTESE E CARACTERIZAÇÃO DO COBALTATO DE CÉRIO ATRAVÉS DO MÉTODO DE COMBUSTÃO (A.C. Chaves*) (L. L. M. SALES), (D. M. A. Melo), (A.G de Souza), UFRN/CCET/DQ/LATMat Cidade Universitária/Natal/RN CEP 59078-970.
1 SÍNTESE E CARACTERIZAÇÃO DO COBALTATO DE CÉRIO ATRAVÉS DO MÉTODO DE COMBUSTÃO (A.C. Chaves*) (L. L. M. SALES), (D. M. A. Melo), (A.G de Souza), UFRN/CCET/DQ/LATMat Cidade Universitária/Natal/RN CEP 59078-970.
Pb 2e Pb E 0,13 v. Ag 2e Ag E +0,80 v. Zn 2e Zn E 0,76 v. Al 3e Al E 1,06 v. Mg 2e Mg E 2,4 v. Cu 2e Cu E +0,34 v
 QUÍMICA 1ª QUESTÃO Umas das reações possíveis para obtenção do anidrido sulfúrico é a oxidação do anidrido sulfuroso por um agente oxidante forte em meio aquoso ácido, como segue a reação. Anidrido sulfuroso
QUÍMICA 1ª QUESTÃO Umas das reações possíveis para obtenção do anidrido sulfúrico é a oxidação do anidrido sulfuroso por um agente oxidante forte em meio aquoso ácido, como segue a reação. Anidrido sulfuroso
Célula de Combustível
 Modelagem Matemática de Células de Combustível Alcalinas Elise Meister Sommer Engenheira Química Bolsista Msc PRH4 ANP Orientador: Prof. José Viriato Coelho Vargas, PhD PGMEC Pós Graduação em Engenharia
Modelagem Matemática de Células de Combustível Alcalinas Elise Meister Sommer Engenheira Química Bolsista Msc PRH4 ANP Orientador: Prof. José Viriato Coelho Vargas, PhD PGMEC Pós Graduação em Engenharia
Vestibular UFSC 2005 (Branca) Química
 Química Geral da Equipe de Química do Curso Energia (Professores Miron, Callegaro, Romero e Pedro Marcos) A CCCV da UFSC está de parabéns pela elaboração das questões da prova de Química, dando prioridade
Química Geral da Equipe de Química do Curso Energia (Professores Miron, Callegaro, Romero e Pedro Marcos) A CCCV da UFSC está de parabéns pela elaboração das questões da prova de Química, dando prioridade
MOTORES TÉRMICOS AULA MISTURAS REAGENTES E COMBUSTÃO
 MOTORES TÉRMICOS AULA 13-17 MISTURAS REAGENTES E COMBUSTÃO PROF.: KAIO DUTRA Nas reações de combustão, a rápida oxidação dos elementos combustíveis do combustível resulta em uma liberação de energia à
MOTORES TÉRMICOS AULA 13-17 MISTURAS REAGENTES E COMBUSTÃO PROF.: KAIO DUTRA Nas reações de combustão, a rápida oxidação dos elementos combustíveis do combustível resulta em uma liberação de energia à
Curso Engenharia de Energia
 UNIVERSIDADE FEDERAL DA GRANDE DOURADOS - UFGD FACULDADE DE ENGENHARIA Curso Engenharia de Energia Prof. Dr. Omar Seye omarseye@ufgd.edu.br Disciplina: COMBUSTÃO E COMBUSTÍVEIS A analise energética é fundamental
UNIVERSIDADE FEDERAL DA GRANDE DOURADOS - UFGD FACULDADE DE ENGENHARIA Curso Engenharia de Energia Prof. Dr. Omar Seye omarseye@ufgd.edu.br Disciplina: COMBUSTÃO E COMBUSTÍVEIS A analise energética é fundamental
ATIVIDADE AVALIATIVA
 ATIVIDADE AVALIATIVA Valor: 2,0 Tempo para responder: 20min Sabendo que o clima não é algo estático, mas sim, um complexo e intrincado sistema de infinitas variáveis agindo simultaneamente e considerando
ATIVIDADE AVALIATIVA Valor: 2,0 Tempo para responder: 20min Sabendo que o clima não é algo estático, mas sim, um complexo e intrincado sistema de infinitas variáveis agindo simultaneamente e considerando
Giane Gonçalves*, Fernando Quilice Martinelli, Creusa Maieru Macedo Costa, Luiz Mario de Matos Jorge e Onélia Aparecida Andreo dos Santos
 Catalisadores sol-gel de Ni-SiO 2 e Ni-Al 2 O 3 aplicados na reforma de metano com CO 2 Giane Gonçalves*, Fernando Quilice Martinelli, Creusa Maieru Macedo Costa, Luiz Mario de Matos Jorge e Onélia Aparecida
Catalisadores sol-gel de Ni-SiO 2 e Ni-Al 2 O 3 aplicados na reforma de metano com CO 2 Giane Gonçalves*, Fernando Quilice Martinelli, Creusa Maieru Macedo Costa, Luiz Mario de Matos Jorge e Onélia Aparecida
4 METODOLOGIA EXPERIMENTAL
 4 METODOLOGIA EXPERIMENTAL A descrição dos procedimentos de laboratório e da linha experimental e métodos de análise serão apresentados neste capítulo, correlacionando os fundamentos teóricos com as soluções
4 METODOLOGIA EXPERIMENTAL A descrição dos procedimentos de laboratório e da linha experimental e métodos de análise serão apresentados neste capítulo, correlacionando os fundamentos teóricos com as soluções
Universidade Estadual de Maringá / Centro de Tecnologia /Maringá, PR. Centro de Tecnologia/Departamento de Engenharia de Alimentos
 DESENVOLVIMENTO DE MÉTODOS VERDES PARA IMPREGNAÇÃO DE NANOPARTÍCULAS EM FILTROS DE CARVÃO PARA TRATAMENTO DE ÁGUA Lucas Yaegashi Campana (PIC/UEM), Raquel Guttierres Gomes (Orientadora), Carole Silveira
DESENVOLVIMENTO DE MÉTODOS VERDES PARA IMPREGNAÇÃO DE NANOPARTÍCULAS EM FILTROS DE CARVÃO PARA TRATAMENTO DE ÁGUA Lucas Yaegashi Campana (PIC/UEM), Raquel Guttierres Gomes (Orientadora), Carole Silveira
Processos de Redução Direta de Minério de Ferro
 Processos de Redução Direta de Minério de Ferro Características do processo em Alto-Forno alta escala de produção ( maior que 1.5 Mt/ano) necessidade de aglomeração do minério necessidade de coque metalúrgico
Processos de Redução Direta de Minério de Ferro Características do processo em Alto-Forno alta escala de produção ( maior que 1.5 Mt/ano) necessidade de aglomeração do minério necessidade de coque metalúrgico
OXIDAÇÃO PARCIAL DO METANO EM CATALISADORES DE NiAl 2 O 4 e NiAl 2 O 4 /Al 2 O 3.
 OXIDAÇÃO PARCIAL DO METANO EM CATALISADORES DE e. D. F.P. SUFFREDINI 1,2, R. S. GOMES 3, L. M. S. RODRIGUES 3 e S. T. BRANDÃO 2 1 Instituto Federal da Bahia, Departamento de Processos Industriais e Engenharia
OXIDAÇÃO PARCIAL DO METANO EM CATALISADORES DE e. D. F.P. SUFFREDINI 1,2, R. S. GOMES 3, L. M. S. RODRIGUES 3 e S. T. BRANDÃO 2 1 Instituto Federal da Bahia, Departamento de Processos Industriais e Engenharia
PROVA DE QUÍMICA. Tendo em vista as propriedades coligativas dessas soluções, é CORRETO afirmar
 17 PROVA DE QUÍMICA Q U E S T Ã O 2 6 Z e X são elementos químicos que apresentam respectivamente 2 e 6 elétrons no nível de valência. A fórmula química resultante da combinação entre átomos dos elementos
17 PROVA DE QUÍMICA Q U E S T Ã O 2 6 Z e X são elementos químicos que apresentam respectivamente 2 e 6 elétrons no nível de valência. A fórmula química resultante da combinação entre átomos dos elementos
UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA EEL-USP MARCELO LEME DO PRADO
 UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA EEL-USP MARCELO LEME DO PRADO ÓXIDO DE NÍQUEL APLICADO A PROCESSOS DE COMBUSTÃO COM CAPTURA DE DIÓXIDO DE CARBONO PARA MITIGAÇÃO DO EFEITO ESTUFA.
UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA EEL-USP MARCELO LEME DO PRADO ÓXIDO DE NÍQUEL APLICADO A PROCESSOS DE COMBUSTÃO COM CAPTURA DE DIÓXIDO DE CARBONO PARA MITIGAÇÃO DO EFEITO ESTUFA.
Fuvest 2009 (Questão 1 a 8)
 (Questão 1 a 8) 1. Água pode ser eletrolisada com a finalidade de se demonstrar sua composição. A figura representa uma aparelhagem em que foi feita a eletrólise da água, usando eletrodos inertes de platina.
(Questão 1 a 8) 1. Água pode ser eletrolisada com a finalidade de se demonstrar sua composição. A figura representa uma aparelhagem em que foi feita a eletrólise da água, usando eletrodos inertes de platina.
AVALIAÇÃO DO COMPORTAMENTO DE CARVÕES BRASILEIROS SUBMETIDOS À COMBUSTÃO ENRIQUECIDA COM OXIGÊNIO
 AVALIAÇÃO DO COMPORTAMENTO DE CARVÕES BRASILEIROS SUBMETIDOS À COMBUSTÃO ENRIQUECIDA COM OXIGÊNIO Amir De Toni Jr., Cristiano Maidana, Leonardo Zimmer, Marina Seelig e Paulo Smith Schneider INTRODUÇÃO
AVALIAÇÃO DO COMPORTAMENTO DE CARVÕES BRASILEIROS SUBMETIDOS À COMBUSTÃO ENRIQUECIDA COM OXIGÊNIO Amir De Toni Jr., Cristiano Maidana, Leonardo Zimmer, Marina Seelig e Paulo Smith Schneider INTRODUÇÃO
QUÍMICA Tabela Algumas propriedades dos elementos químicos do grupo 16
 QUESTÕES de 01 a 06-2012 UFBA UFBA - 2ª - 2ª FASE 2012 Questão 01 Tabela Algumas propriedades dos elementos químicos do grupo 16 A tabela periódica é a mais importante ferramenta que os químicos criaram
QUESTÕES de 01 a 06-2012 UFBA UFBA - 2ª - 2ª FASE 2012 Questão 01 Tabela Algumas propriedades dos elementos químicos do grupo 16 A tabela periódica é a mais importante ferramenta que os químicos criaram
Inicialmente a oxidação do metano em altas temperaturas pode ser realizada através da reação: CH 4 + O2 = CH 3 + HO 2 Ou por: CH 4 + M = CH 3 + H + M
 1 1. Introdução O aumento da produção mundial de aço aliada à crescente preocupação com questões ambientais, tem exigido do setor siderúrgico a melhoria dos processos já existentes e o desenvolvimento
1 1. Introdução O aumento da produção mundial de aço aliada à crescente preocupação com questões ambientais, tem exigido do setor siderúrgico a melhoria dos processos já existentes e o desenvolvimento
CARACTERIZAÇÃO DE CATALISADORES, A BASE DE TITÂNIA, PROMOVIDOS COM PRATA, NA FOTODEGRADAÇÃO CATALÍTICA DE EFLUENTES TÊXTEIS
 CARACTERIZAÇÃO DE CATALISADORES, A BASE DE TITÂNIA, PROMOVIDOS COM PRATA, NA FOTODEGRADAÇÃO CATALÍTICA DE EFLUENTES TÊXTEIS 1 Renata Yuri Dias Tsujioka, 2 Onélia A. Andreo 1 Discente do curso de Engenharia
CARACTERIZAÇÃO DE CATALISADORES, A BASE DE TITÂNIA, PROMOVIDOS COM PRATA, NA FOTODEGRADAÇÃO CATALÍTICA DE EFLUENTES TÊXTEIS 1 Renata Yuri Dias Tsujioka, 2 Onélia A. Andreo 1 Discente do curso de Engenharia
SÍNTESE DO CATALISADOR Ni 0,5 Zn 0,5 Fe 2 O 4 POR REAÇÃO DE COMBUSTÃO E DESEMPENHO PARA OBTENÇÃO DE BIODIESEL, COM DIFERENTES TIPOS DE ÓLEOS.
 SÍNTESE DO CATALISADOR Ni 0,5 Zn 0,5 Fe 2 O 4 POR REAÇÃO DE COMBUSTÃO E DESEMPENHO PARA OBTENÇÃO DE BIODIESEL, COM DIFERENTES TIPOS DE ÓLEOS. Ana Beatriz de Sousa Barros 1, Thales Filipe Barbosa de Moura
SÍNTESE DO CATALISADOR Ni 0,5 Zn 0,5 Fe 2 O 4 POR REAÇÃO DE COMBUSTÃO E DESEMPENHO PARA OBTENÇÃO DE BIODIESEL, COM DIFERENTES TIPOS DE ÓLEOS. Ana Beatriz de Sousa Barros 1, Thales Filipe Barbosa de Moura
Lista de Exercícios. Data limite para entrega da lista: 14/09/2018
 Lista de Exercícios Nome: n.º Santos, de de 2018. Série: 2.ª Turmas: A, B, C Ensino: Médio Prof. Paulo Henrique (PH) Bimestre: 3.º Data limite para entrega da lista: 14/09/2018 Valor: 4,0(quatro) 1) Por
Lista de Exercícios Nome: n.º Santos, de de 2018. Série: 2.ª Turmas: A, B, C Ensino: Médio Prof. Paulo Henrique (PH) Bimestre: 3.º Data limite para entrega da lista: 14/09/2018 Valor: 4,0(quatro) 1) Por
ANÁLISE TÉRMICA Sumário
 ANÁLISE TÉRMICA Sumário 1- Conceito 2- Tipos de métodos térmicos Princípios gerais de cada método Instrumentação Aplicações Conceito Análise Térmica é um termo que abrange um grupo de técnicas nas quais
ANÁLISE TÉRMICA Sumário 1- Conceito 2- Tipos de métodos térmicos Princípios gerais de cada método Instrumentação Aplicações Conceito Análise Térmica é um termo que abrange um grupo de técnicas nas quais
TAREFA DA SEMANA DE 24 a 28 DE FEVEREIRO
 TAREFA DA SEMANA DE 4 a 8 DE FEVEREIRO QUÍMICA 3ª SÉRIE. (Upe) Um dos contaminantes do petróleo e do gás natural brutos é o H S. O gás sulfídrico é originário de processos geológicos, baseados em diversos
TAREFA DA SEMANA DE 4 a 8 DE FEVEREIRO QUÍMICA 3ª SÉRIE. (Upe) Um dos contaminantes do petróleo e do gás natural brutos é o H S. O gás sulfídrico é originário de processos geológicos, baseados em diversos
Química. Questão 17 A gasolina é uma mistura de hidrocarbonetos diversos que apresenta, dentre outros, os seguintes componentes:
 Questão 16 Uma molécula de água, isolada, não apresenta certas propriedades físicas - como ponto de fusão e de ebulição - que dependem de interações entre moléculas. Em 1998, um grupo de pesquisadores
Questão 16 Uma molécula de água, isolada, não apresenta certas propriedades físicas - como ponto de fusão e de ebulição - que dependem de interações entre moléculas. Em 1998, um grupo de pesquisadores
Processos Pré-Extrativos
 Universidade Federal do Pará Instituto de Tecnologia Tecnologia Metalúrgica Prof. Dr. Jorge Teófilo de Barros Lopes Campus de Belém Curso de Engenharia Mecânica 24/05/2018 08:16 TECNOLOGIA METALÚRGICA
Universidade Federal do Pará Instituto de Tecnologia Tecnologia Metalúrgica Prof. Dr. Jorge Teófilo de Barros Lopes Campus de Belém Curso de Engenharia Mecânica 24/05/2018 08:16 TECNOLOGIA METALÚRGICA
QUESTÃO 46 QUESTÃO 47 QUESTÃO 48 QUESTÃO 49 PROVA DE QUÍMICA I
 17 PROVA DE QUÍMICA I QUESTÃO 46 O alumínio metálico, obtido na indústria à alta temperatura na forma líquida, reage com vapor d`água da atmosfera, produzindo óxido de alumínio e gás hidrogênio, conforme
17 PROVA DE QUÍMICA I QUESTÃO 46 O alumínio metálico, obtido na indústria à alta temperatura na forma líquida, reage com vapor d`água da atmosfera, produzindo óxido de alumínio e gás hidrogênio, conforme
1º BIMESTRE. Série Turma (s) Turno 3º A B C D E F G H MATUTINO Disciplina: QUÍMICA Professor: CHARLYS FERNANDES Data: / / 2017 Aluno (a): Nº
 1º BIMESTRE Visto do Professor Nota (Fuvest) A uma determinada temperatura, as substâncias HI, H2 e I2 estão no estado gasoso. A essa temperatura, o equilíbrio entre as três substâncias foi estudado, em
1º BIMESTRE Visto do Professor Nota (Fuvest) A uma determinada temperatura, as substâncias HI, H2 e I2 estão no estado gasoso. A essa temperatura, o equilíbrio entre as três substâncias foi estudado, em
AVALIAÇÃO DO COMPORTAMENTO DA ADIÇÃO DE VANÁDIO E POTÁSSIO SOBRE ALUMINA DE TRANSIÇÃO
 AVALIAÇÃO DO COMPORTAMENTO DA ADIÇÃO DE VANÁDIO E POTÁSSIO SOBRE ALUMINA DE TRANSIÇÃO M. S. P. MARTINS 1, J. A. J. RODRIGUES 2 e G. G. CORTEZ 1 1 Escola de Engenharia de Lorena - USP Departamento de Engenharia
AVALIAÇÃO DO COMPORTAMENTO DA ADIÇÃO DE VANÁDIO E POTÁSSIO SOBRE ALUMINA DE TRANSIÇÃO M. S. P. MARTINS 1, J. A. J. RODRIGUES 2 e G. G. CORTEZ 1 1 Escola de Engenharia de Lorena - USP Departamento de Engenharia
Olimpíada Brasileira de Química Fase III (Etapa 1 nacional)
 Page 1 of 5 Olimpíada Brasileira de Química - 2001 Fase III (Etapa 1 nacional) Questão 1 (48 th Chemistry Olympiad - Final National Competition - 2001 - Estonia) Exame aplicado em 01.09.2001 Os compostos
Page 1 of 5 Olimpíada Brasileira de Química - 2001 Fase III (Etapa 1 nacional) Questão 1 (48 th Chemistry Olympiad - Final National Competition - 2001 - Estonia) Exame aplicado em 01.09.2001 Os compostos
FUVEST Segunda Fase. Química 06/01/2003
 FUVEST 2003 Segunda Fase Química 06/01/2003 Q.01 Em 1861, o pesquisador Kekulé e o professor secundário Loschmidt apresentaram, em seus escritos, as seguintes fórmulas estruturais para o ácido acético
FUVEST 2003 Segunda Fase Química 06/01/2003 Q.01 Em 1861, o pesquisador Kekulé e o professor secundário Loschmidt apresentaram, em seus escritos, as seguintes fórmulas estruturais para o ácido acético
Fisico-Química da Redução de Óxidos de Ferro
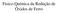 Fisico-Química da Redução de Óxidos de Ferro Análise Termodinâmica da Redução de Óxidos Metálicos Seja a reação de formação de um óxido a partir do metal Me e de oxigênio puro: 2 Me (s,l) + O 2(g) = 2
Fisico-Química da Redução de Óxidos de Ferro Análise Termodinâmica da Redução de Óxidos Metálicos Seja a reação de formação de um óxido a partir do metal Me e de oxigênio puro: 2 Me (s,l) + O 2(g) = 2
02)Numa reação endotérmica, há [1] de calor, a entalpia final (produtos) é [2] que a entalpia inicial (reagentes) e a
![02)Numa reação endotérmica, há [1] de calor, a entalpia final (produtos) é [2] que a entalpia inicial (reagentes) e a 02)Numa reação endotérmica, há [1] de calor, a entalpia final (produtos) é [2] que a entalpia inicial (reagentes) e a](/thumbs/48/23999624.jpg) 01)Numa reação exotérmica, há [1] de calor, a entalpia final (produtos) é [2] que a entalpia inicial (reagentes) e a variação de entalpia é [3] que zero. Completa-se corretamente essa frase substituindo-se
01)Numa reação exotérmica, há [1] de calor, a entalpia final (produtos) é [2] que a entalpia inicial (reagentes) e a variação de entalpia é [3] que zero. Completa-se corretamente essa frase substituindo-se
QUÍMICA. 16. Os elementos químicos A, B e C apresentam para seu átomo, no estado fundamental, a seguinte configuração eletrônica:
 QUÍMICA 16. Os elementos químicos A, B e C apresentam para seu átomo, no estado fundamental, a seguinte configuração eletrônica: A 1s 2 2s 2 2p 6 3s 2 3p 5 B 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 5 C 1s 2 2s
QUÍMICA 16. Os elementos químicos A, B e C apresentam para seu átomo, no estado fundamental, a seguinte configuração eletrônica: A 1s 2 2s 2 2p 6 3s 2 3p 5 B 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 5 C 1s 2 2s
CAPÍTULO 3. Materiais e Métodos
 CAPÍTUL Materiais e Métodos Neste capítulo encontram-se especificados os procedimentos experimentais empregados na preparação dos catalisadores, nos experimentos de caracterização das amostras e nos testes
CAPÍTUL Materiais e Métodos Neste capítulo encontram-se especificados os procedimentos experimentais empregados na preparação dos catalisadores, nos experimentos de caracterização das amostras e nos testes
Exercício. Questão 48 Engenheiro de Processamento Petrobras 02/2010
 Operações Unitárias Apresentação Grandezas Físicas Questão 48 Engenheiro de Processamento Petrobras 02/2010 O número de cavitação (Ca) é um número adimensional empregado na investigação da cavitação em
Operações Unitárias Apresentação Grandezas Físicas Questão 48 Engenheiro de Processamento Petrobras 02/2010 O número de cavitação (Ca) é um número adimensional empregado na investigação da cavitação em
Universidade Federal do Rio Grande do Sul Escola de Engenharia Departamento de Engenharia Química. Porto Alegre, Abril de 2010.
 Universidade Federal do Rio Grande do Sul Escola de Engenharia Departamento de Engenharia Química Captura de CO 2 através de Processos de Separação com Membranas Isabel Cristina Tessaro Porto Alegre, Abril
Universidade Federal do Rio Grande do Sul Escola de Engenharia Departamento de Engenharia Química Captura de CO 2 através de Processos de Separação com Membranas Isabel Cristina Tessaro Porto Alegre, Abril
2º trimestre Sala de Estudo Química Data: 08/05/17 Ensino Médio 2º ano classe: A_B_C Profª Danusa Nome: nº
 2º trimestre Sala de Estudo Química Data: 08/05/17 Ensino Médio 2º ano classe: A_B_C Profª Danusa Nome: nº Conteúdo: Termoquímica (entalpia padrão de formação) Questão 01 - (PUC RS/2017) O metano é uma
2º trimestre Sala de Estudo Química Data: 08/05/17 Ensino Médio 2º ano classe: A_B_C Profª Danusa Nome: nº Conteúdo: Termoquímica (entalpia padrão de formação) Questão 01 - (PUC RS/2017) O metano é uma
1 a Questão: Valor : 1,0 FOLHA DE DADOS. I ) Entalpias de Formação (H o f ) H 2. O (líquida) = - 68,3 kcal / mol. CO 2 (gasoso) = - 94,1 kcal / mol
 PROVA DE QUÍMICA DO VESTIBULAR 96/97 DO INSTITUTO MILITAR DE ENGENHARIA (04/12/96) FOLHA DE DADOS I ) Entalpias de Formação (H o f ) H 2 O (líquida) = - 68,3 kcal / mol CO 2 (gasoso) = - 94,1 kcal / mol
PROVA DE QUÍMICA DO VESTIBULAR 96/97 DO INSTITUTO MILITAR DE ENGENHARIA (04/12/96) FOLHA DE DADOS I ) Entalpias de Formação (H o f ) H 2 O (líquida) = - 68,3 kcal / mol CO 2 (gasoso) = - 94,1 kcal / mol
QUÍMICA ENSINO MÉDIO PROF.ª DARLINDA MONTEIRO 3 ANO PROF.ª YARA GRAÇA
 QUÍMICA 3 ANO PROF.ª YARA GRAÇA ENSINO MÉDIO PROF.ª DARLINDA MONTEIRO CONTEÚDOS E HABILIDADES Unidade I Vida e ambiente 2 CONTEÚDOS E HABILIDADES Aula 6 Conteúdos Efeito estufa. Fontes de energia alternativa.
QUÍMICA 3 ANO PROF.ª YARA GRAÇA ENSINO MÉDIO PROF.ª DARLINDA MONTEIRO CONTEÚDOS E HABILIDADES Unidade I Vida e ambiente 2 CONTEÚDOS E HABILIDADES Aula 6 Conteúdos Efeito estufa. Fontes de energia alternativa.
Qui. Allan Rodrigues Xandão (Gabriel Pereira)
 Semana 15 Allan Rodrigues Xandão (Gabriel Pereira) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. 23
Semana 15 Allan Rodrigues Xandão (Gabriel Pereira) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. 23
ESTUDO DA SELETIVIDADE DO CATALISADOR INDUSTRIAL APLICADO NA REFORMA A VAPOR DE METANOL
 ESTUDO DA SELETIVIDADE DO CATALISADOR INDUSTRIAL APLICADO NA REFORMA A VAPOR DE METANOL R. MENECHINI 1, G. G. LENZI 1, L. M. S. LPINI 2, H. J. ALVES 3, O. A. A. SANTOS 1 e L. M. M. JORGE 1 1 Universidade
ESTUDO DA SELETIVIDADE DO CATALISADOR INDUSTRIAL APLICADO NA REFORMA A VAPOR DE METANOL R. MENECHINI 1, G. G. LENZI 1, L. M. S. LPINI 2, H. J. ALVES 3, O. A. A. SANTOS 1 e L. M. M. JORGE 1 1 Universidade
1 Introdução Introdução ao Planejamento Energético
 1 Introdução 1.1. Introdução ao Planejamento Energético A matriz energética indica os fluxos energéticos de cada fonte de energia, desde a produção de energia até as utilizações finais pelo sistema sócioeconômico,
1 Introdução 1.1. Introdução ao Planejamento Energético A matriz energética indica os fluxos energéticos de cada fonte de energia, desde a produção de energia até as utilizações finais pelo sistema sócioeconômico,
HIDROTRATAMENTO. Prof. Marcos Villela Barcza
 HIDROTRATAMENTO Prof. Marcos Villela Barcza HIDROTRATAMENTO A hidrogenação é empregada especificamente para remoção de compostos de enxofre, nitrogênio, cloretos, saturação de olefinas, entre outras. As
HIDROTRATAMENTO Prof. Marcos Villela Barcza HIDROTRATAMENTO A hidrogenação é empregada especificamente para remoção de compostos de enxofre, nitrogênio, cloretos, saturação de olefinas, entre outras. As
Semana 09. A queima do carvão é representada pela equação química:
 . (Enem 6) O benzeno, um importante solvente para a indústria química, é obtido industrialmente pela destilação do petróleo. Contudo, também pode ser sintetizado pela trimerização do acetileno catalisada
. (Enem 6) O benzeno, um importante solvente para a indústria química, é obtido industrialmente pela destilação do petróleo. Contudo, também pode ser sintetizado pela trimerização do acetileno catalisada
COLÉGIO ESTADUAL DA POLÍCIA MILITAR DE GOIÁS HUGO DE CARVALHO RAMOS ATIVIDADE COMPLEMENTAR. Escola de Civismo e Cidadania
 COLÉGIO ESTADUAL DA POLÍCIA MILITAR DE GOIÁS HUGO DE CARVALHO RAMOS ANO LETIVO 2019 2º BIMESTRE ATIVIDADE COMPLEMENTAR Série Turma (s) Turno 2º do Ensino Médio K L M N O P NOTURNO Professor: HUMBERTO/EMERSON
COLÉGIO ESTADUAL DA POLÍCIA MILITAR DE GOIÁS HUGO DE CARVALHO RAMOS ANO LETIVO 2019 2º BIMESTRE ATIVIDADE COMPLEMENTAR Série Turma (s) Turno 2º do Ensino Médio K L M N O P NOTURNO Professor: HUMBERTO/EMERSON
Produção de gás combustível por meio de processo de gaseificação de Eucalyptus grandis em reator de leito fluidizado
 246 III Encontro de Pesquisa e Inovação da Embrapa Agroenergia: Anais Produção de gás combustível por meio de processo de gaseificação de Eucalyptus grandis em reator de leito fluidizado Albert Reis dos
246 III Encontro de Pesquisa e Inovação da Embrapa Agroenergia: Anais Produção de gás combustível por meio de processo de gaseificação de Eucalyptus grandis em reator de leito fluidizado Albert Reis dos
METALURGIA EXTRATIVA DOS NÃO FERROSOS
 METALURGIA EXTRATIVA DOS NÃO FERROSOS PMT 2509 PMT 3409 Flávio Beneduce Processo Sulfato Ilmenita (FeTiO 3 ) e/ou escória de Ti são as fontes de Ti São atacados com ácido sulfúrico concentrado (H 2 SO
METALURGIA EXTRATIVA DOS NÃO FERROSOS PMT 2509 PMT 3409 Flávio Beneduce Processo Sulfato Ilmenita (FeTiO 3 ) e/ou escória de Ti são as fontes de Ti São atacados com ácido sulfúrico concentrado (H 2 SO
