DIAGRAMA DAS DIAGONAIS. Bohr Sommerfeld Madelung Linus Pauling Diagrama Distribuição eletrônica
|
|
|
- Brenda Pedroso
- 4 Há anos
- Visualizações:
Transcrição
1
2 DIAGRAMA DAS DIAGONAIS PROF. TIAGO QUICK Bohr Sommerfeld Madelung Linus Pauling Diagrama Distribuição eletrônica
3 CAMADAS ELETRÔNICAS & NÍVEIS ENERGÉTICOS Consequências do Modelo Atômico de Bohr (camadas eletrônicas e níveis de energia) e contribuições de Sommerfeld (subníveis de energia) Camada Eletrônica K L M N O P Q Nível Energético N máximo de Elétrons
4 O QUE É O DIAGRAMA DAS DIAGONAIS: O Diagrama de Distribuição Eletrônica ou Diagrama das Diagonais consiste num modelo que auxilia na configuração dos elétrons dos átomos e dos íons através de subníveis de energia. Este método é usado na Química para determinar algumas características dos átomos. Também conhecido como Diagrama de Linus Pauling, O Princípio de Aufbau, do cientista alemão Erwin Madelung, ajuda a traçar algumas propriedades dos átomos, como o número de camadas preenchidas por elétrons e o número de camadas de elétrons que o átomo possui, por exemplo.
5 O QUE É O DIAGRAMA DAS DIAGONAIS: O cientista americano vencedor de dois prêmios Nobel, Linus C. Pauling ( ) é o responsável por desenvolver esta teoria, baseado no princípio da construção (Aufbau em alemão), considerada uma das que melhor explica a distribuição eletrônica ao redor dos átomos. Como se sabe, a tabela periódica organiza os elementos químicos a partir do número atômico em ordem crescente. O Diagrama das diagonais, em conjunto com a tabela periódica, ajuda a fornecer informações sobre os átomos que formam esses elementos. O diagrama se baseia nos subníveis de energia do átomo para organizar os elétrons. Estes são dispostos a partir do de menor para o de maior energia, quando o átomo se encontra no seu estado fundamental.
6 DIAGRAMA DAS DIAGONAIS A eletrosfera dos átomos é formada por 7 (sete) camadas eletrônicas, representadas pelas letras: K, L, M, N, O, P e Q. Cada camada permite um número máximo de elétrons: Camadas Eletrônicas Níveis Energéticos N.º Máximo de Elétrons Subníveis de Energia K 1 2 e - 1s 2 L 2 8 e - 2s 2 2p 6 M 3 18 e - 3s 2 3p 6 3d 10 N 4 32 e - 4s 2 4p 6 4d 10 4f 14 O 5 32 e - 5s 2 5p 6 5d 10 5f 14 P 6 18 e - 6s 2 6p 6 6d 10 Q 7 8 e - 7s 2 7p 6
7 DIAGRAMA DAS DIAGONAIS Nota-se que a camada K apresenta apenas um subnível (s), que permite a existência de até 2 elétrons. A camada L tem dois subnível (s e p), sendo que p comporta até 6 elétrons. Ainda existem os subníveis d (com até 10 elétrons) e f (com 14 elétrons, no máximo). Subnível s = sharp (nítido) p = principal (principal) d = diffuse (difuso) f = fundamental (fundamental) Nº de Elétrons por Subnível até 2 elétrons até 6 elétrons até 10 elétrons até 14 elétrons
8 DIAGRAMA DAS DIAGONAIS Assim, a partir deste esquema, Pauling organizou os elétrons seguindo uma ordem crescente de energia nos diferentes subníveis. Usando setas diagonais, encontra-se a seguinte sequência (energética) no Diagrama de Linus Pauling: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6 7s 2 5f 14 6d 10 7p 6.
9 DIAGRAMA DAS DIAGONAIS
10 DIAGRAMA DAS DIAGONAIS (CONCEITOS INICIAIS)
11 CAMADAS, NÍVEIS, SUBNÍVEIS & ORBITAIS
12
13 Nível Energético ou Camada Eletrônica DISTRIBUIÇÃO ELETRÔNICA Para realizar a distribuição eletrônica, usamos o número atômico do átomo, que é identificado pelo seu número atômico (Z). Para isso usamos também o diagrama das diagonais. 1s 2 N Máximo de Eletrons Subnível Energético Exemplo: 3Li = 1s 2 2s 1 10Ne = 1s 2 2s 2 2p 6 11Na = 1s 2 2s 2 2p 6 3s 1 26Fe = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6
14 CAMADA DE VALÊNCIA A camada de valência é a última camada ocupada por elétrons. Ela pode ser identificada pelo maior nível energético presente na distribuição eletrônica de um átomo Exemplo: 3Li = 1s 2 2s 1 10Ne = 1s 2 2s 2 2p 6 11Na = 1s 2 2s 2 2p 6 3s 1 26Fe = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 Camada de Valência
15 SUBNÍVEL MAIS ENERGÉTICO O subnível mais energético é identificado pelo último subnível escrito numa distribuição eletrônica de um átomo Exemplo: 3Li = 1s 2 2s 1 10Ne = 1s 2 2s 2 2p 6 11Na = 1s 2 2s 2 2p 6 3s 1 26Fe = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 Subnível mais energético
16 CAMADA DE VALÊNCIA X SUBNÍVEL MAIS ENERGÉTICO Nem sempre há uma coincidência entre a camada de valência e o subnível mais energético. Usando a identificação para cada um deles, temos o que é mostrado abaixo: Camada de Valência Exemplo: 3Li = 1s 2 2s 1 10Ne = 1s 2 2s 2 2p 6 11Na = 1s 2 2s 2 2p 6 3s 1 26Fe = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 Subnível mais energético
17 EXERCÍCIOS 1. Identifique a CAMADA DE VALÊNCIA de cada elemento químico a seguir: a) 3Li 7 b) 11Na 23 c) 19K 39 d) 12Mg 24 e) 8O 16 f) 9F 19 g) 17Cl 35 h) 20Ca 40 i) 6C 12 j) 7N 14 k) 35Br 80 l) 13Al 27 m) 16S 32
18 EXERCÍCIOS 1. Identifique o SUBNÍVEL MAIS ENERGÉTICO de cada elemento químico a seguir: a) 3Li 7 b) 11Na 23 c) 19K 39 d) 12Mg 24 e) 8O 16 f) 9F 19 g) 17Cl 35 h) 20Ca 40 i) 6C 12 j) 7N 14 k) 35Br 80 l) 13Al 27 m) 16S 32
19 DISTRIBUIÇÃO ELETRÔNICA Distribuição Eletrônica por níveis e subníveis 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 Distribuição eletrônica por camadas eletrônicas K = 2; L= 8; M= 14; N = 2
20 ORDEM ENERGÉTICA E ORDEM GEOMÉTRICA Exemplos: Distribuição Eletrônica por níveis e subníveis 26 Fe =1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 Distribuição eletrônica por camadas 26 Fe - K = 2; L= 8; M= 14; N = 2. 26Fe = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 Ordem Energética 26Fe = 1s 2 / 2s 2 2p 6 / 3s 2 3p 6 3d 6 / 4s 2 Ordem Geométrica K L M N Camadas Eletrônicas
21 EXERCÍCIOS 1. Realize a distribuição eletrônica POR NÍVEIS E SUBNÍVEIS dos elementos a seguir: a) 3Li 7 b) 11Na 23 c) 19K 39 d) 12Mg 24 e) 8O 16 f) 9F 19 g) 17Cl 35 h) 20Ca 40 i) 6C 12 j) 7N 14 k) 35Br 80 l) 13Al 27 m) 16S 32
22 EXERCÍCIOS 1. Realize a distribuição eletrônica pela ORDEM GEOMÉTRICA dos elementos a seguir: a) 3Li 7 h) 20Ca 40 b) 11Na 23 c) 19K 39 d) 12Mg 24 e) 8O 16 f) 9F 19 g) 17Cl 35 i) 6C 12 j) 7N 14 k) 35Br 80 l) 13Al 27 m) 16S 32
23 EXERCÍCIOS 1. Realize a distribuição eletrônica POR CAMADAS dos elementos a seguir: a) 3Li 7 b) 11Na 23 c) 19K 39 d) 12Mg 24 e) 8O 16 f) 9F 19 g) 17Cl 35 h) 20Ca 40 i) 6C 12 j) 7N 14 k) 35Br 80 l) 13Al 27 m) 16S 32
24 NÚMEROS QUÂNTICOS PROF. TIAGO QUICK De Broglie Heisenberg Schrödinger Números quânticos: Primário, Secundário, Magnético, Spin Orbitais
25 CONCEITOS INICIAIS Louis De Broglie O elétron se comporta ora como partícula, ora como onda, dependendo do tipo de experimento. Se a luz apresenta natureza dual, uma partícula também apresenta propriedades ondulatórias A todo elétron em movimento está associada uma onda característica
26 CONCEITOS INICIAIS Werner Heisenberg PRINCÍPIO DA INCERTEZA: Quanto maior for a precisão da medida da posição do elétron, menor será a precisão na medida de sua velocidade e vice-versa Não é possível calcular a posição e a velocidade de um elétron num mesmo instante
27 CONCEITOS INICIAIS Erwin Schrödinger Propôs um experimento para comprovar o princípio da incerteza, que ficou conhecido como o gato de Schrödinger
28 CONCEITOS INICIAIS Erwin Schrödinger O QUE É O EXPERIMENTO DO GATO DE SCHRÖDINGER? É uma experiência mental, frequentemente descrita como um paradoxo, desenvolvida pelo físico austríaco Erwin Schrödinger, em A experiência procura ilustrar a interpretação de Copenhague da mecânica quântica, imaginando-a aplicada a objetos do dia-a-dia. No exemplo, há um gato encerrado em uma caixa, de forma a não estar apenas vivo ou apenas morto, mas sim "vivomorto". Por sua vida supostamente atrelar-se a um evento aleatório - usualmente o decaimento radioativo - um gato "vivomorto" surgiria como reflexo de um estado físico atípico ao senso comum mas presente em sistemas quânticos: o estado emaranhado. Em termos técnicos, o estado "vivomorto" (claramente distinto do estado vivo e distinto do estado morto) compõe-se pelo emaranhamento desses dois estados e constitui de fato, segundo o que se busca elucidar, a situação do gato no experimento, ao menos enquanto o sistema permanecer fechado, sem ser observado.
29 CONCEITOS INICIAIS A interpretação de Copenhague é a interpretação mais comum da Mecânica Quântica e foi desenvolvida por Niels Bohr e Werner Heisenberg que trabalhavam juntos em Copenhague em Pode ser condensada em três teses: As previsões probabilísticas feitas pela mecânica quântica são irredutíveis no sentido em que não são um mero reflexo da falta de conhecimento de hipotéticas variáveis escondidas. No lançamento de dados, usamos probabilidades para prever o resultado porque não possuímos informação suficiente apesar de acreditarmos que o processo é determinístico. As probabilidades são utilizadas para completar o nosso conhecimento. A interpretação de Copenhague defende que em Mecânica Quântica, os resultados são indeterminísticos. A Física é a ciência dos resultados de processos de medida. Não faz sentido especular para além daquilo que pode ser medido. A interpretação de Copenhaga considera sem sentido perguntas como "onde estava a partícula antes de a sua posição ter sido medida?". O ato de observar provoca o colapso da função de onda, o que significa que, embora antes da medição o estado do sistema permitisse muitas possibilidades, apenas uma delas foi escolhida aleatoriamente pelo processo de medição, e a função de onda modifica-se instantaneamente para refletir essa escolha.
30 CONCEITOS INICIAIS A complexidade da mecânica quântica (tese 1) foi atacada pela experiência (imaginária) de Einstein-Podolsky-Rosen, que pretendia mostrar que têm que existir variáveis escondidas para evitar "efeitos não locais e instantâneos à distância". A desigualdade de Bell sobre os resultados de uma tal experiência foi derivada do pressuposto de que existem variáveis escondidas e não existem "efeitos não-locais". Em 1982, Alain Aspect levou a cabo a experiência e descobriu que a desigualdade de Bell era violada, rejeitando interpretações que postulavam variáveis escondidas e efeitos locais. Esta experiência foi alvo de várias críticas e novas experiências realizadas por Weihs e Rowe confirmaram os resultados de Aspect. Muitos físicos e filósofos notáveis têm criticado a interpretação de Copenhague, com base quer no fato de não ser determinista quer no fato de propor que a realidade é criada por um processo de observação não físico. As frases de Einstein "Deus não joga aos dados" e "Pensas mesmo que a Lua não está lá quando não estás a olhar para ela?" ilustram a posição dos críticos. A experiência do Gato de Schroedinger foi proposta para mostrar que a Interpretação de Copenhague é absurda. A alternativa principal à Interpretação de Copenhague é a Interpretação de Everett dos mundos paralelos.
31 CONFERÊNCIA DE SOLVAY
32
33 ORBITAL É a região do espaço ao redor do núcleo onde é máxima a probabilidade de encontrar um determinado elétron
34 ORBITAIS
35 O QUE SÃO NÚMEROS QUÂNTICOS? Como não é intuito discutir a evolução dos modelos atômicos neste momento, bastanos reconhecer que os números quânticos são conceitos fundamentais evidenciados pelo modelo atômico de Schrödinger. A teoria do modelo atômico de Schrödinger é aceita atualmente e assume a existência de números quânticos conhecidos (s, p, d, f) e também teóricos (g, h, i...), pautando-se em quatro características oriundas da Mecânica Quântica.
36 NÚMEROS QUÂNTICOS Principal (n) corresponde ao nível energético em que o elétron está localizado Pode variar de 1 a 7 Secundário ou Azimutal (l) corresponde ao subnível ocupado pelo referido elétron Pode variar de 0 até 3 (relacionado ao subnível energético)
37 NÚMEROS QUÂNTICOS Magnético (m ou m l ) identifica o orbital ocupado pelo elétron mais energético Pode variar de -3 a +3 (-3, -2, -1, 0, +1, +2, +3)
38 NÚMEROS QUÂNTICOS Spin (s ou m s ) indica o sentido de rotação do elétron (convencionado) Pode ter os valores +½ ou -½
39 REGRA DE HUND A Regra de Hund ou Princípio da Máxima Multiplicidade foi desenvolvida pelo físico alemão Friedrich Hermann Hund, mostra que, quanto maior o número de elétrons com spin paralelos num orbital incompleto, menor será a energia. Em um mesmo subnível, inicialmente, todos os orbitais recebem seu primeiro elétron e somente depois cada orbital recebe o seu segundo elétron
40 PRINCÍPIO DA EXCLUSÃO DE PAULI O princípio de exclusão de Pauli é um princípio da mecânica quântica formulado por Wolfgang Pauli em Para elétrons de um mesmo átomo, ele implica que dois elétrons não podem ter os mesmos quatro números quânticos. Por exemplo, se os números quânticos n, l e m são iguais nos dois elétrons, estes deverão necessariamente ter os números de spin diferentes, e portanto os dois elétrons têm spins opostos. Exemplo: Um orbital comporta no máximo dois elétrons, com spins contrários 1s 2 2s 2 2p 2 e 1s 2 2s 2 2p 5 n = 2 n = 2 l = 1 l = 1 m = 0 m = 0 s = -1/2 s = +1/2
41 REPRESENTAÇÃO DOS ORBITAIS
42 EXERCÍCIOS 1. Escreva os quatro NÚMEROS QUÂNTICOS do último elétron de cada elemento químico a seguir. Não esqueça de desenhar a representação dos orbitais: a) 3Li 7 b) 11Na 23 c) 19K 39 d) 12Mg 24 e) 8O 16 f) 9F 19 g) 17Cl 35 h) 20Ca 40 i) 6C 12 j) 7N 14 k) 35Br 80 l) 13Al 27 m) 16S 32
43
DIAGRAMA DAS DIAGONAIS. Bohr Sommerfeld Madelung Linus Pauling
 DIAGRAMA DAS DIAGONAIS Bohr Sommerfeld Madelung Linus Pauling CAMADAS ELETRÔNICAS & NÍVEIS ENERGÉTICOS Consequências do Modelo Atômico de Bohr e contribuições de Sommerfeld Camada Eletrônica K L M N O
DIAGRAMA DAS DIAGONAIS Bohr Sommerfeld Madelung Linus Pauling CAMADAS ELETRÔNICAS & NÍVEIS ENERGÉTICOS Consequências do Modelo Atômico de Bohr e contribuições de Sommerfeld Camada Eletrônica K L M N O
Estrutura atômica: níveis e subníveis de energia (II) Química Prof.ª Talita Sousa
 Estrutura atômica: níveis e subníveis de energia (II) Relembrando o modelo de Bohr Niels Bohr Por meio de seus estudos, Bohr formulou dois postulados: A existência de um estado estacionário, ou seja, órbitas
Estrutura atômica: níveis e subníveis de energia (II) Relembrando o modelo de Bohr Niels Bohr Por meio de seus estudos, Bohr formulou dois postulados: A existência de um estado estacionário, ou seja, órbitas
Aulas 1 e 2. Atomística
 Aulas 1 e 2 Atomística Modelos Atômicos Dalton - 1808 Primeiro cientista a desenvolver uma teoria atômica, segundo a qual a matéria se compõe de partículas indestrutíveis chamadas átomos. Modelos Atômicos
Aulas 1 e 2 Atomística Modelos Atômicos Dalton - 1808 Primeiro cientista a desenvolver uma teoria atômica, segundo a qual a matéria se compõe de partículas indestrutíveis chamadas átomos. Modelos Atômicos
NÚMEROS QUÂNTICOS. As teorias da MECÂNICA QUÂNTICA (Planck, De Broglie, Schrödinger e Heisenberg e outros), auxiliam na identificação dos elétrons.
 NÚMEROS QUÂNTICOS As teorias da MECÂNICA QUÂNTICA (Planck, De Broglie, Schrödinger e Heisenberg e outros), auxiliam na identificação dos elétrons. Prof. Ailey Aparecida Coelho Tanamati Mecânica = movimento
NÚMEROS QUÂNTICOS As teorias da MECÂNICA QUÂNTICA (Planck, De Broglie, Schrödinger e Heisenberg e outros), auxiliam na identificação dos elétrons. Prof. Ailey Aparecida Coelho Tanamati Mecânica = movimento
UNIVERSIDADE FEDERAL DO ACRE PROGRAMA DE EDUCAÇÃO TUTORIAL. TUTOR: Dr. Ribamar Silva PETIANO: Erlailson Costa dos Santos
 UNIVERSIDADE FEDERAL DO ACRE PROGRAMA DE EDUCAÇÃO TUTORIAL TUTOR: Dr. Ribamar Silva PETIANO: Erlailson Costa dos Santos 1- INTRODUÇÃO --------------------------------------------- Werner Karl Heisenberg
UNIVERSIDADE FEDERAL DO ACRE PROGRAMA DE EDUCAÇÃO TUTORIAL TUTOR: Dr. Ribamar Silva PETIANO: Erlailson Costa dos Santos 1- INTRODUÇÃO --------------------------------------------- Werner Karl Heisenberg
Número quântico secundário, azimutal ou de momento angular (l)
 DISTRIBUIÇÃO ELETRÔNICA E N OS QUÂNTICOS TEORIA PARTE I Introdução Números quânticos formam um conjunto de valores matemáticos que servem para identificar exclusivamente um elétron dentro de um determinado
DISTRIBUIÇÃO ELETRÔNICA E N OS QUÂNTICOS TEORIA PARTE I Introdução Números quânticos formam um conjunto de valores matemáticos que servem para identificar exclusivamente um elétron dentro de um determinado
Qímica Estrutura At mica
 Q ímica Estrutura At mica MODELOS ATÔMICOS Modelo dos Filósofos Gregos: Leucipo (500 a.c.) e Demócrito (460 a.c.) Indestrutível, indivisível e maciço. Modelo baseado apenas na intuição e na lógica. Aristóteles
Q ímica Estrutura At mica MODELOS ATÔMICOS Modelo dos Filósofos Gregos: Leucipo (500 a.c.) e Demócrito (460 a.c.) Indestrutível, indivisível e maciço. Modelo baseado apenas na intuição e na lógica. Aristóteles
ESTRUTURA ATÔMICA. Modelos Atômicos
 ESTRUTURA ATÔMICA Modelos Atômicos 1.Modelo atômico de Dalton 2.Modelo atômico de Thomson 3.Modelo atômico de Rutherford 4.Modelo atômico de Rutherford-Bohr 5.Modelo atômico atual MODELOS ATÔMICOS 1808
ESTRUTURA ATÔMICA Modelos Atômicos 1.Modelo atômico de Dalton 2.Modelo atômico de Thomson 3.Modelo atômico de Rutherford 4.Modelo atômico de Rutherford-Bohr 5.Modelo atômico atual MODELOS ATÔMICOS 1808
ESTRUTURA ELETRÔNICA DOS ÁTOMOS
 ESTRUTURA ELETRÔNICA DOS ÁTOMOS 2 Natureza ondulatória da luz 3 Natureza ondulatória da luz 4 Natureza ondulatória da luz 5 Natureza ondulatória da luz 6 Energia quantizada e fótons Planck quantum h é
ESTRUTURA ELETRÔNICA DOS ÁTOMOS 2 Natureza ondulatória da luz 3 Natureza ondulatória da luz 4 Natureza ondulatória da luz 5 Natureza ondulatória da luz 6 Energia quantizada e fótons Planck quantum h é
ESTRUTURA ATÔMICA. Prof. Dr. Cristiano Torres Miranda Disciplina: Química Geral I QM81B Turmas Q13 e Q14
 ESTRUTURA ATÔMICA Prof. Dr. Cristiano Torres Miranda Disciplina: Química Geral I QM81B Turmas Q13 e Q14 TEORIA ATÔMICA DA MATÉRIA Demócrito e Leucipo (discípulo) (460 370 a.c.) Aristóteles (384 a.c. 322
ESTRUTURA ATÔMICA Prof. Dr. Cristiano Torres Miranda Disciplina: Química Geral I QM81B Turmas Q13 e Q14 TEORIA ATÔMICA DA MATÉRIA Demócrito e Leucipo (discípulo) (460 370 a.c.) Aristóteles (384 a.c. 322
Estrutura eletrônica dos átomos. Mestranda Daniele Potulski Disciplina Química Madeira I
 Estrutura eletrônica dos átomos Mestranda Daniele Potulski danielepotulski@ufpr.br Disciplina Química Madeira I Estrutura geral dos átomos -PRÓTONS situados no núcleo do átomo (representados por +) -NÊUTRONS
Estrutura eletrônica dos átomos Mestranda Daniele Potulski danielepotulski@ufpr.br Disciplina Química Madeira I Estrutura geral dos átomos -PRÓTONS situados no núcleo do átomo (representados por +) -NÊUTRONS
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. Estrutura Eletrônica
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. Estrutura Eletrônica
A Equação de Onda de Schröedinger. O Princípio da Incerteza de Heisenberg. λ =
 O Modelo Mecânico-Quântico Louis de Broglie apresentou a idéia de que, se as ondas luminosas exibiam características de partícula, então talvez as partículas de matéria pudessem mostrar propriedades ondulatórias.
O Modelo Mecânico-Quântico Louis de Broglie apresentou a idéia de que, se as ondas luminosas exibiam características de partícula, então talvez as partículas de matéria pudessem mostrar propriedades ondulatórias.
NÚMEROS QUÂNTICOS. Química Geral Prof.Dr. Augusto Freitas
 NÚMEROS QUÂNTICOS Química Geral Prof.Dr. Augusto Freitas 1 Os números quânticos descrevem a posição (e a energia) dos elétrons nos átomos. Existem quatro números quânticos: 1 - número quântico principal
NÚMEROS QUÂNTICOS Química Geral Prof.Dr. Augusto Freitas 1 Os números quânticos descrevem a posição (e a energia) dos elétrons nos átomos. Existem quatro números quânticos: 1 - número quântico principal
ATIVIDADE DE QUÍMICA REVISÃO 9º ANO. Distribuição Eletrônica de Linus Pauling
 ATIVIDADE DE QUÍMICA REVISÃO 9º ANO Distribuição Eletrônica de Linus Pauling Em anos anteriores ao rearranjo que Linus Pauling fez para distribuir eletronicamente os elementos, os Cientistas Bohr e Sommerfield
ATIVIDADE DE QUÍMICA REVISÃO 9º ANO Distribuição Eletrônica de Linus Pauling Em anos anteriores ao rearranjo que Linus Pauling fez para distribuir eletronicamente os elementos, os Cientistas Bohr e Sommerfield
NÚMEROS QUÂNTICOS PRINCIPAL, SECUNDÁRIO, MAGNÉTICO E SPIN
 NÚMEROS QUÂNTICOS PRINCIPAL, SECUNDÁRIO, MAGNÉTICO E SPIN NÚMEROS QUÂNTICOS Os orbitais atômicos são identificadas por três números quânticos: n número quântico principal; l número quântico de momento
NÚMEROS QUÂNTICOS PRINCIPAL, SECUNDÁRIO, MAGNÉTICO E SPIN NÚMEROS QUÂNTICOS Os orbitais atômicos são identificadas por três números quânticos: n número quântico principal; l número quântico de momento
LCE0143 Química Geral. Estrutura Atômica. Wanessa Melchert Mattos.
 LCE0143 Química Geral Estrutura Atômica Wanessa Melchert Mattos wanemelc@usp.br Princípio da Incerteza Elétron dualidade onda-partícula W. Heisenberg: impossível fixar a posição de um elétron em um átomo
LCE0143 Química Geral Estrutura Atômica Wanessa Melchert Mattos wanemelc@usp.br Princípio da Incerteza Elétron dualidade onda-partícula W. Heisenberg: impossível fixar a posição de um elétron em um átomo
h mc 2 =hν mc 2 =hc/ λ
 Louis de Broglie investigou as propriedades ondulatórias da matéria na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tinha associado a ele um λ. Ele igualou as duas expressões
Louis de Broglie investigou as propriedades ondulatórias da matéria na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tinha associado a ele um λ. Ele igualou as duas expressões
Elétrons como ondas? Um bom modelo deve ser capaz de explicar propriedades atômicas, propriedades periódicas, ligação química
 OS ELÉTRONS O MODELO DA MECÂNICA QUÂNTICA E AS ENERGIAS ELETRÔNICAS Modelo atual se baseia na MECÂNICA QUÂNTICA Considera os conceitos da quantização da energia eletrônica (Bohr), fornecendo uma explicação
OS ELÉTRONS O MODELO DA MECÂNICA QUÂNTICA E AS ENERGIAS ELETRÔNICAS Modelo atual se baseia na MECÂNICA QUÂNTICA Considera os conceitos da quantização da energia eletrônica (Bohr), fornecendo uma explicação
Apostila de Química 11 Atomística
 Apostila de Química 11 Atomística 1.0 Filósofos Leucipo e Demócrito, Grécia 400 a.c. A matéria é formada por pequenas partículas que sempre existiram e que seriam indestrutíveis, os átomos. Esses filósofos
Apostila de Química 11 Atomística 1.0 Filósofos Leucipo e Demócrito, Grécia 400 a.c. A matéria é formada por pequenas partículas que sempre existiram e que seriam indestrutíveis, os átomos. Esses filósofos
ATOMÍSTICA PROF. ADRIANO ALVES
 ATOMÍSTICA PROF. ADRIANO ALVES Demócrito Aristóteles Dalton Thomson Bohr Rutherford Sommerfeld Heisenberg Schrödinger De Broglie DALTON 1. Toda matéria é formada de partículas fundamentais, os átomos.
ATOMÍSTICA PROF. ADRIANO ALVES Demócrito Aristóteles Dalton Thomson Bohr Rutherford Sommerfeld Heisenberg Schrödinger De Broglie DALTON 1. Toda matéria é formada de partículas fundamentais, os átomos.
Aula 01 Estrutura eletrônica
 Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula 01 Estrutura eletrônica Dr. Tiago P. Camargo Átomos - Estrutura Núcleo (prótons e nêutrons) Eletrosfera (elétrons)
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula 01 Estrutura eletrônica Dr. Tiago P. Camargo Átomos - Estrutura Núcleo (prótons e nêutrons) Eletrosfera (elétrons)
Aula 3 Estrutura Atômica cont
 Aula 3 Estrutura Atômica cont Tabela Periódica Mecânica quântica e orbitais atômicos Schrödinger propôs uma equação que contém os termos onda e partícula. A resolução da equação leva às funções de onda.
Aula 3 Estrutura Atômica cont Tabela Periódica Mecânica quântica e orbitais atômicos Schrödinger propôs uma equação que contém os termos onda e partícula. A resolução da equação leva às funções de onda.
A Teoria de Bohr foi aceite com entusiasmo, porque pela primeira vez se conseguiu: Interpretar qualitativamente os espectros atómicos em geral;
 Sumário Das Estrelas ao átomo Unidade temática 1 Como se carateriza o modelo O modelo quântico: Números quânticos. Energia das orbitais. Princípios e regras para a distribuição dos eletrões pelas orbitais.
Sumário Das Estrelas ao átomo Unidade temática 1 Como se carateriza o modelo O modelo quântico: Números quânticos. Energia das orbitais. Princípios e regras para a distribuição dos eletrões pelas orbitais.
PROPRIEDADES ONDULATÓRIAS DO ELÉTRON
 MODELO QUÂNTICO PROPRIEDADES ONDULATÓRIAS DO ELÉTRON EINSTEIN: usou o efeito fotoelétrico para demonstrar que a luz, geralmente imaginada como tendo propriedades de onda, pode também ter propriedades de
MODELO QUÂNTICO PROPRIEDADES ONDULATÓRIAS DO ELÉTRON EINSTEIN: usou o efeito fotoelétrico para demonstrar que a luz, geralmente imaginada como tendo propriedades de onda, pode também ter propriedades de
A Estrutura Eletrônica dos Átomos. Prof. Fernando R. Xavier
 A Estrutura Eletrônica dos Átomos Prof. Fernando R. Xavier UDESC 2015 Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson, etc 400 a.c. até 1897 d.c. Nascimento da Mecânica Quântica
A Estrutura Eletrônica dos Átomos Prof. Fernando R. Xavier UDESC 2015 Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson, etc 400 a.c. até 1897 d.c. Nascimento da Mecânica Quântica
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
Revisão das observações experimentais, modelo de Bohr e Princípios da Mecânica Quântica by Pearson Education. Capítulo 06
 Revisão das observações experimentais, modelo de Bohr e Princípios da Mecânica Quântica Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com
Revisão das observações experimentais, modelo de Bohr e Princípios da Mecânica Quântica Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com
Schrödinger propôs uma equação que contém os termos onda e partícula. A resolução da equação leva às funções de onda. Af função de onda fornece o
 Aula 3 Estrutura Atômica cont Tabela Periódica Mecânica quântica e orbitais atômicos Schrödinger propôs uma equação que contém os termos onda e partícula. A resolução da equação leva às funções de onda.
Aula 3 Estrutura Atômica cont Tabela Periódica Mecânica quântica e orbitais atômicos Schrödinger propôs uma equação que contém os termos onda e partícula. A resolução da equação leva às funções de onda.
Vimos que a radiação eletromagnética comportase como onda e partícula Dualidade ondapartícula da radiação eletromagnética
 Estrutura eletrônica dos átomos Vimos que a radiação eletromagnética comportase como onda e partícula Dualidade ondapartícula da radiação eletromagnética Onda Com propriedades como comprimento de onda,
Estrutura eletrônica dos átomos Vimos que a radiação eletromagnética comportase como onda e partícula Dualidade ondapartícula da radiação eletromagnética Onda Com propriedades como comprimento de onda,
Química. Aula 05 Profº Ricardo Dalla Zanna
 Química Aula 05 Profº Ricardo Dalla Zanna Conteúdo Programático Unidade 2 Átomos e Elementos o Seção 2.1 Evolução do modelo atômico e classificação periódica dos elementos o Seção 2.2 Leis ponderais o
Química Aula 05 Profº Ricardo Dalla Zanna Conteúdo Programático Unidade 2 Átomos e Elementos o Seção 2.1 Evolução do modelo atômico e classificação periódica dos elementos o Seção 2.2 Leis ponderais o
Teoria Atômica QUÍMICA GERAL
 Teoria Atômica QUÍMICA GERAL Do que é feita a matéria? o Por volta de 440 a.c. Empédocles sugeriu que a matéria era composta pela mistura de 4 elementos: água, terra, ar e fogo. o Por volta de 400 a.c.
Teoria Atômica QUÍMICA GERAL Do que é feita a matéria? o Por volta de 440 a.c. Empédocles sugeriu que a matéria era composta pela mistura de 4 elementos: água, terra, ar e fogo. o Por volta de 400 a.c.
Números quânticos e distribuição eletrônica
 Aluno(a): Prof.: Éderson Números quânticos e distribuição eletrônica Questão 1) Quais são os quatro números quânticos principal(n), azimutal (l), magnético (ml) e de momento angular orbital (ms), para
Aluno(a): Prof.: Éderson Números quânticos e distribuição eletrônica Questão 1) Quais são os quatro números quânticos principal(n), azimutal (l), magnético (ml) e de momento angular orbital (ms), para
Estrutura atômica. Modelo quântico do átomo
 Estrutura atômica Modelo quântico do átomo Um bom modelo deve ser capaz de explicar propriedades atômicas, propriedades periódicas, ligação química Mecânica quântica - mecânica ondulatória Elétrons como
Estrutura atômica Modelo quântico do átomo Um bom modelo deve ser capaz de explicar propriedades atômicas, propriedades periódicas, ligação química Mecânica quântica - mecânica ondulatória Elétrons como
Em torno do núcleo do átomo temos uma região denominada ELETROSFERA
 Em torno do núcleo do átomo temos uma região denominada ELETROSFERA A eletrosfera é dividida em 7 partes chamada CAMADAS ELETRÔNICAS ou NÍVEIS DE ENERGIA Do núcleo para fora estas camadas são representadas
Em torno do núcleo do átomo temos uma região denominada ELETROSFERA A eletrosfera é dividida em 7 partes chamada CAMADAS ELETRÔNICAS ou NÍVEIS DE ENERGIA Do núcleo para fora estas camadas são representadas
Química Geral -Aula 2 Átomo e estrutura atômica. *Mas afinal, de que são feitas as coisas?
 Química Geral -Aula 2 Átomo e estrutura atômica *Mas afinal, de que são feitas as coisas? Átomo na Grécia antiga 2 teorias (Demócrito, Leucipo e Aristóteles) Demócrito, Leucipo e Aristóteles Átomo como
Química Geral -Aula 2 Átomo e estrutura atômica *Mas afinal, de que são feitas as coisas? Átomo na Grécia antiga 2 teorias (Demócrito, Leucipo e Aristóteles) Demócrito, Leucipo e Aristóteles Átomo como
K L M N O P Q 7 NÍVEIS DE ENERGIA n =
 Química / profª SIMONE MORGADO Aula 3 Configuração Eletrônica 1. A ELETROSFERA Nossa caminhada hoje é pela eletrosfera, uma região bastante importante, pois nas reações químicas os elétrons são as partículas
Química / profª SIMONE MORGADO Aula 3 Configuração Eletrônica 1. A ELETROSFERA Nossa caminhada hoje é pela eletrosfera, uma região bastante importante, pois nas reações químicas os elétrons são as partículas
C i ê n c i a s d a N a t u r e z a e s u a s T e c n o l o g i a s Q U Í M I C A N O M E: N º T U R M A : D A T A :
 C i ê n c i a s d a N a t u r e z a e s u a s T e c n o l o g i a s Q U Í M I C A P r o f ª M á r c i a R i b e i r o N O M E: N º T U R M A : D A T A : C a m a d a s e l e t r ô n i c a s Os átomos são
C i ê n c i a s d a N a t u r e z a e s u a s T e c n o l o g i a s Q U Í M I C A P r o f ª M á r c i a R i b e i r o N O M E: N º T U R M A : D A T A : C a m a d a s e l e t r ô n i c a s Os átomos são
Tarefa 23 Professor Gustavo
 Química Tarefa Professor Gustavo 01. Entre as afirmações abaixo, assinale a opção ERRADA. a) Os íons He +, Li +, Be +, no estado gasoso são exemplos de hidrogenóides. b) No átomo de hidrogênio, os orbitais
Química Tarefa Professor Gustavo 01. Entre as afirmações abaixo, assinale a opção ERRADA. a) Os íons He +, Li +, Be +, no estado gasoso são exemplos de hidrogenóides. b) No átomo de hidrogênio, os orbitais
QUÍMICA GERAL Cap. 01. Prof. Kristian Sales Vieira
 QUÍMICA GERAL Cap. 01 Prof. Kristian Sales Vieira Modelo atômico O processo de descoberta Grécia século V a.c. Empédocles Explicar a constituição da matéria ; 04 Elementos: fogo, ar, água e terra; Constante
QUÍMICA GERAL Cap. 01 Prof. Kristian Sales Vieira Modelo atômico O processo de descoberta Grécia século V a.c. Empédocles Explicar a constituição da matéria ; 04 Elementos: fogo, ar, água e terra; Constante
ESTRUTURA ATÔMICA - III
 ESTRUTURA ATÔMICA - III Elementos químicos emitem luz em diferentes comprimentos de onda. Esta emissão é descontínua e só ocorre para determinadas faixas de Prof. Bruno Gabriel Química 2ª Bimestre 2016
ESTRUTURA ATÔMICA - III Elementos químicos emitem luz em diferentes comprimentos de onda. Esta emissão é descontínua e só ocorre para determinadas faixas de Prof. Bruno Gabriel Química 2ª Bimestre 2016
Configuração Eletrônica
 TOMO II Configuração Eletrônica Química Geral Professor Celso Rapaci INTRODUÇÃO Neste capítulo aprenderemos como os elétrons estão distribuídos na eletrosfera do átomo, em diferentes níveis e subníveis
TOMO II Configuração Eletrônica Química Geral Professor Celso Rapaci INTRODUÇÃO Neste capítulo aprenderemos como os elétrons estão distribuídos na eletrosfera do átomo, em diferentes níveis e subníveis
TEORIAS ATÔMICAS. Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807)
 TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
QUÌMICA PROFº JAISON MATTEI A IDENTIFICAÇÃO DOS ÁTOMOS
 QUÌMICA PROFº JAISON MATTEI A IDENTIFICAÇÃO DOS ÁTOMOS Número atômico (Z): é o número de prótons existentes no núcleo de um átomo. Número de massa (A): é a soma do número de prótons (Z) e de nêutrons (N)
QUÌMICA PROFº JAISON MATTEI A IDENTIFICAÇÃO DOS ÁTOMOS Número atômico (Z): é o número de prótons existentes no núcleo de um átomo. Número de massa (A): é a soma do número de prótons (Z) e de nêutrons (N)
QUI109 QUÍMICA GERAL (Ciências Biológicas) 6ª aula /
 QUI109 QUÍMICA GERAL (Ciências Biológicas) 6ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) MODELO ATÔMICO J. Dalton a matéria é formada por átomos / as inúmeras
QUI109 QUÍMICA GERAL (Ciências Biológicas) 6ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) MODELO ATÔMICO J. Dalton a matéria é formada por átomos / as inúmeras
CONFIGURAÇÃO ELETRÔNICA
 CONFIGURAÇÃO ELETRÔNICA CONFIGURAÇÕES ELETRÔNICAS DOS ÁTOMOS Configuração eletrônica: descreve a estrutura eletrônica de um átomo com todos os orbitais ocupados e o número de elétrons que cada orbital
CONFIGURAÇÃO ELETRÔNICA CONFIGURAÇÕES ELETRÔNICAS DOS ÁTOMOS Configuração eletrônica: descreve a estrutura eletrônica de um átomo com todos os orbitais ocupados e o número de elétrons que cada orbital
Distribuição dos elétrons
 Distribuição dos elétrons Camadas Eletrônicas ou Níveis de Energia A coroa ou eletrosfera está dividida em 7 níveis ou camadas designadas por K, L, M, N, O, P, Q ou pelos números: n = 1, 2, 3, 4, 5, 6,
Distribuição dos elétrons Camadas Eletrônicas ou Níveis de Energia A coroa ou eletrosfera está dividida em 7 níveis ou camadas designadas por K, L, M, N, O, P, Q ou pelos números: n = 1, 2, 3, 4, 5, 6,
QUÍMICA A Ciência Central 9ª Edição Capítulo 6 Estrutura eletrônica dos átomos David P. White
 QUÍMICA A Ciência Central 9ª Edição Capítulo 6 Estrutura eletrônica dos átomos David P. White Natureza ondulatória da luz Todas as ondas têm um comprimento de onda característico, λ, e uma amplitude, A.
QUÍMICA A Ciência Central 9ª Edição Capítulo 6 Estrutura eletrônica dos átomos David P. White Natureza ondulatória da luz Todas as ondas têm um comprimento de onda característico, λ, e uma amplitude, A.
Universidade Federal do Tocantins
 Universidade Federal do Tocantins Modelos atômicos e configurações eletrônicas dos átomos enicolau@uft.edu.br Blog: profedenilsonniculau.wordpress.com Prof. Dr. Edenilson dos Santos Niculau 2 Sumário ESTRUTURA
Universidade Federal do Tocantins Modelos atômicos e configurações eletrônicas dos átomos enicolau@uft.edu.br Blog: profedenilsonniculau.wordpress.com Prof. Dr. Edenilson dos Santos Niculau 2 Sumário ESTRUTURA
Número de onda Segundo Bohr a existência de certas órbitas estáveis para os elétrons dos átomos, com energias bem definidas, chamadas NÍVEIS ENERGÉTIC
 QUÍMICA I AULA 04: ESTRUTURA ELETRÔNICA DOS ÁTOMOS TÓPICO 03: A TEORIA DE BOHR PARA O ÁTOMO DE HIDROGÊNIO 3.1 O ÁTOMO DE BOHR Em 1913, Niels Bohr, tentando conciliar a ideia de Rutherford com as de Planck,
QUÍMICA I AULA 04: ESTRUTURA ELETRÔNICA DOS ÁTOMOS TÓPICO 03: A TEORIA DE BOHR PARA O ÁTOMO DE HIDROGÊNIO 3.1 O ÁTOMO DE BOHR Em 1913, Niels Bohr, tentando conciliar a ideia de Rutherford com as de Planck,
Química Geral Aula 2 Notação científica / atomística
 Química Geral Aula 2 Notação científica / atomística Revisão Sistema internacional de unidades (SI) 2 O que é o SI? É um sistema de unidades de medida concebido em torno de sete unidades básicas: Visa
Química Geral Aula 2 Notação científica / atomística Revisão Sistema internacional de unidades (SI) 2 O que é o SI? É um sistema de unidades de medida concebido em torno de sete unidades básicas: Visa
TEORIA ATÔMICA. Química Geral
 TEORIA ATÔMICA Química Geral 1 Modelo Atômico de Dalton John Dalton 1766 1844: Físico, Químico e Meteorologista inglês Primeira tentativa de relacionar mudanças químicas a eventos que ocorrem ao nível
TEORIA ATÔMICA Química Geral 1 Modelo Atômico de Dalton John Dalton 1766 1844: Físico, Químico e Meteorologista inglês Primeira tentativa de relacionar mudanças químicas a eventos que ocorrem ao nível
2.4 Configuração eletrónica do átomo. Modelo quântico do átomo e configuração eletrónica
 Modelo quântico do átomo e configuração eletrónica Energia dos eletrões Por se moverem incessantemente em torno do núcleo atómico, os eletrões possuem energia cinética. Os eletrões também possuem energia
Modelo quântico do átomo e configuração eletrónica Energia dos eletrões Por se moverem incessantemente em torno do núcleo atómico, os eletrões possuem energia cinética. Os eletrões também possuem energia
DISTRIBUIÇÃO ELETRÔNICA
 DISTRIBUIÇÃO ELETRÔNICA Profª. Regina Modesto Raszl Um problema para os químicos era construir uma teoria consistente que explicasse como os elétrons se distribuíam ao redor dos átomos, dando-lhes as características
DISTRIBUIÇÃO ELETRÔNICA Profª. Regina Modesto Raszl Um problema para os químicos era construir uma teoria consistente que explicasse como os elétrons se distribuíam ao redor dos átomos, dando-lhes as características
UNIVERSIDADE DE SÃO PAULO
 UNIVERSIDADE DE SÃO PAULO - Instituto de Química - Estrutura Atômica As propriedades ondulatórias do elétron Hermi F. Brito hefbrito@iq.usp.br QFL 1101 Química Geral I, -03-2017 Dualidade onda-partícula
UNIVERSIDADE DE SÃO PAULO - Instituto de Química - Estrutura Atômica As propriedades ondulatórias do elétron Hermi F. Brito hefbrito@iq.usp.br QFL 1101 Química Geral I, -03-2017 Dualidade onda-partícula
Leucipo de Mileto (440 a.c.) & Demócrito (460 a.c. 370 a. C.)
 Leucipo de Mileto (440 a.c.) & Demócrito (460 a.c. 370 a. C.) A ideia de dividirmos uma porção qualquer de matéria até chegarmos a uma partícula que não possa ser mais dividida, é muito antiga e surgiu
Leucipo de Mileto (440 a.c.) & Demócrito (460 a.c. 370 a. C.) A ideia de dividirmos uma porção qualquer de matéria até chegarmos a uma partícula que não possa ser mais dividida, é muito antiga e surgiu
Resoluções das atividades
 Resoluções das atividades Sumário apítulo 6 Modelo atômico segundo a Mecânica ndulatória...1 apítulo 7 lassificação periódica dos elementos...4 apítulo 8 Ligações químicas I...8 apítulo 9 Ligações químicas
Resoluções das atividades Sumário apítulo 6 Modelo atômico segundo a Mecânica ndulatória...1 apítulo 7 lassificação periódica dos elementos...4 apítulo 8 Ligações químicas I...8 apítulo 9 Ligações químicas
ATOMÍSTICA ELETROSFERA PARTE 2
 PROJETO KALI - 2016 QUÍMICA AULA 05 ATOMÍSTICA ELETROSFERA PARTE 2 Definições Iniciais: Diagrama: "Um diagrama é uma representação visual estruturada e simplificada de um determinado conceito, ideia, etc."
PROJETO KALI - 2016 QUÍMICA AULA 05 ATOMÍSTICA ELETROSFERA PARTE 2 Definições Iniciais: Diagrama: "Um diagrama é uma representação visual estruturada e simplificada de um determinado conceito, ideia, etc."
Espectros atômicos e níveis de energia Números quânticos Estrutura atômica do Hidrogênio e de. Energia dos orbitais e configurações eletrônicas
 Espectros atômicos e níveis de energia Números quânticos Estrutura atômica do Hidrogênio e de átomos com mais elétrons Energia dos orbitais e configurações eletrônicas Prof a. MarciaM. Meier UNIVERSIDADE
Espectros atômicos e níveis de energia Números quânticos Estrutura atômica do Hidrogênio e de átomos com mais elétrons Energia dos orbitais e configurações eletrônicas Prof a. MarciaM. Meier UNIVERSIDADE
Atomística. Prof. Fernando R. Xavier
 Atomística Prof. Fernando R. Xavier UDESC 2013 Nem sempre foi tão fácil observar um átomo... Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson 400 a.c. até 1897 d.c. O Modelo de
Atomística Prof. Fernando R. Xavier UDESC 2013 Nem sempre foi tão fácil observar um átomo... Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson 400 a.c. até 1897 d.c. O Modelo de
PROPRIEDADES E COMPOSIÇÃO DA MATÉRIA Aula 1
 PROPRIEDADES E COMPOSIÇÃO DA MATÉRIA Aula 1 Matéria: é qualquer coisa que tem massa e ocupa espaço. Átomo: é a menor partícula possível de um elemento químico. É formado por núcleo e eletrosfera. É constituído
PROPRIEDADES E COMPOSIÇÃO DA MATÉRIA Aula 1 Matéria: é qualquer coisa que tem massa e ocupa espaço. Átomo: é a menor partícula possível de um elemento químico. É formado por núcleo e eletrosfera. É constituído
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Temática: Distribuição eletrônica
 Temática: Distribuição eletrônica Nesta aula, você verá que em átomos com poucos elétrons, todos os orbitais da mesma camada têm a mesma energia, entretanto as energias dos orbitais dos átomos com muitos
Temática: Distribuição eletrônica Nesta aula, você verá que em átomos com poucos elétrons, todos os orbitais da mesma camada têm a mesma energia, entretanto as energias dos orbitais dos átomos com muitos
estrutura atômica e ligações
 Aula 02 estrutura atômica e ligações ZEA 1038 Ciência e Tecnologia dos Materiais Prof. João Adriano Rossignolo Profa. Eliria M.J.A. Pallone introdução conceitos elementares a estrutura dos átomos a estrutura
Aula 02 estrutura atômica e ligações ZEA 1038 Ciência e Tecnologia dos Materiais Prof. João Adriano Rossignolo Profa. Eliria M.J.A. Pallone introdução conceitos elementares a estrutura dos átomos a estrutura
Aula 13 - Capítulo 38 Fótons e Ondas de Matéria
 Aula 13 - Capítulo 38 Fótons e Ondas de Matéria Física 4 Ref. Halliday Volume4 Sumário Elétrons e Ondas de Matéria A Equação de Schrödinger Determinação da Densidade de Probabilidade 2 Elétrons e Ondas
Aula 13 - Capítulo 38 Fótons e Ondas de Matéria Física 4 Ref. Halliday Volume4 Sumário Elétrons e Ondas de Matéria A Equação de Schrödinger Determinação da Densidade de Probabilidade 2 Elétrons e Ondas
Física dos Materiais
 Física dos Materiais 4300502 1º Semestre de 2016 Instituto de Física Universidade de São Paulo Professor: Luiz C C M Nagamine E-mail: nagamine@if.usp.br Fone: 3091.6877 homepagehttp://disciplinas.stoa.usp.br/course/view.php?id=10070
Física dos Materiais 4300502 1º Semestre de 2016 Instituto de Física Universidade de São Paulo Professor: Luiz C C M Nagamine E-mail: nagamine@if.usp.br Fone: 3091.6877 homepagehttp://disciplinas.stoa.usp.br/course/view.php?id=10070
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Exercícios Sobre DistribuiÇão eletrônica
 Exercícios Sobre DistribuiÇão eletrônica Dado: 01. Faça a distribuição eletrônica nas camadas para os átomos: a) Cs (Z= 55) b) Tl (Z= 81) 02. Faça a distribuição eletrônica nas camadas, para os átomos:
Exercícios Sobre DistribuiÇão eletrônica Dado: 01. Faça a distribuição eletrônica nas camadas para os átomos: a) Cs (Z= 55) b) Tl (Z= 81) 02. Faça a distribuição eletrônica nas camadas, para os átomos:
Estrutura dos Materiais. e Engenharia dos Materiais Prof. Douglas Gouvêa
 Ligações Químicas e Estrutura dos Materiais PMT 5783 - Fundamentos de Ciência e Engenharia dos Materiais Prof. Douglas Gouvêa Objetivos Descrever a estrutura atômica e suas conseqüências no tipo de ligação
Ligações Químicas e Estrutura dos Materiais PMT 5783 - Fundamentos de Ciência e Engenharia dos Materiais Prof. Douglas Gouvêa Objetivos Descrever a estrutura atômica e suas conseqüências no tipo de ligação
QUÍMICA ÁTOMOS. Professor: Rafael Odorico
 QUÍMICA ÁTOMOS MODELO DE DALTON A matéria é formada por partículas extremamente pequenas chamadas átomos; Os átomos são esferas maciças e indivisíveis; Os átomos com as mesmas propriedades, constituem
QUÍMICA ÁTOMOS MODELO DE DALTON A matéria é formada por partículas extremamente pequenas chamadas átomos; Os átomos são esferas maciças e indivisíveis; Os átomos com as mesmas propriedades, constituem
Apostila de Química (3º bimestre-2009) Professor: Eduardo Mesquita 1º ano Ensino Médio. Números Quânticos e Diagrama de Pauling;
 Apostila de Química (3º bimestre-2009) Professor: Eduardo Mesquita 1º ano Ensino Médio Números Quânticos e Diagrama de Pauling; Número quântico principal (n): indica o nível de energia do elétron no átomo.
Apostila de Química (3º bimestre-2009) Professor: Eduardo Mesquita 1º ano Ensino Médio Números Quânticos e Diagrama de Pauling; Número quântico principal (n): indica o nível de energia do elétron no átomo.
O átomo de Rutherford
 O átomo de Rutherford Elétrons orbitando o núcleo F Elétrica F Centrifúga Quando uma carga elétrica muda de velocidade ou direção, ela deve irradiar energia. Radiação Eletromagnética É o produto de campos
O átomo de Rutherford Elétrons orbitando o núcleo F Elétrica F Centrifúga Quando uma carga elétrica muda de velocidade ou direção, ela deve irradiar energia. Radiação Eletromagnética É o produto de campos
Configuração Eletrônica
 Configuração Eletrônica Reis, Oswaldo Henrique Barolli. R375c Configuração eletrônica / Oswaldo Henrique Barolli. Varginha, 2015. 21 slides. Sistema requerido: Adobe Acrobat Reader Modo de Acesso: World
Configuração Eletrônica Reis, Oswaldo Henrique Barolli. R375c Configuração eletrônica / Oswaldo Henrique Barolli. Varginha, 2015. 21 slides. Sistema requerido: Adobe Acrobat Reader Modo de Acesso: World
Níveis de energia do átomo
 Níveis de energia do átomo Para um átomo de hidrogénio, a energia das orbitas é: 13.6 ev E n = n 2 Quando um eletrão salta de uma órbita para outra absorve ou perde energia: Δ E=E i E j = 13.6 ev ( 1 n
Níveis de energia do átomo Para um átomo de hidrogénio, a energia das orbitas é: 13.6 ev E n = n 2 Quando um eletrão salta de uma órbita para outra absorve ou perde energia: Δ E=E i E j = 13.6 ev ( 1 n
ÁTOMOS MULTIELETRÔNICOS. QFL-4010 Prof. Gianluca C. Azzellini
 ÁTOMOS MULTIELETRÔNICOS Número Quântico de Spin (m s ) m s = Representa o sentido de rotação do elétron no próprio eixo. m s = +1/2 e 1/2 Experimento Stern-Gerlach Vapor de átomos metálicos Números Quânticos
ÁTOMOS MULTIELETRÔNICOS Número Quântico de Spin (m s ) m s = Representa o sentido de rotação do elétron no próprio eixo. m s = +1/2 e 1/2 Experimento Stern-Gerlach Vapor de átomos metálicos Números Quânticos
Equação de Onda de Schrödinger
 Equação de Onda de Schrödinger Em 1926, Schrödinger escreveu uma equação que descrevia simulteamente a natureza ondulatória e corpuscular do electrão. A função de onda Ψ (psi) descreve: 1. Energia de e
Equação de Onda de Schrödinger Em 1926, Schrödinger escreveu uma equação que descrevia simulteamente a natureza ondulatória e corpuscular do electrão. A função de onda Ψ (psi) descreve: 1. Energia de e
1.2.8 Configuração eletrónica de átomos
 1.2.8 Configuração eletrónica de átomos Adaptado pelo Prof. Luís Perna Princípio de Eclusão de Pauli Cada orbital comporta no máimo dois eletrões, os quais diferem no estado de spin: spin α e spin β. Wolfgang
1.2.8 Configuração eletrónica de átomos Adaptado pelo Prof. Luís Perna Princípio de Eclusão de Pauli Cada orbital comporta no máimo dois eletrões, os quais diferem no estado de spin: spin α e spin β. Wolfgang
N P P N. Ciências de Materiais I Prof. Nilson C. Cruz. Aula 2 Ligação Química. Átomos. Diferença entre materiais = Diferença entre arranjos atômicos e
 Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
11Na 12Mg 15P 16S 17Cl 19K 20Ca. 24Cr 25Mn 26Fe 27Co 29Cu .../.../... TRO TEC CVI TURMA M V N
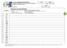 CINAT COORDENADORIA DE QUÍMICA Química I (Inorgânica) 1º semestre 2015 Prof. Éder C. Assunto: Reavaliação 1ª Etapa. DATA CURSO.../.../... TRO TEC CVI Lista: 1h TURMA M V N Z 1 6 7 8 11 12 15 16 17 19 20
CINAT COORDENADORIA DE QUÍMICA Química I (Inorgânica) 1º semestre 2015 Prof. Éder C. Assunto: Reavaliação 1ª Etapa. DATA CURSO.../.../... TRO TEC CVI Lista: 1h TURMA M V N Z 1 6 7 8 11 12 15 16 17 19 20
Química A Extensivo V. 2
 Química A Extensivo V. 2 01) Alternativa correta: B Exercícios a) Errada ao mudar de órbita, o elétrons emite ou absorve energia igual a diferença de energia entre as órbitas; b) Certa; c) Errada de acordo
Química A Extensivo V. 2 01) Alternativa correta: B Exercícios a) Errada ao mudar de órbita, o elétrons emite ou absorve energia igual a diferença de energia entre as órbitas; b) Certa; c) Errada de acordo
Química A Extensivo V. 2
 Química A Extensivo V. 2 Exercícios 01) B 02) A a) Errada. Ao mudar de órbita, os elétrons emite ou absorve energia igual à diferença de energia entre as órbitas. b) Certa. c) Errada. De acordo com a teoria
Química A Extensivo V. 2 Exercícios 01) B 02) A a) Errada. Ao mudar de órbita, os elétrons emite ou absorve energia igual à diferença de energia entre as órbitas. b) Certa. c) Errada. De acordo com a teoria
Estrutura da Matéria Profª Fanny Nascimento Costa
 Estrutura da Matéria Profª Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 08 Átomos multieletrônicos; Spin; Princípio da exclusão de Pauli; Periodicidade Onde está o elétron? https://www.youtube.com/watch?v=8rohpz0a70i
Estrutura da Matéria Profª Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 08 Átomos multieletrônicos; Spin; Princípio da exclusão de Pauli; Periodicidade Onde está o elétron? https://www.youtube.com/watch?v=8rohpz0a70i
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Química A Semiextensivo V. 1
 Química A Semiextensivo V. 1 Exercícios 01) D 02) A a) Errada. A teoria de Dalton não incluía partículas ou cargas elétricas (modelo de bola de bilhar). b) Errada. Essa descrição corresponde à teoria de
Química A Semiextensivo V. 1 Exercícios 01) D 02) A a) Errada. A teoria de Dalton não incluía partículas ou cargas elétricas (modelo de bola de bilhar). b) Errada. Essa descrição corresponde à teoria de
ESTUDO DO ÁTOMO. entre parênteses da equação - e da energia potencial, representando, desta maneira, a energia mecânica.
 ESTUDO DO ÁTOMO 1. Modelo dos Orbitais Atômicos (Modelo Atual) O elétron se comporta ora como partícula, ora como onda, dependendo do tipo de experiência. Devemos assim, entender o elétron como um elemento
ESTUDO DO ÁTOMO 1. Modelo dos Orbitais Atômicos (Modelo Atual) O elétron se comporta ora como partícula, ora como onda, dependendo do tipo de experiência. Devemos assim, entender o elétron como um elemento
Exercícios sobre distribuição eletrônica
 Exercícios sobre distribuição eletrônica Dado: 01. Faça a distribuição eletrônica nas camadas para os átomos: a) Cs (Z = 55) b) T (Z = 81) 0. Faça a distribuição eletrônica nas camadas, para os átomos:
Exercícios sobre distribuição eletrônica Dado: 01. Faça a distribuição eletrônica nas camadas para os átomos: a) Cs (Z = 55) b) T (Z = 81) 0. Faça a distribuição eletrônica nas camadas, para os átomos:
Estrutura Atômica. Clique para editar o estilo do subtítulo mestre
 Estrutura Atômica Clique para editar o estilo do subtítulo mestre Evolução dos Modelos Atômicos 1º) Demócrito e Leucipo (400 a 500 a.c) -filósofos gregos -átomo indivisível. 2º) Modelo Atômico de Dalton
Estrutura Atômica Clique para editar o estilo do subtítulo mestre Evolução dos Modelos Atômicos 1º) Demócrito e Leucipo (400 a 500 a.c) -filósofos gregos -átomo indivisível. 2º) Modelo Atômico de Dalton
QUÍMICA. A) do egípcio kēme ( chem ) = TERRA; B) do árabe AL-Khemy (alquimia) = QUÍMICA
 QUÍMICA A) do egípcio kēme ( chem ) = TERRA; B) do árabe AL-Khemy (alquimia) = QUÍMICA QUÍMICA - É a ciência que estuda a matéria e suas transformações ; - Estuda as interações com as substâncias e energia
QUÍMICA A) do egípcio kēme ( chem ) = TERRA; B) do árabe AL-Khemy (alquimia) = QUÍMICA QUÍMICA - É a ciência que estuda a matéria e suas transformações ; - Estuda as interações com as substâncias e energia
Aula 13 - Capítulo 38 Fótons e Ondas de Matéria
 Aula 13 - Capítulo 38 Fótons e Ondas de Matéria Física 4 Ref. Halliday Volume4 Sumário Elétrons e Ondas de Matéria A Equação de Schrödinger Determinação da Densidade de Probabilidade 2 Elétrons e Ondas
Aula 13 - Capítulo 38 Fótons e Ondas de Matéria Física 4 Ref. Halliday Volume4 Sumário Elétrons e Ondas de Matéria A Equação de Schrödinger Determinação da Densidade de Probabilidade 2 Elétrons e Ondas
Lista de Exercícios Química Geral I Licenciatura em Química Prof. Udo Sinks
 Estrutura Atomica Equação de Planck 1. A luz verde tem um comprimento de onda de 5,0 x 10 2 nm. Qual é a energia em joules de um fóton de luz verde? Qual é a energia em joules de 1,0 mol de fótons de luz
Estrutura Atomica Equação de Planck 1. A luz verde tem um comprimento de onda de 5,0 x 10 2 nm. Qual é a energia em joules de um fóton de luz verde? Qual é a energia em joules de 1,0 mol de fótons de luz
NOVOS AVANÇOS NA TEORIA ATÔMICA
 Disciplina: Química Prof.: Guilherme Turma: IU 20/ 04/2017 Tema da aula: Modelo Atômico de Bohr e Distribuição Eletrônica O desenvolvimento da teoria atômica NOVOS AVANÇOS NA TEORIA ATÔMICA - Ao longo
Disciplina: Química Prof.: Guilherme Turma: IU 20/ 04/2017 Tema da aula: Modelo Atômico de Bohr e Distribuição Eletrônica O desenvolvimento da teoria atômica NOVOS AVANÇOS NA TEORIA ATÔMICA - Ao longo
Estrutura da Matéria Lista 3
 Estrutura da Matéria - 2018.2 Lista 3 1. Em 1820, o filósofo Auguste Comte declarou ser possível ao ser humano saber sobre tudo, menos do que são feitas as estrelas. Ele estava correto? Como os astrofísicos
Estrutura da Matéria - 2018.2 Lista 3 1. Em 1820, o filósofo Auguste Comte declarou ser possível ao ser humano saber sobre tudo, menos do que são feitas as estrelas. Ele estava correto? Como os astrofísicos
Universidade Federal de Sergipe Departamento de Química. Disciplina de Química I. Prof. Dr. Adriano Bof de Oliveira. São Cristóvão, 2011
 Universidade Federal de Sergipe Departamento de Química Disciplina de Química I Prof. Dr. Adriano Bof de Oliveira São Cristóvão, 2011 Avaliações Datas: 21 e 29 de julho Locais: Didática 4 Turma M1 Sala
Universidade Federal de Sergipe Departamento de Química Disciplina de Química I Prof. Dr. Adriano Bof de Oliveira São Cristóvão, 2011 Avaliações Datas: 21 e 29 de julho Locais: Didática 4 Turma M1 Sala
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Modelo quântico. 10º ano. [Imagem: Quantum Atomica software]
![Modelo quântico. 10º ano. [Imagem: Quantum Atomica software] Modelo quântico. 10º ano. [Imagem: Quantum Atomica software]](/thumbs/82/86423832.jpg) [Imagem: Quantum Atomica software] Modelo atómico de Bohr Os eletrões só podem ocupar níveis de energia bem definidos Quantização da energia. Os eletrões giram em torno do núcleo em órbitas com energias
[Imagem: Quantum Atomica software] Modelo atómico de Bohr Os eletrões só podem ocupar níveis de energia bem definidos Quantização da energia. Os eletrões giram em torno do núcleo em órbitas com energias
ÁTOMO: núcleo muito pequeno composto por prótons e nêutrons, que é circundado por elétrons em movimento;
 1.1 CONCEITOS FUNDAMENTAIS ÁTOMO: núcleo muito pequeno composto por prótons e nêutrons, que é circundado por elétrons em movimento; Elétrons e prótons são eletricamente carregados: 1,60 x 10-19 C; Elétrons:
1.1 CONCEITOS FUNDAMENTAIS ÁTOMO: núcleo muito pequeno composto por prótons e nêutrons, que é circundado por elétrons em movimento; Elétrons e prótons são eletricamente carregados: 1,60 x 10-19 C; Elétrons:
SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito)
 SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito) 1 - (UFPR) - Considere um elemento químico (E) com número atômico (Z) igual a 16. a) Qual sua configuração eletrônica para o estado fundamental? a) 1s
SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito) 1 - (UFPR) - Considere um elemento químico (E) com número atômico (Z) igual a 16. a) Qual sua configuração eletrônica para o estado fundamental? a) 1s
Comportamento ondulatório da matéria
 Louis de Broglie investigou as propriedades ondulatórias da na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tina associado a ele um λ. Ele igualou as duas expressões conecidas
Louis de Broglie investigou as propriedades ondulatórias da na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tina associado a ele um λ. Ele igualou as duas expressões conecidas
Aula 12- Íons, níveis e subníveis eletrônicos e a distribuição eletrônica
 Aula 12- Íons, níveis e subníveis eletrônicos e a distribuição eletrônica Nas nossas aulas passadas nós vimos que cada elemento químico é caracterizado pelo seu número atômico (Z). Vimos também que um
Aula 12- Íons, níveis e subníveis eletrônicos e a distribuição eletrônica Nas nossas aulas passadas nós vimos que cada elemento químico é caracterizado pelo seu número atômico (Z). Vimos também que um
