Soluções de Conjunto de Problemas 1
|
|
|
- Bento Mendonça Canário
- 9 Há anos
- Visualizações:
Transcrição
1 Soluções de Conjunto de Problemas 1 Questão 1 a) Quais são os quatro tipos principais de moléculas biológicas discutidos na aula? Cite uma função importante de cada tipo de molécula biológica na célula. Fosfolipídeos: formam as camadas duplas que são as membranas da célula. Carboidratos: açúcares simples que fornecem energia para os processos celulares; a celulose polimerizada atua como um componente estrutural e o glicogênio polimerizado atua como armazenador de energia. Proteínas: São responsáveis por praticamente todas as funções celulares; enzimas para trajetos metabólicos, proteínas estruturais para a estrutura das células, proteínas de membrana para a regulagem das células, reconhecimentos de células e transporte de moléculas para dentro e fora da célula. Ácidos Nucléicos: armazenamento e transferência de material genético. b) Responda brevemente as questões a seguir. i) Quais são as duas principais diferenças entre as células procarióticas e eucarióticas? As células procarióticas não têm um núcleo, ao passo que as eucarióticas têm. Em termos de evolução, as células procarióticas são mais antigas que as eucarióticas. As células eucarióticas têm organelas e membranas internas, as procarióticas não. ii) Qual é a diferença entre organismos unicelulares e multicelulares? Organismos unicelulares vivem e se reproduzem como células isoladas. Cada célula tem o mesmo DNA e a mesma aparência. Organismos multicelulares são compostos por várias células. Cada célula em um organismo multicelular tem o mesmo DNA, porém as células têm aparências diferentes. iii) Os procariotas são unicelulares ou multicelulares? E os eucariotas? Procariotas são unicelulares. Eucariotas podem ser organismos multicelulares ou unicelulares.
2 Questão 1, continuação c) Para os pares de aminoácidos abaixo, faça um círculo em torno de cada cadeia lateral. Forneça o tipo mais forte de interação que ocorre entre os grupos de cadeias laterais de cada par. Aminoácidos Interação GLICINA GLUTAMINA van der Waals TIROSINA ASPARAGINA hidrogênio ÁCIDO GLUTÂMICO LISINA iônica d) Desenhe a estrutura química do polipeptídeo a seguir em ph 7. cisteína-alanina-tirosina-fenilalanina e) Na estrutura desenhada acima, faça um círculo em torno de uma ligação peptídica. Soluções de Conjunto de Problemas 1 2
3 Questão 2 A droga Minoxidil é utilizada por via oral como um agente contra hipertensão e de forma tópica como um estimulante para o crescimento capilar. A estrutura do Minoxidil é mostrada a seguir. *O Minoxidil não apresenta carga em seu estado ativo Minoxidil a) Um esquema do local de ligação do Minoxidil em uma proteína hipotética é mostrado abaixo. i) Desenhe as cadeias laterais nas posições dos aminoácidos 51, 129, 134 e 167. ii) Desenhe o Minoxidil, como mostrado acima, ligando-se no local. Certifique-se de considerar as interações entre o Minoxidil e as cadeias laterais, ao orientá-lo dentro do local de ligação. Soluções de Conjunto de Problemas 1 3
4 Questão 2, continuação b) Liste todas as interações que ocorreriam entre os aminoácidos especificados e o Minoxidil no modelo que você propôs, preenchendo a tabela abaixo. Aminoácido Glu 51 Val 129 Leu 134 Asn 167 Interações com o Minoxidil ligação de hidrogênio, van der Waals van der Waals, hidrofóbica van der Waals, hidrofóbica ligação de hidrogênio, van der Waals c) Para decidir se o seu modelo está correto, você constrói algumas versões alteradas dessa proteína e testa se o Minoxidil ainda se liga. Suponha que todos os outros aminoácidos permanecem inalterados. Os resultados são os seguintes: Proteína Posição 51 Posição 129 Posição 134 Posição 167 Liga? normal Glu 51 Val 129 Leu 134 Asn 167 sim variante 1 Asp 51 Val 129 Leu 134 Asn 167 sim variante 2 Gly 51 Val 129 Leu 134 Asn 167 sim variante 3 Gly 51 Val 129 Leu 134 Ala 167 não variante 4 Glu 51 Lys 129 Leu 134 Ala 167 não variante 5 Glu 51 Phe 129 Leu 134 Asn 167 sim Das possíveis orientações para o Minoxidil no local de ligação, somente uma orientação é consistente com os resultados acima. Verifique o seu modelo cuidadosamente, revise-o se necessário e responda as questões a seguir. No modelo proposto aqui, as características importantes são a ligação de hidrogênio do Minoxidil com Glu51 e Asn167 e a posição do anel hidrofóbico de Minoxidil na bolsa hidrofóbica próxima a Val129 e Leu134. Se você orientou o Minoxidil de alguma outra forma na bolsa, somente as forças de van der Waals existem entre os resíduos do Minoxidil e as alterações acima ainda permitiriam essas forças. Explique em termos de seu modelo e das prováveis interações por que... i) a variante 2 ligará o Minoxidil, mas a variante 3 não. Na variante 2, uma das duas ligações de hidrogênio permanece, assim como a bolsa hidrofóbica, considerando a informação de que isso é suficiente para permitir a ligação. Na variante 3, as duas ligações de hidrogênio teriam sido perdidas e isso interrompe a ligação. ii) a variante 5 ligará o Minoxidil, mas a variante 4 não. Na variante 4, um aminoácido hidrofóbico é substituído por um aminoácido carregado que interrompe a bolsa hidrofóbica. As substituições na variante 5 não interrompem as interações hidrofóbicas. Soluções de Conjunto de Problemas 1 4
5 Questão 3 Os receptores do fator de crescimento (mostrados abaixo) são proteínas de transmembrana encontradas na superfície celular. extracelular Membrana intracelular receptores do fator de crescimento a) A maior parte das moléculas que constituem a membrana acima pertence a qual classe de macromoléculas? fosfolipídeos Explique as qualidades/propriedades importantes dessas moléculas, as quais permitem que elas formem membranas. Os fosfolipídeos possuem cabeças hidrofílicas e caudas hidrofóbicas que permitem sua montagem em duas camadas contendo um núcleo hidrofóbico quando em meio aquoso. Soluções de Conjunto de Problemas 1 5
6 Questão 3, continuação Um pequeno diagrama esquemático do receptor do fator de crescimento é mostrado abaixo. região transmembrana A seqüência dessa região é mostrada abaixo b) Qual trecho dos aminoácidos na seqüência acima é parte da região transmembrana do receptor? Faça um círculo nesses aminoácidos e explique brevemente o seu raciocínio. Esse trecho contém aminoácidos que são não-polares ou hidrofóbicos, os quais prontamente residiriam no ambiente hidrofóbico da membrana. Quando o fator do crescimento se liga ao domínio extracelular do receptor, uma mudança de conformação ocorre no receptor. A ligação do fator do crescimento causa a dimerização de dois receptores adjacentes na membrana da célula. Após a dimerização, os domínios intracelulares dos receptores se tornam ativos. Veja esquema abaixo. domínio ligandoligação extracelular membrana plasmática domínio intracelular ligando ligando Receptor 1 Receptor 2 domínios inativos domínios ativos Soluções de Conjunto de Problemas 1 6
7 Questão 3, continuação As regiões dos dois receptores que interagem na dimerização estão desenhadas abaixo. Nas partes (i iv) abaixo, nomeie o tipo mais forte de interação (escolha entre: ligação de hidrogênio, iônica, covalente e van der Waals) ocorrendo entre as cadeias laterais dos aminoácidos indicados. Receptor 1 Receptor 2 Cadeias laterais interagindo Tipo de Interação i) Phe50 : Val98 van der Waals ii) Asp68 : Lys65 iônica iii) Cys75 : Cys82 covalente iv) Ser53 : Gln12 hidrogênio d) Explique como o Gln12 e o Val98, tão distantes na seqüência primária da proteína, podem estar próximos entre si na região da proteína diagramada acima. Quando a proteína se incorpora em sua forma final, os resíduos de aminoácidos longe da estrutura primária podem ser alinhados próximos uns aos outros. Soluções de Conjunto de Problemas 1 7
8 Soluções de Conjunto de Problemas 1 8
9 Questão 3, continuação e) As interações moleculares entre os dois receptores são importantes para a dimerização. Dessa forma, a substituição de certos aminoácidos na proteína pode afetar a dimerização do receptor. Estime se os receptores serão capazes ou não de dimerizar considerando as substituições (i iv) abaixo. EXPLIQUE seu raciocínio. i) Asp68 Arg: Os receptores não serão capazes de dimerizar porque isso significa a substituição de um aminoácido com carga negativa por um de carga positiva. A ligação iônica entre o Asp68 e o Lys65 é interrompida, ocorrendo uma repulsão. ii) Ser53 Thr: Os receptores serão capazes de dimerizar porque isso significa a substituição de um aminoácido polar que pode participar nas ligações de hidrogênio com outro aminoácido do mesmo tipo. iii) Phe50 Asn: Os receptores serão capazes de dimerizar mesmo que isso signifique a substituição de um ácido hidrofóbico por um aminoácido polar, pois as forças de van der Waals permanecem. (Dentro da região diagramada, a proximidade das espécies carregadas torna improvável a atuação das interações hidrofóbicas como uma força importante na interação entre dois receptores.) iv) Val98 Ile: Os receptores serão capazes de dimerizar porque isso significa a substituição de um ácido hidrofóbico por outro aminoácido do mesmo tipo. As forças de van der Waals permanecem. e) A substituição de um aminoácido, Cys75 Gly, leva à dimerização dos receptores com ou sem o fator do crescimento. Forneça uma breve explicação para essa observação. Essa substituição posiciona dois resíduos de cisteína em oposição entre si. Esses dois resíduos podem formar uma ligação de dissulfeto e, portanto, ligar os dois receptores entre si. Soluções de Conjunto de Problemas 1 9
10 Questão 4 A reação a seguir é o décimo e último passo na glicólise: piruvato cinase Fosfoenolpiruvato + ADP < > piruvato + ATP DG = -7,5 kcal/mol a) Calcule Keq para essa reação sob as condições padrão a 25ºC e faça um círculo na afirmação correta a seguir. G = G 0 + RT ln ([produtos]/[reagentes]) no equilíbrio, G = 0 e Keq = ([produtos]/[reagentes]) portanto G 0 = -RT ln (Keq) Dessa forma: -7,5 kcal / mol = -0,59 kcal / mol ln (Keq) 12,7 = ln (Keq) Keq = e 12,7 Keq = 3,3 x 10 5 No equilíbrio, [fosfoenolpiruvato] > [piruvato] No equilíbrio, [fosfoenolpiruvato] < [piruvato] b) As concentrações a seguir são encontradas nos glóbulos vermelhos do sangue. Calcule G para a reação a 37ºC. Em qual direção essa reação prosseguirá de forma espontânea? [ADP] = 10 mm [ATP] = 81 mm [fosfoenolpiruvato] = 10 mm [piruvato] = 500 nm G = G 0 + RT ln ([produtos]/[reagentes]) G = -7,5 kcal / mol +0,61 kcal / mol x ln (500 x 81)/ (10 x10) G = -3,84 kcal / mol A reação é espontânea da esquerda para a direita: Fosfoenolpiruvato + ADP > piruvato + ATP Soluções de Conjunto de Problemas 1 10
11 Questão 4, continuação c) Desenhe o perfil de energia para essa reação sob condições fisiológicas. No diagrama, certifiquese de: 1) mostrar os níveis relativos de energia dos reagentes e produtos. 2) rotule os eixos 3) rotule reagentes e produtos 4) indique a energia de ativação 5) indique G Energia Livre (G) kcal / mol fosfoenolpiruvato +ATP Energia de ativação piruvato +ADP Andamento da Reação d) Como o piruvato cinase ( a enzima que catalisa essa reação) altera o perfil de energia? A enzima somente reduz a energia de ativação. Ela não altera a energia livre dos reagentes, produtos ou da reação geral. Soluções de Conjunto de Problemas 1 11
12 ESTRUTURAS DOS AMINOÁCIDOS em ph 7,0 ALANINA ARGININA ASPARAGINA ÁCIDO ASPÁRTICO (ala) (arg) (asn) (asp) CISTEÍNA ÁCIDO GLUTÂMICO GLUTAMINA GLICINA (cys) (glu) (gln) (gly) HISTIDINA ISOLEUCINA LEUCINA LISINA (his) (ile) (leu) (lys) METIONINA FENILALANINA PROLINA SERINA (met) (phe) (pro) (ser) TREONINA TRIPTOFAN TIROSINA VALINA (thr) (trp) (tyr) (val) Soluções de Conjunto de Problemas 1 12
13 Para a reação: com G 0 como sua energia livre padrão no equilíbrio: ou onde: se T = 25ºC então se T = 37ºC então sob quaisquer condições: Cinética Enzimática: Para a reação catalisada por enzima: na qual: S = Substrato E = enzima P = produto a velocidade da reação é fornecida por na qual: e Soluções de Conjunto de Problemas 1 13
Soluções para Conjunto de Problemas 1
 Soluções para 7.012 Conjunto de Problemas 1 Pergunta 1 a) Quais são os quatro principais tipos de moléculas biológicas discutidas na palestra? Cite uma função importante para cada tipo de molécula biológica
Soluções para 7.012 Conjunto de Problemas 1 Pergunta 1 a) Quais são os quatro principais tipos de moléculas biológicas discutidas na palestra? Cite uma função importante para cada tipo de molécula biológica
Aminoácidos peptídeos e proteínas
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc [email protected] Algumas funções de proteínas A luz produzida
Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc [email protected] Algumas funções de proteínas A luz produzida
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA. Aminoácidos. Prof. Willame Bezerra
 CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
Aminoácidos não-essenciais: alanina, ácido aspártico, ácido glutâmico, cisteína, glicina, glutamina, hidroxiprolina, prolina, serina e tirosina.
 AMINOÁCIDOS Os aminoácidos são as unidades fundamentais das PROTEÍNAS. Existem cerca de 300 aminoácidos na natureza, mas nas proteínas podemos encontrar 20 aminoácidos principais Estruturalmente são formados
AMINOÁCIDOS Os aminoácidos são as unidades fundamentais das PROTEÍNAS. Existem cerca de 300 aminoácidos na natureza, mas nas proteínas podemos encontrar 20 aminoácidos principais Estruturalmente são formados
Programa de Pós-Graduação em Química
 1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
14/02/2017. Genética. Professora Catarina
 14/02/2017 Genética Professora Catarina 1 A espécie humana Ácidos nucleicos Tipos DNA ácido desoxirribonucleico RNA ácido ribonucleico São formados pela união de nucleotídeos. 2 Composição dos nucleotídeos
14/02/2017 Genética Professora Catarina 1 A espécie humana Ácidos nucleicos Tipos DNA ácido desoxirribonucleico RNA ácido ribonucleico São formados pela união de nucleotídeos. 2 Composição dos nucleotídeos
Aminoácidos. Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP.
 Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
13/08/2018. Escala de ph. Escala de ph. Crescimento básico. Crescimento ácido. Neutro. básico
 Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs
 Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
Aula 1. Referência. Bancos de Dados. Linguagem x Informação. Introdução a Bioquímica: Biomoléculas. Introdução ao Curso: Aminoácidos.
 Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao urso: Aminoácidos eferência Autores: Ignez aracelli e Julio Zukerman-Schpector Editora: EdUFSar Ignez aracelli BioMat DF UNESP/Bauru Julio Zukerman
Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao urso: Aminoácidos eferência Autores: Ignez aracelli e Julio Zukerman-Schpector Editora: EdUFSar Ignez aracelli BioMat DF UNESP/Bauru Julio Zukerman
RMN em proteínas pequenas
 COSY COrrelated SpectroscopY Experimento 2D homonuclear ( 1 H- 1 H) mais simples Primeiro experimento 2D proposto (Jeener, 1971) Período de mistura: 1 único pulso de 90 Transferência da coerência entre
COSY COrrelated SpectroscopY Experimento 2D homonuclear ( 1 H- 1 H) mais simples Primeiro experimento 2D proposto (Jeener, 1971) Período de mistura: 1 único pulso de 90 Transferência da coerência entre
COLÉGIO PEDRO II CAMPUS TIJUCA II. DEPARTAMENTO DE BIOLOGIA E CIÊNCIAS COORD.: PROFa. CRISTIANA LIMONGI
 COLÉGIO PEDRO II CAMPUS TIJUCA II DEPARTAMENTO DE BIOLOGIA E CIÊNCIAS COORD.: PROFa. CRISTIANA LIMONGI 1º & 2º TURNOS 3ª SÉRIE / ENSINO MÉDIO REGULAR & INTEGRADO ANO LETIVO 2015 PROFESSORES: FRED & PEDRO
COLÉGIO PEDRO II CAMPUS TIJUCA II DEPARTAMENTO DE BIOLOGIA E CIÊNCIAS COORD.: PROFa. CRISTIANA LIMONGI 1º & 2º TURNOS 3ª SÉRIE / ENSINO MÉDIO REGULAR & INTEGRADO ANO LETIVO 2015 PROFESSORES: FRED & PEDRO
- Apresentam uma fórmula básica: um átomo central de carbono onde se ligam:
 1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
Aminoácidos FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Aminoácidos Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Introdução Proteínas são as macromoléculas
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Aminoácidos Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Introdução Proteínas são as macromoléculas
Introdução. Estrutura dos Aminoácidos e Proteínas. Aminoácidos componentes de proteínas. Aminoácidos componentes de proteínas 10/02/2012.
 Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
REVISÃO: ENADE BIOQUÍMICA - 1
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
Professor Antônio Ruas
 Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
CÓDIGO GENÉTICO E SÍNTESE PROTEICA
 Terceirão Biologia 1 Professor João CÓDIGO GENÉTICO E SÍNTESE PROTEICA 1. Síntese de proteínas pelos ribossomos a partir do RNAm. a) RNAm: molécula de RNA que contem a informação genética necessária para
Terceirão Biologia 1 Professor João CÓDIGO GENÉTICO E SÍNTESE PROTEICA 1. Síntese de proteínas pelos ribossomos a partir do RNAm. a) RNAm: molécula de RNA que contem a informação genética necessária para
Rafael Mesquita. Aminoácidos
 Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
UFABC Bacharelado em Ciência & Tecnologia
 UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades, funções e transformações de aminoácidos e proteínas
UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades, funções e transformações de aminoácidos e proteínas
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011
 BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
Professor Antônio Ruas
 Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
BIOLOGIA EXERCÍCIOS. Anabolismo Nuclear
 Anabolismo Nuclear EXERCÍCIOS 1. mesmo responsável pela decodificação do genoma humano em 2001, o presidente dos EUA, Barack Obama, pediu a seus conselheiros especializados em biotecnologia para analisarem
Anabolismo Nuclear EXERCÍCIOS 1. mesmo responsável pela decodificação do genoma humano em 2001, o presidente dos EUA, Barack Obama, pediu a seus conselheiros especializados em biotecnologia para analisarem
Biologia Molecular (Parte I)
 Biologia Molecular (Parte I) Introdução 1. Substâncias Inorgânicas 1.1. Água A água faz pontes de hidrogênio Polaridade Propriedades da água Solvente Universal Participa de reações químicas vitais Adesão
Biologia Molecular (Parte I) Introdução 1. Substâncias Inorgânicas 1.1. Água A água faz pontes de hidrogênio Polaridade Propriedades da água Solvente Universal Participa de reações químicas vitais Adesão
Composição química celular
 Natália Paludetto Composição química celular Proteínas Enzimas Ácidos nucléicos Proteínas Substâncias sólidas; Componente orgânico mais abundante da célula. Podem fornecer energia quando oxidadas, mas
Natália Paludetto Composição química celular Proteínas Enzimas Ácidos nucléicos Proteínas Substâncias sólidas; Componente orgânico mais abundante da célula. Podem fornecer energia quando oxidadas, mas
Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia REVISÃO QUÍMICA Principais grupos funcionais em proteômica O que é uma ligação de hidrogênio? átomo eletronegativo
Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia REVISÃO QUÍMICA Principais grupos funcionais em proteômica O que é uma ligação de hidrogênio? átomo eletronegativo
Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila
 Aminoácidos e Peptídios 1 Aminoácidos Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila aaminoácido: têm um grupo carboxila e um grupo amino ligados ao mesmo átomo de carbono
Aminoácidos e Peptídios 1 Aminoácidos Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila aaminoácido: têm um grupo carboxila e um grupo amino ligados ao mesmo átomo de carbono
Componentes Químicos das Células
 Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
CÓDIGO GENÉTICO E SÍNTESE PROTEICA
 Terceirão Biologia 1 Professor João CÓDIGO GENÉTICO E SÍNTESE PROTEICA Dogma central da Biologia Descreve o fluxo unidirecional de informações, do DNA à síntese de proteínas. Duplicação/Replicação Síntese
Terceirão Biologia 1 Professor João CÓDIGO GENÉTICO E SÍNTESE PROTEICA Dogma central da Biologia Descreve o fluxo unidirecional de informações, do DNA à síntese de proteínas. Duplicação/Replicação Síntese
BÁSICA EM IMAGENS. Aminoácidos, peptídeos e proteínas
 Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
Profº Lásaro Henrique
 Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos
 Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
Aminoácidos. Bioquímica Prof. Dr. Marcelo Soares
 Aminoácidos Aminoácidos Nutrição Século XIX: produtos contendo Nitrogênio eram essenciais para a sobrevivência dos animais G. J. Mulder (1839): termo Proteínas Gr Proteios (Primário) Teoria: Proteínas
Aminoácidos Aminoácidos Nutrição Século XIX: produtos contendo Nitrogênio eram essenciais para a sobrevivência dos animais G. J. Mulder (1839): termo Proteínas Gr Proteios (Primário) Teoria: Proteínas
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas
 Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Bioinformática Estrutural Aula 1
 Bioinformática Estrutural Aula 1 03 de Junho de 2013 Paula Kuser-Falcão Laboratório de Bioinformática Aplicada Embrapa Informática Agropecuária [email protected] Pratique Atividade Física Paula
Bioinformática Estrutural Aula 1 03 de Junho de 2013 Paula Kuser-Falcão Laboratório de Bioinformática Aplicada Embrapa Informática Agropecuária [email protected] Pratique Atividade Física Paula
ESCOLA TÉCNICA ESTADUAL FREDERICO GUILHERME SCHMIDT Escola Técnica Industrial. Disciplina de Biologia Primeiro Ano Curso Técnico de Eletromecânica
 ESCOLA TÉCNICA ESTADUAL FREDERICO GUILHERME SCHMIDT Escola Técnica Industrial Disciplina de Biologia Primeiro Ano Curso Técnico de Eletromecânica Prof. Diogo Schott [email protected] Substâncias orgânicas
ESCOLA TÉCNICA ESTADUAL FREDERICO GUILHERME SCHMIDT Escola Técnica Industrial Disciplina de Biologia Primeiro Ano Curso Técnico de Eletromecânica Prof. Diogo Schott [email protected] Substâncias orgânicas
Faculdade Anhanguera Curso de Graduação em Educação Física
 Faculdade Anhanguera Curso de Graduação em Educação Física Profa. Dra. Amabile Vessoni Arias E-mail: [email protected] 2016-2 Mês de agosto Conteúdo 9 Unidade 1 16 Unidade 1 23 Unidade 1 30
Faculdade Anhanguera Curso de Graduação em Educação Física Profa. Dra. Amabile Vessoni Arias E-mail: [email protected] 2016-2 Mês de agosto Conteúdo 9 Unidade 1 16 Unidade 1 23 Unidade 1 30
AMINOÁCIDOS. Dra. Flávia Cristina Goulart. Bioquímica
 AMINOÁCIDOS Dra. Flávia Cristina Goulart Bioquímica Os aminoácidos (aa). O que são? AMINOÁCIDOS São as unidades fundamentais das PROTEÍNAS. São ácidos orgânicos formados por átomos de carbono, hidrogênio,
AMINOÁCIDOS Dra. Flávia Cristina Goulart Bioquímica Os aminoácidos (aa). O que são? AMINOÁCIDOS São as unidades fundamentais das PROTEÍNAS. São ácidos orgânicos formados por átomos de carbono, hidrogênio,
Aminoácidos e Peptideos
 Aminoácidos e Peptideos O que são aminoácidos? Precursores de vários tipos de biomoléculas Compostos formados por : um grupo amina primário [ ] um grupo ácido carboxílico [ ] ambos ligados a um carbono
Aminoácidos e Peptideos O que são aminoácidos? Precursores de vários tipos de biomoléculas Compostos formados por : um grupo amina primário [ ] um grupo ácido carboxílico [ ] ambos ligados a um carbono
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS. Bianca Zingales IQ-USP
 MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
Prof. Marcelo Langer. Curso de Biologia. Aula Genética
 Prof. Marcelo Langer Curso de Biologia Aula Genética CÓDIGO GENÉTICO Uma linguagem de códons e anticódons, sempre constituídos por 3 NUCLEOTÍDEOS. 64 CODONS = 4 tipos diferentes de nucleotídeos, combinação
Prof. Marcelo Langer Curso de Biologia Aula Genética CÓDIGO GENÉTICO Uma linguagem de códons e anticódons, sempre constituídos por 3 NUCLEOTÍDEOS. 64 CODONS = 4 tipos diferentes de nucleotídeos, combinação
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS. Bianca Zingales IQ-USP
 MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
Aminoácidos e Peptídeos. Profa. Alana Cecília
 Aminoácidos e Peptídeos Profa. Alana Cecília O que são aminoácidos? A estrutura geral dos aminoácidos inclui um grupo amina e um grupo carboxila, ambos ligados ao carbono α (aquele próximo ao grupo carboxila);
Aminoácidos e Peptídeos Profa. Alana Cecília O que são aminoácidos? A estrutura geral dos aminoácidos inclui um grupo amina e um grupo carboxila, ambos ligados ao carbono α (aquele próximo ao grupo carboxila);
BÁSICA EM IMAGENS. Aminoácidos, peptídeos e proteínas
 Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Hierarquia estrutural
Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Hierarquia estrutural
Aminoácidos. subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes
 . Aminoácidos subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes aminoácido Para entender a estrutura 3D das proteínas, vamos dissecá-la em níveis organizacionais para facilitar
. Aminoácidos subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes aminoácido Para entender a estrutura 3D das proteínas, vamos dissecá-la em níveis organizacionais para facilitar
Lista de Exercícios Bioquímica de Macromoléculas - Nanotecnologia
 Lista de Exercícios Bioquímica de Macromoléculas - Nanotecnologia 1 - Catecóis substituídos com longas cadeias acilas são os componentes encontrados na urtiga responsáveis pela sensação de queimadura e
Lista de Exercícios Bioquímica de Macromoléculas - Nanotecnologia 1 - Catecóis substituídos com longas cadeias acilas são os componentes encontrados na urtiga responsáveis pela sensação de queimadura e
OBJETIVOS INTERAÇÕES INTERMOLECULARES INTERAÇÕES INTERMOLECULARES.
 OBJETIVOS [email protected] Interações Intermoleculares Mecanismo de Ação Modo de Ligação Complexos Recetor-Ligante Exemplos e Exercícios INTERAÇÕES INTERMOLECULARES INTERAÇÕES INTERMOLECULARES O processo
OBJETIVOS [email protected] Interações Intermoleculares Mecanismo de Ação Modo de Ligação Complexos Recetor-Ligante Exemplos e Exercícios INTERAÇÕES INTERMOLECULARES INTERAÇÕES INTERMOLECULARES O processo
1164 BIOLOGIA ESTRUTURAL Aula 1 Prof. Dr. Valmir Fadel
 H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
Proteínas: aspectos gerais
 Proteínas: aspectos gerais As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (mais de 50% do seu peso seco) As proteínas são omnipresentes na célula, pois estão ligadas a todos
Proteínas: aspectos gerais As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (mais de 50% do seu peso seco) As proteínas são omnipresentes na célula, pois estão ligadas a todos
13/03/2016. Profª. Drª. Andréa Fontes Garcia E -mail:
 Profª. Drª. Andréa Fontes Garcia E -mail: [email protected] 1 Estrutura geral dos amionoácidos de ocorrência biológica Grupamento amino Grupamento carboxilato (ácido carboxílico) Hidrogênio Grupamento
Profª. Drª. Andréa Fontes Garcia E -mail: [email protected] 1 Estrutura geral dos amionoácidos de ocorrência biológica Grupamento amino Grupamento carboxilato (ácido carboxílico) Hidrogênio Grupamento
Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III
 Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III A maioria das cadeias polipeptídicas naturais contém entre 50 e 2.000 aminoácidos e são comumente referidas como proteínas. Peptídeos
Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III A maioria das cadeias polipeptídicas naturais contém entre 50 e 2.000 aminoácidos e são comumente referidas como proteínas. Peptídeos
Você deve desenhar o aminoácido com o grupo amino protonado (pka > 7) e o grupo carboxílico desprotonado (pka <7).
 QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
EXERCÍCIOS DE REVISÃO - BIOLOGIA - PROF. BELAN.
 EXERCÍCIOS DE REVISÃO - BIOLOGIA - PROF. BELAN. 1. (UECE 2017) Qualquer ser vivo precisa de energia para realizar suas funções metabólicas. Seres vivos aeróbios realizam o processo conhecido como respiração
EXERCÍCIOS DE REVISÃO - BIOLOGIA - PROF. BELAN. 1. (UECE 2017) Qualquer ser vivo precisa de energia para realizar suas funções metabólicas. Seres vivos aeróbios realizam o processo conhecido como respiração
A Célula Humana. Disciplina: Anatomia e Fisiologia. Samara Cristina Ferreira Machado. Programa Nacional de Formação em Radioterapia
 Disciplina: Anatomia e Fisiologia A Célula Humana Samara Cristina Ferreira Machado Programa Nacional de Formação em Radioterapia Abordagem Celular - Estrutura Celular - Função Celular - Ciclo Celular Estrutura
Disciplina: Anatomia e Fisiologia A Célula Humana Samara Cristina Ferreira Machado Programa Nacional de Formação em Radioterapia Abordagem Celular - Estrutura Celular - Função Celular - Ciclo Celular Estrutura
UNIVERSO TERRA SERES VIVOS ORIGEM
 UNIVERSO TERRA SERES VIVOS ORIGEM BIOLOGIA Surgiu da observação, da curiosidade de se compreender a vida e da utilização da natureza em benefício humano Grande salto com Aristóteles Baseada na observação
UNIVERSO TERRA SERES VIVOS ORIGEM BIOLOGIA Surgiu da observação, da curiosidade de se compreender a vida e da utilização da natureza em benefício humano Grande salto com Aristóteles Baseada na observação
Aminoácidos e peptídeos. Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I
 Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
AMINOÁCIDOS.! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico NH2 I R - C - C = 0O I I H OH
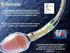 Aminoácidos AMNOÁCDOS! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico radical R C-alfa N2 R - C - C = 0O O amina primária ácido carboxílico Aminoácidos
Aminoácidos AMNOÁCDOS! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico radical R C-alfa N2 R - C - C = 0O O amina primária ácido carboxílico Aminoácidos
AMINOÁCIDOS. - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos;
 1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
 Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem do grego protos
Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem do grego protos
FERTILIZANTE ORGÂNICO COMPOSTO CLASSE A
 FERTILIZANTE ORGÂNICO COMPOSTO CLASSE A REGISTRADO NO MAPA SOB O Nº PA-07526 10001-7 GARANTIAS DE REGISTRO 11% Nitrogênio Total (N) 20% Carbono Orgânico Total (COT) É um fertilizante fluido com alta concentração
FERTILIZANTE ORGÂNICO COMPOSTO CLASSE A REGISTRADO NO MAPA SOB O Nº PA-07526 10001-7 GARANTIAS DE REGISTRO 11% Nitrogênio Total (N) 20% Carbono Orgânico Total (COT) É um fertilizante fluido com alta concentração
Lista de Exercícios Aminoácidos e Proteínas
 Universidade do Estado de Santa Catarina Centro de Ciências Tecnológicas CCT Departamento de Química BIO0001 - Bioquímica Lista de Exercícios Aminoácidos e Proteínas 1) Uma solução de 100 ml de glicina
Universidade do Estado de Santa Catarina Centro de Ciências Tecnológicas CCT Departamento de Química BIO0001 - Bioquímica Lista de Exercícios Aminoácidos e Proteínas 1) Uma solução de 100 ml de glicina
1. INTRODUÇÃO. Polímeros biológicos. Polissacarídeos Proteínas Ácidos Nucléicos. Reservas de energia. Armazenamento e Transmissão de informações
 AMINOÁIDOS 1. INTRODUÇÃO Polímeros biológicos Polissacarídeos Proteínas Ácidos Nucléicos Reservas de energia Materiais estruturais Marcadores bioquímicos Armazenamento e Transmissão de informações PROTEÍNAS
AMINOÁIDOS 1. INTRODUÇÃO Polímeros biológicos Polissacarídeos Proteínas Ácidos Nucléicos Reservas de energia Materiais estruturais Marcadores bioquímicos Armazenamento e Transmissão de informações PROTEÍNAS
(DN D A N / RN R A N ) A...
 Escola de Enfermagem de Ribeirão Preto Universidade de São Paulo Disciplina de Biologia Celular INTRODUÇÃO À BIOQUÍMICA: BIOMOLÉCULAS Objetivos da Aula: 1. Água e Pontes de hidrogênio 2. Biomoléculas (ou
Escola de Enfermagem de Ribeirão Preto Universidade de São Paulo Disciplina de Biologia Celular INTRODUÇÃO À BIOQUÍMICA: BIOMOLÉCULAS Objetivos da Aula: 1. Água e Pontes de hidrogênio 2. Biomoléculas (ou
MACRONUTRIENTES III PROTEÍNAS
 MACRONUTRIENTES III PROTEÍNAS 1 PROTEÍNAS As proteínas são compostos orgânicos de estrutura complexa e massa molecular elevada, elas são sintetizadas pelos organismos vivos através da condensação de um
MACRONUTRIENTES III PROTEÍNAS 1 PROTEÍNAS As proteínas são compostos orgânicos de estrutura complexa e massa molecular elevada, elas são sintetizadas pelos organismos vivos através da condensação de um
Macromolécula mais abundante nas células
 PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
BIOQUÍMICA. Profº André Montillo
 BIOQUÍMICA Profº André Montillo www.montillo.com.br Definição: É uma Molécula Orgânica que contém simultaneamente grupo funcionais amina (NH2) e carboxílico (COOH) É formado pelos seguintes Átomos: o Carbono
BIOQUÍMICA Profº André Montillo www.montillo.com.br Definição: É uma Molécula Orgânica que contém simultaneamente grupo funcionais amina (NH2) e carboxílico (COOH) É formado pelos seguintes Átomos: o Carbono
MANUAL DA DISCIPLINA DE BIOQUÍMICA CURSO DE FISIOTERAPIA MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS
 MANUAL DA DISCIPLINA DE BIOQUÍMICA CURSO DE FISIOTERAPIA 2017 MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS NOTA: Agradecemos ao Professor Bayardo B. Torres pelas sugestões valiosas para a compilação deste manual
MANUAL DA DISCIPLINA DE BIOQUÍMICA CURSO DE FISIOTERAPIA 2017 MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS NOTA: Agradecemos ao Professor Bayardo B. Torres pelas sugestões valiosas para a compilação deste manual
ESTRUTURA DAS PROTEÍNAS
 ESTRUTURA DAS PROTEÍNAS Como é a estrutura tridimensional das proteínas??? 4 níveis estruturais Estrutura primária, secundária, terciária e quaternária Mantidas por: ligações covalentes (ligação peptídica
ESTRUTURA DAS PROTEÍNAS Como é a estrutura tridimensional das proteínas??? 4 níveis estruturais Estrutura primária, secundária, terciária e quaternária Mantidas por: ligações covalentes (ligação peptídica
EVENTOS CO e PÓS TRADUCIONAIS
 EVENTOS CO e PÓS TRADUCIONAIS EVENTOS CO e PÓS TRADUCIONAIS Enovelamento natural e assistido (Chaperonas e HSPs) Ubiquitinação e degradação via proteassomo de proteínas não enoveladas Endereçamento (peptídeo
EVENTOS CO e PÓS TRADUCIONAIS EVENTOS CO e PÓS TRADUCIONAIS Enovelamento natural e assistido (Chaperonas e HSPs) Ubiquitinação e degradação via proteassomo de proteínas não enoveladas Endereçamento (peptídeo
Substrato do Tripeptídeo
 Pergunta 1 Você está estudando uma enzima chamada quinase. Seu substrato é o tripeptídeo Ala-Lys-Thr, com uma molécula incomum em suas terminações C, a molécula GLOW. Quando essa molécula GLOW é segmentada
Pergunta 1 Você está estudando uma enzima chamada quinase. Seu substrato é o tripeptídeo Ala-Lys-Thr, com uma molécula incomum em suas terminações C, a molécula GLOW. Quando essa molécula GLOW é segmentada
Gliconeogênese. Gliconeogênese. Órgãos e gliconeogênese. Fontes de Glicose. Gliconeogênese. Gliconeogênese Metabolismo dos aminoácidos Ciclo da Uréia
 Gliconeogênese Metabolismo dos aminoácidos Ciclo da Uréia Gliconeogênese Alexandre Havt Gliconeogênese Fontes de Energia para as Células Definição Via anabólica que ocorre no fígado e, excepcionalmente
Gliconeogênese Metabolismo dos aminoácidos Ciclo da Uréia Gliconeogênese Alexandre Havt Gliconeogênese Fontes de Energia para as Células Definição Via anabólica que ocorre no fígado e, excepcionalmente
PROTEÍNAS. A palavra proteína derivada de proteos, (grego = primeira ou a mais importante)
 PROTEÍNAS A palavra proteína derivada de proteos, (grego = primeira ou a mais importante) Macromolécula mais abundante nas células Produto final da informação genética (DNA-RNA-Proteína) Diversidade funcional
PROTEÍNAS A palavra proteína derivada de proteos, (grego = primeira ou a mais importante) Macromolécula mais abundante nas células Produto final da informação genética (DNA-RNA-Proteína) Diversidade funcional
CÓDIGO GENÉTICO Lista I 20 Questões Professor Charles Reis Curso Expoente
 CÓDIGO GENÉTICO Lista I 20 Questões Professor Charles Reis Curso Expoente 01. (FUVEST) A seguir está representada a sequência dos 13 primeiros pares de nucleotídeos da região codificadora de um gene. A
CÓDIGO GENÉTICO Lista I 20 Questões Professor Charles Reis Curso Expoente 01. (FUVEST) A seguir está representada a sequência dos 13 primeiros pares de nucleotídeos da região codificadora de um gene. A
Aminoácidos e proteínas
 Aminoácidos e proteínas Visão geral 2 https://www.youtube.com/watch?v=qbrfimcxznm Importância dessa aula Serina Fosfoserina Treonina Fosfotreonina Fosforilação de resíduos de aa modifica a atividade enzimática
Aminoácidos e proteínas Visão geral 2 https://www.youtube.com/watch?v=qbrfimcxznm Importância dessa aula Serina Fosfoserina Treonina Fosfotreonina Fosforilação de resíduos de aa modifica a atividade enzimática
Colégio Notre Dame de Campinas PLANTÕES DE JULHO BIOLOGIA AULA 01
 Roteiro de Estudos Fotossíntese e Respiração Celular Colégio Notre Dame de Campinas PLANTÕES DE JULHO BIOLOGIA AULA 01 Nome: Nº: Série: 2º ANO Profº LAURA BERTAZOLLI Data: JULHO 2018 1. (Unesp 2017) Em
Roteiro de Estudos Fotossíntese e Respiração Celular Colégio Notre Dame de Campinas PLANTÕES DE JULHO BIOLOGIA AULA 01 Nome: Nº: Série: 2º ANO Profº LAURA BERTAZOLLI Data: JULHO 2018 1. (Unesp 2017) Em
Rafael Mesquita. Proteínas. Estrutura
 Proteínas Estrutura Ligação peptídica Ligação peptídica - Rígida e plana - Ligação simples com caráter de dupla ligação Ângulos Φ e Ψ Ligação peptídica limitações estruturais Limitações estruturais impostas
Proteínas Estrutura Ligação peptídica Ligação peptídica - Rígida e plana - Ligação simples com caráter de dupla ligação Ângulos Φ e Ψ Ligação peptídica limitações estruturais Limitações estruturais impostas
Influência da Genética desempenho
 UNIVERSIDADE GAMA FILHO PÓS-GRADUAÇÃO Nível: LATO SENSU Curso: FISIOLOGIA E TREINAMENTO APL. ATIVIDADES DE ACADEMIAS E CLUBES Influência da Genética desempenho Prof. Drd. LUIZ CARLOS CARNEVALI [email protected]
UNIVERSIDADE GAMA FILHO PÓS-GRADUAÇÃO Nível: LATO SENSU Curso: FISIOLOGIA E TREINAMENTO APL. ATIVIDADES DE ACADEMIAS E CLUBES Influência da Genética desempenho Prof. Drd. LUIZ CARLOS CARNEVALI [email protected]
Introdução à Bioquímica Celular
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Introdução à Bioquímica Celular Prof. Msc. Macks Wendhell Gonçalves [email protected] O que é Biologia Celular? É o ramo da ciência
Pontifícia Universidade Católica de Goiás Departamento de Biologia Introdução à Bioquímica Celular Prof. Msc. Macks Wendhell Gonçalves [email protected] O que é Biologia Celular? É o ramo da ciência
INTRODUÇÃO À BIOQUÍMICA DA CÉLULA. Bioquímica Celular Prof. Júnior
 INTRODUÇÃO À BIOQUÍMICA DA CÉLULA Histórico INTRODUÇÃO 1665: Robert Hooke Compartimentos (Células) 1840: Theodor Schwann Teoria Celular 1. Todos os organismos são constituídos de uma ou mais células 2.
INTRODUÇÃO À BIOQUÍMICA DA CÉLULA Histórico INTRODUÇÃO 1665: Robert Hooke Compartimentos (Células) 1840: Theodor Schwann Teoria Celular 1. Todos os organismos são constituídos de uma ou mais células 2.
QBQ0105-Bioquímica e Biologia Molecular. Docentes: Sayuri Miyamoto (B9, sala 951) e Mari Cleide Sogayar (B9, sala 962)
 QBQ0105-Bioquímica e Biologia Molecular Docentes: Sayuri Miyamoto (B9, sala 951) e Mari Cleide Sogayar (B9, sala 962) Monitores: Priscilla BMC Derogis (B9, sala 951) e Thiago CG Mattos (B9, sala 951) LISTA
QBQ0105-Bioquímica e Biologia Molecular Docentes: Sayuri Miyamoto (B9, sala 951) e Mari Cleide Sogayar (B9, sala 962) Monitores: Priscilla BMC Derogis (B9, sala 951) e Thiago CG Mattos (B9, sala 951) LISTA
Fenilalanina (Phe) Treonina (Thr) Tirosina (Tir)
 Pergunta 1 Abaixo estão apresentadas as estruturas de três aminoácidos. Fenilalanina (Phe) Treonina (Thr) Tirosina (Tir) Usando os espaços em branco abaixo, classifique os três na ordem da hidrofobicidade
Pergunta 1 Abaixo estão apresentadas as estruturas de três aminoácidos. Fenilalanina (Phe) Treonina (Thr) Tirosina (Tir) Usando os espaços em branco abaixo, classifique os três na ordem da hidrofobicidade
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Bioinformática. Conceitos Fundamentais de Biologia Molecular. Paulo Henrique Ribeiro Gabriel [email protected]
 Bioinformática Conceitos Fundamentais de Biologia Molecular Paulo Henrique Ribeiro Gabriel [email protected] Faculdade de Computação Universidade Federal de Uberlândia 24 de agosto de 2015 Paulo H. R. Gabriel
Bioinformática Conceitos Fundamentais de Biologia Molecular Paulo Henrique Ribeiro Gabriel [email protected] Faculdade de Computação Universidade Federal de Uberlândia 24 de agosto de 2015 Paulo H. R. Gabriel
Biologia Ensino Médio 2º ano classe: Prof. Cesinha Nome: nº
 PRIMEIR LETR TEREIR LETR Biologia Ensino Médio 2º ano classe: Prof. esinha Nome: nº Valor: 10 Nota:. Lista de ExercíciosTarefa- Segundos nos prof. esinha 2015 1. (ff 2010) figura a seguir representa um
PRIMEIR LETR TEREIR LETR Biologia Ensino Médio 2º ano classe: Prof. esinha Nome: nº Valor: 10 Nota:. Lista de ExercíciosTarefa- Segundos nos prof. esinha 2015 1. (ff 2010) figura a seguir representa um
CICLO DE KREBS. Em condições aeróbias: mitocôndria. citosol. Glicólise. ciclo de Krebs. 2 piruvato. 2 Acetil CoA. Fosforilação oxidativa
 CICLO DE KREBS Em condições aeróbias: citosol mitocôndria Glicólise Acetil CoA ciclo de Krebs Fosforilação oxidativa CICLO DE KREBS OU CICLO DOS ÁCIDOS TRICARBOXÍLICOS Ligação entre a glicólise e o ciclo
CICLO DE KREBS Em condições aeróbias: citosol mitocôndria Glicólise Acetil CoA ciclo de Krebs Fosforilação oxidativa CICLO DE KREBS OU CICLO DOS ÁCIDOS TRICARBOXÍLICOS Ligação entre a glicólise e o ciclo
Biomoléculas e processos Passivos/Ativos na célula
 Biomoléculas e processos Passivos/Ativos na célula ICB Dep. Mofologia Disciplina: Biologia Celular Bases moleculares e Macromoleculares Substâncias Inorgânicas/Orgânicas Processos Celulares Passivos/Ativos
Biomoléculas e processos Passivos/Ativos na célula ICB Dep. Mofologia Disciplina: Biologia Celular Bases moleculares e Macromoleculares Substâncias Inorgânicas/Orgânicas Processos Celulares Passivos/Ativos
BIOLOGIA. Moléculas, células e tecidos. Transcrição e tradução Parte 2. Professor: Alex Santos
 BIOLOGIA Moléculas, células e tecidos Professor: Alex Santos Parte 2: Síntese de proteínas Tópicos em abordagem : I Processamento do imrna em Eucariotos II Código genético III Tradução: Síntese de proteínas
BIOLOGIA Moléculas, células e tecidos Professor: Alex Santos Parte 2: Síntese de proteínas Tópicos em abordagem : I Processamento do imrna em Eucariotos II Código genético III Tradução: Síntese de proteínas
Membranas Biológicas
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Membranas Biológicas Prof Karine P. Naidek Outubro/2016 Membranas Biológicas Membranas
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Membranas Biológicas Prof Karine P. Naidek Outubro/2016 Membranas Biológicas Membranas
Proteínas são organizadas em níveis. Na aula passada... Cadeia polipetídica na conformação estendida
 Na aula passada... Proteínas são organizadas em níveis Proteínas adotam forma tridimensional característica sua forma nativa Uma cadeia polipetídica com uma certa sequência de aminoácidos sempre se dobra
Na aula passada... Proteínas são organizadas em níveis Proteínas adotam forma tridimensional característica sua forma nativa Uma cadeia polipetídica com uma certa sequência de aminoácidos sempre se dobra
BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2016_2017_1º Teste
 BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2016_2017_1º Teste 24/11/2016 (Duração: 1h,30 m) Nome do Aluno: Nº: Curso: Cada uma das questões tem a cotação de 0,5 valores. Nas questões de escolha múltipla será
BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2016_2017_1º Teste 24/11/2016 (Duração: 1h,30 m) Nome do Aluno: Nº: Curso: Cada uma das questões tem a cotação de 0,5 valores. Nas questões de escolha múltipla será
