Uso da técnica de dicroísmo circular para avaliação de proteínas com aplicações biotecnológicas
|
|
|
- Washington Lencastre Escobar
- 6 Há anos
- Visualizações:
Transcrição
1 Centro Nacional de Pesquisa em Energia e Materiais Laboratório Nacional de Ciência e Tecnologia do Bioetanol Memorando Técnico 03/2016 Uso da técnica de dicroísmo circular para avaliação de proteínas com aplicações biotecnológicas Leticia Maria Zanphorlin Murakami Roberto Ruller 2016
2 MEMORANDO TÉCNICO: USO DA TÉCNICA DE DICROÍSMO CIRCULAR PARA AVALIAR ENZIMAS BIOTECNOLÓGICAS Leticia M. Zanphorlin & Roberto Ruller RESUMO A funcionalidade das proteínas e enzimas decorre de suas estruturas tridimensionais. Assim, a grande meta a ser alcançada no estudo de enzimas é o conhecimento de suas estruturas à nível atômico-molecular, suas funções e, consequentemente, as relações estrutura/função, as quais, à medida que se tornam conhecidas, formam a base que possam orientar a modificação deliberada para aperfeiçoar ou criar novas propriedades moleculares. No estado atual do âmbito da Ciência das proteínas/enzimas, o estudo estrutural de uma macromolécula que atenda aos critérios de pureza, segue as seguintes etapas: estrutura primária, que pode ser determinada usando-se cada vez mais a espectrometria de massas; estrutura secundária, obtida via espectrometria dicróica (dicroísmo circular) e espectrometria de infravermelho com transformação de Fourier (FTIR); estrutura terciária, obtida por cristalografia de raios-x ou em solução, por ressonância magnética nuclear (RMN). As enzimas, possuem em suas estruturas unidades opticamente ativas (ligações amídicas sonda de estrutura secundária) que podem ser caracterizadas na região do ultravioleta distante (abaixo de 250 nm). Dessa forma, essas unidades interagem com a luz circularmente polarizada provocando alteração na polarização da luz incidente. Nesse sentido, a técnica de dicroísmo circular (CD) detecta essa alteração, medindo a diferença da absorção da luz circularmente polarizada à direita e à esquerda, permitindo avaliar o conteúdo de estrutura secundária de uma determinada proteína. Como resultado final, obtemos informações cruciais da estrutura secundária de uma proteína em solução. Além disso, uma vez conhecida o perfil de estrutura secundária dessa macromolécula, é possível acessar informações da termoestabilidade obtendo valores de Tm (temperatura de transição) nas condições desejadas. Com isso, é fato que utilizando a técnica de dicroísmo circular, somos capazes de investigar e prever quais as melhores condições (ph, temperatura, tampão, sais, inibidores, ativadores e outros componentes) que uma determinada proteína tem seu ótimo funcional. As vantagens da utilização da técnica de CD envolvem baixo custo (em termos operacionais e de quantidade de amostra) e a principal desvantagem é o fato de ser necessário a enzima estar em solução e purificada em um alto grau de pureza. Palavras-chaves: proteínas, dicroismo circular,enzimas, estrtura e função, biotecnologia industrial 2
3 SUMÁRIO 1. INTRODUÇÃO OBJETIVO ASPECTOS EXPERIMENTAIS Instrumentação Metodologia da preparação das amostras para análise em CD e os parâmetros de leitura Concentração de proteínas recommendados para análise Unidade para medidas de CD Predição de estrutura secundária Experimentos de desenovelamento ou agregação de proteínas CONCLUSÃO REFERÊNCIAS
4 1. INTRODUÇÃO Dicroísmo Circular é uma técnica espectroscópica extensivamente usada para estudar conformação e estabilidade de proteínas em diferentes condições, como por exemplo, temperatura, força iônica, ph, presença de solutos e/ou pequenas moléculas. CD é uma técnica não destrutiva, de fácil manuseio, requer pequenas quantidades de amostra e as análises são relativamente rápidas. CD mede a diferença de luz circularmente polarizada à esquerda e à direita por cromóforos que possuem quiralidade intrínseca ou estão localizados em condições quirais. Proteínas possuem um número de cromóforos que podem originar em sinal de CD. Na região do UV-distante ( nm), que corresponde à absorção da ligação peptídica, o espectro de CD pode ser analisado para dar informações no que diz respeito as características de estrutura secundária, como por exemplo, α-hélice, folha-β e randômica. O espectro de CD na região do próximo ( nm) reflete o ambiente de aminoácidos com cadeia lateral de aromáticos e então fornece informação sobre a estrutura terciária da proteína. Portanto, é evidente que a técnica de CD é bastante versátil em biologia estrutural, com extensa aplicação. 2. OBJETIVO O objetivo desse memorando técnico é abordar os principais aspectos experimentais para se obter resultados de Dicroísmo Circular com boa qualidade experimental. 3. ASPECTOS EXPERIMENTAIS 3.1. Instrumentação O dicroísmo circular ou CD (do inglês circular dichroism) é uma forma de espectroscopia que utiliza a absorção diferenciada da luz polarizada no sentido horário e ou anti-horário. Um fenômeno que é comumente utilizado nos estudos da estrutura secundária de proteínas e destas em soluções e estudos de interações com outras moléculas (RNA, DNA e peptídeos). A fonte de luz para a instrumentação de CD é o xenônio, que gera bons resultados nos comprimentos de onda de 178 à 1000 nm. 4
5 Durante a preparação da análise no espectropolarímetro (maquinário destinado a análise de CD), é necessário um fluxo de N2 para remover O2 e prevenir a formação de ozônio, que pode causar danos para o sistema ótico, além de permitir que medidas sejam feitas abaixo de 200 nm. Um fluxo de N2 constante deve ser usado: geralmente 3L/min para medidas em 260 nm, 5L/min entre 200 até 260 nm, 10L/min entre 180 e 200 nm e 50L/min em 180 nm. A lâmpada deve ser ligada antes de cada experimento com no mínimo 30 minutos de antecedência Metodologia da preparação das amostras para análise em CD e os parâmetros de leitura É importante que cada amostra esteja, pura, homogênea e na ausência de partículas precipitadas (centrifuga-se ou filtra-se em 0.22 m). É essencial minimizar a absorção de outros componentes (como tampão, solutos, solventes, etc). Tampões fosfato, borato ou Tris em baixa molaridade (em torno de 20 mm) possuem baixa absorção acima de 190 nm em cubetas de 0.1 nm de caminho ótico. O indício de absorção da luz é dado pelo módulo de voltagem de dinodo (em volts, V), que mede a resposta da fotomultiplicadora durante o experimento e é um indicador da quantidade de fótons que não são absorvidos ou são espalhados pela amostra. Uma alta absorção causa um aumento no ruído e consequentemente aumenta os erros nas medidas de elipticidade. Em geral, um limite aceitável é de 600V, mas as aquisições até 700 V são permitidas desde que o número de acumulações seja alto o suficiente para reduzir o ruído gerado pela absorção. Além disso, o uso de cubetas de quartzo com menores caminho óticos diminui o número de fótons que a amostra é capaz de absorver. Outros parâmetros são importantes para reduzir o ruído da medida. A largura da fenda, que controla a banda espectral deve ter um valor limite que não seja capaz de deformar e/ou destorcer o espectro. Além disso, o sinal do ruído é proporcional a raiz quadrada do tempo de integração, então a forma mais simples de melhorar a qualidade do espectro é aumentar o tempo de resposta. Para isso, a velocidade de leitura multiplicada pelo tempo de resposta deve ser menos que 0.33 nm (isto é, para uma velocidade de 200 nm/min, o tempo de resposta tem que ser no mínimo de 0.1s e para uma velocidade de 50 nm/min, o tempo de resposta tem 5
6 que ser menos que 0.4s). Parâmetros sugeridos para medidas iniciais de proteínas: bandwidth = 2 nm; tempo de resposta = 1s e velocidade de varredura = 20 nm/min; o número de acumulações deve ser o necessário para que o valor de HT não exceda 700 V A qualidade e concentração de proteína recomendada para análise O espectro de CD de uma proteína depende tanto de sua conformação como concentração da amostra pura analisada. Medidas precisas de concentração é fundamental para a predição de estrutura secundária. Para isso recomenda-se uma quantificação proteica, utilizando metodologias padronizadas de Bradford ou BCA, associados a uma análise de pureza em gel de poliacrilalida SDSPAGE. Uma vez a amostra proteica, centrifugada, filtrada e quantificada, inicia-se a análise por CD. Para cubetas com caminho ótico para medidas entre 1 até 5 mm, pode-se usar concentrações de 0.2 até 1 mg/ml. Dependendo do desenho da cubeta, o volume necessário pode ser de 50 µl até 2 ml. Por exemplo, para cubetas de 1 mm, 300 µl de amostra na concentração de 200 µg/ml deve fornecer bons resultados Unidade para medidas de CD Para proteínas, os resultados são expressos em elipticidade molar residual, [θ]: [θ]= (θ*100*m)/(c*l*n) Onde θ é a elipticidade em graus, l é o caminho ótico em cm, C é a concentração em mg/ml, M é a massa molecular e n é o número de resíduos de aminoácidos da proteína. O resultado, portanto, é dado em graus.cm 2.dmol Predição de estrutura secundária Obviamente, a técnica de CD não pode fornecer detalhes estruturais como outras técnicas de alta resolução como é o caso de cristalografia de raios- X (X-TAL) e ressonância magnética nuclear (RMN); mas pode fornecer uma boa estimativa da fração de resíduos na estrutura que estão envolvidos em α-hélice, 6
7 folha-β e/ou formação desordenada. Muitos métodos (CONTIN-CD, SELCON, DICHROWEB, DICROPROT, K2D2) têm sido desenvolvidos para predizer estrutura secundária de proteínas através do espectro de CD. Esses métodos estabelecem metodologias de estatística que usam combinações do espectro de CD da proteína alvo com proteínas que possuem estrutura terciária conhecida. No entanto, é necessária atenção na interpretação dessas análises, pois o espectro de CD de uma proteína não depende apenas da quantidade de estrutura secundária, mas também da extensão da cadeia polipeptídica Experimentos de desenovelamento ou agregação de proteínas A técnica de CD é extensivamente usada para estudar a estabilidade de uma proteína na presença de condições desnaturantes, como por exemplo, temperatura, químicos (ureia e cloreto de guanidina) e extremos de ph (usualmente ácidos). Conforme a temperatura ou a concentração desses agentes aumentam, a estabilidade da proteína é afetada e, portanto, ocorre a perda de estrutura (desenovelamento). CD é uma técnica conveniente para avaliar a estabilidade uma vez que os espectros de uma proteína enovelada e desenovelada são totalmente diferentes. A transição pode ser facilmente determinada fixando o comprimento de onda onde a diferença de sinal para enovelada e desenovelada é grande. Por exemplo, proteínas predominantemente α-hélice tem um sinal de CD característico em 222 nm e quando se desenovela o sinal é muito baixo ou praticamente zero. 4. CONCLUSÃO CD é uma técnica estrutural que tem um importante papel no estudo de proteínas (conformação, função e estabilidade). Está técnica (desde que respeitada o alto grau de pureza), pode ser utilizada para avaliação de proteínas recombinantes (ou não), frente às condições variadas de temperature, presença de alguns inibidores (que não interfiram na análise por dicroismo), variados phs, interações moleculares com substratos, entre outras; o quais são elementos importantes para possíveis aplicações biotecnológicas. A principal vantagem no uso dessa metodologia está relacionada à economia de amostra e velocidade 7
8 de aquisição dos dados. CD é provavelmente uma das técnicas mais importantes para que se inicie uma investigação estrutural de uma amostra proteica pura. Neste sentido, esse memorando técnico destacou uma série de aspectos experimentais visando a aquisição de dados de boa qualidade auxiliando nas avaliações relacionadas a estrutura de proteínas com aplicações biotecnológicas. 5. REFERÊNCIAS Para mais informações consultar: Sharon M. Kelly and Nicholas C. Price. The Use of Circular Dichroism in the Investigation of Protein Structure and Function. Current Protein and Peptide Science, 2000, 1, Daniel H. A. Corrêa and Carlos H. I. Ramos. The use of circular dichroism spectroscopy to study protein folding, form and function. African Journal of Biochemistry Research Vol.3 (5), pp
Centro de Ciências da Saúde Programa de Pós Graduação em Biotecnologia Disciplina de Bioinformática DICROISMO CIRCULAR
 Centro de Ciências da Saúde Programa de Pós Graduação em Biotecnologia Disciplina de Bioinformática DICROISMO CIRCULAR Iara Pinto Simone Rodrigues Dicroísmo Circular (CD) A ligação peptídica absorve radiação
Centro de Ciências da Saúde Programa de Pós Graduação em Biotecnologia Disciplina de Bioinformática DICROISMO CIRCULAR Iara Pinto Simone Rodrigues Dicroísmo Circular (CD) A ligação peptídica absorve radiação
Abordagens experimentais para caracterização, fracionamento, purificação, identificação e quantificação de Proteínas.
 Abordagens experimentais para caracterização, fracionamento, purificação, identificação e quantificação de Proteínas Rafael Mesquita Estabilidade das proteínas A estabilidade das proteínas pode ser afetada
Abordagens experimentais para caracterização, fracionamento, purificação, identificação e quantificação de Proteínas Rafael Mesquita Estabilidade das proteínas A estabilidade das proteínas pode ser afetada
Luz polarizada. Luz linear polarizada. Luz circular polarizada
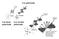 Luz polarizada Luz linear polarizada Luz circular polarizada Atividade óptica φ = 180l( nl nr ) / λ graus θ = 2, 303( A A ) 180 / 4π L R graus Mudança na velocidade de propagação das duas componentes:
Luz polarizada Luz linear polarizada Luz circular polarizada Atividade óptica φ = 180l( nl nr ) / λ graus θ = 2, 303( A A ) 180 / 4π L R graus Mudança na velocidade de propagação das duas componentes:
Espectrofotometria UV-Vis. Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva
 Espectrofotometria UV-Vis Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva Juiz de Fora, 1/2018 1 Terminologia Espectroscopia: Parte da ciência que estuda o fenômeno
Espectrofotometria UV-Vis Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva Juiz de Fora, 1/2018 1 Terminologia Espectroscopia: Parte da ciência que estuda o fenômeno
Determinação da Estrutura de Proteínas
 Centro Brasileiro-Argentino de Biotecnologia Introdução à Biologia Computacional Determinação da Estrutura de Proteínas Paulo enrique C. Godoi Bioinformática objetivo principal é determinar a função de
Centro Brasileiro-Argentino de Biotecnologia Introdução à Biologia Computacional Determinação da Estrutura de Proteínas Paulo enrique C. Godoi Bioinformática objetivo principal é determinar a função de
Purificação de Proteínas
 Aula de Bioquímica I Tema: Purificação de Proteínas Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail:
Aula de Bioquímica I Tema: Purificação de Proteínas Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail:
Graduação em Biotecnologia Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Metodologias para quantificar proteínas Qualquer trabalho com proteína deve envolver a quantificação
Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Metodologias para quantificar proteínas Qualquer trabalho com proteína deve envolver a quantificação
1 de 6 01/11/12 11:08
 OLIMPÍADA BRASILEIRA DE QUÍMICA 2001 - FASE III (nacional) Seletiva para escolha dos 4 estudantes da equipe nacional PROBLEMA 1 Modelo atômico de Bohr As teorias são construções nascidas da especulação
OLIMPÍADA BRASILEIRA DE QUÍMICA 2001 - FASE III (nacional) Seletiva para escolha dos 4 estudantes da equipe nacional PROBLEMA 1 Modelo atômico de Bohr As teorias são construções nascidas da especulação
Espectrofotometria UV-VIS PROF. DR. JÚLIO CÉSAR JOSÉ DA SILVA
 Espectrofotometria UV-VIS QUÍMICA ANALÍTICA V ESTAGIÁRIA A DOCÊNCIA: FERNANDA CERQUEIRA M. FERREIRA PROF. DR. JÚLIO CÉSAR JOSÉ DA SILVA 1 Conceitos Básicos Espectroscopia: É o estudo de sistemas físicos
Espectrofotometria UV-VIS QUÍMICA ANALÍTICA V ESTAGIÁRIA A DOCÊNCIA: FERNANDA CERQUEIRA M. FERREIRA PROF. DR. JÚLIO CÉSAR JOSÉ DA SILVA 1 Conceitos Básicos Espectroscopia: É o estudo de sistemas físicos
Análise de Alimentos II Espectroscopia de Absorção Molecular
 Análise de Alimentos II Espectroscopia de Absorção Molecular Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 2 Introdução A absorção de radiação no UV/Vis por uma espécie química (M) pode
Análise de Alimentos II Espectroscopia de Absorção Molecular Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 2 Introdução A absorção de radiação no UV/Vis por uma espécie química (M) pode
Proteínas. Proteínas são polímeros de aminoácidos
 Proteínas Estrutura & Propriedades Proteínas são polímeros de aminoácidos Existem 20 tipos diferentes de aminoácidos Aminoácidos são ácidos fracos A carga elétrica do aminoácido varia de acordo com o ph
Proteínas Estrutura & Propriedades Proteínas são polímeros de aminoácidos Existem 20 tipos diferentes de aminoácidos Aminoácidos são ácidos fracos A carga elétrica do aminoácido varia de acordo com o ph
7. Resultados e discussão
 7 Resultados e discussão 32 7. Resultados e discussão 7.1 orção ótica Inicialmente foi realizada a análise dos espectros dos BCD em solução de tampão fosfato (PBS) e em etanol, com as soluções estoques
7 Resultados e discussão 32 7. Resultados e discussão 7.1 orção ótica Inicialmente foi realizada a análise dos espectros dos BCD em solução de tampão fosfato (PBS) e em etanol, com as soluções estoques
Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Ligação peptídica Aminoácido 1 Aminoácido 2 um dipeptídeo A ligação peptídica é uma amida. O -C NH 2 Não são reações espontâneas
Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Ligação peptídica Aminoácido 1 Aminoácido 2 um dipeptídeo A ligação peptídica é uma amida. O -C NH 2 Não são reações espontâneas
Espectrofotometria UV-Vis. Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva
 Espectrofotometria UV-Vis Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva Relembrando... Conceitos Comprimento de onda (λ): distância entre dois pontos na mesma
Espectrofotometria UV-Vis Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva Relembrando... Conceitos Comprimento de onda (λ): distância entre dois pontos na mesma
São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas.
 São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas. Proteínas possuem muitas funções dentro do organismo. Aminoácidos
São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas. Proteínas possuem muitas funções dentro do organismo. Aminoácidos
Métodos Físicos de Análise - ESPECTROFOTOMETRIA ULTRAVIOLETA / VISÍVEL
 Métodos Físicos de Análise - ESPECTROFOTOMETRIA ULTRAVIOLETA / VISÍVEL Prof. Dr. Leonardo Lucchetti Mestre e Doutor em Ciências Química de Produtos Naturais NPPN/UFRJ Depto. de Química de Produtos Naturais
Métodos Físicos de Análise - ESPECTROFOTOMETRIA ULTRAVIOLETA / VISÍVEL Prof. Dr. Leonardo Lucchetti Mestre e Doutor em Ciências Química de Produtos Naturais NPPN/UFRJ Depto. de Química de Produtos Naturais
Mestrando: Jefferson Willian Martins Prof. Dr. Júlio César José da Silva Juiz de Fora, 2/2017
 1 ESPECTROFOTOMETRIA DE UV-VIS Mestrando: Jefferson Willian Martins Prof. Dr. Júlio César José da Silva Juiz de Fora, 2/2017 2 CONCEITOS PRINCIPAIS O que é Espectroscopia e Espectrometria? IUPAC, Compendium
1 ESPECTROFOTOMETRIA DE UV-VIS Mestrando: Jefferson Willian Martins Prof. Dr. Júlio César José da Silva Juiz de Fora, 2/2017 2 CONCEITOS PRINCIPAIS O que é Espectroscopia e Espectrometria? IUPAC, Compendium
Avaliação Quantitativa das Preparações Enzimáticas
 Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
UNIVERSIDADE PAULISTA. A espectrofotometria é uma técnica de análise baseadas na interação entre a radiação eletromagnética e a matéria.
 DISCIPLINA: MÉTODOS INSTRUMENTAIS DE ANÁLISE TÓPICO 4: Espectrofotometria de Absorção Molecular UV/Visível A espectrofotometria é uma técnica de análise baseadas na interação entre a radiação eletromagnética
DISCIPLINA: MÉTODOS INSTRUMENTAIS DE ANÁLISE TÓPICO 4: Espectrofotometria de Absorção Molecular UV/Visível A espectrofotometria é uma técnica de análise baseadas na interação entre a radiação eletromagnética
Espectrometria de emissão atômica
 Espectrometria de emissão atômica Técnica analítica que se baseia na emissão de radiação eletromagnética das regiões visível e ultravioleta do espectro eletromagnético por átomos neutros ou átomos ionizados
Espectrometria de emissão atômica Técnica analítica que se baseia na emissão de radiação eletromagnética das regiões visível e ultravioleta do espectro eletromagnético por átomos neutros ou átomos ionizados
PROTEÍNAS. A palavra proteína derivada de proteos, (grego = primeira ou a mais importante)
 PROTEÍNAS A palavra proteína derivada de proteos, (grego = primeira ou a mais importante) Macromolécula mais abundante nas células Produto final da informação genética (DNA-RNA-Proteína) Diversidade funcional
PROTEÍNAS A palavra proteína derivada de proteos, (grego = primeira ou a mais importante) Macromolécula mais abundante nas células Produto final da informação genética (DNA-RNA-Proteína) Diversidade funcional
Peptídeos e Proteínas: Estrutura de Proteínas
 Peptídeos e Proteínas: Estrutura de Proteínas QFL0343 - REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS Adriana Uehara 9820384 Janaína Novais 9819722 Aminoácidos Estruturas carbônicas que possuem
Peptídeos e Proteínas: Estrutura de Proteínas QFL0343 - REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS Adriana Uehara 9820384 Janaína Novais 9819722 Aminoácidos Estruturas carbônicas que possuem
Análise Instrumental ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA
 Análise Instrumental ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA Introdução: Método aplicado na determinação de compostos inorgânicos e orgânicos, como por
Análise Instrumental ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA Introdução: Método aplicado na determinação de compostos inorgânicos e orgânicos, como por
Composição e Estrutura Molecular dos Sistemas Biológicos
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Prof. Hugo Henrique Pádua M.Sc. Fundamentos de Biofísica Composição e Estrutura Molecular dos Sistemas Biológicos Átomos e Moléculas Hierarquia
Pontifícia Universidade Católica de Goiás Departamento de Biologia Prof. Hugo Henrique Pádua M.Sc. Fundamentos de Biofísica Composição e Estrutura Molecular dos Sistemas Biológicos Átomos e Moléculas Hierarquia
FENÓMENOS DE TRANSPORTE. Física Aplicada 2017/19 MICF FFUP
 FENÓMENOS DE TRANSPORTE ELETROFORESE ELETROFORESE:GENERALIDADES Movimento de partículas num campo elétrico externo Técnica usada para separar e às vezes purificar macromoléculas que diferem na carga, conformação
FENÓMENOS DE TRANSPORTE ELETROFORESE ELETROFORESE:GENERALIDADES Movimento de partículas num campo elétrico externo Técnica usada para separar e às vezes purificar macromoléculas que diferem na carga, conformação
PRÁTICA: CARACTERIZAÇÃO DE PROTEÍNAS
 CENTRO DE CIÊNCIAS E TECNOLOGIA DISCIPLINA BIOQUÍMICA Profas. Roziana Jordão e Alexandra Salgueiro PRÁTICA: CARACTERIZAÇÃO DE PROTEÍNAS I Objetivos Caracterizar a presença de proteínas; Verificar experimentalmente
CENTRO DE CIÊNCIAS E TECNOLOGIA DISCIPLINA BIOQUÍMICA Profas. Roziana Jordão e Alexandra Salgueiro PRÁTICA: CARACTERIZAÇÃO DE PROTEÍNAS I Objetivos Caracterizar a presença de proteínas; Verificar experimentalmente
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas
 Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
ESTABILIDADE DE ENZIMAS
 ESTABILIDADE DE ENZIMAS Estabilidade Enzimática X Atividade Enzimática Atividade Enzimática: É dada pela medição da velocidade inicial da reação sob uma faixa de condições determinadas. Establidade Enzimática:
ESTABILIDADE DE ENZIMAS Estabilidade Enzimática X Atividade Enzimática Atividade Enzimática: É dada pela medição da velocidade inicial da reação sob uma faixa de condições determinadas. Establidade Enzimática:
Métodos Físicos de Análise - ESPECTROFOTOMETRIA NO INFRAVERMELHO
 Métodos Físicos de Análise - ESPECTROFOTOMETRIA NO INFRAVERMELHO Prof. Dr. Leonardo Lucchetti Mestre e Doutor em Ciências Química de Produtos Naturais NPPN/UFRJ Depto. de Química de Produtos Naturais Farmanguinhos
Métodos Físicos de Análise - ESPECTROFOTOMETRIA NO INFRAVERMELHO Prof. Dr. Leonardo Lucchetti Mestre e Doutor em Ciências Química de Produtos Naturais NPPN/UFRJ Depto. de Química de Produtos Naturais Farmanguinhos
ESTRUTURA DAS PROTEÍNAS
 ESTRUTURA DAS PROTEÍNAS Todas essas forças são usadas para a manutenção da estrutura tridimensional das proteínas - conformação A conformação de uma proteína é fundamental para a função que ela exerce
ESTRUTURA DAS PROTEÍNAS Todas essas forças são usadas para a manutenção da estrutura tridimensional das proteínas - conformação A conformação de uma proteína é fundamental para a função que ela exerce
Proteínas. Profa. Alana Cecília
 Proteínas Profa. Alana Cecília Proteínas Aminoácidos ligados formam uma cadeia proteica (polipeptídica). As unidades de repetição são planos de amida que contêm ligações peptídicas. Esses planos de amida
Proteínas Profa. Alana Cecília Proteínas Aminoácidos ligados formam uma cadeia proteica (polipeptídica). As unidades de repetição são planos de amida que contêm ligações peptídicas. Esses planos de amida
ESTRUTURA DAS PROTEÍNAS
 ESTRUTURA DAS PROTEÍNAS Como é a estrutura tridimensional das proteínas??? 4 níveis estruturais Estrutura primária, secundária, terciária e quaternária Mantidas por: ligações covalentes (ligação peptídica
ESTRUTURA DAS PROTEÍNAS Como é a estrutura tridimensional das proteínas??? 4 níveis estruturais Estrutura primária, secundária, terciária e quaternária Mantidas por: ligações covalentes (ligação peptídica
Tecnicas analiticas para Joias
 Tecnicas analiticas para Joias Técnicas avançadas de analise A caracterização de gemas e metais da área de gemologia exige a utilização de técnicas analíticas sofisticadas. Estas técnicas devem ser capazes
Tecnicas analiticas para Joias Técnicas avançadas de analise A caracterização de gemas e metais da área de gemologia exige a utilização de técnicas analíticas sofisticadas. Estas técnicas devem ser capazes
QUI346 QUÍMICA ANALÍTICA INSTRUMENTAL
 QUI346 QUÍMICA ANALÍTICA INSTRUMENTAL Prof. Mauricio Xavier Coutrim DEQUI RADIAÇÃO ELETROMAGNÉTICA Onda eletromagnética (vácuo: v = 2,99792.10 8 m.s -1 ) l = comprimento de onda A = amplitude da onda v
QUI346 QUÍMICA ANALÍTICA INSTRUMENTAL Prof. Mauricio Xavier Coutrim DEQUI RADIAÇÃO ELETROMAGNÉTICA Onda eletromagnética (vácuo: v = 2,99792.10 8 m.s -1 ) l = comprimento de onda A = amplitude da onda v
UNIVERSIDADE FEDERAL DO PARANÁ Departamento de Química. CQ122 Química Analítica Instrumental II Prof. Claudio Antonio Tonegutti Aula 01 09/11/2012
 UNIVERSIDADE FEDERAL DO PARANÁ Departamento de Química CQ122 Química Analítica Instrumental II Prof. Claudio Antonio Tonegutti Aula 01 09/11/2012 A Química Analítica A divisão tradicional em química analítica
UNIVERSIDADE FEDERAL DO PARANÁ Departamento de Química CQ122 Química Analítica Instrumental II Prof. Claudio Antonio Tonegutti Aula 01 09/11/2012 A Química Analítica A divisão tradicional em química analítica
Análise de alimentos II Introdução aos Métodos Espectrométricos
 Análise de alimentos II Introdução aos Métodos Espectrométricos Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 Introdução Métodos espectrométricos Abrangem um grupo de métodos analíticos
Análise de alimentos II Introdução aos Métodos Espectrométricos Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 Introdução Métodos espectrométricos Abrangem um grupo de métodos analíticos
ÍNDICE. Prefácio... 5
 ÍNDICE Prefácio... 5 1. INTRODUÇÃO 1.1. Identificação de Estruturas Moleculares.... 1.2. Radiação Electromagnética. Regiões Características e Tipos de Interacção com a Materia.......... 7 9 2. ESPECTROSCOPIA
ÍNDICE Prefácio... 5 1. INTRODUÇÃO 1.1. Identificação de Estruturas Moleculares.... 1.2. Radiação Electromagnética. Regiões Características e Tipos de Interacção com a Materia.......... 7 9 2. ESPECTROSCOPIA
Estrutura Secundária
 Bioinformática I Estrutura Secundária Profa. Dra. Ignez Caracelli bit.603@gmail.com Julio Zukerman Schpector 1 Ignez Caracelli aminoácido em sua forma ionizada forma zwitteriônica cadeia lateral amino-terminal
Bioinformática I Estrutura Secundária Profa. Dra. Ignez Caracelli bit.603@gmail.com Julio Zukerman Schpector 1 Ignez Caracelli aminoácido em sua forma ionizada forma zwitteriônica cadeia lateral amino-terminal
Origem grego (protos) primeira, mais importante
 PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
UNIFESO Engenharia Ambiental Prof.: Edson R. Fernandes dos Santos Aminoácidos
 UNIFESO Engenharia Ambiental Prof.: Edson R. Fernandes dos Santos Aminoácidos Clique para editar o estilo do subtítulo mestre α-aminoácidos Variações possíveis Estrutura básica Amina Ácido Carboxílico
UNIFESO Engenharia Ambiental Prof.: Edson R. Fernandes dos Santos Aminoácidos Clique para editar o estilo do subtítulo mestre α-aminoácidos Variações possíveis Estrutura básica Amina Ácido Carboxílico
Profº Lásaro Henrique
 Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
Detecção de proteínas. Proteínas são heteropolímeros de aminoácidos unidos por ligações peptídicas
 Detecção de proteínas Proteínas são heteropolímeros de aminoácidos unidos por ligações peptídicas A detecção e quantificação de uma proteína através de espectrofotometria se baseia nas propriedades de
Detecção de proteínas Proteínas são heteropolímeros de aminoácidos unidos por ligações peptídicas A detecção e quantificação de uma proteína através de espectrofotometria se baseia nas propriedades de
Agronomia Química Analítica Prof. Dr. Gustavo Rocha de Castro. As medidas baseadas na luz (radiação eletromagnética) são muito empregadas
 ESPECTROMETRIA DE ABSORÇÃO ATÔMICA Introdução As medidas baseadas na luz (radiação eletromagnética) são muito empregadas na química analítica. Estes métodos são baseados na quantidade de radiação emitida
ESPECTROMETRIA DE ABSORÇÃO ATÔMICA Introdução As medidas baseadas na luz (radiação eletromagnética) são muito empregadas na química analítica. Estes métodos são baseados na quantidade de radiação emitida
FFI0750 Biologia Molecular Estrutural
 Objetivos FFI0750 Biologia Molecular Estrutural Prof. Rafael V. C. Guido rvcguido@ifsc.usp.br Estrutura de proteínas Estrutura primária Estrutura secundária Estrutura terciária Estrutura quaternária Aula
Objetivos FFI0750 Biologia Molecular Estrutural Prof. Rafael V. C. Guido rvcguido@ifsc.usp.br Estrutura de proteínas Estrutura primária Estrutura secundária Estrutura terciária Estrutura quaternária Aula
Química Orgânica. Isomeria. Química Orgânica - Prof. Geraldo Lopes Crossetti
 Química Orgânica Isomeria 1 Isomeria Compostos diferentes Mesma fórmula molecular mas diferente estrutura Diferença na ordem em que os átomos estão ligados Isômeros constitucionais (isômeros planos) Isômeros
Química Orgânica Isomeria 1 Isomeria Compostos diferentes Mesma fórmula molecular mas diferente estrutura Diferença na ordem em que os átomos estão ligados Isômeros constitucionais (isômeros planos) Isômeros
Introdução aos métodos instrumentais
 Introdução aos métodos instrumentais Métodos instrumentais Métodos que dependem da medição de propriedades elétricas, e os que estão baseados na: determinação da absorção da radiação, na medida da intensidade
Introdução aos métodos instrumentais Métodos instrumentais Métodos que dependem da medição de propriedades elétricas, e os que estão baseados na: determinação da absorção da radiação, na medida da intensidade
Proteínas. - Revisão - Prof a. Dr a. Elisa d Avila Costa Cavalcanti. Bromatologia EN/UNIRIO
 Proteínas - Revisão - Prof a. Dr a. Elisa d Avila Costa Cavalcanti Bromatologia EN/UNIRIO 2018.2 O que são proteínas? Aminoácidos α 21 tipos Grupos R Tendência de interagir com a água em ph intracelular
Proteínas - Revisão - Prof a. Dr a. Elisa d Avila Costa Cavalcanti Bromatologia EN/UNIRIO 2018.2 O que são proteínas? Aminoácidos α 21 tipos Grupos R Tendência de interagir com a água em ph intracelular
AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES
 Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011
 BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
Aulas 9 Espectroscopia
 Laboratório rio de Física F IV Aulas 9 Espectroscopia Profs.: Eduardo Ribeiro de Azevêdo e Luiz Antonio O. Nunes Técnico de Lab.: Ércio Santoni O ESPECTRO ELETROMAGNÉTICO TICO 0,4 0.7 µm λ = c f Azul 0.4µm
Laboratório rio de Física F IV Aulas 9 Espectroscopia Profs.: Eduardo Ribeiro de Azevêdo e Luiz Antonio O. Nunes Técnico de Lab.: Ércio Santoni O ESPECTRO ELETROMAGNÉTICO TICO 0,4 0.7 µm λ = c f Azul 0.4µm
PROVA DE INGRESSO IFSC PÓS GRADUAÇÃO EM FÍSICA ÁREA: FÍSICA APLICADA SUB ÁREA: FÍSICA BIOMOLECULAR. 20 de outubro de º semestre de 2010
 PROVA DE INGRESSO IFSC PÓS GRADUAÇÃO EM FÍSICA SUB ÁREA: FÍSICA BIOMOLECULAR Número de Inscrição (anote este número em TODAS as folhas da prova): Instruções: A prova contém 15 questões de múltipla escolha
PROVA DE INGRESSO IFSC PÓS GRADUAÇÃO EM FÍSICA SUB ÁREA: FÍSICA BIOMOLECULAR Número de Inscrição (anote este número em TODAS as folhas da prova): Instruções: A prova contém 15 questões de múltipla escolha
Edital lfsc-07/2013 Concurso Público Especialista em Laboratório
 Edital lfsc-07/2013 Concurso Público Especialista em Laboratório RESPOSTAS DA PROVA DISSERTATIVA Questão 1 a) O photobleaching é a destruição do fotossensibilizador para terapia fotodinâmica por processos
Edital lfsc-07/2013 Concurso Público Especialista em Laboratório RESPOSTAS DA PROVA DISSERTATIVA Questão 1 a) O photobleaching é a destruição do fotossensibilizador para terapia fotodinâmica por processos
Lista de Exercício 2ª TVC Química Analítica V Teoria (1º Sem 2016). Obs.: Entregar antes da 2ª TVC.
 Lista de Exercício 2ª TVC Química Analítica V Teoria (1º Sem 2016). Obs.: Entregar antes da 2ª TVC. Capítulo 24 (Skoog) Introdução aos Métodos Espectroquímicos 24-1. Por que uma solução de Cu(NH3)4 2+
Lista de Exercício 2ª TVC Química Analítica V Teoria (1º Sem 2016). Obs.: Entregar antes da 2ª TVC. Capítulo 24 (Skoog) Introdução aos Métodos Espectroquímicos 24-1. Por que uma solução de Cu(NH3)4 2+
Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N Professores. Carlos T. Hotta Ronaldo B.
 Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N 2016 Professores Carlos T. Hotta Ronaldo B. Quaggio 1 1. Um extrato de proteínas foi obtido a partir da
Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N 2016 Professores Carlos T. Hotta Ronaldo B. Quaggio 1 1. Um extrato de proteínas foi obtido a partir da
Departamento de Zoologia da Universidade de Coimbra
 Departamento de Zoologia da Universidade de Coimbra Armando Cristóvão Adaptado de "The Tools of Biochemistry" de Terrance G. Cooper Espectrofotometria de Absorção Uma das primeiras características químicas
Departamento de Zoologia da Universidade de Coimbra Armando Cristóvão Adaptado de "The Tools of Biochemistry" de Terrance G. Cooper Espectrofotometria de Absorção Uma das primeiras características químicas
Aula 12 PRÁTICA 02 ESPECTROFOTOMETRIA DE ABSORÇÃO MOLECULAR NO UV VIS: OPERAÇÃO E RESPOSTA DO ESPECTROFOTÔMETRO. Elisangela de Andrade Passos
 Aula 12 PRÁTICA 02 ESPECTROFOTOMETRIA DE ABSORÇÃO MOLECULAR NO UV VIS: OPERAÇÃO E RESPOSTA DO ESPECTROFOTÔMETRO META Proporcionar o contato do aluno com a instrumentação analítica empregada em análises
Aula 12 PRÁTICA 02 ESPECTROFOTOMETRIA DE ABSORÇÃO MOLECULAR NO UV VIS: OPERAÇÃO E RESPOSTA DO ESPECTROFOTÔMETRO META Proporcionar o contato do aluno com a instrumentação analítica empregada em análises
Macromolécula mais abundante nas células
 PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
Descritivo de produto. Fornecedor.
 Descritivo de produto Fornecedor www.pginstruments.com ESPECTROFOTÔMETRO T70 DESCRIÇÃO T70 é um espectrofotômetro de simples feixe para leituras nas faixas UV-VIS marca PG Instruments de procedência inglesa.
Descritivo de produto Fornecedor www.pginstruments.com ESPECTROFOTÔMETRO T70 DESCRIÇÃO T70 é um espectrofotômetro de simples feixe para leituras nas faixas UV-VIS marca PG Instruments de procedência inglesa.
Prof. Hugo Braibante Química - UFSM
 Prof. Hugo Braibante Química - UFSM estereoquímica Conceitos Forma tridimensional das moléculas Moléculas como objeto-imagens Moléculas com simetria Separação de Enantiômeros Diastereoisômeros Atividade
Prof. Hugo Braibante Química - UFSM estereoquímica Conceitos Forma tridimensional das moléculas Moléculas como objeto-imagens Moléculas com simetria Separação de Enantiômeros Diastereoisômeros Atividade
BOTUCATU, SP - RUBIÃO JUNIOR Fone (0xx14) fax
 Universidade Estadual Paulista Instituto de Biociências Seção de Pós-Graduação BOTUCATU, SP - RUBIÃO JUNIOR - 18618-000 - Fone (0xx14) 68026148 - fax 68023744 e-mail:posgraduacao@ibb.unesp.br Curso de
Universidade Estadual Paulista Instituto de Biociências Seção de Pós-Graduação BOTUCATU, SP - RUBIÃO JUNIOR - 18618-000 - Fone (0xx14) 68026148 - fax 68023744 e-mail:posgraduacao@ibb.unesp.br Curso de
Espectroscopia Óptica Instrumentação e aplicações UV/VIS. CQ122 Química Analítica Instrumental II 1º sem Prof. Claudio Antonio Tonegutti
 Espectroscopia Óptica Instrumentação e aplicações UV/VIS CQ122 Química Analítica Instrumental II 1º sem. 2017 Prof. Claudio Antonio Tonegutti Lei de Beer A = b c A = absorbância = absortividade molar (L
Espectroscopia Óptica Instrumentação e aplicações UV/VIS CQ122 Química Analítica Instrumental II 1º sem. 2017 Prof. Claudio Antonio Tonegutti Lei de Beer A = b c A = absorbância = absortividade molar (L
ESTRUTURA DAS PROTEÍNAS
 ESTRUTURA DAS PROTEÍNAS Como é a estrutura tridimensional das proteínas??? 4 níveis estruturais Estrutura primária, secundária, terciária e quaternária Mantidas por: ligações covalentes (ligação peptídica
ESTRUTURA DAS PROTEÍNAS Como é a estrutura tridimensional das proteínas??? 4 níveis estruturais Estrutura primária, secundária, terciária e quaternária Mantidas por: ligações covalentes (ligação peptídica
Converta os seguintes dados de transmitâncias para as respectivas absorbâncias: (a) 22,7% (b) 0,567 (c) 31,5% (d) 7,93% (e) 0,103 (f ) 58,2%
 Lista de Exercício 2ª TVC Química Analítica V Teoria (2º Sem 2017). Obs.: 1) A lista deve ser entregue antes da 2ª TVC (24/10). 2) O exercícios devem ser feitos a mão Capítulo 24 (Skoog) Introdução aos
Lista de Exercício 2ª TVC Química Analítica V Teoria (2º Sem 2017). Obs.: 1) A lista deve ser entregue antes da 2ª TVC (24/10). 2) O exercícios devem ser feitos a mão Capítulo 24 (Skoog) Introdução aos
Aplica-se à observação de microorganismos vivos, sem preparação prévia (coloração)
 Campo Escuro Campo Escuro Constitui uma técnica especializada de iluminação que utiliza a luz oblíqua para reforçar o contraste em espécimes que não estão bem definidas sob condições normais de iluminação
Campo Escuro Campo Escuro Constitui uma técnica especializada de iluminação que utiliza a luz oblíqua para reforçar o contraste em espécimes que não estão bem definidas sob condições normais de iluminação
Bioinformática RESSONÂNCIA MAGNÉTICA NUCLEAR - RMN. Disciplina de Bioinformática Alunas: Rayssa H Arruda Pereira Taciane Barbosa Henriques
 Bioinformática RESSONÂNCIA MAGNÉTICA NUCLEAR - RMN Disciplina de Bioinformática Alunas: Rayssa H Arruda Pereira Taciane Barbosa Henriques Introdução A espectroscopia por Ressonância Magnética Nuclear (RMN)
Bioinformática RESSONÂNCIA MAGNÉTICA NUCLEAR - RMN Disciplina de Bioinformática Alunas: Rayssa H Arruda Pereira Taciane Barbosa Henriques Introdução A espectroscopia por Ressonância Magnética Nuclear (RMN)
a) ( ) 7,7 ml b) ( ) 15,1 ml c) ( ) 20,7 ml d) ( ) 2,8 ml Resposta Questão 01 Gabarito Questão 1) alternativa C.
 QUESTÕES DE ÂMBITO GERL Questão 01: Sabendo que a pureza do HCl concentrado é de 37%, sua massa molar é de 36,46 g mol -1 e sua densidade é de 1,19 g ml -1, pode-se afirmar que o volume de HCl concentrado
QUESTÕES DE ÂMBITO GERL Questão 01: Sabendo que a pureza do HCl concentrado é de 37%, sua massa molar é de 36,46 g mol -1 e sua densidade é de 1,19 g ml -1, pode-se afirmar que o volume de HCl concentrado
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL. FÍSICA PARA CIÊNCIAS BIOLÓGIAS.
 UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL. FÍSICA PARA CIÊNCIAS BIOLÓGIAS. ASPECTOS FÍSICO-QUÍMICOS DA ABSORÇÃO DE ENERGIA SOLAR NA FOTOSSÍNTESE. Professor: Thomas Braun. Graduando: Carlos Santos Costa.
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL. FÍSICA PARA CIÊNCIAS BIOLÓGIAS. ASPECTOS FÍSICO-QUÍMICOS DA ABSORÇÃO DE ENERGIA SOLAR NA FOTOSSÍNTESE. Professor: Thomas Braun. Graduando: Carlos Santos Costa.
OBJETIVOS BIBLIOGRAFIA ENZIMAS E INIBIDORES ENZIMÁTICOS
 OBJETIVOS Enzimas: Funções, Nomenclatura e Propriedades Fundamentos da Cinética Enzimática Cinética Enzimática: Michaelis-Menten Ensaios Cinéticos: Padronização e Validação Parâmetros Cinéticos: vo, KM,
OBJETIVOS Enzimas: Funções, Nomenclatura e Propriedades Fundamentos da Cinética Enzimática Cinética Enzimática: Michaelis-Menten Ensaios Cinéticos: Padronização e Validação Parâmetros Cinéticos: vo, KM,
LICENCIATURA EM QUÍMICA QUÍMICA ORGÂNICA I SEGUNDO SEMESTRE 2014 PLANO DE CURSO Professora: Ana Júlia Silveira
 LICENCIATURA EM QUÍMICA QUÍMICA ORGÂNICA I SEGUNDO SEMESTRE 2014 PLANO DE CURSO Professora: Ana Júlia Silveira EMENTA QUÍMICA ORGÂNICA I Introdução a química orgânica: teoria estrutural e o átomo de carbono
LICENCIATURA EM QUÍMICA QUÍMICA ORGÂNICA I SEGUNDO SEMESTRE 2014 PLANO DE CURSO Professora: Ana Júlia Silveira EMENTA QUÍMICA ORGÂNICA I Introdução a química orgânica: teoria estrutural e o átomo de carbono
Proteínas. Professora: Luciana Ramalho 2017
 Proteínas Professora: Luciana Ramalho 2017 Introdução Também chamados de Peptídeo As proteínas são macromoléculas orgânicas formadas pela sequência de vários aminoácidos, unidos por ligações peptídicas
Proteínas Professora: Luciana Ramalho 2017 Introdução Também chamados de Peptídeo As proteínas são macromoléculas orgânicas formadas pela sequência de vários aminoácidos, unidos por ligações peptídicas
K P 10. Concentração. Potência a emissão de fluorescência (F) é proporcional à potência radiante do feixe de excitação que é absorvido pelo sistema
 Concentração Potência a emissão de fluorescência (F) é proporcional à potência radiante do feixe de excitação que é absorvido pelo sistema F = emissão de fluorescência P o = potência do feixe incidente
Concentração Potência a emissão de fluorescência (F) é proporcional à potência radiante do feixe de excitação que é absorvido pelo sistema F = emissão de fluorescência P o = potência do feixe incidente
Cristalização de Macromoléculas Biológicas
 Cristalização de Macromoléculas Biológicas Laboratório de Sistemas Biomoleculares Departamento de Física IBILCE-UNESP Aspectos Gerais A cristalografia de raios X revela as posições tridimensionais da maioria
Cristalização de Macromoléculas Biológicas Laboratório de Sistemas Biomoleculares Departamento de Física IBILCE-UNESP Aspectos Gerais A cristalografia de raios X revela as posições tridimensionais da maioria
Física Experimental C. Coeficiente de Atenuação dos Raios Gama
 Carlos Ramos (Poli USP)-2016/Andrius Poškus (Vilnius University) - 2012 4323301 Física Experimental C Coeficiente de Atenuação dos Raios Gama Grupo: Nome No. USP No. Turma OBJETIVOS - Medir curvas de atenuação
Carlos Ramos (Poli USP)-2016/Andrius Poškus (Vilnius University) - 2012 4323301 Física Experimental C Coeficiente de Atenuação dos Raios Gama Grupo: Nome No. USP No. Turma OBJETIVOS - Medir curvas de atenuação
Proteínas. Professora: Luciana Ramalho 2018
 Proteínas Professora: Luciana Ramalho 2018 Introdução Também chamados de Peptídeo As proteínas são macromoléculas orgânicas formadas pela sequência de vários aminoácidos, unidos por ligações peptídicas
Proteínas Professora: Luciana Ramalho 2018 Introdução Também chamados de Peptídeo As proteínas são macromoléculas orgânicas formadas pela sequência de vários aminoácidos, unidos por ligações peptídicas
Grupo 14 - Ácidos Nucléicos: Nucleotídeos, DNA e RNA.
 Grupo 14 - Ácidos Nucléicos: Nucleotídeos, DNA e RNA. Andrés M Gonçalves de Jesus; Danilo Badaró; Diego Oliveira; Erica Saemi Miyasato; Fernando Pereira; Rodolfo M. de Aquino Ácidos nucleicos são biopolímeros,
Grupo 14 - Ácidos Nucléicos: Nucleotídeos, DNA e RNA. Andrés M Gonçalves de Jesus; Danilo Badaró; Diego Oliveira; Erica Saemi Miyasato; Fernando Pereira; Rodolfo M. de Aquino Ácidos nucleicos são biopolímeros,
Programa Analítico de Disciplina BQI450 Bioquímica de Proteínas
 0 Programa Analítico de Disciplina Departamento de Bioquímica e Biologia Molecular - Centro de Ciências Biológicas e da Saúde Número de créditos: 4 Teóricas Práticas Total Duração em semanas: 15 Carga
0 Programa Analítico de Disciplina Departamento de Bioquímica e Biologia Molecular - Centro de Ciências Biológicas e da Saúde Número de créditos: 4 Teóricas Práticas Total Duração em semanas: 15 Carga
ASPECTOS GERAIS. Prof. Harley P. Martins filho
 /6/08 ASPECTOS GERAIS Prof. Harley P. Martins filho Aspectos Gerais Espectroscopia por emissão: Abaixamento de energia de um sistema de um nível permitido para outro, com emissão da energia perdida na
/6/08 ASPECTOS GERAIS Prof. Harley P. Martins filho Aspectos Gerais Espectroscopia por emissão: Abaixamento de energia de um sistema de um nível permitido para outro, com emissão da energia perdida na
Sistema de eletroforese MiniProtean, marca BIO-RAD.
 Sistema de eletroforese MiniProtean, marca BIO-RAD. O sistema de eletroforese SDS-PAGE é utilizado para realizar separar caracterizar ou mesmo determinar a pureza de macromoléculas. O LABIOM dispõe de
Sistema de eletroforese MiniProtean, marca BIO-RAD. O sistema de eletroforese SDS-PAGE é utilizado para realizar separar caracterizar ou mesmo determinar a pureza de macromoléculas. O LABIOM dispõe de
Estudo de um Polimorfismo no Gene da Cadeia Pesada β da Miosina (CPβM)
 Estudo de um Polimorfismo no Gene da Cadeia Pesada β da Miosina (CPβM) Ana Luísa Carvalho Departamento de Zoologia, Universidade de Coimbra Introdução: Neste trabalho pretende-se analisar um polimorfismo
Estudo de um Polimorfismo no Gene da Cadeia Pesada β da Miosina (CPβM) Ana Luísa Carvalho Departamento de Zoologia, Universidade de Coimbra Introdução: Neste trabalho pretende-se analisar um polimorfismo
Lista de exercícios. Biofísica.
 Lista de exercícios. Biofísica. 1) Desenhe a estrutura química dos tripeptídeos (a) Ala-Leu-Phe, (b) Ser-Pro- Asn., (c) Met-Trp-Gly. (a) Ala-Leu-Phe O O + N 3 C C N C C N C C O C 3 O - C C 3 C 3 (b) Ser-Pro-Asn
Lista de exercícios. Biofísica. 1) Desenhe a estrutura química dos tripeptídeos (a) Ala-Leu-Phe, (b) Ser-Pro- Asn., (c) Met-Trp-Gly. (a) Ala-Leu-Phe O O + N 3 C C N C C N C C O C 3 O - C C 3 C 3 (b) Ser-Pro-Asn
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO CENTRO DE CIÊNCIAS MATEMÁTICAS E DA NATUREZA INSTITUTO DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA
 UNIVERSIDADE FEDERAL DO RIO DE JANEIRO CENTRO DE CIÊNCIAS MATEMÁTICAS E DA NATUREZA INSTITUTO DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA DISCIPLINA: IQB-248 - BIOQUÍMICA EQ PRÉ-REQUISITOS: QUÍMICA ORGÂNICA
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO CENTRO DE CIÊNCIAS MATEMÁTICAS E DA NATUREZA INSTITUTO DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA DISCIPLINA: IQB-248 - BIOQUÍMICA EQ PRÉ-REQUISITOS: QUÍMICA ORGÂNICA
USO DE FTIR PARA ANÁLISE DE BACTÉRIAS CAUSADORAS DO CANCRO CÍTRICO E CVC
 ISSN 43-6244 Empresa Brasileira de Pesquisa Agropecuária Centro Nacional de Pesquisa e Desenvolvimento de Instrumentação Agropecuária Ministério da Agricultura e do Abastecimento Rua XV de Novembro, 452
ISSN 43-6244 Empresa Brasileira de Pesquisa Agropecuária Centro Nacional de Pesquisa e Desenvolvimento de Instrumentação Agropecuária Ministério da Agricultura e do Abastecimento Rua XV de Novembro, 452
Os princípios da espectroscopia: Teoria DESENVOLVENDO UMA CIÊNCIAMELHOR AGILENT E VOCÊ
 Os princípios da espectroscopia: Teoria DESENVOLVENDO UMA CIÊNCIAMELHOR AGILENT E VOCÊ 1 A Agilent tem um compromisso com a comunidade educacional e está disposta a conceder acesso ao material de propriedade
Os princípios da espectroscopia: Teoria DESENVOLVENDO UMA CIÊNCIAMELHOR AGILENT E VOCÊ 1 A Agilent tem um compromisso com a comunidade educacional e está disposta a conceder acesso ao material de propriedade
Ressonância Magnética Nuclear
 Ressonância Magnética Nuclear Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Raios-X são as radiações
Ressonância Magnética Nuclear Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Raios-X são as radiações
Curso: FARMÁCIA Disciplina: Bioquímica Clínica Título da Aula: Funcionamento do Espectrofotômetro. Glicemia. Professor: Dr.
 Curso: FARMÁCIA Disciplina: Bioquímica Clínica Título da Aula: Funcionamento do Espectrofotômetro. Glicemia. Professor: Dr. Fernando Ananias NOME: RA: ATIVIDADE PRÁTICA 1 A- ESPECTROFOTOMETRIA Espectroscopia
Curso: FARMÁCIA Disciplina: Bioquímica Clínica Título da Aula: Funcionamento do Espectrofotômetro. Glicemia. Professor: Dr. Fernando Ananias NOME: RA: ATIVIDADE PRÁTICA 1 A- ESPECTROFOTOMETRIA Espectroscopia
Purificação de Potyvirus de ocorrência natural em Hypochaeris brasiliensis
 Purificação de Potyvirus de ocorrência natural em Hypochaeris brasiliensis SILVA, J. A 1.; BRIZOLA, D. C 2.; DIAS, L. A. F 2.; POLICAN, P. M 2.; ALMEIDA, A. M. R 2., 1 Centro Universitário Filadélfia,
Purificação de Potyvirus de ocorrência natural em Hypochaeris brasiliensis SILVA, J. A 1.; BRIZOLA, D. C 2.; DIAS, L. A. F 2.; POLICAN, P. M 2.; ALMEIDA, A. M. R 2., 1 Centro Universitário Filadélfia,
Lentes de Bordos Finos
 Lentes de Bordos Finos Geralmente convergentes, ou seja, convergentes quando n lente >n meio. -O meio que envolve a lente geralmente é o ar, menos refrigente que o vidro. Lentes de Bordos Grossos Geralmente
Lentes de Bordos Finos Geralmente convergentes, ou seja, convergentes quando n lente >n meio. -O meio que envolve a lente geralmente é o ar, menos refrigente que o vidro. Lentes de Bordos Grossos Geralmente
ISOMERIA. Compostos diferentes com a mesma fórmula molecular denominam-se isômeros.
 ISOMERIA Compostos diferentes com a mesma fórmula molecular denominam-se isômeros. Isômeros constitucionais (ou estruturais) são isômeros que diferem devido à diferente ligação dos seus átomos. Por exemplo:
ISOMERIA Compostos diferentes com a mesma fórmula molecular denominam-se isômeros. Isômeros constitucionais (ou estruturais) são isômeros que diferem devido à diferente ligação dos seus átomos. Por exemplo:
Dos genes às proteínas
 Dos genes às proteínas - Estrutura e função Bioinformática aula 1 INTRODUÇÃO O Dogma Central O fluxo de informação nos organismos segue uma direção única: do DNA para o RNA, e do RNA para a proteína DNA
Dos genes às proteínas - Estrutura e função Bioinformática aula 1 INTRODUÇÃO O Dogma Central O fluxo de informação nos organismos segue uma direção única: do DNA para o RNA, e do RNA para a proteína DNA
Engenharia de Proteínas 2017 Ciências Biológicas FCAV/UNESP. Prof. Marcos Túlio Oliveira Depto. Tecnologia
 Engenharia de Proteínas 2017 Ciências Biológicas FCAV/UNESP Prof. Marcos Túlio Oliveira Depto. Tecnologia Engenharia de Proteínas 2017 Ciências Biológicas FCAV/UNESP Green Fluorescent Protein (GFP) Engenharia
Engenharia de Proteínas 2017 Ciências Biológicas FCAV/UNESP Prof. Marcos Túlio Oliveira Depto. Tecnologia Engenharia de Proteínas 2017 Ciências Biológicas FCAV/UNESP Green Fluorescent Protein (GFP) Engenharia
Metodologia Analítica
 Metodologia Analítica Espectrofotometria UV-vis Prof. Renato Camargo Matos http://www.ufjf.br/nupis Prática Otimização de um Método Espectrofotométrico para Quantificação de Ferro Objetivo Estudar as propriedades
Metodologia Analítica Espectrofotometria UV-vis Prof. Renato Camargo Matos http://www.ufjf.br/nupis Prática Otimização de um Método Espectrofotométrico para Quantificação de Ferro Objetivo Estudar as propriedades
Ácidos Nucleicos e Nucleotídeos
 Ácidos Nucleicos e Nucleotídeos Andrés M Gonçalves de Jesus; Danilo Badaró; Diego Oliveira; Erica Saemi Miyasato; Fernando Pereira; Rodolfo M. de Aquino Ácidos nucleicos são constituídos por nucleotídeos
Ácidos Nucleicos e Nucleotídeos Andrés M Gonçalves de Jesus; Danilo Badaró; Diego Oliveira; Erica Saemi Miyasato; Fernando Pereira; Rodolfo M. de Aquino Ácidos nucleicos são constituídos por nucleotídeos
Técnicas de Caracterização de Materiais
 Técnicas de Caracterização de Materiais 4302504 2º Semestre de 2016 Instituto de Física Universidade de São Paulo Professores: Antonio Domingues dos Santos Manfredo H. Tabacniks 23 e 25 de agosto Energia
Técnicas de Caracterização de Materiais 4302504 2º Semestre de 2016 Instituto de Física Universidade de São Paulo Professores: Antonio Domingues dos Santos Manfredo H. Tabacniks 23 e 25 de agosto Energia
Lista de Exercícios de Bioquímica
 Universidade Federal de Santa Catarina - UFSC Departamento de Bioquímica - CCB Disciplina: BQA5125 - Bioquímica para Engenharia Sanitária e Ambiental Bolsistas REUNI: Priscila G. A. Martins e Tiago Bortolotto
Universidade Federal de Santa Catarina - UFSC Departamento de Bioquímica - CCB Disciplina: BQA5125 - Bioquímica para Engenharia Sanitária e Ambiental Bolsistas REUNI: Priscila G. A. Martins e Tiago Bortolotto
Aminoácidos e peptídeos. Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I
 Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
Tópicos em Métodos Espectroquímicos. Aula 2 Revisão Conceitos Fundamentais
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Revisão Conceitos Fundamentais Julio C. J. Silva Juiz de For a, 2015
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Revisão Conceitos Fundamentais Julio C. J. Silva Juiz de For a, 2015
Aplicações de Enzimas e Biocatálise
 Aplicações de Enzimas e Biocatálise Estabilidade enzimática Raúl J. Barros 2012 Uma preparação enzimática geralmente perde atividade ao longo do tempo, à medida que as moléculas proteicas que a constituem
Aplicações de Enzimas e Biocatálise Estabilidade enzimática Raúl J. Barros 2012 Uma preparação enzimática geralmente perde atividade ao longo do tempo, à medida que as moléculas proteicas que a constituem
Tópicos em Métodos Espectroquímicos. Aula 2 Revisão Conceitos Fundamentais
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Revisão Conceitos Fundamentais Julio C. J. Silva Juiz de For a, 2013
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Revisão Conceitos Fundamentais Julio C. J. Silva Juiz de For a, 2013
