TUTORIAL DE ANESTESIA DA SEMANA ABSORVEDORES DE GÁS CARBÔNICO
|
|
|
- Victor Gabriel Sabala Cabreira
- 7 Há anos
- Visualizações:
Transcrição
1 TUTORIAL DE ANESTESIA DA SEMANA ABSORVEDORES DE GÁS CARBÔNICO Dr. Tiago Gomes Búrigo Hospital Governador Celso Ramos, Brasil. Correspondência para AUTO-AVALIAÇÃO Assinale verdadeiro (V) ou falso (F) antes de cada afirmativa: 1. O maior componente da cal sodada é: a. ( ) Hidróxido de sódio b. ( ) Cloreto de cálcio c. ( ) Hidróxido de cálcio d. ( ) Água e. ( ) Hidróxido de potássio 2. Anestésico inalatório que em reação com o absorvedor pode produzir fogo: a. ( ) Sevoflurano b. ( ) Enflurano c. ( ) Isoflurano d. ( ) Desflurano e. ( ) Halotano 3. Sinais clínicos de que a capacidade absortiva da cal sodada esgotou-se: a. ( ) Taquicardia b. ( ) Hipertensão c. ( ) Aumento de atividade parasimpática d. ( ) Acidose metabólica e. ( ) Aumento do sangramento 4. A formação de monóxido de carbono resultante da interação dos anestésicos inalatórios com o material absorvente: a. ( ) É maior com o halotano b. ( ) Ocorre devido ao ressecamento do material c. ( ) Pode interferir com a oximetria de pulso d. ( ) Baixo fluxo de gás diminui a formação e. ( ) Alta temperatura aumenta a formação 5. Aumentam a formação de composto A: a. ( ) Baixo fluxo de gás b. ( ) Cal sodada c. ( ) Circuito fechado d. ( ) Halotano e. ( ) Alta temperatura do absorvedor WFSA-TAS - Absorvedores de gás carbônico Page 1 of 5
2 SUMÁRIO Introdução Tipos de absorvedores Reações químicas Capacidade absortiva Interações com os anestésicos inalatórios Referências INTRODUÇÃO Quando utilizamos circuitos de respiração fechados ou semi-fechados em anestesia, temos que utilizar algum sistema que absorva o gás carbônico que é gerado. Temos algumas características que são tidas como ideais para os absorvedores de CO₂: Pouca reatividade com os agentes inalatórios. Baixa toxicidade. Baixa resistência ao fluxo de ar. Baixo custo. Fácil manuseio. Absorção eficiente. TIPOS DE ABSORVEDORES Temos 3 tipos principais que são: cal sodada, cal baritada, cal de hidróxido de cálcio. Cal sodada: Tem como composição: 80% de hidróxido de cálcio. 15% de água. 4% de hidróxido de sódio 1% de hidróxido de potássio, como ativador Tamanho granular da cal sodada e da baritada deve estar entre 4 e 8 Mesh, pois assim temos uma área absortiva e uma resistência ao fluxo otimizadas. Cal baritada: Em sua composição temos: 20% de hidróxido de bário. 80% de hidróxido de cálcio. Esse tipo de absorvedor está em desuso pois é o mais relacionado a problemas, entre eles produção de fogo nos sistemas de respiração em reação com o sevoflurano. Cal de hidróxido de cálcio: Em sua composição encontramos: Hidróxido de cálcio. Cloreto de cálcio. Tem como vantagens em relação as outras duas: Não tem produção de monóxido de carbono. Não tem produção de composto A Tem como desvantagens: Menor capacidade de absorção, sendo cerca de 50% menor. Custo maior. REAÇÕES QUÍMICAS: WFSA-TAS - Absorvedores de gás carbônico Page 2 of 5
3 A absorção de dióxido de carbono pelos absorvedores é uma reação química. Cal sodada: O CO₂ une-se a água e forma ácido carbônico, que reage com os hidróxidos e forma carbonato de sódio ou de potássio e água. O hidróxido de cálcio reage com o carbonato para formar carbonato de cálcio e hidróxido de sódio ou de potássio. As seguintes equações representam o processo: CO₂ + H₂O D H₂CO₃ H₂CO₃ + 2NaOH(KOH) D Na₂CO₃(K₂CO3) + 2H₂O + calor Na₂CO₃(K₂CO₃) + Ca(OH)₂ D CaCO₃ + 2NaOH(KOH). CAPACIDADE ABSORTIVA: A capacidade absortiva máxima é de 26 litros de CO₂ por 100 gramas de substância absorvente, isso para a cal sodada. Porém, podemos ter a formação de canais entre os grânulos, onde os gases passam sem serem filtrados e isso diminui a capacidade de absorção. Já a capacidade absortiva da cal de hidróxido de cálcio é menor, sendo de 10.2 litros por cada 100 gramas. Indicadores da integridade do absorvedor: Para checar a integridade do absorvedor, é adicionado um corante, o qual muda a cor do absorvedor quando é atingido um ph crítico. Violeta de etila é adicionado tanto na cal sodada, quanto na baritada. Quando a cal já está no seu limite de absorção, o ph dela fica abaixo de 10.3 e então a cor da cal muda de branca para violeta porque ocorre desidratação, o que indica que a sua capacidade absortiva está esgotada. Podemos também ter alguns sinais clínicos de que a capacidade absortiva acabou: Aumento da frequência respiratória, se não estiver sido utilizado relaxante muscular. Aumento, inicialmente, da pressão arterial e da frequência cardíaca e posteriormente decréscimo das duas. Aumento do drive simpático e com isso podemos ter: sudorese, taquiarritmia, estado hipermetabólico. Acidose respiratória. Aumento do sangramento causado pela hipertensão que pode ocorrer. Tomar cuidado, pois se ficar por um tempo ser ser utilizada, a cal que estava violeta pode voltar a ficar branca, porém a sua capacidade absortiva está esgotada. INTERAÇÕES COM OS ANESTÉSICOS INALATÓRIOS: O sevoflurano, em interação com o absorvedor, pode gerar um produto chamado de composto A, que pode ser nefrotóxico. Temos alguns fatores que podem aumentar a produção desse composto, que são: Baixo fluxo ou circuito fechado. Uso de cal baritada. Altas concentrações de sevoflurano no circuito. Alta temperatura do absorvedor. Proveniente da interação dos inalatórios com o absorvedor, podemos ter a formação de monóxido de carbono. Em alguns casos pode-se atingir um nível de carboxihemoglobina de 35% ou mais. Isso também pode interferir com a monitorização da oximetria de pulso. Fatores que ressecam o absorvedor e que causam maior propensão a formação de monóxido de carbono são: Contato prolongado entre absorvedor e anestésicos. Depois do desuso do absorvedor, especialmente se igual ou maior a 2 dias (tomar cuidado quando o aparelho de anestesia fica desligado no final de semana e é utilizado sem ser trocada a cal na segunda-feira). Outros fatores que podem causar aumento do monóxido de carbono e elevar o nível sanguíneo de carboxihemoglobina são: WFSA-TAS - Absorvedores de gás carbônico Page 3 of 5
4 O tipo de anestésico inalatório utilizado, sendo em ordem decrescente os que mais podem produzir: desflurano, enflurano, isoflurano, halotano = sevoflurano. O tipo de material utilizado como absorvedor, sendo a cal baritada a que mais produz. Aumento da temperatura aumenta a produção. Concentrações mais altas de anestésicos. Baixas taxas de fluxo de gás fresco. O sevoflurano, como citado antes, em reação com a cal pode produzir fogo e isso pode ocorrer com maior facilidade se utilizado a cal baritada. REFERÊNCIAS Riutort TK, Brockwell RC, Brull SJ, Andrews JJ The Anesthesia Workstation and Delivery Systems, em: Barash PG, Cullen BF, Stoelting RK, Cahalan MK, Stock MC - Clinical Anesthesia, 6 th ed, Philadelphia, Lippincott Williams & Wilkins, 2009; Brockwell RC, Andrews JJ - Inhaled Anesthetic Delivery, em: Miller RD, Eriksson LI, Fleisher LA, Wiener-Kronish JP, Young WL - Miller s Anesthesia, 7 th Ed, Philadelphia, 2010; RESPOSTAS DA AUTO-AVALIAÇÃO 1. a. F e. F 2. c. F e. F 3. b. V c. F e. V 4. a. F b. V WFSA-TAS - Absorvedores de gás carbônico Page 4 of 5
5 e. V 5. e. V WFSA-TAS - Absorvedores de gás carbônico Page 5 of 5
VERIFICAÇÃO (CHECAGEM) DO APARELHO DE ANESTESIA
 TUTORIAL DE ANESTESIA DA SEMANA VERIFICAÇÃO (CHECAGEM) DO APARELHO DE ANESTESIA Dr. Tiago Gomes Búrigo Florianópolis, Brasil. Correspondência para sba@sba.com.br AUTO-AVALIAÇÃO Assinale verdadeiro (V)
TUTORIAL DE ANESTESIA DA SEMANA VERIFICAÇÃO (CHECAGEM) DO APARELHO DE ANESTESIA Dr. Tiago Gomes Búrigo Florianópolis, Brasil. Correspondência para sba@sba.com.br AUTO-AVALIAÇÃO Assinale verdadeiro (V)
QUESTÕES OBJETIVAS. a) b) +110 c) -55 d) -110 e) -676
 QUESTÕES OBJETIVAS Questão 9: O óxido de cálcio, conhecido como cal virgem, é comumente utilizado na construção civil. Sobre essa substância é INCORRETO afirmar que: a) pode ser obtida pelo aquecimento
QUESTÕES OBJETIVAS Questão 9: O óxido de cálcio, conhecido como cal virgem, é comumente utilizado na construção civil. Sobre essa substância é INCORRETO afirmar que: a) pode ser obtida pelo aquecimento
23/07/14. ! Evolução dos Equipamentos Anestésicos. Século XXI. Século XIX
 Prof. Dr. Adriano Bonfim Carregaro Medicina Veterinária FZEA USP www.anestesia.vet.br http://on.fb.me/anestesiavet! Evolução da Anestesia Inalatória! Século XV Paracelso Fluido anestésico (ácido sulfúrico
Prof. Dr. Adriano Bonfim Carregaro Medicina Veterinária FZEA USP www.anestesia.vet.br http://on.fb.me/anestesiavet! Evolução da Anestesia Inalatória! Século XV Paracelso Fluido anestésico (ácido sulfúrico
Sistemas de Respiração em Anestesia
 B A S I C S C I E N C E Tutorial 333 Sistemas de Respiração em Anestesia Dr Peter Tsim Trainee em Anestesia, Chesterfield Royal Hospital, UK Dr Allan Howatson Consultor em Anestesia e Medicina Intensiva,
B A S I C S C I E N C E Tutorial 333 Sistemas de Respiração em Anestesia Dr Peter Tsim Trainee em Anestesia, Chesterfield Royal Hospital, UK Dr Allan Howatson Consultor em Anestesia e Medicina Intensiva,
Atividade de Autoavaliação Recuperação 2 os anos Rodrigo ago/09
 Química Atividade de Autoavaliação Recuperação 2 os anos Rodrigo ago/09 Re Resolução 1. O carbeto de cálcio CaC 2 (s) (massa molar = 64 g mol 1 ), também conhecido como carbureto, pode ser obtido aquecendo-se
Química Atividade de Autoavaliação Recuperação 2 os anos Rodrigo ago/09 Re Resolução 1. O carbeto de cálcio CaC 2 (s) (massa molar = 64 g mol 1 ), também conhecido como carbureto, pode ser obtido aquecendo-se
12 GAB. 1 1 o DIA PASES 2 a ETAPA TRIÊNIO QUÍMICA QUESTÕES DE 21 A 30
 12 GAB. 1 1 o DIA PASES 2 a ETAPA TRIÊNIO 2004-2006 QUÍMICA QUESTÕES DE 21 A 30 21. Os solos brasileiros são na sua maioria ácidos, de modo que para cultiválos muitas vezes é necessária a aplicação de
12 GAB. 1 1 o DIA PASES 2 a ETAPA TRIÊNIO 2004-2006 QUÍMICA QUESTÕES DE 21 A 30 21. Os solos brasileiros são na sua maioria ácidos, de modo que para cultiválos muitas vezes é necessária a aplicação de
ESTEQUIOMETRIA Reagente em excesso e reagente limitante
 Reagente em excesso e reagente limitante Ao estudarmos as reações, nós as enchergamos como ideais, ou seja, achamos que todos os reagentes reagem completamente, exatamente como descrito nas equações químicas.
Reagente em excesso e reagente limitante Ao estudarmos as reações, nós as enchergamos como ideais, ou seja, achamos que todos os reagentes reagem completamente, exatamente como descrito nas equações químicas.
LISTA DE EXERCÍCIOS 1º ANO
 GAB LISTA - 11 a) Elemento: Carbono; número de massa do isótopo do carbono com 8 nêutrons:14 b) Moléculas com ligações polares: (figura 01) Moléculas com ligações apolares: (figura 02) a) Observe a figura
GAB LISTA - 11 a) Elemento: Carbono; número de massa do isótopo do carbono com 8 nêutrons:14 b) Moléculas com ligações polares: (figura 01) Moléculas com ligações apolares: (figura 02) a) Observe a figura
Anestesia de fluxo mínimo utilizando oxigênio como gás transportador
 Anestesia de fluxo mínimo utilizando oxigênio como gás transportador Esquema do procedimento* (de um paciente com > 6 meses) Pré-medicação Pré-medicação conforme o modelo convencional Indução Pré-oxigenação
Anestesia de fluxo mínimo utilizando oxigênio como gás transportador Esquema do procedimento* (de um paciente com > 6 meses) Pré-medicação Pré-medicação conforme o modelo convencional Indução Pré-oxigenação
1ª Série do Ensino Médio
 1ª Série do Ensino Médio 16. Considere as equações abaixo: I. H 2 + Cl 2 2 HCl II. Zn + H 2 SO 4 ZnSO 4 + H 2 III. HNO 3 + KOH KNO 3 + H 2 O IV. KClO 3 KCl + O 2 As quatro equações representam, nesta ordem,
1ª Série do Ensino Médio 16. Considere as equações abaixo: I. H 2 + Cl 2 2 HCl II. Zn + H 2 SO 4 ZnSO 4 + H 2 III. HNO 3 + KOH KNO 3 + H 2 O IV. KClO 3 KCl + O 2 As quatro equações representam, nesta ordem,
Cálculos envolvendo reações
 Cálculos envolvendo reações Cálculo Estequiométrico Misturamos reagentes que não estão em proporção estequiométrica Reagente limitante: consumido totalmente Reagente em excesso: sobra certa quantidade
Cálculos envolvendo reações Cálculo Estequiométrico Misturamos reagentes que não estão em proporção estequiométrica Reagente limitante: consumido totalmente Reagente em excesso: sobra certa quantidade
FACULDADE ISRAELITA DE CIÊNCIAS DA SAÚDE ALBERT EINSTEIN 2019
 FACULDADE ISRAELITA DE CIÊNCIAS DA SAÚDE ALBERT EINSTEIN 2019 CNHECIMENTS GERAIS E ESPECÍFICS CNHECIMENTS GERAIS 31. quadro apresenta informações sobre quatro substâncias químicas, todas brancas, em pó.
FACULDADE ISRAELITA DE CIÊNCIAS DA SAÚDE ALBERT EINSTEIN 2019 CNHECIMENTS GERAIS E ESPECÍFICS CNHECIMENTS GERAIS 31. quadro apresenta informações sobre quatro substâncias químicas, todas brancas, em pó.
Atividade complementar de Química. Transformação química das substâncias. Atenção
 Atividade complementar de Química Transformação química das substâncias Educação de Jovens e Adultos Nas transformações químicas, também conhecida como reação química, as substâncias são transformadas
Atividade complementar de Química Transformação química das substâncias Educação de Jovens e Adultos Nas transformações químicas, também conhecida como reação química, as substâncias são transformadas
3ª Série / Vestibular. As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar que, na reação:
 3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
1º EDITAL. Associação Médica Brasileira Sociedade Brasileira de Anestesiologia 2011
 1º EDITAL Edital para obtenção do Título de Especialista em Anestesiologia para os médicos que realizaram curso de especialização em Centro de Ensino e Treinamento credenciado pela Sociedade Brasileira
1º EDITAL Edital para obtenção do Título de Especialista em Anestesiologia para os médicos que realizaram curso de especialização em Centro de Ensino e Treinamento credenciado pela Sociedade Brasileira
Protocolo de Atendimento à Hipertermia Maligna
 Protocolo de Atendimento à Hipertermia Maligna Unidade de Anestesia Versão eletrônica atualizada em Março 2009 Protocolo de Atendimento a Hipertermia Maligna HIAE Definição Síndrome de origem fármaco-genética,
Protocolo de Atendimento à Hipertermia Maligna Unidade de Anestesia Versão eletrônica atualizada em Março 2009 Protocolo de Atendimento a Hipertermia Maligna HIAE Definição Síndrome de origem fármaco-genética,
Atividade complementar. Substâncias e transformações químicas, entendendo os aspectos quantitativos
 Atividade complementar Substâncias e transformações químicas, entendendo os aspectos quantitativos Esta atividade tem como objetivo complementar e aprofundar os estudos sobre as transformações químicas,
Atividade complementar Substâncias e transformações químicas, entendendo os aspectos quantitativos Esta atividade tem como objetivo complementar e aprofundar os estudos sobre as transformações químicas,
EXAME Questões Objetivas
 V Questões Objetivas EXAME 2010 RESPONDA AS QUESTÕES DE 1 a 30, MARCANDO UMA DAS ALTERNATIVAS DE ACORDO COM O QUE SE PEDE. Questão 01. ( Peso 2) O gráfico abaixo apresenta as cinco primeiras energias de
V Questões Objetivas EXAME 2010 RESPONDA AS QUESTÕES DE 1 a 30, MARCANDO UMA DAS ALTERNATIVAS DE ACORDO COM O QUE SE PEDE. Questão 01. ( Peso 2) O gráfico abaixo apresenta as cinco primeiras energias de
NOME: ANO: 2º ENSINO: MÉDIO TURMA: DATA: / / PROF(ª).: Luciano Raposo Freitas EXERCÍCIOS TERMOQUÍMICA QUÍMICA II (2º BIM)
 NOME: ANO: 2º ENSINO: MÉDIO TURMA: DATA: / / PROF(ª).: Luciano Raposo Freitas EXERCÍCIOS TERMOQUÍMICA QUÍMICA II (2º BIM) 1. Nos motores de explosão existentes hoje em dia utiliza-se uma mistura de gasolina
NOME: ANO: 2º ENSINO: MÉDIO TURMA: DATA: / / PROF(ª).: Luciano Raposo Freitas EXERCÍCIOS TERMOQUÍMICA QUÍMICA II (2º BIM) 1. Nos motores de explosão existentes hoje em dia utiliza-se uma mistura de gasolina
Resolução de Questões de Provas Específicas de Química (Aula 5)
 Resolução de Questões de Provas Específicas de Química (Aula 5) Resolução de Questões de Provas Específicas (Aula 5) 1. (UECE) A indústria eletroquímica moderna produz atualmente milhões de toneladas de
Resolução de Questões de Provas Específicas de Química (Aula 5) Resolução de Questões de Provas Específicas (Aula 5) 1. (UECE) A indústria eletroquímica moderna produz atualmente milhões de toneladas de
QUESTÃO 46 QUESTÃO 47 QUESTÃO 48 P R O V A D E Q UÍMICA I
 18 P R O V A D E Q UÍMICA I QUESTÃO 46 O número de oxidação (ox) de um elemento quantifica seu estado de oxidação. Qual é o ox de Cr no ânion Cr 2 O 7 2-? a) +3 b) +5 c) +6 d) +7 QUESTÃO 47 Considere o
18 P R O V A D E Q UÍMICA I QUESTÃO 46 O número de oxidação (ox) de um elemento quantifica seu estado de oxidação. Qual é o ox de Cr no ânion Cr 2 O 7 2-? a) +3 b) +5 c) +6 d) +7 QUESTÃO 47 Considere o
ESTEQUIOMETRIA. Estudo das reações. Descrevendo uma reação química. Indicadores de uma reação química:
 ESTEQUIOMETRIA Estudo das reações Indicadores de uma reação química: Produção de um gás Liberação ou absorção de calor Formação de um precipitado Mudança de cor 3 Descrevendo uma reação química Reagentes
ESTEQUIOMETRIA Estudo das reações Indicadores de uma reação química: Produção de um gás Liberação ou absorção de calor Formação de um precipitado Mudança de cor 3 Descrevendo uma reação química Reagentes
ESTEQUIOMETRIA. Estudo das reações. Indicadores de uma reação química:
 ESTEQUIOMETRIA Estudo das reações Indicadores de uma reação química: Produção de um gás Liberação ou absorção de calor Formação de um precipitado Mudança de cor 3 Descrevendo uma reação química Reagentes
ESTEQUIOMETRIA Estudo das reações Indicadores de uma reação química: Produção de um gás Liberação ou absorção de calor Formação de um precipitado Mudança de cor 3 Descrevendo uma reação química Reagentes
ESTEQUIOMETRIA. Estudo das reações. Descrevendo uma reação química. Indicadores de uma reação química:
 ESTEQUIOMETRIA Estudo das reações Indicadores de uma reação química: Produção de um gás Liberação ou absorção de calor Formação de um precipitado Mudança de cor 3 Descrevendo uma reação química Representação
ESTEQUIOMETRIA Estudo das reações Indicadores de uma reação química: Produção de um gás Liberação ou absorção de calor Formação de um precipitado Mudança de cor 3 Descrevendo uma reação química Representação
12 GAB. 1 1 o DIA PASES 1 a ETAPA TRIÊNIO QUÍMICA QUESTÕES DE 21 A 30
 12 GAB. 1 1 o DIA PASES 1 a ETAPA TRIÊNIO 2005-2007 QUÍMICA QUESTÕES DE 21 A 30 21. A hemoglobina das células vermelhas do sangue contém o complexo de ferro com uma porfirina. Sabendo que um indivíduo
12 GAB. 1 1 o DIA PASES 1 a ETAPA TRIÊNIO 2005-2007 QUÍMICA QUESTÕES DE 21 A 30 21. A hemoglobina das células vermelhas do sangue contém o complexo de ferro com uma porfirina. Sabendo que um indivíduo
Ficha Informativa n.º 2 Tipos de Reações Químicas
 FÍSICO-QUÍMICA 8º ANO DE ESCOLARIDADE Ficha Informativa n.º 2 Tipos de Reações Químicas Nome: Data: / /20 INTRODUÇÃO TEÓRICA Reações Químicas Nas reações químicas, uma ou várias substâncias iniciais (reagentes)
FÍSICO-QUÍMICA 8º ANO DE ESCOLARIDADE Ficha Informativa n.º 2 Tipos de Reações Químicas Nome: Data: / /20 INTRODUÇÃO TEÓRICA Reações Químicas Nas reações químicas, uma ou várias substâncias iniciais (reagentes)
CURSINHO ETWB 2012 Componente Curricular: Química Professor: Ricardo Honda
 CURSINHO ETWB 2012 Componente Curricular: Química Professor: Ricardo Honda Data: Terça-feira, 11/09/2012 Tema da aula: Deslocamento de equilíbrios químicos (Princípios de Le Chatelier) Quando um sistema
CURSINHO ETWB 2012 Componente Curricular: Química Professor: Ricardo Honda Data: Terça-feira, 11/09/2012 Tema da aula: Deslocamento de equilíbrios químicos (Princípios de Le Chatelier) Quando um sistema
P R O V A D E Q U Í M I C A I I
 20 P R V A D E Q U Í M I C A I I QUESTÃ 46 Na fabricação de pães, a glicose contida na massa se transforma em álcool etílico e gás carbônico com a ajuda da enzima zimase, de acordo com a seguinte reação,
20 P R V A D E Q U Í M I C A I I QUESTÃ 46 Na fabricação de pães, a glicose contida na massa se transforma em álcool etílico e gás carbônico com a ajuda da enzima zimase, de acordo com a seguinte reação,
REAÇÕES QUÍMICAS REAGENTES E PRODUTOS DE REAÇÃO
 REAÇÕES QUÍMICAS Os materiais podem sofrer transformações químicas ou transformações físicas. As transformações químicas são aquelas em que ocorre a formação de novas substâncias com propriedades diferentes
REAÇÕES QUÍMICAS Os materiais podem sofrer transformações químicas ou transformações físicas. As transformações químicas são aquelas em que ocorre a formação de novas substâncias com propriedades diferentes
Estudo Estudo da Química
 Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 13 INTRODUÇÃO A ESTEQUIOMETRIA
Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 13 INTRODUÇÃO A ESTEQUIOMETRIA
23/07/14 ANESTESIA INALATÓRIA. ! Evolução da Anestesia Inalatória. ! Características da Anestesia Inalatória. ! Administrados por via aérea.
 ANESTESIA INALATÓRIA Prof. Dr. Adriano Bonfim Carregaro Medicina Veterinária FZEA USP www.anestesia.vet.br http://on.fb.me/anestesiavet! Evolução da N 2 O Éter Clorofórmio Ciclopropano Tricloroetileno
ANESTESIA INALATÓRIA Prof. Dr. Adriano Bonfim Carregaro Medicina Veterinária FZEA USP www.anestesia.vet.br http://on.fb.me/anestesiavet! Evolução da N 2 O Éter Clorofórmio Ciclopropano Tricloroetileno
QUÍMICA GERAL. Substâncias e Funções Inorgânicas. Óxidos
 QUÍMICA GERAL Substâncias e Funções Inorgânicas Óxidos Índice Introdução Os óxidos são substâncias presentes no nosso dia-adia. Um bom exemplo de óxido é o gás carbônico, expelido na respiração, principal
QUÍMICA GERAL Substâncias e Funções Inorgânicas Óxidos Índice Introdução Os óxidos são substâncias presentes no nosso dia-adia. Um bom exemplo de óxido é o gás carbônico, expelido na respiração, principal
ESTEQUIOMETRIA Folha 01 João Roberto Mazzei
 01. (UFC 2009) O principal componente da cal, importante produto industrial fabricado no Ceará, é o óxido de cálcio (CaO). A produção de CaO se processa de acordo com a seguinte reação química: CaCO 3(s)
01. (UFC 2009) O principal componente da cal, importante produto industrial fabricado no Ceará, é o óxido de cálcio (CaO). A produção de CaO se processa de acordo com a seguinte reação química: CaCO 3(s)
EXERCÍCIOS DE APLICAÇÃO
 Equilíbrio Químico EXERCÍCIOS DE APLICAÇÃO 01 (PUC-RS) Dada a expressão da constante de equilíbrio em termos de concentração de produtos e reagentes a equação química que pode ser representada por essa
Equilíbrio Químico EXERCÍCIOS DE APLICAÇÃO 01 (PUC-RS) Dada a expressão da constante de equilíbrio em termos de concentração de produtos e reagentes a equação química que pode ser representada por essa
P1 - PROVA DE QUÍMICA GERAL 15/09/2012
 P1 - PROVA DE QUÍMICA GERAL 15/09/01 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 a,5 Total 10,0 Dados R = 0,081 atm L mol -1 K -1 T (K) = T ( C) + 73,15
P1 - PROVA DE QUÍMICA GERAL 15/09/01 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 a,5 Total 10,0 Dados R = 0,081 atm L mol -1 K -1 T (K) = T ( C) + 73,15
Estequiometria. Priscila Milani
 Estequiometria Priscila Milani Cálculo de massa para amostras impuras: Reagentes impuros, principalmente em reações industriais, ou porque eles são mais baratos ou porque eles já são encontrados na Natureza
Estequiometria Priscila Milani Cálculo de massa para amostras impuras: Reagentes impuros, principalmente em reações industriais, ou porque eles são mais baratos ou porque eles já são encontrados na Natureza
INSTITUTO GEREMARIO DANTAS COMPONENTE CURRICULAR: QUÍMICA EXERCÍCIOS EXTRAS 2º TRIMESTRE 2016
 INSTITUTO GEREMARIO DANTAS Educação Infantil, Ensino Fundamental e Médio Fone: (21) 21087900 Rio de Janeiro RJ www.igd.com.br Aluno(a): 1º Ano: C11 Nº Professor: Lúcia Nascimento COMPONENTE CURRICULAR:
INSTITUTO GEREMARIO DANTAS Educação Infantil, Ensino Fundamental e Médio Fone: (21) 21087900 Rio de Janeiro RJ www.igd.com.br Aluno(a): 1º Ano: C11 Nº Professor: Lúcia Nascimento COMPONENTE CURRICULAR:
EXERCÍCIOS DE REVISÃO P/ Avaliação 01/06
 Tema do Ano: Eu e o outro construindo um mundo mais solidário Projeto Interdisciplinar da 2 a Série do Ensino Médio: Segunda metade do século XX e início do século XXI: movimentos, conflitos e desenvolvimento.
Tema do Ano: Eu e o outro construindo um mundo mais solidário Projeto Interdisciplinar da 2 a Série do Ensino Médio: Segunda metade do século XX e início do século XXI: movimentos, conflitos e desenvolvimento.
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 09 TURMA FMJ
 RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 09 TURMA FMJ 01. Item A III Incorreto. A torrefação não consiste em um processo de separação de misturas. IV Incorreto. A trituração não consiste em processo químico
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 09 TURMA FMJ 01. Item A III Incorreto. A torrefação não consiste em um processo de separação de misturas. IV Incorreto. A trituração não consiste em processo químico
Funções Inorgânicas - Ácidos e Sais
 Funções Inorgânicas - Ácidos e Sais Material de Apoio para Monitoria 1. (ITA) A respeito das espécies químicas HNO3, HCN, CH3COOH, HCO3 -, HClO4, HPO4 2-, cada uma em solução aquosa e à temperatura ambiente,
Funções Inorgânicas - Ácidos e Sais Material de Apoio para Monitoria 1. (ITA) A respeito das espécies químicas HNO3, HCN, CH3COOH, HCO3 -, HClO4, HPO4 2-, cada uma em solução aquosa e à temperatura ambiente,
QUÍMICA - 2 o ANO MÓDULO 06 SOLUÇÕES: MISTURAS - PARTE 2
 QUÍMICA - 2 o ANO MÓDULO 06 SOLUÇÕES: MISTURAS - PARTE 2 Fixação 1) 60 ml de uma solução 0,75 mol/l de NaOH neutralizam 30 ml de uma solução de ácido sulfúrico. A molaridade do ácido é: m a) 0,65 d) 0,75
QUÍMICA - 2 o ANO MÓDULO 06 SOLUÇÕES: MISTURAS - PARTE 2 Fixação 1) 60 ml de uma solução 0,75 mol/l de NaOH neutralizam 30 ml de uma solução de ácido sulfúrico. A molaridade do ácido é: m a) 0,65 d) 0,75
Em meio aquoso sofrem dissociação liberando íons na água, o que torna o meio condutor de corrente elétrica.
 Aula 7 Funções Inorgânicas (sais e óxidos) Sal Os sais são compostos que possuem um cátion qualquer (só não pode ser exclusivamente o H +, senão será um ácido) e um ânion qualquer(só não pode ser exclusivamente
Aula 7 Funções Inorgânicas (sais e óxidos) Sal Os sais são compostos que possuem um cátion qualquer (só não pode ser exclusivamente o H +, senão será um ácido) e um ânion qualquer(só não pode ser exclusivamente
PROTOCOLOS HAOC Capítulo JCI Responsável pela elaboração Nº Doc. Data da 1ª Versão
 e Cirurgia - ASC Introdução: A estratégia de abordagem à via aérea deve iniciar-se por uma completa anamnese baseada na história, exame físico e condição geral do paciente. Este protocolo médico assistencial
e Cirurgia - ASC Introdução: A estratégia de abordagem à via aérea deve iniciar-se por uma completa anamnese baseada na história, exame físico e condição geral do paciente. Este protocolo médico assistencial
Disciplina: Química Data: 05 / 05 / Ensino Médio Série: 2º ano Turma: Valor: Média: Assunto: ROTEIRO DE RECUPERAÇÃO Etapa: I Tipo:
 Disciplina: Química Data: 05 / 05 / 2018 Ensino Médio Série: 2º ano Turma: Valor: Média: Assunto: ROTEIRO DE RECUPERAÇÃO Etapa: I Tipo: Aluno(a): Nº: Nota: Professor(a): Thito Ass. do(a) Responsável: PROGRAMA
Disciplina: Química Data: 05 / 05 / 2018 Ensino Médio Série: 2º ano Turma: Valor: Média: Assunto: ROTEIRO DE RECUPERAÇÃO Etapa: I Tipo: Aluno(a): Nº: Nota: Professor(a): Thito Ass. do(a) Responsável: PROGRAMA
Material 4: Estequiometria EQUAÇÕES QUÍMICAS REAGENTES PRODUTOS. Sódio + Água hidróxido de sódio + Hidrogênio
 EQUAÇÕES QUÍMICAS REAÇÃO QUÍMICA: É o processo de uma mudança química (Átkins). Este processo é representado por meio de uma EQUAÇÃO QUÌMICA. As EQUAÇÕES QUÍMICAS são representadas por: REAGENTES PRODUTOS
EQUAÇÕES QUÍMICAS REAÇÃO QUÍMICA: É o processo de uma mudança química (Átkins). Este processo é representado por meio de uma EQUAÇÃO QUÌMICA. As EQUAÇÕES QUÍMICAS são representadas por: REAGENTES PRODUTOS
1 a QUESTÃO: (2,0 pontos) Avaliador Revisor
 1 a QUESTÃO: (2,0 pontos) Avaliador Revisor Considere a reação exotérmica de formação do trióxido de enxofre, a partir do dióxido: 2SO 2(g) + O 2(g) 2SO 3(g) A 900 K, K p = 40,5 atm -1 e ΔH = -198 kj.
1 a QUESTÃO: (2,0 pontos) Avaliador Revisor Considere a reação exotérmica de formação do trióxido de enxofre, a partir do dióxido: 2SO 2(g) + O 2(g) 2SO 3(g) A 900 K, K p = 40,5 atm -1 e ΔH = -198 kj.
MCC I Cal na Construção Civil
 MCC I - AGLOMERANTES MCC I Aglomerantes Aglomerante Aéreo Cal na Construção Civil Definição: A cal é um aglomerante inorgânico, produzido a partir de rochas calcárias, composto basicamente de cálcio e
MCC I - AGLOMERANTES MCC I Aglomerantes Aglomerante Aéreo Cal na Construção Civil Definição: A cal é um aglomerante inorgânico, produzido a partir de rochas calcárias, composto basicamente de cálcio e
GABARITO - QUÍMICA - Grupo A
 GABARITO - QUÍMICA - Grupo A 1 a QUESTÃO: (2,0 pontos) Avaliador Revisor O teor do íon Cl - existente nos fluidos corporais pode ser determinado através de uma analise volumétrica do íon Cl - com o íon
GABARITO - QUÍMICA - Grupo A 1 a QUESTÃO: (2,0 pontos) Avaliador Revisor O teor do íon Cl - existente nos fluidos corporais pode ser determinado através de uma analise volumétrica do íon Cl - com o íon
Exercícios de Equilíbrio Iônico II
 Exercícios de Equilíbrio Iônico II 1. Com relação às funções inorgânicas, assinale a alternativa incorreta. a) O acetato de sódio é um sal de características básicas, pois é resultante da reação entre
Exercícios de Equilíbrio Iônico II 1. Com relação às funções inorgânicas, assinale a alternativa incorreta. a) O acetato de sódio é um sal de características básicas, pois é resultante da reação entre
Lista de exercícios de 4 a U.L
 Lista de exercícios de 4 a U.L 01-Dada a tabela a seguir, e levando-se em consideração que as substâncias se encontram à temperatura de 50 o C, responda o que se pede: SUBSTANCIA T.F ( o C) T.E ( o C)
Lista de exercícios de 4 a U.L 01-Dada a tabela a seguir, e levando-se em consideração que as substâncias se encontram à temperatura de 50 o C, responda o que se pede: SUBSTANCIA T.F ( o C) T.E ( o C)
21. Considere a seguinte expressão de constante de equilíbrio em termos de pressões parciais: K p =
 PASES 2 a ETAPA TRIÊNIO 2003-2005 1 O DIA GABARITO 1 13 QUÍMICA QUESTÕES DE 21 A 30 21. Considere a seguinte expressão de constante de equilíbrio em termos de pressões parciais: K p = 1 p CO2 Dentre as
PASES 2 a ETAPA TRIÊNIO 2003-2005 1 O DIA GABARITO 1 13 QUÍMICA QUESTÕES DE 21 A 30 21. Considere a seguinte expressão de constante de equilíbrio em termos de pressões parciais: K p = 1 p CO2 Dentre as
PROCESSO SELETIVO SIMPLIFICADO/2014
 UFF UNIVERSIDADE FEDERAL FLUMINENSE HUAP HOSPITAL UNIVERSITÁRIO ANTONIO PEDRO PROCESSO SELETIVO SIMPLIFICADO/2014 Edital n o 044/2014 Especialidade: TÉCNICO EM EQUIPAMENTO MÉDICO / ODONTOLÓGICO - ANESTESIA
UFF UNIVERSIDADE FEDERAL FLUMINENSE HUAP HOSPITAL UNIVERSITÁRIO ANTONIO PEDRO PROCESSO SELETIVO SIMPLIFICADO/2014 Edital n o 044/2014 Especialidade: TÉCNICO EM EQUIPAMENTO MÉDICO / ODONTOLÓGICO - ANESTESIA
QUESTÕES COMENTADAS Anatomia e Fisiologia Respiratória PORTAL ANESTESIA CURSO ANESTESIO R1
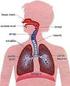 QUESTÕES COMENTADAS Anatomia e Fisiologia Respiratória PORTAL ANESTESIA CURSO ANESTESIO R1 Questões 1. Na espirometria: A) a capacidade vital normal do adulto hígido é de 60 ml.kg -1 (+/- 20%) B) a capacidade
QUESTÕES COMENTADAS Anatomia e Fisiologia Respiratória PORTAL ANESTESIA CURSO ANESTESIO R1 Questões 1. Na espirometria: A) a capacidade vital normal do adulto hígido é de 60 ml.kg -1 (+/- 20%) B) a capacidade
Risco Químico em Serviços de Saúde e a adequação a NR 32
 Risco Químico em Serviços de Saúde e a adequação a NR 32 Dr Denilson de Oliveira Reis HGIS- OSS denilson.reis@hgis.org.br Dos Riscos Químicos Não é possível estabelecer uma regra geral que garanta a segurança
Risco Químico em Serviços de Saúde e a adequação a NR 32 Dr Denilson de Oliveira Reis HGIS- OSS denilson.reis@hgis.org.br Dos Riscos Químicos Não é possível estabelecer uma regra geral que garanta a segurança
Observe o gráfico, cujas curvas representam as variações das massas desses radioisótopos ao longo das duas horas de duração do experimento.
 Revisão Específicas 1. (UERJ 2015) Os preços dos metais para reciclagem variam em função da resistência de cada um à corrosão: quanto menor a tendência do metal à oxidação, maior será o preço. Na tabela,
Revisão Específicas 1. (UERJ 2015) Os preços dos metais para reciclagem variam em função da resistência de cada um à corrosão: quanto menor a tendência do metal à oxidação, maior será o preço. Na tabela,
2.3.1Mineralização das águas e processos de dissolução
 2.3.1Mineralização das águas e processos de dissolução As águas naturais são na verdade soluções aquosas, não contêm apenas água, mas também substâncias dissolvidas. A facilidade de dissolução das substâncias
2.3.1Mineralização das águas e processos de dissolução As águas naturais são na verdade soluções aquosas, não contêm apenas água, mas também substâncias dissolvidas. A facilidade de dissolução das substâncias
ATENÇÃO: assinale ou apresente cuidadosamente as respostas e apresente TODOS os cálculos efectuados.
 Prova de Acesso de Química Maiores de 23 Anos Candidatura 2016-2017 14 de Junho de 2017 10h00 12h30 Nome CCnº ATENÇÃO: assinale ou apresente cuidadosamente as respostas e apresente TODOS os cálculos efectuados.
Prova de Acesso de Química Maiores de 23 Anos Candidatura 2016-2017 14 de Junho de 2017 10h00 12h30 Nome CCnº ATENÇÃO: assinale ou apresente cuidadosamente as respostas e apresente TODOS os cálculos efectuados.
Análise gasométrica volumétrica ou eudiométrica dos gases
 Análise gasométrica volumétrica ou eudiométrica dos gases A análise volumétrica gasométrica também é conhecida como análise eudiométrica, devido ao aparelho utilizado neste processo que é chamado de eudiômetro.
Análise gasométrica volumétrica ou eudiométrica dos gases A análise volumétrica gasométrica também é conhecida como análise eudiométrica, devido ao aparelho utilizado neste processo que é chamado de eudiômetro.
INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA LEIA COM MUITA ATENÇÃO
 1º EM Química B Natália Av. Dissertativa 19/10/16 INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA LEIA COM MUITA ATENÇÃO 1. Verifique, no cabeçalho desta prova, se seu nome, número e turma estão corretos. 2. Esta
1º EM Química B Natália Av. Dissertativa 19/10/16 INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA LEIA COM MUITA ATENÇÃO 1. Verifique, no cabeçalho desta prova, se seu nome, número e turma estão corretos. 2. Esta
QUESTÃO 46 QUESTÃO 47 QUESTÃO 48 QUESTÃO 49 PROVA DE QUÍMICA I
 17 PROVA DE QUÍMICA I QUESTÃO 46 O alumínio metálico, obtido na indústria à alta temperatura na forma líquida, reage com vapor d`água da atmosfera, produzindo óxido de alumínio e gás hidrogênio, conforme
17 PROVA DE QUÍMICA I QUESTÃO 46 O alumínio metálico, obtido na indústria à alta temperatura na forma líquida, reage com vapor d`água da atmosfera, produzindo óxido de alumínio e gás hidrogênio, conforme
Equilíbrio Químico. Controlo da Produção Industrial de Amoníaco
 Equilíbrio Químico Controlo da Produção Industrial de Amoníaco Reações completas Combustão do carvão C (s) + O 2 (g) CO 2 (g) Reações completas Reação do Ácido clorídrico com o Magnésio 2 HCl (aq) + Mg
Equilíbrio Químico Controlo da Produção Industrial de Amoníaco Reações completas Combustão do carvão C (s) + O 2 (g) CO 2 (g) Reações completas Reação do Ácido clorídrico com o Magnésio 2 HCl (aq) + Mg
Funções Químicas: Ácidos, bases, sais e óxidos
 Funções Químicas: Ácidos, bases, sais e óxidos Funções Químicas Grupo de substâncias compostas que possuem propriedades químicas semelhantes; As funções químicas são divididas de acordo com a divisão clássica
Funções Químicas: Ácidos, bases, sais e óxidos Funções Químicas Grupo de substâncias compostas que possuem propriedades químicas semelhantes; As funções químicas são divididas de acordo com a divisão clássica
... 2) Escreva a fórmula e os nomes dos sete ácidos padrões.
 Lista de Exercícios Ácidos Bases e sais 1) Nas colunas abaixo, associe as fórmulas aos seus nomes: I. H 2 S(aq) ( ) ácido bromídrico II. HCl (aq) ( ) ácido fluorídrico III. HCN(aq) ( ) ácido iodídrico
Lista de Exercícios Ácidos Bases e sais 1) Nas colunas abaixo, associe as fórmulas aos seus nomes: I. H 2 S(aq) ( ) ácido bromídrico II. HCl (aq) ( ) ácido fluorídrico III. HCN(aq) ( ) ácido iodídrico
QUÍMICA - 1 o ANO MÓDULO 17 REAÇÕES QUÍMICAS DE SÍNTESE E ANÁLISE
 QUÍMICA - 1 o ANO MÓDULO 17 REAÇÕES QUÍMICAS DE SÍNTESE E ANÁLISE Como pode cair no enem (ENEM) Os oceanos absorvem aproximadamente um terço das emissões de CO 2 procedentes de atividades humanas, como
QUÍMICA - 1 o ANO MÓDULO 17 REAÇÕES QUÍMICAS DE SÍNTESE E ANÁLISE Como pode cair no enem (ENEM) Os oceanos absorvem aproximadamente um terço das emissões de CO 2 procedentes de atividades humanas, como
Lista de exercícios Equilíbrios
 1. (Pucrj 008) Para a síntese do metanol, foram utilizadas as seguintes concentrações das espécies em quantidade de matéria: [CO] = 1,75 mol L -1, [H ] = 0,80 mol L -1 e [CH 3 OH] = 0,65 mol L -1 Ao se
1. (Pucrj 008) Para a síntese do metanol, foram utilizadas as seguintes concentrações das espécies em quantidade de matéria: [CO] = 1,75 mol L -1, [H ] = 0,80 mol L -1 e [CH 3 OH] = 0,65 mol L -1 Ao se
Alterações do equilíbrio hídrico Alterações do equilíbrio hídrico Desidratação Regulação do volume hídrico
 Regulação do volume hídrico Alteração do equilíbrio hídrico em que a perda de líquidos do organismo é maior que o líquido ingerido Diminuição do volume sanguíneo Alterações do equilíbrio Hídrico 1. Consumo
Regulação do volume hídrico Alteração do equilíbrio hídrico em que a perda de líquidos do organismo é maior que o líquido ingerido Diminuição do volume sanguíneo Alterações do equilíbrio Hídrico 1. Consumo
CORPO DE BOMBEIRO MILITAR DO DISTRITO FEDERAL DIRETORIA DE ENSINO E INSTRUÇÃO CENTRO DE ASSISTÊNCIA AO ENSINO/CMDPII COORDENAÇÃO DE CFB
 CORPO DE BOMBEIRO MILITAR DO DISTRITO FEDERAL DIRETORIA DE ENSINO E INSTRUÇÃO CENTRO DE ASSISTÊNCIA AO ENSINO/CMDPII COORDENAÇÃO DE CFB Professor(a): Manoel Everton Aluno (a) : 1º ano Turma: Lista de Exercício
CORPO DE BOMBEIRO MILITAR DO DISTRITO FEDERAL DIRETORIA DE ENSINO E INSTRUÇÃO CENTRO DE ASSISTÊNCIA AO ENSINO/CMDPII COORDENAÇÃO DE CFB Professor(a): Manoel Everton Aluno (a) : 1º ano Turma: Lista de Exercício
Agentes Químicos em Ambiente Hospitalar. Ana Cruz Nogueira Unidade de Ar e Saúde Ocupacional Departamento de Saúde Ambiental
 Agentes Químicos em Ambiente Hospitalar Exposição Profissional a Sevoflurano Ana Cruz Nogueira Unidade de Ar e Saúde Ocupacional Departamento de Saúde Ambiental Agentes Químicos em Ambiente Hospitalar
Agentes Químicos em Ambiente Hospitalar Exposição Profissional a Sevoflurano Ana Cruz Nogueira Unidade de Ar e Saúde Ocupacional Departamento de Saúde Ambiental Agentes Químicos em Ambiente Hospitalar
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. ALUNO(a): Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
 GOIÂNIA, / / 2015 PROFESSORA: Núbia de Andrade DISCIPLINA:QUÌMICA SÉRIE: 3º ALUNO(a): Entrega dia 16/09/2016 No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes
GOIÂNIA, / / 2015 PROFESSORA: Núbia de Andrade DISCIPLINA:QUÌMICA SÉRIE: 3º ALUNO(a): Entrega dia 16/09/2016 No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes
UNIVERSIDADE DE ÉVORA
 UNIVERSIDADE DE ÉVORA ACESSO AO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA ESCRITA DE QUÍMICA 09 de maio de 2017 Duração: 2 horas DADOS NECESSÁRIOS À RESOLUÇÃO DA PROVA V m (PTN) = 22,4 L/mol Grupo I
UNIVERSIDADE DE ÉVORA ACESSO AO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA ESCRITA DE QUÍMICA 09 de maio de 2017 Duração: 2 horas DADOS NECESSÁRIOS À RESOLUÇÃO DA PROVA V m (PTN) = 22,4 L/mol Grupo I
FUVEST 1985 Primeira fase e Segunda fase
 FUVEST 1985 Primeira fase e Segunda fase CONHECIMENTOS GERAIS 85. Qual o método de separação utilizado quanto se usa um coador de pano na preparação do café? a) destilação b) filtração c) decantação d)
FUVEST 1985 Primeira fase e Segunda fase CONHECIMENTOS GERAIS 85. Qual o método de separação utilizado quanto se usa um coador de pano na preparação do café? a) destilação b) filtração c) decantação d)
 Lista de exercícios - Bloco 2 - Aula 25 a 28 - Equilíbrio Químico - Conceitos gerais e cálculo (Kc e Kp) 1. (Unicid - Medicina 2017) Considere os equilíbrios: 1. 2 SO 2 (g) + O 2 (g) 2 SO 3 (g) 25 Kc =
Lista de exercícios - Bloco 2 - Aula 25 a 28 - Equilíbrio Químico - Conceitos gerais e cálculo (Kc e Kp) 1. (Unicid - Medicina 2017) Considere os equilíbrios: 1. 2 SO 2 (g) + O 2 (g) 2 SO 3 (g) 25 Kc =
UNISA MEDICINA 2018 UNIVERSIDADE DE SANTO AMARO
 UNISA MEDIINA 018 UNIVERSIDADE DE SANT AMAR 01. A figura mostra a decomposição térmica do carbonato de cobre (II), produzindo óxido de cobre (II) e dióxido de carbono, conforme a equação: u (s) u(s) +
UNISA MEDIINA 018 UNIVERSIDADE DE SANT AMAR 01. A figura mostra a decomposição térmica do carbonato de cobre (II), produzindo óxido de cobre (II) e dióxido de carbono, conforme a equação: u (s) u(s) +
02)Numa reação endotérmica, há [1] de calor, a entalpia final (produtos) é [2] que a entalpia inicial (reagentes) e a
![02)Numa reação endotérmica, há [1] de calor, a entalpia final (produtos) é [2] que a entalpia inicial (reagentes) e a 02)Numa reação endotérmica, há [1] de calor, a entalpia final (produtos) é [2] que a entalpia inicial (reagentes) e a](/thumbs/48/23999624.jpg) 01)Numa reação exotérmica, há [1] de calor, a entalpia final (produtos) é [2] que a entalpia inicial (reagentes) e a variação de entalpia é [3] que zero. Completa-se corretamente essa frase substituindo-se
01)Numa reação exotérmica, há [1] de calor, a entalpia final (produtos) é [2] que a entalpia inicial (reagentes) e a variação de entalpia é [3] que zero. Completa-se corretamente essa frase substituindo-se
2º trimestre Química Data: 08/2018 Ensino Médio 1º ano classe: Prof. Valéria
 2º trimestre Química Data: 08/2018 Ensino Médio 1º ano classe: Prof. Valéria A Patrícia, que é uma excelente aluna, esteve a determinar o ph de oito soluções, durante o decorrer de uma aula experimental.
2º trimestre Química Data: 08/2018 Ensino Médio 1º ano classe: Prof. Valéria A Patrícia, que é uma excelente aluna, esteve a determinar o ph de oito soluções, durante o decorrer de uma aula experimental.
Docente: Prof a. Dr a. Luciana M. Saran
 FCAV/ UNESP Jaboticabal Disciplina: Química Geral Assunto: Solução Tampão Docente: Prof a. Dr a. Luciana M. Saran 1 1. INTRODUÇÃO Por que a adição de 0,01 mol de HCl à 1L de sangue humano, altera o ph
FCAV/ UNESP Jaboticabal Disciplina: Química Geral Assunto: Solução Tampão Docente: Prof a. Dr a. Luciana M. Saran 1 1. INTRODUÇÃO Por que a adição de 0,01 mol de HCl à 1L de sangue humano, altera o ph
UFU 2008/2-1ª FASE. 1-A substância, representada pela fórmula estrutural abaixo, é bastante utilizada como analgésico (aspirina).
 UFU 2008/2-1ª FASE 1-A substância, representada pela fórmula estrutural abaixo, é bastante utilizada como analgésico (aspirina). Com base nessas informações, marque a alternativa correta. A) Uma massa
UFU 2008/2-1ª FASE 1-A substância, representada pela fórmula estrutural abaixo, é bastante utilizada como analgésico (aspirina). Com base nessas informações, marque a alternativa correta. A) Uma massa
1º BIMESTRE. Série Turma (s) Turno 3º A B C D E F G H MATUTINO Disciplina: QUÍMICA Professor: CHARLYS FERNANDES Data: / / 2017 Aluno (a): Nº
 1º BIMESTRE Visto do Professor Nota (Fuvest) A uma determinada temperatura, as substâncias HI, H2 e I2 estão no estado gasoso. A essa temperatura, o equilíbrio entre as três substâncias foi estudado, em
1º BIMESTRE Visto do Professor Nota (Fuvest) A uma determinada temperatura, as substâncias HI, H2 e I2 estão no estado gasoso. A essa temperatura, o equilíbrio entre as três substâncias foi estudado, em
FISPQ - FICHA DE INFORMAÇÃO DE SEGURANÇA DE PRODUTOS QUÍMICOS
 1. IDENTIFICAÇÃO DO PRODUTO E DA EMPRESA Nome do produto: TEKBOND Categoria: Nome da empresa: ATB Ind. e Com. de Adesivos S/A Endereço: Rua Marcelino Pinto Teixeira, 1268 Parque Industrial Ramos de Oliveira
1. IDENTIFICAÇÃO DO PRODUTO E DA EMPRESA Nome do produto: TEKBOND Categoria: Nome da empresa: ATB Ind. e Com. de Adesivos S/A Endereço: Rua Marcelino Pinto Teixeira, 1268 Parque Industrial Ramos de Oliveira
QUÍMICA - 1 o ANO MÓDULO 30 ESTEQUIOMETRIA: REAÇÕES CONSECUTIVAS
 QUÍMICA - 1 o ANO MÓDULO 30 ESTEQUIOMETRIA: REAÇÕES CONSECUTIVAS Como pode cair no enem Um dos efeitos da chamada chuva ácida causada pelo SO 2(g) lançado na atmosfera, é a transformação do mármore, CaCO
QUÍMICA - 1 o ANO MÓDULO 30 ESTEQUIOMETRIA: REAÇÕES CONSECUTIVAS Como pode cair no enem Um dos efeitos da chamada chuva ácida causada pelo SO 2(g) lançado na atmosfera, é a transformação do mármore, CaCO
FICHA DE INFORMAÇÃO DE SEGURANÇA DE PRODUTO QUÍMICO FISPQ Produto: Solução descorante para Gram Revisão: 02 Página: 1/5
 Revisão: 02 Página: 1/5 1- Identificação do Produto e da Empresa Produto: Descorante Gram Uso da substância/preparação: Dispositivo médico para diagnóstico in vitro Reagente para análise Empresa Fabricante
Revisão: 02 Página: 1/5 1- Identificação do Produto e da Empresa Produto: Descorante Gram Uso da substância/preparação: Dispositivo médico para diagnóstico in vitro Reagente para análise Empresa Fabricante
3) Dadas as equações: I CuCl 2 + H 2 SO 4
 1) Observe as reações I e II abaixo: I NH 3 + HCl NH 4 Cl II 2HgO aquecimento 2Hg + O 2 Podemos afirmar que I e II são, respectivamente, reações de: a) síntese e análise b) simples troca e síntese c) dupla
1) Observe as reações I e II abaixo: I NH 3 + HCl NH 4 Cl II 2HgO aquecimento 2Hg + O 2 Podemos afirmar que I e II são, respectivamente, reações de: a) síntese e análise b) simples troca e síntese c) dupla
8ª LISTA - EXERCÍCIOS DE PROVAS Equilíbrio de Solubilidade
 Pg. 1/6 1 a Questão De acordo com as equações abaixo, a 25 ºC, faça o que se pede. BaF 2 (s) Ba 2+ (aq) + 2F - (aq) K ps (BaF 2 ) = 1,7 x 10-6 BaSO 4 (s) Ba 2+ (aq) + SO 2-4 (aq) K ps (BaSO 4 ) = 1,0 x
Pg. 1/6 1 a Questão De acordo com as equações abaixo, a 25 ºC, faça o que se pede. BaF 2 (s) Ba 2+ (aq) + 2F - (aq) K ps (BaF 2 ) = 1,7 x 10-6 BaSO 4 (s) Ba 2+ (aq) + SO 2-4 (aq) K ps (BaSO 4 ) = 1,0 x
Parâmetros de qualidade de água SANEAMENTO AMBIENTAL EXPERIMENTAL TH 758
 Parâmetros de qualidade de água SANEAMENTO AMBIENTAL EXPERIMENTAL TH 758 Prof. J. Sánez Prof. Dra. H. Knapik Resp. Tec. Lab. L. Prado Universidade Federal do Paraná 3 /2015 Aula 03 Teoria e determinação
Parâmetros de qualidade de água SANEAMENTO AMBIENTAL EXPERIMENTAL TH 758 Prof. J. Sánez Prof. Dra. H. Knapik Resp. Tec. Lab. L. Prado Universidade Federal do Paraná 3 /2015 Aula 03 Teoria e determinação
PROVA DE QUÍMICA. Adaptada da Tabela Periódica da IUPAC/versão 2007 Acesso: PROVA DE QUÍMICA - Caderno 1
 PROVA DE QUÍMICA Adaptada da Tabela Periódica da IUPAC/versão 2007 Acesso: http://wwwiupacorg/reports/periodic_table/ 18 PROVA DE QUÍMICA - Caderno 1 QUESTÃO 25 1 Na extração do ouro, os garimpeiros costumam
PROVA DE QUÍMICA Adaptada da Tabela Periódica da IUPAC/versão 2007 Acesso: http://wwwiupacorg/reports/periodic_table/ 18 PROVA DE QUÍMICA - Caderno 1 QUESTÃO 25 1 Na extração do ouro, os garimpeiros costumam
Introdução à Anestesia Inalatória
 Introdução à Anestesia Inalatória Vantagens (em relação à anestesia injetável) maior controle do plano anestésico biotransformação e eliminação rápida recuperação rápida administração de O2 maior segurança
Introdução à Anestesia Inalatória Vantagens (em relação à anestesia injetável) maior controle do plano anestésico biotransformação e eliminação rápida recuperação rápida administração de O2 maior segurança
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO MÉDIO - FASE 2
 III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com
FUVEST 1991 Primeira fase e Segunda fase
 FUVEST 1991 Primeira fase e Segunda fase CNHECIMENTS GERAIS 01. ar gás carbônico naftaleno iodo latão ouro 18 quilates Se esses materiais forem classificados em substâncias puras e misturas, pertencerão
FUVEST 1991 Primeira fase e Segunda fase CNHECIMENTS GERAIS 01. ar gás carbônico naftaleno iodo latão ouro 18 quilates Se esses materiais forem classificados em substâncias puras e misturas, pertencerão
a) Disponha todos os elementos do Grupo 1 em ordem decrescente de reatividade e explique a sequência.
 QUÍMICA 1 O desenvolvimento da Tabela Periódica culminou na disposição sistemática dos elementos em grupos de acordo com características químicas similares entre si. Os elementos metálicos pertencentes
QUÍMICA 1 O desenvolvimento da Tabela Periódica culminou na disposição sistemática dos elementos em grupos de acordo com características químicas similares entre si. Os elementos metálicos pertencentes
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2012 Disciplina: Química Ano: 2012 Professor (a): Elisa Landim Turma: 2º FG/ADM Caro aluno, você está recebendo o conteúdo de
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2012 Disciplina: Química Ano: 2012 Professor (a): Elisa Landim Turma: 2º FG/ADM Caro aluno, você está recebendo o conteúdo de
QUÍMICA. Geral Funções Inorgânicas (IV)
 QUÍMICA Geral Funções Inorgânicas (IV) Óxidos Óxido é todo composto binário oxigenado, no qual o oxigênio é o elemento mais eletronegativo. F ; O ; N ; Cl ; Br ; I ; S ; C ;... eletronegatividade decrescente
QUÍMICA Geral Funções Inorgânicas (IV) Óxidos Óxido é todo composto binário oxigenado, no qual o oxigênio é o elemento mais eletronegativo. F ; O ; N ; Cl ; Br ; I ; S ; C ;... eletronegatividade decrescente
O aluno deverá elaborar resumos teóricos dos textos do livro e de outras fontes sobre os tópicos do conteúdo.
 Disciplina QUÍMICA Curso ENSINO MÉDIO Professor GUILHERME Série 1ª SÉRIE ROTEIRO DE ESTUDOS DE RECUPERAÇÃO E REVISÃO 1º SEMESTRE / 2012 Aluno (a): Número: 1 - Conteúdo: Ácidos e bases propriedades, conceito
Disciplina QUÍMICA Curso ENSINO MÉDIO Professor GUILHERME Série 1ª SÉRIE ROTEIRO DE ESTUDOS DE RECUPERAÇÃO E REVISÃO 1º SEMESTRE / 2012 Aluno (a): Número: 1 - Conteúdo: Ácidos e bases propriedades, conceito
QUÍMICA. Transformações Químicas e Energia. Termoquímica: Energia Calorífica, Calor de reação, Entalpia, Equações e Lei de Hess - Parte 5
 QUÍMICA Transformações Químicas e Energia Termoquímica: Energia Calorífica, Calor de reação, Entalpia, Equações e Lei de Hess - Parte 5 Prof ª. Giselle Blois Casos particulares das entalpias das reações
QUÍMICA Transformações Químicas e Energia Termoquímica: Energia Calorífica, Calor de reação, Entalpia, Equações e Lei de Hess - Parte 5 Prof ª. Giselle Blois Casos particulares das entalpias das reações
Professora Sonia Exercícios sobre Entropia - Termoquímica
 Exercícios sobre Entropia - Termoquímica 01. (Ufrn) Num teste químico simples, pode-se identificar a presença de uréia nos fertilizantes. A uréia sólida reage a quente com o hidróxido de sódio, liberando
Exercícios sobre Entropia - Termoquímica 01. (Ufrn) Num teste químico simples, pode-se identificar a presença de uréia nos fertilizantes. A uréia sólida reage a quente com o hidróxido de sódio, liberando
1ª Série Ensino Médio. 16. O sistema a seguir mostra a ocorrência de reação química entre um ácido e um metal, com liberação do gás X:
 1ª Série Ensino Médio 16. O sistema a seguir mostra a ocorrência de reação química entre um ácido e um metal, com liberação do gás X: O gás X, liberado neste sistema, é o: (A) O 2 ; (B) Cl 2 ; (C) O 3
1ª Série Ensino Médio 16. O sistema a seguir mostra a ocorrência de reação química entre um ácido e um metal, com liberação do gás X: O gás X, liberado neste sistema, é o: (A) O 2 ; (B) Cl 2 ; (C) O 3
3ª Série / Vestibular _ TD 08 _ 19 de abril
 3ª Série / Vestibular _ TD 08 _ 19 de abril 01. A corrosão de um metal é a sua destruição ou deterioração, devida à reação com o meio ambiente. O enferrujamento é o nome dado à corrosão do ferro: Fe(s)
3ª Série / Vestibular _ TD 08 _ 19 de abril 01. A corrosão de um metal é a sua destruição ou deterioração, devida à reação com o meio ambiente. O enferrujamento é o nome dado à corrosão do ferro: Fe(s)
1-Suponha que um agricultor esteja interessado em fazer uma plantação de girassóis. Procurando informação, leu a seguinte reportagem: Solo ácido não
 1999 1-Suponha que um agricultor esteja interessado em fazer uma plantação de girassóis. Procurando informação, leu a seguinte reportagem: Solo ácido não favorece plantio. Alguns cuidados devem ser tomados
1999 1-Suponha que um agricultor esteja interessado em fazer uma plantação de girassóis. Procurando informação, leu a seguinte reportagem: Solo ácido não favorece plantio. Alguns cuidados devem ser tomados
A partir das informações do texto, assinale a afirmativa INCORRETA.
 23 22 Q U E S T Ã O 3 4 Leia com atenção o texto abaixo. A poluição afeta a saúde de prédios em São Paulo. Fuligem, fumaça e corrosivos dispersos no ar sujam fachadas e desvalorizam imóveis, dizem especialistas.
23 22 Q U E S T Ã O 3 4 Leia com atenção o texto abaixo. A poluição afeta a saúde de prédios em São Paulo. Fuligem, fumaça e corrosivos dispersos no ar sujam fachadas e desvalorizam imóveis, dizem especialistas.
QUÍMICA. Processo Seletivo/UNIFAL - julho ª Prova Comum TIPO 1 QUESTÃO 41 QUESTÃO 42
 QUÍMICA QUESTÃO 41 A substância, representada pela fórmula estrutural abaixo, é bastante utilizada como analgésico (aspirina). Com base nessas informações, marque a alternativa correta. A) Uma massa de
QUÍMICA QUESTÃO 41 A substância, representada pela fórmula estrutural abaixo, é bastante utilizada como analgésico (aspirina). Com base nessas informações, marque a alternativa correta. A) Uma massa de
