benefícios oriundos de uma melhor compreensão do desenvolvimento folicular para a melhoria da eficiência reprodutiva dos caprinos também são
|
|
|
- Herman Madeira Vidal
- 7 Há anos
- Visualizações:
Transcrição
1 1. INTRODUÇÃO Os caprinos são considerados animais economicamente atrativos por serem importantes fontes de carne, leite e pele. Além de estarem presentes em todos os continentes, no Brasil, eles desempenham importantes papéis econômico e social, especialmente na região nordeste do país. Nas últimas décadas, uma quantidade significativa de pesquisas tem sido realizada na área de reprodução animal, visando aumentar o potencial reprodutivo de caprinos de alto valor zootécnico ou em via de extinção. O grande desafio destes estudos é aumentar o número de descendentes de fêmeas de alto valor genético, pois até o momento, um número relativamente pequeno tem sido obtido. Ao nascimento, o ovário dos mamíferos contém milhares de folículos primordiais, os quais são considerados o pool de estoque de folículos ovarianos. No entanto, poucos folículos primordiais desenvolvem-se até o estádio de folículo pré-ovulatório, pois a grande maioria morre por atresia após iniciar o crescimento in vivo (Figueiredo et al., 2002). Neste contexto, torna-se prioritário o desenvolvimento de pesquisas que contribuam para uma melhor compreensão dos processos relacionados com a formação, crescimento e maturação dos oócitos inclusos em folículos ovarianos caprinos. A biotécnica de MOIFOPA (Manipulação de Oócitos Inclusos em Folículos Ovarianos Pré-antrais) surge então como uma importante ferramenta para esse estudo, dando suporte necessário para a elucidação dos mecanismos que envolvem a foliculogênese inicial. Até o momento, sabe-se que durante os estádios iniciais da foliculogênese, os fatores de crescimento localmente produzidos exercem um papel determinante na manutenção da viabilidade e do crescimento folicular (Fortune, 2003). No entanto, o ambiente ovariano que propicia o desenvolvimento folicular é regulado pelos hormônios folículos estimulante (FSH) e luteinizante (LH), também conhecidos como gonadotrofinas. As gonadotrofinas são indispensáveis para o desenvolvimento de folículos antrais, e seu papel sobre a foliculogênese inicial ainda não está claro (Fortune, 2003). Desta forma, a realização de estudos in vitro para avaliar o efeito destes hormônios poderá contribuir para uma melhor compreensão dos diversos componentes implicados na foliculogênese e no processo de atresia folicular nesta espécie. Para um maior esclarecimento da importância deste trabalho, a revisão de literatura a seguir aborda aspectos relacionados ao ovário mamífero, foliculogênese e características dos folículos ovarianos, importância das gonadotrofinas para o crescimento folicular, população e atresia folicular, bem como aos modelos utilizados para estudo da foliculogênese in vitro. Os 17
2 benefícios oriundos de uma melhor compreensão do desenvolvimento folicular para a melhoria da eficiência reprodutiva dos caprinos também são enfatizados. 18
3 2. REVISÃO DE LITERATURA 2.1. Ovário mamífero Como na maioria das espécies mamíferas, o ovário caprino é composto de uma medula e um córtex circundado pelo epitélio germinal. A medula ovariana consiste de um arranjo irregular de tecido conjuntivo fibroelástico e um extensivo tecido nervoso e vascular que chega ao ovário através do hilo. O córtex contém folículos ovarianos e corpos lúteos em vários estádios de desenvolvimento ou regressão. O tecido conectivo do córtex consiste de fibroblastos, colágeno e fibras reticulares (Silva, 2005). Os eventos que marcam a formação do ovário fetal incluem a sua colonização por células germinativas primordiais (CGP) e associação das células germinativas com células somáticas, formando assim os folículos primordiais. Além disso, observa-se o desenvolvimento de uma complexa rede vascular intra-ovariana em ovinos (Juengel et al., 2002). Entre os dias 18 e 28 do desenvolvimento embrionário, as células germinativas primordiais migram para a base do mesentério dorsal e a gônada indiferenciada surge entre os dias de vida embrionária, sendo evidenciada como um espessamento do epitélio celômico na porção medial do mesonéfron. Simultaneamente com a sua formação, a gônoda começa a sofrer mudanças estruturais associadas com o processo de diferenciação sexual (dias da vida embrionária), observando-se atividade esteroidogênica neste estádio em ovinos (Lun et al., 1998; Quirk et al., 2001). Após chegarem ao ovário, as CGP sofrem sucessivas mitoses e após uma reorganização das organelas e crescimento celular as CGP transformam-se em oogônias (Russe, 1983). Embora as oogônias continuem proliferando até o dia 100, o número máximo de células germinativas é alcançado aos 75 dias de desenvolvimento embrionário. A partir do 75º dia inicia-se uma redução da população de oogônias, sendo que no dia 90, mais de 75% das células germinativas são perdidas por apoptose (Smith et al., 1993). Quando as oogônias iniciam a primeira divisão meiótica, ocorre a transformação destas células em oócitos. Em seguida, uma camada de células somáticas planas, conhecidas também como células da prégranulosa, originárias do epitélio celômico, circundam os oócitos formando assim os folículos primordiais, iniciando a foliculogênese. Após a formação dos folículos primordiais, as células da pré-granulosa param de se multiplicar e entram num período de quiescência. Os oócitos primários inclusos nesses folículos encontram-se na fase de prófase I da meiose. A progressão 19
4 da divisão meiótica ocorre somente na puberdade, com a liberação do pico pré-ovulatório de FSH e LH (Erickson, 1986). 2.2 Foliculogênese e características dos folículos ovarianos A foliculogênese, evento iniciado na vida pré-natal na maioria das espécies, pode ser definida como o processo de formação, crescimento e maturação folicular, iniciando-se com a formação do folículo primordial e culminando com o estádio de folículo pré-ovulatório (Van Den Hurk & Zhao, 2005). O folículo ovariano é formado por vários tipos celulares, sendo composto por um oócito circundado por células da granulosa. Durante a foliculogênese, a morfologia folicular é alterada, uma vez que o oócito cresce e as células circundantes se diferenciam (Bristol-Gould & Woodruff, 2006). O folículo é considerado uma unidade morfológica e funcional do ovário mamífero, cuja função é proporcionar um ambiente ideal para o crescimento e maturação do oócito (Cortvrindt & Smitz, 2001), bem como produzir hormônios como o estrógeno, e peptídeos como inibina A e B, ativina e folistatina (Adashi, 1994). De acordo com o grau de evolução, os folículos podem ser classificados em primordiais, primários, secundários e antrais Folículos primordiais Os gametas femininos são estocados no ovário principalmente na forma de folículos primordiais. Tais folículos são constituídos de um oócito imaturo, circundado por uma simples camada de células da pré-granulosa de formato pavimentoso (Hutt et al., 2006). Em caprinos, os folículos primordiais são constituídos por um oócito quiescente, esférico ou oval, circundado por 1 a 14 células da granulosa. O núcleo do oócito é relativamente grande e ocupa uma posição central a excêntrica mostrando seu nucléolo evidente. As organelas são uniformemente distribuídas no citoplasma ou, às vezes, mais próximas ao núcleo. As mitocôndrias são as organelas mais evidentes e são predominantemente arredondadas, normalmente apresentando poucas cristas, organizadas paralelamente à superfície externa da membrana mitocondrial. No entanto, um pequeno número de mitocôndrias alongadas pode ser observado. Alguns retículos endoplasmáticos lisos e complexos de Golgi são observados associados a um número variável de vesículas distribuídas pelo citoplasma. A zona pelúcida 20
5 nesse estádio ainda não é observada, sendo observado apenas uma justaposição do oócito e células da granulosa, sem nenhuma junção específica (Lucci et al., 2001). Os folículos primordiais permanecem quiescentes até seu recrutamento para o grupo de folículos em crescimento (Van Den Hurk & Zhao, 2005 ). Durante toda a vida da fêmea, um pequeno grupo de folículos são gradualmente estimulados à crescer, constituindo a etapa de ativação folicular (Fair, 2003). O primeiro sinal de ativação dos folículos primordiais é a retomada da proliferação das células da granulosa, o que pode acontecer dias, meses ou anos após a sua formação (Hirshfield, 1991). Uma vez ativados, os folículos entram em um curso pré-programado de desenvolvimento e maturação que são necessários para o sucesso da ovulação e fertilização, ou alternativamente são perdidos por atresia (Fair, 2003) Folículos primários Os folículos primários são assim chamados quando uma camada simples de células da granulosa circundando o oócito torna-se cubóide. Tais folículos são circundados por 5 a 26 células da granulosa de formato cubóide dispostas em uma única camada, com as quais o oócito mantém um estreito contato. A comunicação entre o oócito e células da granulosa é mediada por endocitose. A membrana plasmática do oócito apresenta projeções que penetram entre as células da granulosa adjacentes, e algumas microvilosidades aparecem na superfície oocitária. Da mesma forma que observado em folículos primordiais, é possível observar mitocôndrias arredondadas e, com o desenvolvimento folicular, estas se tornam alongadas (Lucci et al., 2001). Na espécie caprina, os folículos primários possuem diâmetro médio de 34,7 µm e sua formação ocorre ao redor do 71 dia de gestação (Bezerra et al., 1998). À medida que os folículos iniciam o crescimento, as proteínas que irão formar a zona pelúcida começam a ser sintetizadas (Lee, 2000). A multiplicação das células da granulosa dos folículos primários leva à formação de várias camadas destas células ao redor do oócito, formando os folículos secundários Folículos secundários Nesses folículos, os oócitos são circundados por 13 a 114 células da granulosa de formato cubóide, formando duas ou mais camadas de células da granulosa com as quais o oócito mantém íntimo contato. O núcleo do oócito assume uma posição excêntrica e as organelas começam a mover-se para a periferia. O número de retículos endoplasmáticos lisos 21
6 aumenta e a grande maioria das mitocôndrias apresenta-se alongada. Com o desenvolvimento dos folículos, também aumenta o número de microvilos e inicia-se a formação da zona pelúcida (Lucci et al., 2001). Neste estádio, a zona pelúcida é claramente identificada ao redor do oócito (Parrot & Skinner, 1999). Os folículos secundários são observados em ovários de fetos caprinos, ovinos e bovinos aos 80, 120 e 210 dias de gestação, respectivamente (Rüsse, 1983; Bezerra et al., 1998; McNatty et al., 1999). Nessa fase, inicia-se a formação das células da teca externa a partir do estroma intersticial (Van Den Hurk & Zhao, 2005). As células da teca interna são definidas quando os folículos apresentam 4 ou mais camadas de células da granulosa (Lucci et al., 2001). Os folículos secundários não são bem vascularizados, o que indica que fatores endócrinos têm pouca importância no seu desenvolvimento. Vários experimentos in vivo e in vitro têm mostrado, no entanto, que um grande número de folículos secundários em desenvolvimento, e as taxas de atresia são influenciados por gonadotrofinas. O FSH é um fator predominante de sobrevivência folicular e tem mostrado estimular a formação das junções GAP nas células da granulosa (Van den Hurk et al., 1997, 2000). Apesar de serem responsivos às gonadotrofinas, os folículos secundários podem desenvolverse até o estádio antral com uma quantidade mínima de FSH circulante (Van den Hurk et al., 2000; McGee & Hsueh, 2000). O LH parece ter uma maior importância para o desenvolvimento de folículos secundários que o FSH. Os receptores de LH são demonstrados nas células da teca de folículos secundários iniciais e a ligação do LH ao seu receptor é responsável pela biossíntese de andrógenos pela teca, que por sua vez estimula a formação de receptores de FSH nas células da granulosa, amplificando o efeito do FSH sobre os folículos secundários (Van den Hurk et al., 2000) Folículos antrais Com o crescimento dos folículos secundários e organização das células da granulosa em várias camadas, ocorre a formação de uma cavidade repleta de líquido denominada antro. A partir deste estádio, os folículos passam a ser denominados terciários ou antrais. A formação dos folículos antrais em caprinos, ovinos e bovinos é observada aos 110, 135 e 230 dias, respectivamente (Rüsse, 1983; Bezerra et al., 1998; McNatty et al., 1999). Em caprinos, o menor diâmetro observado em folículo terciário de fetos foi de 130 µm (Bezerra et al., 1998). A partir deste estádio de desenvolvimento folicular, o diâmetro dos folículos aumenta acentuadamente devido ao crescimento do oócito, multiplicação das células da granulosa, da teca e aumento do fluido antral (Driancourt, 2001). Tal fluido pode servir como uma 22
7 importante fonte de substâncias reguladoras derivadas do sangue ou secreções das células foliculares, i.e., gonadotrofinas, esteróides, fatores de crescimento, enzimas, proteoglicanas e lipoproteínas. Durante o desenvolvimento folicular, a produção de fluido antral é intensificada pelo aumento da vascularização folicular e permeabilidade dos vasos sangüíneos, os quais estão fortemente relacionados com o aumento do folículo antral (Van Den Hurk & Zhao, 2005). O estímulo inicial para a formação do antro não é bem compreendido. Estudos in vitro mostram que o LH (Cortvrindt et al., 1998 a, b) é um dos responsáveis pela formação do antro. Pequenos folículos antrais podem ser similares aos folículos secundários quanto ao diâmetro (~200 µm), mas eles aumentam rapidamente em tamanho com o contínuo acúmulo de fluido folicular (Bristol-Gould & Woodruff, 2006). Os grandes folículos antrais geralmente possuem diâmetro acima de 3mm e contêm células da granulosa diferenciadas em células do cumulus e células murais, muitas camadas de células tecais, um grande espaço contendo líquido folicular e um oócito. O desenvolvimento dos folículos antrais é caracterizado por uma fase de crescimento, recrutamento, seleção e dominância (Van Den Hurk & Zhao, 2005) sendo a formação de folículos pré-ovulatórios um pré-requisito para a ovulação e formação do corpo lúteo, bem como manutenção da fertilidade (Drummond, 2006). No último estádio do desenvolvimento folicular, o folículo pré-ovulatório é caracterizado por um oócito circundado por células da granulosa especializadas que são denominadas de células do cúmulus. As células da granulosa de folículos pré-ovulatórios param de se multiplicar em resposta ao hormônio luteinizante e iniciam o programa final de diferenciação. A ovulação do oócito e células do cúmulus ocorre em resposta ao pico de LH. Em todas as espécies, a formação de folículos pré-ovulatórios ocorre geralmente a partir da puberdade (Driancourt, 2001). 2.3 Importância do FSH e LH no controle da foliculogênese em ruminantes A regulação da proliferação celular, diferenciação e atresia, relacionadas com a foliculogênese, é resultado de uma complexa interação entre fatores locais e endócrinos (Silva et al., 2006). Nesse contexto, observa-se uma grande importância das gonadotrofinas no que se refere tanto ao desenvolvimento folicular normal, como a esteroidogênese (Levi-Setti et al., 2004). As gonadotrofinas apresentam uma maior importância nos estádios mais avançados do desenvolvimento folicular. Entretanto, uma grande quantidade de mudanças foram observadas na população de folículos pré-antrais de camundongas hipofisectomizadas (Edward et al., 23
8 1977) e ovelhas (Dufour et al., 1979) evidenciando que as gonadotrofinas afetam os estádios de desenvolvimento pré-antral. Mais recentemente novos modelos de estudo da foliculogênese inicial em camundongas transgênicas demonstraram que a mutação de genes que controlam a expressão das gonadotrofinas, bem como de seus receptores, afeta diretamente não só a ovulação e formação de corpo lúteo, mas também o processo de formação de folículos primordiais, crescimento folicular e atresia (Barnett et al., 2006) Hormônio Folículo Estimulante (FSH) O hormônio gonadotrófico FSH é crítico regulador da função ovariana. A ligação do FSH é restrita às células da granulosa e resulta em uma variedade de reações, tais como a estimulação da proliferação celular, síntese de esteróides e expressão de receptores para Fator de Crescimento Epidermal (EGF) e LH. Entretanto, estudos mais recentes têm demonstrado a presença de receptores de FSH também em oócitos, sugerindo um efeito adicional do hormônio no ovário (Méduri et al., 2002). Sabe-se que as gonadotrofinas são necessárias para o desenvolvimento de folículos antrais, mas ainda não está claro se o FSH afeta o desenvolvimento de pequenos folículos pré-antrais. A expressão de receptores de FSH nas células da granulosa de folículos primários, secundários e antrais bovinos, bem como em oócitos de folículos primordiais de animais de laboratório, reforçam a idéia da ação do FSH sobre o crescimento dos folículos pré-antrais (Wandji et al., 1992; Roy, 1993). Durante o cultivo de pequenos folículos pré-antrais (30-70 µm) bovinos, o FSH promoveu um aumento do diâmetro folicular (Hulshof et al., 1995). Após seis dias de cultivo na presença de FSH, folículos primários e secundários ( µm), isolados enzimaticamente de ovários de fetos bovinos, aumentaram o diâmetro, a sobrevivência folicular, bem como a secreção de progesterona e estradiol, (Wandji et al., 1996). Gutierrez et al. (2000) isolaram folículos secundários bovinos e, após cultivo de 28 dias, observaram que o FSH promoveu o crescimento folicular e aumentou as taxas de formação de antro. Por outro lado, o FSH não afetou o diâmetro folicular e oocitário, bem como, o número de células da granulosa durante cultivo de fragmentos ovarianos bovinos (Braw-Tal & Yossefi, 1997). Além disso, a adição de 5 ng/ml de FSH (Derrar et al., 2000), bem como de outras concentrações de FSH (1, 10 ou 100 ng/ml) não teve efeito sobre os folículos pré-antrais bovinos cultivados por 7-14 dias (Fortune et al., 1998). Nuttinck et al. (1996) cultivaram pequenos folículos pré-antrais bovinos (30-70 µm) por 7 dias e observaram que o FSH aumentou a degeneração oocitária. Em suínos, o FSH está envolvido na 24
9 proliferação e diferenciação de células da granulosa de folículos pré-antrais (Hirao et al., 1994). Em caprinos, a adição de 50 ng/ml de FSH ao meio de cultivo de folículos pré-antrais inclusos em tecido ovariano foi responsável pela preservação da viabilidade folicular, aumento dos diâmetros folicular e oocitário bem como pela manutenção da integridade ultraestrutural dos folículos (Matos et al., 2007). Vários estudos também mostraram que o FSH pode promover o desenvolvimento de folículos pré-antrais de animais de laboratório. Em hamsters, pequenos folículos pré-antrais mostraram ser dependentes de FSH, pois esse hormônio reduziu significativamente a percentagem de folículos atrésicos (Roy & Greenwald, 1989). Qvist et al. (1990) mostraram que o crescimento de folículos primários é criticamente dependente, ou exige uma adequada concentração de FSH. Liu et al. (1999) observaram que o FSH promoveu o crescimento de folículos pré-antrais ( µm) isolados de ovários de camundongas adultas. Nesta mesma espécie, o FSH aumentou a sobrevivência e proliferação das células da granulosa, a formação do antro e a secreção de estradiol e inibina em folículos isolados ( µm) (Cortvrindt et al., 1997). Por outro lado, Hartshorne et al. (1994) observaram que, em camundongos, após cultivo por quatro dias, o FSH promoveu um aumento do crescimento folicular e da formação do antro em folículos maiores de 200 µm, mas não naqueles menores de 200 µm de diâmetro. Folículos ( µm) isolados de ratas pré-púberes também não cresceram com a adição de FSH ao meio de cultivo (McGEE et al., 1997). Outros estudos realizados com camundongos mostraram que o FSH é indispensável somente para a formação do antro (Nayudu & Osborn, 1992). O FSH pode ainda desempenhar um efeito indireto no desenvolvimento de folículos iniciais através da indução da liberação de fatores de crescimento pelos grandes folículos antrais e células do estroma. Por exemplo, o FSH promove a proliferação de células da granulosa através de fatores parácrinos como o IGF-1 (Fator de Crescimento Semelhante à Insulina-1) e ativina (Van Den Hurk & Zhao, 2005). Adicionalmente, o FSH regula a expressão do Kit Ligand (KL), Fator de Crescimento e Diferenciação-9 (GDF-9) e Proteína Morfogenética do Osso-15 (BMP-15) em folículos murinos (Joyce et al., 1999, Thomas et al., 2005). Esses fatores têm sido implicados na ativação de folículos primordiais (Van Den Hurk & Zhao, 2005) Hormônio Luteinizante (LH) 25
10 O hormônio luteinizante (LH) é uma glicoproteína secretada pela hipófise anterior, junto com o FSH, sendo um regulador primário da função ovariana. O LH pode apresentar múltiplos papéis sobre o desenvolvimento folicular, porém grande parte dos estudos têm focado sua ação em folículos em estádios mais avançados de desenvolvimento, durante a fase pré-ovulatória (Wu et al., 2000). O LH tem um papel bem estabelecido e essencial na síntese de esteróides e na ovulação. Enquanto a ocorrência da ovulação normal é impossível na ausência do LH (Weiss et al., 1992; Toledo et al., 1996) o papel específico deste hormônio na foliculogênese inicial, bem como na maturação oocitária ainda é pouco conhecido. Sabe-se que as células da teca expressam receptores para LH (LHR), e a ligação hormônio/receptor estimula a síntese de substratos androgênicos desde a vida fetal até o final da vida reprodutiva de fêmeas mamíferas (Adashi, 1994; Gougeon, 1996). As células da granulosa adquirem seus próprios receptores para LH em meados da fase final de desenvolvimento folicular sob influência do FSH (Erickson et al. 1979). Nesse estádio o FSH e o LH agem sinergicamente para promover o desenvolvimento folicular, aumentando a atividade da aromatase, a produção de inibina, bem como preparando o folículo pré-ovulatório para o pico de LH (Levy et al., 2000). Embora receptores não-funcionais de LH tenham sido detectadas em gônadas de roedores mesmo antes da formação folicular, o primeiro receptor funcional para LH foi demonstrado em ovários de camundongas 5 dias após o nascimento (O Shaughnessy et al., 1997). Isto coincide com o período de diferenciação morfológica das células intersticiais da teca de folículos primários em crescimento e com a capacidade de expressão da esteroidogênese basal. O FSH e LH utilizados isoladamente têm demonstrado suportar o crescimento folicular in vitro (Nayudu & Osborn, 1992; Cortvrindt et al., 1998a). Wu et al., 2000), realizando experimentos com camundongas, mostraram que o LH é necessário para o desenvolvimento in vitro de pequenos folículos pré-antrais. Além disso observaram que os folículos isolados com diâmetro entre µm cresceram até o estádio antral na presença de soro e FSH, mas os folículos isolados com µm, desenvolveram o antro somente na presença de soro, FSH e LH (10 UI/mL). Outro estudo relatou que 70% dos folículos préantrais alcançaram o estádio de metáfase II quando o cultivo foi realizado por 13 dias em meio contendo FSH e LH juntos (Cortvrindt et al., 1998b). Anteriormente, o LH introduzido ao meio no sexto dia de cultivo, induziu a ovulação in vitro de folículos pré-antrais de camundongas cultivados por 5 dias em FSH (Boland et al., 1993). Apesar da ação do LH ser direcionada para o estádio final da foliculogênese, sua ação conjunta com o FSH auxilia na proliferação celular, diferenciação, produção de estrógeno e posterior maturação (Qvist et al., 26
11 1990). Recentemente, Braw-Tal & Roth (2005), demonstraram a presença de receptores para LH na teca interna de folículos pré-antrais em estádios mais avançados e tais receptores estão diretamente relacionados à viabilidade folicular, sendo sua presença progressivamente reduzida com a atresia. Além da necessidade da obtenção de conhecimentos acerca da importância do LH sobre folículos pré-antrais, torna-se necessário conhecer as concentrações ideais no cultivo in vitro de tais folículos. 2.4 População e atresia folicular Conforme observado, a foliculogênese é um processo complexo que envolve a interação de diferentes hormônios e fatores de crescimento. Como conseqüência, a maioria dos milhares de folículos presentes nos ovários mamíferos ao nascimento não ovula, mas morrem por um processo conhecido por atresia. A população folicular é estabelecida ainda na vida fetal (primatas e ruminantes Betteridge et al., 1989) ou em um curto período de tempo após o nascimento (roedores Hirshfield, 1991). Entretanto, recentemente trabalhos têm demonstrado mecanismos envolvidos na formação, após o nascimento, de novas células germinativas e folículos na mulher (Bukovski et al., 2004) e camundonga adultas (Johnson et al., 2004). Os folículos préantrais representam 90% do total de folículos e constituem o estoque de gametas femininos durante a vida reprodutiva do animal (Liu et al., 2001). O número de folículos pré-antrais por ovário varia entre espécies, sendo de aproximadamente na camundonga (Shaw et al., 2000); na ovelha (Amorim et al., 2000); na cabra (Lucci et al., 1999) e aproximadamente na mulher (Erickson, 1986). Durante a vida reprodutiva da fêmea, ocorre uma redução ordenada, geralmente exponencial, no número de folículos pré-antrais (Shaw et al., 2000). Essa redução é devida a dois fenômenos que ocorrem naturalmente no ovário: (i) a ovulação e (ii) a atresia ou morte folicular. A atresia pode ocorrer por via degenerativa (Saumande, 1981) e/ou apoptótica (Figueiredo et al., 1995). A degeneração pode ser observada após os procedimentos de preservação in vitro, quando ocorrem alterações no fornecimento de oxigênio e nutrientes para o ovário. Nesta situação, a isquemia pode ser uma das principais causas do desencadeamento da morte folicular (Farber, 1982), resultando em alterações na permeabilidade da membrana celular. Essas alterações podem levar ao aumento de água intracelular e do volume celular, vacuolização citoplasmática e, conseqüentemente, degeneração (Barros et al., 2001). Análises histológicas e ultra-estruturais de folículos 27
12 primordiais e primários degenerados, mostraram oócito retraído com núcleo picnótico e numerosos vacúolos no ooplasma, sendo estes os principais sinais de degeneração Tipo 1, (degeneração ocorrida apenas no oócito). Já em folículos secundários, alterações tanto no oócito quanto nas células da granulosa são mais freqüentes, sendo observada uma baixa densidade de células e aumento de volume, caracterizando assim uma degeneração do Tipo 2 (Silva et al., 2001). Já a apoptose é um processo de morte celular individual e ativo, caracterizado pela fragmentação nuclear e pela formação de corpos apoptóticos (Rachid et al., 2000). O processo de apoptose é altamente dependente da expressão de genes (Barnett et al., 2006). O balanço estabelecido entre o produto dos genes pró-apoptóticos e anti-apoptóticos pode determinar a morte celular (Hurwitz & Adashi, 1992). A progressão da apoptose pode ser dividida nas fases de iniciação, execução e terminação. A fase de iniciação pode ser promovida por fatores qua ativam a via extrínseca (receptores de morte localizados na membrana celular), tais como citocinas (ex. Fator de Necrose tumoral-α, Fas ligand) e proteínas virais ou pela remoção de fatores de crescimento. A morte celular também pode ser induzida por fatores que ativam a via intrínseca (mitocondrial), tais como o estresse oxidativo ou irradiação. Independentemente dos tipos de fatores envolvidos, ocorre o envolvimento de uma ou mais caspases de iniciação (caspase 8, caspase 9) (Morita & Tilly, 1999; Johnson & Bridgham, 2002). A fase de execução é caracterizada por mudanças na membrana celular, fragmentação nuclear, condensação da cromatina e degradação do DNA. Esta fase é considerada irreversível e ocorre devido à ativação das caspases efetoras (caspases 3, 6 e 7). Finalmente, a fase de terminação consiste na fagocitose de corpos apoptóticos fragmentados através de um processo não inflamatório. No sentido de evitar a morte celular por apoptose, existem processos de sobrevivência celular que promovem a transcrição de várias proteínas anti-apoptóticas, tais como os membros da família Bcl-2, que bloqueiam a progressão da apoptose em diferentes etapas ao longo deste processo (Johnson et al., 2003). 2.5 Sistema de cultivo in vitro de folículos pré-antrais Para evitar a enorme perda folicular que ocorre naturalmente in vivo, vem sendo desenvolvida a biotécnica MOIFOPA que é constituída pelas fases de isolamento, conservação e cultivo folicular in vitro. No tocante ao cultivo in vitro, vários sistemas têm sido desenvolvidos e os resultados são dependentes do tipo de meio utilizado e da espécie animal (Eppig e Schoeder, 1989, Boland et al., 1994, Fortune, 2003). 28
13 Para o cultivo in vitro de folículos pré-anrais, especialmente nos estádios de folículos primordiais e primários, existem dois sistema bem definidos (Van den Hurk et al., 2000). O mais utilizado envolve o cultivo de pequenos fragmentos de tecido ovariano, cultivo in situ, no qual a integridade estrutural folicular é mantida e as interações entre as células foliculares e células do estroma são permitidas. Através desse método, folículos primordiais de caprinos, bovinos (Braw-tal e Yossefi, 1997) e humanos (Hovatta et al., 1997; Wright et al., 1999; Louhio et al., 2000; Scott et al., 2004 e Zhang et al., 2004) cresceram até folículos secundários. Folículos humanos permaneceram viáveis por quatro semanas quando cultivados em sistema in situ (Hovatta et al., 1997). Já o segundo sistema de cultivo folicular envolve o isolamento, mecânico ou enzimático dos folículos ovarianos pré-antrais (Abir et al., 1999, 2001b). As técnicas de isolamento desenvolvidas possibilitam a recuperação de milhares de folículos pré-antrais a partir de um único ovário (Figueiredo et al., 2002). Além disso, o cultivo de folículos isolados permite o monitoramento diário do crescimento folicular in vitro (Abir et al., 2001a). Os maiores avanços do cultivo folicular foram obtidos em roedores, tendo sido obtido o nascimento de crias viáveis a partir do cultivo de oócitos provenientes de folículos préantrais de camundongas, nos quaia o oócito adquiriu competência para maturação, fertilização e desenvolvimento embrionário (O Brien et al., 2003). Tal crescimento foi obtido através de dois sistemas de cultivo. O primeiro consistiu no cultivo de ovários inteiros para obtenção da transição de primordial para primário. O segundo consistiu no isolamento e cultivo de folículos primários e secundários. Provavelmente essa estratégia é necessária para promover o crescimento de folículos primordiais de espécies domésticas e primatas (Silva et al., 2006). No entanto, o tamanho dos ovários dos animais domésticos impede seu cultivo inteiro, sendo necessária a fragmentação do córtex ovariano. Embora a utilização de fragmentos ovarianos no cultivo, permita a ativação folicular (Hovatta et al., 1999), a variedade de células presentes no cultivo in situ torna o sistema pouco definido e impede estudos mais detalhados sobre a biologia dos oócitos e da foliculogênese nos estádios iniciais de desenvolvimento (Muruvi et al., 2005). O presente desafio é determinar condições de cultivo apropriadas para dar suporte à transição de folículos primários para secundários in vitro. 29
14 3. JUSTIFICATIVA Os folículos primordiais constituem o pool de reserva de folículos quiescentes e compreendem cerca de 90 a 95% de toda população folicular presente no ovário mamífero. No entanto, para que estes folículos possam entrar em fase de crescimento (intermediário, primário, secundário, terciário e/ou pré-ovulatório), é preciso que sejam ativados, ou seja, retomem a proliferação das células da granulosa, bem como aumentem os volumes citoplasmático e nuclear do oócito. Neste contexto, sabendo-se do grande valor econômico que a espécie caprina representa para o Nordeste brasileiro, é de extrema importância o desenvolvimento de um sistema de cultivo in vitro capaz de ativar esses folículos e assegurar seu posterior crescimento e maturação in vitro, otimizando o aproveitamento do potencial oocitário desses animais e incrementando a eficiência da reprodução animal. Além disso, o desenvolvimento de um sistema de cultivo eficiente poderá fornecer subsídios para uma melhor compreensão acerca dos fatores que regulam a foliculogênese na fase pré-antral, fatores esses necessários para a sobrevivência, a ativação e o início do crescimento folicular. Estudos referentes aos fatores e mecanismos envolvidos na regulação e ativação dos folículos primordiais são escassos, especialmente em animais de produção, como os caprinos. Desse modo, diversos autores têm investigado o efeito de vários componentes no cultivo de folículos pré-antrais tanto de animais de laboratório como de animais domésticos como vaca, cabra e ovelha. Substâncias como soro fetal, FSH, estradiol, EGF são largamente utilizadas. Entretanto, os efeitos de diferentes concentrações de LH, bem como sua interação com o FSH não tinham sido testadas no cultivo in vitro de folículos pré-antrais caprinos. Além disso, não eram conhecidos os efeitos deste cultivo sobre as características estruturais e ultra-estruturais de folículos pré-antrais caprinos. Assim, a utilização da microscopia eletrônica de transmissão para determinar a qualidade de folículos pré-antrais caprinos cultivados in vitro pode fornecer dados precisos sobre a qualidade folicular. Desta forma, a realização deste trabalho contribuirá para a compreensão da foliculogênese caprina, o que poderá no futuro, trazer benefícios para otimização da produção de embriões caprinos em larga escala. 30
15 4. HIPÓTESE CIENTÍFICA O FSH e o LH podem influenciar positivamente na ativação e crescimento in vitro de folículos pré-antrais caprinos. EXPERIMENTOS O presente trabalho foi dividido em dois experimentos, a saber: EXPERIMENTO I: Cultivo in vitro de oócitos inclusos em folículos pré-antrais caprinos utilizando diferentes concentrações de LH. EXPERIMENTO II: Avaliação da interação do LH e do FSH no cultivo in vitro de oócitos inclusos em folículos pré-antrais caprinos. 31
16 5. OBJETIVOS EXPERIMENTO I: Cultivo in vitro de oócitos inclusos em folículos pré-antrais caprinos utilizando diferentes concentrações de LH. Objetivo Geral - Estudar o efeito do LH sobre o cultivo de folículos pré-antrais caprinos in vitro. Objetivos Específicos - Estabelecer a melhor concentração de LH para o cultivo de folículos pré-antrais caprinos, tendo como parâmetros a viabilidade, a ativação e o crescimento de folículos préantrais; - Analisar morfológica e ultra-estruturalmente os folículos pré-antrais caprinos cultivados in vitro com LH. EXPERIMENTO II: Avaliação da interação FSH e LH no cultivo in vitro de oócitos inclusos em folículos pré-antrais caprinos. Objetivo Geral - Cultivar in vitro folículos pré-antrais caprinos utilizando o FSH sozinho ou em associação ao LH em diferentes concentrações. Objetivos Específicos - Verificar o efeito do FSH isoladamente ou em associação ao LH sobre a viabilidade, ativação e crescimento in vitro de folículos primordiais caprinos; - Analisar morfológica e ultra-estruturalmente os folículos pré-antrais caprinos cultivados in vitro com LH e FSH. 32
17 6. Capítulo 1 Influence of different concentrations of Luteinizing Hormone (LH) and Follicle Stimulating Hormone (FSH) on caprine preantral follicle development O objetivo deste trabalho foi investigar o efeito do LH, FSH e a interação de ambos sobre o crescimento de folículos pré-antrais caprinos cultivados in vitro. Para realização do experimento oito pares de ovários provenientes de cabras adultas sem raça definida foram coletados de abatedouros locais e transportados até o laboratório. Cada par de ovário foi dividido em 11 fragmentos e, um deles foi imediatamente fixado, para constituir o grupo controle, e os demais foram cultivados em meio essencial mínimo MEM + na ausência ou presença de LH nas concentrações 1, 5,10, 50 ou 100 ng/ml (Experimento 1), ou nas mesmas concentrações associadas ao FSH 50 ng/ml (Experimento 2). O cultivo foi realizado por 1 e 7 dias à 39 C em atmosfera de 5% CO 2. Ao término desse período, proporções relativas de folículos primordiais, primários e secundários foram calculadas e comparadas com aquelas em tecido não cultivado. A morfologia folicular foi analisada por histologia clássica e microscopia eletrônica e os folículos foram classificados em degenerados, de acordo com o grau de comprometimento do oócito e células da granulosa. Os resultados mostram que após 7 dias de cultivo a presença de LH (10, 50 ou 100 ng/ml) no meio de cultivo aumentou significativamente a percentagem de folículos em desenvolvimento. Em adição, os fragmentos cultivados em meio suplementado com FSH sozinho ou associado ao LH aumentaram as taxas de folículos em desenvolvimento após um dia de cultivo (P<0,05), mas no dia sete não foram verificadas diferenças significativas (P>0,05). Ao final do período de cultivo, o LH 1, 5 e 10 ng/ml aumentaram o diâmetro oocitário em relação ao controle, mas apenas o LH 1 e 5 ng/ml aumentaram o diâmetro folicular em relação ao MEM (P<0,05). Em associação ao FSH, estas mesmas concentrações de LH (1 e 5 ng/ml) aumentaram o diâmetro folicular no dia 7 em relação ao MEM. Referente à sobrevivência folicular, a concentração mais baixa de LH (1 ng/ml) manteve a viabilidade semelhante ao grupo controle e ao MEM (P>0,05) após 7 dias de cultivo. Contudo, as concentrações mais altas de LH (5, 10, 50 e 100 ng/ml) induziram atresia dos folículos caprinos cultivados. Após 7 dias, os folículos cultivados em meio suplementado com FSH sozinho ou associado ao LH 1 ng/ml mantiveram as características ultra-estruturais similar ao dia 0. Em conclusão, a adição de baixas concentrações de LH (1 ng/ml) associado ou não ao FSH, mantiveram a integridade ultra-estrutural de folículos pré-antrais caprinos, mas o LH em concentrações superiores a 5 ng/ml induziu a atresia destes folículos. PALAVRAS-CHAVE: Folículo, pré-antral, caprino, cultivo in vitro, LH, FSH. 33
18 Influence of different concentrations of Luteinizing Hormone (LH) and Follicle Stimulating Hormone (FSH) on caprine primordial follicle development M.V.A. Saraiva a, J.J.H. Celestino a, R.N. Chaves a, F.S. Martins a, J.B. Bruno, I.B. Lima Verde a, M.H.T. Matos a, G.M. Silva a ; E. P. Porfirio b, S.N. Báo b, C.C. Campello a, J.R.V. Silva a, J.R. Figueiredo a a Faculty of Veterinary Medicine, LAMOFOPA, PPGCV, State University of Ceara, Fortaleza, CE, Brazil b Laboratory of Electron Microscopy, Department of Cell Biology, University of Brasilia, Brasilia, DF, Brazil *Corresponding address: Programa de Pós-Graduação em Ciências Veterinárias (PPGCV) Laboratório de Manipulação de Oócitos e Folículos Pré-Antrais (LAMOFOPA) Universidade Estadual do Ceará (UECE) Av. Paranjana, 1700, Campus do Itaperi. Fortaleza CE Brasil. CEP: Tel.: ; Fax: address: viviane2507@yahoo.com.br (M.V.A. Saraiva) 34
19 Abstract The roles of gonadotropins in the regulation of primordial follicle development remain poorly understood. The aims of the present study were to investigate the effects of Luteinizing Hormone (LH) alone or in association with Follicle Stimulating Hormone (FSH) on survival, activation and growth of caprine primordial follicles using histological and ultrastructural studies. To this end, pieces of caprine ovarian cortex were cultured for 1 or 7 days, at 39 o C in an atmosphere containing 5% CO 2, in Minimum Essential Medium (MEM - control medium) supplemented with different concentrations of LH (0, 1, 5, 10, 50 or 100 ng/ml experiment 1). In experiment 2, control medium was supplemented with FSH (50 ng/ml) and different concentrations of LH (0, 1, 5, 10 or 50 ng/ml). Small fragments from non-cultured ovarian tissue as well as from those cultured for 1 or 7 days in a specific medium were processed for classical histology and transmission electron microscopy (TEM) to evaluate follicular integrity and to calculate the percentages of normal follicles. Additionally, effects of FSH on oocyte and follicle diameter of cultured follicles were evaluated. The results showed that after 7 days of culture, the presence of LH (10, 50 or 100 ng/ml) in culture media significantly increased the percentages of developing follicles (P<0,05). In addition, fragments cultured in media supplemented with FSH alone or FSH plus LH had higher percentage of developing follicles after one and seven days culture compared with control (P<0,05). At the end of culture period, 1 and 5 ng/ml LH increased follicular diameter, while addition of 1, 5 or 10 ng/ml LH increased oocyte diameter (P<0,05). In association with FSH, LH (1 and 5 ng/ml) increased follicular diameter (P<0,05). With regard to follicle survival, low doses of LH (1 ng/ml) kept follicle viability similar to control medium after 7 days culture. However, higher concentrations of LH (5, 10, 50 and 100 ng/ml) induced atresia in goat follicles. Culture of ovarian cortex for 7 days in medium supplemented with FSH or LH 1 ng/ml alone or FSH 35
20 plus 1ng/mL LH kept ultrastructural characteristics of follicles similar to day 0. In conclusion, addition of low concentrations of LH (1 ng/ml) associated or not with FSH maintain goat follicles ultrastructural integrity, but LH in doses higher than 5 ng/ml induces atresia in goat preantral follicles. Keywords: Caprine, Primordial Follicles, Culture, LH, FSH. 1. Introduction It is well established that gonadotropins are required for antral follicle development, but not for the development of preantral follicles (primordial, primary and secondary follicles). However, large quantitative changes in the population of preantral follicles after hypophysectomy of mice (Edwards et al., 1977) and ewes (Dufour et al., 1979) provide evidence that gonadotropins do affect the development of follicles at preantral stages. Effects of FSH on preantral follicles from humans and domestic species were also observed. When Wright et al. (1999) added FSH to cortical pieces from human ovaries the percentage of atretic follicles was decreased and follicle diameter increased during a 15-day culture period. In contrast, the addition of FSH at 5 ng/ml (Derrar et al., 2000) or graded doses of FSH (Fortune et al., 1998) had no effect on follicular populations during longer cultures (7-14 days) of bovine cortical pieces. However, a recent study with caprine follicles showed that, at a concentration of 50 ng/ml FSH is able to promote the activation of primordial follicles and further growth of activated follicles (Matos et al., 2007). Receptors of FSH are expressed in granulosa cells (Ulloa-Aguirre et al., 1995; O Shaughnessy et al., 1997) from primary follicles and more recent reports indicate its presence in oocytes (Méduri et al., 2002). 36
21 Regarding to LH, much less is known about its potential effects on growth of preantral follicles. Experiments accomplished by Wu et al. (2000) indicated that in mice LH is need for in vitro development of preantral follicles to antral stages. Large preantral follicles ( µm) developed to antral follicles in presence of FSH and serum, but addition of LH, together with serum and FSH, was important to promote the development of small preantral follicles ( µm) to the antral stage. Liu et al. (2002) developed a culture system that allows the maturation of preantral follicles in vitro with recombinant gonadotropins. Receptors of LH have a more widespread distribution and are also found in non gonadal tissues (Reshef et al., 1990; Reiter et al., 1995). In the ovary, LH receptors are found primarily in the interstitial (McFarland et al., 1989) and thecal cells, and only in the mid-follicular phase, granulosa cells acquire LH receptors (Zeleznick and Hillier, 1984; Yamoto et al., 1992) as well as in the preovulatory follicle and the corpus luteum (Zeleznick et al., 1974; McFarland et al., 1989). The acquisition of LH receptors by granulosa cells depends upon the actions of FSH and estradiol together. FSH induces the expression of LH receptors in granulosa cells by increasing transcription of the LH receptor gene (Segaloff, 1996). Although the importance of FSH and LH for antral follicle development in vivo is well know, the effects of both hormones on primordial follicle growth during culture of caprine ovarian cortex was not yet evaluated. Thus, the goal of the present study was to investigate whether LH alone or in combination with FSH, have a beneficial role in the survival, activation and further growth of in vitro cultured goat primordial follicles enclosed in ovarian cortex. To this aim, both histological and ultrastructural studies were performed to investigate and compare the morphology of follicles before and after culture for 1 or 7 days in the absence or presence of LH at different concentrations (1, 5, 10, 50 or 100 ng/ml) alone, or associated with FSH (50 ng/ml). 37
22 2. Material and Methods 2.1. Source of ovaries Ovaries (n = 8 for experiment 1, n = 8 for experiment 2) from eight adult non-pregnant mixed-breed goats were collected at a local slaughterhouse. The animals were cyclic and in good body condition. Then, the ovaries were washed and transported in MEM (Minimum Essential Medium) to the laboratory in thermo flasks with water at 33 o C within 30 minutes Culture medium The control medium was Minimum Essential Medium (Cultilab, Rio de Janeiro, Brazil) supplemented with ITS (insulin 6.25 µg/ml, transferrin 6.25 µg/ml, and selenium 6.25 ng/ml), 0.23 mm pyruvate; 2 mm glutamine; 2 mm hypoxanthine; 1.25 mg/ml BSA, 100 µg/ml penicillin, 100 µg/ml streptomycin (Vetec, Rio de Janeiro, Brazil) (MEM + ). This control medium (MEM) was supplemented with porcine FSH (50 ng/ml) and/or porcine LH (1, 5, 10, 50 or 100 ng/ml) (both provided by Dr. J.F. Beckers, Liège, Belgium). All chemicals used in the present study were purchased from Sigma Chemical Co. (St. Louis, MO, USA) unless otherwise indicated Experimental protocol In experiment one, goat ovaries (n = 8) were collected and stripped of surrounded fat tissue and ligaments, and cut in half, after the medulla, large antral follicles and corpora lutea were removed. Following this, the ovarian cortex was divided into 11 fragments of 38
23 approximately 3 x 3 mm (1 mm thick). One fragment was immediately fixed for classic histological studies (non-cultured controls) while a smaller fragment (1 mm 3 ) was randomly collected and subsequently fixed for ultrastructural examination. The other fragments of ovarian cortex were individually cultured in vitro in 1 ml of culture medium supplemented with different concentrations of porcine LH (1, 5, 10, 50 or 100 ng/ml). To evaluate the interaction between FSH and LH (experiment 2), 8 ovaries were collected and the fragments obtained of ovarian cortex were individually cultured in vitro in 1 ml of culture medium supplemented with porcine FSH (50 ng/ml) alone or associated to LH (1, 5, 10 or 50 ng/ml). The culture was performed for 1 or 7 days at 39 C with 5% CO 2 in air using a 24-well culture dish. Every two days, the culture medium was replaced by fresh medium. Each treatment was repeated four times using the ovaries of four different animals for each experiment Histological analysis and assessment of in vitro follicle growth For both experiments, to evaluate the morphology of caprine follicles after 1 or 7 days of culture, a small part (1 mm 3 ) from each fragment was randomly removed for TEM studies, while the remainder was fixed in Carnoy for 12 h for histological studies. After fixation, the tissue fragments were dehydrated in graded series of ethanol, clarified with xylene and embedded in paraffin wax. For each piece of ovarian cortex, 7µm sections were mounted on slides, stained with periodic acid Schiff and hematoxylin (PAS staining system, Sigma, Inc., St. Louis, MO, USA), and examined by light microscopy (Zeiss, Germany) at 100X and 400X magnification. The follicles were classified as primordial (one layer of flattened granulosa cells around the oocyte), or developing follicles i.e., intermediate (one layer of flattened to cuboidal granulosa cells around the oocyte), primary (a single layer of cuboidal granulosa cells around 39
24 the oocyte), or secondary (oocyte surrounded by two or more layers of cuboidal granulosa cells). These follicles were classified individually as histologically normal (1) when an intact oocyte was present, i.e. an oocyte without a pyknotic nucleus, surrounded by granulosa cells which are well organized in one or more layers and that have no pyknotic nucleus or (2). degenerated follicles were defined as those with a retracted oocyte, which have a pyknotic nucleus, and/or are surrounded by disorganized granulosa cells, which are detached from the basement membrane. From each medium and culture period, approximately 120 follicles were randomly evaluated. To evaluate follicular activation and growth, only intact follicles with a visible oocyte nucleus were recorded, and the proportion of primordial and growing follicles were calculated at day 0 (controls) and after 1 or 7 days of culture in the various media tested. Major and minor axes of each oocyte and follicle were measured with the aid of an ocular micrometer. The averages of the minor and major axes were reported as oocyte and follicle diameters, respectively. These values were used to assess the effect of the hormonal treatment on follicular growth Ultrastructural analysis For ultrastructural analysis, small pieces of ovarian cortex were fixed in 2% paraformaldehyde, 2.5% glutaraldehyde, and 0.1 M sodium cacodylate buffer, ph 7.2. After washing the ovarian pieces with sodium cacodylate buffer, they were post-fixed in 1% osmium tetroxide, 0.8% potassium ferricyanide and 5 mm CaCl 2 in 0.1 M sodium cacodylate buffer. Subsequently, samples were dehydrated in graded series of acetone and embedded in Spurr s epoxy resin. Firstly, semi-thin sections (3 µm) were cut on an ultramicrotome (Reichert Supernova, German) for light microscopy studies and stained with toluidine blue. 40
25 Subsequently, follicles classified as histologically normal in semi-thin toluidin blue stained sections were submitted to ultrastructural analysis. For that purpose, thin sections (70 nm) were cut and then contrasted with uranyl acetate and lead citrate, and examined using a Jeol 1011 (Jeol, Tokyo, Japan) transmission electron microscope Statistical analysis Data for follicles and oocytes diameters were analyzed statistically as follows. Kolmogorov-Smirnov and Bartlett s tests were applied to confirm normal distribution and homogeneity of variance, respectively. Analysis of variance was then made using GLM procedure of SAS (1999) and Dunnett s test was applied for comparison of control groups against each treatment tested (Steel et al., 1997), whilst Student s t-test was used to compare means between one and seven days of cultivation. Differences among groups were considered significant when P<0.05 and results were expressed as means ± standard deviation. Chisquare test was used to compare percentages of viable follicles among the days. 3. Results 3.1. Effects of FSH and LH on primordial follicle activation The percentage of primordial and developing follicles in goat ovarian tissue before and after culture in media supplemented with LH is shown in Table 1. Growth was evaluated only for follicles considered morphologially normal during culture (Figure 1A). After one day culture in medium containing 10 ng/ml LH, a significant reduction of primordial follicles and concomitant increase of developing follicles was observed when compared to day 0 (non- 41
26 cultured control). However, no significant differences were observed among treatmens. At day 7 of culture, the presence of 10, 50 or 100 ng/ml of LH in culture media significantly increased the percentages of developing follicles in relation to day 0, and follicles cultured in MEM (P<0,05). Cultured ovarian tissue in MEM or MEM plus 1 or 5 ng/ml LH had similar percentages of developing follicles when compared to day 0. Increasing the culture period from 1 to 7 days, higher percentages of developing follicles was observed in ovarian tissue cultured in media supplemed with 50 or 100 ng/ml LH (P<0,05). The effects of both FSH and LH on primordial follicle development are shown in Table 2. After one and seven days culture, all treatments showed a significant reduction in the percentage of primordial follicles that was followed by a significant increase of developing follicles when compared to day 0, except for tissue cultured in FSH plus and 10 ng/ml LH for one day. Cortical tissue cultured in media supplemented with FSH alone or FSH plus LH (all concentrations) had higher percentage of developing follicles, as well as lower percentage primordial follicles than MEM after one day culture. After 7 days culture, significant differences were observed among the treatments compared to day 0. When the culture period was increased from 1 to 7 days, ovarian tissue cultured in FSH plus LH 10 ng/ml had higher percentage of developing follicles, as well as lower percentage of primordial follicles (Table 2) Effects of FSH and LH on oocyte and follicle diameters After one day culture in all media, oocyte and follicle diameters were similar to day 0, and no differences were observed among treatmens and MEM (Table 3). After 7 days culture of ovarian tissue in medium supplemented with LH (1, 5, 10, 50, 100) ng/ml a significant increase in oocyte and follicle diameters was observed when compared to day 0, except for 42
27 oocyte diameter in tissue cultured in MEM plus 50 and 100 ng/ml LH. When follicles were cultured for 7 days in MEM plus 1 or 5 ng/ml LH that had higher diameter when compared to MEM. When the culture period was increased from 1 to 7 days, a significant increase in follicle and oocyte diameter was observed after culture in MEM or MEM plus 1, 5 and 10 ng/ml LH, except for oocyte diameter in tissue cultured in MEM alone (Table 3). Table 4 shows the effects of FSH alone or the interaction between FSH and LH on oocyte and follicle diameters. After one day, ovarian tissue cultured in all media had similar oocyte and follicle diameters when compared to day 0. Similar results were observed for oocyte diameter at day 7 of culture. In contrast, a significant increase in follicle diameter was observed after 7 days culture in medium supplemented with FSH or FSH plus LH, when compared to day 0. In addition, cortical tissue cultured for 7 days in FSH plus and 1 or 5 ng/ml LH had significantly higher diameter than MEM and FSH (P<0,05 Table 4) Effects of FSH and LH on follicle survival Cortical tissue cultured for one day in MEM or MEM plus 1 ng/ml LH kept the percentages of normal follicles (Figure 1A) similar to day 0. Degenerated follicle is shown in Figure 1B. After 7 days, tissues cultured in all tested media had significantly lower percentages of normal follicles when compared to day 0 (non-cultured control). After 1 or 7 days culture, addition of 5, 10, 50 or 100 ng/ml LH to culture medium promoted a significant reduction of normal follicles was observed when compared to day 0, MEM or MEM plus 1 ng/ml LH (Table 5). When the culture period was increased from 1 to 7 days, a significant reduction of normal follicles in tissues cultured in MEM plus LH at 5, 10 and 50 ng/ml. With regard to the effect of the interaction between FSH and LH, cortical tissue cultured for one day in MEM or MEM plus FSH kept the percentages of normal follicles similar to day 0. 43
28 After 7 days, tissues cultured in all tested media had significantly lower percentages of normal follicles when compared to day 0. After 1 day culture, addition FSH + LH (1, 5, 10 or 50 ng/ml) together significantly reduced the percentage of normal follicles when compared to MEM or MEM plus FSH alone. Similar results were observed after 7 days, except for FSH plus 1 or 5 ng/ml LH (Table 6). With the increased of culture period from 1 to 7 days, a significant reduction of normal follicles was observed in tissues cultured in all media, except for FSH + LH 50 ng/ml Ultrastructural characteristics of cultured follicles Based on histological results, ultrastructural evaluation was performed in non-cultured tissue and in tissue cultured for 7 days in MEM supplemented or not with 1 ng/ml LH, as well as in FSH plus and LH (1 or 5 ng/ml). Follicles cultured for 7 days in MEM plus 1 ng/ml LH and in MEM plus FSH and LH (1 ng/ml) had ultrastructural characteristics similar to day 0 (non-cultured control). In contrast, follicles cultured in MEM alone or MEM plus FSH and LH (5 ng/ml) had signs of degeneration. Normal follicles had intact oocyte showing nuclear membranes, unpacked nuclear chromatin and cytoplasm rich in organelles (Figure 2A). The cytoplasm contained numerous rounded mitochondria with peripheral cristae and continuous mitochondrial membranes (Figures 2A, B and C). In all the oocytes, a large number of vesicles spread throughout the cytoplasm were observed, but Golgi complexes were rarely seen. Both smooth and rough endoplasmic reticulum was present, either as isolated aggregations or as complex associations with mitochondria. Granulosa cells had irregularly-shaped nuclei, and the cytoplasm contained a great number of elongated mitochondria with lamellar cristae and well-developed rough endoplasmic reticulum (Figure 2C). Degenerated follicles had low cytoplasm density in oocyte and granulosa cells, as well as 44
29 broken oocyte and nuclear membranes (follicles cultured for 7 days in MEM plus FSH and LH (5 ng/ml) - Figure 2D). 4. Discussion This study showed for the first time the effect of different concentration of LH, alone or in association with FSH, on primordial follicle development and viability after culture of goat ovarian cortical tissue in vitro. Higher percentages of primordial follicle activation were observed in ovarian cortex cultured for 7 days in medium supplemented with high concentration of LH (10, 50 or 100 ng/ml). Flaws et al. (1997) demonstrated that high levels of LH can stimulate growth of primordial follicle and their transition to primary and secondary stages. In our study, when associated to FSH, LH (1, 5, 10 or 50 ng/ml) did not increase primordial follicle activation. According to Médure et al. (2002), transition from primordial to primary follicle stage is not directly dependent of FSH. In addition, Silva et al. (2004) did not observe effect of FSH (100ng/mL) on goat primordial follicle activation in vitro. On the other hand, addition of 50ng/mL FSH increased goat primordial follicle activation and growth after 1 day culture (Matos et al., 2007). FSH can act indirectly, since it regulates the production of prarcrine factors, such as kit ligand, BMP-15 and GDF 9, which promote oocyte development (Thomas et al., 2005) and primordial follicle activation (Elvin et al., 1999; Vitt et al., 2000; Kingler and Felici, 2002). Additionally, during follicle development, gonadotropins promote growth and differentiation of granulosa cells, as well as oocyte growth and maturation (Cortvrindt et al., 1998a,b). After 7 days culture, 1, 5 and 10 ng/ml LH increased oocyte diameter, while addition only of LH 1 or 5 ng/ml increased follicular diameter. Furthermore, in association with FSH, 45
30 LH (1 and 5 ng/ml) increased follicular diameter. In mice, addition of both FSH and LH to culture medium also increased follicular growth (Cortvrindt et al., 1997, 1998a,b; Liu et al., 2002). In the ovary, LH receptors are expressed in interstitial cells (McFarland et al., 1989), as well as theca and granulosa cells (McFarland et al., 1989). Probably, these cells are stimulated by LH and then secrete factors that promote preantral follicle growth. To support this hypothesis, Liu et al. (2002) showed that in absence of LH no proliferation of granulosa cells is observed in vitro. With regard to FSH, its receptor is expressed in oocyte (Méduri et al., 2002) and granulosa cells (Xu et al., 1995) of preantral follicles. Studies in vitro showed that FSH stimulates oocyte growth in preantral follicles (caprine: Matos et al., 2207; bovine: Itoh et al., 2002; murine: Cortvrindt et al., 1998a). In addition, FSH, together with estradiol, activates granulosa cell proliferation, increase aromatase activity and promote expression of LH receptors in granulosa cells (Zeleznik et al., 1974; Carson and Smith, 1986; Xu et al., 1995). With regard to follicular survival, low doses of LH (1 ng/ml) kept follicle viability similar to control medium after 7 days culture. However, higher concentrations of LH (5, 10, 50 and 100 ng/ml) induced atresia in up to 85% (LH 100 ng/ml) of follicles. The presence of both FSH and LH (1 and 5 ng/ml) kept follicle survival similar to control. Flaws et al. (1997) demonstrated that high levels of LH promote depletion of primordial follicle population. According to this author, elimination of primordial follicles in mice can be due to the fact that (1) LH, in high levels, stimulates primordial follicle growth and transition to primary and secondary stages (2) or induces apoptosis of primordial follicles. In addition, Simplício (1985) showed that plasmatic level of LH in goats ranges from 0,41 to 4 ng/ml during anestrous and from 6,1 to 28,0 ng/ml during estrus. In human, during the period of perimenopause, the loss of primordial follicles accelerates at a rate twice that seen previously (Richardson et al., 1987). If not for this acceleration, women would remain fertile well into their eighties (Faddy 46
31 et al., 1992). During perimenopause, women experience transient elevations in the levels of both LH and FSH (Sherman et al., 1976; Marcus et al., 1993). This altered endocrine milieu exerts a toxic effect on the primordial follicle pool, accelerating its depletion (Richardson et al., 1987). Studies with transgenic mice also demonstrated that high levels of LH rapidly reduces the pool of primordial follicles (Barnett et al., 2006). The effects of FSH and LH on follicle viability can be via glucose metabolism, since gonadotropins significantly influence several regulators enzymes of glicolysis and Krebs cycle may be influenced differently by FSH and LH, and the influence varies with the maturation status of the follicles (Roy and Terada, 1999). In this study, medium supplemented with FSH alone or FSH plus 1ng/mL LH kept ultrastructural characteristics of 7-day cultured follicles. Recently, Matos et al. (2007) showed similar results after culturing ovarian tissue in medium containing FSH alone. In contrast, follicles cultured with FSH and 5 ng/ml LH had various signs of degeneration, such as numerous vacuoles in the ooplasm. These vacuoles are the first signs of degeneration observed in atretic follicles and may represent endoplasmic reticulum swelling or altered mitochondria (caprine: Silva et al., 2002; ovine: Jorio et al., 1991). Normal follicles had their ultrastructure similar to that previously described for goat (Lucci et al., 2001) and other species (bovine: Van Wezel and Rodgers, 1996; swine: Greenwald and Moor, 1989, human: Oktay et al., 1997). Round or elongated mitochondria were abundant in the ooplasm of goat follicle. The round shape of the mitochondria, indicate immaturity (Perkins and Frey, 2000), in accordance with the quiescent stage of primordial follicle oocytes. In these follicles the round mitochondria were the vast majority in the oocyte cytoplasm, being gradually replaced by elongated mitochondria in the oocytes of primary and secondary follicles (Lucci et al., 2001). 47
32 In conclusion, addition of FSH (50 ng/ml) associated or not with low concentrations of LH (1 ng/ml) maintain goat primordial follicles ultrastructural integrity after cultured follicles. However, LH in doses higher than 5 ng/ml induces atresia and reduces primordial follicle population in cultured goat cortical tissue. Further studies on the effects of LH in the modulation of paracrine growths factors are still needed to understand the effects of LH on early folliculogenesis in goats. Acknowledgements This work was supported by CAPES. Márcia Viviane Alves Saraiva is a recipient of a grant from CAPES (Brazil). We would like to acknowledge the generous donation of FSH and LH by Dr. Jean-François Beckers of the University of Liège, Belgium. References BARNETT, K.R., SCHILLING, C., GREENFELD, C.R., TOMIC, D., FLAWS, J.A., Ovarian follicle development and transgenic mouse models. Hum. Reprod. Update. 12, CARSON, R., SMITH, J., 1986 Development and steroidogenic activity of preantral follicles in the neonatal rat ovary. J. Endoc. 110, CORTVRINDT, R.G., HU, Y., LIU, J. & SMITZ, J.E., 1998a. Timed analysis of the nuclear maturation of oocytes in early preantral mouse follicle culture supplemented with recombinant gonadotrophin. Fertil. Steril. 70,
33 CORTVRINDT, R., HU, Y., SMITZ, J. 1998b. Recombinant Luteinizing Hormone as a survival and differentiation factor increases oocyte maturation in recombinant follicle stimulating hormone-supplemented mouse preantral follicle culture. Human Reprod. 13, CORTVRINDT, R., SMITZ, J. VAN STEIRTEGHEM, A.C., Assesment of the need for follicle stimulating hormone in early preantral mouse follicle culture in vitro. Human Reprod. 12, DERRAR, N., PRICE, C.A., SIRARD, M.A., Effect of growth factors and co-culture with ovarian medulla on the activation of primordial follicles in explants of bovine ovarian cortex. Theriogenology. 54, DUFOUR, J.; CAHILL, L.P.; MAULEON, P., Short and long-term effects of hypophysectomy and unilateral ovariectomy on populations follicular in sheep. J. Reprod. Fert. 7, EDWARDS, R.G., FOWLER, R.E., GORE-LANGTON, R.E., GOSDEN, R.G., JONES, E.C., READHEAD, C.,,STEPTOE, C., Normal and abnormal follicular growth in mouse, rat and human ovaries. J. Reprod. Fertil. 51, ELVIN, J.A., YAN, C.N., WANG,, NISHIMORI, K., MATZUK, M.M., Molecular characterisation of the follicle defects in the growth differentiation factor 9-deficient ovary. Mol. Endocrinol. 13, FADDY, M. J., GOSDEN, R. G., GOUGEON, A, RICHARDSON, S. J., NELSON, J. F., Accelerated disappearance of ovarian follicle sinmid-life:implications for fore casting menopause. Human Reprod. 7, FLAWS, J.A., ABBUD, R., MANN, R.J., NILSON, J.H., HIRSHFIELD, A.N., Chronically elevated luteinizing hormone depletes primordial follicles in the mouse ovary. Biol. Reprod. 57,
34 FORTUNE, J.E., KITO, S, WANDJI, S.A. & SRSEN., Activation of Bovine and Baboon Primordial Follicles in vitro. Theriogenology. 49, FUKU, E., XIA, L., DOWNEY, B.R., Ultrastructural changes in bovine oocytes cryopreserved by vitrification. Cryobiology. 32, GREENWALD, G.S., MOOR, R.M., Isolation and preliminary characterization of pig primordial follicles. J. Reprod. Fert. 87, p ITOH, T., KACCHI, M., ABE, H., SENDAI, Y., HOSHI, H., 2002.Growth, antrum formation, and estradiol production of bovine preantral follicles cultured in a serum-free medium. Biol. Reprod. 67, JORIO, A., MARIANA, J.C., LAHLOU-KASSI, A.,1991. Development of the population of ovarian follicles during the prepubertal period in D man and Timahdit shee. J. Reprod. Fert. 26, KLINGER, F.G., DE FELICI, M., In vitro development of growing oocytes from fetal mouse oocytes: Stage-specific regulation by stem cell factor and granulosa cells. Dev. Biol. 244, LIU, H.C., ZHIYING, H., ROSENWAKS, Z., In vitro culture and in vitro maturation of mouse preantral follicles with recombinant gonadotropins. Fert. Ster. 77, LUCCI, C.M., SILVA, R. CARVALHO, C.A., FIGUEIREDO, R., BÁO, N., Light microscopical and ultrastrutural characterization of goat preantral follicles. Small Rum. Res. 41, MARCUS, M., GRUNFELD, L., BERKOWITZ, G., KAPLANP GODBOLD J., Urinaryfollicle-stimulating hormone as a biological marker of ovarian toxicity. Fert. Ster. 59, MATOS, M.H.T., LIMA-VERDE, I.B., LUQUE, M.C.A., MAIA Jr, J.E., SILVA, J.R., CELESTINO, J.J.H., MARTINS, F.S., BÁO, S.N., LUCCI, A.M., FIGUEIREDO, J.R., 50
35 2007. Essential role of follicle stimulating hormone in the maintenance of caprine preantral follicle viability in vitro. Zygote. 15, McFARLAND, K.C, SPRENGEL, R., PHILLIPS, H.S., KOHLER, M., ROSEMBLIT, N., NIKOLICS, K., SEGALOFF, D.L., SEEBURG, H., Lutropin-choriogonadotropin receptor: an usual member of the G protein-coupled receptor family. Science. 245, MÉDURI, G., CHARNAUX, N., DRIANCOURT, M.A., COMBETTES, L., GRANET,, VANNIER, B., LOOSFELT, H., MIGROM. E., Follicle-stimulating hormone receptors in oocytes? The Journal of Clinical. Endocrinol. Metabol. 87, OKTAY, K., BRIGGS, D., GOSDE, R.G., Ontogeny of follicle-stimulating hormone receptor gene expression in isolated human ovarian follicles. Journal Clinic Endocrinol. Metabol. 82, O SHAUGHNESSY, J., McLELLAND, D., McBRIDE, M.W., Regulation of Luteinizing Hormone Receptor and Follicle-Stimulanting Hormone-Receptor messenger ribonucleic acid levels during development in the neonatal mouse ovarian. Biol. Reprod. 57, PERKINS, G.A., FREY, T.G., Recent structural insight into mitochondria gained by microscope. Micron. 31, REITER, E., McNAMARA. M., CLOSSET. J., HENNEN. G., Expression and functionality of luteinizing hormone/chorionic gonadotrophin receptor in the rat prostate. Endocrinology. 136, RESHEF, E., LEI, Z.M., RAO, C., PRIDHAM, D.D. CHEGINI, N., LUBORSKY, J.L., The presence of gonadotrophin receptors in non-pregnant human uterus, human placenta, fetal membranes and deciduas. J. Clin. Endocrinol. Metabol. 70,
36 RICHARDSON, S. J., SENIKAS, A., NELSON, J. E., Follicular depletion during themenopausal transition: evidence for accelerated loss and ultimate exhaustion. J. Clin. Endocrinol. Metabol. 65, p ROY, S.K., TERADA, D.M., Actives of glucose metabolic enzymes in human preantral follicles: In vitro modulation by Follicle-Stimulating Hormone, Luteinizing Hormone, Epidermal Growth Factor, Insulin-Like Growth Factor 1, and Transforming Growth Factor α1. Biol. Reprod. 60, SEGALOFF, D.L., Regulation of the LH receptor in the ovary during follicular development. In: FILICORE, M., FLAMIGNI, C. Editors. The ovary: Regulation, dysfunction and treatment. Amsterdã: Elsevier SHERMAN, B. M., WEST, J. H., KORENMAN, S. G.,1976. The menopausal transition:analysis of LH, FSH, estradiol, and progesterone concentrations during menstrual cycles of older women. J. Clin. Endocrinol. Metabol. 42, SILVA, J.R., BAO, S.N., LUCCI, C.M., CARVALHO, F.C., ANDRADE, E.R. FERREIRA, M.A., FIGUEIREDO, J.R., Morphological and ultrastructural changes occurring during degeneration of goat preantral follicles preserved in vitro. Anim. Reprod. Scien. 66, SILVA, J.R.V, FERREIRA, M.A.L., COSTA, S.H.F., SANTOS, R.R., CARVALHO, F.C.A, RODRIGUES, A.R., LUCCI, C.M., BÁO, S.N., FIGUEIREDO, J.R., Degeneration rate of preantral follicles in the ovaries of goats. Small Rumin. Res., 43: SILVA, J. R., VAN DEN HURK, R., MATOS, M. H. T., SANTOS, R. R., PESSOA, C., MORAED, M. O., FIGUEIREDO, J. R., Influences of FSH and EGF on primordial follicles during in vitro culture of caprine ovarian cortical tissue. Theriogenology. 61,
37 SIMPLÍCIO, A.A., Reproduction in three native genotypes of goats under two feeding management systems in northeast Brazil, and progesterone and Luteinizing hormone profiles during the estrous cycle and seasonal anestrus in Spanish goats in the United States. Dissertation of Doctor Philosophy, Utah State University, Logan-Utah, XII. STEEL, R. G. D., TORRIE, J. H., DICKEY, D., A. Principles and procedures of statistics: a biometrical approach. 3 rd Ed. McGraw-Hill, New York, NY, 666p. THOMAS, F.H., ETHIER, J.-F., SHIMASAKI, S., VANDERHYDEN, B.C., Folliclestimulating hormone regulates oocyte growth by modulation of expression of oocyte and granulosa cell factors. Endocrinology. 146, ULLOA-AGUIRRE, A., MIDGLEY, A.R. JR., BEITINS, I.Z., PADMANABHAN, Follicle-stimulating isohormones: characterization and physiological relevance. Endocr. Rev. 16, VAN WEZEL, I., RODGERS, R.J., Morphological characterization of primordial follicles and their environment in vivo. Biol. Reprod. 55, VITT, U.A., HAYASHI, M., KLEIN, C., HSUEH, A.J., Growth differentiation factor-9 stimulates proliferation but suppresses the follicle- stimulating hormone- induced differentiation of cultured granulosa cells from small antral and preovulatory rat follicles. Biol. Reprod. 62, WRIGHT, C.S., HOVATTA, O., MARGARA, R., TREW, G, WINSTON, R.M.L., FRANKS, S., HARDY, K., Effects of follicle-stimulating hormone and serum substitution on the in-vitro growth of human ovarian follicles. Human Reprod. 14, WU, J.,NAYUDU, L., KIESEL, S., MICHELMANN, H.W., Luteinizing Hormone has a stage-limited effect on preantral follicle development in vitro. Biol. Reprod. 63,
38 XU, Z., GARVERICK, A., SMITH, G.W., SMITH, M.F., AMILTON, S.A., YOUNQUIST, R., Expression of Follicle Stimulating Hormone and Luteinizing hormone receptor messenger Ribonucleic Acids in bovine follicles during the first follicular wave. Biol. Reprod. 53, YAMOTO, M., SHIMA, K., NAKANO, R., Gonadotrophin receptors in human ovarian follicles and corporea lutea throughout the menstrual cycle. Horm. Res. 37, ZELEZNICK, A.J., HILLIER, S.G., The role of goadotrophins in the selection of the preovulatory follicle. Clin. Obst. Ginecol. 27, ZELEZNICK, A.J., MIDGLEY, A.R., REICHERT, L.E., Granulosa cell maturation in the rat: increased binding of human chorionic gonadotrophin following treatment with follicle-stimulating hormone in vivo. Endocrinology. 95, Table 1. Percentages of primordial or developing follicles in non-cultured tissue (day 0) and in tissues cultured in MEM alone or supplemented with diffferent concentrations of LH (1, 5, 10, 50 or 100 ng/ml) for 1 and 7 days. % Primordial follicles % Growing follicles Treatments Day 1 Day 7 Day 1 Day 7 Control -day 0 44,21 55,26 MEM 34,21 Aa 30,91 Aa 65,79 Aa 69,09 Aa LH 1 34,42 Aa 43,64 Aa 65,57 Aa 56,369 Aa LH 5 38,30 Aa 28,57 Aa 61,70 Aa 71,43 Aa LH 10 25,49 Aa* 17,39 Ba* 74,51 Aa* 82,61 Ba* LH 50 37,04 Aa 11,76 Bb* 62,96 Ab 88,24 Ba* LH ,56 Aa 5,00 Bb* 69,44 Ab 95,00 Ba* * Differs significantly from control A, B Different letters denote significant differences from MEM (Test of X 2 P<0,05) a, b Different letters denote significant differences between culture periods (Test of X 2 P<0,05) 54
39 Table 2. Percentages of primordial or developing follicles in non-cultured tissue (day 0) and in tissues cultured in MEM alone or supplemented with FSH or FSH associated with diffferent concentrations of LH (1, 5, 10 or 50 ng/ml) for 1 and 7 days. % Primordial follicles % Growing follicles Treatments Day 1 Day 7 Day 1 Day 7 Control -day 0 55,70 44,33 MEM 83,46Aa* 31,42Ab* 16,54 Ab* 68,57 Aa* FSH 36,14Ba* 32,31Aa* 63,86 Ba* 67,69 Aa* FSH + LH 1 32,88Ba* 21,21Aa* 67,12 Ba* 78,79 Aa* FSH + LH 5 32,91Ba* 20,00Aa* 67,09 Ba* 80,00 Aa* FSH + LH 10 50,00Ba 26,00Ab* 50,00 Bb 74,00 Aa* FSH + LH 50 30,23Ba* 26,08Aa* 69,76 Ba* 73,91 Aa* * Differs significantly from control A, B Different letters denote significant differences from MEM (Test of Dunnett; P<0,05) a, b Different letters denote significant differences between culture periods (Test t of Student; P<0,05) Table 3. Follicle and oocyte diameters in non-cultured tissue (day 0) and in tissues cultured in MEM alone or supplemented with diffferent concentrations of LH (1, 5, 10, 50 or 100 ng/ml) for 1 and 7 days. Oocyte diameter (µm) Follicle diameter (µm) Treatments Day 1 Day 7 Day 1 Day 7 Control - day 0 38,01 ± 6,02 50,98 ± 8,56 MEM 39,09 ± 5,33 Aa 42,80 ± 6,97 Aa 49,11 ± 4,93 Ab 57,83 ± 6,23 Aa LH 1 38,47 ± 6,14 Ab 46,04 ± 6,48 Aa* 54,48 ± 7,30 Ab 71,69 ± 7,47 Ba* LH 5 40,48 ± 5,39 Ab 48,41 ± 7,11 Aa* 54,89 ± 5,83 Ab 68,91 ± 9,98 Ba* LH 10 42,18 ± 6,67 Ab 47,43 ± 8,16 Aa* 54,69 ± 8,69 Ab 63,50 ± 7,26 Aa* LH 50 42,45 ± 6,74 Aa 41,87 ± 6,61 Aa 55,23 ± 7,30 Aa 62,42 ± 8,12 Aa* LH ,78 ± 5,62 Aa 42,33 ± 5,85 Aa 53,61 ± 7,72 Aa 58,25 ± 7,91 Aa* * Differs significantly from control A, B Different letters denote significant differences from MEM (Test of Dunnett; P<0,05) a, b Different letters denote significant differences between culture periods (Test t of Student; P<0,05) 55
40 Table 4. Follicle and oocyte diameters in non-cultured tissue (day 0) and in tissues cultured in MEM alone or supplemented with FSH and FSH with diffferent concentrations of LH (1, 5, 10 or 50 ng/ml) for 1 and 7 days. Oocyte diameter (µm) Follicle diameter (µm) Treatments Day 1 Day 7 Day 1 Day 7 Control - day 0 40,63 ±6,97 53,46 ± 9,30 MEM 41,25 ± 6,04 Aa 44,03 ± 7,22 Aa 55,46 ± 6,83 Aa 59,64 ± 7,84 Aa FSH 40,48 ± 5,29 Aa 43,10 ± 6,38 Aa 56,55 ± 7,30 Aa 61,34 ± 10,09 Aaβ* FSH + LH 1 39,40 ± 6,64 Ab 45,89 ± 6,82 Aa 56,39 ± 8,26 Ab 70,45 ± 7,67 Baα* FSH + LH5 42,02 ± 5,88 Ab 46,35 ± 4,69 Aa 56,70 ± 7,04 Ab 69,37 ± 9,64 Baα* FSH + LH 10 42,18 ± 6,67 Ab 45,66 ± 5,86 Aa 54,69 ± 8,69 Ab 64,58 ± 7,89 Aaβ* FSH + LH 50 43,26 ± 7,50 Aa 42,18 ± 6,36 Aa 58,40 ± 9,18 Aa 62,57 ± 8,20 Aaβ* * Differs significantly from control A,B Different letters denote significant differences from MEM (Test of Dunnett; P<0,05) a, b Different letters denote significant differences between culture periods (Teste t of Student; P<0,05) α, β Different letters denote significant differences from MEM (Test of Dunnett; P<0,05) Table 5. Percentages of morphologically normal follicles in non-cultured tissue (day 0) and in tissues cultured in MEM alone or supplemented with diffferent concentrations of LH (1, 5, 10, 50 or 100 ng/ml) for 1 and 7 days. % Normal follicles Treatments Day 1 Day 7 Control -day 0 65,90 ± 4,22 MEM 59,95 ± 6,70 Aa 33,32 ± 6,55 Ab* LH1 56,63 ± 5,77 Aa 30,60 ± 9,88 Aa* LH5 39,97 ± 8,18 Ba* 14,00 ± 6,52 Bb* LH10 38,87 ± 5,09 Ba* 17,02 ± 5,48 Bb* LH50 37,77 ± 6,92 Ba* 12,80 ± 7,39 Bb* LH100 29,37 ± 10,87 Ba* 15,36 ± 6,82 Ba* * Differs significantly from control A,B Different letters denote significant differences from MEM (Test of Dunnett; P<0,05) a, b Different letters denote significant differences between culture periods (Teste tof Student; P<0,05) 56
41 Table 6. Percentages of morphologically normal follicles in non-cultured tissue (day 0) and in tissues cultured in MEM alone or supplemented with FSH and diffferent concentration of LH (1, 5, 10 or 50 ng/ml) for 1 and 7 days. % Normal follicles Treatments Day 1 Day 7 Control -day 0 77,6 MEM 78,39 Aa 57,85 Ab* FSH 68,60 Aa 54,17 Ab* FSH + LH1 59,84 Ba* 54,10 Ab* FSH + LH5 64,23 Ba* 50,00 Ab* FSH + LH10 56,20 Ba* 40,98 Bb* FSH + LH50 37,39 Ba* 40,00 Ba* * Differs significantly from control A,B Different letters denote significant differences from MEM (Test of Dunnett; (Test of Dunnett; P<0,05) a, b Different letters denote significant differences between culture periods (Test t of Student; P<0,05) GC O Nu Nu O GC A B Figure 1. Histologically normal (A) and (B) degenerated follicles after in vitro culture (400x). O: oocyte; Nu: nucleus; GC: granulosa cell; 57
42 Nu O GC M Nu GC B A GC ER O O GC C C DD Figure 2: Electron micrography of follicles before and after 7 days culture (A) Normal follicle from day 0 (non-cultured control) (10000x); (B) normal follicle after culture in medium containing 1 ng/ml LH (8000x); (C) or FSH plus 1 ng/ml LH (15000x) and (D) degenerated follicles after 7 days culture in medium supplemented with FSH and 5 ng/ml LH (5000x). O: oocyte; Nu: nucleu; GC: granulosa cell; M: mitochondria; ER: endoplasmic reticulum. 58
EFEITO DO TIPO DE SISTEMAS DE CULTIVO NO DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS CAPRINOS ISOLADOS
 1 EFEITO DO TIPO DE SISTEMAS DE CULTIVO NO DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS CAPRINOS ISOLADOS EFFECT OF TYPE OF CULTURE SYSTEM ON THE IN VITRO DEVELOPMENT OF ISOLATED CAPRINE PREANTRAL
1 EFEITO DO TIPO DE SISTEMAS DE CULTIVO NO DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS CAPRINOS ISOLADOS EFFECT OF TYPE OF CULTURE SYSTEM ON THE IN VITRO DEVELOPMENT OF ISOLATED CAPRINE PREANTRAL
GAMETOGÊNESE DIFERENCIAÇÃO DOS GAMETAS. Profª Msc. Tatiane da Silva Poló
 GAMETOGÊNESE DIFERENCIAÇÃO DOS GAMETAS Profª Msc. Tatiane da Silva Poló ou OOGÊNESE ou OVULOGÊNESE e FOLICULOGÊNESE DEFINIÇÃO OVOGÊNESE: É uma sequência de eventos através dos quais as células germinativas
GAMETOGÊNESE DIFERENCIAÇÃO DOS GAMETAS Profª Msc. Tatiane da Silva Poló ou OOGÊNESE ou OVULOGÊNESE e FOLICULOGÊNESE DEFINIÇÃO OVOGÊNESE: É uma sequência de eventos através dos quais as células germinativas
Eixo hipotalamico-hipofisario-gonadal na femea Funcoes dos hormonios Organizacao das gonadas e desenvolvimento folicular Ciclo estral da vaca
 Topicos Eixo hipotalamico-hipofisario-gonadal na femea Funcoes dos hormonios Organizacao das gonadas e desenvolvimento folicular Ciclo estral da vaca Fertilizacao e desenvolvimento embrionario Cerebro
Topicos Eixo hipotalamico-hipofisario-gonadal na femea Funcoes dos hormonios Organizacao das gonadas e desenvolvimento folicular Ciclo estral da vaca Fertilizacao e desenvolvimento embrionario Cerebro
SISTEMA REPRODUTOR FEMININO
 Universidade Estadual do Ceará Faculdade de Veterinária SISTEMA REPRODUTOR FEMININO Histologia e Embriologia Geral Veterinária Profa. Janaina Serra Azul Monteiro Evangelista SISTEMA REPRODUTOR FEMININO
Universidade Estadual do Ceará Faculdade de Veterinária SISTEMA REPRODUTOR FEMININO Histologia e Embriologia Geral Veterinária Profa. Janaina Serra Azul Monteiro Evangelista SISTEMA REPRODUTOR FEMININO
O sistema reprodutor feminino. Os ovários e os órgãos acessórios. Aula N50
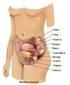 O sistema reprodutor feminino. Os ovários e os órgãos acessórios. Aula N50 Sistema reprodutor feminino Ovários = produz óvulos Tubas uterinas = transportam e protegem os óvulos Útero = prove meio adequado
O sistema reprodutor feminino. Os ovários e os órgãos acessórios. Aula N50 Sistema reprodutor feminino Ovários = produz óvulos Tubas uterinas = transportam e protegem os óvulos Útero = prove meio adequado
Produção in vitro de embriões ovinos
 NUPEEC Núcleo de Pesquisa, Ensino e Extensão em Pecuária Produção in vitro de embriões ovinos Apresentadores: Mauri Mazurek Rodrigo C. de C. de Azambuja Orientação: Liziane Lemos Viana Small Ruminant Resarch
NUPEEC Núcleo de Pesquisa, Ensino e Extensão em Pecuária Produção in vitro de embriões ovinos Apresentadores: Mauri Mazurek Rodrigo C. de C. de Azambuja Orientação: Liziane Lemos Viana Small Ruminant Resarch
Bloco X- Testes- Células germinativas
 Bloco X- Testes- Células germinativas 1) Das células progenitoras dos gametas podemos afirmar: I. São haplóides e migram para as gônadas em desenvolvimento II. São chamadas células germinativas primordiais
Bloco X- Testes- Células germinativas 1) Das células progenitoras dos gametas podemos afirmar: I. São haplóides e migram para as gônadas em desenvolvimento II. São chamadas células germinativas primordiais
hormônios do sistema genital masculino gônadas masculinas
 Gônadas masculinas Os hormônios do sistema genital masculino são produzidos nas gônadas masculinas, muito conhecidas como testículos. São os hormônios que determinam as características sexuais secundárias,
Gônadas masculinas Os hormônios do sistema genital masculino são produzidos nas gônadas masculinas, muito conhecidas como testículos. São os hormônios que determinam as características sexuais secundárias,
Fisiologia da Reprodução
 Texto de Referência Fisiologia da Reprodução Conhecimentos de anatomia e fisiologia são imprescindíveis para o Médico Veterinário que pretende trabalhar de forma correta e tirar o máximo proveito da técnica
Texto de Referência Fisiologia da Reprodução Conhecimentos de anatomia e fisiologia são imprescindíveis para o Médico Veterinário que pretende trabalhar de forma correta e tirar o máximo proveito da técnica
BIOLOGIA. Moléculas, Células e Tecidos Gametogênese. Prof. Daniele Duó
 BIOLOGIA Moléculas, Células e Tecidos https://www.qconcursos.com Prof. Daniele Duó - A reprodução sexuada começa com a formação dos gametas, denominado gametogênese. espermatogênese ovulogênese ou ovogênese
BIOLOGIA Moléculas, Células e Tecidos https://www.qconcursos.com Prof. Daniele Duó - A reprodução sexuada começa com a formação dos gametas, denominado gametogênese. espermatogênese ovulogênese ou ovogênese
Produção in vitro de embriões
 Universidade Estadual do Ceará Faculdade de Veterinária Programa de Pós-Graduação em Ciências Veterinárias Biotécnicas Aplicadas à Reprodução de Fêmeas Caprinas e Ovinas Produção in vitro de embriões Vicente
Universidade Estadual do Ceará Faculdade de Veterinária Programa de Pós-Graduação em Ciências Veterinárias Biotécnicas Aplicadas à Reprodução de Fêmeas Caprinas e Ovinas Produção in vitro de embriões Vicente
Aparelho Reprodutor Feminino
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Aparelho Reprodutor Feminino Prof. Msc. Macks Wendhell Gonçalves mackswenedhell@gmail.com É formado por: Parte interna: - Dois ovários
Pontifícia Universidade Católica de Goiás Departamento de Biologia Aparelho Reprodutor Feminino Prof. Msc. Macks Wendhell Gonçalves mackswenedhell@gmail.com É formado por: Parte interna: - Dois ovários
Regulação da foliculogênese e determinação da taxa de ovulação em ruminantes
 Universidade Federal de Pelotas Núcleo de Pesquisa, Ensino e Extensão em Pecuária Regulação da foliculogênese e determinação da taxa de ovulação em ruminantes Lucas Hax e Patrícia Mattei Pelotas, 18 de
Universidade Federal de Pelotas Núcleo de Pesquisa, Ensino e Extensão em Pecuária Regulação da foliculogênese e determinação da taxa de ovulação em ruminantes Lucas Hax e Patrícia Mattei Pelotas, 18 de
ENDOCRINOLOGIA REPRODUTIVA. M. V. Doutorando Lucas Balinhas Farias
 ENDOCRINOLOGIA REPRODUTIVA M. V. Doutorando Lucas Balinhas Farias Anatomia do sistema reprodutivo feminino Genitália externa, vagina, cérvix, útero, ovidutos e ovários Maturidade Sexual É representada
ENDOCRINOLOGIA REPRODUTIVA M. V. Doutorando Lucas Balinhas Farias Anatomia do sistema reprodutivo feminino Genitália externa, vagina, cérvix, útero, ovidutos e ovários Maturidade Sexual É representada
Competência Oocitária
 Universidade Federal de Pelotas Núcleo de Pesquisa, Ensino e Extensão em Pecuária Laboratório de Reprodução Animal -EMBRAPA Competência Oocitária Lucas Hax Médico Veterinário Doutorando em Biotecnologia
Universidade Federal de Pelotas Núcleo de Pesquisa, Ensino e Extensão em Pecuária Laboratório de Reprodução Animal -EMBRAPA Competência Oocitária Lucas Hax Médico Veterinário Doutorando em Biotecnologia
UNIVERSIDADE ESTADUAL DO CEARÁ FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS JAMILY BEZERRA BRUNO
 UNIVERSIDADE ESTADUAL DO CEARÁ FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS JAMILY BEZERRA BRUNO UTILIZAÇÃO DE SORO NO CULTIVO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS CAPRINOS
UNIVERSIDADE ESTADUAL DO CEARÁ FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS JAMILY BEZERRA BRUNO UTILIZAÇÃO DE SORO NO CULTIVO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS CAPRINOS
INFLUÊNCIA DA ORIGEM E PUREZA DO HORMÔNIO FOLÍCULO ESTIMULANTE (FSH) NA SOBREVIVÊNCIA E NO DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS CAPRINOS
 INFLUÊNCIA DA ORIGEM E PUREZA DO HORMÔNIO FOLÍCULO ESTIMULANTE (FSH) NA SOBREVIVÊNCIA E NO DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS CAPRINOS 1 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO
INFLUÊNCIA DA ORIGEM E PUREZA DO HORMÔNIO FOLÍCULO ESTIMULANTE (FSH) NA SOBREVIVÊNCIA E NO DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS CAPRINOS 1 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO
GAMETOGÊNESE. Processo de formação e desenvolvimento das células germinativas especializadas OS GAMETAS.
 GAMETOGÊNESE 1 GAMETOGÊNESE Processo de formação e desenvolvimento das células germinativas especializadas OS GAMETAS. Gameta masculino Espermatozóide. Gameta feminino Ovócito. Os gametas possuem metade
GAMETOGÊNESE 1 GAMETOGÊNESE Processo de formação e desenvolvimento das células germinativas especializadas OS GAMETAS. Gameta masculino Espermatozóide. Gameta feminino Ovócito. Os gametas possuem metade
ENDOCRINOLOGIA DA REPRODUÇÃO. Elisângela Mirapalheta Madeira Medica Veterinária, MC
 ENDOCRINOLOGIA DA REPRODUÇÃO Elisângela Mirapalheta Madeira Medica Veterinária, MC Introdução Glândulas Endócrinas Hipotálamo Hipófise Gônadas Glândula pineal Glândulas Endócrinas Hipotálamo Glândulas
ENDOCRINOLOGIA DA REPRODUÇÃO Elisângela Mirapalheta Madeira Medica Veterinária, MC Introdução Glândulas Endócrinas Hipotálamo Hipófise Gônadas Glândula pineal Glândulas Endócrinas Hipotálamo Glândulas
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS
 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS GIOVANNA QUINTINO RODRIGUES EFEITO DE DIFERENTES CONCENTRAÇÕES
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS GIOVANNA QUINTINO RODRIGUES EFEITO DE DIFERENTES CONCENTRAÇÕES
UNIVERSIDADE ESTADUAL DO CEARÁ-UECE FACULDADE DE VETERINÁRIA-FAVET PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS- PPGCV
 1 UNIVERSIDADE ESTADUAL DO CEARÁ-UECE FACULDADE DE VETERINÁRIA-FAVET PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS- PPGCV PATRÍCIA MAGALHÃES DE ANDRADE EFEITO DOS MEIOS DE CULTIVO DE BASE α-mem E
1 UNIVERSIDADE ESTADUAL DO CEARÁ-UECE FACULDADE DE VETERINÁRIA-FAVET PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS- PPGCV PATRÍCIA MAGALHÃES DE ANDRADE EFEITO DOS MEIOS DE CULTIVO DE BASE α-mem E
SANELY LOURENÇO DA COSTA CALIMAN
 SANELY LOURENÇO DA COSTA CALIMAN hfsh, T4 E IGF-I NO DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS CAPRINOS Tese apresentada à Universidade Federal de Viçosa, como parte das exigências do Programa
SANELY LOURENÇO DA COSTA CALIMAN hfsh, T4 E IGF-I NO DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS CAPRINOS Tese apresentada à Universidade Federal de Viçosa, como parte das exigências do Programa
ENDOCRINOLOGIA REPRODUTIVA. M.S. Cássio Cassal Brauner FAEM-UFPel
 ENDOCRINOLOGIA REPRODUTIVA M.S. Cássio Cassal Brauner Prof. DZ-FAEM FAEM-UFPel ENDOCRINOLOGIA REPRODUTIVA Endocrinologia é parte das ciências médicas que trata da secreção das glândulas internas (hormônios)
ENDOCRINOLOGIA REPRODUTIVA M.S. Cássio Cassal Brauner Prof. DZ-FAEM FAEM-UFPel ENDOCRINOLOGIA REPRODUTIVA Endocrinologia é parte das ciências médicas que trata da secreção das glândulas internas (hormônios)
Interação dos mecanismos fisiológicos que influenciam a fertilidade em vacas leiteiras
 Ministério da Educação Universidade Federal de Pelotas Faculdade de Medicina Veterinária Núcleo de Ensino, Pesquisa e Extensão em Pecuária-NUPEEC Interação dos mecanismos fisiológicos que influenciam a
Ministério da Educação Universidade Federal de Pelotas Faculdade de Medicina Veterinária Núcleo de Ensino, Pesquisa e Extensão em Pecuária-NUPEEC Interação dos mecanismos fisiológicos que influenciam a
CAMILA BIZARRO DA SILVA
 CENTRO DE PESQUISA EM CIÊNCIAS AGRÁRIAS MESTRADO EM SAÚDE E PRODUÇÃO DE RUMINANTES CAMILA BIZARRO DA SILVA EFEITO DE DIFERENTES CONCENTRAÇÕES DO HORMÔNIO FOLÍCULO ESTIMULANTE (FSH) NO SISTEMA DE CULTIVO
CENTRO DE PESQUISA EM CIÊNCIAS AGRÁRIAS MESTRADO EM SAÚDE E PRODUÇÃO DE RUMINANTES CAMILA BIZARRO DA SILVA EFEITO DE DIFERENTES CONCENTRAÇÕES DO HORMÔNIO FOLÍCULO ESTIMULANTE (FSH) NO SISTEMA DE CULTIVO
ANÁLISE MORFOLÓGICA E ULTRAESTRUTURAL DE FOLÍCULOS PRIMORDIAIS OVINOS CONSERVADOS EM SOLUÇÃO SALINA 0,9% E TCM
 Universidade Estadual do Ceará Pró-Reitoria de Pós-Graduação e Pesquisa Faculdade de Veterinária Programa de Pós-Graduação em Ciências Veterinárias Maria Helena Tavares de Matos ANÁLISE MORFOLÓGICA E ULTRAESTRUTURAL
Universidade Estadual do Ceará Pró-Reitoria de Pós-Graduação e Pesquisa Faculdade de Veterinária Programa de Pós-Graduação em Ciências Veterinárias Maria Helena Tavares de Matos ANÁLISE MORFOLÓGICA E ULTRAESTRUTURAL
Sistema Reprodutor Feminino. Acadêmica de Veterinária Carolina Wickboldt Fonseca
 Sistema Reprodutor Feminino Acadêmica de Veterinária Carolina Wickboldt Fonseca Introdução Apresento este trabalho sobre o Sistema Reprodutor Feminino (SRF), histologicamente, descrevendo algumas estruturas
Sistema Reprodutor Feminino Acadêmica de Veterinária Carolina Wickboldt Fonseca Introdução Apresento este trabalho sobre o Sistema Reprodutor Feminino (SRF), histologicamente, descrevendo algumas estruturas
Gametogênese Ovogênese. Prof a. Marta G. Amaral, Dra. Embriologia molecular
 Gametogênese Ovogênese Prof a. Marta G. Amaral, Dra. Embriologia molecular Cél germinativa primordial (CGP) CGP Oogônias Inicia antes do nascimento Depois entra em repouso Na puberdade termina a diferenciação
Gametogênese Ovogênese Prof a. Marta G. Amaral, Dra. Embriologia molecular Cél germinativa primordial (CGP) CGP Oogônias Inicia antes do nascimento Depois entra em repouso Na puberdade termina a diferenciação
Interações hormonais relacionadas com a reprodução. Professor: Arturo Arnáez Vaella
 Interações hormonais relacionadas com a reprodução Professor: Arturo Arnáez Vaella 1. a paralisação (diplóteno) Fonte: Carlson, B. (2014). Embriologia humana e biologia do desenvolvimento (5 ed.) 1. a
Interações hormonais relacionadas com a reprodução Professor: Arturo Arnáez Vaella 1. a paralisação (diplóteno) Fonte: Carlson, B. (2014). Embriologia humana e biologia do desenvolvimento (5 ed.) 1. a
Efeito da desnutrição materna durante a gestação no desenvolvimento ovariano inicial e subsequente desenvolvimento folicular em fetos de ovelhas
 Universidade Federal de Pelotas Faculdade de Veterinária Núcleo de Pesquisa Ensino e Extensão em Pecuária Efeito da desnutrição materna durante a gestação no desenvolvimento ovariano inicial e subsequente
Universidade Federal de Pelotas Faculdade de Veterinária Núcleo de Pesquisa Ensino e Extensão em Pecuária Efeito da desnutrição materna durante a gestação no desenvolvimento ovariano inicial e subsequente
Divisão celular. A única situação em que dividir e multiplicar significam a mesma coisa
 Divisão celular A única situação em que dividir e multiplicar significam a mesma coisa Todos as células se dividem: 1. Em organismos unicelulares, divisão celular é o modo principal de reprodução 2. Em
Divisão celular A única situação em que dividir e multiplicar significam a mesma coisa Todos as células se dividem: 1. Em organismos unicelulares, divisão celular é o modo principal de reprodução 2. Em
NUPEEC. Núcleo de Pesquisa, Ensino e Extensão em Pecuária
 NUPEEC Núcleo de Pesquisa, Ensino e Extensão em Pecuária Fatores Parácrinos, Autócrinos e Endócrinos que Mediam a Influência da Nutrição na Reprodução em Bovinos e Suínos Journal of Animal Science 1996
NUPEEC Núcleo de Pesquisa, Ensino e Extensão em Pecuária Fatores Parácrinos, Autócrinos e Endócrinos que Mediam a Influência da Nutrição na Reprodução em Bovinos e Suínos Journal of Animal Science 1996
Universidade Federal de Pelotas Núcleo de Pesquisa, Ensino e Extensão em Pecuária
 Universidade Federal de Pelotas Núcleo de Pesquisa, Ensino e Extensão em Pecuária Efeito do ácido lisofosfatídico durante a maturação in vitro do complexo cumulus-oócito: expansão do cumulus, metabolismo
Universidade Federal de Pelotas Núcleo de Pesquisa, Ensino e Extensão em Pecuária Efeito do ácido lisofosfatídico durante a maturação in vitro do complexo cumulus-oócito: expansão do cumulus, metabolismo
A g r u p a m e n t o d e E s c o l a s A n t ó n i o S é r g i o V. N. G a i a E S C O L A S E C U N D Á R I A / 3 A N T Ó N I O S É R G I O
 A g r u p a m e n t o d e E s c o l a s A n t ó n i o S é r g i o V. N. G a i a E S C O L A S E C U N D Á R I A / 3 A N T Ó N I O S É R G I O BIOLOGIA Módulo 1 12º CTec CURSO CIENTÍFICO-HUMANÍSTICO DE
A g r u p a m e n t o d e E s c o l a s A n t ó n i o S é r g i o V. N. G a i a E S C O L A S E C U N D Á R I A / 3 A N T Ó N I O S É R G I O BIOLOGIA Módulo 1 12º CTec CURSO CIENTÍFICO-HUMANÍSTICO DE
SISTEMA REPRODUTOR FEMININO. Prof. Dr. José Gomes Pereira
 Prof. Dr. José Gomes Pereira 1. CONSIDERAÇÕES GERAIS 2. CONSTITUINTES 2.1. Ovários 2.2. Tubas Uterinas 2.3. Útero 2.4. Cérvix 2.5. Vagina 2.6. Vulva 2.7. Clitóris 2.8 Uretra Ovários Glândula Exócrina e
Prof. Dr. José Gomes Pereira 1. CONSIDERAÇÕES GERAIS 2. CONSTITUINTES 2.1. Ovários 2.2. Tubas Uterinas 2.3. Útero 2.4. Cérvix 2.5. Vagina 2.6. Vulva 2.7. Clitóris 2.8 Uretra Ovários Glândula Exócrina e
TALITA FERNANDES DA SILVA
 TALITA FERNANDES DA SILVA EFEITO DA SOMATOTROPINA RECOMBINANTE BOVINA (rbst) NO DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS DE BOVINOS Dissertação apresentada à Universidade Federal de Viçosa, como
TALITA FERNANDES DA SILVA EFEITO DA SOMATOTROPINA RECOMBINANTE BOVINA (rbst) NO DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS DE BOVINOS Dissertação apresentada à Universidade Federal de Viçosa, como
Diferenças metabólicas e endócrinas entre femêas Bos taurus e Bos indicus e o impacto da interação da nutrição com a reprodução
 Diferenças metabólicas e endócrinas entre femêas Bos taurus e Bos indicus e o impacto da interação da nutrição com a reprodução Apresentadores: Med. Vet. Andressa Stein Maffi Kauana Soares FI: 1,79 Qual
Diferenças metabólicas e endócrinas entre femêas Bos taurus e Bos indicus e o impacto da interação da nutrição com a reprodução Apresentadores: Med. Vet. Andressa Stein Maffi Kauana Soares FI: 1,79 Qual
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS
 1 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS ROBERTA NOGUEIRA CHAVES EFEITO DA TEMPERATURA E DO
1 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS ROBERTA NOGUEIRA CHAVES EFEITO DA TEMPERATURA E DO
VALDEVANE ROCHA ARAÚJO INFLUÊNCIA DA PROTEÍNA MORFOGENÉTICA ÓSSEA-7 (BMP-7) SOBRE O DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ- ANTRAIS CAPRINOS
 VALDEVANE ROCHA ARAÚJO INFLUÊNCIA DA PROTEÍNA MORFOGENÉTICA ÓSSEA-7 (BMP-7) SOBRE O DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ- ANTRAIS CAPRINOS FORTALEZA-CE 2008 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA
VALDEVANE ROCHA ARAÚJO INFLUÊNCIA DA PROTEÍNA MORFOGENÉTICA ÓSSEA-7 (BMP-7) SOBRE O DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ- ANTRAIS CAPRINOS FORTALEZA-CE 2008 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA
Biologia Celular e Molecular:
 Disciplina: Biologia Celular e Molecular: Prof.Dr. Antonio Augusto L. Barboza Diferenciação Celular EUCARIONTES Célula Animal Célula Vegetal Células procariontes Pobreza de membranas (somente a membrana
Disciplina: Biologia Celular e Molecular: Prof.Dr. Antonio Augusto L. Barboza Diferenciação Celular EUCARIONTES Célula Animal Célula Vegetal Células procariontes Pobreza de membranas (somente a membrana
UNIVERSIDADE FEDERAL DO VALE DO SÃO FRANCISCO CURSO DE PÓS-GRADUAÇÃO EM CIÊNCIA ANIMAL. Luciana da Paz dos Santos
 1 UNIVERSIDADE FEDERAL DO VALE DO SÃO FRANCISCO CURSO DE PÓS-GRADUAÇÃO EM CIÊNCIA ANIMAL Luciana da Paz dos Santos IMUNOLOCALIZAÇÃO DO FATOR DE CRESCIMENTO EPIDERMAL (EGF) EM OVÁRIOS OVINOS E SEU EFEITO
1 UNIVERSIDADE FEDERAL DO VALE DO SÃO FRANCISCO CURSO DE PÓS-GRADUAÇÃO EM CIÊNCIA ANIMAL Luciana da Paz dos Santos IMUNOLOCALIZAÇÃO DO FATOR DE CRESCIMENTO EPIDERMAL (EGF) EM OVÁRIOS OVINOS E SEU EFEITO
28/04/2010. Espermatozóides são formados e lançados no espaço do tubos. Tubos Seminíferos. Epidídimo. Testículo Células em divisão (mitose x meiose)
 GAMETOGÊNESE - -OVOGÊNESE gustavosimas@gmail.com Tubos Seminíferos Espermatozóides são formados e lançados no espaço do tubos Epidídimo Testículo Células em divisão (mitose x meiose) 1 EPIDÍDIMO (armazena
GAMETOGÊNESE - -OVOGÊNESE gustavosimas@gmail.com Tubos Seminíferos Espermatozóides são formados e lançados no espaço do tubos Epidídimo Testículo Células em divisão (mitose x meiose) 1 EPIDÍDIMO (armazena
GAMETOGÊNESE ESPERMATOGÊNESE OVOLUGÊNESE
 BIOLOGIA FRENTE A SÉRIE: 9º ANO GAMETOGÊNESE ESPERMATOGÊNESE OVOLUGÊNESE Profª. LUCIANA ARAUJO MEIOSE E GAMETAS É por meio da divisão meiótica que as células da linhagem germinativa fabricam os gametas,
BIOLOGIA FRENTE A SÉRIE: 9º ANO GAMETOGÊNESE ESPERMATOGÊNESE OVOLUGÊNESE Profª. LUCIANA ARAUJO MEIOSE E GAMETAS É por meio da divisão meiótica que as células da linhagem germinativa fabricam os gametas,
Inter-relações da nutrição, hormônios metabólicos e reinicio da ovulação em vacas de corte multíparas amamentando manejadas em pastagem subtropical
 Inter-relações da nutrição, hormônios metabólicos e reinicio da ovulação em vacas de corte multíparas amamentando manejadas em pastagem subtropical Apresentadores: Andressa Stein Maffi Tiago Garlet Pelotas,
Inter-relações da nutrição, hormônios metabólicos e reinicio da ovulação em vacas de corte multíparas amamentando manejadas em pastagem subtropical Apresentadores: Andressa Stein Maffi Tiago Garlet Pelotas,
O efeito das taxas de morte embrionária na eficiência de programas de sincronização de cio em vacas
 NUPEEC Núcleo de Pesquisa, Ensino e Extensão em Pecuária O efeito das taxas de morte embrionária na eficiência de programas de sincronização de cio em vacas Apresentadores: Andressa Stein Maffi Mauri Mazurek
NUPEEC Núcleo de Pesquisa, Ensino e Extensão em Pecuária O efeito das taxas de morte embrionária na eficiência de programas de sincronização de cio em vacas Apresentadores: Andressa Stein Maffi Mauri Mazurek
Coleta, Classificação e Maturação in vitrode Oócitos
 Universidade Federal de Pelotas Graduação em Biotecnologias Disciplina de Manipulação de Gametas e Embriões 2ª Aula: Coleta, Classificação e Maturação in vitrode Oócitos Priscila M. M. de Leon Doutoranda
Universidade Federal de Pelotas Graduação em Biotecnologias Disciplina de Manipulação de Gametas e Embriões 2ª Aula: Coleta, Classificação e Maturação in vitrode Oócitos Priscila M. M. de Leon Doutoranda
Reprodução. Biologia Ambiental Professora: Keffn Arantes
 Reprodução Biologia Ambiental Professora: Keffn Arantes GAMETAS E FECUNDAÇÃO NOS ANIMAIS *MEIOSE-significa diminuição. *Seres humanos têm 46 cromossomos nas células corporais. *Gametas apresentam
Reprodução Biologia Ambiental Professora: Keffn Arantes GAMETAS E FECUNDAÇÃO NOS ANIMAIS *MEIOSE-significa diminuição. *Seres humanos têm 46 cromossomos nas células corporais. *Gametas apresentam
ESTUDO DO DESENVOLVIMENTO FOLICULAR INICIAL E ATRESIA EM OVÁRIOS CAPRINOS
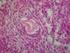 1 Universidade Estadual do Ceará José Roberto Viana Silva ESTUDO DO DESENVOLVIMENTO FOLICULAR INICIAL E ATRESIA EM OVÁRIOS CAPRINOS Fortaleza Ceará Agosto, 2004 2 Universidade Estadual do Ceará José Roberto
1 Universidade Estadual do Ceará José Roberto Viana Silva ESTUDO DO DESENVOLVIMENTO FOLICULAR INICIAL E ATRESIA EM OVÁRIOS CAPRINOS Fortaleza Ceará Agosto, 2004 2 Universidade Estadual do Ceará José Roberto
REGULAÇÃO DA PRODUÇÃO DO HORMÔNIO ANTI- MÜLLERIANO EM VACAS: UM ESTUDO COMPARATIVO EM NÍVEL ENDÓCRINO, OVARIANO, FOLÍCULAR E DE CÉLULAS DA GRANULOSA
 REGULAÇÃO DA PRODUÇÃO DO HORMÔNIO ANTI- MÜLLERIANO EM VACA: UM ETUDO COMPARATIVO EM NÍVEL ENDÓCRINO, OVARIANO, FOLÍCULAR E DE CÉLULA DA GRANULOA Douglas Peraoli & Francielle Bado Augusto chneider FI: 3.300
REGULAÇÃO DA PRODUÇÃO DO HORMÔNIO ANTI- MÜLLERIANO EM VACA: UM ETUDO COMPARATIVO EM NÍVEL ENDÓCRINO, OVARIANO, FOLÍCULAR E DE CÉLULA DA GRANULOA Douglas Peraoli & Francielle Bado Augusto chneider FI: 3.300
GÔNADAS = glândulas endócrinas com funções de sustentar o desenvolvimento e a maturação das células germinativas e sintetizar e secretar hormônios
 Fisiologia do Sistema Reprodutor Fisiologia do Sistema Reprodutor GÔNADAS = glândulas endócrinas com funções de sustentar o desenvolvimento e a maturação das células germinativas e sintetizar e secretar
Fisiologia do Sistema Reprodutor Fisiologia do Sistema Reprodutor GÔNADAS = glândulas endócrinas com funções de sustentar o desenvolvimento e a maturação das células germinativas e sintetizar e secretar
Universidade Federal do Amazonas ICB Dep. Morfologia Disciplina: Biologia Celular Aulas Teóricas
 Universidade Federal do Amazonas ICB Dep. Morfologia Disciplina: Biologia Celular Aulas Teóricas Noções básicas da Mitose e Meiose Ciclo Celular Noções básicas da Mitose e Meiose Ciclo Celular Fase S e
Universidade Federal do Amazonas ICB Dep. Morfologia Disciplina: Biologia Celular Aulas Teóricas Noções básicas da Mitose e Meiose Ciclo Celular Noções básicas da Mitose e Meiose Ciclo Celular Fase S e
ALLANA FERREIRA DA COSTA PESSOA
 1 UNIVERSIDADE ESTADUAL DO CEARÁ- UECE PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA- FAVET PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS-PPGCV ALLANA FERREIRA DA COSTA PESSOA
1 UNIVERSIDADE ESTADUAL DO CEARÁ- UECE PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA- FAVET PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS-PPGCV ALLANA FERREIRA DA COSTA PESSOA
Ciclo Reprodutivo Feminino Parte I. Embriogênese do aparelho reprodutor feminino e desenvolvimento puberal
 Ciclo Reprodutivo Feminino Parte I. Embriogênese do aparelho reprodutor feminino e desenvolvimento puberal Disciplina de Reprodução Humana Departamento de Ginecologia e Obstetrícia FMRP - USP Profa Dra
Ciclo Reprodutivo Feminino Parte I. Embriogênese do aparelho reprodutor feminino e desenvolvimento puberal Disciplina de Reprodução Humana Departamento de Ginecologia e Obstetrícia FMRP - USP Profa Dra
Gametogênese Prof. Dr. Philip Wolff Prof. Dr. Renato M. Salgado
 Prof. Dr. Philip Wolff Prof. Dr. Renato M. Salgado A gametogênese é o processo de produção dos gametas, as células reprodutoras. Esta produção ocorre nas gônadas e seu principal evento é a meiose, responsável
Prof. Dr. Philip Wolff Prof. Dr. Renato M. Salgado A gametogênese é o processo de produção dos gametas, as células reprodutoras. Esta produção ocorre nas gônadas e seu principal evento é a meiose, responsável
BIOLOGIA. Identidade dos Seres Vivos. Sistema Endócrino Humano Parte 2. Prof.ª Daniele Duó
 BIOLOGIA Identidade dos Seres Vivos Parte 2 https://www.qconcursos.com Prof.ª Daniele Duó Principais órgãos que constituem o sistema endócrino são: o o o o o o o Hipófise; Hipotálamo; Tireóide; Paratireóide;
BIOLOGIA Identidade dos Seres Vivos Parte 2 https://www.qconcursos.com Prof.ª Daniele Duó Principais órgãos que constituem o sistema endócrino são: o o o o o o o Hipófise; Hipotálamo; Tireóide; Paratireóide;
BIOLOGIA. Moléculas, células e tecidos. Gametogênese Parte 2. Professor: Alex Santos
 BIOLOGIA Moléculas, células e tecidos Parte 2 Professor: Alex Santos Tópicos em abordagem: Parte 2 Ovocitogênese: I A Ovocitogênese; II Quadro comparativo de gametogêneses; I Ovocitogênese: 1.1 Visão geral:
BIOLOGIA Moléculas, células e tecidos Parte 2 Professor: Alex Santos Tópicos em abordagem: Parte 2 Ovocitogênese: I A Ovocitogênese; II Quadro comparativo de gametogêneses; I Ovocitogênese: 1.1 Visão geral:
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS
 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS LARITZA FERREIRA DE LIMA UTILIZAÇÃO DO HORMÔNIO FOLÍCULO
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS LARITZA FERREIRA DE LIMA UTILIZAÇÃO DO HORMÔNIO FOLÍCULO
UNIVERSIDADE ESTADUAL DO CEARÁ FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS DOUTORADO EM CIÊNCIAS VETERINÁRIAS
 UNIVERSIDADE ESTADUAL DO CEARÁ FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS DOUTORADO EM CIÊNCIAS VETERINÁRIAS HUDSON HENRIQUE VIEIRA CORREIA CULTIVO IN VITRO DE OÓCITOS
UNIVERSIDADE ESTADUAL DO CEARÁ FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS DOUTORADO EM CIÊNCIAS VETERINÁRIAS HUDSON HENRIQUE VIEIRA CORREIA CULTIVO IN VITRO DE OÓCITOS
Biologia Celular. A Célula. Células 02/23/2008. Membrana Celular. Citoplasma. Eucariotes. Procariotes
 Biologia Celular Células Procariotes Procariotes são organismos unicelulares, presentes em todos os meios ambientes. Constituem o maior grupo de organismos da natureza, principalmente porque as bactérias
Biologia Celular Células Procariotes Procariotes são organismos unicelulares, presentes em todos os meios ambientes. Constituem o maior grupo de organismos da natureza, principalmente porque as bactérias
Resumo Sistema Reprodutor Feminino
 Resumo Sistema Reprodutor Feminino SISTEMA REPRODUTOR FEMININO FUNÇÕES OVÁRIOS 2 Ovários: produção de gametas femininos e maturação dessas células. 2 Tubas Uterinas: local de fecundação. Útero Vagina Produzir
Resumo Sistema Reprodutor Feminino SISTEMA REPRODUTOR FEMININO FUNÇÕES OVÁRIOS 2 Ovários: produção de gametas femininos e maturação dessas células. 2 Tubas Uterinas: local de fecundação. Útero Vagina Produzir
CÉLULAS. 8 ano Profª Elisete
 CÉLULAS 8 ano Profª Elisete Quanto ao número de células Os seres vivos podem ser: UNICELULARES apresentam uma única célula. Ex: bactérias e protozoários. PLURICELULARES apresentam mais células. Ex: seres
CÉLULAS 8 ano Profª Elisete Quanto ao número de células Os seres vivos podem ser: UNICELULARES apresentam uma única célula. Ex: bactérias e protozoários. PLURICELULARES apresentam mais células. Ex: seres
PROGRESSÃO MEIÓTICA NA MATURAÇÃO NUCLEAR IN VITRO DE OÓCITOS BOVINOS DE OVÁRIOS COM E SEM A PRESENÇA DE CORPO LÚTEO
 PROGRESSÃO MEIÓTICA NA MATURAÇÃO NUCLEAR IN VITRO DE OÓCITOS BOVINOS DE OVÁRIOS COM E SEM A PRESENÇA DE CORPO LÚTEO Janaina C. Medeiros FONSECA* 1, Leandro Polato LAZARI¹, Matheus montanari de SOUZA 1,
PROGRESSÃO MEIÓTICA NA MATURAÇÃO NUCLEAR IN VITRO DE OÓCITOS BOVINOS DE OVÁRIOS COM E SEM A PRESENÇA DE CORPO LÚTEO Janaina C. Medeiros FONSECA* 1, Leandro Polato LAZARI¹, Matheus montanari de SOUZA 1,
BIOSSÍNTESE DOS HORMÔNIOS (Protéicos) Estoque citoplasmático - secreção
 BIOSSÍNTESE DOS HORMÔNIOS (Protéicos) Estoque citoplasmático - secreção Exemplo HORMÔNIOS ESTEROIDES Sexuais e do tecido interrenal Outros tecidos Os esteroides estão envolvidos na regulação de vários
BIOSSÍNTESE DOS HORMÔNIOS (Protéicos) Estoque citoplasmático - secreção Exemplo HORMÔNIOS ESTEROIDES Sexuais e do tecido interrenal Outros tecidos Os esteroides estão envolvidos na regulação de vários
PROGRAMA DE PÓS-GRADUAÇÃO EM BIOLOGIA QUÍMICA Avaliação para obtenção de bolsa de mestrado/doutorado Capes 16 de Fevereiro de 2017.
 PROGRAMA DE PÓS-GRADUAÇÃO EM BIOLOGIA QUÍMICA Avaliação para obtenção de bolsa de mestrado/doutorado Capes 16 de Fevereiro de 2017 Identificação: ATENÇÃO: A prova vale 10,0 pontos e cada questão vale 2,0
PROGRAMA DE PÓS-GRADUAÇÃO EM BIOLOGIA QUÍMICA Avaliação para obtenção de bolsa de mestrado/doutorado Capes 16 de Fevereiro de 2017 Identificação: ATENÇÃO: A prova vale 10,0 pontos e cada questão vale 2,0
A Célula. A teoria celular, postulada por Schleiden e Schwann, assenta nos seguintes pressupostos:
 A Célula Teoria celular: A teoria celular, postulada por Schleiden e Schwann, assenta nos seguintes pressupostos: A célula é a unidade básica estrutural e funcional de todos os seres vivos (isto é, todos
A Célula Teoria celular: A teoria celular, postulada por Schleiden e Schwann, assenta nos seguintes pressupostos: A célula é a unidade básica estrutural e funcional de todos os seres vivos (isto é, todos
Doenças Metabólicas. Interação Metabolismo x Reprodução. Bruna Mion
 Doenças Metabólicas Interação Metabolismo x Reprodução Bruna Mion Interação Metabolismo x Reprodução Reprodução Processos fisiológicos Produção de leite Processos imunes Mantença Interação Metabolismo
Doenças Metabólicas Interação Metabolismo x Reprodução Bruna Mion Interação Metabolismo x Reprodução Reprodução Processos fisiológicos Produção de leite Processos imunes Mantença Interação Metabolismo
Reparação. Regeneração Tecidual 30/06/2010. Controlada por fatores bioquímicos Liberada em resposta a lesão celular, necrose ou trauma mecânico
 UNIVERSIDADE FEDERAL DO PARANÁ COORDENAÇÃO DO CURSO DE MEDICINA VETERINÁRIA DISCIPLINA DE PATOLOGIA VETERINÁRIA Reparação Prof. Raimundo Tostes Reparação Regeneração: reposição de um grupo de células destruídas
UNIVERSIDADE FEDERAL DO PARANÁ COORDENAÇÃO DO CURSO DE MEDICINA VETERINÁRIA DISCIPLINA DE PATOLOGIA VETERINÁRIA Reparação Prof. Raimundo Tostes Reparação Regeneração: reposição de um grupo de células destruídas
Produção in vitro de embriões
 Universidade Estadual do Ceará Faculdade de Veterinária Programa de Pós- Graduação em Ciências Veterinárias Biotécnicas Aplicadas à Reprodução de Fêmeas Caprinas e Ovinas Produção in vitro de embriões
Universidade Estadual do Ceará Faculdade de Veterinária Programa de Pós- Graduação em Ciências Veterinárias Biotécnicas Aplicadas à Reprodução de Fêmeas Caprinas e Ovinas Produção in vitro de embriões
CULTIVO DE FOLÍCULOS PRÉ-ANTRAIS
 INES CRISTINA GIOMETTI CULTIVO DE FOLÍCULOS PRÉ-ANTRAIS Botucatu 2 0 0 3 INES CRISTINA GIOMETTI CULTIVO DE FOLÍCULOS PRÉ-ANTRAIS Monografia apresentada à disciplina Seminários II, do Programa de Pós-graduação
INES CRISTINA GIOMETTI CULTIVO DE FOLÍCULOS PRÉ-ANTRAIS Botucatu 2 0 0 3 INES CRISTINA GIOMETTI CULTIVO DE FOLÍCULOS PRÉ-ANTRAIS Monografia apresentada à disciplina Seminários II, do Programa de Pós-graduação
Sistema Reprodutor Feminino
 Lâmina 72A: Ovário infantil e trompas uterinas OVÁRIO: (opção lâmina 35 caixa B) Região do Hilo: vasos sanguíneos, inervação e tecido conjuntivo denso Superfície do ovário -epitélio germinativo: tecido
Lâmina 72A: Ovário infantil e trompas uterinas OVÁRIO: (opção lâmina 35 caixa B) Região do Hilo: vasos sanguíneos, inervação e tecido conjuntivo denso Superfície do ovário -epitélio germinativo: tecido
Gametogênese ESPERMATOGÊNESE. Prof a. Marta G. Amaral, Dra. Embriologia molecular
 Gametogênese ESPERMATOGÊNESE Prof a. Marta G. Amaral, Dra. Embriologia molecular Gametogênese CGP se formam no epiblasto na 2ª sem. Na 4ª sem. migram do o saco vitelino para as gônadas em desenvolvimento.
Gametogênese ESPERMATOGÊNESE Prof a. Marta G. Amaral, Dra. Embriologia molecular Gametogênese CGP se formam no epiblasto na 2ª sem. Na 4ª sem. migram do o saco vitelino para as gônadas em desenvolvimento.
ORGANIZAÇÃO DO CORPO HUMANO - CÉLULAS. 8 ano Prof. Jair Nogueira Turma 82 - Ciências
 ORGANIZAÇÃO DO CORPO HUMANO - CÉLULAS 8 ano Prof. Jair Nogueira Turma 82 - Ciências O corpo humano apresenta uma estrutura complexa, formada por vários órgãos que realizam suas funções em conjunto. Assim
ORGANIZAÇÃO DO CORPO HUMANO - CÉLULAS 8 ano Prof. Jair Nogueira Turma 82 - Ciências O corpo humano apresenta uma estrutura complexa, formada por vários órgãos que realizam suas funções em conjunto. Assim
Tecido conjuntivo de preenchimento. Pele
 Tecido conjuntivo de preenchimento Pele derme epiderme Pele papila dérmica crista epidérmica corte histológico da pele observado em microscopia de luz Camadas da Epiderme proliferação e diferenciação dos
Tecido conjuntivo de preenchimento Pele derme epiderme Pele papila dérmica crista epidérmica corte histológico da pele observado em microscopia de luz Camadas da Epiderme proliferação e diferenciação dos
 http://www.boggiostudios.com/galleries/gallery/pregnancy 1 1- Espermatozoide atravessa a corona radiata. 2- Cabeça do espermatozoide adere à zona pelúcida 3- Reação acrossômica: o conteúdo do acrossomo
http://www.boggiostudios.com/galleries/gallery/pregnancy 1 1- Espermatozoide atravessa a corona radiata. 2- Cabeça do espermatozoide adere à zona pelúcida 3- Reação acrossômica: o conteúdo do acrossomo
A CÉLULA EUCARIÓTICA
 A CÉLULA EUCARIÓTICA ... A célula é a unidade básica, estrutural e funcional de todos os seres vivos... A maioria das células têm um tamanho de 10 a 100 micrómetros e formas variadas De acordo com a estrutura
A CÉLULA EUCARIÓTICA ... A célula é a unidade básica, estrutural e funcional de todos os seres vivos... A maioria das células têm um tamanho de 10 a 100 micrómetros e formas variadas De acordo com a estrutura
Fisiologia celular I. Fisiologia Prof. Msc Brunno Macedo
 celular I celular I Objetivo Conhecer os aspectos relacionados a manutenção da homeostasia e sinalização celular Conteúdo Ambiente interno da célula Os meios de comunicação e sinalização As bases moleculares
celular I celular I Objetivo Conhecer os aspectos relacionados a manutenção da homeostasia e sinalização celular Conteúdo Ambiente interno da célula Os meios de comunicação e sinalização As bases moleculares
Ciclo Celular. Dividido em: - Intérfase - Divisão celular: Dois tipos fundamentais. Mitose Meiose
 Meiose Ciclo Celular Dividido em: - Intérfase - Divisão celular: Dois tipos fundamentais Mitose Meiose Antes de qualquer divisão celular há duplicação do DNA durante a intérfase. Divisão Celular O Ciclo
Meiose Ciclo Celular Dividido em: - Intérfase - Divisão celular: Dois tipos fundamentais Mitose Meiose Antes de qualquer divisão celular há duplicação do DNA durante a intérfase. Divisão Celular O Ciclo
Universidade de Brasília (UnB) Universidade Aberta do Brasil (UAB) Aula 1: Gametogênese
 Universidade de Brasília (UnB) Universidade Aberta do Brasil (UAB) Aula 1: Gametogênese Síntese: Aspectos morfogenéticos da formação dos gametas masculino e feminino 1 Informações gerais da aula 1- Objetivos:
Universidade de Brasília (UnB) Universidade Aberta do Brasil (UAB) Aula 1: Gametogênese Síntese: Aspectos morfogenéticos da formação dos gametas masculino e feminino 1 Informações gerais da aula 1- Objetivos:
EXERCÌCIOS GLOBAIS. - as células 3 são duas vezes mais numerosas do que as 2; - as células 4 são duas vezes mais numerosas do que as 3;
 EXERCÌCIOS GLOBAIS 1. Atente às figuras 1 e 2 e responda às questões que se seguem: A fig.1 mostra um corte esquemático de uma estrutura estudada e a sua análise mostra que: - as células 3 são duas vezes
EXERCÌCIOS GLOBAIS 1. Atente às figuras 1 e 2 e responda às questões que se seguem: A fig.1 mostra um corte esquemático de uma estrutura estudada e a sua análise mostra que: - as células 3 são duas vezes
ROTEIRO DE ESTUDO. Ler na bibliografia recomendada os tópicos abordados, listados abaixo, e responder as questões complementares.
 ROTEIRO DE ESTUDO Ler na bibliografia recomendada os tópicos abordados, listados abaixo, e responder as questões complementares. Tópicos abordados 1)Visão Geral da Célula: Origem celular. Células como
ROTEIRO DE ESTUDO Ler na bibliografia recomendada os tópicos abordados, listados abaixo, e responder as questões complementares. Tópicos abordados 1)Visão Geral da Célula: Origem celular. Células como
Avanços, aplicações, limitações e perspectivas da tecnologia do ovário artificial de ruminantes
 Anais do IX Congresso Norte e Nordeste de Reprodução Animal (CONERA 2018); Belém, PA, 10 a 12 de setembro de 2018. Avanços, aplicações, limitações e perspectivas da tecnologia do ovário artificial de ruminantes
Anais do IX Congresso Norte e Nordeste de Reprodução Animal (CONERA 2018); Belém, PA, 10 a 12 de setembro de 2018. Avanços, aplicações, limitações e perspectivas da tecnologia do ovário artificial de ruminantes
UTILIZAÇÃO DO POTENCIAL DE OÓCITOS IMATUROS INCLUSOS EM FOLÍCULOS PRÉ-ANTRAIS NA REPRODUÇÃO DE MAMÍFEROS
 Ciência Animal 1998,8(1):23-29 UTILIZAÇÃO DO POTENCIAL DE OÓCITOS IMATUROS INCLUSOS EM FOLÍCULOS PRÉ-ANTRAIS NA REPRODUÇÃO DE MAMÍFEROS (Potential use of the immature oocytes included in preantral follicles
Ciência Animal 1998,8(1):23-29 UTILIZAÇÃO DO POTENCIAL DE OÓCITOS IMATUROS INCLUSOS EM FOLÍCULOS PRÉ-ANTRAIS NA REPRODUÇÃO DE MAMÍFEROS (Potential use of the immature oocytes included in preantral follicles
REPRODUÇÃO HUMANA. Lásaro Henrique
 REPRODUÇÃO HUMANA Lásaro Henrique GAMETOGÊNESE Processo de formação de gametas. Pode ser: Espermatogênese Ovulogênese ESPERMATOGÊNESE Ocorre nos tubos seminíferos,das paredes para a luz de cada tubo. ETAPAS
REPRODUÇÃO HUMANA Lásaro Henrique GAMETOGÊNESE Processo de formação de gametas. Pode ser: Espermatogênese Ovulogênese ESPERMATOGÊNESE Ocorre nos tubos seminíferos,das paredes para a luz de cada tubo. ETAPAS
SINCRONIZE CICLO ESTRAL: Vaca Poliéstrica, ou seja, manifesta vários cios durante o ano, sendo interrompido pela gestação.
 SINCRONIZE CICLO ESTRAL: Vaca Poliéstrica, ou seja, manifesta vários cios durante o ano, sendo interrompido pela gestação. Estro caracteriza-se pela receptividade sexual da fêmea e é nesta fase que ocorre
SINCRONIZE CICLO ESTRAL: Vaca Poliéstrica, ou seja, manifesta vários cios durante o ano, sendo interrompido pela gestação. Estro caracteriza-se pela receptividade sexual da fêmea e é nesta fase que ocorre
CONCENTRAÇÃO DE ESTRÓGENO E PROGESTERONA NO FLUIDO FOLICULAR SUÍNO OBTIDO A PARTIR DE FOLÍCULOS OVARIANOS DE DIFERENTES DIÂMETROS
 CONCENTRAÇÃO DE ESTRÓGENO E PROGESTERONA NO FLUIDO FOLICULAR SUÍNO OBTIDO A PARTIR DE FOLÍCULOS OVARIANOS DE DIFERENTES DIÂMETROS Guilherme OBERLENDER 1 ; Aryenne K. OLIVEIRA 2 ; Luis D. S. MURGAS 2 ;
CONCENTRAÇÃO DE ESTRÓGENO E PROGESTERONA NO FLUIDO FOLICULAR SUÍNO OBTIDO A PARTIR DE FOLÍCULOS OVARIANOS DE DIFERENTES DIÂMETROS Guilherme OBERLENDER 1 ; Aryenne K. OLIVEIRA 2 ; Luis D. S. MURGAS 2 ;
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS
 UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS REBECA MAGALHÃES PEDROSA ROCHA EFEITO DA MELATONINA E
UNIVERSIDADE ESTADUAL DO CEARÁ PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS REBECA MAGALHÃES PEDROSA ROCHA EFEITO DA MELATONINA E
Desenvolvimento folicular inicial em bovinos Initial follicular development in cattle
 Rev. Bras. Reprod. Anim., Belo Horizonte, v.37, n.4, p.328-333, out./dez. 2013. Disponível em www.cbra.org.br Desenvolvimento folicular inicial em bovinos Initial follicular development in cattle R.R.C.
Rev. Bras. Reprod. Anim., Belo Horizonte, v.37, n.4, p.328-333, out./dez. 2013. Disponível em www.cbra.org.br Desenvolvimento folicular inicial em bovinos Initial follicular development in cattle R.R.C.
Ciclo de Vida Celular. Professora: Luciana Ramalho 2017
 Ciclo de Vida Celular Professora: Luciana Ramalho 2017 Tipos de células Procarionte Sem núcleo Ex: Bactérias Eucarionte Com núcleo Ex: Vegetal, Protozoário, Animal e Fungos Exercício (FEI) Uma célula procarionte
Ciclo de Vida Celular Professora: Luciana Ramalho 2017 Tipos de células Procarionte Sem núcleo Ex: Bactérias Eucarionte Com núcleo Ex: Vegetal, Protozoário, Animal e Fungos Exercício (FEI) Uma célula procarionte
Matriz extracelular e Tecido epitelial
 Matriz extracelular e Tecido epitelial Capítulo 20 - Fundamentos da Biologia Celular Alberts - 3ª edição Capítulo 4 Histologia Básica Junqueira e Carneiro Células são organizadas em tecidos Plantas tem
Matriz extracelular e Tecido epitelial Capítulo 20 - Fundamentos da Biologia Celular Alberts - 3ª edição Capítulo 4 Histologia Básica Junqueira e Carneiro Células são organizadas em tecidos Plantas tem
T AT A A T M A E M NT N O
 Interpretação de exames laboratoriais em RHA Técnicas de Reprodução Assistida Dr. Pedro Augusto Araujo Monteleone pedro@monteleone.med.br 24 de fevereiro de 2012 exames laboratoriais em RHA DIAGNÓSTICO
Interpretação de exames laboratoriais em RHA Técnicas de Reprodução Assistida Dr. Pedro Augusto Araujo Monteleone pedro@monteleone.med.br 24 de fevereiro de 2012 exames laboratoriais em RHA DIAGNÓSTICO
UNIVERSIDADE ESTADUAL DO CEARÁ FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS MESTRADO ACADÊMICO EM CIÊNCIAS VETERINÁRIAS
 UNIVERSIDADE ESTADUAL DO CEARÁ FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS MESTRADO ACADÊMICO EM CIÊNCIAS VETERINÁRIAS LIVIA BRUNETTI APOLLONI EFEITO DO HORMÔNIO ANDROSTENEDIONA
UNIVERSIDADE ESTADUAL DO CEARÁ FACULDADE DE VETERINÁRIA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS MESTRADO ACADÊMICO EM CIÊNCIAS VETERINÁRIAS LIVIA BRUNETTI APOLLONI EFEITO DO HORMÔNIO ANDROSTENEDIONA
Mutações no gene STAT5A estão associadas com a sobrevivência embrionária e produção de leite
 UNIVERSIDADE FEDERAL DE PELOTAS FACULDADE DE VETERINÁRIA Núcleo de Pesquisa, Ensino e Extensão em Pecuária Mutações no gene STAT5A estão associadas com a sobrevivência embrionária e produção de leite Apresentação:
UNIVERSIDADE FEDERAL DE PELOTAS FACULDADE DE VETERINÁRIA Núcleo de Pesquisa, Ensino e Extensão em Pecuária Mutações no gene STAT5A estão associadas com a sobrevivência embrionária e produção de leite Apresentação:
ASPECTOS QUANTITATIVOS E QUALITATIVOS DA FOLICULOGÊNESE PRÉ- NATAL NA ESPÉCIE CAPRINA
 Ciência Animal 1998, 8(2):47-56 ASPECTOS QUANTITATIVOS E QUALITATIVOS DA FOLICULOGÊNESE PRÉ- NATAL NA ESPÉCIE CAPRINA (Quantitative and qualitative aspects of pre-antral folliculogenesis in caprine species)
Ciência Animal 1998, 8(2):47-56 ASPECTOS QUANTITATIVOS E QUALITATIVOS DA FOLICULOGÊNESE PRÉ- NATAL NA ESPÉCIE CAPRINA (Quantitative and qualitative aspects of pre-antral folliculogenesis in caprine species)
Terapia Ocupacional. Fisilogia
 Curso: Terapia Ocupacional Disciplina: Fisilogia Aula: Membrana Plasmática Profº. Ms. Rafael Palhano Fedato rafapalha@gmail.com Membrana Plasmática ou Membrana celular É uma dupla camada de lipídios com
Curso: Terapia Ocupacional Disciplina: Fisilogia Aula: Membrana Plasmática Profº. Ms. Rafael Palhano Fedato rafapalha@gmail.com Membrana Plasmática ou Membrana celular É uma dupla camada de lipídios com
Tecido epitelial. Junqueira, LC & Carneiro J. Histologia Básica.
 Tecido epitelial Junqueira, LC & Carneiro J. Histologia Básica. Tecido epitelial Distribuído pelo corpo recobrindo superfícies internas e externas Presente na maioria de glândulas Ancorados em matriz extracelular
Tecido epitelial Junqueira, LC & Carneiro J. Histologia Básica. Tecido epitelial Distribuído pelo corpo recobrindo superfícies internas e externas Presente na maioria de glândulas Ancorados em matriz extracelular
SANELY LOURENÇO DA COSTA CALIMAN EFEITO DA TIROXINA E DO HORMÔNIO FOLÍCULO ESTIMULANTE NO DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS OVINOS
 SANELY LOURENÇO DA COSTA CALIMAN EFEITO DA TIROXINA E DO HORMÔNIO FOLÍCULO ESTIMULANTE NO DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS OVINOS Dissertação apresentada à Universidade Federal de Viçosa,
SANELY LOURENÇO DA COSTA CALIMAN EFEITO DA TIROXINA E DO HORMÔNIO FOLÍCULO ESTIMULANTE NO DESENVOLVIMENTO IN VITRO DE FOLÍCULOS PRÉ-ANTRAIS OVINOS Dissertação apresentada à Universidade Federal de Viçosa,
Archives of Veterinary Science ISSN X ISOLAMENTO MECÂNICO DE FOLÍCULOS PRÉ-ANTRAIS DE CADELAS - EFEITO DO INTERVALO DE SECÇÃO
 Archives of Veterinary Science ISSN 1517-784X v.17, n.1, p.15-21, 2012 www.ser.ufpr.br/veterinary ISOLAMENTO MECÂNICO DE FOLÍCULOS PRÉ-ANTRAIS DE CADELAS - EFEITO DO INTERVALO DE SECÇÃO Kele Amaral Alves¹,
Archives of Veterinary Science ISSN 1517-784X v.17, n.1, p.15-21, 2012 www.ser.ufpr.br/veterinary ISOLAMENTO MECÂNICO DE FOLÍCULOS PRÉ-ANTRAIS DE CADELAS - EFEITO DO INTERVALO DE SECÇÃO Kele Amaral Alves¹,
CITOLOGIA 8º ano Prof. Graziela Grazziotin Costa
 CITOLOGIA 8º ano - 2017 Prof. Graziela Grazziotin Costa 1 Célula o Partes básicas: a) Membrana plasmática b) Citoplasma c) Núcleo 2 Célula o Menor porção viva de um organismo. o Eucarioto: presença de
CITOLOGIA 8º ano - 2017 Prof. Graziela Grazziotin Costa 1 Célula o Partes básicas: a) Membrana plasmática b) Citoplasma c) Núcleo 2 Célula o Menor porção viva de um organismo. o Eucarioto: presença de
