Revisão. Moléculas. Tipos de ligações moleculares: covalente, iônica que são responsáveis pela maioria das moléculas.
|
|
|
- Clara Caldeira Lacerda
- 6 Há anos
- Visualizações:
Transcrição
1 Moléculas Revisão Tipos de ligações moleculares: covalente, iônica que são responsáveis pela maioria das moléculas. Quando dois átomos se combinam de tal modo que um ou mais e - são dividos pelos átomos Quando dois átomos se combinam de tal modo que um ou mais e - são transferidos de um para outro átomo dipolo-dipolo ou molecular (Ligação de van der Waals) moléculas próximas deveriam estar sujeitas a uma força de origem eletrostática. Mesmo átomos que não formam ligações iônicas ou covalentes estão sujeitos a esse tipo de força. T baixa substâncias líquidos e depois sólidos (não o He). Campo elétrico de um dipolo. Ligação metálica responsável pela formação de grandes moléculas a partir de moléculas menores este tipo de ligação esta presente nos sólidos metálicos e discutiremos quando falarmos em sólidos... 1
2 Moléculas polares: Água: e - tendem a se concentrar nas vizinhanças do átomo de O (extremidade negativa do dipolo e os dois prótons a extremidade positiva), formam o dipolo Moléculas apolares Moléculas que possuem momentos dipolares elétricos permanentes H O e NaCl atraem outras moléculas polares r U r = p. A energia de ligação ~0,5eV por molécula. Corresponde a 10% da energia de ligação H-OH. Força dipolo-dipolo faz com que as moléculas de H O se condensem para formar o gelo A molécula pode ser polarizada pelo campo de uma molécula polar e adquirir um momento de dipolo induzido, e ser atraída pela molécula polar. r F r = U 1 r 7 E d Dipolos induzem organização Energia negativa e a força atrativa de curtíssimo alcance. FNC 0376 Força - Física de Moderna atração entre as moléculas apolares ---- Força de Aula van 8 der Walls
3 Níveis Moleculares As moléculas também emitem radiação eletromagnética A energia de uma molécula - três partes: Rotacionais (rotação das moléculas em torno do eixo do centro de massa) Vibracionais (oscilações dos átomos) Eletrônicos (excitação dos elétrons já vimos e a energia ~1eV) Rotacionais A energia cinética clássica de rotação: E r = MQ E r E L h I 1 1 E r = 1 m1v 1 + mv = Iω = L I = r( r + 1) h h E r = r( r + 1) I quantizado! h r( r + 1) ( r 1 r = I [ ] r r 1 = ) com r = 0, 1,, 3,... As variações de energia crescem com r Espectro FNC 0376 de emissão - Física Moderna da molécula diatômica de HCl com 3 freqüências correspondentes as transições permitidas
4 E v = + ( v 1 )hω com v = 0, 1,, 3,... K ω = µ Vibracionais Valor típico: E r hω 0,04 ev (NaCl). Espectros moleculares h + v = h I h E = hω + I para ( r = + 1) h E = hω r I para ( r = 1) 1 [ r( r + 1) ] + ( v + ) ω ( r + 1), com r, com r = 0,1,,... = 1,, 3,... r r r r r r r r = 1 r = +1 v v v Os níveis de energia são igualmente espaçados nas vizinhanças de r 0 Transições ópticas (emissão ou absorção de fótons). Regras de seleção continuam valendo: r = ±1 e4 v = ±1.
5 Espectro de absorção rotacional do HCl gasoso Efeitos anarmônicos Potencial de Morse <r> cresce com a energia de vibração distância intermolecular aumenta com T dilatação térmica 5
6 Sólidos Iônicos Covalentes Metálicos Moleculares Moleculares: moléculas tão estáveis que mantém individualidades. Não existem ligações covalentes ou iônicas. Ligação por van der Waals (fraca, ~10 - ev) T amb (kt = 0,05 ev) dissociação. Sólidos apenas a T << T amb. Fusão do H a 14 K. Falta de e - livres maus condutores de eletricidade e calor. Facilmente deformáveis. Iônicos: formação regular, alternada, 3D, de íons Na + e Cl. E sist < E íons isol.. Ligação não direcional. Disposição como a de esferas empilhadas. Arranjo depende do tamanho relativos dos íons, minimizando energia. Não existem e - livres. Má condução de eletricidade e calor. Forças eletrostáticas fortes alta T fusão, duros e pouco deformáveis. Interação dominante é a coulombiana entre os íons. No caso do NaCl, cada Na + tem 6 Cl como vizinhos mais próximos. E cada Cl tem 6 Na + como vizinhos mais próximos. NaCl Célula unitária Célula unitária é o menor conjunto de átomos que contém a simetria do cristal, e cuja repetição produz o cristal. 6
7 Covalentes: átomos ligados por e - de valência compartilhados ligações direcionais definem a geometria da estrutura cristalina. Estrutura eletrônica rígida duros, pouco deformáveis e alta T fusão. Não existem e - livres má condução de eletricidade e calor. Alguns (como Si e Ge) são semicondutores. íon do metal gás de e - Célula unitária de C Metálicos: caso limite da ligação covalente: e - compartilhados por todos os íons do cristal. e - externos fracamente ligados aos átomos são liberados pela energia disponibilizada pela ligação e - ligados ao potencial combinado de todos os íons positivos do cristal, formando um gás, que atrai os íons. e - livres, que podem se mover por todo o volume do cristal bons condutores de eletricidade e calor. 7
8 N átomos N x degenerado desdobramento em N níveis. E depende de R (define o grau de superposição entre as autofunções), mas não de N. Quanto maior N mais níveis no mesmo intervalo de E. Para a separação típica dos sólidos, R ~ 10-1 nm E ~ ev. Como N ~ 10 3 banda contínua. Níveis mais baixos não são afetados por serem mais ligados e terem órbitas menores não há superposição! Desdobramento depende das características do nível: níveis s banda com N níveis. Níveis p (3x degenerado, por causa dos m l 3N níveis. Aproximação de 4 átomos Aproximação de átomos Vejamos o caso do Na: 1s s p 6 3s 1 estado fundamental Níveis + baixos não afetados 8
9 Na: 1s s p 6 3s 1 Banda permitida Banda proibida não há níveis de energia eletrônicos Bandas vão se tornando mais largas, maior energia do e -, maior região ocupada por seu movimento e maior interação entre os íons vizinhos Nível 3s se transforma em uma banda Verificação experimental: transições 3s p Na gasoso linha estreita dos R-X L emitidos. Na sólido linha larga (distribuição de energia dos fótons alargada por causa do alargamento do nível 3s) Nível p não foi afetado na separação de equilíbrio 9
10 Condução metais, isolantes e semicondutores O comportamento de um sólido em relação à condução de eletricidade depende da distribuição e população dos seus níveis de energia. As bandas criadas por níveis que, no átomo isolado, correspondiam a subcamadas fechadas têm todos os seus níveis ocupados. As bandas geradas pelos níveis onde se encontram os e - de valência podem estar total ou parcialmente ocupadas. Um campo elétrico aplicado ao material provoca um aumento na energia dos e -, desde que existam níveis de energia disponíveis para serem ocupados. Caso contrário, os e - não conseguem adquirir energia e o material se comporta como um isolante. Condutor Isolante 10
11 Condução elétrica em metais Elétrons livres no metal gás de e -. Freqüência das colisões elétron-imperfeições da rede descrever pelo caminho livre médio: λ. E externo aplicado aceleração entre colisões velocidade de arrasto: v d ,77 v = 0,77v -1 mv σ = ρ = ne λ ee λ a = tcolis = vd = atcolis = m v aλ = v eeλ mv Se tivermos ne - de condução por unidade de volume, e a densidade de corrente for j, temos: F j eeλ vd = = j = ne mv Distância média percorrida por um elétron entre colisões ne λ E mv Notem que nem v nem λ dependem do campo E aplicado. σ Lei de Ohm: j = σe 11
12 Voltando ao modelo de condutividade elétrica, podemos definir a mobilidade: v eλ µ = d = e assim, podemos escrever a condutividade como: σ = neµ E mv De forma mais abrangente, devemos definir a condutividade como: σ = nq µ + pq µ onde n e p designam os portadores de carga negativa n n p p e positiva, respectivamente. A determinação do tipo de portador é feita por efeito Hall. 1
13 Modelo quântico da condução elétrica em metais A ocupação dos estados de energia de um gás de e num poço quadrado, é dada por: 3 1/ 1/ 8πV (m ) E de n( E) = f ( E) g( E) de = 3 ( E EF ) / kt h e + 1 g(ε) g(ε) f(ε) f(ε) n(ε) n(ε) 13
14 Movimento em uma rede periódica Ψ( xt, ) = u( xe ) k i( kx ωt) u ( x) = u ( x+ a) = u ( x+ na) k k k Função de onda do e - : onda progressiva. Em vez de amplitude constante, temos uma função. Função que modula a amplitude da onda pela periodicidade da rede Os e - podem ser espalhados pelos átomos da rede. Isso depende da relação entre o comprimento de onda de de Broglie e o espaçamento dos átomos. Se E << V 0 e b é grande, então temos o e - preso a um poço, com a estrutura de níveis já conhecida. À medida que os poços se aproximam, as funções de onda podem penetrar as barreiras níveis se transformam em bandas. 14
15 e - em um poço de potencial isolado e - em sistema de poços periódicos, com b = l/16 A eq. de Schrödinger pode ser resolvida para o potencial de Kronig- Penney, de onde aparecem as bandas permitidas e as proibidas. É interessante notar que intervalos proibidos aparecem para determinados valores de k. 15
16 Descontinuidades em k π = ±, ± a π, a Concordam com o resultado obtido com base no número de estados da banda! (transparência 5) Rede unidimensional de periodicidade a: 3π ±,L a Podemos entender os intervalos proibidos como resultado da reflexão parcial da onda progressiva pelas sucessivas barreiras. Ondas refletidas em fase a = λ, λ, 3λ,... 16
17 Condutores, isolantes e semicondutores banda de condução banda de valência Metal A razão de porque alguns materiais são condutores enquanto outros são isolantes está na ocupação e distribuição das bandas. Na orbital 3s, que pode abrigar e -, abriga apenas 1. Os átomos de Na quando se unem para formar os cristais a banda de energia é apenas metade preenchida há níveis disponíveis na banda, os e - possam aumentar suas energias ao serem acelerados. Além disso, a banda do orbital 3p está desocupada e coincide parcialmente com o 3s, permitido que os e - passem de uma para outra O Na é um bom condutor Mg, por sua vez, tem a banda 3s completa, mas a 3p também se superpõe a ela, fazendo do Mg um condutor. 17
18 Quando um campo elétrico é suficientemente intenso para promover e - para a banda de condução, ocorre a ruptura do dielétrico. Isolante Isolante E g ~ 10 ev Um sólido é considerado um isolante, quando sua banda de valência está completa e há uma separação, superior a ~ ev, até a primeira banda disponível, a banda de condução. Quase todos os cristais iônicos são isolantes, pois ambos os íons têm suas camadas fechadas, como no caso do NaCl. A banda vazia mais próxima vem dos estados excitados dos íons Na + e Cl -, que apresentam uma diferença de energia muito grande em relação à cama da de valência. A excitação térmica, ou mesmo os campos elétricos usualmente empregados, não são suficientes para conseguir promover um e - da banda de valência para a de condução. 18
19 E Semicondutor banda de valência f FD Semicondutor E g ~ 1 ev Quando a largura da banda proibida é pequena (menor que ev), o sólido é considerado um semicondutor. Consideremos o caso do C, e- em s e eem p e s e p se misturam para formar ligações covalentes com outros C para formar o diamante. Dos 8 estados que o orbital híbrido sp tem, apenas 4 formam estados ligantes. Os outros 4 correspondem a autofunções espaciais anti-simétricas, com energias mais altas. Esses estados vão dar origem às bandas de condução. Dependendo da distância interatômica, a separação entre as bandas de valência e de condução pode fazer do material um isolante (caso do diamante) ou um semicondutor (caso do Si e do Ge). Semicondutor intrínseco: semicondutor puro, sem impurezas que afetem a distribuição de e - ou buracos. 19
20 E Condução elétrica em semicondutores e - de condução Condução buracos elétrons Proibida E r Valência Um campo elétrico aplicado a um semicondutor produz condução elétrica devido ao movimento dos e - na banda de condução, bem como dos buracos na banda de valência. No caso dos buracos, o movimento também se deve aos e -, que, devido ao campo, ocupam sucessivamente a vacância deixada pelo e - promovido à banda de condução, fazendo com que a vacância se desloque no sentido oposto. 0
21 Dopagem de semicondutores O processo de dopagem de semicondutores refere-se à adição, ao cristal intrínseco, de pequena quantidade de impureza, com propriedades adequadas, de forma a afetar o comportamento elétrico do semicondutor da maneira desejada. Existem dopantes doadores e receptores, que produzem os semicondutores tipo n e tipo p, respectivamente. Tipo n Si dopado com As (que tem valência 5) E g ~ 1 ev E d ~ 0,05 ev 1
22 Tipo p Si dopado com Ga (que tem valência 3) E g ~ 1 ev E a ~ 0,07 ev Fixo! Junção p-n: diodo Região de depleção Íons fixos Junção
23 Fórmula de massa semi-empírica Ficamos então, com a expressão para a energia de ligação: E lig = a V A a S A /3 a C Z /A 1/3 a A (A Z) /A ±δ(z,a) a V = 15,56 MeV; a S = 17,3 MeV; a C = 0,697 MeV; a A = 3,85 MeV; a P = 1 MeV. Neste gráfico temos as varias contribuições, falta apenas a de ligação de emparelhamento A equação se ajusta de A>0 ate o fim da tabela periódica Energia de ligação por nucleon (MeV) termo de volume termo de superfície termo coulombiano E lig (Z,A)/A energia de ligação por nucleon Número de massa, A Neste gráfico temos a diferença de energia de ligação do último nêutron e a previsão da fórmula de massa. Números mágicos 8, 50, 8 e 16 3 para os nêutrons e também para os prótons
24 Radioatividade De ~ 3000 nuclídeos conhecidos, apenas cerca de 90 são estáveis. Os outros sofrem algum tipo de decaimento radioativo, transformando-se espontaneamente em outros nuclídeos emitindo radiação. O termo radiação tanto se refere a partículas como onda eletromagnéticas Em 1900 Rutherford descobriu que a taxa de emissão de radiação não e constante mais decai exponencialmente com o tempo Se N(t) é o n o de núcleos radioativos no instante t e dn é o n o de núcleos que decaem no intervalo dt (negativo pois N diminui) dn N( t) = = λndt N 0 e λt λ é a constante de decaimento O meia-vida t 1/ é definida como o tempo necessário para que o n o de núcleos radioativos se reduza a metade do valor inicial O tempo médio de vida dos núcleos: que é o inverso da constante de decaimento τ = 1 λ 4
25 A meia-vida t 1/ para que uma substância seja encontrada na natureza e preciso que sua t 1/ seja muito menor que a idade da Terra (~ 4.5x10 9 anos) ou que ela seja produzida a partir do decaimento de outras substâncias 1 e t λt 1/ N 1/ 0 = = N ln = λ 0 λt 1/ e Depois de um intervalo de meia-vida, tanto o n o de núcleos que restam na amostra como a taxa de decaimento estão reduzidos a metade do valor inicial = = 0.693τ λ SI a unidade becquerel (Bq), definido como uma taxa de um decaimento por segundo: 1 Bq = 1 decaimento/s O Curie (Ci) e uma unidade mais recente 1Ci=3,7x10 10 decaimentos/s=3,7x10 10 Bq Os nuclideos radioativos (transição dos núcleos de um estado quântico para outro estado de menor energia) podem decair através dos seguintes modos: alfa, beta e gama. Há ainda decaimentos que ocorrem através da emissão de p ou n e a fissão espontânea. Os decaimentos nucleares ocorrem sempre que um núcleo, contendo um certo n o de núcleons se encontra em um estado excitado (não o de menor energia) 5
26 Decaimento alfa (emissão espontânea de uma partícula α) Núcleos com Z>83 são instáveis e neste processo o núcleo pai decai nos núcleos filhos através da emissão de um partícula α He (Z= A=4). Há energia suficiente, uma vez que a massa do núcleo pai M Z,A é maior que as somas das massas do núcleo filho M Z-,A-4 mais a da partícula α, Μ,4 Energia do decaimento dos núcleos pais, onde a emissão α é espontânea E = M Z, A ( M Z, A 4 + M,4)] [ c Curva representa o comportamento geral predito pela fórmula de massa Potencial (coulombiano + nuclear) que atua sobre α emitida pelo núcleo pai 6
27 Decaimento beta (emissão ou absorção espontânea de um elétron ou pósitron decaimento radioativo nos qual o no de massa A permanece constante Enquanto Z e N variam de uma unidade) emissão β - = um elétron é emitido e um dos nêutrons do núcleo se transforma em próton (Z =Z+1) (N =N-1), A energia do decaimento, Q, é igual à diferença entre a massa do núcleo pai e a soma das massas dos produtos do decaimento, multiplicado por c Q c = M M P F aparente violação da lei de conservação para energias menores que E máx Os experimentos revelam que a energia do elétron emitido pode ter qualquer valor entre 0 e a energia máxima disponível. lei de conserv emissão de uma terceira partícula (antineutrino) 198 Au 198 Hg + β + ν e 7
28 Decaimento beta emissão β + = um pósitron é emitido e um dos prótons do núcleo se transforma em nêutron Duas massas eletrônicas m positron = m e Q c = = K Qual a energia máxima dos pósitrons? lei de conserv emissão de neutrino β + não pode ocorrer a menos que a energia seja de pelo menos m e c =1.0 MeV captura eletrônica = um próton no interior do núcleo captura um elétron atômico se transforma em nêutron, ao mesmo tempo que emite um neutrino 51 4 Cr 51 3 Para que seja possível a massa de um átomo (Z) seja maior que a massa de um átomo com Z-1 V Ar + ν + + β + ν M P ( M F + me ) 0,000519ux931,5MeV / c. u Q = 0, 483MeV e e M ( M ( m e K) Ar) = 39,964000u = 39,96384u = 5,4858x10 4 u 8
29 Reações Nucleares (nos fornecem informações adicionais sobre os estados excitados dos núcleos) em um choque entre uma partícula com um núcleo vários fenômenos podem ocorrer: 1) Partículas podem ser espalhadas elasticamente ou inelasticamente (no caso inelástico a núcleo é promovido para um estado excitado que decai para o estado fundamental com emissão de fótons ou partículas) ) A partícula original pode ser absorvida e outra(s) partícula(s) pode(m) ser emitida(s). Conservação de Energia: Partícula incidente x+x Y+y+Q Q é a energia liberada na reação: x Núcleo composto Y Q = ( m X x + mx my my ) c Absorção y Q>0 reação nuclear libera energia y reação exotérmica Partícula espalhada Q<0 reação endotérmica Formação de um núcleo composto e depois o seu decaimento 9
30 Fissão A fissão do urânio foi descoberta em 1938 por Hahn e Strassmann, com técnicas químicas encontraram que no bombardeiro de urânio por nêutrons produz elementos no meio da tabela periódica 35U + n 36U* fragmentos + vn EC ~ 6, MeV Núcleo excitado E*= 6,5 MeV n s s n O aumento da área da superfície produz um aumento de energia potencial 35 U 36 U n n A medida que s aumenta o efeito da tensão superficial obriga o núcleo se dividir em duas regiões s A tensão diminui a medida que s aumenta diminuição da repulsão coulombiana 30
31 Fissão Na fissão o 35U é excitado pela captura de um n e se dividi em dois núcleos, cada um com ~ metade da massa. Uma reação típica: U + n Kr + Ba + n + 179, 4MeV Os dois fragmentos, não são em geral simétricos mas possuem ~ a mesma razão Z/N. e a força eletrostático faz com que os fragmentos sejam ejetados em direções com E cin alta. Os fragmentos tendem a ter N demais Aqui temos a distribuição dos fragmentos de fissão do 35 U. Fissão simétrica, o núcleo se divide em dois núcleos de massa ~ iguais 31
32 Fissão (permite produzir energia numa reação em cadeia já que dois ou mais nêutrons são emitidos) Reatores O n o médio N emitidos na reação de fissão induzida é de,4. A razão porque são emitidos vários N é que os fragmentos de fissão possuem N em excesso. A emissão de vários N levou a idéia de utilizá-los para produzir novas fissões reação em cadeia Em 1914 um grupo de cientistas (liderados por Enrico Fermi) produziu a primeira reação em cadeia autosustentável em um reator nuclear na Universidade de Chicago. k é o parâmetro utilizado para determinar o o fator de reprodução n o médio de N que produzem novas fissões. k=1 o reator está crítico (reação autosustentada). k <1 está subcrítico (reação não prossegue) k > 1 está supercrítico (o n o de fissões aumenta rapidamente e a reação se torna explosiva 3
33 Fusão A produção de energia a partir da fusão de núcleos leves vem sendo investigada da abundância de combustível e da ausência de alguns riscos associados ao reatores de fissão. Numa reação de fusão dois núcleos leves se fundem para formar um núcleo mais pesado 3 4 Esta reação libera 4,3 vezes mais energia por quilograma que a reação típica de fissão (Veja exercício lista). Mas utilizar esta tecnologia de fusão uma fonte prática de energia ainda não está disponível!!!! Devido a repulsão eletrostática, os núcleos de H e de 3 H só se aproximam o suficiente para que as forças nucleares predominem se tiverem E cin extremamente elevada ~1 MeV, facilmente obtido por aceleradores. No entanto o espalhamento é mais provável que a fusão. Há um maior consumo de energia do que produção. Como as partículas tem E cin > 3/ kt e algumas podem atravessar a barreira coulombiana por tunelamento. Na prática a T onde kt~10kev é suficiente para ter um n o de reações de fusão adequadas. No entanto a temperatura neste caso é 10 8 K. Temperaturas desta ordem acontecem no interior das estrelas H + H He + n MeV 33
Teoria de bandas nos sólidos
 Teoria de bandas nos sólidos Situação: átomos idênticos, distantes níveis de energia desse sistema têm degenerescência de troca dupla. A parte espacial da autofunção eletrônica pode ser uma combinação
Teoria de bandas nos sólidos Situação: átomos idênticos, distantes níveis de energia desse sistema têm degenerescência de troca dupla. A parte espacial da autofunção eletrônica pode ser uma combinação
Física Moderna II - FNC376
 Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto 1o. Semestre de 008 1 Núcleos não podem conter elétrons O Princípio da Incerteza nos diz que:
Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto 1o. Semestre de 008 1 Núcleos não podem conter elétrons O Princípio da Incerteza nos diz que:
Vimos que a energia de ligação de um núcleo com Z prótons e N nêutrons é dado por:
 Vimos que a energia de ligação de um núcleo com Z prótons e N nêutrons é dado por: E lig = Mc E lig = = Mc Zm H c + = Zm Nm c n p c M Nm c A c n M E como a massa de um átomo é praticamente igual a soma
Vimos que a energia de ligação de um núcleo com Z prótons e N nêutrons é dado por: E lig = Mc E lig = = Mc Zm H c + = Zm Nm c n p c M Nm c A c n M E como a massa de um átomo é praticamente igual a soma
Física Moderna II. Universidade de São Paulo Instituto de Física. Prof. Nemitala Added Profa. Márcia de Almeida Rizzutto 2 o Semestre de 2014
 Universidade de São Paulo Instituto de Física Física Moderna II Prof. Nemitala Added Profa. Márcia de Almeida Rizzutto o Semestre de 014 1 Força Nuclear no modelo atômico (átomo mais simples, H) descrevemos
Universidade de São Paulo Instituto de Física Física Moderna II Prof. Nemitala Added Profa. Márcia de Almeida Rizzutto o Semestre de 014 1 Força Nuclear no modelo atômico (átomo mais simples, H) descrevemos
1 Ψ S. bósons estatística de Bose: n(e) = e α e E/kT 1 1 Ψ A. férmions estatística de Fermi: n(e) = e α e E/kT +1
 Estatística Quântica Boltzmann: n(e) = 1 e α e E/kT Indistinguibilidade Ψ S ou Ψ A 1 Ψ S bósons estatística de Bose: n(e) = e α e E/kT 1 1 Ψ A férmions estatística de Fermi: n(e) = e α e E/kT +1 1 Distribuição
Estatística Quântica Boltzmann: n(e) = 1 e α e E/kT Indistinguibilidade Ψ S ou Ψ A 1 Ψ S bósons estatística de Bose: n(e) = e α e E/kT 1 1 Ψ A férmions estatística de Fermi: n(e) = e α e E/kT +1 1 Distribuição
Física Nuclear: Radioatividade
 Física Nuclear: Radioatividade Descoberta da Radioatividade Becquerel, estudando fenômenos de fluorescência e raios-x Observava fluorescência no Urânio quando exposto ao Sol. Becquerel protegia uma chapa
Física Nuclear: Radioatividade Descoberta da Radioatividade Becquerel, estudando fenômenos de fluorescência e raios-x Observava fluorescência no Urânio quando exposto ao Sol. Becquerel protegia uma chapa
Física Nuclear: Radioatividade
 Física Nuclear: Radioatividade Descoberta da Radioatividade Becquerel, estudando fenômenos de fluorescência e raios-x Observava fluorescência no Urânio quando exposto ao Sol. Becquerel protegia uma chapa
Física Nuclear: Radioatividade Descoberta da Radioatividade Becquerel, estudando fenômenos de fluorescência e raios-x Observava fluorescência no Urânio quando exposto ao Sol. Becquerel protegia uma chapa
Física Moderna II Aula 24
 Universidade de São Paulo Instituto de Física 2 º Semestre de 2015 Profa. Márcia de Almeida Rizzutto Oscar Sala sala 220 rizzutto@if.usp.br Física Moderna II Aula 24 Monitor: Gabriel M. de Souza Santos
Universidade de São Paulo Instituto de Física 2 º Semestre de 2015 Profa. Márcia de Almeida Rizzutto Oscar Sala sala 220 rizzutto@if.usp.br Física Moderna II Aula 24 Monitor: Gabriel M. de Souza Santos
Física Moderna II Aula 08. Marcelo G Munhoz Edifício HEPIC, sala 202, ramal
 Física Moderna II Aula 08 Marcelo G Munhoz Edifício HEPIC, sala 202, ramal 916940 munhoz@if.usp.br 1 Física Moderna II Particle Physics Education CD-ROM 1999 CERN Sólidos Átomos de 1 e - Núcleo Atômico
Física Moderna II Aula 08 Marcelo G Munhoz Edifício HEPIC, sala 202, ramal 916940 munhoz@if.usp.br 1 Física Moderna II Particle Physics Education CD-ROM 1999 CERN Sólidos Átomos de 1 e - Núcleo Atômico
Física IV Poli Engenharia Elétrica: 20ª Aula (04/11/2014)
 Física IV Poli Engenharia Elétrica: ª Aula (4/11/14) Prof. Alvaro Vannucci a última aula vimos: Átomos multi-eletrônicos: as energias dos estados quânticos podem ser avaliadas através da expressão: 13,6
Física IV Poli Engenharia Elétrica: ª Aula (4/11/14) Prof. Alvaro Vannucci a última aula vimos: Átomos multi-eletrônicos: as energias dos estados quânticos podem ser avaliadas através da expressão: 13,6
Ligações Atômicas e Bandas de Energia. Livro Texto - Capítulo 2
 40 Ligações Atômicas e Bandas de Energia Livro Texto - Capítulo 2 Ligação Atômica 41 Porque estudar a estrutura atômica? As propriedades macroscópicas dos materiais dependem essencialmente do tipo de ligação
40 Ligações Atômicas e Bandas de Energia Livro Texto - Capítulo 2 Ligação Atômica 41 Porque estudar a estrutura atômica? As propriedades macroscópicas dos materiais dependem essencialmente do tipo de ligação
Física Moderna II - FNC376
 Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto 1o. Semestre de 2008 1 MQ átomos > < Moléculas moléculas e sólidos núcleos e partículas Moléculas
Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto 1o. Semestre de 2008 1 MQ átomos > < Moléculas moléculas e sólidos núcleos e partículas Moléculas
Descoberta do Núcleo
 Unidade 2: Aula 4 (1a. Parte) Núcleo Atômico Descoberta do Núcleo Propriedades dos Núcleos Forças Nucleares Estabilidade Nuclear Ressonância Magnética Nuclear Consultas http://hyperphysics.phy-astr.gsu.edu/hbase/nuccon.html#nuccon
Unidade 2: Aula 4 (1a. Parte) Núcleo Atômico Descoberta do Núcleo Propriedades dos Núcleos Forças Nucleares Estabilidade Nuclear Ressonância Magnética Nuclear Consultas http://hyperphysics.phy-astr.gsu.edu/hbase/nuccon.html#nuccon
AS RADIAÇÕES NUCLEARES 4 AULA
 AS RADIAÇÕES NUCLEARES 4 AULA Nesta Aula: Caracterização das radiações Nucleares Caracterização das radiações Nucleares UM POUCO DE HISTÓRIA... O físico francês Henri Becquerel (1852-1908), em 1896, acidentalmente
AS RADIAÇÕES NUCLEARES 4 AULA Nesta Aula: Caracterização das radiações Nucleares Caracterização das radiações Nucleares UM POUCO DE HISTÓRIA... O físico francês Henri Becquerel (1852-1908), em 1896, acidentalmente
Aula 21 Física Nuclear
 Aula 21 Física 4 Ref. Halliday Volume4 Sumário Descobrindo o Núcleo; Algumas Propriedades Nucleares; Decaimento Radioativo; Decaimento Alfa; Decaimento Beta; Radiação Ionizante; Analisando os dados, Rutherford
Aula 21 Física 4 Ref. Halliday Volume4 Sumário Descobrindo o Núcleo; Algumas Propriedades Nucleares; Decaimento Radioativo; Decaimento Alfa; Decaimento Beta; Radiação Ionizante; Analisando os dados, Rutherford
FNC Física Moderna 2 Aula 26
 1 Física Nuclear: cronologia do início Descoberta da Radioatividade (Becquerel) 1896 Separação química do Ra (Marie e Pierre Curie) 1898 Modelo atômico de Rutherford 1911 Descoberta de isótopos (J.J. Thomson)
1 Física Nuclear: cronologia do início Descoberta da Radioatividade (Becquerel) 1896 Separação química do Ra (Marie e Pierre Curie) 1898 Modelo atômico de Rutherford 1911 Descoberta de isótopos (J.J. Thomson)
FNC Física Moderna 2 Aula 26
 FNC 0376 - Física Moderna Aula 6 1 Física Nuclear: cronologia do início Descoberta da Radioatividade (Becquerel) 1896 Separação química do Ra (Marie e Pierre Curie) 1898 Modelo atômico de Rutherford 1911
FNC 0376 - Física Moderna Aula 6 1 Física Nuclear: cronologia do início Descoberta da Radioatividade (Becquerel) 1896 Separação química do Ra (Marie e Pierre Curie) 1898 Modelo atômico de Rutherford 1911
Sólidos. Sólidos Cristalinos
 Sólidos Conforme as condições de temperatura e pressão, uma amostra de qualquer substância pode se apresentar no estado sólido, no estado líquido ou no estado gasoso. No estado gasoso, a distância média
Sólidos Conforme as condições de temperatura e pressão, uma amostra de qualquer substância pode se apresentar no estado sólido, no estado líquido ou no estado gasoso. No estado gasoso, a distância média
Moléculas. Usamos a aproximação de Born- Oppenheimer, que considera os núcleos fixos, apenas o e - se movimenta.
 Moléculas Moléculas é uma coleção de 2 ou mais núcleos e seus elétrons associados, com todas as ligações complexas unidas pelas forças Os tipos mais importantes de ligação molecular são: covalente, iônica
Moléculas Moléculas é uma coleção de 2 ou mais núcleos e seus elétrons associados, com todas as ligações complexas unidas pelas forças Os tipos mais importantes de ligação molecular são: covalente, iônica
Cap. 41 -Condução de eletricidade em sólidos
 Cap. 41 -Condução de eletricidade em sólidos Propriedades elétricas dos sólidos; Níveis de energia em um sólido cristalino: Átomo; Molécula; Sólido. Estrutura eletrônica e condução: Isolantes (T = 0);
Cap. 41 -Condução de eletricidade em sólidos Propriedades elétricas dos sólidos; Níveis de energia em um sólido cristalino: Átomo; Molécula; Sólido. Estrutura eletrônica e condução: Isolantes (T = 0);
Desintegração Nuclear. Paulo R. Costa
 Desintegração Nuclear Paulo R. Costa Sumário Introdução Massas atômicas e nucleares Razões para a desintegração nuclear Decaimento nuclear Introdução Unidades e SI Introdução Comprimento metro Tempo segundo
Desintegração Nuclear Paulo R. Costa Sumário Introdução Massas atômicas e nucleares Razões para a desintegração nuclear Decaimento nuclear Introdução Unidades e SI Introdução Comprimento metro Tempo segundo
O ÂTOMO TIPOS DE RADIAÇÕES. TIPOS DE RADIAÇÕES As radiações podem ser classificadas da seguinte forma: Quanto à composição
 O ÂTOMO Prof. André L. C. Conceição DAFIS Curitiba, 27 de março de 2015 TIPOS DE RADIAÇÕES Radiação é energia em trânsito (emitida e transferida por um espaço). Do mesmo jeito que o calor (energia térmica
O ÂTOMO Prof. André L. C. Conceição DAFIS Curitiba, 27 de março de 2015 TIPOS DE RADIAÇÕES Radiação é energia em trânsito (emitida e transferida por um espaço). Do mesmo jeito que o calor (energia térmica
Carga, massa e spin do núcleo
 Carga, massa e spin do núcleo Núcleo: conjunto ligado de prótons e nêutrons. Nuclídeo: configuração particular de um núcleo. Algumas características: E lig ~ MeV; ρ N ~ 10 1 g/cm 3 ~ 10 1 ρ Átomo A Z X
Carga, massa e spin do núcleo Núcleo: conjunto ligado de prótons e nêutrons. Nuclídeo: configuração particular de um núcleo. Algumas características: E lig ~ MeV; ρ N ~ 10 1 g/cm 3 ~ 10 1 ρ Átomo A Z X
Propriedades e classificação dos sólidos Semicondutores Dopados Dispositivos semicondutores Exercícios
 SÓLIDOS Fundamentos de Física Moderna (1108090) - Capítulo 04 I. Paulino* *UAF/CCT/UFCG - Brasil 2015.2 1 / 42 Sumário Propriedades e classificação dos sólidos Propriedades elétricas dos sólidos Isolantes
SÓLIDOS Fundamentos de Física Moderna (1108090) - Capítulo 04 I. Paulino* *UAF/CCT/UFCG - Brasil 2015.2 1 / 42 Sumário Propriedades e classificação dos sólidos Propriedades elétricas dos sólidos Isolantes
Átomos. Retrospectiva do átomo de hidrogênio Estrutura eletrônica do átomo neutro Estrutura nuclear do átomo RMN
 Átomos Retrospectiva do átomo de hidrogênio Estrutura eletrônica do átomo neutro Estrutura nuclear do átomo RMN Átomo neutro O átomo é constituido de um núcleo positivo com Z próton que definem o confinamento
Átomos Retrospectiva do átomo de hidrogênio Estrutura eletrônica do átomo neutro Estrutura nuclear do átomo RMN Átomo neutro O átomo é constituido de um núcleo positivo com Z próton que definem o confinamento
Cap. 42 Física Nuclear
 Radiação Fukushima (2011) Cap. 42 Física Nuclear A descoberta do núcleo. Propriedades do núcleo: Núcleons; Carta de nuclídeos; Raio; Massa; Energia de ligação; Força forte. Decaimento radioativo: Decaimento
Radiação Fukushima (2011) Cap. 42 Física Nuclear A descoberta do núcleo. Propriedades do núcleo: Núcleons; Carta de nuclídeos; Raio; Massa; Energia de ligação; Força forte. Decaimento radioativo: Decaimento
18/Maio/2016 Aula 21. Introdução à Física Nuclear. Estrutura e propriedades do núcleo. 20/Maio/2016 Aula 22
 18/Maio/2016 Aula 21 Introdução à Física Nuclear Estrutura e propriedades do núcleo 20/Maio/2016 Aula 22 Radioactividade: Poder de penetração. Regras de conservação. Actividade radioactiva. Tempo de meia
18/Maio/2016 Aula 21 Introdução à Física Nuclear Estrutura e propriedades do núcleo 20/Maio/2016 Aula 22 Radioactividade: Poder de penetração. Regras de conservação. Actividade radioactiva. Tempo de meia
Decaimento Radioativo
 Unidade 3 Radioatividade Decaimento Radioativo Decaimentos Alfa, Beta, e Gama Nuclídeos Radioativos Datação Radioativa 14 C Medidas de Dose de Radiação Modelos Nucleares Marie e Pierre Curie Marie Curie
Unidade 3 Radioatividade Decaimento Radioativo Decaimentos Alfa, Beta, e Gama Nuclídeos Radioativos Datação Radioativa 14 C Medidas de Dose de Radiação Modelos Nucleares Marie e Pierre Curie Marie Curie
Descoberta do Núcleo
 Unidade 3 Núcleo Atômico Descoberta do Núcleo Propriedades dos Núcleos Forças Nucleares Estabilidade Nuclear Ressonância Magnética Nuclear Consultas http://hyperphysics.phy-astr.gsu.edu/hbase/nuccon.html#nuccon
Unidade 3 Núcleo Atômico Descoberta do Núcleo Propriedades dos Núcleos Forças Nucleares Estabilidade Nuclear Ressonância Magnética Nuclear Consultas http://hyperphysics.phy-astr.gsu.edu/hbase/nuccon.html#nuccon
Física do Estado Sólido: Sólidos Condutores
 Física do Estado Sólido: Sólidos Condutores Trabalho de Física Moderna II Professor Marcelo Gameiro Munhoz 7 de maio de 2012 André E. Zaidan Cristiane Calil Kores Rebeca Bayeh Física do Estado Sólido -
Física do Estado Sólido: Sólidos Condutores Trabalho de Física Moderna II Professor Marcelo Gameiro Munhoz 7 de maio de 2012 André E. Zaidan Cristiane Calil Kores Rebeca Bayeh Física do Estado Sólido -
Definições de Estabilidade
 Radioquímica Definições de Estabilidade 1. Não se deteta radioatividade. Não há transformação em outro nuclídeo.. Sistema nuclear é estável em relação a outro quando a diferença de energia é negativa:
Radioquímica Definições de Estabilidade 1. Não se deteta radioatividade. Não há transformação em outro nuclídeo.. Sistema nuclear é estável em relação a outro quando a diferença de energia é negativa:
Física Moderna II Aula 10
 Física Moderna II Aula 10 Marcelo G. Munhoz munhoz@if.usp.br Lab. Pelletron, sala 245 ramal 6940 Como podemos descrever o núcleo de maneira mais detalhada? n Propriedades estáticas: q Tamanho, q Massa,
Física Moderna II Aula 10 Marcelo G. Munhoz munhoz@if.usp.br Lab. Pelletron, sala 245 ramal 6940 Como podemos descrever o núcleo de maneira mais detalhada? n Propriedades estáticas: q Tamanho, q Massa,
Estrutura Atômica. Prof. Dr. Carlos Roberto Grandini. Bauru 2006
 Estrutura Atômica Prof. Dr. Carlos Roberto Grandini Bauru 2006 O que é nanotecnologia? Nanotecnologia pode ser considerada como um conjunto de atividades ao nível de átomos e moléculas que tem aplicação
Estrutura Atômica Prof. Dr. Carlos Roberto Grandini Bauru 2006 O que é nanotecnologia? Nanotecnologia pode ser considerada como um conjunto de atividades ao nível de átomos e moléculas que tem aplicação
Radioatividade. Prof. Fred
 Radioatividade Prof. Fred Radioatividade, uma introdução Radioatividade O homem sempre conviveu com a radioatividade. Raios cósmicos Fótons, elétrons, múons,... Radioatividade natural: Primordiais urânio,
Radioatividade Prof. Fred Radioatividade, uma introdução Radioatividade O homem sempre conviveu com a radioatividade. Raios cósmicos Fótons, elétrons, múons,... Radioatividade natural: Primordiais urânio,
Outro exemplo de fissão acontece quando um próton, com uma energia cinética de 0,15 MeV, penetra e é absorvido por um núcleo de lítio 7 (Fig.
 Fissão Nuclear Fissão nuclear é o processo pelo qual um núcleo de número de massa grande se divide em dois fragmentos de números de massa comparáveis. Os núcleos com número de massa grande estão sujeitos
Fissão Nuclear Fissão nuclear é o processo pelo qual um núcleo de número de massa grande se divide em dois fragmentos de números de massa comparáveis. Os núcleos com número de massa grande estão sujeitos
Física das Radiações & Radioatividade. Tecnologia em Medicina Nuclear Prof. Leonardo
 Física das Radiações & Radioatividade Tecnologia em Medicina Nuclear Prof. Leonardo ÁTOMO Menor porção da matéria que mantém as propriedades químicas do elemento químico correspondente. Possui um núcleo,
Física das Radiações & Radioatividade Tecnologia em Medicina Nuclear Prof. Leonardo ÁTOMO Menor porção da matéria que mantém as propriedades químicas do elemento químico correspondente. Possui um núcleo,
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Estrutura dos Materiais. e Engenharia dos Materiais Prof. Douglas Gouvêa
 Ligações Químicas e Estrutura dos Materiais PMT 5783 - Fundamentos de Ciência e Engenharia dos Materiais Prof. Douglas Gouvêa Objetivos Descrever a estrutura atômica e suas conseqüências no tipo de ligação
Ligações Químicas e Estrutura dos Materiais PMT 5783 - Fundamentos de Ciência e Engenharia dos Materiais Prof. Douglas Gouvêa Objetivos Descrever a estrutura atômica e suas conseqüências no tipo de ligação
Aula 5: Propriedades e Ligação Química
 Aula 5: Propriedades e Ligação Química Relacionar o tipo de ligação química com as propriedades dos materiais Um entendimento de muitas propriedades físicas dos materiais é previsto através do conhecimento
Aula 5: Propriedades e Ligação Química Relacionar o tipo de ligação química com as propriedades dos materiais Um entendimento de muitas propriedades físicas dos materiais é previsto através do conhecimento
Aula 19 Condução de Eletricidade nos Sólidos
 Aula 19 Condução de Eletricidade nos Sólidos Física 4 Ref. Halliday Volume4 Sumário Semicondutores; Semicondutores Dopados; O Diodo Retificador; Níveis de Energia em um Sólido Cristalino relembrando...
Aula 19 Condução de Eletricidade nos Sólidos Física 4 Ref. Halliday Volume4 Sumário Semicondutores; Semicondutores Dopados; O Diodo Retificador; Níveis de Energia em um Sólido Cristalino relembrando...
A descoberta da radioatividade
 10. Radioatividade Sumário Histórico da radioatividade Lei do decaimento radioativo Decaimentos alfa, beta e gama Séries radioativas Datação pelo Carbono-14 Fissão nuclear Fusão nuclear A descoberta da
10. Radioatividade Sumário Histórico da radioatividade Lei do decaimento radioativo Decaimentos alfa, beta e gama Séries radioativas Datação pelo Carbono-14 Fissão nuclear Fusão nuclear A descoberta da
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Mecânica Quântica e Indiscernibilidade
 Mecânica Quântica e Indiscernibilidade t ou ou?? Mecânica clássica Partículas discerníveis ( A, A ) ψ ( A A ) ψ =, Mecânica quântica Partículas indiscerníveis ( A, A ) ψ ( A A ) ψ = ψ, ou = ( A, A ) ψ
Mecânica Quântica e Indiscernibilidade t ou ou?? Mecânica clássica Partículas discerníveis ( A, A ) ψ ( A A ) ψ =, Mecânica quântica Partículas indiscerníveis ( A, A ) ψ ( A A ) ψ = ψ, ou = ( A, A ) ψ
SEMICONDUTORES. Condução Eletrônica
 Condução Eletrônica SEMICONDUTORES A corrente elétrica é resultante do movimento de partículas carregadas eletricamente como resposta a uma força de natureza elétrica, em função do campo elétrico aplicado.
Condução Eletrônica SEMICONDUTORES A corrente elétrica é resultante do movimento de partículas carregadas eletricamente como resposta a uma força de natureza elétrica, em função do campo elétrico aplicado.
Decaimento radioativo
 Decaimento radioativo Processo pelo qual um nuclídeo instável transforma-se em outro, tendendo a uma configuração energeticamente mais favorável. Tipos de decaimento: (Z, A) * (Z, A) (Z, A) (Z, A)! γ!
Decaimento radioativo Processo pelo qual um nuclídeo instável transforma-se em outro, tendendo a uma configuração energeticamente mais favorável. Tipos de decaimento: (Z, A) * (Z, A) (Z, A) (Z, A)! γ!
PMT Introdução à Ciência dos Materiais para Engenharia 2º semestre de 2005
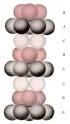 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais PROPRIEDADES ELÉTRICAS DOS MATERIAIS PMT 2100 - Introdução à Ciência dos Materiais para Engenharia
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais PROPRIEDADES ELÉTRICAS DOS MATERIAIS PMT 2100 - Introdução à Ciência dos Materiais para Engenharia
ÁTOMO: núcleo muito pequeno composto por prótons e nêutrons, que é circundado por elétrons em movimento;
 1.1 CONCEITOS FUNDAMENTAIS ÁTOMO: núcleo muito pequeno composto por prótons e nêutrons, que é circundado por elétrons em movimento; Elétrons e prótons são eletricamente carregados: 1,60 x 10-19 C; Elétrons:
1.1 CONCEITOS FUNDAMENTAIS ÁTOMO: núcleo muito pequeno composto por prótons e nêutrons, que é circundado por elétrons em movimento; Elétrons e prótons são eletricamente carregados: 1,60 x 10-19 C; Elétrons:
Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel
 Ligações químicas Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel Ligações Químicas Sacarina Vitamina E Amônia Fulereno LIGAÇÕES IÔNICAS Acontece por atração
Ligações químicas Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel Ligações Químicas Sacarina Vitamina E Amônia Fulereno LIGAÇÕES IÔNICAS Acontece por atração
Os fundamentos da Física Volume 3 1. Resumo do capítulo
 Os fundamentos da Física Volume 1 Capítulo 0 Física Nuclear AS FORÇAS FUNDAMENTAIS DA NATUREZA Força nuclear forte Mantém a coesão do núcleo atômico. Intensidade 10 8 vezes maior do que a força gravitacional.
Os fundamentos da Física Volume 1 Capítulo 0 Física Nuclear AS FORÇAS FUNDAMENTAIS DA NATUREZA Força nuclear forte Mantém a coesão do núcleo atômico. Intensidade 10 8 vezes maior do que a força gravitacional.
Como definir a estabilidade de um átomo? Depende. Eletrosfera. Núcleo. Radioatividade
 Como definir a estabilidade de um átomo? Depende Eletrosfera Ligações Núcleo Radioatividade O que é radioatividade? Tem alguma ver com radiação? Radiação eletromagnética Ampla faixa de frequência Modelos
Como definir a estabilidade de um átomo? Depende Eletrosfera Ligações Núcleo Radioatividade O que é radioatividade? Tem alguma ver com radiação? Radiação eletromagnética Ampla faixa de frequência Modelos
Como definir a estabilidade de um átomo? Depende. Eletrosfera. Núcleo. Radioatividade
 Como definir a estabilidade de um átomo? Depende Eletrosfera Ligações Núcleo Radioatividade O que é radioatividade? Tem alguma ver com radiação? Modelos atômicos Átomo grego Átomo de Thomson Átomo de
Como definir a estabilidade de um átomo? Depende Eletrosfera Ligações Núcleo Radioatividade O que é radioatividade? Tem alguma ver com radiação? Modelos atômicos Átomo grego Átomo de Thomson Átomo de
N P P N. Ciências de Materiais I Prof. Nilson C. Cruz. Aula 2 Ligação Química. Átomos. Diferença entre materiais = Diferença entre arranjos atômicos e
 Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
QB70C:// Química (Turmas S71/S72) Ligação Química
 QB70C:// Química (Turmas S71/S72) Ligação Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Formação das Ligações O modelo RPECV, baseado principalmente nas estruturas de Lewis,
QB70C:// Química (Turmas S71/S72) Ligação Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Formação das Ligações O modelo RPECV, baseado principalmente nas estruturas de Lewis,
CAPÍTULO V MATERIAIS SEMICONDUTORES
 CAPÍTULO V MATERIAIS SEMICONDUTORES 5.1 - Introdução Vimos no primeiro capítulo desta apostila uma maneira de classificar os materiais sólidos de acordo com sua facilidade de conduzir energia. Desta forma
CAPÍTULO V MATERIAIS SEMICONDUTORES 5.1 - Introdução Vimos no primeiro capítulo desta apostila uma maneira de classificar os materiais sólidos de acordo com sua facilidade de conduzir energia. Desta forma
Física Moderna 2. Aula 9. Moléculas. Tipos de ligações. Íon H2 + Iônica Covalente Outras: ponte de hidrogênio van der Waals
 Física Moderna 2 Aula 9 Moléculas Tipos de ligações Iônica Covalente Outras: Íon H2 + ponte de hidrogênio van der Waals 1 Moléculas Uma molécula é um arranjo estável de dois ou mais átomos. Por estável
Física Moderna 2 Aula 9 Moléculas Tipos de ligações Iônica Covalente Outras: Íon H2 + ponte de hidrogênio van der Waals 1 Moléculas Uma molécula é um arranjo estável de dois ou mais átomos. Por estável
Física Moderna II Aula 14
 Física Moderna II Aula 14 Marcelo G. Munhoz munhoz@if.usp.br Lab. Pelletron, sala 245 ramal 6940 Como podemos descrever o núcleo de maneira mais detalhada? n Propriedades estáticas: q Tamanho, q Massa,
Física Moderna II Aula 14 Marcelo G. Munhoz munhoz@if.usp.br Lab. Pelletron, sala 245 ramal 6940 Como podemos descrever o núcleo de maneira mais detalhada? n Propriedades estáticas: q Tamanho, q Massa,
Se as partículas A e B são os átomos que formam uma molécula diatômica, a energia potencial do sistema pode ser expressa pela seguinte função:
 Curvas de Energia Potencial Consideremos o sistema formado por duas partículas, A e B, cujos movimentos estão limitados à mesma linha reta, o eixo x do referencial. Além disso, vamos considerar que o referencial
Curvas de Energia Potencial Consideremos o sistema formado por duas partículas, A e B, cujos movimentos estão limitados à mesma linha reta, o eixo x do referencial. Além disso, vamos considerar que o referencial
Aplicações de Semicondutores em Medicina
 Aplicações de Semicondutores em Medicina A estrutura dos cristais semicondutores Luiz Antonio Pereira dos Santos CNEN-CRCN PRÓ-ENGENHARIAS UFS-IPEN-CRCN Aracaju Março - 010 Como é a estrutura da matéria?
Aplicações de Semicondutores em Medicina A estrutura dos cristais semicondutores Luiz Antonio Pereira dos Santos CNEN-CRCN PRÓ-ENGENHARIAS UFS-IPEN-CRCN Aracaju Março - 010 Como é a estrutura da matéria?
Estrutura atômica e ligação interatômica. Profa. Daniela Becker
 Estrutura atômica e ligação interatômica Profa. Daniela Becker Referências Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 2, 2002. Shackelford, J.F. Ciências dos
Estrutura atômica e ligação interatômica Profa. Daniela Becker Referências Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 2, 2002. Shackelford, J.F. Ciências dos
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
Física Moderna II Aula 25
 Universidade de São Paulo Instituto de Física 2 º Semestre de 2015 Profa. Márcia de Almeida Rizzutto Oscar Sala sala 220 rizzutto@if.usp.br Física Moderna II Aula 25 Monitor: Gabriel M. de Souza Santos
Universidade de São Paulo Instituto de Física 2 º Semestre de 2015 Profa. Márcia de Almeida Rizzutto Oscar Sala sala 220 rizzutto@if.usp.br Física Moderna II Aula 25 Monitor: Gabriel M. de Souza Santos
Aula -12. Condução elétrica em sólidos
 Aula -12 Condução elétrica em sólidos A diversidade atômica Os sólidos cristalinos Os sólidos cristalinos: Exemplos em uma pequena janela Os sólidos cristalinos: Exemplos em uma pequena janela A diversidade
Aula -12 Condução elétrica em sólidos A diversidade atômica Os sólidos cristalinos Os sólidos cristalinos: Exemplos em uma pequena janela Os sólidos cristalinos: Exemplos em uma pequena janela A diversidade
Descoberta do núcleo. Forças nucleares. Nuclídeos experimento de Rutherford Núcleo pequeno e positivo
 Descoberta do núcleo 1911- experimento de Rutherford Núcleo pequeno e positivo Raio nuclear: fentometro (1 fm = 10-15 m) Razão entre os raios (r): r núcleo / r átomo = 10-4 Forças nucleares Prótons muito
Descoberta do núcleo 1911- experimento de Rutherford Núcleo pequeno e positivo Raio nuclear: fentometro (1 fm = 10-15 m) Razão entre os raios (r): r núcleo / r átomo = 10-4 Forças nucleares Prótons muito
CURSO DE RADIOPROTEÇÃO COM ÊNFASE NO USO, PREPARO E MANUSEIO DE FONTES RADIOATIVAS NÃO SELADAS
 CURSO DE RADIOPROTEÇÃO COM ÊNFASE NO USO, PREPARO E MANUSEIO DE FONTES RADIOATIVAS NÃO SELADAS Walter Siqueira Paes DIVISÃO DE HIGIENE, SEGURANÇA E MEDICINA DO TRABALHO SETOR DE PROTEÇÃO RADIOLÓGICA PROGRAMAÇÃO
CURSO DE RADIOPROTEÇÃO COM ÊNFASE NO USO, PREPARO E MANUSEIO DE FONTES RADIOATIVAS NÃO SELADAS Walter Siqueira Paes DIVISÃO DE HIGIENE, SEGURANÇA E MEDICINA DO TRABALHO SETOR DE PROTEÇÃO RADIOLÓGICA PROGRAMAÇÃO
Introdução à Astrofísica. Lição 21 Fontes de Energia Estelar
 Introdução à Astrofísica Lição 21 Fontes de Energia Estelar A taxa de energia que sai de uma estrela é extremamente grande, contudo ainda não tratamos da questão que relaciona à fonte de toda essa energia.
Introdução à Astrofísica Lição 21 Fontes de Energia Estelar A taxa de energia que sai de uma estrela é extremamente grande, contudo ainda não tratamos da questão que relaciona à fonte de toda essa energia.
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA
 NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 11 MOLÉCULAS Primeira Edição junho de 2005 CAPÍTULO 11 MOLÉCULAS ÍNDICE 11-1- Introdução 11.2- Ligação por Tunelamento e a Molécula
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 11 MOLÉCULAS Primeira Edição junho de 2005 CAPÍTULO 11 MOLÉCULAS ÍNDICE 11-1- Introdução 11.2- Ligação por Tunelamento e a Molécula
Leonnardo Cruvinel Furquim PROCESSOS NUCLEARES
 Leonnardo Cruvinel Furquim PROCESSOS NUCLEARES Radioatividade Três espécies de emissões radioativas naturais foram identificadas e caracterizadas e foi demonstrado que todas são emitidas pelo núcleo atomico,
Leonnardo Cruvinel Furquim PROCESSOS NUCLEARES Radioatividade Três espécies de emissões radioativas naturais foram identificadas e caracterizadas e foi demonstrado que todas são emitidas pelo núcleo atomico,
Químicas. Profa. Ms. Loraine Cristina do Valle Jacobs DAQBI.
 Ligações Químicas Profa. Ms. Loraine Cristina do Valle Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Ligações Metálicas LIGAÇÕES METÁLICAS Os metais são materiais
Ligações Químicas Profa. Ms. Loraine Cristina do Valle Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Ligações Metálicas LIGAÇÕES METÁLICAS Os metais são materiais
Raios-x. Proteção e higiene das Radiações Profª: Marina de Carvalho CETEA
 Raios-x Proteção e higiene das Radiações Profª: Marina de Carvalho CETEA Materiais Radioativos 1896 o físico Francês Becquerel descobriu que sais de Urânio emitia radiação capaz de produzir sombras de
Raios-x Proteção e higiene das Radiações Profª: Marina de Carvalho CETEA Materiais Radioativos 1896 o físico Francês Becquerel descobriu que sais de Urânio emitia radiação capaz de produzir sombras de
Aula 18 Condução de Eletricidade nos Sólidos
 Aula 18 Condução de Eletricidade nos Sólidos Física 4 Ref. Halliday Volume4 Sumário Capítulo 41: Condução de Eletricidade nos Sólidos Propriedades Elétricas dos Sólidos Níveis de Energia em um Sólido Cristalino
Aula 18 Condução de Eletricidade nos Sólidos Física 4 Ref. Halliday Volume4 Sumário Capítulo 41: Condução de Eletricidade nos Sólidos Propriedades Elétricas dos Sólidos Níveis de Energia em um Sólido Cristalino
Física dos Semicondutores
 Física dos Semicondutores Resistividade Condutor (fácil fluxo de cargas) Semicondutor Isolante (difícil fluxo de cargas) COBRE: r = 10-6 W.cm GERMÂNIO: r = 50 W.cm SILÍCIO: r = 50 x 10-3 W.cm MICA: r =
Física dos Semicondutores Resistividade Condutor (fácil fluxo de cargas) Semicondutor Isolante (difícil fluxo de cargas) COBRE: r = 10-6 W.cm GERMÂNIO: r = 50 W.cm SILÍCIO: r = 50 x 10-3 W.cm MICA: r =
Espectros moleculares
 E r Espectros moleculares 2 + v = 2 2I 1 [ r( r + 1) ] + ( v + ) ω Transições ópticas (emissão ou absorção de fótons) entre os níveis E 1 e E 2 : f = E 2 E 1 /h ou ΔE = ±hf. Regras de seleção continuam
E r Espectros moleculares 2 + v = 2 2I 1 [ r( r + 1) ] + ( v + ) ω Transições ópticas (emissão ou absorção de fótons) entre os níveis E 1 e E 2 : f = E 2 E 1 /h ou ΔE = ±hf. Regras de seleção continuam
A Estrutura dos Materiais. Conceitos Gerais
 A Estrutura dos Materiais Conceitos Gerais CAPA BIOMIMETISMO O material Fita adesiva para procedimentos cirúrgicos - Aderência mesmo em ambientes úmidos - Biodegradável - Não dissolve - Não dissolve durante
A Estrutura dos Materiais Conceitos Gerais CAPA BIOMIMETISMO O material Fita adesiva para procedimentos cirúrgicos - Aderência mesmo em ambientes úmidos - Biodegradável - Não dissolve - Não dissolve durante
PRINCÍPIO BÁSICO: Isótopo Estável + Partícula incidente (n, p, a, g ) Isótopo Radioativo + Partículas emitidas. Medida das radiações emitidas
 Radioquímica PRINCÍPIO BÁSICO: Isótopo Estável + Partícula incidente (n, p, a, g ) Isótopo Radioativo + Partículas emitidas (n, p, a, g ) Medida das radiações emitidas O Núcleo Atómico Importância de A
Radioquímica PRINCÍPIO BÁSICO: Isótopo Estável + Partícula incidente (n, p, a, g ) Isótopo Radioativo + Partículas emitidas (n, p, a, g ) Medida das radiações emitidas O Núcleo Atómico Importância de A
QUESTÕES DE FÍSICA MODERNA
 QUESTÕES DE FÍSICA MODERNA 1) Em diodos emissores de luz, conhecidos como LEDs, a emissão de luz ocorre quando elétrons passam de um nível de maior energia para um outro de menor energia. Dois tipos comuns
QUESTÕES DE FÍSICA MODERNA 1) Em diodos emissores de luz, conhecidos como LEDs, a emissão de luz ocorre quando elétrons passam de um nível de maior energia para um outro de menor energia. Dois tipos comuns
TEORIAS ATÔMICAS. Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807)
 TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
Interação da radiação com a matéria
 Interação da radiação com a matéria 8 a aula/9 ª aula i - INTRODUÇÃO ii - IONIZAÇÃO, EXCITAÇÃO, ATIVAÇÃO E RADIAÇÃO DE FRENAGEM iii RADIAÇÕES DIRETAMENTE IONIZANTES iv RADIAÇOES INDIRETAMENTE IONIZANTES
Interação da radiação com a matéria 8 a aula/9 ª aula i - INTRODUÇÃO ii - IONIZAÇÃO, EXCITAÇÃO, ATIVAÇÃO E RADIAÇÃO DE FRENAGEM iii RADIAÇÕES DIRETAMENTE IONIZANTES iv RADIAÇOES INDIRETAMENTE IONIZANTES
Aula 21 Física Nuclear
 Aula 21 Física 4 Ref. Halliday Volume4 Sumário Descobrindo o Núcleo; Algumas Propriedades Nucleares; Decaimento Radioativo; Decaimento Alfa; Decaimento Beta; Radiação Ionizante; Analisando os dados, Rutherford
Aula 21 Física 4 Ref. Halliday Volume4 Sumário Descobrindo o Núcleo; Algumas Propriedades Nucleares; Decaimento Radioativo; Decaimento Alfa; Decaimento Beta; Radiação Ionizante; Analisando os dados, Rutherford
Física Molecular Estrutura das Ligações Químicas
 Física Molecular Estrutura das Ligações Químicas 100 É razoável focalizar o estudo de moléculas nas interações entre elétrons e núcleos já reagrupados em caroço atômico (núcleo + camadas fechadas internas),
Física Molecular Estrutura das Ligações Químicas 100 É razoável focalizar o estudo de moléculas nas interações entre elétrons e núcleos já reagrupados em caroço atômico (núcleo + camadas fechadas internas),
Química Básica: Profa. Alessandra Barone
 Química Básica: Átomo Profa. Alessandra Barone www.profbio.com.br Átomo Fermions: formam a matéria Bósons: intermedeiam forças Quarks e leptons -Glúone fóton Partículas Quark up Quark down Quark charmoso
Química Básica: Átomo Profa. Alessandra Barone www.profbio.com.br Átomo Fermions: formam a matéria Bósons: intermedeiam forças Quarks e leptons -Glúone fóton Partículas Quark up Quark down Quark charmoso
Estrutura Atômica e Ligações Químicas. Conceitos
 Estrutura Atômica e Ligações Químicas Conceitos Estrutura esquemática do átomo de sódio 2003 Brooks/Cole Publishing / Thomson Learning A dualidade da matéria (partícula/onda) Louis de Broglie: λ h m.v
Estrutura Atômica e Ligações Químicas Conceitos Estrutura esquemática do átomo de sódio 2003 Brooks/Cole Publishing / Thomson Learning A dualidade da matéria (partícula/onda) Louis de Broglie: λ h m.v
Figura 1: Fotos dos cogumelos formados após a explosão das bombas nucleares Little Boy (à esquerda Hiroshima) e Fat Man (à direita Nagasaki).
 O Núcleo Atômico É do conhecimento de todos o enorme poder energético contido no núcleo dos átomos! Quem nunca ouviu falar sobre as bombas nucleares que foram lançadas, no final da II Guerra Mundial, nas
O Núcleo Atômico É do conhecimento de todos o enorme poder energético contido no núcleo dos átomos! Quem nunca ouviu falar sobre as bombas nucleares que foram lançadas, no final da II Guerra Mundial, nas
PROPRIEDADES TÉRMICAS E ÓPTICAS DOS MATERIAIS
 UNIVERSIDADE FEDERAL DO ABC Centro de Engenharia, Modelagem e Ciências Sociais Aplicadas (CECS) BC-1105: MATERIAIS E SUAS PROPRIEDADES PROPRIEDADES TÉRMICAS E ÓPTICAS DOS MATERIAIS Introdução Propriedades
UNIVERSIDADE FEDERAL DO ABC Centro de Engenharia, Modelagem e Ciências Sociais Aplicadas (CECS) BC-1105: MATERIAIS E SUAS PROPRIEDADES PROPRIEDADES TÉRMICAS E ÓPTICAS DOS MATERIAIS Introdução Propriedades
Dosimetria e Proteção Radiológica
 Dosimetria e Proteção Radiológica Prof. Dr. André L. C. Conceição Departamento Acadêmico de Física (DAFIS) Programa de Pós-Graduação em Engenharia Elétrica e Informática Industrial (CPGEI) Universidade
Dosimetria e Proteção Radiológica Prof. Dr. André L. C. Conceição Departamento Acadêmico de Física (DAFIS) Programa de Pós-Graduação em Engenharia Elétrica e Informática Industrial (CPGEI) Universidade
Aula 19 Condução de Eletricidade nos Sólidos
 Aula 19 Condução de Eletricidade nos Sólidos Física 4 Ref. Halliday Volume4 Sumário Semicondutores; Semicondutores Dopados; O Diodo Retificador; Níveis de Energia em um Sólido Cristalino relembrando...
Aula 19 Condução de Eletricidade nos Sólidos Física 4 Ref. Halliday Volume4 Sumário Semicondutores; Semicondutores Dopados; O Diodo Retificador; Níveis de Energia em um Sólido Cristalino relembrando...
Aula anterior. Equação de Schrödinger a 3 dimensões. d x 2m - E -U. 2m - E -U x, y, z. x y z x py pz cin cin. E E ( x, y,z ) - 2m 2m x y z
 6/Maio/2013 Aula 21 Efeito de túnel quântico: decaimento alfa. Aplicações: nanotecnologias; microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. Átomo de hidrogénio Modelo de Bohr 8/Maio/2013
6/Maio/2013 Aula 21 Efeito de túnel quântico: decaimento alfa. Aplicações: nanotecnologias; microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. Átomo de hidrogénio Modelo de Bohr 8/Maio/2013
Forças Intermoleculares
 Forças Intermoleculares Você já se perguntou por que a água forma gotas ou como os insetos conseguem caminhar sobre a água? Gota d'água caindo sobre a superfície da água. Inseto pousado sobre a superfície
Forças Intermoleculares Você já se perguntou por que a água forma gotas ou como os insetos conseguem caminhar sobre a água? Gota d'água caindo sobre a superfície da água. Inseto pousado sobre a superfície
CAPÍTULO 41 HALLIDAY, RESNICK. 8ª EDIÇÃO
 FÍSICA QUÂNTICA: CONDUÇÃO M SÓLIDOS Prof. André L. C. Conceição DAFIS CAPÍTULO 41 HALLIDAY, RSNICK. 8ª DIÇÃO Condução em sólidos Revisão 1) Átomos podem ser agrupados em famílias 1 Revisão 2) Momento angular
FÍSICA QUÂNTICA: CONDUÇÃO M SÓLIDOS Prof. André L. C. Conceição DAFIS CAPÍTULO 41 HALLIDAY, RSNICK. 8ª DIÇÃO Condução em sólidos Revisão 1) Átomos podem ser agrupados em famílias 1 Revisão 2) Momento angular
ESTADO SÓLIDO. paginapessoal.utfpr.edu.br/lorainejacobs. Profª. Loraine Jacobs
 ESTADO SÓLIDO lorainejacobs@utfpr.edu.br paginapessoal.utfpr.edu.br/lorainejacobs Profª. Loraine Jacobs Estado Sólido Tradicionalmente, um sólido é definido como uma substância que mantém um volume e uma
ESTADO SÓLIDO lorainejacobs@utfpr.edu.br paginapessoal.utfpr.edu.br/lorainejacobs Profª. Loraine Jacobs Estado Sólido Tradicionalmente, um sólido é definido como uma substância que mantém um volume e uma
Lista elaborado por coletânea de exercícios, traduzida e organizado por Emerson Itikawa sob supervisão do Prof. Eder R. Moraes
 Física Nuclear e Decaimento 1) (HOBBIE, R.K.; Interm Phys Med Bio) Calcular a energia de ligação, e a energia de ligação por núcleon, a partir das massas dadas, para os nuclídeos (a) 6 Li, (b) 12 C, (c)
Física Nuclear e Decaimento 1) (HOBBIE, R.K.; Interm Phys Med Bio) Calcular a energia de ligação, e a energia de ligação por núcleon, a partir das massas dadas, para os nuclídeos (a) 6 Li, (b) 12 C, (c)
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 7 SOLUÇÕES DA EQUAÇÃO DE SCHRÖDINGER INDEPENDENTE DO TEMPO Primeira Edição junho de 2005 CAPÍTULO 07 SOLUÇÕES DA EQUAÇÃO DE SCHRÖDINGER
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 7 SOLUÇÕES DA EQUAÇÃO DE SCHRÖDINGER INDEPENDENTE DO TEMPO Primeira Edição junho de 2005 CAPÍTULO 07 SOLUÇÕES DA EQUAÇÃO DE SCHRÖDINGER
Ciências dos materiais- 232
 1 Ciências dos materiais- 232 2 a aula - Ligações químicas - Estruturas Cristalinas Quinta Quinzenal Semana par 10/03/2015 1 Professor: Luis Gustavo Sigward Ericsson Curso: Engenharia Mecânica Série: 5º/
1 Ciências dos materiais- 232 2 a aula - Ligações químicas - Estruturas Cristalinas Quinta Quinzenal Semana par 10/03/2015 1 Professor: Luis Gustavo Sigward Ericsson Curso: Engenharia Mecânica Série: 5º/
Fissão Nuclear. Danilo Leal Raul Miguel Angel Mosquera Molina
 Fissão Nuclear Danilo Leal Raul Miguel Angel Mosquera Molina Estados Excitados dos Núcleos Cada um dos estados de muitas partículas num grupo tem o mesmo impulso angular e paridade que o estado da partícula
Fissão Nuclear Danilo Leal Raul Miguel Angel Mosquera Molina Estados Excitados dos Núcleos Cada um dos estados de muitas partículas num grupo tem o mesmo impulso angular e paridade que o estado da partícula
Eletrônica I. Prof. Cláudio Henrique A. Rodrigues
 Eletrônica I 1 2 Qual o significado de um corpo eletricamentecarregado? A Carga Elétrica é positiva (+) ou negativa(-)? 3 Um corpo apresenta-se eletricamente neutro quando o número total de prótons e de
Eletrônica I 1 2 Qual o significado de um corpo eletricamentecarregado? A Carga Elétrica é positiva (+) ou negativa(-)? 3 Um corpo apresenta-se eletricamente neutro quando o número total de prótons e de
Cap. 10. Interiores Estelares. Fontes de energia. Transporte de energia: radiação. AGA 0293, Astro?sica Estelar Jorge Meléndez
 Cap. 10. Interiores Estelares. Fontes de energia. Transporte de energia: radiação AGA 0293, Astro?sica Estelar Jorge Meléndez Equação de Conservação de Massa dm r = ρ dv dr Equilíbrio hidrostálco P+dP
Cap. 10. Interiores Estelares. Fontes de energia. Transporte de energia: radiação AGA 0293, Astro?sica Estelar Jorge Meléndez Equação de Conservação de Massa dm r = ρ dv dr Equilíbrio hidrostálco P+dP
Descoberta o elétron século XIX por Thomsom. Próton - - século XX por Rutherford. Neutron 1932 por Chadwick
 Estrutura Atômica Átomo 3 partículas Quais são? Descoberta o elétron século XIX por Thomsom Próton - - século XX por Rutherford Neutron 1932 por Chadwick Modelo atômico Núcleo prótons e neutros Elétrons
Estrutura Atômica Átomo 3 partículas Quais são? Descoberta o elétron século XIX por Thomsom Próton - - século XX por Rutherford Neutron 1932 por Chadwick Modelo atômico Núcleo prótons e neutros Elétrons
Materiais Semicondutores
 Materiais Semicondutores 1 + V - V R.I A I R.L A L Resistividade (W.cm) Material Classificação Resistividade ( ) Cobre Condutor 10-6 [W.cm] Mica Isolante 10 12 [W.cm] Silício (S i ) Semicondutor 50.10
Materiais Semicondutores 1 + V - V R.I A I R.L A L Resistividade (W.cm) Material Classificação Resistividade ( ) Cobre Condutor 10-6 [W.cm] Mica Isolante 10 12 [W.cm] Silício (S i ) Semicondutor 50.10
Materiais e Equipamentos Elétricos. Aula 5 Materiais semicondutores
 Materiais e Equipamentos Elétricos Aula 5 Semicondutores são sólidos cristalinos com condutividade intermediária entre condutores e isolantes Silício (Si), germânio (Ge) Possuem 4 elétrons na camada de
Materiais e Equipamentos Elétricos Aula 5 Semicondutores são sólidos cristalinos com condutividade intermediária entre condutores e isolantes Silício (Si), germânio (Ge) Possuem 4 elétrons na camada de
A Tabela Periódica pode ser um guia para a ordem na qual os orbitais são preenchidos...
 Aula 02 - Tabela Periódica TABELA PERIÓDICA e Lothar Meyer A Tabela Periódica pode ser um guia para a ordem na qual os orbitais são preenchidos... Pode-se escrever a distribuição eletrônica de um elemento
Aula 02 - Tabela Periódica TABELA PERIÓDICA e Lothar Meyer A Tabela Periódica pode ser um guia para a ordem na qual os orbitais são preenchidos... Pode-se escrever a distribuição eletrônica de um elemento
As constantes acima são determinadas experimentalmente: b1 = 14 MeV b2 = 13 MeV. A Z b5 par par -33,5MeV impar 0 par impar 33,5MeV
 Parte I Modelos Nucleares. Modelo da Gota Liquida. C. von Weiszäcker reconheceu, em 1935, que as propriedades nucleares associadas com o tamanho, a massa e a energia de ligação de um núcleo são similares
Parte I Modelos Nucleares. Modelo da Gota Liquida. C. von Weiszäcker reconheceu, em 1935, que as propriedades nucleares associadas com o tamanho, a massa e a energia de ligação de um núcleo são similares
