Física Geral e Experimental III
|
|
|
- Rodrigo Marinho Brunelli
- 7 Há anos
- Visualizações:
Transcrição
1 Física Geral e Experimental III Temperatura e Calor Um dos principais ramos da física e da engenharia é a termodinâmica, que é o estudo das leis que regem a relação entre calor, trabalho e outras formas de energia. Temperatura A temperatura é uma das sete grandezas fundamentais no SI. A unidade mais utilizada pelos físicos é o kelvin (K). Quando um corpo é aquecido ou resfriado, algumas de suas propriedades físicas se alteram. Se um sólido ou um líquido é aquecido, seu volume usualmente aumenta. Se um gás é aquecido e sua pressão é mantida constante, seu volume aumenta. No entanto, se um gás é aquecido e seu volume é mantido constante, é sua pressão que aumenta. Uma propriedade física que varia com a temperatura é chamada de propriedade termométrica. Uma variação de uma propriedade termométrica indica uma variação da temperatura de um corpo.
2 Seja uma barra de cobre aquecida colocada em contato com uma barra de ferro resfriada, de forma que a barra de cobre esfria e a barra de ferro aquece. Dizemos que as duas barras estão em contato térmico. A barra de cobre se contrai levemente ao ser resfriada e a barra de ferro se expande levemente ao ser aquecida. Quando este processo termina, os comprimentos das barras passam a ser constantes. Então, as duas barras estão em equilíbrio térmico entre si. Suponha agora que uma barra aquecida de cobre seja colocada em uma corrente de água fria. A barra esfria até parar de se contrair, quando estiver em equilíbrio térmico com a água. Depois, colocamos uma barra fria de ferro na corrente, próximo da barra de cobre, mas sem tocá-la. A barra de ferro se aquecerá até também atingir o equilíbrio térmico com a água. Se tomarmos as barras e as colocarmos em contato térmico entre si, verificamos que seus comprimentos não variam. Elas estão em equilíbrio térmico entre si. Esta situação ilustra a lei zero da termodinâmica. Se dois corpos estão em equilíbrio térmico com um terceiro, então os três corpos estão em equilíbrio térmico entre si. (Lei Zero da Termodinâmica) Em uma linguagem menos formal, a lei nos diz o seguinte: Todo corpo possui uma propriedade chamada temperatura. Quando dois corpos estão em equilíbrio térmico, suas temperaturas são iguais e vice-versa. A lei zero foi formulada tardiamente, depois da primeira e da segunda lei da termodinâmica. Como o conceito de temperatura é fundamental para essas duas leis, a lei que estabelece a T como um conceito válido deve ter uma numeração menor, por isso zero. Medindo a Temperatura O ponto triplo da água Para criar uma escala de T escolhemos um fenômeno térmico reprodutível e, arbitrariamente, atribuímos a ele uma temperatura. Poderíamos, por exemplo,
3 escolher o ponto de fusão do gelo ou o ponto de ebulição da água, mas, por razões técnicas, foi optado pelo ponto triplo da água. A água, o gelo e o vapor de água podem coexistir, em equilíbrio térmico, para apenas um conjunto de valores de pressão e temperatura. A figura a seguir mostra uma célula de ponto triplo, obtido em laboratório. Foi atribuído ao ponto triplo da água o valor de 273,16 K: T 3 = 273,16 K (temperatura do ponto triplo) O termômetro de gás a volume constante O termômetro padrão, em relação ao qual todos os outros termômetros são calibrados, se baseia na pressão de um gás em um volume fixo. Ele é composto por um bulbo cheio de gás ligado por um tubo a um manômetro de mercúrio. Levantando ou baixando o reservatório R é sempre possível fazer com que o nível de mercúrio no lado esquerdo do tubo em U fique no zero da escala para manter o volume do gás constante. As escalas de temperatura Celsius e Fahrenheit A escala Kelvin é usada principalmente por cientistas. A escala Fahrenheit é mais comum nos Estados Unidos. Usualmente, podemos utilizar a seguinte relação:
4 C 5 = K = F 32 9 O conceito de zero absoluto foi criado pelo físico William Thonsom e ocorre quando um corpo não contém energia alguma, e suas moléculas estão paradas. O conceito de zero absoluto corresponderia à temperatura mais baixa existente. Até bem pouco tempo, se acreditava que o zero absoluto jamais poderia ser alcançado. No entanto, cientistas da universidade alemã Ludwig Maximilian (2013) foram capazes de alcançar e ultrapassar o zero absoluto (em bilionésimos de kelvin). Essa proeza foi alcançada com a ajuda de lasers e campos magnéticos, através da criação de um gás quântico com átomos de potássio, alinhados adequadamente. A nova técnica criada pelos alemães abre portas para o desenvolvimento de dispositivos quânticos e materiais com temperatura abaixo de 0 Kelvin. Em baixas temperaturas um corpo pode passar por três efeitos colaterais: a supercondutividade, a superfluidez e a condensação de Bose-Einstein. Como supercondutor, ele cria um campo magnético que seria capaz de levitar um imã. Já a superfluidez, com a ausência de resistência mecânica, permitiria que um líquido subisse pelas paredes de um copo. A última teoria, a de Bose-Einstein, é a de que o comportamento da matéria muda radicalmente um corpo composto de diversas partículas agiria como um condensado, ou seja, como um único átomo gigante.
5 Dilatação térmica Às vezes, para conseguir abrir a tampa metálica de um pote de vidro basta colocar o pote debaixo de uma torneira de água quente. Tanto o metal da tampa quanto o vidro do pote se expandem quando a água quente fornece energia aos átomos (com a energia adicional, os átomos se afastam mais uns dos outros, atingindo um novo ponto de equilíbrio com as forças elásticas interatômicas que mantém os átomos unidos em um sólido). Entretanto, como os átomos no metal se afastam mais uns dos outros que os átomos do vidro, a tampa se dilata mais do que o pote e, portanto, fica frouxa. Esse processo é chamado de dilatação térmica. E cada material tem capacidades diferentes de dilatação. Dilatação linear Se a temperatura de uma barra metálica de comprimento L aumenta de um valor T, seu comprimento aumento de um valor L = Lα T onde é uma constante chamada coeficiente de dilatação linear (C 0-1 ou K -1 ). Embora varie ligeiramente com a T, na maioria dos casos pode ser considerado constante para um dado material. A dilatação térmica de um sólido é como a ampliação de uma fotografia, exceto pelo fato de que ocorre nas três dimensões.
6 Dilatação Volumétrica Se todas as dimensões de um sólido aumentam com a temperatura, é evidente que o volume do sólido aumente também. No caso dos líquidos, a dilatação volumétrica é a única que faz sentido. Se a T de um sólido ou de um líquido cujo volume V aumenta de um valor T, o aumento do volume correspondente é V = V β T Onde é o coeficiente de dilataçao volumétrica do sólido ou líquido. Os coeficientes de dilatação volumétrica e de dilatação linear de um sólido estão relacionados através da equação β = 3 α O líquido mais comum, a água, não se comporta como outros líquidos. Acima de 4ºC a água se dilata quando a T aumenta, como era de se esperar. Entre 0 E 4ºC, porém, a água se contrai quando a T aumenta. Assim, por volta de 4ºC a massa específica da água passa por um máximo. Esse comportamento da água é a razão pela qual os lagos congelam de cima para baixo, e não o contrário. Quando a água da superfície é resfriada a partir de, digamos, 10ºC, em direção ao ponto de congelamento, ela fica mais densa que a água abaixo dela, e afunda. Abaixo de 4ºC, porém, um resfriamento adicional faz com que a água que está na superfície fique menos densa que a água abaixo dela,
7 e ela permanece na superfície até congelar. Se os lagos congelassem de baixo para cima, o gelo assim formado não derreteria totalmente no verão, pois ele estaria isolado pela água mais acima. Após alguns anos, muitos mares e lagos nas zonas temperadas da Terra permaneceriam congelados o ano inteiro, o que tornaria impossível a vida aquática. Temperatura e Calor Dois corpos com diferentes temperaturas entram em contato e a temperatura destes dois corpos se iguala e o equilíbrio térmico é estabelecido. Essa variação de temperatura se deve a uma mudança da energia térmica do sistema por causa da troca de energia entre o sistema e o ambiente. A energia transferida é chamada de calor e é simbolizada pela letra Q. O calor é positivo se a energia é transferida do ambiente para a energia térmica do sistema (dizemos que o calor é absorvido pelo sistema). O calor é negativo quando a energia é transferida da energia térmica do sistema para o ambiente (dizemos que o calor é cedido ou perdido pelo sistema). A figura a seguir representa a transferência de energia. Na primeira situação (a), TS > TA, ou seja, a energia é transferida do sistema (TS) para o ambiente (TA), de modo que Q é negativo. Na situação (b), TS = TA, e não há transferência de energia, Q é zero e não há calor cedido nem absorvido. Na situação (c), TS < TA, e a transferência é do ambiente para o sistema, e Q é positivo. Assim, chegamos à seguinte definição de calor:
8 Calor é a energia transferida de um sistema para o ambiente ou vice-versa devido a uma diferença de temperatura. A energia também pode ser transferida de um sistema para o ambiente ou vice-versa através do trabalho W realizado por uma força. Ao contrário da temperatura, pressão e volume, o calor e o trabalho não são propriedades intrínsecas de um sistema; tem significado apenas quando descrevem a transferência de energia para dentro ou para fora do sistema. Antes que os cientistas percebessem que o calor é energia transferida, o calor era medido em termos da capacidade de aumentar a temperatura da água. Assim, a caloria (cal) foi definida como a quantidade de calor necessária para aumentar a temperatura de 1 g de água de 14,5ºC para 15,5ºC. Como calor é energia transferida, a unidade de calor no SI é a mesma de energia, ou seja, o joule. A caloria é definida como 4,1868 J, sem qualquer referência ao aquecimento da água. A Absorção de Calor por Sólidos e Líquidos Capacidade Térmica A capacidade térmica C de um objeto é a constante de proporcionalidade entre o calor Q recebido ou cedido por um objeto e a variação de temperatura T do objeto, ou ainda, a variação de energia interna necessária para aumentar em um grau a temperatura de uma amostra: Q = C T = C (T f T i ) onde Ti e Tf são as temperaturas inicial e final do objeto, respectivamente. A capacidade térmica C é medida em unidades de energia por grau ou energia por Kelvin. Calor Específico Dois objetos feitos do mesmo material têm capacidades térmicas proporcionais a suas massas. Assim, é conveniente definir como capacidade
9 térmica por unidade de massa, ou calor específico c, que se refere não a um objeto, mas a uma massa unitária do material de que é feito o objeto. Assim: Q = m c T Calor Específico Molar Em algumas situações, a unidade mais conveniente para especificar a quantidade de uma substância é o mol, ou seja: 1 mol = 6,02 x unidades elementares Quando a quantidade de uma substância é expressa em mols o calor específico deve ser expresso na forma de quantidade de calor por mol, ou seja, é o calor específico molar. Calores de Transformação Quando calor é transferido para uma amostra sólida ou líquida nem sempre a T aumenta. Em vez disso, a amostra pode mudar de fase.
10 Fundir um sólido significa fazê-lo passar do estado sólido para o líquido. Este processo requer energia porque os átomos ou moléculas do sólido devem ser liberados de sua estrutura rígida. Solidificar um líquido é o inverso de fundir, e exige a retirada de energia do líquido para que os átomos ou moléculas voltem a formar a estrutura rígida de um sólido. Vaporizar um líquido significa fazê-lo passar do estado líquido para o estado gasoso. Este processo também requer energia porque os átomos ou moléculas devem ser liberados de seus aglomerados. Condensar um gás é o inverso de vaporizar e exige a retirada de energia para que os átomos voltem a se aglomerar. A quantidade de energia por unidade de massa que deve ser transferida em forma de calor para que uma amostra mude totalmente de fase é chamada de calor de transformação, L. Quando uma amostra de massa m sofre uma mudança de fase a energia total transferida é Q = L m Quando a mudança é da fase líquida para a gasosa ou da fase gasosa para a líquida, o calor de transformação é chamado de calor de vaporização, Lv. Para a água à T normal de vaporização é L V = 539 cal g kj = 40,7 = 2256 kj/kg mol Quando a mudança é da fase sólida para a fase líquida ou da líquida para a sólida, o calor de transformação é chamado de calor de fusão e representado por LF. Para a água à T normal de solidificação ou de fusão é: L F = 79,5 cal g kj = 6,01 = 333 kj/kg mol
11 Calor e Trabalho Um gás pode trocar energia com o ambiente através do trabalho. O trabalho W realizado por um gás quando ao se expandir ou se contrair de um volume inicial Vi para um volume final Vf é dado por: V = volume [ m 3 ] p = pressão [Pa] V f W = dw = p dv [ J ] V i Primeira Lei da Termodinâmica A lei de conservação da energia para os processos termodinâmicos é expressa através da primeira lei da termodinâmica, que pode assumir duas formas: E int = E int,f E int,i = Q W ou de int = dq dw E int = energia interna do material (depende apenas do estado material, T, P e V); [J]. Q = energia trocada entre o sistema e o ambiente na forma de calor (Q é positivo se o sistema absorve calor e negativo se o sistema libera calor); [ J ]. W = trabalho realizado pelo sistema (W é positivo se o sistema se expande contra uma força externa e negativo se o sistema se contrai sob o efeito de uma força externa); [ J ]. Aplicações da Primeira Lei Processos Adiabáticos: Acontece tão depressa ou em um sistema tão bem isolado que não há trocas de calor entre o sistema e o ambiente. Fazendo Q = 0 na primeira lei, obtemos: E int = W
12 Processos a volume constante: Se o volume de um sistema (como um gás) é mantido constante, o sistema não pode realizar trabalho. Fazendo W = 0 na primeira lei, obtemos: E int = Q Processos cíclicos: Existem processos nos quais, após certas trocas de calor e de trabalho, o sistema volta ao estado inicial. Nesse caso, nenhuma propriedade intrínseca do sistema (incluindo a energia interna) pode variar. Fazendo E int = 0 na primeira lei, obtemos: Q = W Expansões livres: São processos adiabáticos nos quais nenhum trabalho é realizado. Assim, Q = W = 0 e, de acordo com a primeira lei: E int = 0 Tabela 1: A Primeira Lei da Termodinâmica: quatro casos especiais. Mecanismos de Transferência de Calor Existem três mecanismos e transferência de calor: condução, convecção e radiação. Condução:
13 Se você deixar uma panela com cabo de metal no fogo por algum tempo o cabo da panela fica quente. A energia é transferida da panela para o cabo por condução. Os elétrons e átomos da panela vibram intensamente por causa da alta temperatura a que estão expostos. Essas vibrações, e a energia associada, são transferidas para o cabo através de colisões entre os átomos. P cond = Q t = k A T Q T F L [J/s] Pcond = taxa de condução [ J/s ] k = condutividade térmica (variável para cada material) [ W/m.K ] A = área [ m 2 ] L = espessura [ m ] TQ e TF = temperaturas da fonte quente e da fonte fria [ K ] t = tempo [ s ] Q = calor [ J ]. Resistência Térmica: se o objetivo é manter a casa aquecida nos dias frios ou conservar a cerveja gelada, precisa mais de maus condutores de calor do que de bons condutores. Por essa razão, o conceito de resistência térmica (R) é: R = L k [m 2.K/W] Ou seja, quanto menor a condutividade térmica do material (k), maior a resistência térmica da placa. Assim, um objeto com uma resistência térmica elevada é um mau condutor de calor e, portanto, um bom isolante térmico. Convecção Quando a transferência de energia ocorrer entre uma superfície e um fluido em movimento em virtude da diferença de temperatura entre eles. A temperatura da parte do fluido que está em contato com o objeto quente aumenta e essa parte do fluido se expande, ficando menos densa. Como esse fluido expandido é mais leve do que o fluido que o cerca, mais frio, a força de empuxo o faz subir. O fluido mais
14 frio escoa para tomar o lugar do fluido mais quente que sobe, e o processo pode continuar indefinidamente. Ex: A convecção faz parte de muitos processos naturais. A convecção atmosférica desempenha um papel fundamental na formação de padrões climáticos globais e nas variações do tempo a curto prazo. No sol, a energia térmica produzida por reações de fusão nuclear é transportada do centro para a superfície através de gigantescas células de convecção, nas quais o gás mais quente sobe pela parte central da célula e o gás mais frio desce pelos lados. Radiação Quando, na ausência de um meio interveniente, existe uma troca líquida de energia (emitida na forma de ondas eletromagnéticas) entre duas superfícies a diferentes temperaturas, usamos o termo radiação. A radiação é a transferência de energia através de ondas eletromagnéticas. A taxa Prad com a qual um objeto emite energia por radiação térmica é dada por P rad = σεat 4 = 5,6704 x 10-8 [ W/m 2. K 4 ] (constante de Stefan-Boltzmann) = emissividade da superfície do objeto A = área da superfície T = temperatura da superfície [K] TEORIA CINÉTICA DOS GASES Um dos principais tópicos da termodinâmica é a física dos gases. Um gás é formado de átomos que ocupam totalmente o volume do recipiente em que se encontram e exercem pressão sobre suas paredes. A teoria cinética dos gases relaciona as propriedades macroscópicas dos gases (pressão, temperatura e volume) às propriedades microscópicas das moléculas do gás (velocidade e energia cinética), ou seja, ao movimento dos átomos. O volume é resultado da liberdade que os átomos tem para se espalhar por
15 todo o recipiente, a pressão é causada por colisões dos átomos com as paredes do recipiente e a temperatura está associada à energia cinética dos átomos. O Número de Avogrado Um mol de uma substância contém NA (número de Avogrado) unidades elementares, onde NA é uma constante cujo valor experimental é N A = 6, mol 1 A massa molar M de uma substância é a massa de um mol da substância, e está relacionada à massa m de uma molécula da substância através da equação M = m N A O número de mols n em uma amostra de massa Mam, que contém N moléculas é dado por n = N N A = M am M = M am mn A Gases Ideais Um gás ideal é composto de partículas com tamanho desprezível, a interação elétrica entre as partículas é quase nula e há a ocorrência de interação apenas durante as colisões, que são perfeitamente elásticas; e após esta colisão entre duas partículas, não há perda de energia na forma de calor. Embora não exista na natureza um gás com as propriedades exatas de um gás ideal, todos os gases reais se aproximam do estado ideal em concentrações baixas, ou seja, em condições nas quais as moléculas estão distantes umas das outras que praticamente não interagem. A Lei dos gases ideais nos permite determinar o valor de uma das variáveis de estado de um gás se conhecermos as outras três. Assim, a Lei dos Gases Ideais é expressa pela seguinte equação: p V = nrt onde p é a pressão absoluta, n é o número de mols do gás, T é a temperatura (em Kelvins). R é a constante dos gases ideias, e possui o mesmo valor para todos os gases: R = 8, 31 J mol. K
16 Essa lei se aplica a qualquer gás ou mistura de gases, desde que a concentração do gás seja baixa (no caso de uma mistura, n é o número total de mols da mistura). A lei dos Gases Ideias pode ser escrita também da seguinte forma: p V = NkT Onde N é o número de moléculas e k é a Constante de Boltzmann: k = R = 1, J/K N A Trabalho realizado por um Gás Ideal a Temperatura Constante W = nrt ln V f V i (gás ideal, processo isotérmico). Trabalho realizado a Volume Constante e a Pressão Constante Se V é constante, W = 0 (processo a volume constante) Agora, se p é constante, então: W = p V (Processo a pressão constante) ENTROPIA Em termodinâmica, entropia é a razão pela qual os processos unidirecionais não podem ser invertidos. Utiliza-se a letra S para representar esta grandeza. A associação entre o caráter unidirecional dos processos e a irreversibilidade é tão universal que a aceitamos como natural. Se um desses processos ocorresse espontaneamente no sentido inverso, ficaríamos perplexos (batida de um carro, esquentar a mão a tocar um objeto frio, quebrar uma xícara...). Mas, nenhum desses processos no sentido errado violaria a lei da conservação da energia, pois a energia total do sistema fechado seria igual à energia total se o processo acontecesse no sentido correto.
17 Assim, não são as mudanças de energia em um sistema fechado que determinam o sentido dos processos irreversíveis; esse sentido é determinado por outra propriedade, a variação de entropia, S, do sistema. Se um processo irreversível ocorre em um sistema fechado, a entropia S do sistema sempre aumenta. A entropia é diferente da energia no sentido de que a entropia não obedece a uma lei de conservação. A energia de um sistema fechado é conservada, permanece constante. Nos processos irreversíveis, a entropia de um sistema fechado aumenta. Podemos associar a explosão de um milho de pipoca no sentido positivo do tempo e ao aumento da entropia. O sentido negativo do tempo (um filme passado ao contrário) corresponde a uma pipoca se transformando em milho. Como esse processo resultaria em uma diminuição de entropia, ele jamais acontece. Existem duas formas de definir a variação da entropia de um sistema: 1) Em termos da temperatura do sistema e da energia que o sistema ganha ou perde em forma de calor; 2) Contando as diferentes formas de distribuir os átomos ou moléculas que compõem o sistema. Assim, considerando a primeira forma de calcular a variação de entropia usaremos a seguinte equação: S = Q T onde Q é a energia absorvida ou cedida como calor pelo sistema durante o processo e T é a temperatura do sistema em Kelvins (processo isotérmico). quando um sistema recebe calor Q>0, sua entropia aumenta; quando um sistema cede calor Q<0, sua entropia diminui; se o sistema não troca calor Q=0, sua entropia permanece constante. Para determinar a variação de entropia em um processo irreversível que ocorre em um sistema fechado substituímos esse processo por qualquer outro processo
18 reversível que ligue os mesmos estados inicial e final e calculamos a variação de entropia para esse processo reversível usando a equação acima. A S para um gás ideal é calculada da seguinte forma: S = nr ln V f V i + nc V ln T f T i Bibliografia HALLIDAY, D.; RESNICK, R. Fundamentos da física vol 2. 8ª. ed. Rio de Janeiro: LTC, 2009.
O sistema A é posto em contato térmico com T até atingir o equilíbrio térmico.
 TERMODINÂMICA 18 TEMPERATURA, CALOR E PRIMEIRA LEI DA TERMODINÂMICA 18.2 TEMPERATURA Temperatura é uma das sete grandezas fundamentais do SI. Escala Kelvin (graduada em kelvins, K). Limite inferior de
TERMODINÂMICA 18 TEMPERATURA, CALOR E PRIMEIRA LEI DA TERMODINÂMICA 18.2 TEMPERATURA Temperatura é uma das sete grandezas fundamentais do SI. Escala Kelvin (graduada em kelvins, K). Limite inferior de
Cap 18 (8 a edição) Temperatura, Calor e Primeira lei da termodinâmica
 Termodinâmica: estuda a energia térmica. Cap 18 (8 a edição) Temperatura, Calor e Primeira lei da termodinâmica O que é temperatura: mede o grau de agitação das moléculas. Um pedaço de metal a 10 o C e
Termodinâmica: estuda a energia térmica. Cap 18 (8 a edição) Temperatura, Calor e Primeira lei da termodinâmica O que é temperatura: mede o grau de agitação das moléculas. Um pedaço de metal a 10 o C e
TEMPERATURA, CALOR E A PRIMEIRA LEI DA TERMODINÂMICA
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II TEMPERATURA, CALOR E A PRIMEIRA LEI DA TERMODINÂMICA Prof. Bruno Farias Bibliografia HALLIDAY,
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II TEMPERATURA, CALOR E A PRIMEIRA LEI DA TERMODINÂMICA Prof. Bruno Farias Bibliografia HALLIDAY,
Universidade Estadual do Sudoeste da Bahia
 Universidade Estadual do Sudoeste da Bahia Departamento de Ciências Exatas e Naturais 3 ermologia Física II Prof. Roberto Claudino Ferreira Prof. Roberto Claudino 1 ÍNDICE 1. Conceitos Fundamentais; 2.
Universidade Estadual do Sudoeste da Bahia Departamento de Ciências Exatas e Naturais 3 ermologia Física II Prof. Roberto Claudino Ferreira Prof. Roberto Claudino 1 ÍNDICE 1. Conceitos Fundamentais; 2.
Universidade Estadual do Sudoeste da Bahia
 Universidade Estadual do Sudoeste da Bahia Departamento de Estudos Básicos e Instrumentais 3 Termologia Física II Prof. Roberto Claudino Ferreira Prof. Roberto Claudino 1 ÍNDICE 1. Conceitos Fundamentais;
Universidade Estadual do Sudoeste da Bahia Departamento de Estudos Básicos e Instrumentais 3 Termologia Física II Prof. Roberto Claudino Ferreira Prof. Roberto Claudino 1 ÍNDICE 1. Conceitos Fundamentais;
CALORIMETRIA E TERMOLOGIA
 CALORIMETRIA E TERMOLOGIA CALORIMETRIA Calor É a transferência de energia de um corpo para outro, decorrente da diferença de temperatura entre eles. quente Fluxo de calor frio BTU = British Thermal Unit
CALORIMETRIA E TERMOLOGIA CALORIMETRIA Calor É a transferência de energia de um corpo para outro, decorrente da diferença de temperatura entre eles. quente Fluxo de calor frio BTU = British Thermal Unit
Descrição Macroscópica de um Gás ideal
 Descrição Macroscópica de um Gás ideal O gás não tem volume fixo ou uma pressão fixa O volume do gás é o volume do recipiente A pressão do gás depende do tamanho do recipiente A equação de estado relaciona
Descrição Macroscópica de um Gás ideal O gás não tem volume fixo ou uma pressão fixa O volume do gás é o volume do recipiente A pressão do gás depende do tamanho do recipiente A equação de estado relaciona
Segunda Lei da Termodinâmica, Entropia e Máquinas Térmicas Biblografia: Halliday, Resnick e Walker, vol 2, cap20 8 a Ed, vol2
 Segunda Lei da Termodinâmica, Entropia e Máquinas Térmicas Biblografia: Halliday, Resnick e Walker, vol 2, cap20 8 a Ed, vol2 O tempo tem um sentido, que é aquele no qual envelhecemos.! Na natureza, os
Segunda Lei da Termodinâmica, Entropia e Máquinas Térmicas Biblografia: Halliday, Resnick e Walker, vol 2, cap20 8 a Ed, vol2 O tempo tem um sentido, que é aquele no qual envelhecemos.! Na natureza, os
UFABC Fenômenos Térmicos Prof. Germán Lugones. Aula 3: lei zero da Termodinâmica; expansão térmica
 UFABC Fenômenos Térmicos Prof. Germán Lugones Aula 3: lei zero da Termodinâmica; expansão térmica Introdução Vamos iniciar o estudo de uma nova área da física, a TERMODINÂMICA, que lida com fenômenos associados
UFABC Fenômenos Térmicos Prof. Germán Lugones Aula 3: lei zero da Termodinâmica; expansão térmica Introdução Vamos iniciar o estudo de uma nova área da física, a TERMODINÂMICA, que lida com fenômenos associados
FÍSICA TÉRMICA TEMPERATURA, DILATAÇÃO TÉRMICA, CALORIMETRIA E TRANSMISSÃO DE CALOR
 FÍSICA TÉRMICA TEMPERATURA, DILATAÇÃO TÉRMICA, CALORIMETRIA E TRANSMISSÃO DE CALOR TEMPERATURA Grandeza Fundamental do S.I. Medida aproximada de agitação média de moléculas Unidade Principal: (Kelvin)
FÍSICA TÉRMICA TEMPERATURA, DILATAÇÃO TÉRMICA, CALORIMETRIA E TRANSMISSÃO DE CALOR TEMPERATURA Grandeza Fundamental do S.I. Medida aproximada de agitação média de moléculas Unidade Principal: (Kelvin)
Temperatura e Calor. Leis da Termodinâmica
 Temperatura e Calor Leis da Termodinâmica Temperatura O conceito de temperatura está intuitivamente ligado a ideia de quente e frio. Para se medir a temperatura, é necessário uma escala. Para determinar
Temperatura e Calor Leis da Termodinâmica Temperatura O conceito de temperatura está intuitivamente ligado a ideia de quente e frio. Para se medir a temperatura, é necessário uma escala. Para determinar
Termodinâmica. Lucy V. C. Assali
 Termodinâmica Calor Física II 2016 - IO Calor Final do século XVIII: duas hipóteses alternativas 1) Fluido indestrutível (calórico) que preencheria os poros dos corpos, escoando-se de um corpo mais quente
Termodinâmica Calor Física II 2016 - IO Calor Final do século XVIII: duas hipóteses alternativas 1) Fluido indestrutível (calórico) que preencheria os poros dos corpos, escoando-se de um corpo mais quente
Elementos de Termodinâmica
 TERMODINÂMICA ESCALAS DE TEMPERATURA Estuda as relações entre grandezas como a temperatura, a pressão, o volume, o calor e a energia interna Reparar na necessidade de definir uma escala de temperaturas
TERMODINÂMICA ESCALAS DE TEMPERATURA Estuda as relações entre grandezas como a temperatura, a pressão, o volume, o calor e a energia interna Reparar na necessidade de definir uma escala de temperaturas
Temperatura Calor Transmissão de calor 1 a Lei da Termodinâmica
 Temperatura Calor Transmissão de calor 1 a Lei da Termodinâmica Temperatura Temperatura Temperatura: é o grau de agitação das partículas (átomos, moléculas) de um corpo. Lei zero da termodinâmica Se dois
Temperatura Calor Transmissão de calor 1 a Lei da Termodinâmica Temperatura Temperatura Temperatura: é o grau de agitação das partículas (átomos, moléculas) de um corpo. Lei zero da termodinâmica Se dois
TERMODINÂMICA. Prof. Otávio Castellani
 TERMODINÂMICA Prof. Otávio Castellani TERMODINÂMICA Termo + Dinâmica Calor movimento Ramo da Física F que estuda os fenômenos relacionados ao aquecimento e resfriamento dos corpos. TEMPERATURA Grandeza
TERMODINÂMICA Prof. Otávio Castellani TERMODINÂMICA Termo + Dinâmica Calor movimento Ramo da Física F que estuda os fenômenos relacionados ao aquecimento e resfriamento dos corpos. TEMPERATURA Grandeza
Note que, no Sistema Internacional de Unidades (SI) o calor é medido em calorias (cal) ou joules (J).
 Calor e temperatura Prof. lucasmarqui Calor e Temperatura são dois conceitos fundamentais na termologia (Termofísica) os quais, são considerados sinônimos. No entanto, o calor designa a troca de energia
Calor e temperatura Prof. lucasmarqui Calor e Temperatura são dois conceitos fundamentais na termologia (Termofísica) os quais, são considerados sinônimos. No entanto, o calor designa a troca de energia
Capítulo 18 Temperatura, calor e primeira lei da termodinâmica
 Capítulo 18 Temperatura, calor e primeira lei da termodinâmica Neste capítulo vamos explorar os seguintes tópicos: Temperatura e a lei zero da termodinâmica Termômetros e escalas de temperatura A expansão
Capítulo 18 Temperatura, calor e primeira lei da termodinâmica Neste capítulo vamos explorar os seguintes tópicos: Temperatura e a lei zero da termodinâmica Termômetros e escalas de temperatura A expansão
Cap. 18 T E M P E R A T U R A, C A L O R E A P R I M E I R A L E I D A T E R M O D I N Â M I C A
 Cap. 18 T E M P E R A T U R A, C A L O R E A P R I M E I R A L E I D A T E R M O D I N Â M I C A 18.1 Introdução A termodinâmica estuda a energia térmica (energia interna) de um sistema, bem como suas
Cap. 18 T E M P E R A T U R A, C A L O R E A P R I M E I R A L E I D A T E R M O D I N Â M I C A 18.1 Introdução A termodinâmica estuda a energia térmica (energia interna) de um sistema, bem como suas
Temperatura. Escalas de Temperatura. Aula 8 Termodinâmica por Luiz Otávio Limurci. Lei zero da termodinâmica. Conversão de Temperaturas
 Física Aula 8 Termodinâmica por Luiz Otávio Limurci Temperatura A primeira noção que se tem de temperatura é a sensação de frio ou quente, verificada ao tocar um corpo. Porém, isso não pode ser considerado
Física Aula 8 Termodinâmica por Luiz Otávio Limurci Temperatura A primeira noção que se tem de temperatura é a sensação de frio ou quente, verificada ao tocar um corpo. Porém, isso não pode ser considerado
TEMPERATURA. Os constituintes da matéria (moléculas, átomos etc.) movem-se continuamente em um movimento de agitação.
 TEMPERATURA Os constituintes da matéria (moléculas, átomos etc.) movem-se continuamente em um movimento de agitação. É possível associar a existência de uma energia à energia cinética média desses constituintes
TEMPERATURA Os constituintes da matéria (moléculas, átomos etc.) movem-se continuamente em um movimento de agitação. É possível associar a existência de uma energia à energia cinética média desses constituintes
Aulas Multimídias Santa Cecília Profº Rafael Rodrigues Disciplina: Física Série: 1º Ano EM
 Aulas Multimídias Santa Cecília Profº Rafael Rodrigues Disciplina: Física Série: 1º Ano EM CALORIMETRIA TEMPERATURA Todo corpo que esteja a uma temperatura acima do zero absoluto é constituído de partículas
Aulas Multimídias Santa Cecília Profº Rafael Rodrigues Disciplina: Física Série: 1º Ano EM CALORIMETRIA TEMPERATURA Todo corpo que esteja a uma temperatura acima do zero absoluto é constituído de partículas
Física Geral e Experimental -3 Termodinâmica. Prof. Ettore Baldini-Neto
 Física Geral e Experimental -3 Termodinâmica Prof. Ettore Baldini-Neto baldini@uninove.br Ementa do Curso Introdução Temperatura: Equilíbrio Térmico, Termômetros, Escalas Termométricas Expansão Térmica
Física Geral e Experimental -3 Termodinâmica Prof. Ettore Baldini-Neto baldini@uninove.br Ementa do Curso Introdução Temperatura: Equilíbrio Térmico, Termômetros, Escalas Termométricas Expansão Térmica
Fenômenos Térmicos : primeiro conjunto de problemas
 Fenômenos Térmicos - 2014: primeiro conjunto de problemas Termômetros, temperatura e escalas de temperatura 1. Suponha que em uma escala linear de temperatura X, a água ferva a 81.5 o X e congele a-190
Fenômenos Térmicos - 2014: primeiro conjunto de problemas Termômetros, temperatura e escalas de temperatura 1. Suponha que em uma escala linear de temperatura X, a água ferva a 81.5 o X e congele a-190
Expansão Térmica de Sólidos e Líquidos. A maior parte dos sólidos e líquidos sofre uma expansão quando a sua temperatura aumenta:
 23/Mar/2018 Aula 8 Expansão Térmica de Sólidos e Líquidos Coeficiente de expansão térmica Expansão Volumétrica Expansão da água Mecanismos de transferência de calor Condução; convecção; radiação 1 Expansão
23/Mar/2018 Aula 8 Expansão Térmica de Sólidos e Líquidos Coeficiente de expansão térmica Expansão Volumétrica Expansão da água Mecanismos de transferência de calor Condução; convecção; radiação 1 Expansão
CALORIMETRIA Calor. CALORIMETRIA Potência ou Fluxo de Calor
 CALORIMETRIA Calor É a transferência de energia de um corpo para outro, decorrente da diferença de temperatura entre eles. quente frio Unidades de calor 1 cal = 4,186 J (no SI) 1 kcal = 1000 cal Fluxo
CALORIMETRIA Calor É a transferência de energia de um corpo para outro, decorrente da diferença de temperatura entre eles. quente frio Unidades de calor 1 cal = 4,186 J (no SI) 1 kcal = 1000 cal Fluxo
O QUE É TERMOMETRIA E TEMPERATURA??
 TERMOMETRIA O QUE É TERMOMETRIA E TEMPERATURA?? Termometria: Área específica da Termodinâmica que estuda a temperatura e suas diferentes escalas usadas pelo mundo Temperatura: Parâmetro termométrico que
TERMOMETRIA O QUE É TERMOMETRIA E TEMPERATURA?? Termometria: Área específica da Termodinâmica que estuda a temperatura e suas diferentes escalas usadas pelo mundo Temperatura: Parâmetro termométrico que
Capítulo 21 Temperatura
 Capítulo 21 Temperatura 21.1 Temperatura e equilíbrio térmico Mecânica: lida com partículas. Variáveis microscópicas: posição, velocidade, etc. Termodinâmica: lida com sistemas de muitas partículas. Variáveis
Capítulo 21 Temperatura 21.1 Temperatura e equilíbrio térmico Mecânica: lida com partículas. Variáveis microscópicas: posição, velocidade, etc. Termodinâmica: lida com sistemas de muitas partículas. Variáveis
Halliday Fundamentos de Física Volume 2
 Halliday Fundamentos de Física Volume 2 www.grupogen.com.br http://gen-io.grupogen.com.br O GEN Grupo Editorial Nacional reúne as editoras Guanabara Koogan, Santos, Roca, AC Farmacêutica, LTC, Forense,
Halliday Fundamentos de Física Volume 2 www.grupogen.com.br http://gen-io.grupogen.com.br O GEN Grupo Editorial Nacional reúne as editoras Guanabara Koogan, Santos, Roca, AC Farmacêutica, LTC, Forense,
2. Conceitos e Definições
 2. Conceitos e Definições Sistema e Volume de Controle Sistema Termodinâmico: região do espaço delimitada fisicamente por superfícies geométricas arbitrárias reais ou imaginárias, que podem ser fixas ou
2. Conceitos e Definições Sistema e Volume de Controle Sistema Termodinâmico: região do espaço delimitada fisicamente por superfícies geométricas arbitrárias reais ou imaginárias, que podem ser fixas ou
Calor e Temperatura, Trocas de Calor Bibliografia e figuras desta aula: Fundamentos da Física, Halliday, Resnick e Walker, 8a Ed., vol 2 pág
 Calor e Temperatura, Trocas de Calor Bibliografia e figuras desta aula: Fundamentos da Física, Halliday, Resnick e Walker, 8a Ed., vol 2 pág2 188-190 Até agora aprendemos: O conceito de temperatura A lei
Calor e Temperatura, Trocas de Calor Bibliografia e figuras desta aula: Fundamentos da Física, Halliday, Resnick e Walker, 8a Ed., vol 2 pág2 188-190 Até agora aprendemos: O conceito de temperatura A lei
Temperatura, Calor e a Primeira Lei da Termodinâmica
 Temperatura, Calor e a Primeira Temperatura; A Lei Zero da Termodinâmica; Medindo a Temperatura; Escala Celsius e Fahrenheit; Dilatação Térmica; Temperatura e Calor; Absorção de Calor por Sólidos e Líquidos;
Temperatura, Calor e a Primeira Temperatura; A Lei Zero da Termodinâmica; Medindo a Temperatura; Escala Celsius e Fahrenheit; Dilatação Térmica; Temperatura e Calor; Absorção de Calor por Sólidos e Líquidos;
Termo- estatística REVISÃO DE TERMODINÂMICA. Alguns conceitos importante que aparecem nesta lei:
 Lei Zero da Termodinâmica 4300259 Termo- estatística REVISÃO DE TERMODINÂMICA Se dois sistema estão em equilíbrio térmico com um terceiro sistema, então eles também estão em equilíbrio entre si. Alguns
Lei Zero da Termodinâmica 4300259 Termo- estatística REVISÃO DE TERMODINÂMICA Se dois sistema estão em equilíbrio térmico com um terceiro sistema, então eles também estão em equilíbrio entre si. Alguns
BC0205. Fenômenos Térmicos Gustavo M. Dalpian Terceiro Trimestre/2009. Aula 2 Dalpian
 BC0205 Fenômenos Térmicos Gustavo M. Dalpian Terceiro Trimestre/2009 Fenômenos Térmicos? Ementa: Temperatura e calor. Sistemas termodinâmicos. Variáveis termodinâmicas e sua natureza macroscópica. Teoria
BC0205 Fenômenos Térmicos Gustavo M. Dalpian Terceiro Trimestre/2009 Fenômenos Térmicos? Ementa: Temperatura e calor. Sistemas termodinâmicos. Variáveis termodinâmicas e sua natureza macroscópica. Teoria
INSTRUMENTAÇÃO INDUSTRIAL. Prof. Eduardo Calsan. Polímeros/Engenharias
 INSTRUMENTAÇÃO INDUSTRIAL Prof. Eduardo Calsan Polímeros/Engenharias Introdução: II Medição de Temperatura Energia térmica: é energia de agitação ou movimento das moléculas devido ao estado de constante
INSTRUMENTAÇÃO INDUSTRIAL Prof. Eduardo Calsan Polímeros/Engenharias Introdução: II Medição de Temperatura Energia térmica: é energia de agitação ou movimento das moléculas devido ao estado de constante
ELEMENTOS DE TERMODINÂMICA
 ELEMENTOS DE TERMODINÂMICA TERMODINÂMICA ESCALAS DE TEMPERATURA Estuda as relações entre grandezas como a temperatura, a pressão, o volume, o calor e a energia interna Reparar na necessidade de definir
ELEMENTOS DE TERMODINÂMICA TERMODINÂMICA ESCALAS DE TEMPERATURA Estuda as relações entre grandezas como a temperatura, a pressão, o volume, o calor e a energia interna Reparar na necessidade de definir
25/Mar/2015 Aula /Mar/2015 Aula 9
 20/Mar/2015 Aula 9 Processos Politrópicos Relações politrópicas num gás ideal Trabalho: aplicação aos gases perfeitos Calor: aplicação aos gases perfeitos Calor específico politrópico Variação de entropia
20/Mar/2015 Aula 9 Processos Politrópicos Relações politrópicas num gás ideal Trabalho: aplicação aos gases perfeitos Calor: aplicação aos gases perfeitos Calor específico politrópico Variação de entropia
Mecanismos de Transferência de Calor
 Mecanismos de Transferência de Calor Bibliografia de Aula: Halliday, Resnick e Walker, 8 a Ed; Vol 2, capítulo 18. Já estudamos como ocorrem as trocas de calor entre sistemas físicos. Aprendemos que em
Mecanismos de Transferência de Calor Bibliografia de Aula: Halliday, Resnick e Walker, 8 a Ed; Vol 2, capítulo 18. Já estudamos como ocorrem as trocas de calor entre sistemas físicos. Aprendemos que em
FENÔMENOS OSCILATÓRIOS TERMODINÂMICA
 FENÔMENOS OSCILATÓRIOS E TERMODINÂMICA AULA 8 TEMPERATURA, CALOR E PRIMEIRA LEI DA TERMODINÂMICA PROF.: KAIO DUTRA Termodinâmica A termodinâmica é o estudo das leis que regem a relação entre o calor, trabalho
FENÔMENOS OSCILATÓRIOS E TERMODINÂMICA AULA 8 TEMPERATURA, CALOR E PRIMEIRA LEI DA TERMODINÂMICA PROF.: KAIO DUTRA Termodinâmica A termodinâmica é o estudo das leis que regem a relação entre o calor, trabalho
Cap. 20 A Entropia e a Segunda Lei da Termodinâmica
 Cap. 20 A Entropia e a Segunda Lei da Processos Irreversíveis e Entropia; Variação de Entropia; A Segunda Lei da ; Entropia no Mundo Real: Máquinas Térmicas; Entropia no Mundo Real: Refrigeradores; Eficiência
Cap. 20 A Entropia e a Segunda Lei da Processos Irreversíveis e Entropia; Variação de Entropia; A Segunda Lei da ; Entropia no Mundo Real: Máquinas Térmicas; Entropia no Mundo Real: Refrigeradores; Eficiência
IFSP - Pirituba Prof. Renato Pugliese renatopugliese.wordpress.com. Curso Preparatório para o ENEM (frente 2) 2º semestre de 2016
 IFSP - Pirituba Prof. Renato Pugliese renatopugliese.wordpress.com Curso Preparatório para o ENEM (frente 2) 2º semestre de 2016 Aula 1 - Temperatura e Equilíbrio térmico; Escalas Apresentação - Professor
IFSP - Pirituba Prof. Renato Pugliese renatopugliese.wordpress.com Curso Preparatório para o ENEM (frente 2) 2º semestre de 2016 Aula 1 - Temperatura e Equilíbrio térmico; Escalas Apresentação - Professor
Transferência de calor
 Transferência de calor 1.1 Calor: Forma de energia que se transmite espontaneamente de um corpo para o outro quando entre eles existir uma diferença de temperatura. O calor é uma energia em trânsito provocada
Transferência de calor 1.1 Calor: Forma de energia que se transmite espontaneamente de um corpo para o outro quando entre eles existir uma diferença de temperatura. O calor é uma energia em trânsito provocada
Fisica do Calor ( ) Prof. Adriano Mesquita Alencar Dep. Física Geral Instituto de Física da USP A01. Introdução
 Fisica do Calor (4300159) Prof. Adriano Mesquita Alencar Dep. Física Geral Instituto de Física da USP A01 Introdução Data Programa do curso agosto 9 agosto 12 agosto 16 agosto 19 agosto 23 agosto 26 Temperatura
Fisica do Calor (4300159) Prof. Adriano Mesquita Alencar Dep. Física Geral Instituto de Física da USP A01 Introdução Data Programa do curso agosto 9 agosto 12 agosto 16 agosto 19 agosto 23 agosto 26 Temperatura
Energia: Capacidade de realizar trabalho.
 Energia: Capacidade de realizar trabalho. Formas de energia: Matéria: - Cinética (movim. macroscópico, térmica, etc) - Potencial (elétrica, gravitacional, elástica, etc) Tudo que tem massa e ocupa lugar
Energia: Capacidade de realizar trabalho. Formas de energia: Matéria: - Cinética (movim. macroscópico, térmica, etc) - Potencial (elétrica, gravitacional, elástica, etc) Tudo que tem massa e ocupa lugar
Termodinâmica. Lucy V. C. Assali
 Termodinâmica Temperatura Lucy V. C. Assali Física II 2016 - IO Temperatura Não confiável Por exemplo: metal e papel tirados do congelador, sentimos o metal mais frio, mas é só porque ele é um melhor condutor
Termodinâmica Temperatura Lucy V. C. Assali Física II 2016 - IO Temperatura Não confiável Por exemplo: metal e papel tirados do congelador, sentimos o metal mais frio, mas é só porque ele é um melhor condutor
2.1 Breve história da termodinâmica
 2.1 Breve história da termodinâmica TERMODINÂMICA calor força, movimento No início, estudava os processos que permitiam converter calor em trabalho (força e movimento). 2.1 Breve história da termodinâmica
2.1 Breve história da termodinâmica TERMODINÂMICA calor força, movimento No início, estudava os processos que permitiam converter calor em trabalho (força e movimento). 2.1 Breve história da termodinâmica
2 Temperatura Empírica, Princípio de Carnot e Temperatura Termodinâmica
 2 Temperatura Empírica, Princípio de Carnot e Temperatura Termodinâmica 2.1 Temperatura empírica: medidas de temperatura Termômetro: Sistema com uma propriedade mensurável que varia com a temperatura (propriedade
2 Temperatura Empírica, Princípio de Carnot e Temperatura Termodinâmica 2.1 Temperatura empírica: medidas de temperatura Termômetro: Sistema com uma propriedade mensurável que varia com a temperatura (propriedade
ESCALAS TERMOMÉTRICAS E DILATAÇÃO
 REVISÃO ENEM ESCALAS TERMOMÉTRICAS E DILATAÇÃO Temperatura é a grandeza física escalar que nos permite avaliar o grau de agitação das moléculas de um corpo. Quanto maior for o grau de agitação molecular,
REVISÃO ENEM ESCALAS TERMOMÉTRICAS E DILATAÇÃO Temperatura é a grandeza física escalar que nos permite avaliar o grau de agitação das moléculas de um corpo. Quanto maior for o grau de agitação molecular,
Universidade Federal Rural do Semiárido - UFERSA
 Universidade Federal Rural do Semiárido - UFERSA Temperatura e Calor Jusciane da Costa e Silva Mossoró, Junho de 2010 Introdução temperatura Termodinâmica calor energia interna Típico sistema termodinâmico,
Universidade Federal Rural do Semiárido - UFERSA Temperatura e Calor Jusciane da Costa e Silva Mossoró, Junho de 2010 Introdução temperatura Termodinâmica calor energia interna Típico sistema termodinâmico,
Universidade Estadual do Sudoeste da Bahia
 Universidade Estadual do Sudoeste da Bahia Departamento de Estudos Básicos e Instrumentais 4 Termodinâmica Física II Ferreira 1 ÍNDICE 1. Conceitos Fundamentais; 2. Sistemas Termodinâmicos; 3. Leis da
Universidade Estadual do Sudoeste da Bahia Departamento de Estudos Básicos e Instrumentais 4 Termodinâmica Física II Ferreira 1 ÍNDICE 1. Conceitos Fundamentais; 2. Sistemas Termodinâmicos; 3. Leis da
UFABC - Fenômenos Térmicos - Prof. Lugones AULA 2. o termômetro de gás a volume constante o expansão térmica
 UFABC - Fenômenos Térmicos - Prof. Lugones AULA 2 o termômetro de gás a volume constante o expansão térmica O termômetro de gás a volume constante Régua P P P 0 Primeiramente, o frasco de gás é introduzido
UFABC - Fenômenos Térmicos - Prof. Lugones AULA 2 o termômetro de gás a volume constante o expansão térmica O termômetro de gás a volume constante Régua P P P 0 Primeiramente, o frasco de gás é introduzido
Testes gerais
 Testes gerais Termometria. Em uma escala termométrica arbitrária A, atribui-se 0ºA à temperatura de fusão do gelo e 20ºA à temperatura de ebulição da água. Quando a temperatura for de 20ºC, na escala A,
Testes gerais Termometria. Em uma escala termométrica arbitrária A, atribui-se 0ºA à temperatura de fusão do gelo e 20ºA à temperatura de ebulição da água. Quando a temperatura for de 20ºC, na escala A,
Capitulo-4 Calor e Temperatura
 Capitulo-4 Calor e Temperatura www.plantaofisica.blogspot.com.br 1 Resumo de aula: Termometria. 1- Temperatura Termometria é a parte da física que se preocupa unicamente em formas de se medir a temperatura
Capitulo-4 Calor e Temperatura www.plantaofisica.blogspot.com.br 1 Resumo de aula: Termometria. 1- Temperatura Termometria é a parte da física que se preocupa unicamente em formas de se medir a temperatura
Física II. Capítulo 03 Transferência de Calor. Técnico em Edificações (PROEJA) Prof. Márcio T. de Castro 17/05/2017
 Física II Capítulo 03 Transferência de Calor Técnico em Edificações (PROEJA) 17/05/2017 Prof. Márcio T. de Castro Parte I 2 Quantidade de Calor Quantidade de Calor (Q): energia térmica em trânsito entre
Física II Capítulo 03 Transferência de Calor Técnico em Edificações (PROEJA) 17/05/2017 Prof. Márcio T. de Castro Parte I 2 Quantidade de Calor Quantidade de Calor (Q): energia térmica em trânsito entre
EP34D Fenômenos de Transporte
 EP34D Fenômenos de Transporte Prof. Dr. André Damiani Rocha arocha@utfpr.edu.br Introdução à Transferência de Calor 2 Introdução à Transferência de Calor O que é Transferência de Calor? Transferência de
EP34D Fenômenos de Transporte Prof. Dr. André Damiani Rocha arocha@utfpr.edu.br Introdução à Transferência de Calor 2 Introdução à Transferência de Calor O que é Transferência de Calor? Transferência de
Física II FEP 112 ( ) 1º Semestre de Instituto de Física - Universidade de São Paulo. Professor: Valdir Guimarães
 Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
FÍSICA TÉRMICA. Prof. Neemias Alves de Lima Instituto de Pesquisa em Ciência dos Materiais Universidade Federal do Vale do São Francisco 1
 FÍSICA TÉRMICA Prof. Neemias Alves de Lima Instituto de Pesquisa em Ciência dos Materiais Universidade Federal do Vale do São Francisco 1 Domínio da Física Térmica Como pode água aprisionada ser ejetada
FÍSICA TÉRMICA Prof. Neemias Alves de Lima Instituto de Pesquisa em Ciência dos Materiais Universidade Federal do Vale do São Francisco 1 Domínio da Física Térmica Como pode água aprisionada ser ejetada
Termologia. Calor: Energia em trânsito de um corpo para outro devido a diferença de temperaturas entre eles.
 Calor e Temperatura Termologia Estuda os fenômenos ligados a calor e temperatura Calor: Energia em trânsito de um corpo para outro devido a diferença de temperaturas entre eles. Temperatura: É uma grandeza
Calor e Temperatura Termologia Estuda os fenômenos ligados a calor e temperatura Calor: Energia em trânsito de um corpo para outro devido a diferença de temperaturas entre eles. Temperatura: É uma grandeza
TERMOLOGIA. Calorimetria:
 TERMOLOGIA Calorimetria: Calor: é energia térmica em trânsito. Ela ocorre sempre entre dois corpos com temperaturas diferentes. O corpo com temperatura maior sede espontaneamente calor para o corpo que
TERMOLOGIA Calorimetria: Calor: é energia térmica em trânsito. Ela ocorre sempre entre dois corpos com temperaturas diferentes. O corpo com temperatura maior sede espontaneamente calor para o corpo que
Propagação do calor. Condução térmica
 Propagação do calor A propagação do calor entre dois sistemas pode ocorrer através de três processos diferentes: a condução, a convecção e a irradiação. Condução térmica A condução térmica é um processo
Propagação do calor A propagação do calor entre dois sistemas pode ocorrer através de três processos diferentes: a condução, a convecção e a irradiação. Condução térmica A condução térmica é um processo
Aula 9: Entropia e a Segunda Lei da Termodinâmica
 UFABC Fenômenos Térmicos Prof. Germán Lugones Aula 9: Entropia e a Segunda Lei da Termodinâmica Sadi Carnot [1796-1832] R. Clausius [1822-1888] W. Thomson (Lord Kelvin) [1824-1907] Quando um saco de pipocas
UFABC Fenômenos Térmicos Prof. Germán Lugones Aula 9: Entropia e a Segunda Lei da Termodinâmica Sadi Carnot [1796-1832] R. Clausius [1822-1888] W. Thomson (Lord Kelvin) [1824-1907] Quando um saco de pipocas
Curso engenharia de Energia
 UNIVERSIDADE FEDERAL DA GRANDE DOURADOS - UFGD FACULDADE DE ENGENHARIA Curso engenharia de Energia Prof. Dr. Omar Seye omarseye@ufgd.edu.br Disciplina: COMBUSTÃO E COMBUSTÍVEIS Introdução: Leis da Conservação
UNIVERSIDADE FEDERAL DA GRANDE DOURADOS - UFGD FACULDADE DE ENGENHARIA Curso engenharia de Energia Prof. Dr. Omar Seye omarseye@ufgd.edu.br Disciplina: COMBUSTÃO E COMBUSTÍVEIS Introdução: Leis da Conservação
Podemos definir como quente um corpo que tem suas moléculas agitando-se muito, ou seja, com alta energia cinética. Analogamente, um corpo frio, é
 Podemos definir como quente um corpo que tem suas moléculas agitando-se muito, ou seja, com alta energia cinética. Analogamente, um corpo frio, é aquele que tem baixa agitação das suas moléculas. Tem
Podemos definir como quente um corpo que tem suas moléculas agitando-se muito, ou seja, com alta energia cinética. Analogamente, um corpo frio, é aquele que tem baixa agitação das suas moléculas. Tem
Física e Química A 10.º ano
 Energia, fenómenos térmicos e radiação II Física e Química A 10.º ano 1. Responde às seguintes questões. Num dia de inverno, a temperatura no exterior é de - 3ºC e a temperatura no interior de um apartamento
Energia, fenómenos térmicos e radiação II Física e Química A 10.º ano 1. Responde às seguintes questões. Num dia de inverno, a temperatura no exterior é de - 3ºC e a temperatura no interior de um apartamento
Termometria. Temperatura
 Termometria Termometria Temperatura A Física Térmica, também conhecida como Termologia, é a área da Física que investiga os fenômenos relacionados à energia térmica. Dentre esses fenômenos, podemos citar
Termometria Termometria Temperatura A Física Térmica, também conhecida como Termologia, é a área da Física que investiga os fenômenos relacionados à energia térmica. Dentre esses fenômenos, podemos citar
1. Suponha que em uma escala linear de temperatura X a água ferva a 53,3 o X e congele a -170 o X. Qual a temperatura de 340K na escala X?
 BC0303: Fenômenos Térmicos - 1 a Lista de Exercícios Termômetros, Temperatura e Escalas de Temperatura 1. Suponha que em uma escala linear de temperatura X a água ferva a 53,3 o X e congele a -170 o X.
BC0303: Fenômenos Térmicos - 1 a Lista de Exercícios Termômetros, Temperatura e Escalas de Temperatura 1. Suponha que em uma escala linear de temperatura X a água ferva a 53,3 o X e congele a -170 o X.
Turma: 2301 Turno: Manhã Professor: Douglas Baroni
 Colégio Zaccaria TELEFAX: (0 XX 21) 3235-9400 www.zaccaria.g12.br Lista de exercícios Física II (Recuperação) 1º Período 2014 Aluno(a): N.º Turma: 2301 Turno: Manhã Professor: Douglas Baroni QUESTÃO 1
Colégio Zaccaria TELEFAX: (0 XX 21) 3235-9400 www.zaccaria.g12.br Lista de exercícios Física II (Recuperação) 1º Período 2014 Aluno(a): N.º Turma: 2301 Turno: Manhã Professor: Douglas Baroni QUESTÃO 1
Notas de Aula FIS1059 Termodinâmica, Teoria Cinética e Entropia. Material para prova do dia 01/12/2011
 Notas de Aula FIS1059 - Termodinâmica, T. Cinética e Entropia Ezequiel C. Siqueira 2011 Notas de Aula FIS1059 Termodinâmica, Teoria Cinética e Entropia Material para prova do dia 01/12/2011 Ezequiel C.
Notas de Aula FIS1059 - Termodinâmica, T. Cinética e Entropia Ezequiel C. Siqueira 2011 Notas de Aula FIS1059 Termodinâmica, Teoria Cinética e Entropia Material para prova do dia 01/12/2011 Ezequiel C.
Primeira Lei da Termodinâmica
 Físico-Química I Profa. Dra. Carla Dalmolin Primeira Lei da Termodinâmica Definição de energia, calor e trabalho Trabalho de expansão Trocas térmicas Entalpia Termodinâmica Estudo das transformações de
Físico-Química I Profa. Dra. Carla Dalmolin Primeira Lei da Termodinâmica Definição de energia, calor e trabalho Trabalho de expansão Trocas térmicas Entalpia Termodinâmica Estudo das transformações de
ENGENHARIA DE MATERIAIS. Fenômenos de Transporte em Engenharia de Materiais (Transferência de Calor e Massa)
 ENGENHARIA DE MATERIAIS Fenômenos de Transporte em Engenharia de Materiais (Transferência de Calor e Massa) Prof. Dr. Sérgio R. Montoro sergio.montoro@usp.br srmontoro@dequi.eel.usp.br AULA 1 INTRODUÇÃO
ENGENHARIA DE MATERIAIS Fenômenos de Transporte em Engenharia de Materiais (Transferência de Calor e Massa) Prof. Dr. Sérgio R. Montoro sergio.montoro@usp.br srmontoro@dequi.eel.usp.br AULA 1 INTRODUÇÃO
2/Mar/2016 Aula 4. 26/Fev/2016 Aula 3
 6/Fev/016 Aula 3 Calor e Primeira Lei da Termodinâmica Calor e energia térmica Capacidade calorífica e calor específico Calor latente Diagrama de fases para a água Primeira Lei da Termodinâmica Trabalho
6/Fev/016 Aula 3 Calor e Primeira Lei da Termodinâmica Calor e energia térmica Capacidade calorífica e calor específico Calor latente Diagrama de fases para a água Primeira Lei da Termodinâmica Trabalho
TERMODINÂMICA. Radiação Solar. Anjo Albuquerque
 TERMODINÂMICA Radiação Solar 1 Anjo Albuquerque TERMODINÂMICA Termodinâmica - é a área da Física que nos permite compreender o mundo que nos rodeia, desde a escala dos átomos até à escala do universo.
TERMODINÂMICA Radiação Solar 1 Anjo Albuquerque TERMODINÂMICA Termodinâmica - é a área da Física que nos permite compreender o mundo que nos rodeia, desde a escala dos átomos até à escala do universo.
Mecanismos de Transferência de Calor. Gustavo Dalpian
 Mecanismos de Transferência de Calor Gustavo Dalpian Monitoria Segunda: 14 18hs (Sala 405, disponível a par8r de 26/10) 14 16 hs Luiz Felipe Lopes 16 18 hs Felipe Marcilio Terca: 10 12hs Mariana Barbosa
Mecanismos de Transferência de Calor Gustavo Dalpian Monitoria Segunda: 14 18hs (Sala 405, disponível a par8r de 26/10) 14 16 hs Luiz Felipe Lopes 16 18 hs Felipe Marcilio Terca: 10 12hs Mariana Barbosa
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RN CAMPUS: CURSO: ALUNO:
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RN CAMPUS: CURSO: ALUNO: DISCIPLINA: FÍSICA PROFESSOR: EDSON JOSÉ Lista de exercícios 9 1. Defina o ponto triplo da água e seu valor na escala Kelvin.
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RN CAMPUS: CURSO: ALUNO: DISCIPLINA: FÍSICA PROFESSOR: EDSON JOSÉ Lista de exercícios 9 1. Defina o ponto triplo da água e seu valor na escala Kelvin.
Professor Marco Antonio
 Professor Marco Antonio observações macroscópicas interpretações microscópicas Termologia Quente ou frio? Termologia Temperatura é uma grandeza física que mede o estado de agitação das partículas de um
Professor Marco Antonio observações macroscópicas interpretações microscópicas Termologia Quente ou frio? Termologia Temperatura é uma grandeza física que mede o estado de agitação das partículas de um
CURSO: Engenharia Civil DISCIPLINA: Tópicos de Física Geral e Experimental PROFº: MSc. Demetrius Leão
 CURSO: Engenharia Civil DISCIPLINA: Tópicos de Física Geral e Experimental PROFº: MSc. Demetrius Leão 1 ACOMPANHE A DISCIPLINA PELA INTERNET Página com as aulas e listas de exercícios: Palavra-chave no
CURSO: Engenharia Civil DISCIPLINA: Tópicos de Física Geral e Experimental PROFº: MSc. Demetrius Leão 1 ACOMPANHE A DISCIPLINA PELA INTERNET Página com as aulas e listas de exercícios: Palavra-chave no
Aula Calor e 1ª Lei da Termodinâmica. As leis da Termodinâmica foram inicialmente obtidas empiricamente e somente
 1 Aula Calor e 1ª Lei da Termodinâmica Tema: Termodinâmica a serem abordados os assuntos: - Lei zero da Termodinâmica; - 1ª Lei da Termodinâmica calor e energia; - 2ª Lei entropia; - Aplicações da Termodinâmica
1 Aula Calor e 1ª Lei da Termodinâmica Tema: Termodinâmica a serem abordados os assuntos: - Lei zero da Termodinâmica; - 1ª Lei da Termodinâmica calor e energia; - 2ª Lei entropia; - Aplicações da Termodinâmica
A) condensação do vapor de água dissolvido no ar ao encontrar uma superfície à temperatura mais baixa.
 lista_1-conceitos_iniciais_em_termologia Questão 1 Os cálculos dos pesquisadores sugerem que a temperatura média dessa estrela é de T i = 2.700 C. Considere uma estrela como um corpo homogêneo de massa
lista_1-conceitos_iniciais_em_termologia Questão 1 Os cálculos dos pesquisadores sugerem que a temperatura média dessa estrela é de T i = 2.700 C. Considere uma estrela como um corpo homogêneo de massa
Processos Irreversíveis
 Processos Irreversíveis Objeto solto de uma altura h v = 0 2gh Objeto lançado com velocidade V em superfície com atrito V V = 0 O que há de comum em todos os fenômenos irreversíveis? Movimentos organizados
Processos Irreversíveis Objeto solto de uma altura h v = 0 2gh Objeto lançado com velocidade V em superfície com atrito V V = 0 O que há de comum em todos os fenômenos irreversíveis? Movimentos organizados
CIÊNCIA E TECNOLOGIA DE MATERIAIS
 Faculdade Sudoeste Paulista Engenharia Civil/Produção Notas de aula: CIÊNCIA E TECNOLOGIA DE MATERIAIS PROPRIEDADES TÉRMICAS Prof. Msc. Patrícia Corrêa Avaré, 2014 Propriedades de materiais: 1. Térmica
Faculdade Sudoeste Paulista Engenharia Civil/Produção Notas de aula: CIÊNCIA E TECNOLOGIA DE MATERIAIS PROPRIEDADES TÉRMICAS Prof. Msc. Patrícia Corrêa Avaré, 2014 Propriedades de materiais: 1. Térmica
Linguagem da Termodinâmica
 Linguagem da Termodinâmica Sistemas macroscópicos contêm um grande número de partículas constituintes (átomos, moléculas, iões,...) N A = 6, 022 10 23 Em Termodinâmica, Princípios e Leis são independentes
Linguagem da Termodinâmica Sistemas macroscópicos contêm um grande número de partículas constituintes (átomos, moléculas, iões,...) N A = 6, 022 10 23 Em Termodinâmica, Princípios e Leis são independentes
Profa.. Dra. Ana Maria Pereira Neto
 5/09/0 Universidade Federal do ABC BC309 Termodinâmica Aplicada Profa.. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre, sala 637 Calor, Trabalho e Primeira Lei da Termodinâmica 5/09/0
5/09/0 Universidade Federal do ABC BC309 Termodinâmica Aplicada Profa.. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre, sala 637 Calor, Trabalho e Primeira Lei da Termodinâmica 5/09/0
TERMOLOGIA. Calorimetria:
 TERMOLOGIA Calorimetria: Calor: é energia térmica em trânsito. Ela ocorre sempre entre dois corpos com temperaturas diferentes. O corpo com temperatura maior sede espontaneamente calor para o corpo que
TERMOLOGIA Calorimetria: Calor: é energia térmica em trânsito. Ela ocorre sempre entre dois corpos com temperaturas diferentes. O corpo com temperatura maior sede espontaneamente calor para o corpo que
BANCO DE QUESTÕES - FÍSICA - 9º ANO - ENSINO FUNDAMENTAL
 PROFESSOR: EQUIPE DE FÍSICA BANCO DE QUESTÕES - FÍSICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================= 01- Um copo de água está à temperatura
PROFESSOR: EQUIPE DE FÍSICA BANCO DE QUESTÕES - FÍSICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================= 01- Um copo de água está à temperatura
Física II FEP º Semestre de Instituto de Física - Universidade de São Paulo. Professor: Valdir Guimarães
 Física II FEP 112 2º Semestre de 2012 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104 Aula 3 Irreversibilidade e Segunda Lei
Física II FEP 112 2º Semestre de 2012 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104 Aula 3 Irreversibilidade e Segunda Lei
CPOG. Prof. Felipe Cardoso. Escalas Termométricas Dilatação Calorimetria
 AULA DO CPOG Prof. Felipe Cardoso Escalas Termométricas Dilatação Calorimetria Escalas termométricas Em um gráfico Relações de variação Petrobras maio 2010 TO prova 35 Petrobras 2010 TO prova 40 Petrobras
AULA DO CPOG Prof. Felipe Cardoso Escalas Termométricas Dilatação Calorimetria Escalas termométricas Em um gráfico Relações de variação Petrobras maio 2010 TO prova 35 Petrobras 2010 TO prova 40 Petrobras
09- (PUC-PR) Um menino inglês mediu sua temperatura com um termômetro graduado na escala Fahrenheit e encontrou 96,8 F.
 01- (UFPR) A água pode ser encontrada na natureza nos estados sólido, líquido ou gasoso. Conforme as condições, a água pode passar de um estado para outro através de processos que recebem nomes específicos.
01- (UFPR) A água pode ser encontrada na natureza nos estados sólido, líquido ou gasoso. Conforme as condições, a água pode passar de um estado para outro através de processos que recebem nomes específicos.
1ª Aula do cap. 19 Termologia
 1ª Aula do cap. 19 Termologia T e m p e r a t u r a O valor da temperatura está associada ao nível de agitação das partículas de um corpo. A temperatura é uma medida da agitação térmica das partículas
1ª Aula do cap. 19 Termologia T e m p e r a t u r a O valor da temperatura está associada ao nível de agitação das partículas de um corpo. A temperatura é uma medida da agitação térmica das partículas
Exercício 1. Exercício 2.
 Exercício 1. Como resultado de um aumento de temperatura de 32 o C, uma barra com uma rachadura no seu centro dobra para cima (Figura). Se a distância fixa for 3,77 m e o coeficiente de expansão linear
Exercício 1. Como resultado de um aumento de temperatura de 32 o C, uma barra com uma rachadura no seu centro dobra para cima (Figura). Se a distância fixa for 3,77 m e o coeficiente de expansão linear
2
 1 2 3 4 5 6 7 8 9 10 11 12 13 Degradação de energia e rendimento 14 Anjo Albuquerque Degradação de energia e rendimento 15 Anjo Albuquerque Módulo inicial Degradação de energia e rendimento Módulo inicial
1 2 3 4 5 6 7 8 9 10 11 12 13 Degradação de energia e rendimento 14 Anjo Albuquerque Degradação de energia e rendimento 15 Anjo Albuquerque Módulo inicial Degradação de energia e rendimento Módulo inicial
Aula anterior: Esta Aula: Próxima aula:
 Aula anterior: Composição da atmosfera: do que é composta; fontes e sumidouros; como alcançou o estado atual. Breve discussão sobre pressão, densidade, temperatura. Esta Aula: Temperatura, pressão e densidade
Aula anterior: Composição da atmosfera: do que é composta; fontes e sumidouros; como alcançou o estado atual. Breve discussão sobre pressão, densidade, temperatura. Esta Aula: Temperatura, pressão e densidade
ESZO Fenômenos de Transporte
 Universidade Federal do ABC ESZO 001-15 Fenômenos de Transporte Profa. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre 1, sala 637 Mecanismos de Transferência de Calor Calor Calor pode
Universidade Federal do ABC ESZO 001-15 Fenômenos de Transporte Profa. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre 1, sala 637 Mecanismos de Transferência de Calor Calor Calor pode
Professora : Elisângela Moraes
 UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA -EEL Professora : Elisângela Moraes 02/03/2012 PROGRAMA RESUMIDO 1. Gases Ideais; 2. Gases Reais; 3. Termodinâmica; 4. Termoquímica; 5. Entropia;
UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA -EEL Professora : Elisângela Moraes 02/03/2012 PROGRAMA RESUMIDO 1. Gases Ideais; 2. Gases Reais; 3. Termodinâmica; 4. Termoquímica; 5. Entropia;
CONDUÇÃO EM UMA PLACA COMPOSTA
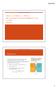 FÍSICA 2 PROVA 3 TEMA 1 MECANISMOS DE TRANSFERÊNCIA DE CALOR PROF. NECKEL CONDUÇÃO A condução de calor de uma fonte quente de temperatura para uma fonte de fria de temperatura por meio de uma condução
FÍSICA 2 PROVA 3 TEMA 1 MECANISMOS DE TRANSFERÊNCIA DE CALOR PROF. NECKEL CONDUÇÃO A condução de calor de uma fonte quente de temperatura para uma fonte de fria de temperatura por meio de uma condução
Temperatura, calor e processos de transmissão de calor
 REVISÃO ENEM Temperatura, calor e processos de transmissão de calor TEMPERATURA Temperatura é a grandeza física escalar que nos permite avaliar o grau de agitação das moléculas. Quanto maior for o grau
REVISÃO ENEM Temperatura, calor e processos de transmissão de calor TEMPERATURA Temperatura é a grandeza física escalar que nos permite avaliar o grau de agitação das moléculas. Quanto maior for o grau
2.5 Primeiro Princípio da Termodinâmica
 2.5 Primeiro Princípio da Termodinâmica amos considerar o caso especial do princípio da conservação de energia, no qual a única variação na energia de um sistema é a variação na sua energia interna U,
2.5 Primeiro Princípio da Termodinâmica amos considerar o caso especial do princípio da conservação de energia, no qual a única variação na energia de um sistema é a variação na sua energia interna U,
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO SUL CAMPUS RIO GRANDE INSTRUMENTAÇÃO INDUSTRIAL
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO SUL CAMPUS RIO GRANDE INSTRUMENTAÇÃO INDUSTRIAL Aula 16 2 MEDIDORES DE TEMPERATURA 3 INTRODUÇÃO Todas as substâncias são constituídas
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO SUL CAMPUS RIO GRANDE INSTRUMENTAÇÃO INDUSTRIAL Aula 16 2 MEDIDORES DE TEMPERATURA 3 INTRODUÇÃO Todas as substâncias são constituídas
Termodina ˆmica. Wagner Maciel Castilho. Anhanguera - Indaiatuba
 Termodina ˆmica Wagner Maciel Castilho castilho.w@gmail.com Wagner Maciel Castilho 19 de fevereiro de 2018 Anhanguera 1 / 39 Sumário Introdução Wagner Maciel Castilho 19 de fevereiro de 2018 Anhanguera
Termodina ˆmica Wagner Maciel Castilho castilho.w@gmail.com Wagner Maciel Castilho 19 de fevereiro de 2018 Anhanguera 1 / 39 Sumário Introdução Wagner Maciel Castilho 19 de fevereiro de 2018 Anhanguera
CAPITULO 2 A Primeira lei da termodinâmica
 Neste capítulo são introduzidos alguns dos conceitos fundamentais da termodinâmica. O foco da exposição é a conservação de energia a observação experimental de que a energia não pode ser destruída nem
Neste capítulo são introduzidos alguns dos conceitos fundamentais da termodinâmica. O foco da exposição é a conservação de energia a observação experimental de que a energia não pode ser destruída nem
Em todas as questões explicite seu raciocínio e os cálculos realizados. Boa prova!
 FIS01183 Prova 1 Semestre 2010/1 Turma H/HH Nome: Matrícula: Em todas as questões explicite seu raciocínio e os cálculos realizados. Boa prova! 1. Uma nova escala de temperatura, com a temperatura sendo
FIS01183 Prova 1 Semestre 2010/1 Turma H/HH Nome: Matrícula: Em todas as questões explicite seu raciocínio e os cálculos realizados. Boa prova! 1. Uma nova escala de temperatura, com a temperatura sendo
QB70C:// Química (Turmas S71/S72) Termodinâmica. Prof. Dr. Eduard Westphal ( Capítulo 8 Atkins (5ª ed.
 QB70C:// Química (Turmas S71/S72) Termodinâmica Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 8 Atkins (5ª ed.) Entalpia Em um sistema rígido (onde não exista outra forma
QB70C:// Química (Turmas S71/S72) Termodinâmica Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 8 Atkins (5ª ed.) Entalpia Em um sistema rígido (onde não exista outra forma
