Resolução: Simulado Dissertativo
|
|
|
- Vitória Beltrão Amaral
- 7 Há anos
- Visualizações:
Transcrição
1 Resolução: Simulado Dissertativo PROVA D-3 GRUPO EXTN 1ª QUESTÃO (FUVEST). Um analgésico é aplicado via intravenosa. Sua concentração no sangue, até atingir a concentração nula, varia com o tempo de acordo com a seguinte relação: c(t) = 400 k log 3(at + 1), em que t é dado em horas e c(t) é dado em mg/l. As constantes a e k são positivas. a) Qual é a concentração do analgésico no instante inicial t = 0? b) Calcule as constantes a e k, sabendo que, no instante t =, a concentração do analgésico no sangue é metade da concentração no instante inicial e que, no instante t = 8, a concentração do analgésico no sangue é nula. a) Queremos calcular c(0). Logo, temos c(0) = 400 k log3 1 = 400mg L. b) Sabendo que c() = 00mg L, vem 00 = 400 k log 3(a + 1) a = 3 00 k 1. Por outro lado, como c(8) = 0, temos = 400 k log 3(a 8 + 1) 8a + 1 = 3 k (3 k 1) + 1 = 3 k Logo, segue que a = (3 k ) = k = k = 3 k = 00. ª QUESTÃO (PUC RJ). Mônica tem uma blusa de cada uma das seguintes cores: branca, vermelha, amarela, preta e verde. Ela também tem uma calça de cada uma das seguintes cores: preta, azul, cinza e branca. a) De quantas maneiras Mônica pode escolher uma blusa e uma calça para sair? b) De quantas maneiras Mônica pode escolher uma blusa e uma calça de cores diferentes uma da outra? c) Na segunda-feira, Mônica usou calça azul e camisa preta. Na terça-feira, ela quer escolher uma calça e uma camisa de cores diferentes uma da outra. Sabendo que as roupas que ela usou na segunda-feira estão lavando (e apenas estas), de quantas maneiras ela pode escolher suas roupas? a) Como Mônica possui 5 blusas distintas e 4 calças distintas, o total de maneiras de escolher uma blusa e uma calça para sair é dado pelo princípio fundamental da contagem. Seja x o total de maneiras, temos: x = 5 4 x = 0 b) Se Mônica escolher a blusa de cor branca, há 3 possibilidades de escolha para a calça. Se Mônica escolher a blusa de cor vermelha, há 4 possibilidades de escolha para a calça. Se Mônica escolher a blusa de cor amarela, há 4 possibilidades de escolha para a calça. Se Mônica escolher a blusa de cor preta, há 3 possibilidades de escolha para a calça. Se Mônica escolher a blusa de cor verde, há 4 possibilidades de escolha para a calça. Então, nas condições dadas, há = 18 maneiras de Mônica escolher suas roupas.
2 c) Admitindo blusa e camisa como sinônimos, temos: Se Mônica escolher a blusa de cor branca, há possibilidades de escolha para a calça. Se Mônica escolher a blusa de cor vermelha, há 3 possibilidades de escolha para a calça. Se Mônica escolher a blusa de cor amarela, há 3 possibilidades de escolha para a calça. Se Mônica escolher a blusa de cor verde, há 3 possibilidades de escolha para a calça. Então, nas condições dadas, há = 11 maneiras de Mônica escolher suas roupas. 3ª QUESTÃO (FGV). Um sorvete de casquinha consiste de uma esfera (sorvete congelado) de raio 3 cm e um cone circular reto (casquinha), também com 3 cm de raio. Se o sorvete derreter, ele encherá a casquinha completa e exatamente. Suponha que o sorvete derretido ocupe 80% do volume que ele ocupa quando está congelado. Calcule a altura da casquinha. Seja h a altura que o sorvete derretido atinge na casquinha. Tem-se que: π 3 π 3 h = 3 h = 9,6cm ª QUESTÃO (UEL). As fórmulas de linhas na química orgânica são muitas vezes empregadas na tentativa de simplificar a notação de substâncias. Dessa maneira, as fórmulas de linhas para o butano e o metil-butano são representadas, respectivamente, por: Considere a substância representada pela estrutura a seguir. A partir dessas informações, responda aos itens a seguir. a) Qual a fórmula molecular dessa substância? b) Quantos substituintes estão ligados na cadeia principal? a) A partir da fórmula fornecida no enunciado, vem: b) Dois substituintes (radical metil) estão ligados na cadeia principal.
3 5ª QUESTÃO (UFJF). É comum a adição de metabissulfito de sódio (NaSO5) como substância conservante em vinhos. Essa prática é amparada pela legislação e tem procedimentos regulamentados. Um dos problemas com esse procedimento é que a decomposição desse conservante gera SO, que pode causar reações adversas nos consumidores. Responda aos itens abaixo. a) Escreva a equação química balanceada para decomposição térmica do metabissulfito de sódio em sulfito de sódio e dióxido de enxofre. Dado: íon sulfito = SO3 - b) Uma maneira de se determinar a concentração de dióxido de enxofre em vinhos é através da reação com iodo em meio aquoso, que gera ácido iodídrico e ácido sulfúrico. Escreva a equação química balanceada que representa a reação entre SO e I em água. c) A concentração máxima permitida para o SO em vinhos é de 60 ppm. Se para reagir completamente com 5 ml de uma amostra de vinho forem utilizados 13,5 ml de uma solução 0,001 mol L -1 de iodo, calcule a concentração de SO no vinho. Esse vinho tem concentração de SO dentro do limite imposto pela legislação? Justifique a sua resposta. a) NaSO5(s) NaSO3(s) + SO Δ (g) b) I (aq) + SO (aq) + H O ( ) HI (aq) + H SO 4(aq) c) Teremos: C1V1 = CV 3 C1 5 = (1,0 10 ) (13,5) 3 C1 =,7 10 mol / L 1 mol de SO 64g 3,7 10 mol x x = 0,173g de SO ou 173mg / L = 173ppm O vinho encontra-se dentro dos limites da legislação, pois a concentração determinada (173ppm) é menor que a permitida de 60 ppm. 6ª QUESTÃO (UFJF). Analise o diagrama de uma reação química: a) O processo representado pelo diagrama é endotérmico ou exotérmico? Justifique sua resposta. b) Considere as equações: C + S CS H = + 9 kj (s) (s) ( ) C(s) + O(g) CO(g) H = 393 kj N(g) + O(g) NO(g) H = kj 1 H (g) + O(g) H O( ) H = 86 kj Selecione as reações químicas que podem ser usadas como exemplos para o diagrama. Justifique sua resposta. a) Processo endotérmico, pois ocorre absorção de energia. b) Todas as reações cujo ΔH 0, ou seja, a primeira e a terceira reação.
4 7ª QUESTÃO (UEL). Messias está preparando um almoço e deseja gelar 10 latas da sua bebida preferida. Ele então as coloca dentro de uma caixa com isolamento térmico perfeito e sobre elas despeja gelo que está a uma temperatura de 0 C. Considerando que as trocas de calor se dão, única e exclusivamente, entre o gelo e as latas, pode-se afirmar que o módulo do calor perdido pelas latas é igual ao módulo do calor recebido pelo gelo. Sabendo que a temperatura inicial das latas é de 0 C, que a capacidade térmica de cada lata é de 400 cal/ C e que o calor latente de fusão do gelo é de 80 cal/g, responda aos itens a seguir. a) Determine a quantidade de calor extraído das latas até elas atingirem a temperatura de 0 C. Justifique sua resposta, apresentando os cálculos envolvidos na resolução deste item. b) Calcule a massa de gelo necessária para baixar a temperatura das latas para 0 C. Justifique sua resposta, apresentando os cálculos envolvidos na resolução deste item. Q a) A quantidade de calor ( ) Onde capacidade térmica das latas; variação de temperatura. C = Δ T = trocada entre as latas e o gelo é dada por: Q C T = Δ Assim, calculando para todas as latas, a quantidade de calor trocada pelas latas com o gelo é de: cal Q = C ΔT Q = latas ( 0 0) C Q = cal C lata Logo, em módulo, o calor trocado é de cal. b) Para determinar a massa mínima de gelo que o sistema deve ter, supondo que não existem perdas térmicas para o meio externo e para o recipiente, usamos a expressão do calor latente: Q m L Onde: massa de gelo fundente em gramas; calor latente de fusão do gelo. m = L = Q cal Q = m L m = m = m = 1000 g L 80 cal g = 8ª QUESTÃO (UERJ). No esquema, está representado um bloco de massa igual a 100 kg em equilíbrio estático. Determine, em newtons, a tração no fio ideal AB. P = mg P = P = N sen30 = ,5 = = =.000 N 0,5 cos30 = TAB = TAB TAB = N
5 9ª QUESTÃO (UFPR). Um paraquedista salta de um avião e cai livremente por uma distância vertical de 80m, antes de abrir o paraquedas. Quando este se abre, ele passa a sofrer uma desaceleração vertical de 4 m/s², chegando ao solo com uma velocidade vertical de módulo m/s. Supondo que, ao saltar do avião, a velocidade inicial do paraquedista na vertical era igual a zero e considerando g = 10 m/s², determine: a) O tempo total que o paraquedista permaneceu no ar, desde o salto até atingir o solo. b) A distância vertical total percorrida pelo paraquedista. a) Tempo total do salto até atingir o solo: t = t1+ t No primeiro momento, na queda livre do paraquedista. a t ΔS 1 1= vo t + 10 t 80 = 1 t1 = 16 t1 = 4 s Encontrando a velocidade no final do primeiro momento, v = v + a t 1 o 1 v1 = 10 4 v1 = 40 m s Assim, achando o tempo do segundo momento, temos que: v = v + a t 1 = 40 4 t t = 9,5 s Por fim, o tempo total será: t = t + t = 4 + 9,5 1 t = 13,5 s b) A distância total percorrida: ΔSt = ΔS1 + ΔS A distância percorrida no primeiro momento foi dada no enunciado (80 m). Para o segundo momento, temos que: v = v1 + a ΔS = 40 + ( 4) ΔS 40 ΔS = 8 ΔS = 199,5 m Logo, ΔS = ,5 t ΔSt = 79,5 m
6 10ª QUESTÃO (UNICAMP). Duas fatias iguais de batata, rica em amido, foram colocadas em dois recipientes, um com NaCl 5M e outro com HO. A cada 30 minutos as fatias eram retiradas da solução de NaCl 5M e da água, enxugadas e pesadas. A variação de peso dessas fatias e mostrada no gráfico a seguir. a) Explique a variação de peso observada na fatia de batata colocada em NaCl 5M e a observada na fatia de batata colocada em água. b) Hemácias colocadas em água teriam o mesmo comportamento das células da fatia da batata em água? Justifique. a) Em uma solução hipertônica (NaCl 5M) a fatia de batata perde água por osmose e perde peso. Colocadas na água há ganho de água, fato que justifica o ganho de peso. b) Não. Hemácias são células desprovidas de parede celular. O ganho excessivo de água provoca a ruptura da membrana plasmática. As células da fatia de batata não se rompem, pois apresentam a parede celular celulósica. 11ª QUESTÃO (FUVEST). As Figuras I, II e III esquematizam a circulação sanguínea em diferentes vertebrados. a) Analise a Figura II. A partir da cavidade apontada pela seta, ordene as demais cavidades cardíacas e os circuitos 1 e, na sequência correspondente à circulação do sangue. b) Faça o mesmo, em relação à Figura III. c) Qual(is) das três figuras mostra(m) o coração em que há mistura de sangue arterial e sangue venoso? d) Dê um exemplo de grupo de vertebrados para o tipo de circulação esquematizado em cada uma das três figuras. a) O sangue venoso presente na cavidade X (átrio esquerdo), da figura II, passa para o ventrículo e é bombeado para os pulmões (circuito 1). O sangue arterial retorna ao coração para a cavidade Z (átrio esquerdo), é bombeado para o ventrículo (Y) e é enviado para o circuito, correspondente à circulação sistêmica. b) O sangue venoso presente na cavidade X (átrio direito) é enviado para a cavidade Y (ventrículo direito) e é bombeado para as artérias pulmonares atingindo o circuito 1 (pulmões). O sangue arterial retorna para a cavidade W (átrio esquerdo) e é enviado para a cavidade Z (ventrículo esquerdo), de onde é bombeado para a artéria aorta em direção ao circuito, correspondente à circulação sistêmica. c) Figura II. d) Figura I: peixes. Figura II: répteis não crocodilianos Figura III: mamíferos
7 1ª QUESTÃO (UFU). Nos vertebrados, a digestão é extracelular. Com base nessa afirmação, responda: a) As aves apresentam moela. O que é esta estrutura e para que ela serve? b) No intestino delgado humano desembocam duas glândulas importantes: o pâncreas e o fígado. O que as diferencia? Qual é a função do fígado? c) Para que servem as vilosidades intestinais presentes no intestino delgado humano? a) A moela é o estômago mecânico das aves. Sua parede é musculosa e suas contrações auxiliam a redução do alimento a porções menores. È especialmente desenvolvidas nas aves granívoras. b) O fígado lança a bile no intestino delgado. O pâncreas secreta o suco digestório pancreático nesse órgão. O fígado produz e secreta a bile, cuja função é emulsificar as gorduras da dieta, facilitando a ação das enzimas lipases pancreática e entérica. c) As vilosidades intestinais presentes no intestino delgado humano aumentam a superfície de absorção alimentar
RESOLUÇÃO DO SIMULADO DISSERTATVIO
 RESOLUÇÃO DO SIMULADO DISSERTATVIO PROVA D-1 GRUPO EXTN 1. (FUVEST) A atividade das enzimas é influenciada pelo ph do meio. O gráfico abaixo mostra a velocidade de reação de duas enzimas que atuam na digestão
RESOLUÇÃO DO SIMULADO DISSERTATVIO PROVA D-1 GRUPO EXTN 1. (FUVEST) A atividade das enzimas é influenciada pelo ph do meio. O gráfico abaixo mostra a velocidade de reação de duas enzimas que atuam na digestão
PROVA DE QUÍMICA INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA
 CMISSÃ PERMANENTE DE SELEÇÃ CPESE MÓDUL II D PISM TRIÊNI 2013-2015 PRVA DE QUÍMICA INSTRUÇÕES PARA A REALIZAÇÃ DA PRVA Será excluído do concurso o candidato que for flagrado portando ou mantendo consigo
CMISSÃ PERMANENTE DE SELEÇÃ CPESE MÓDUL II D PISM TRIÊNI 2013-2015 PRVA DE QUÍMICA INSTRUÇÕES PARA A REALIZAÇÃ DA PRVA Será excluído do concurso o candidato que for flagrado portando ou mantendo consigo
EXERCÍCIO DE CIÊNCIAS COM GABARITO 8º ANO 1. (PUC-SP) O esquema abaixo é referente ao coração de um mamífero
 EXERCÍCIO DE CIÊNCIAS COM GABARITO 8º ANO 1. (PUC-SP) O esquema abaixo é referente ao coração de um mamífero a) Que números indicam artérias e veias? b) Que números indicam vasos por onde circulam sangue
EXERCÍCIO DE CIÊNCIAS COM GABARITO 8º ANO 1. (PUC-SP) O esquema abaixo é referente ao coração de um mamífero a) Que números indicam artérias e veias? b) Que números indicam vasos por onde circulam sangue
Exercícios de Tipos celulares e membranas
 Exercícios de Tipos celulares e membranas 1. (UFF, 2011) As células animais, vegetais e bacterianas apresentam diferenças estruturais relacionadas às suas características fisiológicas. A tabela abaixo
Exercícios de Tipos celulares e membranas 1. (UFF, 2011) As células animais, vegetais e bacterianas apresentam diferenças estruturais relacionadas às suas características fisiológicas. A tabela abaixo
LISTA DE EXERCÍCIOS FÍSICA - 1º EM CAPÍTULO 20 CALORIMETRIA PROF. BETO E PH
 LISTA DE EXERCÍCIOS FÍSICA - 1º EM CAPÍTULO 20 CALORIMETRIA PROF. BETO E PH 1) Um dos materiais que a artista Gilda Prieto utiliza em suas esculturas é o bronze. Esse material apresenta calor específico
LISTA DE EXERCÍCIOS FÍSICA - 1º EM CAPÍTULO 20 CALORIMETRIA PROF. BETO E PH 1) Um dos materiais que a artista Gilda Prieto utiliza em suas esculturas é o bronze. Esse material apresenta calor específico
Roteiro de Recuperação 1 Semestre 1, 2, 3 e 4 Momento INSTRUÇÕES PARA A PARTICIPAÇÃO NA RECUPERAÇÃO
 Roteiro de Recuperação 1 Semestre 1, 2, 3 e 4 Momento Nome: nº 3ª Série: Disciplina: Física Professor: Caio, João, Kobax Período de recuperação: de / a / INSTRUÇÕES PARA A PARTICIPAÇÃO NA RECUPERAÇÃO 1.
Roteiro de Recuperação 1 Semestre 1, 2, 3 e 4 Momento Nome: nº 3ª Série: Disciplina: Física Professor: Caio, João, Kobax Período de recuperação: de / a / INSTRUÇÕES PARA A PARTICIPAÇÃO NA RECUPERAÇÃO 1.
Ciências / 8º Ano / 1º Trimestre. Fornecimento e uso de energia
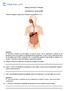 Ciências / 8º Ano / 1º Trimestre Fornecimento e uso de energia Observe a imagem a seguir para responder às questões 1, 2 e 3. Questão 1 Se retirarmos metade de nosso fígado, em poucos meses, ele se regenerará
Ciências / 8º Ano / 1º Trimestre Fornecimento e uso de energia Observe a imagem a seguir para responder às questões 1, 2 e 3. Questão 1 Se retirarmos metade de nosso fígado, em poucos meses, ele se regenerará
QUESTÃO 1 EXPECTATIVA DE RESPOSTA
 FÍSICA 1 Messias está preparando um almoço e deseja gelar 10 latas da sua bebida preferida. Ele então as coloca dentro de uma caixa com isolamento térmico perfeito e sobre elas despeja gelo que está a
FÍSICA 1 Messias está preparando um almoço e deseja gelar 10 latas da sua bebida preferida. Ele então as coloca dentro de uma caixa com isolamento térmico perfeito e sobre elas despeja gelo que está a
Fisiologia é o estudo das funções e funcionamento dos organismos vivos.
 Fisiologia Fisiologia é o estudo das funções e funcionamento dos organismos vivos. A fisiologia humana compreende os estudos sobre os principais sistemas presentes no organismo humano. Sistema Digestório
Fisiologia Fisiologia é o estudo das funções e funcionamento dos organismos vivos. A fisiologia humana compreende os estudos sobre os principais sistemas presentes no organismo humano. Sistema Digestório
SISTEMA DIGESTÓRIO MÓDULO 7 FISIOLOGIA
 SISTEMA DIGESTÓRIO MÓDULO 7 FISIOLOGIA SISTEMA DIGESTÓRIO O sistema digestório, responsável pela quebra dos alimentos e absorção dos nutrientes, é composto pelo tubo digestório e pelas glândulas anexas.
SISTEMA DIGESTÓRIO MÓDULO 7 FISIOLOGIA SISTEMA DIGESTÓRIO O sistema digestório, responsável pela quebra dos alimentos e absorção dos nutrientes, é composto pelo tubo digestório e pelas glândulas anexas.
LABORATÓRIO DE QUÍMICA QUI126 2ª LISTA DE EXERCÍCIOS
 Exercício 1. (UFMG, Adapt.) O rótulo de uma garrafa de vinagre indica que a concentração de ácido acético (CH3COOH) é 42g/L. A fim de verificar se a concentração da solução ácida corresponde à indicada
Exercício 1. (UFMG, Adapt.) O rótulo de uma garrafa de vinagre indica que a concentração de ácido acético (CH3COOH) é 42g/L. A fim de verificar se a concentração da solução ácida corresponde à indicada
Lista de exercícios de Química nº 10
 Nome: nº: Bimestre: 3º Ano/série: 3ª série Ensino: Médio Componente Curricular: Química Professor: Ricardo Honda Data: / / Lista de exercícios de Química nº 10 Revisão dos principais tópicos sobre Equilíbrio
Nome: nº: Bimestre: 3º Ano/série: 3ª série Ensino: Médio Componente Curricular: Química Professor: Ricardo Honda Data: / / Lista de exercícios de Química nº 10 Revisão dos principais tópicos sobre Equilíbrio
UFPR º Fase Física
 UFPR 05 º Fase Física. (Ufpr 05) Um paraquedista salta de um avião e cai livremente por uma distância vertical de 80m, antes de abrir o paraquedas. Quando este se abre, ele passa a sofrer uma desaceleração
UFPR 05 º Fase Física. (Ufpr 05) Um paraquedista salta de um avião e cai livremente por uma distância vertical de 80m, antes de abrir o paraquedas. Quando este se abre, ele passa a sofrer uma desaceleração
Exercícios de Circulação Comparada
 Exercícios de Circulação Comparada 1. (PUC) Relacione as descrições dos Sistemas Circulatórios com seus respectivos Filos animais: I - Ausente. O alimento é distribuído diretamente da cavidade gastrovascular.
Exercícios de Circulação Comparada 1. (PUC) Relacione as descrições dos Sistemas Circulatórios com seus respectivos Filos animais: I - Ausente. O alimento é distribuído diretamente da cavidade gastrovascular.
ROTEIRO DE ESTUDOS 2017 Disciplina: Ciências Ano: 8º ano Ensino: FII Nome:
 ROTEIRO DE ESTUDOS 2017 Disciplina: Ciências Ano: 8º ano Ensino: FII Nome: Orientações para estudo: Refazer as avaliações; Fazer exercícios dos capítulos sobre os sistemas digestório e respiratório. Entregar
ROTEIRO DE ESTUDOS 2017 Disciplina: Ciências Ano: 8º ano Ensino: FII Nome: Orientações para estudo: Refazer as avaliações; Fazer exercícios dos capítulos sobre os sistemas digestório e respiratório. Entregar
Revisão Específicas. Química Monitores: Luciana Lima e Rafael França 16-21/11/2015. Material de Apoio para Monitoria
 Revisão Específicas 1. (Ufpr) Considere as soluções I, II e III, descritas a seguir. I - Solução obtida pela adição de 9,80 g de H2SO4 (massa molar = 98,0 g) em água suficiente para completar o volume
Revisão Específicas 1. (Ufpr) Considere as soluções I, II e III, descritas a seguir. I - Solução obtida pela adição de 9,80 g de H2SO4 (massa molar = 98,0 g) em água suficiente para completar o volume
Instruções: Titulação: análise laboratorial de soluções. Entalpia e energia nas transformações químicas. Entalpia de ligação. Ciências da Natureza
 Ciências da Natureza Química Gabriela Rosa TRABALHO DE RECUPERAÇÃO 1ª ETAPA 1ª 10 pts 6,5 pts 18 2º A/B Instruções: Leia atentamente cada questão antes de resolvê-la. A interpretação faz parte desse trabalho.
Ciências da Natureza Química Gabriela Rosa TRABALHO DE RECUPERAÇÃO 1ª ETAPA 1ª 10 pts 6,5 pts 18 2º A/B Instruções: Leia atentamente cada questão antes de resolvê-la. A interpretação faz parte desse trabalho.
02- Analise a imagem abaixo: Nomeie os órgãos numerados de 1 a 5.
 PROFESSOR: EQUIPE DE CIÊNCIAS BANCO DE QUESTÕES - CIÊNCIAS - 8º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Associe as colunas.
PROFESSOR: EQUIPE DE CIÊNCIAS BANCO DE QUESTÕES - CIÊNCIAS - 8º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Associe as colunas.
1g / cm. 1g / cm. 80cal/ g
 1. (Unifesp 2015) Em um copo, de capacidade térmica 60cal / C e a 20 C, foram colocados 300mL de suco de laranja, também a 20 C, e, em seguida, dois cubos de gelo com 20 g cada um, a 0 C. Considere os
1. (Unifesp 2015) Em um copo, de capacidade térmica 60cal / C e a 20 C, foram colocados 300mL de suco de laranja, também a 20 C, e, em seguida, dois cubos de gelo com 20 g cada um, a 0 C. Considere os
17/11/2016. Válvula em espiral e cecos pilóricos = aumentam área de absorção no intestino. Anfíbios: cloaca; não apresentam dentes; língua protrátil.
 Peixes cartilaginosos Sistema digestório Sistema cardiovascular Peixes ósseos Válvula em espiral e cecos pilóricos = aumentam área de absorção no intestino. Aves: Anfíbios: cloaca; não apresentam dentes;
Peixes cartilaginosos Sistema digestório Sistema cardiovascular Peixes ósseos Válvula em espiral e cecos pilóricos = aumentam área de absorção no intestino. Aves: Anfíbios: cloaca; não apresentam dentes;
COLÉGIO DA POLÍCIA MILITAR
 COLÉGIO DA POLÍCIA MILITAR ASSESSORIA TÉCNICA Processo Avaliativo Recuperação - 3º Bimestre/2015 Disciplina: QUÍMICA 3ª série EM A/B Nome do aluno Nº Turma A Recuperação deve ser entregue no dia 08/09/2015.
COLÉGIO DA POLÍCIA MILITAR ASSESSORIA TÉCNICA Processo Avaliativo Recuperação - 3º Bimestre/2015 Disciplina: QUÍMICA 3ª série EM A/B Nome do aluno Nº Turma A Recuperação deve ser entregue no dia 08/09/2015.
LISTA DE EXERCÍCIOS 3º ANO
 . Em situação de desnutrição proteica severa, a pressão osmótica do plasma sanguíneo fica abaixo do normal e, consequentemente, ocorrera acúmulo de líquido intersticial nos tecidos periféricos do organismo
. Em situação de desnutrição proteica severa, a pressão osmótica do plasma sanguíneo fica abaixo do normal e, consequentemente, ocorrera acúmulo de líquido intersticial nos tecidos periféricos do organismo
 Lista de exercícios - Bloco 2 - Aula 25 a 28 - Equilíbrio Químico - Conceitos gerais e cálculo (Kc e Kp) 1. (Unicid - Medicina 2017) Considere os equilíbrios: 1. 2 SO 2 (g) + O 2 (g) 2 SO 3 (g) 25 Kc =
Lista de exercícios - Bloco 2 - Aula 25 a 28 - Equilíbrio Químico - Conceitos gerais e cálculo (Kc e Kp) 1. (Unicid - Medicina 2017) Considere os equilíbrios: 1. 2 SO 2 (g) + O 2 (g) 2 SO 3 (g) 25 Kc =
Termoquímica. Química 10/08/2015. Enem 15 Semanas. 1. Observando o diagrama a seguir, é correto afirmar que:
 Termoquímica 1. Observando o diagrama a seguir, é correto afirmar que: [Dadas as massas molares (g/mol): H=1 e O=16] a) para vaporizar 18g de água são liberados 10,5 kcal. b) o calor de reação, na síntese
Termoquímica 1. Observando o diagrama a seguir, é correto afirmar que: [Dadas as massas molares (g/mol): H=1 e O=16] a) para vaporizar 18g de água são liberados 10,5 kcal. b) o calor de reação, na síntese
Cinética e Eq. Químico Folha 10 João Roberto Fortes Mazzei
 01. Em um recipiente de 500 ml, encontram-se, em condições de equilíbrio, 10 mol/l de H 2 (g) e 0,01 mol/l de I 2 (g). Qual é a concentração do HI(g), sabendo-se que, nas condições do experimento, a constante
01. Em um recipiente de 500 ml, encontram-se, em condições de equilíbrio, 10 mol/l de H 2 (g) e 0,01 mol/l de I 2 (g). Qual é a concentração do HI(g), sabendo-se que, nas condições do experimento, a constante
Qui. Professores: Allan Rodrigues Xandão Monitor: Renan Micha
 Semana 19 Professores: Allan Rodrigues Xandão Monitor: Renan Micha Ao adicionarmos solutos não voláteis a um solv EXERCÍCIOS DE AULA 1. 2NaHCO 3(s) Na 2CO 3(s) + CO 2(g) + H 2O (g) Relativamente à equação
Semana 19 Professores: Allan Rodrigues Xandão Monitor: Renan Micha Ao adicionarmos solutos não voláteis a um solv EXERCÍCIOS DE AULA 1. 2NaHCO 3(s) Na 2CO 3(s) + CO 2(g) + H 2O (g) Relativamente à equação
FÍSICA Professores: Cezar, Luciano e Maragato.
 FÍSICA Professores: Cezar, Luciano e Maragato. Prova bem elaborada e com um bom nível de exigência. Parabéns à comissão da UFP responsável pela prova. A equipe de física do curso DOMÍNIO está muito feliz
FÍSICA Professores: Cezar, Luciano e Maragato. Prova bem elaborada e com um bom nível de exigência. Parabéns à comissão da UFP responsável pela prova. A equipe de física do curso DOMÍNIO está muito feliz
Dados: calor latente do gelo Lg = 80cal/g, calor específico da água c(h O) = 1,0 cal g C, calor específico do alumínio c(aø) = 0,22 cal g C.
 1. (Unicamp 95) Numa câmara frigorífica, um bloco de gelo de massa m=8,0kg desliza sobre rampa de madeira da figura a seguir, partindo do repouso, de uma altura h=1,8m. a) Se o atrito entre o gelo e a
1. (Unicamp 95) Numa câmara frigorífica, um bloco de gelo de massa m=8,0kg desliza sobre rampa de madeira da figura a seguir, partindo do repouso, de uma altura h=1,8m. a) Se o atrito entre o gelo e a
a) a velocidade do carrinho no ponto C; b) a aceleração do carrinho no ponto C; c) a força feita pelos trilhos sobre o carrinho no ponto C.
 1. (Fuvest-gv) Na figura a seguir, tem-se uma mola de massa desprezível e constante elástica 200 N/m, comprimida de 20 cm entre uma parede e um carrinho de 2,0 kg. Quando o carrinho é solto, toda a energia
1. (Fuvest-gv) Na figura a seguir, tem-se uma mola de massa desprezível e constante elástica 200 N/m, comprimida de 20 cm entre uma parede e um carrinho de 2,0 kg. Quando o carrinho é solto, toda a energia
Química: Termoquímica Vestibulares UNICAMP
 Química: Termoquímica Vestibulares 2015-2011 - UNICAMP 1. (Unicamp 2015) Água potável pode ser obtida a partir da água do mar basicamente através de três processos. Um desses processos é a osmose reversa;
Química: Termoquímica Vestibulares 2015-2011 - UNICAMP 1. (Unicamp 2015) Água potável pode ser obtida a partir da água do mar basicamente através de três processos. Um desses processos é a osmose reversa;
As figuras acima mostram as linhas de indução de um campo magnético uniforme B r
 1) No sistema mostrado abaixo, as roldanas e os fios são ideais e o atrito é considerado desprezível. As roldanas A, B, e C são fixas e as demais são móveis sendo que o raio da roldana F é o dobro do raio
1) No sistema mostrado abaixo, as roldanas e os fios são ideais e o atrito é considerado desprezível. As roldanas A, B, e C são fixas e as demais são móveis sendo que o raio da roldana F é o dobro do raio
E S C O L A S E C U N D Á R I A /3 A N T Ó N I O S É R G I O. Nome Nº Tª G R U P O I
 E S C O L A S E C U N D Á R I A /3 A N T Ó N I O S É R G I O Teste Escrito Data: 25 / 05 / 2018 CLASSIFICAÇÃO O PROFESSOR Nome Nº Tª G R U P O I 1. Na figura 1, A e B são relativos aos transportes de seiva
E S C O L A S E C U N D Á R I A /3 A N T Ó N I O S É R G I O Teste Escrito Data: 25 / 05 / 2018 CLASSIFICAÇÃO O PROFESSOR Nome Nº Tª G R U P O I 1. Na figura 1, A e B são relativos aos transportes de seiva
BANCO DE QUESTÕES - CIÊNCIAS - 8º ANO - ENSINO FUNDAMENTAL
 PROFESSOR: EQUIPE DE CIÊNCIAS BANCO DE QUESTÕES - CIÊNCIAS - 8º ANO - ENSINO FUNDAMENTAL ============================================================================ 01- Associe as colunas. (A) Fígado
PROFESSOR: EQUIPE DE CIÊNCIAS BANCO DE QUESTÕES - CIÊNCIAS - 8º ANO - ENSINO FUNDAMENTAL ============================================================================ 01- Associe as colunas. (A) Fígado
28 C 29 E. A bússola deve orientar-se obedecendo o campo magnético resultante no ponto P, ou seja, levando-se em conta a influência dos dois fios.
 FÍSICA 8 C O Eletromagnetismo estuda os fenômenos que surgem da interação entre campo elétrico e campo magnético. Hans Christian Oersted, em 80, realizou uma experiência fundamental para o desenvolvimento
FÍSICA 8 C O Eletromagnetismo estuda os fenômenos que surgem da interação entre campo elétrico e campo magnético. Hans Christian Oersted, em 80, realizou uma experiência fundamental para o desenvolvimento
COLÉGIO MONJOLO 1 SEMESTRE QUÍMICA PROF. RICARDO MENON
 COLÉGIO MONJOLO 1 SEMESTRE - 2018 QUÍMICA PROF. RICARDO MENON Aluno(a): Série: SuperExatas LISTA DE EXERCÍCIOS EQUILÍBRIO QUÍMICO 1) Escreva a equação de equilíbrio para as seguintes reações: a) N2(g)
COLÉGIO MONJOLO 1 SEMESTRE - 2018 QUÍMICA PROF. RICARDO MENON Aluno(a): Série: SuperExatas LISTA DE EXERCÍCIOS EQUILÍBRIO QUÍMICO 1) Escreva a equação de equilíbrio para as seguintes reações: a) N2(g)
Plano de Recuperação Semestral 1º Semestre 2016
 Disciplina: CIÊNCIAS Série/Ano: 8º ANO Professores: Cybelle / José Henrique / Sarah / Tiê Objetivo: Proporcionar ao aluno a oportunidade de resgatar os conteúdos trabalhados durante o 1º semestre nos quais
Disciplina: CIÊNCIAS Série/Ano: 8º ANO Professores: Cybelle / José Henrique / Sarah / Tiê Objetivo: Proporcionar ao aluno a oportunidade de resgatar os conteúdos trabalhados durante o 1º semestre nos quais
2. Considere um bloco de gelo de massa 300g á temperatura de 20 C, sob pressão normal. Sendo L F
 1. Considere um bloco de gelo de massa 300g encontra-se a 0 C. Para que todo gelo se derreta, obtendo água a 0 C são necessárias 24.000 cal. Determine o calor latente de fusão do gelo. 2. Considere um
1. Considere um bloco de gelo de massa 300g encontra-se a 0 C. Para que todo gelo se derreta, obtendo água a 0 C são necessárias 24.000 cal. Determine o calor latente de fusão do gelo. 2. Considere um
a) Calcular a energia cinética com que a moeda chega ao piso.
 Dados: Considere, quando necessário: g = 10 m/s 2 ; sen 30 = cos 60 = 1/2; cos 30 = sen 60 = 3/2; calor específico da água = 1 cal/g C. 1) Uma pessoa deixa uma moeda cair, e, então, ouve-se o barulho do
Dados: Considere, quando necessário: g = 10 m/s 2 ; sen 30 = cos 60 = 1/2; cos 30 = sen 60 = 3/2; calor específico da água = 1 cal/g C. 1) Uma pessoa deixa uma moeda cair, e, então, ouve-se o barulho do
2.a SÉRIE: Ensino: Médio Valor: 4,0 (quatro) pontos
 Nome: nº. 2.a SÉRIE: Ensino: Médio Valor: 4,0 (quatro) pontos Prof. PH Disciplina: Química Lista de Exercícios valor 4,0 (quatro) pontos DATA DE ENTREGA: 10 DE NOVEMBRO (SEXTA-FEIRA) Equilíbrio Químico
Nome: nº. 2.a SÉRIE: Ensino: Médio Valor: 4,0 (quatro) pontos Prof. PH Disciplina: Química Lista de Exercícios valor 4,0 (quatro) pontos DATA DE ENTREGA: 10 DE NOVEMBRO (SEXTA-FEIRA) Equilíbrio Químico
2 ª Fase Exame Discursivo
 02/12/2007 2 ª Fase Exame Discursivo física Caderno de prova Este caderno, com doze páginas numeradas seqüencialmente, contém dez questões de Física. Não abra o caderno antes de receber autorização. INSTRUÇÕES
02/12/2007 2 ª Fase Exame Discursivo física Caderno de prova Este caderno, com doze páginas numeradas seqüencialmente, contém dez questões de Física. Não abra o caderno antes de receber autorização. INSTRUÇÕES
COLÉGIO VISCONDE DE PORTO SEGURO Unidade I Ensino Fundamental e Ensino Médio
 COLÉGIO VISCONDE DE PORTO SEGURO Unidade I - 2008 Ensino Fundamental e Ensino Médio Aluno (a): nº Classe: 2-2 Lista de exercícios para estudos de recuperação de Física Trimestre: 2º Data: / /2008 1. (Ufpr)
COLÉGIO VISCONDE DE PORTO SEGURO Unidade I - 2008 Ensino Fundamental e Ensino Médio Aluno (a): nº Classe: 2-2 Lista de exercícios para estudos de recuperação de Física Trimestre: 2º Data: / /2008 1. (Ufpr)
P2 - PROVA DE QUÍMICA GERAL - 12/05/12
 P2 - PROVA DE QUÍMICA GERAL - 12/05/12 Nome: GABARITO Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados: T (K) = T ( C) + 273,15 R = 8,314
P2 - PROVA DE QUÍMICA GERAL - 12/05/12 Nome: GABARITO Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados: T (K) = T ( C) + 273,15 R = 8,314
Matemática. Educa teu filho no caminho que deve andar, e quando grande não se desviará dele Prov.22.6
 Educa teu filho no caminho que deve andar, e quando grande não se desviará dele Prov.22.6 Bateria de Exercícios Data: 20/05/2016 Turma: 2º Ano Área II Aluno (a): Prezado aluno caso prefira responder na
Educa teu filho no caminho que deve andar, e quando grande não se desviará dele Prov.22.6 Bateria de Exercícios Data: 20/05/2016 Turma: 2º Ano Área II Aluno (a): Prezado aluno caso prefira responder na
01- Qual é o nome dado ao sistema responsável pela extração dos nutrientes dos alimentos e como podemos classificar este processo? R.
 PROFESSOR: EQUIPE DE CIÊNCIAS BANCO DE QUESTÕES - CIÊNCIAS - 8º ANO - ENSINO FUNDAMENTAL ============================================================================ 01- Qual é o nome dado ao sistema responsável
PROFESSOR: EQUIPE DE CIÊNCIAS BANCO DE QUESTÕES - CIÊNCIAS - 8º ANO - ENSINO FUNDAMENTAL ============================================================================ 01- Qual é o nome dado ao sistema responsável
LISTA DE RECUPERAÇÃO. Química SÉRIE: 2º ANO DATA: 04 / 10 / mol L s, a velocidade de desaparecimento do ozônio na
 LISTA DE RECUPERAÇÃO Professor: Rodney Química SÉRIE: º ANO DATA: 04 / 10 / 016 Conteúdo para a recuperação do 3º Bimestre : Cinética Química Equilíbrio Químico 1. Os veículos emitem óxidos de nitrogênio
LISTA DE RECUPERAÇÃO Professor: Rodney Química SÉRIE: º ANO DATA: 04 / 10 / 016 Conteúdo para a recuperação do 3º Bimestre : Cinética Química Equilíbrio Químico 1. Os veículos emitem óxidos de nitrogênio
UNIVERSIDADE FEDERAL DE OURO PRETO Instituto de Ciências Exatas e Biológicas. Mestrado Profissional em Ensino de Ciências
 UNIVERSIDADE FEDERAL DE OURO PRETO Instituto de Ciências Exatas e Biológicas Mestrado Profissional em Ensino de Ciências Seleção da primeira etapa de avaliação em conhecimentos específicos Instruções para
UNIVERSIDADE FEDERAL DE OURO PRETO Instituto de Ciências Exatas e Biológicas Mestrado Profissional em Ensino de Ciências Seleção da primeira etapa de avaliação em conhecimentos específicos Instruções para
4. (G1) Se soltarmos um tijolo ele vai (ganhar ou perder?) energia cinética. Para onde vai ou de onde vem essa energia cinética?
 1. (Unicamp) Uma atração muito popular nos circos é o "Globo da Morte", que consiste numa gaiola de forma esférica no interior da qual se movimenta uma pessoa pilotando uma motocicleta. Considere um globo
1. (Unicamp) Uma atração muito popular nos circos é o "Globo da Morte", que consiste numa gaiola de forma esférica no interior da qual se movimenta uma pessoa pilotando uma motocicleta. Considere um globo
Plano de Recuperação Semestral 1º Semestre 2017
 Disciplina: CIÊNCIAS Série/Ano: 8º ANO Professores: Cybelle / José Henrique / Sarah / Tiê Objetivo: Proporcionar ao aluno a oportunidade de resgatar os conteúdos trabalhados durante o 1º semestre nos quais
Disciplina: CIÊNCIAS Série/Ano: 8º ANO Professores: Cybelle / José Henrique / Sarah / Tiê Objetivo: Proporcionar ao aluno a oportunidade de resgatar os conteúdos trabalhados durante o 1º semestre nos quais
Lista de Exercícios Lei de Hess, Cinética Química e Equilíbrio Químico Prof. Benfica
 Lista de Exercícios Lei de Hess, Cinética Química e Equilíbrio Químico Prof. Benfica 1) A entalpia da reação (I) não pode ser medida diretamente em um calorímetro porque a reação de carbono com excesso
Lista de Exercícios Lei de Hess, Cinética Química e Equilíbrio Químico Prof. Benfica 1) A entalpia da reação (I) não pode ser medida diretamente em um calorímetro porque a reação de carbono com excesso
(aq) + H 3 O + (aq) K 1 = 1,0 x (aq) + H 3 O + (aq) K 2 = 1,0 x 10-11
 Questão 1 O ácido carbônico é formado quando se borbulha o dióxido de carbono em água. Ele está presente em águas gaseificadas e refrigerantes. Em solução aquosa, ele pode sofrer duas dissociações conforme
Questão 1 O ácido carbônico é formado quando se borbulha o dióxido de carbono em água. Ele está presente em águas gaseificadas e refrigerantes. Em solução aquosa, ele pode sofrer duas dissociações conforme
Questões de Exame Resolvidas. Física e Química A. 11. ano. Química
 Questões de Exame Resolvidas Física e Química A 11. ano Química Índice Apresentação 3 Questões de Exame e de Testes Intermédios Química 10.º ano Domínio 1 Elementos químicos e sua organização 7 Subdomínio
Questões de Exame Resolvidas Física e Química A 11. ano Química Índice Apresentação 3 Questões de Exame e de Testes Intermédios Química 10.º ano Domínio 1 Elementos químicos e sua organização 7 Subdomínio
DATA: 19/12 / 2017 VALOR: 20,0 NOTA:
 DISCIPLINA: CIÊNCIAS PROFESSORES: MÁRCIA DATA: 19/12 / 2017 VALOR: 20,0 NOTA: TRABALHO DE RECUPERAÇÃO FINAL SÉRIE: 8º ano TURMAS:A/B ALUNO (A): Nº: 01. RELAÇÃO DOS CONTEÚDOS CAPÍTULO 2 - Alimentos e sistema
DISCIPLINA: CIÊNCIAS PROFESSORES: MÁRCIA DATA: 19/12 / 2017 VALOR: 20,0 NOTA: TRABALHO DE RECUPERAÇÃO FINAL SÉRIE: 8º ano TURMAS:A/B ALUNO (A): Nº: 01. RELAÇÃO DOS CONTEÚDOS CAPÍTULO 2 - Alimentos e sistema
PROVA PARA ALUNOS DO 1 E 2 ANO
 LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: a 3 FASE o o PROVA PARA ALUNOS DO 1 E 2 ANO 1 Essa prova destina-se exclusivamente aos alunos do 1 o e 2 o ano e contém vinte (20) questões. 2 Os alunos do 1 o ano
LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: a 3 FASE o o PROVA PARA ALUNOS DO 1 E 2 ANO 1 Essa prova destina-se exclusivamente aos alunos do 1 o e 2 o ano e contém vinte (20) questões. 2 Os alunos do 1 o ano
Escola Prof. Reynaldo dos Santos P á g i n a 1. Teste Tema 3 Biologia
 Escola Prof. Reynaldo dos Santos P á g i n a 1 1. A figura ao lado mostra um esquema que representa o corte transversal de uma folha de angiospérmica 1.1. O que representam as setas? 1.2. Faça a legenda
Escola Prof. Reynaldo dos Santos P á g i n a 1 1. A figura ao lado mostra um esquema que representa o corte transversal de uma folha de angiospérmica 1.1. O que representam as setas? 1.2. Faça a legenda
PROVA PARA AVALIAÇÃO DE CAPACIDADE PARA FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS 2016/2017. Instituto Superior de Engenharia (ISE)
 PROVA PARA AVALIAÇÃO DE CAPACIDADE PARA FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS 2016/2017 Instituto Superior de Engenharia (ISE) Licenciaturas em Engenharia Civil (ISE), Engenharia Elétrica
PROVA PARA AVALIAÇÃO DE CAPACIDADE PARA FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS 2016/2017 Instituto Superior de Engenharia (ISE) Licenciaturas em Engenharia Civil (ISE), Engenharia Elétrica
SISTEMA DIGESTÓRIO 3ª SÉRIE BIOLOGIA PROF. GRANGEIRO 1º BIM
 SISTEMA DIGESTÓRIO 3ª SÉRIE BIOLOGIA PROF. GRANGEIRO 1º BIM QUESTÃO 1 O gráfico abaixo se refere à atividade de uma enzima proteolítica que atua no trato digestório: A enzima em questão é a: a) Tripsina,
SISTEMA DIGESTÓRIO 3ª SÉRIE BIOLOGIA PROF. GRANGEIRO 1º BIM QUESTÃO 1 O gráfico abaixo se refere à atividade de uma enzima proteolítica que atua no trato digestório: A enzima em questão é a: a) Tripsina,
Equilíbrio Químico Folha 2.1 Prof.: João Roberto Mazzei
 01. A cisteína é um aminoácido que contém enxofre e é encontrada na feijoada, devido às proteínas da carne e derivados. A reação de conversão da cisteína em cistina ocorre de acordo com a seguinte equação
01. A cisteína é um aminoácido que contém enxofre e é encontrada na feijoada, devido às proteínas da carne e derivados. A reação de conversão da cisteína em cistina ocorre de acordo com a seguinte equação
Lista 10: Energia. Questões. encontrar razões plausíveis para justificar suas respostas sem o uso de equações.
 Lista 10: Energia Importante: 1. Ler os enunciados com atenção. 2. Responder a questão de forma organizada, mostrando o seu raciocínio de forma coerente. 3. Siga a estratégia para resolução de problemas
Lista 10: Energia Importante: 1. Ler os enunciados com atenção. 2. Responder a questão de forma organizada, mostrando o seu raciocínio de forma coerente. 3. Siga a estratégia para resolução de problemas
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. ALUNO(a): Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
 GOIÂNIA, / / 2015 PROFESSORA: Núbia de Andrade DISCIPLINA:QUÌMICA SÉRIE: 3º ALUNO(a): Entrega dia 16/09/2016 No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes
GOIÂNIA, / / 2015 PROFESSORA: Núbia de Andrade DISCIPLINA:QUÌMICA SÉRIE: 3º ALUNO(a): Entrega dia 16/09/2016 No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes
Esta avaliação é composta de 13 questões, das quais você deverá escolher apenas 10 para responder.
 2º EM Biologia B Marli Av. Trimestral 30/10/15 INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA LEIA COM MUITA ATENÇÃO 1. Verifique, no cabeçalho desta prova, se seu nome, número e turma estão corretos. 2. Esta prova
2º EM Biologia B Marli Av. Trimestral 30/10/15 INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA LEIA COM MUITA ATENÇÃO 1. Verifique, no cabeçalho desta prova, se seu nome, número e turma estão corretos. 2. Esta prova
Sistema circulatório
 Ficha de Treino FT SC1 1. Em laboratório, é possível separar os constituintes do sangue. 1.1. Diz quais são os constituintes do sangue. 1.2. Das células sanguíneas, refere as que desempenham um papel importante
Ficha de Treino FT SC1 1. Em laboratório, é possível separar os constituintes do sangue. 1.1. Diz quais são os constituintes do sangue. 1.2. Das células sanguíneas, refere as que desempenham um papel importante
A maioria dos alimentos precisa ser transformada para entrar nas células e realmente nutrir o organismo.
 Science Photo Library/Latinstock A maioria dos alimentos precisa ser transformada para entrar nas células e realmente nutrir o organismo. O que acontece com o amido de um sanduíche de queijo na boca? E
Science Photo Library/Latinstock A maioria dos alimentos precisa ser transformada para entrar nas células e realmente nutrir o organismo. O que acontece com o amido de um sanduíche de queijo na boca? E
PROCESSO SELETIVO TURMA DE 2016 FASE 1 PROVA DE FÍSICA E SEU ENSINO
 PROCESSO SELETIVO TURMA DE 2016 FASE 1 PROVA DE FÍSICA E SEU ENSINO Caro professor, cara professora, esta prova tem 2 partes; a primeira parte é objetiva, constituída por 14 questões de múltipla escolha,
PROCESSO SELETIVO TURMA DE 2016 FASE 1 PROVA DE FÍSICA E SEU ENSINO Caro professor, cara professora, esta prova tem 2 partes; a primeira parte é objetiva, constituída por 14 questões de múltipla escolha,
MAMÍFEROS. 15 Sistema Poliedro de Ensino Professora Giselle Cherutti
 MAMÍFEROS Capítulo 15 Sistema Poliedro de Ensino Professora Giselle Cherutti CARACTERÍSTICAS GERAIS DOS MAMÍFEROS Aquáticos: Habitat: Mamíferos podem ser terrestres: Único mamífero que voa: Pelos Estratificada
MAMÍFEROS Capítulo 15 Sistema Poliedro de Ensino Professora Giselle Cherutti CARACTERÍSTICAS GERAIS DOS MAMÍFEROS Aquáticos: Habitat: Mamíferos podem ser terrestres: Único mamífero que voa: Pelos Estratificada
DISCIPLINA: SÉRIE: 2º. ALUNO(a):
 GOIÂNIA, / / 2015 PROFESSOR: DISCIPLINA: SÉRIE: 2º ALUNO(a): NOTA: No Anhanguera você é + Enem 1) (UFSCar/2009) O sistema circulatório dos vertebrados mostra uma evolução ocorrida entre os grandes grupos.
GOIÂNIA, / / 2015 PROFESSOR: DISCIPLINA: SÉRIE: 2º ALUNO(a): NOTA: No Anhanguera você é + Enem 1) (UFSCar/2009) O sistema circulatório dos vertebrados mostra uma evolução ocorrida entre os grandes grupos.
TA Teste de Avaliação 1
 TA Escola Data Nome N.º Turma Professor Classificação Utilize apenas caneta ou esferográfica de tinta indelével azul ou preta. Pode utilizar régua, esquadro, transferidor e máquina de calcular gráfica.
TA Escola Data Nome N.º Turma Professor Classificação Utilize apenas caneta ou esferográfica de tinta indelével azul ou preta. Pode utilizar régua, esquadro, transferidor e máquina de calcular gráfica.
Fisiologia: Digestão, Respiração e Circulação
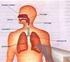 Fisiologia: Digestão, Respiração e Circulação Fisiologia: Digestão, Respiração e Circulação 1. Um laboratório analisou algumas reações ocorridas durante o processo de digestão do amido em seres humanos.
Fisiologia: Digestão, Respiração e Circulação Fisiologia: Digestão, Respiração e Circulação 1. Um laboratório analisou algumas reações ocorridas durante o processo de digestão do amido em seres humanos.
Exercícios de Digestão Comparada
 Exercícios de Digestão Comparada 1. (UEL) No esquema a seguir, estão representados 4 tubos de ensaio com os seus componentes. O material retirado de determinado órgão do rato foi adicionado aos tubos de
Exercícios de Digestão Comparada 1. (UEL) No esquema a seguir, estão representados 4 tubos de ensaio com os seus componentes. O material retirado de determinado órgão do rato foi adicionado aos tubos de
Dinâmica aula 02 Atrito e Plano Inclinado
 1) figura abaixo ilustra três corpos, e C unidos por fio inextensível e de massa desprezível. s massas dos corpos são, respectivamente, iguais a 10 kg, 15 kg e 25 C kg. intensidade da força F é 100 N e
1) figura abaixo ilustra três corpos, e C unidos por fio inextensível e de massa desprezível. s massas dos corpos são, respectivamente, iguais a 10 kg, 15 kg e 25 C kg. intensidade da força F é 100 N e
GOIÂNIA, / / PROFESSOR: Mário Neto. Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
 GOIÂNIA, / / 2016 PROFESSOR: Mário Neto DISCIPLINA: Ciências da natureza SÉRIE: 2º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
GOIÂNIA, / / 2016 PROFESSOR: Mário Neto DISCIPLINA: Ciências da natureza SÉRIE: 2º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
Sala de Estudos FÍSICA - Lucas 2 trimestre Ensino Médio 3º ano classe: Prof.LUCAS Nome: nº Sala de Estudos Força Elástica e Trabalho Mecânico
 Sala de Estudos FÍSICA - Lucas 2 trimestre Ensino Médio 3º ano classe: Prof.LUCAS Nome: nº Sala de Estudos Força Elástica e Trabalho Mecânico 1. (Uern 2013) A tabela apresenta a força elástica e a deformação
Sala de Estudos FÍSICA - Lucas 2 trimestre Ensino Médio 3º ano classe: Prof.LUCAS Nome: nº Sala de Estudos Força Elástica e Trabalho Mecânico 1. (Uern 2013) A tabela apresenta a força elástica e a deformação
Escola Secundária de Lagoa. Ficha de Trabalho 16. Exercícios. Física e Química A 11º Ano Paula Melo Silva
 Escola Secundária de Lagoa Física e Química A 11º Ano Paula Melo Silva Exercícios Ficha de Trabalho 16 Global 1. Um certo ião negativo, X 3-, tem um número total de eletrões de 18 e o seu número de massa
Escola Secundária de Lagoa Física e Química A 11º Ano Paula Melo Silva Exercícios Ficha de Trabalho 16 Global 1. Um certo ião negativo, X 3-, tem um número total de eletrões de 18 e o seu número de massa
GABARITO - QUÍMICA - Grupo A
 GABARITO - QUÍMICA - Grupo A 1 a QUESTÃO: (2,0 pontos) Avaliador Revisor O teor do íon Cl - existente nos fluidos corporais pode ser determinado através de uma analise volumétrica do íon Cl - com o íon
GABARITO - QUÍMICA - Grupo A 1 a QUESTÃO: (2,0 pontos) Avaliador Revisor O teor do íon Cl - existente nos fluidos corporais pode ser determinado através de uma analise volumétrica do íon Cl - com o íon
ESTUDO DIRIGIDO DE FÍSICA 2º EM
 ESTUDO DIRIGIDO DE FÍSICA 2º EM 01 (Vunesp) Dado o circuito a seguir, onde G é um galvanômetro e ε uma bateria, calcule X em função das resistências R 1, R 2 e R 3, para que a corrente por G seja nula.
ESTUDO DIRIGIDO DE FÍSICA 2º EM 01 (Vunesp) Dado o circuito a seguir, onde G é um galvanômetro e ε uma bateria, calcule X em função das resistências R 1, R 2 e R 3, para que a corrente por G seja nula.
CIÊNCIAS HUMANAS E SUAS TECNOLOGIAS. voltar índice próximo CIÊNCIAS. Unidade º ANO» UNIDADE 1» CAPÍTULO 3
 HUMANAS E SUAS TECNOLOGIAS CIÊNCIAS Unidade 41 www.sejaetico.com.br 8º ANO ALIMENTAÇÃO E DIGESTÃO NO SER HUMANO Índice ÍNDICE Por que nos alimentamos? www.sejaetico.com.br 3 Por que nos alimentamos? Os
HUMANAS E SUAS TECNOLOGIAS CIÊNCIAS Unidade 41 www.sejaetico.com.br 8º ANO ALIMENTAÇÃO E DIGESTÃO NO SER HUMANO Índice ÍNDICE Por que nos alimentamos? www.sejaetico.com.br 3 Por que nos alimentamos? Os
SOS QUÍMICA - O SITE DO PROFESSOR SAUL SANTANA.
 SOS QUÍMICA - O SITE DO PROFESSOR SAUL SANTANA. QUESTÕES LISTA DE EXERCÍCIOS Cinética Química. 1) A tabela abaixo mostra a variação da massa de peróxido de hidrogênio que ocorre na reação de decomposição
SOS QUÍMICA - O SITE DO PROFESSOR SAUL SANTANA. QUESTÕES LISTA DE EXERCÍCIOS Cinética Química. 1) A tabela abaixo mostra a variação da massa de peróxido de hidrogênio que ocorre na reação de decomposição
QUÍMICA. Prof. Daniel Pires TERMOQUÍMICA
 QUÍMICA Prof. Daniel Pires TERMOQUÍMICA 1 QUESTÕES 1. (Uerj 13) A equação química abaixo representa a reação da produção industrial de gás hidrogênio. H O g C s CO g H g Na determinação da variação de
QUÍMICA Prof. Daniel Pires TERMOQUÍMICA 1 QUESTÕES 1. (Uerj 13) A equação química abaixo representa a reação da produção industrial de gás hidrogênio. H O g C s CO g H g Na determinação da variação de
Processo Seletivo/UFU - julho ª Prova Comum FÍSICA QUESTÃO 11
 TIPO 1 Processo Seletivo/UFU - julho 2007-2ª Prova Comum FÍSICA QUESTÃO 11 Uma pequena esfera de massa M 1, inicialmente em repouso, é abandonada de uma altura de 1,8 m de altura, posição A da figura abaixo.
TIPO 1 Processo Seletivo/UFU - julho 2007-2ª Prova Comum FÍSICA QUESTÃO 11 Uma pequena esfera de massa M 1, inicialmente em repouso, é abandonada de uma altura de 1,8 m de altura, posição A da figura abaixo.
Calorimetria (Unesp 92) Considere as seguintes afirmações incompletas:
 1. (Fuvest 93) Um recipiente de vidro de 500 g e calor específico 0,20 cal/g C contém 500 g de água cujo calor específico é 1,0 cal/g C. O sistema encontra-se isolado e em equilíbrio térmico. Quando recebe
1. (Fuvest 93) Um recipiente de vidro de 500 g e calor específico 0,20 cal/g C contém 500 g de água cujo calor específico é 1,0 cal/g C. O sistema encontra-se isolado e em equilíbrio térmico. Quando recebe
P4 - PROVA DE QUÍMICA GERAL 05/12/12
 P4 - PROVA DE QUÍMICA GERAL 05/12/12 Nome: GABARITO Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Constantes e equações: 273,15 K = 0 C R = 0,0821
P4 - PROVA DE QUÍMICA GERAL 05/12/12 Nome: GABARITO Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Constantes e equações: 273,15 K = 0 C R = 0,0821
RESOLUÇÃO DO SIMULADO DISSERTATVIO
 RESOLUÇÃO DO SIMULADO DISSERTATVIO PROVA D-3 GRUPO EXTN 01. (UFG) Uma indústria armazena um produto em cilindros circulares retos com quatro metros de altura e raio da base medindo R metros. Prevendo-se
RESOLUÇÃO DO SIMULADO DISSERTATVIO PROVA D-3 GRUPO EXTN 01. (UFG) Uma indústria armazena um produto em cilindros circulares retos com quatro metros de altura e raio da base medindo R metros. Prevendo-se
Gabarito da lista de revisão sobre Sistema Circulatório Prof: Marcus Ferrassoli
 Gabarito da lista de revisão sobre Sistema Circulatório Prof: Marcus Ferrassoli Resposta da questão 1: No coração humano a saída do sangue rico em oxigênio (arterial) se dá pela artéria aorta. Resposta
Gabarito da lista de revisão sobre Sistema Circulatório Prof: Marcus Ferrassoli Resposta da questão 1: No coração humano a saída do sangue rico em oxigênio (arterial) se dá pela artéria aorta. Resposta
1º BIMESTRE. Série Turma (s) Turno 3º A B C D E F G H MATUTINO Disciplina: QUÍMICA Professor: CHARLYS FERNANDES Data: / / 2017 Aluno (a): Nº
 1º BIMESTRE Visto do Professor Nota (Fuvest) A uma determinada temperatura, as substâncias HI, H2 e I2 estão no estado gasoso. A essa temperatura, o equilíbrio entre as três substâncias foi estudado, em
1º BIMESTRE Visto do Professor Nota (Fuvest) A uma determinada temperatura, as substâncias HI, H2 e I2 estão no estado gasoso. A essa temperatura, o equilíbrio entre as três substâncias foi estudado, em
Olimpíada Brasileira de Física ª Fase
 Olimpíada Brasileira de Física 2001 3ª Fase 1º e 2º Anos eia com atenção todas as instruções seguintes. As questões 01 a 16 são destinadas exclusivamente aos alunos do 1º e 2º anos, os quais devem escolher
Olimpíada Brasileira de Física 2001 3ª Fase 1º e 2º Anos eia com atenção todas as instruções seguintes. As questões 01 a 16 são destinadas exclusivamente aos alunos do 1º e 2º anos, os quais devem escolher
Com base nos dados acima, responda as questões propostas (cuidado com as unidades):
 Curso: Farmácia Atenção, dois dos exercícios da lista entrarão na P1. Concentrações: 01. Em uma rápida pesquisa pela internet é possível achar diversas receitas relacionadas à preparação de alguns cosméticos
Curso: Farmácia Atenção, dois dos exercícios da lista entrarão na P1. Concentrações: 01. Em uma rápida pesquisa pela internet é possível achar diversas receitas relacionadas à preparação de alguns cosméticos
UNIVERSIDADE ESTADUAL DO SUDOESTE DA BAHIA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA EXAME GERAL EM QUÍMICA EDITAL N 002/2017
 UNIVERSIDADE ESTADUAL DO SUDOESTE DA BAHIA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA EXAME GERAL EM QUÍMICA EDITAL N 002/2017 Seleção para o 1º Semestre de 2017 14 de Fevereiro de 2017 CADERNO DE QUESTÕES Tempo
UNIVERSIDADE ESTADUAL DO SUDOESTE DA BAHIA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA EXAME GERAL EM QUÍMICA EDITAL N 002/2017 Seleção para o 1º Semestre de 2017 14 de Fevereiro de 2017 CADERNO DE QUESTÕES Tempo
ESCOLA SECUNDÁRIA DE CASQUILHOS
 ESCOLA SECUNDÁRIA DE CASQUILHOS 5º teste sumativo de FQA 02. março. 2015 Versão 1 11º Ano Turma A Professor: Maria do Anjo Albuquerque Duração da prova: 90 minutos. Este teste é constituído por 8 páginas
ESCOLA SECUNDÁRIA DE CASQUILHOS 5º teste sumativo de FQA 02. março. 2015 Versão 1 11º Ano Turma A Professor: Maria do Anjo Albuquerque Duração da prova: 90 minutos. Este teste é constituído por 8 páginas
1ª QUESTÃO Valor 1,0 = 1. Dados: índice de refração do ar: n 2. massa específica da cortiça: 200 kg/m 3. 1 of :36
 1ª QUESTÃO Valor 1,0 Uma lâmpada é colocada no fundo de um recipiente com líquido, diretamente abaixo do centro de um cubo de cortiça de 10 cm de lado que flutua no líquido. Sabendo que o índice de refração
1ª QUESTÃO Valor 1,0 Uma lâmpada é colocada no fundo de um recipiente com líquido, diretamente abaixo do centro de um cubo de cortiça de 10 cm de lado que flutua no líquido. Sabendo que o índice de refração
Centro Educacional Colúmbia 2000
 Discente: Centro Educacional Colúmbia 2000 Tri. 1º/2017 Dependência Docente: Marcos Vinicius Machado Rio, / / Ens. Médio Turma: 2º ano Disciplina: QUÍMICA Nº 1) O gráfico representa as curvas de solubilidade
Discente: Centro Educacional Colúmbia 2000 Tri. 1º/2017 Dependência Docente: Marcos Vinicius Machado Rio, / / Ens. Médio Turma: 2º ano Disciplina: QUÍMICA Nº 1) O gráfico representa as curvas de solubilidade
EXERCÍCIOS DE ENTROPIA E ENERGIA LIVRE
 QUÍMICA Prof. Jorginho EXERCÍCIOS DE ENTROPIA E ENERGIA LIVRE 1. (Uespi) A sacarose, C 1 H O 11, também conhecida como açúcar de mesa ou açúcar comum comercial, é encontrada na cana de açúcar e na beterraba.
QUÍMICA Prof. Jorginho EXERCÍCIOS DE ENTROPIA E ENERGIA LIVRE 1. (Uespi) A sacarose, C 1 H O 11, também conhecida como açúcar de mesa ou açúcar comum comercial, é encontrada na cana de açúcar e na beterraba.
Lista de Exercícios de Revisão Prova 04
 Lista de Exercícios de Revisão Prova 04 1) (UnB DF) Um bloco de gelo de 40g, a 10ºC, é colocado em um recipiente contendo 120g de água a 25ºC. Qual é a temperatura de equilíbrio do sistema (em ºC)? Calor
Lista de Exercícios de Revisão Prova 04 1) (UnB DF) Um bloco de gelo de 40g, a 10ºC, é colocado em um recipiente contendo 120g de água a 25ºC. Qual é a temperatura de equilíbrio do sistema (em ºC)? Calor
CRONOGRAMA DE RECUPERAÇÃO ATIVIDADE DE RECUPERAÇÃO
 CRONOGRAMA DE RECUPERAÇÃO SÉRIE: 2ª série do EM DISCIPLINA: QUÍMICA 1 Caderno Número(s) da(s) Assuntos aula(s) 06 15, 16 e 17 Misturas de soluções com reação e titulação. 06 18 e 19 Termoquímica 07 28
CRONOGRAMA DE RECUPERAÇÃO SÉRIE: 2ª série do EM DISCIPLINA: QUÍMICA 1 Caderno Número(s) da(s) Assuntos aula(s) 06 15, 16 e 17 Misturas de soluções com reação e titulação. 06 18 e 19 Termoquímica 07 28
DATA: 19/12 /2017 VALOR: 20,0 NOTA:
 DISCIPLINA: CIÊNCIAS PROFESSORA: LUDMILA DATA: 19/12 /2017 VALOR: 20,0 NOTA: TRABALHO DE RECUPERAÇÃO FINAL SÉRIE: 8º ano TURMAS: Anchieta ALUNO (A): Nº: 01. RELAÇÃO DOS CONTEÚDOS CAPÍTULO 2 - Alimentos
DISCIPLINA: CIÊNCIAS PROFESSORA: LUDMILA DATA: 19/12 /2017 VALOR: 20,0 NOTA: TRABALHO DE RECUPERAÇÃO FINAL SÉRIE: 8º ano TURMAS: Anchieta ALUNO (A): Nº: 01. RELAÇÃO DOS CONTEÚDOS CAPÍTULO 2 - Alimentos
COMISSÃO PERMANENTE DE SELEÇÃO COPESE PRÓ-REITORIA DE GRADUAÇÃO PROGRAD PISM III- TRIÊNIO PROVA DE QUÍMICA
 Questão 1: O butano é um gás usado, por exemplo, como combustível em isqueiros, onde, sob pressão, é armazenado como líquido. Na presença de catalisador, o equilíbrio é estabelecido entre os isômeros butano
Questão 1: O butano é um gás usado, por exemplo, como combustível em isqueiros, onde, sob pressão, é armazenado como líquido. Na presença de catalisador, o equilíbrio é estabelecido entre os isômeros butano
1 a QUESTÃO: (2,0 pontos) Avaliador Revisor
 1 a QUESTÃO: (2,0 pontos) Avaliador Revisor Considere a reação exotérmica de formação do trióxido de enxofre, a partir do dióxido: 2SO 2(g) + O 2(g) 2SO 3(g) A 900 K, K p = 40,5 atm -1 e ΔH = -198 kj.
1 a QUESTÃO: (2,0 pontos) Avaliador Revisor Considere a reação exotérmica de formação do trióxido de enxofre, a partir do dióxido: 2SO 2(g) + O 2(g) 2SO 3(g) A 900 K, K p = 40,5 atm -1 e ΔH = -198 kj.
Exercícios de Recuperação
 Ensino Fundamental Nível II Comp. Curricular: Ciências Data: 1º e 2ª Período Aluno(a): Nº Turma: 1-8 Professor: Ana Cristina D Azevedo Visto: Nota: Exercícios de Recuperação Método científico 1. Na maioria
Ensino Fundamental Nível II Comp. Curricular: Ciências Data: 1º e 2ª Período Aluno(a): Nº Turma: 1-8 Professor: Ana Cristina D Azevedo Visto: Nota: Exercícios de Recuperação Método científico 1. Na maioria
Observação Calor x Temperatura
 Prof. Jackson Alves Definição Parte da química que estuda a energia na forma de calor envolvido, seja nos processos químicos ou físicos. Observação Calor x Temperatura Instrumento de medição: Calorímetro
Prof. Jackson Alves Definição Parte da química que estuda a energia na forma de calor envolvido, seja nos processos químicos ou físicos. Observação Calor x Temperatura Instrumento de medição: Calorímetro
SIMULADO 1ª- Fase. Nome: Série: Nº- Nascimento: / / Tel.res/Cel: Escola:
 www.cursoanglo.com.br Treinamento para Olimpíadas de ísica 9 º- a n o E SIMULDO 1ª- ase Nome: Série: Nº- Nascimento: / / Tel.res/Cel: Escola: Quando for o caso use g = 10m/s 2 para o campo gravitacional
www.cursoanglo.com.br Treinamento para Olimpíadas de ísica 9 º- a n o E SIMULDO 1ª- ase Nome: Série: Nº- Nascimento: / / Tel.res/Cel: Escola: Quando for o caso use g = 10m/s 2 para o campo gravitacional
