RICARDO CESAR GONÇALVES POLLERY
|
|
|
- Ângelo Franca Miranda
- 6 Há anos
- Visualizações:
Transcrição
1 UNIVERVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DOUTORADO EM GEOCIÊNCIAS (GEOQUÍMICA) RICARDO CESAR GONÇALVES POLLERY DISPONIBILIDADE E DISTRIBUIÇÃO DOS NUTRIENTES E CLOROFILA-A NAS ÁGUAS ADJACENTES À PENÍNSULA ANTÁRTICA (VERÕES DE 2/1, 21/2 E 22/3) NITERÓI 25
2 RICARDO CESAR GONÇALVES POLLERY DISPONIBILIDADE E DISTRIBUIÇÃO DOS NUTRIENTES E CLOROFILA-A NAS ÁGUAS ADJACENTES À PENÍNSULA ANTÁRTICA (VERÕES DE 2/1, 21/2 E 22/3) Tese apresentada ao Curso de Pós-Graduação em Geociências da Universidade Federal Fluminense, como requisito parcial para obtenção do Grau de Doutor. Área de concentração: Geoquímica Ambiental. Orientador : Prof. Dr. SAMBASIVA RAO PATCHINEELAM Co-orientadora: Profa. Dra. Maria Cordélia S. Machado NITERÓI 25
3
4 À minha amada mãe, que mesmo não estando aqui entre nós, sempre esteve e sempre estará em minha mente e em meu coração.
5 AGRADECIMENTOS Ao Programa Antártico Brasileiro (PROANTAR) pela oportunidade de estudar este ambiente fantástico. À Marinha do Brasil pelo apoio dado pelo Navio de Apoio Oceanográfico Ary Rongel e sua tripulação. À Universidade Santa Úrsula, na pessoa da Chanceler Madre Maria de Fátima Maron Ramos, pelo apoio e infra-estrutura laboratorial. À minha esposa Valéria e aos meus filhos Allan, Clara e Lívia, pela paciência de me esperar das longas viagens e de minhas ausências em prol de meu trabalho. Aos coordenadores do Grupo de Oceanografia de Altas Latitudes (GOAL) Carlos Alberto Eiras Garcia e Maurício da Mata pelo apoio e incentivo. Ao coordenador do sub-projeto no Rio de Janeiro Frederico Kurtz, pelo apoio, incentivo. A todos os estagiários atuais e antigos do Laboratório de Oceanografia Química da Universidade Santa Úrsula, pela ajuda nas análises. A todos os alunos estagiários do laboratório de fitoplâncton da Universidade Santa Úrsula, pelas análises de clorofila. Ao amigo e ex-assistente Rodrigo Kerr, pela grande ajuda nas coletas e análises. Á todos que direta ou indiretamente contribuíram para a realização deste trabalho. Meu especial agradecimento ao Prof. Dr. Sambasiva Rao Patchineelam, meu orientador, pela coragem de me orientar numa tese de doutorado na Antártica. Meu especial agradecimento profa. Dra. Maria Cordélia Machado, minha coorientadora, por ter me apresentado o lugar mais frio, seco e inóspito do mundo, mas também o mais maravilhoso.
6 SUMÁRIO 1 INTRODUÇÃO O PAPEL DA ANTÁRTICA NO CICLO GLOBAL DO CARBONO O PARADOXO ANTÁRTICO CONTROLE DA PRODUTIVIDADE PRIMÁRIA POR NUTRIENTES HETEROGENEIDADE DOS ECOSSISTEMAS ANTÁRTICOS CONTRIBUIÇÃO DESTE TRABALHO O PROGRAMA ANTÁRTICO BRASILEIRO HIPÓTESE OBJETIVOS BASE TEÓRICA NITROGÊNIO FÓSFORO SILÍCIO CLOROFILA-a ÁREAS DE ESTUDO CLIMA ÁREAS DE COLETA Mar de Weddell Mar de Bellingshausen Estreito de Gerlache Estreito de Bransfield MATERIAIS E MÉTODOS... 35
7 4.1 ESTAÇÕES DE COLETA Mar de Weddell Mar de Bellingshausen Estreito de Gerlache Estreito de Bransfield ANÁLISE DE NUTRIENTES Amônio Nitrito Nitrato Fosfato Silicato ANÁLISE DE CLOROFILA-a ANÁLISE DE OXIGÊNIO DISSOLVIDO ANÁLISE DE ph INTERPOLAÇÃO GRÁFICA RESULTADOS MAR DE WEDDELL Transecto A Transecto B MAR DE BELLINGSHAUSEN Estação Estação Estação Estação ESTREITO DE GERLACHE Verão de 21/ Verão de 22/ ESTREITO DE BRANSFIELD Transecto A Transecto B... 93
8 4.4.3 Transecto C Variação espacial na camada de até 5 metros no estreito de Bransfield DISCUSSÃO MAR DE WEDDELL MAR DE BELLINGSHAUSEN ESTREITO DE GERLACHE ESTREITO DE BRANSFIELD CONSIDERAÇÕES FINAIS CONCLUSÃO BIBLIOGRAFIA ANEXOS
9 LISTA DE TABELAS Tabela 1 - Porcentagem das espécies iônicas de fosfato presentes em soluções com diferentes ph, segundo Esteves (1988) Tabela 2 Concentrações médias dos nutrientes, da clorofila-a e da razão N/P em cada profundidade amostrada no transecto A do mar de Weddell Tabela 3 Valores médios da temperatura e salinidade em cada profundidade amostrada no transecto A do mar de Weddell Tabela 4 Concentrações médias dos nutrientes e da clorofila-a em cada profundidade amostrada no transecto B do mar de Weddell Tabela 5 Valores médios da temperatura e salinidade em cada profundidade amostrada no transecto B do mar de Weddell Tabela 6 Concentrações médias dos nutrientes e da clorofila-a em cada profundidade amostrada no mar de Bellingshausen Tabela 7 Valores médios da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no mar de Bellingshausen Tabela 8 Concentrações médias dos nutrientes e da clorofila-a em cada profundidade amostrada no estreito de Gerlache no verão de 21/ Tabela 9 Valores médios da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no estreito de Gerlache no verão de 21/ Tabela 1 Concentrações médias dos nutrientes e da clorofila-a em cada profundidade amostrada no estreito de Gerlache Tabela 11 Valores médios da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no estreito de Gerlache Tabela 12 Concentrações médias dos nutrientes e da clorofila-a em cada profundidade amostrada no estreito de Bransfield no transecto A Tabela 13 Valores médios da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no estreito de Bransfield no transecto A... 93
10 Tabela 14 Concentrações médias dos nutrientes e da clorofila-a em cada profundidade amostrada no estreito de Bransfield no transecto B Tabela 15 Valores médios da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no Estreito de Bransfield no transecto B Tabela 16 Concentrações médias dos nutrientes e da clorofila-a em cada profundidade amostrada no estreito de Bransfield no transecto C Tabela 17 Valores médios da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no estreito de Bransfield no transecto C Tabela 18 Valores de R 2 para regressão linear entre os nutrientes, clorofila-a, temperatura e salinidade (n=271) Tabela 19 - Tabela de comparação entre os dados deste trabalho com os dados de Maturana et al. (1997) e Holm Hansen et al. (1997) Tabela 2 - Comparação entre os dados deste trabalho com os dados de Whitehouse et al. (1995) (valores máximos e mínimos até 2 metros) Tabela 21 Tabela de comparação entre os dados deste trabalho com os dados de Maturana e Silva (1997) nos primeiros 5 metros de profundidade Tabela 22 Comparação dos valores de temperatura, salinidade, concentrações de nutrientes, concentrações de clorofila-a, valores da razão N/P e Si/N deste trabalho com os de outros autores, levando em consideração uma região tropical, dados gerais do oceano sul como área ANBC e águas nas proximidades da ilha Geórgia do Sul
11 LISTA DE FIGURAS Figura 1 - Distribuição de clorofila-a global na face da América do Sul SeaWifs verão (acima); distribuição de clorofila-a na costa oeste da península antártica média do mês de março de 24 (abaixo) Figura 2 - Fórmula plana da molécula de clorofila-a Figura 3 - Localização do Continente Antártico Figura 4 - Localização das regiões de coleta: mar de Weddell, mar de Bellingshausen, estreito de Gerlache e estreito de Bransfield Figura 5 - Mapa de localização das estações do mar de Weddell Figura 6 - Mapa de localização das estações mar de Bellingshausen Figura 7 - Mapa de localização das estações no estreito de Gerlache no verão de Figura 8 - Mapa de localização das estações no estreito de Gerlache no verão de Figura 9 - Mapa de localização das estações no estreito de Bransfield Figura 1 - Distribuição das concentrações de NID (µm) no transecto A no mar de Weddell Figura 11 - Distribuição das concentrações de fosfato (µm) no transecto A no mar de Weddell Figura 12 - Distribuição das concentrações de silicato (µm) no transecto A no mar de Weddell Figura 13 - Distribuição das concentrações de clorofila-a (µg/l) no transecto A no mar de Weddell Figura 14 - Distribuição dos valores da razão N/P no transecto A no mar de Weddell... 5 Figura 15 - Distribuição dos valores da razão Si/N no transecto A no mar de Weddell... 5 Figura 16 - Distribuição da temperatura ( C) no transecto A no mar de Weddell Figura 17 - Distribuição da salinidade (PSU) no transecto A no mar de Weddell Figura 18 - Distribuição das concentrações de NID (µm) no transecto B no mar de Weddell... 55
12 Figura 19 - Distribuição das concentrações de fosfato (µm) no transecto B no mar de Weddell Figura 2 - Distribuição das concentrações de silicato (µm) no transecto B no mar de Weddell Figura 21 - Distribuição das concentrações de clorofila-a (µg/l) no transecto B no mar de Weddell Figura 22 - Distribuição dos valores da razão N/P no transecto B no mar de Weddell Figura 23 - Distribuição dos valores da razão Si/N no transecto B no mar de Weddell Figura 24 - Distribuição da temperatura (ºC) no transecto B no mar de Weddell Figura 25 - Distribuição da salinidade (PSU)no transect B no mar de Weddell Figura 26 - Distribuição das concentrações de NID, fosfato, silicato e clorofila-a na estação 4 no mar de Bellingshausen Figura 27 Distribuição dos valores de temperatura, salinidade, oxigênio dissolvido e ph na estação 4 no mar de Bellingshausen Figura 28 - Distribuição das concentrações de NID, fosfato, silicato e clorofila-a na estação 5 no mar de Bellingshausen Figura 29 Distribuição dos valores de temperatura, salinidade, oxigênio dissolvido e ph na estação 5 no mar de Bellingshausen Figura 3 - Distribuição das concentrações de NID, fosfato, silicato e clorofila-a na estação 6 no mar de Bellingshausen Figura 31 Distribuição dos valores de temperatura, salinidade, oxigênio dissolvido e ph na estação 6 no mar de Bellingshausen Figura 32 Distribuição das concentrações de NID, fosfato, silicato e clorofila-a na estação 7 no mar de Bellingshausen Figura 33 Distribuição dos valores de temperatura, salinidade, oxigênio dissolvido e ph na estação 7 no mar de Bellingshausen Figura 34 Valores da razão N/P nas estações do mar de Bellingshausen Figura 35 Valores da razão Si/N nas estações do mar de Bellingshausen Figura 36 Distribuição das concentrações de NID (µm) no estreito de Gerlache no verão de 21/ Figura 37 Distribuição das concentrações de fosfato (µm) no estreito de Gerlache no verão de 21/ Figura 38 Distribuição das concentrações de silicato (µm) no estreito de Gerlache no verão de 21/ Figura 39 Distribuição das concentrações de clorofila-a (µg/l) no estreito de Gerlache no verão de 21/ Figura 4 Distribuição dos valores das razões N/P no estreito de Gerlache no verão de 21/ Figura 41 Distribuição dos valores das razões Si/N no estreito de Gerlache no verão de 21/
13 Figura 42 Distribuição dos valores de temperatura ( C) no estreito de Gerlache no verão de 21/ Figura 43 Distribuição dos valores de salinidade (PSU) no estreito de Gerlache no verão de 21/ Figura 44 Distribuição das concentrações de oxigênio dissolvido no estreito de Gerlache no verão de 21/ Figura 45 Distribuição dos valores de ph no estreito de Gerlache no verão de 21/ Figura 46 Distribuição das concentrações de NID (µm) no estreito de Gerlache no verão de 22/ Figura 47 - Distribuição das concentrações de fosfato (µm) no estreito de Gerlache no verão de 22/ Figura 48 Distribuição das concentrações de silicato (µm) no estreito de Gerlache no verão de 22/ Figura 49 - Distribuição das concentrações de clorofila-a (µg/l) no estreito de Gerlache no verão de 22/ Figura 5 Distribuição das razões N/P no estreito de Gerlache no verão de 22/ Figura 51 Distribuição das razões Si/N no estreito de Gerlache no verão de 22/ Figura 52 Distribuição dos valores de temperatura ( C) no estreito de Gerlache no verão de 22/ Figura 53 Distribuição dos valores de salinidade (PSU) no estreito de Gerlache no verão de 22/ Figura 54 Distribuição dos valores de ph no estreito de Gerlache no verão de 22/ Figura 55 Distribuição das concentrações de NID (µm) no transecto A do estreito de Bransfield Figura 56 Distribuição das concentrações de fosfato (µm) no transecto A do estreito de Bransfield Figura 57 Distribuição das concentrações de silicato (µm) no transecto A do estreito de Bransfield Figura 58 Distribuição das concentrações de clorofila-a (µg/l) no transecto A do estreito de Bransfield Figura 59 - Distribuição dos valores da razão N/P no transecto A do estreito de Bransfield Figura 6 - Distribuição dos valores da razão Si/N no transecto A do estreito de Bransfield Figura 61 Distribuição das concentrações de temperatura ( C) no transecto A do estreito de Bransfield Figura 62 Distribuição das concentrações de salinidade no transecto A do estreito de Bransfield Figura 63 Distribuição das concentrações de oxigênio (mg/l) dissolvido no transecto A do estreito de Bransfield... 92
14 Figura 64 Distribuição das concentrações de ph no transecto A do estreito de Bransfield Figura 65 Distribuição das concentrações de NID (µm) no transecto B do estreito de Bransfield Figura 66 Distribuição das concentrações de fosfato (µm) no transecto B do estreito de Bransfield Figura 67 Distribuição das concentrações de silicato (µm) no transecto B do estreito de Bransfield Figura 68 Distribuição das concentrações de clorofila-a (µg/l) no transecto B do estreito de Bransfield Figura 69 - Distribuição dos valores da Razão N/P no transecto B do estreito de Bransfield Figura 7 - Distribuição dos valores da Razão Si/N no transecto B do estreito de Bransfield Figura 71 Distribuição das concentrações de temperatura ( C) no transecto B do estreito de Bransfield... Figura 72 Distribuição das concentrações de salinidade no transecto B do estreito de Bransfield... Figura 73 Distribuição das concentrações de oxigênio dissolvido no transecto B do estreito de Bransfield Figura 74 Distribuição dos valores de ph no transecto B do estreito de Bransfield Figura 75 Distribuição das concentrações de NID (µm) no transecto C do estreito de Bransfield Figura 76 Distribuição das concentrações de fosfato (µm) no transecto C do estreito de Bransfield Figura 77 Distribuição das concentrações de silicato (µm) no transecto C do estreito de Bransfield Figura 78 Distribuição das concentrações de clorofila-a (µg/l) no transecto C do estreito de Bransfield Figura 79 - Distribuição dos valores da Razão N/P no transecto B do Estreito de Bransfield Figura 8 - Distribuição dos valores da Razão Si/N no transecto B do Estreito de Bransfield Figura 81 Distribuição das concentrações de temperatura ( C) no transecto C do estreito de Bransfield Figura 82 Distribuição das concentrações de salinidade no transecto C do Estreito de Bransfield Figura 83 Distribuição das concentrações de oxigênio (mg/l) dissolvido no transecto C do estreito de Bransfield Figura 84 Distribuição das concentrações de ph no transecto C do estreito de Bransfield... 11
15 Figura 85 Distribuição das concentrações de NID na superfície no estreito de Bransfield Figura 86 Distribuição das concentrações de fosfato na superfície no estreito de Bransfield Figura 87 Distribuição das concentrações de silicato na superfície no estreito de Bransfield Figura 88 Distribuição das concentrações de clorofila-a na superfície no estreito de Bransfield Figura 89 Distribuição razões N/P na superfície no estreito de Bransfield Figura 9 Distribuição razões Si/N na superfície no estreito de Bransfield Figura 91 Distribuição da temperatura na superfície no estreito de Bransfield Figura 92 Distribuição da salinidade na superfície no estreito de Bransfield Figura 93 Distribuição das concentrações de oxigênio dissolvido na superfície no estreito de Bransfield Figura 94 Distribuição do ph na superfície no estreito de Bransfield Figura 95 Diagrama T-S das águas do mar de Weddell nos transectos A e B e mar de Bellingshausen Figura 96 Diagrama T-S das águas dos estreitos de Gerlache e Bransfield Figura 97 Média e desvio padrão das concentrações de nutrientes e clorofila-a em cada região amostrada em seus respectivos anos de coleta Figura 98 Média e desvio padrão dos valores de temperatura em cada região amostrada em seus respectivos anos de coleta Figura 99 Média e desvio padrão dos valores de salinidade em cada região amostrada em seus respectivos anos de coleta Figura Comparação da distribuição de nitrogênio, fósforo e silício inorgânicos dissolvidos e clorofila-a segundo Maturana e Silva (1997) (à esquerda) com os deste trabalho (à direita) Figura 11 Razão N/P de todas as áreas de coleta Figura 12 Relação entre a razão N/P e a clorofila-a em todas as áreas de coleta Figura 13 Relação entre a razão Si/N e a clorofila-a em todas as áreas de coleta
16 RESUMO O ecossistema Antártico há muito vem sendo caracterizado como uma região de alta concentração de nutrientes e baixas concentrações de clorofila, constituindo o paradoxo antártico. Muitos autores, porém vem mostrando que embora a biomassa fitoplanctônica seja baixa em algumas regiões, em outras esta biomassa pode ser bastante elevada, principalmente se associada a águas pouco profundas, ocasionando uma camada de mistura mais ativa ou ressurgências, sem depleção de nutrientes. Para a realização deste trabalho coletou-se água em profundidades que variaram desde a superfície até 2 metros no mar de Weddell,, no mar de Bellingshausen, no estreito de Gerlache e no estreito de Bransfield nas operações XXI, XX e XXI, verões de 2/1, 21/2 e 22/3 no navio de apoio oceanográfico Ary Rongel. A dinâmica de nutrientes foi bastante diferente nas áreas amostradas, com valores de clorofila-a que não chegaram a serem detectados a valores de bastante elevados de 15x1 µg/l, como no estreito de Gerlache. O nitrogênio inorgânico dissolvido (NID) e o silicato tiveram variações semelhantes e encontram-se com valores elevados, mesmo quando houve consumo acentuados destes nutrientes pela produção primária. Esperava-se que o fosfato tivesse distribuição semelhante ao NID e ao silicato, mas em algumas regiões, as concentrações elevadas de fosfato coincidiam com os valores mais elevados de clorofila-a e em uma única região no mar de Weddell, concentrações muito baixas de fosfato coincidiram com valores muito baixos de clorofila-a, o que nos levou a acreditar num certo controle da produtividade primária pelo fosfato. A diferente distribuição de nutrientes encontradas nas regiões amostradas demonstram existir vários subsistemas, onde as condições variam conforme a profundidade local, proximidade de ilhas ou do continente, regime de ventos, cobertura de gelo, dentre outras variáveis físicas, químicas e biológicas. O projeto deste trabalho atualmente encontra-se inserido no Grupo de Oceanografia de Altas Latitudes (GOAL), pertencente à Rede 1 (Antártica, Mudanças Globais e Teleconexões com o Continente Sul-americano) do Programa Antártico Brasileiro (PROANTAR). O GOAL propõe um plano de coleta e análise sistemática dos componentes físicos, químicos e biológicos do Oceano Austral, no intuito de contribuir na investigação de processos relevantes para a compreensão do impacto das mudanças globais neste ecossistema, além de possíveis conexões com a zona costeira do Brasil. Palavras Chave: Nutrientes Clorofila-a - Antártica
17 ABSTRACT The Antarctic ecosystem has long been characterised as a region with high nutrient concentrations and low Chlorophyll concentration, in what constitutes the antarctic paradox. However, many authors have shown that despite the low concentration of phytoplankton in some regions, this biomass may be high in others, especially if it is associated with lower depth waters causing an water mixture zone or upwelling with no nutrient depletion. To carry out this investigation, water was collected in depths varying from the near surface to 2 metres in the Sea of Weddell, the Sea of Bellinshausen, in the Strait of Gerlache and in the Straight of Bransfield in operations XXI, XX and XXI, Summers of 2/1, 21/2 and 22/3, on the oceanographic vessel Ary Rongel. The nutrient dynamic was quite different in the areas sampled, with Chlorophyll-a values ranging from below detection to high values of 15x1 µg/l, such as in the Straight of Gerlache. Dissolved Inorganic Nitrogen (DIN) and Silicate had similar variations and have high values even when no noticeable consumption of these nutrients by primary production. It was expected that Phosphate would have a similar distribution as that of DIN and Silicate but in some regions, the high Phosphate concentrations coincided with higher values of Chlorophyll-a, and in one specific region of the Sea of Weddell, very low concentrations of Phosphate coincided with very low values of Chlorophyll-a which led us to believe in a certain control of primary productivity by Phosphorus. The different nutrient distribution found in the areas studied show us various subsystems, where conditions vary according to local depth proximity to islands or the continent, wind regime, ice cover, among other physical, chemical and biological variables. The project of this investigation currently is under the Grupo de Oceanografia de Altas Latitudes (GOAL), of Rede 1 (Antártica, Mudanças Globais e Teleconexões com o Continente Sul-americano) of the Brazilian Antarctic Program (PROANTAR). GOAL proposes a systematic sampling and analysis plan of physical, chemical and biological components of the Austral Ocean in order to contribute to relevant processes investigation, to understand the impact of global changes in this ecosystem as well as possible connections with the coastal zone of Brasil. Key words: Nutrients Chlorophill-a Antarctic
18 1 INTRODUÇÃO O Continente Antártico está situado na região polar austral; é formado por uma massa continental, localizada quase inteiramente dentro do círculo polar antártico. É cercado pelo Oceano Antártico, de limites imprecisos, formado pelo encontro das águas dos Oceanos Atlântico, Pacífico e Índico, a chamada confluência antártica. A Antártica constitui quase 1% da área continental do planeta, ou seja, 14.. de Km 2, aproximadamente o tamanho da América do Sul. Cerca de 98% do Continente Antártico está coberto de gelo e de neve durante todo o ano, com uma espessura média de 2. m que, em algumas regiões, pode ultrapassar 4.8 m. 1.1 O PAPEL DA ANTÁRTICA NO CICLO GLOBAL DO CARBONO O estudo do ciclo do carbono global é uma tarefa complexa que deve ser sustentada por modelos (LIU et al., 2). A precisão de qualquer modelo está relacionada à quantidade e qualidade dos dados coletados em campo e o grande desafio é fechar este ciclo, visto que existe uma grande diversidade de fontes e depósitos marinhos. Nos oceanos a produtividade primária tende a reduzir as concentrações de CO 2 gasoso na camada eufótica e convertê-lo a carbono orgânico particulado. O conhecimento da distribuição da produtividade primária, em larga escala, é necessário para o entendimento do papel dos oceanos no ciclo global do carbono. As células do fitoplâncton são responsáveis pela transformação de aproximadamente 5x1 15 gramas de CO 2 em biomassa e representam uma fonte potencial de transferência do CO 2 atmosférico para o oceano (PLATT; SATHYENDRANATH, 1988). No processo de fixação do CO 2, os nutrientes são convertidos em compostos orgânicos, que são o ponto de partida do fluxo do carbono na cadeia trófica (LIBES, 1992). A mudança na concentração dos nutrientes pode causar alterações no crescimento das algas e até modificar a composição dos grupos fitoplanctônicos (PARSONS et al., 1984). Do ponto de vista do ecossistema, o fitoplâncton é a base da cadeia trófica marinha e, portanto, sua ecologia é parte fundamental em estudos relativos a mudanças globais.
19 19 Devido a sua grande extensão, o oceano antártico tem importância capital para o ciclo global do carbono, devido à disponibilidade de nutrientes para a produtividade primária 1.2 O PARADOXO ANTÁRTICO O oceano Antártico é caracterizado por disponibilidade de nutrientes, que deveria sustentar uma alta produtividade primária, e apesar das altas concentrações de nutrientes, a clorofila e a produtividade primária são típicas de um oceano oligotrófico para mesotrófico (HART, 1934; JAQUES, 1989; PIDDLE, 1992; MINAS & MINAS, 1992; TRÉGUER et al., 1995; ANTOINE et al. 1995; FIALA et al., 1998; FIALA et al., 22). Hart (1934) já conhecia o desequilíbrio entre a abundancia de nutrientes e o desenvolvimento do fitoplâncton na águas antárticas. Ele identificou o ferro como um possível elemento limitante, independentemente da complexidade dos sistemas marinhos, mas também enfatizou que a produção do plâncton sempre é governada por muitos fatores independentes.... esta condição indica algum outro controle que o do nitrato e fosfato, mas a natureza deste o controle até o momento não está clara...(hart, 1934). Vários autores, até hoje, tentam provar definitivamente que o ferro é realmente o agente limitante da produtividade na Antártica durante o verão. Numa revisão recente, de Baar e Boyd (1999) sugeriram que o crescimento do fitoplâncton no oceano sul está sujeito a um triplo controle: disponibilidade de luz, cobertura de gelo e ventos, disponibilidade de ferro e pastoreio. Porém o grau com que os fatores físicos, químicos e biológicos podem limitar o crescimento fitoplanctônico ainda não está completamente entendido, e sua importância pode variar conforme a localização, tempo e condições metereológicas locais (LANCELOT et al., 1993). 1.3 CONTROLE DA PRODUTIVIDADE PRIMÁRIA POR NUTRIENTES Os principais fatores que controlam a produtividade primária nos oceanos são: disponibilidade luz, de nutrientes e hidrografia (movimento de massas de água, ressurgência, convecção, correntes e marés) da região. A partir interação destes fatores temos um modelo de distribuição da produtividade primária global (fig. 1) Os principais nutrientes inorgânicos necessários para o desenvolvimento da produtividade primária são: o nitrogênio encontrado na forma de amônio, nitrato e nitrato, o fosfato e o silicato. A carência de nitrogênio e fósforo levaria a limitação de todos os grupos
20 2 fitoplanctônicos, pois estes elementos são utilizados diretamente mo metabolismo das células. Dentre vários compostos que utilizam o nitrogênio podemos destacar as bases nitrogenadas dos ácidos nucléicos e quanto ao fosfato à molécula da adenosina tri-fosfato (ATP). O silicato seria limitante apenas para os grupos fitoplanctônicos que utilizam o silício para formar suas frústulas, como as diatomáceas e os silicoflagelados. Nas águas antárticas raramente se percebe limitação de nutrientes, sendo o principal limitante a luz e possivelmente o ferro, mas estudos baseados em medidas da assimilação de 15 NH + 4 e 15 NO - 3, indicam que mais de 5% de produção primária pode ser atribuída à regeneração microbiana destes nutrientes (SLAWYK, 1979; OLSON, 198; GLIBERT et al., 1982; RONNER et al., 1983; KOIKE et al., 1986), sugerindo que uma grande da produção primária poderia ser sustentada por nutrientes reciclados combinados com o pastoreio do micro e macrozooplancton.
21 Figura 1 - Distribuição de clorofila-a global na face da América do Sul SeaWifs verão (acima); distribuição de clorofila-a na costa oeste da península antártica média do mês de março de 24 (abaixo). 21
22 HETEROGENEIDADE DOS ECOSSISTEMAS ANTÁRTICOS A maior parte das características da Antártica são consideradas anômalas se comparadas ao ambiente das latitudes mais baixas, que são comumente considerados normais (BENNINGHOFF, 1987). O oceano antártico é um mar circunglobal com fortes correntes. Águas do fundo são levadas em direção à superfície através de divergências e ressurgências onde o fitoplâncton floresce, graças aos nutrientes transportados das regiões mais profundas, desta maneira, e o ecossistema marinho é estimulado localmente (EL SAYED, 1985). O gelo que cerca o continente (banquisas de gelo) ao longo do ano aumenta ou diminui sua extensão de acordo com as mudanças sazonais. Estas banquisas podem ser consideradas como uma região de ecótone, anualmente renovando os habitats. No final do inverno, com o reaparecimento da luz solar o desenvolvimento de algas embaixo do gelo favorece o desenvolvimento do plâncton (LAWS, 1985; EL SAYED,, 1985). A Antártica é um mosaico de subsistemas. Esta foi à forma que Zhou et al (22) definiu a variedade de ecossistemas encontrados no entorno deste continente. A Antártica pode ser dividida na parte continental e marítima, devido ao grande número de ilhas encontradas nesta região. Estreitos das mais variadas dimensões, baías e enseadas com a mais variada morfologia e profundidade podem formar verdadeiros viveiros onde a vida fervilha. Ilhas vulcânicas, vulcões continentais ainda ativos e grandes geleiras e grandes áreas de mar aberto também fazem parte da região mais fria e seca do planeta. 1.5 CONTRIBUIÇÃO DESTE TRABALHO Com o encerramento do programa WOCE (World Ocean Circulation Experiment), em 22, a pesquisa oceanográfica de larga escala com aplicações para estudos climáticos estará centrada em programas como o CLIVAR (Climate Variability and Predictability) e o GOOS (Global Ocean Observing System). Pelas características destes programas internacionais, as linhas principais da pesquisa oceanográfica voltar-se-ão para o estudo e monitoramento da variabilidade oceânica, pois esta é fundamental para melhorar a compreensão da importante influência dos oceanos no clima global. Este aspecto é particularmente importante nas altas latitudes, próximas ao continente Antártico, devido à comprovada sensibilidade deste sistema a mudanças climáticas. Como o Brasil vem participando do programa DOVETAIL (Deep Ocean Ventilation Through Antarctic Intermediate Layers), dentro do IanZone/SCOR, através
23 23 do Programa Antártico, os dados gerados neste trabalho aprofundam o conhecimento da distribuição de nutrientes e da clorofila-a em águas adjacentes a península antártica. Este trabalho se insere no projeto da rede 1 no Grupo de Oceanografia de Altas Latitudes, e sub-projeto Estrutura e Dinâmica da Comunidade Planctônica do Ecossistema Antártico, que foi aprovado pelo Programa Antártico Brasileiro (PROANTAR) que é elaborado e implementado pela Comissão Interministerial para os Recursos do mar (CIRM), em consonância com os compromissos internacionais assumidos pelo Brasil no âmbito do Tratado da Antártica. A rede 1 - Antártica, Mudanças Globais, Meio-Ambiente e Teleconexões com o continente Sul-Americano, que propõe caracterizar, monitorar e modelar de maneira integrada as interações da Atmosfera-Criosfera-Geoespaço-Oceano na região polar antártica, procurando inter-relações com o ambiente sul-americano e teleconexões com processos extrapolares que afetam principalmente o meio-ambiente brasileiro. A Rede 1 é formada por três áreas de conhecimento delimitadas pelo objeto de estudo, a saber: 1) Meio espacial e impacto ambiental; 2) Oceanografia de Altas Latitudes; e 3) inter-relação Criosfera-Troposfera. O Grupo de Oceanografia de Altas Latitudes (Goal) pretende contribuir para o entendimento da relação entre o ambiente físico/químico, os microorganismos marinhos, e os predadores de topo da cadeia trófica (mamíferos marinhos). Estes componentes eram estudados separadamente no ambiente antártico dentro do PROANTAR, porém o entendimento dessas relações é crucial para que se possa avaliar o efeito de mudanças ambientais globais sobre cada segmento. No entanto, a dificuldade de acesso ao ambiente marinho no Oceano Austral requer um planejamento especifico e eficiente para se determinar os possíveis efeitos das mudanças globais sobre aquela área. É necessária inicialmente a compreensão da variabilidade oceânica devido a processos naturais/climáticos, para que se possa, posteriormente, isolar os efeitos devidos a mudanças globais. Estes somente podem ser obtidos através de programas plurianuais, de longo prazo, de coleta e análise de dados bióticos e abióticos do meio marinho. Portanto, estudos integrados do ecossistema marinho, visando sua relação com o quadro atual de mudanças globais, são objetivos permanentes do GOAL/Rede 1 ( 1.6 O PROGRAMA ANTÁRTICO BRASILEIRO O Programa Antártico Brasileiro (PROANTAR) é regido por uma parceria entre ministérios e uma agencia de fomento. Efetivamente, participam do PROANTAR os ministérios das Relações Exteriores, da Defesa (Marinha e Aeronáutica), da Ciência e
24 24 Tecnologia, das Minas e Energia, e o Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq). Considerando a importância estratégica da Antártica, em 1959, vários países assinaram o Tratado da Antártida, no qual se firma o compromisso do uso deste continente apenas para fins pacíficos e de cooperação internacional para o desenvolvimento de pesquisas científicas. O Brasil aderiu a este Tratado em Os projetos de pesquisa do PROANTAR são selecionados tendo em vista sua vinculação às questões científicas referentes ao ambiente antártico e competência do pesquisador proponente. As ênfases científicas do programa levam em conta os objetivos e diretrizes emanados da Política Nacional para Assuntos Antárticos (POLANTAR), e os programas e iniciativas científicas apoiados pelo Comitê Científico de Pesquisa Antártica (SCAR), organismo internacional vinculado ao Conselho Internacional para as Ciências (ICSU). Outras informações sobre o Programa Antártico Brasileiro encontram-se nos anexos. 1.7 HIPÓTESE Embora a região antártica seja caracterizada como região de alta concentração de nutrientes e baixa concentração de clorofila (ANBC), as variações temporais, localização, condições metereológicas e hidrológicas, levam a variações na distribuição e concentração dos nutrientes, provocando um maior ou menor (limitação do meio) fornecimento de nutrientes nas camadas iluminadas e conseqüentemente ao controle da produtividade primária. Portanto, a comparação de diferentes áreas (regiões costeiras, estreitos e oceano aberto) ao longo do tempo, poderá mostrar se esta disponibilidade ocorre de uma forma geral ou localizada em regiões específica. 1.8 OBJETIVOS Verificar a variação espacial dos nutrientes nas áreas de estudo e derrota do Napoc Ary Rongel, isto é, mar de Weddell, mar de Bellingshausen, estreito de Gerlache e estreito de Bransfield; Detectar se há limitação do meio por algum nutriente nas águas superficiais (até 2 metros) Relacionar as concentrações de nutrientes com as concentrações de clorofila-a.
25 25 Contribuir com o GOAL, gerando dados para o monitoramento e modelamento de maneira integrada das interações da Atmosfera-Criosfera-Geoespaço-Oceano na região polar antártica.
26 26 2 BASE TEÓRICA 2.1 NITROGÊNIO O nitrogênio mantém uma estreita relação entre a química do meio ambiente e os sistemas biológicos. Na molécula de nitrogênio (N 2 ), a ligação tripla entre os átomos é uma das mais estáveis, necessitando de uma energia de dissociação da ordem de 224,5 Kcal.mol -1 ; assim sendo, apesar de existir em grande quantidade na natureza, o nitrogênio é praticamente inerte, e por isso os sistemas biológicos procuram suprir suas necessidades em outras fontes. Elas são os diferentes compostos nitrogenados, nos quais o nitrogênio pode se apresentar em estados de oxidação que variam de 3 - (no íon NH + 4 e no NH 3 ) a 5 + (no íon NO - 3 ). As concentrações de nitrogênio orgânico e inorgânico, em meio marinho, são controladas por fatores biológicos e sua distribuição fica por conta da morte dos organismos e possíveis fenômenos físicos, tais como: ressurgências, vórtices ciclônicos, camada de mistura na coluna d água e etc. Em ambientes aquáticos, o nitrogênio se apresenta sob várias formas, como por exemplo: N 5+ : NO - 3 (nitrato) N 1+ : N 2 O (óxido nitroso) N 3+ : NO - 2 (nitrito) N : N 2 (nitrogênio molecular) N 3+ : NH + 4 (íon amônio) e NH 3 (amônia) NOD: nitrogênio orgânico dissolvido (peptídeos, purinas, etc.) NOP: nitrogênio orgânico particulado (bactérias, fitoplâncton, zooplâncton, detritos, etc.) Nos ecossistemas aquáticos, os compostos nitrogenados mais importantes, são sem dúvida nenhuma os íons nitrato e amônio, pois representam as principais fontes de nitrogênio para os produtores primários. As bactérias dominam o processo que conduz a transformação dos compostos orgânicos em nitrato, e esse processo é chamado de nitrificação.
27 27 Esse tipo de metabolismo (nitrificação), que utiliza compostos reduzidos como tiossulfato (S 2 O 3 = ), sulfito (SO 3 = ), ferro II (Fe 2+ ), manganês II (Mn 2+ ), além de amônia (NH 3 ), amônio (NH 4 + ) e nitrito (NO 2 - ), é denominado de "quimiolitrofia" (SCHLEGEL, 1976). Na transformação do amônio em nitrato, participam dois gêneros de bactérias: Nitrossomonas: oxidam o íon amônio a nitrito Nitrossomonas 2NH OH - + 3O 2 2NO H 2 O + 2H + ( = -59,4 Kcal.mol -1 ) Nitrobacter: oxidam o íon nitrito a nitrato Nitrobacter NO O 2 2NO 3 - ( = -18 Kcal.mol -1 ) A nitrificação é um processo predominantemente aeróbico e, portanto, deve ocorrer somente em locais contendo oxigênio livre ou disponível (coluna d água ou superfície dos sedimentos). Após a utilização do oxigênio livre, as bactérias começam a utilizar o oxigênio encontrado, no meio aquático, sob a forma de óxido e hidróxido a fim de suprirem suas necessidades alimentares. O nitrogênio molecular (N 2 ) é fixado por algas azuis e verdes, fermentos, e bactérias. O íon nitrato é absorvido, em ambientes marinhos aeróbicos por algas e bactérias, e uma vez dentro das células, é reduzido através de um processo que envolve enzimas, entre elas a nitrato redutase, a formas aminadas, que são então usadas em processos metabólicos. O íon nitrito é encontrado em baixas concentrações, notadamente em ambientes oxigenados. A assimilação do nitrito pelo fitoplâncton só ocorre em períodos de escassez ou falta de amônio e nitrato; quando isto ocorre o nitrito é reduzido a amônio, no interior da célula, pela ação da enzima nitrito redutase (McCARTHY; GOLDMAN, 1979). O íon amônio é muito importante em ambientes aquáticos, principalmente porque sua absorção é energeticamente mais viável, pois não há necessidade da célula gastar energia com a sua redução. A etapa inicial no processo de assimilação do amônio é a sua transformação em ácido glutâmico, segundo a equação a seguir:
28 28 A partir do ácido glutâmico, por transaminação, é possível sintetizar os demais aminoácidos necessários para a construção das proteínas algáceas. O primeiro produto resultante é o íon amônio, e portanto, esse é um processo tipicamente redutor, e é catalisado por um sistema enzimático denominado nitrogenase. Esse processo é endotérmico, e a energia necessária para a sua realização pode ser obtida de dois modos diferentes: através da fotossíntese: nesse caso os elétrons são obtidos a partir da ferrodoxina, que faz parte do sistema de transporte de elétrons da fotossíntese. A energia para o transporte dos elétrons provem do trifosfato de adenosina (ATP). pela respiração: nesse caso a disponibilidade de carboidrato exógenos é fundamental. A ferrodoxina fornece hidrogenase e a respiração o ATP. A fixação do nitrogênio é um processo extremamente sensível ao oxigênio. Os organismos aeróbios, fixadores de nitrogênio, dispõem de mecanismos especiais que protegem o sistema nitrogenase do oxigênio. 2.2 FÓSFORO A importância do fósforo nos sistemas biológicos há muito tempo é conhecida, sendo o mesmo necessário ao desenvolvimento de todos os organismos vivos. Essa importância deve-se ao fato de que ele é um constituinte universal do protoplasma, e também componente essencial do principal fornecedor de energia das células, a molécula de ATP. Os principais elementos formadores das substâncias orgânicas (O, C, N e H) podem ser encontrados ou em sua forma elementar (O 2, N 2, H 2 e C grafite ) ou combinados formando outras substâncias (H 2 O, CO 2, NO - 3, etc.), quer na atmosfera quer dissolvidos na água; entretanto o fósforo tem sua origem na terra, e só pode ser encontrado sob a forma principalmente de fosfatos, que podem ser solúveis ou insolúveis. Já o fósforo elementar não ocorre livre na natureza. Essa origem terrestre pode ser natural ou artificial; a principal fonte natural são as rochas, onde o fósforo está presente sob a forma de apatita [Ca 1 (PO 4 ) 6 (OH,F ou Cl 2 )]. O fosfato é liberado das rochas por intemperização e carreado pelas chuvas para as bacias de drenagem. Ao atingir os sistemas aquáticos ele pode permanecer sob uma forma solúvel ou ser adsorvido pelas argilas. Outras fontes naturais de fosfato são o material particulado existente na atmosfera e o fosfato proveniente da decomposição de organismos de origem alóctone. Geralmente a presença de fósforo na atmosfera, está associada à poluição industrial, onde ele aparece como ácido fosfórico, óxidos de fósforo e compostos orgânicos fosforados.
29 29 Uma boa parte do fosfato que alcança os ecossistemas aquáticos se precipita nos sedimentos, e muitas vezes não mais retorna a coluna d água. Assim sendo a quantidade de fósforo reciclado no ambiente depende das condições físicas e químicas do meio, e da taxa de decomposição da matéria orgânica. As principais formas com que o fósforo se apresenta nos ambientes aquáticos são: fosfato particulado (P-part.) fosfato orgânico dissolvido (POD) fosfato inorgânico dissolvido ou fosfato reativo (PID ou PO 4 -P) A fração mais importante é a do fosfato inorgânico dissolvido (PID), por ser a principal forma de fosfato assimilada pelo fitoplâncton. O PID pode se apresentar sob diversas formas iônicas encontradas na tabela 1. A fração de POD existente em ecossistemas aquáticos é formada principalmente de ésteres fosfatados, fosfolipídios, fosfatases e fosfoproteínas. O principal deles são os ésteres fosfatados que provenientes das células vivas podem ser hidrolisados a fosfatos, e liberados no meio ambiente. Tabela 1 - Porcentagem das espécies iônicas de fosfato presentes em soluções com diferentes ph. ESPÉCIE IÔNICA EM % ph H 3 PO 4 H 2 PO 4 HPO 4 PO 4 4,9 99,2 7x1-1 5, x x x x x x x x1-8,5 99,5 4x1-2 O ciclo do fósforo em ambientes marinhos aparece formando compostos com número de oxidação 5 +. O ciclo não é totalmente fechado, pois ao morrer os organismos vão para o fundo, e liberam compostos fosforados para a água; todavia parte deles sofre uma troca diagenética sendo convertida em fosfato mineral, a apatita. Essa perda de massa é compensada pela entrada no meio marinho, de fosfato de origem terrestre.
30 3 As principais etapas do ciclo do fósforo são: absorção do fosfato iônico e de algumas formas orgânicas (glicerofosfatos e ácido fitônico) pelo fitoplâncton e macrófitas aquáticas; herbivoria, o zooplâncton e pequenos peixes se alimentam do fitoplâncton, seguido da excreção de fezes ricas em fosfato; liberação para a coluna d água, do fosfato contido na biomassa do fitoplâncton, macrófitas aquáticas, zooplâncton, nécton e bentos, após a morte dos mesmos; precipitação de parte desse fósforo, nos sedimentos e liberação pelo sedimento. No caso do fitoplâncton, a liberação do fosfato pode ser um fenômeno muito rápido, pois as fosfatases das próprias células desfosforilam o fosfato particulado para solúvel, que desta maneira é mineralizado pelas bactérias até PID. As bactérias têm um papel fundamental nessa decomposição do fósforo orgânico, e elas podem ser de dois tipos: aeróbicas: aquelas ligadas à decomposição do fitoplâncton; anaeróbicas: aquelas que se localizam nos sedimentos e que têm maior desenvolvimento quando a concentração de oxigênio atinge níveis muito baixos ou nulos. 2.3 SILÍCIO Em sistemas aquáticos o silício é utilizado principalmente para elaborar as frústulas das diatomáceas e dos silicoflagelados. O silicato dissolvido (ou sílica reativa) na água do mar é proveniente principalmente da decomposição dos silicatos, presentes principalmente nas rochas sedimentares. Na água a sílica pode se apresentar sob três formas principais: solúvel: 95% como ácido ortosilícico [Si(OH) 4 ] e 5% sob a forma ionizada de [SiO(OH) 3 ] - em ph em torno de 8; sílica particulada: está incorporada ao fitoplâncton constituindo a chamada sílica biogênica (SiO 2 ), ou nos detritos orgânicos sob a forma de quartzo e minerais silicatados em suspensão; sílica coloidal. A absorção da sílica por diatomáceas ocorre tanto na presença como na ausência de luz, e segundo Steinberg e Melzer (1982) a taxa de absorção na ausência de luz chega mesmo a ser maior que durante o período fotossintético.
31 CLOROFILA-a A clorofila-a está presente nos organismos fotossintetizadores. Têm um peso molecular em torno de 9 e possuem uma molécula tetrapirrólica, com um átomo central de magnésio e dois grupos ésteres (Fig. 2). São lipossolúveis e altamente instáveis. O estudo dos pigmentos fotossintéticos e seus derivados podem fornecer informações importantes sobre a biomassa, taxonomia, produtividade e estado fisiológico do fitoplâncton nos ecossistemas aquáticos (NEVEUX et al. 199). A concentração de clorofila-a é amplamente utilizada para determinar a biomassa total em ecossistemas aquáticos, pois além de ser um pigmento do reino vegetal, sua dosagem não necessita de separação entre o fitoplâncton e do resto do material particulado (NEVEUX, 1976). Figura 2 - Fórmula plana da molécula de clorofila-a. Figura 2 - Fórmula plana da molécula de clorofila-a.
32 32 3 ÁREAS DE ESTUDO O continente Antártico está situado na região polar austral e é formado por uma massa continental localizada quase inteiramente dentro do círculo polar antártico. É cercado pelo Oceano Antártico, formado pelo encontro das águas dos Oceanos Atlântico, Pacífico e Índico, a chamada Confluência Antártica. (Fig. 3) Está localizado quase concentricamente em torno do Pólo Sul, sendo o quinto maior e o mais austral dos continentes. Figura 3 Localização do Continente Antártico. 3.1 CLIMA O clima da Antártida é o mais rigoroso do mundo, devido a uma série de fatores, a saber: a proximidade do pólo sul; a grande elevação, que intensifica o frio polar; a cobertura
33 33 de gelos eternos, com fortes características de reflexão e radiação, que também intensifica o clima polar; o completo isolamento do continente. O clima polar austral ainda sofre pela circulação do ar, que sem obstáculo que sirvam de anteparo, gera ventos violentos (ventos catabáticos), tempestade de neve e freqüentes nevoeiro (blizzards). A região é um centro de altas pressões atmosféricas e irradia correntes de ar frio que atingem todo o hemisfério austral. A Antártica marítima é formada pelas ilhas Sandwich do sul, Orçadas do sul, Shetland do sul e o oeste da península antártica, com as ilhas adjacentes até aproximadamente 7 de latitude sul. O clima marítimo desta região é frio e úmido e as temperaturas raramente estão abaixo de 1 C e uma precipitação de 35 a 5 mm/ano (BENNINGHOFF, 1987) ÁREAS DE COLETA Na costa oeste foram estudadas as áreas do mar de Bellingshausen, do estreito de Gerlache e o estreito de Bransfield e a leste o mar de Weddell (fig. 4) Figura 4 Localização das regiões de coleta: mar de Weddell, mar de Bellingshausen, estreito de Gerlache e estreito de Bransfield Mar de Weddell O mar de Weddell se localiza no setor atlântico das águas antárticas. O limite norte é formado por uma seqüência de feições submersas denominadas, de oeste para leste, como cordilheira Scotia do sul, cordilheira norte de Weddell e cordilheira Sudoeste do Índico. O limite sul é o continente antártico e o oeste da Península antártica (ABSY, 23)
34 Mar de Bellingshausen O mar de Bellingshausen localiza-se a oeste da península antártica, fazendo limite sul com o mar de Ross e limite norte com as águas da passagem de Drake Estreito de Gerlache O estreito de Gerlache está localizado a oeste da península antártica, estende-se de 65 S a 63 4 S a oeste temos o arquipélago Palmer, onde se destacam as ilhas Amberes e Brabante O comprimento total do canal é de 17 Km e representa a parte ocidental da bacia de Brasfield (PRIETO et al., 1998) Estreito de Bransfield O estreito de Bransfield possui uma série de passagens da água profundas entre a Península Antártica e as Ilhas de Shetland do Sul. Para o norte das Shetlands Sul encontra-se a Passagem de Drake. O entorno das ilhas Shetlands do Sul e na franja do norte da Península Antártica temos uma plataforma continental larga. A entrada ocidental para o estreito é parcialmente obstruída por um arquipélago e cumes topográficos rasos (<25 m) (HUNTLEY et al., 1991). O estreito de Bransfield está no fim ocidental da confluência de duas massas da água principais do Oceano Meridional: o mar de Weddell e o mar da Escócia (PATTESSON ; SIERVERS, 198).
35 35 4 MATERIAIS E MÉTODOS As amostras foram coletadas nas campanhas oceanográfica XIX, XX e XXI (anos de 21, 22 e 23 consecutivamente) do PROANTAR, no Navio de Apoio Oceanográfico (NApOc) Ary Rongel. Na campanha XIX foram realizadas as coletas do mar de Weddell, na campanha XX a coleta no mar de Bellingshausen e no estreito de Gerlache no verão 21/2 e na campanha XXI a coleta no estreito de Bransfield e no estreito de Gerlache verão 22/3. Na campanha XIX (mar de Weddell) utilizou-se um CTD da marca Sea-Bird modelo 9plus com rosete de 12 garrafas com capacidade de 5 litros de volume e coletou-se água para análise de clorofila-a e nutrientes, nas profundidades de, 2, 4, 6, 8,, 12, 16 e 2 metros. Na campanha XX, (mar de Bellingshausen e estreito de Gerlache) problemas com o CTD da marca Falmonth, nos obrigou a realizar as coletas com garrafas de Niskin de 1 litros. No mar de Bellingshausen foram coletadas nas profundidades de, 25, 5, 75 e metros e no estreito de Gerlache nas profundidades de, 25, 5, 75, e 15 metros, onde se coletou água para análise oxigênio dissolvido, temperatura, salinidade, clorofila-a, nutrientes e ph. A temperatura, salinidade e ph foram medidos por potenciometria no momento da coleta e o oxigênio dissolvido fixado quimicamente pelo método de Winkler e titulado a bordo. Na campanha XXI (estreito de Bransfield e estreito de Gerlache) utilizou-se o mesmo CTD e rosete da campanha XX e coletou-se água para análise de oxigênio dissolvido, clorofila-a, nutrientes e ph. O ph foi medido por potenciometria no momento da coleta e o oxigênio dissolvido fixado quimicamente pelo método de Winkler e titulado a bordo. As profundidades coletadas foram de, 2, 4, 6, 8,, 15 e 2 metros.
36 ESTAÇÕES DE COLETA Mar de Weddell Em janeiro do ano de 21 no mar de Weddell, foram coletadas amostras em 15 estações separadas por 2 transectos. O transecto A foi composto de 8 estações com coordenadas de latitudes entre 61,8 e 62,65 S e longitudes entre 46,97 e 55, W. O transecto B com 7 estações com coordenadas de latitudes entre 61,52 e 61,92 S e longitudes entre 47,3 e 55, W (fig. 5). Estas estações foram escolhidas em função das estações estipuladas pelo grupo oceanografia física, devido a esta região ser a passagem das águas de fundo, formadas no mar de Weddell, para os outros oceanos do mundo. Figura 5 - Mapa de localização das estações do mar de Weddell Mar de Bellingshausen Em janeiro do ano de 22, foram coletadas no mar de Bellingshausen amostras em 4 estações numeradas de 4 a 7, em latitudes plenas entre 65, e 68, S e longitudes 65,95 e 69,68 W (fig. 6).
37 37 Figura 6 - Mapa de Localização das estações do mar de Bellingshausen Estreito de Gerlache Em janeiro do ano de 22, no estreito de Gerlache foram coletadas amostras em 11 estações e numeradas de 9 a 18 entre as latitudes 63,93 e 64,64 S e longitudes 61,32 e 62,86 W(fig. 7). Figura 7 - Mapa de localização das estações no estreito de Gerlache no verão de Em janeiro do ano de 23 foram coletadas amostras em 8 estações e numeradas de 1 a 8 entre as latitudes 64,17 e 64,98 S e longitudes 61,4 e 63,37 W (fig 8).
38 38 Figura 8 - Mapa de Localização das estações no Estreito de Gerlache no verão de Estreito de Bransfield Em janeiro do ano de 23, no estreito de Bransfield foram coletadas amostras em 17 estações divididas em três transectos. No transecto A, se coletou amostras em seis estações ao longo das Ilhas Shetlands do Sul em direção a Ilha Elefante, entre as coordenadas de latitude 61,6 e 62,71 S e longitude 55,63 e 59,88 W. No transecto B, se coletou amostras em seis estações no canal central entre as coordenadas de latitude 62,12 e 62,99ºS e longitude 55,65 e 59,52 W e no transecto C, se coletou amostras em cinco estações ao longo da Península Antártica em direção a Ilha Joinville entre as coordenadas de latitude 62,63 e 63,29 S e longitude 55,88 e 59,17 W (fig. 9). Figura 9 - Mapa de Localização das estações no Estreito de Bransfield. 4.2 ANÁLISE DE NUTRIENTES As amostras foram coletadas em frascos de polipropileno, foram rinsadas 3 vezes com água da própria amostra e congeladas em um freezer de temperatura abaixo de 2 C até a
39 39 chegada do Navio de apoio Oceanográfico (Napoc) Ary Rongel no Arsenal de Marinha no Rio de Janeiro. No laboratório as amostras foram descongeladas à temperatura ambiente e filtradas em filtros de acetato de celulose para a análise de nutrientes. O nitrato foi a forma de nitrogênio inorgânico encontrada em maior concentração, correspondendo a 9% das formas nitrogenadas, desta forma, foram somadas as concentrações de amônio, nitrito e nitrato, formando o nitrogênio inorgânico dissolvido (NID) Amônio O método descrito mede a totalidade do "nitrogênio amoniacal" (NH 3 -N e NH 4 -N) e é derivado do método de Koroleff (1969) que é simples e oferece uma boa precisão e sensibilidade. Este método é uma aplicação para águas salgadas, da reação de Berthelot, que é a seguinte: 2 C 6 H 5 O NH ClO - O=C 6 H 4 -N=N-C 6 H 5 O H 2 O + 3 HO Cl - Haverá a formação de uma solução azul de "azul de indofenol", cuja absorbância é medida a 63nm em um espectrofotômetro. Usou-se o nitroprussiato de sódio para acelerar a reação (PATTON e CROUCH, 1977). Na determinação do amônio, substituiu-se o hipoclorito pelo trione (ácido dicloroisociânico) como agente oxidante (GRASSOFF e JOHANNSEN, 1972); e a precipitação dos íons alcalino terrosos da água do mar em ph elevado foi evitada pela complexação feita com citrato de sódio (SOLORZANO, 1969). O método é considerado específico para o nitrogênio amoniacal e a interferência provocada pela uréia e pelos aminoácidos é desprezível. O íon sulfeto (S = ) só interfere em concentrações maiores que 2 mg.l -1, e o íon nitrito (NO - 2 ) só em concentrações superiores a algumas dezenas de micromoles por litro. A correção do efeito salino foi realizada segundo a UNEP (1991). No desenvolvimento do método, seguiram-se as recomendações de Aminot e Chaussepied (1983), e a precisão do método é da ordem de ± 5% Nitrito
40 4 O método utilizado está baseado na reação de Griess, e foi aplicado a águas salgadas por Bendschneider e Robinson (1952),sendo um dos mais sensíveis e específicos para a analise de íons nitrito. - Os íons NO 2 formam um diazóico com a sulfanilamida em meio ácido (ph < 2) segundo a equação: NH 2 SO 2 C 6 H 4 -NH 2 + NO H + 2 H 2 O + (NH 2 SO 2 C 6 H 4 -N N) + em seguida o diazóico reage com o N-naftilétilenodiamino para formar o corante. (NH 2 SO 2 C 6 H 4 -N N) + + C 1 H 7 -NH-(CH 2 ) 2 -NH 2 H + + NH 2 SO 2 C 6 H 4 -N=N-C 1 H 6 -NH-(CH 2 ) 2 -NH 2 A absorbância do corante é determinada espectrofotometricamente a 543 nm. A reação é considerada específica para os íons nitrito, mas algumas interferências podem ocorrer, causadas pela presença de aminas aromáticas, cobre (acima de,5 mg.l -1 ) e iodo (acima de,1 mg.l -1 ) (FAO, 1975). Na determinação dos nitritos, seguiu-se o protocolo recomendado por Aminot e Chaussepied (1983), e a precisão do método varia de ± 5% (ao nível de,2 µm) a ± 2,5% (ao nível de 2, µm) Nitrato O método utilizado foi baseado na redução quantitativa (> 95%) dos íons NO a NO 2 e posterior analise destes, conforme descrito no item anterior. O resultado analítico que se obtém, é a soma das concentrações dos íons nitrito e nitrato. Como o nitrito é determinado analisando-se a alíquota sem que a mesma tenha sido reduzida, a concentração de nitrato é então calculada pela fórmula abaixo: [NO - 3 ] = ([NO - 3 ] + [NO - 2 ]) - [NO - 2 ] A redução é efetuada pela passagem da alíquota através de uma coluna de cádmio tratada com cobre (WOOD et al., 1967). O método utilizado sofreu apenas uma pequena modificação em relação ao originalmente descrito: substituição do EDTA pelo NH 4 Cl (GRASSHOFF, 1972). A redução do nitrato pode ser representada pela equação: NO Me (s) + 2 H + NO Me 2+ + H 2 O
41 41 O rendimento da redução do nitrato a nitrito, depende do metal utilizado na coluna redutora, do ph da solução e da atividade na superfície do metal. Reações em soluções fortemente alcalinas, ou em superfícies metálicas inativas, darão apenas reduções parciais; soluções muito ácidas, ou o uso de metais fortemente eletronegativos, ou superfícies metálicas muito ativas, resultarão na redução do nitrato para um nível de oxidação inferior ao do nitrito. Em ambos os casos obteremos valores subestimados para o nitrato. O potencial normal (E ) das duas reações passíveis de ocorrer são semelhantes: NO H e - HNO 2 + H 2 O E =,94 v (1) NO H e - NO + 2 H 2 O E =,97 v (2) Em solução neutra ou alcalina o potencial normal é: NO H 2 O + 2 e - NO HO - E =,15 v (3) Grãos de cádmio revestidos de cobre são ótimos para uma redução heterogênea, mas em meio neutro ou fracamente alcalino os íons cádmio (Cd 2+ ), formados durante a redução do nitrato, reagem com os íons HO - e formam um precipitado. Por outro lado, o potencial de redução necessário para a redução do NO - 3 a NO - 2 depende da atividade do H +, de acordo com a equação de Nernst: E = E - RT/nF ln αno 2 -. αho- αno 3 - (4) Isto implica em trocas no valor do ph se a solução não for tamponada, especialmente nas vizinhanças da superfície metálica. A água salgada capacidade tampão, a qual é reforçada pela adição de NH 4 Cl, que também funciona como agente complexante. 2 NH NH H + (5) Cd NH 3 [Cd(NH 3 ) 2 ] 2+ (6) Podemos observar pelas equações (3) e (5) que as duas hidroxilas formadas (3) são neutralizadas pelos íons H + liberados (5), enquanto a amônia é transformada em um complexo diamínico.
42 42 A duração da redução deve ser controlada, dentro de certos limites, pois neste caso o nitrito existente na solução, passará pela coluna sem sofrer redução. Após a redução dos íons NO - 3 a NO - 2, procede-se a determinação destes últimos como foi descrito no item anterior. O preparo, ativação, uso da coluna, determinação do rendimento em NO - 3 e NO - 2 e cálculo da concentração de NO - 3, foi feito de acordo com as recomendações de AMINOT e CHAUSSEPIED (1983), e a precisão do método varia de ± 3% (ao nível de 2 µm) a ± 5% (ao nível de 1 µm) Fosfato O fósforo é um elemento nutritivo cuja forma mineral majoritária, ortofosfato, é encontrada nas águas salgadas sob duas formas principais: (PO 4 ) 3- e (HPO 4 ) 2- - ; o H 2 PO 4 representa muito pouco em relação aos outros. O método de Murphy e Riley (1962) é ainda hoje um dos mais rápidos e simples para a dosagem dos íons ortofosfato em águas salgadas. O íon fosfato reage com o molibdato de amônio, em presença de Sb 3+ para formar um complexo que se reduz pelo ácido ascórbico; esta forma reduzida, de coloração azul, tem uma absorção máxima em 885 nm. Os polifosfatos e o fósforo orgânico não são dosados por este método. Os íons arseniato reagem de maneira idêntica aos íons fosfato, mas sua concentração é geralmente baixa, o que o torna negligenciável. Além disso, a velocidade da reação é menor para o arseniato do que para o fosfato, e se a medida for feita rapidamente, a interferência é evitada. O ferro, o cobre e os silicatos só interferem quando em altas concentrações, e os sulfetos só em concentrações superiores a 2 mg/l. As partículas em suspensão podem perturbar as medidas, não somente pela turbidez provocada, mas igualmente pelo fato de que os compostos orgânicos e minerais de fósforo adsorvidos à sua superfície são susceptíveis de reagir com o molibdato nas condições da reação, principalmente os fosfatos de cálcio e ferro, e ainda os fosfatos provenientes das células vegetais (STRICKLAND e PARSONS, 1972). O protocolo seguido foi o recomendado por Aminot e Chaussepied (1983) e a precisão do método varia de ± 15% (ao nível de,2 µm) a 3% (para concentrações superiores a 3 µm).
43 Silicato A analise do silício é efetuada pelo método de Mullin e Riley (1955) adaptado por Strickland e Parsons (1972). A dosagem colorimétrica é baseada na formação de um complexo silícico-molíbdico (amarelo) o qual, pela adição de uma mistura redutora de metol (sulfato de p-metilamino fenol) e de sulfito de sódio, é reduzido ao azul de silicomolibdato, cuja absorção máxima é a 81 nm. O ácido ortosilícico tem a tendência de formar polímeros, dos quais só as formas mono e dímeras reagem com o molibdato nas condições da dosagem, daí a expressão "silício reativo" ser a mais apropriada. Nas condições da reação, os silicatos coloidais são também analisados junto com os silicatos dissolvidos (KOROLEFF, 1976). H 2 SO 4 + (NH 4 ) 6 Mo 7 O 24. 4H 2 O + HCl molibdato H 4 SiMo 12 O 4 + C 14 H 2 N 2 O 6.S + Na 2 SO 2 Ac. silicomolibdato reduzido ac. silicomolibdato metol sulfito de sódio Adiciona-se ainda o ácido oxálico ((COOH) 2 2H 2 O)na mistura redutora para conter a interferência do fosfato da amostra na reação de formação do composto colorido e reduzir o excesso de molibdato adicionado. Íons férricos em altas concentrações, interferem deviso à preciptação de compostos avermelhados (molibdato férrico). Essa precipitação pode ser amenizada, quando se acidifica a amostra com seus próprios reagentes, permitindo assism a determinação do silício na presença de 3 mg/l de íons férricos, com 5% de erro. Os sulfetos com concentrações abaixo de 5mg/L não interferem. A salinidade influencia no desenvolvimento da cor. Há uma redução de 1% da absorvância, entre e 35 de salinidade. Esse efeito é proporcional à salinidade. O efeito salino foi corrigido preparando-se um fator de correção com água do mar sintética (BAUMGARTEN et al. 1996) O desenvolvimento do método, foi feito seguindo as recomendações de Aminot e Chaussepied (1983), e a precisão do método deve ficar em torno de 1% para níveis de concentração superiores a 15 µm, e ± 5% para níveis menores que 15 µm de silício. 4.3 ANÁLISE DE CLOROFILA-a Para obtenção da clorofila-a as amostras foram filtradas a bordo 5 ml de água do mar em filtros de microfibras de vidro (GF/F) Whatman de 47 mm de diâmetro, montados
44 44 sobre um sistema de filtração Milipore com capaciade de 3 filtrações simultâneas. A filtração ocorreu sob um vácuo menor que 1 cm Hg, através de uma bomba de vácuo. Após a filtração os filtros foram acondicionados em criotubos e imediatamente colocados num galão criogênico com nitrogênio líquido, permitindo uma excelente conservação até a chegada no laboratório. No laboratório os filtros foram extraídos em 6 ml de acetona a %. Os filtros GF/F retém um volume de água de aproximadamente,6 ml, o que leva a um volume de 6,6 ml de acetona a 9%. Em seguida os filtros são macerados com um bastão de vidro. Para uma extração completa as amostras foram deixadas na geladeira, ao abrigo da luz por um período de 6 a 12 horas. Após este período, as amostras foram centrifugadas por 1 minutos a 35 rotações por minuto. A medida de fluerescência foi realizada por um espectrofluorímetro Perkin-Elmer modelo LS 5B com fotomultiplicador Hamamatsu R928 e calibrado segundo Neveux & Lantoine (1993). 4.4 ANÁLISE DE OXIGÊNIO DISSOLVIDO O método utilizado para a determinação do oxigênio foi o método de Winkler, otimizado por Carpenter (1965) e Carrit e Carpenter (1966). Este método consiste na oxidação do Mn 2+ em meio alcalino, pelo oxigênio dissolvido na amostra de água coletada, e posterior redução desse manganês (Mn 3+ e Mn 4+ ) pelo I -, a Mn 2+. Esta operação é chamada de fixação do oxigênio dissolvido, e é obtida pela adição de MnSO 4 3M e solução alcalina de iodeto de potássio à amostra. As reações que vão ocorrer são as seguintes: Mn HO - Mn(OH) 2 2 Mn(OH) 2 + ½ O 2 2 Mn(OH) 3 Mn(OH) 2 + ½ O 2 MnO(OH) 2 O oxigênio existente na amostra é então fixado sob a forma de precipitados de Mn(OH) 3 e MnO(OH) 2. A segunda etapa do método consiste na dissolução dos precipitados de manganês e posterior redução dos íons Mn 3+ e Mn 4+ para Mn 2+ e liberação de iodo. Isto é conseguido pela adição de H 2 SO 4 1M, e as reações são as seguintes: 2 Mn(OH) I H + 2 Mn H 2 O + I 2 MnO(OH) I H + Mn H 2 O + I 2
45 45 O iodo (I 2 ) em presença de excesso de íon iodeto (I - ) estabelece o equilíbrio abaixo: I 2 + I - I 3 8O iodo liberado, é finalmente dosado pelo tiossulfato de sódio, utilizando-se o amido a 1% como indicador. A reação é a seguinte: 2 S 2 O I 3 S 4 O I - A padronização do tiossulfato de sódio é feita pelo iodato de potássio o qual na presença de iodeto de potássio, em meio ácido, libera iodo segundo a reação abaixo: KIO KI + 3 H 2 SO 4 3 K 2 SO I H 2 O I S 2 O 2-3 S 4 O I - As soluções reagentes, a analise e os cálculos, foram feitos de acordo com o procedimento recomendado por Aminot e Chaussepied (1983), e o valor correto deve se situar a ±,7 mg.l ANÁLISE DE ph A medida do ph foi feita utilizando-se um ph-metro digital Hanna equipado com um eletrodo de vidro e de referência combinados, formando um eletrodo duplo e eletrodo de temperatura para compensação da mesma. 4.6 INTERPOLAÇÃO GRÁFICA Os gráficos de isolíneas foram traçados pelo programa SURFER versão 7., utilizando o método Kriging.
46 46 5 RESULTADOS 5.1 MAR DE WEDDELL Transecto A As concentrações de NID variaram de 5,8 a 29 µm e não apresentaram um padrão nítido de distribuição espacial, embora concentrações menos elevadas sejam detectadas na camada de a 2 metros entre as estações 2A e 8A, bem como, aos e 16 metros entre as estações 1A e 4A (fig. 1). Na figura 11 estão representadas as concentrações de fosfato, que variaram entre,4 a 2,7 µm. O fosfato apresentou concentrações mais elevadas nas camadas de a 2 metros entre as estações 2A e 4A e também entre as estações 6A e 7A na mesma profundidade. Entre as camadas de 4 a 6 metros percebe-se uma faixa longitudinal com concentrações mais baixa (em torno de,6 µm). Abaixo de 6 metros as concentrações não apresentaram padrões de distribuição bem definidos. As concentrações de silicato variaram entre de 26 a 81 µm e estão representados na figura 12. As concentrações mais baixas de silicato foram detectadas nas estações 3A e 4A na camada de a 2 metros e entre as estações 6A e 7A na profundidade de 4 metros. A distribuição é irregular, não demonstrando um padrão nítido. metros A clorofila-a apresentou concentrações que variaram de não detectado (ND) a 2,2 µg/l. Como era de se esperar as concentrações foram mais elevadas nas camadas superiores, onde não há limitação de luz. As concentrações mais elevadas deste transecto encontram-se entre as estações 3A e 4A na camada de a 2 metros e nas proximidades da estação 8A nesta mesma camada, diminuindo com o aumento da profundidade e conseqüente diminuição da luz, mas se detectou valores ate na profundidade de 2 metros (fig. 13).
47 47 Na figura 14 estão representados os valores da razão N/P, que variou entre 5, e 69. Baixos valores desta razão foram detectados entre as estações 2A e 4A até a camada de 2 metros, bem como entre as estações 6A e 7A na mesma camada e entre as estações 1A e 4A nas profundidades entre e 16 metros, tendendo longitudinalmente nestas profundidades a valores próximos a 16. Entre as camadas de 2 a 4 metros os valores da razão N/P tendem a ter valores mais elevados ao longo do transecto. Os valores mais elevados foram detectados nas estações 1A na superfície, próximos a ilha Elefante e na estação 3A na profundidade de 4 metros. Os valores da razão Si/N estão plotados na figura 15 sua variação foi de 1,8 a 8,5. Todos os valores encontrados são superiores a razão de Redfield, que é de 1:1, mas os valores menos elevados destacam-se entre as profundidades de 4 a 6 metros, entre as estações 3A e 7A. As razões mais elevadas foram detectadas entre as estações 1A e 2A nas profundidades de e 16 metros consecutivamente. Tabela 2 Concentrações médias dos nutrientes, da clorofila-a e das razões N/P e Si/N em cada profundidade amostrada no transecto A do mar de Weddell. Prof. metros NID µm Fosfato µm Silicato µm Clorofila-a µg/l Razão N/P Razão Si/N 14 (6,1) 1,3 (,9) 46 (12),7 (,3) 22 (24) 3,5 (1,3) 9,6-25,4-2, ,3 -,9 5, ,9-4, (6,1) 1,2 (,6) 43 (8,2) 1,1 (,6) 22 (19) 3, (1,) 9,2-27,4-1, ,4-2,2 5,5-48 1,9-4, (3,3),8 (,4) 42 (12),7 (,3) 28 (15) 2,3 (,8) 14-23,4-1, ,5-1, ,8-3, (7,7),5 (,1) 46 (8,8),5 (,1) 31 (16) 4,4 (3,5) 5,6-21,4 -, ,5 -, ,2-8,5 8 2 (5,2) 1,7 (,3) 55 (11),3 (,1) 12 (4,5) 2,9 (,7) ,3-2, ,1 -,4 5,2-2 2,1-4,1 15 (5,9) 1,3 (,5) 57 (17),2 (,1) 13 (7,5) 4,3 (1,8) 8,9-29,6-1, ,1 -,3 6,5-29 2,3-7, (5,7) 1 1,3 (,6) 56 (2),1 (,1) 17 (7,7) 3,2 (1,7) 4-27,6-2, ND -,2 6,9-25 2,2-5, (7,2) 1,7 (,7) 54 (8,9),1 (,1) 12 (8,5) 4, (2,3) 7,6-26,8-2, ND -,2 5, ,8-8, (5,6) 1,3 (1,) 57 (1) 26 (21) 3,1 (,8) ND 13-3,4-2, , ,2-4,3 *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação.
48 48 Figura 1 Distribuição das concentrações de NID (µm) no transecto A no mar de Weddell. Estações 1A 2A 3A 4A 5A 6A 7A 8A Longitudes (W) Figura 11 Distribuição das concentrações de fosfato (µm) no transecto A no mar de Weddell. Estações 1A 2A 3A 4A 5A 6A 7A 8A Longitudes (W)
49 49 Figura 12 - Distribuição das concentrações de silicato (µm) no transecto A no mar de Weddell. Estações 1A 2A 3A 4A 5A 6A 7A 8A Longitudes (W) Figura 13 - Distribuição das concentrações de clorofila-a (µg/l) no transecto A no mar de Weddell Estações 1A 2A 3A 4A 5A 6A 7A 8A Longitudes (W)
50 5 Figura 14 - Distribuição dos valores da razão N/P no transecto A no mar de Weddell Estações 1A 2A 3A 4A 5A 6A 7A 8A Longitudes (W) Figura 15 - Distribuição dos valores da razão Si/N no transecto A no mar de Weddell Estações 1A 2A 3A 4A 5A 6A 7A 8A Longitudes (W)
51 51 Na figura 16 são observadas as seções verticais da temperatura, cuja variação foi de - 1,8 a -1,4 ºC. As águas superficiais apresentam-se menos frias, entre as estações 1A e 2A, até a profundidade de 2 metros as temperaturas encontram-se menos baixas. Entre as estações 4A e 8A entre as profundidades de 6 a 14 metros foram detectados os menores valores de temperaturas. A variação da salinidade esteve entre 33,1 e 34,5, como podemos observar na figura 17. As águas superficiais tendem a apresentar valores de salinidade menores. A estação 8A nas proximidades das ilhas Orcadas do Sul, destaca-se com os menores valores deste transecto. Na tabela 3, podemos observar os valores médios da temperatura e salinidade em cada profundidade amostrada no transecto A do mar de Weddell. Tabela 3 Valores médios dos valores da temperatura e salinidade em cada profundidade amostrada no transecto A do mar de Weddell. Profundidade metros Temperatura C Salinidade ,43 (,66) -,39-1,4,31 (,46) -,41-1,1 -,58 (,91) -1,45 -,7 -,95 (1,17) -1,67 -,4-1,3 (,77) -1,74 -,3-1,44 (,68) -1,79 -,2-1,2 (,85) -1,8 -,6-1,39 (,59) -1,71 -,5 33,79 (,36) 33,14-34,16 33,77 (,39) 33,14-34,17 34,1 (,16) 33,76-34,18 34,23 (,5) 34,2-34,29 34,31 (,4) 34,24-34,36 34,34 (,3) 34,28-34,39 34,34 (,4) 34,29-34,38 34,4 (,4) 34,32-34,44 *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação.
52 52 Figura 16 Distribuição dos valores da temperatura ( C) no transecto A no mar de Weddell. Estações 1A 2A 3A 4A 5A 6A 7A 8A Longitudes (W) Figura 17 Distribuição dos valores da salinidade no transecto A no mar de Weddell. Estações 1A 2A 3A 4A 5A 6A 7A 8A Longitudes (W)
53 Transecto B Na figura 18 são apresentados os valores das concentrações de NID, que variaram de 6,4 a 27 µm. Os valores de NID neste transecto não apresentam um padrão nítido de distribuição, valores mais elevados foram detectados pontualmente em estações e profundidades de forma aleatória, como na estação 1B nas profundidades de 8 e 2 metros, na estação 3B aos metros e na estação 6B aos 2metros. As concentrações menos elevadas distribuíram-se da mesma maneira, com os menores valores na estação 1B aos 4 e 12 metros, na estação 4B aos 6 metros e na estação 6B aos 6 metros. Com relação às concentrações de fosfato, estas variaram de,2 a 2,6 µm. Neste transecto as concentrações de fosfato no perfil entre as estações 1B e 3B se distribuíram de forma variada. A estação mais central do transecto (4B) e a estação mais a leste (7B) apresentam concentrações mais elevadas e com perfilagens mais homogenias. Destacam-se as baixas concentrações encontradas nas estações 2B e 3B na profundidade de 8, e 16 metros e as concentrações entre as estações 5B e 6B, entre as profundidades de 2 e 4 metros (fig. 19). As variações nas concentrações de silicato encontram-se entre 16 a 94 µm. A distribuição silicato foi semelhante a do fosfato, nos perfis verticais das estações 1B e 2B houve uma variabilidade maior entre as profundidades amostradas. As estações mais no centro do transecto, entre as estações 3B e 5B, o perfil vertical tende a ser mais homogêneo, onde se destaca o valor da estação 4B na profundidade de 12 metros (fig. 2). As concentrações de clorofila-a variaram de ND a 1,5 µg/l. Como ocorrido no transecto A, neste transecto as concentrações de clorofila-a também foram mais elevadas nas camadas superiores, onde não há limitação de luz. As concentrações mais elevadas foram detectadas na estação 1B, próxima da Ilha Elefante e as menores concentrações foram detectadas entre as estações 4B e 6B nas profundidades de 2 e 4 metros Neste transecto foram detectadas concentrações de clorofila-a até a profundidade de 18 metros nas adjacências da estação 2B até a estação 4B. Na estação 7B se detectou valores ligeiramente maiores entre as profundidades de 4 a 6 metros (fig 21). Os valores da razão N/P encontram-se com uma variação entre 5,1 e 13. Os valores desta razão estão visivelmente relacionados com a distribuição das concentrações de fosfato Onde as concentrações de fosfato foram mais baixas ou mais altas, foram detectados os valores mais elevados e menos elevados da razão N/P, isto é, valores elevados na camada de 6 a metros das estações de 1B a 3B, na superfície das estações 5B e 6B até 4 metros e nas estações 5B e 6B na profundidade de 18 a 2 metros e valores menos elevados na
54 54 profundidade de 6 metros entre as estações 1B e 4B e no perfil entre as estações 4B e 5B, nas profundidades de 6 a 16 metros (fig. 22). Os valores da razão Si/N variaram de 1,8 a 8,5. Os valores mais elevados desta razão foram detectados na estação 4B, na parte central do transecto, tendendo a diminuição em direção as extremidades (fig. 23). Na tabela 4 podemos observar as concentrações médias dos nutrientes e da clorofila-a em cada profundidade amostrada no transecto B do mar de Weddell. Tabela 4 Concentrações médias dos nutrientes, da clorofila-a e das razões N/P e Si/N em cada profundidade amostrada no transecto B do mar de Weddell. Prof. metros NID µm Fosfato µm Silicato µm Clorofila-a µg/l Razão N/P Razão Si/N 16 (3,8) 1, 5 (,8) 41 (15),7 (,2) 22 (28) 2,7 (1,1) 11-21,3-2, ,3 -,9 5,1-79,7-4, 2 17 (4,2) 1,1 (,6) 49 (9,3),5 (,7) 25 (22) 2,9 (,6) 11-23,3-1, ,1-1,5 8,3-57 1,8-3, (4,) 1,1 (,8) 43 (19),5 (,5) 23 (21) 3, (1,) 6,4-17,3-2, >,1-1,4 6,7-51 1,6-4, (4,8) 1,4 (,5) 42 (8,5),5 (,4) 14 (14) 3,2 (,9) 8,7-2,5-1, >,1-1, 2 5,4-44 2,2-4, (5,9) 1,1 (,7) 44 (11),5 (,2) 29 (25) 2,8 (1,2) 1-25,2-2, ,3 -,9 5,1-67 1,7-4,7 18 (4,4) 1,2 (,9) 47 (13),2 (,1) 26 (2) 2,6 (,6) 11-26,2-2, >,1 -,4 7,7-55 1,9-3, (5,4) 1,4 (,7) 54 (25),6 (,1) 15 (13) 3,5 (1,1) 7,5-26,3-2, >,1 -,3 5,2-44 2,3-5, (4,1) 1,1 (,8) 41 (11),1 (,1) 25 (2) 2,8 (1,3) 9,8-21,3-1, >,1 -,3 6,1-55 1,8-5, (6,1) 1,1 (,8) 39 (11),1 (,1) 34 (36) 2,6 (1,5) 9,8-27,2-2, >,1 -,2 5,7-13 1,3-5,6 *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação.
55 55 Figura 18 Distribuição das concentrações de NID (µm) no transecto B no mar de Weddell. Estações 1B 2B 3B 4B 5B 6B 7B Longitude (W) Figura 19 Distribuição das concentrações de fosfato (µm) no transecto B no mar de Weddell. Estações 1B 2B 3B 4B 5B 6B 7B Longitude (W)
56 56 Figura 2 - Distribuição das concentrações de silicato (µm) no transecto B no mar de Weddell. Estações 1B 2B 3B 4B 5B 6B 7B Longitude (W) Figura 21 - Distribuição das concentrações de clorofila-a (µg/l) no transecto B no mar de Weddell. Estações 1B 2B 3B 4B 5B 6B 7B Longitude (W)
57 57 Figura 22 Distribuição dos valores da razão N/P no transecto B no mar de Weddell. Estações 1B 2B 3B 4B 5B 6B 7B Longitude (W) Figura 23 Distribuição dos valores da razão Si/N no transecto B no mar de Weddell. Estações 1B 2B 3B 4B 5B 6B 7B Longitude (W)
58 58 Na figura 24 estão plotados os valores da temperatura, que variaram de -1,3 a 1,6 C. Destaca-se nesta figura a diminuição da temperatura da água superficial em relação à diminuição da longitude. A distribuição destes valores sugere a presença de uma outra massa de água com temperatura menor, entre as estações 2B e 4B. Por motivos técnicos não temos os dados das estações 6B e 7B. A seção vertical dos valores da salinidade corrobora para a hipótese da presença de outra massa de água. A partir dos valores detectados nas águas de profundidade de 2 metros entre as estações 5B e 4B, os valores distribuem-se em forma de cone em direção a superfície (fig. 25). A tabela 5 mostra os valores médios da temperatura e salinidade em cada profundidade amostrada no transecto B do mar de Weddell. Tabela 5 Valores médios da temperatura e salinidade em cada profundidade amostrada no transecto B do mar de Weddell. Profundidade metros Temperatura C Salinidade PSU ,39 (,78) -,37-1,6,38 (,78) -,39-1,6,15 (,5) -,39 -,94 -,12 (,56) -,67 -,8 -,31 (,72) -1,3 -,69 -,32 (,68) -1,3 -,64 -,36 (,68) -1,3 -,57 -,33 (,52) -1, -,41 -,32 (,47) -,97 -,32 34,18 (,14) 34,5-34,37 34,24 (,16) 34,6-34,38 34,27 (,13) 34,13-34,41 34,31 (,8) 34,22-34,41 34,35 (,7) 34,25-34,43 34,37 (,6) 34,26-34,43 34,38 (,7) 34,27-34,44 34,4 (,5) 34,32-34,44 34,43 (,4) 34,4-34,48 *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação.
59 59 Figura 24 Distribuição dos valores da temperatura ( C) no transecto B no mar de Weddell. Estações 1B 2B 3B 4B 5B 6B 7B ? Longitude (W) Figura 25 Distribuição dos valores da salinidade (PSU) no transecto B no mar de Weddell. Estações 1B 2B 3B 4B 5B 6B 7B ? Longitude (W)
60 6 5.2 MAR DE BELLINGSHAUSEN ESTAÇÃO 4 As concentrações de NID variaram de 9,1 a 18 µm. As concentrações foram menos elevadas na superfície, tendendo a um aumento até a profundidade de 5 metros, onde se detecta sua maior concentração, diminui levemente na profundidade de 75 metros e volta a se elevar aos metros (fig. 26). O fosfato variou nesta estação de,32 a 1,4 µm. O perfil do fosfato foi semelhante ao do NID, com concentrações menos elevadas na superfície, tendendo a valores mais elevados até a profundidade de 5 metros, diminuindo levemente aos 75 metros e tornando a aumentar aos metros (fig. 26). O silicato variou de 21 a 43 µm e teve um perfil de distribuição semelhante ao do NID e do fosfato, isto é, concentrações menores na superfície, tendendo a valores mais elevados até a profundidade de 5 metros diminuindo aos 75 metros e tornando a aumentar aos metros (fig. 26). A clorofila-a obteve os valores mais elevados de todas as estações neste ponto. Sua variação foi de 1 a 36 µg/l, tendendo a diminuição com o aumento da profundidade e conseqüente diminuição da luz. Por razões técnicas não temos os valores aos 25 metros (fig. 26). Os valores da temperatura variaram de -,8 a,1 C. A temperatura na superfície e aos 25 metros foram positivas e ligeiramente acima de C, enquanto que abaixo desta profundidade a temperatura tende a diminuir até os metros de profundidade (fig. 27). No perfil vertical da salinidade observamos os valores mais baixos na superfície, aumentando com a profundidade. A salinidade variou de 32,5 a 33,9 (fig. 27). O oxigênio dissolvido variou entre 7,7 e 11 mg/l com valores mais elevados na superfície, diminuindo com a profundidade (fig. 27). O ph variou de 7,6 a 8,2, os valores mais elevados foram detectados na superfície e os valores mais baixos na profundidade de metros (fig. 27).
61 61 Figura 26 Distribuição das concentrações de NID, fosfato, silicato e clorofila-a na estação 4 no mar de Bellingshausen. Estação 4 Concentração NID (um) Fosfato (um) Silicato (um) Clorofila a (ug/l) Figura 27 Distribuição dos valores de temperatura, salinidade, oxigênio dissolvido e ph na estação 4 no mar de Bellingshausen. Estação 4 Concentração/Valores Temperatura ( C) Salinidade (PSU) OD (mg/l) ph
62 Estação 5 As concentrações de NID variaram de 15 a 22 µm. As concentrações foram menos elevadas na superfície, tendendo a aumentar, mas com uma leve diminuição na profundidade de 5 metros (fig. 28). O fosfato variou entre 1,1 e 1,8 µm com concentrações menos elevadas na superfície, aumentando os valores até a profundidade de metros (fig. 29). O silicato variou de 22 a 44 µm, também aumentando os valores até a profundidade de metros (fig. 28). A clorofila-a obteve valores mais elevados na superfície, mas muito inferiores aos encontrados na estação 4. Sua variação foi de,1 a 1,8 µg/l, tendendo a diminuição com o aumento da profundidade e conseqüente diminuição da luz (fig. 28). Nesta estação no perfil vertical da temperatura desta estação, detectaram-se valores positivos da superfície até os 5 metros de profundidade, daí em diante os valores diminuem e ao chegar aos 75 metros encontram-se negativos e assim permaneces até os metros de profundidade. A variação da temperatura foi de -,2 a 1,4 C (fig. 29). A salinidade encontra-se com valores ligeiramente mais elevados que a estação 4, mas com o mesmo tipo de perfil, isto é, valores menores na superfície e elevando com o aumento da profundidade. A salinidade variou de 33,8 a 34,3 (fig. 29). O oxigênio dissolvido também manteve o mesmo tipo de perfil que a estação 4 e variou de 5, a 7,7 mg/l. Os valores detectados a metros de profundidade foram os valores baixos detectados dentre todas as estações desta região (fig. 29). Os valores de ph nesta estação foram baixos, se tratando de água do mar. Sua variação foi de 7, a 7,4, oscilando entre estes valores ao longo do perfil, mas com uma leve tendência de diminuição com o aumento da profundidade (fig. 29).
63 63 Figura 28 Distribuição das concentrações de NID, fosfato, silicato e clorofila-a na estação 5 no mar de Bellingshausen. Estação 5 Concentração NID (um) Fosfato (um) Silicato (um) Clorofila a (ug/l) Figura 29 Distribuição dos valores de temperatura, salinidade, oxigênio dissolvido e ph na estação 5 no mar de Bellingshausen. Estação 5 Concentração/Valores Temperatura ( C) Salinidade (PSU) OD (mg/l) ph
64 Estação 6 As concentrações de NID nesta estação variaram de 17 a 22 µm. As concentrações foram menos elevadas na superfície, aumentando até o final do perfil (fig. 3). O fosfato variou entre 1, e 2,4 µm. Como o NID o fosfato também obteve concentrações menos elevadas na superfície, aumentando os valores até a profundidade de metros (fig. 3). O silicato variou de 28 a 59 µm. Nesta estação detectaram-se os valores mais elevados de todas as estações coletadas no mar de Bellingshausen e seu perfil acompanha o perfil dos outros nutrientes, isto é, concentrações menores na superfície e mais elevadas nas profundidades maiores (fig. 3). A clorofila-a variou de,1 a 3,4 µg/l. Também nesta estação clorofila-a obteve valores mais elevados na superfície, sendo este perfil semelhante ao da estação 5, apenas com valores ligeiramente mais elevados na superfície (fig. 3). Nesta estação a temperatura variou de,1 a 1, C. Surpreendentemente, a temperatura menos baixa foi detectada aos 25 metros de profundidade, ligeiramente acima da temperatura superficial. Dos 25 metros em diante tende a ter temperaturas menores, mas neste perfil não foram detectadas temperaturas negativas (fig. 31). A salinidade obteve um perfil semelhante à estação 5 e seus valores, que variaram de 32,8 a 34,2 (fig. 31). O oxigênio também obteve um perfil semelhante ao da estação 5, mas seus valores na profundidade de metros não foi tão baixo como na estação anterior. A variação do oxigênio dissolvido esteve entre 7,7 e 5,8 mg/l (fig. 31) Nesta estação os valores de ph oscilaram menos que na estação 5 e obtiveram valores mais próximos dos encontrados normalmente na água do mar. Variaram de 7,5 a 7,8 e amplitude dos resultados não foi elevada (fig. 31).
65 65 Figura 3 Distribuição das concentrações de NID, fosfato, silicato e clorofila-a na estação 6 no mar de Bellingshausen. Estação 6 Concentração NID (um) Fosfato (um) Silicato (um) Clorofila a (ug/l) Figura 31 Distribuição dos valores de temperatura, salinidade, oxigênio dissolvido e ph na estação 6 no mar de Bellingshausen. Estação 6 Concentração/Valores Temperatura ( C) Salinidade (PSU) OD (mg/l) ph Estação 7
66 66 As concentrações de NID encontram-se entre 17 a 21 µm. As concentrações aos 25 metros foram menos elevadas que na superfície, mas depois tendem a aumentar até o final do perfil, onde se detecta um a leve diminuição (fig. 32). O fosfato variou entre 1,1 e 3,1 µm. Novamente com concentrações menos elevadas na superfície, aumentando com a profundidade. Os valores detectados aos 75 e metros foram os mais elevados entre as 4 estações analisadas nesta região (fig. 32). O silicato variou de 18 a 45 µm. O perfil do silicato foi semelhante ao perfil do NID, isto é, as concentrações foram menores aos 25 metros que na superfície e depois tendem ao aumento até os metros (fig. 32). A clorofila-a variou de,2 a 2,8 µg/l. Como nas estações anteriores a clorofila-a obteve valores mais elevados na superfície, sendo este perfil semelhante aos das estações 5 e 6. Por razões técnicas não temos os valores aos 25 metros (fig. 32). A temperatura superficial desta estação foi a menos baixa das estações amostradas, mesmo porque os números das estações aumentam em relação à diminuição da latitude, mas mesmo assim as águas abaixo de 5 metros chegam a temperaturas negativas. A variação da temperatura nesta estação foi de -,2 a 1,6 C (fig. 33) A salinidade variou de 1,2 a 2,2 e teve um perfil muito semelhante a da estação 6, tanto na distribuição como nos valores (fig. 33) O oxigênio dissolvido variou de 5,7 a 9, mg/l, nas camadas superiores os valores foram ligeiramente mais elevados que as estações 5 e 6, mas inferiores aos valores da estação 4. A profundidade de metros apresentou um valor baixo, próximo dos valores detectados nesta mesma profundidade nas estações 5 e 6 (fig. 33) Nesta estação os valores de ph também obtiveram valores mais próximos dos encontrados normalmente na água do mar. Variaram de 7,4 a 7,8 e amplitude dos resultados também não foi elevada (fig. 33).
67 67 Figura 32 Distribuição das concentrações de NID, fosfato, silicato e clorofila-a na estação 7 no mar de Bellingshausen. Estação 7 Concentração NID (um) Fosfato (um) Silicato (um) Clorofila a (ug/l) Figura 33 Distribuição dos valores de temperatura, salinidade, oxigênio dissolvido e ph na estação 7 no mar de Bellingshausen. Estação 7 Concentração/Valores Temperatura ( C) Salinidade (PSU) OD (mg/l) ph A razão N/P apresentou valores entre 7, e 28. Somente a estação 4 na superfície obteve um valor acima de 2 e as estações 5 aos 5 metros, 6 aos metros e 7 aos 75 e
68 68 metros obtiveram valores menores que 1, enquanto que nas outras estações os valores estiveram mais próximos à razão de Redfield, isto é, entre 1 e 2 (fig. 34). Figura 34 Valores da razão N/P nas estações do mar de Bellingshausen Razão N/P Estação 4 Estação 5 Estação 6 Estação 7 A razão Si/N variou entre 1,1 e 2,7. Todos os valores foram mais elevados que a razão ideal, que é de 1:1. A estação 7 na superfície e a 25 metros apresentou os valores mais baixos e próximos de 1. Todas as outras estações apresentaram valores mais elevados, destacando-se a estação 4 na superfície e 25 metros e a estação 6 aos metros (fig. 35). Figura 35 Valores da razão Si/N nas estações do mar de Bellingshausen Razão Si/N,,5 1, 1,5 2, 2,5 3, Estação 4 Estação 5 Estação 6 Estação 7
69 69 Na tabela 6 podemos observar as concentrações médias dos nutrientes e da clorofila-a em cada profundidade amostrada mar de Bellingshausen. Tabela 6 Concentrações médias dos nutrientes, clorofila-a e razões N/P e Si/N em cada profundidade amostrada no mar de Bellingshausen. Profundidade metros NID µm Fosfato µm Silicato µm Clorofila-a µg/l Razão N/P Razão Si/N 15 (3,7),9 (,4) 23 (3,5) 11 (16) 19 (6,6) 1,6 (,5) 9,1-17,3-1, , ,2-2, (2,5) 1, (,3) 28 (8,6) 1,6 (,4) 16 (2,9) 1,8 (,7) 13-18,7-1, ,3-1, ,1-2, (1,8) 1,4 (,3) 37 (4,7) 2,9 (2,9) 15 (4,5) 1,9 (,2) , - 1, ,8-7,3 9,3-2 1,7-2, (1,8) 2, (,9) 4 (5,1) 1, (1,) 12 (4,4) 2, (,1) , - 3, ,2-2,4 7, ,8-2,1 21 (1,2) 2,1 (,6) 47 (7,8),3 (,5) 11 (2,8) 2,2 (,3) ,4-2, ,1-1, 7,8-14 2, - 2,7 *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação. Na tabela 7 podemos observar os valores médios da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no mar de Bellingshausen. Tabela 7 Valores médios da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no mar de Bellingshausen. Profundidade metros Temperatura C Salinidade PSU Oxigênio Dissol. mg/l ph,9 (,7) 33,2 (,6) 8,6 (1,8) 7,7 (,5),1-1,6 32,5-33,8 7, , - 8,2 25 1,1 (,1) 33,8 (,1) 7,4 (,2) 7,5 (,2),1-1,2 33, - 33,9 7,3-1 7,4-7,9 5,3 (,5) 33,7 (,2) 7,8 (,8) 7,6 (,2) -,3 -,9 33,4-33,9 7,2-9, 7,4-7,9 75 -,3 (,3) 33,9 (,2) 7,1 (1,) 7,5 (,2) -,5 -,1 33,7-34, 6,5-8,5 7,2-7,7 -,3 (,4) 34,1 (,2) 6,1 (1,2) 7,4 (,2) -,8 -,1 33,9-34,3 5, - 7,7 7,1-7,6 *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação.
70 7 5.3 ESTREITO DE GERLACHE Verão de 21/2 As concentrações de NID variaram entre 6,7 a 27µM. Os valores menos elevados foram detectados entre a estação 8 e a estação 12 na camada de a 25 metros. Entre as estações 12 e 15 há um ligeiro aumento das concentrações em toda perfilagem, tendendo a uma diminuição em direção estação 18 que está mais ao norte, rumo ao estreito de Bransfield (fig. 36). O fosfato teve suas concentrações variando entre,87 a 5,6 µm. As concentrações mais elevadas são detectadas nas águas na camada de 15 metros da estação 8 a estação 14. Estas concentrações mais elevadas tendem a continuar elevadas, afunilando-se com a diminuição da profundidade até aflorar entre as estações 9 e 12. Em direção norte, onde se encontra a estação 18, as concentrações de fosfato tende a diminuírem (fig. 37). As concentrações de silicato variaram de 1 a 45 µm sem demonstrar um padrão nítido de distribuição. As concentrações mais elevadas foram detectadas, principalmente, entre as estações 13 e 17 entre as profundidades de 75 a 15 metros. As concentrações menos elevadas apresentaram-se no perfil das estações 8 a 12, 17 e 18 (fig. 38). As concentrações de clorofila-a variaram de ND a 15x1 µg/l. Esta diferença entre máximos e mínimos surgiu devido aos valores encontrados entre as estações 9 e 12, onde foram detectados altos valores de clorofila-a. Da estação 14 em diante os valores da camada de até 5 metros de profundidade oscilaram entorno de 1 µg/l e nas camadas inferiores a 75 metros entorno de,1 µg/l. Os valores mais elevados de clorofila-a foram detectados na estação 1 na superfície e na estação 11 a 25 metros. (fig. 39). Os valores da razão N/P variaram de 2, a 21. Os valores mais baixos foram detectados entre as estações 9 e 11 até a profundidade de 15 metros. Os valores tendem a serem mais próximos a 16 em direção a estação 18 (fig. 4). Os valores da razão Si/N variaram de,7 a 5,1. Os valores mais elevados foram detectados entre as estações 1 e 11 nas profundidades da superfície e 25 metros consecutivamente. Ao longo do transecto as variações não demonstraram um padrão nítido e o menor valor encontrado foi detectado (menor que 1), foi encontrado na estação 18 aos 75 metros (fig. 41).
71 71 Figura 36 Distribuição das concentrações de NID (µm) no estreito de Gerlache no verão de 21/2 Estações Latitudes (S). Figura 37 Distribuição das concentrações de fosfato (µm) no estreito de Gerlache no verão de 21/2. Estações Latitudes (S)
72 72 Figura 38 Distribuição das concentrações de silicato (µm) no estreito de Gerlache no verão de 21/2. 8 Estações Latitudes (S) Figura 39 Distribuição das concentrações de clorofila-a no estreito de Gerlache no verão de 21/2. Estações Latitudes (S)
73 73 Figura 4 Distribuição dos valores das razões N/P no estreito de Gerlache no verão de 21/2. 8 Estações Latitudes (S) Figura 41 Distribuição dos valores das razões Si/N no estreito de Gerlache no verão de 21/2. 8 Estações Latitudes (S)
74 74 Na tabela 8 podemos observar as concentrações médias dos nutrientes e da clorofila-a em cada profundidade amostrada no estreito de Gerlache no verão de 21/2. Tabela 8 Concentrações médias dos nutrientes e da clorofila-a em cada profundidade amostrada no Estreito de Gerlache no verão de 21/2. Prof. metros NID µm Fosfato µm Silicato µm Clorofila-a µg/l Razão N/P Razão Si/N (5,4) 6, (4,) (3,7) (3,) (4,2) (3,3) , (,8) 1, - 3,3 2,1 (,9),9-4,1 2,5 (1,2) 1,2-5,6 3, (1,3) 1,1-5,4 3,1 (1,2) 1,6-5,4 3,3 (1,1) 1,6-4,8 3 (6,6) (7,4) (6,) (9,8) (9,9) (8,1) (45), (28),3-94 2,4 (3,9),1-13 1, (1,1),1-2,8,3 (,4),1-1,3,1 (,1) ND -,3 1 (5,4) 2, , (3,7) 2,6-15 8,7 (3,4) 3,3-16 7,8 (3,6) 3,4-14 7,7 (3,2) 3,6-15 6,7 (3,2) 3,5-15 *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação. 2,1 (1,1) 1,2-5,1 1,8 (,7) 1,1-3,6 1,4 (,2) 1,1-1,8 1,5 (,4),7-1,9 1,5 (,4) 1, - 2,2 1,6 (,5) 1,1-2,8 No estreito de Gerlache a temperatura da água variou de,6 a 4,4 C. As camadas superiores foram menos frias e as águas da superfície da estação 11 apresentaram o valor mais elevado de todas as estações. O perfil vertical da estação 11, em relação às mesmas profundidades das outras estações, também apresenta os valores mais elevados (fig. 42) A salinidade apresentou um perfil de valores crescentes com o aumento da profundidade e variando entre 33 a 35 PSU. A variação da salinidade na estação 11 variou de forma semelhante e inversa à temperatura, isto é, valores de salinidade menos elevados em todo o perfil vertical, em relação às mesmas profundidades das outras estações (fig. 43). O oxigênio dissolvido também se apresentou com perfil de concentrações descendentes com o aumento de profundidade, os valores variaram de 6 a 16 mg/l. As maiores concentrações foram nas camadas superiores. Os valores de saturação de oxigênio encontram-se em torno da camada de 75 metros, estando com valores de supersaturação nas camadas superiores e ligeiramente abaixo da saturação nas camadas até 15 metros. O valor mais elevado foi detectado na superfície da estação 11. (fig. 44). Os valores de ph situaram-se entre 7, e 8,. Considerando-se que o ph médio da água do mar é em torno de 8,3, os resultados encontrados foram baixos. Os valores de ph mais baixos foram detectados no perfil da estação 11. (fig. 45).
75 75 Figura 42 Distribuição dos valores de temperatura ( C) no estreito de Gerlache no verão de 21/2. Estações Latitudes (S) Figura 43 Distribuição dos valores de salinidade (PSU) no estreito de Gerlache no verão de 21/2. Estações Latitudes (S)
76 76 Figura 44 Distribuição das concentrações de oxigênio dissolvido no Estreito de Gerlache no verão de 21/2. Estações Latitudes (S) Figura 45 Distribuição dos valores de ph no estreito de Gerlache no verão de 21/2. 8 Estações Latitudes (S)
77 77 Na tabela 9 podemos observar os valores médios da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no estreito de Gerlache no verão de 21/2. Tabela 9 Valores médios da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no Estreito de Gerlache no verão de 21/2. Profundidade metros Temperatura C Salinidade PSU Oxigênio Dissol. mg/l ph ,5 (,9) 1,4-4,4 1,7 (,6),6-2,5 1,1 (,3),6-1,7 1, (,3),6-1,6,9 (,3),6-1,6 33,5 (,2) 33,1-33,8 33,7 (,1) 33,5-33,9 34, (,1) 33,8-34,2 34,2 (,1) 34, - 34,4 34,4 (,1) 34,2-34,5 13 (1,5) (,9) ,7 (,7) 8,6-11 8,3 (,7) 7,6-9,5 7,6 (,4) 7, - 8,2 1, (,3) 15 34,5 (,1) 7,2 (,4),6-1,4 34,2-34,6 6,5-8, *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação. 7,7 (,2) 7,3-8, 7,7 (,2) 7,3-7,9 7,6 (,1) 7,4-7,8 7,4 (,2) 7, - 7,6 7,4 (,2) 7, - 7,8 7,4 (,2) 7, - 7,6
78 Verão de 22/3 As concentrações do NID variaram de 19 a 31µM. O menor valor foi detectado na estação 3 a 25 metros e os mais elevados na perfilagem da estação 4 na profundidade de metros. Na estação 5 obtemos uma perfilagem com concentrações menos elevadas, tendendo para valores mais elevados em direção às estações 7 e 8. O NID parece não seguir um padrão nítido de distribuição (fig. 46). A figura 47 apresenta a seção vertical de fosfato, onde a variação de concentração deste nutriente foi de 1,4 a 4,6µM. As menores concentrações foram encontradas entre as estações 2 e 3 até a profundidades de metros. Na estação 4, como na perfilagem de NID detectam-se os valores mais elevados na profundidade de metros. O perfil da estação 8 também apresentou valores elevados. O silicato apresentou uma variação de concentração entre 43 e 82 µm. Como podemos observar na figura 48 as menores concentrações foram obtidas na estação 3 na profundidade de 25 metros e a concentração mais elevada, como no NID e no fosfato, na estação 4 aos metros. Da estação 6 a estação 8 as concentrações de silicato tendem a aumentar ligeiramente. A figura 49 mostra a seção vertical das concentrações de clorofila-a, cuja variação foi desde ND a 1,8 µg/l. A clorofila obteve seus maiores valores nas camadas superficiais entre a superfície e 2 metros, tendendo a diminuição com o aumento da profundidade. Latitudinalmente os valores menos baixos encontram-se entre as regiões das estações 1 e 2 na camada superficial nas estações 7 e 8 na camada de 25 metros. A razão molar N/P neste transecto variou entre 7 e 2. Os valores mais elevados foram detectados na estação 2 entre as profundidades de 5 a metros e com os valores menos elevados na estação 4 na profundidade de metros e na estação 8, aos 25 e 75 metros (fig. 5). A razão Si/N variou de 3,1 a 1,8. A distribuição desta razão foi heterogenia e o valor mais elevado foi detectado na estação 1 aos 75 metros de profundidade e os valores menos elevados estação 1 aos metros e na estação 5 aos 75 metros (fig. 51)
79 79 Figura 46 Distribuição das concentrações de NID (µm) no estreito de Gerlache no verão de 22/3. Estações Latitude (S) Figura 47 - Distribuição das concentrações de fosfato (µm) no estreito de Gerlache no verão de 22/3. Estações Latitude (S)
80 8 Figura 48 Distribuição das concentrações de silicato (µm) no estreito de Gerlache no verão de 22/3. Estações Latitude (S) Figura 49 - Distribuição das concentrações de clorofila-a (µg/l) no estreito de Gerlache no verão de 22/3. Estações Latitude (S)
81 81 Figura 5 Distribuição das razões N/P no estreito de Gerlache no verão de 22/ Estações Latitude (S) Figura 51 Distribuição das razões Si/N no estreito de Gerlache no verão de 22/3. Estações Latitude (S)
82 82 Na tabela 1 podemos observar as concentrações médias dos nutrientes e da clorofilaa em cada profundidade amostrada no estreito de Gerlache no verão de 22/3. Tabela 1 Concentrações médias dos nutrientes e da clorofila-a em cada profundidade amostrada no estreito de Gerlache. no verão de 22/3. Prof. metros NID µm Fosfato µm Silicato µm Clorofila-a µg/l Razão N/P Razão Si/N (1,4) (3,3) (3,4) (3,) (3,2) ,4 (,6) 1,7-3,3 2,5 (,8) 1,6-4,1 2,7 (1,) 1,7-4,9 2,6 (,8) 1,4-3,9 2,9 (1,) 1,5-4,6 58 (6,1) (9,5) (9,7) (8,9) (1) 56-82,7 (,4),1-1,1,8 (,4),5-1,6,5 (,3),2-1,2,2 (,1),1 -,3,1 (,4),1 -,2 1 (2) (2) (3) (4) (3) (2,8) 2,8 (,7) 59 (1) 15 ND 1 (2) , - 4, *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação. 2,4 (,2) 2,1-2,6 2,4 (,2) 2,1-2,7 2,3 (,1) 2,2-2,4 2,4 (,4) 2, - 3,1 2,1 (,2) 1,8-2,4 2,2 (,2) 1,9-2,5 A figura 52 mostra a distribuição da temperatura no estreito de Gerlache no verão de 22/3, onde a variação foi de,3 a 2, C. As camadas superficiais são menos frias, destacando-se os valores na camada de a 25 metros a partir da estação 5 até a estação 8, onde se detectam os valores mais elevados do transecto. Entre as estações 3 e 4 há uma ligeira diminuição de temperatura, possivelmente, por influencia do canal formado pelas ilhas Amberes e Brabante. Na figura 53 a seguir observamos a distribuição dos valores de salinidade, que variaram de 33,4 a 34,4. Os valores menos elevados de salinidade encontram-se nas águas mais superficiais da estação 5 e 7 e os valores mais elevados nas água mais profundas, como na estação 2 e 7 aos 15 metros. Na salinidade também se percebe diferença entre as estações 3 e 4, possivelmente, pelo mesmo motivo citado acima. Os valores de ph podem ser observados na figura 54, onde a sua variação foi de 8, a 8,2 (tabela 11). A variação do ph não foi grande, mas podemos observar em sua seção vertical que na estação 5 os valores tenderam a uma elevação inversamente proporcional à profundidade. Entre as estações 5 e 6 até a profundidade de metros, percebemos as diferenças mais marcantes do transecto.
83 83 Figura 52 Distribuição dos valores de temperatura ( C) no estreito de Gerlache no verão de 22/3. Estações Latitude (S) Figura 53 Distribuição dos valores de salinidade (PSU) no estreito de Gerlache no verão de 22/3. Estações Latitude (S)
84 84 Figura 54 Distribuição dos valores de ph no estreito de Gerlache no verão de 22/ Estações Latitude (S) Na tabela 11 podemos observar os valores médios da temperatura, salinidade e ph em cada profundidade amostrada no estreito de Gerlache no verão de 22/3. Tabela 11 Valores médios da temperatura, salinidade e ph em cada profundidade amostrada no estreito de Gerlache no verão de 22/3. Profundidade metros Temperatura C Salinidade PSU ph 1,4 (,4) 1, - 2, 25 1,2 (,3),8-1,9 5,8 (,2),5-1, 75,5 (,2),3 -,8,4 (,2),2 -,6 33,5 (,1) 33,4-33,7 33,7 (,1) 33,5-33,8 33,9 (,1) 33,7-34,1 34,1 (,1) 33,8-34,2 34,2 (,1) 34, - 34,3 8,2 (,1) 8,2-8,4 8,2 (,1) 8,2-8,4 8,2 (,1) 8,1-8,3 8,2 (,1) 8,1-8,3 8,1 (,1) 8, - 8,3 15,3 (,2) 34,4 (,) 8,1 (,1),1 -,6 34,3-34,4 8, - 8,2 *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação
85 ESTREITO DE BRANSFIELD Transecto A A figura 55 mostra a seção vertical do NID, a variação esteve entre 13 e 32 µm. A diferença entre as concentrações não foi elevada, exceto pela estação 5A a metros, onde se obteve o menor valor. A Estação 4A é a região menos profunda, com cerca de 12 metros e a proximidade do fundo, bem como a abertura da baía do Almirantado e a costa da ilha George do Sul, parece influenciar as concentrações do NID elevando seus valores ainda mais. As concentrações de fosfato variaram de,6 a 5,2µM. As menores concentrações foram detectadas no perfil da estação 2A até a profundidade de metros, localizada próximo à passagem entre as ilhas Nelson e Robert e as concentrações mais elevadas entre as estações 3A e 4A, pelos mesmos motivos descritos para o NID. As estações 5A e 6A tendem a concentrações menos elevadas em direção a região de oceano mais aberto, isto é, mais afastada das ilhas, em direção a Ilha Gibbs, próxima a Ilha Elefante (fig. 56). Na figura 57 observamos as seções verticais do silicato, onde as concentrações variaram de 25 a 64 µm. Concentrações menos elevadas foram detectadas nas estações 2A e 3A na profundidade de 2 metros e na estação 5A na profundidade de metros, esta baixa concentração também foi detectada no perfil NID. Novamente neste transecto aparecem concentrações mais elevadas na estação 4A, onde a profundidade é menor. O perfil vertical de clorofila-a ao longo do transecto A pode ser observado na figura 58, as variações foram de ND a 2,4 µg/l. As concentrações mais elevadas, como era de se esperar estão nas camadas superficiais de até 2 metros. Os valores mais elevados encontramse entre as estações 3A e 5A, localizadas próximas à ilha Rei George, sendo a estação 3A em frente à abertura da baía do Almirantado e a estação 4A, onde se destacam os valores mais elevados do transecto e a menor profundidade, encontra-se na extremidade leste da ilha Rei George, região chamada de Melville. Os valores da razão molar N/P variaram de 5,6 a 4. Os valores mais elevados desta razão encontram-se na estação 2A, desde a superfície até a profundidade de metros. Os menores valores encontram-se distribuídos no perfil da estação 3A. Seguindo o transecto para leste, os valores apresentaram-se próximos da razão de Redfiled (fig. 59). Na figura 6 observamos a seção vertical da razão Si/N, que vaiou de 1,1 a 2,7. Excetuando-se a estação 3A aos 25 metros, os valores não tiveram diferenças importantes, visto que, todos os valores foram superiores a 1 e estes não apresentaram um padrão nítido de distribuição.
86 86 Figura 55 Distribuição das concentrações de NID (µm) no transecto A do estreito de Bransfield Estações 1A 2A 3A 4A 5A 6A Longitude (W) Figura 56 Distribuição das concentrações de fosfato (µm) no transecto A do estreito de Bransfield Estações 1A 2A 3A 4A 5A 6A Longitude (W)
87 87 Figura 57 Distribuição das concentrações de Silicato (µm) no transecto A do estreito de Bransfield Estações 1A 2A 3A 4A 5A 6A Longitude (W) Figura 58 Distribuição das concentrações de clorofila-a (µg/l) no transecto A do estreito de Bransfield Estações 1A 2A 3A 4A 5A 6A Longitude (W)
88 88 Figura 59 - Distribuição dos valores da razão N/P no transecto A do estreito de Bransfield 2 4 Estações 1A 2A 3A 4A 5A 6A Longitude (W) Figura 6 - Distribuição dos valores da razão Si/N no transecto A do estreito de Bransfield 2 4 Estações 1A 2A 3A 4A 5A 6A Longitude (W)
89 89 A tabela 12 mostra os valores médios, desvio padrão, valores mínimos e máximos de NID, fosfato, silicato, clorofila-a e as razões molares N/P e Si/N em cada profundidade amostrada. Tabela 12 Concentrações médias dos nutrientes, da clorofila-a e as razões molares N/P e Si/N em cada profundidade amostrada no Estreito de Bransfield no transecto A. Prof. metros NID µm Fosfato µm Silicato µm Clorofila-a µg/l Razão N/P Razão Si/N (4,2) (4,1) (2,8) (2,3) (3,7) (6,) (4,9) (2,3) , (1,),8-3,3 2, (1,2),7-3,6 2,3 (1,3) 1,1-4, 2,4 (1,2) 1,2-4,3 2,3 (1,6),6-5,1 2,5 (1,5) 1, - 5,2 1,8 (,5) 1,2-2,3 2,2 (,4) 1,6-2,6 54 (4,6) (13) (4,4) (3,) (7,) (14) (3,8) (7,8) 44-64,8 (,3),4-1,1,8 (,8),4-2,4,3 (,1),2 -,5,3 (,3x1-1 ),2 -,3,3 (,2),1 -,6,1 (,4x1-1 ),1 -,2,1 (,3x1-1 ) ND -,1 ND 18 (12) 6, (8,6) 7, (8,7) 6, (7,2) 6, (11) 5, (4,4) 5, (7,6) (3,3) 9,4-17 *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação. 2,1 (,2) 1,7-2,4 1,9 (,5) 1,1-2,5 2, (,2) 1,7-2,2 2,1 (,2) 1,8-2,2 2,1 (,2) 1,8-2,3 2,1 (,2) 1,9-2,4 2,1 (,4) 1,5-2,7 2,1 (,3) 1,8-2,5 Na seção vertical da temperatura ilustrada pela figura 61, esta teve variação entre -,8 e 2, C, as águas mais superficiais apresentam-se com temperaturas menos frias. A estação 3A apresenta um perfil de temperatura com valores menos baixos até 2 metros, possivelmente, esta anomalia ocorre devido à estação estar localizada em frente à abertura da baía do Almirantado. As figuras apresentadas nos anexos mostram as perfilagens do CTD para a temperatura das estações deste transecto. A salinidade variou de 34,1 a 34,5 PSU, como se observa na seção vertical ilustrada na figura 62. As camadas mais superficiais possuem valores de salinidade menores. A estação 3A apresenta valores ligeiramente menores ao longo do perfil vertical, possivelmente, influenciado fluxo de água da baía do Almirantado. Neste transecto o oxigênio dissolvido se apresentou com perfil de concentrações variando de 5,6 a 12mg/L. As concentrações mais elevadas foram detectadas nas camadas superiores, onde os valores encontram-se ligeiramente supersaturados. A baixa profundidade da estação 4A parece não ter interferido nas concentrações do oxigênio dissolvido. Devido a
90 9 problemas logísticos não foi possível coletar amostras para análise de oxigênio dissolvido nas estações 5A e 6A (fig. 63). Os valores de ph encontram-se plotados na figura 64 e variaram entre 7,7e 8,3. A variação mais importante está na profundidade de metros da estação 4A, próximo ao fundo, onde se detectou o valor mais baixo. Neste transecto, também por problemas logísticos, não foi possível coletar amostras para análise do ph nas estações 5A e 6A.
91 91 Figura 61 Distribuição das concentrações de temperatura ( C) no transecto A do estreito de Bransfield Estações 1A 2A 3A 4A 5A 6A Longitude (W) Figura 62 Distribuição das concentrações de salinidade no transecto A do estreito de Bransfield Estações 1A 2A 3A 4A 5A 6A Longitude (W)
92 92 Figura 63 Distribuição das concentrações de oxigênio (mg/l) dissolvido no transecto A do estreito de Bransfield Estações 1A 2A 3A 4A 5A 6A ? Longitude (W) Figura 64 Distribuição das concentrações de ph no transecto A do estreito de Bransfield Estações 1A 2A 3A 4A 5A 6A? Longitude (W)
93 93 A tabela 13 mostra os valores médios, desvio padrão, valores mínimos e máximos de temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada. Tabela 13 Valores médios da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no estreito de Bransfield no transecto A. Profundidade metros Temperatura C Salinidade PSU Oxigênio Dissol. mg/l ph 1,4 (,4),9-2, 2 1,1 (,3),7-1,5 4,7 (,2),5-1, 6,6 (,2),3 -,8 8,4 (,3), -,7,2 (,4) -,3 -,6 15 -,1 (,6) -,8 -,7 -,1 (,6) 2 -,8 -,6 34,2 (,3) 34,1-34,2 34,2 (,2) 34,2-34,2 34,2 (,2) 34,2-34,2 34,3 (,3) 34,2-34,3 34,3 (,4) 34,2-34,3 34,3 (,5) 34,3-34,4 34,4 (,7) 34,3-34,5 12 (,4) (,6) (,6) 9, (,4) 9, (,3) 9,8-1 1 (,4) 9,8-11 9,8 (,6) 9,2-1 34,4 (,8) 7,8 (2,2) 34,3-34,5 5,6-1 *Em cima Média e desvio padrão (entre parênteses); Em baixo Amplitude de variação Transecto B 8,21 (,5) 8,16-8,26 8,16 (,5) 8,1-8,22 8,16 (,2) 8,15-8,18 8,1 (,12) 7,92-8,17 8,7 (,15) 7,85-8,15 8,3 (,2) 7,74-8,15 8,12 (,2) 8,11-8,14 8,9 (,3) 8,7-8,12 Neste transecto a variação do NID oscilou entre 15 e 37 µm, a seção vertical pode ser observada na figura 65. As menores concentrações foram detectadas entre as estações 2B e 3B nas profundidades de 2, 6 e 8 metros. A distribuição de NID neste transecto não parece demonstrar um padrão nítido de distribuição, tanto em relação à profundidade como longitudinalmente. Na figura 66 a seguir estão plotadas concentrações de fosfato, que variaram de,8 a 3,7µM. As concentrações de fosfato variaram muito ao longo deste transecto e nas profundidades. Concentrações mais elevadas foram detectadas nas estações 1B, 2B e 4B e menos elevadas nas estações 3B até a profundidade de metros e na estação 5B até a profundidade de 8 metros. As concentrações de silicato variaram de 38 a 69 µm. Valores menos elevados foram detectados nas estações 2B nas profundidades de 2 e 8 metros, como se observa na figura 67. Neste transecto detectamos uma faixa de concentração mais elevada da estação 4B a 5B entre duas faixas de concentração menos elevadas, que vão da estação 2B a 4B e da 5B a 6B.
94 94 O perfil plotado na figura 68 mostra a distribuição de clorofila-a. Esta variou de,1 a 6,9 µg/l e apresentou-se logitudinalmente de forma homogenia, sem variações importantes e com o perfil vertical típico, isto é, camadas mais profundas limitadas pela luz. Entre as estações 3B e 4B percebemos valores ligeiramente mais elevados na profundidade de 6 metros. Na figura 69 temos a seção vertical da razão N/P, que variou de 6, a 25. Os valores da razão N/P ao longo do transecto indicam valores menores na estação 2B e valores marcadamente mais próximos da razão de Redfield nas estação 5B. Neste transecto a maior parte das estações encontram-se com valores entre 1 e 2. A variação da razão Si/N foi de 1,6 a 3,7. Os valores mais baixos foram detectados entre as estações 1B e 2B nas profundidades de 16 a 2 metros e o valor mais elevado encontra-se na estação 3B a 2 metros de profundidade. Nas outras estações ao longo deste transecto as variações não foram importantes, estando sempre acima de 1, e normalmente oscilando entre 2, e 2.2 (fig. 7).
95 95 Figura 65 Distribuição das concentrações de NID (µm) no transecto B do estreito de Bransfield Estações 1B 2B 3B 4B 5B 6B Longitude (W) Figura 66 Distribuição das concentrações de fosfato (µm) no transecto B do estreito de Bransfield Estações 1B 2B 3B 4B 5B 6B Longitude (W)
96 96 Figura 67 Distribuição das concentrações de silicato (µm) no transecto B do estreito de Bransfield Estações 1B 2B 3B 4B 5B 6B Longitude (W) Figura 68 Distribuição das concentrações de clorofila-a (µg/l) no transecto B do estreito de Bransfield Estações 1B 2B 3B 4B 5B 6B Longitude (W)
97 97 Figura 69 - Distribuição dos valores da Razão N/P no transecto B do estreito de Bransfield Estações 1B 2B 3B 4B 5B 6B Longitude (W) Figura 7 - Distribuição dos valores da Razão Si/N no transecto B do estreito de Bransfield Estações 1B 2B 3B 4B 5B 6B Longitude (W)
98 98 A tabela 14 mostra os valores médios, desvio padrão, valores mínimos e máximos de NID, fosfato, silicato, clorofila-a e as razões molares N/P e Si/N em cada profundidade amostrada. Tabela 14 Concentrações médias dos nutrientes e da clorofila-a e as razões molares N/P e Si/N em cada profundidade amostrada no estreito de Bransfield no transecto B. Prof. metros NID µm Fosfato µm Silicato µm Clorofila-a µg/l Razão N/P Razão Si/N (3,2) (7,2) (1,9) (4,9) (4,8) (3,2) (2,7) (6,3) ,1 (,9),8-3,4 2,1 (,6) 1,3-2,9 2,1 (1,) 1,1-3,7 2,3 (,9) 1,2-3,5 2,1 (,6) 1,6-3,1 2,3 (,7) 1,7-3,1 2,4 (,8) 1,3-3,5 3, (,7) 1,5-3,7 56 (7,6) (9,6) (6,2) (7,3) (7,2) (8,9) (4,7) (4,) 51-61,63 (,19),37 -,95,62 (,11),49 -,77,41 (,13),19 -,56,4 (,16),18 -,57,25 (,13),1 -,47,15 (,1),1 -,31 ND ND 14 (6) 8, (4) 6, (6) 6, (3) 7, (2) (3) 8, (4) 8, (3) 8,8-16 *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação. 2,2 (,27) 1,8-2,5 2,4 (,64) 1,9-3,7 2,2 (,12) 2, - 2,4 2,2 (,26) 1,8-2,5 2,1 (,22) 1,7-2,3 2,1 (,33) 1,8-2,7 2, (,27) 1,6-2,3 1,8 (,4) 1,7-2,6 A temperatura na seção vertical do transecto B apresenta-se com valores menos baixos na superfície até aproximadamente 4 metros, sendo marcante esta diferença nas estações de 1B a 4B. As estações 5B e 6B em direção ao mar de Weddell apresentam temperaturas superficiais menos elevadas e a estação 3B na superfície apresentou o valor mais elevado do transecto. A variação da temperatura foi de -1,1 a 2, C (fig 71). A observação da plotagem dos dados de salinidade na figura 72, que variaram de 34,23 a 34,49 PSU nos mostra que, as camadas superiores possuem valores mais baixos na superfície, aproximadamente até a camada de 4 metros, desde a estação 1B até a estação 4B, daí tendendo a valores ligeiramente mais elevados. Destaca-se valores de salinidade entre as estações 3B e 4B com os menores valores do transecto. O oxigênio dissolvido se apresentou com valores variando entre 9,8 e 12 mg/l, como se observa na figura 73. As maiores concentrações foram detectadas na camada superior a partir da estação 3B até 6B, tendendo para diminuição com o aumento da profundidade. Entre
99 99 as estações 1B e 2B observa-se valores menos elevados formando uma faixa desde as águas mais profundas até a profundidade de 2 metros. Na figura 74 estão plotados os valores de ph, que oscilaram entre 8,1 e 8,24. Os valores mais elevados foram detectados na estação 3B até a profundidade de metros e na estação 4B na profundidade de 4 metros, tendendo a valores mais baixos nas camadas mais profundas. Na estação 1B da profundidade de 8 a 2 metros, na estacai 2B na profundidade de 15 a 2 metros e na estação 5B aos 2 metros detectou-se os menores valores de ph.
100 Figura 71 Distribuição das concentrações de temperatura ( C) no transecto B do estreito de Bransfield Estações 1B 2B 3B 4B 5B 6B Longitude (W) Figura 72 Distribuição das concentrações de salinidade (PSU) no transecto B do estreito de Bransfield Estações 1B 2B 3B 4B 5B 6B Longitude (W)
101 11 Figura 73 Distribuição das concentrações de oxigênio dissolvido (mg/l) no transecto B do estreito de Bransfield Estações 1B 2B 3B 4B 5B 6B Longitude (W) Figura 74 Distribuição dos valores de ph no transecto B do estreito de Bransfield. Estações 1B 2B 3B 4B 5B 6B Longitude (W)
102 12 A tabela 15 mostra os valores médios, desvio padrão, valores mínimos e máximos de temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada. Tabela 15 Valores médios da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no estreito de Bransfield no transecto B. Profundidade metros Temperatura C Salinidade PSU Oxigênio Dissol. mg/l ph 1,5 (,7),1-2, 2 1,2 (,9) -,2-2, 4,5 (,8) -,3-1,5 6 -,1 (,4) -,5 -,7 8 -,5 (,2) -,7 - -,1 -,7 (,1) -,9 - -,6 15 -,8 (,1) -,9 - -,7 34,26 (,3) 34,23-34,31 34,27 (,3) 34,24-34,32 34,3 (,4) 34,26-34,35 34,34 (,3) 34,29-34,37 34,37 (,2) 34,34-34,39 34,39 (,2) 34,36-34,41 34,44 (,2) 34,4-34,47 11 (,5) (,5) (,6) (,5) (,6) (,6) (,5) 9, ,9 (,2) 34,47 (,2) 1 (,4) -1,1 - -,6 34,43-34, *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação. 8,18 (,4) 8,13-8,24 8,19 (,4) 8,15-8,24 8,19 (,4) 8,13-8,23 8,18 (,4) 8,13-8,23 8,17 (,4) 8,12-8,23 8,16 (,3) 8,12-8,21 8,13 (,2) 8,11-8,15 8,12 (,2) 8,1-8,14
103 Transecto C Na figura 75 as concentrações de NID no transecto C variaram entre 14 e 34µM. As concentrações foram ligeiramente menores no perfil da estação 2C até a profundidade de 6 metros e no perfil da estação 5C nas profundidades de 8 a metros. Nas profundidades abaixo de 8 metros até a estação 3C as concentrações foram mais elevadas, tendendo a valores menores mantendo estas profundidades, mas em direção a estação 5C. A seção vertical de fosfato neste transecto variou de,6 a 4,3µM. O transecto inicia o perfil com concentrações mais elevadas na estação 1C diminuindo as concentrações p na estação 2C, elevando os valores na estação 4C e tendendo para valores menos elevados na estação 5C. Os valores menos elevados são detectados no perfil da estação 2C nas profundidade de 4 a 6 metros e aos 15 metros e os valores mais elevados são detectados na estação 4C entre a superfície e 12 metros (fig. 76) As concentrações de silicato variaram de 33 a 63µM. Na figura 77 observam-se os valores menos elevados nas águas superficiais e aos 4 metros da estação 2C, na profundidade de 4 metros da estação 3C e na estação 5C na profundidade de 8 metros. As concentrações de silicato apresentam valores mais elevados nas águas abaixo de 8 metros, principalmente nas estações 2C e 3C. Na figura 78 observa-se a seção vertical de clorofila-a, onde, de forma geral, foram detectados os menores valores de todo o estreito, variando de ND a,4 µg/l. Os valores de clorofila-a foram bastante homogêneos ao longo do transecto, sem apresentar variações importantes, além da variação normal com a profundidade. Entre as estações 3C e 4C detectou-se uma ligeira diminuição dos valores entre as profundidades de 8 e 4 metros, bem como na camada mais superficial. A razão molar N/P deste transecto está plotada na figura 79. A variação esteve entre 5,7 e 38. Os valores mostram-se bem marcados, com os mais elevados em todo o perfil da estação 2C, principalmente nas profundidade de 4, 6 e 15 metros, tendendo a diminuição em direção a estação 4C, onde os menores valores foram encontrados desde a profundidade de 2 até metros de profundidade. A variação da Razão Si/N foi de 1,6 a 2,7. Com exceção da camada de 4 a 8 metros de profundidade entre as estações 3C e 4C, o perfil vertical da razão Si/N neste transecto mostra uma tendência a diminuição de seus valores desde a estação 1C até a estação 5C. Todos os valores detectados fora superiores a 1 (fig. 8).
104 14 Figura 75 Distribuição das concentrações de NID (µm) no transecto C do estreito de Bransfield Estações 1C 2C 3C 4C 5C Longitude (W) Figura 76 Distribuição das concentrações de fosfato (µm) no transecto C do estreito de Bransfield Estações 1C 2C 3C 4C 5C Longitude (W)
105 15 Figura 77 Distribuição das concentrações de silicato (µm) no transecto C do estreito de Bransfield Estações 1C 2C 3C 4C 5C Longitude (W) Figura 78 Distribuição das concentrações de clorofila-a (µg/l) no transecto C do estreito de Bransfield Estações 1C 2C 3C 4C 5C Longitude (W)
106 16 Figura 79 - Distribuição dos valores da Razão N/P no transecto B do Estreito de Bransfield Estações 1C 2C 3C 4C 5C Longitude (W) Figura 8 - Distribuição dos valores da Razão Si/N no transecto B do Estreito de Bransfield Estações 1C 2C 3C 4C 5C Longitude (W)
107 17 A tabela 16 mostra os valores médios, desvio padrão, valores mínimos e máximos de NID, fosfato, silicato, clorofila-a e as razões molares N/P e Si/N em cada profundidade amostrada. Tabela 16 Concentrações médias dos nutrientes e da clorofila-a e as razões molares N/P e Si/N em cada profundidade amostrada no estreito de Bransfield no transecto C. Prof. metros NID µm Fosfato µm Silicato µm Clorofila-a µg/l Razão N/P Razão Si/N (4,5) (6,2) (3,1) (3,6) (6,5) (5,4) (4,) (3,8) ,4 (1,),9-3,7 2,3 (1,2) 1,1-4,1 2,4 (1,3),6-4,3 2,5 (1,3),6-4,3 2,3 (1,) 1,4-3,7 2,5 (1,2) 1,2-4,2 2,1 (,8),8-2,8 1,7 (,7) 1,2-2,8 45 (11) (7,2) (6,4) (1,1) (14) (9,3) (5,5) (5,6) 49-61,32 (,6x1-1 ),24 -,4,28 (,4 x1-1 ),25 -,35,23 (,3 x1-1 ),2 -,26,22 (,5 x1-1 ),16 -,29,21 (,2 x1-1 ),19 -,23,17 (,2 x1-1 ),14 -,19,1 (,2 x1-1 ) ND -,11 ND 11 (4,7) 7, (4,8) 6, (11) 6, (12) 7, (6,8) 5, (6,9) 5, (12) 9, (7,5) 7,8-25 *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação. 2, (,24) 1,7-2,3 2,1 (,27) 1,7-2,4 2, (,9) 1,9-2,1 1,9 (,24) 1,7-2,2 2,2 (,14) 2, - 2,3 2,2 (,2) 1,9-2,5 2,1 (,33) 1,8-2,7 2, (,19) 1,8-2,3 Na figura 81 estão plotados os dados de temperatura deste transecto, onde as águas superficiais são ligeiramente menos frias, e os valores oscilam entre,4 e -,9 C. O valor menos baixo foi detectado na superfície da estação 5C e os mais baixos na profundidade de 2 metros, principalmente, entre as estações 4C e 5C. Destaca-se nesta figura a distribuição dos valores de temperatura entre as estações 3C e 4C, sugerindo uma possível intrusão de uma massa d água mais fria. Os valores de salinidade variaram de 34,27 a 35, 45. Os valores extremos foram detectados nas mesmas estações que os extremos da temperatura. A plotagem dos dados corrobora com a hipótese de estar havendo uma intrusão de outra massa d água entre as estações 3C e 4C (fig. 82). As concentrações de oxigênio dissolvido variaram entre 8,7 e 11 mg/l, o transecto apresenta-se com pequenas variações nas concentrações, exceto pela faixa entre a profundidade de 2 metros compreendida entre as estações 2C e 3C. Por problemas logísticos não foi possível coletar amostras para análise de oxigênio dissolvido na estação 5C (fig. 83).
108 18 A seção vertical na figura 84 mostra a variação de ph, que oscilou entre 8,9 e 8,23. Nas estações 1C e 2C até a profundidade de 8 metros, detectou-se os valores ligeiramente mais elevados. Os valores de ph tendem a diminuir nas águas abaixo de 8 metros e no perfil das estações 3C e 4C. Por problemas logísticos, também não foi possível coletar amostras para análise de ph na estação 5C.
109 19 Figura 81 Distribuição das concentrações de temperatura ( C) no transecto C do estreito de Bransfield Estações 1C 2C 3C 4C 5C Longitude (W) Figura 82 Distribuição das concentrações de salinidade (PSU) no transecto C do Estreito de Bransfield Estações 1C 2C 3C 4C 5C Longitude (W)
110 11 Figura 83 Distribuição das concentrações de oxigênio (mg/l) dissolvido no transecto C do estreito de Bransfield Estações 1C 2C 3C 4C 5C ? Longitude (W) Figura 84 Distribuição das concentrações de ph no transecto C do Estreito de Bransfield. Estações 1C 2C 3C 4C 5C ? Longitude (W)
111 111 A tabela 17 mostra os valores médios, desvio padrão, valores mínimos e máximos de da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no estreito de Bransfield no transecto C. Tabela 17 Valores médios da temperatura, salinidade, oxigênio dissolvido e ph em cada profundidade amostrada no estreito de Bransfield no transecto C. Profundidade metros Temperatura C Salinidade PSU Oxigênio Dissol. mg/l ph,4 (,7) -,4-1,3 2 -,1 (,4) -,6 -,4 4 -,2 (,4) -,7 -,2 6 -,4 (,3) -,7 - -,1 8 -,5 (,2) -,8 - -,2 -,6 (,1) -,8 - -,4 15 -,8 (,1) -,9 - -,7 34,34 (,5) 34,27-34,41 34,37 (,4) 34,31-34,41 34,38 (,4) 34,33-34,42 34,39 (,3) 34,34-34,42 34,4 (,3) 34,35-34,42 34,41 (,2) 34,39-34,43 34,42 (,1) 34,42-34,43 11,1 (,5) 1,6-11,7 1,1 (1,3) 8,7-11,7 1,9 (,3) 1,6-11,3 1,9 (,2) 1,6-11,2 1,8 (,1) 1,7-11, 1,7 (,4) 1,3-11,2 1,5 (,4) 9,9-1,8 2 -,8 (,1) 34,43 (,1) 1,4 (,3) -,9 - -,7 34,42-34,45 1,2-1,8 *Em cima Média e desvio padrão (entre parênteses); Embaixo Amplitude de variação. 8,15 (,5) 8,9-8,21 8,17 (,6) 8,12-8,23 8,16 (,4) 8,11-8,21 8,16 (,3) 8,12-8,18 8,13 (,3) 8,1-8,16 8,12 (,5) 8,6-8,16 8,13 (,2) 8,11-8,16 8,8 (,5) 8,4-8, VARIAÇÃO ESPACIAL NA CAMADA DE ATÉ 5 METROS NO ESTREITO DE BRANSFIELD Nas figuras abaixo foram representadas as distribuições dos nutrientes, clorofila-a, temperatura, salinidade, oxigênio dissolvido e ph na camada superficial (até 5 metros de profundidade). A variação superficial do NID está demonstrada na figura 85. As concentrações mais elevadas foram detectadas na estação 2A, nas proximidades da ilha Nelson e na estação 4B no canal central do estreito. As concentrações menos elevadas foram detectadas na estação 2C, próximo a península Antártica; na estação 3A, próximo a abertura da baía do Almirantado e na estação 5C mais próxima à região do mar de Weddell.
112 112 Figura 85 Distribuição das concentrações de NID na superfície no estreito de Bransfield Na distribuição superficial do fosfato na figura 86 abaixo podemos destacar as concentrações mais elevadas entre as estações 3A e 4A, próximas à ilha Rei George e entre as estações 3C e 4C. As concentrações menos elevadas encontram-se na estação 2A, próximo a ilha Nelson e entre as estações 2C e 3C, próximo à península Antártica. Figura 86 Distribuição das concentrações de fosfato na superfície no estreito de Bransfield Na figura 87 se encontra a distribuição de silicato, onde as concentrações mais elevadas encontram-se na parte mais a oeste do estreito (estações 1A, 1B e 1C). Os menores valores de concentração são encontrados na estação 2C, próximo a península; na estação 3A, próximo a abertura da baía do Almirantado e na estação 5C, mais próxima à região do mar de Weddell.
113 113 Figura 87 Distribuição das concentrações de silicato na superfície no estreito de Bransfield Na figura 88 estão plotados os dados de clorofila-a, cuja concentração mais elevada encontra-se na estação 3A, localizada em frente da abertura da baía do Almirantado. Toda região em frente à ilha Rei George os valores de clorofila foram mais elevados, até a estação 5B, mais no centro do estreito. No transecto C no sul do estreito e próximo a península antártica as concentrações de clorofila-a foram mais baixas, principalmente nas imediações da estação 4C. Figura 88 Distribuição das concentrações de clorofila a na superfície no estreito de Bransfield Os valores da razão N/P estão plotados na figura 89. Nesta figura podemos observar que os valores mais elevados encontram-se entre as estações 1A e 2A, próximo à ilha Livingston e ilha Nelson, consecutivamente, 2C próximo à península antártica e 5B, na parte
114 114 leste e central do estreito. Destacam-se os valores mais baixos entre as estações 3A e 4A na abertura da baía do Almirantado até a parte mais a leste da ilha Rei George (Melville). Figura 89 Distribuição razões N/P na superfície no estreito de Bransfield A razão Si/N tiveram seus menores valores entre as estações 2A e 2C e na estação 4C, próximo a ilha d Urville. Os valores mais elevados foram detectados nas proximidades da estação 1B e 5ª. A variação nos valores da razão Si/N não foi elevada, mas sempre acima de 1 (fig. 9). Figura 9 Distribuição razões Si/N na superfície no estreito de Bransfield A distribuição dos valores de temperatura podem ser observados na figura 91, onde se percebe a região ao norte (próximo às ilhas Shetlands do Sul) com águas menos frias, principalmente, na região em frente à abertura da baía do Almirantado, águas mais frias ao
115 115 sul, próximo à península antártica e ilhas D Urville e Joinville e uma região no canal central do estreito onde estas água com temperaturas diferentes se encontram. Nas imediações da estação 4C encontram-se os menores valores de temperatura. Figura 91 Distribuição da temperatura na superfície no estreito de Bransfield Na figura 92 onde estão plotados os valores de salinidade observa-se que os menores valores de salinidade encontram-se próximos às ilhas Shetlands do Sul, isto é, na parte norte do estreito. Na parte sul, próximo à península antártica e ilhas d Urville e Joinville os valores de salinidade são mais elevados, destacando-se os valores das imediações da estação 4C, onde são os mais elevados. No transecto, na região central do estreito há o encontro das águas com salinidade menor da região norte com as águas de salinidade maior da região sul. Figura 92 Distribuição da salinidade na superfície no estreito de Bransfield
Ciclos biogeoquímicos
 Ciclos biogeoquímicos Conceitos Os elementos químicos essenciais à vida são aproximadamente 40. São incorporados nos seres na forma de compostos orgânicos. - ciclos sedimentares: quando o elemento circula
Ciclos biogeoquímicos Conceitos Os elementos químicos essenciais à vida são aproximadamente 40. São incorporados nos seres na forma de compostos orgânicos. - ciclos sedimentares: quando o elemento circula
Ciclos Biogeoquímicos
 Ciclos Biogeoquímicos Matéria orgânica: são os restos dos seres vivos. É composta essencialmente de compostos de carbono. Decompositores: são responsáveis pela degradação da matéria orgânica e favorecem
Ciclos Biogeoquímicos Matéria orgânica: são os restos dos seres vivos. É composta essencialmente de compostos de carbono. Decompositores: são responsáveis pela degradação da matéria orgânica e favorecem
Dr. Carlos Alberto Eiras Garcia Dr. Maurício M. Mata Dra. Mônica M. Muelbert Dr. Paul Kinas Dra. Virginia Maria Tavano Garcia. MSc.
 Universidade Santa Ursula USU Oceanographic Group of High Latitude Dr. Carlos Alberto Eiras Garcia Dr. Maurício M. Mata Dra. Mônica M. Muelbert Dr. Paul Kinas Dra. Virginia Maria Tavano Garcia Fundação
Universidade Santa Ursula USU Oceanographic Group of High Latitude Dr. Carlos Alberto Eiras Garcia Dr. Maurício M. Mata Dra. Mônica M. Muelbert Dr. Paul Kinas Dra. Virginia Maria Tavano Garcia Fundação
A Antártica, o Ano Polar Internacional ( ) e o Programa Antártico Brasileiro (PROANTAR)
 A Antártica, o Ano Polar Internacional (2007-2009) e o Programa Antártico Brasileiro (PROANTAR) Jefferson Cardia Simões (PhD, Cambridge) Núcleo de Pesquisas Antárticas e Climáticas Instituto de Geociências
A Antártica, o Ano Polar Internacional (2007-2009) e o Programa Antártico Brasileiro (PROANTAR) Jefferson Cardia Simões (PhD, Cambridge) Núcleo de Pesquisas Antárticas e Climáticas Instituto de Geociências
Prof. Marcelo Langer. Curso de Biologia. Aula 12 Ecologia
 Prof. Marcelo Langer Curso de Biologia Aula 12 Ecologia Fundamental na constituição bioquímica dos organismos vivos. Faz parte das moléculas orgânicas (DNA, RNA, Proteínas, ATP, ADP, vitaminas, clorofila
Prof. Marcelo Langer Curso de Biologia Aula 12 Ecologia Fundamental na constituição bioquímica dos organismos vivos. Faz parte das moléculas orgânicas (DNA, RNA, Proteínas, ATP, ADP, vitaminas, clorofila
1. Objetivo. 2. Introdução
 MINISTERIO DA EDUCAÇAO UNIVERSIDADE FEDERAL DE PELOTAS INSTITUTO DE QUÍMICA E GEOCIÊNCIAS DEPARTAMENTO DE QUÍMICA ANALÍTICA E INORGÂNICA CURSO DE LICENCIATURA PLENA EM QUÍMICA (1) CURSO DE BACHARELADO
MINISTERIO DA EDUCAÇAO UNIVERSIDADE FEDERAL DE PELOTAS INSTITUTO DE QUÍMICA E GEOCIÊNCIAS DEPARTAMENTO DE QUÍMICA ANALÍTICA E INORGÂNICA CURSO DE LICENCIATURA PLENA EM QUÍMICA (1) CURSO DE BACHARELADO
Na natureza nada se cria, nada se perde, tudo se transforma. Antoine de Lavoisier
 Na natureza nada se cria, nada se perde, tudo se transforma. Antoine de Lavoisier Transferência de elementos químicos entre os seres vivos e o ambiente. Ciclo da Água Ciclo do Oxigênio Ciclo do Fósforo
Na natureza nada se cria, nada se perde, tudo se transforma. Antoine de Lavoisier Transferência de elementos químicos entre os seres vivos e o ambiente. Ciclo da Água Ciclo do Oxigênio Ciclo do Fósforo
INTRODUÇÃO. Na natureza nada se cria, nada se perde, tudo se transforma. Antoine de Lavoisier
 INTRODUÇÃO Na natureza nada se cria, nada se perde, tudo se transforma. Antoine de Lavoisier Transferência de elementos químicos entre os seres vivos e o ambiente. Ciclo da Água Ciclo do Oxigênio Ciclo
INTRODUÇÃO Na natureza nada se cria, nada se perde, tudo se transforma. Antoine de Lavoisier Transferência de elementos químicos entre os seres vivos e o ambiente. Ciclo da Água Ciclo do Oxigênio Ciclo
Ciclos Biogeoquímicos
 Ciclos Biogeoquímicos Disciplina de Biologia Profa. Daniela Bueno Sudatti Livro 3, Parte III Cap 10.4 O Que é? Circulação de matéria (orgânica e inorgânica) no planeta. BIOSFERA HIDROSFERA ATMOSFERA LITOSFERA
Ciclos Biogeoquímicos Disciplina de Biologia Profa. Daniela Bueno Sudatti Livro 3, Parte III Cap 10.4 O Que é? Circulação de matéria (orgânica e inorgânica) no planeta. BIOSFERA HIDROSFERA ATMOSFERA LITOSFERA
Composição da água do mar
 Composição da água do mar Vanessa Hatje Sumário das propriedades da água Pontes de Hidrogênio são responsáveis pelo alto calor latente de fusão e evaporação e alta capacidade calorífica da água. Transporte
Composição da água do mar Vanessa Hatje Sumário das propriedades da água Pontes de Hidrogênio são responsáveis pelo alto calor latente de fusão e evaporação e alta capacidade calorífica da água. Transporte
CICLOS BIOGEOQUÍMICOS
 CICLOS BIOGEOQUÍMICOS É o trânsito da matéria entre o meio físico e os seres vivos. Quando os organismos vivos realizam os processos vitais essenciais, eles incorporam moléculas de água, carbono, nitrogênio
CICLOS BIOGEOQUÍMICOS É o trânsito da matéria entre o meio físico e os seres vivos. Quando os organismos vivos realizam os processos vitais essenciais, eles incorporam moléculas de água, carbono, nitrogênio
INTERAÇÃO MICRO-ORGANISMOS E MEIO AMBIENTE - CICLOS BIOGEOQUÍMICOS
 INTERAÇÃO MICRO-ORGANISMOS E MEIO AMBIENTE - CICLOS BIOGEOQUÍMICOS Profa. Dra. Vivian C. C. Hyodo 1 Diagrama de produção fotossintética e do consumo orgânico numa floresta, mostrando fontes, fluxos de
INTERAÇÃO MICRO-ORGANISMOS E MEIO AMBIENTE - CICLOS BIOGEOQUÍMICOS Profa. Dra. Vivian C. C. Hyodo 1 Diagrama de produção fotossintética e do consumo orgânico numa floresta, mostrando fontes, fluxos de
Plataforma continental: processos químicos
 Disciplina: Dinâmica de Ecossistemas Marinhos Plataforma continental: processos químicos Profa. Mônica Wallner-Kersanach Julho 2014 Conteúdo Plataforma continental: definição e extensão; Transporte de
Disciplina: Dinâmica de Ecossistemas Marinhos Plataforma continental: processos químicos Profa. Mônica Wallner-Kersanach Julho 2014 Conteúdo Plataforma continental: definição e extensão; Transporte de
Ilhas de Cabo Verde Islands
 Ilhas de Cabo Verde Islands Desafios duma Oceanografia Costeira em Cabo Verde Challenges of Coastal Oceanography in Cabo Verde Rui Freitas (FECM/Uni-CV) Faculdade de Engenharia e Ciências do Mar Universidade
Ilhas de Cabo Verde Islands Desafios duma Oceanografia Costeira em Cabo Verde Challenges of Coastal Oceanography in Cabo Verde Rui Freitas (FECM/Uni-CV) Faculdade de Engenharia e Ciências do Mar Universidade
Ciclos em escala global, de elementos ou substâncias químicas que necessariamente contam com a participação de seres vivos.
 Ciclos em escala global, de elementos ou substâncias químicas que necessariamente contam com a participação de seres vivos. Principais ciclos: Água Carbono Nitrogênio Mais abundante componente dos seres
Ciclos em escala global, de elementos ou substâncias químicas que necessariamente contam com a participação de seres vivos. Principais ciclos: Água Carbono Nitrogênio Mais abundante componente dos seres
Poluição Ambiental Nitrogênio e Fósforo. Prof. Dr. Antonio Donizetti G. de Souza UNIFAL-MG Campus Poços de Caldas
 Poluição Ambiental Nitrogênio e Fósforo Prof. Dr. Antonio Donizetti G. de Souza UNIFAL-MG Campus Poços de Caldas Nitrogênio Importância Componente básico da biomassa (proteínas) Fator limitante p/ Produção
Poluição Ambiental Nitrogênio e Fósforo Prof. Dr. Antonio Donizetti G. de Souza UNIFAL-MG Campus Poços de Caldas Nitrogênio Importância Componente básico da biomassa (proteínas) Fator limitante p/ Produção
Poluição Ambiental Nitrogênio e Fósforo. Prof. Dr. Antonio Donizetti G. de Souza UNIFAL-MG Campus Poços de Caldas
 Poluição Ambiental Nitrogênio e Fósforo Prof. Dr. Antonio Donizetti G. de Souza UNIFAL-MG Campus Poços de Caldas Nitrogênio Importância Componente básico da biomassa (proteínas) Fator limitante p/ Produção
Poluição Ambiental Nitrogênio e Fósforo Prof. Dr. Antonio Donizetti G. de Souza UNIFAL-MG Campus Poços de Caldas Nitrogênio Importância Componente básico da biomassa (proteínas) Fator limitante p/ Produção
UNIVERSIDADE FEDERAL DO PAMPA TRANSFORMAÇÕES DA MATÉRIA E QUANTIDADES LICENCIATURA EM CIÊNCIAS DA NATUREZA. Uruguaiana, maio de 2016.
 UNIVERSIDADE FEDERAL DO PAMPA TRANSFORMAÇÕES DA MATÉRIA E QUANTIDADES LICENCIATURA EM CIÊNCIAS DA NATUREZA CICLOS BIOGEOQUÍMICOS Uruguaiana, maio de 2016. 1 Na natureza nada se cria, nada se perde, tudo
UNIVERSIDADE FEDERAL DO PAMPA TRANSFORMAÇÕES DA MATÉRIA E QUANTIDADES LICENCIATURA EM CIÊNCIAS DA NATUREZA CICLOS BIOGEOQUÍMICOS Uruguaiana, maio de 2016. 1 Na natureza nada se cria, nada se perde, tudo
Composição da água do mar. Salinidade nos oceanos. Composição da água do mar. Vanessa Hatje. Média Hipersalinos S > 40. Hiposalinos S < 25
 Composição da água do mar Vanessa Hatje Salinidade nos oceanos Média 33 37 Hipersalinos S > 40 Mar Morto, Vermelho Hiposalinos S < 25 Estuários e baías costeiras Composição da água de mar é constante de
Composição da água do mar Vanessa Hatje Salinidade nos oceanos Média 33 37 Hipersalinos S > 40 Mar Morto, Vermelho Hiposalinos S < 25 Estuários e baías costeiras Composição da água de mar é constante de
Ecologia: definição. OIKOS Casa LOGOS Estudo. Ciência que estuda as relações entre os seres vivos e desses com o ambiente.
 Ecologia: definição OIKOS Casa LOGOS Estudo Ciência que estuda as relações entre os seres vivos e desses com o ambiente. Meio Ambiente Conjunto de condições que afetam a existência, desenvolvimento e
Ecologia: definição OIKOS Casa LOGOS Estudo Ciência que estuda as relações entre os seres vivos e desses com o ambiente. Meio Ambiente Conjunto de condições que afetam a existência, desenvolvimento e
Ciclos Biogeoquímicos
 Ciclos Biogeoquímicos CICLOS BIOGEOQUÍMICOS Ciclos: troca e circulação de matéria entre os fatores bióticos e abióticos. Bio: síntese orgânica e decomposição dos elementos. Geo: o meio terrestre (solo)
Ciclos Biogeoquímicos CICLOS BIOGEOQUÍMICOS Ciclos: troca e circulação de matéria entre os fatores bióticos e abióticos. Bio: síntese orgânica e decomposição dos elementos. Geo: o meio terrestre (solo)
Variáveis reguladoras da produção primária
 Variáveis reguladoras da produção primária 1. Regulação do crescimento (bottom-up control) Concentração de macro-nutrientes inorgânicos dissolvidos e biodisponíveis (exs.: nitratos, amónia, fosfatos, silicatos
Variáveis reguladoras da produção primária 1. Regulação do crescimento (bottom-up control) Concentração de macro-nutrientes inorgânicos dissolvidos e biodisponíveis (exs.: nitratos, amónia, fosfatos, silicatos
IFRN CICLOS BIOGEOQUÍMICOS
 IFRN CICLOS BIOGEOQUÍMICOS Prof. Hanniel Freitas Ciclos biogeoquímicos Elementos químicos tendem a circular na biosfera. Ciclagem de nutrientes - movimento desses elementos e compostos inorgânicos essenciais
IFRN CICLOS BIOGEOQUÍMICOS Prof. Hanniel Freitas Ciclos biogeoquímicos Elementos químicos tendem a circular na biosfera. Ciclagem de nutrientes - movimento desses elementos e compostos inorgânicos essenciais
Escopo do Grupo de Trabalho 1 Base Científica das Mudanças Climáticas
 CONTRIBUIÇÃO DO PAINEL BRASILEIRO DE MUDANÇAS CLIMÁTICAS PARA O PRIMEIRO RELATÓRIO DE AVALIAÇÃO NACIONAL (RAN1) PBMC.GT1.RT.I DOC.2 Minuta do Escopo do Grupo de Trabalho 1 (versão_03) Volume 1 do Primeiro
CONTRIBUIÇÃO DO PAINEL BRASILEIRO DE MUDANÇAS CLIMÁTICAS PARA O PRIMEIRO RELATÓRIO DE AVALIAÇÃO NACIONAL (RAN1) PBMC.GT1.RT.I DOC.2 Minuta do Escopo do Grupo de Trabalho 1 (versão_03) Volume 1 do Primeiro
Troca de materiais entre os componentes bióticos e abióticos dos ecossistemas.
 Troca de materiais entre os componentes bióticos e abióticos dos ecossistemas. CICLO do FÓSFORO CICLO SEDIMENTAR APATITA Ca 3 (PO 4 ) 2 erosão de rochas fosfatadas CICLO RÁPIDO CICLO LENTO PICO DO FÓSFORO
Troca de materiais entre os componentes bióticos e abióticos dos ecossistemas. CICLO do FÓSFORO CICLO SEDIMENTAR APATITA Ca 3 (PO 4 ) 2 erosão de rochas fosfatadas CICLO RÁPIDO CICLO LENTO PICO DO FÓSFORO
Talassociclo e Limnociclo. Profa. Dra. Vivian C. C. Hyodo
 Talassociclo e Limnociclo Profa. Dra. Vivian C. C. Hyodo BIOMAS DISTRIBUIÇÃO DOS NUTRIENTES VARIAÇÃO DO CLIMA SUPERFÍCIE DA TERRA GRANDE DIVERSIDADE DE HÁBITATS TOPOGRAFIA, ETC. GRANDE VARIEDADE DE SERES
Talassociclo e Limnociclo Profa. Dra. Vivian C. C. Hyodo BIOMAS DISTRIBUIÇÃO DOS NUTRIENTES VARIAÇÃO DO CLIMA SUPERFÍCIE DA TERRA GRANDE DIVERSIDADE DE HÁBITATS TOPOGRAFIA, ETC. GRANDE VARIEDADE DE SERES
FUNDAMENTOS EM ECOLOGIA
 FUNDAMENTOS EM ECOLOGIA PROFª Luciana Giacomini 1º semestre FLUXO DE ENERGIA E MATÉRIA TODO FLUXO DE ENERGIA OBEDECE ÀS DUAS PRIMEIRAS LEIS DA TERMODINÂMICA: Num sistema fechado a energia NÃO se perde,
FUNDAMENTOS EM ECOLOGIA PROFª Luciana Giacomini 1º semestre FLUXO DE ENERGIA E MATÉRIA TODO FLUXO DE ENERGIA OBEDECE ÀS DUAS PRIMEIRAS LEIS DA TERMODINÂMICA: Num sistema fechado a energia NÃO se perde,
BEV LIMNOLOGIA. Prof. Roberth Fagundes om
 BEV 180 - LIMNOLOGIA Prof. Roberth Fagundes roberthfagundes@gmail.c om O AMBIENTE AQUÁTICO BIODIVERSIDADE AQUÁTICA I pássaros homens tartarugas peixes Algas e bactérias Nutrientes Biodiversidade aquática
BEV 180 - LIMNOLOGIA Prof. Roberth Fagundes roberthfagundes@gmail.c om O AMBIENTE AQUÁTICO BIODIVERSIDADE AQUÁTICA I pássaros homens tartarugas peixes Algas e bactérias Nutrientes Biodiversidade aquática
Ciclos Biogeoquímicos
 BIOLOGIA Luisinho Ciclos Biogeoquímicos CICLOS BIOGEOQUÍMICOS A Biogeoquímica é a ciência que estuda a troca ou a circulação de matéria entre os componentes vivos e físico-químicos da Biosfera (Odum, 1971).
BIOLOGIA Luisinho Ciclos Biogeoquímicos CICLOS BIOGEOQUÍMICOS A Biogeoquímica é a ciência que estuda a troca ou a circulação de matéria entre os componentes vivos e físico-químicos da Biosfera (Odum, 1971).
Ecossistemas Biomas Ciclos Biogeoquímicos Alteração da qualidade das águas. Prof. Ms. Alonso Goes Guimarães
 Ecossistemas Biomas Ciclos Biogeoquímicos Alteração da qualidade das águas Poluição Ambiental Águas Prof. Ms. Alonso Goes Guimarães Ecossistemas Segundo Braga et al (2005): Sistema estável; Equilibrado;
Ecossistemas Biomas Ciclos Biogeoquímicos Alteração da qualidade das águas Poluição Ambiental Águas Prof. Ms. Alonso Goes Guimarães Ecossistemas Segundo Braga et al (2005): Sistema estável; Equilibrado;
Transporte de nutrientes, clorofila a
 Transporte de nutrientes, clorofila a e sólidos em suspensão na foz do Rio Mira, Vila Nova de Milfontes, ao longo de um ciclo de maré viva, Outubro 2013 A. Rosa, C. Pereira, N. Simões, A. Ovelheiro, A.
Transporte de nutrientes, clorofila a e sólidos em suspensão na foz do Rio Mira, Vila Nova de Milfontes, ao longo de um ciclo de maré viva, Outubro 2013 A. Rosa, C. Pereira, N. Simões, A. Ovelheiro, A.
METABOLISMO DO NITROGÊNIO Prof. Dr. Roberto Cezar Lobo da Costa
 METABOLISMO DO NITROGÊNIO Prof. Dr. Roberto Cezar Lobo da Costa ROTEIRO DE AULA 1. Introdução, importância e funções do nitrogênio 2. Formas nitrogenadas que podem ser absorvidas 3. Redutase do nitrato
METABOLISMO DO NITROGÊNIO Prof. Dr. Roberto Cezar Lobo da Costa ROTEIRO DE AULA 1. Introdução, importância e funções do nitrogênio 2. Formas nitrogenadas que podem ser absorvidas 3. Redutase do nitrato
4.2 - Poluição por Nutrientes Eutrofização Aumento de nutrientes, tipicamente compostos contendo N e P, no ecossistema.
 4.2 - Poluição por Nutrientes Eutrofização Aumento de nutrientes, tipicamente compostos contendo N e P, no ecossistema. O termo vem do grego: "eu bom, verdadeiro "trophein nutrir Assim, eutrófico significa
4.2 - Poluição por Nutrientes Eutrofização Aumento de nutrientes, tipicamente compostos contendo N e P, no ecossistema. O termo vem do grego: "eu bom, verdadeiro "trophein nutrir Assim, eutrófico significa
Troposfera: é a camada que se estende do solo terrestre (nível do mar) até atingir 12 quilômetros de altitude. Conforme a altitude se eleva, a
 ATMOSFERA A atmosfera é uma camada formada por argônio, hélio, dióxido de carbono, ozônio, vapor de água e, principalmente, por nitrogênio e oxigênio. Essa camada é de fundamental importância para a manutenção
ATMOSFERA A atmosfera é uma camada formada por argônio, hélio, dióxido de carbono, ozônio, vapor de água e, principalmente, por nitrogênio e oxigênio. Essa camada é de fundamental importância para a manutenção
Prof. Dr. Francisco Soares Santos Filho (UESPI)
 Prof. Dr. Francisco Soares Santos Filho (UESPI) Visão termodinâmica Alfred J. Lotka trabalhou populações e comunidades em sistemas termodinâmicos. Cada sistema apresenta um conjunto de transformações e
Prof. Dr. Francisco Soares Santos Filho (UESPI) Visão termodinâmica Alfred J. Lotka trabalhou populações e comunidades em sistemas termodinâmicos. Cada sistema apresenta um conjunto de transformações e
CURSO: CIÊNCIAS BIOLÓGICAS DISCIPLINA: FUNDAMENTOS EM ECOLOGIA PROFª LUCIANA GIACOMINI
 CENTRO UNIVERSITÁRIO NOSSA SENHORA DO PATROCÍNIO CURSO: CIÊNCIAS BIOLÓGICAS DISCIPLINA: FUNDAMENTOS EM ECOLOGIA PROFª LUCIANA GIACOMINI CICLOS BIOGEOQUÍMICOS Os elementos químicos que os organismos necessitam
CENTRO UNIVERSITÁRIO NOSSA SENHORA DO PATROCÍNIO CURSO: CIÊNCIAS BIOLÓGICAS DISCIPLINA: FUNDAMENTOS EM ECOLOGIA PROFª LUCIANA GIACOMINI CICLOS BIOGEOQUÍMICOS Os elementos químicos que os organismos necessitam
Ciclos Biogeoquímicos Luciana Ramalho 2015
 Ciclos Biogeoquímicos Luciana Ramalho 2015 Ciclos biogeoquímicos Conceito: É o trajeto das substâncias do ambiente abiótico para biótico e o seu retorno ao mundo abiótico. Há um movimento cíclico de elementos
Ciclos Biogeoquímicos Luciana Ramalho 2015 Ciclos biogeoquímicos Conceito: É o trajeto das substâncias do ambiente abiótico para biótico e o seu retorno ao mundo abiótico. Há um movimento cíclico de elementos
é a herança para os nossos filhos e netos com a sua atmosfera rica em oxigénio, permite-nos respirar com a camada de ozono, protege-nos das radiações
 é a herança para os nossos filhos e netos com a sua atmosfera rica em oxigénio, permite-nos respirar com a camada de ozono, protege-nos das radiações ultravioletas com a água evita a desidratação com as
é a herança para os nossos filhos e netos com a sua atmosfera rica em oxigénio, permite-nos respirar com a camada de ozono, protege-nos das radiações ultravioletas com a água evita a desidratação com as
Minha experiência na Antártida OPERANTAR XXIV
 III Seminário A Filosofia das Origens Minha experiência na Antártida OPERANTAR XXIV 21 de outubro 2005 a 20 de novembro 2005 Elaine Alves dos Santos Data: 30/07/2006 O continente Antártico Breve Histórico
III Seminário A Filosofia das Origens Minha experiência na Antártida OPERANTAR XXIV 21 de outubro 2005 a 20 de novembro 2005 Elaine Alves dos Santos Data: 30/07/2006 O continente Antártico Breve Histórico
Denise Mello do Prado Biologia
 Energia Solar Estima-se queapenas1% daenergiasolar quechegaà Terra é incorporada pelos vegetais por meio da fotossíntese Denise Mello do Prado Biologia www.e-conhecimento.com.br 1% absorvido fotossíntese
Energia Solar Estima-se queapenas1% daenergiasolar quechegaà Terra é incorporada pelos vegetais por meio da fotossíntese Denise Mello do Prado Biologia www.e-conhecimento.com.br 1% absorvido fotossíntese
01/03/2013 FLUXO DE ENERGIA E MATÉRIA. A matéria obedece a um ciclo FLUXO CÍCLICO PRODUTORES CONSUMIDORES. MATÉRIA INORGÂNICA pobre em energia química
 ECOLOGIA Prof. Gassem ECOSSISTEMAS FLUXO DE ENERGIA E MATÉRIA A matéria obedece a um ciclo FLUXO CÍCLICO PRODUTORES MATÉRIA INORGÂNICA pobre em energia química MATÉRIA ORGÂNICA rica em energia química
ECOLOGIA Prof. Gassem ECOSSISTEMAS FLUXO DE ENERGIA E MATÉRIA A matéria obedece a um ciclo FLUXO CÍCLICO PRODUTORES MATÉRIA INORGÂNICA pobre em energia química MATÉRIA ORGÂNICA rica em energia química
Assimilação de Nutrientes Minerais
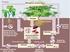 Assimilação de Nutrientes Minerais plantas são organismos fotoautoróficos: todos os compostos orgânicos necessários são formados em seu próprio corpo (macro e micro moléculas) a energia necessária para
Assimilação de Nutrientes Minerais plantas são organismos fotoautoróficos: todos os compostos orgânicos necessários são formados em seu próprio corpo (macro e micro moléculas) a energia necessária para
Ciclos Biogeoquímicos. Prof. Fernando Belan - BIOLOGIA MAIS
 Ciclos Biogeoquímicos Prof. Fernando Belan - BIOLOGIA MAIS INTRODUÇÃO CICLO DA ÁGUA; CICLO DO CARBONO; CICLO DO OXIGÊNIO; CICLO DO NITROGÊNIO; CICLO DA ÁGUA CICLO DA ÁGUA Origens do vapor-d água: Evaporação:
Ciclos Biogeoquímicos Prof. Fernando Belan - BIOLOGIA MAIS INTRODUÇÃO CICLO DA ÁGUA; CICLO DO CARBONO; CICLO DO OXIGÊNIO; CICLO DO NITROGÊNIO; CICLO DA ÁGUA CICLO DA ÁGUA Origens do vapor-d água: Evaporação:
Fisiologia e Crescimento Bacteriano
 UNIVERSIDADE FEDERAL DE JUIZ DE FORA DEPARTAMENTO DE PARASITOLOGIA, MICROBIOLOGIA E IMUNOLOGIA Fisiologia e Crescimento Bacteriano Professora: Vânia Silva Composição macromolecular de uma célula procariótica
UNIVERSIDADE FEDERAL DE JUIZ DE FORA DEPARTAMENTO DE PARASITOLOGIA, MICROBIOLOGIA E IMUNOLOGIA Fisiologia e Crescimento Bacteriano Professora: Vânia Silva Composição macromolecular de uma célula procariótica
Sedimentos Límnicos 15/06/2015. Disciplina: Limnologia Docente: Elisabete L. Nascimento. Integrantes: Gabriel Jussara Natalia Nilza Solange
 Sedimentos Límnicos 1 Autores: Francisco de Assis Esteves e Antônio Fernando Monteiro Camargo. Capítulo 19 Universidade Federal de Rondônia UNIR. 2 Disciplina: Limnologia Docente: Elisabete L. Nascimento
Sedimentos Límnicos 1 Autores: Francisco de Assis Esteves e Antônio Fernando Monteiro Camargo. Capítulo 19 Universidade Federal de Rondônia UNIR. 2 Disciplina: Limnologia Docente: Elisabete L. Nascimento
ASPECTOS DA HIDROLOGIA CONTINENTAL
 ASPECTOS DA HIDROLOGIA CONTINENTAL Quinta 8 às 12h IC2 Sala 5 Turma: 2016/01 Profª. Larissa Bertoldi larabertoldi@gmail.com Estudos Limnológicos Lagos Lagoas Lagunas LIMNOLOGIA Ciência que estuda as águas
ASPECTOS DA HIDROLOGIA CONTINENTAL Quinta 8 às 12h IC2 Sala 5 Turma: 2016/01 Profª. Larissa Bertoldi larabertoldi@gmail.com Estudos Limnológicos Lagos Lagoas Lagunas LIMNOLOGIA Ciência que estuda as águas
ECOSSISTEMA. inseparavelmente ligados. Organismos vivos + Ambiente (abiótico) interagem entre si
 ECOSSISTEMA inseparavelmente ligados Organismos vivos + Ambiente (abiótico) interagem entre si Ciclos de Diversidade Estrutura Materiais Biótica Trófica Troca de materiais vivos e não vivos Componente
ECOSSISTEMA inseparavelmente ligados Organismos vivos + Ambiente (abiótico) interagem entre si Ciclos de Diversidade Estrutura Materiais Biótica Trófica Troca de materiais vivos e não vivos Componente
Fisiologia e Crescimento Bacteriano
 UNIVERSIDADE FEDERAL DE JUIZ DE FORA DEPARTAMENTO DE PARASITOLOGIA, MICROBIOLOGIA E IMUNOLOGIA Fisiologia e Crescimento Bacteriano Professora: Vânia Silva Composição macromolecular de uma célula procariótica
UNIVERSIDADE FEDERAL DE JUIZ DE FORA DEPARTAMENTO DE PARASITOLOGIA, MICROBIOLOGIA E IMUNOLOGIA Fisiologia e Crescimento Bacteriano Professora: Vânia Silva Composição macromolecular de uma célula procariótica
Ecologia. Pirâmides Ecológicas Teias Alimentares. Conceitos Ecológicos Fundamentais. Cadeias Alimentares. Professor Fernando Stuchi
 Pirâmides Ecológicas Teias Alimentares Cadeias Alimentares Conceitos Ecológicos Fundamentais Ecologia Ecologia Os organismos da terra não vivem isolados: interagem entre si e com o meio ambiente. A ecologia
Pirâmides Ecológicas Teias Alimentares Cadeias Alimentares Conceitos Ecológicos Fundamentais Ecologia Ecologia Os organismos da terra não vivem isolados: interagem entre si e com o meio ambiente. A ecologia
BIOSFERA E SEUS ECOSSISTEMAS Cap.2
 BIOSFERA E SEUS ECOSSISTEMAS Cap.2 Conceitos Básicos ECOLOGIA Oikos =casa; logos= ciência É a ciência que estuda as relações entre os seres vivos entre si e com o ambiente onde eles vivem Estuda as formas
BIOSFERA E SEUS ECOSSISTEMAS Cap.2 Conceitos Básicos ECOLOGIA Oikos =casa; logos= ciência É a ciência que estuda as relações entre os seres vivos entre si e com o ambiente onde eles vivem Estuda as formas
Ecologia BIE210. A energia nos ecossistemas. A radiação solar.
 Ecologia BIE210 A radiação solar. A energia nos ecossistemas Fixação e transferência de energia nos ecossistemas. Eficiência ecológica. Pirâmides ecológicas. Produção e produtividade. Subsídios energéticos
Ecologia BIE210 A radiação solar. A energia nos ecossistemas Fixação e transferência de energia nos ecossistemas. Eficiência ecológica. Pirâmides ecológicas. Produção e produtividade. Subsídios energéticos
SER340 - Sensoriamento Remoto dos Oceanos Ensaio Teórico: Dinâmica dos Oceanos
 SER340 - Sensoriamento Remoto dos Oceanos Ensaio Teórico: Dinâmica dos Oceanos Sandro Klippel 3 de outubro de 2012 A Terra recebe radiação solar na forma de ondas curtas, absorvendo cerca de 65% dessa
SER340 - Sensoriamento Remoto dos Oceanos Ensaio Teórico: Dinâmica dos Oceanos Sandro Klippel 3 de outubro de 2012 A Terra recebe radiação solar na forma de ondas curtas, absorvendo cerca de 65% dessa
O OCEANO NO CLIMA. Ressurgência Camada de Ekman Giro das circulações, Circulação termohalina ENSO. correntes oceânicas a oeste
 O OCEANO NO CLIMA Ressurgência Camada de Ekman Giro das circulações, correntes oceânicas a oeste Circulação termohalina ENSO Correntes Oceânicas Correntes oceânicas têm um papel importante no transporte
O OCEANO NO CLIMA Ressurgência Camada de Ekman Giro das circulações, correntes oceânicas a oeste Circulação termohalina ENSO Correntes Oceânicas Correntes oceânicas têm um papel importante no transporte
A importância da água e os carboidratos
 A importância da água e os carboidratos Paola Stephany e Elena Mateus A água é um recurso natural de valor inestimável. Mais que um insumo indispensável à produção e um recurso estratégico para o desenvolvimento
A importância da água e os carboidratos Paola Stephany e Elena Mateus A água é um recurso natural de valor inestimável. Mais que um insumo indispensável à produção e um recurso estratégico para o desenvolvimento
BIOLOGIA. Ecologia e ciências ambientais. Ciclos biogeoquímicos Parte 1. Professor: Alex Santos
 BIOLOGIA Ecologia e ciências ambientais Parte 1 Professor: Alex Santos Tópicos em abordagem: Parte 1 Introdução a biogeoquímica e ciclo do carbono: I Características gerais dos ciclos biogeoquímicos II
BIOLOGIA Ecologia e ciências ambientais Parte 1 Professor: Alex Santos Tópicos em abordagem: Parte 1 Introdução a biogeoquímica e ciclo do carbono: I Características gerais dos ciclos biogeoquímicos II
NITROGÊNIO. Princípios da Modelagem e Controle da Qualidade da Água Superficial Regina Kishi, 7/24/2015, Página 1
 NITROGÊNIO Princípios da Modelagem e Controle da Qualidade da Água Superficial Regina Kishi, 7/24/2015, Página 1 Entradas de Nitrogênio Esgoto Compostos de nitrogênio orgânico (ex.: proteínas, uréia) e
NITROGÊNIO Princípios da Modelagem e Controle da Qualidade da Água Superficial Regina Kishi, 7/24/2015, Página 1 Entradas de Nitrogênio Esgoto Compostos de nitrogênio orgânico (ex.: proteínas, uréia) e
Da aula passada... Gases Dissolvidos não Conservativos. Concentração Normal de Equilíbrio da ATM (NAEC)
 Da aula passada... Gases Dissolvidos não Conservativos Concentração Normal de Equilíbrio da ATM (NAEC) Concentração de gás dissolvido em equilíbrio com a concentração atmosférica [A (l) ] = α P A Principais
Da aula passada... Gases Dissolvidos não Conservativos Concentração Normal de Equilíbrio da ATM (NAEC) Concentração de gás dissolvido em equilíbrio com a concentração atmosférica [A (l) ] = α P A Principais
Produtividade. Prof. Dr. Francisco Soares Santos Filho (UESPI)
 Produtividade Prof. Dr. Francisco Soares Santos Filho (UESPI) Estudo de energia do ecossistema Foram iniciados em 1942 por R. L. Lindeman The trophic dynamic aspect of ecology A idéia geral foi converter
Produtividade Prof. Dr. Francisco Soares Santos Filho (UESPI) Estudo de energia do ecossistema Foram iniciados em 1942 por R. L. Lindeman The trophic dynamic aspect of ecology A idéia geral foi converter
A profundidade do oceano é de 3794 m (em média), mais de cinco vezes a altura média dos continentes.
 Hidrosfera Compreende todos os rios, lagos,lagoas e mares e todas as águas subterrâneas, bem como as águas marinhas e salobras, águas glaciais e lençóis de gelo, vapor de água, as quais correspondem a
Hidrosfera Compreende todos os rios, lagos,lagoas e mares e todas as águas subterrâneas, bem como as águas marinhas e salobras, águas glaciais e lençóis de gelo, vapor de água, as quais correspondem a
Ciclos biogeoquímicos. A energia flui. A matéria é cíclica. Esses elementos são fundamentais para os seres vivos e embora em abundancia são finitos.
 Ciclos biogeoquímicos A energia flui. A matéria é cíclica. Esses elementos são fundamentais para os seres vivos e embora em abundancia são finitos. Ciclo da Água - O mais simples. A água não sofre transformação
Ciclos biogeoquímicos A energia flui. A matéria é cíclica. Esses elementos são fundamentais para os seres vivos e embora em abundancia são finitos. Ciclo da Água - O mais simples. A água não sofre transformação
BIOMAS. Professora Débora Lia Ciências/Biologia
 BIOMAS Professora Débora Lia Ciências/Biologia BIOMAS - Aquáticos Mares e oceanos Talássicos São as regiões com a maior variedade de vida do planeta, nem as florestas tropicais igualam-se às regiões litorâneas;
BIOMAS Professora Débora Lia Ciências/Biologia BIOMAS - Aquáticos Mares e oceanos Talássicos São as regiões com a maior variedade de vida do planeta, nem as florestas tropicais igualam-se às regiões litorâneas;
BIOLOGIA. Ecologia I. Matéria e Energia nos Ecossistemas. Professora: Brenda Braga
 BIOLOGIA Ecologia I Matéria e Energia nos Ecossistemas Professora: Brenda Braga Níveis de Organização Fatores: Bióticos+Abióticos Nicho x Habitat predadores outros lobos parasitas tipo de reprodução alimento
BIOLOGIA Ecologia I Matéria e Energia nos Ecossistemas Professora: Brenda Braga Níveis de Organização Fatores: Bióticos+Abióticos Nicho x Habitat predadores outros lobos parasitas tipo de reprodução alimento
NÍVEIS DE ORGANIZAÇÃO ORGANISMO. POPULAÇÃO. COMUNIDADE. ECOLOGIA ECOSSISTEMA. CURSINHO 2018 BIOSFERA.
 NÍVEIS DE ORGANIZAÇÃO ORGANISMO. POPULAÇÃO. ECOLOGIA CURSINHO 2018 COMUNIDADE. ECOSSISTEMA. BIOSFERA. ORGANISMO ORGANISMO POPULAÇÃO POPULAÇÃO COMUNIDADE COMUNIDADE ECOSSISTEMA BIOSFERA TALASSOCICLO: marinho
NÍVEIS DE ORGANIZAÇÃO ORGANISMO. POPULAÇÃO. ECOLOGIA CURSINHO 2018 COMUNIDADE. ECOSSISTEMA. BIOSFERA. ORGANISMO ORGANISMO POPULAÇÃO POPULAÇÃO COMUNIDADE COMUNIDADE ECOSSISTEMA BIOSFERA TALASSOCICLO: marinho
Ciclos Biogeoquímicos
 PONTIFÍCIA UNIVERSIDADE CATÓLICA DE GOIÁS Disciplina: Ciências do Ambiente ENG 4201 Ciclos Biogeoquímicos Características do Ciclos Biogeoquímicos. Biológicas porque ocorrem transformações com a participação
PONTIFÍCIA UNIVERSIDADE CATÓLICA DE GOIÁS Disciplina: Ciências do Ambiente ENG 4201 Ciclos Biogeoquímicos Características do Ciclos Biogeoquímicos. Biológicas porque ocorrem transformações com a participação
TIS. Papel do Azoto e dos micro organismos na Agricultura
 Papel do Azoto e dos micro organismos na Agricultura 1 O Azoto O azoto ou nitrogénio, de símbolo químico N, encontramo-lo no estado gasoso e constitui cerca de 78 % do ar da atmosfera terrestre. É um gás
Papel do Azoto e dos micro organismos na Agricultura 1 O Azoto O azoto ou nitrogénio, de símbolo químico N, encontramo-lo no estado gasoso e constitui cerca de 78 % do ar da atmosfera terrestre. É um gás
CICLO DO ENXOFRE. O enxofre é indispensável na elaboração de proteínas. cisteina H 2 N CH C CH 2
 CICLO DO ENXOFRE O enxofre é o 16º elemento mais abundante na crosta terrestre, constituindo 0,034% em peso,ocorrendo principalmente nas rochas, na forma de sulfatos solúveis presentes na água, nos sedimentos
CICLO DO ENXOFRE O enxofre é o 16º elemento mais abundante na crosta terrestre, constituindo 0,034% em peso,ocorrendo principalmente nas rochas, na forma de sulfatos solúveis presentes na água, nos sedimentos
1. (UNIPAM) Nas últimas décadas, diversos fenômenos climáticos têm sido foco de discussões na academia e na mídia, devido às implicações sociais,
 1. (UNIPAM) Nas últimas décadas, diversos fenômenos climáticos têm sido foco de discussões na academia e na mídia, devido às implicações sociais, econômicas e ambientais que desencadeiam. Entre esses fenômenos,
1. (UNIPAM) Nas últimas décadas, diversos fenômenos climáticos têm sido foco de discussões na academia e na mídia, devido às implicações sociais, econômicas e ambientais que desencadeiam. Entre esses fenômenos,
Ecologia Microbiana. Microbiologia do Solo. Microbiologia da Água
 Ecologia Microbiana Microbiologia do Solo Microbiologia da Água Camadas do solo (horizontes) Camada A: Solo superficial (rico em matéria orgânica) A Alta atividade microbiana Camada B: Subsolo (pobre
Ecologia Microbiana Microbiologia do Solo Microbiologia da Água Camadas do solo (horizontes) Camada A: Solo superficial (rico em matéria orgânica) A Alta atividade microbiana Camada B: Subsolo (pobre
é a herança para os nossos filhos e netos com a sua atmosfera rica em oxigénio, permite-nos respirar com a camada de ozono, protege-nos das radiações
 é a herança para os nossos filhos e netos com a sua atmosfera rica em oxigénio, permite-nos respirar com a camada de ozono, protege-nos das radiações ultravioletas com a água evita a desidratação com as
é a herança para os nossos filhos e netos com a sua atmosfera rica em oxigénio, permite-nos respirar com a camada de ozono, protege-nos das radiações ultravioletas com a água evita a desidratação com as
AULA 4 -Limnologia. Patricia M. P. Trindade Waterloo Pereira Filho
 AULA 4 -Limnologia Patricia M. P. Trindade Waterloo Pereira Filho O que é Limnologia É o estudo ecológico de todas as massas d água continentais. Portanto, são inúmeros corpos d água objeto de estudo da
AULA 4 -Limnologia Patricia M. P. Trindade Waterloo Pereira Filho O que é Limnologia É o estudo ecológico de todas as massas d água continentais. Portanto, são inúmeros corpos d água objeto de estudo da
Oceanografia por Satélites
 Oceanografia por Satélites Sensor de Cor do Oceano. Aplicação em Medidas de Concentração de Clorofila Paulo S. Polito, Ph.D. polito@usp.br Instituto Oceanográfico da Universidade de São Paulo http://los.io.usp.br
Oceanografia por Satélites Sensor de Cor do Oceano. Aplicação em Medidas de Concentração de Clorofila Paulo S. Polito, Ph.D. polito@usp.br Instituto Oceanográfico da Universidade de São Paulo http://los.io.usp.br
2º TRIMESTRE REVISÃO PARA O TESTE
 2º TRIMESTRE REVISÃO PARA O TESTE CAPÍTULOS 2 E 3 Disciplina: Ciências Série: 6º anos Professora: Daniela AMBIENTES AQUÁTICOS E TERRESTRES Ambientes de água doce: são pouco profundos, boa luminosidade,
2º TRIMESTRE REVISÃO PARA O TESTE CAPÍTULOS 2 E 3 Disciplina: Ciências Série: 6º anos Professora: Daniela AMBIENTES AQUÁTICOS E TERRESTRES Ambientes de água doce: são pouco profundos, boa luminosidade,
CICLOS BIOGEOQUÍMICOS
 CLAUDIO POZZATTI CICLOS BIOGEOQUÍMICOS Demonstram a maneira como a mãe-terra empresta seus elementos para a organização do corpo dos seres vivos e que esses mesmos elementos serão um dia devolvidos ao
CLAUDIO POZZATTI CICLOS BIOGEOQUÍMICOS Demonstram a maneira como a mãe-terra empresta seus elementos para a organização do corpo dos seres vivos e que esses mesmos elementos serão um dia devolvidos ao
MaCS/SiMCo - Marine and Coastal Systems Master Program. Teórica 2 Lecture 2
 MaCS/SiMCo - Marine and Coastal Systems Master Program Dinâmica Trófica Marinha Marine Trophic Dynamics Docentes/lecturers: Helena Galvão Sofia Gamito Karim Erzini Teórica 2 Lecture 2 Importância da Teia
MaCS/SiMCo - Marine and Coastal Systems Master Program Dinâmica Trófica Marinha Marine Trophic Dynamics Docentes/lecturers: Helena Galvão Sofia Gamito Karim Erzini Teórica 2 Lecture 2 Importância da Teia
NUTRIÇÃO MINERAL GÊNESE DO SOLO. Rochas da Litosfera expostas ao calor, água e ar. Alterações físicas e químicas (intemperismo)
 NUTRIÇÃO MINERAL GÊNESE DO SOLO Rochas da Litosfera expostas ao calor, água e ar Alterações físicas e químicas (intemperismo) Físico (Altera o tamanho) Químico (Altera a composição) Intemperismo Físico
NUTRIÇÃO MINERAL GÊNESE DO SOLO Rochas da Litosfera expostas ao calor, água e ar Alterações físicas e químicas (intemperismo) Físico (Altera o tamanho) Químico (Altera a composição) Intemperismo Físico
Ecossistemas I. Umberto Kubota Laboratório de Interações Inseto-Planta Dep. Zoologia IB Unicamp. Produtividade secundária
 Ecossistemas I Umberto Kubota ukubota@gmail.com Laboratório de Interações Inseto-Planta Dep. Zoologia IB Unicamp Ecossistemas I Conceitos básicos Fluxo de energia Produtividade primária Ecossistema: Conceitos
Ecossistemas I Umberto Kubota ukubota@gmail.com Laboratório de Interações Inseto-Planta Dep. Zoologia IB Unicamp Ecossistemas I Conceitos básicos Fluxo de energia Produtividade primária Ecossistema: Conceitos
II. INVESTIGANDO O INACESSÍVEL
 II. INVESTIGANDO O INACESSÍVEL A Terra é um dos nove planetas do Sistema Solar e é o maior dos planetas interiores. A Terra é quase esférica, sendo que o diâmetro maior é o equatorial, com 12.756 km. O
II. INVESTIGANDO O INACESSÍVEL A Terra é um dos nove planetas do Sistema Solar e é o maior dos planetas interiores. A Terra é quase esférica, sendo que o diâmetro maior é o equatorial, com 12.756 km. O
GEOGRAFIA. Prof. Daniel San.
 GEOGRAFIA Prof. Daniel San daniel.san@lasalle.org.br SOLOS Solo é o substrato onde os seres humanos constroem suas vidas, por sobre a astenosfera (Crosta), abaixo da atmosfera. O solo é produto da intemperização
GEOGRAFIA Prof. Daniel San daniel.san@lasalle.org.br SOLOS Solo é o substrato onde os seres humanos constroem suas vidas, por sobre a astenosfera (Crosta), abaixo da atmosfera. O solo é produto da intemperização
NITROGÊNIO. Universidade Estadual Paulista Júlio de Mesquita Filho Campus Experimental de Dracena Faculdade de Zootecnia
 Universidade Estadual Paulista Júlio de Mesquita Filho Campus Experimental de Dracena Faculdade de Zootecnia NITROGÊNIO Curso : Zootecnia Disciplina: Fertilidade do Solo e Fertilizantes Prof. Dr. Reges
Universidade Estadual Paulista Júlio de Mesquita Filho Campus Experimental de Dracena Faculdade de Zootecnia NITROGÊNIO Curso : Zootecnia Disciplina: Fertilidade do Solo e Fertilizantes Prof. Dr. Reges
Ecologia I -Conceitos
 Ecologia I -Conceitos -Pirâmides ecológicas -Fluxo de energia Professora: Luciana Ramalho 2018 Introdução Ecologia é uma ciência que estuda os seres vivos e suas interações com o meio ambiente onde vivem.
Ecologia I -Conceitos -Pirâmides ecológicas -Fluxo de energia Professora: Luciana Ramalho 2018 Introdução Ecologia é uma ciência que estuda os seres vivos e suas interações com o meio ambiente onde vivem.
CICLOS BIOGEOQUÍMICOS. O processo contínuo de retirada e devolução de elementos químicos à natureza constitui os chamados ciclos biogeoquímicos.
 CICLOS BIOGEOQUÍMICOS O processo contínuo de retirada e devolução de elementos químicos à natureza constitui os chamados ciclos biogeoquímicos. CICLO HIDROLÓGICO A sobrevivência de cada ser vivo de toda
CICLOS BIOGEOQUÍMICOS O processo contínuo de retirada e devolução de elementos químicos à natureza constitui os chamados ciclos biogeoquímicos. CICLO HIDROLÓGICO A sobrevivência de cada ser vivo de toda
As terras submersas e a água no globo terrestre
 As terras submersas e a água no globo terrestre CONTINENTES Blocos continentais que resultaram da divisão do continente único: Pangeia. Quatro grandes massas continentais: Continente Tríplipe (África,
As terras submersas e a água no globo terrestre CONTINENTES Blocos continentais que resultaram da divisão do continente único: Pangeia. Quatro grandes massas continentais: Continente Tríplipe (África,
Ciclos Biogeoquímicos
 Ciclos Biogeoquímicos DEFINIÇÃO Trata-se de movimentos cíclicos que envolvem elementos químicos presentes no meio biológico e o ambiente geológico; Elementos que são necessários ao desenvolvimento dos
Ciclos Biogeoquímicos DEFINIÇÃO Trata-se de movimentos cíclicos que envolvem elementos químicos presentes no meio biológico e o ambiente geológico; Elementos que são necessários ao desenvolvimento dos
CIÊNCIAS. Prof. Diângelo
 CIÊNCIAS Prof. Diângelo TABELA PERÍODICA Aula 18 Respiração Celular Respiração celular é o processo de conversão das ligações químicas de moléculas ricas em energia que poderão ser usadas nos processos
CIÊNCIAS Prof. Diângelo TABELA PERÍODICA Aula 18 Respiração Celular Respiração celular é o processo de conversão das ligações químicas de moléculas ricas em energia que poderão ser usadas nos processos
O Ecossistema Aquático
 UNIVERSIDADE FEDERAL DO RIO GRANDE LICENCIATURA EM CIÊNCIAS INTERDISCIPLINA FENÔMENOS DA NATUREZA II O Ecossistema Aquático Dr. Cleber Palma Silva Dra. Edélti Faria Albertoni Lab. Limnologia O Pensamento
UNIVERSIDADE FEDERAL DO RIO GRANDE LICENCIATURA EM CIÊNCIAS INTERDISCIPLINA FENÔMENOS DA NATUREZA II O Ecossistema Aquático Dr. Cleber Palma Silva Dra. Edélti Faria Albertoni Lab. Limnologia O Pensamento
CICLO DO NITROGÊNIO RELAÇÃO DE DEPENDÊNICIA ENTRE OS COMPOSTOS NITROGENADOS DA BIOSFERA - NITRATO NO 2 NO 3 - NITRITO NH 3 - AMÔNIA
 CICLO DO NITROGÊNIO RELAÇÃO DE DEPENDÊNICIA ENTRE OS COMPOSTOS NITROGENADOS DA BIOSFERA N 2 NITROGÊNIO MOLECULAR INORGÂNICOS NO 3 NITRATO NO 2 NITRITO NH 3 AMÔNIA ORGÂNICOS AMINOÁCIDOS, AMINAS, ALCALÓIDES,
CICLO DO NITROGÊNIO RELAÇÃO DE DEPENDÊNICIA ENTRE OS COMPOSTOS NITROGENADOS DA BIOSFERA N 2 NITROGÊNIO MOLECULAR INORGÂNICOS NO 3 NITRATO NO 2 NITRITO NH 3 AMÔNIA ORGÂNICOS AMINOÁCIDOS, AMINAS, ALCALÓIDES,
Salvar os oceanos. Escola Básica e Secundária de Muralhas do Minho, Valença. A. Lê Conhecer o Oceano princípio 1 e completa as palavras cruzadas.
 A. Lê Conhecer o Oceano princípio 1 e completa as palavras cruzadas. Componente física dominante no nosso planeta (10) Uma das bacias do Oceano (7) Tipo de planícies que o relevo das bacias oceânicas contém
A. Lê Conhecer o Oceano princípio 1 e completa as palavras cruzadas. Componente física dominante no nosso planeta (10) Uma das bacias do Oceano (7) Tipo de planícies que o relevo das bacias oceânicas contém
O SOLO COMO F0RNECEDOR DE NUTRIENTES
 O SOLO COMO F0RNECEDOR DE NUTRIENTES LIQUIDA (SOLUÇÃO DO SOLO) ÍONS INORGÂNICOS E ORGÂNICOS/MICROPOROS SÓLIDA - RESERVATORIO DE NUTRIENTES - SUPERFÍCIE QUE REGULA A CONCENTRAÇÃO DOS ELEMENTOS NA SOLUÇÃO
O SOLO COMO F0RNECEDOR DE NUTRIENTES LIQUIDA (SOLUÇÃO DO SOLO) ÍONS INORGÂNICOS E ORGÂNICOS/MICROPOROS SÓLIDA - RESERVATORIO DE NUTRIENTES - SUPERFÍCIE QUE REGULA A CONCENTRAÇÃO DOS ELEMENTOS NA SOLUÇÃO
CIÊNCIAS DO AMBIENTE E ECOLOGIA
 CIÊNCIAS DO AMBIENTE E ECOLOGIA CIÊNCIAS DO AMBIENTE E ECOLOGIA INTRODUÇÃO E CONCEITOS DE ECOLOGIA: A CRISE AMBIENTAL, CONCEITOS BÁSICOS EM ECOLOGIA, FATORES LIMITANTES. DINÂMICA POPULACIONAL: CONCEITOS,
CIÊNCIAS DO AMBIENTE E ECOLOGIA CIÊNCIAS DO AMBIENTE E ECOLOGIA INTRODUÇÃO E CONCEITOS DE ECOLOGIA: A CRISE AMBIENTAL, CONCEITOS BÁSICOS EM ECOLOGIA, FATORES LIMITANTES. DINÂMICA POPULACIONAL: CONCEITOS,
3. Área de Estudo Localização da Área de Estudo
 40 3. Área de Estudo 3.1. Localização da Área de Estudo A área escolhida para a realização desse estudo foi a região de Cabo Frio localizada na baixada litorânea do Estado do Rio de Janeiro (Figura 2),
40 3. Área de Estudo 3.1. Localização da Área de Estudo A área escolhida para a realização desse estudo foi a região de Cabo Frio localizada na baixada litorânea do Estado do Rio de Janeiro (Figura 2),
GOIÂNIA, / / 2016 PROFESSOR: MARIO NETO
 GOIÂNIA, / / 2016 PROFESSOR: MARIO NETO DISCIPLINA:CIÊNCIA NATURAIS SÉRIE: 1º ALUNO(a): No Anhanguera você é + Enem 1) (UDESC/2009) Com relação aos ciclos biogeoquímicos, analise as seguintes afirmativas:
GOIÂNIA, / / 2016 PROFESSOR: MARIO NETO DISCIPLINA:CIÊNCIA NATURAIS SÉRIE: 1º ALUNO(a): No Anhanguera você é + Enem 1) (UDESC/2009) Com relação aos ciclos biogeoquímicos, analise as seguintes afirmativas:
Microbiologia do Ambiente. Sistemas aquáticos
 Microbiologia do Ambiente Sistemas aquáticos Ciclo da Água Precipitaçã o Evaporaçã o Infiltração Escorrênci a Classificação das águas Águas atmosféricas Águas superficiais doces Águas subterrâneas Águas
Microbiologia do Ambiente Sistemas aquáticos Ciclo da Água Precipitaçã o Evaporaçã o Infiltração Escorrênci a Classificação das águas Águas atmosféricas Águas superficiais doces Águas subterrâneas Águas
BIOLOGIA. Ecologia e ciências ambientais. Ciclos biogeoquímicos Parte 2. Professor: Alex Santos
 BIOLOGIA Ecologia e ciências ambientais Parte 2 Professor: Alex Santos Tópicos em abordagem: Parte 1 Introdução a biogeoquímica e ciclo do carbono: I Características gerais do nitrogênio II Ciclo do nitrogênio
BIOLOGIA Ecologia e ciências ambientais Parte 2 Professor: Alex Santos Tópicos em abordagem: Parte 1 Introdução a biogeoquímica e ciclo do carbono: I Características gerais do nitrogênio II Ciclo do nitrogênio
UNIVERSIDADE DO ESTADO DE SANTA CATARINA UDESC CENTRO DE ECAÇÃO SUPERIOR DO ALTO VALE DO ITAJAÍ CEAVI PLANO DE ENSINO
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA UDESC CENTRO DE ECAÇÃO SUPERIOR DO ALTO VALE DO ITAJAÍ CEAVI PLANO DE ENSINO DEPARTAMENTO: Engenharia Sanitária DISCIPLINA: FUNDAMENTOS DE ECOLOGIA E LIMNOLOGIA
UNIVERSIDADE DO ESTADO DE SANTA CATARINA UDESC CENTRO DE ECAÇÃO SUPERIOR DO ALTO VALE DO ITAJAÍ CEAVI PLANO DE ENSINO DEPARTAMENTO: Engenharia Sanitária DISCIPLINA: FUNDAMENTOS DE ECOLOGIA E LIMNOLOGIA
Biomas Terrestres. Prof. Bosco Ribeiro
 Biomas Terrestres Prof. Bosco Ribeiro Introdução São regiões de grande extensão onde se desenvolveu, predominantemente, um determinado tipo de vida, as quais são, em grande parte, distribuídas pela superfície
Biomas Terrestres Prof. Bosco Ribeiro Introdução São regiões de grande extensão onde se desenvolveu, predominantemente, um determinado tipo de vida, as quais são, em grande parte, distribuídas pela superfície
