Nimenrix vacina meningocócica ACWY (conjugada)
|
|
|
- João Guilherme Camilo Benevides
- 6 Há anos
- Visualizações:
Transcrição
1 vacina meningocócica AWY (conjugada) I - IDETIFIAÇÃO DO MEDIAMETO ome comercial: ome genérico: vacina meningocócica AWY (conjugada) APRESETAÇÕES Pó liofilizado para reconstituição com diluente Embalagem com: 1 frasco-ampola + 1 seringa preenchida com diluente (0,5 ml) VIA DE ADMIISTRAÇÃO: USO ITRAMUSULAR USO ADULTO E PEDIÁTRIO (A PARTIR DE 12 MESES DE IDADE) OMPOSIÇÃO ada dose (0,5 ml) da vacina reconstituída contém: Polissacarídeo de eisseria meningitidis do sorogrupo A mcg Polissacarídeo de eisseria meningitidis do sorogrupo mcg Polissacarídeo de eisseria meningitidis do sorogrupo W mcg Polissacarídeo de eisseria meningitidis do sorogrupo Y mcg 1 conjugado à proteína carreadora toxoide tetânico. Excipientes*... q.s.p.... 0,5 ml * Excipientes: sacarose, trometamol, cloreto de sódio, água para injetáveis. LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 1
2 II - IFORMAÇÕES TÉIAS AOS PROFISSIOAIS DE SAÚDE 1. IDIAÇÕES é indicado para imunização ativa de indivíduos com idade a partir de 12 meses contra doenças meningocócicas invasivas causadas por eisseria meningitidis dos sorogrupos A,, W-135 e Y (ver o item Efeitos Farmacodinâmicos). 2. RESULTADOS DE EFIÁIA Efeitos Farmacodinâmicos Avaliou-se a imunogenicidade de uma dose dessa vacina em mais de indivíduos com idade a 12 meses. oncluiu-se sobre a eficácia de pela demonstração de sua não inferioridade imunológica (com base principalmente na comparação das proporções de títulos de rsba de pelo menos 1:8) em relação a vacinas meningocócicas registradas. Para medir a imunogenicidade usou-se o rsba ou o hsba; ambos são biomarcadores da eficácia protetora contra os sorogrupos meningocócicos A,, W-135 e Y. Definiu-se a resposta à vacina em indivíduos a 2 anos de idade como a proporção de vacinados com: título 32 no rsba entre os indivíduos inicialmente soronegativos (ou seja, com título <8 no rsba prévacinação); aumento de pelo menos 4 vezes no título mostrado no rsba pós-vacinação em relação à pré-vacinação entre os indivíduos inicialmente soropositivos (ou seja, com título 8 no rsba pré-vacinação). Imunogenicidade da vacina Imunogenicidade em crianças de 12 a 23 meses: os estudos clínicos MenAWY-TT-039 e MenAWY-TT-040, uma dose única de induziu a resposta rsba contra os quatro grupos meningocócicos, e a resposta contra o sorogrupo foi comparável à induzida pela vacina registrada Men-RM em termos de porcentagens com títulos 8 no rsba (Tabela 1). Tabela 1: Respostas de anticorpos bactericidas (medidas por rsba*) em crianças de 12 a 23 meses Sorogrupo Resposta a: Estudo MenAWY-TT-039 (1) Estudo MenAWY-TT-040 (2) 8 A ,7% (98,4; 100) ,7% (98,4; 100) vacina ,5% Men- (92,9; 99,5) RM W % (99,0; 100) Y % (2.008; 2.422) 478 (437; 522) 212 (170; 265) ,4% (95,3; 99,7) ,3% (93,7; 99,1) ,2% (93,8; 99,8) (2.453; 2.932) ,4% (95,4; 99,7) ,3% (99,0; 100) (2.473; 3.013) (93,8; 99,1) A análise da imunogenicidade foi conduzida nas coortes de acordo com o protocolo (ATP) de imunogenicidade. (1) Amostras de sangue coletadas 42 a 56 dias pós-vacinação. (2) Amostras de sangue coletadas 30 a 42 dias pós-vacinação. *Testado nos laboratórios da GlaxoSmithKline : título médio geométrico (2.577; 3.899) 829 (672; 1.021) 691 (521; 918) (3.269; 4.949) (2.522; 3.979) o estudo MenAWY-TT-039, também se mediu atividade bactericida sérica, com soro humano como fonte de complemento (teste hsba), utilizando-se como endpoint secundário os títulos obtidos (Tabela 2). LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 2
3 Tabela 2: Respostas de anticorpos bactericidas (medidas por hsba*) em crianças de 12 a 23 meses Grupo Resposta a: Estudo MenAWY-TT-039 * 8 A ,2% (72,4; 81,6) 19,0 (16,4; 22,1) ,5% (96,6; 99,5) 196 (175; 219) vacina Men-RM ,9% (73,7; 88,4) 40,3 (29,5; 55,1) W ,5% 48,9 (83,5; 90,8) Y ,3% (74,5; 83,6) A análise da imunogenicidade foi conduzida na coorte ATP de imunogenicidade. (1) Amostras de sangue coletadas 42 a 56 dias pós-vacinação. *Testado nos laboratórios da GlaxoSmithKline (41,2; 58,0) 30,9 (25,8; 37,1) o estudo MenAWY-TT-104, a resposta imune após uma ou duas doses de com 2 meses de intervalo foi avaliada um mês após a última vacinação. provocou respostas bactericidas contra os quatro grupos semelhantes em termos de % com rsba 8 e GMT, após uma ou duas doses (Tabela 3). Tabela 3: Respostas de anticorpos bactericidas (rsba*) em crianças com idade entre meses 2 Estudo MenAWY-TT-104 (1) Grupo Resposta a: Período 8 (95%I) 1 dose Pós dose ,8 (94,4; 99,4) 1445,4 (1126,1; 1855,2) A 2 doses Pós dose Pós dose ,8 (92,8; 99,0) 98,0 (94,3; 99,6) 1275,2 (970,5; 1675,4) 1176,3 (921,8; 1501) 1 dose Pós dose ,0 (90,7; 97,7) 454,4 (347,7; 593,8) 2 doses Pós dose Pós dose ,5 (91,0; 98,2) 98,7 (95,3; 99,8) 369,3 (280,9; 485,5) 639,1 (521,8; 782,9) 1 dose Pós dose ,0 (90,8; 97,7) 2136,1 (1614,9; 2825,5) W doses Pós dose Pós dose ,9 (90,3; 97,8) 100 (97,6; 100) 2030,1 (1510,7; 2728,2) 3533 (2914,5; 4282,7) Y 1 dose Pós dose ,8 (88,0; 96,1) 955,8 (709,1; 1288,3) LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 3
4 2 doses Pós dose ,6 (88,6; 96,9) 933,3 (692,3; 1258,3) 99,3 1133,6 Pós dose (96,3; 100) (944,5; 1360,5) A análise da imunogenicidade foi realizada na coorte de acordo com protocolo (ATP) para imunogenicidade. (1) amostragem de sangue realizada dias após a vacinação. * Testado nos laboratórios da Public Health England o estudo MenAWY-TT-104, a atividade bactericida do soro também foi medida usando hsba como um endpoint secundário. provocou respostas bactericidas contra os grupos W-135 e Y que foram maiores em termos de % com título hsba 8 quando duas doses foram administradas em comparação com uma. Respostas semelhantes em termos de % com título hsba 8 foram observadas com os grupos A e (Tabela 4). Tabela 4: Respostas de anticorpos bactericidas (hsba *) em crianças com idade entre meses 2,3 Estudo em homens AWY-TT-104 (1) Grupo Resposta a: Período 8 (95%I) 1 dose Pós dose ,0 (88,8; 99,2) 119,3 (88,0; 161,7) A 2 doses Pós dose 1 66 Pós dose ,0 (89,5; 99,6) 97,0 (89,5; 99,6) (98,1; 180,1) 170,5 (126,2; 230,2) 1 dose Pós dose ,7 (93,1; 100) 151,2 (104,7; 218,3) 2 doses Pós dose 1 70 Pós dose ,7 (88,0; 99,1) 100 (94,8; 100) 161 (110; 236) 1753,3 (1277,7; 2404,2) 1 dose Pós dose ,5 (50,3; 73,6) 27,5 (16,1; 46,8) W doses Pós dose 1 61 Pós dose ,9 (55,7; 80,1) 97.1 (90,1, 99,7) 26,2 (16,0; 43,0) 756,8 (550,1; 1041,3) 1 dose Pós dose ,6 (55,5; 78,20) 41,2 (23,7; 71,5) Y 2 doses Pós dose ,3 (50,4; 76,6) 31,9 (17,6; 57,9) 95,3 513,0 Pós dose 2 64 (86,9; 99,0) (339,4; 775,4) A análise da imunogenicidade foi realizada na coorte de acordo com protocolo (ATP) para imunogenicidade. (1) amostragem de sangue realizada dias após a vacinação. * Testado nos laboratórios GSK LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 4
5 Imunogenicidade em crianças de 2 a 10 anos: Em dois estudos comparativos conduzidos em crianças de 2 a 10 anos, um grupo de participantes recebeu uma dose de e um segundo grupo recebeu outra vacina para comparação. Em um dos estudos, o MenAWY-TT-081, usou-se como comparador uma dose de Men-RM registrada e no outro, o MenAWY- TT-038, uma dose da vacina meningocócica simples de polissacarídeos dos sorogrupos A,, W-135 e Y (AWY-PS) registrada de GlaxoSmithKline Biologicals. o estudo MenAWY-TT-038, demonstrou ser não inferior à AWY-PS registrada em termos de resposta relativamente aos quatro sorogrupos (A,, W-135 e Y) (Tabela 5). Tabela 5: Respostas de anticorpos bactericidas (medidas por rsba*) à e à vacina AWY-PS em crianças de 2 a 10 anos um mês após a vacinação (estudo MenAWY-TT-038) Sorogrupo vacina AWY-PS RV RV A ,1% (86,3; 91,5) (5.998; 6.708) ,6% (57,4; 71,3) (2.023; 2.577) ,1% (94,4; 97,4) (4.342; 5.335) ,7% (85,1; 93,3) (1.043; 1.663) W ,4% ,6% (95,9; 98,4) (10.873; ) Y ,7% (90,5; 94,5) (10.233; ) A análise da imunogenicidade foi conduzida na coorte ATP de imunogenicidade. RV: resposta à vacina. *Testado nos laboratórios da GlaxoSmithKline (77,2; 87,2) % (62,5; 74,6) (1.815; 2.565) (2.237; 3.052) o estudo MenAWY-TT-081, (=268) demonstrou ser não inferior à Men-RM registrada (=92) em termos de resposta relativamente ao sorogrupo Men [respostas de 94,8% (I de 95%: 91,4; 97,1) e 95,7% (I de 95%: 89,2; 98,8), respectivamente]. Os s foram mais baixos no grupo de [2.795 (I de 95%: 2.393; 3.263)] em comparação com a Men-RM [5.292 (I de 95%: 3.815; 7.340)]. Imunogenicidade em adolescentes de 11 a 17 anos e em adultos a partir de 18 anos: Em dois estudos clínicos, um deles conduzido em adolescentes de 11 a 17 anos (o MenAWY-TT-036) e o outro em adultos de 18 a 55 anos (o MenAWY-TT-035), administrou-se uma dose de ou uma dose da vacina AWY-PS. Em adolescentes e adultos, demonstrou ser imunologicamente não inferior à AWY-PS em termos de resposta. A resposta induzida por relativamente aos quatro sorogrupos meningocócicos foi similar ou mais alta do que a induzida pela vacina AWY-PS (Tabela 6). Tabela 6: Respostas de anticorpos bactericidas (medidas por rsba*) à e à vacina AWY-PS em crianças de 11 a 17 anos e adultos (idade 18 anos) um mês após a vacinação Estudo Sorogrupo vacina AWY-PS (faixa etária) RV RV A ,4% ,5% (82,1; 88.2) (5.557; 6.324) (70,9; 83,2) (2.612; 3.326) Estudo ,4% ,7% MenAWY- (95,8; 98,5) (11.939; ) (93,3; 98,7) (6.807; 9.930) TT-036 (11 a 17 W ,4% ,5% anos) (94,6; 97,7) (7.639; 8.903) (82,3; 91,6) (2.299; 3.014) Y ,8% ,5% (91,6; 95,5) (13.168; ) (72,5; 83,8) (4.463; 5.751) Estudo MenAWY- A ,1% (77,0; 82,9) (3.372; 3.897) ,8% (63,8; 75,4) (1.909; 2.370) LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 5
6 TT-035 (18 a 55 anos) W ,5% (89,4; 93,3) 90,2% (8.011; 9.812) ,0% (88,3; 94,9) 85,5% (88,1; 92,1) (4.699; 5.614) (80,9; 89,4) Y ,0% ,8% (84,6; 89,2) (7.100; 8.374) (73,6; 83,4) A análise da imunogenicidade foi conduzida na coorte ATP de imunogenicidade. RV: resposta à vacina. *Testado nos laboratórios da GlaxoSmithKline (6.297; 8.628) (2.081; 2.911) (3.782; 4.921) Em um estudo descritivo, realizado em 194 indivíduos adultos de 56 anos de idade ou mais (estudo MenAWY- TT-085), apresentou imunogenicidade, com uma taxa de resposta à vacina 63,4% e com 97,4% dos indivíduos com títulos de rsba 8, contra todos os quatro sorogrupos. Além disso, pelo menos 93,2% dos indivíduos atingiram o limite mais conservador de proteção de títulos de rsba 128. Persistência da resposta imune A persistência da resposta imune induzida por foi avaliada em mais de 48 meses após a vacinação em indivíduos com idade de 12 meses a 55 anos. onsiderando-se todos os sorogrupos (A,, W-135 e Y), a persistência dos anticorpos induzidos por foi similar ou mais alta do que a dos anticorpos induzidos pelas vacinas meningocócicas registradas [ou seja, vacina Men-RM em indivíduos com idade entre meses, vacina meningocócica quadrivalente conjugada com toxoide diftérico (DT) registrada (AWY-DT) em indivíduos com idade entre anos e a vacina AWY-PS em indivíduos com idade superior a 2 anos (Tabelas 5 a 10). Em contraste com a persistência de MenA medida por rsba observada entre as faixas etárias, quando se usou o teste com complemento humano (hsba) houve um declínio mais rápido (medido dos 12 meses pós-dose em diante) dos títulos de anticorpos bactericidas séricos contra MenA do que contra os sorogrupos, W-135 e Y (Tabelas 5, 6, 7, 8 e 10). Esse rápido declínio de anticorpos contra MenA observado no hsba também ocorreu com outras vacinas meningocócicas. A relevância clínica do rápido declínio dos títulos de anticorpos contra MenA no hsba é desconhecida (vide item 5. Advertências e Precauções). Persistência da resposta imune em crianças de 12 a 23 meses de idade: Em crianças vacinadas na idade de 12 a 23 meses, a persistência da resposta imune foi avaliada por rsba e hsba em até quatro anos no estudo MenAWY-TT-048 (Tabela 7) e em até cinco anos no estudo MenAWY- TT-032 (Tabela 8). Tabela 7: Quatro anos de dados de persistência em crianças com 12 a 23 meses de idade na ocasião da vacinação (estudo MenAWY-TT-048) Sorogrupo Resposta a: A Vacina Men-RM Timepoint (Ano) W rsba* 8 59,9% (53,7; 65,9) 74,1% (67,9; 79,7) 35,9% (30,1; 42,0) 40,4% (34,0; 47,2) 13,0% (4,9; 26,3) 35,6% (21,9; 51,2) 49,8% (43,6; 56,0) 19,3 (15,7; 23,6) 107 (77,6; 148) 9,8 (8,1; 11,7) 12,3 (9,8; 15,3) 5,7 (4,2; 7,7) 13,5 (7,4; 24,5) 24,9 (19,2; 32,4) hsba** 8 35,9% 5,8 (29,9; 42,1) (4,8; 7,0) 28,8% 4,9 (22,6; 35,6) (4,0; 6,0) 78,3% 37,8 (72,7; 83,2) (29,4; 48,6) 73,2% 32,0 (66,7; 79,1) (23,8; 43,0) 41,9% 6,2 (24,5; 60,9) (3,7; 10,3) 46,9% 11,3 (29,1; 65,3) (4,9; 25,6) 82,3% 52,0 (77,0; 86,8) (41,4; 65,2) LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 6
7 49,3% 30,5 80,6% (42,6; 56,1) (22,4; 41,5) (73,7; 86,3) 53,8% 22,3 72,0% (47,6; 60,0) (17,6; 28,4) (66,0; 77,5) Y 58,2% 36,2 65,4% (51,5; 64,7) (27,1; 48,4) (56,5; 73,5) A análise da imunogenicidade foi conduzida na coorte ATP de persistência* Teste rsba foi realizado nos laboratórios da Public Health England (PHE), no Reino Unido ** Testado nos laboratórios da GlaxoSmithKline 47,1 (35,7; 62,2) 33,2 (25,9; 42,5) 29,8 (20,2; 44,1) Tabela 8: inco anos de dados de persistência em crianças com 12 a 23 meses de idade na ocasião da vacinação (estudo MenAWU-TT-032) Timepoint rsba* 8 Grupo Resposta a: (Ano) A ,4% 35,1 (48,8; 78,1) (19,4; 63,4) ,5% 37,4 (58,9; 85,1) (22,1; 63,2) 45 97,8% (88,2; 99,9) (62,7; 192) 77,6% 48, (63,4; 88,2) (28,5; 84,0) 80,0% Vacina (44,4; 97,5) (22,6; 832) Men-RM 63,6% 26, (30,8; 89,1) (6,5; 107) 11 W ,0% 50,8 (44,3; 74,3) (24,0; 108) ,7% 18,2 (21,7; 49,6) (9,3; 35,3) 46 Y ,2% 44,9 (46,5; 76,2) (22,6; 89,3) ,9% 20,6 (28,8; 57,8) (10,9; 39,2) 45 Persistência da imunogenicidade foi analisada utilizando o ano 5 do coorte ATP. * Teste rsba foi realizado nos laboratórios da Public Health England (PHE), no Reino Unido ** Testado nos laboratórios da GlaxoSmithKline hsba** 8 52,3% (36,7; 67,5) 35,6% (21,9; 51,2) 97,8% (88,2; 99,9) 91,7% (80,0; 97,7) 70,0% (34,8; 93,3) 90,9% (58,7; 99,8) 84,4% (70,5; 93,5) 82,6% (68,6; 92,2) 87,8% (73,8; 95,9) 80,0% (65,4; 90,4) 8,8 (5,4; 14,2) 5,2 (3,4; 7,8) 370 (214; 640) 216 (124; 379) 91,9 (9,8; 859) 109 (21,2; 557) 76,9 (44,0; 134) 59,7 (35,1; 101) 74,6 (44,5; 125) 70,6 (38,7; 129) Persistência da resposta imune em crianças de 2-10 anos de idade: o estudo MenAWY-TT-088, a persistência da resposta imune foi avaliada por rsba até 44 meses depois da vacinação em crianças de 2-10 anos de idade que haviam sido imunizadas no estudo AWY-TT-081 (Tabela 9). Tabela 9: 44 meses de dados de persistência em crianças de 2-10 anos de idade na ocasião vacinação A Resposta a: Sorogrupo Timepoint rsba* hsba** 8 8 (Meses) ,5% ,6% 4,6 90 (80,9; 91,0) (144; 267) (16,9; 35,8) (3,3; 6,3) ,7% ,8% 4,8 89 (79,9; 90,4) (224; 423) (17,1; 36,2) (3,4; 6,7) ,6% 34,8 95,6% 75,9 90 (57,4; 71,3) (26,0; 46,4) (89,0; 98,8) (53,4; 108) ,0% 14, ,8% 36,4 LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 7
8 (30,1; 44,3) (10,9; 19,2) (66,2; 85,4) (23,1; 57,2) 76,8% 86,5 90,9% 82, Vacina (65,1; 86,1) (47,3; 158) (75,7; 98,1) (34,6; 196) Men-RM 45,5% 31,0 64,5% 38, (33,1; 58,2) (16,6; 58,0) (45,4; 80,8) (13,3; 113) W ,2% ,9% 69,9 86 (70,6; 82,9) (149; 307) (75,5; 91,7) (48,2; 101) ,3% ,5% 64,3 87 (61,1; 74,8) (72,5; 148) (70,6; 88,2) (42,7; 96,8) Y ,3% ,3% 79,2 91 (75,1; 86,6) (165; 314) (71,8; 88,7) (52,5; 119) ,4% 78,9 82,9% (55,1; 69,4) (54,6; 114) (72,5; 90,6) (78,0; 206) A análise da imunogenicidade foi conduzida em coorte ATP de persistência adaptado para cada time-point. * Teste rsba foi realizado nos laboratórios da Public Health England (PHE), no Reino Unido ** Testado nos laboratórios da GlaxoSmithKline Persistência da resposta imune em crianças de 6 a 10 anos de idade: o estudo MenAWY-TT-028, a persistência da resposta imune foi avaliada por hsba um ano após a vacinação em crianças de 6 a 10 anos de idade que haviam sido imunizadas no estudo MenAWY-TT-027 (Tabela 10). LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 8
9 Tabela 10: Dados obtidos um mês após a vacinação e dados de persistência um ano depois (medida por hsba*) em crianças de 6 a 10 anos de idade Um mês após a vacinação Persistência um ano depois Sorogrupo Resposta a: ,0% 53,4 16,3% 3, (71,1; 87,2) (37,3; 76,2) (9,8; 24,9) (2,7; 4,4) A 25,7% 4,1 5,7% 2,5 AWY-PS (12,5; 43,3) (2,6; 6,5) (0,7; 19,2) (1,9; 3,3) 89,1% ,2% (81,3; 94,4) (99,3; 244) (89,2; 98,4) (95,4; 176) 39,5% 13,1 32,3% 7,7 AWY-PS (24,0; 56,6) (5,4; 32,0) (16,7; 51,4) (3,5; 17,3) 95,1% % (89,0; 98,4) (99,9; 178) (96,5; 100) (218; 302) W ,3% 5,8 12,9% 3,4 AWY-PS (19,1; 52,2) (3,3; 9,9) (3,6; 29,8) (2,0; 5,8) 83,1% 95,1 99,1% (73,7; 90,2) (62,4; 145) (94,9; 100) (213; 330) Y 43,8% 12,5 33,3% 9,3 AWY-PS (26,4; 62,3) (5,6; 27,7) (18,6; 51,0) (4,3; 19,9) A análise da imunogenicidade foi conduzida na coorte ATP de persistência. * Testado nos laboratórios da GlaxoSmithKline Persistência da resposta imune em adolescentes de 11 a 17 anos de idade: o estudo MenAWY-TT-043, a persistência da resposta imune foi avaliada até quatro anos após a vacinação em adolescentes que haviam sido imunizados no estudo MenAWY-TT-036 (Tabela 11). A Tabela 4 contém os resultados primários desse último estudo. Tabela 11: Quatro anos de dados de persistência (medida por rsba*) em adolescentes com 11 a 17 anos na ocasião da vacinação Vacina AWY-PS Time-point Sorogrupo 8 8 (Ano) 92,9% ,7% (90,1; 95,1) (381; 527) (75,6; 88,4) (147; 288) A 90,3% ,8% (86,9; 93,0) (321; 466) (72,9; 87,2) (121; 251) 91,1% ,0% (88,1; 93,6) (309; 446) (79,4; 91,1) (262; 580) 94,1% ,9% (91,3; 96,2) (320; 448) (79,9; 92,2) (243; 546) 82,0% ,0% 16, (78,1; 85,4) (268; 426) (22,8; 38,0) (10,9; 23,6) W ,2% ,9% 11, (72,7; 81,3) (164; 269) (19,5; 35,4) (8,2; 16,8) 93,1% ,0% 69, (90,3; 95,3) (620; 884) (49,7; 66,0) (44,6; 109) Y 89,5% ,5% 49, (86,0; 92,3) (430; 662) (39,6; 57,4) (30,7; 80,9) A análise da imunogenicidade foi conduzida em coorte ATP de persistência adaptado para cada time-point. * Teste rsba foi realizado nos laboratórios da Public Health England (PHE), no Reino Unido LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 9
10 Persistência da resposta imune avaliada por hsba em adolescentes e adultos (11 a 25 anos): o estudo MenAWY-TT-059, a persistência da resposta imune foi avaliada por hsba um e três anos após a vacinação em adolescentes e adultos (faixa etária de 11 a 25 anos) que haviam sido imunizados no estudo MenAWY-TT-052. onsiderando-se todos os sorogrupos (A,, W-135 e Y), a persistência dos anticorpos induzidos por foi similar ou maior do que a dos anticorpos induzidos pela vacina meningocócica quadrivalente conjugada com toxoide diftérico (DT) registrada (AWY-DT) (Tabela 12). Tabela 12: Dados obtidos um mês após a vacinação e três anos de dados de persistência em adolescentes e adultos (de 11 a 25 anos) avaliados por hsba* Sorogrupo Resposta a: Time-point 8 Mês ,0% (77,6; 85,9) 58,7 (48,6; 70,9) Ano ,1% (24,4; 34,2) 5,4 (4,5; 6,4) A Ano ,3% (32,0; 42,9) 6,2 (5,2; 7,3) Mês ,1% (63,8; 81,2) 41,3 (27,7; 61,5) AWY-DT Ano ,3% (22,8; 40,7) 6,0 (4,3; 8,4) Ano ,1% (36,7; 59,6) 10,0 (6,5; 15,3) Mês ,1% (93,5; 97,9) 532 (424; 668) Ano ,9% (92,0; 97,0) 172 (142; 207) Ano ,1% (89,7; 95,6) 119 (95,5; 149) Mês ,1% (95,2; 100) 320 (220; 465) AWY-DT Ano ,3% (63,8; 81,5) 46,7 (30,2; 72,1) Ano ,5% (71,3; 89,2) 54,4 (33,8; 87,6) Mês ,0% (87,4; 93,9) 117 (96,8; 141) Ano ,5% (96,5; 99,5) 197 (173;, 225) W-135 Ano ,4% (92,5; 97,4) 144 (125; 166) Mês ,3% (65,5; 83,5) 71,9 (44,8; 115) AWY-DT Ano ,9% (66,7; 83,6) 49,5 (33,0; 74,4) Ano ,0% (75,3; 92,0) 79,4 (50,9; 124) Mês ,1% (92,3; 97,0) 246 (208; 291) Ano ,8% (95,6; 99,0) 272 (237; 311) Y Ano ,0% (93,2; 97,8) 209 (180; 243) Mês ,3% (72,8; 88,0) 104 (68,0; 158) AWY-DT Ano ,7% (79,1; 92,4) 101 (69,9; 146) Ano ,8% (79,7; 94,7) 145 (97,6; 217) A análise da imunogenicidade foi conduzida em coorte ATP de persistência adaptado para cada time-point. * Testado nos laboratórios da GlaxoSmithKline Memória imune o estudo MenAWY-TT-014, a indução de memória imune foi avaliada um mês após a administração de um quinto da dose da vacina AWY-PS (10 μg de cada polissacarídeo) a crianças no terceiro ano de vida que haviam sido imunizadas no estudo MenAWY-TT-013, aos 12 a 14 meses de idade, com ou com a vacina Men-RM registrada. Um mês após a dose de estímulo, os s induzidos nos indivíduos previamente imunizados com aumentaram 6,5 a 8 vezes relativamente aos sorogrupos A,, W-135 e Y e indicam que induz memória imune contra os quatro sorogrupos. O contra Men pós-estímulo medido por rsba foi similar nos dois grupos de estudo, indicando que induz memória imune contra o sorogrupo análoga à induzida pela vacina Men-RM registrada (Tabela 13). LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 10
11 Tabela 13: Resposta imune (medida por rsba*) um mês após vacinação de estímulo em indivíduos já imunizados aos 12 a 14 meses de idade com ou com vacina Men-RM Sorogrupo Resposta a: Pré-estímulo Pós-estímulo A (325; 911) (2.294; 4.810) (105; 289) (4.128; 8.621) Vacina 34, Men-RM (15,8; 75,3) (3.437; 8.065) W (394; 1.052) (8.587; ) Y (274; 706) (4.216; 7.806) A análise da imunogenicidade foi conduzida na coorte ATP de imunogenicidade. * Testado nos laboratórios da GlaxoSmithKline Resposta ao reforço o estudo MenAWY-TT-048, uma resposta ao reforço foi avaliada em crianças vacinadas quatro anos antes (com 12 a 23 meses de idade) no estudo MenAWY-TT-039 (Tabela 2). rianças receberam a primeira dose e o reforço da mesma vacina: ou vacina Men-RM. Um aumento significativo dos s medidos por rsba e por hsba foi observado desde a dose pré reforço até um mês após a dose de reforço da vacina (Tabela 14). Tabela 14: Dados referentes a dose pré-reforço e a dose de reforço após um mês em crianças vacinadas quatro anos antes (com 12 a 23 meses de idade) com ou com a vacina Men-RM Sorogruppoint Resposta a: Time- rsba* hsba** 8 8 A Préreforço (68,1; 80,2) (80,3; 156) (22,5; 35,9) (3,9; 5,9) 74,5% ,9% 4, Pósreforço (98,3; 100) (6389; 8053) (97,3; 100) (1119; 1612) 100% ,5% Préreforço (33,3; 46,8) (9,6; 15,2) (66,3; 79,0) (23,0; 42,2) 39,9% 12,1 73,0% 31, Pósreforço (98,3; 100) (3936; 5172) (98,3; 100) (13626; 18394) 100% % Préreforço (23,0; 53,3) (7,7; 26,5) (30,2; 66,9) (5,1; 27,6) 37,2% 14,3 48,4% 11, Vacina Men-RM Pósreforço (91,8; 100) (2596; 5326) (89,4; 100) (5887; 12699) 100% % W-135 Préreforço (41,9; 55,7) (21,9; 41,5) (74,7; 87,3) (36,5; 63,9) 48,8% 30,2 81,6% 48, Pósreforço (98,3; 100) (9531; 12579) (98,1; 100) (12972; 16010) 100% % Y Préreforço (51,3; 64,9) (27,6; 50,4) (56,8; 74,2) (20,2; 45,0) 58,2% 37,3 65,9% 30, Pósreforço (98,3; 100) (4129; 5092) (97,9; 100) (5961; 7701) 100% % A análise da imunogenicidade foi conduzida na coorte ATP de reforço para imunogenicidade * Teste rsba foi realizado nos laboratórios da Public Health England (PHE), no Reino Unido ** Testado nos laboratórios da GlaxoSmithKline LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 11
12 Imunogenicidade em indivíduos previamente imunizados com uma vacina meningocócica de polissacarídeos comum o estudo MenAWY-TT-021, conduzido em indivíduos de 4,5 a 34 anos de idade, a imunogenicidade de administrado entre 30 e 42 meses após a imunização com a vacina AWY-PS foi comparada com a imunogenicidade de administrado a indivíduos com idades equivalentes que não haviam tomado nenhuma vacina meningocócica nos dez anos anteriores. Os s medidos por rsba foram significativamente mais baixos nos indivíduos que haviam recebido uma dose da vacina AWY-PS 30 a 42 meses antes de (Tabela 15). A relevância clínica dessa observação é desconhecida, já que todos os participantes atingiram títulos 8 no rsba relativamente a todos os sorogrupos (A,, W-135 e Y). Tabela 15: Resposta imune (medida por rsba*) um mês após o uso de, de acordo com o histórico de imunização meningocócica dos indivíduos vacinados Sorogrupo Indivíduos vacinados com AWY-PS 30 a 42 meses antes Indivíduos que não haviam recebido nenhuma vacina meningocócica nos dez anos anteriores 8 8 A % % (97,5; 100) (6.045; 7.805) (94,8; 100) (10.722; ) % % (97,8; 100) (1.583; 2.391) (95,2; 100) (4.266; 7.076) W % % (97,8; 100) (3.942; 5.451) (95,2; 100) (7.088; ) Y % % (97,8; 100) (6.683; 9.104) (95,2; 100) (11.186; ) A análise da imunogenicidade foi conduzida na coorte ATP de imunogenicidade. ** Testado nos laboratórios da GlaxoSmithKline 3. ARATERÍSTIAS FARMAOLÓGIAS Os anticorpos meningocócicos anticapsulares protegem contra doenças meningocócicas por meio de eliminação bactericida mediada por complemento. induz a produção de anticorpos contra os polissacarídeos capsulares dos sorogrupos A,, W-135 e Y, conforme medido por testes que usam complemento de coelho (rsba) ou complemento humano (hsba). Ao conjugar o polissacarídeo capsular com uma proteína carreadora que contém epítopos de células T, as vacinas meningocócicas conjugadas, como, modificam a natureza da resposta imune ao polissacarídeo capsular - ou seja, a resposta passa de independente das células T para dependente das células T. 4. OTRAIDIAÇÕES não deve ser administrado a indivíduos com hipersensibilidade aos princípios ativos ou a qualquer um dos excipientes da vacina. 5. ADVERTÊIAS E PREAUÇÕES não deve, em nenhuma circunstância, ser administrado por via intravascular, intradérmica ou subcutânea. É uma norma de boas práticas clínicas que a vacinação seja precedida da avaliação do histórico clínico (principalmente com relação à imunização prévia e à possível ocorrência de efeitos indesejáveis) e do exame clínico. omo com todas as vacinas injetáveis, o tratamento médico e a supervisão médica apropriados devem sempre estar prontamente disponíveis caso ocorra um evento anafilático, que é raro, após a administração desta vacina. Doenças intercorrentes onforme recomendado na imunização com outras vacinas, deve-se adiar o uso de em indivíduos com doença febril grave aguda. A presença de infecção de menor gravidade, como um resfriado, não deve resultar no adiamento da vacinação. LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 12
13 Síncope Pode ocorrer uma síncope (desmaio) depois, ou mesmo antes, de qualquer vacinação, como resposta psicogênica à inserção da agulha. É importante que se apliquem os procedimentos necessários para evitar ferimentos decorrentes de desmaios. Trombocitopenia e distúrbios da coagulação Assim como outras vacinas de administração intramuscular, deve ser aplicado com cautela em indivíduos com trombocitopenia ou qualquer distúrbio de coagulação, nos quais há risco de sangramento após injeção intramuscular. Imunodeficiência Pode-se esperar que, em pacientes que recebem tratamento imunossupressor ou em pacientes com imunodeficiência, uma resposta imune adequada pode não ser induzida. A segurança e a imunogenicidade não foram avaliadas em pacientes com maior susceptibilidade à infecção meningocócica devido a condições como deficiências do complemento terminal e asplenia anatômica ou funcional. esses indivíduos, uma resposta imune adequada pode não ser induzida. Proteção contra doenças meningocóccicas confere proteção somente contra eisseria meningitidis dos sorogrupos A,, W-135 e Y. ão protege contra eisseria meningitidis de outros grupos. omo ocorre com qualquer vacina, pode não haver resposta imune em todos os vacinados. Respostas imunes em crianças de 12 a 14 meses de idade Um mês após a dose, crianças com idades entre meses tiveram respostas rsba semelhantes aos grupos A,, W-135 e Y após uma dose de ou duas doses de com dois meses de intervalo. Uma dose única foi associada com anticorpo bactericida sérico de complemento humano inferior (hsba) aos grupos W-135 e Y em comparação com duas doses com dois meses de intervalo. Foram observadas respostas semelhantes aos grupos A e após uma ou duas doses (ver o item "Efeitos Farmacodinâmicos"). A relevância clínica dos achados é desconhecida. Se for esperado que uma criança pequena esteja em risco particular de doença meningocócica invasiva devido à exposição aos grupos W-135 e Y, pode-se considerar a administração de uma segunda dose após um intervalo de 2 meses. Quanto à diminuição do anticorpo contra MenA ou Men após uma primeira dose de em crianças com idades entre meses, ver item Persistência de títulos de anticorpos bactericidas séricos. Persistência de títulos de anticorpos bactericidas séricos A persistência de anticorpos foi avaliada até 5 anos após a vacinação. Os estudos de persistência com mostraram uma diminuição do anticorpo bactericida sérico contra MenA ao usar o complemento humano no ensaio (hsba) (ver o item "Efeitos Farmacodinâmicos"). A relevância clínica da diminuição do anticorpo bactericida sérico hsba MenA é desconhecida. Atualmente, há informações limitadas disponíveis sobre a segurança de uma dose de reforço. o entanto, se um indivíduo estiver em risco especial de exposição a MenA e receber uma dose de aproximadamente um ano antes, pode-se considerar a administração de uma dose de reforço. Semelhante ao comparador monovalente Men, observou-se um declínio nos títulos de anticorpos ao longo do tempo. A relevância clínica dos títulos de anticorpos decrescentes é desconhecida. Uma dose de reforço pode ser considerada em indivíduos vacinados em idade de criança que permanecem em alto risco de exposição a doença meningocócica causada pelos grupos A,, W-135 e Y (ver o item "Efeitos Farmacodinâmicos"). Embora contenha toxoide tetânico, não substitui a imunização contra o tétano. Efeitos sobre a capacidade de dirigir veículos ou operar máquinas ão foram realizados estudos para avaliar os efeitos desta vacina sobre a habilidade de dirigir veículos ou operar máquinas. LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 13
14 Gravidez e lactação Gravidez A experiência no uso de em gestantes é limitada. Estudos com em animais não indicam efeitos prejudiciais diretos ou indiretos relacionados à fertilidade, à gestação, ao desenvolvimento embriofetal, ao parto ou ao desenvolvimento pós-natal. só deve ser usado durante a gravidez se isso for claramente necessário e se as possíveis vantagens superarem os riscos potenciais para o feto. Lactação ão se avaliou a segurança do uso de em mulheres que estejam amamentando. ão se sabe se é excretado no leite humano. só deve ser usado durante o aleitamento se as possíveis vantagens superarem os riscos potenciais. é um medicamento classificado na categoria de risco de gravidez. Portanto, este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgiãodentista. Esta vacina não deve ser usada por mulheres grávidas, ou que estejam amamentando, sem orientação médica ou do cirurgião dentista. 6. ITERAÇÕES MEDIAMETOSAS pode ser administrado concomitantemente com qualquer uma das seguintes: vacina contra hepatite A (HAV), vacina contra hepatite B (HBV), vacina contra sarampo, caxumba e rubéola (SR), vacina contra sarampo, caxumba, rubéola e varicela (SRV), vacina pneumocócica 10-valente conjugada, vacina contra a gripe sazonal sem adjuvante. também pode ser administrado concomitantemente com vacinas combinadas contra difteria, tétano e pertussis acelular (DTPa), ou mesmo com a combinação da DTPa com as vacinas para hepatite B, pólio inativada ou Haemophilus influenzae tipo b, como a DTPa-HBV-IPV/Hib e vacina conjugada pneumocócica 13- valente no segundo ano de vida. A segurança e a imunogenicidade de foram avaliadas após sua administração sequencial ou sua coadministração com uma vacina DTPa-HBV-IPV/Hib no segundo ano de vida. A administração de um mês após a DTPa-HBV-IPV/Hib resultou em títulos médios geométricos (s) mais baixos relativamente a MenA, Men e MenW-135 no teste bactericida do soro com complemento de coelho (rsba). A relevância clínica desse resultado é desconhecida, já que em pelo menos 99,4% dos participantes (=178) os títulos obtidos no rsba relativamente a cada sorogrupo (A,, W-135 ou Y) foram 8. Sempre que possível, deve ser coadministrado com uma vacina que contenha toxoide tetânico (TT), como a DTPa-HBV-IPV/Hib, ou administrada pelo menos um mês antes de uma vacina que contenha TT. Um mês após a coadministração de com uma vacina conjugada pneumocócica 10-valente, observouse a redução das concentrações médias geométricas (MGs) de anticorpos e dos s de anticorpos no ensaio opsonofagocítico (OPA) relativamente a um sorotipo pneumocócico (o 18, conjugado à proteína carreadora toxoide tetânico). A relevância clínica dessa observação é desconhecida. ão houve impacto da coadministração sobre os outros nove sorotipos pneumocócicos. Se tiver de ser coadministrado com outra vacina injetável, ambas devem sempre ser aplicadas em locais diferentes. omo ocorre com outras vacinas, é previsível que em pacientes que recebem tratamento com imunossupressores a vacina não induza uma resposta imune adequada. LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 14
15 7. UIDADOS DE ARMAZEAMETO DO MEDIAMETO deve ser conservado sob-refrigeração (de +2 a +8 ). ão congelar. onservar o produto na embalagem original a fim de protegê-lo da luz. O prazo de validade do medicamento é de 36 meses a partir da data de fabricação impressa na embalagem do produto. úmero do lote e datas de fabricação e validade: vide embalagem. ão use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original. Antes de usar, observe o aspecto do medicamento. Todo medicamento deve ser mantido fora do alcance das crianças. aracterísticas físicas e organolépticas: O pó da vacina é branco. O diluente é transparente e incolor. 8. POSOLOGIA E MODO DE USAR Vacinação primária Uma dose única de 0,5 ml da vacina reconstituída é usada para a imunização. Vacinação de reforço pode ser administrado em indivíduos que já tenham sido imunizados com uma vacina comum de polissacarídeos meningocócicos. ão há dados disponíveis sobre indivíduos previamente imunizados com a vacina meningocócica conjugada. deve ser usado de acordo com as recomendações oficiais disponíveis. População Pediátrica A segurança e a eficácia de em crianças com menos de 12 meses de idade não foram ainda estabelecidas. A segunda dose de pode ser considerada apropriada para alguns casos individuais (veja item 5. Advertências e Precauções). Modo de usar deve ser aplicado somente por meio de injeção intramuscular, de preferência no músculo deltoide. Em crianças de 12 a 23 meses de idade, a vacina também pode ser administrada na parte anterolateral da coxa (vide item 5. Advertências e Precauções e item 6. Interações Medicamentosas). Instruções para reconstituição da vacina com o diluente apresentado em ampola tem de ser reconstituído adicionando-se todo o diluente contido na ampola ao pó contido no frascoampola. Para fazer isso, quebre a parte superior da ampola, extraia o diluente com uma seringa e acrescente-o ao pó. A mistura deve ser bem agitada, até que o pó esteja completamente dissolvido no diluente. A vacina reconstituída é uma solução transparente e incolor. Antes da administração, deve-se inspecionar visualmente a vacina reconstituída para detecção de qualquer material particulado e/ou variação de aspecto físico. aso observe uma dessas características, descarte a vacina. Após a reconstituição, a vacina deve ser usada imediatamente. Embora esta demora não seja recomendada, foi demonstrada estabilidade por 8 horas a 30 após reconstituição. aso a vacina não seja utilizada no prazo de 8 horas, a mesma não deve ser administrada. Deve-se utilizar uma agulha nova para administrar a vacina. Instruções para reconstituição da vacina com o diluente apresentado em seringa preenchida tem de ser reconstituído adicionando-se todo o diluente contido na seringa preenchida ao pó contido no frasco-ampola. Para encaixar a agulha na seringa, consulte a ilustração abaixo. o entanto, a seringa fornecida com pode ser ligeiramente diferente daquela apresentada na ilustração. LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 15
16 1. Segurando o cilindro da seringa em uma das mãos (evite segurar o êmbolo), desatarraxe a tampa da seringa girando-a no sentido anti-horário. 2. Para encaixar a agulha, gire o encaixe da agulha na seringa no sentido horário até perceber que ele está travado (veja a figura). 3. Remova o protetor da agulha, que algumas vezes está um tanto rígido. Adicione o diluente ao pó. Feito isso, a mistura deve ser bem agitada, até que o pó esteja completamente dissolvido no diluente. A vacina reconstituída é uma solução transparente e incolor. Antes da administração, deve-se inspecionar visualmente a vacina reconstituída para detecção de qualquer material particulado e/ou variação de aspecto físico. aso observe uma dessas características, descarte a vacina. Após a reconstituição, a vacina deve ser usada imediatamente. Embora esta demora não seja recomendada, foi demonstrada estabilidade por 8 horas a 30 após reconstituição. aso a vacina não seja utilizada no prazo de 8 horas, a mesma não deve ser administrada. Deve-se utilizar uma agulha nova para administrar a vacina. É necessário descartar qualquer produto não usado ou material residual, em conformidade com a legislação local. Incompatibilidades a ausência de estudos de compatibilidade, este medicamento não deve ser misturado com outros medicamentos. 9. REAÇÕES ADVERSAS O perfil de segurança apresentado abaixo baseia-se em uma análise combinada de mais de indivíduos que receberam uma dose de em estudos clínicos. Essa análise combinada inclui dados de crianças (12 a 23 meses de idade), 909 crianças (2 e 5 anos de idade), 990 crianças (6 e 10 anos de idade), adolescentes (11 a 17 anos de idade) e adultos (18 a 55 anos de idade). o grupo de faixa etária de 12 a 14 meses que receberam 2 doses de com 2 meses de intervalo, a primeira e a segunda doses foram associadas com reactogenicidade local e sistêmica semelhante. As reações adversas relatadas são listadas abaixo de acordo com a seguinte frequência: Muito comuns: >1/10 omuns: >1/100 a <1/10 Incomuns: >1/1.000 a <1/100 Raras: >1/ a <1/1.000 Muito raras: <1/ Reações muito comuns (>1/10): perda de apetite, irritabilidade, sonolência, cefaleia, febre, inchaço, dor e rubor no local da injeção, fadiga. LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 16
17 Reações comuns (>1/100 a <1/10): sintomas gastrointestinais (incluindo diarreia, vômito e náusea), hematoma no local da injeção. Reações incomuns (>1/1.000 a <1/100): insônia, choro, hipoestesia, vertigem, prurido, rash, mialgia, dor nas extremidades, mal-estar, reação no local da injeção (incluindo induração, prurido, calor, anestesia). Dados pós-comercialização: Reação rara (>1/ a <1/1.000): Inchaço extenso no membro do local da injeção, frequentemente associada a eritema, algumas vezes envolvendo a articulação adjacente ou inchaço de todo o membro. Atenção: este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente podem ocorrer eventos imprevisíveis ou desconhecidos. esse caso, notifique os eventos adversos ao Sistema de otificações em Vigilância Sanitária OTIVISA, disponível em ou à Vigilância Sanitária Estadual ou Municipal. 10. SUPERDOSE enhum caso de superdosagem foi relatado. Em caso de intoxicação ligue para , se você precisar de mais orientações. LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 17
18 III DIZERES LEGAIS MS Farmacêutica Responsável: arolina. S. Rizoli - RF-SP º Registrado e Importado por: Laboratórios Pfizer Ltda. Rodovia Presidente astelo Branco, nº 32501, Km 32,5 EP Itapevi SP PJ nº / Fabricado por: GlaxoSmithKline Biologicals S.A. Rue de I Institut, Rixensart Bélgica OU GlaxoSmithKline Biologicals S.A. Parc de La oire Epine Rue Fleming, Wavre Bélgica Embalado por: GlaxoSmithKline Biologicals S.A. Parc de la oire Epine, Rue Fleming, Wavre Bélgica OU GlaxoSmithKline Biologicals S.A. Rue des Aulnois, Saint-Amand-Les-Eaux França VEDA SOB PRESRIÇÃO MÉDIA. Esta bula foi aprovada pela Anvisa em 12/03/2018. MXPOI_09 LLD_Bra_DS9.0_18Jul2016_v4_MXPOI_09_VPS 18
Nimenrix GlaxoSmithKline Brasil Ltda. Pó liofilizado 0,5mL
 Nimenrix GlaxoSmithKline Brasil Ltda. Pó liofilizado 0,5mL LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO. I) IDENTIFICAÇÃO DO MEDICAMENTO Nimenrix APRESENTAÇÕES Pó liofilizado para reconstituição
Nimenrix GlaxoSmithKline Brasil Ltda. Pó liofilizado 0,5mL LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO. I) IDENTIFICAÇÃO DO MEDICAMENTO Nimenrix APRESENTAÇÕES Pó liofilizado para reconstituição
VACINA PNEUMOCÓCICA 10 VALENTE (CONJUGADA) INSTITUTO DE TECNOLOGIA EM IMUNOBIOLÓGICOS BIO- MANGUINHOS / FIOCRUZ SUSPENSÃO INJETÁVEL 1DOSE
 VACINA PNEUMOCÓCICA 10 VALENTE (CONJUGADA) INSTITUTO DE TECNOLOGIA EM IMUNOBIOLÓGICOS BIO- MANGUINHOS / FIOCRUZ SUSPENSÃO INJETÁVEL 1DOSE BULA PACIENTE INFORMAÇÕES AO PACIENTE IDENTIFICAÇÃO DO MEDICAMENTO
VACINA PNEUMOCÓCICA 10 VALENTE (CONJUGADA) INSTITUTO DE TECNOLOGIA EM IMUNOBIOLÓGICOS BIO- MANGUINHOS / FIOCRUZ SUSPENSÃO INJETÁVEL 1DOSE BULA PACIENTE INFORMAÇÕES AO PACIENTE IDENTIFICAÇÃO DO MEDICAMENTO
Fluarix Tetra GlaxoSmithkline Brasil Ltda Suspensão Injetável 0,5 ml
 GlaxoSmithkline Brasil Ltda Suspensão Injetável 0,5 ml LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO. I IDENTIFICAÇÃO DO MEDICAMENTO Fluarix Tetra APRESENTAÇÃO Suspensão injetável para administração
GlaxoSmithkline Brasil Ltda Suspensão Injetável 0,5 ml LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO. I IDENTIFICAÇÃO DO MEDICAMENTO Fluarix Tetra APRESENTAÇÃO Suspensão injetável para administração
vacina tétano Sanofi-Aventis Farmacêutica Ltda. Suspensão Injetável
 vacina tétano Sanofi-Aventis Farmacêutica Ltda. Suspensão Injetável - 1 dose de 0,5mL contém: Polissacarídeo capsular Vi purificado de Salmonella typhi (cepa Ty2)... 0,025mg Modelo de Bula Página 1 de
vacina tétano Sanofi-Aventis Farmacêutica Ltda. Suspensão Injetável - 1 dose de 0,5mL contém: Polissacarídeo capsular Vi purificado de Salmonella typhi (cepa Ty2)... 0,025mg Modelo de Bula Página 1 de
FORMA FARMACÊUTICA E APRESENTAÇÃO
 1 MODELO DE BULA 1 FA x 1 dose + 1 Ser x 0,5 ml vacina Haemophilus influenzae b (conjugada) FORMA FARMACÊUTICA E APRESENTAÇÃO Pó liofilizado injetável. - Cartucho contendo 1 frasco-ampola de uma dose e
1 MODELO DE BULA 1 FA x 1 dose + 1 Ser x 0,5 ml vacina Haemophilus influenzae b (conjugada) FORMA FARMACÊUTICA E APRESENTAÇÃO Pó liofilizado injetável. - Cartucho contendo 1 frasco-ampola de uma dose e
USO INTRAMUSCULAR. USO ADULTO E PEDIÁTRICO (CRIANÇAS A PARTIR DE 9 ANOS DE IDADE).
 I IDENTIFICAÇÃO DO MEDICAMENTO APRESENTAÇÕES Suspensão injetável para administração intramuscular. Embalagem que contém 1 seringa preenchida com 0,5 ml. USO INTRAMUSCULAR. USO ADULTO E PEDIÁTRICO (CRIANÇAS
I IDENTIFICAÇÃO DO MEDICAMENTO APRESENTAÇÕES Suspensão injetável para administração intramuscular. Embalagem que contém 1 seringa preenchida com 0,5 ml. USO INTRAMUSCULAR. USO ADULTO E PEDIÁTRICO (CRIANÇAS
FluQuadri vacina influenza tetravalente (fragmentada, inativada)
 Página 1 de 6 FluQuadri vacina influenza tetravalente (fragmentada, inativada) CEPAS 2016 - Hemisfério Sul FORMA FARMACÊUTICA E APRESENTAÇÃO Suspensão para injeção. - Cartucho com 5 seringas preenchidas
Página 1 de 6 FluQuadri vacina influenza tetravalente (fragmentada, inativada) CEPAS 2016 - Hemisfério Sul FORMA FARMACÊUTICA E APRESENTAÇÃO Suspensão para injeção. - Cartucho com 5 seringas preenchidas
Conjugado de Streptococcus pneumoniae tipo 14 e proteína D de Haemophilus influenzae (proporção média PD/PS:
 LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO I - IDENTIFICAÇÃO DO MEDICAMENTO vacina pneumocócica 10-valente (conjugada) APRESENTAÇÃO Suspensão injetável para administração intramuscular. Apresentada
LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO I - IDENTIFICAÇÃO DO MEDICAMENTO vacina pneumocócica 10-valente (conjugada) APRESENTAÇÃO Suspensão injetável para administração intramuscular. Apresentada
CALENDÁRIO DE VACINAÇÃO DA REDE PÚBLICA DE SANTA CATARINA Última atualização em 05 de janeiro de 2016
 Grupo alvo Idade BCG Hepatite B (1) VIP e VOP (10) Pentavalente Pneumo 10 Rotavírus (2) Meningo C Hepatite A Febre Amarela (3) Tríplice Viral (4) Tetraviral (5) HPV dtpa (8) Influenza (gripe) (9) Dupla
Grupo alvo Idade BCG Hepatite B (1) VIP e VOP (10) Pentavalente Pneumo 10 Rotavírus (2) Meningo C Hepatite A Febre Amarela (3) Tríplice Viral (4) Tetraviral (5) HPV dtpa (8) Influenza (gripe) (9) Dupla
Modelo de texto de bula Profissional de Saúde Menveo
 I IDENTIFICAÇÃO DO MEDICAMENTO vacina meningocócica ACWY (conjugada) APRESENTAÇÃO A vacina é apresentada sob a forma de um pó liofilizado e um diluente para solução injetável e está disponível em embalagens
I IDENTIFICAÇÃO DO MEDICAMENTO vacina meningocócica ACWY (conjugada) APRESENTAÇÃO A vacina é apresentada sob a forma de um pó liofilizado e um diluente para solução injetável e está disponível em embalagens
Vacina adsorvida meningocócica C (conjugada)
 Vacina adsorvida meningocócica C (conjugada) vacina adsorvida meningocócica C (conjugada) Novartis Biociências S.A. Suspensão injetável (10mcg/0,5mL + diluente 0,6mL) TEXTO DE BULA VACINA ADSORVIDA MENINGOCÓCICA
Vacina adsorvida meningocócica C (conjugada) vacina adsorvida meningocócica C (conjugada) Novartis Biociências S.A. Suspensão injetável (10mcg/0,5mL + diluente 0,6mL) TEXTO DE BULA VACINA ADSORVIDA MENINGOCÓCICA
Menjugate - Suspensão injetável Vacina adsorvida meningocócica C (conjugada) Modelo de texto de bula Profissional de Saúde
 Menjugate - Suspensão injetável Modelo de texto de bula Profissional de Saúde I IDENTIFICAÇÃO DO MEDICAMENTO Menjugate vacina adsorvida meningocócica C (conjugada) APRESENTAÇÕES Menjugate é apresentada
Menjugate - Suspensão injetável Modelo de texto de bula Profissional de Saúde I IDENTIFICAÇÃO DO MEDICAMENTO Menjugate vacina adsorvida meningocócica C (conjugada) APRESENTAÇÕES Menjugate é apresentada
Dra. Tatiana C. Lawrence PEDIATRIA, ALERGIA E IMUNOLOGIA
 Vacinação As vacinas são as ferramentas mais poderosas e inofensivas que temos para combater as doenças. Protegem milhões de crianças e adultos das doenças que ameaçam nossas vidas, como poliomielite (paralisia
Vacinação As vacinas são as ferramentas mais poderosas e inofensivas que temos para combater as doenças. Protegem milhões de crianças e adultos das doenças que ameaçam nossas vidas, como poliomielite (paralisia
Vacina adsorvida hepatite A (inativada) GlaxoSmithKline Brasil Ltda. Suspensão injetável 0,5 ml ou 1,0 ml
 Vacina adsorvida hepatite A (inativada) GlaxoSmithKline Brasil Ltda. Suspensão injetável 0,5 ml ou 1,0 ml LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO I IDENTIFICAÇÃO DO MEDICAMENTO vacina
Vacina adsorvida hepatite A (inativada) GlaxoSmithKline Brasil Ltda. Suspensão injetável 0,5 ml ou 1,0 ml LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO I IDENTIFICAÇÃO DO MEDICAMENTO vacina
1. PARA QUE ESTE MEDICAMENTO É INDICADO?
 SYNAGIS palivizumabe I - IDENTIFICAÇÃO DO MEDICAMENTO APRESENTAÇÕES Pó liófilo injetável de: - 50 mg em embalagem com 01 frasco-ampola para dose única contendo palivizumabe na forma de pó liofilizado estéril
SYNAGIS palivizumabe I - IDENTIFICAÇÃO DO MEDICAMENTO APRESENTAÇÕES Pó liófilo injetável de: - 50 mg em embalagem com 01 frasco-ampola para dose única contendo palivizumabe na forma de pó liofilizado estéril
Modelo de texto de bula Profissional de Saúde Bexsero TM
 I IDENTIFICAÇÃO DO MEDICAMENTO vacina adsorvida meningocócica B (recombinante) APRESENTAÇÃO A vacina é uma suspensão injetável, disponível em seringa preenchida de vidro Tipo I, com êmbolo e tampa protetora
I IDENTIFICAÇÃO DO MEDICAMENTO vacina adsorvida meningocócica B (recombinante) APRESENTAÇÃO A vacina é uma suspensão injetável, disponível em seringa preenchida de vidro Tipo I, com êmbolo e tampa protetora
VACINA MENINGOCÓCICA ACWY (CONJUGADA) Novartis Biociências S.A. Pó liofilizado e Diluente para Solução Injetável 10 MCG + 5 MCG + 5 MCG + 5 MCG
 VACINA MENINGOCÓCICA ACWY (CONJUGADA) Novartis Biociências S.A. Pó liofilizado e Diluente para Solução Injetável 10 MCG + 5 MCG + 5 MCG + 5 MCG 1 VACINA MENINGOCÓCICA ACWY (CONJUGADA) APRESENTAÇÕES A vacina
VACINA MENINGOCÓCICA ACWY (CONJUGADA) Novartis Biociências S.A. Pó liofilizado e Diluente para Solução Injetável 10 MCG + 5 MCG + 5 MCG + 5 MCG 1 VACINA MENINGOCÓCICA ACWY (CONJUGADA) APRESENTAÇÕES A vacina
Vacina combinada contra hepatite A e B r-dna inativada
 I) Identificação do medicamento FORMAS FARMACÊUTICAS E APRESENTAÇÕES USO ADULTO E PEDIÁTRICO Suspensão injetável para administração intramuscular A Vacina contra HA e HB r-dna inativada é uma vacina formulada
I) Identificação do medicamento FORMAS FARMACÊUTICAS E APRESENTAÇÕES USO ADULTO E PEDIÁTRICO Suspensão injetável para administração intramuscular A Vacina contra HA e HB r-dna inativada é uma vacina formulada
Vacina combinada contra difteria-tétano-pertussis acelular, pólio inativado e Haemophilus influenzae tipo b (DTPa-IPV+Hib)
 Vacina combinada contra difteria-tétano-pertussis acelular, pólio inativado e I) Identificação do medicamento Vacina combinada contra difteria-tétano-pertussis acelular, pólio inativado e Haemophilus influenzae
Vacina combinada contra difteria-tétano-pertussis acelular, pólio inativado e I) Identificação do medicamento Vacina combinada contra difteria-tétano-pertussis acelular, pólio inativado e Haemophilus influenzae
Menjugate Vacina adsorvida meningocócica C (conjugada) Modelo de texto de bula Profissional de Saúde
 Modelo de texto de bula Profissional de Saúde I IDENTIFICAÇÃO DO MEDICAMENTO Menjugate vacina adsorvida meningocócica C (conjugada) APRESENTAÇÕES Cartucho com 01 frasco-ampola (vidro tipo I), com vedação
Modelo de texto de bula Profissional de Saúde I IDENTIFICAÇÃO DO MEDICAMENTO Menjugate vacina adsorvida meningocócica C (conjugada) APRESENTAÇÕES Cartucho com 01 frasco-ampola (vidro tipo I), com vedação
Modelo de Bula Pneumo23 Página 1 de 7. vacina pneumocócica 23-valente (polissacarídica)
 Modelo de Bula Pneumo23 Página 1 de 7 vacina pneumocócica 23-valente (polissacarídica) FORMA FARMACÊUTICA E APRESENTAÇÕES: Solução injetável. - Cartucho com uma seringa contendo uma dose de 0,5mL. - Cartucho
Modelo de Bula Pneumo23 Página 1 de 7 vacina pneumocócica 23-valente (polissacarídica) FORMA FARMACÊUTICA E APRESENTAÇÕES: Solução injetável. - Cartucho com uma seringa contendo uma dose de 0,5mL. - Cartucho
PREVENAR 13 vacina pneumocócica 13-valente (conjugada)
 PREVENAR 13 vacina pneumocócica 13-valente (conjugada) Wyeth Indústria Farmacêutica Ltda. Suspensão injetável 0,5 ml PREVENAR 13 VACINA PNEUMOCÓCICA 13-VALENTE (CONJUGADA) I - IDENTIFICAÇÃO DO MEDICAMENTO
PREVENAR 13 vacina pneumocócica 13-valente (conjugada) Wyeth Indústria Farmacêutica Ltda. Suspensão injetável 0,5 ml PREVENAR 13 VACINA PNEUMOCÓCICA 13-VALENTE (CONJUGADA) I - IDENTIFICAÇÃO DO MEDICAMENTO
vacina hepatite B (recombinante)
 vacina hepatite B (recombinante) FORMA FARMACÊUTICA E APRESENTAÇÕES Suspensão injetável - Cartucho contendo 1 frasco-ampola com 1 dose de 0,5mL; - Cartucho contendo 20 frascos-ampola com 1 dose de 0,5mL;
vacina hepatite B (recombinante) FORMA FARMACÊUTICA E APRESENTAÇÕES Suspensão injetável - Cartucho contendo 1 frasco-ampola com 1 dose de 0,5mL; - Cartucho contendo 20 frascos-ampola com 1 dose de 0,5mL;
BACTRONEO. (mupirocina)
 BACTRONEO (mupirocina) Brainfarma Indústria Química e Farmacêutica S.A. Pomada Dermatológica 20mg/g I - IDENTIFICAÇÃO DO MEDICAMENTO: BACTRONEO mupirocina APRESENTAÇÕES Pomada dermatológica com 2% de mupirocina
BACTRONEO (mupirocina) Brainfarma Indústria Química e Farmacêutica S.A. Pomada Dermatológica 20mg/g I - IDENTIFICAÇÃO DO MEDICAMENTO: BACTRONEO mupirocina APRESENTAÇÕES Pomada dermatológica com 2% de mupirocina
vacina adsorvida meningocócica C (conjugada)
 vacina adsorvida meningocócica C (conjugada) pó liofilizado injetável + solução diluente 10 mcg + 0,8 ml 0,5 ml (1 dose) Importado e Embalado por: FUNED Fundação Ezequiel Dias Fabricado por: NOVARTIS Novartis
vacina adsorvida meningocócica C (conjugada) pó liofilizado injetável + solução diluente 10 mcg + 0,8 ml 0,5 ml (1 dose) Importado e Embalado por: FUNED Fundação Ezequiel Dias Fabricado por: NOVARTIS Novartis
KITNOS. Comprimido. 500 mg
 KITNOS Comprimido 500 mg KITNOS etofamida I - IDENTIFICAÇÃO DO MEDICAMENTO: Nome comercial: Kitnos Nome genérico: etofamida APRESENTAÇÃO Kitnos comprimidos de 500 mg em embalagem contendo 6 comprimidos.
KITNOS Comprimido 500 mg KITNOS etofamida I - IDENTIFICAÇÃO DO MEDICAMENTO: Nome comercial: Kitnos Nome genérico: etofamida APRESENTAÇÃO Kitnos comprimidos de 500 mg em embalagem contendo 6 comprimidos.
Calendário. ideal para Adolecentes
 Calendário SBP - So c i e d a d e Br a s i l e i r a d e Pediatria ideal para Adolecentes D e p a r t a m e n t o d e In f e c t o l o g i a d a SBP Calendário de Vacinação para Crianças - 2008 Idade Vacina
Calendário SBP - So c i e d a d e Br a s i l e i r a d e Pediatria ideal para Adolecentes D e p a r t a m e n t o d e In f e c t o l o g i a d a SBP Calendário de Vacinação para Crianças - 2008 Idade Vacina
vacina adsorvida difteria, tétano, pertussis (acelular) e poliomielite 1, 2 e 3 (inativada) reforço (dtpa-ipv [reforço])
![vacina adsorvida difteria, tétano, pertussis (acelular) e poliomielite 1, 2 e 3 (inativada) reforço (dtpa-ipv [reforço]) vacina adsorvida difteria, tétano, pertussis (acelular) e poliomielite 1, 2 e 3 (inativada) reforço (dtpa-ipv [reforço])](/thumbs/48/24062579.jpg) vacina adsorvida difteria, tétano, pertussis (acelular) e poliomielite 1, 2 e 3 (inativada) reforço - (dtpa-ipv [reforço]) Modelo de texto de bula - profissional de saúde LEIA ATENTAMENTE ESTA BULA ANTES
vacina adsorvida difteria, tétano, pertussis (acelular) e poliomielite 1, 2 e 3 (inativada) reforço - (dtpa-ipv [reforço]) Modelo de texto de bula - profissional de saúde LEIA ATENTAMENTE ESTA BULA ANTES
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 5 1. NOME DO MEDICAMENTO VETERINÁRIO PORCILIS APP, suspensão injetável para suínos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada dose de 2 ml contém:
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 5 1. NOME DO MEDICAMENTO VETERINÁRIO PORCILIS APP, suspensão injetável para suínos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada dose de 2 ml contém:
CLORIDRATO DE BROMEXINA
 CLORIDRATO DE BROMEXINA Geolab Indústria Farmacêutica S/A Xarope infantil 4mg/5mL Xarope adulto 8mg/5mL Você não deve usar o cloridrato de bromexina se tiver alergia a bromexina (substância ativa) ou
CLORIDRATO DE BROMEXINA Geolab Indústria Farmacêutica S/A Xarope infantil 4mg/5mL Xarope adulto 8mg/5mL Você não deve usar o cloridrato de bromexina se tiver alergia a bromexina (substância ativa) ou
Este medicamento é contraindicado para uso por pacientes com alterações hepáticas ou renais graves.
 IDENTIFICAÇÃO DO MEDICAMENTO Fluibron A cloridrato de ambroxol APRESENTAÇÕES Solução para nebulização. Cada flaconete contém 7,5 mg/ml de cloridrato de ambroxol. Embalagem com 10 flaconetes contendo 2
IDENTIFICAÇÃO DO MEDICAMENTO Fluibron A cloridrato de ambroxol APRESENTAÇÕES Solução para nebulização. Cada flaconete contém 7,5 mg/ml de cloridrato de ambroxol. Embalagem com 10 flaconetes contendo 2
VACINA PNEUMOCÓCICA 10 VALENTE (CONJUGADA) INSTITUTO DE TECNOLOGIA EM IMUNOBIOLÓGICOS BIO- MANGUINHOS / FIOCRUZ SUSPENSÃO INJETÁVEL 1DOSE
 VACINA PNEUMOCÓCICA 10 VALENTE (CONJUGADA) INSTITUTO DE TECNOLOGIA EM IMUNOBIOLÓGICOS BIO- MANGUINHOS / FIOCRUZ SUSPENSÃO INJETÁVEL 1DOSE I)IDENTIFICAÇÃO DO MEDICAMENTO VACINA PNEUMOCÓCICA 10-VALENTE (CONJUGADA)
VACINA PNEUMOCÓCICA 10 VALENTE (CONJUGADA) INSTITUTO DE TECNOLOGIA EM IMUNOBIOLÓGICOS BIO- MANGUINHOS / FIOCRUZ SUSPENSÃO INJETÁVEL 1DOSE I)IDENTIFICAÇÃO DO MEDICAMENTO VACINA PNEUMOCÓCICA 10-VALENTE (CONJUGADA)
Vacina adsorvida difteria, tétano, pertussis (acelular), hepatite B (recombinante), poliomielite 1, 2, 3 (inativada) e Haemophilus influenzae b
 Vacina adsorvida difteria, tétano, pertussis (acelular), hepatite B (recombinante), poliomielite 1, 2, 3 (inativada) e Haemophilus influenzae b (conjugada) GlaxoSmithKline Brasil Ltda. Pó liófilo injetável
Vacina adsorvida difteria, tétano, pertussis (acelular), hepatite B (recombinante), poliomielite 1, 2, 3 (inativada) e Haemophilus influenzae b (conjugada) GlaxoSmithKline Brasil Ltda. Pó liófilo injetável
Tetanogamma. (imunoglobulina humana antitétano) CSL Behring Comércio de Produtos Farmacêuticos Ltda. Solução injetável 250 UI/mL
 Tetanogamma (imunoglobulina humana antitétano) CSL Behring Comércio de Produtos Farmacêuticos Ltda. Solução injetável 250 UI/mL IDENTIFICAÇÃO DO MEDICAMENTO Tetanogamma imunoglobulina humana antitétano
Tetanogamma (imunoglobulina humana antitétano) CSL Behring Comércio de Produtos Farmacêuticos Ltda. Solução injetável 250 UI/mL IDENTIFICAÇÃO DO MEDICAMENTO Tetanogamma imunoglobulina humana antitétano
Dropropizina. Prati-Donaduzzi Xarope 1,5 mg/ml e 3 mg/ml. Dropropizina_bula_paciente
 Dropropizina Prati-Donaduzzi 1,5 mg/ml e 3 mg/ml Dropropizina_bula_paciente INFORMAÇÕES AO PACIENTE dropropizina Medicamento genérico Lei n 9.787, de 1999 APRESENTAÇÕES de 1,5 mg/ml ou 3 mg/ml em embalagem
Dropropizina Prati-Donaduzzi 1,5 mg/ml e 3 mg/ml Dropropizina_bula_paciente INFORMAÇÕES AO PACIENTE dropropizina Medicamento genérico Lei n 9.787, de 1999 APRESENTAÇÕES de 1,5 mg/ml ou 3 mg/ml em embalagem
BLAUIMUNO. Blau Farmacêutica S.A. Pó Injetável 0,6 g, 3,0 g e 9,0 g. Blau Farmacêutica S/A.
 BLAUIMUNO Blau Farmacêutica S.A. Pó Injetável 0,6 g, 3,0 g e 9,0 g MODELO DE BULA PACIENTE RDC 47/09 BLAUIMUNO imunoglobulina humana APRESENTAÇÕES Pó injetável. Embalagens contendo 1 frasco-ampola de 0,6
BLAUIMUNO Blau Farmacêutica S.A. Pó Injetável 0,6 g, 3,0 g e 9,0 g MODELO DE BULA PACIENTE RDC 47/09 BLAUIMUNO imunoglobulina humana APRESENTAÇÕES Pó injetável. Embalagens contendo 1 frasco-ampola de 0,6
LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO.
 LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO. I IDENTIFICAÇÃO DO MEDICAMENTO Benlysta belimumabe APRESENTAÇÃO Pó liofilizado para solução para infusão intravenosa. Benlysta é apresentado em
LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO. I IDENTIFICAÇÃO DO MEDICAMENTO Benlysta belimumabe APRESENTAÇÃO Pó liofilizado para solução para infusão intravenosa. Benlysta é apresentado em
Excipientes: sorbitol, ácido acético glacial, hidróxido de sódio e água para injetáveis...
 XGEVA denosumabe APRESENTAÇÃO Solução injetável 120 mg em embalagens com 1 frasco-ampola de 1,7 ml. USO SUBCUTÂNEO USO ADULTO COMPOSIÇÃO Cada 1,7 ml contém: denosumabe... Excipientes: sorbitol, ácido acético
XGEVA denosumabe APRESENTAÇÃO Solução injetável 120 mg em embalagens com 1 frasco-ampola de 1,7 ml. USO SUBCUTÂNEO USO ADULTO COMPOSIÇÃO Cada 1,7 ml contém: denosumabe... Excipientes: sorbitol, ácido acético
Nome do medicamento: LUFTAL MAX. Forma farmacêutica: cápsulas. Concentrações: 125 mg
 Nome do medicamento: LUFTAL MAX Forma farmacêutica: cápsulas Concentrações: 125 mg APRESENTAÇÕES Cápsulas gelatinosas de 125 mg em embalagem com 10 cápsulas. USO ORAL USO ADULTO COMPOSIÇÃO Cada cápsula
Nome do medicamento: LUFTAL MAX Forma farmacêutica: cápsulas Concentrações: 125 mg APRESENTAÇÕES Cápsulas gelatinosas de 125 mg em embalagem com 10 cápsulas. USO ORAL USO ADULTO COMPOSIÇÃO Cada cápsula
CALENDÁRIO DE VACINAÇÃO PARA O ESTADO DE SÃO PAULO
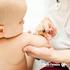 CALENDÁRIO DE VACINAÇÃO PARA O ESTADO DE SÃO PAULO - 2016 IDADE VACINAS A PARTIR DO NASCIMENTO BCG 1 2 3 2 MESES ROTAVÍRUS 4 3 MESES MENINGOCÓCICA C 3 4 MESES ROTAVÍRUS 5 5 MESES MENINGOCÓCICA C 6 MESES
CALENDÁRIO DE VACINAÇÃO PARA O ESTADO DE SÃO PAULO - 2016 IDADE VACINAS A PARTIR DO NASCIMENTO BCG 1 2 3 2 MESES ROTAVÍRUS 4 3 MESES MENINGOCÓCICA C 3 4 MESES ROTAVÍRUS 5 5 MESES MENINGOCÓCICA C 6 MESES
Imunizações Prof. Orlando A. Pereira FCM - Unifenas
 Imunizações Prof. Orlando A. Pereira FCM - Unifenas Imunização ativa A imunização ativa é realizada pela introdução no organismo de diferentes tipos de antígenos, representados tanto por cepas vivas e
Imunizações Prof. Orlando A. Pereira FCM - Unifenas Imunização ativa A imunização ativa é realizada pela introdução no organismo de diferentes tipos de antígenos, representados tanto por cepas vivas e
Rotarix vacina rotavírus humano G1P[8] (atenuada) Modelo de texto de bula Profissional de Saúde
![Rotarix vacina rotavírus humano G1P[8] (atenuada) Modelo de texto de bula Profissional de Saúde Rotarix vacina rotavírus humano G1P[8] (atenuada) Modelo de texto de bula Profissional de Saúde](/thumbs/50/27117762.jpg) I - IDENTIFICAÇÃO DO MEDICAMENTO Rotarix Cepa RIX4414 (vírus vivos atenuados) APRESENTAÇÃO Suspensão oral. Rotarix é apresentada em embalagem com 1 seringa para administração oral, contendo 1 dose. USO
I - IDENTIFICAÇÃO DO MEDICAMENTO Rotarix Cepa RIX4414 (vírus vivos atenuados) APRESENTAÇÃO Suspensão oral. Rotarix é apresentada em embalagem com 1 seringa para administração oral, contendo 1 dose. USO
Calendário de Vacinação da Criança
 Calendário de Vacinação da Criança Calendário Nacional de Vacinação da Criança (PNI) - 2016 (1) BCG - ID Administrar dose única, o mais precocemente possível, preferencialmente nas primeiras 12 horas após
Calendário de Vacinação da Criança Calendário Nacional de Vacinação da Criança (PNI) - 2016 (1) BCG - ID Administrar dose única, o mais precocemente possível, preferencialmente nas primeiras 12 horas após
Synflorix GlaxoSmithKline Brasil Ltda. Suspensão injetável 0,5mL
 Synflorix GlaxoSmithKline Brasil Ltda. Suspensão injetável 0,5mL I - IDENTIFICAÇÃO DO MEDICAMENTO vacina pneumocócica 10-valente (conjugada) APRESENTAÇÃO Suspensão injetável para administração intramuscular.
Synflorix GlaxoSmithKline Brasil Ltda. Suspensão injetável 0,5mL I - IDENTIFICAÇÃO DO MEDICAMENTO vacina pneumocócica 10-valente (conjugada) APRESENTAÇÃO Suspensão injetável para administração intramuscular.
ESTA PALESTRA NÃO PODERÁ SER REPRODUZIDA SEM A REFERÊNCIA DO AUTOR
 ESTA PALESTRA NÃO PODERÁ SER REPRODUZIDA SEM A REFERÊNCIA DO AUTOR Workshop do Programa Nacional de Imunização IV Encontro de Enfermagem em Hematologia e Hemoterapia Secretaria da Saúde do Estado do Ceará
ESTA PALESTRA NÃO PODERÁ SER REPRODUZIDA SEM A REFERÊNCIA DO AUTOR Workshop do Programa Nacional de Imunização IV Encontro de Enfermagem em Hematologia e Hemoterapia Secretaria da Saúde do Estado do Ceará
ADACEL. Sanofi-Aventis Farmacêutica Ltda. Suspensão Injetável
 ADACEL Sanofi-Aventis Farmacêutica Ltda. Suspensão Injetável 1 dose de 0,5mL contém: Toxoide diftérico... 2,0 UI* (2Lf) Toxoide tetânico... 20,0 UI* (5Lf) Toxoide pertussis...2,5 µg Hemaglutinina filamentosa...5,0
ADACEL Sanofi-Aventis Farmacêutica Ltda. Suspensão Injetável 1 dose de 0,5mL contém: Toxoide diftérico... 2,0 UI* (2Lf) Toxoide tetânico... 20,0 UI* (5Lf) Toxoide pertussis...2,5 µg Hemaglutinina filamentosa...5,0
Incorporação do Palivizumabe para Imunização contra o vírus sincicial respiratório (VSR)
 Incorporação do Palivizumabe para Imunização contra o vírus sincicial respiratório (VSR) O vírus sincicial respiratório (VSR) é um dos principais agentes etiológicos envolvidos nas infecções respiratórias
Incorporação do Palivizumabe para Imunização contra o vírus sincicial respiratório (VSR) O vírus sincicial respiratório (VSR) é um dos principais agentes etiológicos envolvidos nas infecções respiratórias
Infanrix Penta GlaxoSmithKline Brasil Ltda. Pó liofilizado 0,5 ml
 GlaxoSmithKline Brasil Ltda. Pó liofilizado 0,5 ml LEIA ESTA BULA ATENTAMENTE ANTES DE INICIAR O TRATAMENTO. I - IDENTIFICAÇÃO DO MEDICAMENTO Infanrix Penta vacina adsorvida difteria, tétano, pertussis
GlaxoSmithKline Brasil Ltda. Pó liofilizado 0,5 ml LEIA ESTA BULA ATENTAMENTE ANTES DE INICIAR O TRATAMENTO. I - IDENTIFICAÇÃO DO MEDICAMENTO Infanrix Penta vacina adsorvida difteria, tétano, pertussis
Modelo de texto de bula profissional de saúde vacina sarampo, caxumba, rubéola e varicela (atenuada)
 LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO I) IDENTIFICAÇÃO DO MEDICAMENTO APRESENTAÇÕES Pó liofilizado para reconstituição com diluente para administração subcutânea. Embalagens com: 1 ou
LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO I) IDENTIFICAÇÃO DO MEDICAMENTO APRESENTAÇÕES Pó liofilizado para reconstituição com diluente para administração subcutânea. Embalagens com: 1 ou
APRESENTAÇÃO - LUFTAL
 LUFTAL BULA PARA O PACIENTE LUFTAL comprimidos e gotas LUFTAL simeticona ATENÇÃO: O NOME DA SUBSTÂNCIA ATIVA DE LUFTAL FOI MODIFICADO DE DIMETICONA PARA SIMETICONA. A QUALIDADE, SEGURANÇA E EFICÁCIA DO
LUFTAL BULA PARA O PACIENTE LUFTAL comprimidos e gotas LUFTAL simeticona ATENÇÃO: O NOME DA SUBSTÂNCIA ATIVA DE LUFTAL FOI MODIFICADO DE DIMETICONA PARA SIMETICONA. A QUALIDADE, SEGURANÇA E EFICÁCIA DO
Vacina de Rotavírus Humano Vivo Atenuado
 cepa RIX4414 (vírus atenuados) I ) Identificação do medicamento FORMAS FARMACÊUTICAS E APRESENTAÇÕES USO PEDIÁTRICO Suspensão oral. A VACINA DE ROTAVÍRUS HUMANO VIVO ATENUADO é apresentada em embalagens
cepa RIX4414 (vírus atenuados) I ) Identificação do medicamento FORMAS FARMACÊUTICAS E APRESENTAÇÕES USO PEDIÁTRICO Suspensão oral. A VACINA DE ROTAVÍRUS HUMANO VIVO ATENUADO é apresentada em embalagens
IDENTIFICAÇÃO DO MEDICAMENTO - Tylenol Bebê Suspensão Oral. FORMAS FARMACÊUTICAS E APRESENTAÇÕES - Tylenol Bebê Suspensão Oral
 Tylenol Bebê Suspensão Oral IDENTIFICAÇÃO DO MEDICAMENTO - Tylenol Bebê Suspensão Oral FORMAS FARMACÊUTICAS E APRESENTAÇÕES - Tylenol Bebê Suspensão Oral TYLENOL Bebê Suspensão Oral Concentrada 100 mg/ml
Tylenol Bebê Suspensão Oral IDENTIFICAÇÃO DO MEDICAMENTO - Tylenol Bebê Suspensão Oral FORMAS FARMACÊUTICAS E APRESENTAÇÕES - Tylenol Bebê Suspensão Oral TYLENOL Bebê Suspensão Oral Concentrada 100 mg/ml
MODELO DE BULA (Profissionais de Saúde)
 MODELO DE BULA (Profissionais de Saúde) CPHD SMP 35 FRAÇÃO ÁCIDA cloreto de sódio + cloreto de potássio + associações APRESENTAÇÃO E FORMA FARMACÊUTICA Solução para hemodiálise bombona plástica de 5 ou
MODELO DE BULA (Profissionais de Saúde) CPHD SMP 35 FRAÇÃO ÁCIDA cloreto de sódio + cloreto de potássio + associações APRESENTAÇÃO E FORMA FARMACÊUTICA Solução para hemodiálise bombona plástica de 5 ou
vacina poliomielite 1, 2 e 3 (inativada)
 vacina poliomielite 1, 2 e 3 (inativada) Sanofi-Aventis Farmacêutica Ltda. Solução injetável Cada 1 dose de 0,5mL contém: Poliovírus inativados do tipo 1... 40 unidades de antígeno UD* Poliovírus inativados
vacina poliomielite 1, 2 e 3 (inativada) Sanofi-Aventis Farmacêutica Ltda. Solução injetável Cada 1 dose de 0,5mL contém: Poliovírus inativados do tipo 1... 40 unidades de antígeno UD* Poliovírus inativados
CALENDÁRIO DE VACINAÇÃO CRIANÇA ATÉ 6 ANOS DE IDADE
 CALENDÁRIO DE VACINAÇÃO CRIANÇA ATÉ 6 ANOS DE IDADE CALENDÁRIO DE VACINAÇÃO CRIANÇA ATÉ 6 ANOS DE IDADE 2013 IDADE VACINA A PARTIR DO NASCIMENTO 2 MESES BCG 1 HEPATITE B 2 VACINA VIP 3 PENTAVALENTE 7 ROTAVÍRUS
CALENDÁRIO DE VACINAÇÃO CRIANÇA ATÉ 6 ANOS DE IDADE CALENDÁRIO DE VACINAÇÃO CRIANÇA ATÉ 6 ANOS DE IDADE 2013 IDADE VACINA A PARTIR DO NASCIMENTO 2 MESES BCG 1 HEPATITE B 2 VACINA VIP 3 PENTAVALENTE 7 ROTAVÍRUS
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 18 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO VETERINÁRIO Bovilis BVD Suspensão injetável para bovinos 2. COMPOSIÇÃO
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 18 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO VETERINÁRIO Bovilis BVD Suspensão injetável para bovinos 2. COMPOSIÇÃO
VISAZUL. (cloridrato de nafazolina + fenolsulfonato de zinco + sulfato de berberina)
 VISAZUL (cloridrato de nafazolina + fenolsulfonato de zinco + sulfato de berberina) Brainfarma Indústria Química e Farmacêutica S.A. Solução Gotas 0,5mg/mL + 1,0mg/mL + 0,025mg/mL I - IDENTIFICAÇÃO DO
VISAZUL (cloridrato de nafazolina + fenolsulfonato de zinco + sulfato de berberina) Brainfarma Indústria Química e Farmacêutica S.A. Solução Gotas 0,5mg/mL + 1,0mg/mL + 0,025mg/mL I - IDENTIFICAÇÃO DO
UNTRAL (biotina) Aché Laboratórios Farmacêuticos S.A. cápsula 2,5 mg
 UNTRAL (biotina) Aché Laboratórios Farmacêuticos S.A. cápsula 2,5 mg BULA PARA O PACIENTE Bula de acordo com a Resolução-RDC nº 47/2009 I- IDENTIFICAÇÃO DO MEDICAMENTO UNTRAL biotina APRESENTAÇÕES Cápsulas
UNTRAL (biotina) Aché Laboratórios Farmacêuticos S.A. cápsula 2,5 mg BULA PARA O PACIENTE Bula de acordo com a Resolução-RDC nº 47/2009 I- IDENTIFICAÇÃO DO MEDICAMENTO UNTRAL biotina APRESENTAÇÕES Cápsulas
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 14 1. NOME DO MEDICAMENTO VETERINÁRIO Porcilis Glässer, suspensão injetável para suínos. 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Por dose de 2 ml:
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 14 1. NOME DO MEDICAMENTO VETERINÁRIO Porcilis Glässer, suspensão injetável para suínos. 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Por dose de 2 ml:
CPHD Bicabonato de Sódio 8,4%
 CPHD Bicabonato de Sódio 8,4% Fresenius Medical Care Ltda Solução para Hemodiálise 8,4% MODELO DE BULA (Profissionais de Saúde) CPHD BICARBONATO DE SÓDIO 8,4% bicarbonato de sódio FRAÇÃO BÁSICA APRESENTAÇÃO
CPHD Bicabonato de Sódio 8,4% Fresenius Medical Care Ltda Solução para Hemodiálise 8,4% MODELO DE BULA (Profissionais de Saúde) CPHD BICARBONATO DE SÓDIO 8,4% bicarbonato de sódio FRAÇÃO BÁSICA APRESENTAÇÃO
APRESENTAÇÃO Spray nasal - solução de cloreto de sódio 0,9% - Embalagem contendo 100 ml.
 Maresis Solução de cloreto de sódio 0,9% - estéril APRESENTAÇÃO Spray nasal - solução de cloreto de sódio 0,9% - Embalagem contendo 100 ml. VIA NASAL USO ADULTO E PEDIÁTRICO COMPOSIÇÃO Cada um ml de spray
Maresis Solução de cloreto de sódio 0,9% - estéril APRESENTAÇÃO Spray nasal - solução de cloreto de sódio 0,9% - Embalagem contendo 100 ml. VIA NASAL USO ADULTO E PEDIÁTRICO COMPOSIÇÃO Cada um ml de spray
Infanrix Hexa Vacina DTPa-HB-IPV+Hib Modelo de texto de bula Profissional de Saúde
 LEIA ESTA BULA ATENTAMENTE ANTES DE INICIAR O TRATAMENTO. I - IDENTIFICAÇÃO DO MEDICAMENTO Infanrix Hexa vacina adsorvida difteria, tétano, pertussis (acelular), hepatite B (recombinante), poliomielite
LEIA ESTA BULA ATENTAMENTE ANTES DE INICIAR O TRATAMENTO. I - IDENTIFICAÇÃO DO MEDICAMENTO Infanrix Hexa vacina adsorvida difteria, tétano, pertussis (acelular), hepatite B (recombinante), poliomielite
Projeto Diretrizes. Elaboração Final: de Julho Outubro de 2001 de 2002
 Vacina Conjugada Tratamento Contra da Fase Neisseria Aguda do Acidente Meningitidis Vascular Sorogrupo Cerebral C Academia Sociedade Brasileira de de Neurologia Pediatria Elaboração Final: 24 31 de Julho
Vacina Conjugada Tratamento Contra da Fase Neisseria Aguda do Acidente Meningitidis Vascular Sorogrupo Cerebral C Academia Sociedade Brasileira de de Neurologia Pediatria Elaboração Final: 24 31 de Julho
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 18 1. NOME DO MEDICAMENTO VETERINÁRIO PORCILIS APP, suspensão injetável para suínos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada dose de 2 ml contém:
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 18 1. NOME DO MEDICAMENTO VETERINÁRIO PORCILIS APP, suspensão injetável para suínos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada dose de 2 ml contém:
BULA PACIENTE. MARESIS Solução de cloreto de sódio 0,9% - estéril. Jato Forte
 BULA PACIENTE MARESIS Solução de cloreto de sódio 0,9% - estéril Jato Forte APRESENTAÇÃO: Spray nasal em jato contínuo - solução de cloreto de sódio 0,9% - embalagem contendo um frasco spray com 100 ml
BULA PACIENTE MARESIS Solução de cloreto de sódio 0,9% - estéril Jato Forte APRESENTAÇÃO: Spray nasal em jato contínuo - solução de cloreto de sódio 0,9% - embalagem contendo um frasco spray com 100 ml
PAXORAL. (lisado bacteriano)
 PAXORAL (lisado bacteriano) Cosmed Indústria de Cosméticos e Medicamentos S.A. Cápsula 3,5 mg e 7,0 mg I - IDENTIFICAÇÃO DO MEDICAMENTO: PAXORAL lisado bacteriano APRESENTAÇÕES Cápsula gelatinosa dura
PAXORAL (lisado bacteriano) Cosmed Indústria de Cosméticos e Medicamentos S.A. Cápsula 3,5 mg e 7,0 mg I - IDENTIFICAÇÃO DO MEDICAMENTO: PAXORAL lisado bacteriano APRESENTAÇÕES Cápsula gelatinosa dura
Varilrix vacina varicela (atenuada) Modelo de texto de bula - profissional de saúde LEIA ESTA BULA ATENTAMENTE ANTES DE INICIAR O TRATAMENTO.
 Modelo de texto de bula - profissional de saúde LEIA ESTA BULA ATENTAMENTE ANTES DE INICIAR O TRATAMENTO. I) IDENTIFICAÇÃO DO MEDICAMENTO Varilrix APRESENTAÇÕES Pó liófilo injetável + diluente para administração
Modelo de texto de bula - profissional de saúde LEIA ESTA BULA ATENTAMENTE ANTES DE INICIAR O TRATAMENTO. I) IDENTIFICAÇÃO DO MEDICAMENTO Varilrix APRESENTAÇÕES Pó liófilo injetável + diluente para administração
cloridrato de tansulosina
 cloridrato de tansulosina Sandoz do Brasil Ind. Farm. Ltda. Cápsula gelatinosa dura de liberação prolongada 0,4 mg 1 I) IDENTIFICAÇÃO DO MEDICAMENTO cloridrato de tansulosina Medicamento genérico Lei n
cloridrato de tansulosina Sandoz do Brasil Ind. Farm. Ltda. Cápsula gelatinosa dura de liberação prolongada 0,4 mg 1 I) IDENTIFICAÇÃO DO MEDICAMENTO cloridrato de tansulosina Medicamento genérico Lei n
Infanrix Hexa Vacina DTPa-HB-IPV+Hib Modelo de texto de bula Profissional de Saúde
 LEIA ESTA BULA ATENTAMENTE ANTES DE INICIAR O TRATAMENTO. I - IDENTIFICAÇÃO DO MEDICAMENTO Infanrix Hexa vacina adsorvida difteria, tétano, pertussis (acelular), hepatite B (recombinante), poliomielite
LEIA ESTA BULA ATENTAMENTE ANTES DE INICIAR O TRATAMENTO. I - IDENTIFICAÇÃO DO MEDICAMENTO Infanrix Hexa vacina adsorvida difteria, tétano, pertussis (acelular), hepatite B (recombinante), poliomielite
Excipientes: hidróxido de alumínio, fosfato de alumínio, cloreto de sódio e água para injeção.
 LEIA ESTA BULA ATENTAMENTE ANTES DE INICIAR O TRATAMENTO. I - IDENTIFICAÇÃO DO MEDICAMENTO Twinrix APRESENTAÇÃO Twinrix, suspensão injetável, é apresentada em embalagem com 1 seringa preenchida de vidro
LEIA ESTA BULA ATENTAMENTE ANTES DE INICIAR O TRATAMENTO. I - IDENTIFICAÇÃO DO MEDICAMENTO Twinrix APRESENTAÇÃO Twinrix, suspensão injetável, é apresentada em embalagem com 1 seringa preenchida de vidro
Ascarizole. (cloridrato de levamisol) Laboratório Globo Ltda. Comprimidos 80 mg e 150 mg
 Ascarizole (cloridrato de levamisol) Laboratório Globo Ltda. Comprimidos 80 mg e 150 mg Ascarizole cloridrato de levamisol FORMA FARMACÊUTICA E APRESENTAÇÕES: Comprimido de 80 mg (crianças). Embalagem
Ascarizole (cloridrato de levamisol) Laboratório Globo Ltda. Comprimidos 80 mg e 150 mg Ascarizole cloridrato de levamisol FORMA FARMACÊUTICA E APRESENTAÇÕES: Comprimido de 80 mg (crianças). Embalagem
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 14 1. NOME DO MEDICAMENTO VETERINÁRIO Nobilis Ma5 + Clone 30 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Por dose: Substâncias ativas: Vírus vivo da Bronquite
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 14 1. NOME DO MEDICAMENTO VETERINÁRIO Nobilis Ma5 + Clone 30 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Por dose: Substâncias ativas: Vírus vivo da Bronquite
VACINA SARAMPO, CAXUMBA E RUBÉOLA INSTITUTO DE TECNOLOGIA EM IMUNOBIOLÓGICOS BIO- MANGUINHOS / FIOCRUZ PÓ LIOFILIZADO INJETÁVEL + SOLUÇÃO DILUENTE
 VACINA SARAMPO, CAXUMBA E RUBÉOLA INSTITUTO DE TECNOLOGIA EM IMUNOBIOLÓGICOS BIO- MANGUINHOS / FIOCRUZ PÓ LIOFILIZADO INJETÁVEL + SOLUÇÃO DILUENTE 10 DOSES BULA PARA O PROFISSIONAL DE SAÚDE I) IDENTIFICAÇÃO
VACINA SARAMPO, CAXUMBA E RUBÉOLA INSTITUTO DE TECNOLOGIA EM IMUNOBIOLÓGICOS BIO- MANGUINHOS / FIOCRUZ PÓ LIOFILIZADO INJETÁVEL + SOLUÇÃO DILUENTE 10 DOSES BULA PARA O PROFISSIONAL DE SAÚDE I) IDENTIFICAÇÃO
CALENDÁRIO VACINAL Superintendência de Vigilância em Saúde Gerência de Imunizações e Rede de Frio
 CALENDÁRIO VACINAL 2016 Superintendência de Vigilância em Saúde Gerência de Imunizações e Rede de Frio CALENDÁRIO VACINAL 2016 Historicamente, diversos calendários de vacinação foram propostos em função
CALENDÁRIO VACINAL 2016 Superintendência de Vigilância em Saúde Gerência de Imunizações e Rede de Frio CALENDÁRIO VACINAL 2016 Historicamente, diversos calendários de vacinação foram propostos em função
Cartucho com 1 estojo contendo 1 seringa preenchida com dose única de 0,5 ml e 1 agulha.
 I) IDENTIFICAÇÃO DO MEDICAMENTO Suspensão injetável SOMENTE USO INTRAMUSCULAR APRESENTAÇÃO Cartucho com 1 estojo contendo 1 seringa preenchida com dose única de 0,5 ml e 1 agulha. USO PEDIÁTRICO COMPOSIÇÃO
I) IDENTIFICAÇÃO DO MEDICAMENTO Suspensão injetável SOMENTE USO INTRAMUSCULAR APRESENTAÇÃO Cartucho com 1 estojo contendo 1 seringa preenchida com dose única de 0,5 ml e 1 agulha. USO PEDIÁTRICO COMPOSIÇÃO
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 16 1. NOME DO MEDICAMENTO VETERINÁRIO Nobivac DHPPi, suspensão injetável para cães (cachorros). 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Por
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 16 1. NOME DO MEDICAMENTO VETERINÁRIO Nobivac DHPPi, suspensão injetável para cães (cachorros). 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Por
Visual Sandoz do Brasil Ind. Farm. Ltda. solução oftálmica cloridrato de nafazolina 0,15 mg/ml + sulfato de zinco heptaidratado 0,3 mg/ml
 Visual Sandoz do Brasil Ind. Farm. Ltda. solução oftálmica cloridrato de nafazolina 0,15 mg/ml + sulfato de zinco heptaidratado 0,3 mg/ml I) IDENTIFICAÇÃO DO MEDICAMENTO Visual cloridrato de nafazolina
Visual Sandoz do Brasil Ind. Farm. Ltda. solução oftálmica cloridrato de nafazolina 0,15 mg/ml + sulfato de zinco heptaidratado 0,3 mg/ml I) IDENTIFICAÇÃO DO MEDICAMENTO Visual cloridrato de nafazolina
Ministério da Saúde Gabinete do Ministro PORTARIA Nº 1.946, DE 19 DE JULHO DE 2010
 Ministério da Saúde Gabinete do Ministro PORTARIA Nº 1.946, DE 19 DE JULHO DE 2010 Institui, em todo o território nacional, o Calendário de Vacinação para os Povos Indígenas. O MINISTRO DE ESTADO DA SAÚDE,
Ministério da Saúde Gabinete do Ministro PORTARIA Nº 1.946, DE 19 DE JULHO DE 2010 Institui, em todo o território nacional, o Calendário de Vacinação para os Povos Indígenas. O MINISTRO DE ESTADO DA SAÚDE,
Paracetamol. Prati-Donaduzzi Comprimido e Comprimido revestido 500 mg e 750 mg. Paracetamol_bula_paciente
 Paracetamol Prati-Donaduzzi Comprimido e Comprimido revestido 500 mg e 750 mg Paracetamol_bula_paciente INFORMAÇÕES AO PACIENTE paracetamol Medicamento genérico Lei n 9.787, de 1999 APRESENTAÇÕES Comprimido
Paracetamol Prati-Donaduzzi Comprimido e Comprimido revestido 500 mg e 750 mg Paracetamol_bula_paciente INFORMAÇÕES AO PACIENTE paracetamol Medicamento genérico Lei n 9.787, de 1999 APRESENTAÇÕES Comprimido
BIO-MANGUINHOS / FIOCRUZ SUSPENSÃO ORAL 1 DOSE
 VACINA ROTAVÍRUS HUMANO G1P[8] (ATENUADA) INSTITUTO DE TECNOLOGIA EM IMUNOBIOLÓGICOS BIO-MANGUINHOS / FIOCRUZ SUSPENSÃO ORAL 1 DOSE BULA PROFISSIONAL DE SAÚDE I - IDENTIFICAÇÃO DO MEDICAMENTO Cepa RIX4414
VACINA ROTAVÍRUS HUMANO G1P[8] (ATENUADA) INSTITUTO DE TECNOLOGIA EM IMUNOBIOLÓGICOS BIO-MANGUINHOS / FIOCRUZ SUSPENSÃO ORAL 1 DOSE BULA PROFISSIONAL DE SAÚDE I - IDENTIFICAÇÃO DO MEDICAMENTO Cepa RIX4414
COLTRAX INJ tiocolchicosídeo
 Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. COLTRAX INJ tiocolchicosídeo SANOFI-AVENTIS FORMAS FARMACÊUTICAS E APRESENTAÇÕES Solução Injetável -
Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. COLTRAX INJ tiocolchicosídeo SANOFI-AVENTIS FORMAS FARMACÊUTICAS E APRESENTAÇÕES Solução Injetável -
Engerix B vacina hepatite B (recombinante) Modelo de texto de bula - profissional de saúde I IDENTIFICAÇÃO DO MEDICAMENTO
 I IDENTIFICAÇÃO DO MEDICAMENTO Engerix B APRESENTAÇÕES Engerix B é apresentada em 1 seringa monodose de 10 mcg/0,5 ml ou 20 mcg/1,0ml. USO INTRAMUSCULAR USO ADULTO E PEDIÁTRICO COMPOSIÇÃO Cada dose da
I IDENTIFICAÇÃO DO MEDICAMENTO Engerix B APRESENTAÇÕES Engerix B é apresentada em 1 seringa monodose de 10 mcg/0,5 ml ou 20 mcg/1,0ml. USO INTRAMUSCULAR USO ADULTO E PEDIÁTRICO COMPOSIÇÃO Cada dose da
Vacina combinada contra difteria-tétano-pertussis acelular, hepatite B r-dna, pólio inativada e Haemophilus influenzae tipo b (DTPa-HB-IPV+Hib)
 MODELO DE BULA Vacina combinada contra difteria-tétano-pertussis acelular, hepatite B r-dna, pólio inativada e Haemophilus influenzae tipo b (DTPa-HB-IPV+Hib) Descrição: DTPa-HB-IPV+Hib contém toxóide
MODELO DE BULA Vacina combinada contra difteria-tétano-pertussis acelular, hepatite B r-dna, pólio inativada e Haemophilus influenzae tipo b (DTPa-HB-IPV+Hib) Descrição: DTPa-HB-IPV+Hib contém toxóide
FORMA FARMACÊUTICA E APRESENTAÇÃO Solução otológica - Frasco com 10 ml, provido de conta-gotas.
 Lidosporin lidocaína 43,4 mg/ml sulfato de polimixina B 10.000 UI/ml Solução otológica FORMA FARMACÊUTICA E APRESENTAÇÃO Solução otológica - Frasco com 10 ml, provido de conta-gotas. USO ADULTO E PEDIÁTRICO
Lidosporin lidocaína 43,4 mg/ml sulfato de polimixina B 10.000 UI/ml Solução otológica FORMA FARMACÊUTICA E APRESENTAÇÃO Solução otológica - Frasco com 10 ml, provido de conta-gotas. USO ADULTO E PEDIÁTRICO
NORIPURUM. Takeda Pharma Ltda. Solução injetável. 50 mg/ml. Página 19 de 24
 NORIPURUM Takeda Pharma Ltda. Solução injetável 50 mg/ml Página 19 de 24 APRESENTAÇÕES Solução injetável 50 mg/ml. Embalagem contendo cinco ampolas de 2 ml e cinco agulhas longas de 5 cm. USO INTRAMUSCULAR
NORIPURUM Takeda Pharma Ltda. Solução injetável 50 mg/ml Página 19 de 24 APRESENTAÇÕES Solução injetável 50 mg/ml. Embalagem contendo cinco ampolas de 2 ml e cinco agulhas longas de 5 cm. USO INTRAMUSCULAR
CLORIDRATO DE AMBROXOL. Biosintética Farmacêutica Ltda. xarope 5mg/5mL 30mg/5mL
 CLORIDRATO DE AMBROXOL Biosintética Farmacêutica Ltda. xarope 5mg/5mL 30mg/5mL BULA PARA PACIENTE Bula de acordo com a Resolução-RDC nº 47/2009 CLORIDRATO DE AMBROXOL Medicamento genérico Lei nº 9.787,
CLORIDRATO DE AMBROXOL Biosintética Farmacêutica Ltda. xarope 5mg/5mL 30mg/5mL BULA PARA PACIENTE Bula de acordo com a Resolução-RDC nº 47/2009 CLORIDRATO DE AMBROXOL Medicamento genérico Lei nº 9.787,
INSTRUÇÃO NORMATIVA CALENDÁRIO NACIONAL DE VACINAÇÃO ADAPTAÇÃO: NÚCLEO DE IMUNIZAÇÕES/DVE/CEVS/SES
 INSTRUÇÃO NORMATIVA CALENDÁRIO NACIONAL DE VACINAÇÃO ADAPTAÇÃO: NÚCLEO DE IMUNIZAÇÕES/DVE/CEVS/SES Porto Alegre, janeiro de 2016 INSTRUÇÃO NORMATIVA CALENDÁRIO NACIONAL DE VACINAÇÃO ADAPTAÇÃO RIO GRANDE
INSTRUÇÃO NORMATIVA CALENDÁRIO NACIONAL DE VACINAÇÃO ADAPTAÇÃO: NÚCLEO DE IMUNIZAÇÕES/DVE/CEVS/SES Porto Alegre, janeiro de 2016 INSTRUÇÃO NORMATIVA CALENDÁRIO NACIONAL DE VACINAÇÃO ADAPTAÇÃO RIO GRANDE
Protovit Plus. Bayer S.A. Solução oral. Polivitamínico sem minerais
 Protovit Plus Bayer S.A. Solução oral Polivitamínico sem minerais Protovit Plus polivitamínico APRESENTAÇÃO Solução oral. Embalagem contendo 1 frasco de 20 ml. USO ORAL USO PEDIÁTRICO COMPOSIÇÃO Cada ml
Protovit Plus Bayer S.A. Solução oral Polivitamínico sem minerais Protovit Plus polivitamínico APRESENTAÇÃO Solução oral. Embalagem contendo 1 frasco de 20 ml. USO ORAL USO PEDIÁTRICO COMPOSIÇÃO Cada ml
Simeco Plus. Bula para paciente. Suspensão. 600mg+300mg+35mg
 Simeco Plus Bula para paciente Suspensão 600mg+300mg+35mg Simeco plus (hidróxido de alumínio + hidróxido de magnésio + simeticona) Suspensão FORMAS FARMACÊUTICAS E APRESENTAÇÕES Embalagens com frascos
Simeco Plus Bula para paciente Suspensão 600mg+300mg+35mg Simeco plus (hidróxido de alumínio + hidróxido de magnésio + simeticona) Suspensão FORMAS FARMACÊUTICAS E APRESENTAÇÕES Embalagens com frascos
CALCIOFAR (FOSFATO DE CÁLCIO TRIBÁSICO, CIANOCOBALAMINA, COLECALCIFEROL, FLUORETO DE SÓDIO) BELFAR LTDA SUSPENSÃO ORAL
 CALCIOFAR (FOSFATO DE CÁLCIO TRIBÁSICO, CIANOCOBALAMINA, COLECALCIFEROL, FLUORETO DE SÓDIO) BELFAR LTDA SUSPENSÃO ORAL 30mg/mL + 3mcg/mL + 15UI/mL + 0,1mg/mL CALCIOFAR Fosfato de cálcio tribásico, cianocobalamina,
CALCIOFAR (FOSFATO DE CÁLCIO TRIBÁSICO, CIANOCOBALAMINA, COLECALCIFEROL, FLUORETO DE SÓDIO) BELFAR LTDA SUSPENSÃO ORAL 30mg/mL + 3mcg/mL + 15UI/mL + 0,1mg/mL CALCIOFAR Fosfato de cálcio tribásico, cianocobalamina,
COLÍRIO MOURA BRASIL Sanofi-Aventis Farmacêutica Ltda. Solução Oftálmica 0,15 MG/ML de cloridrato de nafazolina 0,3 MG/ML de sulfato de zinco
 COLÍRIO MOURA BRASIL Solução Oftálmica 0,15 MG/ML de cloridrato de nafazolina 0,3 MG/ML de sulfato de zinco heptaidratado Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar
COLÍRIO MOURA BRASIL Solução Oftálmica 0,15 MG/ML de cloridrato de nafazolina 0,3 MG/ML de sulfato de zinco heptaidratado Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar
paracetamol Multilab Ind. e Com. de Produtos Farmacêuticos Ltda comprimido revestido 500 mg e 750 mg Bula Paciente REV.A Page 1
 paracetamol Multilab Ind. e Com. de Produtos Farmacêuticos Ltda comprimido revestido 500 mg e 750 mg Bula Paciente REV.A Page 1 paracetamol Medicamento genérico Lei nº 9.787, de 1999 FORMA FARMACÊUTICA
paracetamol Multilab Ind. e Com. de Produtos Farmacêuticos Ltda comprimido revestido 500 mg e 750 mg Bula Paciente REV.A Page 1 paracetamol Medicamento genérico Lei nº 9.787, de 1999 FORMA FARMACÊUTICA
Azelan. Bayer S.A. Creme dermatológico 200 mg/g Gel 150 mg/g
 Azelan Bayer S.A. Creme dermatológico 200 mg/g Gel 150 mg/g Azelan ácido azelaico APRESENTAÇÕES Creme dermatológico 200 mg/g: cartucho contendo bisnaga com 30 g de creme. Gel 150 mg/g: cartucho contendo
Azelan Bayer S.A. Creme dermatológico 200 mg/g Gel 150 mg/g Azelan ácido azelaico APRESENTAÇÕES Creme dermatológico 200 mg/g: cartucho contendo bisnaga com 30 g de creme. Gel 150 mg/g: cartucho contendo
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 21 1. NOME DO MEDICAMENTO VETERINÁRIO Porcilis PRRS Liofilizado e solvente para suspensão injetável para suínos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 21 1. NOME DO MEDICAMENTO VETERINÁRIO Porcilis PRRS Liofilizado e solvente para suspensão injetável para suínos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
Dose: 3 gotas ao dia UI 150% 125% 750 UI 250% 250%
 AD-VITAM Vitamina A (acetato de retinol); Vitamina D (colecalciferol) FORMA FARMACÊUTICA Solução oral - gotas APRESENTAÇÕES Linha Farma: Frasco com gotejador contendo 20 ml. USO ORAL USO ADULTO E PEDIÁTRICO
AD-VITAM Vitamina A (acetato de retinol); Vitamina D (colecalciferol) FORMA FARMACÊUTICA Solução oral - gotas APRESENTAÇÕES Linha Farma: Frasco com gotejador contendo 20 ml. USO ORAL USO ADULTO E PEDIÁTRICO
tobramicina Brainfarma Indústria Química e Farmacêutica S.A. Solução Gotas 3mg/mL
 tobramicina Brainfarma Indústria Química e Farmacêutica S.A. Solução Gotas 3mg/mL I - IDENTIFICAÇÃO DO MEDICAMENTO: tobramicina Medicamento genérico Lei nº 9.787, de 1999. APRESENTAÇÃO Solução Gotas Embalagem
tobramicina Brainfarma Indústria Química e Farmacêutica S.A. Solução Gotas 3mg/mL I - IDENTIFICAÇÃO DO MEDICAMENTO: tobramicina Medicamento genérico Lei nº 9.787, de 1999. APRESENTAÇÃO Solução Gotas Embalagem
FLORATIL (Saccharomyces boulardii) Merck S/A Cápsulas 100 & 200 mg
 FLORATIL (Saccharomyces boulardii) Merck S/A Cápsulas 100 & 200 mg APRESENTAÇÕES Cápsulas de gelatina. Floratil 100 mg - Embalagem contendo 12 cápsulas. Floratil 200 mg - Embalagem contendo 6 cápsulas.
FLORATIL (Saccharomyces boulardii) Merck S/A Cápsulas 100 & 200 mg APRESENTAÇÕES Cápsulas de gelatina. Floratil 100 mg - Embalagem contendo 12 cápsulas. Floratil 200 mg - Embalagem contendo 6 cápsulas.
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 AEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMETO 1 Este medicamento está sujeito a monitorização adicional. Isto irá permitir a rápida identificação de nova informação de segurança. Pede-se aos profissionais
AEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMETO 1 Este medicamento está sujeito a monitorização adicional. Isto irá permitir a rápida identificação de nova informação de segurança. Pede-se aos profissionais
