CINÉTICA DA OXICOMBUSTÃO DO CARVÃO DA MINA DE CANDIOTA RS COM ALTO TEOR DE CINZAS
|
|
|
- Sara Figueira Ramalho
- 7 Há anos
- Visualizações:
Transcrição
1 CINÉTICA DA OXICOMBUSTÃO DO CARVÃO DA MINA DE CANDIOTA RS COM ALTO TEOR DE CINZAS K. G. P. NUNES 1, P. J. MELO 1, E. OSÓRIO 2, N. R. MARCÍLIO 1 1 Universidade Federal do Rio Grande do Sul, Departamento de Engenharia Química 2 Universidade Federal do Rio Grande do Sul, Departamento de Minas, Metalúrgica e Materiais keilagpn@gmail.com RESUMO O trabalho apresenta o estudo cinético da reação de oxicombustão do carvão mineral extraído da mina de Candiota/RS, com alto teor de cinzas. Na tecnologia da oxicombustão a queima ocorre com uma mistura de O 2 com alto teor de CO 2. Os experimentos foram realizados em termobalança nas temperaturas de 600 C a 900 C, em pressão atmosférica, com concentrações de O 2 variando entre 10 e 30 % v/v em CO 2. Primeiramente, se determinou a temperatura de pirólise do carvão a fim de eliminar os compostos voláteis, evitando assim a sua influência na reação de oxicombustão. Os resultados experimentais foram tratados matematicamente com modelos retirados da literatura para determinação dos parâmetros cinéticos, como energia de ativação e ordem de reação. 1. INTRODUÇÃO O Brasil é responsável pelo lançamento de 2 bilhões de toneladas de CO 2 na atmosfera anualmente. Esse índice corresponde a 5 % das emissões mundiais desse gás, deixando o Brasil entre os 5 países que mais poluem (BEN, 2013). As emissões de CO 2 correspondem a 80 % do total dos gases emitidos, por isso as pesquisas para a captura o e armazenamento se concentram sobre esse gás (IEA, 2013). A oxicombustão de carvão mineral vem sendo estudada como alternativa tecnológica devido à facilidade de captação integral de CO 2 resultante da combustão, bem como a captação de outros poluentes, de forma a permitir seu uso de forma pouco nociva ao meio. A técnica consiste na utilização de uma corrente de oxigênio diluído pelos gases exaustos reciclados como comburente, produzindo um gás rico em CO 2, facilitando assim a sua captura (TOFTEGAARD et al., 2010). No Brasil, o estudo cinético da gaseificação de carvão iniciou na década de 1980 com Schmal et al. (1982) e José H. J. (1989). Atualmente, as pesquisas sobre oxicombustão estão direcionadas a caracterização, modelagem e análise cinética em leito fluidizado (DUAN et al, 2014; LECKNER, et al. 2014; ROY and BHATTACHARYA, 2014). A aquisição permanente de dados sobre a combustão do carvão mineral nessa nova condição de operação é necessária para o dimensionamento ou adaptação de equipamentos a uma Área temática: Engenharia de Reações Químicas e Catálise 1
2 forma de produção energética mais limpa, acompanhando a evolução das legislações ambientais cada vez mais restritivas quanto uso de combustíveis fósseis. O alto teor de cinzas presente nos carvões brasileiros faz com que os processos de beneficiamento tenham custo elevado especialmente para seu uso energético. Como representam a maior reserva energética do Brasil, é constante a busca por processos cada vez mais eficientes, técnica e economicamente, para seu uso energético. O carvão utilizado para o estudo termogravimétrico em condições de oxicombustão foi coletado da mina de Candiota, localizada no município de Candiota no Rio Grande do Sul. Os experimentos foram realizados utilizando concentrações de O 2 em CO 2 entre 10 % e 30 % e temperaturas variando de 600 C a 900 C. 2. MATERIAIS E MÉTODOS 2.1. Produção de char O char, produto da desvolatilização do carvão na ausência de ar, foi preparado em atmosfera de N 2, a partir de três faixas granulométricas de carvão: A (0,5 a 0,85 mm), B (0,85 a 1,00 mm) e C (1,68 a 2,00 mm). Diferentes granulometrias foram utilizadas para que fosse observado o efeito dessas no tamanho dos poros e na área superficial do char. Cerca de 150 g foram colocadas em um reator de aço inox, descrito em Nunes e Marcílio (2012). A amostra permaneceu 60 minutos na temperatura pré-determinada. Utilizaram-se duas temperaturas para desvolatilização, 880 C e 900 C para observar a quantidade de matéria volátil remanescente no char e seu possível efeito sobre a estrutura do char produzido. Com base nesses resultados selecionou-se a temperatura para as reações de oxicombustão. As amostras produzidas foram submetidas às análises imediata, elementar, diâmetro de poro e área superficial. Os resultados se encontram na Tabela Oxicombustão Os experimentos de oxicombustão do char foram conduzidos em uma termobalança a pressão atmosférica, utilizando-se aproximadamente 30 mg de char num cadinho tipo prato. Um termopar localizado abaixo do prato monitorava a temperatura, que variou de 600 a 900 C. Os gases utilizados nos experimentos foram introduzidos na termobalança a uma taxa de 125 ml.min. -1, com concentrações de O 2 em CO 2 variando de 10 a 30 %. A conversão X do char foi calculada segundo a equação 1. X = M i M M i M C (1) Onde M i representa a massa inicial de char (mg), M a massa instantânea (mg), M c a massa Área temática: Engenharia de Reações Químicas e Catálise 2
3 após a reação de oxicombustão (mg). Para o tratamento e discussão dos dados cinéticos obtidos utilizou-se o modelo matemático do núcleo não reagido, que considera que a reação se inicia na superfície externa à partícula e se move em direção ao centro do sólido deixando para trás uma camada de sólido inerte, ou seja, as cinzas. A equação matemática em função da conversão ao longo do tempo será apresentada durante a discussão dos resultados. 3. RESULTADOS E DISCUSSÕES 3.1. Efeito da temperatura de pirólise Uma amostra contendo cerca de 3 kg de carvão beneficiado foi submetida a análise imediata e elementar e sua composição encontra-se na Tabela 1. Tabela 1 Composição do carvão Análises Teores (%) Análise imediata¹ Matéria volátil 21,1 Cinzas 52,8 Carbono fixo 26,1 Análise elementar 2 C 74,85 N 1,50 S 3,40 H 8,25 O 12,00 ¹ base seca 2 base seca isenta de cinzas (dados a serem confirmados) Para avaliar o efeito da estrutura do char após a pirólise, utilizaram-se duas temperaturas. Com as faixas granulométricas A e C procedeu-se a pirólise a 900 C e com a faixa granulométrica B, a desvolatilização ocorreu a 880 C. Os teores de matéria volátil remanescente nas amostras, a área superficial e o diâmetro do poro resultante encontram-se na Tabela 2. Tabela 2: Caracterização dos chars produzidos com diferentes temperaturas Char Temperatura Granulometria Matéria volátil Área superficial Diâmetro do poro ( C) (mm) (%) BET (m².g -¹ ) (nm) A 900 0,5 0,85 1,23 95,852 1,091 B 880 0,85-1,00 1,47 91,818 1,024 C 900 1,68 2,00 1,34 94,114 0,970 Observando os resultados apresentados na Tabela 2, para uma mesma temperatura de pirólise, o teor de matéria volátil liberado é ligeiramente maior para um char de granulometria Área temática: Engenharia de Reações Químicas e Catálise 3
4 inferior. Também é possível observar que partículas menores tem maior área superficial e poros com diâmetros maiores disponíveis para reação. O efeito da matéria volátil presente no char durante a oxicombustão é mais pronunciado quando observamos seu comportamento em termobalança, como é mostrado na Figura 1. 1,0 0,8 0,6 0,4 0,50-0,85 mm 0,85-1,00 mm 0,2 1,68-2,00 mm 0,0 0,0 2,0 4,0 6,0 8,0 tempo (min) Figura 1 Taxa de conversão para as granulometrias A, B e C com 10 % de O 2 em CO 2. conversão Nesta figura observa-se que os chars pirolisados a 900 C, apresentam uma alta taxa de conversão, enquanto que o char pirolisado a 880 C, por ainda possuir uma maior quantidade de matéria volátil no seu interior, reage mais lentamente nas condições de oxicombustão. Com base no resultado apresentado, selecionou-se a granulometria A (0,50 0,85 mm) para dar continuidade aos ensaios termogravimétricos em condição de oxicombustão. Ao utilizar uma partícula de menor tamanho minimizam-se os efeitos difusivos, podendo considerar para fins de cálculo somente a reação química Efeito da temperatura de oxicombustão A fim de avaliar o efeito da temperatura sobre a taxa de reação de oxicombustão do char utilizou-se temperaturas de 600 C, 700 C, 800 C e 900 C, fixando as demais variáveis. Estas temperaturas foram escolhidas em função dos resultados preliminares obtidos no ensaio termogravimétrico, mostrado na Figura 2. perda de massa (mg) C tempo (min) Figura 2 Perda de massa do carvão em função do tempo (granulometria B: 0,85 1,00 mm). Conforme se observa na Figura 2 o consumo de carbono, ou seja, a reação de Boudouard inicia-se próximo aos 720 C, ponto em que as curvas passam a ter comportamento distinto. N2 CO2 T Temperatura ( C) Área temática: Engenharia de Reações Químicas e Catálise 4
5 Portanto selecionou-se temperaturas anteriores a reação de consumo de carbono e posterior para observarmos esse efeito na reação de oxicombustão. A Figura 3, a seguir, mostra as curvas de conversão do char em função do tempo para as temperaturas de 600 C, 700 C, 800 C e 900 C, utilizando como gás reagente uma mistura 30 %O 2 /70 %CO 2 v/v. conversão 1,0 0,8 0,6 0,4 0,2 0,0 T = 600 C T = 700 C T = 800 C T = 900 C 0,0 2,0 4,0 6,0 8,0 tempo (min) Figura 3 Taxa de reação em função da temperatura para a mistura 30 % O 2 /70 %CO 2. Observa-se na Figura 3 que aumentando a temperatura da reação, a taxa de conversão do char se intensifica. Este comportamento pode ser um indicativo de que o regime cinético controla o processo. A temperatura de oxicombustão foi limitada a 900 C, pois como já foi observado por Pohlmann et al (2010) e Nunes e Marcílio (2012), por volta de 1000 C ocorre o predomínio do controle reacional misto Influência da concentração de O 2 na mistura gasosa Segundo Khatami, et al. (2012), para se obter, em condições de oxicombustão, o mesmo perfil de temperaturas de combustão em ar atmosférico deve-se usar uma mistura reagente contendo 30% de O 2 em CO 2. Neste trabalho, além de utilizar essa concentração recomendada, utilizou-se também concentrações de 10 % e 20 % de O 2 em CO 2 a fim de determinar o fenômeno químico que rege a reação. A Figura 4 apresenta a curva de conversão do char em diferentes concentrações de O 2 na temperatura de 600 C. 1,0 0,8 0,6 0,4 10 % O2 0,2 20 % O2 30 % O2 0,0 0,0 2,0 4,0 6,0 8,0 tempo (min) Figura 4 Conversão de char versus o tempo para diferentes concentrações de mistura O 2 /CO 2 a 600 C. conversão Observa-se que o aumento na concentração de O 2 na mistura gasosa aumenta a velocidade de conversão do char. Para as demais concentrações o mesmo efeito também é observado. Esse fenômeno indica que o processo é determinado pela reação química. Área temática: Engenharia de Reações Químicas e Catálise 5
6 3.4. Modelo cinético Modelo do Núcleo não Reagido A Figura 5 apresenta a tentativa de ajustar o modelo do núcleo não reagido aos dados experimentais em três situações: (a) quando a difusão do reagente na camada de cinzas controla o processo, (b) quando a reação química controla o processo e (c) quando a difusão na camada gasosa externa à partícula controla o processo. Figura 5 Ajuste do modelo do núcleo não reagido aos resultados experimentais quando: a) quando a difusão do reagente na camada de cinzas controla o processo, b) quando a reação química controla o processo e c) quando a difusão na camada gasosa externa à partícula controla o processo, para as temperaturas de 600 C, 700 C, 800 C e 900 C, respectivamente. Área temática: Engenharia de Reações Químicas e Catálise 6
7 Conforme se observa na Figura 5a e 5c, não há um bom ajuste do modelo aos dados experimentais, pois os modelos não reproduzem adequadamente as medidas realizadas. Na Figura 5b o ajuste do modelo do núcleo não reagido aos dados experimentais foi realizado considerando o regime cinético como a etapa controladora. Verifica-se, neste caso, que pelo bom ajuste do modelo aos dados experimentais, a reação química seja a etapa determinante do processo reacional. A Figura 6 apresenta uma amostra de char sobre o cadinho de reação antes e após a reação de oxicombustão em termobalança. Devido a grande quantidade de cinzas na matriz carbonosa, não há uma redução significativa no tamanho da partícula, justificando, assim, o uso do modelo do núcleo não reagido para o tratamento matemático dos dados experimentais. Figura 6 Amostra de char antes de depois da reação de oxicombustão. Nesse caso, utilizando o modelo do núcleo não reagido com controle cinético determinando o sistema, o tempo (τ) para a conversão completa da partícula é dado pela equação (2): τ = ρ R (2) k P O2 Onde ρ é a massa específica da amostra (g.cm - ³), R é o raio médio da partícula (cm) e k é a velocidade específica da reação (gmol - ¹.min - ¹.cm - ².atm -n ) e P O2 é a pressão parcial de O 2 (atm). Supondo que a taxa da reação obedeça a equação (3): ( r A ) n = k P O2 (3) Portanto, a taxa de reação (-r A ) pode ser calculada através da equação (4), ou seja: ( r A ) = R. ρ τ (4) Onde R = 0,03375 cm, ρ = 1,96g.cm - ³ e τ = valores experimentais obtidos a partir dos gráficos de conversão, como o da Figura 4. Com a equação (3), determinam-se os valores de k e a ordem da reação, n. Utilizando a equação de Arrhenius (equação 5) calcula-se, então, o fator pré-exponencial, k o (gmol.min -1.cm - Área temática: Engenharia de Reações Químicas e Catálise 7
8 2 ) e a energia de ativação da reação, E a (kj.mol -1 ). k = A exp E a (5) RT -4,2 T -1 (s -1 ) 0,0008 0,0009 0,0010 0,0011 0,0012 Figura 7 Efeito da temperatura sobre a reação C + O 2 CO 2. A Figura 7 apresenta o gráfico onde a equação de Arrhenius linearizada foi plotada. Analisando o comportamento dos resultados, pode-se observar que há um ajuste satisfatório do modelo, indicando que nas temperaturas em que foram realizados os testes, trabalhou-se dentro do regime químico. Portanto, para a energia de ativação obteve-se 10,8 kj.mol -1 e 13,817 gmol.min -1.cm -2 para o fator pré-exponencial. Já para a ordem da reação, os valores foram decrescentes ao longo da temperatura. Para a temperatura de 600 C obteve-se uma ordem de 0,6 e para a temperatura de 900 C a ordem obtida foi de 0,2. Indicando que a medida que a Reação de Boudouard se faz presente é necessário considerar a concentração de CO 2 para fins de cálculo. 4. CONCLUSÕES Com base nos resultados preliminares obtidos nas análises realizadas em termobalança e o tratamento dos dados, se pode inferir que o modelo proposto é válido para o trabalho realizado. Para os cálculos utilizou-se o modelo do núcleo não reagido, onde se observou que há predomínio de controle cinético, com energia de ativação de 10,8 kj.mol - ¹ e fator préexponencial de 13,817 gmol.min -1.cm -2. Observa-se que para o cálculo dos parâmetros cinéticos considerou-se apenas a reação C + O 2 CO 2. Este fenômeno ocorre em temperaturas inferiores à 720 C. Entretanto, para temperaturas mais elevadas, além da reação de oxidação do char, também ocorre a reação de Boudouard C + CO 2 2CO. Esta consideração pode explicar a ordem da reação ser decrescente ao longo da temperatura. 6. REFERÊNCIAS ln k -3,6-3,8-4,0 BEN - Balanço Energético Nacional 2013: Ano base 2012, Empresa de Pesquisa Energética. Rio de Janeiro EPE, DUAN, L., SUN, H., ZHAO, C., ZHOU, W., CHEN, X. Coal combustion characteristics on an oxy-fuel circulating fluidized bed combustor with warm flue gas recycle. Fuel, v. 127, p. Área temática: Engenharia de Reações Químicas e Catálise 8
9 47 51, IEA International Energy Agency. CO 2 emission from fuel combustion, França, JOSÉ H. J. Zur Reaktivität von Koksen aus Santa Catarina-Steinkohle, Brasilien, bei der Vergasung mit Wasserdampf und Kohlendioxid. Thesis, RWTH Aachen, Germany, KATHAMI, R; STIVERS, C.; JOSHI, K.; LEVENDIS, Y. A.; SAROFIM, A. F. Combustion behavior of single particles from three different coal ranks and from sugar cane bagasse in O 2 /N 2 and O 2 /CO 2 atmospheres. Combustion and Flame, v. 159, p , LECKNER, B., GOMÉS-BAREA, A. Oxy-fuel combustion in circulating fluidized bed boilers, Applied Energy, v. 125, p , LEVENSPIEL, O. Chemical Reaction Engineering, 3ª ed., John Wiley & Sons, Nova Iorque, NUNES, K. G. P., MARCÍLIO, N. R. Determinação dos parâmetros cinéticos da reação de oxicombustão de carvão mineral. Dissertação de mestrado Programa de pós-graduação em Engenharia Química Universidade Federal do Rio Grande do Sul, POHLMANN, J. G., OSÓRIO, E., VILELA, A. C. F., BORREGO, A. G. Reactivity to CO 2 of chars prepared in O 2 /N 2 and O 2 /CO 2 mixtures for pulverized coal injection (PCI) in blast furnace in relation to char petrographic characteristics. International Journal of Coal Geology, v. 84, p , ROY, B. and BHATTACHARYA, S. Oxy-fuel fluidized bed combustion using Victorian brown coal: An experimental investigation. Fuel Processing Technology, v. 117, p 23-29, SCHMAL, M.; MONTEIRO, J. L. F.; CASTELLAN, J. L. Kinetics of coal gasification, Ind. Eng. Chem. Process Des. Dev., 21, p , (1982). TOFTEGAARD, M. B.; BRIX, J.; JENSEN, P. A.; GLARBORG, P.; JENSEN, A. D. Oxyfuel combustion of solid fuel, Progress. in Energy and Combustion. Science., v. 36, p , Área temática: Engenharia de Reações Químicas e Catálise 9
Avaliação Cinética da Gaseificação com CO 2 do Bagaço de Maçã
 Avaliação Cinética da Gaseificação com CO 2 do Bagaço de Maçã M. F. P. ROSA, D. SOARES, M. D. DOMENICO, T. R. PACIONI, R. F. P. M. MOREIRA, H. J. JOSÉ Universidade Federal de Santa Catarina, Departamento
Avaliação Cinética da Gaseificação com CO 2 do Bagaço de Maçã M. F. P. ROSA, D. SOARES, M. D. DOMENICO, T. R. PACIONI, R. F. P. M. MOREIRA, H. J. JOSÉ Universidade Federal de Santa Catarina, Departamento
EFEITO DA TORREFAÇÃO NA GASEIFICAÇÃO DE SERRAGEM COM VAPOR DE ÁGUA
 EFEITO DA TORREFAÇÃO NA GASEIFICAÇÃO DE SERRAGEM M VAPOR DE ÁGUA M. F. P. ROSA 1, T. R. PACIONI 1, M. D. DOMENI 2, D. SOARES 1, M. F. M. NOGUEIRA 3, H. J. JOSÉ 1 1 Universidade Federal de Santa Catarina,
EFEITO DA TORREFAÇÃO NA GASEIFICAÇÃO DE SERRAGEM M VAPOR DE ÁGUA M. F. P. ROSA 1, T. R. PACIONI 1, M. D. DOMENI 2, D. SOARES 1, M. F. M. NOGUEIRA 3, H. J. JOSÉ 1 1 Universidade Federal de Santa Catarina,
Fundamentos da Combustão
 Fundamentos da Combustão based on the works of Stephen Turns An Introduction to Combustion and Francisco Domingues de Sousa Curso de Combustão Combustão de Sólidos 1 Fundamentos da Combustão Etapas da
Fundamentos da Combustão based on the works of Stephen Turns An Introduction to Combustion and Francisco Domingues de Sousa Curso de Combustão Combustão de Sólidos 1 Fundamentos da Combustão Etapas da
Lista de Exercícios. Data limite para entrega da lista: 14/09/2018
 Lista de Exercícios Nome: n.º Santos, de de 2018. Série: 2.ª Turmas: A, B, C Ensino: Médio Prof. Paulo Henrique (PH) Bimestre: 3.º Data limite para entrega da lista: 14/09/2018 Valor: 4,0(quatro) 1) Por
Lista de Exercícios Nome: n.º Santos, de de 2018. Série: 2.ª Turmas: A, B, C Ensino: Médio Prof. Paulo Henrique (PH) Bimestre: 3.º Data limite para entrega da lista: 14/09/2018 Valor: 4,0(quatro) 1) Por
GASEIFICAÇÃO DE BIOCHAR OBTIDO DA PIRÓLISE DE BAGAÇO DE MAÇÃ VISANDO SUA UTILIZAÇÃO PARA GERAÇÃO DE ENERGIA
 GASEIFICAÇÃO DE BIOCHAR OBTIDO DA PIRÓLISE DE BAGAÇO DE MAÇÃ VISANDO SUA UTILIZAÇÃO PARA GERAÇÃO DE ENERGIA T. R. PACIONI 1, R. F. P. M. MOREIRA 1 e H. J. JOSÉ 1 1 Universidade Federal de Santa Catarina,
GASEIFICAÇÃO DE BIOCHAR OBTIDO DA PIRÓLISE DE BAGAÇO DE MAÇÃ VISANDO SUA UTILIZAÇÃO PARA GERAÇÃO DE ENERGIA T. R. PACIONI 1, R. F. P. M. MOREIRA 1 e H. J. JOSÉ 1 1 Universidade Federal de Santa Catarina,
COMPARAÇÃO DA ESTRUTURA E REATIVIDADE DE CHARS OBTIDOS EM FORNO DTF E SIMULADOR DA ZONA DE COMBUSTÃO DO ALTO-FORNO
 COMPARAÇÃO DA ESTRUTURA E REATIVIDADE DE CHARS OBTIDOS EM FORNO DTF E SIMULADOR DA ZONA DE COMBUSTÃO DO ALTO-FORNO André da S. Machado, Juliana G. Pohlmann Antônio C. F. Vilela & Eduardo Osório Sumário
COMPARAÇÃO DA ESTRUTURA E REATIVIDADE DE CHARS OBTIDOS EM FORNO DTF E SIMULADOR DA ZONA DE COMBUSTÃO DO ALTO-FORNO André da S. Machado, Juliana G. Pohlmann Antônio C. F. Vilela & Eduardo Osório Sumário
Avaliação da Reatividade do Carvão Vegetal, Carvão Mineral Nacional e Mistura Visando a Injeção em Altos- Fornos
 Avaliação da Reatividade do Carvão Vegetal, Carvão Mineral Nacional e Mistura Visando a Injeção em Altos- Fornos Janaína Machado, Eduardo Osório, Antônio C. F. Vilela Sumário Introdução Objetivo Parte
Avaliação da Reatividade do Carvão Vegetal, Carvão Mineral Nacional e Mistura Visando a Injeção em Altos- Fornos Janaína Machado, Eduardo Osório, Antônio C. F. Vilela Sumário Introdução Objetivo Parte
4. Parte Experimental.
 4. Parte Experimental. Este capítulo expõe os métodos e procedimentos que foram aplicados no transcorrer de todo trabalho, apresenta o desenho de um reator industrial, dados de operação do processo de
4. Parte Experimental. Este capítulo expõe os métodos e procedimentos que foram aplicados no transcorrer de todo trabalho, apresenta o desenho de um reator industrial, dados de operação do processo de
APLICAÇÃO DO MODELO DE EQUILÍBRIO QUÍMICO PARA DETERMINAR AS ZONAS DE CAPTURA DE POLUENTES POR PEDRAS CALCÁRIAS NA QUEIMA DE CARVÃO 1
 APLICAÇÃO DO MODELO DE EQUILÍBRIO QUÍMICO PARA DETERMINAR AS ZONAS DE CAPTURA DE POLUENTES POR PEDRAS CALCÁRIAS NA QUEIMA DE CARVÃO 1 Sandra Beatriz Neuckamp 2, Ângela Patricia Grajales Spilimbergo 3.
APLICAÇÃO DO MODELO DE EQUILÍBRIO QUÍMICO PARA DETERMINAR AS ZONAS DE CAPTURA DE POLUENTES POR PEDRAS CALCÁRIAS NA QUEIMA DE CARVÃO 1 Sandra Beatriz Neuckamp 2, Ângela Patricia Grajales Spilimbergo 3.
PROJETO DO DISTRIBUIDOR DE AR DE UM GASEIFICADOR DE LEITO FLUIDIZADO.
 PROJETO DO DISTRIBUIDOR DE AR DE UM GASEIFICADOR DE LEITO FLUIDIZADO diogo.kaminski@satc.edu.br Objetivo Projetar o distribuidor de ar de um gaseificador em Leito Fluidizado, tendo como ferramenta o software
PROJETO DO DISTRIBUIDOR DE AR DE UM GASEIFICADOR DE LEITO FLUIDIZADO diogo.kaminski@satc.edu.br Objetivo Projetar o distribuidor de ar de um gaseificador em Leito Fluidizado, tendo como ferramenta o software
ESTUDO PRÉVIO DA TAXA DE QUEIMA DE CARVÃO DE CORTIÇA EM LEITO FLUIDIZADO BORBULHANTE
 CIBIM 1, Oporto, Portugal, ESTUDO 211 PRÉVIO DA TAXA DE QUEIMA DE CARVÃO DE CORTIÇA EM LEITO FLUIDIZADO CIBEM 1, Porto, BORBULHANTE Portugal, 211 RM Natal Jorge, JMRS Tavares, JL Alexandre, AJM Ferreira,
CIBIM 1, Oporto, Portugal, ESTUDO 211 PRÉVIO DA TAXA DE QUEIMA DE CARVÃO DE CORTIÇA EM LEITO FLUIDIZADO CIBEM 1, Porto, BORBULHANTE Portugal, 211 RM Natal Jorge, JMRS Tavares, JL Alexandre, AJM Ferreira,
Avaliação da queima de serragem em fornalha
 Avaliação da queima de serragem em fornalha Adriano Divino Lima Afonso 1, Helton Aparecido Rosa 2, Gustavo Veloso 2, Danilo Bonini de Souza 2, Cledemar Busnello 2 37 1 Eng. Agrícola, Prof. Doutor Departamento
Avaliação da queima de serragem em fornalha Adriano Divino Lima Afonso 1, Helton Aparecido Rosa 2, Gustavo Veloso 2, Danilo Bonini de Souza 2, Cledemar Busnello 2 37 1 Eng. Agrícola, Prof. Doutor Departamento
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL Seminário do Programa de Pós-Graduação em Engenharia Química. 04 a 07 de outubro de 2011
 UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL Seminário do Programa de Pós-Graduação em Engenharia Química X Oktoberfórum PPGEQ 04 a 07 de outubro de 2011 AVALIAÇÃO PRELIMINAR DO COMPORTAMENTO DE CHAR DO CARVÃO
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL Seminário do Programa de Pós-Graduação em Engenharia Química X Oktoberfórum PPGEQ 04 a 07 de outubro de 2011 AVALIAÇÃO PRELIMINAR DO COMPORTAMENTO DE CHAR DO CARVÃO
4. Desenvolvimento Experimental
 72 4. Desenvolvimento Experimental Conforme citado anteriormente, dito trabalho é a continuidade ao estudo feito pela bibliografia descrita, cumprindo e seguindo os mesmos parâmetros de trabalho na preparação
72 4. Desenvolvimento Experimental Conforme citado anteriormente, dito trabalho é a continuidade ao estudo feito pela bibliografia descrita, cumprindo e seguindo os mesmos parâmetros de trabalho na preparação
5 Apresentação e discussão dos resultados
 Apresentação e discussão dos resultados 5 Apresentação e discussão dos resultados No presente capítulo, são apresentados e discutidos os ensaios voltados para a determinação da vazão de trabalho do gás
Apresentação e discussão dos resultados 5 Apresentação e discussão dos resultados No presente capítulo, são apresentados e discutidos os ensaios voltados para a determinação da vazão de trabalho do gás
DEPARTAMENTO DE ENGENHARIA METALÚRGICA. Cinética das Reações Heterogêneas
 DEPARTAMENTO DE ENGENHARIA METALÚRGICA Cinética das Reações Heterogêneas 1 Processos heterogêneos em metalurgia extrativa Os estudos termodinâmicos permitem a determinação da posição de equilíbrio alcançada
DEPARTAMENTO DE ENGENHARIA METALÚRGICA Cinética das Reações Heterogêneas 1 Processos heterogêneos em metalurgia extrativa Os estudos termodinâmicos permitem a determinação da posição de equilíbrio alcançada
EFEITO DA TEMPERATURA DE GASEIFICAÇÃO DE BIOMASSA NA ADSORÇÃO DE CORANTE REATIVO
 EFEITO DA TEMPERATURA DE GASEIFICAÇÃO DE BIOMASSA NA ADSORÇÃO DE CORANTE REATIVO J. J. SORNAS¹, W. UTECH JUNIOR¹, R. F. dos SANTOS¹, A. R. VASQUES², C. MARANGON¹I, C. R. L. de AGUIAR¹, E. FONTANA¹, R.
EFEITO DA TEMPERATURA DE GASEIFICAÇÃO DE BIOMASSA NA ADSORÇÃO DE CORANTE REATIVO J. J. SORNAS¹, W. UTECH JUNIOR¹, R. F. dos SANTOS¹, A. R. VASQUES², C. MARANGON¹I, C. R. L. de AGUIAR¹, E. FONTANA¹, R.
AVALIAÇÃO DO COMPORTAMENTO DE CARVÕES BRASILEIROS SUBMETIDOS À COMBUSTÃO ENRIQUECIDA COM OXIGÊNIO
 AVALIAÇÃO DO COMPORTAMENTO DE CARVÕES BRASILEIROS SUBMETIDOS À COMBUSTÃO ENRIQUECIDA COM OXIGÊNIO Amir De Toni Jr., Cristiano Maidana, Leonardo Zimmer, Marina Seelig e Paulo Smith Schneider INTRODUÇÃO
AVALIAÇÃO DO COMPORTAMENTO DE CARVÕES BRASILEIROS SUBMETIDOS À COMBUSTÃO ENRIQUECIDA COM OXIGÊNIO Amir De Toni Jr., Cristiano Maidana, Leonardo Zimmer, Marina Seelig e Paulo Smith Schneider INTRODUÇÃO
EXERCÍCIOS REAÇÕES SÓLIDO/GÁS
 EXERCÍCIOS REAÇÕES SÓLIDO/GÁS Dados: Para resolver os problemas de cinética entre sólidos e gases, podem ser utilizados os gráficos das funções tamanho do núcleo não reagido (r c ) ou fração convertida
EXERCÍCIOS REAÇÕES SÓLIDO/GÁS Dados: Para resolver os problemas de cinética entre sólidos e gases, podem ser utilizados os gráficos das funções tamanho do núcleo não reagido (r c ) ou fração convertida
COMPARATIVO DA CINÉTICA DE DECOMPOSIÇÃO TÉRMICA DA PALHA DE CANA-DE-AÇÚCAR EM ATMOSFERA OXIDANTE E INERTE
 COMPARATIVO DA CINÉTICA DE DECOMPOSIÇÃO TÉRMICA DA PALHA DE CANA-DE-AÇÚCAR EM ATMOSFERA OXIDANTE E INERTE L. A. HIGUCHI, Y. J. RUEDA-ORDÓÑEZ e K. TANNOUS Universidade Estadual de Campinas, Faculdade de
COMPARATIVO DA CINÉTICA DE DECOMPOSIÇÃO TÉRMICA DA PALHA DE CANA-DE-AÇÚCAR EM ATMOSFERA OXIDANTE E INERTE L. A. HIGUCHI, Y. J. RUEDA-ORDÓÑEZ e K. TANNOUS Universidade Estadual de Campinas, Faculdade de
Reações Heterogêneas - Sólido / Fluido
 Reações Heterogêneas - Sólido / Fluido MODELOS Modelo 1: Núcleo Não Reagido: SÓLIDOS DENSOS Partícula de Tamanho Constante Camada Limite Gasosa Camada de Cinza Reação Química Partícula em Diminuição de
Reações Heterogêneas - Sólido / Fluido MODELOS Modelo 1: Núcleo Não Reagido: SÓLIDOS DENSOS Partícula de Tamanho Constante Camada Limite Gasosa Camada de Cinza Reação Química Partícula em Diminuição de
APLICAÇÃO DE MODELOS MODEL-FREE E MODEL-FITTING NA CINÉTICA DA PIRÓLISE DE XISTO
 XXXVII NMP APLICAÇÃO D MODLOS MODL-FR MODL-FITTING NA CINÉTICA DA PIRÓLIS D XISTO J. P. FOLTIN 1*, A. C. L. LISBOA 1 1 Universidade stadual de Campinas, Faculdade de ngenharia Química * e-mail: juliana.p.foltin@gmail.com
XXXVII NMP APLICAÇÃO D MODLOS MODL-FR MODL-FITTING NA CINÉTICA DA PIRÓLIS D XISTO J. P. FOLTIN 1*, A. C. L. LISBOA 1 1 Universidade stadual de Campinas, Faculdade de ngenharia Química * e-mail: juliana.p.foltin@gmail.com
Curso Engenharia de Energia
 UNIVERSIDADE FEDERAL DA GRANDE DOURADOS - UFGD FACULDADE DE ENGENHARIA Curso Engenharia de Energia Prof. Dr. Omar Seye omarseye@ufgd.edu.br Disciplina: COMBUSTÃO E COMBUSTÍVEIS A queima direta, ou combustão,
UNIVERSIDADE FEDERAL DA GRANDE DOURADOS - UFGD FACULDADE DE ENGENHARIA Curso Engenharia de Energia Prof. Dr. Omar Seye omarseye@ufgd.edu.br Disciplina: COMBUSTÃO E COMBUSTÍVEIS A queima direta, ou combustão,
CINÉTICA DE LIXIVIAÇÃO SULFÚRICA DE CONCENTRADO DE ZINCO WILLEMÍTICO COM PRESENÇA DE ESFALERITA
 CINÉTICA DE LIXIVIAÇÃO SULFÚRICA DE CONCENTRADO DE ZINCO WILLEMÍTICO COM PRESENÇA DE ESFALERITA M. J. Dias, J. C. Balarini, C. Konzen, T. L. S. Miranda, A. Salum. Departamento de Engenharia Química, Universidade
CINÉTICA DE LIXIVIAÇÃO SULFÚRICA DE CONCENTRADO DE ZINCO WILLEMÍTICO COM PRESENÇA DE ESFALERITA M. J. Dias, J. C. Balarini, C. Konzen, T. L. S. Miranda, A. Salum. Departamento de Engenharia Química, Universidade
EFEITO DA TEMPERATURA NA DECOMPOSIÇÃO TÉRMICA DE RESÍDUOS PLÁSTICOS E DE BIOMASSA
 EFEITO DA TEMPERATURA NA DECOMPOSIÇÃO TÉRMICA DE RESÍDUOS PLÁSTICOS E DE BIOMASSA 1. INTRODUÇÃO Danyellen Dheyniffer Monteiro Galindo Universidade Estadual Paulista (UNESP), Rio Claro (SP) Departamento
EFEITO DA TEMPERATURA NA DECOMPOSIÇÃO TÉRMICA DE RESÍDUOS PLÁSTICOS E DE BIOMASSA 1. INTRODUÇÃO Danyellen Dheyniffer Monteiro Galindo Universidade Estadual Paulista (UNESP), Rio Claro (SP) Departamento
Tratamento térmico da biomassa. Patrick ROUSSET (Cirad)
 Tratamento térmico da biomassa Patrick ROUSSET (Cirad) Contexto : Limitations of biomass as fuel Comparada com combustíveis fósseis: Baixa densidade a granel. Alto teor de umidade. Natureza hidrofílica.
Tratamento térmico da biomassa Patrick ROUSSET (Cirad) Contexto : Limitations of biomass as fuel Comparada com combustíveis fósseis: Baixa densidade a granel. Alto teor de umidade. Natureza hidrofílica.
C + 2H 2 CH 4. 3 o LISTA DE EXERCÍCIOS DE TRANSFERÊNCIA DE MASSA. Prof. Dr. Gilberto Garcia Cortez
 3 o LIST DE EXEÍIOS DE TNSFEÊNI DE MSS 1- Em um reator catalítico, partículas de carbono em forma de cilindro são consumidas pela passagem de um fluxo de hidrogênio para formar metano através da seguinte
3 o LIST DE EXEÍIOS DE TNSFEÊNI DE MSS 1- Em um reator catalítico, partículas de carbono em forma de cilindro são consumidas pela passagem de um fluxo de hidrogênio para formar metano através da seguinte
SIMULADO de QUÍMICA 2 os anos 2008 TODOS COLÉGIOS
 SIMULADO de QUÍMICA 2 os anos 2008 TODOS COLÉGIOS ) Foram misturados 400 mililitros de solução 0,25 molar de ácido sulfúrico com 600 mililitros,5 molar do mesmo ácido. A molaridade da solução final é:
SIMULADO de QUÍMICA 2 os anos 2008 TODOS COLÉGIOS ) Foram misturados 400 mililitros de solução 0,25 molar de ácido sulfúrico com 600 mililitros,5 molar do mesmo ácido. A molaridade da solução final é:
Quí. Monitor: Marcos Melo
 Professor: Xandão Monitor: Marcos Melo Específicas: Cinética Química 27 nov EXERCÍCIOS DE AULA 1. A água oxigenada H 2O 2 (aq) se decompõe, produzindo água e gás oxigênio, de acordo com a equação: H 2O
Professor: Xandão Monitor: Marcos Melo Específicas: Cinética Química 27 nov EXERCÍCIOS DE AULA 1. A água oxigenada H 2O 2 (aq) se decompõe, produzindo água e gás oxigênio, de acordo com a equação: H 2O
Produção de gás combustível por meio de processo de gaseificação de Eucalyptus grandis em reator de leito fluidizado
 246 III Encontro de Pesquisa e Inovação da Embrapa Agroenergia: Anais Produção de gás combustível por meio de processo de gaseificação de Eucalyptus grandis em reator de leito fluidizado Albert Reis dos
246 III Encontro de Pesquisa e Inovação da Embrapa Agroenergia: Anais Produção de gás combustível por meio de processo de gaseificação de Eucalyptus grandis em reator de leito fluidizado Albert Reis dos
ESTUDO DA SOLUBILIDADE DO PARACETAMOL EM ALGUNS SOLVENTES UTILIZANDO O MODELO NRTL
 ESTUDO DA SOLUBILIDADE DO PARACETAMOL EM ALGUNS SOLVENTES UTILIZANDO O MODELO NRTL H. A. R. GOMES 1, A. B. N. BRITO 1 1 Universidade Federal do Espírito Santo, Centro Universitário Norte do Espírito Santo,
ESTUDO DA SOLUBILIDADE DO PARACETAMOL EM ALGUNS SOLVENTES UTILIZANDO O MODELO NRTL H. A. R. GOMES 1, A. B. N. BRITO 1 1 Universidade Federal do Espírito Santo, Centro Universitário Norte do Espírito Santo,
R: a) t r = 2,23 h b) nº bateladas = 7 c) N Rt = 179,4 kmol por dia
 Reator batelada 1- Uma solução aquosa de acetato de etila deve ser saponificada com uma solução diluída de hidróxido de sódio. A concentração inicial de acetato é 5 g/l e a densidade de mistura reacional
Reator batelada 1- Uma solução aquosa de acetato de etila deve ser saponificada com uma solução diluída de hidróxido de sódio. A concentração inicial de acetato é 5 g/l e a densidade de mistura reacional
4. Desenvolvimento Experimental
 82 4. Desenvolvimento Experimental 4.1. Materiais e Equipamentos 4.1.1. Caracterização dos Materiais Utilizados As matérias primas utilizadas para a fabricação dos briquetes cilíndricas de carvão vegetal,
82 4. Desenvolvimento Experimental 4.1. Materiais e Equipamentos 4.1.1. Caracterização dos Materiais Utilizados As matérias primas utilizadas para a fabricação dos briquetes cilíndricas de carvão vegetal,
FUNDAMENTOS DA REDUÇÃO DE ÓXIDOS METÁLICOS
 FUNDAMENTOS DA REDUÇÃO DE ÓXIDOS METÁLICOS Análise Termodinâmica da Redução de Óxidos Metálicos Energia livre de formação de óxidos metálicos 2 Me + O 2 = 2 MeO Me é um metal e O 2(g) oxigênio puro. variação
FUNDAMENTOS DA REDUÇÃO DE ÓXIDOS METÁLICOS Análise Termodinâmica da Redução de Óxidos Metálicos Energia livre de formação de óxidos metálicos 2 Me + O 2 = 2 MeO Me é um metal e O 2(g) oxigênio puro. variação
REVISIONAL DE QUÍMICA 1º ANO PROF. RICARDO
 REVISIONAL DE QUÍMICA 1º ANO PROF. RICARDO 1- Um aluno de química, ao investigar as propriedades de gases, colocou uma garrafa plástica (PET), contendo ar e devidamente fechada, em um freezer e observou
REVISIONAL DE QUÍMICA 1º ANO PROF. RICARDO 1- Um aluno de química, ao investigar as propriedades de gases, colocou uma garrafa plástica (PET), contendo ar e devidamente fechada, em um freezer e observou
7ª Ficha de Avaliação de Conhecimentos Turma: 11ºA
 Página1 7ª Ficha de Avaliação de Conhecimentos Turma: 11ºA Física e Química A - 11ºAno (Versão 1) Professora Paula Melo Silva Data: 20 de março Ano Letivo: 2018/2019 90 min + 15 min 1. O ácido acético,
Página1 7ª Ficha de Avaliação de Conhecimentos Turma: 11ºA Física e Química A - 11ºAno (Versão 1) Professora Paula Melo Silva Data: 20 de março Ano Letivo: 2018/2019 90 min + 15 min 1. O ácido acético,
COMBUSTÃO DE CARVÃO E BIOMASSA EM FORNO DTF
 COMBUSTÃO DE CARVÃO E BIOMASSA EM FORNO DTF Claudia Cristina ROHLOFF 1 ; Juliana Gonçalves POHLMANN 2 ; Isaías Mortari MACHADO 3 ; Renan Balbinotti KOPS 4 ; Fernando Marcelo PEREIRA 5 1 Universidade Federal
COMBUSTÃO DE CARVÃO E BIOMASSA EM FORNO DTF Claudia Cristina ROHLOFF 1 ; Juliana Gonçalves POHLMANN 2 ; Isaías Mortari MACHADO 3 ; Renan Balbinotti KOPS 4 ; Fernando Marcelo PEREIRA 5 1 Universidade Federal
5. Resultados e Discussões
 86 5. Resultados e Discussões 5.1. Ensaios de Reatividade no forno combustol Sendo que os resultados dos ensaios de reatividade são calculados tanto para amostras sem desvolatilizaҫão como desvolatilizados,
86 5. Resultados e Discussões 5.1. Ensaios de Reatividade no forno combustol Sendo que os resultados dos ensaios de reatividade são calculados tanto para amostras sem desvolatilizaҫão como desvolatilizados,
CRAQUEAMENTO TÉRMICO DE ÓLEO DE FRITURA: UMA PROPOSTA DE MECANISMO CINÉTICO COM BASE EM AGRUPAMENTOS DE COMPOSTOS
 CRAQUEAMENTO TÉRMICO DE ÓLEO DE FRITURA: UMA PROPOSTA DE MECANISMO CINÉTICO COM BASE EM AGRUPAMENTOS DE COMPOSTOS B. L. M. FRAINER, H. F. MEIER, V. R. WIGGERS, E. L. SIMIONATTO, L. ENDER Fundação Universidade
CRAQUEAMENTO TÉRMICO DE ÓLEO DE FRITURA: UMA PROPOSTA DE MECANISMO CINÉTICO COM BASE EM AGRUPAMENTOS DE COMPOSTOS B. L. M. FRAINER, H. F. MEIER, V. R. WIGGERS, E. L. SIMIONATTO, L. ENDER Fundação Universidade
RESUMO 1. INTRODUÇÃO. Palavras-chave: Carvão, Char, PCI, Reatividade, Oxi-combustão
 AVALIAÇÃO DA COMBUSTIBILIDADE E REATIVIDADE AO CO 2 DE CHARS DE CARVÃO BRASILEIRO E DE CARVÕES IMPORTADOS OBTIDOS EM ATMOSFERAS CONVENCIONAL (O 2 /N 2 ) E DE OXI-COMBUSTÃO (O 2 /CO 2 ) Juliana G. Pohlmann*,
AVALIAÇÃO DA COMBUSTIBILIDADE E REATIVIDADE AO CO 2 DE CHARS DE CARVÃO BRASILEIRO E DE CARVÕES IMPORTADOS OBTIDOS EM ATMOSFERAS CONVENCIONAL (O 2 /N 2 ) E DE OXI-COMBUSTÃO (O 2 /CO 2 ) Juliana G. Pohlmann*,
Combustão. Objetivos. O Professor Responsável. J M C Mendes Lopes
 Combustão Objetivos Objetivo de ordem geral: Integrar num assunto específico os conhecimentos adquiridos em disciplinas a montante (termodinâmica, química, mecânica de fluidos, transmissão de calor e de
Combustão Objetivos Objetivo de ordem geral: Integrar num assunto específico os conhecimentos adquiridos em disciplinas a montante (termodinâmica, química, mecânica de fluidos, transmissão de calor e de
OBTENÇÃO DE ÁCIDO FOSFÓRICO DE ALTA PUREZA A PARTIR DE CALCINADO DE OSSOS BOVINOS
 OBTENÇÃO DE ÁCIDO FOSFÓRICO DE ALTA PUREZA A PARTIR DE CALCINADO DE OSSOS BOVINOS C.M.S. dos Santos¹, P. C. Bastos², S.D.F. Rocha 3 ¹,3 Departamento de Engenharia de Minas, Universidade Federal de Minas
OBTENÇÃO DE ÁCIDO FOSFÓRICO DE ALTA PUREZA A PARTIR DE CALCINADO DE OSSOS BOVINOS C.M.S. dos Santos¹, P. C. Bastos², S.D.F. Rocha 3 ¹,3 Departamento de Engenharia de Minas, Universidade Federal de Minas
QUÍMICA PROFº JAISON MATTEI
 QUÍMICA PROFº JAISON MATTEI. O hidrogênio cada vez mais tem ganhado atenção na produção de energia. Recentemente, a empresa britânica Intelligent Energy desenvolveu uma tecnologia que pode fazer a bateria
QUÍMICA PROFº JAISON MATTEI. O hidrogênio cada vez mais tem ganhado atenção na produção de energia. Recentemente, a empresa britânica Intelligent Energy desenvolveu uma tecnologia que pode fazer a bateria
Estudo do uso de carvão vegetal de resíduos de biomassa no sistema de aquecimento dos fornos de produção do clínquer de cimento portland.
 Estudo do uso de carvão vegetal de resíduos de biomassa no sistema de aquecimento dos fornos de produção do clínquer de cimento portland. Aluno: Bruno Damacena de Souza Orientador: Francisco José Moura
Estudo do uso de carvão vegetal de resíduos de biomassa no sistema de aquecimento dos fornos de produção do clínquer de cimento portland. Aluno: Bruno Damacena de Souza Orientador: Francisco José Moura
Semana 09. A queima do carvão é representada pela equação química:
 . (Enem 6) O benzeno, um importante solvente para a indústria química, é obtido industrialmente pela destilação do petróleo. Contudo, também pode ser sintetizado pela trimerização do acetileno catalisada
. (Enem 6) O benzeno, um importante solvente para a indústria química, é obtido industrialmente pela destilação do petróleo. Contudo, também pode ser sintetizado pela trimerização do acetileno catalisada
PROCESSO SELETIVO MESTRADO 2018 Projeto de Pesquisa
 Título do projeto: PROCESSO SELETIVO MESTRADO 2018 Projeto de Pesquisa Modelagem tridimensional da zona de combustão de um alto-forno a coque, com injeção de carvão vegetal e carvão mineral pulverizados
Título do projeto: PROCESSO SELETIVO MESTRADO 2018 Projeto de Pesquisa Modelagem tridimensional da zona de combustão de um alto-forno a coque, com injeção de carvão vegetal e carvão mineral pulverizados
AUTORA: Letícia Xavier Corbini. ORIENTADOR: Nilson Romeu Marcílio
 AUTORA: Letícia Xavier Corbini ORIENTADOR: Nilson Romeu Marcílio INTRODUÇÃO O Brasil possui reservas significativas de carvão mineral. Este combustível representa 6 % da demanda total de energia no país.
AUTORA: Letícia Xavier Corbini ORIENTADOR: Nilson Romeu Marcílio INTRODUÇÃO O Brasil possui reservas significativas de carvão mineral. Este combustível representa 6 % da demanda total de energia no país.
YURI CARVALHO FERREIRA
 UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA YURI CARVALHO FERREIRA DETERMINAÇÃO DOS PARÂMETROS CINÉTICOS DE GASEIFICAÇÃO DE COQUE PROVENIENTE DA REGIÃO DE LUSATIA, NA ALEMANHA, EM REATOR DE
UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA YURI CARVALHO FERREIRA DETERMINAÇÃO DOS PARÂMETROS CINÉTICOS DE GASEIFICAÇÃO DE COQUE PROVENIENTE DA REGIÃO DE LUSATIA, NA ALEMANHA, EM REATOR DE
Fisico-Química da Redução de Óxidos de Ferro
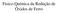 Fisico-Química da Redução de Óxidos de Ferro Análise Termodinâmica da Redução de Óxidos Metálicos Seja a reação de formação de um óxido a partir do metal Me e de oxigênio puro: 2 Me (s,l) + O 2(g) = 2
Fisico-Química da Redução de Óxidos de Ferro Análise Termodinâmica da Redução de Óxidos Metálicos Seja a reação de formação de um óxido a partir do metal Me e de oxigênio puro: 2 Me (s,l) + O 2(g) = 2
6 RESULTADOS E DISCUSSÃO
 6 RESULTADOS E DISCUSSÃO Nesta seção serão apresentados e discutidos os resultados em relação à influência da temperatura e do tempo espacial sobre as características dos pósproduzidos. Os pós de nitreto
6 RESULTADOS E DISCUSSÃO Nesta seção serão apresentados e discutidos os resultados em relação à influência da temperatura e do tempo espacial sobre as características dos pósproduzidos. Os pós de nitreto
Análise Termogravimétrica Aplicações
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais Análise Termogravimétrica Aplicações APLICAÇÃO DE MÉTODOS TERMOANALÍTICOS AOS MATERIAIS PMT 5872 2
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais Análise Termogravimétrica Aplicações APLICAÇÃO DE MÉTODOS TERMOANALÍTICOS AOS MATERIAIS PMT 5872 2
EFEITO DA TEMPERATURA E TEMPO SOBRE A REATIVIDADE E RESISTÊNCIA DO COQUE APÓS A REAÇÃO AO CO 2 *
 EFEITO DA TEMPERATURA E TEMPO SOBRE A REATIVIDADE E RESISTÊNCIA DO COQUE APÓS A REAÇÃO AO CO 2 * Guilherme Bougleux Michelin Assunção¹ José Artur Albano de Guimaraes² Leandro Rocha Lemos³ Guilherme Liziero
EFEITO DA TEMPERATURA E TEMPO SOBRE A REATIVIDADE E RESISTÊNCIA DO COQUE APÓS A REAÇÃO AO CO 2 * Guilherme Bougleux Michelin Assunção¹ José Artur Albano de Guimaraes² Leandro Rocha Lemos³ Guilherme Liziero
ESTUDO CINÉTICO DA DECOMPOSIÇÃO TÉRMICA DOS ÁCIDOS MIRÍSTICO E OLÉICO E DO ÓLEO DE PINHÃO MANSO VIA ANÁLISE TERMOGRAVIMÉTRICA
 ESTUDO CINÉTICO DA DECOMPOSIÇÃO TÉRMICA DOS ÁCIDOS MIRÍSTICO E OLÉICO E DO ÓLEO DE PINHÃO MANSO VIA ANÁLISE TERMOGRAVIMÉTRICA C. M. T. de ALMEIDA 1, E. D. V. BRUCE 2, C. M. B. M. BARBOSA 3, R. T. F. FRETY
ESTUDO CINÉTICO DA DECOMPOSIÇÃO TÉRMICA DOS ÁCIDOS MIRÍSTICO E OLÉICO E DO ÓLEO DE PINHÃO MANSO VIA ANÁLISE TERMOGRAVIMÉTRICA C. M. T. de ALMEIDA 1, E. D. V. BRUCE 2, C. M. B. M. BARBOSA 3, R. T. F. FRETY
METALURGIA EXTRATIVA DOS NÃO FERROSOS
 METALURGIA EXTRATIVA DOS NÃO FERROSOS PMT 2509 PMT 3409 Flávio Beneduce COQUEIFICAÇÃO COQUEIFICAÇÃO Pirólise de carvão: aquecimento na ausência de ar O carvão coqueificável é o betuminoso O ciclo pode
METALURGIA EXTRATIVA DOS NÃO FERROSOS PMT 2509 PMT 3409 Flávio Beneduce COQUEIFICAÇÃO COQUEIFICAÇÃO Pirólise de carvão: aquecimento na ausência de ar O carvão coqueificável é o betuminoso O ciclo pode
AVALIAÇÃO TÉRMICA DO PROCESSO DE SECAGEM DE MISTURAS DE GRAVIOLA E LEITE EM SECADOR DE LEITO DE JORRO
 AVALIAÇÃO TÉRMICA DO PROCESSO DE SECAGEM DE MISTURAS DE GRAVIOLA E LEITE EM SECADOR DE LEITO DE JORRO T. M. DELMIRO 1, I. P. MACHADO 1, M. F. D. de MEDEIROS 2 1 Universidade Federal do Rio Grande do Norte,
AVALIAÇÃO TÉRMICA DO PROCESSO DE SECAGEM DE MISTURAS DE GRAVIOLA E LEITE EM SECADOR DE LEITO DE JORRO T. M. DELMIRO 1, I. P. MACHADO 1, M. F. D. de MEDEIROS 2 1 Universidade Federal do Rio Grande do Norte,
CO2: Tecnologia de Captura em Sólidos Adsorventes
 CO2: Tecnologia de Captura em Sólidos Adsorventes E Q U I P A Q 1 F Q I 0 1 _ 1 : E S T U D A N T E S & A U T O R E S : F R A N C I S C A L E A L G E R S O N T R I S T Ã O H E L E N A C R U Z H U G O M
CO2: Tecnologia de Captura em Sólidos Adsorventes E Q U I P A Q 1 F Q I 0 1 _ 1 : E S T U D A N T E S & A U T O R E S : F R A N C I S C A L E A L G E R S O N T R I S T Ã O H E L E N A C R U Z H U G O M
ANÁLISE DO PROCESSO DA PIRÓLISE DE XISTO UTILIZANDO TERMOGRAVIMETRIA
 ANÁLIS DO PROCSSO DA PIRÓLIS D XISO UILIZANDO RMOGRAVIMRIA RSUMO Amostras de xisto de São Mateus do Sul, Paraná, fornecidas pela Unidade de Negócios da Industrialização do Xisto (SIX), da Petrobras, foram
ANÁLIS DO PROCSSO DA PIRÓLIS D XISO UILIZANDO RMOGRAVIMRIA RSUMO Amostras de xisto de São Mateus do Sul, Paraná, fornecidas pela Unidade de Negócios da Industrialização do Xisto (SIX), da Petrobras, foram
8 Apresentação e discussão dos resultados
 120 8 Apresentação e discussão dos resultados Neste capitulo são apresentados os diagramas de predominância operacionais Mn-O-C levantados, bem como os resultados das experiências de redução do Minério
120 8 Apresentação e discussão dos resultados Neste capitulo são apresentados os diagramas de predominância operacionais Mn-O-C levantados, bem como os resultados das experiências de redução do Minério
BIOENGENHARIA I PROF. MARCELO HENRIQUE ENGENHARIA DE ALIMENTOS
 BIOENGENHARIA I PROF. MARCELO HENRIQUE ENGENHARIA DE ALIMENTOS Introdução à Cinética das reações químicas O termo cinética está relacionado a movimento quando se pensa nele a partir de seu conceito físico.
BIOENGENHARIA I PROF. MARCELO HENRIQUE ENGENHARIA DE ALIMENTOS Introdução à Cinética das reações químicas O termo cinética está relacionado a movimento quando se pensa nele a partir de seu conceito físico.
FUP - Faculdade UnB Planaltina Disciplina: Energia e Dinâmica das Transformações Químicas Professor: Alex Fabiano C. Campos
 FUP - Faculdade UnB Planaltina Disciplina: Energia e Dinâmica das Transformações Químicas Professor: Alex Fabiano C. Campos 1. Conceitue colisão efetiva, colisão não-efetiva, energia de ativação e complexo
FUP - Faculdade UnB Planaltina Disciplina: Energia e Dinâmica das Transformações Químicas Professor: Alex Fabiano C. Campos 1. Conceitue colisão efetiva, colisão não-efetiva, energia de ativação e complexo
Combustíveis e Redutores ENERGIA PARA METALURGIA
 Combustíveis e Redutores ENERGIA PARA METALURGIA Energia para Metalurgia Principal fonte energética: Carbono Carvão mineral e carvão vegetal C + O 2 >> CO 2 + energia Portanto, carbono é redutor, usado
Combustíveis e Redutores ENERGIA PARA METALURGIA Energia para Metalurgia Principal fonte energética: Carbono Carvão mineral e carvão vegetal C + O 2 >> CO 2 + energia Portanto, carbono é redutor, usado
2.Objetivos. Equipamentos para limpeza de gases. Câmara de Póscombustão. Reator de Gaseificação. Filtro seco
 Universidade Federal do Rio Grande do Sul (1) Departamento de Engenharia Química DEQUI/UFRGS Universidade de Caxias do Sul (2) Universidade Federal do Rio de Janeiro COPPE/PEQ (3) Eng. M.Sc. Cleiton Bittencourt
Universidade Federal do Rio Grande do Sul (1) Departamento de Engenharia Química DEQUI/UFRGS Universidade de Caxias do Sul (2) Universidade Federal do Rio de Janeiro COPPE/PEQ (3) Eng. M.Sc. Cleiton Bittencourt
CAPTURA DE POLUENTES NA QUEIMA DE CARVÃO DO TIPO ANTRACITO 1
 CAPTURA DE POLUENTES NA QUEIMA DE CARVÃO DO TIPO ANTRACITO 1 Sandra Beatriz Neuckamp 2, A. Patricia Grajales Spilimbergo 3. 1 Projeto de Iniciação Científica 2 Aluna do Curso de Matemática - Licenciatura,
CAPTURA DE POLUENTES NA QUEIMA DE CARVÃO DO TIPO ANTRACITO 1 Sandra Beatriz Neuckamp 2, A. Patricia Grajales Spilimbergo 3. 1 Projeto de Iniciação Científica 2 Aluna do Curso de Matemática - Licenciatura,
5 Metodologia e planejamento experimental
 Metodologia experimental 5 Metodologia e planejamento experimental Neste capítulo serão descritos a metodologia e o planejamento experimental utilizados no presente estudo, além da descrição do equipamento
Metodologia experimental 5 Metodologia e planejamento experimental Neste capítulo serão descritos a metodologia e o planejamento experimental utilizados no presente estudo, além da descrição do equipamento
Pirólise sob pressão. Uma nova abordagem para a carbonização. 3º Congresso Internacional de BIOENERGIA. Curitiba PR 24 a 26/06/08
 3º Congresso Internacional de BIOENERGIA Curitiba PR 24 a 26/06/08 Pirólise sob pressão Uma nova abordagem para a carbonização Cristiano Kléber de Figueiredo Eng. Florestal Ponto de Partida Consumo brasileiro
3º Congresso Internacional de BIOENERGIA Curitiba PR 24 a 26/06/08 Pirólise sob pressão Uma nova abordagem para a carbonização Cristiano Kléber de Figueiredo Eng. Florestal Ponto de Partida Consumo brasileiro
ESTUDO DO DESEMPENHO DE CORRELAÇÕES DE ARRASTO SÓLIDO-GÁS NA SIMULAÇÃO NUMÉRICA DE UM LEITO FLUIDIZADO BORBULHANTE
 ESTUDO DO DESEMPENHO DE CORRELAÇÕES DE ARRASTO SÓLIDO-GÁS NA SIMULAÇÃO NUMÉRICA DE UM LEITO FLUIDIZADO BORBULHANTE Flávia Zinani, Paulo Conceição, Caterina G. Philippsen, Maria Luiza S. Indrusiak Programa
ESTUDO DO DESEMPENHO DE CORRELAÇÕES DE ARRASTO SÓLIDO-GÁS NA SIMULAÇÃO NUMÉRICA DE UM LEITO FLUIDIZADO BORBULHANTE Flávia Zinani, Paulo Conceição, Caterina G. Philippsen, Maria Luiza S. Indrusiak Programa
1 a Questão: Valor : 1,0 FOLHA DE DADOS. I ) Entalpias de Formação (H o f ) H 2. O (líquida) = - 68,3 kcal / mol. CO 2 (gasoso) = - 94,1 kcal / mol
 PROVA DE QUÍMICA DO VESTIBULAR 96/97 DO INSTITUTO MILITAR DE ENGENHARIA (04/12/96) FOLHA DE DADOS I ) Entalpias de Formação (H o f ) H 2 O (líquida) = - 68,3 kcal / mol CO 2 (gasoso) = - 94,1 kcal / mol
PROVA DE QUÍMICA DO VESTIBULAR 96/97 DO INSTITUTO MILITAR DE ENGENHARIA (04/12/96) FOLHA DE DADOS I ) Entalpias de Formação (H o f ) H 2 O (líquida) = - 68,3 kcal / mol CO 2 (gasoso) = - 94,1 kcal / mol
Noções de Cinética Química
 QB70C:// Química (Turmas S7/S72) Noções de Cinética Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 4 Atkins (5ed.) Cinética X Termodinâmica O G para a reação abaixo
QB70C:// Química (Turmas S7/S72) Noções de Cinética Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 4 Atkins (5ed.) Cinética X Termodinâmica O G para a reação abaixo
Simulação de Gás Natural Injetado pelas Ventaneiras do Alto Forno
 Elis Regina Lima Siqueira Simulação de Gás Natural Injetado pelas Ventaneiras do Alto Forno Dissertação de Mestrado Dissertação apresentada ao Programa de Pósgraduação em Engenharia de Materiais e Processos
Elis Regina Lima Siqueira Simulação de Gás Natural Injetado pelas Ventaneiras do Alto Forno Dissertação de Mestrado Dissertação apresentada ao Programa de Pósgraduação em Engenharia de Materiais e Processos
IME º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR
 IME - 2003 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR Química Questão 01 Uma fonte de vanádio é o mineral vanadinita, cuja fórmula é Pb 5 (VO 4 ) 3 Cl. DETERMINE: A) A porcentagem em massa de vanádio
IME - 2003 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR Química Questão 01 Uma fonte de vanádio é o mineral vanadinita, cuja fórmula é Pb 5 (VO 4 ) 3 Cl. DETERMINE: A) A porcentagem em massa de vanádio
PRODUÇÃO DE ETANOL ENRIQUECIDO UTILIZANDO ADSORÇÃO EM FASE LÍQUIDA COM MULTIESTÁGIOS OPERANDO EM BATELADA E ALTA EFICIÊNCIA DE ENERGIA
 PRODUÇÃO DE ETANOL ENRIQUECIDO UTILIZANDO ADSORÇÃO EM FASE LÍQUIDA COM MULTIESTÁGIOS OPERANDO EM BATELADA E ALTA EFICIÊNCIA DE ENERGIA Mairlane Silva de Alencar 1 ; Marcelo José do Carmo 2 ; Gabriela Rodrigues
PRODUÇÃO DE ETANOL ENRIQUECIDO UTILIZANDO ADSORÇÃO EM FASE LÍQUIDA COM MULTIESTÁGIOS OPERANDO EM BATELADA E ALTA EFICIÊNCIA DE ENERGIA Mairlane Silva de Alencar 1 ; Marcelo José do Carmo 2 ; Gabriela Rodrigues
a) Qual deverá ser o volume do PFR para converter 80% de A em fase líquida? Considerar alimentação a 44 L min -1 e C A0 = C B0 = 1 mol L -1
 501) Um dado composto A se decompõe conforme a cinética enzimática de Michaelis-Menten,. Determine os parâmetros V máx e K M, considerando os dados experimentais a seguir. C A (kmol m -3 ) 0,1 0,01 0,005
501) Um dado composto A se decompõe conforme a cinética enzimática de Michaelis-Menten,. Determine os parâmetros V máx e K M, considerando os dados experimentais a seguir. C A (kmol m -3 ) 0,1 0,01 0,005
Susana Sequeira Simão
 Susana Sequeira Simão Dissertação apresentada à Universidade Nova de Lisboa, Faculdade de Ciências e Tecnologia, para a obtenção do grau de Mestre em Energia e Bioenergia Orientador: Doutor Pedro Abelha
Susana Sequeira Simão Dissertação apresentada à Universidade Nova de Lisboa, Faculdade de Ciências e Tecnologia, para a obtenção do grau de Mestre em Energia e Bioenergia Orientador: Doutor Pedro Abelha
UM MODELO APROXIMADO COM REAÇÃO DA DISPERSÃO DE GASES DE UMA CENTRAL TERMOELÉTRICA
 UM MODELO APROXIMADO COM REAÇÃO DA DISPERSÃO DE GASES DE UMA CENTRAL TERMOELÉTRICA E. A. S. CHIARAMONTE 1 Universidade Federal do Pampa, Campus Bagé, Engenharia Química E-mail para contato: edsonchi@portoweb.com.br
UM MODELO APROXIMADO COM REAÇÃO DA DISPERSÃO DE GASES DE UMA CENTRAL TERMOELÉTRICA E. A. S. CHIARAMONTE 1 Universidade Federal do Pampa, Campus Bagé, Engenharia Química E-mail para contato: edsonchi@portoweb.com.br
Determinação dos parâmetros cinéticos da reação de oxicombustão de carvão mineral
 UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL ESCOLA DE ENGENHARIA DEPARTAMENTO DE ENGENHARIA QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM ENGENHARIA QUÍMICA Determinação dos parâmetros cinéticos da reação de oxicombustão
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL ESCOLA DE ENGENHARIA DEPARTAMENTO DE ENGENHARIA QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM ENGENHARIA QUÍMICA Determinação dos parâmetros cinéticos da reação de oxicombustão
Velocidade de reação. Química Geral. Prof. Edson Nossol
 Velocidade de reação Química Geral Prof. Edson Nossol Uberlândia, 02/12/2016 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H - T S
Velocidade de reação Química Geral Prof. Edson Nossol Uberlândia, 02/12/2016 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H - T S
CINÉTICA DA REAÇÃO DE OXICOMBUSTÃO DE CARVÕES MINERAIS COM ALTOS TEORES DE CINZAS
 UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL ESCOLA DE ENGENHARIA DEPARTAMENTO DE ENGENHARIA QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM ENGENHARIA QUÍMICA CINÉTICA DA REAÇÃO DE OXICOMBUSTÃO DE CARVÕES MINERAIS
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL ESCOLA DE ENGENHARIA DEPARTAMENTO DE ENGENHARIA QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM ENGENHARIA QUÍMICA CINÉTICA DA REAÇÃO DE OXICOMBUSTÃO DE CARVÕES MINERAIS
PRÁTICA: DETERMINAÇÃO DA CONSTANTE R DOS GASES. pv= nrt (01) Gás Ideal : obedece pv=n RT em qualquer condição de T e p.
 PRÁTICA: DETERMINAÇÃO DA CONSTANTE R DOS GASES 1. Introdução A matéria pode se apresentar nos estados sólido, líquido e gasoso. A temperatura e a pressão são as variáveis responsáveis pelo seu estado físico.
PRÁTICA: DETERMINAÇÃO DA CONSTANTE R DOS GASES 1. Introdução A matéria pode se apresentar nos estados sólido, líquido e gasoso. A temperatura e a pressão são as variáveis responsáveis pelo seu estado físico.
PRODUÇÃO DE ETILENO A PARTIR DO ETANOL COM USO DE DIFERENTES ALUMINAS COMERCIAIS COMO CATALISADORES
 PRODUÇÃO DE ETILENO A PARTIR DO ETANOL COM USO DE DIFERENTES ALUMINAS COMERCIAIS COMO CATALISADORES L. T. SILVA 1, T. F. BRAGA 1, F. S. FERRATO 1, K. A. RESENDE 2 e S. C. DANTAS 1 1 Universidade Federal
PRODUÇÃO DE ETILENO A PARTIR DO ETANOL COM USO DE DIFERENTES ALUMINAS COMERCIAIS COMO CATALISADORES L. T. SILVA 1, T. F. BRAGA 1, F. S. FERRATO 1, K. A. RESENDE 2 e S. C. DANTAS 1 1 Universidade Federal
Efeito da Temperatura. PMT Físico-Química para Engenharia Metalúrgica e de Materiais II - Neusa Alonso-Falleiros 1
 Efeito da Temperatura PMT 2306 - Físico-Química para Engenharia Metalúrgica e de Materiais II - Neusa Alonso-Falleiros 1 1ª. Aula Processos em Metalurgia e Materiais: são Reações Químicas/Eletroquímicas
Efeito da Temperatura PMT 2306 - Físico-Química para Engenharia Metalúrgica e de Materiais II - Neusa Alonso-Falleiros 1 1ª. Aula Processos em Metalurgia e Materiais: são Reações Químicas/Eletroquímicas
CINÉTICA DAS REAÇÕES QUÍMICAS
 CINÉTICA DAS REAÇÕES QUÍMICAS INTRODUÇÃO Termodinâmica fornece informações sobre: O estado de equilíbrio; Formas de atuação no sistema; Poucas informações sobre velocidade e; Nenhuma informação sobre a
CINÉTICA DAS REAÇÕES QUÍMICAS INTRODUÇÃO Termodinâmica fornece informações sobre: O estado de equilíbrio; Formas de atuação no sistema; Poucas informações sobre velocidade e; Nenhuma informação sobre a
Lista de Exercícios Lei de Hess, Cinética Química e Equilíbrio Químico Prof. Benfica
 Lista de Exercícios Lei de Hess, Cinética Química e Equilíbrio Químico Prof. Benfica 1) A entalpia da reação (I) não pode ser medida diretamente em um calorímetro porque a reação de carbono com excesso
Lista de Exercícios Lei de Hess, Cinética Química e Equilíbrio Químico Prof. Benfica 1) A entalpia da reação (I) não pode ser medida diretamente em um calorímetro porque a reação de carbono com excesso
5 Metodologia experimental
 5 Metodologia experimental 5.1. Métodos de caracterização e análise do resíduo original e dos resíduos reacionais Antes de iniciar a metodologia de caracterização, será detalhada de maneira breve, através
5 Metodologia experimental 5.1. Métodos de caracterização e análise do resíduo original e dos resíduos reacionais Antes de iniciar a metodologia de caracterização, será detalhada de maneira breve, através
Combustão Industrial
 Combustão Industrial JOSÉ EDUARDO MAUTONE BARROS Professor Adjunto da Universidade Federal de Minas Gerais Coordenador do Laboratório de Combustíveis e Combustão Doutor em Engenharia Mecânica - Térmica
Combustão Industrial JOSÉ EDUARDO MAUTONE BARROS Professor Adjunto da Universidade Federal de Minas Gerais Coordenador do Laboratório de Combustíveis e Combustão Doutor em Engenharia Mecânica - Térmica
Caracterização química e gaseificação em leito fluidizado borbulhante de bagaço de cana e engaço de dendê
 190 Caracterização química e gaseificação em leito fluidizado borbulhante de bagaço de cana e engaço de dendê Amanda Assunção Rosa 1, Albert Reis dos Anjos 2, Anna Letícia Montenegro Turtelli Pighinelli
190 Caracterização química e gaseificação em leito fluidizado borbulhante de bagaço de cana e engaço de dendê Amanda Assunção Rosa 1, Albert Reis dos Anjos 2, Anna Letícia Montenegro Turtelli Pighinelli
Modelagem e Simulação da Câmara de Reação de uma Caldeira a Carvão Pulverizado
 UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL ESCOLA DE ENGENHARIA DEPARTAMENTO DE ENGENHARIA QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM ENGENHARIA QUÍMICA Modelagem e Simulação da Câmara de Reação de uma Caldeira
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL ESCOLA DE ENGENHARIA DEPARTAMENTO DE ENGENHARIA QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM ENGENHARIA QUÍMICA Modelagem e Simulação da Câmara de Reação de uma Caldeira
Exemplo 2: A baixas temperaturas a lei de velocidade da reação A + B C + D é r A =
 Determine a energia de ativação desta reação. Exemplo 1: Para a reação SO 2 + 1 2 O 2 SO 3, se a velocidade de formação de SO 3 é de 2 mol m -3 s -1, então as velocidades de desaparecimento de SO 2, de
Determine a energia de ativação desta reação. Exemplo 1: Para a reação SO 2 + 1 2 O 2 SO 3, se a velocidade de formação de SO 3 é de 2 mol m -3 s -1, então as velocidades de desaparecimento de SO 2, de
Torrefacção de CDRs industriais: Aplicações energéticas e materiais
 Torrefacção de CDRs industriais: Aplicações energéticas e materiais Catarina Nobre (1), Margarida Gonçalves (1), Cândida Vilarinho (2), Benilde Mendes (1) (1) METRICS, Departamento de Ciências e Tecnologia
Torrefacção de CDRs industriais: Aplicações energéticas e materiais Catarina Nobre (1), Margarida Gonçalves (1), Cândida Vilarinho (2), Benilde Mendes (1) (1) METRICS, Departamento de Ciências e Tecnologia
SIMULAÇÃO DE GASEIFICAÇÃO DE BIOMASSA DE TAMAREIRA PARA PRODUÇÃO DE GÁS DE SÍNTESE
 SIMULAÇÃO DE GASEIFICAÇÃO DE BIOMASSA DE TAMAREIRA PARA PRODUÇÃO DE GÁS DE SÍNTESE A. E. de OLIVEIRA 1, J. B. O. SANTOS 1 1 Universidade Federal de São Carlos, Departamento de Engenharia Química E-mail
SIMULAÇÃO DE GASEIFICAÇÃO DE BIOMASSA DE TAMAREIRA PARA PRODUÇÃO DE GÁS DE SÍNTESE A. E. de OLIVEIRA 1, J. B. O. SANTOS 1 1 Universidade Federal de São Carlos, Departamento de Engenharia Química E-mail
Produção de carvão ativado a partir de madeira tratada com arseniato de cobre cromatado (CCA) para adsorção de CO 2
 UNIVERSIDADE DE CAXIAS DO SUL CENTRO DE CIÊNCIAS EXATAS E TECNOLOGIA LABORATÓRIO DE ENERGIA E BIOPROCESSOS Produção de carvão ativado a partir de madeira tratada com arseniato de cobre cromatado (CCA)
UNIVERSIDADE DE CAXIAS DO SUL CENTRO DE CIÊNCIAS EXATAS E TECNOLOGIA LABORATÓRIO DE ENERGIA E BIOPROCESSOS Produção de carvão ativado a partir de madeira tratada com arseniato de cobre cromatado (CCA)
4 Considerações teóricas
 Considerações teóricas 4 Considerações teóricas A utilização do Ga 2 O como fonte de gálio, em atmosfera nitretante, para a obtenção de GaN, foi estudada em algumas rotas de síntese sob diferentes condições
Considerações teóricas 4 Considerações teóricas A utilização do Ga 2 O como fonte de gálio, em atmosfera nitretante, para a obtenção de GaN, foi estudada em algumas rotas de síntese sob diferentes condições
4. Resultados e Discussão
 Absorbância 4. Resultados e Discussão 4.1. Obtenção da curva de calibração A obtenção da curva de calibração, absorbância vs. concentração de Paraquat, é necessária para a análise química do pesticida.
Absorbância 4. Resultados e Discussão 4.1. Obtenção da curva de calibração A obtenção da curva de calibração, absorbância vs. concentração de Paraquat, é necessária para a análise química do pesticida.
CINÉTICA DE EVAPORAÇÃO DO ÓXIDO DE ZINCO. N. Duarte 1, W.B. Ferraz 2, A.C.S.Sabioni 3. Universidade Federal de Ouro Preto Ouro Preto, Brasil
 CINÉTICA DE EVAPORAÇÃO DO ÓXIDO DE ZINCO N. Duarte 1, W.B. Ferraz 2, A.C.S.Sabioni 3 1 Departamento de Metalurgia / EM / UFOP Universidade Federal de Ouro Preto 35400-000 Ouro Preto, Brasil 2 Centro de
CINÉTICA DE EVAPORAÇÃO DO ÓXIDO DE ZINCO N. Duarte 1, W.B. Ferraz 2, A.C.S.Sabioni 3 1 Departamento de Metalurgia / EM / UFOP Universidade Federal de Ouro Preto 35400-000 Ouro Preto, Brasil 2 Centro de
3 Fundamentos teóricos
 Fundamentos teóricos 3 Fundamentos teóricos A fundamentação teórica de um determinado processo químico envolve, normalmente, o estudo tanto de aspectos termodinâmicos como cinéticos relativos às reações
Fundamentos teóricos 3 Fundamentos teóricos A fundamentação teórica de um determinado processo químico envolve, normalmente, o estudo tanto de aspectos termodinâmicos como cinéticos relativos às reações
PAG Química Estequiometria
 1. 2. 3. Em países de clima desfavorável ao cultivo de cana-de-açúcar, o etanol (C 2 H 6 O) é sintetizado através da reação de eteno (C 2 H 4 ) com vapor de água, a alta temperatura e alta pressão, segundo
1. 2. 3. Em países de clima desfavorável ao cultivo de cana-de-açúcar, o etanol (C 2 H 6 O) é sintetizado através da reação de eteno (C 2 H 4 ) com vapor de água, a alta temperatura e alta pressão, segundo
OBTENÇÃO DE PARÂMETROS CINÉTICOS DA PIRÓLISE DE CASCA DE ARROZ E BAGAÇO DE CANA EM LEITO FLUIDIZADO
 OBTENÇÃO DE PARÂMETROS CINÉTICOS DA PIRÓLISE DE CASCA DE ARROZ E BAGAÇO DE CANA EM LEITO FLUIDIZADO Caio Glauco Sánchez Universidade Estadual de Campinas, Faculdade de Engenharia Mecânica Depto. de Engenharia
OBTENÇÃO DE PARÂMETROS CINÉTICOS DA PIRÓLISE DE CASCA DE ARROZ E BAGAÇO DE CANA EM LEITO FLUIDIZADO Caio Glauco Sánchez Universidade Estadual de Campinas, Faculdade de Engenharia Mecânica Depto. de Engenharia
Catálise heterogênea. Catalisador sólido. Reação na interface sólido-fluido
 Catálise heterogênea Catalisador sólido Reação na interface sólido-fluido Tipos de catalisadores Poroso: elevada área superficial Tipos de catalisadores Peneiras moleculares: capacidade de distinção entre
Catálise heterogênea Catalisador sólido Reação na interface sólido-fluido Tipos de catalisadores Poroso: elevada área superficial Tipos de catalisadores Peneiras moleculares: capacidade de distinção entre
Introdução. Definição
 Introdução Definição O carvão vegetal é um subproduto florestal resultante da pirólise da madeira, também conhecida como carbonização ou destilação seca da madeira. É um método destrutivo. No processo
Introdução Definição O carvão vegetal é um subproduto florestal resultante da pirólise da madeira, também conhecida como carbonização ou destilação seca da madeira. É um método destrutivo. No processo
Vm A = [A] t. Vm B = [B] t. Vm C = [C] t. Vm = Vm A = Vm B = Vm C a b c. 1
![Vm A = [A] t. Vm B = [B] t. Vm C = [C] t. Vm = Vm A = Vm B = Vm C a b c. 1 Vm A = [A] t. Vm B = [B] t. Vm C = [C] t. Vm = Vm A = Vm B = Vm C a b c. 1](/thumbs/53/31499278.jpg) I. INTRODUÇÃO É à parte da química que estuda a maior ou menor rapidez com que uma reação química ocorre e os fatores que a influenciam. Este estudo é importante para o nosso dia-a-dia, pois explica alguns
I. INTRODUÇÃO É à parte da química que estuda a maior ou menor rapidez com que uma reação química ocorre e os fatores que a influenciam. Este estudo é importante para o nosso dia-a-dia, pois explica alguns
