Doença dos Eritrócitos
|
|
|
- Thalita Beretta Valente
- 10 Há anos
- Visualizações:
Transcrição
1 Doença dos Eritrócitos Autor: Prof. Dr. Paulo Cesar Naoum Célula Falciforme Palavras chaves das doenças causadas pelas Células Falciformes... 4 Células Falciformes... 4 Anemia Falciforme... 5 Doença Falciforme... 6 Hb S / Talassemia Beta... 9 Microdrepanocitose Hb SC - Doença da Hb SC Hb SS / Persistência Hereditária de Hb Fetal (Hb SS / PHHF) Traço Falcêmico (O Portador Assintomático) ou Hb AS Histórico da Hb S Introdução A Origem e Dispersão da Hb S As Principais Descobertas Científicas Resistência das Células com Hb S ao Plasmodium faciparum Genética, Química E Biologia Molecular Da Hb S Mutação e Consequências Estruturais na Globina Beta S O Fenótipo Falcêmico Os Genótipos Falcêmicos Hb AS - Traço Falciforme ou Falcemia Heterozigota Anemia Falciforme (Hb SS) Hb SD - Doença da Hb SD Hb SC - Doença da Hb SC Hb S / Talassemia β 0 ou Hb SF (Micro-Drepanocitose) Hb S / Talassemia β + ou Hb SFA Hb SS / Talassemia Alfa ou Hb SH Hb S/PHHF ou Hb SF Os Haplótipos da Hb SS Fisiopatogia da Hb S Os Efeitos na Molécula da Hb S, na Célula Falciforme e na Circulação Sangüínea do Doente Falcêmico
2 A Polimerização da Hb S A Degradação Oxidativa da Hb S As Lesões da Membrana da Célula Falciforme A heterogeneidade das Células Falciformes A Anemia Hemolítica no Doente Falcêmico Os Processos VASO-OCLUSIVOSOCLUSIVOS Alterações Laboratoriais nas Doenças Falciformes Anemia Falciforme S/β Talassemia ou Micro Drepanocitose Hb S/talassemia α Hb SC Hb SD Hb S/Persistência Hereditária de Hb Fetal O Traço Falciforme (Hb AS) Controle Clínico dos Doentes Falcêmicos Aspectos Gerais da Anemia Dactilite (Síndrome Mão-Pé) Síndrome do Quadrante Superior Direito Síndrome Torácica Aguda (STA) Priapismo Úlceras de Perna Necrose Avascular Acidente Vascular Cerebral (AVC) Crises Dolorosas Tratamento das Crises Dolorosas Interferentes que acentuam ou minimizam a Anemia Falciforme Principais consequências dos interferentes ambientais, sociais e econômicos na anemia falciforme Interações da Hb SS com Deficiência de G-6PD Interações da Hb SS com Persistência Hereditária de Hb Fetal Interações da Hb SS com Esferocitoses e Eliptocitoses Deficiência de Enzimas Eritrocitárias Anti-Oxidantes (SOD, catalase, GPx) Prevalência e Controle do Gene da Hb S Distribuição Geográfica Mundial
3 Distribuição Geográfica no Brasil Relação entre Sobrenomes e Hb S no Brasil Interferentes Eritrocitários e ambientais na Anemia Falciforme Controle e Prevenção das Doenças Falciformes Testes Laboratoriais Específicos para Hb S
4 CÉLULA FALCIFORME Palavras chaves das doenças causadas pelas Células Falciformes Células Falciformes As células falciformes são eritrócitos com morfologias drasticamente alteradas pela presença de moléculas de hemoglobinas S (ou Hb S). Quando as moléculas de Hb S estão oxigenadas (oxi- Hb S), suas estruturas são globulares e, por isso, mantém os eritrócitos com formas discóides. Quando as moléculas de Hb S liberam oxigênio se tornam desoxigenadas (deoxi-hb S). As moléculas de Hb S deoxigenadas alteram suas configurações estruturais devido a formações de polímeros deixando de ser globulares. A polimerização das moléculas de deoxi-hb S causa a formação de estruturas moleculares alongadas como se fossem feixes, e assim os eritrócitos com deoxi-hb deixam de ser discóides e apresentam diferentes formas das quais as mais comuns tem a forma de foice. O predomínio de eritrócitos com a forma afoiçada resulta na denominação de células falciformes.por outro lado, a denominação da hemoglobina que causa as células falciformes foi extraída do termo inglês Sickle cell.. Em 1945, com a utilização da técnica de eletroforese para o fracionamento de proteínas, observou-se que os eritrócitos normais tinham hemoglobina diferente daqueles com as formas afoiçadas (obtidos de pacientes com anemia falciforme). Para designar a diferença entre essas hemoglobinas, denominou-se por HbA as hemoglobinas consideradas normais e de Hb S (a letra foi extraída do Sickle cell) para as hemoglobinas extraídas das células falciformes. Células Falciformes - Eritrócitos falcizados em sangue periférico de doente com anemia falciforme. A forma delgada dessas células é indicativo de falcização irreversível. Essas células quando analisadas por microscopia eletrônica mostram lesões de membrana. 4
5 Célula Falciforme em microscopia eletrônica - Observar duas lesões na membrana eritrocitária de um eritrócito falcizado. As lesões de membrana ocorrem após uma série de eventos provocados pela polimerização da deoxi-hb S, geração de espécies ativadas de oxigênio, e por ação macrofágica durante a passagem desses eritrócitos danificados pelo sistema retículo endotelial. Anemia Falciforme É uma designação clínica usada para doentes homozigotos com Hb S (ou Hb SS). Há uma certa variabilidade clínica e laboratorial entre os doentes com anemia falciforme que pode ser explicada por meio de interferentes biológicos (doenças crônicas ou agudas associadas), eritrocitários (associação com talassemia alfa, enzimopatias, doenças de membrana e persistência hereditária de Hb Fetal) ) e sociais (pobreza, cultura, atendimento de saúde). Além desses interferentes, ocorre também a diversificação dos componentes unitários - as bases nitrogenadas - do agrupamento dos genes tipo beta (epsilon, gama-a, gama-g, delta e beta S) que não expressam proteínas, mas diferenciam etnicamente alguns grupos populacionais. A composição diferenciada dessas bases nitrogenadas é denominada haplótipos. Assim, um mesmo genótipo de Hb SS pode ser qualificado por meio de técnicas de biologia molecular em pelo menos cinco haplótipos: Hb SS-Benin, Hb SS-Bantú, Hb SS- Camarões, Hb SS-Senegal e Hb SS-Árabe/Indiano.. Alguns desses haplótipos caracterizam-se por maior gravidade da anemia falciforme (ex.: Hb SS-Benin e Hb SS-Bantú) ou por menor gravidade (Hb SS-Árabe/Indiano). A forma mais comum de herança genética da anemia falciforme se deve a ambos genitores serem portadores de Hb AS ou traço falciforme. 5
6 Eritrócitos na Anemia Falciforme - Esfregaço de sangue periférico de paciente, cujo sangue foi coletado durante episódio de crise dolorosa. A figura mostra vários eritrócitos falcizados (do tipo irreversível) el) com a morfologia muito delgada e eritrócitos do tipo equinócitos. Doença Falciforme É uma denominação clinicamente ampla utilizada quando se desconhece o genótipo da doença falcêmica. Inclui, portanto, todos os genótipos que causam ofenótipo da doença: anemia, icterícia, bilirrubinemia, dores, etc. Fazem parte desse grupo a anemia falciforme caracterizada pelo genótipo SS (Hb SS), a interação da Hb S com talassemia beta (Hb S/talassemia beta) também conhecida por microdrepanocitose,, a interação da anemia falciforme com talassemia alfa (Hb SS/talassemia alfa), a interação da anemia falciforme com a persistência hereditária de Hb Fetal (Hb S/PHHF), e de Hb S com hemoglobinas variantes, especialmente com a Hb D (Hb SD) e Hb C (Hb SC). Eritrócito no Traço falciforme ou Hb AS 6
7 Hb S/ Talassemia beta ou micro-drepanocitose. Eritrócitos na Hb SC 7
8 Eritrócitos na Hb SD Eritrócitos da Hb SS / persistência hereditária de Hb Fetal ou Hb SS / PHHF 8
9 Hb S/talassemia beta ou micro- drepanocitose Hb S / Talassemia Beta Esfregaço de sangue periférico de paciente com interação Hb S/talassemia beta ou Hb S./tal. B+. Observar a presença de células falcizadas, eritrócitos em alvo (ou codócitos), eritrócitos microcíticos e hipocrômicos. 9
10 Esfregaço de sangue periférico de paciente com interação Hb S/talassemia beta ou Hb S./tal. Bº. A presença de aniso-poiquilocitose é marcante pelos eritrócitos falcizados ados ou em fase de falcização, dacriócitos, em alvo, microcíticos, hipocrômicos, e um eritroblasto ortocromático. Microdrepanocitose É uma designação antiga da Hb S / Talassemia beta, que foi descrita em 1950 por Enzo Silvestrano e Ida Bianco, na Itália. Há basicamente dois tipos dessa interação e diferenciados pelo grau de lesão da talassemia beta. Quando a lesão genética que causa a talassemia beta suprime totalmente a expressão de síntese do gene da globina beta, denomina-se por talassemia beta-zero (ou tal. b 0 ). Se a lesão do gene da globina beta for parcial, a talassemia é classificada por talassemia beta-mais (ou tal. b + ). Assim, a microdrepanocitose ou a Hb S/talassemia beta pode ser de dois tipos: Hb S/tal. b 0 ou Hb S/tal. b +. Na Hb S/tal. b 0 não há síntese de Hb A,, portanto na eletroforese a Hb S predomina com concentrações variáveis entre 70 a 90%, seguida da Hb Fetal (5 a 20%) e Hb A2 com valores normais ou elevados. Na Hb S/tal. b + ocorre a síntese de Hb A com concentração abaixo da Hb S; Hb S (50 a 80%); Hb A (10 a 40%), Hb Fetal (5 a 10%) e Hb A2 normal ou elevada. O grau de anemia no genótipo Hb S/b 0 tal. é maior que na Hb S/tal. b +. Os doentes com microdrepanocitose ou Hb S/talassemia beta apresentam crises intermitentes de dores, infartos ósseos seos e nas articulações. Hematologicamente, o sangue periférico mostra eritrócitos microcíticos e hipocrômicos juntamente com células falcizadas, eritrócitos em alvo e policromáticos. Finalmente, a forma mais comum de herança genética desses dois tipos de doença se caracteriza por um dos genitores ser portador assintomático de Hb AS e o outro também portador assintomático de talassemia beta menor (Hb Ab menor). 10
11 Hb SC - Doença da Hb SC Essa doença é comum no oeste da África. No Brasil sua prevalência é baixa em relação à anemia falciforme (consultar o item Prevalência e distribuição geográfica da Hb S). É caracterizada por anemia de grau moderado (Hb: 9-13 g/dl) e muitas vezes são identificadas na idade adulta quando pode apresentar complicações. Geralmente e as complicações de devem a lesões da microvasculatura, provavelmente devido aos efeitos causados pela falcização da Hb S e da rigidez celular provocada pela Hb C (processos de cristalização da Hb C). Entre as complicações mais comuns da doença da Hb SC destacam necroses assépticas da cabeça do fêmur e do úmero, bem como manifestações da hematúria. Pode ocorrer também episódios trombóticos abrangentes envolvendo particularmente os pulmões especialmente durante infecções intercorrentes, na gestação e puerpério. rio. Outra complicação grave se deve a lesões causadas por repetidas oclusões vasculares da retina. Geralmente a doença da Hb SC é diagnosticada pela presença de anemia moderada, esplenomegalia, e alterações morfológicas dos eritrócitos incluindo células em alvo, cristais de hemoglobina C e células falciformes. A forma mais comum de herança se deve a um dos genitores ser portador de traço falciforme (Hb AS) e outro portador de Hb AC. Esfregaço de sangue periférico de paciente com doença falciforme SC, ou Hb SC. É comum a presença de eritrócitos falcizados juntamente com eritrócitos em alvo ou com cristais de Hb C (apontados por setas). Hb SS / Persistência Hereditária de Hb Fetal (Hb SS / PHHF) A persistência hereditária de Hb Fetal (PHHF) é um termo que abrange uma variedade de condições, todas associadas com a produção persistente de Hb Fetal após o período neonatal e, geralmente, com ausência de anormalidades hematológicas importantes. A associação entre anemia falciforme e persistência hereditária de Hb Fetal, ou Hb SS/PHHF,, tem sido encontrada 11
12 em todas as regiões do Brasil. Na Hb SS/PHHF a falcização não ocorre facilmente pois a Hb Fetal está elevada com níveis entre 15 e 30% e se distribui homogeneamente entre todos eritrócitos. Como se sabe a Hb Fetal não se co-polimeriza com ahb S e devido a isso o desencadeamento do processo da falcização é mínimo. Clinicamente os portadores dessa interação possuem eritrócitos com características falcizantes diferentes entre si - fato inverso ao que ocorre na anemia a falciforme - e desta forma não padecem das seqüelas da doença. Muitas vezes o diagnóstico desses portadores ocorre na fase adulta devido à ausência de anemia e sintomatologia. Geralmente o portador de Hb SS/PHHF tem a herança de genitores com os seguintes fenótipos: AS/PHHF e AS, ou AS/PHHF e AS/PHHF. Esfregaço de sangue periférico de pessoa adulta (32 anos de idade), diagnosticada como portadora de Hb SS/PHHF. A concentração de hemoglobina era de 11,8 b/dl. Observar anisocromia e um eritrócito em vias de se tornar falcizado. As alterações morfológicas nessa interação são muito discretas. Traço Falcêmico (O Portador Assintomático) ou Hb AS O portador do traço falcêmico tem o genótipo de Hb AS com concentração da Hb A sempre maior que a Hb S.. Em geral, a contração dahb A oscila entre 60 e 80% e a Hb S entre 20 e 40%. A Hb A2 apresenta-se com valores dentro da normalidade, e da mesma forma a Hb Fetal tem concentração normal após o sexto mês de vida. Como a Hb A inibe a polimerização da Hb S dentro dos eritrócitos, resulta que a morbidade clínica é nula. Não é incomum a associação da Hb AS com talassemia alfa - detectável pela presença de Hb H na eletroforese alcalina - e nesses casos pode ocorrer discreta anemia microcítica e hipocrômica.. Da mesma forma há muitos casos descritos da associação entre Hb AS edeficiência de glicose-6-fosfato desidrogenase (G-6-PD),, uma vez que ambas situações têm elevada prevalência entre negros. É possível que nesta associação possa ocorrer hematúria e embolia pulmonar. São bem documentados episódios de infarto esplênico em altitudes acima de metros, em pessoas com traço falciforme. Cuidados referentes ao controle de oxigenação em pacientes anestesiados para cirurgias são sempre necessários. 12
13 Por fim, o trabalho de conscientização ntização do portador do traço falcêmico em relação à sua prole é muito importante, uma vez que instruído a respeito poderá contribuir para o controle de nascimento de doentes falcêmicos, ou então ter conhecimentos adequados das conseqüências da doença e de seus cuidados básicos. O traço falciforme é uma situação cuja herança se deve principalmente a um dos genitores ter Hb AS e outro Hb AA. Porém, em famílias de doentes falcêmicos, o portador de traço pode ter pais com os seguintes genótipo: AS e AS; Ab menor e AS; AS e AC; AS e AD; SS e AA; S/b tal. e AA, entre outros. Esfregaço de sangue periférico de pessoa com traço falciforme. Os eritrócitos são normocíticos e normocrômicos. Histórico da Hb S Introdução Anteriormente à primeira descrição formal, as doenças falciformes certamente já eram conhecidas, mas não eram diagnosticadas pois suas principais manifestações eram comuns a outras doenças. Episódios de dor articular se assemelham ao reumatismo agudo. A icterícia e a hemólise são manifestações da malária e úlceras de perna são comuns em países de regiões tropicais. Segundo Konotey-Ahulu, esta doença já era do conhecimento de algumas tribos da África Ocidental, onde a denominação "reumatismo do frio" recebeu várias denominações relacionadas com uma condição crônica e recorrente. A tribo Ga se referia a essa condição como "Chwecheechwe", os Twi, como "Ahututuo", os Ewe como "Nuidudui"" e os Fante como "Nwiiwii". Konotey-Ahulu, neste mesmo trabalho, relata 13
14 informações de anciões destas tribos relatando vários casos de morte de indivíduos jovens da tribo, como óbitos devidos provavelmente à anemia falciforme. Entretanto, acredita-se que a primeira descrição da doença na África tenha sido feita por Africanus Horton (1874), que observou febre, crises de dor generalizadas e dores articulares que se exacerbavam nas estações de chuva, manifestações essas associadas a anormalidades no sangue periférico. Parece que vários grupos étnicos em Gana, incluindo os Twi, Ewe e Ga, identificaram a Anemia Falciforme como uma entidade que era caracterizada por alguns sintomas gerais, tais como: crises agudas de dor nos ossos e nas articulações, gravidade variável, tendência familiar e até que os pais de crianças afetadas pareciam normais. Estas descrições são particularmente precisas em uma determinada família da tribo Krobo onde o Dr. Konotey-Ahulu, em 1974, foi capaz de resgatar os dados referentes à existência da anemia falciforme em nove gerações sucessivas desde 1670, com retrospecto genotípico de todos os membros da família incluindo a idade do óbito de cada um. Não existe no entanto, qualquer evidência de que estes grupos étnicos relacionassem os vários sintomas a alguma doença do sangue. Outras comunidades da África negra não caracterizaram com esta fidelidade a anemia falciforme. Na Nigéria, a maior nação negra africana, a anemia falciforme aparentemente permaneceu desconhecida como uma entidade distinta até recentemente. Embora os vários dialetos nigerianos sejam ricos em palavras e expressões que descrevem vários dos sintomas comumente encontrados na anemia falciforme, estes termos não são, entretanto, específicos desta patologia. Assim, não existem evidências de que a anemia falciforme tenha sido identificada como uma entidade distinta nas sociedades tradicionais da Nigéria antes da sua descrição pela Medicina. Entretanto, as descrições mais modernas na imprensa médica estão inevitavelmente baseadas em características da patologia da mesma forma que as observadas pelos povos africanos há algumas centenas de anos. Duas observações, ainda anteriores ao relato de Herrick, apresentavam características muito sugestivas de doença falciforme. A primeira descrevia achados clínicos e de necrópsia de um escravo, nos Estados Unidos, que apresentava quadro de febre. A segunda referia-se ao caso de um homem, negro, que apresentava episódios de dor generalizadas, sintomas pleuríticos, icterícia e escaras nas regiões anteriores de ambas as pernas. Após sua morte, a necrópsia não localizou baço, mesmo após cuidadoso exame. Em 1910, o Dr. James B. Herrick descreve então, pela primeira vez, a presença de poiquilócitos observados numa preparação corada do sangue de um estudante de Odontologia. Este estudante também apresentava episódios de dor, que Herrick sugeriu, estivessem associados à presença dos eritrócitos anormais. Após a descrição original de Herrick, uma segunda observação foi feita no Hospital da Universidade de Virgínia. Uma mulher negra de 25 anos de idade apresentava a sintomatologia descrita por Herrick, além de cálculos biliares e bilirrubinúria. O terceiro caso, descrito no Hospital da Universidade de Washington, foi o de uma mulher de 21 anos. O quarto caso era semelhante aos descritos anteriormente quanto à apresentação clínica e laboratorial, ratificando a descoberta de uma nova entidade patológica. Nesse trabalho foi, pela primeira vez, utilizada a denominação anemia falciforme (Mason, 1922). 14
15 A demonstração do fenômeno de falcização in vitro foi feita por Emmel em 1917 usando preparações de sangue seladas entre lâmina e lamínula. A partir destes dados, foi estabelecida a natureza familiar da doença e sugerida a relação entre o processo de afoiçamento e a baixa tensão de oxigênio. Huck, em 1923, observou que o processo de afoiçamento era reversível. Mais tarde, Sydenstricker relatou a contagem elevada de reticulócitos e a notável hiperplasia eritróide na medula óssea, características nas doenças falciformes. O mesmo autor, posteriormente estudando vários casos, relatou a variabilidade no curso da doença associando à anemia e à icterícia. Estabeleceu o conceito de crise hemolítica, associada a um conjunto de achados clínicos, como a dor em articulações que, via de regra, não vinha vinculada a exacerbação da hemólise. As várias manifestações clínicas da anemia falciforme bem como a descrição dos diversos comprometimentos a nível sistêmico foram descritos nos anos subseqüentes. Os trabalhos de Han e Gillespie, em 1927, mostraram a dependência do oxigênio nas mudanças de forma dos eritrócitos. Estes dois pesquisadores atribuíram corretamente o defeito causador do fenômeno falcizante à hemoglobina e não ao eritrócito. Mais tarde, outros pesquisadores, demonstraram que as células com a forma de foice apareciam em suspensão de eritrócitos em tensões de oxigênio menores que 45 mm Hg e que, o fenômeno de falcização era inibido em soluções de ph superiores a 7,4. Por volta de 1940, foi demonstrado que o afoiçamento de eritrócitos, in vitro, ocorria em 7 a 10% dos afro-americanos e que este fenômeno ocorreria também in vivo. Ainda em 1930, são descritos "trombos frescos e organizados em vasos sangüíneos de pequeno e médio calibre e conseqüente infarto" (Steinberg, 1930). A presença de múltiplos infartos em rim e pulmões foi relatada. (Yater & Mollari, 1931). Em seu trabalho de 1934 Diggs, relata, pela primeira vez, estudos minuciosos, post mortem, de pacientes com anemia falciforme nos Estados Unidos e demonstra que repetidos infartos esplênicos levavam à progressiva fibrose desse órgão. O próprio Diggs, alguns anos mais tarde, estuda alguns parâmetros hematológicos em pacientes com anemia falciforme (HCM, fragilidade celular e morfologia minuciosa dos eritrócitos. Foi notada, pela primeira vez, a presença de eritrócitos que estavam irreversivelmente afoiçados mesmo após adequada reoxigenação. As décadas de 30 e 40 presenciaram uma grande variedade de registros dos aspectos clínicos associados à hemólise e vaso-oclusão. oclusão. As úlceras de perna foram relacionadas à anemia falciforme, nesse período. O priapismo foi pela primeira vez reconhecido como uma complicação na anemia falciforme em 1934, assim como lesões do sistema nervoso central (Diggs, 1934). Rápidos avanços no entendimento das várias facetas da doença ocorreram no período entre 1940 e Ham e Castle em 1940 estabeleceram o círculo vicioso o da patogenia do afoiçamento in vivo, isto é, resultados de afoiçamento em viscosidade sangüínea aumentada, que acarreta uma circulação mais lenta e menor oxigenação, que por sua vez causa mais afoiçamento. 15
16 O estudos de Sherman em 1946 levaram à constatação de que o afoiçamento era mais eficientemente induzido em células obtidas de pacientes anêmicos do que naqueles sem anemia e também que os eritrócitos em foice desoxigenados exibiam birrefringência ótica, um fenômeno que não era observado em células normais. Isto, provavelmente, foi a primeira evidência de que a forma desoxigenada da hemoglobina falcizante possuía uma estrutura organizada. Na metade da década de 40 estava claro que existiam duas classes distintas de indivíduos que apresentavam eritrócitos que se afoiçavam: a) os indivíduos assintomáticos com o traço falcêmico e b) os pacientes com sintomas e anemia falciforme. Neel, no ano de 1947, sugeriu que a diferença entre estas duas classes de indivíduos poderia ser explicada da mesma forma que a diferença entre talassemia maior e menor, ou seja, o traço falcêmico e a anemia falciforme eram, respectivamente, manifestações heterozigota e homozigota do mesmo gene e não o resultado da expressão de um gene cujo efeito era de variável intensidade. Dois anos mais tarde, Beet demonstrou a natureza hereditária da anemia falciforme e do traço falcêmico trabalhando em Zâmbia. No mesmo ano, Neel apresenta evidências similares em pacientes norte-americanos. Uma pediatra de Nova York, Janet Watson, e colaboradores sugeriram em 1948 que a pequena quantidade de células afoiçadas em recém nascidos afro-americanos americanos seria explicada por uma anormalidade da hemoglobina de adultos com anemia falciforme e que esta anomalia não estaria presente na hemoglobina de neonatos. Após este longo período de aquisição de conhecimentos, dois grandes avanços ocorreram ao final dos anos 40. Primeiramente em 1949, Linus Pauling demonstra que a hemoglobina obtida de pacientes com anemia falciforme difere eletroforeticamente da hemoglobina de indivíduos normais; e que os indivíduos portadores do traço falcêmico apresentam uma mistura das hemoglobinas normal (hemoglobina A) e anormal (hemoglobina S). O segundo avanço veio através da análise genética formal de famílias realizada por vários pesquisadores sadores com especial referência ao trabalho de Neel que demonstrou que ambos os pais de crianças com anemia falciforme apresentavam traço falcêmico. Em 1950 Harris descreve a forma de agulhas para os cristais de hemoglobina S com tamanho de 1 a 15 micra de comprimento. Nos anos que se passaram, algumas outras hemoglobinas com mobilidade eletroforética anormal foram descritas, sem, no entanto, serem capazes de causar o fenômeno de afoiçamento. A primeira delas foi a hemoglobina C, que foi observada associada à hemoglobina S em um paciente que apresentava uma forma mais branda de anemia falciforme. Por volta de 1953 Singer & Singer demonstraram que a polimerização ou gelificação da deoxihemoglobina seria inibida pela presença de hemoglobina fetal e favorecida na presença de hemoglobina C. Usando a técnica de "fingerprinting", Ingram em 1956 identificou a anormalidade molecular da hemoglobina "S", confirmando o conceito original de Pauling de que a anemia falciforme era uma doença molecular. Após a descoberta de que a hemoglobina S apresentava padrão eletroforético distinto da hemoglobina A, muitas outras variantes foram encontradas. Inicialmente, as letras do alfabeto foram utilizadas para designá-las; posteriormente, outras designações foram atribuídas às hemoglobinas anormais, como por exemplo, os nomes dos locais geográficos onde foram encontradas. 16
17 Considerando a distribuição geográfica e a incidência mundial dos diferentes tipos de hemoglobinopatias, várias interações entre elas são encontradas. Entre estas interações, as de maior importância, por causa das conseqüências clínicas, são aquelas relacionadas à hemoglobina S, que recebem a denominação genérica de doença falciforme. As doenças falciformes foram então caracterizadas como aquelas nas quais a falcização produz significantes manifestações clínicas. Entre estas figuram as hemoglobinopatias SC, a hemoglobinopatia SD, as S-talassemias e a anemia falciforme, sendo esta última designação reservada ao estado homozigoto para o gene. Assim sendo, o termo doença falciforme refere-se aos casos em que a hemoglobina S se polimeriza, tornando-se falcizada quando desoxigenada. Entre as hemoglobinopatias, as doenças falciformes são as mais freqüentes patologias chegando a atingir 1 em cada 500 indivíduos da raça negra (WHO, 1983). Estas doenças são associadas a manifestações clínicas de gravidade variável e a alta incidência de morbidade e mortalidade. Como exemplo, podemos citar que, sem medidas preventivas para infecções, a taxa de mortalidade em crianças com anemia falciforme atinge 25% até os cinco anos de idade (Leiken et al., 1989). Observa-se nestes pacientes uma maior susceptibilidade às infecções provocadas por germes encapsulados como Streptococcus pneumoniae e Haemophilus influenzae.. O risco de sepsis pelo Streptococcus pneumoniae é 600 vezes maior quando comparado a crianças normais, causado pela diminuição da capacidade de opsonização e pela hipofuncionalidade esplênica (Leiken et al., 1989). Uma outra infecção relacionada com grave manifestação clínica da anemia falciforme é a parvovirose, causada pelo parvovírus B19, que é associada a pelo menos 90% dos casos de anemia aplástica entre estes pacientes (Mallouh & Qudah, 1995). Causa freqüente de mortalidade precoce em crianças é o seqüestro esplênico agudo, circunstância em que, com o rápido aumento do baço a maior parte do sangue fica retida em seu interior, provocando choque hipovolêmico. Ainda entre os fatores que impedem crianças em idade escolar e adultos jovens de terem uma qualidade de vida satisfatória, são as freqüentes crises vaso-oclusivas oclusivas que, provocando danos teciduais e disfunções orgânicas importantes, também aumentam a mortalidade (Leiken et al., 1989). Embora não haja cura para as doenças falciformes algumas medidas de caráter clínico são indispensáveis para o conhecimento da patologia em questão, bem como para a diminuição da morbidade e mortalidade. Entre estas, as mais freqüentemente observadas na literatura são: 1. A orientação aos familiares, fornecendo-se explicações minuciosas sobre a doença, para o reconhecimento precoce das eventuais complicações, bem como sobre a necessidade de acompanhamento médico sistemático. 2. Uso profilático de antibióticos a partir do 3º mês de vida na prevenção das infecções. 3. Uso adicional, ao esquema de imunização tradicional, de vacinações específicas para Streptococcus pneumoniae, Haemophilus influenzae e hepatite. É preconizado também, na doença falciforme, a criação de programas voltados para o diagnóstico laboratorial precoce, o conhecimento das manifestações clínicas e programas de tratamento e profilaxia das complicações. 17
18 A Origem e Dispersão da Hb S Estudos antropológicos associados às análises biomoleculares, sugerem que o gene anormal para a síntese da Hb S pode ter ocorrido entre os períodos Paleolíticos e Mesolítico, aproximadamente há 50 e 100 mil anos, nas regiões centro-oeste oeste da África, Índia e leste da Ásia. A causa que motivou a mutação do gene da hemoglobina normal (Hb A) para o gene da Hb S ainda permanece desconhecida. Admite-se, porém, que a origem da Hb S foi multiregional, atingindo populações com diferentes características genéticas. Estudos realizados em populações africanas mostram que a expansão do gene da Hb S se deu efetivamente no período pré-neolítico entre 10 mil e 2 mil anos antes de Cristo, e foi marcada pela miscigenação entre os povos da região do Saara. Nesse período o Saara era composto por terras férteis, com agricultura desenvolvida para o abastecimento de suas populações. No período Neolítico ( anos a.c.) ocorreu a transmissão da malária causada pelo Plasmodium falciparum proveniente da região que hoje corresponde à Etiópia. Destaca-se durante esse período o aumento do processo migratório, o assentamento de grupos populacionais e o estabelecimento de grandes centros de civilização no vale do rio Nilo, bem como na Mesopotâmia, Índia e sul da China. No continente africano, a malária se propagou da costa oriental para a costa ocidental formando uma faixa coincidente com a alta prevalência de Hb AS. Esse fato levou Allison, em 1954, a estabelecer uma relação entre o efeito protetivo da Hb S em portadores heterozigotos (Hb AS) frente ao desenvolvimento da malária causada pelo Plasmodium falciparum.. Com a desertificação do Saara ocorrida no período Neolítico posterior (2.000 a 500 anos a.c.), suas populações migraram para outras regiões da África, atingindo aquelas banhadas pelo mar Mediterrâneo, fato que facilitou sua introdução no continente europeu notadamente no sul da Itália e Grécia. No período Medieval, entre os séculos 1 e 15, o gene da Hb S se expandiu para o leste e sudeste europeu. A introdução da Hb S nas Américas e no Brasil se deu com maior intensidade entre os séculos 16 e 19, motivado pelo tráfico de escravos africanos. A tabela resume a evolução cronológica da mutação do gene para Hb S. A trajetória dos negros africanos para o Brasil foi heterogênea, uma vez que o tráfico de escravos se desenvolveu ao longo de 300 anos, carreando escravos de quase toda a costa ocidental da África. Acredita-se que nesse período entraram pelos portos da Bahia e Rio de Janeiro, pelo menos 3,6 milhões de negros africanos, conforme pode ser verificado na tabela Por outro lado, a migração européia e asiática para o Brasil também foi diversificada destacando principalmente os imigrantes portugueses, italianos e espanhóis, além de várias outras raças de origens européia e asiática, conforme mostram as tabelas e Admitese, portanto, que esses contingentes populacionais também portadores de alterações genéticas, contribuíram para a introdução de vários tipos de hemoglobinas variantes, talassemias, enzimopatias e doenças de membrana eritrocitária, entre outras. Os processos miscigenatórios entre os diferentes povos que constituem a atual população brasileira ocorreram de forma gradual ao longo dos séculos, tornando-se abrangentes a partir do século 20. Este fato pode ser avaliado na literatura disponível, bem como em censos demográficos, de tal forma que até os anos 80 nossa população era composta por 54,2% de brancos, 39,2% de mistos (pardos e mulatos), 5,8% de negros, 0,6% de asiáticos e 0,2% de índios (tabela 2.2.5). Por essas razões, o gene da Hb S dispersou-se se amplamente na população brasileira, interagindo geneticamente com outras hemoglobinas variantes, talassemias, enzimopatias e esferocitose. 18
19 Tabela 2.2.1: Evolução Cronológica da Mutação do Gene para Hb S Período Paleolítico/Mesolítico Pré-Neolítico Neolítico Neolítico Posterior Medieval Moderno Contemporâneo Ano anos A.C anos A.C anos A.C. 700 anos D.C. século 15 Séculos Século 19 Evento Ocorrência da mutação do gene beta A para beta S na região centro-oeste oeste da África Crescimento populacional no Saara com marcante miscigenação entre povos diferentes O aumento da transmissão da malária acompanha a revolução agrícola, e exerce pressão seletiva para o gene beta S Desertificação do Saara promove intensa migração populacional para todas direções, e conseqüente dispersão do gene beta S Dispersão do gene beta S para o sudeste e leste europeu Dispersão do gene beta S pelo tráfico de escravos africanos para Américas (Brasil) Fase final do tráfico de escravos africanos (1880) e início da imigração européia para o Brasil Tabela 2.2.2: Migrações para o Brasil em diferentes períodos, com enfoque para indígenas e africanos. ANCESTRAIS DOS INDÍGENAS Período 8500 a.c a.c. Nº de indivíduos? Origem Mongólia, passando pelo estreito de Bering Migrações através do Oceano Pacífico e da América do Sul, no entanto, não devem ser totalmente afastadas AFRICANOS Período Nº de indivíduos Origem Século XVI: principalmente da área entre a ilha São Tomé e Angola Século XVII: principalmente de Angola, pelos portos de Luanda e Benguela. Outros da Costa da Mina 19
20 Período Nº de indivíduos Origem Aproximadamente 2/3 vieram de Angola, pelos portos de Luanda e Benguela, de uma região situada entre os cabos Lopez e Negro. Os restantes vieram da Costa da Mina e da região limitada pelos cabos Monte e Lopez, com Ajudá como porto principal Período Nº de indivíduos Origem Principalmente de Angola, em grande parte saindo pelo porto de Benguela fonte: Salzano F. M. Em busca das raízes. Ciência Hoje 1986; 5; Tabela 2.2.3: Migrações para o Brasil em valores quantitativos de portugueses, europeus, japoneses e chineses para o Brasil. EUROPEUS Período Nº de indivíduos Origem Período Nº de indivíduos Origem Período Nº de indivíduos Origem Período Nº de indivíduos Origem Período Nº de indivíduos Origem Portugal Portugal Europa em geral ASIÁTICOS RECENTES Japão China fonte: Salzano F. M. Em busca das raízes. Ciência Hoje 1986; 5;
21 Tabela 2.2.4: Valores estimativos da composição básica racial brasileira, dispostos cronologicamente desde ANO (*) (*) (*) (*) ORIGEM ÉTNICA OU RACIAL indígenas africanos portugueses italianos espanhóis europeus e asiáticos POPULAÇÃO 2.0 milhões 3.6 milhões 2.6 milhões 1.2 milhão 600 mil 1.0 milhão (*) 1944 foi o último censo realizado pelo IBGE, com procedência de estrangeiros para o Brasil Tabela 2.2.5: Variação estimada da composição étnica brasileira em 480 anos. GRUPO ÉTNICA OU GEOGRÁFICO Indígena Brancos Mistos Negros Asiáticos recentes fonte: Censos demográficos Salzano F. M. Em busca das raízes. Ciência Hoje 1986; 5; As Principais Descobertas Científicas A anemia falciforme é conhecida há séculos por povos de diferentes regiões da África. Exames radiológicos de ossos de pessoas que viveram na África há mais de anos mostraram lesões características dessa condição mórbida. É interessante destacar que os doentes eram identificados por tatuagem incisional para facilitar o diagnóstico e proibir o casamento com membros sadios do grupo. 21
22 Observações científicas da doença das células falciformes datam de um século e meio. Os trabalhos de Cruz Jobim, no Rio de Janeiro, em 1835; de Accioli, na Bahia, em 1908; de Lebby, em 1846; e de Hodenpyl, em 1896, nos Estados Unidos podem ser considerados como os pioneiros a respeito dessa doença. Entretanto, foi Herrick, em 1910, quem observou a forma anormal dos eritrócitos do sangue periférico de um estudante negro, procedente da Jamaica, portador de um grave quadro anêmico acompanhado de icterícia, complicações pulmonares e úlceras de membros inferiores. Quando o terceiro caso, semelhante ao descrito por Herrick, foi relatado, em 1917, cogitou-se a possibilidade de essa doença ser de origem hereditária pelo fato de se encontrar eritrócitos com idênticas deformações no sangue dos pais do paciente. O termo doença falciforme - "sickle cell disease" - foi empregado pela primeira vez, em 1922, por Mason. Este autor relacionou, inclusive, algumas características comuns entre os portadores dessa doença: todos eram negróides, apresentavam icterícia, anemia intensa, reticulocitose e eritrócitos falcizados no sangue periférico. Em 1927, Hahn e Gillespie demonstraram a dependência do fenômeno da falcização com a tensão de oxigênio, atribuindo o defeito à hemoglobina, e não somente ao glóbulo vermelho. Três anos depois, esses resultados foram confirmados in vivo,, quando se observou a formação de células falcizadas, especialmente quando a tensão de oxigênio caía abaixo de 40 a 45 mmhg. Em 1935, Diggs e Bill notaram que algumas dessas células se mantinham na forma falcizada, mesmo após a reoxigenação. Um ano depois, Ham e Castle propuseram uma explanação da fisiopatologia do processo de falcização. Essa teoria sustentava a hipótese de que ocorria um "ciclo vicioso de estase eritrocitária" nas células falcizadas do sangue periférico, causando um aumento de viscosidade sangüínea com demora do fluxo sangüíneo através dos capilares e diminuição da tensão de oxigênio, provocando mais falcização. Qualquer fato que aumentasse a viscosidade do sangue exacerbaria a falcização dos eritrócitos. Em 1946, Sherman demonstrou que as células falciformes, ao serem desoxigenadas, exibiam birrefringência óptica. Esse fato consistiu na primeira evidência de que a hemoglobina S, na ausência de oxigênio, apresentava uma estrutura ordenada no interior dos eritrócitos, e sugeriu a Linus Pauling que a Hb S era diferente da hemoglobina normal. Em 1949, Pauling e seus colaboradores mostraram essa diferença por meio da mobilidade eletroforética e atribuíram esse fenômeno à mudança de carga da globina (fig 2.3.1). Em 1956, Ingram, utilizando a técnica de "fingerprint" (eletroforese bidimensional, associada com cromatografia), demonstrou que a anormalidade química da Hb S era devida à substituição do ácido glutâmico pela valina, na posição número 6 da cadeia beta (b 6 Glu Val), produzindo a perda de duas cargas negativas por molécula da hemoglobina (fig ). 22
23 Figura Eletroforese de hemoglobinas em acetato ato de celulose, tampão alcalino, mostrando a separação dos genótipos AA, AS e SS. Figura Fingerprinting das hemoglobinas AA e SS, acima a seta 1 mostra a posição normal do péptido que contém o aminoácido glutâmico na posição 6 da globina beta (Hb AA). Abaixo a seta 2 mostra a mudança do péptido, devido a troca do aminoácido glutâmico pela valina na posição 6 da globina beta (Hb SS). 23
24 A partir de 1978, com as observações iniciais de Kan e Dozy, novo impulso foi dado ao estudo da Hb S, pela introdução de técnicas de biologia molecular. Por meio de enzimas obtidas de bacteriófagos específicos, foi possível admitir que a Hb S teve múltiplas origens. Esses estudos foram realizados em populações da raça negra da África, Jamaica e em afro-americanos, americanos, e pela análise do agrupamento dos genes tipo beta do cromossomo 11 concluíram que há, pelo menos, cinco tipos de Hb S: SS-Benin, SS-Bantu, SS-Senegal, SS-Camarões, SS-Árabe-indiano, todas com resultado final da troca de ácido glutâmico por valina, na posição o 6 da globina beta, porém, com diferentes extensões de lesões moleculares ocorridas ao longo do agrupamento dos genes beta, delta, gama-alanina, alanina, gama-glicina, glicina, pseudogene beta e épsilon. Essas descobertas esclareceram a diversidade clínica que se observa em diferentes doentes com anemia falciforme, alguns com evolução clínica benigna, e outros com constantes complicações. Os estudos que sucederam as descobertas de Kan e Dozy evoluíram para outros objetivos, entre os quais se destacam aqueles que visam ao uso da quimioterapia para estimulação específica da síntese de Hb Fetal pelos genes gama. Esses estudos se basearam no fato de que, quando um indivíduo com anemia falciforme (Hb SS) tem, associada a esta condição, um outro defeito genético caracterizado pela persistência hereditária de Hb Fetal (PHHF), com razoável elevação do nível de Hb Fetal, suas condições fisiopatológicas são muito melhores do que as daquele que é apenas homozigoto SS. Assim, a busca de drogas que pudessem estimular os genes gama "adormecidos" após o nascimento, fez com que De Simone e seus colaboradores, em 1982, utilizassem a droga antileucêmica 5-azacitidina que produzia sensível aumento da síntese de Hb Fetal nos doentes leucêmicos. Essa droga, utilizada em doente com anemia falciforme, também causava a elevação da Hb Fetal, cuja presença nos eritrócitos com Hb S "inibe" o processo de falcização. Pelo fato de 5-azacitidina ser tóxica e potencialmente carcinogênica, seu uso foi desestimulado, mas a busca de outras drogas estimulantes dos genes gama continuou com a hidroxiuréia e, atualmente, com os butiratos. Finalmente, destaca-se se que com a evolução tecnológica oferecida pela biologia molecular, especialmente as técnicas de isolamento e clonagem de genes de globina, tem estimulado estudos no sentido da realização da terapia gênica. A terapia gênica se resume na correção das alterações ou substituições das bases nitrogenadas no DNA ou no RNA mensageiro, revertendo 24
25 o defeito desde as células hematopoiéticas mais primitivas. Além disso, essa tecnologia tem permitido também a realização de análises de DNA da globina beta, visando à prevenção prénatal de recém-nascidos com doença falciforme. Resistência das Células com Hb S ao Plasmodium faciparum Há ampla aceitação científica de que a alta freqüência da anemia falciforme, talassemias e deficiência de glicose-6-fosfato desidrogenase (G6PD) observada em algumas áreas tropical e subtropical da África e Ásia se devem à resistência contra os efeitos deletérios da malária (Plasmodium falciparum) conferidos aos portadores heterozigotos dos traços falcêmicos (Hb AS) e talassêmico, bem como aos deficientes de G-6PD (fig ). Figura Acima: distribuição da malária causada por P. falciparum na África e Ásia e Oceania. Abaixo: distribuição da anemia falciforme, talassemia e outras hemoglobinopatias em áreas coincidentes à da malária. Especialmente com referência à possível proteção dos heterozigotos falcêmicos contra o P. falciparum,, Allison, 1954, obteve três diferentes formas de evidências dessa relação. Primeiro, ele demonstrou que crianças com traço falciforme tinham baixa parasitemia; segundo, ele observou que adultos com traço falcêmico inoculados com P. falciparum não tinham infecções 25
26 tão freqüentes quanto àqueles com hemoglobinas normais (Hb AA); e terceiro, ele mostrou que a freqüência do gene beta S (b S ) na África oriental está relacionada com a endemicidade da malária. Outras evidências deram suporte à teoria de Allison, e uma em particular se refere ao fato de que os óbitos ocorridos os por malária cerebral na infância era muito menos comuns em crianças com traço falcêmico quando comparado com crianças portadoras de hemoglobinas normais. Qual ou quais as bases científicas que dão consistência à hipótese malária? Luzzato e colaboradores, em 1970, sugeriram que quando o parasita entra em eritrócitos contendo Hb S, utilizam o oxigênio celular e desencadeiam a polimerização da deoxi-hb S e, conseqüentemente, a falcização do eritrócito. O eritrócito falcizado é seqüestrado no sistema retículo endotelial (SRE) do baço ou de outros órgãos, impedindo que o P. falciparum complete seu ciclo vital. Pesquisas realizadas por Friedman, 1978, demonstraram que eritrócitos com Hb S cultivados "in vivo" e sob baixa tensão de oxigênio similar ao do sangue venoso, impediam o desenvolvimento do P. falciparum.. Por outro lado, pesquisas realizadas em eritrócitos de pessoas com deficiência de G-6PD concluíram que a oxidação que se processa no interior da célula é um outro fator que impede o desenvolvimento do ciclo do P. falciparum. Recentes pesquisas realizadas em nosso laboratório mostraram que o nível de oxidação da Hb S no traço falcêmico é 2,5 vezes superior ao dos eritrócitos com hemoglobinas normais, e certamente a contínua oxidação causada pela metahemoglobina obina S (meta Hb S) deve ser deletéria ao P. falciparum.. O processo da oxidação da Hb S está exposto com detalhes no item 4.3 (os efeitos oxidativos da deoxi-hb S). Genética, Química E Biologia Molecular Da Hb S Mutação e Consequências Estruturais na Globina Beta S A Hb S é causada por uma mutação do gene beta da globina, produzindo uma alteração estrutural na molécula. Por ser uma anomalia da globina beta, as características clínicas do estado homozigoto só serão percebidas após a estabilização da produção das globinas que ocorre por volta do sexto mês de vida. No gene da globina beta S, há a substituição de uma base nitrogenada do códon GAG para a GTG, resultando na substituição do ácido glutâmico (Glu) pela valina (Val) na posição número 6 da globina beta (figura 3.1.1). A valina é um aminoácido neutro (pi ~ 6) e o ácido glutâmico é carregado negativamente (pi=2,8). Essa troca altera o pi da Hb S, tornando-a a carregada menos negativamente (pi da Hb A= 6,8; pi da Hb S > 6,8) fato que resulta em uma mobilidade mais lenta da Hb S, quando comparada com a Hb A em eletroforese alcalina (ph 8 a 9), conforme mostra a figura A troca de aminoácidos que resulta na Hb S abala estruturalmente a molécula, pois se na Hb A o ácido glutâmico da posição 6 da globina beta auxilia no afastamento das moléculas desoxigenadas de hemoglobinas, a entrada da valina nesta posição favorece a polimerização sob condições de baixo teor de oxigênio, resultando na deformação do eritrócito com a forma afoiçada (figura 3.1.3). 26
27 Figura Modelo da estrutura terciária da globina beta com a seta indicando a posição do sexto aminoácido, em que o ácido glutâmico é substituído pela valina. Figura Eletroforese de hemoglobinas em acetado de celulose, tampão alcalino (ph 8.5). A mobilidade das hemoglobinas se desenvolve do pólo negativo para o positivo. A análise eletroforética de três amostras de sangue de pessoas com o traço falciforme (Hb S) mostra que a Hb A se move com maior velocidade em direção ao pólo negativo quando comparada com a Hb S. A Hb A tem o ácido glutâmico na posição 6 da globina beta, fato que a deixa com maior número de 27
28 cargas negativas. A Hb S é produto da substituição do ácido glutâmico pela valina - um aminoácido neutro, assim a Hb S é menos carregada negativamente, fato que influi no seu deslocamento mais lento em direção ao pólo positivo. Figura Deformação do eritrócito com Hb S, geralmente caracterizado pela forma afoiçada. As consequências provenientes da desoxigenação da Hb S resulta na agregação ação de moléculas...2ß S 2 que se juntam e se cristalizam facilitando contatos entre aminoácidos distantes entre si. Esses contatos, realizados pela valina na posição 6 da globina beta com fenilalanina da posição 85 e leucina da posição 88 da mesma globina, promovem a formação de longos polímeros em forma de feixes de moléculas de Hb S agregados. A desestruturação da molécula da Hb S desoxigenada é, portanto, o principal desencadeamento do processo da falcização dos eritrócitos com Hb S. Informações detalhadas das desse processo estão apresentadas no item 4 desse capítulo (Fisiopatologia da Hb S). O Fenótipo Falcêmico A doença falciforme agrupa vários tipos de associações entre a Hb S e outras hemoglobinas variantes, com talassemias alfa e beta, além do estado de homozigose (Hb SS). O uso da designação doença falciforme sintetiza situações clínicas e patológicas comuns, com variável gravidade, cujo conjunto caracteriza o fenótipo da doença. Assim, o fenótipo falcêmico se destaca principalmente por anemia hemolítica crônica, crises de dores, icterícia, infecções constantes, e graus diversificados de morbidade e mortalidade. Desde o início da descoberta científica da anemia falciforme tem sido observado ampla diversidade clínica entre os doentes, fato que atrai o interesse de pesquisadores na busca de explicações para os diversos fenômenos decorrentes da falcização. Com o avanço da tecnologia laboratorial foi possível caracterizar diferentesgenótipos que explicam em parte a diversidade genotípica da doença. Entretanto, o fenótipo tem um valor histórico, enriquecido por detalhes que foram obtidos dos muitos casos descritos na literatura científica. 28
29 Os Genótipos Falcêmicos Com a aplicação da técnica de eletroforese no estudo das hemoglobinas humanas foi possível identificar várias combinações entre diferentes hemoglobinas variantes com hemoglobina normal, com talassemias alfa e beta, e dessa forma estabelecer os genótipos das hemoglobinas. Os genótipos falcêmicos incluem todas associações em que faz parte a Hb S. Entre os principais genótipos falcêmicos destacam-se os seguintes: 1. Hb AS (a A 2 b A 2 / a A 2 b S 2 ) - traço falciforme ou falcemia heterozigota 2. Hb SS (a A 2 b S 2 ) - anemia falciforme 3. Hb SD (a A 2 b S 2 / a A 2 b D 2 ) - doença da Hb SD 4. Hb SC (a A 2 b S 2 / a A 2 b C 2 ) - doença da Hb SC 5. Hb S / talassemia b 0 ou Hb SF (a A b S / a A g ) - microdrepanocitose ou S/Beta zero talassemia 6. Hb S / talassemia b + ou Hb SFA (a A 2 b S 2 / a A 2 b A 2 / a 2 g 2 ) - microdrepanocitose ou S/Beta mais talassemia 7. Hb SS / talassemia alfa (a A 2 b S 2 / b S 4 ) ou Hb SH 8. Hb S / P.H.H.F. ou Hb SF (a A 2 b S A 2 / a 2 g 2 ) - Hb S associada à persistência hereditária da Hb Fetal Além desses genótipos descritos na população brasileira e em várias regiões do mundo, há outros genótipos mais raros, restritos a alguns povos e regiões, como são os casos dos genótipos Hb SE (sudeste asiático), Hb SO Arábia (Arábia Saudita e Emiratos Árabes), Hb S/Menphis (USA). A tabela resume as principais características clínicas e laboratoriais dos genótipos de Hb S. Detalhes sobre as alterações laboratoriais poderão ser obtidos no item 5 (Alterações Laboratoriais nas Doenças das Células Falciformes). A seguir, apresentamos breve resumo sobre os principais genótipos descritos na população brasileira. Hb AS - Traço Falciforme ou Falcemia Heterozigota O traço falciforme caracteriza o portador assintomático, pois é o heterozigoto falcêmico representado por Hb AS. Assim, o portador de Hb AS não padece de doença e não apresenta alterações hematológicas (tabela 3.3.1). Os processos vaso-oclusivos oclusivos sob condições fisiológicas normais inexistem, e portanto não há mortalidade e nem morbidade seletivas. Geralmente detecta-se o portador de Hb AS em estudos populacionais, pulacionais, ou análise devido à presença do gene da hemoglobina S em algum membro da família. 29
30 Figura Eletroforese de hemoglobinas em acetato de celulose, ph 8,5, de três amostras de hemolisado de eritrócitos. (1) Hb A + Lepore; (2) Hb AA; (3) Hb AS. A Hb S e Hb Lepore apresentam a mesma mobilidade eletroforética em ph alcalino (ph 8 a 9). A Hb Lepore geralmente tem concentração baixa (10 a 15%) em relação à Hb S do traço falcêmico (20 a 45%). Na Hb A + Lepore é comum a Hb A 2 estar diminuída e o portador apresentar anemia microcitica e hipocrômica, similar à da talassemia beta menor. Figura Eletroforese de hemoglobinas em agarose ácida, ph 6.0, de três amostras de solução de hemoglobina. (1) Hb AS; (2) Hb AA; (3) Hb AC. Neste tipo de eletroforese o sentido se faz do pólo positivo para o pólo negativo, devido ao tampão ácido. A eletroforese em agarose ácida é aplicada para diferenciar a Hb S da Hb D, e a Hb S da Hb Lepore, todas com igual posição na eletroforese alcalina. Na eletroforese ácida, as hemoglobinas D e Lepore migram na mesma posição da Hb A, enquanto a Hb S se separa da Hb A. Outra característica da eletroforese ácida é a separação da Hb Fetal, que migra com maior mobilidade em relação à Hb A. 30
31 Figura Teste de solubilidade para diferenciar Hb S de outras hemoglobinas. A Hb S (AS, SS, SC, S/tal. b, etc.) é insolúvel em soluções hipertônicas quando submetida à redução com ditionito de sódio. É um método qualitativo para indicar, ou não, presença de Hb S sem qualificar o genótipo. O tubo da esquerda (transparente) é de Hb AA, e o da direita é de Hb AS. Geneticamente a condição heterozigota se deve à herança do gene da globina b S por parte de um dos pais, juntamente com o gene da globina b A proveniente do outro. Nessa condição, a concentração da Hb A é sempre mais elevada do que a Hb S (figuras e 3.3.1). O diagnóstico laboratorial é feito por técnicas eletroforéticas em ph alcalino (8 a 9) ou ph ácido (5 a 6,5), conforme mostram as figuras e Outros testes que apenas acusam a presença de Hb S, sem identificar o seu genótipo (AS, SS, SC, etc.), são os testes de falcização e solubilidade (figura 3.3.3). O traço falciforme pode estar associado ocasionalmente a condições clínicas graves, que incluem: hipotermia, hematúria, aumento do risco às infecções do trato urinário durante a gravidez e retardo constitucional da puberdade. Os portadores de Hb AS, quando iniciam quadro de hipóxia, raramente desenvolvem sintomas relacionados à vaso-oclusão. oclusão. No entanto, existem relatos de morte súbita e complicações clínicas em portadores de traço falciforme expostos a condições de baixa tensão de oxigênio, como ocorre em anestesias sem eficiente suplementação de oxigênio durante e após os processos cirúrgicos, em esforços físicos extenuantes associados à desidratação e em condições adversas de trabalho, por exemplo, locais com baixa tensão de oxigênio. 31
32 Tabela Aspectos laboratoriais e clínicos de hemoglobinopatias S. Genóti po AS Anemia Esplenomeg alia Nenhu ma Não SS Grave Sim. Raro após a infância SC S/b-tal SD SO ARÁBI A SE Discreta a modera da Modera da ou grave Discreta a modera da Grave Comum Ocasional Comum Discreta Não Sim. Raro após a infância Outras Característi cas Clínicas Geralmente nenhuma Crises de dores irregulares. Infartos ósseos. Aumento de infecções bacterianas Crises de dores irregulares. Infartos ósseos. Retinopatia nos adultos Crises de dores irregulares. Infartos ósseos Pode haver artralgias. Dores abdominais Similar à Hb SS Geralmente nenhuma Sangue Periférico Falcizaç ão Clínica Normal Positivo Nenhu ma Formas falcizadas. Células em alvo. Hipocromia. Policromasi a Anisopoiquilocito se, células em alvo. Hipocromia. Policromasi a Anisopoiquilocito se, células em alvo. Hipocromia. Policromasi a Formas falcizadas. Células em alvo. Policromasi a Similar à Hb SS Hipocromia. Positivo Positivo Positivo Positivo Positivo Positivo Grave Discreta ou modera da Modera da a grave Discreta a modera da Modera da a grave Observaç ões Pode ocorrer hematúria Incapacida de progressiv a. Diminuiçã o do período de vida Gravidade clínica durante a gestação. Cristais intracelula res Ausência de Hb A na S/b 0 -tal. Distinguese Hb SS da Hb SD por eletrofores e em ágarácido Pode ser confundid a com Hb SC. Distinguese por eletrofores e em ágarácido Discreta Distinguese da Hb 32
33 Microcitose SC por eletrofores e em ágarácido S/a-tal. Nenhu ma a discreta Não Geralmente nenhuma Hipocromia. Microcitose Positivo Nenhu ma a discreta Presença de Hb H na eletrofores e S/PHH F Nenhu ma a discreta Não Não há infartos recorrentes Normal. A Hb F apresentase distribuída homogenea -mente por eluição ácida Positivo Nenhu ma a discreta Por eletrofores e confundese com S/b 0 -tal. Anemia Falciforme (Hb SS) Em contradição com os portadores de traço falciforme, a história de pacientes com anemia falciforme revela, quase invariavelmente, uma doença continuamente agressiva, caracterizada por repetidos episódios agudos, geralmente do tipo vasculoclusivo, com ou sem efeitos mielodepressivos (deficiência temporária da medula óssea em produzir eritrócitos). Os sinais e sintomas são especialmente causados por: anemia crônica, episódios de agravamento de anemia, dores nas juntas e nas extremidades de mãos e pés, dores abdominais, necrose asséptica da medula óssea, acidentes cerebrovasculares, infartos pulmonares, etc. Os recém-nascidos, portadores de anemia falciforme, geralmente não apresentam os problemas causados por essa hemoglobinopatia devido à alta concentração de Hb Fetal presente nos eritrócitos, durante as primeiras semanas de vida. Entretanto, os sintomas e os efeitos dessa anemia podem ocorrer quando a mãe - portadora de Hb SS - apresenta anemia e complicações durante a gravidez. A doença é detectada durante os primeiros anos de vida, com manifestação de anemia grave, hepatomegalia, esplenomegalia, ou por crises dolorosas manifestadas por inchaço e calor nas mãos ou pés e que são conhecidas por síndromes de mãos e pés. Essa doença apresenta um curso constante, em que se combinam os sinais, sintomas e limitações da anemia persistente com a ocorrência freqüente de vários tipos de crises. Os exames laboratoriais indicam a presença de anemia grave (tabela 3.3.2). Os valores de hemoglobina variam de 5 a 9 g/dl, que associados a uma acentuada queda de hematócrito e contagem de eritrócitos itos resultam em índices normocíticos e normocrômicos. No esfregaço de sangue periférico observa-se variações nos tamanhos e nas formas dos eritrócitos. De 0,5 a 20% dos eritrócitos estão falcizados; formas de células em alvo, microcitos e alguns esferócitos também podem ser observados no sangue periférico. Os reticulócitos estão geralmente elevados acima de 10%. Os normoblastos são freqüentemente identificados no sangue periférico, bem como pontilhados basófilos e corpos de Howell-Jolly. A leucocitose é moderada ( a 33
34 17.000/mm 3 ), contendo alguns granulócitos (neutrófilos) imaturos na circulação periférica. As plaquetas podem estar discretamente elevadas. O exame da medula óssea apresenta hiperplasia normoblástica e áreas de medula vermelha ativa podem ser encontradas em regiões geralmente ocupadas por medulas amarelas. A coloração de ferro na medula revela sobrecarga desse mineral nos eritrócitos e eritroblastos. Haptoglobinas livres (proteínas encontradas no plasma normal que especificamente se liga e transporta hemoglobina extracelular) estão geralmente ausentes. A clínica dos pacientes portadores de anemia falciforme é descrita no capítulo 6 (Controle Clínico das Doenças Falciformes) Tabela Alterações laboratoriais específicas na anemia falciforme. Concentração da Hb S 90 a 100% Dosagem de Hb Fetal 2 a 10% Tipo de anemia Dosagem de Hb g/dl 5-9 Reticulócitos Leucócitos Plaquetas Fragilidade osmótica Fragilidade térmica e mecânica Bilirrubina indireta Urobilinogênio urinário Urobilinogênio fecal Hematúria Ácido úrico sérico Fosfatase alcalina sérica Medula óssea Ferro sérico Normocítica e normocrômica 5 a 30% acima de 10 mil durante as crises. Pode ocorrer desvio à esquerda. plaquetose, com formas anormais diminuída aumentada elevada, acima de 5 mg/dl elevado elevado freqüente pode estar elevado elevada nas crises hiperplasia das células eritróides normal ou amentado 34
35 Hb SD - Doença da Hb SD A Hb D é uma hemoglobina variante com a mesma mobilidade eletroforética da Hb S, porém sem causar danos fisiológicos ou morfológicos ao eritrócito. Há vários tipos diferentes de Hb D descritos em diversas regiões: Hb D Punjab ou Los Angeles (b 121 glutâmico glutamina), Hb D Ibadan (b 87 treonina lisina), Hb D Bushman (b 16 glicina arginina) e Hb D Iran (b 22 glutâmico glutamina). Desses tipos a Hb D Punjab ou Los Angeles é a mais comum de ser identificada em várias regiões do mundo. No Brasil a Hb AD Punjab é prevalente na proporção de 1 caso para cada analisados, em média. Assim, é possível a associação da Hb S com Hb D Punjab em nossa população, e essa dupla heterozigose é conhecida por Hb SD ou doença da Hb SD. A anemia é similar a Hb S/talassemia beta, com graus variáveis entre discreta a moderada, concentração de hemoglobina total entre 9 a 13 g/dl, VCM normal e ausência de Hb Fetal. Ocasionalmente o doente SD pode apresentar esplenomegalia, e da mesma forma pode ocorrer artralgias e dores abdominais. No esfregaço sangüíneo a morfologia eritrocitária mostra células em falcização, células em alvo e policromasia (figura 3.3.4). Pelo fato da Hb SD ter a mesma mobilidade eletroforética que a Hb SS em tampão alcalino, a melhor forma de diferenciá-las é por meio de eletroforese de hemoglobina em gel de agarose com tampão ácido. Neste tipo de eletroforese ácida a Hb D separa-se da Hb S, posicionando-se na mesma região da Hb A. Figura Esfregaço de sangue periférico de paciente com Hb SD - Doença da Hb SD. Observar células em alvo, eritrócito em falcização, esferócitos, etc. A presença de esferócitos se deve à hemólise. Hb SC - Doença da Hb SC A Hb C é uma hemoglobina variante comum na costa ocidental da África, especificamente na região noroeste daquele continente. No Brasil, a prevalência do genótipo Hb AC é em média 0,5%, e entre pessoas negras chega a 3%. Há dois tipos de Hb C descritas na literatura, a Hb C 35
36 (b6 glutâmico lisina) e Hb C Harlem (b73 aspártico asparagina + b6 glutâmico valina). A Hb C Harlem é muito rara e por ter dupla mutação, uma das quais similar à da Hb S, pode causar discreta falcização eritrocitária. Assim, a Hb C é a forma mais freqüente de associação com a Hb S, causando a doença da Hb SC. A anemia a é variável de discreta a moderada, com a hemoglobina total situando-se se entre 9 e 13 g/dl. O VCM é normal, apesar da moderada alteração morfológica dos eritrócitos no esfregaço sangüíneo. É comum a presença de células em falcização, eritrócitos em alvo (codócitos), hipocromia, policromasia e cristais de Hb C (figura 3.3.5). Os doentes com Hb SC apresentam crises de dores intermitentes, infartos ósseos, e retinopatia nos adultos. Gestantes portadoras de Hb SC devem ter acompanhamento especial durante a gestação. A análise laboratorial específica é realizada por meio de eletroforese de hemoglobina em tampão alcalino, com a Hb C separando-se da Hb S e posicionando-se junto com a Hb A 2 (figura 3.3.6). Em eletroforese de hemoglobina em gel de agarose com tampão ácido a Hb C é mais lenta que a Hb S e posiciona-se se junto ao local de aplicação da amostra (figura 3.3.2). Figura Eletroforese de hemoglobinas em agarose ácida, ph 6.0, de três amostras de solução de hemoglobina. (1) Hb AS; (2) Hb AA; (3) Hb AC. Neste tipo de eletroforese o sentido se faz do pólo positivo para o pólo negativo, devido ao tampão ácido. A eletroforese em agarose ácida é aplicada para diferenciar a Hb S da Hb D, e a Hb S da Hb Lepore, todas com igual posição na eletroforese alcalina. Na eletroforese ácida, as hemoglobinas D e Lepore migram na mesma posição da Hb A, enquanto a Hb S se separa da Hb A. Outra característica da eletroforese ácida é a separação da Hb Fetal, que migra com maior mobilidade em relação à Hb A. 36
37 Figura Esfregaço de sangue periférico de paciente com Hb SC - Doença de Hb SC. O destaque desta foto é a presença de cristais de Hb C acumulados na periferia de um eritrócito (seta). Figura Eletroforese de hemoglobinas em acetato de celulose, ph 8.5. Da esquerda para direita (1) AF; (2) AF; (3) SC; (4) AA; (5) AA; (6) SC. As duas primeiras amostras, com Hb Fetal elevada, são de pacientes com talassemia beta maior que receberam transfusão de sangue com hemoglobinas normais. Outra observação mais detalhada mostra que adiante da Hb A nas aplicações 1, 2, 4 e 5 há em todas elas uma fração rápida e difusa, com baixa concentração, onde estão concentradas as hemoglobinas. A1a, A1b e A1c, sem que seja possível distinguí-las. Na Hb SC as concentrações de Hb S e Hb C são equilibradas. 37
38 Hb S / Talassemia β 0 ou Hb SF (Micro-Drepanocitose) A ocorrência da interação entre Hb S e talassemia b no Brasil se deve ao alto grau de miscigenação entre as etnias que participaram da formação do brasileiro. Embora a Hb S seja muito prevalente por meio de genótipo AS entre africanos, outros povos também apresentam prevalências elevadas, por exemplo: sul da Itália, Arábia Saudita e Emiratos Árabes. Por outro lado, a talassemia beta que apresenta alta prevalência do seu estado heterozigoto (Hb A/btal) entre povos dos países banhados pelo mar Mediterrâneo, teve ao longo dos anos a sua disseminação entre povos da península ibérica (Portugal e Espanha) e África. Por essas razões, o genótipo S/talassemia beta pode ser encontrado entre pessoas soas de cor branca e de cor negra. A Organização Mundial da Saúde estima que nascem anualmente no Brasil perto de 600 crianças com o genótipo S/talassemia beta. A Hb S/talassemia beta pode ser identificada laboratorialmente em dois genótipos distintos, a Hb S/talassemia b 0 e Hb S/talassemia b +. A talassemia b 0 é indicativo que o gene da globina beta está totalmente inativo para sintetizar a Hb A, assim os portadores do genótipo Hb S/tal b 0 apresentam apenas as hemoglobinas S (com concentrações variáveis entre 70 e 90%), Fetal (5 a 20%) e Hb A 2 (entre 4 e 7%). Essas hemoglobinas podem ser facilmente fracionadas por eletroforese de tampão alcalino em acetato de celulose ou em gel de agarose. A anemia nos pacientes com o genótipo S/b 0 talassemia é geralmente grave, com a concentração de hemoglobina total oscilando entre 7 e 10 g/dl. O VCM e HCM estão diminuídos e a análise da morfologia eritrocitária mostra acentuada aniso-poiquilocitose, com microcitose, esquisócitos, eritroblastos, policromasia e células em alvo, além de células em fase de falcização (figura 3.3.7). Figura Esfregaço de sangue periférico de paciente com Hb S/talassemia b 0, ou Hb SF. Por meio desse esfregaço observa-se presença de células microcíticas, hipocrômicas e falcizadas, daí a denominação de micro-drepanocitose. 38
39 Hb S / Talassemia β + ou Hb SFA A introdução do genótipo Hb S/talassemia b + é a mesma descrita no item (Hb S/tal. b 0 ). O genótipo específico de Hb S/tal. b + se deve quando o gene herdado da globina beta sintetiza apenas parte da Hb A e, por isso, a concentração da Hb A é menor que da Hb S (figuras e 3.3.9). A Hb A 2 geralmente está discretamente elevada. Por vezes é possível identificar na eletroforese de hemoglobina em tampão alcalino a presença de Hb Fetal entre 5 a 10%. Figura Eletroforese de hemoglobinas em acetato de celulose, ph 8.5. Da esquerda para a direita: (1) Hb AA; (2) Hb AA; (3) Hb AS. Observar que a Hb AS apresenta maior concentração da Hb S em relação à Hb A. Esse fato se deve ao gene da globina beta A estar parcialmente "bloqueado" para sintetizar Hb A, caracterizando a talassemia b +. Se o gene da globina beta A estivesse íntegro, a concentração da Hb A seria maior que a da Hb S. Na maioria dos casos de Hb S/tal.b + a Hb A está elevada, como mostra a figura. 2 39
40 Figura Eletroforese de hemoglobinas em acetato de celulose, ph 8.5. Da esquerda para a direita: (1) A + A 2 aumentada; (2) Hb AJ; (3) Hb AJ; (4) Hb S/tal.b +. Observar a Hb A 2 aumentada na Hb S/tal.b +. A primeira amostra aplicada é de um portador de talassemia beta menor. A segunda e terceira amostras pertencem a dois portadores de Hb J Oxford em heterozigose (AJ). A ocorrência da anemia nos portadores desta dupla heterozigose é de grau moderado, com a hemoglobina total variando entre 9 e 11 g/dl. Na análise da morfologia eritrocitária é possível observar moderada aniso-poiquilocitose, com micrócitos, dacriócitos, codócitos, policromasia, e algumas células em falcização. O VCM e HCM estão diminuídos. O genótipo Hb S/tal. b + é pouco freqüente em nossa população quando comparado com o genótipo Hb S/tal. b 0. É importante destacar que ocorre certa confusão na análise laboratorial por eletroforese de hemoglobina quando se examina amostra de sangue de paciente com anemia falciforme (Hb SS) que recebeu sangue normal (Hb A) por transfusão. Nestes casos, o valor quantitativo de Hb S em relação à da Hb A transfundida se parece com o resultado eletroforético do genótipo b S/tal. b +. Portanto, é fundamental ser informado se o sangue do paciente a ser analisado foi ou não transfundido. Hb SS / Talassemia Alfa ou Hb SH A talassemia alfa é uma alteração que pode ter origem genética ou adquirida. A origem genética está bem definida e se deve à falha na síntese de globinas alfa, devido à lesão molecular de um ou mais genes alfa dos quatro normalmente dispostos nos dois cromossomos 16 (aa/aa) de cada pessoa. A causa adquirida da talassemia alfa tem sido relatada em pacientes com doenças linfo ou mieloproliferativas, cuja prevalência chega a 60% de talassemia alfa entre eles. Entretanto, pouco se sabe de que forma a talassemia alfa foi adquirida. Em ambos os casos, a talassemia alfa se deve à lesão de apenas um gene alfa (-a/aa), ou lesões de dois (-a/-a;--/aa)/aa) e de três (--/-a) genes alfa. A lesão de quatro genes alfa (--/--) é restrita à causa genética. 40
41 Especialmente nos negros, a talassemia alfa resulta geralmente na deleção de um gene ou de dois genes alfa. Estudos realizados nos Estados Unidos da América indicam que cerca de 30% dos negros tem talassemia alfa. No Brasil, Sonati, em 1992, descreveu a prevalência de 21,3% de talassemia alfa heterozigota (-a/aa) entre os negros. A interação de anemia falciforme com talassemia alfa representa um fator modulador dos parâmetros hematológicos, com elevação da contagem de eritrócitos e redução dos índices hematimétricos VCM (volume corpuscular médio), HCM (hemoglobina corpuscular média) e CHCM (concentração da hemoglobina corpuscular média), em relação ao doente com anemia falciforme. Fisiologicamente, a redução da concentração da hemoglobina (Hb S) corpuscular média diminui a formação de polímeros de Hb S nos eritrócitos, e conseqüentemente do número de células densas - fato que favoreceria à indução dos eritrócitos falciformes irreversíveis. Dessa forma, a diminuição do grau de anemia na interação Hb SS / talassemia alfa ocorre na deleção de um, dois ou três genes alfa. Entretanto, é na deleção de dois genes alfa: HbSS (-a/-a) que o grau de anemia é menos acentuado (tabela 3.3.3). Outro importante efeito da talassemia alfa na interação com anemia falciforme se deve à elevação da Hb Fetal e da Hb A 2 (tabela 3.3.3). Estas influências assumiram importância quando se pensou que as elevações das hemoglobinas A 2 e Fetal promoveriam a "diluição" da Hb S e, conseqüentemente, a diminuição do processo da polimerização da deoxi-hb S. Entretanto, está bem estabelecido que a Hb Fetal - e somente ela - exerce potente efeito inibidor da polimerização da Hb S, reduzindo o número de células falcizadas irreversivelmente. Apesar dos conhecimentos adquiridos até o presente, os relatos da literatura científica mostram que os efeitos "benéficos" da influência da talassemia alfa na anemia falciforme ainda são inconclusivos, conforme mostra a avaliação abaixo extraída de várias publicações: a. os eventos vaso-oclusivos oclusivos não diminuem; b. a freqüência e a gravidade das crises vaso-oclusivas oclusivas são maiores em pacientes com maior deformidade dos eritrócitos e níveis de hemoglobina mais altos, independente do número de genes alfa presentes; c. maior ocorrência de osteonecrose; d. diminuem as úlceras dos membros inferiores; e. diminuem as doenças vasculares de retina. A identificação laboratorial da interação Hb SS/talassemia alfa pode ser feita por um simples processo eletroforético em tampão alcalino, desde que se aplique amostra de sangue hemolisado com saponina a 1%. Quando o paciente é portador da interação é possível observar a Hb H (agregados de b S 4) de forma difusa, bem à frente da Hb S (figura ). 41
42 Figura Eletroforese de hemoglobinas em acetato de celulose ph 8.5. As amostras de hemoglobinas foram obtidas por hemólise dos eritrócitos com saponina a 1%. Da esquerda para a direita: Hb SS/tal. alfa ou Hb SH, dois casos de traço falcêmico (Hb AS), e o padrão normal (Hb AA). Tabela Valores hematológicos na anemia falciforme homozigota (Hb SS aa/aa) e nas interações com talassemia alfa (Hb SS - a/aa ou Hb SS -a/-a). Genótipo Hb (g/dl) VCM (fl) Retic. (%) SS (aa/aa) 8,0 ± 1,1 92 ± 7 11 ± 6 SS (-a/aa) 8,6 ± 1,1 83 ± 7 9 ± 6 SS (-a/-a) 9,2 ± 1,3 72 ± 4 7 ± 5 Hb A 2 (%) 2,8 ± 0,4 3,3 ± 0,6 3,8 ± 0,4 fonte: Steinberg & Embury,
43 Hb S/PHHF ou Hb SF A associação entre anemia falciforme e persistência hereditária de Hb Fetal resulta na identificação do genótipo de Hb SF, com valores de Hb Fetal oscilando entre 15 e 30%. Dois fatores contribuem para a diminuição da gravidade do quadro clínico e hematológico dessa associação. O primeiro é a exclusão da Hb Fetal no processo da polimerização da deoxi-hb S, fato que diminui significativamente a cinética da falcização. O segundo fator se deve a diminuição da concentração da Hb S intra-eritrocitária devido à presença da Hb Fetal; quando o nível de Hb S está abaixo de 75% o processo da falcização é drasticamente inibido. Há evidências de que o nível elevado de Hb Fetal modifica a expressão clínica da anemia falciforme e outras formas sintomáticas da doença. Em geral, na anemia falciforme, há discreta elevação da Hb Fetal (2 a 10% de concentração) sem que se caracterize a PHHF. Neste caso há eritrócitos com Hb Fetal e outros sem Hb Fetal, caracterizando a distribuição heterogênea de Hb Fetal quando submetida à eluição ácida e corada com eritrosina (coloração de Kleihauer) conforme mostra a figura Na associação Hb S/PHHF a Hb Fetal está presente em todos os eritrócitos caracterizando a distribuição homogênea e inibindo a polimerização da Hb S. Figura Esfregaço de sangue periférico de paciente com Hb S/PHHF, submetido a coloração específica para Hb Fetal. Observar a distribuição heterogênea, com eritrócitos corados (Hb Fetal) e eritrócitos sem coloração (sem Hb Fetal). 43
44 Os Haplótipos da Hb SS As observações clínicas realizadas por grande número de médicos em seus pacientes com anemia falciforme, sempre deram destaques a variabilidade clínica e evolução da doença. Essa variabilidade era coincidente com a diversidade étnica entre grupos de doentes falcêmicos da África. Inicialmente relacionou-se a menor gravidade da anemia falciforme com níveis elevados de Hb Fetal e, posteriormente com a interação entre HbSS/talassemia alfa. Com o desenvolvimento envolvimento da biologia molecular e técnicas que caracterizam sequências de DNA foi possível esclarecer que entre indivíduos com o mesmo genótipo da anemia falciforme - a Hb SS - haviam diferenças entre as bases nitrogenadas que compunham o agrupamento de genes de globina beta, delta, gama e epsilon dispostos numa região do cromossomo 11. Todos os indivíduos são geneticamente diferentes e essas características são transmitidas de geração a geração. Entretanto, destaca-se se que grande parte das diferenças individuais representam variações patológicas do DNA, enquanto outras tantas são variações silenciosas. As variações silenciosas são designadas polimorfismos e podem ser detectadas por duas vias: 1. Diferenças na sequência de DNA que podem ser identificadas pela análise sequencial de fragmentos de DNA clonados. Com as atuais técnicas de biologia molecular é possível isolar determinado gene do restante do genoma humano. 2. Muitas vezes as substituições de nucleotídeos neutros podem introduzir ou remover regiões dos genes sem que o produto final seja alterado, como é o caso da Hb S. Entretanto, com o uso de enzimas de restrição, tem sido possível caracterizar esses defeitos. A presença de numerosas regiões polimórficas, ao longo do complexo gênico beta, permite clivagens realizadas por diferentes enzimas de restrição, entre as quais destacam-se: se: Hinc II, Xmnl, Hind III, Pvu II, Hinf I, Hgi II, Ava II, Hpa I, Bam HI entre outras; conforme mostra a figura no cromossomo 11, e a ação de clivagem (ou quebra de pedaços dessas regiões do complexo gênico) pela ação das enzimas acima citadas. Logo abaixo da representação esquemática do complexo gênico beta, a figura mostra também, quatro diferentes tipos de homozigoses de Hb S, denominados por haplótipos de Hb S, e caracterizadas pela ação dessas enzimas de restrição. Para entender a ação das enzimas de restrição usaremos o exemplo clássico da enzima Mst II, que tem a capacidade de fragmentar o DNA ao detectar a sequência de bases nitrogenadas representada por citosina-citosina-timina qualquer base-adenina-guanina-guanina, ou simplesmente CCTNAGG (onde N pode ser qualquer uma das quatro bases: A, T, G, C). A região de ataque da Mst II é uma sequência de sete bases, que no DNA da globina beta normal (Hb A) é CCTGAGG. Entretanto, na mutação que resulta a Hb S esta sequência passa a ser CCTGTGG. Dessa forma, a Mst II não reconhece a sequência de bases desse pedaço do gene da globina beta S e, por isso, não o fragmenta, conforme representa a figura Os fragmentos do DNA-b A, com um tamanho correspondente a bases nitrogenadas (ou 1,15Kb), são menores do que os DNA-b S, com bases nitrogenadas (ou 1,35Kb), e ambos são diferenciados por meio de eletroforese de DNA em gel de agarose. Esse é um dos processos utilizados no diagnóstico pré-natal de casais de risco para gerarem filhos com doenças falciformes. Por outro lado, as características clínicas de anemia falciforme são marcadas pela diversidade de manifestação entre os portadores da doença, devido a fatores conhecidos e já relatados como, por exemplo, concentração da Hb Fetal e talassemia alfa. Além desses, concorrem para essa variabilidade os fatores ecológicos (clima, por exemplo), sócio-econômico, atenção médica. Entretanto, a grande maioria das diferenças clínicas e hematológicas deve-se a fatores genéticos 44
45 relacionados a outros genes que podem estar ligados ou não ao gene da globina b S, que são capazes de modificar a expressão da doença. Portanto, o curso clínico e a gravidade da anemia falciforme (Hb SS) estao relacionados ao haplótipo herdado e caraterizados pela ação de enzimas de restrição. Até o presente, foram identificados cinco tipos diferentes de mutações para o gene da globina b S, e certamente todos se originaram separadamente. Os tipos (ou haplótipos) diferenciados pela ação de diferentes enzimas de restrição foram identificados por SS-Árabe-Indiano, SS-Senegal, Senegal, SS-Benin, SS-Bantu ou República Centro Africana (RAC) e SS-Camarões, conforme mostra a tabela Os haplótipos Benin e Bantu (RAC) estão associados ao aumento da gravidade clínica da doença e são também os mais frequentes na população mundial. Já os portadores dos haplótipos Senegal e Árabe-Indiano apresentam níveis de Hb Fetal significativamente elevados, favorecendo o desenvolvimento o clínico benigno. Na África os indivíduos com anemia falciforme são haplotipicamente homozigotos. Nas Américas, devido ao alto grau de miscigenação, os portadores de anemia falciforme são haplotipicamente heterozigotos. No Brasil, estudos realizados em diferentes regiões mostraram que a maior frequência do gene da Hb S é proveniente do haplótipo SS-Bantu. Steinberg e cols., publicaram em 1998 uma relação entre gravidade clínica, concentração de hemoglobina total e níveis porcentuais de Hb Fetal, com os cinco co haplótipos de Hb S em pacientes com anemia falciforme. Dessa relação obteve-se que os diferentes haplótipos apresentam relação com a clínica dos doentes falcêmicos, entretanto, a menor gravidade da doença se deve ao haplótipo que apresenta nível elevado de Hb Fetal, conforme mostra a tabela Tabela Haplótipos de Hb SS caracterizados por nove enzimas de restrição diferentes. Estas enzimas tem a capacidade de fragmentar o complexo gênico da globina beta S em diferentes posições, conforme o haplótipo do portador da Hb SS. Sítio SS- Árabe-indiano SS-Senegal SS-Benin SS-Bantu (RAC) SS-Camarões 1 Hc 2 Xm 3 Hd 4 Hd 5 Hc 6 Hc Hf Hp 9 Ba Tabela Haplótipos da anemia falciforme e seus efeitos na gravidade clínica e hematológica, associados ao nível de Hb Fetal. Haplótipos Benin Bantu Senegal Camarões Árabe-Indiano Gravidade Hb (g/dl) Hb Fetal (%) Grave Mais grave Moderada Mod. / grave ~ Discreta ~
46 Figura Complexo gênico beta no cromossomo 11. Enzimas de restrições e locais de clivagem ou fragmentação. Relação entre enzimas de restrição e quatro tipos de Hb SS, caracterizados pela análise de biologia molecular. Figura Ação da enzima Mst II no DNA das globinas BA e BS, com produção de fragmentos de DNA com diferentes tamanhos; BA: 1,15kb; bs:1,35kb. 46
47 Fisiopatogia da Hb S Os Efeitos na Molécula da Hb S, na Célula Falciforme e na Circulação Sangüínea do Doente Falcêmico. O processo mutacional que deu origem à Hb S é a causa das profundas alterações fisiopatológicas que afetam a molécula no seu estado desoxigenado, e que são desencadeadas por meio da forma de polímeros de Hb S, degradação oxidativa da Hb S com precipitação de corpos de Heinz, e geração de radicais livres oxidantes. Todas essas três formas de agressões intra-eritrocitárias atuam contra a estrutura e o desempenho fisiológico da membrana do eritrócito falcêmico, provocando lesões e perda da sua maleabilidade. A polimerização da Hb S ocorre preferencialmente em três níveis: molecular, celular e circulatório. No nível molecular o desenvolvimento do processo da falcização se dá a partir do momento em que a oxi-hb S perde o oxigênio e se torna deoxi-hb S. A deoxi-hb S promove a formação de pontes de hidrogênio entre os aminoácidos valina da posição número 1 da globina beta S, que é normalmente sintetizada para esta posição, e a valina mutante que substituiu o ácido glutâmico na posição 6 da mesma globina. A formação dessas pontes de hidrogênio modifica a estrutura espacial da molécula de Hb S e promove contatos intermoleculares com outros aminoácidos da globina beta S que participam da formação do tetrâmero a A 2b S 2. Os principais aminoácidos envolvidos são a fenilalanina da posição 85 e a leucina da posição 88. Como conseqüência, formam-se agregados desses filamentos que se polimerizam e alteram a estrutura globular das moléculas de Hb S, modificando do também a morfologia discóide do eritrócito para formas bizarras das quais a mais conhecida é o afoiçamento (figura 4.1.1). As variáveis que interferem na formação e na cinética da polimerização da Hb S são o oxigênio, a concentração da hemoglobina (Hb S) corpuscular média ou C[Hb S]CM, a temperatura e outras hemoglobinas normais e variantes. O oxigênio é o elemento mais importante, pois somente a deoxi-hb S se polimeriza, e qualquer fator que o estabilize (ex.: a queda o ph sangüíneo e o aumento da concentração centração do 2,3 di-fosfoglicerato) reduzirá a afinidade pelo oxigênio, perpetuando o estado desoxigenado da Hb S e a sua polimerização. A C[Hb S]CM é normalmente superior ao limite da solubilidade da Hb S em condições experimentais, fato que pode explicar sua facilidade em cristalizar-se se e formar polímeros. A redução da temperatura desfaz a polimerização em condições experimentais. As hemoglobinas normais, principalmente a Hb A, seguida da Hb Fetal, tem um maior efeito inibidor da polimerização que outras hemoglobinas variantes. As Hb variantes que melhor se co-polimerizam com a Hb S são as seguintes, em ordem decrescente: C, D, O Arábia e J. No nível celular, os homozigotos para Hb S (ou Hb SS) conservam seus eritrócitos com a forma bicôncova se o nível da saturação de oxigênio da Hb S estiver acima de 65% ca. e retornam à forma discóide quando oxigenadas, porém acumulam-se gradativamente produtos de degradação celular provenientes da falência parcial das bombas de sódio, potássio, cálcio e ATPase. Com a perda de potássio e da água, a C[Hb S]CM se eleva e favorece a polimerização, que se intensifica com a falência da bomba de cálcio/atpase, alterando a permeabilidade da membrana eritrocitária (figura 4.1.2). Esse processo deletério é a principal causa dos eritrócitos que se tornam irreversivelmente falcizados. A membrana eritrocitária é muito afetada durante a falcização, caracterizada por desarranjos das proteínas espectrina-actina, actina, diminuição das glicoproteínas, geração de radicais livres oxidantes e orientação anormal dos fosfolipídeos, apresentando deformações sob forma de escavações na membrana dos eritrócitos (figura 4.1.3). No nível circulatório, a alteração da plasticidade 47
48 normal dos eritrócitos desencadeada pelos efeitos polimerizantes da Hb S tornam os eritrócitos falcêmicos com maior possibilidade de aderirem ao endotélio vascular. Esta aderência decorre de interações entre as células endoteliais e os eritrócitos falcêmicos, com a participação de antígenos de superfície celular (CD36 e CD44) e integrinas proteínas de membranas que juntamente com fibronectina e laminina se ligam às células falcêmicas. As proteínas plasmáticas também participam da ligação dos eritrócitos falcêmicos com as células endoteliais, com destaques para o fator de Willebrand, trombospondina, fibrinogênio e fibronectina. As células endoteliais interagem com CD36, lamininas, glicoproteína 1B, molécula de adesão vascular e receptor Fe, conforme resume a figura Como conseqüência da elevada adesividade do eritrócito falcêmico ao endotélio vascular dos capilares, ocorre a estase venosa que desencadeia a hipoxia tecidual, fato que leva mais moléculas de Hb S ao estado de deoxi-hb S, exarcebando uma situação circulatória já desfavorável e lesando os tecidos perfundidos por esses capilares. Eventualmente pode ocorrer oclusão total dos capilares (vaso-oclusão) oclusão) com trombose, e desencadeamento de mecanismos da coagulação. Os tecidos malperfundidos sofrem infartos com necrose e formação de fibrose, principalmente no baço, medula óssea e placenta. Todos esses eventos provocam lesões teciduais agudas, com crises de dores e lesões crônicas de órgãos, conforme mostra as seqüências de eventos desencadeados a partir da desoxigenação de Hb S esquematizados na figura Figura Microscopia eletrônica da célula falciforme. Observar as projeções arredondadas que indicam as regiões do eritrócito falcêmico em que estão acomodados os corpos de Heinz. Figura Eritrócitos com Hb S na forma oxigenada (oxi-hb S). Das cinco células incluídas na foto, apenas uma ainda conserva a forma normal. As restantes apresentam lesões de membrana 48
49 causadas durante as contínuas degradações da deoxi-hb S, meta-hb S e geração de radicais oxidantes. Essas lesões prejudicam a deformabilidade natural dos eritrócitos, favorecendo a formação dos eritrócitos falciformes irreversíveis. Figura Possíveis interações (-) entre o eritrócito falcêmico, célula endotelial e matriz sub- endotelial. GPIb = glicoproteína 1b; CD 36 e CD 44 = antígenos de superfície celular; FcR = receptor Fc; VCAM = molécula de adesão vascular; TSP = trombospondina; LM = laminina; vwf = fator de von Willebrand; Ig = imunoglobulina; GLS = glicolipídeo sulfatado. 49
50 Figura Processo interativo de oxigenação, polimerização e degradação dação da hemoglobina S, que ocorrem respectivamente na oxi-hb S, deoxi-hb S e meta-hb S. 50
51 A Polimerização da Hb S A polimerização é o fenômeno determinante das alterações morfológicas dos eritrócitos SS. A hemoglobina S, em condições de baixa tensão de oxigênio, é transformada de oxihemoglobina para desoxihemoglobina, sendo sua configuração alterada, de modo que as subunidades b se afastam. A porção hidrofóbica b6 valina de um dos tetrâmeros reposiciona-se se mostrando uma projeção que se liga com a porção b 85 fenilalanina ou b 88 leucina de um outro tetrâmero. Apenas uma subunidade de cada tetrâmero faz o contato; assim são formados ninhos de polimerização. Quando 30 tetrâmeros estão agregados, é formado um núcleo crítico, que constitui a primeira fase da nucleação. Sobre este núcleo crítico, outros tetrâmeros podem aderir e formar então um polímero. Um polímero é uma fita de 220 hm, de diâmetro helicoidal, constituída de 14 fibras, 10 na superfície e 4 no interior. Os polímeros estáveis fornecem uma área necessária para iniciação de uma segunda fase de nucleação, na qual fibras adicionais podem ser agregadas, formando feixes paralelos, chamados tactóides. A dupla nucleação é responsável pelo crescimento exponencial dos polímeros (figuras 4.2.1, 4.2.2, 4.2.3, e 4.2.5). Figura Esquema representativo de eritrócitos normais oxigenados, oxi-hb A (círculos claros), e na forma desoxigenada ou desoxi-hb A (círculos escuros). A oxi-hb e a desoxi-hb A são solúveis e não apresentam disposição diferenciada num meio líquido. 51
52 Figura Esquema representativo de eritrócitos falcêmicos oxigenados oxi-hb S (círculos claros), e na forma desoxigenada ou desoxi-hb S (círculos escuros). A oxi-hb S é solúvel, enquanto o tetrâmero de desoxi-hb S se agrega a outro o tetrâmero similar devido a contatos intermoleculares com a fenilalanina da posição 85 e a leucina da posição 88, e se torna insolúvel. Figura Microscopia eletrônica da formação de fibras em célula falcizada. 52
53 Figura Microscopia eletrônica da célula falciforme com grande número de fibras se dispondo no sentido longitudinal da célula. Figura Microscopia eletrônica de um eritrócito falcizado com disposição assimétrica das fibras. A taxa e extensão da polimerização intracelular da desoxihemoglobina são complexas e dependem de vários fatores, como: concentração intracelular de hemoglobina S, proporção intracelular das diferentes hemoglobinas, porcentagem da saturação de oxigênio, temperatura, ph e 2,3-DPG. Quanto maior a concentração intracelular da hemoglobina S, menor o tempo necessário para formação do polímero; assim células SS, que contém altos níveis de hemoglobina S, necessitam de menor tempo para formar polímeros e conseqüentemente alterar sua forma; já as células SC possuem menor concentração intracelular de hemoglobina S, necessitando assim de um maior tempo para alcançar a formação de um núcleo crítico de polimerização e formação do tetrâmero. A hemoglobina fetal, além de influenciar a 53
54 concentração intracelular de hemoglobina S, também inibe a polimerização devido a um resíduo glutamínico g 87 que impede um contato lateral da dupla fita da fibra de hemoglobina. Quando ocorre uma desoxigenação rápida, são formados vários ninhos de polimerização e conseqüentemente vários polímeros de tamanho pequeno, resultando em muitas projeções na membrana celular, dando à célula o aspecto de uma clava, porém sem a perda da forma discóide dos eritrócitos. Quando a desoxigenação é lenta, permite a formação de longos polímeros, e estes provocam a alteração para a forma clássica em foice dos eritrócitos da anemia falciforme. Estas projeções são críticas para perturbar a estrutura e função das células SS. O tempo em que a célula SS é mantida em baixas taxas de oxigenação também é importante na formação do polímero. O tempo necessário para formação do polímero é maior que o tempo gasto pelo eritrócito falciforme na passagem pela microcirculação. Devido a esta relação de tempo, os polímeros são formados em apenas 20% das células SS, durante o fluxo entre arteríolas e capilares. Se os polímeros ocorressem apenas na dependência da tensão de oxigênio da microcirculação, sem a influência do fator tempo, todas as células SS formariam polímeros, resultando acentuado decréscimo na deformabilidade, vaso-oclusão generalizada e óbito. Conseqüências da Polimerização Os eritrócitos medem 8 mm e os capilares 5 mm, portanto a célula precisa de uma grande deformabilidade para passar na microcirculação; outros obstáculos dificultam a passagem pela microcirculação. Células com hemoglobina S sofrem de anormalidades que fazem esta passagem pela microcirculação ser ainda mais desafiante. Estas anormalidades podem ser divididas em alterações que diminuem a deformabilidade e alterações que aumentam a aderência das células falciformes ao endotélio. As alterações que diminuem a deformabilidade das células falciformes são: 1) a formação de rígidos polímeros de hemoglobina S nas células desoxigenadas; 2) a desidratação celular devido às alterações no transporte de íons da membrana a e conseqüente formação de células densas. Entre as alterações que aumentam a aderência das células falciformes estão: 1) a destruição de células levando à produção de uma população de células jovens que têm um potencial de aderência aumentado, como demonstrado por alguns estudos, nos quais os reticulócitos dos pacientes com anemia falciforme apresentam maior aderência ao endotélio vascular; 2) a exposição de fosfatidilserina na superfície dos eritrócitos falciformes, que facilita a aderência e a hemólise. Diminuição da Deformabilidade das Células Falciformes São várias as alterações observadas nas células falciformes. A redução da deformabilidade das células SS é uma delas e é multifatorial, sendo conseqüência principalmente da formação dos polímeros de hemoglobina S, mas também tendo como fatores contribuintes, e importantes, as alterações da membrana celular e do seu citoesqueleto, as quais também podem ser secundárias às lesões provocadas pelos polímeros. A desidratação celular é uma das conseqüências das lesões à membrana e ao citoesqueleto celular. A membrana celular falciforme apresenta alteração da permeabilidade aos cátions e à água. A perda de cátions, levando à saída de água da célula, provoca a desidratação celular, com aumento da concentração intracelular de hemoglobina, determinando aumento do CHCM. A perda de potássio é a principal causa da desidratação dos eritrócitos falciformes. Os fatores que mais contribuem para a perda de potássio são o co-transporte de K + Cl - e a formação dos canais de Gardos (Ca +2 atividade dependente de K + ). O co-transporte de K + Cl - é ativado pelo edema celular e por acidose. Esta pode ocorrer, in vivo,, particularmente em condições de circulação 54
55 estagnante. As alterações do co-transporte de K + Cl - ocorrem também nas células CC e SC, resultando na característica morfológica comum que é a célula em alvo. As células SS têm maior conteúdo de Ca +2, e este é compartimentalizado em vesículas intracelulares, mantendo a concentração de Ca +2, no citosol, normal. Quando há distorção da membrana, como no processo de falcização, ocorre aumento da permeabilidade da membrana celular ao cálcio, aumentando a concentração de cálcio citoplasmático. Como os eritrócitos têm uma pequena capacidade de tampão para o cálcio, a mínima entrada de cálcio leva a um aumento significativo na sua concentração citoplasmática. Assim, para manter o gradiente de equilíbrio no citosol da célula, os canais de Gardos são ativados. Estes são canais de Ca +2, cuja ativação é dependente de K +. A ativação dos canais de Gardos leva à entrada de potássio na célula. Quando potássio entra na célula, decorrente da ativação dos canais de Gardos, a membrana celular torna-se eletricamente mais negativa, fazendo com que o Cl - saia da célula, levando consigo o K +. A perda de KCl é acompanhada da perda de água. Outro mecanismo envolvido na perda de potássio são alterações na bomba de Na + /K -. Clark et al. demonstraram que alterações na bomba de Na + /K - são responsáveis pela desidratação celular, porém, de uma forma lenta. A Degradação Oxidativa da Hb S O processo de desoxigenação da Hb S favorece a metahemoglobinização da Hb S, aumentando sua concentração e superando a ação da enzima meta Hb-redutase, fato que causa a formação de hemicromos e precipitação de globina S sob forma de corpos de Heinz (figura 4.3.1) promovendo o desalinhamento da proteína banda-3 da membrana do eritrócito. Os eritrócitos falcizados e com alterações na estrutura da membrana alteram a distribuição das moléculas de imunoglobinas G (IgG) em suas superfícies, cujas concentrações elevadas em determinadas regiões dos eritrócitos facilitam as ligações com os receptores Fc das células endoteliais e, dessa forma, induzem a ação fagocitária dos macrófagos no sistema retículo endotelial (SRE), causando hemólise e anemia (figura 4.1.2). Em recente pesquisa realizada no Centro de Referência de Hemoglobinas da UNESP de São José do Rio Preto, evidenciou-se que a simples presença de Hb S, independente do genótipo e de sua concentração, é suficiente para produzir a metahemoglobinização desta hemoglobina. Nesse estudo, o genótipo SS apresentou maior concentração média de meta-hb (3,97%), seguido da interação Hb S / Tal. Beta (2,67%) e da Hb AS (1,07%). A mesma pesquisa revelou que a intensidade da presença de corpos de Heinz apresenta relação direta com o aumento da concentração da Hb S nos eritrócitos, assim no genótipo SS o índice médio de presença de eritrócitos com corpos de Heinz foi de 22 células positivas para cada mil analisadas, enquanto que para Hb S / Tal. Beta foi de 14 por mil, na Hb AS 4 por mil, e no grupo controle Hb AA 1 por mil. 55
56 Figura Esfregaço de sangue de paciente com anemia falciforme, previamente incubado com azul de crezil brilhante a 1% por 60 minutos a 37ºC. Observar a reticulocitose acentuada e várias células com corpos de Heinz que são estruturas esféricas e escuras agregadas à membrana do eritrócito. A geração de radicais livres nos eritrócitos com Hb S ocorre quando a oxi-hb S se muda para a forma deoxi-hb S. A liberação do oxigênio o torna suscetível ao ataque de elétrons que se encontram no interior da célula. Para evitar que o oxigênio fique eletrizado e se transforme em íon superóxido (O. 2), a enzima anti-oxidante eritrocitária conhecida por superóxido dismutase (SOD) atua no sentido de mudar o radical superóxido para peróxido de hidrogênio (H 2 O 2 ). O peróxido de hidrogênio, que também é um radical livre, sofre a ação anti-oxidante de outras duas enzimas eritrocitárias: a glutationa peroxidase (GSH-Px) e a catalase, transformando-o em moléculas de água (figura 4.1.2). A deficiência hereditária de enzimas anti-oxidantes tem sido relatada em diversas populações, e quando associada à anemia falciforme contribui ainda mais na oxidação da Hb S, elevando a formação de produtos de degradação desta hemoglobina, fatos que causam a redução da vida média do eritrócito falcêmico, aumento do grau de hemólise e intensificação da anemia. 56
57 Figura Microscopia eletrônica de varredura de eritrócitos falcizados irreversivelmente, com múltiplas deformações estruturais que comprometem a membrana do eritrócito. Figura Lesões da membrana do eritrócito causada pela fagocitose do corpo de Heinz por macrófago do sistema retículo endotelial (SRE). Microscopia eletrônica de varredura. De uma forma geral, as proteínas da membrana celular podem ser alvos dos ataques de radicais livres quando estes estão dentro ou fora das células em altas concentrações, desnaturando-as. O acúmulo de proteínas desnaturadas interfere nas funções celulares. Vários aminoácidos de importância para a função protéica são suscetíveis às lesões causadas pelos radicais livres: metionina, triptofano, histidina, cisteína e tirosina. As proteínas lesadas por radicais livres podem dar origem a outros radicais, por exemplo: radicais hidroxila (HO) gerados do acúmulo de H 2 O 2 na presença de ferro proveniente da degradação da hemoglobina S; entre os radicais livres intermediários destacamos hidroperóxidos lipídicos que ao reagirem com ferro geram os radicais alcoxil (RO. ) e peroxil (ROO. ). A geração desses radicais amplificam as lesões celulares devido aos contínuos processos de novos ciclos de peroxidação lipídica, resultando na liberação de alcanos (malonaldeídos) e alquenos (4-hidroxinonenal), causando lesões irreversíveis nos eritrócitos falcizados e tendência a deformações, conforme mostram as figuras e
58 As Lesões da Membrana da Célula Falciforme Como se pode observar, todos os efeitos deletérios aos eritrócitos com Hb S ocorre no momento em que a oxi-hb S se transforma em deoxi-hb S, desencadeando três processos fisiopatológicos caracterizados pela formação de polímeros de Hb S, metahemoglobinização da Hb S, e liberação de radicais livres de oxigênio (figura 4.1.2). Os produtos e subprodutos provenientes desses processos fisiopatológicos atacam a membrana do eritrócito com Hb S lesando-a biologicamente, fato que propicia além da redução da vida da célula, outros eventos fisiopatológicos que caracterizam a doença falciforme. No caso da anemia falciforme, o genótipo SS é suscetível à maior intensidade de degradação oxidativa, que laboratorialmente podem ser demonstradas pela alta concentração de metahemoglobina e precipitação intra- eritrocitária de corpos de Heinz. Autora: Adelina Elisabeth Lehmkuhl A assimetria da membrana plasmática foi inicialmente descrita em eritrócitos e plaquetas, há mais de 20 anos e após foi observado que também ocorria em todas as células nucleadas. A perda da assimetria da membrana dos eritrócitos falciformes foi demonstrada pela primeira vez por CHIU et al.,, em 1981 (CHIU, 1981; HERBELL, 1991). A membrana celular é uma bicamada de fosfolipídios medindo cerca de 10 hm de espessura. Os principais componentes são lipídios e proteínas. Os três principais lipídios são: os fosfolipídios, colesterol e glicolipídios. ios. Os fosfolipídios são anfipáticos, isto é, possuem uma cabeça polar hidrofílica que interage fortemente com a água e uma cauda hidrofóbica que interage, por sua vez, fortemente com a outra porção hidrofóbica (cauda de outro fosfolipídio) da bicamada. Com esta propriedade anfipática, os fosfolipídios em meio aquoso formam espontaneamente uma bicamada planar, pois esta é a configuração de menor gasto de energia. A membrana celular dos eritrócitos e também de outras células, como postulado por Brestscher há mais de 20 anos, apresenta uma distribuição assimétrica dos fosfolipídios. Na camada externa da membrana celular está 75% a 80% do total de fosfolipídios; estes contêm colina e são: fosfatidilcolina e esfingomielina; o restante, 20% a 25% dos fosfolipídios está na superfície interna da membrana celular, e são os aminofosfolipídios: fosfatidilserina e fosfatidiletanolamina (figura 4.4.1). 58
59 Figura Distribuição dos principais fosfolipídios na membrana celular. Uma molécula lipídica polar, na superfície de uma membrana, é livre para se mover no seu próprio lado da bicamada, mas é impedida de deslocar-se se para superfície do outro lado. A resistência da bicamada à transferência de lipídios de uma face da membrana para outra mantém e preserva a assimetria da bicamada. Esta resistência é causada pela grande quantidade de energia necessária para empurrar as cabeças carregadas polares dos fosfolipídios ao longo da base hidrocarbonada da membrana. Outros mecanismos envolvidos na estabilidade dos fosfolipídios são: a interação da fosfatidilserina com proteínas do citoesqueleto celular, como a espectrina e banda 4.1, e a ativa manutenção da orientação por uma proteína de translocação de fosfolipídios ATP dependente, a aminofosfolipídios transferase. A relação entre e os lipídios da camada interna e externa é o maior determinante da forma discóide dos eritrócitos. Um transporte ativo é necessário para manter um espontâneo equilíbrio de lipídios nas monocamadas, e para recuperar sua forma normal após a deformação. Alterações na forma dos eritrócitos são acompanhadas de uma troca na relação de área da camada externa com a camada interna. A reversibilidade da deformação que um eritrócito sofre, após passar pela microcirculação, depende de um rápido fluxo de lipídios de um lado para outro, implicando que a deformabilidade da célula é influenciada pela taxa de difusão transversal de lipídios. A assimetria dos fosfolipídios é essencialmente conservada por toda a vida da célula, sendo os fosfolipídios mantidos na membrana em um equilíbrio dinâmico. Todos os fosfolipídios se difundem passivamente através da bicamada, em uma taxa lenta. Os aminofosfolipídios são transportados ativamente pela aminofosfolipídio transferase, sendo esta responsável pelo rápido transporte da fosfatidilserina para a monocamada interna. Poderia se esperar que as alterações 59
60 na aminofosfolipídio transferase levassem à perda da assimetria por difusão por meio de um gradiente de concentração, mas esse é um processo muito lento. Em condições em que a atividade de aminofosfolipídio transferase é prejudicada, como acontece no estoque de sangue, não se observa a perda da assimetria, pois o movimento da fosfatidilserina para cada externa é extremamente lento. Essa é observada quando, além da alteração na atividade da aminofosfolipídio transferase, existe lesão da membrana que pode ser provocada in vitro por cálcio e ionofore e, in vivo,, pela formação dos polímeros de hemoglobina S. A exposição da fosfatidilserina na superfície externa da bicamada pode contribuir com os processos de vaso-oclusão, oclusão, aumentando a aderência das células falciformes ao endotélio vascular e levando a um estado de hipercoagulabilidade. A fosfatidilserina é um sinalizador para a fagocitose pelos monócitos: este reconhecimento poderia ser uma das causas da vida curta das células falciformes e conseqüente anemia (figura 4.4.2). Figura Fosfolipídios da membrana celular eritrócito falciforme e normal. 60
61 A heterogeneidade das Células Falciformes Este ítem contou com a colaboração de Adelina Elisabeth Lehmkulil HEBBEL et al. foram os primeiros a demonstrar que as células falciformes têm aderência anormal ao endotélio. Contribuem, para este fato, a densidade celular, presença de receptores nas células falciformes para substâncias mediadoras da aderência ao endotélio vascular, como o Fator de von Willebrand, e exposição de fosfatidilserina na superfície da membrana celular. Como conseqüência da desidratação celular, existe uma heterogeneidade das células falciformes, que pode ser demonstrada pela separação, por meio de centrifugação de vários grupos de células SS com gradiente de densidade diferentes. A densidade das células falciformes é determinada pela concentração de hemoglobina corpuscular média (CHCM): quanto maior a concentração de hemoglobina S, dentro da célula, maior é o CHCM, e maior é a densidade da célula. As células com densidade alta são referidas como células densas. Podem ser definidas quatro categorias de células baseadas no gradiente densidade por centrifugação. As quatro categorias de células SS são: 1. células SS1, reticulócitos (fig ); Fig Microscopia eletrônica de varredura (M.E.V.) de reticulócito obtido de sangue de doente com anemia falciforme. Nesta fase ocorrem as primeiras lesões visíveis, representadas por pequenas depressões na membrana da célula. 61
62 2. células SS2, células discóides (fig ); Fig M.E.V. de um eritrócito falcêmico discóide (SS2) e de outro eritrócito falcêmico com lesões de membrana. Essas lesões induzem a transformação dos eritrócitos falcêmicos a se tornarem células falciformes densas (SS3). 3. células SS3, células discóides densas (fig ); Fig M.E.V. de células falciformes densas (SS3), com notável alteração morfológica. 62
63 4. células SS4, células falciformes irreversíveis (fig ). Fig M.E.V. de célula falciforme irreversível, com a forma achatada e alongada, em fase de aderência ao endotélio vascular. Cada uma dessas categorias de células tem características morfológicas e propriedades distintas, contribuindo de forma diferente com a vaso-oclusão e hemólise. KAUL et al. mostraram que as células falciformes aderem exclusivamente ao endotélio venular e a aderência é inversamente relacionada ao diâmetro da vênula. Estudos com cultura de células endoteliais mostraram que, quanto maior a densidade da hemácia falciforme, maior o poder de aderência. Porém, estudos com as células durante o fluxo sangüíneo, mostraram que a aderência ao endotélio está inversamente relacionada ao CHCM; assim KAUL et al. propuseram um modelo de vaso- oclusão. Neste modelo, o processo de vaso-oclusão oclusão é iniciado com a aderência de células de baixa densidade ao sistema venular pós-capilar, diminuindo o fluxo sangüíneo local, e facilitando a aderência de células falciformes irreversíveis e vaso-oclusão. A Anemia Hemolítica no Doente Falcêmico A anemia que ocorre nos doentes com anemia falciforme (Hb SS) é caracterizada por uma anemia hemolítica parcialmente compensatória, com valores de hemoglobina se situando entre 6 e 9 g/dl. A anemia hemolítica compensatória se deve a um aumento da eritropoiese, verificado no sangue periférico por reticulocitose acentuada. Em vista disso, ocorre constante utilização de vitamina B12 e folatos, necessitando reposição adequada para evitar o agravamento da anemia. A anemia entre as doenças falciformes é mais expressiva na anemia falciforme, pois o grau de lesão da membrana do eritrócito falcêmico é muito intenso (fig ). Conforme ilustra a figura, a membrana do eritrócito falcêmico sofre pelo menos quatro tipos de agressões: a) ação de radicais superóxidos (O. 2 ); b) alteração da permeabilidade devido às falhas das bombas de sódio, potássio, cálcio e ATPase; c) a oxidação da membrana causada pelo ferro no estado férrico (Fe +++ ) liberado da degradação da metahemoglobina; d) alteração da conformação espacial da proteína banda-3 da membrana eritrocitária devido à impregnação dos corpos de Heinz junto a sua estrutura. Todos esses processos que ocorrem cumulativamente, deformam os 63
64 eritrócitos falcêmicos, tornando-os os irreversíveis e susceptíveis às ações macrofágicas das células do sistema retículo endotelial (SRE). É importante considerar que o grau de variabilidade da anemia hemolítica que ocorre na anemia falciforme depende de vários fatores ou interferentes, que podem ser desde os de causas ambientais, sociais e econômicas, como biológicos (ex.: doenças crônicas associadas), ou eritrocitárias (ex.: interações com deficiência de G-6PD, esferocitose, etc.), entre outros. Detalhes sobre interferentes que influenciam o grau de anemia na doença falciforme podem ser verificados no item 7 desse capítulo. 64
65 Os Processos VASO-OCLUSIVOSOCLUSIVOS A circulação sangüínea no ser humano desenvolve quase exclusivamente na microvasculatura composta por arteríolas, capilares, sinusóides e vênulas. No indivíduo adulto há cerca de 1,2 x 10 9 de vasos sangüíneos dos quais 99% estão na microvasculatura. É justamente nessa ampla área vascularizada que ocorrem as trocas de substâncias orgânicas e inorgânicas essenciais para as atividades das células. A maioria dos capilares são inelásticos, com diâmetros variáveis entre 3 a 16m, enquanto que os eritrócitos apresentam-se com diâmetro médio de 8m (fig ). Dessa forma, a flexibilidade do eritrócito é fundamental para executar a função de transporte de oxigênio (fig ). As trocas de gases, líquidos, proteínas, sais minerais, principalmente, ocorrem de forma transvascular na imensa rede da microvasculatura. O conteúdo de oxigênio nesses vasos diminui à medida que o sangue flui em direção aos vasos de menor calibre, como as vênulas. Para se ter noção da perda de oxigênio durante o fluxo sangüíneo, é necessário comparar que a PO 2 no sangue arteriolar é de aproximadamente 100 mmhg, e que decresce pela necessidade de distribuir o oxigênio pelos órgãos em que passa, até cair para níveis variáveis entre 12 e 17 mmhg ao chegar às vênulas. Algumas áreas da microvasculatura, caracterizadas pelas dobraduras dos vasos, prejudicam o fluxo sangüíneo e conseqüentemente a desoxigenação. Nessa situação, os eritrócitos com Hb SS podem sofrer deformações e iniciar os processo vaso-oclusivos. oclusivos. A obstrução das arteríolas impede a circulação para os capilares, entretanto os canais adjacentes geralmente impede o colapso, drenando o fluxo sangüíneo em vias de estagnação e permitindo a irrigação de tecidos e órgãos. Quando a desoxigenação da Hb S na microvasculatura é rápida, os processos vaso-oclusivos podem ser evitados. Porém, quando a falcização intravascular progride, inclusive com a participação de eritrócitos falciformes irreversíveis, essas células tendem a aderir ao endotélio vascular. Várias situações contribuem para o desencadeamento da oclusão vascular, com particular destaque à alta viscosidade do sangue e pela elevação dos níveis de fibrinogênio. A alta viscosidade do sangue ocorre não somente pelos processos vaso-oclusivos, oclusivos, mas também pela desidratação; os níveis elevados de fibrinogênio decorrem como resposta natural às infecções contraídas pelo doente falcêmico. Fig Microscopia eletrônica de varredura de arteríola com diâmetro suficiente para passagem de apenas um eritrócito por vez. 65
66 Fig Figura representando a microscopia eletrônica de um vaso estreito, obrigando os eritrócitos a se deformarem para poderem acompanhar o fluxo sangüíneo. Como conseqüência da estase venosa causada pela oclusão vascular, outros setores da microvasculatura desencadeiam processos de oclusão, levando mais moléculas de Hb S ao estado desoxigenado, piorando a situação circulatória já desfavorável e lesando os tecidos perfundidos por esses vasos. Eventualmente pode ocorrer oclusão total dos capilares, causando tromboses, formação de fibrina e, também, ativação do mecanismo de coagulação. Os tecidos mal perfundidos podem sofrer infartos com necrose e formação de fibrose, principalmente do baço, medula óssea e placenta. Todos esses eventos podem causar lesões tissulares agudas, com crises dolorosas, cronificação e lesões orgânicas permanentes (capítulo 6 Controle Clínico das Doenças Falciformes). Alterações Laboratoriais nas Doenças Falciformes Anemia Falciforme a.) Análise de Sangue Periférico O genótipo falcêmico mais importante sob o ponto de vista médico é a anemia falciforme, uma vez que os outros genótipos que causam a doença falciforme podem ser melhor controlados. A anemia falciforme cursa com graus de anemias que variam entre grave (Hb:5 g/dl) a moderado (Hb:9 g/dl), com o eritrograma mostrando valores de VCM e HCM normais, embora haja evidente anisocitose, poiquilocitose e anisocromia. Assim, embora a classificação do tipo de anemia é em geral normocítica e normocrômica, as alterações morfológicas são bastante abrangentes pela presença de células falciformes, esquisócitos, células em alvo, etc., conforme mostra a tabela A distribuição da amplitude dos eritrócitos (RDW) está sempre elevada. Os eritrócitos que se transformam várias vezes na forma falciforme durante a desoxigenação, e retornam à forma discóide na oxigenação, se tornam irreversivelmente falcizados após as lesões constantes das suas membranas (figura 4.2.2), e podem ser identificados como eritrócitos afoiçados de forma muito delgada (figura 5.1). É também muito freqüente a policromasia (devido à reticulocitose) e eritroblastos ortocromáticos (figura 5.2), além de pontilhados basófilos. As presenças de corpos de Howell-Jolly e de Pappenheimer são indicativas do não funcionamento do baço devido à auto-esplenectomia. 66
67 Figura 5.1. Eritrócitos rócitos irreversivelmente falcizados em esfregaço de sangue periférico de paciente com anemia falciforme. 67
68 Figura 5.2. Eritroblasto ortocromático em esfregaço de sangue periférico de paciente com anemia falciforme. A leucocitose (12 a 30x10 9 /L) e neutrofilia são ocorrências comuns nas análises dos leucogramas. Na vigência de processos infecciosos, pode ocorrer o desvio à esquerda por aumento do número de neutrófilos bastonetes e o aparecimento de formas mais jovens de neutrófilos (metamielócitos e mielócitos). A trombocitose é comum, com contagens de plaquetas ultrapassando 450x10 9 /L, e este fato se deve ao fibrosamento do baço que não pode seqüestrar as plaquetas do sangue periférico como faria o baço normal. É possível encontrar plaquetas gigantes quando ocorre infartos medulares. Entretanto, durante as crises vaso- oclusivas, o número de plaquetas pode diminuir acentuadamente. b) Testes Específicos O principal teste de identificação do genótipo SS que caracteriza a anemia falciforme é a eletroforese de hemoglobina em tampão alcalino (agarose alcalina ou acetato de celulose) ph 8 a 9. Por meio desse teste identifica-se a Hb S, cuja mobilidade se dispõe entre a Hb A e Hb A 2 (figura 5.3). Geralmente a anemia falciforme é acompanhada de discreta a moderada elevação da Hb Fetal (2 a 10%) e Hb A 2 normal. Há entretanto que considerar que outro genótipo da doença falciforme, a Hb SD, se comporta eletroforeticamente como a Hb SS, uma vez que a Hb D tem a mesma mobilidade da Hb S, conforme mostra o mapa de eletroforese exposto na figura Análises mais cuidadosas podem diferenciá-las, inicialmente com relação à maior gravidade clínica da Hb SS em relação a Hb SD, bem como das alterações dos resultados do eritrograma (tabelas 5.1 e 5.2). É importante destacar que no genótipo Hb SS ocorre a presença da Hb Fetal (figura 5.4), enquanto que na Hb SD a concentração de Hb Fetal é normal. Porém, como melhor teste específico para diferenciar os genótipos SS e SD é a eletroforese em agarose ácida (tampão fosfato ou citrato ph 6,2). Na eletroforese em agarose ácida a Hb S se separa da Hb A, enquanto que a Hb D se posiciona na mesma linha da Hb A (figura 5.4). Afigura 5.5 mostra a separação das frações de hemoglobinias Fetal, A, S e C por meio da eletroforese em agarose ácida. Outros testes como o de falcização e solubilidade não conseguem diferenciar a Hb SS da Hb SD, pois ambos positivam a reação. 68
69 Figura 5.5. Eletroforese de hemoglobinas em agarose ácida (ph 6.2). (1) Hb AS; (2) controle: Hb ASC; (3) controle normal: Hb AA. Observar traços de Hb Fetal nas três amostras analisadas. Tabela 5.1. Alterações da morfologia eritrocitária nos diferentes genótipos das síndromes talassêmicas. Genótipo AS SS S/tal. beta S/tal. alfa SC SD S/PHHF Alterações da Morfologia Eritrocitária Normocitose, normocromia Células falcizadas e em alvo. Hipocromia e policromasia. Eritroblastos, corpos de Howell-Joly. Anisocitose, microcitose, poiquilocitose, células falcizadas, dacriócitos, células em alvo. Hipocromia e policromasia. Anisocitose, microcitose, células falcizadas. Hipocromia e policromasia. Aniso-poiquilocitose. Hipocromia. Células falcizadas e em alvo. Policromasia. Discreta anisocitose, ou normocitose e normocromia. 69
70 Tabela 5.2. Principais alterações laboratoriais nas doenças falciformes. Doença Falciforme Hb S Hb SS Hb S/b 0 tal Hb S/b + tal Hb SS/atal.* Hb SC Hb SD Hb S/PHHF Hb AS Porcentagens de Hb F Hb A A 2 VCM HCM N N N N 0 0 N N N 0 0 N N N N N N N N N Hbg/dl * pode ser detectada a Hb H (conc.: 2 a 5%), ou agregados, intraeritrocitários de Hb H 0=ausência, N=normal, =aumentado, =diminuído S/β Talassemia ou Micro Drepanocitose a) Análise do Sangue Periférico A condição de dupla heterozigose Hb S/tal. b está associada com aspectos clínicos similares, embora não tão grave, ao da anemia falciforme. O genótipo S/tal. b 0 que não há síntese de Hb A é clinicamente mais grave que o S/tal. b +, e é similar em gravidade à anemia falciforme. É importante destacar que clinicamente o genótipo S/tal. b + é classificado em tipo 1 (clinicamente grave e hematologicamente anormal, embora menos grave que a Hb S/tal. b 0 ), e o tipo 2 (causa apenas anemia moderada e os pacientes são assintomáticos). O eritograma dos pacientes com Hb S/tal. b 0 mostram valores de hemoglobina variáveis entre 5 e 10 g/dl, contagem de reticulócitos entre 10 e 20%. Os eritrócitos são microcíticos e hipocrômicos, com marcante aniso-poiquilocitose (figura 5.6, tabelas 5.1 e 5.2), além de elevação do RDW, presença de pontilhados basófilos e células em alvo. Na Hb S/tal. b + - tipo 1,, a concentração da hemoglobina varia entre 7 e 10 g/dl, os valores de VCM e HCM estão diminuídos, podem ser encontradas células falciformes, e os reticulócitos podem estar normais ou discretamente elevados. Na Hb S/tal. b + tipo 2,, há discreto grau de anemia, com diminuição do VCM e HCM, e poucas alterações morfológicas dos eritrócitos. 70
71 b) Testes Específicos A eletroforese de hemoglobina em tampão alcalino é o melhor teste específico para caracterizar os genótipos Hb S/tal. b 0 e Hb S/tal. b +, conforme mostra a figura Na Hb S/tal. b 0 há o fracionamento da Hb S e Hb Fetal com a concentração elevada, a, além da Hb A 2 (figura 5.7), enquanto que o genótipo Hb S/tal. b + se destaca pela presença da Hb S com concentração superior à da Hb A (figura 5.8); é comum a Hb Fetal estar discretamente elevada neste genótipo. Outro teste importante para compor os resultados da Hb S/tal. b é a dosagem da Hb Fetal por meio da avaliação da resistência alcalina desta hemoglobina. 71
72 Figura 5.6. Esfregaço de sangue periférico de paciente com Hb S/talassemia b. Aniso-poiquilocitose pela presença de eritrócitos microcíticos, normocíticos, hipocrômicos, em alvo e células falcizadas. Figura 5.7. Eletroforese de hemoglobinas em acetato de celulose, tampão alcalino (ph: 8.5). (1) Hb AS; (2) Hb SF: resultado típico da Hb S/tal. β 0. 72
73 Figura 5.8. Eletroforese de hemoglobinas em acetato de celulose, tampão acalino (ph 8.5). (1) Hb AA; (2) Hb AA; (3) Hb S com maior concentração que a Hb A + A 2 aumentado: resultado típico de Hb S/tal. β +. Tabela 5.1. Alterações da morfologia eritrocitária nos diferentes genótipos das síndromes talassêmicas. Genótipo AS SS S/tal. beta S/tal. alfa SC SD S/PHHF Alterações da Morfologia Eritrocitária Normocitose, normocromia Células falcizadas e em alvo. Hipocromia e policromasia. Eritroblastos, corpos de Howell-Joly. Anisocitose, microcitose, poiquilocitose, células falcizadas, as, dacriócitos, células em alvo. Hipocromia e policromasia. Anisocitose, microcitose, células falcizadas. Hipocromia e policromasia. Aniso-poiquilocitose. Hipocromia. Células falcizadas e em alvo. Policromasia. Discreta anisocitose, ou normocitose e normocromia. 73
74 Tabela 5.2. Principais alterações laboratoriais nas doenças falciformes. Doença Falciforme Hb S Hb SS Hb S/b 0 tal Hb S/b + tal Hb SS/atal.* Hb SC Hb SD Hb S/PHHF Hb AS Porcentagens de Hb F Hb A A 2 VCM HCM N N N N 0 0 N N N 0 0 N N N N N N N N N Hbg/dl * pode ser detectada a Hb H (conc.: 2 a 5%), ou agregados, intraeritrocitários de Hb H 0=ausência, N=normal, =aumentado, =diminuído Hb S/talassemia α A associação entre a anemia falciforme (Hb SS) e talassemia alfa de um, dois ou três genes alfa deficientes, faz surgir a Hb S/tal. a. Geralmente os pacientes com essa doença são filhos de pais com traço falciforme (Hb AS), em que um ou ambos tem a talassemia alfa associada (Hb AS/tal. a). A análise do sangue periférico mostra anemia microcítica e hopocrômica, com hemoglobina entre 9 e 11 g/dl, alterações morfológicas evidentes (tabela 5.1). Os testes específicos são eletroforese de hemoglobina em tampão alcalino que permite visualizar a Hb H formada por tetrâmeros de B S 4 (figura 5.9), e a pesquisa de Hb H intra- eritrocitária que permite ver a precipitação da Hb H nos eritrócitos desses pacientes (figura 5.10). 74
75 Figura 5.9. Eletroforese de hemoglobinas em acetato de celulose, tampão alcalino (ph 8.5). Observar a primeira aplicação à esquerda: Hb SS (anemia falciforme) associada à Hb H (talassemia alfa). A seta indica a posição da Hb H, constituída por tetrâmero de globinas b S ou b S 4. Figura Sangue de paciente com anemia falciforme associada a talassemia alfa (Hb S/tal. a), incubado a 37ºC com azul de crezil brilhante a 1%. O esfregaço obtido mostra a presença, por contraste de fase, de eritrócitos com precipitados de Hb H. 75
76 Tabela 5.1. Alterações da morfologia eritrocitária nos diferentes genótipos das síndromes talassêmicas. Genótipo AS SS S/tal. beta S/tal. alfa SC SD S/PHHF Alterações da Morfologia Eritrocitária Normocitose, normocromia Células falcizadas e em alvo. Hipocromia e policromasia. Eritroblastos, corpos de Howell-Joly. Anisocitose, microcitose, poiquilocitose, células falcizadas, dacriócitos, células em alvo. Hipocromia e policromasia. Anisocitose, microcitose, células falcizadas. Hipocromia e policromasia. Aniso-poiquilocitose. Hipocromia. Células falcizadas e em alvo. Policromasia. Discreta anisocitose, ou normocitose e normocromia. Hb SC A Hb SC é uma condição de dupla heterozigose, onde as concentrações de Hb S e Hb C se equilibram. Em comparação com a anemia falciforme, a doença da Hb SC apresenta-se com moderados sintomas clínicos e poucas complicações. Os primeiros sintomas mais significativos ocorrem na adolescência, e incluem anemia, dores nas articulações, abdominais e esqueléticas, causadas pelas oclusões vasculares. A anemia do sangue periférico mostra anemia normocítica e normocrômica (VCM e HCM normais) de grau moderado, com a concentração de hemoglobina entre 9 e 13 g/dl, e aniso- poiquilocitose com células em alvo (tabelas 5.1, 5.2 e 5.11). O teste específico mais eficiente é a eletroforese de hemoglobina em ph alcalino (figura 5.4), onde é possível fracionar com muita clareza as hemoglobinas S e C (figura 5.12). A eletroforese em agarose ácida também pode ser usada com sucesso (figura 5.5). Figura 5.5. Eletroforese de hemoglobinas em agarose ácida (ph 6.2). (1) Hb S; (2) controle: Hb ASC; (3) controle normal: Hb AA. Observar traços de Hb Fetal nas três amostras analisadas. 76
77 Figura Eletroforese de hemoglobinas em acetato de celulose, tampão alcalino (ph 8.5). (1) Hb AS; (2) controle: Hb ASC; (3) Hb SC; (4) controle normal: Hb AA 2. Tabela 5.1. Alterações da morfologia eritrocitária nos diferentes genótipos das síndromes talassêmicas. Genótipo AS SS S/tal. beta S/tal. alfa SC SD S/PHHF Alterações da Morfologia Eritrocitária Normocitose, normocromia Células falcizadas e em alvo. Hipocromia e policromasia. Eritroblastos, corpos de Howell-Joly. Anisocitose, microcitose, poiquilocitose, células falcizadas, dacriócitos, células em alvo. Hipocromia e policromasia. Anisocitose, microcitose, células falcizadas. Hipocromia e policromasia. Aniso-poiquilocitose. Hipocromia. Células falcizadas e em alvo. Policromasia. Discreta anisocitose, ou normocitose e normocromia. Tabela 5.2. Principais alterações laboratoriais nas doenças falciformes. Doença Falciforme Porcentagens de Hb S Hb SS Hb S/b 0 tal Hb S/b + tal. 50- Hb F Hb A A 2 VCM HCM Hbg/dl N N N
78 80 Hb SS/atal.* Hb SC Hb SD Hb S/PHHF Hb AS N N N N N N N N N N N N N * pode ser detectada a Hb H (conc.: 2 a 5%), ou agregados, intraeritrocitários de Hb H Hb SD É uma condição de dupla heterozigose observada entre Hb S e variantes anormais que migram na mesma posição eletroforética da Hb S (figura 5.4) ) mas não falcizam, pois foram originadas por mutações de aminoácidos diferentes à da Hb S. Essas hemoglobinas variantes foram denominadas por tipo D. Entre os 16 tipos diferentes de Hb D, as associações da Hb S foram descritas com 9 tipos diferentes de Hb D, porém quando a associação ocorre entre a Hb S com a Hb D Punjab ou Los Angeles (Sd-Punjab ou Los Angeles) produz sintomas clínicos e alterações hematológicas moderados, conforme mostram as tabelas 5.1 e Os testes específicos são eletroforeses em ph alcalino e agarose em ph ácido (figura 5.4). Maiores detalhes da diferenciação laboratorial entre Hb SS e Hb SD foram apresentados no item
79 Figura 5.4. Posições eletroforéticas padrões em tampão alcalino (ph 8.5) e em agarose-ácida (ph 6.2) Tabela 5.1. Alterações da morfologia eritrocitária ia nos diferentes genótipos das síndromes talassêmicas. Genótipo AS SS S/tal. beta S/tal. alfa SC Alterações da Morfologia Eritrocitária Normocitose, normocromia Células falcizadas e em alvo. Hipocromia e policromasia. Eritroblastos, corpos de Howell-Joly. Anisocitose, microcitose, poiquilocitose, células falcizadas, dacriócitos, células em alvo. Hipocromia e policromasia. Anisocitose, microcitose, células falcizadas. Hipocromia e policromasia. Aniso-poiquilocitose. Hipocromia. 79
80 SD S/PHHF Células falcizadas e em alvo. Policromasia. Discreta anisocitose, ou normocitose e normocromia. Tabela 5.2. Principais alterações laboratoriais nas doenças falciformes. Doença Falciforme Porcentagens de Hb S Hb F Hb A A 2 VCM HCM Hbg/dl Hb SS N N N Hb S/b 0 tal Hb S/b + tal Hb SS/atal.* Hb SC N N N Hb SD N N N Hb S/PHHF N 0 N N N Hb AS N N N * pode ser detectada a Hb H (conc.: 2 a 5%), ou agregados, intraeritrocitários de Hb H Hb S/Persistência Hereditária de Hb Fetal A interação entre anemia falciforme (Hb SS) e persistência hereditária de Hb Fetal (PHHF), ou Hb S/PHHF, produz um quadro hematológico com discretas alterações morfológicas, concentração de hemoglobina geralmente dentro dos limites de normalidade (tabelas 5.1 e 5.2). Os testes específicos mais eficientes são a eletroforese de hemoglobina em ph alcalino, dosagem de Hb Fetal e coloração intra-eritrocitária de Hb Fetal (figura 5.13). A concentração de Hb Fetal varia entre 15 e 30%, e pelo fato de não se co-polimerizar com a Hb S, a ocorrência do desencadeamento do processo da falcização é mínimo (consultar os ítens 1.9, 3.3 e 7.4). 80
81 Figura Esfregaço preparado para coloração citoquímica de Hb Fetal intra-eritrocitária. Somente os eritrócitos corados em vermelho contêm Hb Fetal. Neste esfregaço a distribuição é heterogênea, característica de tal. beta. Quando há persistência hereditária de Hb Fetal (PHHF) todos os eritrócitos ficam homogeneamente corados pela presença de Hb Fetal. Tabela 5.1. Alterações da morfologia eritrocitária nos diferentes genótipos das síndromes talassêmicas. Genótipo AS SS S/tal. beta S/tal. alfa SC SD S/PHHF Alterações da Morfologia Eritrocitária Normocitose, normocromia Células falcizadas e em alvo. Hipocromia e policromasia. Eritroblastos, corpos de Howell-Joly. Anisocitose, microcitose, poiquilocitose, células falcizadas, dacriócitos, células em alvo. Hipocromia e policromasia. Anisocitose, microcitose, células falcizadas. Hipocromia e policromasia. Aniso-poiquilocitose. Hipocromia. Células falcizadas e em alvo. Policromasia. Discreta anisocitose, ou normocitose e normocromia. Tabela 5.2. Principais alterações laboratoriais nas doenças falciformes. Doença Falciforme Hb S Hb SS Hb S/b 0 tal Hb S/b + tal Porcentagens de Hb F Hb A A 2 VCM HCM N N N Hbg/dl
82 Hb SS/atal.* Hb SC Hb SD Hb S/PHHF Hb AS N 0 0 N N N 0 0 N N N N N N N N N * pode ser detectada a Hb H (conc.: 2 a 5%), ou agregados, intraeritrocitários de Hb H O Traço Falciforme (Hb AS) O traço falciforme é o estado de heterozigose das doenças falciformes (Hb AS). A Hb A sempre está com concentração superior à da Hb S, e por isso os portadores são assintomáticos, com eritrograma normal. Em situações especiais de extrema hipoxia tecidual, o portador de Hb AS pode ter crises de dores, sem alterações hematimétricas importantes. Em ocasiões raras, podem ocorrer hematúria, assim como hipostenúria por falha dos rins em concentrar a urina. Os testes específicos mais comuns são: teste de falcização (atualmente em desuso pela ineficácia), o teste de solubilidade (também em desuso pelas mesmas razões), as eletroforeses de hemoglobinas em ph alcalino (figura 5.14), em agarose-ácida (figura 5.5) ) e eletroforese de focalização isoelétrica (figura 5.15). Pela eletroforese de focalização isoelétrica, é possível diferenciar a Hb D que tem a mesma posição eletroforética da Hb S em eletroforese de ph alcalino em acetato de celulose e agarose alcalina. Da mesma forma a eletroforese em agarose- ácida é eficiente na diferenciação entre as hemoglobinas S e D, conforme mostra a figura 5.4. Figura 5.5. Eletroforese de hemoglobinas em agarose ácida (ph 6.2). (1) Hb S; (2) controle: Hb ASC; (3) controle normal: Hb AA. Observar traços de Hb Fetal nas três amostras analisadas. 82
83 Figura Eletroforese de hemoglobinas em acetato de celulose, tampão alcalino (ph 8.5). (1) Controle: Hb ASC; (2) Hb A + Lepore A Hb Lepore migra na mesma posição da Hb S, porém sua concentração é abaixo de 15% e o portador tem anemia microcítica e hipocrômica; (3) Hb AS; (4) Hb AC; (5) Hb AS. 83
84 Controle Clínico dos Doentes Falcêmicos Aspectos Gerais da Anemia As manifestações clínicas na anemia falciforme (HbSS) geralmente não são notadas até a segunda metade do primeiro ano de vida, quando os níveis de HbF que até então eram suficientes para limitar uma falcização clinicamente importante, caem em relação aos níveis crescentes de HbS presentes nos eritrócitos produzidos na medula óssea. O quadro clínico da doença falciforme apresenta grande variabilidade entre os pacientes, assim como no mesmo indivíduo ao longo de sua evolução. Dentre as síndromes falciformes, a anemia falciforme cursa com maior gravidade clínica, seguido pela Sβ 0 -talassemia, doença da HbSC e Sβ+-talassemia. Recentemente Platt e cols. estudaram um grupo de 3764 pacientes onde mais de 50% dos pacientes acompanhados sobreviveram além da quinta década, sendo a maior sobrevida detectada no sexo feminino e nos pacientes com HbSC (em relação à HbSS). Os pacientes mais sintomáticos apresentaram maior risco de morte precoce; leucocitose e baixo nível de HbF foram os fatores (laboratoriais) de risco mais importantes. As principais complicações clínicas que acometem os portadores de doença falciforme na sua forma homozigota ou em combinação de heterozigose são: Dactilite (Síndrome Mão-Pé) Acomete crianças na primeira infância, principalmente entre 6 meses a 2 anos de idade. Os episódios são tipicamente caracterizados por dor intensa e edema (sem eritema) no dorso das mãos e dos pés (fig ). Pelo menos duas e geralmente as quatro extremidades estão envolvidas, carretando um crescimento desproporcional entre os dedos (fig ). São comuns a febre e a leucocitose; as alterações radiográficas com afinamento cortical e destruição dos metacarpos, metatarsos e falanges, aparecem em 2 a 3 semanas após o início dos sintomas. Os episódios são autolimitados e se resolvem dentro de 1 a 2 semanas, sendo a recorrência comum. Tratamento com sintomáticos. 84
85 Figura Síndrome mão-pé. Mão de uma criança com anemia falciforme, com edema e dor. Figura Dactilite (Síndrome mão-pé). Mão de uma jovem de 16 anos, com marcante encurtamento do dedo médio da mão direita, por alteração no crescimento da epífise. Síndrome do Quadrante Superior Direito Na anemia falciforme, a análise histológica do fígado revela distensão dos sinusóides com células falciformes, eritrofagocitose das células de Kupffer, graus variados de fibrose periportal e pigmento de hemossiderina. Pode haver distúrbios da função hepática, e a dilatação aguda do fígado (por seqüestro de células falciformes, infarto subcapsular ou trombose de veia hepática) está associada a sensibilidade ou dor do quadrante superior direito. 85
86 A síndrome é caracterizada por dor abdominal, febre e icterícia. A diferenciação entre colecistite e a crise hepática pode ser difícil, sendo que o quadro clínico, os níveis de bilirrubina direta e indireta, e a ultrassonografia abdominal são dados úteis para elucidar o diagnóstico. A colelitíase acomete 75% dos pacientes com HbSS, e 90% destes realizam colescistectomia (profilática ou terapêutica); os cálculos biliares foram documentados em crianças com menos de 5 anos de idade, e sua incidência aumenta com a faixa etária. O seqüestro agudo de eritrócitos falcizados nos sinusóides hepáticos é caracterizado ado por hepatomegalia associada a uma queda da hemoglobina, mas sem alterações significativas na função hepática. A crise hepática (também chamada de colestase intra-hepática falciforme) é caracterizada por episódio súbito de dor no hipocôndrio direito, hepatomegalia progressiva, aumento importante do nível de bilirrubinas (principalmente indireta) e alteração do coagulograma. O nível das enzimas hepáticas também encontram-se aumentados mas não como nas hepatites virais. A gravidade dos episódios variam de leve à grave (com risco de vida). O diagnóstico diferencial dessas condições devem ser feitos com hepatite viral, doença hepática auto-imune, colangite esclerosante, coledocolitíase e colecistite, todos os quais podem ser encontrados nos pacientes com doença falciforme. Nesses casos, a biópsia hepática é importante para elucidação do diagnóstico. O tratamento para a hepatopatia falciforme inclui ex-sangüíneo transfusão e infusão de plasma fresco para corrigir a coagulopatia e reverter a colestase intra-hepática. Síndrome Torácica Aguda (STA) Caracterizada por dor torácica, febre, dispnéia, infiltrados pulmonares e declínio do nível basal de hemoglobina. Consiste na maior causa de morte e hospitalização entre os pacientes com doença falciforme. É três vezes mais freqüente em crianças do que em adultos e é mais comum na HbSS, seguido pela Sb 0 -talassemia, doença da HbSC e Sb + -talassemia. A incidência da STA é inversamente proporcional ao nível de HbF e ao grau de anemia, mas diretamente proporcional ao nível basal de leucócitos, além disso, está intimamente associada às crises dolorosas principalmente em adultos (30 a 50% dos episódios de STA são precedidos ou acompanhados por crises dolorosas). Para avançar no conhecimento da causa e evolução da síndrome, um recente estudo prospectivo e multicêntrico envolvendo 538 pacientes com STA foi desenvolvido. O tempo médio de hospitalização destes pacientes foi >10 dias, sendo associado à idade avançada, dor nos membros à apresentação, febre, diminuição do nível de plaquetas, alterações radiológicas extensas, terapia transfusional e insuficiência respiratória (principalmente em pacientes cardiopatas, com 4 ou mais lobos pulmonares afetados e com plaquetas < ). Cerca de 22% dos pacientes com STA desenvolveram complicações cações neurológicas, e metade destes evoluiu com insuficiência respiratória; o mecanismo provável seria uma queda súbita da oxigenação no leito vascular do sistema nervoso central. As causas da STA até então raramente identificadas puderam ser estabelecidas em 38% dos casos, e o infarto pulmonar presumido em 16% dos casos, onde a embolia gordurosa (liberação de gordura secundária a infarto da medula óssea) e a infecção (especialmente a pneumonia 86
87 adquirida na comunidade) foram causas comuns. Dentre os organismos identificados e associados à STA, achlamydia pneumoniae foi o mais freqüente, seguida por Mycoplasma pneumoniae e o vírus (vírus sincicial respiratório e parvovírus). O tratamento da STA consiste em antibioticoterapia de amplo espectro, associada a um macrolídeo; broncodilatadores devido à hiperreatividade das vias aéreas; transfusão precoce e de rotina para os pacientes de alto risco, incluindo adultos com história de cardiopatia e dor intensa nos membros à apresentação; na maioria dos pacientes com anemia, a transfusão simples cruzada e pobre em leucócitos é segura e eficaz. Priapismo Ocorre pela diminuição da drenagem sangüínea do pênis decorrente da congestão dos corpos cavernosos e esponjosos pelas células falcizadas. A apresentação aguda é caracterizada por ereção dolorosa e persistente, que ocorre geralmente após uma relação sexual ou acorda o paciente pela manhã, sendo freqüente a necessidade de intervenção cirúrgica - uma vez que respondem mal à eritrocitoaférese. O priapismo crônico é caracterizado acterizado por semi-ereção nãodolorosa do pênis; os pacientes podem ficar impotentes, sendo beneficiados neste caso com aconselhamento psicológico e uso de próteses. Úlceras de Perna A ruptura da pele sobre o maléolo e porções distais das pernas é um problema recorrente durante a vida adulta (fig ). Ocorre em cerca de 5 a 10% dos pacientes adultos com HbSS, sendo mais comum no sexo masculino e em pacientes adultos. É menos comum nos pacientes com deleção do gene a, com alto nível de Hb total, e naqueles com aumento de HbF. A etiologia é provavelmente multifocal e associada à hipóxia local e deficiência do fluxo sangüíneo na microvasculatura do músculo gastrocnêmio. São características a infecção secundária da úlcera com destruição das bordas e a extensão progressiva. Osteomielite pode complicar úlceras crônicas, principalmente aquelas com feridas profundas. 87
88 Figura Necroses e ulterações no tornozelo de um paciente com anemia falciforme devido a estase vascular e isquemia nas regiões inferiores das pernas. O tratamento é feito principalmente com cuidados locais, mas pode requerer terapia transfusional, enxerto de pele, e uso de sulfato de zinco e oxigênio hiperbárico. Necrose Avascular No fêmur, ela ocorre em cerca de 10% dos pacientes com doença falciforme. Acomete principalmente as cabeças do fêmur e úmero, assim como corpos vertebrais, devido ao suprimento sangüíneo terminal limitado e à pouca circulação colateral dessas áreas tornando- as mais vulneráveis à falcização e lesão óssea. Os pacientes com doença falciforme e deleção do gene a(talassemia alfa) têm maior incidência de necrose avascular. A efusão das articulações, dor, febre e leucocitose que acompanham tais infartos tornam difícil a diferenciação de atrite séptica. O tratamento é sintomático, mas nas formas avançadas pode ser preciso a substituição total do osso; artroplastia e colocação de próteses podem ser feitas, mas são dotadas de muitas complicações. Acidente Vascular Cerebral (AVC) O AVC é uma complicação catastrófica da doença falciforme, e uma das maiores causas de morte em crianças e adultos. Frempong e cols. encontraram uma prevalência de 3,7% desta complicação na doença falciforme, sendo maior nos pacientes com HbSS (4,0%), seguido pela Sb-talassemia (2,4%), Sb+talassemia semia (1,3%) e HbSC (0,8%). A incidência é igual em ambos os sexos, sendo mais freqüente nos pacientes com 1 a 9 anos de idade. Mais da metade dos AVCs são isquêmicos (54%), seguido pelos hemorrágicos (cerca de 34%) e pelos acidentes vasculares transitórios (AIT - 10%). O AVC isquêmico é mais freqüente em pacientes com menos de 20 anos de idade, e o hemorrágico - responsável por alta taxa de mortalidade (24% nas duas primeiras semanas após o evento) - tem sua maior incidência dos 20 aos 29 anos de idade. 88
89 A recorrência após um episódio de AVC é alta, cerca de dois terços das crianças não transfundidas apresentarão um novo episódio em 3 anos. O principal fator de risco é o AIT prévio, seguido por baixo nível de Hb, antecedentes de STA e pressão arterial sistólica elevada. O quadro clínico inicial é caracterizado por hemiparesia aguda e convulsões, tendo pior prognóstico nas crianças mais jovens. Hemiparesia residual crônica, retardo mental e episódios convulsivos de difícil controle constituem a evolução habitual. A ocorrência desta complicação é provavelmente multifatorial e sua fisiopatologia pouco conhecida. O local da oclusão ocorre mais ao nível dos vasos cerebrais maiores do que na microvasculatura (principalmente artéria cerebral média e carótida interna). Além disso, outros fatores têm sido implicados, como a presença de um estado hipercoagulável demonstrado pelos baixos níveis de proteína C e hiperhomocisteinemia nos pacientes com doença falciforme que desenvolveram AVC. Além da adesão aumentada dos eritrócitos rócitos falcizados ao endotélio vascular, a regulação anormal dos tônus vascular também contribui para a vaso-oclusão, e têm- se demonstrado que os níveis de óxido nítrico um importante regulador do tônus vascular normal, adesão celular e trombose podem estar diminuídos na doença falciforme. O ultrassom-doppler-transcraniano transcraniano pode detectar lesões obstrutivas nas artérias cerebrais e, deste modo, identificar os pacientes falcêmicos com alto risco de desenvolver AVC. O tratamento consiste em ex-sangüíneo transfusão ou hipertransfusão. Na terapia transfusional crônica, o objetivo é manter a HbS < 30%, o que reduz o risco de recorrência para menos de 10%. Em geral, as transfusões são realizadas por um mínimo de 5 anos, após os quais a continuação da terapia transfusional é individualizada. Dados crescentes vêm defendendo a necessidade de terapia prolongada, possivelmente por toda vida em alguns pacientes. O AVC agudo ou iminente é indicação absoluta de ex-sangüíneo transfusão, cujo objetivo é manter a Hb em torno de 10 g/dl e a HbS abaixo de 30%, além de evitar a hiperviscosidade e as alterações de volume. A principal conseqüência do regime transfusional crônico é a sobrecarga de ferro e a necessidade de quelação com a deferoxamina, sendo reportada a eritrocitaférese como modalidade terapêutica para esta complicação. Crises Dolorosas É a complicação mais comum dos pacientes com anemia falciforme, cuja freqüência e gravidade variam consideravelmente de paciente para paciente, e no mesmo paciente. Estima-se que anualmente, cerca de 60% dos pacientes terão um episódio grave de dor. Estresse de qualquer tipo (infecção, temperaturas extremas, estresse físico ou emocional) pode precipitar o episódio doloroso, que geralmente afeta os ossos longos e articulações, sendo a região lombar o local mais freqüentemente referido. A freqüência das crises dolorosas variam diretamente com o hematócrito e inversamente com o nível de hemoglobina Fetal. Pacientes com HbSS e Sb 0 -talassemia têm duas vezes mais crises por ano que aqueles com HbSC e Sb + -talassemia. A oclusão microvascular, em maior parte na medula óssea, inicia o episódio agudo de dor. Acredita-se que a isquemia tecidual decorrente da oclusão microvascular pela falcização "in situ", causa lesões e infarto do tecido que por sua vez deflagra uma resposta inflamatória secundária, e esta, leva ao aumento da atividade do sistema simpático com conseqüente aumento da isquemia tecidual, criando um ciclo vicioso. 89
90 Uma crise dolorosa grave tem sido definida como aquela que requer tratamento com opióide parenteral por 4 horas ou mais, tal evento é geralmente tratado no hospital com uma média de permanência em torno de 10 dias para o adulto. A ocorrência de três ou mais crises por ano no mesmo paciente indica doença falciforme grave. As crises dolorosas são mais comuns durante a terceira e quarta décadas de vida, e a mortalidade aumenta nos adultos com maior número de episódios dolorosos. Tratamento das Crises Dolorosas Tratar a causa da crise (caso possa ser identificada). Iniciar analgesia prontamente. Hidratação vigorosa com 3 a 4 litros/dia em pacientes adultos (via oral se possível, intravenoso se necessário). Tratar crises dolorosas agudas e graves da seguinte forma: 1. administrar morfina, meperidina ou hidromorfone parenteral, em doses cheias, com intervalo de 2 a 4 horas. Checar a dor freqüentemente. 2. Não especificar tratamento "se necessário". 3. Considerar a associação de drogas como hidroxizine, difenidramina, prometazina ou um anti-inflamatório não esteroidal. 4. Considerar analgesia paciente-controlada, controlada, caso sejam necessárias doses mais freqüentes. Usar escalas de dor (escala análoga, 0 [ausente] até 10 [insuportável] para guiar a eficácia do tratamento e determinar as doses. Tratar dor crônica ou dor leve a moderada como se segue: 1. usar adesivos de fentanil para dor moderada a grave prolongada. 2. Usar acetaminofen com codeína para dor leve a moderada, sem necessidade de atendimento médico. 3. Administrar anti-inflamatório inflamatório não esteroidal para a dor de osteonecrose, quando não houver contra-indicação cação de seu uso por insuficiência renal ou hepática. Interferentes que acentuam ou minimizam a Anemia Falciforme A anemia falciforme tem um desenvolvimento clínico extremamente variável que se caracteriza principalmente por diferentes graus de intensidade de da anemia hemolítica. As razões dessa variabilidade são parcialmente conhecidas na expressão fenotípica da doença. Apesar de ter um mesmo defeito genético, a anemia falciforme pode estar associada com níveis diferentes de Hb Fetal e interações com talassemia semia alfa que atuam como moduladores genéticos da doença. Entretanto, outros defeitos genéticos dos eritrócitos, com destaques para a deficiência de G- 6PD, a esferocitose e as deficiências de enzimas anti-oxidantes (SOD, GPx e catalase) certamente interferem rem no curso clínico da doença. Os diferentes haplóticos de Hb S denominados por Banto, Benin, Senegal, Camarões e Asiático, tem sido apontados também como possíveis causas da heterogeneidade fenotípica da anemia falciforme. Toda essa diversidade que caracteriza a anemia falciforme está, em parte, relacionada à sua origem multicêntrica (consultar item 2.2) e que envolvem populações com diferentes anormalidades genéticas de proteínas e enzimas eritrocitárias. Por outro lado, além desses fatores caracterizados como interferentes eritrocitários, há os interferentes do meio ambiente em que 90
91 está inserido o doente falciforme. Entre os interferentes ambientais destacam-se as situações sociais, econômicas e culturais do doente, e que tem influencia no curso de sua doença. Principais consequências dos interferentes ambientais, sociais e econômicos na anemia falciforme Os principais interferentes ambientais que certamente tem influência nas consequências fisiopatológicas da anemia falciforme podem ser agrupados em três classes distintas, muitas vezes indissociáveis, e aqui identificados por: (a) meio ambiente, (b) deficiência alimentar e qualidade nutricional inadequada e (c) deficiência nas assistências médica, social e psicológica. Como se sabe, a grande maioria dos doentes falcêmicos e, notadamente aqueles com anemia falciforme, no Brasil, tem sua origem proveniente dos negros africanos. Historicamente os negros foram introduzidos como escravos nesse país e, mesmo com a libertação desse regime, seus descendentes tiveram poucas oportunidades de se desenvolverem social e economicamente como seria de se desejar. Nesse contexto, a maioria da população negra brasileira e, consequentemente os doentes falcêmicos, habitam as regiões mais pobres e carentes das nossas cidades. Os aspectos ambientais desses locais de moradias se caracterizam, em geral, pelas deficiências de saneamento básico, poluição ambiental, violência, qualidades inadequadas do ar, da água, de transportes e de higiêne, entre outros. A pobreza a que estão subjugados a maioria da população negra em nosso país, determina uma situação nutricional deficiente e desbalanceada, notadamente de proteínas e vitaminas. As águas contaminadas por nitritos e microorganismos provenientes de dejetos humanos e animais são fatores que concorrem para acentuar a mortalidade dos pacientes falcêmicos. As deficiências nos atendimentos médico e social, por sua vez, são determinantes para a queda da expectativa de vida e falta de auto-estima do doente falcêmico. O atendimento médico especializado para o falcêmico está restrito a pouquíssimos centros, fato que o torna inexpressivo em nosso país. Somam-se a esta situação o desconhecimento o médico e paramédico no que se refere à clínica, ao tratamento, ao diagnóstico clínico e laboratorial, e ao acompanhamento adequado e seguro do doente. Por outro lado, os atendimentos social e psicológico sofrem idênticas insuficiências acima expostas. Todos esses fatores listados como interferentes ambientais contribuem com as diversidades clínicas e hematológicas da anemia falciforme. Um exemplo específico dos interferentes decorre da oxidação da Hb S por gases poluentes (No x e So x ), bem como dos alimentos e água contaminados por nitritos. A susceptibilidade à oxidação da hemoglobina é muito maior em pessoas com deficiências de enzimas anti-oxidantes, como são os casos de superóxido dismutase (SOD) glutatião peroxidase (GPx) e catalase. Assim, é de se esperar erar que na Hb SS a deficiência de uma dessas enzimas anti-oxidantes tenha influência na destruição precoce do eritrócito, e essa destruição poderá ser muito maior se o ambiente em que vive o paciente falcêmico contém gases poluentes oxidantes. Dessa forma, é importante para os profissionais médicos e paramédicos que se dispõe a prestar assistência médica, social, psicológica e laboratorial, tenham também amplo conhecimento da história relatada de cada um dos pacientes falcêmicos, com referências ao seu modo o de vida, dos ambientes em que vivem e trabalham, bem como das suas dificuldades diárias (transportes, alimentação, desemprego, violência, etc.). 91
92 Interações da Hb SS com Deficiência de G-6PD A deficiência de G-6PD é uma alteração genética recessiva ligada ao cromossomo X, cujo grau de heterogeneidade clínica e hematológica está na dependência de um dos cinco tipos em que é classificada (tabela 7.3.1). A deficiência de G-6PD tem elevada prevalência na África, alcançando valores de 30% em determinadas regiões, se distribui coincidentemente no continente africano na mesma faixa da Hb S e, da mesma forma que no traço falcêmico, há evidências de que o portador desta enzimopatia seja também resistente ao desenvolvimento do ciclo da parasitose do Plasmodium.. No Brasil a prevalência da deficiência de G-6PD é variável entre 1 e 4% nas pessoas brancas e entre 9 e 15% entre as pessoas negras. Por essas razões não é rara a observação da associação entre anemia falciforme e deficiência de G-6PD numa mesma pessoa. As vantagens ou desvantagens seletivas nessas associações ainda são discutíveis, mas por outro lado há evidências comprovadas de que sob circunstâncias que desencadeiam a oxidação da hemoglobina, como são os casos do uso de drogas oxidantes, ocorrem graves crises hemolíticas quando há associação entre anemia falciforme e deficiência de G-6PD. Entretanto, há de se considerar a heterogeneidade da hemólise e anemia causadas pela deficiência dessa enzima devido aos diferentes tipos (tabela 7.3.1), fato que certamente interfere em graus diversos quando associados à anemia falciforme. Tabela Relação entre as cinco classes de G-6PD e Anemia Hemolítica. Classe 1 Classe 2 Classe 3 Classe 4 Classe 5 Variantes deficientes associadas à anemia hemolítica crônica. Exemplo: variante New York Variantes com deficiência acentuada da atividade da enzima G-6-PD (menos de 10% da atividade normal). Exemplo: Variante Mediterrânea. Variantes com deficiência moderada da atividade da enzima G-6-PD (10 a 60% da atividade normal). Exemplo: Variante Africana ou 6-GPD A. Variantes com deficiência discreta da atividade da enzima G-6-PD (60 a 100% da atividade normal). Variantes com atividade da enzimática aumentada da enzima G-6-PD. A Classe 1 é muito rara As Classes 2 e 3 são as mais importantes sob o ponto de vista clínico, pois causam crises de hemólises quando o portador é exposto à drogas oxidantes. No Brasil, a deficiência de G-6-PD mais comum é a de classe 3 - Africana (87% dos casos), seguida de classe 2 - Mediterrânea (com 12% dos casos). Interações da Hb SS com Persistência Hereditária de Hb Fetal A concentração máxima de Hb Fetal no sangue de uma pessoa com idade superior a seis meses é variável de 1 a 2%, dependendo do método usado para sua avaliação, e está restrita a poucos eritrócitos identificados por células-f. Cerca de 3 a 7% dos eritrócitos contém Hb Fetal e cada um deles tem 4 a 8 picogramas (pg) de Hb Fetal juntamente com 22 a 26 pg de Hb A. O número 92
93 de células-f de um indivíduo está sob controle genético, embora não se sabe se é do tipo monogênico ou poligênico. Tanto o número de células-f e a quantidade de Hb Fetal em cada célula-f pode estar aumentado em várias condições genéticas ou adquiridas. Entretanto, as duas principais situações em que o nível de Hb Fetal está elevado são a persistência hereditária de Hb Fetal (PHHF) e nas diversas formas de talassemias beta. Em ambos os casos as alteraçòes hematológicas avaliadas laboratorialmente são diferentes (tabela ). Por outro lado, o aumento de Hb Fetal causada por situação adquirida se deve especialmente ao uso de determinadas drogas, como se verá adiante. Na PHHF a síntese de Hb Fetal continua mesmo após o sexto mês de vida, com valores cujas elevações são variáveis entre 1 a 100%. As duas principais causas da PHHF se devem a diferentes deleções que atingem os dois genes gama (glicina e alanina) do cromossomo 11, e às mutações que não são por deleção (mutações de não-deleção). Entre as pessoas soas de raça negra, a PHHF se deve às deleções nos genes gama, com concentrações de Hb Fetal variáveis de 5 a 30% entre os heterozigotos, e os portadores são clínica e hematologicamente normais (tabela ). Na PHHF homozigota os níveis de Hb Fetal podem chegar entre 90 e 100%, e apesar dos portadores serem saudáveis é comum a presença de eritrocitose e a hipocromia, com valores hematimétricos similares ao da talassemia beta menor. Os portadores de PHHF por mutações de não-deleção tem eritrócitos normais e ausência de manifestações clínicas. A elevação de Hb Fetal nesses casos é muito variável e, da mesma forma, a distribuição intraeritrocitária pode ser pancelular ou heterocelular (tabela ). O significado clínico da associação da PHHF na anemia falciforme se mostra favorável hematologicamente conforme mostra a tabela 3.3.1, pois nesta interação Hb SS/PHHF as células-f tem baixas concentrações de Hb S, fato que inibe a polimerização da Hb S bem como o desencadeamente da falcização dos eritrócitos. Assim, admite-se que a concentração intraeritrocitária da Hb Fetal seja particularmente útil na proteção contra o processo de falcização por não interagir com a Hb S quando esta se insolubiliza. Testes realizados "in vitro" em soluções desoxigenadas contendo Hb Ae Hb S, mostraram que ocorre a insolubilização e precipitação somente da Hb S, e ao se redissolver o precipitado se detecta ambas hemoglobinas A e S. O mesmo experimento realizado em soluções contendo Hb Fetal e Hb S mostraram que a Hb Fetal não se precipita como a Hb S, e este fato sugere que as globinas gama exercem um efeito inibidor sobre a polimerização das globinas beta S, evitando a falcização. As evidências de que a elevação de Hb Fetal em pacientes com anemia falciforme seja um fator moderador das consequências clínicas do processo da falcização, fizeram com que muitos pesquisadores se interessassem em conhecer as situações fisiológicas e terapêuticas capazes de elevarem evarem a síntese de Hb Fetal. Assim, um dos primeiros trabalhos nesse sentido se deu pela observação de que gestantes a partir do segundo trimestre de gestação apresentavam níveis elevados de Hb Fetal. Com base nesses dados Beutler, em 1969, administrou gonadotrofina coriônica humana (hcg) em pacientes com anemia falciforme e obteve discretas elevações no nível de Hb Fetal. Da mesma forma, a progesterona foi administrada em pacientes com Hb SS, cujos resultados divulgados em 1969 por Beutler, e em 1982 por De Ceulaer e cols, mostraram outra vez que a Hb Fetal apresentava-se com discretas elevações de seus níveis em relação ao nível basal de cada paciente. Os estudos na busca de medicamentos que elevassem os níveis de Hb Fetal continuaram com De Simone e cols em 1982 de forma experimental em babuinos anêmicos, que passaram a receber por via sub-cutânea a droga 5-azacitidina (Aza-C) (16). Os animais que receberam a Aza-C tiveram elevações de síntese de Hb Fetal entre 70 e 80% do conteúdo total de hemoglobina e o aumento de células-f em 90% dos eritrócitos, enquanto que reciprocamente a síntese de globina-beta s diminuía. Esses primeiros relatos promoveram buscas incessantes de medicamentos que pudessem ser aplicados de forma terapêutica em pacientes com doenças graves causadas por anormalidades de síntese de globina-beta. beta. A partir desses relatos vários pacientes com talassemia maior e anemia falciforme foram estudados por Ley e cols em 1982 e 1983, Charache e cols em Esses pacientes após terem recebido Aza-C por 93
94 via intravenosa, apresentaram aumento na concentração de Hb Fetal e no número de células F, geralmente nos primeiros 2 e 3 dias, e atingido níveis máximos de elevação entre quatro e sete vezes acima do valor da Hb Fetal dosada antes do tratamento. As avaliações das células falcêmicas desses pacientes mostraram que o número de células densas diminuíram, bem como o grau de hemólise. Estudos realizados com outros agentes quimioterápicos como a citosina arabinosídeo (ARA-C) e efetuados por Papayannopoulo e cols em 1984, a vinblastina por Veith e cols em 1985, e Mileran por Liu e cols em 1990, também mostraram efetivo estímulo na síntese de Hb Fetal. Apesar da eficácia dessas drogas em elevar a síntese de Hb Fetal, os efeitos citotóxicos, e inclusive sua potencialidade carcinogênica, fizeram com que as mesmas fossem abandonadas como uso terapêutico na anemia falciforme e talassemia beta. Paralelamente a esses estudos, as pesquisas desenvolvidas com hidroxiuréia (HU) - um agente quimioterápico usado desde os anos 60 passaram a ser mais promissores. Primeiramente porque esta droga não é incorporada ao DNA, como são os casos de Aza-C, Ara-C e Mileran, e sua ação decorre por inibir a ribonucleotíde-redutase, redutase, uma enzima que converte ribonucleotídeos em desoxiribonucletídeos para a síntese de DNA. Embora a HU tenha modestos efeitos em vários tipos de tumores, o seu uso clínico em oncologia está limitado ao controle das fases crônicas da leucemia mielóide crônica e na rápida redução do número de células blásticas em pacientes com leucemias agudas durante a fase inicial de tratamento, além do uso também no tratamento da policitemia primária ou policitemia vera. Os primeiros resultados dos efeitos positivos da HU, caracterizados pela elevação dos níveis de Hb Fetal em pacientes com anemia falciforme surgiu em Embora a HU também tenha seus efeitos avaliados em 299 pacientes falcêmicos, americanos e canadenses, mostraram que os episódios de crises dolorosas diminuíram significativamente ao longo de um ano de rigorosa avaliação. Apesar disso, estudos multicêntricos estão levantando os resultados do uso da HU associados com várias características clínicas, genéticas e de efeitos terapêuticos. Finalmente, a busca de outras drogas que elevam os níveis de Hb Fetal, como são os casos da eritropoietina (Epo) e butiratos, ainda apresentam grandes diversidades de resultados, fatos que tornam suas eficácias ainda inconclusivas. A tabela apresenta as principais drogas capazes de elevarem os níveis de Hb Fetal em humanos. Tabela Fenótipos de persistência hereditária de Hb Fetal (PHHF) heterozigota e talassemia beta menor, relacionados com alterações hematológicas, concentração e distribuição celular de Hb Fetal. Aspectos laboratoriais PHHF Talassemia beta menor Morfologia ogia dos eritrócitos Normal Microcítica Hemoglobina corpuscular média Normal (*) Diminuida Hematócrito Normal (*) Diminuído Hb Fetal (%) Distribuição eritrocitária da Hb Fetal Pancelular Heterocelular (*)Podem estar diminuidos na homozigose 94
95 Tabela Persistência hereditária de Hb Fetal por deleções nos genes gama. Grupo Étnico Tamanho da Deleção (Kb) % de Hb Fetal (*) Negro (USA) >70, Negro (gana) >70, Italiano 38, Italiano 44, Negro (Kenya) 22,8 5-8 (*) A distribuição intra-eritrocitária da Hb Fetal é pancelular (ou homogêneo) em todos estes grupos étnicos. Tabela Persistência hereditária de Hb Fetal por não deleção Grupo Étnico Defeito Molecular % de Hb Fetal Distribuição de Hb Fetal Negro C à at Pancelular Italiano C à at Pancelular Grego G à A at Pancelular Chinês C à T at Heterocelular Alemão Não determinado 5-8 Heterocelular Inglês T à C at Heterocelular Suiço Não determinado 1-3 Heterocelular Tabela Drogas capazes de elevar o nível de Hb Fetal. Origem Hormonal Agentes Citotóxicos Fator eritropoiético Drogas HCG - Progesterona Aza-C, Ara-C, Metotrexato, HU Eritropoietina Ácidos graxos de Butirato-arginina, arginina, Isobutiratos, Fenilacetato, cadeia curta Fenil-butirato, Ácido valpróico Interações da Hb SS com Esferocitoses e Eliptocitoses A esferocitose hereditária é uma doença geneticamente heterogênea do tipo dominante, causada por alterações nas composições protéicas da membrana eritrocitária. A associação entre anemia 95
96 falciforme e esferocitose hereditária está, portanto, na dependência dos interferentes da própria anemia falciforme (exemplo: talassemia alfa, Hb Fetal, etc.) e o grau de lesão protéica causadora da esferocitose hereditária. Entretanto, de forma geral, a simples associação entre essas duas patologias causa anemia hemolítica com maior intensidade e esplenomegalia, do que usualmente se verificam na anemia falciforme. Presume-se, se, assim, que a piora do quadro hematológico se deve à combinação dos efeitos hemolíticos das duas doenças. Por outro lado há relatos de pacientes com Hb SS e Hb Fetal elevada (entre 13 e 20%) que, apesar da associação com a esferocitose, apresentavam poucas crises de hemólises. Deficiência de Enzimas Eritrocitárias Anti-Oxidantes (SOD, catalase, GPx) Consultar o ítem 4.3 deste capítulo e o capítulo específico "Radicais Livres e danos eritrocitários". Prevalência e Controle do Gene da Hb S Distribuição Geográfica Mundial. Desde os anos 50 muitos estudos tem sido realizados em diferentes partes do mundo com o objetivo, inicialmente de se conhecer prevalência e medidas preventivas, e mais recentemente para o conhecimento dos haplótipos. As mais altas prevalências do gene ß s, caracterizado pela identificação do heterozigoto ou portador do traço falcêmico (Hb AS) superam 40% em alguns vilarejos do leste africano, e situa-se se acima de 20% nos países da África equatorial: Camarões, Guiné, Zaire, Uganda e Kenia. Também, em países asiáticos como Arábia Saudita, Emirados Árabes e regiões da India, a prevalência da Hb AS atinge até 20% da população. Em regiões próximo ao extremo asiático como o Nepal, a freqüência do gene ß s (Hb AS) é de 5%. Na região que circunda o mar Mediterrâneo, incluindo a costa norte da África, Turquia, Líbano, Síria e Grécia, bem como em Portugal e Irã, as prevalências situam-se se entre 2 e 5%. Entretanto é importante destacar que dentro dessas regiões (ou países) a prevalência varia consideravelmente entre vilarejos ou grupos raciais, como são os casos dos Eti-Turcos na Turquia (14%), e entre os Khazramah na Síria (25%). Em todas as regiões descritas, pode-se invocar a hipótese malária como fator das altas freqüências do gene ß S. Porém, a presença da Hb S no "novo mundo", onde se incluem principalmente os Estados Unidos da América, Venezuela, Colombia, Jamaica, Cuba e Brasil, a presença de Hb S não pode ser explicada pela hipótese-malária, uma vez que foram introduzidos notadamente por escravos africanos. Outros países europeus como a Itália, principalmente na Sicília e Calábria Holanda, Inglaterra e França, apresentam prevalências variáveis entre a 3% do gene ß S. Na Itália a indrodução do gene ß S certamente ocorreu a partir das conquistas efetuadas pelo Império Romano na África, enquanto que na Holanda, Inglaterra e França a imigração de africanos pertencentes a ex- colonias tende a elevar prevalência de Hb S ao longo dos próximos anos. 96
97 As hemoglobinopatias se apresentam como doenças de importância na saúde pública de vários países latino-americanos. americanos. Particularmente nas ilhas do Caribe, onde a população é predominantemente de negros e a frequência de doenças faciformes é significativamente alta. Alguns desses países desenvolveram programas de controle de hemoglobinopatias com sucesso, como são os casos de Martinica, Guadalupe, Jamaica e Cuba. Por outro lado, dois dos países com altas prevalência de doenças falciformes: República Dominicana e Haiti, caracterizados como os países mais pobres das Américas, carecem de qualquer tipo de programa preventino e de controle. Especialmente com relação a Cuba, cuja população é constituída por 65% de brancos de descendência espanhola e 35% de negros do oeste da África, e que apresenta atualmente uma população muito miscigenada, onde 10 milhões de pessoas são mulatas, desde o início dos anos 60, este país desenvolveu um sistema de saúde preventiva com ênfases aos cuidados primários, e o mesmo tempo investiu em tecnologia ogia para os centros especializados em Medicina terciária. Além de ter desenvolvido programa de controle às infecções e à subnutrição, com resultados positivos que diminuíram os índices de mortalidade (em 1990: 10,8 por 1.000) e morbidade, desenvolveu também controles preventivos para hemoglobinoptias. As frequências de Hb AS e Hb AC variam entre 3 a 7% e a expectativa de nascimento anual de crianças com doenças falciformes é cerca de 100 casos novos. Esse reduzido número de nascimento de crianças com doenças falciforme se deve aos programas de prevenção em gestantes, com aproximadamente 160 mil análises eletroforéticas de hemoglobinas por ano. Para as gestantes portadoras de Hb AS, os estudos se ampliam aos seus companheiros e familiares. Além da identificação de casais de risco (ambos com Hb AS), o serviço de saúde oferece o diagnóstico pré-natal por meio de análise do DNA, e na positividade do feto ser portador de anemia falciforme, sugere-se o aborto. A Venezuela e a Colômbia apresentam populações com significativas freqüência de negros e mulatos e, consequentemente, as prevalências de Hb S nos dois países também são altas. Estudos realizados em indígenas venezuelanos e colombianos não revelaram a presença de hemoglobinopatias em suas populações nativas. As talassemia beta representam baixos índices de prevalência nos países, e ambos não têm nenhum programa de prevenção até o presente. A Argentina, composta predominantemente por populações nativas e de origens européias, estas provenientes da Itália e principalmente ipalmente da Espanha, tem na talassemia beta o tipo mais comum de hemoglobinopatias e somente em Buenos Aires, em 1990, havia registrado cerca de 100 casos de talassemia maior. Também nesse país não há programas preventivos de hemoglobinopatias. Entre os países da América Central que incluem Guatemala, Honduras, El Salvador, Nicarágua, Costa Rica e Panamá, com uma população total próxima de 30 milhões de habitantes a maioria das hemoglobinopatias foi encontrada entre os negros e mulatos. As prevalências de Hb S e Hb C apresentam grande variabilidade, de um país para outro. Por exemplo, na Costa Rica, a freqüência média de Hb AS é de 11% na sua população negra, enquanto entre os negros da Guatemala é de 18% e do Panamá é de 20%. Na Costa Rica, por ter um Centro de Hemoglobinopatias mais avançado entre os países da América Central, detectou-se 2,0% de talassemia alfa e 0,2% de talassemia beta heterozigota em estudos populacionais. Finalmente, o México, que tem a segunda maior população entre os países latino-americanos (cerca de 90 milhões de habitantes), apresenta sua composição étnica predominantemente de origem indígena, além de mestiços provenientes do cruzamento com espanhóis. entre as hemoglobinopatias mais prevalentes destaca-se a talassemia beta heterozigota (0,1%), enquanto os casos de Hb S são esporádicos. Outros países latino-americanos, americanos, como o Uruguai, Bolívia, Equador, Paraguai, Peru e Chile, carecem de informações a respeito da prevalência de hemoglobinopatias em suas populações. 97
98 Distribuição Geográfica no Brasil As populações brasileiras caracterizam-se, em geral, por apresentarem grande heterogeneidade genética, derivada da contribuição que lhes deram os seus grupos raciais formadores, de si também já muito diversificados, e dos diferentes graus com que eles se intercruzaram nas várias regiões do país. O processo de miscigenação pode ser analisado sob o ponto de vista de distribuição geográfica. Os estados de Minas Gerais e Rio de Janeiro e a região litorânea do Nordeste apresentam, de forma mais intensa, a miscigenação branco-negra. negra. Já o interior do nordeste e o extremo norte (Amazonas, Pará e parte do Maranhão) serviram de palco principalmente para a o processo de mestiçagem branco-indígena, que também se pode observar nos estados de Mato Grosso, Mato Grosso do Sul e Goiás. Na região sul, por sua vez há visível predominância do indivíduo branco, pois como já foi citado anteriormente sobre a heterogeneidade eidade étnica, pode-se constatar que enquanto nos estados do norte e nordeste a contribuição por portugueses predominou de forma quase absoluta, nos do sul as diferentes correntes imigratórias condicionaram maior variabilidade étnica. Assim, as prevalências das hemoglobinopatias e talassemias estão intimamente relacionadas com as etnias que compõe a nossa população. Nesse contexto se insere o estudo que realizamos sobre a prevalência do gene ß S na população brasileira. O estudo efetuado por meio de análises de 101 mil amostras de sangue provenientes de 65 cidades de dezesseis estados do Brasil (tabelas e 8.2.2) revelaram que a prevalência do portador do traço falcêmico na população brasileira em geral é de 2,1%, entre pessoas de cor branca é de 1.18%, e entre pessoas de cor negra é de 4.87%, com ampla variação regional (figura 8.2.1). É notável a diminuição da prevalência de Hb AS na população total na direção norte-sul do Brasil (tabela 8.2.2), enquanto que a prevalência entre as pessoas de cor negra se mantém num nível quase homogêneo entre 4,03% e 5,54%. As prevalências de Hb AS por faixas etárias nas populações gerais (brancos e negros) das diferentes regiões do Brasil podem ser avaliadas na tabela Os valores obtidos e analisados estatisticamente, mostram que não há alterações significantes entre as faixas etárias analisadas. Tabela Distribuição porcentual da Hb AS em 101 mil amostras de sangue provenientes de quinze estados brasileiros e Distrito Estados Alagoas Bahia Ceará Distrito Federal Goiás (*) Maranhão Mato Grosso 1,89 3,85 3,05 (*) Minas Gerais Brancos Negros Total 1,67 6,93 4,83 3,68 6,21 5,48 1,38 4,78 2,80 1,83 3,70 2,92 1,91 5,26 3,61 2,48 3,51 3,06 2,44 6,14 3,72 98
99 Pará Paraíba Paraná Pernambuco Piauí Rio de Janeiro 2,80 1,19 1,18 0,88 3,63 2,08 5,02 3,29 4,19 1,80 5,10 5,27 4,40 2,19 1,82 1,33 4,77 3,12 Rio Grande do 1,04 Norte 5,11 3,43 São Paulo Total (média) 0,96 1,18 4,92 4,87 1,54 2,10 (*) Na época das análises não havia a subdivisão dos estados de Goiás e Mato Grosso em Tocantins e Mato Grosso do Sul, respectivamente. Tabela Distribuição porcentual da Hb AS em 101 mil amostras de sangue provenientes das regiões norte, nordeste, centro-oeste, sudeste e leste. Região Norte Nordeste Centro-Oeste Sudeste Sul Caucasóide 2,80 2,18 1,85 1,12 1,18 Negróide 5,14 5,13 4,03 5,54 4,53 Total 4,49 4,05 3,11 1,87 1,87 Tabela Distribuição percentual dos portadores de Hb AS por faixa etária na população geral analisada, obtida de 101 mil amostras de sangue, por região do Brasil. Região Norte Faixa Etária % de Hb AS 5,93 5,45 3,56 5,33 3,36 51 ou ,13 - Nordeste 99
100 Centro-Oeste Sudeste Sul ou ou ou ou + 5,25 3,92 5,00 2,81 2,21 5,08 3,26 3,04 3,27 2,78 2,04 2,12 1,66 2,03 2,35 2,18 1,34 2,71 1,88 1,54 1,65 1,47 1,88 100
101 Figura Distribuição da frequência do gene beta S obtida durante a determinação da prevalência de Hb AS na análise de 101 mil pessoas de todas as regiões do Brasil. Relação entre Sobrenomes e Hb S no Brasil Na avaliação referente ao mapeamento da prevalência do gene ß S nas diferentes regiões do Brasil, analisamos sobrenomes que foram agrupados pela suas semelhanças, resultando 297 sobrenomes no total. O estudo das raízes dos sobrenomes da população estudada indicaram que 69,3% são de origem ibérica, 11,7% religiosa, 10,4% itálica e 8,4% de outras origens. A relação entre os sobrenomes mais freqüentes e pertencentes a pessoas com gene ß S nas cinco regiões do Brasil (norte, nordeste, centro-oeste, sudeste e sul) mostraram que há determinados sobrenomes mais prevalentes em portadores de Hb S, conforme mostra a tabela
102 Tabela Relação dos sobrenomes de portadores do gene ß S, com maior freqüência nas cinco regiões do Brasil. Sobrenome Freqüência % Regiões mais freqüentes Anjos 7,8 ND, CO,SD Galvão 7,4 ND, SD, S Passos 6,1 N, ND, CO Cruz 5,4 ND, CO, SD, S Braga 5,4 N, ND, CO, SD, S Bonfim 4,3 ND, SD, S Gouveia 4,2 N, SD, S Reis 4,0 N, ND, CO, SD, S ND: Nordeste; CO: Centro-Oeste; SD: Sudeste; N: Norte; S: Sul Interferentes Eritrocitários e ambientais na Anemia Falciforme Entre os vários genótipos falciformes identificados na população brasileira, a anemia falciforme é o mais grave e também o que necessita de cuidados médicos com maior freqüência. A anemia falciforme tem um desenvolvimento clínico extremamente variável que se caracteriza principalmente por diferentes graus de intensidade da anemia hemolítica. As razões dessa variabilidade são parcialmente conhecidas na expressão fenotípica da doença. Apesar de ter um mesmo defeito genético, a anemia falciforme pode estar associada com níveis diferentes de Hb Fetal e interações com talassemia assemia alfa que atuam como modeladores genéticos da doença. Entretanto, outros defeitos genéticos dos eritrócitos com destaques para a deficiência de G-6PD, a esferocitose e as deficiências de enzimas antioxidantes (SOD, GPx e catalase) certamente interferem rem no curso clínico da doença. Os diferentes haplótipos da Hb S denominados por Banto, Benin, Senegal, Camarões e Asiático, tem sido apontados também como possíveis causas da heterogeneidade fenotípica da anemia falciforme. Toda essa diversidade que caracteriza a anemia falciforme está, em parte, relacionada à sua origem multicêntrica e que envolvem populações com diferentes anormalidades genética de proteínas e enzimas eritrocitárias (consultar os ítens 2.2 e 7.1 a 7.6). Por outro lado, além desses fatores caracterizados como interferentes eritrocitários, há os interferentes do meio ambiente em que está inserido o doente com anemia falciforme. Entre os interferentes ambientais destacam-se as situações sociais, is, econômicas e culturais do doente, e que tem influência no curso de sua doença. 102
103 Controle e Prevenção das Doenças Falciformes A Organização Mundial da Saúde em sua publicação de 1985 estimou que anualmente nascem no Brasil cerca de crianças com doenças falciformes, das quais com a anemia falciforme, 700 com a dupla heterozigose SC (Hb SC), e 350 com a interação Hb S/tal. ß. Nossos estudos estimam em aproximadamente 10 mil pessoas com doenças falciformes no Brasil. Diante dessas duas avaliações conclui-se que a maioria dos doentes falcêmicos não vivem além dos 4 anos de idade. Assim, o problema das doenças falciformes é muito mais grave do que se pensa, principalmente a vários fatores que incluem: a) o desconhecimento da doença, da clínica e da conduta, por grande maioria dos médicos; b) deficiências no sistema médico, de atendimento de urgências, e assistência social; c) desinformação do profissional de apoio médico: laboratoristas, enfermagem, psicólogos, etc. ; d) condições sócio-econômica-cultural dos doentes e familiares; e) impotência e/ou desinteresse dos governos (municipal, estadual e federal). Com relação ao governo federal o Ministério da Saúde constituiu em 1992 o Comitê de Hemoglobinopatias ligado à Coordenadoria do Sangue e de Hemoderivados (COSAH), que iniciou um trabalho elogiável ao longo de 7 anos e, inexplicavelmente, o comitê foi desfeito. A despeito da falta da organização governamental há esforços mediados por competentes profissionais, em diferentes regiões do Brasil, que preocupados com o descaso, sensibilizaram setores governamentais regionais e conseguiram realizar testes de triagens neonatal. Esses centros obtiveram excelentes resultados, como são os casos do NUPAD de Belo Horizonte, ligado à Universidade Federal de Minas Gerais, do Serviço de Hematologia do Hospital de Clínicas de Porto Alegre (Universidade Federal do Rio Grande do Sul), e do Centro Infantil de Investigações Hematológicas Dr. Boldrini, de Campinas (UNICAMP). Além desses serviços, com grande expressão de resultados, vários outros estão sendo implantados, muitos dos quais pertencentes a universidades, hospitais e hemocentros. Durante trinta anos de atividades em hemoglobinopatias, tivemos a oportunidade de realizar programas preventivos não só de doenças falciformes, mas também de talassemias e outras hemoglobinopatias. Trabalhamos com recém-nascidos, primeira infância, escolares de 2º grau e universitários, operários, gestantes e pacientes ambulatoriais. Os melhores resultados foram obtidos nos programas realizados com os escolares, pois o interesse em conhecer os problemas relacionados à doença começou a fazer parte da divulgação da disciplina de biologia. Penso, portanto, que este é o caminho ideal, pois está intimamente relacionado à educação. Testes Laboratoriais Específicos para Hb S 1. Eletroforese Alcalina 2. Eletroforese Ácida 3. Dosagem de Hb Fetal 4. Pesquisa de Talassemia Alfa 5. Pesquisa de Corpos de Heinz 6. Teste de Falcização 7. Teste de Solubilidade 8. Dosagem de Metahemoglobina 9. Interpretação de Resultados Os testes acima podem ser acionados no capítulo "Técnicas laboratoriais aplicadas aos eritrócitos". 103
Glóbulos vermelhos (hemácias ou eritrócitos)
 Doença Falciforme Glóbulos vermelhos (hemácias ou eritrócitos) Fonte: BESSIS, M. - Corpuscules - essai sur la forme des globules rouges de l homme springer international - 1976 Hemoglobina Função: Captar
Doença Falciforme Glóbulos vermelhos (hemácias ou eritrócitos) Fonte: BESSIS, M. - Corpuscules - essai sur la forme des globules rouges de l homme springer international - 1976 Hemoglobina Função: Captar
CAPÍTULO 1 A DOENÇA DAS CÉLULAS FALCIFORMES
 CAPÍTULO 1 1 A DOENÇA DAS CÉLULAS FALCIFORMES Fenótipos, genótipos e haplótipos A doença causada pelas células falciformes se caracteriza por um conjunto de sinais e sintomas provocados pela deformação
CAPÍTULO 1 1 A DOENÇA DAS CÉLULAS FALCIFORMES Fenótipos, genótipos e haplótipos A doença causada pelas células falciformes se caracteriza por um conjunto de sinais e sintomas provocados pela deformação
CITOLOGIA DA TALASSEMIA ALFA
 CITOLOGIA DA TALASSEMIA ALFA Foto 1: Talassemia Alfa Mínima em sangue periférico corado com azul de crezil brilhante. Comentários: A investigação laboratorial da talassemia alfa mínima se faz por meio
CITOLOGIA DA TALASSEMIA ALFA Foto 1: Talassemia Alfa Mínima em sangue periférico corado com azul de crezil brilhante. Comentários: A investigação laboratorial da talassemia alfa mínima se faz por meio
Este manual tem como objetivo fornecer informações aos pacientes e seus familiares a respeito do Traço Falcêmico
 MANUAL DO PACIENTE - TENHO TRAÇO FALCÊMICO.... E AGORA? EDIÇÃO REVISADA 02/2004 Este manual tem como objetivo fornecer informações aos pacientes e seus familiares a respeito do Traço Falcêmico Sabemos
MANUAL DO PACIENTE - TENHO TRAÇO FALCÊMICO.... E AGORA? EDIÇÃO REVISADA 02/2004 Este manual tem como objetivo fornecer informações aos pacientes e seus familiares a respeito do Traço Falcêmico Sabemos
Diagnóstico de hemoglobinopatias pela triagem neonatal
 1º Congresso Médico de Guarulhos Práticas Clínicas no SUS 5 a 7 novembro de 2015 Diagnóstico de hemoglobinopatias pela triagem neonatal Dra Christiane M. S. Pinto Hematologista Pediatrica HMCA Guarulhos
1º Congresso Médico de Guarulhos Práticas Clínicas no SUS 5 a 7 novembro de 2015 Diagnóstico de hemoglobinopatias pela triagem neonatal Dra Christiane M. S. Pinto Hematologista Pediatrica HMCA Guarulhos
Hemoglobinopatias. Dra. Débora Silva Carmo
 Hemoglobinopatias Dra. Débora Silva Carmo Hemoglobinopatias O que é hemoglobina É a proteína do sangue responsável em carregar o oxigênio para os tecidos Qual é a hemoglobina normal? FA recém-nascido AA
Hemoglobinopatias Dra. Débora Silva Carmo Hemoglobinopatias O que é hemoglobina É a proteína do sangue responsável em carregar o oxigênio para os tecidos Qual é a hemoglobina normal? FA recém-nascido AA
Profa. Dra. Claudia Regina Bonini Domingos Laboratório de Hemoglobinas e Genética das Doenças Hematológicas Departamento de Biologia Instituto de
 Hemoglobinopatias e Talassemias Profa. Dra. Claudia Regina Bonini Domingos Laboratório de Hemoglobinas e Genética das Doenças Hematológicas Departamento de Biologia Instituto de Biociências, Letras e Ciências
Hemoglobinopatias e Talassemias Profa. Dra. Claudia Regina Bonini Domingos Laboratório de Hemoglobinas e Genética das Doenças Hematológicas Departamento de Biologia Instituto de Biociências, Letras e Ciências
ANEMIAS HEMOLÍTICAS. Hye, 2013 www.uff.br/hematolab
 ANEMIAS HEMOLÍTICAS Hye, 2013 www.uff.br/hematolab Anemias Hemolíticas Destruição acelerada de eritrócitos; Podem ser destruídas na medula óssea, no sangue periférico ou pelo baço; drjeffchandler.blogspot.com
ANEMIAS HEMOLÍTICAS Hye, 2013 www.uff.br/hematolab Anemias Hemolíticas Destruição acelerada de eritrócitos; Podem ser destruídas na medula óssea, no sangue periférico ou pelo baço; drjeffchandler.blogspot.com
Doença de Células Falciformes
 Doença de Células Falciformes Pedro P. A. Santos Médico Oncologista - Hematologista Setor de Oncologia e Hematologia Hospital da Criança Conceição Porto Alegre RS Setembro 2015 Doença Falciforme Breve
Doença de Células Falciformes Pedro P. A. Santos Médico Oncologista - Hematologista Setor de Oncologia e Hematologia Hospital da Criança Conceição Porto Alegre RS Setembro 2015 Doença Falciforme Breve
Prevalência de hemoglobinopatias e talassemias em pacientes com anemia na cidade de São Carlos
 Prevalência de hemoglobinopatias e talassemias em pacientes com anemia na cidade de São Carlos Ana Paula Rodrigues RESUMO Com o objetivo de estabelecer a freqüência de hemoglobinas variantes e β-talassemias
Prevalência de hemoglobinopatias e talassemias em pacientes com anemia na cidade de São Carlos Ana Paula Rodrigues RESUMO Com o objetivo de estabelecer a freqüência de hemoglobinas variantes e β-talassemias
ANEMIAS parte IV. Profª Carolina Garrido Zinn
 ANEMIAS parte IV Profª Carolina Garrido Zinn Hemoglobinopatias Doenças hereditárias causadas por diminuição ou anomalia da síntese de globina Afetam cerca de 7% da população mundial Hemoglobina Proteína
ANEMIAS parte IV Profª Carolina Garrido Zinn Hemoglobinopatias Doenças hereditárias causadas por diminuição ou anomalia da síntese de globina Afetam cerca de 7% da população mundial Hemoglobina Proteína
Primeira Lei de Mendel e Heredograma
 Primeira Lei de Mendel e Heredograma 1. (UFC-2006) Leia o texto a seguir. A Doença de Alzheimer (D.A.) (...) é uma afecção neurodegenerativa progressiva e irreversível, que acarreta perda de memória e
Primeira Lei de Mendel e Heredograma 1. (UFC-2006) Leia o texto a seguir. A Doença de Alzheimer (D.A.) (...) é uma afecção neurodegenerativa progressiva e irreversível, que acarreta perda de memória e
Alterações congénitas da formação da hemoglobina:
 ANEMIAS CAUSADAS POR DEFEITOS GENÉTICOS DA HEMOGLOBINA Alterações congénitas da formação da hemoglobina: TALASSEMIAS há uma síntese desequilibrada das cadeias globínicas HEMOGLOBINOPATIAS por alteração
ANEMIAS CAUSADAS POR DEFEITOS GENÉTICOS DA HEMOGLOBINA Alterações congénitas da formação da hemoglobina: TALASSEMIAS há uma síntese desequilibrada das cadeias globínicas HEMOGLOBINOPATIAS por alteração
PAULO CESAR NAOUM AC&T- 2013
 PAULO CESAR NAOUM AC&T- 2013 HEMOGLOBINAS NORMAIS MOLÉCULA DA HEMOGLOBINA HUMANA NORMAL Hb A AS HEMOGLOBINAS HUMANAS SÀO COMPOSTAS POR QUATRO CADEIAS DE AMINOÁCIDOS CONHECIDAS POR GLOBINAS E INSERIDO EM
PAULO CESAR NAOUM AC&T- 2013 HEMOGLOBINAS NORMAIS MOLÉCULA DA HEMOGLOBINA HUMANA NORMAL Hb A AS HEMOGLOBINAS HUMANAS SÀO COMPOSTAS POR QUATRO CADEIAS DE AMINOÁCIDOS CONHECIDAS POR GLOBINAS E INSERIDO EM
CAPÍTULO 12 BIOLOGIA SOCIAL DA DOENÇA FALCIFORME
 CAPÍTULO 12 343 BIOLOGIA SOCIAL DA DOENÇA FALCIFORME INTRODUÇÃO A biologia social agrupa uma série de situações vivenciadas pelo falcêmico no âmbito social que inclui qualidade de vida e relacionamento.
CAPÍTULO 12 343 BIOLOGIA SOCIAL DA DOENÇA FALCIFORME INTRODUÇÃO A biologia social agrupa uma série de situações vivenciadas pelo falcêmico no âmbito social que inclui qualidade de vida e relacionamento.
Informação pode ser o melhor remédio. Hepatite
 Informação pode ser o melhor remédio. Hepatite HEPATITE A hepatite é uma inflamação do fígado provocada na maioria das vezes por um vírus. Diferentes tipos de vírus podem provocar hepatite aguda, que se
Informação pode ser o melhor remédio. Hepatite HEPATITE A hepatite é uma inflamação do fígado provocada na maioria das vezes por um vírus. Diferentes tipos de vírus podem provocar hepatite aguda, que se
Perguntas e respostas sobre imunodeficiências primárias
 Perguntas e respostas sobre imunodeficiências primárias Texto elaborado pelos Drs Pérsio Roxo Júnior e Tatiana Lawrence 1. O que é imunodeficiência? 2. Estas alterações do sistema imunológico são hereditárias?
Perguntas e respostas sobre imunodeficiências primárias Texto elaborado pelos Drs Pérsio Roxo Júnior e Tatiana Lawrence 1. O que é imunodeficiência? 2. Estas alterações do sistema imunológico são hereditárias?
Câncer de Próstata. Fernando Magioni Enfermeiro do Trabalho
 Câncer de Próstata Fernando Magioni Enfermeiro do Trabalho O que é próstata? A próstata é uma glândula que só o homem possui e que se localiza na parte baixa do abdômen. Ela é um órgão muito pequeno, tem
Câncer de Próstata Fernando Magioni Enfermeiro do Trabalho O que é próstata? A próstata é uma glândula que só o homem possui e que se localiza na parte baixa do abdômen. Ela é um órgão muito pequeno, tem
Por outro lado, na avaliação citológica e tecidual, o câncer tem seis fases, conhecidas por fases biológicas do câncer, conforme se segue:
 8 - O câncer também tem fases de desenvolvimento? Sim, o câncer tem fases de desenvolvimento que podem ser avaliadas de diferentes formas. Na avaliação clínica feita por médicos é possível identificar
8 - O câncer também tem fases de desenvolvimento? Sim, o câncer tem fases de desenvolvimento que podem ser avaliadas de diferentes formas. Na avaliação clínica feita por médicos é possível identificar
Ancestralidade Materna polimorfismos matrilínea DNA Mitocondrial (mtdna).
 Ancestralidade Materna A atual população dos países latino-americanos foi gerada por um complexo processo de mistura genética entre ameríndios, europeus e africanos. As porcentagens relativas destas três
Ancestralidade Materna A atual população dos países latino-americanos foi gerada por um complexo processo de mistura genética entre ameríndios, europeus e africanos. As porcentagens relativas destas três
História da Habitação em Florianópolis
 História da Habitação em Florianópolis CARACTERIZAÇÃO DAS FAVELAS EM FLORIANÓPOLIS No início do século XX temos as favelas mais antigas, sendo que as primeiras se instalaram em torno da região central,
História da Habitação em Florianópolis CARACTERIZAÇÃO DAS FAVELAS EM FLORIANÓPOLIS No início do século XX temos as favelas mais antigas, sendo que as primeiras se instalaram em torno da região central,
A IMPRENSA E A QUESTÃO INDÍGENA NO BRASIL
 FACULDADE SETE DE SETEMBRO INICIAÇÃO CIENTÍFICA CURSO DE COMUNICAÇÃO SOCIAL COM HABILITAÇÃO EM PUBLICIDADE E PROPAGANDA ALUNA: NATÁLIA DE ARAGÃO PINTO ORIENTADOR: PROF. DR. TIAGO SEIXAS THEMUDO A IMPRENSA
FACULDADE SETE DE SETEMBRO INICIAÇÃO CIENTÍFICA CURSO DE COMUNICAÇÃO SOCIAL COM HABILITAÇÃO EM PUBLICIDADE E PROPAGANDA ALUNA: NATÁLIA DE ARAGÃO PINTO ORIENTADOR: PROF. DR. TIAGO SEIXAS THEMUDO A IMPRENSA
TALASSEMIAS: UMA ANÁLISE AMPLA E CORRELAÇÕES CLÍNICAS
 TALASSEMIAS: UMA ANÁLISE AMPLA E CORRELAÇÕES CLÍNICAS Antonio Jose Dias Martins, Rassan Dyego Romão Silva e Bruna Rezende Faculdade Alfredo Nasser Aparecida de Goiânia GO Brasil [email protected]
TALASSEMIAS: UMA ANÁLISE AMPLA E CORRELAÇÕES CLÍNICAS Antonio Jose Dias Martins, Rassan Dyego Romão Silva e Bruna Rezende Faculdade Alfredo Nasser Aparecida de Goiânia GO Brasil [email protected]
Lista de Exercícios Herança Sexual
 Meus queridos alunos, preparei para vocês uma lista de atividades abordando o conteúdo estudado por nós esta semana. Espero que vocês aproveitem o final de semana para resolver esses exercícios segundo
Meus queridos alunos, preparei para vocês uma lista de atividades abordando o conteúdo estudado por nós esta semana. Espero que vocês aproveitem o final de semana para resolver esses exercícios segundo
O DNA é formado por pedaços capazes de serem convertidos em algumas características. Esses pedaços são
 Atividade extra Fascículo 2 Biologia Unidade 4 Questão 1 O DNA é formado por pedaços capazes de serem convertidos em algumas características. Esses pedaços são chamados de genes. Assinale abaixo quais
Atividade extra Fascículo 2 Biologia Unidade 4 Questão 1 O DNA é formado por pedaços capazes de serem convertidos em algumas características. Esses pedaços são chamados de genes. Assinale abaixo quais
O que é Hemofilia? O que são os fatores de coagulação? A hemofilia tem cura?
 Volume1 O que é? O que é Hemofilia? Hemofilia é uma alteração hereditária da coagulação do sangue que causa hemorragias e é provocada por uma deficiência na quantidade ou qualidade dos fatores VIII (oito)
Volume1 O que é? O que é Hemofilia? Hemofilia é uma alteração hereditária da coagulação do sangue que causa hemorragias e é provocada por uma deficiência na quantidade ou qualidade dos fatores VIII (oito)
Entendendo a herança genética (capítulo 5) Ana Paula Souto 2012
 Entendendo a herança genética (capítulo 5) Ana Paula Souto 2012 CÂNCER 1) O que é? 2) Como surge? CÂNCER 1) O que é? É o nome dado a um conjunto de mais de 100 doenças que têm em comum o crescimento desordenado
Entendendo a herança genética (capítulo 5) Ana Paula Souto 2012 CÂNCER 1) O que é? 2) Como surge? CÂNCER 1) O que é? É o nome dado a um conjunto de mais de 100 doenças que têm em comum o crescimento desordenado
Rio de Janeiro. Tabela 1: Indicadores selecionados: mediana, 1º e 3º quartis nos municípios do estado do Rio de Janeiro (1991, 2000 e 2010)
 Rio de Janeiro Em, no estado do Rio de Janeiro (RJ), moravam 16 milhões de pessoas, onde 8,9% (1,4 milhões) tinham 65 ou mais anos de idade. O estado era composto de 92 municípios, dos quais sete (7,6%)
Rio de Janeiro Em, no estado do Rio de Janeiro (RJ), moravam 16 milhões de pessoas, onde 8,9% (1,4 milhões) tinham 65 ou mais anos de idade. O estado era composto de 92 municípios, dos quais sete (7,6%)
Azul. Novembro. cosbem. Mergulhe nessa onda! A cor da coragem é azul. Mês de Conscientização, Preveção e Combate ao Câncer De Próstata.
 cosbem COORDENAÇÃO DE SAÚDE E BEM-ESTAR Novembro Azul Mês de Conscientização, Preveção e Combate ao Câncer De Próstata. Mergulhe nessa onda! A cor da coragem é azul. NOVEMBRO AZUL Mês de Conscientização,
cosbem COORDENAÇÃO DE SAÚDE E BEM-ESTAR Novembro Azul Mês de Conscientização, Preveção e Combate ao Câncer De Próstata. Mergulhe nessa onda! A cor da coragem é azul. NOVEMBRO AZUL Mês de Conscientização,
Papilomavírus Humano HPV
 Papilomavírus Humano HPV -BIOLOGIA- Alunos: André Aroeira, Antonio Lopes, Carlos Eduardo Rozário, João Marcos Fagundes, João Paulo Sobral e Hélio Gastão Prof.: Fragoso 1º Ano E.M. T. 13 Agente Causador
Papilomavírus Humano HPV -BIOLOGIA- Alunos: André Aroeira, Antonio Lopes, Carlos Eduardo Rozário, João Marcos Fagundes, João Paulo Sobral e Hélio Gastão Prof.: Fragoso 1º Ano E.M. T. 13 Agente Causador
Ensino Médio 2º ano classe: Prof. Gustavo Nome: nº. Lista de Exercícios 1ª Lei de Mendel, exceções e Sistema ABO e Rh
 . Ensino Médio 2º ano classe: Prof. Gustavo Nome: nº Lista de Exercícios 1ª Lei de Mendel, exceções e Sistema ABO e Rh. 1- Em um experimento, preparou-se um conjunto de plantas por técnica de clonagem
. Ensino Médio 2º ano classe: Prof. Gustavo Nome: nº Lista de Exercícios 1ª Lei de Mendel, exceções e Sistema ABO e Rh. 1- Em um experimento, preparou-se um conjunto de plantas por técnica de clonagem
INSTITUIÇÃO: CENTRO UNIVERSITÁRIO DAS FACULDADES METROPOLITANAS UNIDAS
 TÍTULO: MÉTODOS DE DIAGNÓSTICO LABORATORIAL DA ANEMIA FALCIFORME CATEGORIA: CONCLUÍDO ÁREA: CIÊNCIAS BIOLÓGICAS E SAÚDE SUBÁREA: BIOMEDICINA INSTITUIÇÃO: CENTRO UNIVERSITÁRIO DAS FACULDADES METROPOLITANAS
TÍTULO: MÉTODOS DE DIAGNÓSTICO LABORATORIAL DA ANEMIA FALCIFORME CATEGORIA: CONCLUÍDO ÁREA: CIÊNCIAS BIOLÓGICAS E SAÚDE SUBÁREA: BIOMEDICINA INSTITUIÇÃO: CENTRO UNIVERSITÁRIO DAS FACULDADES METROPOLITANAS
Brasil é 2º em ranking de redução de mortalidade infantil 3
 Publicação Científica do Curso de Bacharelado em Enfermagem do CEUT. Ano 2011(3). Edição 38 Aline da Silva Oliveira 1 Cristiana Maria de Sousa Macedo 1 Mércia da Silva Sousa 1 Márcia Andrea Lial Sertão
Publicação Científica do Curso de Bacharelado em Enfermagem do CEUT. Ano 2011(3). Edição 38 Aline da Silva Oliveira 1 Cristiana Maria de Sousa Macedo 1 Mércia da Silva Sousa 1 Márcia Andrea Lial Sertão
Desigualdades em saúde - Mortalidade infantil. Palavras-chave: mortalidade infantil; qualidade de vida; desigualdade.
 Desigualdades em saúde - Mortalidade infantil Ruth Rangel * Fernanda Azevedo * Palavras-chave: mortalidade infantil; qualidade de vida; desigualdade. Resumo A redução das desigualdades sociais tem sido
Desigualdades em saúde - Mortalidade infantil Ruth Rangel * Fernanda Azevedo * Palavras-chave: mortalidade infantil; qualidade de vida; desigualdade. Resumo A redução das desigualdades sociais tem sido
CASUÍSTICA DE HEMOGLOBINOPATIAS NA POPULAÇÃO DO HFF
 CASUÍSTICA DE HEMOGLOBINOPATIAS NA POPULAÇÃO DO HFF Serviço Patologia Clínica 21 de Maio 2015 Elzara Aliyeva Sónia Faria OBJECTIVO Efectuar um estudo casuístico das hemoglobinopatias na população da área
CASUÍSTICA DE HEMOGLOBINOPATIAS NA POPULAÇÃO DO HFF Serviço Patologia Clínica 21 de Maio 2015 Elzara Aliyeva Sónia Faria OBJECTIVO Efectuar um estudo casuístico das hemoglobinopatias na população da área
Protocolo. Transplante de células-tronco hematopoiéticas nas hemoglobinopatias
 Protocolo Transplante de células-tronco hematopoiéticas nas hemoglobinopatias Versão eletrônica atualizada em Abril 2012 Embora a sobrevida dos pacientes com talassemia major e anemia falciforme (AF) tenha
Protocolo Transplante de células-tronco hematopoiéticas nas hemoglobinopatias Versão eletrônica atualizada em Abril 2012 Embora a sobrevida dos pacientes com talassemia major e anemia falciforme (AF) tenha
Mutações. Escola Secundária Quinta do Marquês. Disciplina: Biologia e Geologia Professor: António Gonçalves Ano letivo: 2013/2014
 Escola Secundária Quinta do Marquês Mutações Disciplina: Biologia e Geologia Professor: António Gonçalves Ano letivo: 2013/2014 Trabalho realizado por: Bárbara Dória, nº4, 11ºB Definição de mutação As
Escola Secundária Quinta do Marquês Mutações Disciplina: Biologia e Geologia Professor: António Gonçalves Ano letivo: 2013/2014 Trabalho realizado por: Bárbara Dória, nº4, 11ºB Definição de mutação As
GENÉTICA DE POPULAÇÕES:
 Genética Animal Fatores Evolutivos 1 GENÉTICA DE POPULAÇÕES: A genética de populações lida com populações naturais. Estas consistem em todos os indivíduos que, ao se reproduzir uns com os outros, compartilham
Genética Animal Fatores Evolutivos 1 GENÉTICA DE POPULAÇÕES: A genética de populações lida com populações naturais. Estas consistem em todos os indivíduos que, ao se reproduzir uns com os outros, compartilham
AMH Hemolíticas ANEMIAS HEMOLÍTICAS
 HEMATOLOGIA II Curso de Farmácia 8 º período AMH Hemolíticas ANEMIAS HEMOLÍTICAS Anemias causadas por um aumento da destruição dos eritrócitos em relação à produção. Rompe-se o equilíbrio entre a produção
HEMATOLOGIA II Curso de Farmácia 8 º período AMH Hemolíticas ANEMIAS HEMOLÍTICAS Anemias causadas por um aumento da destruição dos eritrócitos em relação à produção. Rompe-se o equilíbrio entre a produção
PNAD - Segurança Alimentar 2004 2009. Insegurança alimentar diminui, mas ainda atinge 30,2% dos domicílios brasileiros
 1 of 5 11/26/2010 2:57 PM Comunicação Social 26 de novembro de 2010 PNAD - Segurança Alimentar 2004 2009 Insegurança alimentar diminui, mas ainda atinge 30,2% dos domicílios brasileiros O número de domicílios
1 of 5 11/26/2010 2:57 PM Comunicação Social 26 de novembro de 2010 PNAD - Segurança Alimentar 2004 2009 Insegurança alimentar diminui, mas ainda atinge 30,2% dos domicílios brasileiros O número de domicílios
Analfabetismo no Brasil
 Analfabetismo no Brasil Ricardo Paes de Barros (IPEA) Mirela de Carvalho (IETS) Samuel Franco (IETS) Parte 1: Magnitude e evolução do analfabetismo no Brasil Magnitude Segundo estimativas obtidas com base
Analfabetismo no Brasil Ricardo Paes de Barros (IPEA) Mirela de Carvalho (IETS) Samuel Franco (IETS) Parte 1: Magnitude e evolução do analfabetismo no Brasil Magnitude Segundo estimativas obtidas com base
Maconha. Alessandro Alves. Conhecendo a planta
 Maconha Alessandro Alves Entenda bem. A maconha é a droga ilícita mais utilizada no mundo. Está entre as plantas mais antigas cultivadas pelo homem. Na China seus grãos são utilizados como alimento e no
Maconha Alessandro Alves Entenda bem. A maconha é a droga ilícita mais utilizada no mundo. Está entre as plantas mais antigas cultivadas pelo homem. Na China seus grãos são utilizados como alimento e no
A situação do câncer no Brasil 1
 A situação do câncer no Brasil 1 Fisiopatologia do câncer 23 Introdução O câncer é responsável por cerca de 13% de todas as causas de óbito no mundo: mais de 7 milhões de pessoas morrem anualmente da
A situação do câncer no Brasil 1 Fisiopatologia do câncer 23 Introdução O câncer é responsável por cerca de 13% de todas as causas de óbito no mundo: mais de 7 milhões de pessoas morrem anualmente da
TRÁFICO HUMANO E AS MIGRAÇÕES INTERNACIONAIS
 TRÁFICO HUMANO E AS MIGRAÇÕES INTERNACIONAIS MOVIMENTOS MIGRATÓRIOS INTERNACIONAIS 1. RAZÕES DAS MIGRAÇÕES FATORES ATRATIVOS X FATORES REPULSIVOS - CONDIÇÕES DE VIDA - OFERTAS DE EMPREGO - SEGURANÇA -
TRÁFICO HUMANO E AS MIGRAÇÕES INTERNACIONAIS MOVIMENTOS MIGRATÓRIOS INTERNACIONAIS 1. RAZÕES DAS MIGRAÇÕES FATORES ATRATIVOS X FATORES REPULSIVOS - CONDIÇÕES DE VIDA - OFERTAS DE EMPREGO - SEGURANÇA -
Você conhece a Medicina de Família e Comunidade?
 Texto divulgado na forma de um caderno, editorado, para a comunidade, profissionais de saúde e mídia SBMFC - 2006 Você conhece a Medicina de Família e Comunidade? Não? Então, convidamos você a conhecer
Texto divulgado na forma de um caderno, editorado, para a comunidade, profissionais de saúde e mídia SBMFC - 2006 Você conhece a Medicina de Família e Comunidade? Não? Então, convidamos você a conhecer
Homeopatia. Copyrights - Movimento Nacional de Valorização e Divulgação da Homeopatia [email protected] 2
 Homeopatia A Homeopatia é um sistema terapêutico baseado no princípio dos semelhantes (princípio parecido com o das vacinas) que cuida e trata de vários tipos de organismos (homem, animais e plantas) usando
Homeopatia A Homeopatia é um sistema terapêutico baseado no princípio dos semelhantes (princípio parecido com o das vacinas) que cuida e trata de vários tipos de organismos (homem, animais e plantas) usando
Também conhecido como densidade populacional ou população relativa. É a medida expressa pela relação entre a população e a superfície do território.
 Também conhecido como densidade populacional ou população relativa. É a medida expressa pela relação entre a população e a superfície do território. É geralmente expressa em habitantes por quilômetro quadrado
Também conhecido como densidade populacional ou população relativa. É a medida expressa pela relação entre a população e a superfície do território. É geralmente expressa em habitantes por quilômetro quadrado
HEMOGRAMA ANEMIA FERROPRIVA. Hemoglobina. PDF created with pdffactory Pro trial version www.pdffactory.com. Ferro
 HEMOGRAMA Profª. Francis Fregonesi Brinholi [email protected]. Hb = 0,8 g/dl Microcítica VCM < 78fL VCM:? Dosagem de ferritina Baixa Normal Alta Microcítica VCM < 78fL Normocítica VCM: 78-98fL Macrocítica
HEMOGRAMA Profª. Francis Fregonesi Brinholi [email protected]. Hb = 0,8 g/dl Microcítica VCM < 78fL VCM:? Dosagem de ferritina Baixa Normal Alta Microcítica VCM < 78fL Normocítica VCM: 78-98fL Macrocítica
Saúde. reprodutiva: gravidez, assistência. pré-natal, parto. e baixo peso. ao nascer
 2 Saúde reprodutiva: gravidez, assistência pré-natal, parto e baixo peso ao nascer SAÚDE BRASIL 2004 UMA ANÁLISE DA SITUAÇÃO DE SAÚDE INTRODUÇÃO No Brasil, as questões relativas à saúde reprodutiva têm
2 Saúde reprodutiva: gravidez, assistência pré-natal, parto e baixo peso ao nascer SAÚDE BRASIL 2004 UMA ANÁLISE DA SITUAÇÃO DE SAÚDE INTRODUÇÃO No Brasil, as questões relativas à saúde reprodutiva têm
ATIVIDADE DE RECUPERAÇÃO PARALELA PREVENTIVA 3º Trimestre/2014 GABARITO
 NOME: ANO: 2º EM Nº: PROF.(A): Claudia Lobo DATA: ATIVIDADE DE RECUPERAÇÃO PARALELA PREVENTIVA 3º Trimestre/2014 GABARITO 1. A fenilcetonúria é uma doença que tem herança autossômica recessiva. Considere
NOME: ANO: 2º EM Nº: PROF.(A): Claudia Lobo DATA: ATIVIDADE DE RECUPERAÇÃO PARALELA PREVENTIVA 3º Trimestre/2014 GABARITO 1. A fenilcetonúria é uma doença que tem herança autossômica recessiva. Considere
Santa Catarina. Tabela 1: Indicadores selecionados: mediana, 1º e 3º quartis nos municípios do estado de Santa Catarina (1991, 2000 e 2010)
 Santa Catarina Em 21, no estado de Santa Catarina (SC), moravam 6,3 milhões de pessoas, onde parcela relevante (6,9%, 43,7 mil) tinha 65 ou mais anos de idade. O estado era composto de 293 municípios,
Santa Catarina Em 21, no estado de Santa Catarina (SC), moravam 6,3 milhões de pessoas, onde parcela relevante (6,9%, 43,7 mil) tinha 65 ou mais anos de idade. O estado era composto de 293 municípios,
Biologia. Sistema circulatório
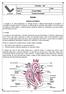 Aluno (a): Série: 3ª Turma: TUTORIAL 10R Ensino Médio Equipe de Biologia Data: Biologia Sistema circulatório O coração e os vasos sanguíneos e o sangue formam o sistema cardiovascular ou circulatório.
Aluno (a): Série: 3ª Turma: TUTORIAL 10R Ensino Médio Equipe de Biologia Data: Biologia Sistema circulatório O coração e os vasos sanguíneos e o sangue formam o sistema cardiovascular ou circulatório.
Doença de Alzheimer: uma visão epidemiológica quanto ao processo de saúde-doença.
 Doença de Alzheimer: uma visão epidemiológica quanto ao processo de saúde-doença. Bruno Araújo da Silva Dantas¹ [email protected] Luciane Alves Lopes² [email protected] ¹ ²Acadêmico(a) do
Doença de Alzheimer: uma visão epidemiológica quanto ao processo de saúde-doença. Bruno Araújo da Silva Dantas¹ [email protected] Luciane Alves Lopes² [email protected] ¹ ²Acadêmico(a) do
O que é câncer de mama?
 Câncer de Mama O que é câncer de mama? O câncer de mama é a doença em que as células normais da mama começam a se modificar, multiplicando-se sem controle e deixando de morrer, formando uma massa de células
Câncer de Mama O que é câncer de mama? O câncer de mama é a doença em que as células normais da mama começam a se modificar, multiplicando-se sem controle e deixando de morrer, formando uma massa de células
OUTUBRO. um mes PARA RELEMBRAR A IMPORTANCIA DA. prevencao. COMPARTILHE ESSA IDEIA.
 OUTUBRO ROSA ^ um mes PARA RELEMBRAR A IMPORTANCIA DA ~ prevencao. COMPARTILHE ESSA IDEIA. ~ ^ O movimento popular internacionalmente conhecido como Outubro Rosa é comemorado em todo o mundo. O nome remete
OUTUBRO ROSA ^ um mes PARA RELEMBRAR A IMPORTANCIA DA ~ prevencao. COMPARTILHE ESSA IDEIA. ~ ^ O movimento popular internacionalmente conhecido como Outubro Rosa é comemorado em todo o mundo. O nome remete
As bactérias operárias
 A U A UL LA As bactérias operárias Na Aula 47 você viu a importância da insulina no nosso corpo e, na Aula 48, aprendeu como as células de nosso organismo produzem insulina e outras proteínas. As pessoas
A U A UL LA As bactérias operárias Na Aula 47 você viu a importância da insulina no nosso corpo e, na Aula 48, aprendeu como as células de nosso organismo produzem insulina e outras proteínas. As pessoas
Portuguese Summary. Resumo
 Portuguese Summary Resumo 176 Resumo Cerca de 1 em 100 indivíduos não podem comer pão, macarrão ou biscoitos, pois eles têm uma condição chamada de doença celíaca (DC). DC é causada por uma das intolerâncias
Portuguese Summary Resumo 176 Resumo Cerca de 1 em 100 indivíduos não podem comer pão, macarrão ou biscoitos, pois eles têm uma condição chamada de doença celíaca (DC). DC é causada por uma das intolerâncias
Entendendo a herança genética. Capítulo 5 CSA 2015
 Entendendo a herança genética Capítulo 5 CSA 2015 Como explicar as semelhanças entre gerações diferentes? Pai e filha Avó e neta Pai e filho Avó, mãe e filha Histórico Acreditava na produção, por todas
Entendendo a herança genética Capítulo 5 CSA 2015 Como explicar as semelhanças entre gerações diferentes? Pai e filha Avó e neta Pai e filho Avó, mãe e filha Histórico Acreditava na produção, por todas
Saiba quais são os diferentes tipos de diabetes
 Saiba quais são os diferentes tipos de diabetes Diabetes é uma doença ocasionada pela total falta de produção de insulina pelo pâncreas ou pela quantidade insuficiente da substância no corpo. A insulina
Saiba quais são os diferentes tipos de diabetes Diabetes é uma doença ocasionada pela total falta de produção de insulina pelo pâncreas ou pela quantidade insuficiente da substância no corpo. A insulina
Aula 14 Sistema ABO. Grupo sangüíneo (fenótipo) Aglutinogênio (hemácias) Aglutinina (soro) Anti - B. Anti - A. A e B.
 Aula 14 Sistema ABO A transfusão de sangue incompatível pode provocar queda de pressão, escurecimento da visão, desmaio e até a morte. Esses efeitos são devidos a uma reação de aglutinação, ou seja reunião
Aula 14 Sistema ABO A transfusão de sangue incompatível pode provocar queda de pressão, escurecimento da visão, desmaio e até a morte. Esses efeitos são devidos a uma reação de aglutinação, ou seja reunião
Parte 1 Formação geológica
 AULA 1 CONTINENTES Parte 1 Formação geológica O Planeta Terra é formado por seis continentes: África, América, Antártica, Ásia, Europa e Oceania. A Terra apresenta 149.440.850 quilômetros quadrados de
AULA 1 CONTINENTES Parte 1 Formação geológica O Planeta Terra é formado por seis continentes: África, América, Antártica, Ásia, Europa e Oceania. A Terra apresenta 149.440.850 quilômetros quadrados de
7ºano 2º período vespertino 25 de abril de 2014
 GEOGRAFIA QUESTÃO 1 A Demografia é a ciência que estuda as características das populações humanas e exprime-se geralmente através de valores estatísticos. As características da população estudadas pela
GEOGRAFIA QUESTÃO 1 A Demografia é a ciência que estuda as características das populações humanas e exprime-se geralmente através de valores estatísticos. As características da população estudadas pela
Pisa 2012: O que os dados dizem sobre o Brasil
 Pisa 2012: O que os dados dizem sobre o Brasil A OCDE (Organização para Cooperação e Desenvolvimento Econômico) divulgou nesta terça-feira os resultados do Programa Internacional de Avaliação de Alunos,
Pisa 2012: O que os dados dizem sobre o Brasil A OCDE (Organização para Cooperação e Desenvolvimento Econômico) divulgou nesta terça-feira os resultados do Programa Internacional de Avaliação de Alunos,
Biologia - Grupos A e B - Gabarito revisto
 revisto 1 a QUESTÃO: (2, pontos) Avaliador Revisor Em estudos com um vegetal terrestre foram utilizadas plantas jovens com genótipo mutante (M), que não apresentam a formação de uma estrutura presente
revisto 1 a QUESTÃO: (2, pontos) Avaliador Revisor Em estudos com um vegetal terrestre foram utilizadas plantas jovens com genótipo mutante (M), que não apresentam a formação de uma estrutura presente
Dinâmica demográfica e qualidade de vida da população brasileira Parte II
 Dinâmica demográfica e qualidade de vida da população brasileira Parte II A nova Pirâmide Etária do Brasil; Crescimento horizontal devido às migrações; É um tipo de gráfico que representa os dados sobre
Dinâmica demográfica e qualidade de vida da população brasileira Parte II A nova Pirâmide Etária do Brasil; Crescimento horizontal devido às migrações; É um tipo de gráfico que representa os dados sobre
O Sr. CELSO RUSSOMANNO (PP-SP) pronuncia o. seguinte discurso: Senhor Presidente, Senhoras e Senhores
 O Sr. CELSO RUSSOMANNO (PP-SP) pronuncia o seguinte discurso: Senhor Presidente, Senhoras e Senhores Deputados, transcorreram já mais de duas décadas desde que a Síndrome da Imunodeficiência Adquirida
O Sr. CELSO RUSSOMANNO (PP-SP) pronuncia o seguinte discurso: Senhor Presidente, Senhoras e Senhores Deputados, transcorreram já mais de duas décadas desde que a Síndrome da Imunodeficiência Adquirida
Lei da Segregação. Experimentos de Mendel
 Lei da Segregação Os trabalhos do monge Agostinho Gregor Mendel, realizados há mais de um século, estabeleceram os princípios básicos da herança, que, até hoje, são aplicados nos estudos da Genética. A
Lei da Segregação Os trabalhos do monge Agostinho Gregor Mendel, realizados há mais de um século, estabeleceram os princípios básicos da herança, que, até hoje, são aplicados nos estudos da Genética. A
Glaucoma. O que é glaucoma? Como acontece?
 Glaucoma O que é glaucoma? Glaucoma é uma doença crônica do olho (que dura toda a vida), que ocorre quando há elevação da pressão intra-ocular (PIO), que provoca lesões no nervo ótico e, como conseqüência,
Glaucoma O que é glaucoma? Glaucoma é uma doença crônica do olho (que dura toda a vida), que ocorre quando há elevação da pressão intra-ocular (PIO), que provoca lesões no nervo ótico e, como conseqüência,
A criança com anemia falciforme e a assistência de enfermagem à criança e sua família. DrªTania Vignuda de Souza Prof. Adjunto do DEMI/EEAN/UFRJ
 A criança com anemia falciforme e a assistência de enfermagem à criança e sua família. DrªTania Vignuda de Souza Prof. Adjunto do DEMI/EEAN/UFRJ Considerações iniciais Grupo das hemoglobinopatias Doença
A criança com anemia falciforme e a assistência de enfermagem à criança e sua família. DrªTania Vignuda de Souza Prof. Adjunto do DEMI/EEAN/UFRJ Considerações iniciais Grupo das hemoglobinopatias Doença
CLINICA MÉDICA HEMATOLOGIA 2003-2004 SANGUE
 1 CLINICA MÉDICA HEMATOLOGIA 2003-2004 2 SANGUE 3 4 5 6 7 PATOLOGIA DO GLÓBULO RUBRO ANEMIAS POLICITEMIAS Valores de referência Hemoglobina g/dl recém-nascido
1 CLINICA MÉDICA HEMATOLOGIA 2003-2004 2 SANGUE 3 4 5 6 7 PATOLOGIA DO GLÓBULO RUBRO ANEMIAS POLICITEMIAS Valores de referência Hemoglobina g/dl recém-nascido
Sumário Executivo. Amanda Reis. Luiz Augusto Carneiro Superintendente Executivo
 Comparativo entre o rendimento médio dos beneficiários de planos de saúde individuais e da população não coberta por planos de saúde regional e por faixa etária Amanda Reis Luiz Augusto Carneiro Superintendente
Comparativo entre o rendimento médio dos beneficiários de planos de saúde individuais e da população não coberta por planos de saúde regional e por faixa etária Amanda Reis Luiz Augusto Carneiro Superintendente
Rio Grande do Sul. Tabela 1: Indicadores selecionados: mediana, 1º e 3º quartis nos municípios do estado do Rio Grande do Sul (1991, 2000 e 2010)
 Rio Grande do Sul Em 21, no estado do Rio Grande do Sul (RS), moravam 1,7 milhões de pessoas, onde parcela importante (9,3%, 989,9 mil) tinha 65 ou mais anos de idade. O estado era composto de 496 municípios,
Rio Grande do Sul Em 21, no estado do Rio Grande do Sul (RS), moravam 1,7 milhões de pessoas, onde parcela importante (9,3%, 989,9 mil) tinha 65 ou mais anos de idade. O estado era composto de 496 municípios,
Hoje estudaremos a bioquímica dos ácidos nucléicos. Acompanhe!
 Aula: 2 Temática: Ácidos Nucléicos Hoje estudaremos a bioquímica dos ácidos nucléicos. Acompanhe! Introdução: Os ácidos nucléicos são as moléculas com a função de armazenamento e expressão da informação
Aula: 2 Temática: Ácidos Nucléicos Hoje estudaremos a bioquímica dos ácidos nucléicos. Acompanhe! Introdução: Os ácidos nucléicos são as moléculas com a função de armazenamento e expressão da informação
MISSÃO Ser uma instituição de excelência técnico-científica em hemoterapia e hematologia com elevado padrão ético e compromisso com a população.
 ESTA PALESTRA NÃO PODERÁ SER REPRODUZIDA SEM A REFERÊNCIA DO AUTOR. Política Nacional de Atenção Integral à pessoa com Doença Falciforme ADRIANA TORRES SÁ ENFERMEIRA HEMOCE CRATO DOENÇA FALCIFORME DOENÇA
ESTA PALESTRA NÃO PODERÁ SER REPRODUZIDA SEM A REFERÊNCIA DO AUTOR. Política Nacional de Atenção Integral à pessoa com Doença Falciforme ADRIANA TORRES SÁ ENFERMEIRA HEMOCE CRATO DOENÇA FALCIFORME DOENÇA
Programa de Pós-Graduação em Comunicação e Cultura Contemporâneas. Grupo de Pesquisa em Interação, Tecnologias Digitais e Sociedade - GITS
 Universidade Federal da Bahia Programa de Pós-Graduação em Comunicação e Cultura Contemporâneas Grupo de Pesquisa em Interação, Tecnologias Digitais e Sociedade - GITS Reunião de 18 de junho de 2010 Resumo
Universidade Federal da Bahia Programa de Pós-Graduação em Comunicação e Cultura Contemporâneas Grupo de Pesquisa em Interação, Tecnologias Digitais e Sociedade - GITS Reunião de 18 de junho de 2010 Resumo
SAÍDA DO MERCADO DE TRABALHO: QUAL É A IDADE?
 SAÍDA DO MERCADO DE TRABALHO: QUAL É A IDADE? Ana Amélia Camarano* Solange Kanso** Daniele Fernandes** 1 INTRODUÇÃO Assume-se que idade avançada e invalidez resultam em perda da capacidade laboral, o que
SAÍDA DO MERCADO DE TRABALHO: QUAL É A IDADE? Ana Amélia Camarano* Solange Kanso** Daniele Fernandes** 1 INTRODUÇÃO Assume-se que idade avançada e invalidez resultam em perda da capacidade laboral, o que
Colégio Senhora de Fátima
 Colégio Senhora de Fátima A formação do território brasileiro 7 ano Professora: Jenifer Geografia A formação do território brasileiro As imagens a seguir tem como principal objetivo levar a refletir sobre
Colégio Senhora de Fátima A formação do território brasileiro 7 ano Professora: Jenifer Geografia A formação do território brasileiro As imagens a seguir tem como principal objetivo levar a refletir sobre
Alelos múltiplos na determinação de um caráter
 Alelos múltiplos na determinação de um caráter Determinados gene pode sofrer ao longo do tempo diversas mutações e originar vários alelos esse fenômeno é chamado de polialelia. São bastante frequentes
Alelos múltiplos na determinação de um caráter Determinados gene pode sofrer ao longo do tempo diversas mutações e originar vários alelos esse fenômeno é chamado de polialelia. São bastante frequentes
Paraná. Tabela 1: Indicadores selecionados: mediana, 1º e 3º quartis nos municípios do estado do Paraná (1991, 2000 e 2010)
 Paraná Em, no estado do Paraná (PR), moravam 1,4 milhões de pessoas, onde uma parcela considerável (7,5%, 786,6 mil) tinha 65 ou mais anos de idade. O estado era composto de 399 municípios, dos quais 23
Paraná Em, no estado do Paraná (PR), moravam 1,4 milhões de pessoas, onde uma parcela considerável (7,5%, 786,6 mil) tinha 65 ou mais anos de idade. O estado era composto de 399 municípios, dos quais 23
Abordagem da reestenosee. Renato Sanchez Antonio
 Abordagem da reestenosee oclusões crônicas coronárias Renato Sanchez Antonio Estudos iniciais de seguimento clínico de pacientes com angina estável demonstraram que o percentual de mortalidade aumentou
Abordagem da reestenosee oclusões crônicas coronárias Renato Sanchez Antonio Estudos iniciais de seguimento clínico de pacientes com angina estável demonstraram que o percentual de mortalidade aumentou
Entendendo a herança genética (capítulo 5) Ana Paula Souto 2012
 Entendendo a herança genética (capítulo 5) Ana Paula Souto 2012 CÂNCER 1) O que é? 2) Como surge? CÂNCER 1) O que é? É o nome dado a um conjunto de mais de 100 doenças que têm em comum o crescimento desordenado
Entendendo a herança genética (capítulo 5) Ana Paula Souto 2012 CÂNCER 1) O que é? 2) Como surge? CÂNCER 1) O que é? É o nome dado a um conjunto de mais de 100 doenças que têm em comum o crescimento desordenado
CARACTERÍSTICAS SOCIODEMOGRÁFICAS DE IDOSAS. UM OLHAR PARA VIÇOSA, MINAS GERAIS, BRASIL
 CARACTERÍSTICAS SOCIODEMOGRÁFICAS DE IDOSAS. UM OLHAR PARA VIÇOSA, MINAS GERAIS, BRASIL Nubia C. Freitas - UFV [email protected] Estela S. Fonseca UFV [email protected] Alessandra V. Almeida UFV
CARACTERÍSTICAS SOCIODEMOGRÁFICAS DE IDOSAS. UM OLHAR PARA VIÇOSA, MINAS GERAIS, BRASIL Nubia C. Freitas - UFV [email protected] Estela S. Fonseca UFV [email protected] Alessandra V. Almeida UFV
Protocolo em Rampa Manual de Referência Rápida
 Protocolo em Rampa Manual de Referência Rápida 1 O que é o Protocolo em Rampa O protocolo em rampa é um protocolo para testes de esforço que não possui estágios. Nele o incremento da carga se dá de maneira
Protocolo em Rampa Manual de Referência Rápida 1 O que é o Protocolo em Rampa O protocolo em rampa é um protocolo para testes de esforço que não possui estágios. Nele o incremento da carga se dá de maneira
CAMPANHA PELA INCLUSÃO DA ANÁLISE MOLECULAR DO GENE RET EM PACIENTES COM CARCINOMA MEDULAR E SEUS FAMILIARES PELO SUS.
 Laura S. W ard CAMPANHA PELA INCLUSÃO DA ANÁLISE MOLECULAR DO GENE RET EM PACIENTES COM CARCINOMA MEDULAR E SEUS FAMILIARES PELO SUS. Nódulos da Tiróide e o Carcinoma Medular Nódulos da tiróide são um
Laura S. W ard CAMPANHA PELA INCLUSÃO DA ANÁLISE MOLECULAR DO GENE RET EM PACIENTES COM CARCINOMA MEDULAR E SEUS FAMILIARES PELO SUS. Nódulos da Tiróide e o Carcinoma Medular Nódulos da tiróide são um
EPIDEMIOLOGIA. CONCEITOS EPIDÊMICOS Professor Esp. André Luís Souza Stella
 EPIDEMIOLOGIA CONCEITOS EPIDÊMICOS Professor Esp. André Luís Souza Stella CONCEITOS EPIDÊMICOS - ENDEMIA ENDEMIA: É uma doença localizada em um espaço limitado denominado faixa endêmica. Isso quer dizer
EPIDEMIOLOGIA CONCEITOS EPIDÊMICOS Professor Esp. André Luís Souza Stella CONCEITOS EPIDÊMICOS - ENDEMIA ENDEMIA: É uma doença localizada em um espaço limitado denominado faixa endêmica. Isso quer dizer
AS TEORIAS MOTIVACIONAIS DE MASLOW E HERZBERG
 AS TEORIAS MOTIVACIONAIS DE MASLOW E HERZBERG 1. Introdução 2. Maslow e a Hierarquia das necessidades 3. Teoria dos dois Fatores de Herzberg 1. Introdução Sabemos que considerar as atitudes e valores dos
AS TEORIAS MOTIVACIONAIS DE MASLOW E HERZBERG 1. Introdução 2. Maslow e a Hierarquia das necessidades 3. Teoria dos dois Fatores de Herzberg 1. Introdução Sabemos que considerar as atitudes e valores dos
Especificidades das mortes violentas no Brasil e suas lições. Maria Cecília de Souza Minayo
 Especificidades das mortes violentas no Brasil e suas lições Maria Cecília de Souza Minayo 1ª. característica: elevadas e crescentes taxas de homicídios nos últimos 25 anos Persistência das causas externas
Especificidades das mortes violentas no Brasil e suas lições Maria Cecília de Souza Minayo 1ª. característica: elevadas e crescentes taxas de homicídios nos últimos 25 anos Persistência das causas externas
3 Classificação. 3.1. Resumo do algoritmo proposto
 3 Classificação Este capítulo apresenta primeiramente o algoritmo proposto para a classificação de áudio codificado em MPEG-1 Layer 2 em detalhes. Em seguida, são analisadas as inovações apresentadas.
3 Classificação Este capítulo apresenta primeiramente o algoritmo proposto para a classificação de áudio codificado em MPEG-1 Layer 2 em detalhes. Em seguida, são analisadas as inovações apresentadas.
[PARVOVIROSE CANINA]
![[PARVOVIROSE CANINA] [PARVOVIROSE CANINA]](/thumbs/27/11911534.jpg) [PARVOVIROSE CANINA] 2 Parvovirose Canina A Parvovirose é uma doença infecto-contagiosa causada por um vírus da família Parvoviridae. Acomete mais comumente animais jovens, geralmente com menos de 1 ano
[PARVOVIROSE CANINA] 2 Parvovirose Canina A Parvovirose é uma doença infecto-contagiosa causada por um vírus da família Parvoviridae. Acomete mais comumente animais jovens, geralmente com menos de 1 ano
A importância do continente europeu reside no fato de este ter
 Conhecido como velho mundo, o continente europeu limitase a oeste com o Oceano Atlântico, ao sul com o Mediterrâneo, ao norte com o oceano Glacial Ártico e a leste com a Ásia, sendo que os Montes Urais
Conhecido como velho mundo, o continente europeu limitase a oeste com o Oceano Atlântico, ao sul com o Mediterrâneo, ao norte com o oceano Glacial Ártico e a leste com a Ásia, sendo que os Montes Urais
Equipe: Ronaldo Laranjeira Helena Sakiyama Maria de Fátima Rato Padin Sandro Mitsuhiro Clarice Sandi Madruga
 Equipe: Ronaldo Laranjeira Helena Sakiyama Maria de Fátima Rato Padin Sandro Mitsuhiro Clarice Sandi Madruga 1. Por que este estudo é relevante? Segundo o relatório sobre a Carga Global das Doenças (Global
Equipe: Ronaldo Laranjeira Helena Sakiyama Maria de Fátima Rato Padin Sandro Mitsuhiro Clarice Sandi Madruga 1. Por que este estudo é relevante? Segundo o relatório sobre a Carga Global das Doenças (Global
MOBILIDADE DOS EMPREENDEDORES E VARIAÇÕES NOS RENDIMENTOS
 MOBILIDADE DOS EMPREENDEDORES NOTA CONJUNTURAL ABRIL DE 2014 Nº31 E VARIAÇÕES NOS RENDIMENTOS NOTA CONJUNTURAL ABRIL DE 2014 Nº31 PANORAMA GERAL Os movimentos de transição da população ocupada entre as
MOBILIDADE DOS EMPREENDEDORES NOTA CONJUNTURAL ABRIL DE 2014 Nº31 E VARIAÇÕES NOS RENDIMENTOS NOTA CONJUNTURAL ABRIL DE 2014 Nº31 PANORAMA GERAL Os movimentos de transição da população ocupada entre as
O albinismo é uma doença metabólica hereditária, resultado de disfunção gênica na produção de melanina. Para que a doença se manifeste é necessário
 O albinismo é uma doença metabólica hereditária, resultado de disfunção gênica na produção de melanina. Para que a doença se manifeste é necessário que a mutação esteja em homozigose (doença autossômica
O albinismo é uma doença metabólica hereditária, resultado de disfunção gênica na produção de melanina. Para que a doença se manifeste é necessário que a mutação esteja em homozigose (doença autossômica
