Novas Tecnologias de Ativação para Oxidação Química In Situ com Persulfato de Sódio
|
|
|
- Manuela di Castro Beretta
- 8 Há anos
- Visualizações:
Transcrição
1 Pré-impressão: Ata da Quarta Conferência Internacional de Remediação de Compostos Clorados e Recalcitrantes (2004) Novas Tecnologias de Ativação para Oxidação Química In Situ com Persulfato de Sódio Philip A. Block (philip_block@fmc.com) (FMC Corporation, Filadélfia, PA) Richard A. Brown (dick.brown@erm.com) (ERM, Inc., Ewing, NJ) David Robinson (david.robinson@erm.com) (ERM, Inc., Ewing, NJ) RESUMO: a química de oxidação com persulfato é uma tecnologia emergente de oxidação química in situ de compostos orgânicos clorados e não-clorados. A ativação do persulfato para formar radicais sulfato é uma potente ferramenta de remediação de uma ampla variedade de contaminantes, incluindo solventes clorados (etenos, etanos e metanos), BTEX, MTBE, 1,4- dioxano, PCBs e PAHs. Várias novas tecnologias de ativação existem agora para catalisar a formação de radicais sulfato, incluindo persulfato combinado com complexos de metais quelados, persulfato combinado com peróxido de hidrogênio e persulfato alcalino. A amplitude de sistemas ativadores permite a escolha de tecnologia de persulfato adequada para determinados contaminantes e condições do local. Introdução Persulfatos (especialmente dipersulfatos) são oxidantes poderosos que têm sido amplamente utilizados em muitas indústrias para iniciar reações de polimerização de emulsão, clarear piscinas, clarear cabelos, micro-gravação de placas de cobre de circuito impresso e análise de TOC. Nos últimos anos tem aumentado o interesse em persulfato de sódio como um oxidante para a destruição de uma ampla gama de contaminantes do solo e da água subterrânea. Persulfatos são tipicamente manufaturados como sais de sódio, potássio e amônio. A forma de sódio é a mais comumente utilizada em aplicações ambientais. O ânion persulfato é o oxidante mais poderoso da família de compostos de peroxigênio e um dos mais potentes oxidantes utilizados em remediação. O potencial-padrão de oxidaçãoredução para a reação S 2 O H + + 2e - 2HSO - 4 Equação 1 é 2,1 V, em comparação com 1,8 V para o peróxido de hidrogênio (H 2 O 2 ) e 1,4 V para o ânion peroximonosulfato (HSO 5 - ). Esse potencial é superior ao potencial de oxi-redução do ânion permanganato (MnO 4 - ), 1,7 V, mas ligeiramente inferior que o do ozônio, 2,2 V. Além da oxidação direta, o persulfato de sódio pode ser induzido para formar radicais sulfato, fornecendo, assim, mecanismos de reação de radical livre similares aos métodos de radical hidroxila gerados pela química Fenton. A geração de radicais sulfato é S 2 O initiator SO (SO 4 - or SO 4-2 ) Equação 2 O radical sulfato é uma das mais potentes espécies oxidantes aquosas com um potencial de oxi-redução estimado de 2,6 V, similar ao do radical hidroxila, 2,7 V. Além de seu potencial oxidante, a oxidação com persulfato e radical sulfato tem várias vantagens em relação a outros sistemas oxidantes. Primeiro, é cineticamente mais rápida. Segundo, o radical sulfato é mais estável que o radial hidroxila e, conseqüentemente, capaz de transportar distâncias
2 maiores na sub-superfície. Terceiro, o persulfato tem menos atração por orgânicos naturais do solo do que o íon permanganato (Brown 2003) e é, portanto, mais eficaz em solos altamente orgânicos. Esses atributos combinam-se para fazer do persulfato uma opção viável para a oxidação química de uma ampla gama de contaminantes. Ativação por Persulfato Convencional No início dos anos 1960, um corpo significativo de trabalho examinou a cinética e a dinâmica associada à oxidação com persulfato (House, 1962 e Haikola, 1963). Embora se tenha constatado que o ânion persulfato por si só era um oxidante potente, suas taxas de reação são cineticamente lentas para a maioria dos contaminantes recalcitrantes, tais como, o tricloroetileno. Entretanto, a cinética de oxidação com persulfato pode ser significativamente intensificada pela geração de radicais sulfato. A iniciação com radical sulfato (Equação 2) pode ser conseguida por meio da aplicação de calor, catalisadores de metal de transição ou radiação UV. Esses processos são examinados em várias referências (House, 1962; Behrman, 1980; Balazs, 2000). Com ativação por metais de transição, Balazs destaca que embora o mecanismo seja independente do tipo de catalisador, a equação da taxa pode ser geralmente descrita da seguinte maneira: d[s 2 O 8-2 ] / dt = -k [S 2 O 8-2 ] x [catalyst] y Equação 3 onde ½ < x < 3/2 e 0 < y < 3/2. Isso sugere que a taxa de reação é independente da carga de contaminante. Várias patentes recentes têm exposto especialmente a ativação do persulfato para a oxidação de contaminantes orgânicos ou por calor ou por metais de transição. Pugh (1999) trata tanto dos catalisadores metálicos como da ativação por calor, a temperaturas acima de 20 C, para oxidar contaminantes orgânicos. Hoag (2000, 2002) discute os catalisadores metálicos bivalentes e a aplicação de calor na fixa de 40 a 99 C para oxidar VOCs. Esse corpo de literatura basicamente leva-nos a concluir que a utilização efetiva de persulfato para aplicações ambientais necessita uma ativação por calor ou pela adição de ferro II. No laboratório, o persulfato ativado por calor tem-se demonstrado aplicável a uma vasta gama de contaminantes em sistemas aquosos. A temperatura de ativação necessária varia de acordo com o composto. A tabela 1 lista a oxidação de vários compostos em função da temperatura. A 45 ºC e acima dessa temperatura, todos os compostos testados foram oxidados. Bruell (2001) mostrou que essa oxidação de compostos orgânicos com persulfato catalisado por calor em um ambiente de solo requer temperaturas mais altas do que em sistemas aquosos. Para a ativação por catalisadores de metal de transição, o ferro ferroso (Fe +2 ) é o ativador mais comum e prontamente disponível, com as formas mais comuns sendo o sulfato ferroso (FeSO 4 ) e o cloreto ferroso (FeCl 2 ). Geralmente, 100 a 250 mg / l de ferro são necessários para efetivamente ativar o persulfato. A adição de ferro ferroso em excesso, mais do que 750 mg / l, pode levar a uma rápida decomposição do persulfato e perda de desempenho da remediação. Tabela 1 Lista de contaminantes Com > 90% de decomposição tratada com persulfato a 20ºC Tolueno, Etilbenzeno; Xileno; 1,1-DCE; 1,2-Diclorobenzeno; 1,3-Diclorobenzeno, 1,2,4-Triclorobenzeno Lista de contaminantes adicionais Com > 90% de decomposição tratada com persulfato a 35º C 1,2-DCE, PCE, TCE, Cloreto de vinila, Tetracloreto de carbono, 1,1-DCA; 1,2-DCA, Benzeno, Clorobenzeno, MTBE Lista de contaminantes adicionais Com > 90% de decomposição tratada com persulfato a 45º C Cloreto de metileno, Clorofôrmio, 1,1,1-TCA
3 Se quantidades significativas de metais reduzidos estiverem disponíveis na subsuperfície, a adição de catalisadores metálicos pode não ser necessária para catalisar o persulfato. O persulfato ativado por ferro bivalente efetivamente oxida muitos dos compostos sensíveis ao persulfato ativado por calor, incluindo BTEX, clorobenzeno, diclorobenzeno, DCE, TCE, e PCE. Entretanto, sua eficácia contra etanos clorados, tais como, TCA, e metanos clorados, tal como clorofórmio, é limitada. Embora a ativação de persulfato por calor e ferro II seja eficaz em estudos de oxidação em laboratório, ambas têm limitações para aplicação em campo. A ativação por calor requer a instalação de um sistema de aquecimento paralelo para aquecer a matriz do aqüífero à temperatura desejada. Isso requer tanto gastos de capital como despesas operacionais adicionais. As opções de aquecimento in situ incluem injeção de vapor ou ar quente, aquecimento por resistência elétrica (joule), ou aquecimento por radiofreqüência. Geralmente, o calor é mais bem aplicado para tratamento com fonte onde a área-alvo é limitada. O aquecimento in situ com uma fonte de calor externa não é prático para tratar grandes plumas na água subterrânea. O problema com a utilização de ferro II como ativador é sua transportabilidade. O ferro II é conseqüentemente oxidado pelo persulfato em ferro III, o qual, a ph acima de 4, é insolúvel. A reação líquida é: 2Fe +2 + S 2 O 8-2 2Fe +3 + SO 4-2 ; Fe H 2 O Fe(OH) 3 + 3H + Equação 4 Meyers (Meyers, 2002) discutiu o efeito da precipitação de ferro na perda de ativação do persulfato em aplicações de campo. Por exemplo, em um teste de tratamento piloto de TCE com persulfato, uma mistura de persulfato com ferro (10% de persulfato de sódio e 174 mg/l de Fe +2 disponível) foi injetada em silte arenoso. Nove dias depois da injeção, um ponto de monitoramento 1,5 M abaixo do ponto de injeção foi amostrado, e encontrou-se uma concentração de ferro de 0,3 mg/l, e a concentração de TCE, 9,3 mg/l. Amostras da água subterrânea no ponto de monitoramento foram coletadas e redosadas ou com o ferro sozinho ou com persulfato sem ferro adicional. Após 7 dias as amostras redosadas foram reanalisadas quanto a TCE. Os resultados são mostrados na tabela 2. Obteve-se maior redução dos níveis de TCE quando com adição de Fe +2 adicional, em comparação com adição apenas de persulfato adicional, sugerindo a falta de catalisador disponível, e não oxidante, na subsuperfície no ponto de monitoramento descendente. Novas Tecnologias de Ativação Tabela 2: 7 Dias Dose Material TCE, µg/l Controle nenhuma dose g/l Persulfato mg/l Fe As restrições práticas na formação de radical sulfato por aquecimento ou adição de ferro ferroso indicam uma necessidade de sistemas aprimorados de ativação de persulfato. Tais tecnologias deveriam: ser transportáveis em um sistema de água subterrânea aumentar a reatividade de persulfato com uma ampla gama de contaminantes orgânicos ser fácil de aplicar em uma variedade de condições de subsuperfície. Vários novos sistemas de ativação de persulfato têm sido recentemente desenvolvidos (FMC - ERM, 2002; FMC - Orin, 2003) e abordam essas questões. Poucas dessas tecnologias utilizam
4 vias não-metálicas para gerar radicais sulfato. O que segue trata desses novos ativadores. A. Catalisadores de metal quelado Catalisadores de metal quelado são complexos de metais de transição legados a poderosos agentes quelantes. Os exemplos de agentes quelantes incluem: ácido etilenodiaminotetracético (EDTA), citrato, polifosfato, ácido glicólico, catecol, ácido nitrilotriacético (NTA), tetrahidroquinolina (THQ) e outros nessa classe de materiais. Um trabalho anterior (Pignatello, 1992) demonstrou o benefício de complexos de ferro quelado na ativação de peróxido de hidrogênio para a destruição de pesticidas complexos. Constatou-se que o ferro quelado trivalente (Fe +3 ), além do Fe +2, tinha excelente desempenho de oxidação. Testes de laboratório foram realizados para verificar a eficácia dos catalisadores de ferro quelado na ativação de persulfato utilizando vários complexos diferentes de ferro - quelante. O complexo quelante de melhor desempenho, Fe(III) EDTA será destacado para fins de discussão. Todas as amostras foram preparadas como soluções aquosas em garrafas VOA com zero de espaço livre. Uma mistura de contaminante-padrão foi utilizada: vinte e oito diferentes VOCs foram dissolvidos em água destilada desionizada para atingir concentrações individuais de VOC de mg/l. O complexo Fe-EDTA foi gerado pela reação de concentrações equimolares de cloreto férrico e EDTA. O complexo Fe - EDTA foi dosado para fornecer 550 mg/l de ferro disponível à solução. Um nível de dosagem de oxidante de 10 % de persulfato de sódio foi utilizado. Amostras foram tomadas no tempo 0, e nos dias 7, 14 e 21 e analisadas via GC-MS. Todos os estudos foram realizados à temperatura e ph ambientes. Os resultados de 21 dias são mostrados na tabela 3, que compara o persulfato sozinho e o persulfato com: ferro II (não-quelado), Fe(III) (não quelado), e Fe(III)-EDTA. Um controle da água deionizada também foi realizado. A tabela mostra os resultados para Tabela 3 Desempenho do Persulfato + catalisadores de ferro, ph ambiente, resultados 21º dia Persulfato µg / l Controle Persulfato Persulfato Fe(II) Persulfato Fe(III) Fe(III)- EDTA Clorometanos Cloroetanos Cloroetetilenos Clorobenzenos BTEX Oxigenados ph 6,9 2,2 2,3 2,3 2,2 diferentes classes de contaminantes. Várias observações podem ser feitas a partir dos dados. Primeiro, nenhum persulfato/catalisadores de ferro é eficaz com cloroetanos ou clorometanos. Segundo, todas as soluções de persulfato resultaram em baixo ph. Terceiro, o Fe(II) foi o catalisado mais eficaz. O segundo melhor catalisador foi o complexo Fe EDTA. Quarto, a oxidação de BTEX foi eficaz com o persulfato sozinho (sem catalisador). E quinto, o Fe(III), em ph baixo, é um catalisador moderadamente eficaz. Deve-se observar que os resultados na tabela 3 são em ph 2, onde a solubilidade e atividade do metal não é um problema. Sob condições de ph neutro que podem ser encontradas em campo, quelar catalisadores de metal de transição fornece proteção contra hidratação e preciptação (veja Eq. 4). A tabela 4 mostra os resultados para diferentes catalisadores de ferro, com persulfato a ph controlado, de 7-8. As condições experimentais foram aquelas utilizadas para gerar a tabela 3, exceto: 1) pela utilização de Fe (III) - EDTA (Aldrich) comercial com o nível de dosagem de ferro 100 mg/l e 2) a concentração de persulfato foi 2,5% (em vez de 10%). Como pode ser visto na tabela 4,
5 a ph 7-8, apenas o catalisador Fe-EDTA com persulfato foi eficaz, enquanto os catalisadores de ferro não-quelado reduziram a atividade. A solubilidade dos catalisadores de metal de transição são fatores críticos na ativação de persulfato. A quelação é um meio eficaz de manter a atividade de um metal em condições de água subterrânea neutra ou alcalina. B. Sistema de oxidante duplo: Persulfato de sódio e Peróxido de hidrogênio A tecnologia do peróxido de hidrogênio, conhecida como reagente Fenton, tem sido amplamente aplicada no tratamento de contaminantes da água subterrânea, com resultados variantes. Em geral, ele é altamente reativo e é capaz de oxidar uma vasta gama de contaminantes. Entretanto, a limitação do peróxido de hidrogênio é sua estabilidade em algumas matrizes de solo, onde rapidamente decompõem-se, limitando seu transporte e sua eficácia. Um sistema de oxidante duplo (FMC - Orin, 2003) utilizando peróxido de hidrogênio e persulfato de sódio foi desenvolvido, combinando a reatividade do peróxido na redução dos compostos em questão com a estabilidade aprimorada pelo persulfato. Supõe-se que o peróxido de hidrogênio e o persulfato possam ter vários atributos sinérgicos. Primeiro, os radicais hidroxila podem iniciar a formação de radical persulfato. Similarmente, os radicais sulfato podem estimular a formação de radicais hidroxila. Segundo, o peróxido de hidrogênio pode reagir com uma porção significativa dos contaminantes mais reativos, permitindo que os radicais sulfato destruam os compostos mais recalcitrantes em questão. Finalmente, uma combinação de peróxido e radicais sulfato pode fornecer um mecanismo de ataque multiradical, resultando em mais eficiência na destruição de contaminantes ou permitindo que os compostos recalcitrantes sejam mais rapidamente degradados. Os testes iniciais de laboratório pela Orin RT (FMC - Orin, 2003) foram realizados com a adição de solventes clorados a uma solução aquosa à temperatura ambiente. Dois gramas de persulfato de sódio e 8 ml de peróxido de hidrogênio a 12,5% foram adicionados por 100 gramas de solução contaminada. As amostras Tabela 4 Desempenho de catalisadores de ferro com persulfato, ph controlado (7-8), resultados no 21º dia µg / l Controle Persulfato Fe (II) Fe (II) Fe (III) Fe-EDTA ph contr ph amb ph contr ph contr ph contr Etilenos Etanos Metanos , BTEX , Clorobenzenos , Oxigenados , ph 6,7 8,5 2 7,5 8 7,6 Tabela 5 Degradação de contaminantes com persulfato + peróxido (mg/l) Tempo 0 8º Dia 1,1-DCE 4,5 0,1 TCE 2,8 não-detectável 1,1-DCA 1,1 não-detectável 1,1,1-TCA 12,0 0,6 foram colhidas no 8º dia e analisadas por GC-MS. A tabela 5 mostra os resultados do estudo. Reduções significativas foram medidas não apenas para etilenos clorados, mas também para etanos clorados. Um segundo estudo de laboratório foi realizado utilizando solos de uma MGP (indústria de gás manufaturado). Foi feita uma pasta utilizando 400 g de solo processado e 1,08l de água destilada. Adicionou-se então o persulfato de sódio a uma concentração de 11,5 g/l e deixou-se misturar. Em seguida, 120 ml de peróxido 50% foram adicionados. A pasta foi então analisada via GC-MS.Os resultados são mostrados na
6 Figura 1. Os VOCs presentes eram BTEX e estireno. Os SVOCs eram PAHs de 3 a 5 anéis. Diciclopentadieno (DCPD) estava presente como o principal constituinte. Como pode ser visto na figura 1, o sistema combinado peróxido-persulfato foi eficaz contra todos esses contaminantes. O sistema de reação do combinado peróxido-persulfato parece ter uma ampla gama de aplicabilidade. Ele não apenas oxida compostos geralmente sensíveis a oxidação com persulfato, mas também oxida compostos não rapidamente oxidados pela tecnologia de persulfato convencional. D. Persulfato alcalino Sabe-se que o persulfato é altamente reativo em ph baixo (<3), mas ele é também altamente reativo em ph superior a 10. Poderia então ser possível ativar o persulfato aumentando o ph a valores elevados. Os testes inicias em laboratório indicaram que a oxidação de contaminantes com persulfato não era apenas uma questão de ph alto, mas também da capacidade de tampão (razão molar do modificador de ph do persulfato). Os estudos foram realizados em frascos VOA com zero de espaço livre. Embora se tenha observado que vários modificadores de ph ativavam persulfato, o KOH será utilizado para argumentação. Amostras foram preparadas adicionando-se persulfato a uma concentração de 25 g/l e KOH para atingir razões molares de 0,2, 0,4, 0,5 e 0,8 de KOH por persulfato. As amostras foram analisadas após 7 dias por GC-MS. Um controle sem persulfato ou KOH também foi analisado. Nenhum outro catalisador foi adicionado às amostras. A ativação do persulfato que foi observada é exclusivamente devida à base adicionada. Os resultados desses estudos são mostrados na figura 2. Os dados estão agrupados por classe de contaminante. Efeito da razão de KOH na reatividade do persulfato Várias observações podem ser feitas a partir desses resultados. Primeiro, a reatividade do persulfato aumenta com os níveis crescentes de KOH. Segundo, parece haver um efeito de limiar na oxidação de alguns VOCs clorados. A razão molar precisa ser 0,4 ou superior para que o persulfato efetivamente reaja com os VOCs clorados recalcitrantes (etanos e metanos). O efeito da quantidade de KOH na oxidação de BTEX e oxigenados (MTBE, TBA, 1,4-dioxano) é
7 mais gradual. A quantidade oxidada aumenta com o aumento de KOH. A tabela 6 lista o ph observado nos dias 7 e 14 para diferentes razões molares de KOH e persulfato. O ph parece ter um ponto de ruptura semelhante ao observado para a reatividade. Uma razão molar de 0,4 ou superior é necessária para atingir um ph acima de 10,0. Um resultado interessante desse estudo é o efeito do ph alcalino na dificuldade histórica de destruição de compostos, tais como, etanos e metanos clorados. A tabela 7 mostra os resultados do 14º dia de estudo de uma seleção de compostos para duas razões diferentes de KOH/persulfato. Na maioria dos casos, houve destruição completa desses compostos. Várias conclusões podem ser tiradas desses estudos. Primeiro, o persulfato alcalino tem uma ampla reatividade. Segundo, a ativação alcalina de persulfato parece ser possível com várias bases diferentes. Cada base deve ter uma razão ideal diferente e/ou ponto de ruptura. Terceiro, ao aplicar a tecnologia de ativador alcalino de persulfato, é importante adicionar base suficiente (excedendo a capacidade de tampão). A quantidade de base precisa levar em conta qualquer acidez do solo. Tabela 6: ph versus razão molar de KOH Razão molar ph, 7º dia ph, 14º dia 0 1,3 0,5 0,2 4,3 4,5 0,38 11,5 10,4 0,5 11,5 10,5 0,8 12,2 13 Tabela 7: destruição de compostos recalcitrantes com persulfato alcalino - Resultados do 14º dia µg/l Controle 14º dia 0,5 mol KOH/persulfato 0,8 mol KOH/persulfato 1,1,1-TCA ,1,2-TCA ND ND 1,2-DCA ND ND 1,1-DCA ND Tetracloreto ND ND de carbono Cloreto de ND ND metileno Cloreto de 195 ND ND vinila ND - não detectado Quarto, há vias de reação de persulfato que não são atualmente bem compreendidas e podem potencialmente ser otimizadas no futuro. A reação do persulfato sob condições básicas é uma tecnologia nova que merece mais estudo. Resumo A química de oxidação com persulfato é uma tecnologia Os emergente para oxidação in situ de contaminantes são apenas BTEX? compostos orgânicos clorados e não-clorados. A ativação de persulfato para formar radicais Apenas sulfato resulta em uma ferramenta BTEX e MTBE? poderosa para a remediação de uma ampla variedade de contaminantes, incluindo solventes clorados São CVOCs? (etilenos, etanos e metanos), BTEX, MTBE, 1,4-dioxano, PCBs e hidrocarbonetos poliaromáticos. São CVOCs, Existe uma variedade de Cloroetanos, Clorometanos químicas que podem ser escolhidas? para catalisar a formação de radicais sulfato. A escolha do sistema ativador a utilizar é primordial para maximizar a eficácia da Figura 3: Escolhendo o ativador correto Persulfato sozinho (por exemplo, PAHs, Estireno, 1,4-Dioxano, etc.) (Etilenos e Benzenos) Oxidação Leve Persulfato, Fe-ETDA Vapor disponível e utilizável? Solos permeáveis? Oxidação forte Persulfato aquecido, Persulfato-peróxido, Persulfato alcalino Persulfato-peróxido, Persulfato alcalino Persulfato alcalino Oxidação Agressiva
8 oxidação com persulfato. A figura 3 fornece um fluxo lógico para avaliar os diferentes sistemas de ativador. Há três níveis de ativadores de persulfato que podem ser utilizados. Eles incluem Oxidação Leve, na qual o persulfato sozinho é utilizado. Isso pode ser apropriado para locais com BTEX. Se MTBE estiver presente, então o sistema de Oxidação Forte, no qual se utiliza persulfato ativado com Fe - EDTA, é apropriado. O sistema de Oxidação Forte também é adequado para locais com apenas etilenos clorados (PCE, TCE, DCE) ou clorobenzenos. Se houver presença de etanos ou metanos clorados que necessitam de tratamento, então os sistemas de Oxidação Agressiva deveriam ser avaliados. Eles incluem persulfato alcalino, combinado de peróxido e persulfato, e persulfato aquecido. Essas químicas de ativação agressivas podem ser aplicadas também para BTEX e locais de etileno clorado se for desejada uma rápida remediação, ou se houver uma alta carga de contaminante. A avaliação adequada das condições do local é também necessária para a aplicação eficaz da tecnologia de persulfato adequada. A geologia e hidrologia do local, as propriedades do solo, a demanda de oxidante do solo e as metas de remediação são todos fatores-chave para avaliar. A tecnologia de persulfato não é uma tecnologia um tipo serve para todos os casos. Há uma rica e variada química que pode ser trazida para lidar com os problemas de uma ampla variedade de contaminantes. Referências Balazs, G.B., J.F. Cooper, P.R. Lewis and G.M. Adamson. Emerging Technologies in Hazardous Waste Management 8, ed. Tedder and Pohland, Kluwer Academic / Plenum Publishers, New York, Behrman, E.J. and J.O. Edwards. Reviews in Inorganic Chemistry, 2, p 179 (1980) Brown, R.A., D. Robinson and G. Skladany. Response to Naturally Occurring Organic Material: Permanganate versus Persulfate, ConSoil 2003, Ghent Belgium, (2003) Bruell, C. J. Kinetics of Thermally Activated Persulfate Oxidation of Trichloroethylene (TCE) and 1,1,1- Trichloroethane (TCA), The First International Conference on Oxidation and Reduction Technologies for In-Situ Treatment of Soil and Groundwater, Niagara Falls, Ontario, Canada, June 25-29, 2001 Elmendorf, C., F. Sessa. Poster at the 4 th Annual Batelle Conference On the Remediation of Chlorinated and Recalcitrant Compounds, Panther Technologies and FMC Corporation (2004) FMC Corporation and Environmental Resources Management, patent pending technology (2002) FMC Corporation and Orin RT, patent pending technology (2003) Hakoila, E. Ann. Univ. Turku, Ser A, 66, (1963). Hoag, G.E., P.V. Chhedda, B.A. Woody and G.M. Dobbs. US Patent 6,019,548 (2000) Hoag, G.E., P.V. Chhedda, B.A. Woody and G.M. Dobbs. US Patent 6,474,908 (2002) House, D.A. Chem Rev, 62, p 185 (1962). Huang, K.C., R.A. Couttenye, and G.E. Hoag. Chemosphere, 49, p 413 (2002) Meyer, M., Sodium Persulfate Oxidation of TCE Plume In Belgium, The Second International Conference on Oxidation and Reduction Technologies for In-Situ Treatment of Soil and Groundwater, Toronto, Ontario, November 19-22, 2002 Pugh, J.R., US Patent 5,976,348 (1999) Pignatello, J.J and Y. Sun. J. Agr. Food Chem., 40, p. 322 (1992)
Parte 2 A abordagem da ORIN Estratégia da remoçao de fase livre Estudo de casos EIT-DL
 Parte I Peroxychem Overview Química do Klozur Persulfato Tratamento e considerações sobre LNAPL residual Considerações sobre dosage do Klozur Persulfato Parte 2 A abordagem da ORIN Estratégia da remoçao
Parte I Peroxychem Overview Química do Klozur Persulfato Tratamento e considerações sobre LNAPL residual Considerações sobre dosage do Klozur Persulfato Parte 2 A abordagem da ORIN Estratégia da remoçao
SurTec 872 Processo de Cromo Decorativo
 SurTec 872 Processo de Cromo Decorativo 1- DESCRIÇÃO O SurTec 872 é uma mistura de catalisadores e ácido crômico desenvolvido especialmente, para um processo de cromação decorativa de alto desempenho.
SurTec 872 Processo de Cromo Decorativo 1- DESCRIÇÃO O SurTec 872 é uma mistura de catalisadores e ácido crômico desenvolvido especialmente, para um processo de cromação decorativa de alto desempenho.
Oxidação Química In Situ. Sander Eskes
 Oxidação Química In Situ Sander Eskes Oxidação Química In Situ Definição: Introdução no aqüífero um composto químico capaz de oxidar os contaminantes na fase dissolvida, fase adsorvida e fase residual
Oxidação Química In Situ Sander Eskes Oxidação Química In Situ Definição: Introdução no aqüífero um composto químico capaz de oxidar os contaminantes na fase dissolvida, fase adsorvida e fase residual
3ª Série / Vestibular. As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar que, na reação:
 3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
Mesa Redonda sobre Produtos Remediadores
 Mesa Redonda sobre Produtos Remediadores (CONAMA 314) São Paulo, Setembro de 2013 Alexandre Maximiano, MsC. Diretor Técnico AESAS TECNOHIDRO Projetos Ambientais São Paulo, SP copyright 2013. Alexandre
Mesa Redonda sobre Produtos Remediadores (CONAMA 314) São Paulo, Setembro de 2013 Alexandre Maximiano, MsC. Diretor Técnico AESAS TECNOHIDRO Projetos Ambientais São Paulo, SP copyright 2013. Alexandre
Determinação das Durezas Temporária, Permanente e Total de uma Água
 Determinação das Durezas Temporária, Permanente e Total de uma Água Dureza: Parâmetro característico das águas de abastecimento industrial e doméstico. Em suma é a dificuldade de uma água não dissolver
Determinação das Durezas Temporária, Permanente e Total de uma Água Dureza: Parâmetro característico das águas de abastecimento industrial e doméstico. Em suma é a dificuldade de uma água não dissolver
ISCO ou ISCR? Integrando tecnologias na Remediação
 ISCO ou ISCR? Integrando tecnologias na Remediação Remediação de Solo e Água Subterrânea Visão Geral das Tecnologias Afonso Matsura - PeroxyChem Paulino Rodriguez - EnviroChem Soluções Tecnológicas comprovadas
ISCO ou ISCR? Integrando tecnologias na Remediação Remediação de Solo e Água Subterrânea Visão Geral das Tecnologias Afonso Matsura - PeroxyChem Paulino Rodriguez - EnviroChem Soluções Tecnológicas comprovadas
USO DE OXIDANTES QUÍMICOS NA REMEDIAÇÃO DE AQUÍFEROS CONTAMINADOS POR DNAPLs
 USO DE OXIDANTES QUÍMICOS NA REMEDIAÇÃO DE AQUÍFEROS CONTAMINADOS POR DNAPLs R. C. M. Nobre Universidade Federal de Alagoas M.de M. M. Nobre Universidade Federal de Alagoas, Maia Nobre Engenharia RESUMO:
USO DE OXIDANTES QUÍMICOS NA REMEDIAÇÃO DE AQUÍFEROS CONTAMINADOS POR DNAPLs R. C. M. Nobre Universidade Federal de Alagoas M.de M. M. Nobre Universidade Federal de Alagoas, Maia Nobre Engenharia RESUMO:
4 Apresentação e Discussão dos Resultados
 4 Apresentação e Discussão dos Resultados 4.1. Biodegradação Os primeiros ensaios de tratabilidade foram realizados apenas com o uso de lodo ativado, visando promover a degradação biológica dos compostos
4 Apresentação e Discussão dos Resultados 4.1. Biodegradação Os primeiros ensaios de tratabilidade foram realizados apenas com o uso de lodo ativado, visando promover a degradação biológica dos compostos
(B) CaCO 3 CaO + CO 2 CO 2 + H 2 O H 2 CO 3. (C) CaCO 3 + 2 HCl CaCl 2 + H 2 O + CO 2. (D) Ca(HCO 3 ) 2 + 2 HCl CaCl 2 + 2 H 2 O + 2 CO 2
 UNESP 2008/2 1-A figura ilustra o sistema utilizado, em 1953, por Stanley L. Miller e Harold C. Urey, da Universidade de Chicago, no estudo da origem da vida no planeta Terra. O experimento simulava condições
UNESP 2008/2 1-A figura ilustra o sistema utilizado, em 1953, por Stanley L. Miller e Harold C. Urey, da Universidade de Chicago, no estudo da origem da vida no planeta Terra. O experimento simulava condições
1 - Universidade Federal Fluminense UFF,Niterói RJ, 2 Instituto Nacional de Tecnologia INT Rio de Janeito - RJ
 DEGRADAÇÃO DO HERBICIDA 2,4-D EM ÁGUA VIA OXIDAÇÃO POR PERSULFATO ATIVADO POR Fe 2+, Fe 3+ E SEUS COMPLEXOS Adriana C. Velosa 1,2 ; Emmanoel V. S. Filho 1 1 - Universidade Federal Fluminense UFF,Niterói
DEGRADAÇÃO DO HERBICIDA 2,4-D EM ÁGUA VIA OXIDAÇÃO POR PERSULFATO ATIVADO POR Fe 2+, Fe 3+ E SEUS COMPLEXOS Adriana C. Velosa 1,2 ; Emmanoel V. S. Filho 1 1 - Universidade Federal Fluminense UFF,Niterói
TRATAMENTO DE FENANTRENO UTILIZANDO PERSULFATO DE SÓDIO ATIVADO POR DIATOMITA MODIFICADA POR FERRO
 TRATAMENTO DE FENANTRENO UTILIZANDO PERSULFATO DE SÓDIO ATIVADO POR DIATOMITA MODIFICADA POR FERRO S.S.O. SILVA. 1 ; A.R. SOUZA 1 ; A. G. CÂMARA 1 ; C. K. O. SILVA 2 ; M.M.G.R. VIANNA 2, O. CHIAVONE-FILHO
TRATAMENTO DE FENANTRENO UTILIZANDO PERSULFATO DE SÓDIO ATIVADO POR DIATOMITA MODIFICADA POR FERRO S.S.O. SILVA. 1 ; A.R. SOUZA 1 ; A. G. CÂMARA 1 ; C. K. O. SILVA 2 ; M.M.G.R. VIANNA 2, O. CHIAVONE-FILHO
AVALIAÇÃO DO USO DE MgO 2 COMO FONTE DE H 2 O 2 PARA A REMEDIAÇÃO DE ÁGUA SUBTERRÂNEA VIA REAÇÃO DE FENTON MODIFICADA
 AVALIAÇÃO DO USO DE MgO 2 COMO FONTE DE H 2 O 2 PARA A REMEDIAÇÃO DE ÁGUA SUBTERRÂNEA VIA REAÇÃO DE FENTON MODIFICADA A. C. VELOSA 1, C. A. O. NASCIMENTO 1 1 Universidade de São Paulo, Departamento de
AVALIAÇÃO DO USO DE MgO 2 COMO FONTE DE H 2 O 2 PARA A REMEDIAÇÃO DE ÁGUA SUBTERRÂNEA VIA REAÇÃO DE FENTON MODIFICADA A. C. VELOSA 1, C. A. O. NASCIMENTO 1 1 Universidade de São Paulo, Departamento de
Lista Prova - Gás Ideal
 Lista Prova - Gás Ideal 1) Se 2 mols de um gás, à temperatura de 27ºC, ocupam um volume igual a 57,4 litros, qual é a pressão aproximada deste gás? Considere R=0,082 atm.l/mol.k (Constante dos Gases) a)
Lista Prova - Gás Ideal 1) Se 2 mols de um gás, à temperatura de 27ºC, ocupam um volume igual a 57,4 litros, qual é a pressão aproximada deste gás? Considere R=0,082 atm.l/mol.k (Constante dos Gases) a)
Substâncias puras e misturas; análise imediata
 Segmento: Pré-vestibular Resoluções Coleção: Alfa, Beta e Gama Disciplina: Química Volume: 1 Série: 5 Substâncias puras e misturas; análise imediata 1. C Considerando as ilustrações, temos: I. Mistura
Segmento: Pré-vestibular Resoluções Coleção: Alfa, Beta e Gama Disciplina: Química Volume: 1 Série: 5 Substâncias puras e misturas; análise imediata 1. C Considerando as ilustrações, temos: I. Mistura
MF-0427.R-2 - MÉTODO DE DETERMINAÇÃO DE FÓSFORO TOTAL (DIGESTÃO COM HNO 3 + HClO 4 E REAÇÃO COM MOLIBDATO DE AMÔNIO E ÁCIDO ASCÓRBICO)
 MF-0427.R-2 - MÉTODO DE DETERMINAÇÃO DE FÓSFORO TOTAL (DIGESTÃO COM HNO 3 + HClO 4 E REAÇÃO COM MOLIBDATO DE AMÔNIO E ÁCIDO ASCÓRBICO) Notas: Aprovado pela Deliberação CECA nº 0424, de 24 de fevereiro
MF-0427.R-2 - MÉTODO DE DETERMINAÇÃO DE FÓSFORO TOTAL (DIGESTÃO COM HNO 3 + HClO 4 E REAÇÃO COM MOLIBDATO DE AMÔNIO E ÁCIDO ASCÓRBICO) Notas: Aprovado pela Deliberação CECA nº 0424, de 24 de fevereiro
TITULAÇÃO EM QUÍMICA ANALÍTICA
 TITULAÇÃO EM QUÍMICA ANALÍTICA Titulação Procedimento analítico, no qual a quantidade desconhecida de um composto é determinada através da reação deste com um reagente padrão ou padronizado. Titulante
TITULAÇÃO EM QUÍMICA ANALÍTICA Titulação Procedimento analítico, no qual a quantidade desconhecida de um composto é determinada através da reação deste com um reagente padrão ou padronizado. Titulante
AVALIAÇÃO TÉCNICA DA REMEDIAÇÃO DE SOLO UTILIZANDO PERSULFATO/ PERÓXIDO DE HIDROGÊNIO
 AVALIAÇÃO TÉCNICA DA REMEDIAÇÃO DE SOLO UTILIZANDO PERSULFATO/ PERÓXIDO DE HIDROGÊNIO EVALUATION OF THE TECHNIQUE USING PERSULFATE IN SOIL REMEDIATIO Hermano Gomes Fernandes Mestrando em Engenharia Química.
AVALIAÇÃO TÉCNICA DA REMEDIAÇÃO DE SOLO UTILIZANDO PERSULFATO/ PERÓXIDO DE HIDROGÊNIO EVALUATION OF THE TECHNIQUE USING PERSULFATE IN SOIL REMEDIATIO Hermano Gomes Fernandes Mestrando em Engenharia Química.
AVALIAÇÃO DO DESEMPENHO DE SURFACTANTES PARA A SOLUBILIZAÇÃO E REMOÇÃO DE DNAPLs DE ÁGUAS SUBTERRÂNEAS
 AVALIAÇÃO DO DESEMPENHO DE SURFACTANTES PARA A SOLUBILIZAÇÃO E REMOÇÃO DE DNAPLs DE ÁGUAS SUBTERRÂNEAS Elizabeth Fátima de Souza e Mariana Rodrigues Peres Faculdade de Química CEATEC PUC-Campinas Campinas
AVALIAÇÃO DO DESEMPENHO DE SURFACTANTES PARA A SOLUBILIZAÇÃO E REMOÇÃO DE DNAPLs DE ÁGUAS SUBTERRÂNEAS Elizabeth Fátima de Souza e Mariana Rodrigues Peres Faculdade de Química CEATEC PUC-Campinas Campinas
Na industria de alimentos a formação de filmes e depósitos minerais na superfície de equipamentos, prejudica o processo de higienização.
 Determinação da Dureza Total em água de abastecimento A dureza é provocada pela presença de sais de cálcio e magnésio. Não apresenta importância sanitária, mas o uso de uma água com excesso deste íons
Determinação da Dureza Total em água de abastecimento A dureza é provocada pela presença de sais de cálcio e magnésio. Não apresenta importância sanitária, mas o uso de uma água com excesso deste íons
TRATAMENTO DE ÁGUAS CONTAMINADAS
 4º SEMINÁRIO ESTADUAL ÁREAS CONTAMINADAS E SAÚDE: CONTAMINAÇÃO DO SOLO E RECURSOS HÍDRICOS TRATAMENTO DE ÁGUAS CONTAMINADAS Profª Drª Dione Mari Morita Escola Politécnica Universidade de São Paulo 4º SEMINÁRIO
4º SEMINÁRIO ESTADUAL ÁREAS CONTAMINADAS E SAÚDE: CONTAMINAÇÃO DO SOLO E RECURSOS HÍDRICOS TRATAMENTO DE ÁGUAS CONTAMINADAS Profª Drª Dione Mari Morita Escola Politécnica Universidade de São Paulo 4º SEMINÁRIO
QUÍMICA (2ºBimestre 1ºano)
 QUÍMICA (2ºBimestre 1ºano) TABELA PERIÓDICA ATUAL Exemplo: Se o K (potássio) encontra-se no 4º período ele possui 4 camadas. Nº atômico = Z 19 K-2; L-8, M-8; N-1 Propriedades gerais dos elementos Metais:
QUÍMICA (2ºBimestre 1ºano) TABELA PERIÓDICA ATUAL Exemplo: Se o K (potássio) encontra-se no 4º período ele possui 4 camadas. Nº atômico = Z 19 K-2; L-8, M-8; N-1 Propriedades gerais dos elementos Metais:
FÓRUM DE MEIO AMBIENTE CRQ IV SP Tecnologias de Tratamento de Áreas Contaminadas Remediação Ambiental In situ
 FÓRUM DE MEIO AMBIENTE CRQ IV SP Tecnologias de Tratamento de Áreas Contaminadas Remediação Ambiental In situ JULIANO DE ALMEIDA ANDRADE juliano@oxiambiental.combr CRQ IV SP, 20 de setembro de 2018 POPULAÇÃO
FÓRUM DE MEIO AMBIENTE CRQ IV SP Tecnologias de Tratamento de Áreas Contaminadas Remediação Ambiental In situ JULIANO DE ALMEIDA ANDRADE juliano@oxiambiental.combr CRQ IV SP, 20 de setembro de 2018 POPULAÇÃO
4. Resultados e Discussão
 Absorbância 4. Resultados e Discussão 4.1. Obtenção da curva de calibração A obtenção da curva de calibração, absorbância vs. concentração de Paraquat, é necessária para a análise química do pesticida.
Absorbância 4. Resultados e Discussão 4.1. Obtenção da curva de calibração A obtenção da curva de calibração, absorbância vs. concentração de Paraquat, é necessária para a análise química do pesticida.
TRATAMENTO DE SOLO ARENOSO CONTAMINADO COM DIESEL UTILIZANDO MÉTODO INOVADOR DE ATIVAÇÃO PARA O PERÓXIDO DE HIDROGÊNIO
 TRATAMENTO DE SOLO ARENOSO CONTAMINADO COM DIESEL UTILIZANDO MÉTODO INOVADOR DE ATIVAÇÃO PARA O PERÓXIDO DE HIDROGÊNIO A. R. de SOUZA 1, A. G. da CÂMARA 1, S. S. O. da SILVA 1, C. K. O. SILVA 2 ; M. M.
TRATAMENTO DE SOLO ARENOSO CONTAMINADO COM DIESEL UTILIZANDO MÉTODO INOVADOR DE ATIVAÇÃO PARA O PERÓXIDO DE HIDROGÊNIO A. R. de SOUZA 1, A. G. da CÂMARA 1, S. S. O. da SILVA 1, C. K. O. SILVA 2 ; M. M.
PAG Química Estequiometria
 1. 2. 3. Em países de clima desfavorável ao cultivo de cana-de-açúcar, o etanol (C 2 H 6 O) é sintetizado através da reação de eteno (C 2 H 4 ) com vapor de água, a alta temperatura e alta pressão, segundo
1. 2. 3. Em países de clima desfavorável ao cultivo de cana-de-açúcar, o etanol (C 2 H 6 O) é sintetizado através da reação de eteno (C 2 H 4 ) com vapor de água, a alta temperatura e alta pressão, segundo
ANEXO I VALORES LIMITE DE EMISSÃO DE PARÂMETROS CARACTERÍSTICOS DAS ÁGUAS RESIDUAIS INDUSTRIAIS
 VALORES LIMITE DE EMISSÃO DE PARÂMETROS CARACTERÍSTICOS DAS ÁGUAS RESIDUAIS INDUSTRIAIS 1. Com excepção dos casos particulares a definir pela Entidade Licenciadora SMAS - as aguas residuais industriais
VALORES LIMITE DE EMISSÃO DE PARÂMETROS CARACTERÍSTICOS DAS ÁGUAS RESIDUAIS INDUSTRIAIS 1. Com excepção dos casos particulares a definir pela Entidade Licenciadora SMAS - as aguas residuais industriais
FÍSICO-QUÍMICA PROF. ALEXANDRE LIMA
 FÍSICO-QUÍMICA PROF. ALEXANDRE LIMA 1. Uma solução contendo 14g de cloreto de sódio dissolvidos em 200mL de água foi deixada em um frasco aberto, a 30 C. Após algum tempo, começou a cristalizar o soluto.
FÍSICO-QUÍMICA PROF. ALEXANDRE LIMA 1. Uma solução contendo 14g de cloreto de sódio dissolvidos em 200mL de água foi deixada em um frasco aberto, a 30 C. Após algum tempo, começou a cristalizar o soluto.
A prova escrita é composta de 10 questões, sendo 4 obrigatórias e 6 eletivas.
 A prova escrita é composta de 10 questões, sendo 4 obrigatórias e 6 eletivas. O candidato deverá responder 8 questões: as 4 obrigatórias (questões de números 1 a 4) e outras 4 escolhidas dentre as eletivas
A prova escrita é composta de 10 questões, sendo 4 obrigatórias e 6 eletivas. O candidato deverá responder 8 questões: as 4 obrigatórias (questões de números 1 a 4) e outras 4 escolhidas dentre as eletivas
BANHO DE CROMO BRILHANTE
 Rev. 004 Data: 06/11/14 Página 1 1 DESCRIÇÃO O PROCESSO CROMO DECORATIVO foi especialmente formulado para operar com baixa concentração e baixa temperatura, obtendo assim uma ótima penetração. O PROCESSO
Rev. 004 Data: 06/11/14 Página 1 1 DESCRIÇÃO O PROCESSO CROMO DECORATIVO foi especialmente formulado para operar com baixa concentração e baixa temperatura, obtendo assim uma ótima penetração. O PROCESSO
ANEXO I VALORES LIMITE DE EMISSÃO DE PARÂMETROS CARACTERÍSTICOS DAS ÁGUAS RESIDUAIS INDUSTRIAIS
 VALORES LIMITE DE EMISSÃO DE PARÂMETROS CARACTERÍSTICOS DAS ÁGUAS RESIDUAIS INDUSTRIAIS 1. Com excepção dos casos particulares a definir pela Entidade Licenciadora SMAS - as aguas residuais industriais
VALORES LIMITE DE EMISSÃO DE PARÂMETROS CARACTERÍSTICOS DAS ÁGUAS RESIDUAIS INDUSTRIAIS 1. Com excepção dos casos particulares a definir pela Entidade Licenciadora SMAS - as aguas residuais industriais
Estudo Estudo da Química
 Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 16 CONCENTRAÇÃO DE SOLUÇÕES 1.
Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 16 CONCENTRAÇÃO DE SOLUÇÕES 1.
Reações de Oxidação e Substituição. Karla Gomes Diamantina-MG
 Reações de Oxidação e Substituição Karla Gomes Diamantina-MG Reações de oxidação Envolvem aumento no estado de oxidação (Nox) dos átomos presentes em uma molécula. De forma geral: Substância orgânica (redutora)
Reações de Oxidação e Substituição Karla Gomes Diamantina-MG Reações de oxidação Envolvem aumento no estado de oxidação (Nox) dos átomos presentes em uma molécula. De forma geral: Substância orgânica (redutora)
Tratamento de Água/Água Residual. Professora Elizabeth Duarte
 Tratamento de Água/Água Residual Professora Elizabeth Duarte 2012/2013 2015-2016 Química Ambiental Índice 1. Introdução 1.1 Considerações gerais 1.2 Processos de oxidação avançados 1.3 Mecanismos de reacção
Tratamento de Água/Água Residual Professora Elizabeth Duarte 2012/2013 2015-2016 Química Ambiental Índice 1. Introdução 1.1 Considerações gerais 1.2 Processos de oxidação avançados 1.3 Mecanismos de reacção
RESUMO DOS RESULTADOS DA AMOSTRA N / Processo Comercial N 28837/2013-1
 RESUMO DOS RESULTADOS DA AMOSTRA N 301129/2013-0 Processo Comercial N 28837/2013-1 DADOS REFERENTES AO CLIENTE Empresa solicitante: Universidade de São Paulo Endereço: Avenida Arlindo Bettio, 1000 - -
RESUMO DOS RESULTADOS DA AMOSTRA N 301129/2013-0 Processo Comercial N 28837/2013-1 DADOS REFERENTES AO CLIENTE Empresa solicitante: Universidade de São Paulo Endereço: Avenida Arlindo Bettio, 1000 - -
Combustíveis e Redutores ENERGIA PARA METALURGIA
 Combustíveis e Redutores ENERGIA PARA METALURGIA Energia para Metalurgia Principal fonte energética: Carbono Carvão mineral e carvão vegetal C + O 2 >> CO 2 + energia Portanto, carbono é redutor, usado
Combustíveis e Redutores ENERGIA PARA METALURGIA Energia para Metalurgia Principal fonte energética: Carbono Carvão mineral e carvão vegetal C + O 2 >> CO 2 + energia Portanto, carbono é redutor, usado
Olimpíada Brasileira de Química Fase III (Etapa 1 nacional)
 Page 1 of 5 Olimpíada Brasileira de Química - 2001 Fase III (Etapa 1 nacional) Questão 1 (48 th Chemistry Olympiad - Final National Competition - 2001 - Estonia) Exame aplicado em 01.09.2001 Os compostos
Page 1 of 5 Olimpíada Brasileira de Química - 2001 Fase III (Etapa 1 nacional) Questão 1 (48 th Chemistry Olympiad - Final National Competition - 2001 - Estonia) Exame aplicado em 01.09.2001 Os compostos
ABNT NBR 15847 - Amostragem de água subterrânea em poços de monitoramento - Métodos de purga
 CEET-00:001.68 Comissão de Estudo Especial Temporária de Avaliação da Qualidade do Solo e da Água para Levantamento de Passivo Ambiental e Avaliação de Risco à Saúde Humana ABNT NBR 15847 - Amostragem
CEET-00:001.68 Comissão de Estudo Especial Temporária de Avaliação da Qualidade do Solo e da Água para Levantamento de Passivo Ambiental e Avaliação de Risco à Saúde Humana ABNT NBR 15847 - Amostragem
4 Materiais e métodos
 40 4 Materiais e métodos 4.1. Reagentes O fenol (C 6 H 5 OH) utilizado foi fornecido pela Merck, com pureza de 99,8%. O peróxido de hidrogênio (H 2 O 2 ) 50% P/V foi fornecido pela Peróxidos do Brasil
40 4 Materiais e métodos 4.1. Reagentes O fenol (C 6 H 5 OH) utilizado foi fornecido pela Merck, com pureza de 99,8%. O peróxido de hidrogênio (H 2 O 2 ) 50% P/V foi fornecido pela Peróxidos do Brasil
Colégio Avanço de Ensino Programado
 α Colégio Avanço de Ensino Programado Trabalho Bimestral 1º Semestre - 1º Bim. /2016 Nota: Professor (a): Cintia Disciplina: Química Turma: 3ª Série Médio Nome: Nº: Atividade deverá ser entregue em pasta
α Colégio Avanço de Ensino Programado Trabalho Bimestral 1º Semestre - 1º Bim. /2016 Nota: Professor (a): Cintia Disciplina: Química Turma: 3ª Série Médio Nome: Nº: Atividade deverá ser entregue em pasta
QUÍMICA GERAL Soluções
 QUÍMICA GERAL Prof. Dr. Anselmo E. de Oliveira Instituto de Química, UFG anselmo.quimica.ufg.br anselmo.disciplinas@gmail.com 2 de Abril de 2018 Engenharia Ambiental e Sanitária QUÍMICA GERAL 1 Pressão
QUÍMICA GERAL Prof. Dr. Anselmo E. de Oliveira Instituto de Química, UFG anselmo.quimica.ufg.br anselmo.disciplinas@gmail.com 2 de Abril de 2018 Engenharia Ambiental e Sanitária QUÍMICA GERAL 1 Pressão
Diluição de soluções
 COLÉGIO ESTADUAL DA POLÍCIA MILITAR DE GOIÁS HUGO DE CARVALHO RAMOS ANO LETIVO 2018 3º BIMESTRE ATIVIDADE COMPLEMENTAR Série Turma (s) Turno 2º do Ensino Médio A B C D E F G H I MATUTINO Professor: CHARLYS
COLÉGIO ESTADUAL DA POLÍCIA MILITAR DE GOIÁS HUGO DE CARVALHO RAMOS ANO LETIVO 2018 3º BIMESTRE ATIVIDADE COMPLEMENTAR Série Turma (s) Turno 2º do Ensino Médio A B C D E F G H I MATUTINO Professor: CHARLYS
P1 - PROVA DE QUÍMICA GERAL 09/09/11
 P1 - PROVA DE QUÍMICA GERAL 09/09/11 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Dados R = 0,081 atm L -1 K -1 T (K) = T ( C) + 73,15
P1 - PROVA DE QUÍMICA GERAL 09/09/11 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Dados R = 0,081 atm L -1 K -1 T (K) = T ( C) + 73,15
Remediação de solos in situ usando POA: ensaios preliminares de tratabilidade
 Remediação de solos in situ usando POA: ensaios preliminares de tratabilidade Wilson F. Jardim Laboratório de Química Ambiental - LQA Instituto de Química - UNICAMP http://lqa.iqm.unicamp.br wfjardim@iqm.unicamp.br
Remediação de solos in situ usando POA: ensaios preliminares de tratabilidade Wilson F. Jardim Laboratório de Química Ambiental - LQA Instituto de Química - UNICAMP http://lqa.iqm.unicamp.br wfjardim@iqm.unicamp.br
Introdução à Biorremediação. Michaye McMaster Geosyntec Consultants
 Introdução à Biorremediação Michaye McMaster Geosyntec Consultants mmcmaster@geosyntec.com Ms. Michaye McMaster Michaye has more than 18 years of experience in managing and leading complex contaminant
Introdução à Biorremediação Michaye McMaster Geosyntec Consultants mmcmaster@geosyntec.com Ms. Michaye McMaster Michaye has more than 18 years of experience in managing and leading complex contaminant
QUÍMICA PRIMEIRA ETAPA
 QUÍMICA PRIMEIRA ETAPA - 1998 QUESTÃO 01 Uma mistura de hidrogênio, H 2 (g), e oxigênio, O 2 (g), reage, num recipiente hermeticamente fechado, em alta temperatura e em presença de um catalisador, produzindo
QUÍMICA PRIMEIRA ETAPA - 1998 QUESTÃO 01 Uma mistura de hidrogênio, H 2 (g), e oxigênio, O 2 (g), reage, num recipiente hermeticamente fechado, em alta temperatura e em presença de um catalisador, produzindo
2º trimestre Sala de Estudo Química Data: 29/05/17 Ensino Médio 2º ano classe: A_B_C Profª Danusa Nome: nº
 º trimestre Sala de Estudo Química Data: 9/05/17 Ensino Médio º ano classe: A_B_C Profª Danusa Nome: nº Conteúdo: Termoquímica (Energia de ligação e Lei de Hess) Questão 01 - (FUVEST SP/017) Sob certas
º trimestre Sala de Estudo Química Data: 9/05/17 Ensino Médio º ano classe: A_B_C Profª Danusa Nome: nº Conteúdo: Termoquímica (Energia de ligação e Lei de Hess) Questão 01 - (FUVEST SP/017) Sob certas
QUÍMICA. a) linha horizontal. b) órbita. c) família. d) série. e) camada de valência.
 13 QUÍMICA A posição dos elementos na Tabela Periódica permite prever as fórmulas das substâncias que contêm esses elementos e os tipos de ligação apropriados a essas substâncias. Na Tabela Periódica atual,
13 QUÍMICA A posição dos elementos na Tabela Periódica permite prever as fórmulas das substâncias que contêm esses elementos e os tipos de ligação apropriados a essas substâncias. Na Tabela Periódica atual,
Contaminação do solo e das águas subterrâneas em aeroportos: origem e risco potencial
 Contaminação do solo e das águas subterrâneas em aeroportos: origem e risco potencial Nunes L. M. Faculdade de Ciências e Tecnologia Universidade do Algarve lnunes@ualg.pt 9º Seminário sobre águas subterrâneas
Contaminação do solo e das águas subterrâneas em aeroportos: origem e risco potencial Nunes L. M. Faculdade de Ciências e Tecnologia Universidade do Algarve lnunes@ualg.pt 9º Seminário sobre águas subterrâneas
DETERMINAÇÃO DE ALGUNS PARÂMETROS CINÉTICOS DA REAÇÃO DE DECOMPOSIÇÃO DO PERÓXIDO DE HIDROGÊNIO.
 DETERMINAÇÃO DE ALGUNS PARÂMETROS CINÉTICOS DA REAÇÃO DE DECOMPOSIÇÃO DO PERÓXIDO DE HIDROGÊNIO. Glauber Silva Godoi Aula 13 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros
DETERMINAÇÃO DE ALGUNS PARÂMETROS CINÉTICOS DA REAÇÃO DE DECOMPOSIÇÃO DO PERÓXIDO DE HIDROGÊNIO. Glauber Silva Godoi Aula 13 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros
Errata da Tese de Doutorado
 UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA Uso do Reagente de Fenton como Oxidante Secundário em Sistemas de Destruíção de Resíduos Através de Oxidação Térmica. Carlos Augusto Blasques Tooge Errata
UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA Uso do Reagente de Fenton como Oxidante Secundário em Sistemas de Destruíção de Resíduos Através de Oxidação Térmica. Carlos Augusto Blasques Tooge Errata
ESCOPO DA ACREDITAÇÃO ABNT NBR ISO/IEC 17025 ENSAIO. Determinação de Alumínio Total pelo método colorimétrico LQ: 0,008 mg/l
 ESCOPO DA ACREDITAÇÃO ABNT NBR ISO/IEC 17025 ENSAIO Norma de Origem: NIT-DICLA-016 Folha: 1 Total de Folhas: 8 RAZÃO SOCIAL/DESIGNAÇÃO DO LABORATÓRIO ACQUA BOOM SANEAMENTO AMBIENTAL LTDA - EPP Determinação
ESCOPO DA ACREDITAÇÃO ABNT NBR ISO/IEC 17025 ENSAIO Norma de Origem: NIT-DICLA-016 Folha: 1 Total de Folhas: 8 RAZÃO SOCIAL/DESIGNAÇÃO DO LABORATÓRIO ACQUA BOOM SANEAMENTO AMBIENTAL LTDA - EPP Determinação
Questão 32. Questão 31. Questão 33. alternativa D. alternativa D
 Texto para as questões 31 e 32. Um sinal de que o bico do queimador do fogão está entupido é o aparecimento de chama amarela, quando o fogo é aceso. Nessa situação, ocorre a formação de carbono finamente
Texto para as questões 31 e 32. Um sinal de que o bico do queimador do fogão está entupido é o aparecimento de chama amarela, quando o fogo é aceso. Nessa situação, ocorre a formação de carbono finamente
Termoquímica e Soluções
 Ensino Médio QUÍMICA Data: / /01 Atividade : Exercícios de Recuperação Paralela e Anual aula Nome : n o Classe: MB Termoquímica e Soluções 1. (Upf) Para a completa neutralização do ácido acético (ácido
Ensino Médio QUÍMICA Data: / /01 Atividade : Exercícios de Recuperação Paralela e Anual aula Nome : n o Classe: MB Termoquímica e Soluções 1. (Upf) Para a completa neutralização do ácido acético (ácido
CQ136 Química Experimental I
 CQ136 Química Experimental I DIAGRAMAS DE POURBAIX, LATIMER, E FROST Introdução O poder oxidante ou redutor pode ser muitas vezes previsto pelos valores tabelados de potencial padrão (E 0 ), porém somente
CQ136 Química Experimental I DIAGRAMAS DE POURBAIX, LATIMER, E FROST Introdução O poder oxidante ou redutor pode ser muitas vezes previsto pelos valores tabelados de potencial padrão (E 0 ), porém somente
1. A fermentação é um processo químico complexo do fabrico de vinho no qual a glucose é convertida em etanol e dióxido de carbono:
 EB: QUÍMICA GERAL/ EQB: QUÍMICA GERAL I Capítulo 4. Reacções químicas II Ficha de exercícios 1. A fermentação é um processo químico complexo do fabrico de vinho no qual a glucose é convertida em etanol
EB: QUÍMICA GERAL/ EQB: QUÍMICA GERAL I Capítulo 4. Reacções químicas II Ficha de exercícios 1. A fermentação é um processo químico complexo do fabrico de vinho no qual a glucose é convertida em etanol
Fe 3+ (aq) + H 2 O + hv Fe 2+ (aq) HO H + Reação 2
 Tratamento de Efluente Industrial com Peróxido de Hidrogênio Ativado por Radiação Solar Pesquisa desenvolvida em conjunto e em apoio à dissertação se mestrado de Bruno García Leiva (Julho 2016) Aluna:
Tratamento de Efluente Industrial com Peróxido de Hidrogênio Ativado por Radiação Solar Pesquisa desenvolvida em conjunto e em apoio à dissertação se mestrado de Bruno García Leiva (Julho 2016) Aluna:
QUÍMICA. em 100mL dessa solução.
 QUÍMICA 36. Essa questão trata sobre soluções aquosas e as diferentes formas de expressar suas concentrações. Trata ainda de suas propriedades e das reações que podem ocorrer entre elas. 0 0 A concentração
QUÍMICA 36. Essa questão trata sobre soluções aquosas e as diferentes formas de expressar suas concentrações. Trata ainda de suas propriedades e das reações que podem ocorrer entre elas. 0 0 A concentração
Texto para as questões 31 e 32.
 QUÍMICA Texto para as questões 31 e 32. Um sinal de que o bico do queimador do fogão está entupido é o aparecimento de chama amarela, quando o fogo é aceso. Nessa situação, ocorre a formação de carbono
QUÍMICA Texto para as questões 31 e 32. Um sinal de que o bico do queimador do fogão está entupido é o aparecimento de chama amarela, quando o fogo é aceso. Nessa situação, ocorre a formação de carbono
Após agitação, mantendo-se a temperatura a 20ºC, coexistirão solução saturada e fase sólida no(s) tubo(s)
 01) (Covest-2006) Uma solução composta por duas colheres de sopa de açúcar (34,2g) e uma colher de sopa de água (18,0 g) foi preparada. Sabendo que: MMsacarose = 342,0g mol -1, MMágua = 18,0 g mol -1,
01) (Covest-2006) Uma solução composta por duas colheres de sopa de açúcar (34,2g) e uma colher de sopa de água (18,0 g) foi preparada. Sabendo que: MMsacarose = 342,0g mol -1, MMágua = 18,0 g mol -1,
AVALIAÇÃO DA EFICIÊNCIA DE BARREIRA REATIVA INSTALADA EM ESCALA PILOTO PARA DEGRADAÇÃO ABIÓTICA DE SOLVENTES ORGANOCLORADOS
 Flávio Augusto Ferlini Salles e Uriel Duarte AVALIAÇÃO DA EFICIÊNCIA DE BARREIRA REATIVA INSTALADA EM ESCALA PILOTO PARA DEGRADAÇÃO ABIÓTICA DE SOLVENTES ORGANOCLORADOS Flávio Augusto Ferlini Salles e
Flávio Augusto Ferlini Salles e Uriel Duarte AVALIAÇÃO DA EFICIÊNCIA DE BARREIRA REATIVA INSTALADA EM ESCALA PILOTO PARA DEGRADAÇÃO ABIÓTICA DE SOLVENTES ORGANOCLORADOS Flávio Augusto Ferlini Salles e
LISTA DE EXERCÍCIOS 12
 UNIVERSIDADE DE SÃO PAULO ESCOLA SUPERIOR DE AGRICULTURA LUIZ DE QUEIROZ DEPARTAMENTO DE CIÊNCIAS EXATAS LCE 151 FUNDAMENTOS DE QUÍMICA INORGÂNICA E ANALÍTICA LISTA DE EXERCÍCIOS 12 1. A partir de uma
UNIVERSIDADE DE SÃO PAULO ESCOLA SUPERIOR DE AGRICULTURA LUIZ DE QUEIROZ DEPARTAMENTO DE CIÊNCIAS EXATAS LCE 151 FUNDAMENTOS DE QUÍMICA INORGÂNICA E ANALÍTICA LISTA DE EXERCÍCIOS 12 1. A partir de uma
Questão 76. Questão 78. Questão 77. alternativa D. alternativa C. alternativa A
 Questão 76 O hidrogênio natural é encontrado na forma de três isótopos de números de massa, 1, 2 e 3, respectivamente: 1 1 H, 2 1 H e 3 1 H As tabelas periódicas trazem o valor 1,008 para a sua massa atômica,
Questão 76 O hidrogênio natural é encontrado na forma de três isótopos de números de massa, 1, 2 e 3, respectivamente: 1 1 H, 2 1 H e 3 1 H As tabelas periódicas trazem o valor 1,008 para a sua massa atômica,
PROVA DE QUÍMICA 44 PROVA DE QUÍMICA
 44 QUESTÃO 46 1 Uma certa quantidade de água é colocada em um congelador, cuja temperatura é de 20 o C. Após estar formado e em equilíbrio térmico com o congelador, o gelo é transferido para outro congelador,
44 QUESTÃO 46 1 Uma certa quantidade de água é colocada em um congelador, cuja temperatura é de 20 o C. Após estar formado e em equilíbrio térmico com o congelador, o gelo é transferido para outro congelador,
Tratamento e descarte de Resíduos Químicos dos laboratórios da Unipampa Itaqui
 Unipampa 1 OBJETIVO Fornecer informações acerca do armazenamento, tratamento e descarte final dos resíduos químicos gerados nas fontes gerados do campus. 2 APLICAÇÃO Procedimento operacional de estocagem
Unipampa 1 OBJETIVO Fornecer informações acerca do armazenamento, tratamento e descarte final dos resíduos químicos gerados nas fontes gerados do campus. 2 APLICAÇÃO Procedimento operacional de estocagem
AULA 12 PRECIPITAÇÃO FRACIONADA E TRANSFORMAÇÕES METATÉTICAS
 Fundamentos de Química Analítica (009) AULA 1 PRECIPITAÇÃO FRACIONADA E TRANSFORMAÇÕES METATÉTICAS OBJETIVOS Definir precipitação fracionada. Determinar as condições para ocorrer a precipitação fracionada.
Fundamentos de Química Analítica (009) AULA 1 PRECIPITAÇÃO FRACIONADA E TRANSFORMAÇÕES METATÉTICAS OBJETIVOS Definir precipitação fracionada. Determinar as condições para ocorrer a precipitação fracionada.
BioSoil Group & BioSoil Brasil. Eng. Sérgio Veríssimo Filho
 BioSoil Group & BioSoil Brasil Eng. Sérgio Veríssimo Filho BioSoil B.V. Empreiteira Ambiental Desde 1993; Multinacional; Especialista em remediações In situ / on; Tratamento de efluentes Inovação & Conhecimento
BioSoil Group & BioSoil Brasil Eng. Sérgio Veríssimo Filho BioSoil B.V. Empreiteira Ambiental Desde 1993; Multinacional; Especialista em remediações In situ / on; Tratamento de efluentes Inovação & Conhecimento
Equilíbrio de Precipitação
 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina Química das Soluções QUI084 I semestre 2017 AULA 05 Equilíbrio de Precipitação Profa. Maria Auxiliadora
Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina Química das Soluções QUI084 I semestre 2017 AULA 05 Equilíbrio de Precipitação Profa. Maria Auxiliadora
AULA 10 EQUILÍBRIO DE SOLUBILIDADE
 Fundamentos de Química Analítica (009) AULA 10 EQUILÍBRIO DE SOLUBILIDADE OBJETIVOS Definir solubilidade do soluto. Definir solução saturada, não saturada e supersaturada. Conhecer as regras de solubilidade.
Fundamentos de Química Analítica (009) AULA 10 EQUILÍBRIO DE SOLUBILIDADE OBJETIVOS Definir solubilidade do soluto. Definir solução saturada, não saturada e supersaturada. Conhecer as regras de solubilidade.
QUÍMICA Exercícios de revisão resolvidos
 9. (ENEM 2013) A produção de aço envolve o aquecimento do minério de ferro, junto com carvão (carbono) e ar atmosférico em uma série de reações de oxirredução. O produto é chamado de ferro-gusa e contém
9. (ENEM 2013) A produção de aço envolve o aquecimento do minério de ferro, junto com carvão (carbono) e ar atmosférico em uma série de reações de oxirredução. O produto é chamado de ferro-gusa e contém
Energia para Metalurgia
 Energia para Metalurgia Energia para Metalurgia Principal fonte energética: Carbono Carvão mineral e carvão vegetal C + O 2 CO 2 + energia Carbono é combustível, usado para gerar energia reagindo com oxigênio
Energia para Metalurgia Energia para Metalurgia Principal fonte energética: Carbono Carvão mineral e carvão vegetal C + O 2 CO 2 + energia Carbono é combustível, usado para gerar energia reagindo com oxigênio
Processos Oxidativos Avançados (POA s)
 Processos Oxidativos Avançados (POA s) Nomes: Arthur Barra Pâmmella Ribeiro Professor: Dr. Rafael Arromba de Sousa Sumário 2 Contextualização; Introdução; Classes; Literatura; Conclusões; Referências.
Processos Oxidativos Avançados (POA s) Nomes: Arthur Barra Pâmmella Ribeiro Professor: Dr. Rafael Arromba de Sousa Sumário 2 Contextualização; Introdução; Classes; Literatura; Conclusões; Referências.
Revisão Específicas. Química Monitores: Luciana Lima e Rafael França 16-21/11/2015. Material de Apoio para Monitoria
 Revisão Específicas 1. (Ufpr) Considere as soluções I, II e III, descritas a seguir. I - Solução obtida pela adição de 9,80 g de H2SO4 (massa molar = 98,0 g) em água suficiente para completar o volume
Revisão Específicas 1. (Ufpr) Considere as soluções I, II e III, descritas a seguir. I - Solução obtida pela adição de 9,80 g de H2SO4 (massa molar = 98,0 g) em água suficiente para completar o volume
INTERFACE SÓLIDO - LÍQUIDO
 INTERFACE SÓLIDO - LÍQUIDO ADSORÇÃO DE LÍQUIDOS EM SUPERFÍCIES SÓLIDAS Física Aplicada 2017/18 MICF FFUP 1 ADSORÇÃO DE LÍQUIDOS NA SUPERFÍCIE DE UM SÓLIDO Na interface sólido-líquido as moléculas têm tendência
INTERFACE SÓLIDO - LÍQUIDO ADSORÇÃO DE LÍQUIDOS EM SUPERFÍCIES SÓLIDAS Física Aplicada 2017/18 MICF FFUP 1 ADSORÇÃO DE LÍQUIDOS NA SUPERFÍCIE DE UM SÓLIDO Na interface sólido-líquido as moléculas têm tendência
RELATÓRIO DE MONITORAMENTO ANALÍTICO DA ÁGUA SUBTERRÂNEA OUTUBRO/2011 MA/11925/12/BLS
 RELATÓRIO DE MONITORAMENTO ANALÍTICO DA ÁGUA SUBTERRÂNEA OUTUBRO/2011 MA/11925/12/BLS UNIPAC EMBALAGENS LTDA. (Rua Arnaldo Magniccaro, 521 São Paulo SP) Servmar Serviços Técnicos Ambientais Ltda. São Paulo,
RELATÓRIO DE MONITORAMENTO ANALÍTICO DA ÁGUA SUBTERRÂNEA OUTUBRO/2011 MA/11925/12/BLS UNIPAC EMBALAGENS LTDA. (Rua Arnaldo Magniccaro, 521 São Paulo SP) Servmar Serviços Técnicos Ambientais Ltda. São Paulo,
Reações Químicas. Principais Tipos de Reações. Reações de combinação e decomposição. Combustão ao ar. Combinação. Decomposição
 Reações Químicas Principais Tipos de Reações Reações de síntese ou combinação Combinação Decomposição Reações de análise ou decomposição Reações de deslocamento e de troca Reações de neutralização (ácido-base)
Reações Químicas Principais Tipos de Reações Reações de síntese ou combinação Combinação Decomposição Reações de análise ou decomposição Reações de deslocamento e de troca Reações de neutralização (ácido-base)
QUÍMICA GERAL Soluções
 QUÍMICA GERAL Prof. Dr. Anselmo E. de Oliveira Instituto de Química, UFG anselmo.quimica.ufg.br anselmo.disciplinas@gmail.com 8 de Novembro de 2018 Agronomia QUÍMICA GERAL 1 Pressão de vapor A presença
QUÍMICA GERAL Prof. Dr. Anselmo E. de Oliveira Instituto de Química, UFG anselmo.quimica.ufg.br anselmo.disciplinas@gmail.com 8 de Novembro de 2018 Agronomia QUÍMICA GERAL 1 Pressão de vapor A presença
Nome: Nº BI: Data - Local Emissão: / / -
 PROVA DE QUÍMICA Nome: Nº BI: Data - Local Emissão: / / - Pergunta / Opção 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 a) b) c) d) PROVA DE QUÍMICA Duração da prova: 60 minutos +
PROVA DE QUÍMICA Nome: Nº BI: Data - Local Emissão: / / - Pergunta / Opção 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 a) b) c) d) PROVA DE QUÍMICA Duração da prova: 60 minutos +
Desenvolvimento de um método
 Desenvolvimento de um método -Espectro: registro de um espectro na região de interesse seleção do comprimento de onda -Fixação de comprimento de onda: monitoramento da absorbância no comprimento de onda
Desenvolvimento de um método -Espectro: registro de um espectro na região de interesse seleção do comprimento de onda -Fixação de comprimento de onda: monitoramento da absorbância no comprimento de onda
Determinação de Compostos Orgânicos Voláteis no Solo e em Sedimentos
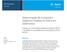 Nota de aplicação Ambiental Determinação de Compostos Orgânicos Voláteis no Solo e em Sedimentos Usando um amostrador headspace Agilent 7697A, o GC 8890 e uma plataforma combinada GC/MSD 5977B Autor Zhang
Nota de aplicação Ambiental Determinação de Compostos Orgânicos Voláteis no Solo e em Sedimentos Usando um amostrador headspace Agilent 7697A, o GC 8890 e uma plataforma combinada GC/MSD 5977B Autor Zhang
Inicialmente a oxidação do metano em altas temperaturas pode ser realizada através da reação: CH 4 + O2 = CH 3 + HO 2 Ou por: CH 4 + M = CH 3 + H + M
 1 1. Introdução O aumento da produção mundial de aço aliada à crescente preocupação com questões ambientais, tem exigido do setor siderúrgico a melhoria dos processos já existentes e o desenvolvimento
1 1. Introdução O aumento da produção mundial de aço aliada à crescente preocupação com questões ambientais, tem exigido do setor siderúrgico a melhoria dos processos já existentes e o desenvolvimento
UNIVERSIDADE ESTADUAL DE PONTA GROSSA COMISSÃO PERMANENTE DE SELEÇÃO 2 o CONCURSO VESTIBULAR DE Questões de Química
 UNIVERSIDADE ESTADUAL DE PONTA GROSSA COMISSÃO PERMANENTE DE SELEÇÃO 2 o CONCURSO VESTIBULAR DE 2011 Questões de Química 01 Sobre o modelo de Rutherford, assinale o que for correto. 01) O átomo não é maciço,
UNIVERSIDADE ESTADUAL DE PONTA GROSSA COMISSÃO PERMANENTE DE SELEÇÃO 2 o CONCURSO VESTIBULAR DE 2011 Questões de Química 01 Sobre o modelo de Rutherford, assinale o que for correto. 01) O átomo não é maciço,
O diagrama abaixo relaciona a solubilidade de dois sais A e B com a temperatura.
 13 PRVA D E Q U Í M I C A Q U E S T Ã 21 diagrama abaixo relaciona a solubilidade de dois sais A e B com a temperatura. Com relação ao diagrama, é INCRRET afirmar que: a) a 100ºC, a solubilidade de B é
13 PRVA D E Q U Í M I C A Q U E S T Ã 21 diagrama abaixo relaciona a solubilidade de dois sais A e B com a temperatura. Com relação ao diagrama, é INCRRET afirmar que: a) a 100ºC, a solubilidade de B é
Como Escolher a Sua Água
 Como Escolher a Sua Água Por que Escolher? Apesar da grande variedade de produtos com alta concentração de sais minerais e sódio, nenhum composto hidrata mais uma pessoa do que a água. Bebê-la não tem
Como Escolher a Sua Água Por que Escolher? Apesar da grande variedade de produtos com alta concentração de sais minerais e sódio, nenhum composto hidrata mais uma pessoa do que a água. Bebê-la não tem
TIPOS DE REAÇÕES QUÍMICAS
 Tipos de Reações químicas 1 TIPOS DE REAÇÕES QUÍMICAS Introdução Várias reações da química inorgânica podem ser classificadas em uma das quatro categorias: combinação, decomposição, deslocamento simples
Tipos de Reações químicas 1 TIPOS DE REAÇÕES QUÍMICAS Introdução Várias reações da química inorgânica podem ser classificadas em uma das quatro categorias: combinação, decomposição, deslocamento simples
QUÍMICA ORGÂNICA. Prof. Jorginho GABARITO SÉRIE AULA - PILHAS 1. C 2. A 3.
 QUÍMICA ORGÂNICA Prof. Jorginho GABARITO SÉRIE AULA - PILHAS 1. C 2. A 3. 2+ Global 2+ Zn(s) + Cu (aq) Zn (aq) + Cu(s) Δ E = + 1,10 V 4. CORRETAS: 01, 02, 08. 5. a) Depósito de cobre: Cu (aq) + 2e Cu(s)
QUÍMICA ORGÂNICA Prof. Jorginho GABARITO SÉRIE AULA - PILHAS 1. C 2. A 3. 2+ Global 2+ Zn(s) + Cu (aq) Zn (aq) + Cu(s) Δ E = + 1,10 V 4. CORRETAS: 01, 02, 08. 5. a) Depósito de cobre: Cu (aq) + 2e Cu(s)
Reações com transferência de elétrons: oxirredução
 Reações com transferência de elétrons: oxirredução Química Geral Prof. Edson Nossol Uberlândia, 09/09/2016 Número de oxidação: número de cargas que um átomo teria em uma molécula (em um composto iônico)
Reações com transferência de elétrons: oxirredução Química Geral Prof. Edson Nossol Uberlândia, 09/09/2016 Número de oxidação: número de cargas que um átomo teria em uma molécula (em um composto iônico)
Controle da população microbiana
 Controle da população microbiana Microbiologia Prof a. Vânia Taxa de Morte Microbiana Quando as populações bacterianas são aquecidas ou tratadas com substâncias químicas antimicrobianas, elas normalmente
Controle da população microbiana Microbiologia Prof a. Vânia Taxa de Morte Microbiana Quando as populações bacterianas são aquecidas ou tratadas com substâncias químicas antimicrobianas, elas normalmente
DEPARTAMENTO DE MEIO AMBIENTE - DMA/FIESP FEDERAÇÃO DAS INDÚSTRIAS DO ESTADO DE SÃO PAULO FIESP
 FEDERAÇÃO DAS INDÚSTRIAS DO ESTADO DE SÃO PAULO FIESP DD 045/2014/E/C/I, de 20 de fevereiro de 2014 MAIO - 2014 Sumário - Base Legal para realização da investigação de áreas contaminadas - Principais alterações
FEDERAÇÃO DAS INDÚSTRIAS DO ESTADO DE SÃO PAULO FIESP DD 045/2014/E/C/I, de 20 de fevereiro de 2014 MAIO - 2014 Sumário - Base Legal para realização da investigação de áreas contaminadas - Principais alterações
PROCESSOS OXIDATIVOS AVANÇADOS
 PROCESSOS OXIDATIVOS AVANÇADOS Disciplina de Química Ambiental Alunos: Hugo Camarano, Nathalia Campos, Pâmela Souza. Professor: Rafael Arromba Estagiário: Felipe Reis INTRODUÇÃO O descarte inapropriado
PROCESSOS OXIDATIVOS AVANÇADOS Disciplina de Química Ambiental Alunos: Hugo Camarano, Nathalia Campos, Pâmela Souza. Professor: Rafael Arromba Estagiário: Felipe Reis INTRODUÇÃO O descarte inapropriado
Tratamento térmico de solos contaminados Unidade de Dessorção Térmica TDU
 Tratamento térmico de solos contaminados Unidade de Dessorção Térmica TDU Desenvolvimento e Inovação Tecnológica Fabiano do Vale de Souza Setembro/2010 Objetivo Dessorção térmica é um processo físico de
Tratamento térmico de solos contaminados Unidade de Dessorção Térmica TDU Desenvolvimento e Inovação Tecnológica Fabiano do Vale de Souza Setembro/2010 Objetivo Dessorção térmica é um processo físico de
Recuperação de Vapores
 Recuperação de Vapores Paulo R. Bittar RECUPERAÇÃO DE VAPORES DURANTE O CARREGAMENTO DE CAMINHÕES-TANQUES RESUMO Combustíveis voláteis como gasolina e etanol, e em menor grau o diesel, apresentam pressão
Recuperação de Vapores Paulo R. Bittar RECUPERAÇÃO DE VAPORES DURANTE O CARREGAMENTO DE CAMINHÕES-TANQUES RESUMO Combustíveis voláteis como gasolina e etanol, e em menor grau o diesel, apresentam pressão
Prova de seleção ao Mestrado e Doutorado em Química Programa de Pós-graduação Multicêntrico em Química de Minas Gerais PPGMQMG Edital 1/2016
 PPGMQMG Edital 1/2016 Orientações gerais Somente identifique sua prova com o número de inscrição (não coloque seu nome); Não é permitida consulta bibliográfica; Realizar a prova com caneta azul ou preta;
PPGMQMG Edital 1/2016 Orientações gerais Somente identifique sua prova com o número de inscrição (não coloque seu nome); Não é permitida consulta bibliográfica; Realizar a prova com caneta azul ou preta;
UTILIZAÇÃO DA REAÇÃO FOTO-FENTON PARA REMEDIAÇÃO DE EFLUENTE FENÓLICO EM REATOR PARABÓLICO
 UTILIZAÇÃO DA REAÇÃO FOTO-FENTON PARA REMEDIAÇÃO DE EFLUENTE FENÓLICO EM REATOR PARABÓLICO José Daladiê Barreto da Costa Filho; Gabriel Henrique Moreira Gomes; Osvaldo Chiavone-Filho Universidade Federal
UTILIZAÇÃO DA REAÇÃO FOTO-FENTON PARA REMEDIAÇÃO DE EFLUENTE FENÓLICO EM REATOR PARABÓLICO José Daladiê Barreto da Costa Filho; Gabriel Henrique Moreira Gomes; Osvaldo Chiavone-Filho Universidade Federal
FUVEST 1981 Primeira fase e Segunda fase
 FUVEST 1981 Primeira fase e Segunda fase CONHECIMENTOS GERAIS 5. Nas condições ambientes, pastilhas de hidróxido de sódio, expostas ao ar durante várias horas, transformam-se em um líquido claro. Este
FUVEST 1981 Primeira fase e Segunda fase CONHECIMENTOS GERAIS 5. Nas condições ambientes, pastilhas de hidróxido de sódio, expostas ao ar durante várias horas, transformam-se em um líquido claro. Este
Química. Energia de formação (KJ mol -1 )
 Química 01. A formação dos compostos iônicos é geralmente um processo exotérmico cuja energia liberada será tanto maior quanto maior for a força de interação entre o cátion e o ânion. gráfico abaixo apresenta
Química 01. A formação dos compostos iônicos é geralmente um processo exotérmico cuja energia liberada será tanto maior quanto maior for a força de interação entre o cátion e o ânion. gráfico abaixo apresenta
TRATAMENTO DE CALDO E A SUA IMPORTÂNCIA. Carlos A. Tambellini
 TRATAMENTO DE CALDO E A SUA IMPORTÂNCIA Carlos A. Tambellini PRÉ TRATAMENTO DE CALDO Limpeza da Cana Peneiramento de Caldo Bruto Regeneração de Calor TRATAMENTO DE CALDO Sulfitação Calagem / Dosagem por
TRATAMENTO DE CALDO E A SUA IMPORTÂNCIA Carlos A. Tambellini PRÉ TRATAMENTO DE CALDO Limpeza da Cana Peneiramento de Caldo Bruto Regeneração de Calor TRATAMENTO DE CALDO Sulfitação Calagem / Dosagem por
ESPECIFICAÇÃO TÉCNICA DO PRODUTO
 Página 1 de 7 Produto: Branqueador óptico de Alta Substantividade para Fibras Celulósicas CAMPOS DE APLICAÇÃO: Fibras celulósicas: Processo por esgotamento; Alvejamento com peróxido, não contínuo; Alvejamento
Página 1 de 7 Produto: Branqueador óptico de Alta Substantividade para Fibras Celulósicas CAMPOS DE APLICAÇÃO: Fibras celulósicas: Processo por esgotamento; Alvejamento com peróxido, não contínuo; Alvejamento
DURAÇÃO DA PROVA: 03 HORAS
 INSTRUÇÕES: PRCESS SELETIV 2013/2 - CPS PRVA DISCURSIVA DE QUÍMICA CURS DE GRADUAÇÃ EM MEDICINA 1. Só abra a prova quando autorizado. 2. Veja se este caderno contém 5 (cinco) questões discursivas. Caso
INSTRUÇÕES: PRCESS SELETIV 2013/2 - CPS PRVA DISCURSIVA DE QUÍMICA CURS DE GRADUAÇÃ EM MEDICINA 1. Só abra a prova quando autorizado. 2. Veja se este caderno contém 5 (cinco) questões discursivas. Caso
