ESPECTROFOTOMETRIA NO ULTRAVIOLETA E VISÍVEL
|
|
|
- Adelino Camilo Azevedo
- 7 Há anos
- Visualizações:
Transcrição
1 ESPECTROFOTOMETRIA NO ULTRAVIOLETA E VISÍVEL Henrique Bergamin Filho т Francisco José Krug Elias Ayres Guidetti Zagatto Fábio Rodrigo Piovezani Rocha т) In memoriam CENTRO DE ENERGIA NUCLEAR NA AGRICULTURA UNIVERSIDADE DE SÃO PAULO 2010
2 1 ESPECTROFOTOMETRIA NO ULTRAVIOLETA E VISÍVEL A espectrofotometria é uma das técnicas analíticas mais utilizadas para determinações quantitativas de espécies químicas, devido à robustez, instrumentação relativamente simples e de baixo custo e ao grande número de aplicações desenvolvidas. Esta técnica se baseia na medida da absorção de radiação eletromagnética nas regiões visível e ultravioleta por espécies químicas (moléculas ou íons) em solução. Na análise quantitativa, a atenuação do feixe de radiação é, dentro de certos limites, proporcional à concentração da espécie química a ser determinada. As espécies químicas de interesse geralmente estão presentes em solução líquida, embora seja também possível medidas em fase sólida ou gasosa. Outros termos, como espectrometria de absorção molecular e espectrofotometria de absorção em solução tem sido também utilizados para designar esta técnica analítica. I. A radiação eletromagnética Muitos experimentos realizados em laboratório são melhor interpretados partindo da idéia de que a radiação se propaga na forma de ondas. Estas ondas são caracterizadas com respeito a algumas propriedades, tais como freqüência, comprimento de onda e número de onda. O comprimento de onda (λ) refere-se à distância entre dos pontos equivalentes de ondas subseqüentes, por exemplo, duas cristas adjacentes, conforme ilustrado na Figura 1. O recíproco do comprimento de onda é denominado número de onda ν. Outra característica importante de uma onda eletromagnética é a sua frequência (ν), ou seja, o número de unidades completas de comprimentos de onda que passam por um ponto fixo por unidade de tempo. Isto decorre do fato de a onda se propagar a uma velocidade constante. Comprimento de onda, número de onda e frequência estão relacionadas com a velocidade da luz no vácuo (c, cerca de 3x10 12 m s -1 ), conforme as expressões:
3 2 1 ν = (1) e λ c ν = (2) λ Figura 1. Ilustração de uma onda eletromagnética plano-polarizada: E = campo elétrico; H = campo magnético; λ = comprimento de onda. A teoria ondulatória da radiação eletromagnética explica muitos fenômenos óticos, tais como a reflexão, a refração e a difração. No entanto, em alguns casos é conveniente considerar que a radiação é constituída de partículas portadoras de energia chamadas fótons. Assim, torna-se útil pensar no feixe de luz como sendo constituído por um conjunto de fótons. Cada fóton possui uma energia (E) característica, que está relacionada à frequência da radiação pelas equações: E = hν (3) E = hc/λ (4) onde h =constante de Planck (6,624x10-27 J.s). Dessa forma, a cada comprimento de onda está associado uma quantidade definida de energia. A intensidade de um feixe de radiação é proporcional ao número
4 3 de fótons e independe da energia de cada fóton. Considerando o modelo ondulatório, a intensidade o feixe é proporcional ao módulo dos vetores indicados na Figura 1. A absorção de radiação tem como consequência a diminuição do número de fótons e da amplitude das ondas que constituem a radiação eletromagnética. Em outras palavras, a absorção de radiação não altera a energia do feixe e, consequentemente, o comprimento de onda da radiação incidente. II. O espectro eletromagnético As radiações de interesse para a humanidade variam desde aquelas de altíssima energia (raios gama) até aquelas de baixa energia (ondas de rádio). Dá-se o nome de espectro eletromagnético ao conjunto de radiações eletromagnéticas divididas em função do comprimento de onda ou (energia), as quais recebem as denominações indicadas na Figura 2. A região relativamente estreita do espectro cujas radiações são perceptíveis pelo olho humano é chamada de região visível. Dependendo da região do espectro eletromagnético considerada, diferentes unidades são empregadas para caracterizar as radiações. Para as regiões do visível (Vis) e ultravioleta (UV), o comprimento de onda é geralmente expresso em nanômetros (nm). Figura 2. Representação parcial do espectro eletromagnético.
5 4 III. A absorção da radiação Quando um feixe atravessa a camada de um sólido, líquido ou gás, radiações de certas frequências podem ser seletivamente absorvidas. Neste processo de absorção, a energia é transferida aos átomos, moléculas ou íons presentes na amostra. Como resultado, as espécies passam de um estado de baixa energia para estados mais energéticos (estado excitado). O estado de energia mais baixa é denominado estado fundamental. As conseqüências da absorção de radiação por espécies químicas dependem da quantidade de energia absorvida e, portanto, do comprimento de onda da radiação. Sendo a energia E inversamente proporcional ao comprimento de onda, radiações com menores λ provocam alterações mais significativas nas espécies absorventes (eq. 4). Enquanto os raios γ são suficientemente energéticos para promover alterações nos núcleos atômicos, radiações na região das micro-ondas, com comprimentos de onda muito maiores, alteram somente o estado rotacional das moléculas. Radiações eletromagnéticas das regiões UV-Vis apresentam comprimentos de onda com dimensões comparáveis às de vírus e bactérias ( nm). Estes comprimentos de onda correspondem a energias suficientes para promover rotação, vibração e transições eletrônicas em espécies absorventes. Somente radiações ultravioleta com λ < 250 nm são suficientemente energéticas para quebrar ligações químicas. Em espectrometria UV-Vis, somente radiações com λ > 200 nm encontram aplicações práticas, visto que radiação com comprimentos de onda menores pode ser absorvida pela água ou por outras espécies presentes no ar. Desta forma, espectrômetros para medidas abaixo de 200 nm requerem sistemas ópticos purgados para a remoção destas espécies absorventes. Moléculas e íons são caracterizados por um número muito grande de níveis energéticos que decorrem das variações em suas energias eletrônicas, vibracionais e rotacionais. A Figura 3 é uma representação esquemática de alguns dos níveis de energia eletrônicos, vibracionais e rotacionais, onde pode se observar que cada nível eletrônico apresenta diversos estados vibracionais e rotacionais. Observa-se que a diferença de energia entre os níveis eletrônicos é muito maior do que aquela entre os estados vibracionais de um mesmo nível eletrônico e
6 5 que a diferença entre os estados vibracionais é significativamente maior do que aquela entre os estados rotacionais. Assim, para cada nível eletrônico de uma molécula há, também, superposições entre os estados vibracional e rotacional. Uma dada transição eletrônica pode também envolver mudanças vibracionais e rotacionais, o que permite a absorção de fótons de uma faixa de energias, caracterizando uma banda (espectro de absorção contínuo). Em um espectro contínuo de absorção, o comprimento de onda de máxima absorção corresponde à transição mais provável. E 2 v 23 v 22 v 21 r 134 r 133 r 132 v 13 r 131 v 12 v 11 E 1 v 03 v 02 v 01 E 0 Figura 3. Diagrama de níveis de energia para uma molécula. Os níveis E o, E 1 e E 2 referem-se a três níveis eletrônicos, cada um deles com três níveis vibracionais (e.g. v 01 a v 03 para o nível E o ); os níveis rotacionais r 131 a r 134 estão associados ao nível vibracional v 13. São mostradas apenas as transições eletrônicas a partir do estado fundamental (E 0 ). Na prática, os níveis de energia não são equidistantes.
7 6 A absorção de radiação na região visível do espectro eletromagnético é responsável pela coloração das soluções. Utilizando-se o conceito de cores complementares, é possível deduzir a região do espectro na qual ocorre absorção de radiação. Por exemplo, uma solução que absorve radiação na região correspondente ao verde ( nm) apresentará coloração vermelha, que corresponde à combinação das cores transmitidas (i.e. não absorvidas) pela solução. Na prática, a região espectral na qual ocorre absorção de radiação é determinada a partir de um espectro de absorção. Este espectro consiste em um gráfico, que correlaciona um parâmetro proporcional à quantidade de radiação absorvida (absorbância, transmitância ou absortividade molar), com o comprimento de onda da radiação incidente. Geralmente utilizam-se medidas de absorbância (vide p.12). Tomando-se por base apenas algumas transições eletrônicas, semelhante às mostradas na Figura 3, hipoteticamente poder-se-ia obter o espectro da Figura 4a. Entretanto, devido ao grande número de transições, às pequenas diferenças de energia entre as transições e a resolução espectral dos espectrômetros existentes, observa-se na prática um espectro contínuo (Figura 4b). a) b) Absorbância Absorbância comprimento de onda / λ comprimento de onda / λ Figura 4. Representação de espectros de absorção na região do visível mostrando a) valores hipotéticos para as transições eletrônicas e b) espectro contínuo obtido na prática.
8 7 A partir dos espectros de absorção, é possível deduzir as transições eletrônicas possíveis e, consequentemente, obter informações que subsidiam a identificação de estruturas moleculares com informações obtidas por outras técnicas. Espectros de absorção também permitem identificar os comprimentos de onda de máxima absorção. Medidas de absorção nestes comprimentos de onda levam à maior atenuação do feixe de radiação e, portanto, à maior sensibilidade analítica. Espectros de absorção da espécie de interesse e de espécies concomitantes permitem conclusões relativas à seletividade das medidas (avaliação de possíveis interferências espectrais). A maioria das espécies orgânicas, contendo duplas e triplas ligações, absorve radiação na região ultravioleta do espectro eletromagnético. A Figura 5 mostra um espectro típico de absorção de benzeno em etanol ilustrando estas considerações. Absorbância Comprimento de onda / nm Figura 5. Espectro de absorção do benzeno em etanol. Com referência à absorção de radiação visível e ultravioleta por átomos gasosos, caso particular da espectrometria de absorção atômica, deve-se ressaltar que as transições eletrônicas envolvem um número relativamente limitado de níveis de energia. Assim, a absorção da radiação eletromagnética por um átomo pode ocorrer somente se o fóton incidente possuir energia exatamente correspondente à
9 8 diferença de energia entre dois níveis energéticos. Neste caso, um espectro de absorção discreto (formado por linhas e não bandas) é observado. A espectrometria de absorção atômica será abordada em outro texto. IV. Lei de Beer Quando um feixe de radiação de comprimento de onda definido (i.e. de energia apropriada) e de intensidade I o incide sobre uma amostra (Figura 6), uma parte desta energia é absorvida (I a ), uma parte é transmitida (I t ) e outra é refletida ou espalhada (I r ), de forma que: I o = I a + I t + I r (5) Feixe incidente I o I t Feixe transmitido Fluido b Figura 6. Cubeta com solução absorvente: I o e I t correspondem às intensidades de radiação incidente e emergente (transmitida), b é a largura interna da cubeta (caminho óptico) e o fluido contem teor c da espécie absorvente. Sob o ponto de vista de instrumental, I r pode ser mantido constante (ou mesmo compensado) fixando-se as condições de medida (e.g. usando celas semelhantes para as medidas na presença e ausência de absorção) e evitando a presença de sólidos em suspensão que poderiam causar espalhamento de radiação). Nestas condições, a absorção da radiação dependerá do caminho percorrido no meio absorvente (caminho óptico) e da concentração da espécie, ou seja, do número total de espécies absorventes que interagem com o feixe de
10 9 radiação. O resultado destas observações foi expresso por uma equação relacionando a absorção da radiação com a concentração da espécie absorvente (c) e com o caminho ótico da cela de medida (b): A I I o = abc = log (6) t onde: A = absorbância (ou absorvância) a = absortividade Esta equação representa a expressão mais usual da Lei de Beer, a qual se constitui na base para aplicações quantitativas da espectrofotometria. A razão I t /I o denota a fração da radiação transmitida, a qual é denominada transmitância (T). As seguintes relações podem ser utilizadas: A = -log T = log T 1 = abc (7) Quando a concentração do analito é expressa em mol l -1, a constante a é denominado absortividade molar (ε). Esta constante é característica de cada espécie química e é sempre referida a um determinado comprimento de onda, geralmente o de maior absorção (λ max ). Consistentemente com a equação 7, a absortividade molar é expressa em l mol -1 cm -1. De um modo geral, métodos com boa sensibilidade são aqueles envolvendo absortividades molares maiores do que 10 4 l mol -1 cm -1. Na prática, a absortividade pode ser empregada para se estimar a mínima concentração detectável de uma espécie química, fornecidos o caminho ótico (b) e a menor absorbância mensurável. Assim, supondo um equipamento com boa estabilidade, o menor valor mensurável de absorbância diferente de 0,000 é de 0,001. Por exemplo, empregando-se o método de determinação de ferro com 1,10 fenantrolina (ε = 1,1x10 4 l mol -1 cm -1 a 512 nm) em espectrofotômetro com
11 10 cubeta com b = 1,0 cm, a concentração mínima detectável de ferro, C min, pode ser calculada: A,001 8 Cmin = = = 9,1.10 mol / 4 bc 1, Fe Esta concentração pode ser expressa em mg l -1 Fe: C min = 9,1x10-8 mol l -1 x 55,85 g mol -1 = 5,1x10-6 g l -1 Fe ou C min 0,0051 mg l -1 Fe ou 5,1 µg l -1 Fe Evidentemente, este valor mínimo é considerado em ausência de incertezas nas medidas de absorbância e ausência de espécies químicas interferentes, aspectos que serão discutidos oportunamente. A Lei de Beer pode ser aplicada com sucesso somente para descrever o comportamento da absorção de soluções diluídas. Em altas concentrações, a absortividade sofre pequena alteração em função de interações intermoleculares. Em soluções muito concentradas, desvios determinados pela variação da absortividade com o índice de refração da solução também podem ocorrer. Na prática, recomendase a diluição da amostra para superar estes efeitos de forma que a absorbância seja inferior a 1,000 (10% de transmissão), visando minimizar erros associados às medidas instrumentais de It (ver equação 6). Outras limitações à aplicabilidade da Lei de Beer são devidas a características instrumentais e às reações químicas envolvidas. VI. Espectrofotômetros Os equipamentos para medidas espectrofotométricas são denominados espectrofotômetros e várias configurações são disponíveis comercialmente. Apesar do uso coloquial, a IUPAC não recomenda o uso do termo colorímetro. Em alguns casos, a baixa resolução espectral muda o nome de espectrofotometria para fotometria, por exemplo quando filtros são utilizados para a seleção da faixa de
12 11 radiação incidente. A Figura 7 mostra um diagrama de blocos de um espectrofotômetro de feixe único, também denominado de espectrofotômetro simples feixe. fonte de radiação monocromador solução detector amplificador sinal Figura 7. Diagrama de blocos de espectrofotômetro com feixe único. Como o próprio nome indica, espectrofotômetros de feixe único (também denominados de simples feixe) são instrumentos que operam com um único feixe de radiação, o qual vai da fonte ao detector, passando diretamente pelo sistema de seleção de comprimento de onda e pela amostra, ou vice-versa. Os espectrofotômetros de duplo feixe têm seu feixe de radiação original dividido em dois, um dos quais passa pela referência (e.g. cubeta com o solvente) e o outro pela amostra. Existem dois tipos de espectrofotômetros de duplo feixe. Em um tipo, os dois feixes são separados no espaço e simultâneos no tempo; no outro, os feixes são alternados no tempo e quase coincidentes no espaço. Comparativamente aos espectrofotômetros duplo feixe, os espectrofotômetros de feixe único a) são mais simples em construção e, conseqüentemente, de menor custo; b) apresentam maior razão sinal/ ruído e, conseqüentemente, melhor limite de detecção; c) podem apresentar maior instabilidade com o tempo ( drift ) causada por alterações na resposta do detector ou na emissão da fonte;
13 12 Espectrofotômetros duplo feixe (Figura 8) são caracterizados por: a) compensação automática de eventuais variações na intensidade de emissão da fonte; b) obtenção de espectros de maneira bastante simples, por varredura mecânica, envolvendo menor número de operações relativamente aos espectrofotômetros de feixe único. c) menor razão sinal/ruído. Em todos os espectrofotômetros ocorre uma diminuição na intensidade da radiação (I o ) durante o transporte em direção ao detector. Esta diminuição ocorre em cada componente óptico no trajeto (lentes, espelhos, elementos dispersores, fendas). Um feixe pode ser atenuado de 10 a 30% quando é refletido por um simples espelho. Os espectrofotômetros de duplo feixe possuem entre 10 e 15 elementos no trajeto da radiação, ao passo que, em um feixe único, este número varia geralmente de 3 a 6. Conseqüentemente, em um espectrofotômetro de duplo feixe, a intensidade de radiação que incide na amostra é menor do que num feixe único, partindo de uma mesma fonte de radiação. d) exigência de cubetas idênticas (casadas) para amostra e para a referência. motor fonte de radiação monocromador amostra detector amplificador referência sinal Figura 8. Diagrama de blocos de um espectrofotômetro de duplo feixe. Com eletrônica mais moderna, incluindo circuitos de realimentação, flutuações na alimentação da fonte de radiação são desprezíveis. Desta forma, espectrofotômetros de feixe único são equipamentos perfeitamente adequados para as análises quantitativas, quando um único comprimento de onda é utilizado, face à razão sinal/ruído mais favorável. Para a obtenção de espectros de absorção, a
14 13 escolha pode recair ou num equipamento de feixe único multicanal (e.g. espectrofotômetro com arranjo de diodos) ou num duplo feixe tradicional. Fontes de radiação. Idealmente, uma fonte deve ser estável e emitir um feixe de radiação com intensidade suficiente para ser detectável mesmo após sua monocromação e absorção parcial. A sua estabilidade está, em geral, associada à sua fonte de alimentação, a qual é geralmente regulada. Em alguns instrumentos, o problema da instabilidade da fonte é superado dividindo-se o feixe de radiação em dois (equipamentos de duplo feixe). Como fontes de radiação, em geral são empregadas fontes contínuas. Lâmpadas de filamento de tungstênio. Apresentam emissão apreciável na faixa de 320 a 2500 nm, sendo largamente utilizadas para a região visível (400 a 700 nm) e do infravermelho próximo (NIR). Estas lâmpadas consistem de um filamento de tungstênio, que se torna incandescente pela passagem de corrente elétrica (aquecimento resistivo). O filamento é mantido em atmosfera inerte (argônio) dentro de um bulbo de vidro transparente à radiação emitida. O espectro de emissão da lâmpada se assemelha ao espectro de emissão contínua de um corpo negro (lâmpada usualmente opera a temperatura entre C). A elevação da temperatura desloca o máximo de emissão para regiões de menores comprimentos de onda, ou seja, do infra-vermelho próximo para o visível. Desta forma, para evitar flutuações da emissão da fonte, é necessário que o filamento atinja uma temperatura constante, o que justifica ligar a lâmpada no mínimo 10 min antes das medidas. Lâmpadas de tungstênio-halogênio. Contém uma pequena quantidade de iodo dentro do envelope de quartzo onde está também o filamento de tungstênio. Apresenta vida útil superior à lâmpada de tungstênio comum. O iodo adicionado reage com vapor de tungstênio, formando WI 2 que se redeposita sobre o filamento aquecido na forma de tungstênio. Lâmpadas de deutério. A lâmpada de deutério consiste de um invólucro de vidro com uma janela de quartzo (sílica fundida), preenchido com gás deutério (ou hidrogênio) a baixa pressão. Produz um espectro contínuo sendo geralmente usada
15 14 para medidas na região entre 200 e 400 nm. A emissão é produzida por excitação elétrica do gás. A corrente de descarga entre 2 eletrodos excita as moléculas de * deutério formando moléculas excitadas D 2. Estas moléculas se dissociam liberando energia na forma de um contínuo na região UV: A Figura 9 mostra como varia a intensidade de emissão das lâmpadas de deutério e de filamento de tungstênio em função do comprimento de onda. Intensidade deutério tungstênio λ / nm Figura 9. Espectros de emissão de fontes contínuas de deutério e de filamento de tungstênio. Adaptada da referência 7. Outras fontes de radiação usadas em espectrometria UV-Vis são os diodos emissores de luz (LEDs), lâmpadas de xenônio e lasers. Seleção de comprimentos de onda Rigorosamente, a lei de Beer somente é obedecida para feixes de radiação monocromáticos (i.e. feixes de radiação em uma faixa estreita de comprimentos de onda). Como fontes de emissão contínuas são normalmente empregadas, é necessário o emprego de seletores de comprimentos de onda (filtros de absorção ou interferência e monocromadores). O emprego de uma banda mais estreita de
16 15 radiação também tende a melhorar a sensibilidade e a seletividade das medidas espectrofotométricas. O efeito da banda passante na absortividade pode ser melhor compreeendido com auxílio da Figura 10. O ponto de máximo do espectro de absorção corresponde à máxima absortividade pela espécie. Desta forma, quando um feixe de radiação de largura espectral muito pequena (1 1 ) e comprimentos de onda próximos àquele de máxima absorção for utilizado, a absortividade assumirá valor máximo. Se a seleção de comprimentos de onda for feita para bandas passantes maiores, a absorbância medida será a média das absorbâncias relativas aos intervalos de comprimentos de ondas considerados (2 2 e 3 3 ) e, portanto, menor que a absortividade máxima. Absorbância Comprimento de onda Figura 10. Dependência entre absortividade molar e largura espectral (adaptada de Marczenko, 1976) A seleção de comprimentos de onda é geralmente feita com monocromadores, que permitem uma variação contínua de comprimentos de onda. Filtros de absorção (vidro ou polímeros coloridos) ou de interferência (Figura 11) são utilizados em equipamentos mais simples que operam na região visível. Os filtros transmitem radiações com uma largura de banda efetiva geralmente de nm. Os filtros de
17 16 interferência apresentam como vantagens bandas passantes mais estreitas e melhor transmissão de radiação. Transmitância (%) filtro de interferência ~ 10 nm filtro de absorção ~ 50 nm λ / nm Figura 11. Transparência e largura espectral de dois tipos de filtros. Adaptada da referência 7. Monocromadores são constituídos por uma fenda de entrada, um espelho ou lente colimador para produção de feixe paralelo de radiação, um prisma ou uma rede de difração para a dispersão da radiação e um espelho (ou lente) focalizador para projeção das imagens formadas sobre um plano focal onde reside uma fenda de saída. A Figura 12 mostra um tipo de monocromador com rede, bastante utilizado em espectrofotômetros, cuja fenda de entrada é iluminada por uma fonte de radiação contínua. A radiação passa através de fenda de entrada retangular, é colimada pelo espelho côncavo e atinge a superfície da rede de difração. Nesta rede, ocorre uma dispersão angular que promove a separação das radiações de diferentes comprimentos de onda. Finalmente, com auxílio do segundo espelho côncavo, a radiação de comprimento de onda desejado é focalizada diretamente na fenda de saída.
18 17 Espelho côncavo Espelho côncavo Imagem da luz dispersa pela rede antes da fenda de saída Rede de difração Fenda de saída Fenda de entrada Ângulo da rede e fenda de saída determinam o comprimento de onda (banda espectral) na fenda de saída Fonte de radiação Figura 12. Ilustração de um monocromador Czerny-Turner com fonte de radiação iluminando a fenda de entrada, dispersão da radiação por uma rede de difração e seleção do comprimento de onda através da fenda de saída. Recipientes de amostra Recipientes para amostras, usualmente denominados cubetas (Figura 11), são construídos de material transparente à radiação na região espectral de interesse. Suas janelas devem ser perfeitamente normais à direção do feixe incidente, de forma a serem minimizadas as perdas por refração, que são mais pronunciadas em cubetas cilíndricas. Dentre os materiais para sua confecção destacam-se o vidro borossilicato, transparente entre 380 e 2000 nm e o quartzo ou sílica fundida (transparente entre 160 e 3500 nm). Somente cubetas de quartzo são apropriadas
19 18 para medidas na região ultravioleta, enquanto cubetas de quartzo, vidro ou acrílico (descartáveis) podem ser empregadas na região visível. (a) (b) Figura 11. Cubetas retangulares com 10 mm de caminho óptico: (a) convencional e (b) para medidas em fluxo. Detectores de radiação Os primeiros detectores utilizados foram o olho humano e as emulsões fotosensíveis (filmes fotográficos). Nos espectrofotômetros são utilizados transdutores que convertem a energia radiante em sinal elétrico. Idealmente, um detector deve apresentar alta sensibilidade, alta razão sinal/ruído e resposta para uma faixa considerável de comprimentos de onda. Além disto, é fundamental que o tempo de resposta seja bastante curto e que, na ausência de iluminação, o sinal gerado seja o menor possível. O sinal elétrico produzido pelo transdutor deve ser proporcional à intensidade de radiação (I). Assim, se S é a resposta elétrica em termos de corrente, voltagem ou resistência e k é uma constante de calibração, S = k x I. A maioria dos detectores apresenta uma pequena e constante resposta na ausência de radiação a qual é denominada corrente de fundo, ou corrente de escuro, do inglês dark current. Entretanto, a maioria dos equipamentos possui um circuito eletrônico que compensa esta corrente. Em espectrofotômetros UV-Vis são utilizados transdutores que respondem à radiação incidente, os quais são denominados detectores fotoelétricos ou transdutores fotônicos. Estes transdutores têm uma superfície ativa capaz de
20 19 absorver a energia da radiação. Em alguns casos, a absorção da radiação promove a emissão de elétrons produzindo uma fotocorrente. Em outros, a absorção da radiação promove aumento da condutividade, o fenômeno sendo denominado de fotocondução. Existem vários tipos de detectores fotoelétricos: a) Células fotovoltaicas. A energia radiante gera uma corrente elétrica na interface entre uma camada semi-condutora e um metal. Estas células são usadas principalmente na região do visível. b) Válvulas fotoelétricas. A energia radiante provoca emissão de elétrons quando incide em uma superfície sólida de material adequado (efeito fotoelétrico). Estas células são usadas nas regiões UV e visível. c) Válvulas fotomultiplicadoras. A energia radiante causa emissão (ejeção) de elétrons de uma superfície sólida (cátodo semi cilíndrico), também por efeito fotoelétrico. Os elétrons ejetados são acelerados em direção a um eletrodo (dinodo), devido a uma diferença de potencial da ordem de 90 V em relação ao cátodo, removendo outros elétrons que são acelerados para a superfície de um segundo dinodo, e assim sucessivamente, resultando em amplificação em cascata. Tipicamente, 10 7 elétrons são coletados no anodo para cada fóton incidente no catodo. As válvulas fotomultiplicadoras apresentam excelente desempenho em termos de sensibilidade para a região UV-Vis, com resposta muito rápida. d) Fotodiodos de silício. Os fótons aumentam a condutância através de uma junção p-n reversamente polarizada. São usados também nas regiões visível e UV. Os fotodiodos são semi-condutores, normalmente obtidos por dopagem em silício que, quando inversamente polarizados, resultam na separação de cargas elétricas e, consequentemente, em baixa condutividade elétrica na ausência de radiação. A absorção de radiação com energia apropriada promove a formação de elétrons e lacunas, provocando um fluxo de corrente proporcional à intensidade (potência) do feixe de radiação. Existem instrumentos cujo sistema de detecção é constituído por um arranjo (normalmente linear) de diodos (do inglês diode array ) fotossensíveis (Figura 14). Em geral estes dispositivos empregam de 512 a 4096 elementos sensíveis e
21 20 permitem a detecção simultânea de radiações de comprimento de onda na faixa de 200 a 800 nm com resolução ao redor de 1 nm. Neste caso, todos os elementos do espectro são observados simultaneamente, em contraste com os chamados espectrofotômetros de varredura ou monocanais. Espectrômetros portáteis são produzidos comercialmente usando estes arranjos de detectores, inclusive empregando módulos independentes (fonte de radiação, suporte para a cubeta e interface contendo o monocromador e o arranjo de fotodiodos) conectados por fibras ópticas. arranjo de fotodetectores espelho fonte de radiação amostra rede de difração Figura 14. Representação esquemática de um espectrofotômetro multicanal. Referências Bibliográficas D.C. Harris, Análise Química Quantitativa, 6 a Ed, Rio de Janeiro, LTC, 876 pp, D.A. Skoog, F.J. Holler e T.A. Nieman. Princípios de Análise Instrumental, 5 a Ed, Bookman, Porto Alegre, 836 pp, R.A. Day e A.L. Underwood. Quantitative analysis, 3 a Ed, Prentice Hall, Englewood Cliffs, 534 pp, H.H. Willard, L.L. Merrit, J.A. Dean e F.A. Settle. Instrumental methods of analysis, 6 a Ed, van Nostrand, New York, 1030 pp, Z. Marczenko. Spectrophotometric determination of elements, Ellis Horwood, Chichester, 641 pp, 1976.
QUI 154 Química Analítica V Análise Instrumental. Aula 2 Espectrometria Molecular UV-VIS (parte 2)
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 154 Química Analítica V Análise Instrumental Aula 2 Espectrometria Molecular UV-VIS (parte 2) Julio C. J.
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 154 Química Analítica V Análise Instrumental Aula 2 Espectrometria Molecular UV-VIS (parte 2) Julio C. J.
QUI 154 Química Analítica V Análise Instrumental. Aula 2 Espectrometria Molecular UV-VIS (parte 2)
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 154 Química Analítica V Análise Instrumental Aula 2 Espectrometria Molecular UV-VIS (parte 2) Julio C. J.
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 154 Química Analítica V Análise Instrumental Aula 2 Espectrometria Molecular UV-VIS (parte 2) Julio C. J.
Espectrofotometria UV-Vis. Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva
 Espectrofotometria UV-Vis Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva Relembrando... Conceitos Comprimento de onda (λ): distância entre dois pontos na mesma
Espectrofotometria UV-Vis Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva Relembrando... Conceitos Comprimento de onda (λ): distância entre dois pontos na mesma
UNIVERSIDADE FEDERAL DO PARANÁ Departamento de Química. CQ122 Química Analítica Instrumental II Prof. Claudio Antonio Tonegutti Aula 01 09/11/2012
 UNIVERSIDADE FEDERAL DO PARANÁ Departamento de Química CQ122 Química Analítica Instrumental II Prof. Claudio Antonio Tonegutti Aula 01 09/11/2012 A Química Analítica A divisão tradicional em química analítica
UNIVERSIDADE FEDERAL DO PARANÁ Departamento de Química CQ122 Química Analítica Instrumental II Prof. Claudio Antonio Tonegutti Aula 01 09/11/2012 A Química Analítica A divisão tradicional em química analítica
Análise Instrumental ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA
 Análise Instrumental ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA Introdução: Método aplicado na determinação de compostos inorgânicos e orgânicos, como por
Análise Instrumental ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA Introdução: Método aplicado na determinação de compostos inorgânicos e orgânicos, como por
Tópicos em Métodos Espectroquímicos. Aula 2 Revisão Conceitos Fundamentais
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Revisão Conceitos Fundamentais Julio C. J. Silva Juiz de For a, 2013
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Revisão Conceitos Fundamentais Julio C. J. Silva Juiz de For a, 2013
Tópicos em Métodos Espectroquímicos. Aula 2 Revisão Conceitos Fundamentais
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Revisão Conceitos Fundamentais Julio C. J. Silva Juiz de For a, 2015
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Revisão Conceitos Fundamentais Julio C. J. Silva Juiz de For a, 2015
Espectrofotometria UV-Vis. Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva
 Espectrofotometria UV-Vis Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva Juiz de Fora, 1/2018 1 Terminologia Espectroscopia: Parte da ciência que estuda o fenômeno
Espectrofotometria UV-Vis Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva Juiz de Fora, 1/2018 1 Terminologia Espectroscopia: Parte da ciência que estuda o fenômeno
Espectrofotometria UV-VIS PROF. DR. JÚLIO CÉSAR JOSÉ DA SILVA
 Espectrofotometria UV-VIS QUÍMICA ANALÍTICA V ESTAGIÁRIA A DOCÊNCIA: FERNANDA CERQUEIRA M. FERREIRA PROF. DR. JÚLIO CÉSAR JOSÉ DA SILVA 1 Conceitos Básicos Espectroscopia: É o estudo de sistemas físicos
Espectrofotometria UV-VIS QUÍMICA ANALÍTICA V ESTAGIÁRIA A DOCÊNCIA: FERNANDA CERQUEIRA M. FERREIRA PROF. DR. JÚLIO CÉSAR JOSÉ DA SILVA 1 Conceitos Básicos Espectroscopia: É o estudo de sistemas físicos
Análise de alimentos II Introdução aos Métodos Espectrométricos
 Análise de alimentos II Introdução aos Métodos Espectrométricos Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 Introdução Métodos espectrométricos Abrangem um grupo de métodos analíticos
Análise de alimentos II Introdução aos Métodos Espectrométricos Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 Introdução Métodos espectrométricos Abrangem um grupo de métodos analíticos
Análise de Alimentos II Espectroscopia de Absorção Molecular
 Análise de Alimentos II Espectroscopia de Absorção Molecular Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 2 Introdução A absorção de radiação no UV/Vis por uma espécie química (M) pode
Análise de Alimentos II Espectroscopia de Absorção Molecular Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 2 Introdução A absorção de radiação no UV/Vis por uma espécie química (M) pode
Espectroscopia Óptica Instrumentação e aplicações UV/VIS. CQ122 Química Analítica Instrumental II 1º sem Prof. Claudio Antonio Tonegutti
 Espectroscopia Óptica Instrumentação e aplicações UV/VIS CQ122 Química Analítica Instrumental II 1º sem. 2017 Prof. Claudio Antonio Tonegutti Lei de Beer A = b c A = absorbância = absortividade molar (L
Espectroscopia Óptica Instrumentação e aplicações UV/VIS CQ122 Química Analítica Instrumental II 1º sem. 2017 Prof. Claudio Antonio Tonegutti Lei de Beer A = b c A = absorbância = absortividade molar (L
QUI 070 Química Analítica V Análise Instrumental. Aula 3 introdução a UV-VIS
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 070 Química Analítica V Análise Instrumental Aula 3 introdução a UV-VIS Julio C. J. Silva Juiz de For a, 2013
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 070 Química Analítica V Análise Instrumental Aula 3 introdução a UV-VIS Julio C. J. Silva Juiz de For a, 2013
UNIVERSIDADE PAULISTA. A espectrofotometria é uma técnica de análise baseadas na interação entre a radiação eletromagnética e a matéria.
 DISCIPLINA: MÉTODOS INSTRUMENTAIS DE ANÁLISE TÓPICO 4: Espectrofotometria de Absorção Molecular UV/Visível A espectrofotometria é uma técnica de análise baseadas na interação entre a radiação eletromagnética
DISCIPLINA: MÉTODOS INSTRUMENTAIS DE ANÁLISE TÓPICO 4: Espectrofotometria de Absorção Molecular UV/Visível A espectrofotometria é uma técnica de análise baseadas na interação entre a radiação eletromagnética
Tópicos em Métodos Espectroquímicos. Aula 2 Espectrometria molecular (parte 1)
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Espectrometria molecular (parte 1) Julio C. J. Silva Juiz de Fora,
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Espectrometria molecular (parte 1) Julio C. J. Silva Juiz de Fora,
Tópicos em Métodos Espectroquímicos. Aula 2 Revisão Conceitos Fundamentais
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Revisão Conceitos Fundamentais Julio C. J. Silva Juiz de For a, 2013
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Revisão Conceitos Fundamentais Julio C. J. Silva Juiz de For a, 2013
Disciplina: Bioquímica Clínica Curso: Análises Clínicas 2º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini
 Disciplina: Bioquímica Clínica Curso: Análises Clínicas 2º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Fundamentos da Espectrofotometria Uma maneira boa de cutucar moléculas, é com radiação
Disciplina: Bioquímica Clínica Curso: Análises Clínicas 2º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Fundamentos da Espectrofotometria Uma maneira boa de cutucar moléculas, é com radiação
Introdução aos métodos espectrométricos. Propriedades da radiação eletromagnética
 Introdução aos métodos espectrométricos A espectrometria compreende um grupo de métodos analíticos baseados nas propriedades dos átomos e moléculas de absorver ou emitir energia eletromagnética em uma
Introdução aos métodos espectrométricos A espectrometria compreende um grupo de métodos analíticos baseados nas propriedades dos átomos e moléculas de absorver ou emitir energia eletromagnética em uma
CQ122 Química Analítica Instrumental II. Turma B 2º semestre 2012 Prof. Claudio Antonio Tonegutti. 1ª Avaliação Teórica 21/12/2012 GABARITO
 CQ122 Química Analítica Instrumental II Turma B 2º semestre 2012 Prof. Claudio Antonio Tonegutti 1ª Avaliação Teórica 21/12/2012 GABARITO 1) A figura abaixo apresenta o espectro eletromagnético com as
CQ122 Química Analítica Instrumental II Turma B 2º semestre 2012 Prof. Claudio Antonio Tonegutti 1ª Avaliação Teórica 21/12/2012 GABARITO 1) A figura abaixo apresenta o espectro eletromagnético com as
Tópicos em Métodos Espectroquímicos. Aula 2 Espectrometria molecular (parte 1)
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Espectrometria molecular (parte 1) Julio C. J. Silva Juiz de Fora,
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química Tópicos em Métodos Espectroquímicos Aula 2 Espectrometria molecular (parte 1) Julio C. J. Silva Juiz de Fora,
Centro Universitário Padre Anchieta
 1) Quais são os cinco componentes principais utilizados nos equipamentos de espectroscopia óptica (molecular e atômica). Resposta: Os cinco componentes são: 1- Fonte de radiação (energia): Responsável
1) Quais são os cinco componentes principais utilizados nos equipamentos de espectroscopia óptica (molecular e atômica). Resposta: Os cinco componentes são: 1- Fonte de radiação (energia): Responsável
3/9/2011 ANALÍTICA V 2S Prof. Rafael Sousa. Notas de aula:
 ANALÍTICA V 2S 2011 Aula 4 Espectrofotometria no UV-VisVis Prof. Rafael Sousa Departamento de Química - ICE [email protected] Notas de aula: www.ufjf.br/baccan Relembrando a aula 3... 2 Espectrofotometria:
ANALÍTICA V 2S 2011 Aula 4 Espectrofotometria no UV-VisVis Prof. Rafael Sousa Departamento de Química - ICE [email protected] Notas de aula: www.ufjf.br/baccan Relembrando a aula 3... 2 Espectrofotometria:
ESPECTROFOTOMETRIA UV-VISÍVEL. Departamento de Engenharia Química DEQUI ESCOLA DE ENGENHARIA DE LORENA EEL/USP
 ESPECTROFOTOMETRIA UV-VISÍVEL Departamento de Engenharia Química DEQUI ESCOLA DE ENGENHARIA DE LORENA EEL/USP Fundamentos da Espectrofotometria Uma maneira boa de cutucar moléculas, é com radiação eletromagnética
ESPECTROFOTOMETRIA UV-VISÍVEL Departamento de Engenharia Química DEQUI ESCOLA DE ENGENHARIA DE LORENA EEL/USP Fundamentos da Espectrofotometria Uma maneira boa de cutucar moléculas, é com radiação eletromagnética
Mestrando: Jefferson Willian Martins Prof. Dr. Júlio César José da Silva Juiz de Fora, 2/2017
 1 ESPECTROFOTOMETRIA DE UV-VIS Mestrando: Jefferson Willian Martins Prof. Dr. Júlio César José da Silva Juiz de Fora, 2/2017 2 CONCEITOS PRINCIPAIS O que é Espectroscopia e Espectrometria? IUPAC, Compendium
1 ESPECTROFOTOMETRIA DE UV-VIS Mestrando: Jefferson Willian Martins Prof. Dr. Júlio César José da Silva Juiz de Fora, 2/2017 2 CONCEITOS PRINCIPAIS O que é Espectroscopia e Espectrometria? IUPAC, Compendium
Lista de Exercício 2ª TVC Química Analítica V Teoria (1º Sem 2016). Obs.: Entregar antes da 2ª TVC.
 Lista de Exercício 2ª TVC Química Analítica V Teoria (1º Sem 2016). Obs.: Entregar antes da 2ª TVC. Capítulo 24 (Skoog) Introdução aos Métodos Espectroquímicos 24-1. Por que uma solução de Cu(NH3)4 2+
Lista de Exercício 2ª TVC Química Analítica V Teoria (1º Sem 2016). Obs.: Entregar antes da 2ª TVC. Capítulo 24 (Skoog) Introdução aos Métodos Espectroquímicos 24-1. Por que uma solução de Cu(NH3)4 2+
Disciplina: SQM0415 Análise Instrumental I. Professores: Álvaro José dos Santos Neto Emanuel Carrilho
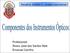 Disciplina: SQM0415 Análise Instrumental I Professores: Álvaro José dos Santos Neto Emanuel Carrilho Diagrama de blocos - Colorimetria Fotoelétrica (Fotômetro Vis) - Espectrofotometria UV/Vis PROCESSAMENTO
Disciplina: SQM0415 Análise Instrumental I Professores: Álvaro José dos Santos Neto Emanuel Carrilho Diagrama de blocos - Colorimetria Fotoelétrica (Fotômetro Vis) - Espectrofotometria UV/Vis PROCESSAMENTO
ANÁLISE QUÍMICA INSTRUMENTAL. Métodos espectrais e opticos
 ANÁLISE QUÍMICA INSTRUMENTAL Métodos espectrais e opticos 6 Ed. Cap. 6 Pg.147-151 6 Ed. Cap. 1 Pg.1-28 6 Ed. Cap. 24 Pg.669-690 07/03/2018 2 Espectro eletromagnético Fonte: www.cena.usp.br/ irradiacao/espectro.htm
ANÁLISE QUÍMICA INSTRUMENTAL Métodos espectrais e opticos 6 Ed. Cap. 6 Pg.147-151 6 Ed. Cap. 1 Pg.1-28 6 Ed. Cap. 24 Pg.669-690 07/03/2018 2 Espectro eletromagnético Fonte: www.cena.usp.br/ irradiacao/espectro.htm
10/03/2016. Diagrama de blocos. 1.Fontes de radiação. - Colorimetria Fotoelétrica (Fotômetro Vis) - Espectrofotometria UV/Vis
 Disciplina: SQM0415 Análise Instrumental I Diagrama de blocos - Colorimetria Fotoelétrica (Fotômetro Vis) - Espectrofotometria UV/Vis PROCESSAMENTO DO SINAL / APRESENTAÇÃO Professores: Álvaro José dos
Disciplina: SQM0415 Análise Instrumental I Diagrama de blocos - Colorimetria Fotoelétrica (Fotômetro Vis) - Espectrofotometria UV/Vis PROCESSAMENTO DO SINAL / APRESENTAÇÃO Professores: Álvaro José dos
Espectrometria de emissão atômica
 Espectrometria de emissão atômica Técnica analítica que se baseia na emissão de radiação eletromagnética das regiões visível e ultravioleta do espectro eletromagnético por átomos neutros ou átomos ionizados
Espectrometria de emissão atômica Técnica analítica que se baseia na emissão de radiação eletromagnética das regiões visível e ultravioleta do espectro eletromagnético por átomos neutros ou átomos ionizados
K P 10. Concentração. Potência a emissão de fluorescência (F) é proporcional à potência radiante do feixe de excitação que é absorvido pelo sistema
 Concentração Potência a emissão de fluorescência (F) é proporcional à potência radiante do feixe de excitação que é absorvido pelo sistema F = emissão de fluorescência P o = potência do feixe incidente
Concentração Potência a emissão de fluorescência (F) é proporcional à potência radiante do feixe de excitação que é absorvido pelo sistema F = emissão de fluorescência P o = potência do feixe incidente
Introdução aos métodos instrumentais
 Introdução aos métodos instrumentais Métodos instrumentais Métodos que dependem da medição de propriedades elétricas, e os que estão baseados na: determinação da absorção da radiação, na medida da intensidade
Introdução aos métodos instrumentais Métodos instrumentais Métodos que dependem da medição de propriedades elétricas, e os que estão baseados na: determinação da absorção da radiação, na medida da intensidade
Converta os seguintes dados de transmitâncias para as respectivas absorbâncias: (a) 22,7% (b) 0,567 (c) 31,5% (d) 7,93% (e) 0,103 (f ) 58,2%
 Lista de Exercício 2ª TVC Química Analítica V Teoria (2º Sem 2017). Obs.: 1) A lista deve ser entregue antes da 2ª TVC (24/10). 2) O exercícios devem ser feitos a mão Capítulo 24 (Skoog) Introdução aos
Lista de Exercício 2ª TVC Química Analítica V Teoria (2º Sem 2017). Obs.: 1) A lista deve ser entregue antes da 2ª TVC (24/10). 2) O exercícios devem ser feitos a mão Capítulo 24 (Skoog) Introdução aos
Departamento de Zoologia da Universidade de Coimbra
 Departamento de Zoologia da Universidade de Coimbra Armando Cristóvão Adaptado de "The Tools of Biochemistry" de Terrance G. Cooper Espectrofotometria de Absorção Uma das primeiras características químicas
Departamento de Zoologia da Universidade de Coimbra Armando Cristóvão Adaptado de "The Tools of Biochemistry" de Terrance G. Cooper Espectrofotometria de Absorção Uma das primeiras características químicas
Agronomia Química Analítica Prof. Dr. Gustavo Rocha de Castro. As medidas baseadas na luz (radiação eletromagnética) são muito empregadas
 ESPECTROMETRIA DE ABSORÇÃO ATÔMICA Introdução As medidas baseadas na luz (radiação eletromagnética) são muito empregadas na química analítica. Estes métodos são baseados na quantidade de radiação emitida
ESPECTROMETRIA DE ABSORÇÃO ATÔMICA Introdução As medidas baseadas na luz (radiação eletromagnética) são muito empregadas na química analítica. Estes métodos são baseados na quantidade de radiação emitida
QUI346 ESPECTROMETRIA ATÔMICA
 QUI346 ESPECTROMETRIA ATÔMICA EMISSÃO ABSORÇÃO ENERGIA RADIANTE Quantidades discretas de energia radiante (quantum, E = h.n) absorvida pelos átomos promovem elétrons de um nível de energia fundamental
QUI346 ESPECTROMETRIA ATÔMICA EMISSÃO ABSORÇÃO ENERGIA RADIANTE Quantidades discretas de energia radiante (quantum, E = h.n) absorvida pelos átomos promovem elétrons de um nível de energia fundamental
FCVA/ UNESP JABOTICABAL FUNDAMENTOS DA ESPECTROSCOPIA MOLECULAR UV-VISÍVEL. Prof a. Dr a. Luciana Maria Saran
 FCVA/ UNESP JABOTICABAL FUNDAMENTOS DA ESPECTROSCOPIA MOLECULAR UV-VISÍVEL Prof a. Dr a. Luciana Maria Saran 1. Introdução Espectroscopia é qualquer processo que utiliza a luz para medir as concentrações
FCVA/ UNESP JABOTICABAL FUNDAMENTOS DA ESPECTROSCOPIA MOLECULAR UV-VISÍVEL Prof a. Dr a. Luciana Maria Saran 1. Introdução Espectroscopia é qualquer processo que utiliza a luz para medir as concentrações
FCVA/ UNESP JABOTICABAL FUNDAMENTOS DE ESPECTROSCOPIA MOLECULAR UV-VISÍVEL. Prof a. Dr a. Luciana Maria Saran
 FCVA/ UNESP JABOTICABAL FUNDAMENTOS DE ESPECTROSCOPIA MOLECULAR UV-VISÍVEL Prof a. Dr a. Luciana Maria Saran 1. Introdução Espectroscopia é qualquer processo que utiliza a luz para medir as concentrações
FCVA/ UNESP JABOTICABAL FUNDAMENTOS DE ESPECTROSCOPIA MOLECULAR UV-VISÍVEL Prof a. Dr a. Luciana Maria Saran 1. Introdução Espectroscopia é qualquer processo que utiliza a luz para medir as concentrações
Química Analítica Ambiental II
 Química Analítica Ambiental II Prof. Morun Bernardino Neto, DSc ESPECTROFOTOMETRIA II INSTRUMENTOS E APLICAÇÕES BREVE REVISÃO O gráfico abaixo mostra o espectro de absorção de um protetor solar que absorve
Química Analítica Ambiental II Prof. Morun Bernardino Neto, DSc ESPECTROFOTOMETRIA II INSTRUMENTOS E APLICAÇÕES BREVE REVISÃO O gráfico abaixo mostra o espectro de absorção de um protetor solar que absorve
QUI346 ESPECTROMETRIA ATÔMICA
 QUI346 ESPECTROMETRIA ATÔMICA EMISSÃO ABSORÇÃO EMISSÃO ATÔMICA Uma experiência envolvendo átomos de metal alcalino Fonte: Krug, FJ. Fundamentos de Espectroscopia Atômica: http://web.cena.usp.br/apost ilas/krug/aas%20fundamen
QUI346 ESPECTROMETRIA ATÔMICA EMISSÃO ABSORÇÃO EMISSÃO ATÔMICA Uma experiência envolvendo átomos de metal alcalino Fonte: Krug, FJ. Fundamentos de Espectroscopia Atômica: http://web.cena.usp.br/apost ilas/krug/aas%20fundamen
Disciplina: Bioquímica Clínica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini
 Disciplina: Bioquímica Clínica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Fundamentos da Espectrofotometria Uma maneira boa de cutucar moléculas, é com radiação
Disciplina: Bioquímica Clínica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Fundamentos da Espectrofotometria Uma maneira boa de cutucar moléculas, é com radiação
2. Propriedades Corpusculares das Ondas
 2. Propriedades Corpusculares das Ondas Sumário Revisão sobre ondas eletromagnéticas Radiação térmica Hipótese dos quanta de Planck Efeito Fotoelétrico Geração de raios-x Absorção de raios-x Ondas eletromagnéticas
2. Propriedades Corpusculares das Ondas Sumário Revisão sobre ondas eletromagnéticas Radiação térmica Hipótese dos quanta de Planck Efeito Fotoelétrico Geração de raios-x Absorção de raios-x Ondas eletromagnéticas
UNIVERSIDADE FEDERAL DE PELOTAS INSPEÇÃO DE LEITE E DERIVADOS ESPECTROSCOPIA DENISE HENTGES PELOTAS, 2008.
 UNIVERSIDADE FEDERAL DE PELOTAS INSPEÇÃO DE LEITE E DERIVADOS ESPECTROSCOPIA DENISE HENTGES PELOTAS, 2008. Espectroscopia de Infravermelho (IR) Issac Newton Feixe de luz; A luz violeta é a que mais é deslocada
UNIVERSIDADE FEDERAL DE PELOTAS INSPEÇÃO DE LEITE E DERIVADOS ESPECTROSCOPIA DENISE HENTGES PELOTAS, 2008. Espectroscopia de Infravermelho (IR) Issac Newton Feixe de luz; A luz violeta é a que mais é deslocada
Nome: Jeremias Christian Honorato Costa Disciplina: Materiais para Engenharia
 Nome: Jeremias Christian Honorato Costa Disciplina: Materiais para Engenharia Por propriedade ótica subentende-se a reposta do material à exposição à radiação eletromagnética e, em particular, à luz visível.
Nome: Jeremias Christian Honorato Costa Disciplina: Materiais para Engenharia Por propriedade ótica subentende-se a reposta do material à exposição à radiação eletromagnética e, em particular, à luz visível.
ANÁLISE QUÍMICA III COLORIMETRIA / ESPECTROFOTOMETRIA
 ANÁLISE QUÍMICA III COLORIMETRIA / ESPECTROFOTOMETRIA 1) Colorimetria Em prática analítica, é necessário freqüentemente determinar quantidades muito pequenas (traços) de substâncias presentes como impurezas
ANÁLISE QUÍMICA III COLORIMETRIA / ESPECTROFOTOMETRIA 1) Colorimetria Em prática analítica, é necessário freqüentemente determinar quantidades muito pequenas (traços) de substâncias presentes como impurezas
Noções básicas de quântica. Prof. Ms. Vanderlei Inácio de Paula
 Noções básicas de quântica Prof. Ms. Vanderlei Inácio de Paula Noções de quântica O professor recomenda: Estude pelos seguintes livros/páginas sobre a Ligações químicas e faça os exercícios! Shriver Ed
Noções básicas de quântica Prof. Ms. Vanderlei Inácio de Paula Noções de quântica O professor recomenda: Estude pelos seguintes livros/páginas sobre a Ligações químicas e faça os exercícios! Shriver Ed
Os princípios da espectroscopia: Teoria DESENVOLVENDO UMA CIÊNCIAMELHOR AGILENT E VOCÊ
 Os princípios da espectroscopia: Teoria DESENVOLVENDO UMA CIÊNCIAMELHOR AGILENT E VOCÊ 1 A Agilent tem um compromisso com a comunidade educacional e está disposta a conceder acesso ao material de propriedade
Os princípios da espectroscopia: Teoria DESENVOLVENDO UMA CIÊNCIAMELHOR AGILENT E VOCÊ 1 A Agilent tem um compromisso com a comunidade educacional e está disposta a conceder acesso ao material de propriedade
ELÉTRONS EM ÁTOMOS. Depois do modelo de Rutherford: Como é o comportamento dos elétrons nos átomos? Rutherford: estrutura planetária, com o
 ELÉTRONS EM ÁTOMOS Depois do modelo de Rutherford: Como é o comportamento dos elétrons nos átomos? Rutherford: estrutura planetária, com o núcleo correspondendo ao sol no nosso sistema solar e os elétrons
ELÉTRONS EM ÁTOMOS Depois do modelo de Rutherford: Como é o comportamento dos elétrons nos átomos? Rutherford: estrutura planetária, com o núcleo correspondendo ao sol no nosso sistema solar e os elétrons
QUI346 ESPECTROFOTOMETRIA
 QUI346 ESPECTROFOTOMETRIA ABSORÇÃO FOTOQUÍMICA 3ª Parte (cont.) A QUANTIFICAÇÃO 07/10/2013 Mauricio X. Coutrim QUANTIFICAÇÃO: BRANCO O BRANCO NA DETERMINAÇÃO A radiação absorvida não é a simples diferença
QUI346 ESPECTROFOTOMETRIA ABSORÇÃO FOTOQUÍMICA 3ª Parte (cont.) A QUANTIFICAÇÃO 07/10/2013 Mauricio X. Coutrim QUANTIFICAÇÃO: BRANCO O BRANCO NA DETERMINAÇÃO A radiação absorvida não é a simples diferença
Determinação de permanganato em água
 ESPECTROFOTOMETRIA NO UV-VIS Ficha técnica do equipamento Espectrofotômetro Shimadzu UV-1650PC Fontes de excitação: Lâmpada de deutério e Lâmpada de tungstênio-halogênio Seletores de comprimento de onda:
ESPECTROFOTOMETRIA NO UV-VIS Ficha técnica do equipamento Espectrofotômetro Shimadzu UV-1650PC Fontes de excitação: Lâmpada de deutério e Lâmpada de tungstênio-halogênio Seletores de comprimento de onda:
Espectrofotometria UV-VIS
 Espectrofotometria UV-VIS Aula 2 Química Analítica V Estagiária a Docência: Fernanda Cerqueira M. Ferreira Prof. Dr. Júlio César José da Silva 1 Relembrando Campo elétrico da radiação eletromagnética Matéria
Espectrofotometria UV-VIS Aula 2 Química Analítica V Estagiária a Docência: Fernanda Cerqueira M. Ferreira Prof. Dr. Júlio César José da Silva 1 Relembrando Campo elétrico da radiação eletromagnética Matéria
ESPECTROS ATÔMICOS E MOLECULARES
 ESPECTROS ATÔMICOS E MOLECULARES Material Utilizado: - um conjunto (PASCO OS-8500) constituído de um banco óptico com escala milimetrada, um portacomponentes, uma rede de difração (600 linhas / mm), e
ESPECTROS ATÔMICOS E MOLECULARES Material Utilizado: - um conjunto (PASCO OS-8500) constituído de um banco óptico com escala milimetrada, um portacomponentes, uma rede de difração (600 linhas / mm), e
QUI346 QUÍMICA ANALÍTICA INSTRUMENTAL
 QUI346 QUÍMICA ANALÍTICA INSTRUMENTAL Prof. Mauricio Xavier Coutrim DEQUI RADIAÇÃO ELETROMAGNÉTICA Onda eletromagnética (vácuo: v = 2,99792.10 8 m.s -1 ) l = comprimento de onda A = amplitude da onda v
QUI346 QUÍMICA ANALÍTICA INSTRUMENTAL Prof. Mauricio Xavier Coutrim DEQUI RADIAÇÃO ELETROMAGNÉTICA Onda eletromagnética (vácuo: v = 2,99792.10 8 m.s -1 ) l = comprimento de onda A = amplitude da onda v
Princípios da Interação da Luz com o tecido: Refração, Absorção e Espalhamento. Prof. Emery Lins Curso Eng. Biomédica
 Princípios da Interação da Luz com o tecido: Refração, Absorção e Espalhamento Prof. Emery Lins Curso Eng. Biomédica Introdução Breve revisão: Questões... O que é uma radiação? E uma partícula? Como elas
Princípios da Interação da Luz com o tecido: Refração, Absorção e Espalhamento Prof. Emery Lins Curso Eng. Biomédica Introdução Breve revisão: Questões... O que é uma radiação? E uma partícula? Como elas
ANALÍTICA V 1º semestre de Aula 4: ESPECTROSCOPIA. Prof. Rafael Sousa. Notas de aula:
 ANALÍTICA V 1º semestre de 2013 Aula 4: 28-05-13 ESPECTROSCOPIA Espectrofotometria no UV-Vis Vis - Parte I Prof. Rafael Sousa Departamento de Química - ICE [email protected] Notas de aula: www.ufjf.br/baccan
ANALÍTICA V 1º semestre de 2013 Aula 4: 28-05-13 ESPECTROSCOPIA Espectrofotometria no UV-Vis Vis - Parte I Prof. Rafael Sousa Departamento de Química - ICE [email protected] Notas de aula: www.ufjf.br/baccan
ANALÍTICA V 2S Aula 6: ESPECTROSCOPIA. Prof. Rafael Sousa
 ANALÍTICA V 2S 2012 Aula 6: 08-01-13 ESPECTROSCOPIA Espectrotometria de Absorção Atômica - Parte I Prof. Rafael Sousa Departamento de Química - ICE [email protected] Notas de aula: www.ufjf.br/baccan
ANALÍTICA V 2S 2012 Aula 6: 08-01-13 ESPECTROSCOPIA Espectrotometria de Absorção Atômica - Parte I Prof. Rafael Sousa Departamento de Química - ICE [email protected] Notas de aula: www.ufjf.br/baccan
ANÁLISES QUÍMICAS EMPREGANDO AS TÉCNICAS DE ABSORÇÃO ATÔMICA, ESPECTROMETRIA DE EMISSÃO ÓTICA E DE MASSAS: POTENCIALIDADES E APLICAÇÕES
 ANÁLISES QUÍMICAS EMPREGANDO AS TÉCNICAS DE ABSORÇÃO ATÔMICA, ESPECTROMETRIA DE EMISSÃO ÓTICA E DE MASSAS: POTENCIALIDADES E APLICAÇÕES Fernando V. Silva fernando.vitorino [email protected] Espectroscopia
ANÁLISES QUÍMICAS EMPREGANDO AS TÉCNICAS DE ABSORÇÃO ATÔMICA, ESPECTROMETRIA DE EMISSÃO ÓTICA E DE MASSAS: POTENCIALIDADES E APLICAÇÕES Fernando V. Silva fernando.vitorino [email protected] Espectroscopia
AULA 21 INTRODUÇÃO À RADIAÇÃO TÉRMICA
 Notas de aula de PME 3361 Processos de Transferência de Calor 180 AULA 1 INTRODUÇÃO À RADIAÇÃO TÉRMICA A radiação térmica é a terceira e última forma de transferência de calor existente. Das três formas,
Notas de aula de PME 3361 Processos de Transferência de Calor 180 AULA 1 INTRODUÇÃO À RADIAÇÃO TÉRMICA A radiação térmica é a terceira e última forma de transferência de calor existente. Das três formas,
Tecnicas analiticas para Joias
 Tecnicas analiticas para Joias Técnicas avançadas de analise A caracterização de gemas e metais da área de gemologia exige a utilização de técnicas analíticas sofisticadas. Estas técnicas devem ser capazes
Tecnicas analiticas para Joias Técnicas avançadas de analise A caracterização de gemas e metais da área de gemologia exige a utilização de técnicas analíticas sofisticadas. Estas técnicas devem ser capazes
Física D Extensivo V. 8
 Física D Extensivo V. 8 Exercícios 0) C f R X > f WZ 0) B 03) E 04) E raios X > luz Raios X são radiações eletromagnéticas com um comprimento de onda muito curto, aproximadamente de 0,06 até 0 Å. Formam-se
Física D Extensivo V. 8 Exercícios 0) C f R X > f WZ 0) B 03) E 04) E raios X > luz Raios X são radiações eletromagnéticas com um comprimento de onda muito curto, aproximadamente de 0,06 até 0 Å. Formam-se
Capítulo 33. Ondas eletromagnéticas
 Capítulo 33 Ondas eletromagnéticas O Arco-íris de Maxwell James Clerk Maxwell: - raio luminoso = onda eletromagnética - óptica (luz visível) = ramo do eletrom. Meados do séc. XIX: - espectro = UV-Vis +
Capítulo 33 Ondas eletromagnéticas O Arco-íris de Maxwell James Clerk Maxwell: - raio luminoso = onda eletromagnética - óptica (luz visível) = ramo do eletrom. Meados do séc. XIX: - espectro = UV-Vis +
QUI346 ESPECTROFOTOMETRIA
 QUI346 ESPECTROFOTOMETRIA ABSORÇÃO FOTOQUÍMICA 3ª Parte (cont.) A QUANTIFICAÇÃO Mauricio X. Coutrim QUANTIFICAÇÃO: BRANCO O BRANCO NA DETERMINAÇÃO A radiação absorvida não é a simples diferença entre as
QUI346 ESPECTROFOTOMETRIA ABSORÇÃO FOTOQUÍMICA 3ª Parte (cont.) A QUANTIFICAÇÃO Mauricio X. Coutrim QUANTIFICAÇÃO: BRANCO O BRANCO NA DETERMINAÇÃO A radiação absorvida não é a simples diferença entre as
PROPRIEDADES TÉRMICAS E ÓPTICAS DOS MATERIAIS
 UNIVERSIDADE FEDERAL DO ABC Centro de Engenharia, Modelagem e Ciências Sociais Aplicadas (CECS) BC-1105: MATERIAIS E SUAS PROPRIEDADES PROPRIEDADES TÉRMICAS E ÓPTICAS DOS MATERIAIS Introdução Propriedades
UNIVERSIDADE FEDERAL DO ABC Centro de Engenharia, Modelagem e Ciências Sociais Aplicadas (CECS) BC-1105: MATERIAIS E SUAS PROPRIEDADES PROPRIEDADES TÉRMICAS E ÓPTICAS DOS MATERIAIS Introdução Propriedades
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO Edição de novembro de 2011 CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO ÍNDICE 3.1- Efeito
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO Edição de novembro de 2011 CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO ÍNDICE 3.1- Efeito
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO SUL CAMPUS RIO GRANDE INSTRUMENTAÇÃO INDUSTRIAL
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO SUL CAMPUS RIO GRANDE INSTRUMENTAÇÃO INDUSTRIAL Aula 24 2 TERMÔMETROS DE RADIAÇÃO São medidores de temperatura sem contato. Os componentes
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO SUL CAMPUS RIO GRANDE INSTRUMENTAÇÃO INDUSTRIAL Aula 24 2 TERMÔMETROS DE RADIAÇÃO São medidores de temperatura sem contato. Os componentes
Espectroscopia: uma breve introdução. J.R.Kaschny (2014)
 Espectroscopia: uma breve introdução J.R.Kaschny (2014) Introdução Talvez o inicio de tudo (Newton) se deu com a observação do arco-íris, ou mesmo quando se fez incidir sobre um feixe de luz do sol em
Espectroscopia: uma breve introdução J.R.Kaschny (2014) Introdução Talvez o inicio de tudo (Newton) se deu com a observação do arco-íris, ou mesmo quando se fez incidir sobre um feixe de luz do sol em
FUNDAMENTOS DA ESPECTROFOTOMETRIA
 FUNDAMENTOS DA ESPECTROFOTOMETRIA SUMÁRIO INTRODUÇÃO AOS MÉTODOS ESPECTROMÉTRICOS PROPRIEDADES GERAIS DA ONDA PROPRIEDADES DA LUZ PARÂMETROS DA ONDA RELAÇÃO ENTRE FREQUÊNCIA E COMPRIMENTO DE ONDA RELAÇÃO
FUNDAMENTOS DA ESPECTROFOTOMETRIA SUMÁRIO INTRODUÇÃO AOS MÉTODOS ESPECTROMÉTRICOS PROPRIEDADES GERAIS DA ONDA PROPRIEDADES DA LUZ PARÂMETROS DA ONDA RELAÇÃO ENTRE FREQUÊNCIA E COMPRIMENTO DE ONDA RELAÇÃO
Introdução à Química Moderna
 Introdução à Química Moderna Prof. Alex Fabiano C. Campos, Dr Radiação de Corpo Negro Objeto com T 0K:emite radiação eletromagnética. T 0K Física Clássica: vibração térmica dos átomos e moléculas, provoca
Introdução à Química Moderna Prof. Alex Fabiano C. Campos, Dr Radiação de Corpo Negro Objeto com T 0K:emite radiação eletromagnética. T 0K Física Clássica: vibração térmica dos átomos e moléculas, provoca
Fonte de plasma - DCP
 Fonte de plasma - DCP Dois anodos de grafite e um catodo de tungstênio, em forma de Y invertido Plasma é formado, colocando-se momentaneamente os eletrodos em contato Ocorre ionização, gerando corrente
Fonte de plasma - DCP Dois anodos de grafite e um catodo de tungstênio, em forma de Y invertido Plasma é formado, colocando-se momentaneamente os eletrodos em contato Ocorre ionização, gerando corrente
Introd. Física Médica
 Introd. Física Médica O Efeito Foto Elétrico (EFE) Introdução a Física Médica O Efeito Foto Elétrico (EFE) Introdução a Fís sica Médica Heinrich HERTZ descobriu o Efeito FotoElétrico (1887): Quando a luz
Introd. Física Médica O Efeito Foto Elétrico (EFE) Introdução a Física Médica O Efeito Foto Elétrico (EFE) Introdução a Fís sica Médica Heinrich HERTZ descobriu o Efeito FotoElétrico (1887): Quando a luz
SEL PRINCÍPIOS FÍSICOS DE FORMAÇÃO DE IMAGENS MÉDICAS. Prof. Homero Schiabel
 SEL 397 - PRINCÍPIOS FÍSICOS DE FORMAÇÃO DE IMAGENS MÉDICAS Prof. Homero Schiabel Max Planck (1901): teoria dos quanta E depende da freqüência de radiação (ou de λ): E = h ν ν = c / λ E = h c / λ 4. PRODUÇÃO
SEL 397 - PRINCÍPIOS FÍSICOS DE FORMAÇÃO DE IMAGENS MÉDICAS Prof. Homero Schiabel Max Planck (1901): teoria dos quanta E depende da freqüência de radiação (ou de λ): E = h ν ν = c / λ E = h c / λ 4. PRODUÇÃO
O ESPECTRO ELETROMAGNÉTICO
 O ESPECTRO ELETROMAGNÉTICO ONDAS: Interferência construtiva e destrutiva Onda 1 Onda 2 Onda composta a b c d e A luz apresenta interferência: natureza ondulatória: O experimento de Young (~1800) Efeito
O ESPECTRO ELETROMAGNÉTICO ONDAS: Interferência construtiva e destrutiva Onda 1 Onda 2 Onda composta a b c d e A luz apresenta interferência: natureza ondulatória: O experimento de Young (~1800) Efeito
SISTEMAS ÓPTICOS. Atenuação e Dispersão
 MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA Instituto Federal de Educação, Ciência e Tecnologia de Santa Catarina Campus São José Área de Telecomunicações Curso Superior Tecnológico
MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA Instituto Federal de Educação, Ciência e Tecnologia de Santa Catarina Campus São José Área de Telecomunicações Curso Superior Tecnológico
Luz & Radiação. Roberto Ortiz EACH USP
 Luz & Radiação Roberto Ortiz EACH USP A luz é uma onda eletromagnética A figura acima ilustra os campos elétrico (E) e magnético (B) que compõem a luz Eles são perpendiculares entre si e perpendiculares
Luz & Radiação Roberto Ortiz EACH USP A luz é uma onda eletromagnética A figura acima ilustra os campos elétrico (E) e magnético (B) que compõem a luz Eles são perpendiculares entre si e perpendiculares
QUI346 Absorção Molecular no UV-Vis
 QUI346 Absorção Molecular no UV-Vis (2ª parte) ABSORÇÃO FOTOQUÍMICA. POR QUÊ? COMO? QUANDO? 01 PORQUÊ A DIFERENÇA DE CORES? Cach Campo, ago14 Camp, nov06 2 INTERAÇÃO ENERGIA MATÉRIA LUZ FÓTONS (QUANTA)
QUI346 Absorção Molecular no UV-Vis (2ª parte) ABSORÇÃO FOTOQUÍMICA. POR QUÊ? COMO? QUANDO? 01 PORQUÊ A DIFERENÇA DE CORES? Cach Campo, ago14 Camp, nov06 2 INTERAÇÃO ENERGIA MATÉRIA LUZ FÓTONS (QUANTA)
Aula 12 PRÁTICA 02 ESPECTROFOTOMETRIA DE ABSORÇÃO MOLECULAR NO UV VIS: OPERAÇÃO E RESPOSTA DO ESPECTROFOTÔMETRO. Elisangela de Andrade Passos
 Aula 12 PRÁTICA 02 ESPECTROFOTOMETRIA DE ABSORÇÃO MOLECULAR NO UV VIS: OPERAÇÃO E RESPOSTA DO ESPECTROFOTÔMETRO META Proporcionar o contato do aluno com a instrumentação analítica empregada em análises
Aula 12 PRÁTICA 02 ESPECTROFOTOMETRIA DE ABSORÇÃO MOLECULAR NO UV VIS: OPERAÇÃO E RESPOSTA DO ESPECTROFOTÔMETRO META Proporcionar o contato do aluno com a instrumentação analítica empregada em análises
Energia certa significa: quando a energia do fóton corresponde à diferença nos níveis de energia entre as duas órbitas permitidas do átomo de H.
 ESPECTROSCOPIA II A relação da luz com as linhas espectrais O que acontece se átomos de H forem bombardeados por fótons? R. Existem três possibilidades: 1) a maioria dos fótons passa sem nenhuma interação
ESPECTROSCOPIA II A relação da luz com as linhas espectrais O que acontece se átomos de H forem bombardeados por fótons? R. Existem três possibilidades: 1) a maioria dos fótons passa sem nenhuma interação
Física IV Escola Politécnica GABARITO DA P2 16 de outubro de 2012
 Física IV - 4320402 Escola Politécnica - 2012 GABARITO DA P2 16 de outubro de 2012 Questão 1 Ondas longas de rádio, com comprimento de onda λ, de uma estação radioemissora E podem chegar a um receptor
Física IV - 4320402 Escola Politécnica - 2012 GABARITO DA P2 16 de outubro de 2012 Questão 1 Ondas longas de rádio, com comprimento de onda λ, de uma estação radioemissora E podem chegar a um receptor
Doseamento do Fe 2+ por espectroscopia de absorção
 Práticas Laboratoriais de Diagnóstico e Teoria do Restauro I (Ciências da Arte e do Património) Doseamento do Fe 2+ por espectroscopia de absorção Objectivo Determinar a concentração do ferro(ii) numa
Práticas Laboratoriais de Diagnóstico e Teoria do Restauro I (Ciências da Arte e do Património) Doseamento do Fe 2+ por espectroscopia de absorção Objectivo Determinar a concentração do ferro(ii) numa
Luís H. Melo de Carvalho Química Analítica II Luís H. Melo de Carvalho Química Analítica II
 Luís H. Melo de Carvalho Luís H. Melo de Carvalho 1 Luís H. Melo de Carvalho Luís H. Melo de Carvalho 2 Luís H. Melo de Carvalho 3 Luís H. Melo de Carvalho Luís H. Melo de Carvalho 4 Luís H. Melo de Carvalho
Luís H. Melo de Carvalho Luís H. Melo de Carvalho 1 Luís H. Melo de Carvalho Luís H. Melo de Carvalho 2 Luís H. Melo de Carvalho 3 Luís H. Melo de Carvalho Luís H. Melo de Carvalho 4 Luís H. Melo de Carvalho
Lista de Exercício 1ª TVC Química Analítica V Teoria
 Lista de Exercício 1ª TVC Química Analítica V Teoria Capítulo 7 Tratamento e Avaliação Estatística de Dados 7-3. Discuta como a dimensão do intervalo de confiança da média é influenciada pelos seguintes
Lista de Exercício 1ª TVC Química Analítica V Teoria Capítulo 7 Tratamento e Avaliação Estatística de Dados 7-3. Discuta como a dimensão do intervalo de confiança da média é influenciada pelos seguintes
Utilização da lei de Lambert-Beer para determinação da concentração de soluções
 Experimental Method Utilização da lei de Lambert-Beer para determinação da concentração de soluções DOI: 10.30609/JETI.2018-2.5930 Thalita A. Canassa 1 *, Anna L. Lamonato 2, Allan V. Ribeiro 2 1 UFMS
Experimental Method Utilização da lei de Lambert-Beer para determinação da concentração de soluções DOI: 10.30609/JETI.2018-2.5930 Thalita A. Canassa 1 *, Anna L. Lamonato 2, Allan V. Ribeiro 2 1 UFMS
QUESTÕES DE FÍSICA MODERNA
 QUESTÕES DE FÍSICA MODERNA 1) Em diodos emissores de luz, conhecidos como LEDs, a emissão de luz ocorre quando elétrons passam de um nível de maior energia para um outro de menor energia. Dois tipos comuns
QUESTÕES DE FÍSICA MODERNA 1) Em diodos emissores de luz, conhecidos como LEDs, a emissão de luz ocorre quando elétrons passam de um nível de maior energia para um outro de menor energia. Dois tipos comuns
RAIOS-X (RAIOS RÖNTGEN)
 RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
Adsorção de Azul de Metileno em Fibras de Algodão
 Adsorção de Azul de Metileno em Fibras de Algodão 1. Introdução A adsorção está intimamente ligada à tensão superficial das soluções e a intensidade desse fenômeno depende da temperatura, da natureza e
Adsorção de Azul de Metileno em Fibras de Algodão 1. Introdução A adsorção está intimamente ligada à tensão superficial das soluções e a intensidade desse fenômeno depende da temperatura, da natureza e
RAIOS-X (RAIOS RÖNTGEN)
 RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
Universidade Federal do Rio Grande do Sul. Instituto de Física Departamento de Física. FIS01184 Física IV-C Área 1 Lista 1
 Universidade Federal do Rio Grande do Sul Instituto de Física Departamento de Física FIS01184 Física IV-C Área 1 Lista 1 1.A luz do Sol no limite superior da atmosfera terrestre tem uma intensidade de
Universidade Federal do Rio Grande do Sul Instituto de Física Departamento de Física FIS01184 Física IV-C Área 1 Lista 1 1.A luz do Sol no limite superior da atmosfera terrestre tem uma intensidade de
Material: 1 lâmpada incandescente 1 resistor 10 Ω 2 multímetros
 Um corpo negro trata se de um objeto que emite, na forma de radiação eletromagnética, toda energia que lhe é fornecida. Embora tal definição seja uma conveniência teórica, muitos objetos na natureza se
Um corpo negro trata se de um objeto que emite, na forma de radiação eletromagnética, toda energia que lhe é fornecida. Embora tal definição seja uma conveniência teórica, muitos objetos na natureza se
Espectrometria de Absorção Atômica. Prof. Luiz Carlos Farmácia UNIP
 Espectrometria de Absorção Atômica Prof. Luiz Carlos Farmácia UNIP Conceito Técnica baseada na atomização de amostras para detecção de elementos químicos individuais. Envolve a medida da absorção de uma
Espectrometria de Absorção Atômica Prof. Luiz Carlos Farmácia UNIP Conceito Técnica baseada na atomização de amostras para detecção de elementos químicos individuais. Envolve a medida da absorção de uma
Sensoriamento remoto 1. Prof. Dr. Jorge Antonio Silva Centeno Universidade Federal do Paraná 2016
 Sensoriamento remoto 1 Prof. Dr. Jorge Antonio Silva Centeno Universidade Federal do Paraná 2016 Súmula princípios e leis da radiação eletromagnética radiação solar conceito de corpo negro REM e sensoriamento
Sensoriamento remoto 1 Prof. Dr. Jorge Antonio Silva Centeno Universidade Federal do Paraná 2016 Súmula princípios e leis da radiação eletromagnética radiação solar conceito de corpo negro REM e sensoriamento
O espectro eletromagnético
 Difração de Raios X O espectro eletromagnético luz visível raios-x microondas raios gama UV infravermelho ondas de rádio Comprimento de onda (nm) Raios Absorção, um fóton de energia é absorvido promovendo
Difração de Raios X O espectro eletromagnético luz visível raios-x microondas raios gama UV infravermelho ondas de rádio Comprimento de onda (nm) Raios Absorção, um fóton de energia é absorvido promovendo
Graduação em Biotecnologia Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Metodologias para quantificar proteínas Qualquer trabalho com proteína deve envolver a quantificação
Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Metodologias para quantificar proteínas Qualquer trabalho com proteína deve envolver a quantificação
PROPRIEDADES TÉRMICAS E ÓPTICAS DOS MATERIAIS
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais PROPRIEDADES TÉRMICAS E ÓPTICAS DOS MATERIAIS PMT 2100 - Introdução à Ciência dos Materiais para Engenharia
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais PROPRIEDADES TÉRMICAS E ÓPTICAS DOS MATERIAIS PMT 2100 - Introdução à Ciência dos Materiais para Engenharia
Meios físicos. Par Trançado (TP) dois fios de cobre isolados
 Meios físicos bit: propaga entre pares de transmissor/receptor enlace físico: o que fica entre transmissor e receptor meio guiado: sinais se propagam em meio sólido: cobre, fibra, coaxial meio não guiado:
Meios físicos bit: propaga entre pares de transmissor/receptor enlace físico: o que fica entre transmissor e receptor meio guiado: sinais se propagam em meio sólido: cobre, fibra, coaxial meio não guiado:
Prática 10 Determinação da constante de equilíbrio entre íons Fe 3+ e SCN -
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 10 Determinação da constante de equilíbrio
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 10 Determinação da constante de equilíbrio
