PROJETO DE RECUPERAÇÃO PARALELA 1º Trimestre
|
|
|
- Elias Belo Guterres
- 6 Há anos
- Visualizações:
Transcrição
1 PROJETO DE RECUPERAÇÃO PARALELA 1º Trimestre Disciplina: Química Série: 1ª série do Ensino Médio Professor(a): Paola Araújo Objetivo: Recuperar o conteúdo referente ao 1º trimestre, mesclando conteúdos trabalhados nas provas mensal, trimestral, simulados e multi. 1. CONTEÚDOS Estados físicos dos materiais. Mudanças de estados físicos com fenômenos físicos presentes no dia a dia. Propriedades específicas dos materiais: Densidade, temperatura de fusão e ebulição. Gráficos e tabelas, que envolvem temperatura de fusão e ebulição e também. Substância pura: simples e composta. Misturas: homogêneas e heterogêneas. Processos de separação de misturas homogêneas e heterogêneas. Leis ponderais da Químicas: de Lavoisier e de Proust. 2. ROTEIRO DE ESTUDO Para estudar os estados físicos e as mudanças de estado físico faça o exercício 1 da lista de recuperação e coloque em seu resumo o mesmo. Estudar as conversões de unidades: massa e volume - Colocar também em seu resumo o quadro abaixo: Para os processos de separação de misturas, resumidamente temos: - Para separa misturas homogêneas: Nome do processo Tipo Baseiase em Usa-se Destilação simples S + L PE Balão e condensador Evaporação S + L PE Tempo Destilação fracionada L + L PE Balão, coluna e condensador
2 - Para separa misturas heterogêneas: Nome do Tipo Baseia-se em Usa-se processo Catação tamanho Mãos Peneiração tamanho Peneira Ventilação Corrente de ar Levigação Corrente de água Imantação magnetismo Imã Dissolução fracionada solubilidade Solvente Flotação solubilidade Líquido com intermediária Decantação L + L S + L Funil de decantação Tempo Filtração S + L S + G tamanho Filtro Centrifugação S + L Centrífuga Os outros conteúdos devem ser estudados através da resolução de exercícios, tanto da lista de recuperação, quanto os exercícios efetuados em aula e em tarefas, bem como a resolução das provas aplicadas no 1º TRI. 3. FORMA DE AVALIAÇÃO: - Durante o período de recuperação o aluno realizará uma lista com exercícios de revisão que terá o valor máximo de 2,0. A lista deverá ser realizada e entregue no dia da prova de REC para o aplicador; - Os alunos participarão de plantões de dúvidas agendados pela coordenação, se necessário. - Realização de Prova escrita com o valor de 8,0 agendada pela coordenação. 4. Lista de exercícios:
3 LISTA DE EXERCÍCIOS DE RECUPERAÇÃO DE QUÍMICA 1 TRIMESTRE Prof. Paola Araújo Série: 1ª série EM Nome: Nº Data: /05/2018 1) Complete o desenho a seguir com o modelo cinéticos de partículas nos determinados estados físicos e ainda: a) Dê o nome dos processos de mudança de estado ocorrida. b) Quais os processos absorvem energia, ou seja, são endotérmicos? c) Quais os processos liberam energia, ou seja, são exotérmicos? 2) Nos quadrinhos da tira, a mãe menciona as fases da água conforme a mudança das estações. Entendendo boneco de neve como sendo boneco de gelo e que com o termo evaporou a mãe se refira à transição água e vapor, pode-se supor que ela imaginou a sequência gelo e água e vapor e água. As mudanças de estado que ocorrem nessa sequência são a) fusão, sublimação e condensação. b) fusão, vaporização e condensação. c) sublimação, vaporização e condensação. d) condensação, vaporização e fusão. e) fusão, vaporização e sublimação.
4 3) Em uma noite de inverno rigoroso uma dona de casa estendeu as roupas recém lavadas no varal, expostas ao tempo. Pela manhã as roupas congelaram, em função do frio intenso. Com a elevação da temperatura no decorrer da manhã, começou a pingar água das roupas, em seguida elas ficaram apenas úmidas, e elas logo estavam secas. Explique as mudanças de estado físico da água observada pela dona de casa. 4) Observe os seguintes fatos e coloque o nome das mudanças de estado físico ocorrida em cada um deles: I) Uma pedra de naftalina deixada no armário. II) III) IV) Uma vasilha com água deixada no freezer. Uma vasilha com água deixada no fogo. O derretimento de um pedaço de chumbo quando aquecido. V) Formação de gotículas na parede de um copo com água gelada. VI) Desaparecimento de álcool deixado em um copo aberto. 5) Uma pessoa comprou um frasco de álcool anidro. Para se certificar de que o conteúdo do frasco não foi fraudado com a adição de água, basta que ela determine, com exatidão, I. a II. o volume III. a temperatura de ebulição IV. a massa Qual ou quais dessas afirmações, são corretas? Justifique sua resposta. 6) Considere as substâncias abaixo: Qual o estado físico das substâncias da tabela acima, quando as mesmas se encontram no Deserto da Arábia, à temperatura de 50 C? 7) Analise as proposições em relação aos gráficos abaixo, coloque V ou F e corrija as afirmativas falsas. I. O gráfico (X) representa uma substância pura. II. O gráfico (Y) representa uma substância pura.
5 III. IV. No gráfico (X) o caminho representado pela letra (b) corresponde à coexistência das fases sólida e líquida. No gráfico (Y) o caminho representado pela letra (b) corresponde apenas à existência da fase sólida. V. No gráfico (X) a mudança de estado físico representada pela letra (d) é a fusão. VI. VII. No gráfico (Y) o caminho representado pela letra (e) corresponde apenas à existência da fase gasosa. Ambos os gráficos são de aquecimento. 8) O gráfico abaixo representa a de três substâncias arbitrariamente designadas como X, Y e Z. Julgue as afirmações abaixo em (V) verdadeiro ou (F) falso. I) A da substância X é maior que a da substância Z. II) III) IV) Nas mesmas condições de temperatura e pressão, massas iguais das substâncias Y e Z, X tem uma massa maior que Y. Nas mesmas condições de temperatura e pressão, volumes iguais das substâncias X e Y, X ocupa um volume menos que Y. A aproximada da substância Y é de 0,5 g/ml. Dados para resolução das questões 8 e 9: A massa e o volume dos materiais A, B e C foram determinados a 30 C; amostras sólidas dos três materiais foram aquecidas, mantendo a temperatura controlada a partir 0 C durante todo este processo de aquecimento. Os gráficos representam os resultados obtidos.
6 9) Com base nas informações disponíveis sobre os materiais A, B e C, e sabendo-se que eles não interagem entre si, a figura que melhor representa uma mistura dos três materiais, a 30 C, é a: a) I b) II c) III d) IV e) V 10) A massa e o volume da amostra de um dos três materiais foram determinados a 30 C, encontrando-se os valores de 25 g e 50 ml, respectivamente. Com base nesta informação e nas figuras I e II é INCORRETO afirmar com relação à amostra: a) O seu ponto de ebulição é de 60 C. b) É constituída do material mais denso entre os três. c) Durante a determinação da massa e do volume, ela se encontrava no estado líquido. d) A 80 C, ela será um gás. e) É constituída do material C. 11) Uma barra de certo metal, de massa igual a 37,8 Kg, foi introduzida num cilindro graduado em litros contendo água. O nível da água contida no cilindro, antes (1) e após (2) a imersão da barra metálica é mostrado na figura. METAIS DENSIDADE (g/cm 3 ) Prata 10,50 Alumínio 2,70 Ferro 7,87 Magnésio 1,74 Chumbo 11,30 Com base em seus conhecimentos de propriedades específicas da matéria, de qual metal a barra é formada? Prove através de cálculos e considere a tabela anterior para responder. 12) Três líquidos (água, benzeno e clorofórmio) foram colocados numa proveta, originando o seguinte aspecto:
7 Temos acima uma tabela com as s de cada líquido. Baseando-se nessas informações e em seus conhecimentos sobre, relacione as substâncias A, B e C com as mencionadas na tabela. Justifique sua resposta. 13) O volume de uma amostra de sólido, pesando mg, é 12,9 cm 3. Calcule a desse sólido e diga em qual dos seguintes líquidos haverá flutuação desse sólido? - tetracloreto de carbono (d = 1,60 g/ cm 3 ); - brometo de metileno (d = 2,50 g/ cm 3 ); - tetrabromo-etano (d = 2,96 g/ cm 3 ); - iodeto de metileno (d = 3,33 g/ cm 3 ) Justifique sua resposta através de cálculos. 14) Observe os sistemas abaixo: Responda ao que se pede para cada sistema (S1, S2 e S3) a) Quantos átomos? b) Quanto elementos químicos? c) Quantas moléculas? d) Qual ou quais são substâncias puras? Justifique e ainda responda se é pura simples ou pura composta. e) Qual ou quais são misturas? Justifique. 15) A maioria dos materiais não é nem elementos puros nem compostos puros; são misturas de substâncias mais simples. Por exemplo, um medicamento, tal como xarope expectorante, é uma mistura de vários ingredientes formulados para conseguir um efeito biológico. Um sistema constituído por açúcar dissolvido em água, limalha de ferro, vapor d água e nitrogênio gasoso pode ser classificado como: a) sistema heterogêneo com 4 fases e 3 componentes. b) sistema homogêneo com 4 fases e 4 componentes.
8 c) sistema heterogêneo com 3 fases e 3 componentes. d) sistema homogêneo com 3 fases e 4 componentes. e) sistema heterogêneo com 3 fases e 4 componentes. 16) Faça um fluxograma para separar a mistura de: areia, água, sal de cozinha, óleo, álcool e pregos de ferro. 17) A água potável é um recurso natural considerado escasso em diversas regiões do nosso planeta. Mesmo em locais onde a água é relativamente abundante, às vezes é necessário submetê-la a algum tipo de tratamento antes de distribuí-la para consumo humano. O tratamento pode, além de outros processos, envolver as seguintes etapas: I. manter a água em repouso por um tempo adequado, para a deposição, no fundo do recipiente, do material em suspensão mecânica. II. remoção das partículas menores, em suspensão, não separáveis pelo processo descrito na etapa I. III. evaporação e condensação da água, para diminuição da concentração de sais (no caso de água salobra ou do mar). Neste caso, pode ser necessária a adição de quantidade conveniente de sais minerais após o processo. Às etapas I, II e III correspondem, respectivamente, os processos de separação denominados a) filtração, decantação e dissolução. b) destilação, filtração e decantação. c) decantação, filtração e dissolução. d) decantação, filtração e destilação. e) filtração, destilação e dissolução. 18) O diagrama a seguir ilustra as etapas de separação de uma mistura. Pela análise do diagrama, todas as afirmativas estão corretas, exceto: a) O sólido B é uma substância pura.
9 b) O filtrado C foi separado por destilação simples. c) O líquido E é uma mistura homogênea. d) O sólido D é uma mistura. e) O material A pode ser uma solução aquosa de cloreto de sódio. 19) Um sistema heterogêneo bifásico é formado por três líquidos diferentes A, B e C. Sabe-se que: - A e B são miscíveis entre si; - C é imiscível com A e com B; - A é mais volátil que B. Com base nessas informações, os métodos mais adequados para separar os três líquidos são a) centrifugação e decantação. b) decantação e fusão fracionada. c) filtração e centrifugação. d) filtração e destilação fracionada. e) decantação e destilação fracionada. 20) Determina (apresentando os cálculos convenientes) os valores de X, Y e Z, de modo a que se verifique a Lei de Lavoisier. 21) Aquecendo-se 21 g de ferro com 15 g de enxofre obtém-se 33 g de sulfeto ferroso, restando 3 g de enxofre. Aquecendo-se 30 g de ferro com 16 g de enxofre obtém-se 44 g de sulfeto ferroso, e restando 2 g de ferro. Demonstrar que esses dados obedecem às leis de Lavoisier (conservação da massa) e de Proust (proporções definidas). 22) Adicionando-se 4,5 g de gás hidrogênio a 31,5 g de gás nitrogênio originam-se 25,5 g de amônia, sobrando ainda nitrogênio que não reagiu. Para se obtiver 85 g de amônia, a quantidade de hidrogênio e de nitrogênio necessária é, respectivamente: a) 15,0 g e 70,0 g. b) 10,6 g e 74,4 g. c) 13,5 g e 71,5 g. d) 1,5 g e 83,5 g. e) 40,0 g e 45,0 g. 23) Completando-se a tabela abaixo, sabendo que o ácido, a base e o sal das duas reações são os mesmos, calcule os valores de X, Y, Z e W.
Exercícios Métodos de Separação. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017
 Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
Tarefa 22 Professor Gustavo
 6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
TAREFA DA SEMANA DE 28 DE ABRIL A 02 DE MAIO
 TAREFA DA SEMANA DE 28 DE ABRIL A 02 DE MAIO QUÍMICA 1ª SÉRIE TEXTO PARA A PRÓXIMA QUESTÃO: DADOS: Constante universal dos gases perfeitos: 0,082 atm.l/mol.k Elemento Número Massa atômico atômica H 1 1,0
TAREFA DA SEMANA DE 28 DE ABRIL A 02 DE MAIO QUÍMICA 1ª SÉRIE TEXTO PARA A PRÓXIMA QUESTÃO: DADOS: Constante universal dos gases perfeitos: 0,082 atm.l/mol.k Elemento Número Massa atômico atômica H 1 1,0
Prof. José Valter SEPARAÇÃO DE MISTURAS
 1 Separação de misturas heterogêneas: LEVIGAÇÃO É usada para componentes de misturas de sólidos, quando um dos componentes é facilmente arrastado pelo líquido. Separação do ouro das areias auríferas Separação
1 Separação de misturas heterogêneas: LEVIGAÇÃO É usada para componentes de misturas de sólidos, quando um dos componentes é facilmente arrastado pelo líquido. Separação do ouro das areias auríferas Separação
Separação de misturas
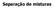 Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
Roteiro de estudos para recuperação trimestral
 Roteiro de estudos para recuperação trimestral Disciplina: Professor (a): QUIMICA DAIANE LIMA Conteúdo: Referência para estudo: Propriedades da matéria, densidade, mudanças de fase da matéria, substâncias
Roteiro de estudos para recuperação trimestral Disciplina: Professor (a): QUIMICA DAIANE LIMA Conteúdo: Referência para estudo: Propriedades da matéria, densidade, mudanças de fase da matéria, substâncias
Sistemas, Substâncias puras e Misturas Separação de Misturas
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
d) Separação Magnética: Esse processo é empregado quando um dos componentes da mistura é atraído por um imã.
 8. PROCESSOS DE SEPARAÇÃO DE MISTURAS A natureza comporta uma imensa mistura de substancias. A maioria dos materiais que utilizamos no cotidiano é composta de misturas. Na maioria das vezes o que interessa,
8. PROCESSOS DE SEPARAÇÃO DE MISTURAS A natureza comporta uma imensa mistura de substancias. A maioria dos materiais que utilizamos no cotidiano é composta de misturas. Na maioria das vezes o que interessa,
Sistemas, Substâncias puras e Misturas Separação de Misturas
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
PROCESSOS DE SEPARAÇÃO. Prof. Ms. George Verçoza
 PROCESSOS DE SEPARAÇÃO Prof. Ms. George Verçoza Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas e é atraído por um ímã. Ex: Ferro e areia.
PROCESSOS DE SEPARAÇÃO Prof. Ms. George Verçoza Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas e é atraído por um ímã. Ex: Ferro e areia.
Plano de Recuperação 1º Semestre EF2-2013
 Professor: Cybelle e Ângela Ano: 9º Objetivos: Proporcionar ao aluno a oportunidade de resgatar os conteúdos trabalhados em Ciências nos quais apresentou defasagens e os quais lhe servirão como pré-requisitos
Professor: Cybelle e Ângela Ano: 9º Objetivos: Proporcionar ao aluno a oportunidade de resgatar os conteúdos trabalhados em Ciências nos quais apresentou defasagens e os quais lhe servirão como pré-requisitos
MÉTODOS DE SEPARAÇÃO DE MISTURAS. 9º ano
 MÉTODOS DE SEPARAÇÃO DE MISTURAS 9º ano Separações de Misturas são utilizadas para decompor misturas de substâncias em um sistema qualquer nos dois ou mais componentes originais. Podem ser para separar
MÉTODOS DE SEPARAÇÃO DE MISTURAS 9º ano Separações de Misturas são utilizadas para decompor misturas de substâncias em um sistema qualquer nos dois ou mais componentes originais. Podem ser para separar
SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS.
 SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS. CAPÍTULOS 6 E 7 Prof.ª Tatiana Lima Substâncias Puras * Conceito Toda matéria cuja fusão e ebulição ocorrem a uma temperatura constante. SIMPLES * Tipos
SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS. CAPÍTULOS 6 E 7 Prof.ª Tatiana Lima Substâncias Puras * Conceito Toda matéria cuja fusão e ebulição ocorrem a uma temperatura constante. SIMPLES * Tipos
PROCESSOS DE SEPARAÇÃO. Jeosafá Lima
 PROCESSOS DE SEPARAÇÃO Jeosafá Lima Misturas homogêneas e heterogêneas Uma mistura é constituída por duas ou mais substâncias, sejam elas simples ou compostas. https://www.youtube.com/watch?v=6jcxdhovkcm
PROCESSOS DE SEPARAÇÃO Jeosafá Lima Misturas homogêneas e heterogêneas Uma mistura é constituída por duas ou mais substâncias, sejam elas simples ou compostas. https://www.youtube.com/watch?v=6jcxdhovkcm
PROCESSOS DE SEPARAÇÃO. Professor Cassio Pacheco
 PROCESSOS DE SEPARAÇÃO Professor Cassio Pacheco SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido
PROCESSOS DE SEPARAÇÃO Professor Cassio Pacheco SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido
Atividade extra. Questão 1 Cecierj Questão 2 Cecierj Ciências da Natureza e suas Tecnologias Química
 Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
Processos de separação de misturas
 Disciplina: Química Prof.: Ivo Turma: IU 23/03/2017 Tema da aula: Métodos de separação de misturas Processos de separação de misturas 1) Separação de misturas heterogêneas Misturas sólido sólido Catação
Disciplina: Química Prof.: Ivo Turma: IU 23/03/2017 Tema da aula: Métodos de separação de misturas Processos de separação de misturas 1) Separação de misturas heterogêneas Misturas sólido sólido Catação
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano
 EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas:
 Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas: Resposta da questão 1: a) Cromo (Cr), manganês (Mn), alumínio ( (A l ) ) e Ferro (Fe). b) A distribuição: 2 2 6 2 6 2 5 1s 2s
Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas: Resposta da questão 1: a) Cromo (Cr), manganês (Mn), alumínio ( (A l ) ) e Ferro (Fe). b) A distribuição: 2 2 6 2 6 2 5 1s 2s
Processos de Separação Misturas Para misturas Heterogêneas
 Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
LOUCOS POR QUÍMICA. PROF. Neif Nagib
 LOUCOS POR QUÍMICA PROF. Neif Nagib SEPARAÇÃO DE MISTURAS Prof. Neif Nagib CATAÇÃO É um método rudimentar baseado na diferença de tamanho e aspecto das partículas de uma mistura de sólidos granulados.
LOUCOS POR QUÍMICA PROF. Neif Nagib SEPARAÇÃO DE MISTURAS Prof. Neif Nagib CATAÇÃO É um método rudimentar baseado na diferença de tamanho e aspecto das partículas de uma mistura de sólidos granulados.
Processos físicos de separação de misturas
 Processos físicos de separação de misturas Misturas heterogêneas sólido-sólido Catação Peneiração Flutuação Separação Magnética Dissolução Fracionada Sublimação CATAÇÃO Baseia-se na identificação visual
Processos físicos de separação de misturas Misturas heterogêneas sólido-sólido Catação Peneiração Flutuação Separação Magnética Dissolução Fracionada Sublimação CATAÇÃO Baseia-se na identificação visual
1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão:
 1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão: Substância PF ( C) PE ( C) Cloro -101,0-34,6 Flúor -219,6-188,1 Bromo -7,2 58,8 Mercúrio -38,8 356,6 Iodo
1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão: Substância PF ( C) PE ( C) Cloro -101,0-34,6 Flúor -219,6-188,1 Bromo -7,2 58,8 Mercúrio -38,8 356,6 Iodo
Processos de Separação Misturas Para misturas Heterogêneas
 Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Ciências Físico-Químicas 7º ano Ficha de trabalho nº14 Separação dos componentes de uma mistura
 Para separar os constituintes de uma mistura pode-se recorrer a diferentes processos de separação. Os processos de separação permitem separar diferentes substâncias que inicialmente foram juntas, mantendo
Para separar os constituintes de uma mistura pode-se recorrer a diferentes processos de separação. Os processos de separação permitem separar diferentes substâncias que inicialmente foram juntas, mantendo
O Que é Química? Pra que serve a Química?²
 O Que é Química? Ciência que estuda as propriedades das substâncias e as leis que regem as suas combinações e decomposições ¹ Pra que serve a Química?² 1 Dicionário Michaelis 2 Figuras retiradas da Web
O Que é Química? Ciência que estuda as propriedades das substâncias e as leis que regem as suas combinações e decomposições ¹ Pra que serve a Química?² 1 Dicionário Michaelis 2 Figuras retiradas da Web
SEPARAÇÃO DE MISTURAS
 SEPARAÇÃO DE MISTURAS Métodos de separação de misturas HETEROGÊNEAS SÓLIDO SÓLIDO: Catação Ventilação Levigação Separação magnética Dissolução fracionada Peneiração Flotação SÓLIDO LÍQUIDO: Decantação
SEPARAÇÃO DE MISTURAS Métodos de separação de misturas HETEROGÊNEAS SÓLIDO SÓLIDO: Catação Ventilação Levigação Separação magnética Dissolução fracionada Peneiração Flotação SÓLIDO LÍQUIDO: Decantação
02- Quais das propriedades a seguir são as mais indicadas para verificar se é pura uma certa amostra sólida de uma substância conhecida?
 PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
Métodos de Separação de Misturas
 Métodos de Separação de Misturas O que é uma mistura? Mistura: associação de duas ou mais substâncias em porções arbitrárias, separáveis por meios mecânicos ou físicos e em que cada um dos componentes
Métodos de Separação de Misturas O que é uma mistura? Mistura: associação de duas ou mais substâncias em porções arbitrárias, separáveis por meios mecânicos ou físicos e em que cada um dos componentes
LOGO. Classificação da matéria. Profa. Samara Garcia
 LOGO Classificação da matéria Profa. Samara Garcia Classificação da matéria Substância pura: matéria formada por unidades químicas iguais, sejam átomos ou moléculas, e assim apresentam propriedades químicas
LOGO Classificação da matéria Profa. Samara Garcia Classificação da matéria Substância pura: matéria formada por unidades químicas iguais, sejam átomos ou moléculas, e assim apresentam propriedades químicas
01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas:
 01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas: a) I é correta. d) I e II são corretas. b) II é correta. e) II e III são corretas. c) III é correta. 05) (UFPE-PE)
01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas: a) I é correta. d) I e II são corretas. b) II é correta. e) II e III são corretas. c) III é correta. 05) (UFPE-PE)
LISTA B QUÍMICA TONI ATITUDE
 LISTA B QUÍMICA TONI ATITUDE Site: www.sosprofessor.xpg.com.br Lei da conservação (lei de Lavoisier)= em um sistema fechado a massa total não varia Lei da proporção constante (lei de Proust)= os elementos
LISTA B QUÍMICA TONI ATITUDE Site: www.sosprofessor.xpg.com.br Lei da conservação (lei de Lavoisier)= em um sistema fechado a massa total não varia Lei da proporção constante (lei de Proust)= os elementos
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
1. Estados físicos da matéria Mudanças de estado Substâncias puras Misturas 4 Exercícios Densidade 6 1.
 1. Estados físicos da matéria 3 1.1 Mudanças de estado 3 1.2 Substâncias puras 4 1.3 Misturas 4 Exercícios 5 1.4 Densidade 6 1.5 Transformação da matéria 6 1.6 Alotropia 6 1.7 Diagramas de fases 6 1.8
1. Estados físicos da matéria 3 1.1 Mudanças de estado 3 1.2 Substâncias puras 4 1.3 Misturas 4 Exercícios 5 1.4 Densidade 6 1.5 Transformação da matéria 6 1.6 Alotropia 6 1.7 Diagramas de fases 6 1.8
ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA
 ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA Nome: Nº Série: 9º EFII Data: / /2015 Professor: Gustavo/Priscila Anual I. Introdução Caro aluno, Neste ano de 2015 você não obteve o mínimo de pontos e, por isso
ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA Nome: Nº Série: 9º EFII Data: / /2015 Professor: Gustavo/Priscila Anual I. Introdução Caro aluno, Neste ano de 2015 você não obteve o mínimo de pontos e, por isso
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017
 III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
Segunda aula de química
 Segunda aula de química Nome: Laísa 17/04/2017 Relembrando... Questão 3: Relembrando... (UNESP 2015) Alguns historiadores da Ciência atribuem ao filósofo pré-socrático. Empédocles a Teoria dos Quatro elementos.
Segunda aula de química Nome: Laísa 17/04/2017 Relembrando... Questão 3: Relembrando... (UNESP 2015) Alguns historiadores da Ciência atribuem ao filósofo pré-socrático. Empédocles a Teoria dos Quatro elementos.
Lista de exercícios 1- Dos processos abaixo, qual pode ser caracterizado como fenômeno físico?
 Colégio FAAT Ensino Fundamental e Médio Lista de exercícios de Química - 1º Bimestre Nome: Ano: 9ºA/B/C Prof. Marcos Miranda N.: / /17 Pensamento cientifico Laboratório químico Estados físicos e as transformações
Colégio FAAT Ensino Fundamental e Médio Lista de exercícios de Química - 1º Bimestre Nome: Ano: 9ºA/B/C Prof. Marcos Miranda N.: / /17 Pensamento cientifico Laboratório químico Estados físicos e as transformações
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011
 ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Classifique as transformações
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Classifique as transformações
SIMPLES SUBSTÂNCIA PURA COMPOSTA HOMOGÊNEO MISTURA HOMOGÊNEA SISTEMA SUBSTÂNCIA PURA HETEROGÊNEO MISTURA HETEROGÊNEA
 Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico que contenha ou não matéria,
Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico que contenha ou não matéria,
ORIENTAÇÃO DE ESTUDOS
 ORIENTAÇÃO DE ESTUDOS RECUPERAÇÃO SEMESTRAL 9º Ano do Ensino Fundamental Disciplina: Química 1. Observe os fatos abaixo: I) Uma pedra de naftalina deixada no armário. II) Uma vasilha com água deixada no
ORIENTAÇÃO DE ESTUDOS RECUPERAÇÃO SEMESTRAL 9º Ano do Ensino Fundamental Disciplina: Química 1. Observe os fatos abaixo: I) Uma pedra de naftalina deixada no armário. II) Uma vasilha com água deixada no
TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma:
 TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma: ROTEIRO E INSTRUÇÕES: Estados físicos da matéria. Mudanças de estado físico. Substâncias e misturas. O trabalho deve ser respondido à
TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma: ROTEIRO E INSTRUÇÕES: Estados físicos da matéria. Mudanças de estado físico. Substâncias e misturas. O trabalho deve ser respondido à
FÍSICA PROFº JAISON MATTEI
 FÍSICA PROFº JAISON MATTEI A MATÉRIA E SUAS TRANSFORMAÇÕES As mudanças de estado físico da água. Diagrama de mudanças de estado físico. 01. Um cientista recebeu uma substância desconhecida, no estado sólido,
FÍSICA PROFº JAISON MATTEI A MATÉRIA E SUAS TRANSFORMAÇÕES As mudanças de estado físico da água. Diagrama de mudanças de estado físico. 01. Um cientista recebeu uma substância desconhecida, no estado sólido,
Tratamento de água. Adaptado de Luciana de Araújo
 Tratamento de água Adaptado de Luciana de Araújo A Química está presente no tratamento da água que chega nas nossas casas? Se sim, como? Estados físicos da água Mudança de estado físico No vídeo... Ouvimos
Tratamento de água Adaptado de Luciana de Araújo A Química está presente no tratamento da água que chega nas nossas casas? Se sim, como? Estados físicos da água Mudança de estado físico No vídeo... Ouvimos
Cópia autorizada. II
 II Sugestões de avaliação Ciências 9 o ano Unidade 1 5 Unidade 1 Nome: Data: 1. Qual é a importância do Sistema Internacional de Unidades (SI)? 2. O que diferencia as propriedades gerais e específicas
II Sugestões de avaliação Ciências 9 o ano Unidade 1 5 Unidade 1 Nome: Data: 1. Qual é a importância do Sistema Internacional de Unidades (SI)? 2. O que diferencia as propriedades gerais e específicas
Exercícios de Revisão
 Aluno: Ano: 9º Revisão: Avaliação Trimestral Disciplina: Física/Química Trimestre: 2º Nome do Professor: Marcos Benfica Exercícios de Revisão 1) Um garçom, desejoso por demonstrar suas habilidades, puxou
Aluno: Ano: 9º Revisão: Avaliação Trimestral Disciplina: Física/Química Trimestre: 2º Nome do Professor: Marcos Benfica Exercícios de Revisão 1) Um garçom, desejoso por demonstrar suas habilidades, puxou
Apostila de Química 12 A Matéria
 Apostila de Química 12 A Matéria 1.0 Átomo x Elemento Átomo é uma partícula fundamental que compõe toda a matéria. Elemento químico é um conjunto de átomos quimicamente iguais (com o mesmo número atômico).
Apostila de Química 12 A Matéria 1.0 Átomo x Elemento Átomo é uma partícula fundamental que compõe toda a matéria. Elemento químico é um conjunto de átomos quimicamente iguais (com o mesmo número atômico).
Unidade São Judas Tadeu
 Unidade São Judas Tadeu Professor: Me. DIOGO LOPES Aluno (a): Ano: 9º Data: / / 2017. Lista de QUÍMICA Orientações: - A lista deverá ser respondida na própria folha impressa ou em folha de papel almaço.
Unidade São Judas Tadeu Professor: Me. DIOGO LOPES Aluno (a): Ano: 9º Data: / / 2017. Lista de QUÍMICA Orientações: - A lista deverá ser respondida na própria folha impressa ou em folha de papel almaço.
Equipamentos e Técnicas laboratoriais: Amostragem e separação de misturas
 MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA CÂMPUS LAGES Equipamentos e Técnicas laboratoriais: Amostragem e separação de
MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA CÂMPUS LAGES Equipamentos e Técnicas laboratoriais: Amostragem e separação de
Química B Intensivo V. 1
 1 Química B Intensivo V. 1 Exercícios 01) B 02) B a) Falsa. O leite in natura é uma mistura heterogênea e não apresenta as mesmas propriedades em toda a extensão da amostra. b) Verdadeira. A gelatina é
1 Química B Intensivo V. 1 Exercícios 01) B 02) B a) Falsa. O leite in natura é uma mistura heterogênea e não apresenta as mesmas propriedades em toda a extensão da amostra. b) Verdadeira. A gelatina é
Tabela 1: Solubilidade em água de alguns compostos presentes na água do mar a 25 ºC
 1. Enem Devido ao seu alto teor de sais, a água do mar é imprópria para o consumo humano e para a maioria dos usos da água doce. No entanto, para a indústria, a água do mar é de grande interesse, uma vez
1. Enem Devido ao seu alto teor de sais, a água do mar é imprópria para o consumo humano e para a maioria dos usos da água doce. No entanto, para a indústria, a água do mar é de grande interesse, uma vez
RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO
 6 anos ETAPA Rec Final 2017 RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO DISCIPLINA PROFESSOR CONTEÚDOS QUÍMICA Claudia Figueiredo Apostila 5 Substâncias puras e misturas. Apostila 6,7 e 8 Separação
6 anos ETAPA Rec Final 2017 RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO DISCIPLINA PROFESSOR CONTEÚDOS QUÍMICA Claudia Figueiredo Apostila 5 Substâncias puras e misturas. Apostila 6,7 e 8 Separação
A MATÉRIA. O que é matéria? MATÉRIA: tudo que tem massa e ocupa espaço, isto é, volume.
 Disciplina: Química Prof.: Guilherme Turma: IU 16/ 03/2017 Tema da aula: A Matéria e suas Propriedades A MATÉRIA O que é matéria? MATÉRIA: tudo que tem massa e ocupa espaço, isto é, volume. - Massa e volume
Disciplina: Química Prof.: Guilherme Turma: IU 16/ 03/2017 Tema da aula: A Matéria e suas Propriedades A MATÉRIA O que é matéria? MATÉRIA: tudo que tem massa e ocupa espaço, isto é, volume. - Massa e volume
EXERCÍCIOS DE QUÍMICA
 INTRODUÇÃO AO ESTUDO DA QUÍMICA FENÔMENOS FÍSICOS E QUÍMICOS SUBSTÂNCIAS PURAS E MISTURAS ATOMICIDADE - ALOTROPIA 1. (UFPE) Em quais das passagens a seguir está ocorrendo transformação química? (1) O reflexo
INTRODUÇÃO AO ESTUDO DA QUÍMICA FENÔMENOS FÍSICOS E QUÍMICOS SUBSTÂNCIAS PURAS E MISTURAS ATOMICIDADE - ALOTROPIA 1. (UFPE) Em quais das passagens a seguir está ocorrendo transformação química? (1) O reflexo
QUÍMICA. Lista de Exercícios / 1º ano. Professora: Geiziane Oliveira Data: / / Aluno(a):
 QUÍMICA Lista de Exercícios / 1º ano. Professora: Geiziane Oliveira Data: / / 2017. Um novo com a tradição de sempre! Aluno(a): 1. (UESC BA) Uma análise da curva de aquecimento dessa amostra de material
QUÍMICA Lista de Exercícios / 1º ano. Professora: Geiziane Oliveira Data: / / 2017. Um novo com a tradição de sempre! Aluno(a): 1. (UESC BA) Uma análise da curva de aquecimento dessa amostra de material
3ªHumanas e Master - Química Prof os João Lins e Alexandre Estevão
 3ªHumanas e Master - Química Prof os João Lins e Alexandre Estevão 1) Um sistema heterogêneo, S, é constituído por uma solução colorida e um sólido branco. O sistema foi submetido ao seguinte esquema de
3ªHumanas e Master - Química Prof os João Lins e Alexandre Estevão 1) Um sistema heterogêneo, S, é constituído por uma solução colorida e um sólido branco. O sistema foi submetido ao seguinte esquema de
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ANO. 1- Considere as temperaturas de fusão e ebulição (pressão = 1 atm) de quatro compostos dados na tabela abaixo.
 EXERCÍCIOS DE CIÊNCIAS PARA O 9 ANO 1- Considere as temperaturas de fusão e ebulição (pressão = 1 atm) de quatro compostos dados na tabela abaixo. Com base nos dados da tabela, responda as questões a seguir.
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ANO 1- Considere as temperaturas de fusão e ebulição (pressão = 1 atm) de quatro compostos dados na tabela abaixo. Com base nos dados da tabela, responda as questões a seguir.
QiD 1 1ª SÉRIE PARTE 3 FÍSICA
 QiD 1 1ª SÉRIE PARTE 3 FÍSICA 1. (1,0) Estime a ordem de grandeza do numero de passos que um atleta dá durante uma prova de maratona, sabendo que seu deslocamento é cerca de 42km e que um passo de um atleta
QiD 1 1ª SÉRIE PARTE 3 FÍSICA 1. (1,0) Estime a ordem de grandeza do numero de passos que um atleta dá durante uma prova de maratona, sabendo que seu deslocamento é cerca de 42km e que um passo de um atleta
Exercitando Ciências Tema: Transformações físicas e o conceito de densidade
 Exercitando Ciências Tema: Transformações físicas e o conceito de densidade Esta lista de exercícios aborda o conteúdo curricular: transformações físicas e o conceito de densidade. 1. O naftaleno, comercialmente
Exercitando Ciências Tema: Transformações físicas e o conceito de densidade Esta lista de exercícios aborda o conteúdo curricular: transformações físicas e o conceito de densidade. 1. O naftaleno, comercialmente
QUÍMICA. Lista de Exercícios / 3º ano. Professora: Geiziane Oliveira Data: /02/2017. Aluno(a):
 QUÍMICA Lista de Exercícios / 3º ano. Professora: Geiziane Oliveira Data: /02/2017. Um novo com a tradição de sempre! Aluno(a): 1. (UESC BA) Uma análise da curva de aquecimento dessa amostra de material
QUÍMICA Lista de Exercícios / 3º ano. Professora: Geiziane Oliveira Data: /02/2017. Um novo com a tradição de sempre! Aluno(a): 1. (UESC BA) Uma análise da curva de aquecimento dessa amostra de material
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
 GOIÂNIA, / / 2017 PROFESSORA: Núbia de Andrade DISCIPLINA: SÉRIE:1º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações: - É fundamental
GOIÂNIA, / / 2017 PROFESSORA: Núbia de Andrade DISCIPLINA: SÉRIE:1º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações: - É fundamental
09) Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão:
 01) Indique a alternativa que completa corretamente as lacunas do seguinte período: Um elemento químico é representado pelo seu..., é identificado pelo número de... e pode apresentar diferentes números
01) Indique a alternativa que completa corretamente as lacunas do seguinte período: Um elemento químico é representado pelo seu..., é identificado pelo número de... e pode apresentar diferentes números
QUÍMICA INORGÂNICA ESTRUTURA ATÔMICA PROF. NEIF NAGIB
 QUÍMICA INORGÂNICA ESTRUTURA ATÔMICA PROF. NEIF NAGIB JONH DALTON: Postulados de Dalton: 1- Toda matéria é formada por entidades extremamente pequenas, os átomos. 2- Os átomos são indivisíveis. 3- O número
QUÍMICA INORGÂNICA ESTRUTURA ATÔMICA PROF. NEIF NAGIB JONH DALTON: Postulados de Dalton: 1- Toda matéria é formada por entidades extremamente pequenas, os átomos. 2- Os átomos são indivisíveis. 3- O número
DIAGRAMA DE FASES. 4) (ITA) Considere as seguintes afirmações relativas aos sistemas descritos a seguir, sob
 DIAGRAMA DE FASES 1) O gráfico abaixo apresenta a variação das pressões de vapor do sulfeto de carbono, metanol, etanol e água em função da temperatura. De acordo com o gráfico, assinale a afirmativa INCORRETA.
DIAGRAMA DE FASES 1) O gráfico abaixo apresenta a variação das pressões de vapor do sulfeto de carbono, metanol, etanol e água em função da temperatura. De acordo com o gráfico, assinale a afirmativa INCORRETA.
1) As substâncias puras benzeno, clorofórmio, hexano e álcool etílico encontram-se em frascos identificados apenas pelas letras A, B, C e D.
 Química Gabarito Avaliação de Sala 1B 1 os anos Décio mar/12 Nome: Nº: Turma: 1) As substâncias puras benzeno, clorofórmio, hexano e álcool etílico encontram-se em frascos identificados apenas pelas letras
Química Gabarito Avaliação de Sala 1B 1 os anos Décio mar/12 Nome: Nº: Turma: 1) As substâncias puras benzeno, clorofórmio, hexano e álcool etílico encontram-se em frascos identificados apenas pelas letras
INSTITUTO GEREMARIO DANTAS COMPONENTE CURRICULAR: QUÍMICA EXERCÍCIOS DE RECUPERAÇÃO PARCIAL 2016
 INSTITUTO GEREMARIO DANTAS Educação Infantil, Ensino Fundamental e Médio Fone: (21) 21087900 Rio de Janeiro RJ www.igd.com.br Aluno(a): 9º Ano: Nº Professora: Lúcia Nascimento COMPONENTE CURRICULAR: QUÍMICA
INSTITUTO GEREMARIO DANTAS Educação Infantil, Ensino Fundamental e Médio Fone: (21) 21087900 Rio de Janeiro RJ www.igd.com.br Aluno(a): 9º Ano: Nº Professora: Lúcia Nascimento COMPONENTE CURRICULAR: QUÍMICA
IX OSEQUIM - Olimpíada Sergipana de Química 2ª Etapa - Modalidade A
 Bom dia aluno! Está é a prova da segunda etapa da IX OSEQUIM, Olimpíada Sergipana de Química, modalidade A, para alunos que se encontram cursando o 1º. Ano do ensino médio em 2015. Confira se a sua prova
Bom dia aluno! Está é a prova da segunda etapa da IX OSEQUIM, Olimpíada Sergipana de Química, modalidade A, para alunos que se encontram cursando o 1º. Ano do ensino médio em 2015. Confira se a sua prova
Curso Pré-ENEM. Química. Profª M.ª Juliana Silva Leite
 Curso Pré-ENEM Química Profª M.ª Juliana Silva Leite O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES
Curso Pré-ENEM Química Profª M.ª Juliana Silva Leite O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES
Cirlei Xavier Bacharel e Mestre em Física pela Universidade Federal da Bahia
 Sônia Lopes SOLUÇÃO CIÊNCIAS DA NATUREZA - 9º ANO Bacharel e Mestre em Física pela Universidade Federal da Bahia Maracás Bahia Abril de 2017 Sumário 1 A matéria e suas propriedades 3 1.1 Construir e aplicar..................................
Sônia Lopes SOLUÇÃO CIÊNCIAS DA NATUREZA - 9º ANO Bacharel e Mestre em Física pela Universidade Federal da Bahia Maracás Bahia Abril de 2017 Sumário 1 A matéria e suas propriedades 3 1.1 Construir e aplicar..................................
Atividade complementar de Química. Como escolher a melhor técnica de separação de misturas?
 Atividade complementar de Química Como escolher a melhor técnica de separação de misturas? Educação de Jovens e Adultos Existem inúmeras técnicas de separação de misturas, algumas muito simples que não
Atividade complementar de Química Como escolher a melhor técnica de separação de misturas? Educação de Jovens e Adultos Existem inúmeras técnicas de separação de misturas, algumas muito simples que não
Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria.
 O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES PROBLEMA HIPÓTESE(S) EXPERIMENTOS CONCLUSÕES CIÊNCIA:
O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES PROBLEMA HIPÓTESE(S) EXPERIMENTOS CONCLUSÕES CIÊNCIA:
LISTA DE EXERCÍCIO PARA A PROVA MENSAL
 Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011
 ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Leia atentamente o texto que
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Leia atentamente o texto que
Sumário. 1 A matéria e suas propriedades Construir e aplicar Fracionamento de misturas Construir e aplicar...
 IEM - INSTITUTO DE EDUCAÇÃO DE MARACÁS ENSINO: ENSINO FUNDAMENTAL II DISCIPLINA: CIÊNCIAS DA NATUREZA PROFESSOR: CIRLEI XAVIER SÉRIE: 9º ANO ANO: 2017 ALUNOS: xxxxxxxxxxxxxxxxxxx MARACÁS BAHIA Sumário
IEM - INSTITUTO DE EDUCAÇÃO DE MARACÁS ENSINO: ENSINO FUNDAMENTAL II DISCIPLINA: CIÊNCIAS DA NATUREZA PROFESSOR: CIRLEI XAVIER SÉRIE: 9º ANO ANO: 2017 ALUNOS: xxxxxxxxxxxxxxxxxxx MARACÁS BAHIA Sumário
Lista de Exercício. 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada sistema?
 Professor: Cassio Pacheco Disciplina: Química 1 Ano Data de entrega: 07/04/2016 Lista de Exercício 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada
Professor: Cassio Pacheco Disciplina: Química 1 Ano Data de entrega: 07/04/2016 Lista de Exercício 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada
Figura 1 Mistura Fonte: Brasil escola
 MISTURAS E TÉCNICAS DE SEPARAÇÃO Figura 1 Mistura Fonte: Brasil escola CONTEÚDOS Tipos de misturas (homogênea e heterogênea) Técnicas de separação dos componentes de uma mistura Substâncias puras simples
MISTURAS E TÉCNICAS DE SEPARAÇÃO Figura 1 Mistura Fonte: Brasil escola CONTEÚDOS Tipos de misturas (homogênea e heterogênea) Técnicas de separação dos componentes de uma mistura Substâncias puras simples
9º Ano/Turma: Data / /2014 VELOCIDADE MÉDIA
 Estudante: Educadora: Daiana Araújo 9º Ano/Turma: Data / /2014 C. Curricular: Ciências Naturais/ Química 1. O quadro seguinte mostra a velocidade média de corrida de alguns animais. ANIMAIS cavalo coelho
Estudante: Educadora: Daiana Araújo 9º Ano/Turma: Data / /2014 C. Curricular: Ciências Naturais/ Química 1. O quadro seguinte mostra a velocidade média de corrida de alguns animais. ANIMAIS cavalo coelho
2-) Observe os sistemas
 SOLUBILIDADE Boa atividade!!! Professora Luciane 1-) Um determinado sal tem coeficiente de solubilidade igual a 34g/100g de água, a 20ºC. Tendo-se 450g de água a 20 ºC, qual a quantidade, em gramas, desse
SOLUBILIDADE Boa atividade!!! Professora Luciane 1-) Um determinado sal tem coeficiente de solubilidade igual a 34g/100g de água, a 20ºC. Tendo-se 450g de água a 20 ºC, qual a quantidade, em gramas, desse
Os processos físicos de separação dos componentes das misturas são escolhidos de acordo com:
 Separação dos componentes de misturas heterogéneas (Pp. 55 a 58) Processos de separação dos componentes de misturas heterogéneas Separação magnética Peneiração Sublimação Dissolução fracionada Decantação
Separação dos componentes de misturas heterogéneas (Pp. 55 a 58) Processos de separação dos componentes de misturas heterogéneas Separação magnética Peneiração Sublimação Dissolução fracionada Decantação
Estado Físico Características Macroscópicas Características Microscópicas
 Sistemas materiais Estados de agregação Estado Físico Características Macroscópicas Características Microscópicas Sólido forma e volume constantes. partículas com arranjo característico; formam estruturas
Sistemas materiais Estados de agregação Estado Físico Características Macroscópicas Características Microscópicas Sólido forma e volume constantes. partículas com arranjo característico; formam estruturas
Química B Extensivo V. 2
 Química B Extensivo V. 2 Exercícios Sistema Componentes Fases Classificação Água + gelo 1 2 Heterogêneo Água + 3 cubos de gelo 1 2 Heterogêneo Açúcar + sal 2 2 Heterogêneo Areia + enxofre + sal 3 3 Heterogêneo
Química B Extensivo V. 2 Exercícios Sistema Componentes Fases Classificação Água + gelo 1 2 Heterogêneo Água + 3 cubos de gelo 1 2 Heterogêneo Açúcar + sal 2 2 Heterogêneo Areia + enxofre + sal 3 3 Heterogêneo
04) (Unicap-PE) Julgue os itens abaixo:
 01) (UNB-DF) Julgue os itens abaixo, indicando aqueles que se referem a propriedades químicas das substâncias e, aqueles que se referem a propriedades físicas das substâncias. 1) A glicose é um sólido
01) (UNB-DF) Julgue os itens abaixo, indicando aqueles que se referem a propriedades químicas das substâncias e, aqueles que se referem a propriedades físicas das substâncias. 1) A glicose é um sólido
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOVO ANGLO DE JABOTICABAL (QUÍMICA) PROFESSOR: JOÃO MEDEIROS
 COLÉGIO NOVO ANGLO DE JABOTICABAL (QUÍMICA) PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: JOÃO MEDEIROS 2012 Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias.
COLÉGIO NOVO ANGLO DE JABOTICABAL (QUÍMICA) PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: JOÃO MEDEIROS 2012 Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias.
Sumário. Química. Frente 1. Frente 2. Capítulo 2: Separação de misturas, fenômenos físicos e químicos 88. Capítulo 4: A Tabela Periódica 96
 Sumário Química Frente 1 Capítulo 2: Separação de misturas, fenômenos físicos e químicos 88 Frente 2 Capítulo 4: A Tabela Periódica 96 QUÍMICA frente 1 ARTHUR HSIEH DREAMSTIME.COM Separação de misturas,
Sumário Química Frente 1 Capítulo 2: Separação de misturas, fenômenos físicos e químicos 88 Frente 2 Capítulo 4: A Tabela Periódica 96 QUÍMICA frente 1 ARTHUR HSIEH DREAMSTIME.COM Separação de misturas,
Composição Densidade (g/mol) Carvão 0,3 0,6 Ossos 1,7 2,0 Areia 2,0 2,4 Solo 2,6 2,8 Pedras 2,6 5,0
 QUÍMICA Arqueologistas usam diferenças de densidade para separar as misturas que eles obtêm por escavação. Indique a opção correta para uma mostra que contém a seguinte composição: Composição Densidade
QUÍMICA Arqueologistas usam diferenças de densidade para separar as misturas que eles obtêm por escavação. Indique a opção correta para uma mostra que contém a seguinte composição: Composição Densidade
QUESTÕES DISSERTATIVAS - GABARITO RESOLVIDO
 Química Avaliação Bimestral 1 o ano Vivian março/ 2011 Nome: Turma: QUESTÕES DISSERTATIVAS - GABARITO RESOLVIDO Substância T. F. (ºC) T.E. (ºC) Densidade a 20ºC (g/cm 3 ) Solubilidade (g/100 g de água)
Química Avaliação Bimestral 1 o ano Vivian março/ 2011 Nome: Turma: QUESTÕES DISSERTATIVAS - GABARITO RESOLVIDO Substância T. F. (ºC) T.E. (ºC) Densidade a 20ºC (g/cm 3 ) Solubilidade (g/100 g de água)
Resoluções das Atividades
 Resoluções das Atividades Sumário Módulo 1 Substâncias puras, misturas e sistemas Análise imediata... 1 Módulo 2 Cálculos químicos... 3 Módulo 3 úmero de oidação (o) idação e redução (redo)... 6 Módulo
Resoluções das Atividades Sumário Módulo 1 Substâncias puras, misturas e sistemas Análise imediata... 1 Módulo 2 Cálculos químicos... 3 Módulo 3 úmero de oidação (o) idação e redução (redo)... 6 Módulo
INTRODUÇÃO À QUÍMICA
 INTRODUÇÃO À QUÍMICA O QUE É QUÍMICA? É a ciência que estuda a matéria, suas propriedades, transformações e interações, bem como a energia envolvida nestes processos. QUAL A IMPORTÂNCIA DA QUÍMICA? Entender
INTRODUÇÃO À QUÍMICA O QUE É QUÍMICA? É a ciência que estuda a matéria, suas propriedades, transformações e interações, bem como a energia envolvida nestes processos. QUAL A IMPORTÂNCIA DA QUÍMICA? Entender
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011
 ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Assinale como verdadeiras
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Assinale como verdadeiras
Ficha de Avaliação Sumativa 5
 Ficha de Avaliação Sumativa 5 DISCIPLINA: Física e Química 7 ºAno de escolaridade 2015/2016 Data: Nome: Turma: N.º Classificação: (%) A Docente: E. E: As respostas às questões deste enunciado devem ser
Ficha de Avaliação Sumativa 5 DISCIPLINA: Física e Química 7 ºAno de escolaridade 2015/2016 Data: Nome: Turma: N.º Classificação: (%) A Docente: E. E: As respostas às questões deste enunciado devem ser
FORMULÁRIO DE DIVULGAÇÃO DO CONTEÚDO DA PROVA FINAL E RECUPERAÇÃO FINAL
 FORMULÁRIO DE DIVULGAÇÃO DO CONTEÚDO DA PROVA FINAL E RECUPERAÇÃO FINAL A) SÉRIE/ANO: 2º Ano Médio B) DISCIPLINA: Química - Enio C) CONTEÚDO A SER EXIGIDO/ORIENTAÇÃO PARA O ESTUDO: SOLUÇÕES: Coeficiente
FORMULÁRIO DE DIVULGAÇÃO DO CONTEÚDO DA PROVA FINAL E RECUPERAÇÃO FINAL A) SÉRIE/ANO: 2º Ano Médio B) DISCIPLINA: Química - Enio C) CONTEÚDO A SER EXIGIDO/ORIENTAÇÃO PARA O ESTUDO: SOLUÇÕES: Coeficiente
PLANO DE ESTUDO TRIMESTRE: 1º
 C O L É G I O K E N N E D Y / R E D E P I T Á G O R A S PLANO DE ESTUDO TRIMESTRE: 1º PLANO DE ESTUDO Nº 02 PROFESSORA: Rose Barbosa DATA DA AVALIAÇÃO: 14/04/2018 DISCIPLINA : Química ANO/SÉRIE: 1º ANO
C O L É G I O K E N N E D Y / R E D E P I T Á G O R A S PLANO DE ESTUDO TRIMESTRE: 1º PLANO DE ESTUDO Nº 02 PROFESSORA: Rose Barbosa DATA DA AVALIAÇÃO: 14/04/2018 DISCIPLINA : Química ANO/SÉRIE: 1º ANO
A diferença entre misturas homogêneas e heterogêneas é o número de fases.
 Separação de misturas e saneamento RESUMO Vamos descrever os diversos processos de separação das misturas heterogêneas e homogêneas. Esses processos são de grande importância e largamente empregados nas
Separação de misturas e saneamento RESUMO Vamos descrever os diversos processos de separação das misturas heterogêneas e homogêneas. Esses processos são de grande importância e largamente empregados nas
Lista de Exercicios 1 o ano Patrícia Cecilia abril/2015
 Química Lista de Exercicios 1 o ano Patrícia Cecilia abril/2015 1. (Ufv 1999 - adaptada) Dadas as afirmativas: I. A molécula de N 2 é diatômica. II. Substância composta é aquela formada por dois ou mais
Química Lista de Exercicios 1 o ano Patrícia Cecilia abril/2015 1. (Ufv 1999 - adaptada) Dadas as afirmativas: I. A molécula de N 2 é diatômica. II. Substância composta é aquela formada por dois ou mais
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. DISCIPLINA:Química SÉRIE: 3º. ALUNO(a): Lista de Exercícios P1 I Bimestre
 GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 3º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 3º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
EXERCÍCIOS SUBSTÂNCIAS E MISTURAS
 EXERCÍCIOS SUBSTÂNCIAS E MISTURAS 1- Considere o sistema e responda as questões: A) Quantos átomos estão representados? B) Quantos elementos químicos há no sistema? C) Quantas moléculas estão representadas
EXERCÍCIOS SUBSTÂNCIAS E MISTURAS 1- Considere o sistema e responda as questões: A) Quantos átomos estão representados? B) Quantos elementos químicos há no sistema? C) Quantas moléculas estão representadas
2-Nos sistemas abaixo, diga quantos átomos, elementos, moléculas e substâncias estão representados:
 LISTA DE EXERCÍCIOS- 1 1-Classifique os processos em físicos ou químicos: a) Sublimação do gelo seco b) Solidificação da água c) Queima da gasolina d) Roupa secando no varal e) Amassar papel - f) Combustão
LISTA DE EXERCÍCIOS- 1 1-Classifique os processos em físicos ou químicos: a) Sublimação do gelo seco b) Solidificação da água c) Queima da gasolina d) Roupa secando no varal e) Amassar papel - f) Combustão
2005 by Pearson Education. Capítulo 01
 QUÍMICA A Ciência Central 9ª Edição Capítulo 1 Introdução: matéria & medida David P. White O estudo da química A perspectiva molecular da química A matéria é o material físico do universo. A matéria é
QUÍMICA A Ciência Central 9ª Edição Capítulo 1 Introdução: matéria & medida David P. White O estudo da química A perspectiva molecular da química A matéria é o material físico do universo. A matéria é
JAMILE ROSA RAMPINELLI
 Química Geral JAMILE ROSA RAMPINELLI Bacharel em Química Ind. UNIVILLE Mestre em Engenharia de Alimentos UFSC Doutora em Engenharia Química UFSC QUÍMICA A Ciência Central 9ª Edição Capítulo 1 Introdução:
Química Geral JAMILE ROSA RAMPINELLI Bacharel em Química Ind. UNIVILLE Mestre em Engenharia de Alimentos UFSC Doutora em Engenharia Química UFSC QUÍMICA A Ciência Central 9ª Edição Capítulo 1 Introdução:
