RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO
|
|
|
- Renato Mota Canto
- 6 Há anos
- Visualizações:
Transcrição
1 RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI Apixabano N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM PVP comprimidos revestidos doseados a 2,5 mg 25, Eliquis 60 comprimidos revestidos doseados a 2,5 mg 20 comprimidos revestidos doseados a 5 mg Bristol-Myers Squibb/Pfizer EEIG 74,25 26, comprimidos revestidos doseados a 5 mg 76,59 Escalão de comparticipação: Regime Geral B (69 %); Data de Comparticipação: 16/06/2014 Estatuto quanto à dispensa: Medicamento Sujeito a Receita Médica Medicamento Genérico: Sim Não Indicações Terapêuticas à data da avaliação: [2,5 mg] Prevenção de acontecimentos tromboembólicos venosos (TEV) em doentes adultos que foram submetidos a artroplastia eletiva da anca ou joelho. [2,5 mg e 5 mg] Prevenção de acidente vascular cerebral e embolismo sistémico em doentes adultos com fibrilhação auricular não valvular com um ou mais fatores de risco tais como acidente vascular cerebral ou acidente isquémico transitório prévios; idade 75 anos; hipertensão; diabetes mellitus; insuficiência cardíaca sintomática (Classe NYHA II) Classificação Farmacoterapêutica: (Sangue - Anticoagulantes e antitrombóticos - Anticoagulantes - Outros anticoagulantes) Código ATC: B01AF02 Nota: Os preços aprovados no âmbito da comparticipação e outras informações podem ser revistos periodicamente. Para informação actualizada, consultar o Infomed. 1. CONCLUSÕES DA AVALIAÇÃO Artroplastia eletiva da anca ou joelho Apixabano demonstrou ser não inferior ao dabigatrano. O tratamento com apixabano demonstrou vantagem económica, pois tem um custo inferior ao do tratamento com dabigatrano. Fibrilhação auricular não valvular Apixabano demonstrou ser não inferior à varfarina, com eventual maior segurança e conveniência M-COMP-021/3 1 / 9
2 posológica. O tratamento com apixabano foi considerado custo-efetivo relativamente à varfarina. 2. AVALIAÇÃO FARMACOTERAPÊUTICA Propriedades farmacológicas Adequação das apresentações à posologia Enquadramento legal Comparador selecionado O apixabano é um inibidor potente, oral, reversível, direto e altamente seletivo para o local ativo do fator Xa. Não necessita de antitrombina III para a atividade antitrombótica. O apixabano inibe o fator Xa livre e ligado ao coágulo e a atividade protrombinase. O apixabano não tem efeito direto na agregação plaquetária, mas indiretamente, inibe a agregação plaquetária induzida pela trombina. Ao inibir o fator Xa, o apixabano previne a formação de trombina e o desenvolvimento do trombo. Para informação adicional sobre o perfil farmacológico e farmacocinético, consultar o RCM disponível no Infomed. Cumpre o estipulado na Portaria n.º 1471/2004, de 21 de dezembro. Alínea d) do n.º 2 do artigo 4.º do Anexo I do Decreto-Lei n.º 48-A/2010, de 13 de maio Justificação, se aplicável Artroplastia electiva da anca ou joelho: Dabigatrano Potencialmente poderiam ser considerados todos os medicamentos com indicação na profilaxia de tromboembolismo venosos (TEV) em cirurgia electiva de anca e joelho; com exceção dos cumarínicos que, embora indicados na profilaxia do TEV não possuírem dados de profilaxia em cirurgia ortopédica. O dabigatrano é inbidor da trombina com mecanismo de acção comparável ao apixabano, que se encontra comparticipado e com perfil de segurança sobreponível; de facto apesar das pequenas diferenças entre o mecanismo de acção do dabigatrano em relação ao apixabano e rivaroxabano, na prática não há diferenças clinicamente. Ao contrário do rivaroxabano: a) a população dos ensaios com dabigatrano aproxima-se mais da do apixabano que a do rivaroxabano, claramente traduzido pela mais similar taxa de eventos hemorrágicos major com a enoxaparina, transversal aos estudos; b) os consumos em DDD de dabigatrano são cerca de 9 vezes maiores que rivaroxabano, traduzindo claramente mais extensa prática clínica; por fim e embora evidentemente menos significativo, c) o dabigatrano apresenta toma diária de duas unidades como o apixabano (o que faz com que haja um risco comparável de falha de toma de comprimidos no tratamento diário). M-COMP-021/3 2 / 9
3 Fibrilhação auricular não valvular: varfarina O VKA mais usado em Portugal, e aquele que é considerado o gold standard dos VKA. O acecumarol é o outro anticoagulante oral VKA disponível em Portugal, mas não é tão usado, enão é o gold standard internacional. As heparinas de baixo peso molecular podem ser usadas temporariamente quando há contraindicação formal para anticoagulação oral com VKA (por exemplo na gravidez), mas não são uma alternativa ao uso continuado, como o são na profilaxia de TEP pós-operatório. Não são usadas na profilaxia de eventos vasculares de forma continuada, nem têm indicação de acordo com a ESC no tratamento crónico. Valor terapêutico acrescentado Artroplastia electiva da anca ou joelho Trata-se de mais um novo anticoagulante com indicações iniciais na profilaxia da TEP em ambiente pericirurgico ortopédico. Os 2 estudos principais apresentados que usaram doses terapêuticas europeias de enoxaparina foram os que levaram à AIM por procedimento centralizado. O dossier que acompanha a proposta de comparticipação foi bem preparado, mas escolheu o rivaroxabano como comparador, não explicando porque não considerou o dabigatrano, que parece o comparador mais adequado. É certo que o dabigatrano apresenta pontos de segurança relevantes, nomeadamente a interferência com os inibidores da P-glicoproteina como a amiodarona, quinidina ou verapamil, e populações especiais - doentes com insuficiência renal e hepática, mas tal deve-se ào plano continuado dedesenvolvimento, e ao facto de na outra (nova) indicação do dabigatrano estes medicamentos serem comummente usados (fibrilhação auricular). O conhecimento destes dados de segurança só reduziram o potencial maleficente do comparador e não são neste momento problemas para o comparador. Além disso, o dabigatrano possui de facto outra indicação há algum tempo, o que aumenta o número de expostos e robustece os dados de segurança do comparador. Neste momento o apixabano já possui também as mesmas indicações, pelo que os dados de segurança do medicamento em avaliação são também mais robustos. A questão da eficácia (ausência de PE / mortes por PE no rivaroxabano, e presença no apixabano e dabigatrano) aproxima mais o apixabano do dabigatrano, embora tal possa apenas dever-se ao facto de a dose inicial poder ser administrada mais tarde no caso do apixabano, aumentando o risco de ocorrência de PE nas primeiras horas, como de facto foi identificado e é discutido no EPAR. M-COMP-021/3 3 / 9
4 Após a análise da contra argumentação do detentor de aim em relação à escolha do comparador dabigatrano vs. rivaroxabano, consideramos que a argumentação apresentada não justifica a mudança de escolha de comparador: tanto pela relação benefício / risco (incluindo a segurança mesmo tendo em conta os eventos major, dado que a população dos diferentes estudos aponta claramente para uma maior similitude de população do apixabano com o dabigatrano, que com o rivaroxabano), como pela questão do mecanismo de acção básico, visto que o que é considerado como padrão é o efeito terapêutico mais do que o mecanismo molecular sensu strictu. No que respeita à segurança, merece ainda ser destacada a informação da tabela de eventos hemorrágicos dos estudos que conduziram à aprovação, salientando o facto de que o estudo em que houve mais (e mais graves) eventos hemorrágicos, a enoxaparina era administrada em 30 mg BID (EPAR SD): M-COMP-021/3 4 / 9
5 O número de unidades utilizadas após a alta depende obviamente dos dias de internamento. Este assunto foi já discutido para o dabigatrano e rivaroxabano, tendo sido adotados os 10 e 30 das de tratamento após a alta. Como não há dados robustos que indiquem que com qualquer dos outros (dabigatrano e mesmo rivaroxabano) há diferença no período de internamento, consideramos a mesma abordagem legítima. O número de doentes a considerar na indicação presente está dependente do número de doentes tratados com artroplastia. O valor previamente definido no parecer de , (avaliação ainda não aceite pelo detentor de AIM) considerava doentes sujeitos a artroplastia anualmente. Estes valores baseavam-se em dados de consumo do dabigatrano e rivaroxabano. Sabemos agora que a maior parte do número de prescrições não foi efetuada por ortopedistas, e - mais M-COMP-021/3 5 / 9
6 importante ainda correspondem a novas prescrições. Estes dados confirmam que a maior parte das prescrições não são usadas na indicação Prevenção de acontecimentos tromboembólicos venosos (TEV) em doentes adultos que foram submetidos a artroplastia eletiva da anca ou joelho. Deste modo é necessário efetuar uma reapreciação do número de doentes a beneficiar dos novos anticoagulantes nesta indicação. A melhor referência encontrada é a do Portal da Saúde, que refere que no ano de 2008, no sistema de saúde português, foram registados mais de episódios. Deste modo consideramos que serão executadas por ano cerca de artroplastias, e assumindo por excesso que todas serão tratadas profilaticamente com os novos anticoagulantes (o que seguramente não acontece neste momento (vestigial prescrição por ortopedistas), então admitimos que nesta indicação cerca de 5000 doentes poderão vir a ser tratados com apixabano. Assim consideramos que no primeiro ano poderão ser tratados 2500 doentes com apixabano e no segundo ano 5000 doentes com apixabano. O tempo de duração estimado neste tratamento para o cálculo económico deve ser de 20 dias. Fibrilhação auricular não valvular Trata-se de um medicamento que tem vantagens em termos de segurança em doentes selecionados. As recomendações internacionais favorecem o uso de VKA (Vitamin K antagonism) em doentes com pelo menos um factor de risco vascular, podendo em alternativa ser usado o ácido acetil salicílico, mas as recomendações referem que os VKA são mais eficazes; por outro lado, para os doentes com 2 ou mais fatores de risco, a recomendação é o uso de VKA. (US: AHA; EU: ESC). Os ensaios clínicos de não inferioridade não nos permitem confirmar superioridade ou vantagem, nomeadamente em termos de segurança, onde mesmo que haja aparente menor número de reações adversas, o n necessário tratar para que ocorra robusta vantagem seria enorme. Assim, mesmo o menor número de eventos hemorrágicos nos ensaios não é garante de ocorrência de vantagem em termos de segurança. Muitos doentes não podem fazer uso da anticoagulação oral por VKA. A ESC em 2012 alargou a recomendação da terapêutica anticoagulante de doentes CHADS2 >=1 para os novos anticoagulantes com esta indicação aprovada na Europa (na altura o rivaroxabano e o dabigatrano). Deste modo, o uso de anticoagulação oral não dependente da vitamina K é considerada uma mais-valia. M-COMP-021/3 6 / 9
7 O requerente refere que Apesar das recomendações terapêuticas, apenas 30 a 50% dos doentes com pelo menos um fator de risco para a ocorrência de AVC decorrente da FA recebe tratamento com anticoagulante (Ogilvie IM. et al 2010). Os antagonistas da vitamina K são, atualmente, a terapêutica utilizada na prática clínica corrente na prevenção do AVC em doentes com FA. No entanto, os medicamentos deste grupo terapêutico estão associados a um elevado risco de ocorrência de hemorragias e de interações com outros medicamentos e alimentos, e são caracterizados por terem uma janela terapêutica muito estreita (Merli GJ. et al 2008). Os doentes que efetuam tratamento com antagonistas da vitamina K têm o inconveniente de efetuar ajustes na dose e avaliação do INR com alguma frequência (Hylek EM. et al 1996; Merli GJ. et al 2009). Mais de 50% dos doentes tratados com antagonistas da vitamina K não conseguem manter o INR controlado (2-3), o que resulta num aumento do risco de ocorrência do AVC e de hemorragias (Baker WL. et al 2009). Cerca de 30 a 50% dos doentes tratados com antagonistas da vitamina K descontinuam a terapêutica ao fim de um ano (Reynolds MR. et al 2006; Nieuwlaat R. et al 2008; Mazzaglia G. et al 2010). Devemos comentar que o estudo de Ogilvie não é específico para a população portuguesa; não obstante, e assumindo que os dados dos médicos sentinela de 2004 eram sobreponíveis aos então publicados na Europa (Eur Heart J 2001; 22: ), as populações serão comparáveis (em 2004 apenas 30 a 40% dos doentes que deviam estar anticoagulados, o estavam). Também o controle do INR dos nossos doentes é um problema constante, seja pela interação medicamentosa da varfarina com outros medicamentos usados no controle dos outros fatores de risco vascular que o doente possui, seja pela dieta. No nosso país há uma variabilidade sazonal significativa no consumo de alimentos frescos como as saladas, que contêm alimentos ricos em vitamina K, e que diminuem a eficácia dos VKA, com necessidade de aumento da dose. Por outro lado, os sistemas eletrónicos de ajuste posológico mediante a variabilidade dos doentes e a atividade metabólica genética, tem permitido (embora discretamente) melhorar a segurança do uso dos VKA. Estes sistemas já são aplicados desde 2007, e portanto considera-se a análise de Ogilvie atualizada. O estudo CV denominado ARISTOTLE é um estudo de não inferioridade (não de equivalência ou superioridade) comparado contra um comparador ativo (varfarina) e não contra placebo, na profilaxia dos eventos vasculares a indicação aprovada por procedimento centralizado. Envolveu doentes. Devemos referir M-COMP-021/3 7 / 9
8 que a escolha da metodologia de não inferioridade se encontra de acordo com as orientações da EMA para desenho de estudos conducentes a aprovação de novas indicações. Recordamos que o apixabano tinha já AIM na dose 2,5 mg bid em outras indicações. O estudo CV (AVERROES) compara apixabano contra aspirina, sendo um estudo de superioridade terapêutica. Apesar de ter sido demonstrada superioridade vs. aspirina nos doentes com contraindicação para VKA, a escolha de aspirina para tratar estes doentes é criticável, na medida em que o clopidogrel pode ser a melhor escolha, pelo menos em parte significativa dos doentes recrutados no estudo. Deste modo a EMA não considerou relevante o estudo de modo a que em doentes com contraindicação para VKA fosse o apixabano o medicamento de primeira escolha. Globalmente, e em relação à indicação aprovada, o apixabano demonstrou no estudo de não inferioridade, ter melhor resultado na profilaxia de eventos vasculares de qualquer tipo, especialmente AVCs (independentemente de se tratarem de isquémicos ou hemorrágicos) e de AVCs isquémicos, aparentemente com vantagem sobre o dabigatrano, no que respeita à protecção de novos enfartes do miocárdio In conclusion, apixaban has shown to be a beneficial anti-thrombotic for the prevention of stroke/se in AF patients, with no extra burden in the bleeding risk compared to VKA. Of note, apixaban treatment was associated with a lower incidence of MI (0.53%/yr) compared to VKA (0.61%), HR =0.88 (95% CI: ). These results compare favourably with dabigatran which was associated with a slightly higher incidence of MI compared to VKA (overall rate in RELY: 0.82, 0.81, and 0.64 % / year for dabigatran 110 mg BID and 150 mg BID and VKA respectively). EMA, AVALIAÇÃO ECONÓMICA Termos de comparação Tipo de análise Vantagem económica Artroplastia eletiva da anca ou joelho: apixabano vs dabigatrano (DDD) Fibrilhação auricular não valvular: apixabano vs varfarina Artroplastia eletiva da anca ou joelho: minimização de custos Fibrilhação auricular não valvular: análise de custo-efetividade e custo-utilidade Artroplastia eletiva da anca ou joelho: O tratamento com apixabano demonstrou vantagem económica, pois tem um custo inferior ao do tratamento com dabigatrano. Fibrilhação auricular não valvular: Para demonstração da vantagem económica foi M-COMP-021/3 8 / 9
9 submetido um estudo de avaliação económica (EAEM) nos seguintes termos: Tipo de estudo: Custo-efetividade/Custo-utilidade Perspetiva: Social Horizonte temporal: tempo de vida dos doentes Endpoints: Anos de vida ganhos e Anos de vida ajustados pela Qualidade. O estudo demonstrou que o medicamento é custo-efetivo. 4. CONDIÇÕES CONTRATUAIS A comparticipação deste medicamento foi condicionada através da celebração de um acordo entre o INFARMED, I.P. e o titular da autorização de introdução no mercado, ao abrigo do disposto no art.º 6.º do regime geral das comparticipações do Estado no preço dos medicamentos, aprovado em anexo ao Decreto-Lei n.º 48-A/2010, de 13 de Maio, na sua redação atual, que define as seguintes obrigações: Respeitar os limites de encargos máximos a suportar pelo Serviço Nacional de Saúde com este medicamento nos termos deste contrato. Providenciar o reembolso do Serviço Nacional de Saúde, nos casos previstos no contrato. 5. REFERÊNCIAS BIBLIOGRÁFICAS 1. Resumo das Características do medicamento Eliquis 2. Gouveia, M; Borges, M. (2013). Estudo de avaliação económica de Eliquis (Apixabano) na Prevenção de Acidente Vascular Cerebral em Doentes com Fibrilhação Auricular. Centro de Estudos de Medicina Baseada na Evidência da Faculdade de Medicina da Universidade de Lisboa e Centro de Estudos Aplicados da Católica Lisbon School of Business and Economics [não publicado]. M-COMP-021/3 9 / 9
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO
 RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI Rotigotina N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM PVP 5943980 doseados
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI Rotigotina N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM PVP 5943980 doseados
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO
 RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM PVP 5586623 5586631 Relvar Ellipta 30
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM PVP 5586623 5586631 Relvar Ellipta 30
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI ustecinumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5279062
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI ustecinumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5279062
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MAIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MAIO HOSPITALAR DCI LAPATINIB N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM Embalagem
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MAIO HOSPITALAR DCI LAPATINIB N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM Embalagem
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI aflibercept N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5487368
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI aflibercept N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5487368
Curso prático de atualização em anticoagulação oral na FANV Casos especiais. Arminda Veiga
 Curso prático de atualização em anticoagulação oral na FANV Casos especiais Arminda Veiga Anticoagulação oral em populações especiais O doente com doença renal O doente com doença com doença coronária
Curso prático de atualização em anticoagulação oral na FANV Casos especiais Arminda Veiga Anticoagulação oral em populações especiais O doente com doença renal O doente com doença com doença coronária
RELATÓRIO PÚBLICO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO EM MEIO HOSPITALAR
 RELATÓRIO PÚBLICO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO EM MEIO HOSPITALAR DCI carfilzomib N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM 5688304 Frasco para injetáveis
RELATÓRIO PÚBLICO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO EM MEIO HOSPITALAR DCI carfilzomib N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM 5688304 Frasco para injetáveis
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO
 RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI sacubitril + valsartan N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM PVP 5682760
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI sacubitril + valsartan N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM PVP 5682760
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO
 RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI palmitato de paliperidona N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM PVP 5683974
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI palmitato de paliperidona N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM PVP 5683974
ELIQUIS (apixabano) Guia do Prescritor
 A notificação de suspeitas de reações adversas após a autorização do medicamento é importante, uma vez que permite uma monitorização contínua da relação benefício-risco do medicamento. Pede-se aos profissionais
A notificação de suspeitas de reações adversas após a autorização do medicamento é importante, uma vez que permite uma monitorização contínua da relação benefício-risco do medicamento. Pede-se aos profissionais
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI Pembrolizumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 1 frasco
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI Pembrolizumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 1 frasco
O Pradaxa é um medicamento que contém a substância ativa etexilato de dabigatran. Está disponível em cápsulas (75, 110 e 150 mg).
 EMA/47517/2015 EMEA/H/C/000829 Resumo do EPAR destinado ao público etexilato de dabigatran Este é um resumo do Relatório Público Europeu de Avaliação (EPAR) relativo ao. O seu objetivo é explicar o modo
EMA/47517/2015 EMEA/H/C/000829 Resumo do EPAR destinado ao público etexilato de dabigatran Este é um resumo do Relatório Público Europeu de Avaliação (EPAR) relativo ao. O seu objetivo é explicar o modo
FA e DAC: Como abordar esse paciente? Ricardo Gusmão
 FA e DAC: Como abordar esse paciente? Ricardo Gusmão Coordenador do Serviço de Cardiologia do H. Barra D Or Médico da U.C. do I.N.Cardiologia ORBIT-AF: Registro anticoagulação Estimated Change in the Number
FA e DAC: Como abordar esse paciente? Ricardo Gusmão Coordenador do Serviço de Cardiologia do H. Barra D Or Médico da U.C. do I.N.Cardiologia ORBIT-AF: Registro anticoagulação Estimated Change in the Number
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO
 RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI Empagliflozina N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM 5607411 5607403 5607429
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI Empagliflozina N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM 5607411 5607403 5607429
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI atalureno N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5644729 suspensão
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI atalureno N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5644729 suspensão
Síndromes Coronários Agudos O que há de novo na terapêutica farmacológica
 Síndromes Coronários Agudos O que há de novo na terapêutica farmacológica J. A. Duarte Unidade de Cardiologia de Intervenção Joaquim Oliveira Serviço de Cardiologia I Centro Hospital de Lisboa Norte Congresso
Síndromes Coronários Agudos O que há de novo na terapêutica farmacológica J. A. Duarte Unidade de Cardiologia de Intervenção Joaquim Oliveira Serviço de Cardiologia I Centro Hospital de Lisboa Norte Congresso
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI Secucinumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5635107
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI Secucinumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5635107
RISCO TROMBO-EMBÓLICO E OS NOVOS ANTICOAGULANTES NA FIBRILHAÇÃO AURICULAR: COMO É A PRÁTICA CLÍNICA?
 RISCO TROMBO-EMBÓLICO E OS NOVOS ANTICOAGULANTES NA FIBRILHAÇÃO AURICULAR: COMO É A PRÁTICA CLÍNICA? Luis Sargento, Hospital de Dia de Insuficiencia Cardiaca, Cardiologia II. Centro Hospitalar Lisboa Norte.
RISCO TROMBO-EMBÓLICO E OS NOVOS ANTICOAGULANTES NA FIBRILHAÇÃO AURICULAR: COMO É A PRÁTICA CLÍNICA? Luis Sargento, Hospital de Dia de Insuficiencia Cardiaca, Cardiologia II. Centro Hospitalar Lisboa Norte.
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO
 RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI Opicapona N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM PVP 5686670 10 cápsulas
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI Opicapona N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM PVP 5686670 10 cápsulas
A fibrilhação auricular (FA) está associada a um aumento importante da morbilidade e
 Resumo A fibrilhação auricular (FA) está associada a um aumento importante da morbilidade e mortalidade por causas cardíacas. A estase a nível auricular verificada durante a arritmia predispõe para a ocorrência
Resumo A fibrilhação auricular (FA) está associada a um aumento importante da morbilidade e mortalidade por causas cardíacas. A estase a nível auricular verificada durante a arritmia predispõe para a ocorrência
Anexo III. Adenda às secções relevantes do Resumo das Características do Medicamento e Folheto Informativo
 Anexo III Adenda às secções relevantes do Resumo das Características do Medicamento e Folheto Informativo Nota: Esta adenda às secções relevantes do Resumo das Características do Medicamento e Folheto
Anexo III Adenda às secções relevantes do Resumo das Características do Medicamento e Folheto Informativo Nota: Esta adenda às secções relevantes do Resumo das Características do Medicamento e Folheto
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI ranibizumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5588744
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI ranibizumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5588744
O doente sob terapêutica anticoagulante oral e a intervenção farmacêutica
 Faculdade de Farmácia da Universidade de Lisboa O doente sob terapêutica anticoagulante oral e a intervenção farmacêutica Cláudia Sofia Godinho André da Graça Oliveira MESTRADO EM FARMÁCIA (ESPECIALIDADE
Faculdade de Farmácia da Universidade de Lisboa O doente sob terapêutica anticoagulante oral e a intervenção farmacêutica Cláudia Sofia Godinho André da Graça Oliveira MESTRADO EM FARMÁCIA (ESPECIALIDADE
Guia do prescritor rivaroxabano
 Guia do prescritor rivaroxabano Informação importante de segurança Bayer Portugal, S.A. Rua Quinta do Pinheiro, nº 5 2794-003 Carnaxide NIF: 500 043256 Versão 5, outubro 2015 Este medicamento está sujeito
Guia do prescritor rivaroxabano Informação importante de segurança Bayer Portugal, S.A. Rua Quinta do Pinheiro, nº 5 2794-003 Carnaxide NIF: 500 043256 Versão 5, outubro 2015 Este medicamento está sujeito
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 Este medicamento está sujeito a monitorização adicional. Isto irá permitir a rápida identificação de nova informação de segurança. Pede-se aos profissionais
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 Este medicamento está sujeito a monitorização adicional. Isto irá permitir a rápida identificação de nova informação de segurança. Pede-se aos profissionais
Coração Outono/Inverno: casos clínicos. O que posso fazer pelo meu doente idoso com: Fibrilhação auricular
 Coração Outono/Inverno: casos clínicos. O que posso fazer pelo meu doente idoso com: Fibrilhação auricular Homem; 79 anos FRCV: Antecedentes: 1. HTA 1. Úlcera duodenal 2. Diabetes mellitus Medicação habitual:
Coração Outono/Inverno: casos clínicos. O que posso fazer pelo meu doente idoso com: Fibrilhação auricular Homem; 79 anos FRCV: Antecedentes: 1. HTA 1. Úlcera duodenal 2. Diabetes mellitus Medicação habitual:
Anticoagulação no ciclo. Adolfo Liao
 Anticoagulação no ciclo gravídico-puerperal Adolfo Liao Agenda Razão de mortalidade materna (óbitos maternos / 100.000 NV) Sistema de Informações sobre Mortalidade Mortalidade Materna OMS, 2014 embolia
Anticoagulação no ciclo gravídico-puerperal Adolfo Liao Agenda Razão de mortalidade materna (óbitos maternos / 100.000 NV) Sistema de Informações sobre Mortalidade Mortalidade Materna OMS, 2014 embolia
Novos anticoagulantes orais no tromboembolismo venoso e fibrilhação auricular
 ARTIGO DE REVISÃO Novos anticoagulantes orais no tromboembolismo venoso e fibrilhação auricular New oral anticoagulants in the treatment of venous thromboembolism and atrial fibrillation Centro Hospitalar
ARTIGO DE REVISÃO Novos anticoagulantes orais no tromboembolismo venoso e fibrilhação auricular New oral anticoagulants in the treatment of venous thromboembolism and atrial fibrillation Centro Hospitalar
Conclusões científicas
 ANEXO II CONCLUSÕES CIENTÍFICAS E FUNDAMENTOS PARA A ALTERAÇÃO DO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO, DA ROTULAGEM E DO FOLHETO INFORMATIVO APRESENTADOS PELA AGÊNCIA EUROPEIA DE MEDICAMENTOS 14
ANEXO II CONCLUSÕES CIENTÍFICAS E FUNDAMENTOS PARA A ALTERAÇÃO DO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO, DA ROTULAGEM E DO FOLHETO INFORMATIVO APRESENTADOS PELA AGÊNCIA EUROPEIA DE MEDICAMENTOS 14
Manuseio Peri-operatório do Doente medicado com Outros Anticoagulantes
 Manuseio Peri-operatório do Doente medicado com Outros Anticoagulantes I. Bloqueio do Neuroeixo e Outros Anticoagulantes a) Bloqueio do Neuroeixo e HEPARINAS NÃO FRACIONADAS (HNF) Tabela 1. HNF-Tempos
Manuseio Peri-operatório do Doente medicado com Outros Anticoagulantes I. Bloqueio do Neuroeixo e Outros Anticoagulantes a) Bloqueio do Neuroeixo e HEPARINAS NÃO FRACIONADAS (HNF) Tabela 1. HNF-Tempos
Avaliação Económica. Bruno Costa Economista. DEMPS/AER, INFARMED, I.P. Lisboa, 19 de Junho de 2008
 Avaliação Económica Bruno Costa Economista DEMPS/AER, INFARMED, I.P. Lisboa, 19 de Junho de 2008 1 Procedimento de avaliação Parecer negativo Mais valia vs comparador (VTA) Equivalência clínica Análise
Avaliação Económica Bruno Costa Economista DEMPS/AER, INFARMED, I.P. Lisboa, 19 de Junho de 2008 1 Procedimento de avaliação Parecer negativo Mais valia vs comparador (VTA) Equivalência clínica Análise
FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR
 FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR Venorix 100, 100 mg /2 ml, Solução injectável Venorix 200, 200 mg /2 ml, Solução injectável Venorix 300, 300 mg /3 ml, Solução injectável Sulfato de dermatano
FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR Venorix 100, 100 mg /2 ml, Solução injectável Venorix 200, 200 mg /2 ml, Solução injectável Venorix 300, 300 mg /3 ml, Solução injectável Sulfato de dermatano
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI ranibizumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5588744
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI ranibizumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5588744
Anexo III Resumo das características do medicamento, rotulagem e folheto informativo
 Anexo III Resumo das características do medicamento, rotulagem e folheto informativo Nota: Estas alterações ao Resumo das Características do Medicamento e ao Folheto Informativo são válidas no momento
Anexo III Resumo das características do medicamento, rotulagem e folheto informativo Nota: Estas alterações ao Resumo das Características do Medicamento e ao Folheto Informativo são válidas no momento
Aplicação de metodologias quantitativas para avaliação da relação benefício/risco: caso de estudo com rosiglitazona e pioglitazona
 Aplicação de metodologias quantitativas para avaliação da relação benefício/risco: caso de estudo com rosiglitazona e pioglitazona Diogo Mendes 1,2, Carlos Alves 1,2, Francisco Batel Marques 1,2 1. Unidade
Aplicação de metodologias quantitativas para avaliação da relação benefício/risco: caso de estudo com rosiglitazona e pioglitazona Diogo Mendes 1,2, Carlos Alves 1,2, Francisco Batel Marques 1,2 1. Unidade
ANTICOAGULANTES ORAIS DIRETOS. Manuel Morgado Lisboa, 17 de Maio 2019
 ANTICOAGULANTES ORAIS DIRETOS Manuel Morgado Lisboa, 17 de Maio 2019 1 Conflito de interesses O autor não tem nada a declarar. Manuel Morgado mmorgado@fcsaude.ubi.pt Lisboa, 17 de Maio 2019 2 Índice Anticoagulantes
ANTICOAGULANTES ORAIS DIRETOS Manuel Morgado Lisboa, 17 de Maio 2019 1 Conflito de interesses O autor não tem nada a declarar. Manuel Morgado mmorgado@fcsaude.ubi.pt Lisboa, 17 de Maio 2019 2 Índice Anticoagulantes
INFARMED Gabinete Jurídico e Contencioso
 Procede à quarta alteração ao Decreto-Lei n.º 48-A/2010, de 13 de maio, que aprova o regime geral das comparticipações do Estado no preço dos medicamentos, e à terceira alteração ao Decreto-Lei n.º 112/2011,
Procede à quarta alteração ao Decreto-Lei n.º 48-A/2010, de 13 de maio, que aprova o regime geral das comparticipações do Estado no preço dos medicamentos, e à terceira alteração ao Decreto-Lei n.º 112/2011,
Farmacoterapia do Sistema Hematopoiético. Prof. Dr. Marcelo Polacow Bisson
 Farmacoterapia do Sistema Hematopoiético Prof. Dr. Marcelo Polacow Bisson Aspectos Importantes da Coagulação São três os fatores importantes para coagulação: Parede do vaso Atividade plaquetária Fatores
Farmacoterapia do Sistema Hematopoiético Prof. Dr. Marcelo Polacow Bisson Aspectos Importantes da Coagulação São três os fatores importantes para coagulação: Parede do vaso Atividade plaquetária Fatores
CONJUNTO DE DADOS DUQUE PARA FRACTURA GRAVE DA ANCA
 Inclusão Definições Fractura da anca CONJUNTO DE DADOS DUQUE PARA FRACTURA GRAVE DA ANCA Critérios de diagnóstico Os doentes com idade superior a 65 anos que preencham os seguintes três critérios de diagnóstico
Inclusão Definições Fractura da anca CONJUNTO DE DADOS DUQUE PARA FRACTURA GRAVE DA ANCA Critérios de diagnóstico Os doentes com idade superior a 65 anos que preencham os seguintes três critérios de diagnóstico
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI crizotinib N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5479316
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI crizotinib N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 5479316
Quais as novas opções para tratamento da doença tromboembólica venosa
 Quais as novas opções para tratamento da doença tromboembólica venosa Daniel Mendes Pinto Cirurgia Vascular Hospital Mater Dei Hospital Felício Rocho Disponível em www.vascularbh.com.br Não tenho conflito
Quais as novas opções para tratamento da doença tromboembólica venosa Daniel Mendes Pinto Cirurgia Vascular Hospital Mater Dei Hospital Felício Rocho Disponível em www.vascularbh.com.br Não tenho conflito
Os Novos Anticoagulantes Orais no Tratamento do Tromboembolismo Pulmonar
 Faculdade de Medicina da Universidade de Lisboa Trabalho Final do Mestrado Integrado em Medicina Os Novos Anticoagulantes Orais no Tratamento do Tromboembolismo Pulmonar Clínica Universitária de Cardiologia
Faculdade de Medicina da Universidade de Lisboa Trabalho Final do Mestrado Integrado em Medicina Os Novos Anticoagulantes Orais no Tratamento do Tromboembolismo Pulmonar Clínica Universitária de Cardiologia
Deliberação n.º 1028/2009, de 7 de Janeiro (DR, 2.ª série, n.º 68, de 7 de Abril de 2009)
 (DR, 2.ª série, n.º 68, de 7 de Abril de 2009) Instruções aos requerentes de pedidos de comparticipação de medicamentos de uso humano O crescente desenvolvimento do mercado de medicamentos genéricos nos
(DR, 2.ª série, n.º 68, de 7 de Abril de 2009) Instruções aos requerentes de pedidos de comparticipação de medicamentos de uso humano O crescente desenvolvimento do mercado de medicamentos genéricos nos
NOVOS ANTICOAGULANTES ORAIS CONTROLO DA HEMORRAGIA IATROGÉNICA
 Serviço de Sangue/Medicina Transfusional Edgar Cardoso Interno do 4º ano do Internato Complementar de Imuno-hemoterapia Diretora de Serviço: Drª Anabela Barradas Orientador de Formação: Dr António Barra
Serviço de Sangue/Medicina Transfusional Edgar Cardoso Interno do 4º ano do Internato Complementar de Imuno-hemoterapia Diretora de Serviço: Drª Anabela Barradas Orientador de Formação: Dr António Barra
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Eliquis 2,5 mg comprimidos revestidos por película 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada comprimido revestido por película
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Eliquis 2,5 mg comprimidos revestidos por película 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada comprimido revestido por película
Novos Antiagregantes e Anticoagulantes Orais Manejo na endoscopia - maio 2015
 Um grande número de pacientes tem feito uso de antiagregação plaquetária e anticoagulação contínuas em situações clínicas como fibrilação atrial, implante de valvas mecânicas, trombose venosa profunda
Um grande número de pacientes tem feito uso de antiagregação plaquetária e anticoagulação contínuas em situações clínicas como fibrilação atrial, implante de valvas mecânicas, trombose venosa profunda
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI Pertuzumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 1 frasco
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI Pertuzumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 1 frasco
NOVOS ANTICOAGULANTES ORAIS: POR QUE EU ESCOLHO MARCO TULIO ARAUJO PEDATELLA
 NOVOS ANTICOAGULANTES ORAIS: POR QUE EU ESCOLHO MARCO TULIO ARAUJO PEDATELLA DECLARAÇÃO DE CONFLITOS DE INTERESSE Declaro ter recebido honorários referente palestras: Boehringer Ingelheim, Pfizer. Declaro
NOVOS ANTICOAGULANTES ORAIS: POR QUE EU ESCOLHO MARCO TULIO ARAUJO PEDATELLA DECLARAÇÃO DE CONFLITOS DE INTERESSE Declaro ter recebido honorários referente palestras: Boehringer Ingelheim, Pfizer. Declaro
Eliquis apixabana I - IDENTIFICAÇÃO DO MEDICAMENTO
 Eliquis I - IDENTIFICAÇÃO DO MEDICAMENTO APRESENTAÇÕES Eliquis () é apresentado na forma farmacêutica de comprimidos revestidos de 2,5 mg ou 5 mg em embalagens contendo 20 ou 60 comprimidos. USO ORAL USO
Eliquis I - IDENTIFICAÇÃO DO MEDICAMENTO APRESENTAÇÕES Eliquis () é apresentado na forma farmacêutica de comprimidos revestidos de 2,5 mg ou 5 mg em embalagens contendo 20 ou 60 comprimidos. USO ORAL USO
Portaria n.º 195-A/2015, de 30 de junho 1 Aprova o procedimento comum de comparticipação e de avaliação prévia de medicamentos
 1 Aprova o procedimento comum de comparticipação e de avaliação prévia de medicamentos O Decreto-Lei n.º 97/2015, de 1 de junho, criou o Sistema Nacional de Avaliação de Tecnologias da saúde e estabeleceu
1 Aprova o procedimento comum de comparticipação e de avaliação prévia de medicamentos O Decreto-Lei n.º 97/2015, de 1 de junho, criou o Sistema Nacional de Avaliação de Tecnologias da saúde e estabeleceu
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Eliquis 2,5 mg comprimidos revestidos por película 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada comprimido revestido por película
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Eliquis 2,5 mg comprimidos revestidos por película 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada comprimido revestido por película
NOVOS ANTICICOAGULANTES
 NOVOS ANTI NOVOS ANTICICOAGULANTES COAGULANTES TROMBOEMBOLISMO VENOSO O tromboembolismo venoso (TEV) é a terceira causa de mortalidade cardiovascular no mundo. O TEV, que é a formação de coágulos no sangue,
NOVOS ANTI NOVOS ANTICICOAGULANTES COAGULANTES TROMBOEMBOLISMO VENOSO O tromboembolismo venoso (TEV) é a terceira causa de mortalidade cardiovascular no mundo. O TEV, que é a formação de coágulos no sangue,
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MAIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MAIO HOSPITALAR DCI Micafungina N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 1 frasco
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MAIO HOSPITALAR DCI Micafungina N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM 1 frasco
 AVC Sangramento Estratificar os riscos de AVC e de Sangramento maior EHRA/ESC Position Paper : Lip GYH et al. Europace 2011;13:723 746. Reações Adversas à Warfarina Tromboprofilaxia
AVC Sangramento Estratificar os riscos de AVC e de Sangramento maior EHRA/ESC Position Paper : Lip GYH et al. Europace 2011;13:723 746. Reações Adversas à Warfarina Tromboprofilaxia
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Eliquis 2,5 mg comprimidos revestidos por película 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada comprimido revestido por película
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Eliquis 2,5 mg comprimidos revestidos por película 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada comprimido revestido por película
Intoxicação por anticoagulantes. Pos-Graduação em Medicina de Emergência -Sílvia Coelho, Nefrologista e Intensivista
 Intoxicação por anticoagulantes Pos-Graduação em Medicina de Emergência -Sílvia Coelho, Nefrologista e Intensivista Caso Clínico 1 Homem, 65 anos AP: HTA, obesidade, dislipidémia, TVP há 3 meses Medicação
Intoxicação por anticoagulantes Pos-Graduação em Medicina de Emergência -Sílvia Coelho, Nefrologista e Intensivista Caso Clínico 1 Homem, 65 anos AP: HTA, obesidade, dislipidémia, TVP há 3 meses Medicação
Deliberação n.º 638/98, de 3 de Dezembro (DR, 2.ª série, n.º 294, de 22 de Dezembro de 1998)
 (DR, 2.ª série, n.º 294, de 22 de Dezembro de 1998) Instruções aos requerentes de pedidos de comparticipação de medicamentos para uso humano (Revogado pela Deliberação n.º 1028/2009, de 7 de Janeiro) Para
(DR, 2.ª série, n.º 294, de 22 de Dezembro de 1998) Instruções aos requerentes de pedidos de comparticipação de medicamentos para uso humano (Revogado pela Deliberação n.º 1028/2009, de 7 de Janeiro) Para
Trombocitopenia induzida pela heparina
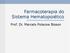
 Trombocitopenia induzida pela heparina Novembro 2012 ULSM Hospital Pedro Hispano, Matosinhos Distinguir Terapêutica curta duração: Profilática Emergência Heparina via parentérica Heparinas baixo peso molecular
Trombocitopenia induzida pela heparina Novembro 2012 ULSM Hospital Pedro Hispano, Matosinhos Distinguir Terapêutica curta duração: Profilática Emergência Heparina via parentérica Heparinas baixo peso molecular
RELATÓRIO PÚBLICO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO EM MEIO HOSPITALAR
 RELATÓRIO PÚBLICO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO EM MEIO HOSPITALAR DCI brodalumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM 5721956 Kyntheum 2 unidades de 1,5ml/
RELATÓRIO PÚBLICO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO EM MEIO HOSPITALAR DCI brodalumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM 5721956 Kyntheum 2 unidades de 1,5ml/
Eliquis. Comprimidos revestidos. 2,5mg e 5,0mg
 Eliquis Comprimidos revestidos 2,5mg e 5,0mg APRESENTAÇÕES ELIQUIS (apixabana) é apresentado na forma farmacêutica de comprimidos revestidos de 2,5 mg em embalagens contendo 20 ou 60 comprimidos. ELIQUIS
Eliquis Comprimidos revestidos 2,5mg e 5,0mg APRESENTAÇÕES ELIQUIS (apixabana) é apresentado na forma farmacêutica de comprimidos revestidos de 2,5 mg em embalagens contendo 20 ou 60 comprimidos. ELIQUIS
Dimensão Segurança do Doente Check-list Procedimentos de Segurança
 Check-list Procedimentos de Segurança 1. 1.1 1.2 Cultura de Segurança Existe um elemento(s) definido(s) com responsabilidade atribuída para a segurança do doente Promove o trabalho em equipa multidisciplinar
Check-list Procedimentos de Segurança 1. 1.1 1.2 Cultura de Segurança Existe um elemento(s) definido(s) com responsabilidade atribuída para a segurança do doente Promove o trabalho em equipa multidisciplinar
Despacho n.º /2000, de 10 de Agosto (DR, 2.ª Série, n.º 198, de 28 de Agosto de 2000) (Revogado pelo Despacho n.º B/2001, de 31 de Maio)
 Despacho n.º 17 495/2000, de 10 (DR, 2.ª Série, n.º 198, de 28 de 2000) (Revogado pelo Despacho n.º 13 484-B/2001, de 31 de Maio) De acordo com o artigo 60.º do Decreto-Lei n.º 72/91, de 8 de Fevereiro,
Despacho n.º 17 495/2000, de 10 (DR, 2.ª Série, n.º 198, de 28 de 2000) (Revogado pelo Despacho n.º 13 484-B/2001, de 31 de Maio) De acordo com o artigo 60.º do Decreto-Lei n.º 72/91, de 8 de Fevereiro,
Trombose Associada ao Cancro. Epidemiologia / Dados Nacionais
 Trombose Associada ao Cancro Epidemiologia / Dados Nacionais Miguel Barbosa Serviço de Oncologia Médica Centro Hospitalar Trás-os-Montes e Alto Douro 12 Outubro de 2018 Dados Internacionais O diagnóstico
Trombose Associada ao Cancro Epidemiologia / Dados Nacionais Miguel Barbosa Serviço de Oncologia Médica Centro Hospitalar Trás-os-Montes e Alto Douro 12 Outubro de 2018 Dados Internacionais O diagnóstico
2009/2010. Susana Patrícia Dias de Sá Terapêutica Anticoagulante da Fibrilação Auricular
 2009/2010 Susana Patrícia Dias de Sá Terapêutica Anticoagulante da Fibrilação Auricular Abril 2010 Susana Patrícia Dias de Sá Terapêutica Anticoagulante da Fibrilação Auricular Mestrado Integrado em Medicina
2009/2010 Susana Patrícia Dias de Sá Terapêutica Anticoagulante da Fibrilação Auricular Abril 2010 Susana Patrícia Dias de Sá Terapêutica Anticoagulante da Fibrilação Auricular Mestrado Integrado em Medicina
Anexo II. Conclusões científicas
 Anexo II Conclusões científicas 36 Conclusões científicas A enoxaparina sódica é uma heparina de baixo peso molecular comercializada sob a designação comercial Lovenox e nomes associados. Este anticoagulante
Anexo II Conclusões científicas 36 Conclusões científicas A enoxaparina sódica é uma heparina de baixo peso molecular comercializada sob a designação comercial Lovenox e nomes associados. Este anticoagulante
Ictiose Doenças Raras Eurico Castro Alves Presidente do Conselho Diretivo
 Ictiose Doenças Raras Eurico Castro Alves Presidente do Conselho Diretivo INFARMED - Autoridade Nacional do Medicamento e Produtos de Saúde, I.P. 09 de abril de 2014 Ictiose - caracterização Grupo heterogéneo
Ictiose Doenças Raras Eurico Castro Alves Presidente do Conselho Diretivo INFARMED - Autoridade Nacional do Medicamento e Produtos de Saúde, I.P. 09 de abril de 2014 Ictiose - caracterização Grupo heterogéneo
Formulário para Aprovação de Preços de Medicamentos Não Genéricos INSTRUÇÕES DE PREENCHIMENTO
 Formulário para Aprovação de Preços de Medicamentos Não Genéricos INSTRUÇÕES DE PREENCHIMENTO Bloco 1 A informação a prestar refere-se à especialidade farmacêutica em causa no pedido de aprovação de preços
Formulário para Aprovação de Preços de Medicamentos Não Genéricos INSTRUÇÕES DE PREENCHIMENTO Bloco 1 A informação a prestar refere-se à especialidade farmacêutica em causa no pedido de aprovação de preços
RESPOSTA RÁPIDA 107/2013
 RESPOSTA RÁPIDA 107/2013 SOLICITANTE Emerson de Oliveira Corrêa Juiz de Direito Município de Candeias - MG NÚMERO DO PROCESSO 0120.13.000607-1 DATA 15/06/2013 SOLICITAÇÃO O autor, pessoa de poucos recursos
RESPOSTA RÁPIDA 107/2013 SOLICITANTE Emerson de Oliveira Corrêa Juiz de Direito Município de Candeias - MG NÚMERO DO PROCESSO 0120.13.000607-1 DATA 15/06/2013 SOLICITAÇÃO O autor, pessoa de poucos recursos
Dissertação Artigo de Revisão Bibliográfica Mestrado Integrado em Medicina 2014/2015
 Dissertação Artigo de Revisão Bibliográfica Mestrado Integrado em Medicina 2014/2015 TERAPÊUTICA ANTITROMBÓTICA NOS DOENTES COM FIBRILHAÇÃO AURICULAR SITUAÇÃO ATUAL Autor: Francisca Araújo Alves Estudante
Dissertação Artigo de Revisão Bibliográfica Mestrado Integrado em Medicina 2014/2015 TERAPÊUTICA ANTITROMBÓTICA NOS DOENTES COM FIBRILHAÇÃO AURICULAR SITUAÇÃO ATUAL Autor: Francisca Araújo Alves Estudante
IMPORTÂNCIA DO ACOMPANHAMENTO FARMACOTERAPÊUTICO DE PACIENTES QUE UTILIZAM VARFARINA
 IMPORTÂNCIA DO ACOMPANHAMENTO FARMACOTERAPÊUTICO DE PACIENTES QUE UTILIZAM VARFARINA Sandra Navarro Ferro, Suleimy Marinho Fernandes, Stela Ramirez de Oliveira Faculdade Alfredo Nasser sandra.tecpav@gmail.com
IMPORTÂNCIA DO ACOMPANHAMENTO FARMACOTERAPÊUTICO DE PACIENTES QUE UTILIZAM VARFARINA Sandra Navarro Ferro, Suleimy Marinho Fernandes, Stela Ramirez de Oliveira Faculdade Alfredo Nasser sandra.tecpav@gmail.com
Dilemas da Anticoagulação na Fibrilação Atrial
 Dilemas da Anticoagulação na Fibrilação Atrial Dra Olga F. de Souza Doutora em Cardiologia pela UFRJ Coordenadora do Serviço de Arritmia e Eletrofisiologia da Rede D or São Luiz olga.souza@rededor.com.br
Dilemas da Anticoagulação na Fibrilação Atrial Dra Olga F. de Souza Doutora em Cardiologia pela UFRJ Coordenadora do Serviço de Arritmia e Eletrofisiologia da Rede D or São Luiz olga.souza@rededor.com.br
Caso clínico. S.A.G, 35 anos
 Caso clínico S.A.G, 35 anos Negra, casada, prendas domésticas. Natural de Poços de Caldas - MG, Procedente de Botucatu - SP. G4 P3 A0 C0 DUM: 23/07/2014 1º US: 27/10/2014 (14s 1d DUM correta) IG: 32s 5d
Caso clínico S.A.G, 35 anos Negra, casada, prendas domésticas. Natural de Poços de Caldas - MG, Procedente de Botucatu - SP. G4 P3 A0 C0 DUM: 23/07/2014 1º US: 27/10/2014 (14s 1d DUM correta) IG: 32s 5d
INFARMED Gabinete Jurídico e Contencioso
 Decreto-Lei n.º 195/2006, de 3 de Outubro Estabelece as regras a que obedece a avaliação prévia, para efeitos da sua aquisição pelos hospitais do Serviço Nacional de Saúde, de medicamentos que devam ser
Decreto-Lei n.º 195/2006, de 3 de Outubro Estabelece as regras a que obedece a avaliação prévia, para efeitos da sua aquisição pelos hospitais do Serviço Nacional de Saúde, de medicamentos que devam ser
Rastrear Medicamentos em Ambiente Hospitalar
 Rastrear Medicamentos em Ambiente Hospitalar Como melhorar as operações logísticas e garantir a segurança do paciente no circuito da Farmácia Hospitalar? Sofia Valongo Vasco Antunes Pereira 25 Junho 2015
Rastrear Medicamentos em Ambiente Hospitalar Como melhorar as operações logísticas e garantir a segurança do paciente no circuito da Farmácia Hospitalar? Sofia Valongo Vasco Antunes Pereira 25 Junho 2015
ANTICOAGULANTES ORAIS NÃO ANTAGONISTAS DA VITAMINA K (nacos)
 ANTICOAGULANTES ORAIS NÃO ANTAGONISTAS DA VITAMINA K (nacos) ASPETOS GERAIS Avaliação inicial Avaliação do risco/benefício Avaliação laboratorial [1] Educação do doente e familiares Avaliação clínica [2]
ANTICOAGULANTES ORAIS NÃO ANTAGONISTAS DA VITAMINA K (nacos) ASPETOS GERAIS Avaliação inicial Avaliação do risco/benefício Avaliação laboratorial [1] Educação do doente e familiares Avaliação clínica [2]
CH Lisboa Ocidental, EPE - Hospital Egas Moniz
 CH Lisboa Ocidental, EPE - Hospital Egas Moniz Dimensão Excelência Clínica Área de Ortopedia Artroplastias da Anca e Joelho e Fraturas proximais do fémur Alteração de apresentação da área Área de Ortopedia
CH Lisboa Ocidental, EPE - Hospital Egas Moniz Dimensão Excelência Clínica Área de Ortopedia Artroplastias da Anca e Joelho e Fraturas proximais do fémur Alteração de apresentação da área Área de Ortopedia
Terapêutica Antitrombótica da Fibrilhação Auricular
 Terapêutica Antitrombótica da Fibrilhação Auricular Terapêutica Antitrombótica da Fibrilhação Auricular Publicação da Coordenação Nacional para as Doenças Cardiovasculares Coordenador Nacional: Dr. Rui
Terapêutica Antitrombótica da Fibrilhação Auricular Terapêutica Antitrombótica da Fibrilhação Auricular Publicação da Coordenação Nacional para as Doenças Cardiovasculares Coordenador Nacional: Dr. Rui
Nome do medicamento: ELIQUIS. Forma farmacêutica: comprimido revestido. Concentrações: 2,5 mg e 5,0 mg
 Nome do medicamento: ELIQUIS Forma farmacêutica: comprimido revestido Concentrações: 2,5 mg e 5,0 mg APRESENTAÇÕES ELIQUIS (apixabana) é apresentado na forma farmacêutica de comprimidos revestidos de 2,5
Nome do medicamento: ELIQUIS Forma farmacêutica: comprimido revestido Concentrações: 2,5 mg e 5,0 mg APRESENTAÇÕES ELIQUIS (apixabana) é apresentado na forma farmacêutica de comprimidos revestidos de 2,5
ONTARGET - Telmisartan, Ramipril, or Both in Patients at High Risk for Vascular Events N Engl J Med 2008;358:
 ONTARGET - Telmisartan, Ramipril, or Both in Patients at High Risk for Vascular Events N Engl J Med 2008;358:1547-59 Alexandre Alessi Doutor em Ciências da Saúde pela Pontifícia Universidade Católica do
ONTARGET - Telmisartan, Ramipril, or Both in Patients at High Risk for Vascular Events N Engl J Med 2008;358:1547-59 Alexandre Alessi Doutor em Ciências da Saúde pela Pontifícia Universidade Católica do
10ª Conferência Nacional de Economia da Saúde
 10ª Conferência Nacional de Economia da Saúde 23 de Novembro de 2007 Fundação Calouste Gulbenkian, Lisboa Mercado de Medicamentos em Portugal: Análise da Evolução da Utilização e da Despesa entre 20 e
10ª Conferência Nacional de Economia da Saúde 23 de Novembro de 2007 Fundação Calouste Gulbenkian, Lisboa Mercado de Medicamentos em Portugal: Análise da Evolução da Utilização e da Despesa entre 20 e
Prevenção do Acidente Vascular Cerebral na Fibrilação Atrial: Foco na América Latina
 Prevenção do Acidente Vascular Cerebral na Fibrilação Atrial: Foco na América Latina Stroke Prevention in Atrial Fibrillation: Focus on Latin America Ayrton R. Massaro 1,2 e Gregory Y. H. Lip 3,4 Hospital
Prevenção do Acidente Vascular Cerebral na Fibrilação Atrial: Foco na América Latina Stroke Prevention in Atrial Fibrillation: Focus on Latin America Ayrton R. Massaro 1,2 e Gregory Y. H. Lip 3,4 Hospital
Resumo da avaliação científica de medicamentos contendo nimesulida para uso sistémico (ver Anexo I)
 Anexo II Conclusões científicas e fundamentos para as alterações dos Resumos das Características do Medicamento e dos Folhetos Informativos apresentados pela EMA 41 Conclusões científicas Resumo da avaliação
Anexo II Conclusões científicas e fundamentos para as alterações dos Resumos das Características do Medicamento e dos Folhetos Informativos apresentados pela EMA 41 Conclusões científicas Resumo da avaliação
Colírio, solução. Solução oleosa, amarelo claro com aspeto límpido e cheiro característico.
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Diomicete 10 mg/ml colírio, solução 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Um ml de solução contém 10 mg de clotrimazol. Excipientes com
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Diomicete 10 mg/ml colírio, solução 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Um ml de solução contém 10 mg de clotrimazol. Excipientes com
Dimensão Segurança do Doente Check-list Procedimentos de Segurança
 1. 1.1 1.2 Cultura de Segurança Existe um elemento(s) definido(s) com responsabilidade atribuída para a segurança do doente Promove o trabalho em equipa multidisciplinar na implementação de processos relativos
1. 1.1 1.2 Cultura de Segurança Existe um elemento(s) definido(s) com responsabilidade atribuída para a segurança do doente Promove o trabalho em equipa multidisciplinar na implementação de processos relativos
PREVENÇÃO DA HEMORRAGIA EM DOENTES HIPOCOAGULADOS OU SOB TERAPÊUTICA ANTIAGREGANTE PLAQUETÁRIA SUBMETIDOS A TÉCNICAS ENDOSCÓPICAS ELECTIVAS
 PREVENÇÃO DA HEMORRAGIA EM DOENTES HIPOCOAGULADOS OU SOB TERAPÊUTICA ANTIAGREGANTE PLAQUETÁRIA SUBMETIDOS A TÉCNICAS ENDOSCÓPICAS ELECTIVAS A. DOENTES HIPOCOAGULADOS O risco de hemorragia digestiva varia
PREVENÇÃO DA HEMORRAGIA EM DOENTES HIPOCOAGULADOS OU SOB TERAPÊUTICA ANTIAGREGANTE PLAQUETÁRIA SUBMETIDOS A TÉCNICAS ENDOSCÓPICAS ELECTIVAS A. DOENTES HIPOCOAGULADOS O risco de hemorragia digestiva varia
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO. Cada cápsula contém 300 mg de diosmina como substância ativa.
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Venex 300 mg Cápsulas 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada cápsula contém 300 mg de diosmina como substância ativa. Excipiente(s)
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Venex 300 mg Cápsulas 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada cápsula contém 300 mg de diosmina como substância ativa. Excipiente(s)
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR
 RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI nivolumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM Frasco de
RELATÓRIO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO PARA USO HUMANO EM MEIO HOSPITALAR DCI nivolumab N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem PVH PVH com IVA Titular de AIM Frasco de
TROMBOEMBOLISMO VENOSO. Evidência em Abílio Reis Chefe de Serviço de Medicina Interna Hospital Sto António Porto
 TROMBOEMBOLISMO VENOSO Evidência em 2012 Abílio Reis Chefe de Serviço de Medicina Interna Hospital Sto António Porto TEV Importância da doença Em estudos de autópsia qual a % de TEV diagnosticada premorten
TROMBOEMBOLISMO VENOSO Evidência em 2012 Abílio Reis Chefe de Serviço de Medicina Interna Hospital Sto António Porto TEV Importância da doença Em estudos de autópsia qual a % de TEV diagnosticada premorten
PROTOCOLO HOSPITAL ALEMÃO OSWALDO CRUZ Capítulo JCI Responsável pela elaboração Número do documento Data da 1ª versão
 Objetivos gerais e específicos Discriminar dentre os pacientes internados, aqueles que devem receber profilaxia para (TEV) além de descrever as medidas específicas para esta profilaxia. Critério de inclusão
Objetivos gerais e específicos Discriminar dentre os pacientes internados, aqueles que devem receber profilaxia para (TEV) além de descrever as medidas específicas para esta profilaxia. Critério de inclusão
Anexo II. Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado
 Anexo II Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado 13 Conclusões científicas e fundamentos para a alteração dos termos das Autorizações
Anexo II Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado 13 Conclusões científicas e fundamentos para a alteração dos termos das Autorizações
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO
 RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI Lixisenatido N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM 5551502 5551528 Lyxumia
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI Lixisenatido N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM 5551502 5551528 Lyxumia
