ESTRESSE OXIDATIVO: RELAÇÃO ENTRE GERAÇÃO DE ESPÉCIES REATIVAS E DEFESA DO ORGANISMO
|
|
|
- Ana Júlia de Andrade Rocha
- 8 Há anos
- Visualizações:
Transcrição
1 Quim. Nova, Vol. 29, No. 1, , 2006 ESTRESSE OXIDATIVO: RELAÇÃO ENTRE GERAÇÃO DE ESPÉCIES REATIVAS E DEFESA DO ORGANISMO André L. B. S. Barreiros e Jorge M. David* Instituto de Química, Universidade Federal da Bahia, Salvador-BA Juceni P. David Faculdade de Farmácia, Universidade Federal da Bahia, Salvador-BA Recebido em 1/7/04; aceito em 18/5/05; publicado na web em 24/8/05 Divulgação OXIDATIVE STRESS: RELATIONS BETWEEN THE FORMATION OF REACTIVE SPECIES AND THE ORGANISM S DEFENSE. This work describes the mechanism of action of some reactive oxygen species (ROS) and reactive nitrogen species (RNS) in the oxidative stress of the human body, and their consequences on damage to DNA, RNA, proteins and lipids. It also illustrates the defense system of our organism against these ROS and RNS species. The action of nonenzymatic protection systems is reported, with emphasis on micromolecules like Q10 coenzyme, vitamin C, α-tocopherol, carotenoids and flavonoids. The importance of flavonoids is also emphasized, and their body protection mechanism is detailed. Keywords: oxidative stress; antioxidants; reactive species. INTRODUÇÃO Atualmente existe um grande interesse no estudo dos antioxidantes devido, principalmente, às descobertas sobre o efeito dos radicais livres no organismo. A oxidação é parte fundamental da vida aeróbica e do nosso metabolismo e, assim, os radicais livres são produzidos naturalmente ou por alguma disfunção biológica. Esses radicais livres cujo elétron desemparelhado encontra-se centrado nos átomos de oxigênio ou nitrogênio são denominados ERO ou ERN 1-4. No organismo, encontram-se envolvidos na produção de energia, fagocitose, regulação do crescimento celular, sinalização intercelular e síntese de substâncias biológicas importantes. No entanto, seu excesso apresenta efeitos prejudiciais, tais como a peroxidação dos lipídios de membrana e agressão às proteínas dos tecidos e das membranas, às enzimas, carboidratos e DNA 5. Dessa forma, encontram-se relacionados com várias patologias, tais como artrite, choque hemorrágico, doenças do coração, catarata, disfunções cognitivas, câncer e AIDS, podendo ser a causa ou o fator agravante do quadro geral 6. O excesso de radicais livres no organismo é combatido por antioxidantes produzidos pelo corpo ou absorvidos da dieta. De acordo com Halliwell 3 Antioxidante é qualquer substância que, quando presente em baixa concentração comparada à do substrato oxidável, regenera o substrato ou previne significativamente a oxidação do mesmo. Os antioxidantes produzidos pelo corpo agem enzimaticamente, a exemplo da GPx, CAT e SOD 2 ou, nãoenzimaticamente a exemplo de GSH, peptídeos de histidina, proteínas ligadas ao ferro (transferrina e ferritina), ácido diidrolipóico e CoQH 2. Além dos antioxidantes produzidos pelo corpo, o organismo utiliza aqueles provenientes da dieta como o a-tocoferol (vitamina-e), β-caroteno (pro-vitamina-a), ácido ascórbico (vitamina- C), e compostos fenólicos onde se destacam os flavonóides e poliflavonóides 4,7. Dentre os aspectos preventivos, é interessante ressaltar a correlação existente entre atividade antioxidante de substâncias polares e capacidade de inibir ou retardar o aparecimento de células cancerígenas, além de retardar o envelhecimento das células em geral 8. Outro interesse ligado aos antioxidantes é a sua * jmdavid@ufba.br aplicação na indústria, para a proteção de cosméticos, fármacos e alimentos, prevenindo a decomposição oxidativa desses pela ação da luz, temperatura e umidade 9. O ESTRESSE OXIDATIVO O organismo humano sofre ação constante de ERO e ERN geradas em processos inflamatórios, por alguma disfunção biológica ou provenientes dos alimentos. As principais ERO distribuem-se em dois grupos, os radicalares: hidroxila (HO ), superóxido ( ), peroxila (ROO ) e alcoxila (RO ); e os não-radicalares: oxigênio, peróxido de hidrogênio e ácido hipocloroso. Dentre as ERN incluem-se o óxido nítrico (NO ), óxido nitroso (N 2 O 3 ), ácido nitroso (HN ), nitritos (N ), nitratos (NO 3 ) e peroxinitritos (ONOO ) 10. Enquanto alguns deles podem ser altamente reativos no organismo atacando lipídios, proteínas e DNA, outros são reativos apenas com os lipídios. Existem ainda alguns que são pouco reativos, mas apesar disso podem gerar espécies danosas. O radical HO é o mais deletério ao organismo, pois devido a sua meia-vida muito curta dificilmente pode ser seqüestrado in vivo. Estes radicais freqüentemente atacam as moléculas por abstração de hidrogênio e por adição a insaturações. Nos experimentos de laboratório o HO pode facilmente ser seqüestrado in vitro por inúmeras moléculas, devido a sua alta reatividade. No entanto, para que os resultados in vitro se reproduzam in vivo, é necessário ministrar alta concentração do antioxidante para que este alcance o local onde o radical HO está presente em concentração suficiente para suprimí-lo. Existem duas maneiras de controlar a presença do radical HO : reparar os danos causados por ele ou inibir sua formação. O radical HO é formado no organismo principalmente por dois mecanismos: reação de H 2 com metais de transição e homólise da água por exposição à radiação ionizante 6 (Equação 1). A incidência de radiação no ultravioleta, radiação γ e raios X podem produzir o radical HO nas células da pele. O ataque intensivo e freqüente deste radical pode originar mutações no DNA e, conseqüentemente, levar ao desenvolvimento de câncer em seres humanos no período de 15 a 20 anos. luz UV H 2 O HO + H (1)
2 114 Barreiros et al. Quim. Nova O peróxido de hidrogênio isoladamente é praticamente inócuo, porém pode se difundir facilmente através das membranas celulares como, por ex., a membrana do núcleo. Devido ao fato da célula possuir metais de transição, ocorre geração do radical HO em seu interior 5 (Equação 2). M n+ + H 2 M (n+1)+ + HO + HO (2) Em nosso organismo, os metais de transição mais importantes para a ocorrência dessa reação são Cu 1+ e Fe 2+. Nesse sistema, a importância do ferro é mais pronunciada devido a sua maior biodisponibilidade e, no organismo, na maior parte do tempo ele encontra-se complexado com proteínas de transporte (ex. transferrina), e armazenamento (ex. ferritina e hemosiderina). A reação do Fe 2+ com o H 2 (reação de Fenton) pode ser representada de maneira simplificada na Equação 3 ou de forma mais complexa na Equação 4. Fe 2+ + H 2 Fe 3+ + HO + HO (3) com as bases púricas por adição a C-4 e C-8, e em menor proporção com C-5, gerando 2,6-diamino-4-hidroxi-5- formamidopirimidina (FapyG) (6), 4,6-diamino-5-formamidopirimidina (FapyA) (7), 8-oxo-7,8-diidro-2 -desoxiguanosídeo (8- oxog) (8), 8-oxoA (9) 11 (Figura 1). O ataque às bases pirimidínicas dá-se por adição à ligação dupla Δ 5,6, e produz os radicais livres em C-6 e C-5 nas proporções aproximadamente de 70 e 30%, respectivamente (14 e 15), gerando 5-hidroxi-6-hidrocitosina (16), 6-hidroxi-5-hidrocitosina (17), 5-hidroxi-6-peroxicitosina (20), 6-hidroxi-5-peroxicitosina (21), 5-hidroxi-6-oxocitosina (22) e 6- hidroxi-5-oxocitosina (23). Os radicais peroxila (18 e 19) podem decompor-se gerando citosinaglicol (24) como produto majoritário. A timina sofre a adição do radical à ligação dupla Δ 5,6, formando os radicais livres em C-5 e C-6 (25 e 26), e em menor teor o radical decorrente da abstração de um próton da metila em C-5 (27), que gera 5-hidroxi-6-hidrotimina (28), 6-hidroxi-5- hidrotimina (29), 5-hidroxi-6-oxotimina (36) e timinaglicol (37) como principais produtos 10. A fragmentação completa da citosina e da timina é mostrada na Figura 2. (4) O radical hidroxila causa danos ao DNA, RNA, às proteínas, lipídios e membranas celulares do núcleo e mitocondrial. No DNA ele ataca tanto as bases nitrogenadas quanto a desoxirribose (Figura 1). O ataque ao açúcar pode ser realizado por abstração de um dos átomos de hidrogênio (1-3) e quase sempre leva à ruptura da cadeia de DNA 10. O mecanismo dessa ruptura tem como principais produtos 5-8-ciclo-2 -desoxiadenosina 8OHdA (4) e 5-8-ciclo-2 -desoxiguanosina 8OHdG (5). A eletrofilicidade do HO possibilita sua interação com as bases nitrogenadas por adição às insaturações em sítios de alta densidade eletrônica. Assim, reage Figura 2. Fragmentação oxidativa das bases pirimidínicas Figura 1. Principais produtos da oxidação do DNA por ERO e ERN Nos aminoácidos e proteínas, HO pode reagir na cadeia lateral, onde ataca preferencialmente cisteína, histidina, triptofano, metionina e fenilalanina, e, em menores proporções, arginina e asparagina 11. Os ataques aos aminoácidos que compõem as proteínas podem gerar danos como clivagens de ligações com ou sem geração de fragmentos e ligações cruzadas, o que pode ter como
3 Vol. 29, No. 1 Estresse Oxidativo: Relação entre Geração de Espécies Reativas 115 conseqüência perda de atividade enzimática, dificuldades no transporte ativo através das membranas celulares, citólise e morte celular. O ataque ocorre por adição do radical ou por abstração de hidrogênio. Todos os aminoácidos podem sofrer abstração do hidrogênio do carbono Cα -COO ligado ao carboxilato e ao grupo amino. Essa abstração, com exceção da glicina, leva à perda de C e formação de carbono radicalar 11. Na Figura 3 são mostrados os principais produtos dessas reações, destacando-se o tiohidroperóxido (42), cistina (43) 12, 2-oxo-histidina (44) em equilíbrio com a 2-hidroxi-histidina (45) 13, metionina sulfóxido (46), metionina sulfona (47) 14, derivados da arginina, lisina e prolina (48, 49 e 50), nitroacetato (51), oxima (52), hidroxilamina (53) 14, oxalato (54) 11 e derivados da tirosina (55-60). 4-oxo-2-nonenal (67) e 4,5-epóxi-2(E)-decenal (68). Aldeídos α,βinsaturados são conhecidos por sua ação genotóxica, pois em presença do 2 -desoxiguanosídeo e do 2 -desoxiadenosídeo sofrem adição gerando heptanona-eteno-desoxiguanosídeo (69), heptanonaeteno-desoxiadenosídeo (70), eteno-desoxiadenosídeo (71), etenoadenosídeo e hexanol-1,n-2-propano-desoxiguanosídeo (72). A decomposição dos ácidos graxos com três ou mais insaturações gera como produto adicional o aldeído malônico (73), que pode se adicionar ao 2 -desoxiguanosídeo gerando pirimidol-[1,2a]purin-10- ona desoxiguanosídeo (74) 15 (Figura 4). Figura 4. Compostos genotóxicos produzidos pela oxidação dos lipídios por ERO e ERN, e produtos resultantes de seu ataque ao DNA Figura 3. Principais produtos da oxidação dos aminoácidos e proteínas por ERO e ERN O exemplo mais comum do ataque de radicais hidroxila a lipídios é a ação deste nos lipídios de membrana. Os radicais livres centrados no oxigênio (HO ) atacam a cadeia lipídica em sítios susceptíveis como o grupo metilênico alílico, convertendo-o em novo centro de radical livre. O carbono radicalar facilmente adiciona oxigênio gerando o radical lipídio-peroxila, que pode facilmente atacar as proteínas de membrana, produzindo danos nas células A Figura 6 traz exemplos dessa atuação. Os ácidos graxos poliinsaturados são mais susceptíveis ao ataque por radicais livres, devido ao carbono metilênico bis-alílico. O radical formado pela abstração do hidrogênio gera os ácidos decadienóicos HPODE, 13- Z,E-HPODE (61), 9-E,Z-HPODE (62), 9-E,E-HPODE (63) e 13- E,E-HPODE (64) e a decomposição destes gera os aldeídos α,βinsaturados 4-hidroperoxi-2-nonenal (65), 4-hidroxi-2-nonenal (66), A forma mais deletéria do oxigênio ao organismo é o oxigênio singleto ( 1 ), pois é a causa ou o intermediário da toxicidade fotoinduzida do em organismos vivos. O seu tempo de meiavida depende muito do meio onde se encontra. Em meio aquoso, sua meia-vida é muito pequena, pois ele se choca com as moléculas de H 2 O transferindo sua energia, desativando-se e retornando à forma de oxigênio tripleto. Em meio orgânico é mais comum a ocorrência de choque com transferência de energia, sem reação química, seguida da dissipação dessa energia na forma de calor. Esse tipo de choque é denominado quenching colisional e representa a forma como a água desativa o 1. Porém, em meio orgânico, a meia-vida do oxigênio singleto é maior e, portanto, pode causar algumas reações químicas com determinados aceptores por incorporação do. O oxigênio singleto reage com algumas classes de biomoléculas e, em geral, essas reações são do tipo eno (Equação 5) e dieno (reações de Diels-Alder) (Equação 6). Os compostos naturais mais reativos frente ao 1 são os carotenóides, devido as múltiplas insaturações conjugadas. Assim, o 1 reage mais lentamente com os ácidos graxos que com o β-caroteno, e quanto maior o número de insaturações presentes
4 116 Barreiros et al. Quim. Nova nos ácidos graxos, mais rapidamente eles irão reagir. Essa reação se dá por incorporação do oxigênio à cadeia com conseqüente migração da ligação dupla, formando ácidos hidroperóxidos como os HPODE 16 (Figura 4). (5) (6) (HOO ) é mais reativo (Equação 13) H + H 2 + (12) + H + HOO (13) O radical ânion superóxido ( ) participa de certos processos químicos importantes no contexto biológico. O principal deles é auxiliar na produção de radical HO, através da redução de quelatos de Fe (III) (Equação 14), formando Fe +2. Assim, o HO pode ser obtido através da reação de Haber-Weiss 6,20 (Equação 15). Fe 3+ + [Fe 3+ Fe 2+ ] Fe 2+ + (14) Na Figura 3 estão representados os produtos da reação do 1 com os aminoácidos cisteína, metionina, triptofano, tirosina e histidina 27. A reação do oxigênio singleto com os ácidos nucléicos é significativa apenas para a base guanina, que origina 8OHG (8). O peróxido de hidrogênio (H 2 ) é pouco reativo frente às moléculas orgânicas na ausência de metais de transição. No entanto, exerce papel importante no estresse oxidativo por ser capaz de transpor as membranas celulares facilmente e gerar o radical hidroxila. Ele somente oxida proteínas que apresentem resíduos de metionina ou grupos tiol muito reativos, GSH por ex. O H 2 é gerado in vivo pela dismutação do ânion-radical superóxido ( ) por enzimas oxidases ou pela β-oxidação de ácidos graxos. As mitocôndrias são importantes fontes de e, como a presença deste ânion-radical pode causar sérios danos, elas são ricas em SOD que o converte em H 2. O peróxido de hidrogênio gerado é então parcialmente eliminado por catalases, glutationa peroxidase e peroxidases ligadas à tioredoxina, mas como essa eliminação tem baixa eficiência, grande parte do H 2 é liberado para a célula 18. O H 2 também pode ser encontrado em bebidas como chás e principalmente café instantâneo e, rapidamente se difunde pelas células da cavidade oral e do trato gastrintestinal. Pode também ser produzido por bactérias presentes na boca, sendo utilizado pela peroxidase salivar para oxidar o tiocianeto (SCN ) em tiocianato (OSCN ), um produto tóxico para certas bactérias. Ele é utilizado pelos fagócitos na produção de ácidos hipoalogenosos, que são oxidantes muito efetivos no combate a vírus, bactérias e outros corpos estranhos, mas que por outro lado apresentam efeitos deletérios quando expostos às moléculas biológicas 14,18. A maior fonte de energia para os organismos aeróbicos está na terceira etapa da respiração, que ocorre no interior da mitocôndria, onde uma molécula de é reduzida a duas moléculas de H 2 O, com consumo de 4 elétrons (Equação 7). Nas equações seguintes (Equações 8-11) estão descritas as etapas da redução de, formação de radical hidroxila e a segunda molécula de água (Equação 11) e + 4H + 2H 2 O (7) + e (8) + e + 2H + H 2 (9) H 2 + e + H + OH + H 2 O (10) OH + e + H + H 2 O (11) O radical ânion superóxido ( ) ao contrário da maioria dos radicais livres é inativo. Em meio aquoso, sua reação principal é a dismutação, na qual se produz uma molécula de peróxido de hidrogênio e uma molécula de oxigênio (Equação 12). Ele também é uma base fraca cujo ácido conjugado, o radical hidroperóxido Fe + H 2 HO + HO + (15) Além disso, o radical ânion possui a habilidade de liberar Fe 2+ das proteínas de armazenamento e de ferro-sulfoproteínas, tais como ferritina e aconitase, respectivamente. O radical ânion também reage com o radical HO produzindo oxigênio singleto 1 (Equação 16) e com o óxido nítrico (NO ) produzindo peroxinitrito (ONOO ) (Equação 17). + OH 1 + HO (16) NO + ONOO (17) A atuação do radical ânion superóxido ( ) como oxidante direto é irrelevante. Dentre os aminoácidos, o único que sofre oxidação com o radical é a cisteína. A partir dessa reação formase um superóxido (42) e o tio-radical (43) (Figura 3) 18. Além disso, o radical ânion superóxido presente no organismo é eliminado pela enzima superóxido dismutase, que catalisa a dismutação de duas moléculas de em oxigênio e peróxido de hidrogênio (Equação 12). Este último, quando não eliminado do organismo pelas enzimas peroxidases e catalase, pode gerar radicais hidroxila 18. Apesar destes efeitos danosos, o radical tem importância vital para as células de defesa e sem ele o organismo está desprotegido contra infecções causadas por vírus, bactérias e fungos. O radical é gerado in vivo por fagócitos ou linfócitos e fibroblastos durante o processo inflamatório, para combater corpos estranhos. Os fagócitos o produzem com auxílio da enzima leucócito NADPH oxidase, que catalisa a redução por um elétron do com gasto de uma molécula de NADPH (Equação 18) 18, NADPH 2 + NADP + + H + (18) O radical ânion superóxido formado é bactericida fraco, capaz de inativar proteínas ferro-sulfurosas das bactérias, porém gera alguns produtos que possuem forte atividade antimicrobiana, tais como ácido hipocloroso (HOCl), peróxido de hidrogênio (H 2 ) e peroxinitrito (ONOO ) que são os principais responsáveis pelo combate a corpos estranhos. Em alguns casos o radical ânion age como antioxidante, reduzindo semiquinonas para que elas possam retomar suas atividades metabólicas na célula. Um exemplo é a redução da ubiquinona para ubiquinol, no interior da mitocôndria 18,19. Por fim, o radical ânion superóxido funciona como sinalizador molecular através da sua capacidade de oxidar grupos SH em ligações dissulfeto (Equação 19), podendo ativar e desativar enzimas que contenham metionina RSH 2HOO + RSSR (19)
5 Vol. 29, No. 1 Estresse Oxidativo: Relação entre Geração de Espécies Reativas 117 O radical óxido nítrico (NO ) pode ser produzido no organismo pela ação da enzima óxido nítrico sintase a partir de arginina, oxigênio e NADPH, gerando também NADP + e citrulina 21. Esse radical também pode ser produzido em maiores quantidades através dos fagócitos humanos, quando estimulados 10,18. O nitrato pode transformar-se em nitrito, que reage com os ácidos gástricos gerando o ácido nitroso (HN ). O óxido nitroso (N 2 O 3 ) também é precursor do HN através da sua reação com a água. O HN promove a desaminação das bases do DNA que contêm grupo NH 2 livre que são citosina, adenina e guanina, formando-se uracila, hipoxantina (11) e xantina (12), respectivamente (Figura 1) 10. O óxido nítrico NO não é suficientemente reativo para atacar o DNA diretamente, mas pode reagir com o radical ânion superóxido, produzido pelos fagócitos, gerando peroxinitrito. Esse último, por sua vez, pode sofrer reações secundárias formando agentes capazes de nitrar aminoácidos aromáticos, a exemplo da tirosina gerando nitrotirosina (59) e as bases do DNA, em particular a guanina, na qual o produto principal é a 8-nitroguanina (13) 10,18,22. A presença do tampão C /HCO 3 contribui para a nitração de biomoléculas pois o carbonato ao ser protonado forma o radical HCO 3 e este oxida anéis aromáticos, produzindo bicarbonato (HCO 3 ) e o radical aromático correspondente, facilitando a entrada do radical N 23. A PROTEÇÃO AO ORGANISMO CONTRA O ESTRESSE OXIDATIVO Os radicais livres promovem reações com substratos biológicos podendo ocasionar danos às biomoléculas e, conseqüentemente, afetar a saúde humana. Os danos mais graves são aqueles causados ao DNA e RNA. Se a cadeia do DNA é quebrada, pode ser reconectada em outra posição alterando, assim, a ordem de suas bases. Esse é um dos processos básicos da mutação e o acúmulo de bases danificadas pode desencadear a oncogênese. Uma enzima que tenha seus aminoácidos alterados pode perder sua atividade ou, ainda, assumir atividade diferente. Ocorrendo na membrana celular, a oxidação de lipídios interfere no transporte ativo e passivo normal através da membrana, ou ocasiona a ruptura dessa, levando à morte celular. A oxidação de lipídios no sangue agride as paredes das artérias e veias, facilitando o acúmulo desses lipídios, com conseqüente aterosclerose, podendo causar trombose, infarto ou acidente vascular cerebral. As proteções conhecidas do organismo contra as ERO e ERN abrangem a proteção enzimática ou por micromoléculas, que podem ter origem no próprio organismo ou são adquiridas através da dieta. As macromoléculas são representadas pelas enzimas e podem atuar diretamente contra as ERO e ERN ou, ainda, reparar os danos causados ao organismo por essas espécies. Um exemplo é a catalase (CAT) que converte o peróxido de hidrogênio em H 2 O e. Outras são capazes de eliminar a molécula ou a unidade dessa que se encontra danificada, como por ex., as enzimas responsáveis pela excisão das bases nitrogenadas danificadas e substituição por outras intactas 10,19. São conhecidos três sistemas enzimáticos antioxidantes: o primeiro é composto por dois tipos de enzimas SOD, que catalisam a destruição do radical ânion superóxido, convertendo-o em oxigênio e peróxido de hidrogênio. A decomposição do radical ânion superóxido ocorre naturalmente porém, por ser uma reação de segunda ordem, necessita que ocorra colisão entre duas moléculas de, de forma que há necessidade de maior concentração do radical ânion superóxido. A presença da enzima SOD favorece essa dismutação tornando a reação de primeira ordem, eliminando a necessidade da colisão entre as moléculas. A ação desta enzima permite a eliminação do mesmo em baixas concentrações. Existem duas formas de SOD no organismo, a primeira contém Cu 2+ e Zn 2+ como centros redox e ocorre no citosol, sendo que sua atividade não é afetada pelo estresse oxidativo. A segunda contém Mn 2+ como centro redox, ocorre na mitocôndria e sua atividade aumenta com o estresse oxidativo 19. O segundo sistema de prevenção é muito mais simples, sendo formado pela enzima catalase que atua na dismutação do peróxido de hidrogênio (H 2 ) em oxigênio e água 19 (Equação 20). (20) O terceiro sistema é composto pela GSH em conjunto com duas enzimas GPx e GR. A presença do selênio na enzima (selenocisteína) explica a importância desse metal e sua atuação como antioxidante nos organismos vivos. Esse sistema também catalisa a dismutação do peróxido de hidrogênio em água e oxigênio, sendo que a glutationa opera em ciclos entre sua forma oxidada e sua forma reduzida 19. A GSH reduz o H 2 a H 2 O em presença de GPx, formando uma ponte dissulfeto e, em seguida, a GSH é regenerada (Equações 21-23). (21) (22) (23) Dentre os antioxidantes biológicos de baixo peso molecular, podem ser destacados os carotenóides, a bilirrubina, a ubiquinona e o ácido úrico. Porém, as mais importantes micromoléculas no combate ao estresse oxidativo são os tocoferóis e o ácido ascórbico (vitamina C) 19. Vitamina C no ciclo oxidativo O ácido ascórbico ou vitamina C é comumente encontrado em nosso organismo na forma de ascorbato (75). Por ser muito solúvel em água, está localizado nos compartimentos aquosos dos tecidos orgânicos. O ascorbato desempenha papéis metabólicos fundamentais no organismo humano, atuando como agente redutor, reduzindo metais de transição (em particular Fe 3+ e Cu 2+ ) presentes nos sítios ativos das enzimas ou nas formas livres no organismo 24. Por ser um bom agente redutor o ascorbato pode ser oxidado pela maioria das ERO e ERN que chegam ou são formadas nos compartimentos aquosos dos tecidos orgânicos. Sua oxidação produz inicialmente o radical semidesidroascorbato (76), que é pouco reativo. Esse radical pode ser reconvertido em ascorbato, ou duas moléculas dele podem sofrer desproporcionamento originando uma molécula de desidroascorbato (77) e regenerando uma molécula de ascorbato. O desidroascorbato pode ser então regenerado para ascorbato através de um sistema enzimático, ou ser oxidado irreversivelmente gerando oxalato (78) e treonato (79) 19,24 (Figura 5). Tendo em vista que o ascorbato converte as ERO e ERN em espécies inofensivas e que os derivados do ascorbato são pouco reativos, esse age como antioxidante in vivo. Devido a estas propriedades, muitos autores sugerem a ingestão diária de doses maiores de ascorbato, para proteção contra o desenvolvimento de doenças crônicas, cardiovasculares e de alguns tipos de câncer 24. O ascorbato possui também propriedades pró-oxidantes pois os íons Fe 2+ e Cu 1+ reagem com o peróxido de hidrogênio (reação de Fenton, Equação 3) gerando o radical hidroxila. Indiretamente, o ascorbato pode induzir as reações de radicais livres.
6 118 Barreiros et al. Quim. Nova Figura 5. Ciclo oxidativo do ascorbato Porém, em função do Fe encontrar-se, na maior parte do tempo, ligado a proteínas de transporte ou armazenamento, em situação normal, as propriedades antioxidantes do ascorbato suplantam suas propriedades pró-oxidantes 24. O ascorbato pode atuar contra a peroxidação de lipídios de duas maneiras: no plasma sanguíneo, atua na prevenção através da reação com as ERO e ERN presentes, ou na restauração doando hidrogênio ao radical lipídio (80). Isso explica seu papel na prevenção de doenças cardiovasculares, devido ao fato de que sem a formação dos radicais lipídio-peroxila (81) não ocorre o ataque às proteínas das paredes dos vasos e artérias sanguíneos, causando o acúmulo de lipídios nessas paredes e, conseqüentemente, seu entupimento. Por outro lado, nas membranas celulares ele atua em parceria com o α-tocoferol (82). O radical livre normalmente abstrai um próton do carbono metilênico alílico, e o radical lipídio formado (80) rapidamente adiciona oxigênio tripleto gerando o radical lipídio-peroxila (81). Nesta etapa, o tocoferol (82) age doando um hidrogênio para esse radical formando o lipídio-hidroperóxido (83) e o radical tocoferoxila (84). O ascorbato (75) na interface da membrana celular regenera o tocoferol doando um hidrogênio, transformando-se em semidesidroascorbato (76) (Figura 6). As enzimas fosfolipase A 2, fosfolipídio hidroperóxido glutationa peroxidase, GPx e ácido graxo coenzima A restauram o lipídio 25. O papel do ascorbato na proteção à oxidação do DNA e, conseqüentemente, sua ação preventiva no câncer é ambíguo. Estudos indicam que o consumo de ascorbato inferior ao recomendado (40-60 mg/dia), por ex., consumo de 5 mg/dia aumentou os níveis de 8OHdG (5) em 91%. O consumo de 60 mg/dia reduziu os níveis de 8OHdG e 8OHG (8) no organismo reduzindo-se, assim, o risco de câncer. Foi verificado que uma suplementação superior a 500 mg/dia de ascorbato fez com que os níveis de 8OHdG e 8OHG decrescessem ainda mais, porém ocorrendo aumento nos níveis de 8OHA (9), Fapy-A (7) e Fapy-G (6). Mesmo com o aumento dessas espécies, o processo pode ser considerado benéfico, pois o 8OHdG e o 8OHG têm maior poder mutagênico que 8OHA, Fapy- A e Fapy-G. Não está estabelecido se a queda nos níveis de 8OHdG e 8OHG é conseqüência direta da ação do ascorbato como antioxidante ou da sua atuação como cofator das enzimas de reparo. Além disso, os níveis de 8OHA, Fapy-A e Fapy-G só aumentam expressivamente quando a concentração de ascorbato no plasma sanguíneo está acima de 70 μm. Como a ingestão de 100 mg/dia promovia uma concentração de 60 μm no plasma, recomendou-se uma ingestão entre mg/dia, para otimizar suas propriedades antioxidantes sem causar danos ao DNA 24. A vitamina E no ciclo oxidativo A vitamina E é constituída principalmente por quatro tocoferóis, e secundariamente por quatro tocotrienóis, sendo o α-tocoferol (82) o mais ativo 26. Estudos comprovam que a vitamina E é um eficiente inibidor da peroxidação de lipídios in vivo. Estas substâncias agem como doadores de H para o radical peroxila, interrompendo a reação radicalar em cadeia. Cada tocoferol pode reagir com até dois radicais peroxila e, nesse caso, o tocoferol é irreversivelmente desativado. Para que eles não se desativem, necessitam do mecanismo de regeneração sinergético com o ascorbato nas membranas celulares e com a ubiquinona na membrana mitocondrial 25,27 (Figura 6). A reação de doação do H radicalar fenólico para os radicais peroxila é acelerada pela presença de um grupo metoxi em para, pois este estabiliza o radical formado por ressonância, e grupos metila em orto ou em orto e meta que apresentam pequeno impedimento estérico. Ao mesmo tempo, essa reação é retardada quando a hidroxila fenólica se encontra estericamente impedida por grupos alquila maiores em orto, ou quando em presença de um grupo retirador de elétrons em para. Deste modo, não é possível prever qual dos tocoferóis tem maior atividade. No entanto, estudos cinéticos realizados in vitro Figura 6. Ataque à membrana celular e proteção pelo tocoferol e ascorbato. Esquema baseado na ref. 25
7 Vol. 29, No. 1 Estresse Oxidativo: Relação entre Geração de Espécies Reativas 119 Essa diferença de atividade é justificada por uma distribuição mais uniforme na bicamada lipídica das membranas, que leva à interação mais eficiente do anel cromano com os radicais lipídicos e à maior eficiência na reciclagem do radical cromanoxila 26. O papel dos carotenóides e da vitamina A no ciclo oxidativo Figura 7. Representação das estruturas dos radicais 4-metoxifenoxil, TMMP e PMHC com os orbitais dos átomos de oxigênio. Reproduzido da ref. 28, com permissão da American Chemical Society demonstram que o α-tocoferol possui uma constante de velocidade grande (k= 235 ± 50 M -1 s -1 ) para a transferência do H para um radical peroxila. Essa constante é maior que para a maioria dos antioxidantes sintéticos e ligeiramente superior aos outros tocoferóis: β-tocoferol (k= 166 ± 33 M -1 s -1 ), γ-tocoferol (k= 159 ± 42 M -1 s -1 ) e δ-tocoferol (k= 65 ± 13 M -1 s -1 ). Esses resultados estão em acordo com o observado em testes in vivo 28. As observações do efeito cinético em α-tocoferol com a hidroxila fenólica marcada com deutério confirmam que a reatividade reside na porção fenólica da molécula. Com base nessa observação foram avaliadas as constantes de velocidade de doação do H para o 2,3,5,6- tetrametil-4-metoxifenol (TMMP) (85) e o 2,2,5,7,8-pentametil-6- hidroxicromano (PMHC) (86). Observa-se que a constante de velocidade para o TMMP (k= 21 ± 2 M -1 s -1 ) representa apenas 9% da atividade do a-tocoferol, enquanto que para o PMHC (k= 214 ± 81 M -1 s -1 ) é aproximadamente idêntica à atividade do α-tocoferol. Esta aparente incoerência pode ser explicada por efeitos estéricos. A presença do grupo metoxi em para nos fenóis (87) aumenta a velocidade de doação do H radicalar. Isso é devido ao fato que o elétron não ligante do oxigênio metoxílico pode se deslocalizar migrando para o oxigênio do radical fenóxido (88) formando o íon fenolato, que é estabilizado por sua deslocalização com o anel aromático. O radical TMMP não apresenta esse aumento de velocidade na doação do H, devido ao impedimento estérico dos grupos metila. Esses grupos promovem o deslocamento da metoxila por efeito estérico para fora do plano do anel aromático, de modo que o orbital p com o seu par de elétrons fique no plano do anel aromático, inviabilizando a migração do elétron. Com o PMHC e os tocoferóis ocorre o aumento da velocidade de doação do H. Esse fato é explicado pela presença de um segundo anel com o oxigênio, que impede o giro do grupo e mantém o orbital p perpendicular ao anel aromático. Assim, torna-se possível a migração do elétron não ligante do oxigênio do anel para o orbital semipreenchido do oxigênio radicalar (89). Embora o α-tocoferol e o PMHC apresentem atividades semelhantes in vitro, o PMHC apresenta pouca ou nenhuma atividade in vivo. Esse fato é explicado pela cadeia carbônica lateral dos tocoferóis que aumenta sua solubilidade nas biomembranas, sítio onde eles atuam 28. Com base em observações estruturais é de se esperar que os tocotrienóis apresentem atividade semelhante à dos tocoferóis perante as ERO e ERN. Porém a atividade do α-tocotrienol contra a peroxidação de lipídios é maior que a do α-tocoferol, assim como a atividade dos tocotrienóis é maior que a dos respectivos tocoferóis. Dentre os carotenóides, o β-caroteno é a mais importante fonte de vitamina A 29. Eles formam um tipo incomum de agentes redutores biológicos, pois reduzem melhor os produtos de oxidação a baixos níveis de oxigênio. Altos níveis de oxigênio levam à destruição dos carotenóides. Na maioria dos tecidos biológicos, o nível de oxigênio é baixo, de modo que os carotenóides adquirem importância como antioxidantes. Os carotenóides agem in vivo como desativadores do oxigênio singleto ou como seqüestradores dos radicais peroxila, reduzindo a oxidação do DNA e lipídios, que está associada a doenças degenerativas, como câncer e doenças cardíacas 29. A principal atividade antioxidante dos carotenóides é a desativação do oxigênio singleto, sendo que a velocidade para essa reação é superior à dos tocoferóis. A desativação do 1 pode se dar de duas formas, pela transferência física da energia de excitação do 1 para o carotenóide e pela reação química do carotenóide com o 1. Em condições normais no organismo, 95% da desativação do 1 é física, restando somente 5% para reagir quimicamente, o que torna os carotenóides antioxidantes mais efetivos. Os produtos destas reações são apresentados na Figura 8 29,30. Figura 8. Principais produtos do ciclo oxidativo do β-caroteno Uma outra atividade recentemente estudada é do seqüestro de radicais peroxila. Os radicais peroxila adicionam-se à dupla ligação 5-6, 5-6 ou da cadeia do caroteno. Estudos de mecanismo revelaram a preferência pela adição em 5,6 ou 5,6, geran-
8 120 Barreiros et al. Quim. Nova do o radical altamente estabilizado por ressonância (93). Esse radical sofre, então, uma substituição homolítica intramolecular, originando os éteres cíclicos (91 e 92), interconversíveis em meio ácido, além do radical alcoxila 30 (Figura 8). O processo completo de oxidação dos carotenóides pode ser dividido em duas etapas. Na primeira, ocorre a formação de éteres cíclicos e compostos carbonílicos. Na segunda etapa os produtos primários são convertidos em compostos carbonílicos de cadeias menores, com liberação de C e ácidos carboxílicos. O processo completo é descrito por Woodall et al. 30,31. Os mecanismos propostos esclarecem a atividade dos carotenóides frente ao oxigênio singleto e aos radicais peroxila, porém não esclarecem a atividade contra outros radicais e se esses são capazes de interromper a reação radicalar em cadeia. Observa-se também a menor atividade antioxidante para os carotenóides que possuem substituição em 4 e/ou 4, em relação aos outros. Essas observações podem ser explicadas pela presença de carbonos metilênico em 4 e 4 vizinhos às insaturações conjugadas, que doam um hidrogênio para os radicais livres, devido ao fato do radical gerado ser extremamente estabilizado por ressonância (94) 31. Outro aspecto da atividade dos carotenóides diz respeito à polaridade. Aqueles que possuem grupos polares nos anéis A e B são efetivos na prevenção da oxidação das membranas. Essa polaridade os localiza de maneira tal que estão em contato mais próximo com a fase aquosa, reagindo com os radicais que penetram a membrana. Os apolares, tais como o licopeno e o β-caroteno são mais regeneradores que preventivos, combatendo os radicais formados com mais eficiência no interior da membrana 31. Os retinóides (vitamina A) possuem grupos polares que os localizam na membrana celular na região próxima à fase aquosa. No entanto, eles apresentam atividade antioxidante cerca de cinco vezes menor que a do β- caroteno sendo, provavelmente, a menor extensão da conjugação 29,31. forma, citocromos reduzem o para H 2 O com esses elétrons e prótons da matriz. Todo esse processo é indispensável para produção de ATP 33. O ciclo redox da ubiquinona, porém, também é capaz de transferir elétrons desemparelhados para aceptores que não participam da cadeia respiratória. A oxidação do ubiquinol dá-se pela doação de hidrogênio para um radical livre, gerando a respectiva semiquinona. O prosseguimento da oxidação leva à formação da ubiquinona com a desativação final de dois radicais livres. Dessa maneira, essa substância possui grande poder antioxidante através do seqüestro de radicais livres, bem como se mostra eficiente na interrupção de reações radicalares em cadeia. Tal atividade está limitada ao meio lipossolúvel, devido a sua longa cadeia lateral 16,33. Outra importante função da ubiquinona é a regeneração do tocoferol na membrana mitocondrial, onde exerce a mesma função regenerativa que o ascorbato exerce na membrana celular. O ubiquinol (101) doa um hidrogênio radicalar para o radical tocoferil (84), gerando ubiquinona semiquinona (102) e α-tocoferol (82). O prosseguimento dessa reação gera ubiquinona e regenera mais uma molécula de α-tocoferol 25,27,35 (Figura 9). Coenzima Q 10 no ciclo oxidativo A coenzima Q 10 é uma ubiquinona lipossolúvel que possui uma cadeia longa isoprenóide lateral. A ubiquinona é o único lipídio endogenamente sintetizado que apresenta função redox 32. Embora de forma diferenciada e bem específica essa é biossintetizada por todas as células, o que a torna o maior constituinte da membrana mitocondrial interna, membrana do complexo de Golgi e membrana dos lisossomos. Por outro lado, apenas poucas moléculas são encontradas na membrana do LDL. Essa variação na distribuição sugere funções diferentes para diferentes membranas biológicas. A ubiquinona ingerida como suplemento alimentar distribui-se principalmente entre o fígado e o plasma sanguíneo, não sendo absorvida pelas membranas com concentração elevada desta substância. Nos humanos, sua biossíntese é muito ativa até os 30 anos de idade, época que ocorre a estagnação de sua produção e, a partir desta idade, os níveis de ubiquinona começam a decrescer. Estudos indicam que a administração de suplementos de ubiquinona possui efeito benéfico no tratamento de doenças do coração, degeneração muscular e outras doenças degenerativas 33. Sua forma reduzida ubiquinol-10 (CoQH 2 ) é uma hidroquinona que ocorre predominantemente no coração, rins e fígado e a forma oxidada ubiquinona (CoQ 10 ) é abundante no cérebro e no intestino 34. A principal função da ubiquinona acontece na membrana mitocondrial interna, onde participa da cadeia de transporte de elétrons e translocação de prótons H + na mitocôndria, juntamente com os citocromos e as desidrogenases mitocondriais. As desidrogenases oxidam os NADH, NADPH e FADH 2 e transferem prótons e elétrons para a ubiquinona, convertendo-a em ubiquinol. Este por sua vez transfere prótons para a matriz mitocondrial e elétrons para os citocromos. Dessa Figura 9. Regeneração do tocoferol pelo ubiquinol A ubiquinona também exerce papel considerável na desativação do radical ânion superóxido, pois este após ser gerado na mitocôndria é prontamente oxidado pela ubiquinona formando oxigênio e a forma reduzida ubiquinol 18,19. A cadeia lateral da ubiquinona e ubiquinol também exerce função importante na atividade desses, uma vez que suas insaturações participam na desativação do oxigênio singleto 1, tanto por desativação física colisional quanto por adição às insaturações 16. Uma última atividade relevante da ubiquinona na mitocôndria é a redução do nitrito (N- ) a óxido nítrico (NO), que é um agente bioregulador 33. Toda essa atividade antioxidante está favorecida na mitocôndria devido à estabilização do radical livre intermediário (102) pelos seus pares redox, através do fluxo de elétrons da cadeia respiratória. Em ph = 6,0 da mitocôndria esse radical encontra-se predominantemente na forma desprotonada. Nesse estado, sem a presença de seus pares redox ele se desestabiliza em presença de oxigênio, gerando ubiquinona e radical ânion superóxido. Porém, em situações de acúmulo de NADH e/ou NADPH, tal como na isquemia, ou em outras membranas que não possuem tal estabilização, o acúmulo da forma desprotonada aumenta a reação de formação do radical ânion superóxido. Como o ubiquinol possui atividade análoga à SOD, o superóxido é dismutado gerando H 2. O contato da ubiquinona semiquinona desprotonada com o peróxido de hidrogênio ou o radical peroxila é desastroso, gerando radicais hidroxila (HO ) e alcoxila (RO ), respectivamente. Na membrana dos lisossomos a atividade apresentada pela
9 Vol. 29, No. 1 Estresse Oxidativo: Relação entre Geração de Espécies Reativas 121 ubiquinona é diferente. Esta membrana é muito rica em ubiquinona, com a peculiaridade de que a espécie dominante é a CoQ 9, que se encontra 70% na forma reduzida desprotonada. Sua função é o transporte de H + para o interior do lisossomo, além de ter uma função prooxidante. Nesse caso, a geração de radicais livres auxilia na função do lisossomo 33,34. Nas outras membranas e no plasma, o papel da ubiquinona é fundamentalmente de antioxidante. Como não há a presença dos pares redox da mitocôndria para estabilizar as ubiquinonas semiquinonas, elas são controladas por desproporcionamento onde duas moléculas de semiquinonas geram uma molécula de ubiquinol e uma de ubiquinona. Outra forma de eliminação do excesso de semiquinonas é sua regeneração pelo ascorbato, gerando ubiquinol e semidesidroascorbato. Os efeitos deletérios das semiquinonas são eliminados em condições normais. Isso favorece os efeitos benéficos da ubiquinona, tornando-a útil como antioxidante para o organismo 33,34. Ácido úrico no ciclo oxidativo O ácido úrico é a principal forma de excreção de nitrogênio das aves e dos répteis. Nos mamíferos, é produto secundário de excreção, derivado das bases purínicas. Na maioria dos tecidos orgânicos encontra-se na forma de ânion urato (pka 1 =5,4). Somente a partir dos anos 80 foi demonstrado que é um antioxidante efetivo nos sistemas biológicos, capaz de proteger o DNA e lipídios de ERO e ERN. A alta polaridade do ácido úrico restringe sua atividade ao meio aquoso. A sua concentração nos compartimentos aquosos do organismo encontra-se muito próxima do limite de solubilidade (300 μm). Indivíduos com aterosclerose podem apresentar nível elevado de ácido úrico no sangue, que é indicativo da existência de um mecanismo compensatório encontrado pelo organismo para controlar o estresse oxidativo 16,36. O mecanismo antioxidante do urato (103) pode ser resumido pela reação com a maioria dos agentes oxidantes em velocidade superior a das outras purinas (Figura 10). Nessa reação, há formação do radical urato (104) estabilizado. Devido ao baixo pka=3,1 do radical urato, esse se encontra na forma de ânion radical urato (105), o que facilita a doação de um próton em conjunto com o elétron. O pka de segunda ionização de 9,5 não permite que o radical urato se encontre na forma de um diânion no organismo 36. ânion superóxido ( ), peróxidos (ROOH) e peróxido de hidrogênio (H 2 ). Sozinho não é capaz de desativar o oxigênio singleto 1, porém no meio biológico ele causa indiretamente sua desativação através da desativação de outras espécies excitadas. Sua reação mais importante é com os radicais peroxila (ROO ) e N (gerando N ). Essa grande atividade contra os radicais peroxila é a base do seu efeito antioxidante protetor do DNA e lipídios. Como ocorre em meio aquoso, o urato reage com os radicais peroxila antes desses penetrarem a membrana e iniciarem seus danos. O urato é capaz de recuperar estruturas já atacadas que se tornaram radicais livres através da doação de um elétron e um próton. Ele também é responsável pela estabilização do ascorbato no plasma sanguíneo, inibindo a reação de Fenton 16,36 através de sua capacidade de quelar íons metálicos como Fe +3, Fe +2, Cu +2 e Cu + (106 e 107) (Figura 10). O ânion radical urato pode ser regenerado a urato pelo ascorbato, gerando semidesidroascorbato. Porém, o urato não é capaz de regenerar a vitamina E. A decomposição oxidativa irreversível do urato leva à formação inicialmente da alantoína (108) e prossegue gerando o ácido alantoínico (109), ácido cianúrico, ácido parabânico, ácido oxálico e ácido glioxílico 36. O papel da hemoglobina no ciclo oxidativo A degradação da hemoglobina libera o grupo heme no organismo. A ferroporfirina ou grupo heme da hemoglobina é liberada no baço, originária das células vermelhas mortas. A sua degradação libera Fe +3 e produz a biliverdina, um intermediário tetrapirrolico linear, que é reduzido pelo NADPH sob ação da enzima biliverdina redutase a bilirrubina, que pode se apresentar na forma lactâmina ou lactímica. O heme não é diretamente transportado pelo sangue devido à sua atividade prooxidante. Devido ao Fe central, esse é capaz de reagir com peróxidos ROOH ou H 2 originando vários radicais livres (Equações 24-28). ROOH + Heme-Fe +3 ROO + Heme-Fe +2 + H + (24) ROOH + Heme-Fe +2 RO + Heme-Fe +3 + HO (25) 2ROOH ROO + RO + H 2 O (26) RSH + Heme-Fe +3 RS + Heme-Fe +2 + H + (27) Heme-Fe +2 + Heme-Fe +3 + (28) Figura 10. Sumário das reações envolvendo a atividade antioxidante do ácido úrico O urato reage rapidamente com o radical hidroxila HO, no entanto, o urato é inerte às espécies superóxido (HOO ), radical Tanto a biliverdina quanto a bilirrubina possuem propriedades pró e antioxidantes, além de propriedades tóxicas in vitro e in vivo. O aumento da biliverdina é detectado em indivíduos com necrose hepática e pode ampliar a atividade de certos oncogenes do fígado, ocasionando câncer. No entanto, em condições normais a atividade antioxidante da bilirrubina suplanta sua atividade prooxidante 38. A atividade antioxidante da bilirrubina ocorre principalmente quando se encontra ligada à albumina sérica, sendo esse complexo considerado um dos antioxidantes naturais dos fluidos extracelulares. Essa atividade acontece principalmente devido à sua grande reatividade com radicais peroxila (ROO ). No entanto, ela também reage com radicais superóxido a 1/10 da velocidade do ascorbato. A reação da bilirrubina com o oxigênio singleto é variável, podendo ser tanto um gerador a partir do oxigênio tripleto, quanto um desativador físico efetivo. Por último, essa exerce o papel de regeneradora do α-tocoferol, embora com menor importância que outros regeneradores, tais como o ascorbato (75) e a CoQ 10 (101) 16,38.
10 122 Barreiros et al. Quim. Nova Flavonóides como antioxidantes De modo geral, os polifenóis e em particular os flavonóides possuem estrutura ideal para o seqüestro de radicais, sendo antioxidantes mais efetivos que as vitaminas C e E. A atividade antioxidante dos flavonóides depende da sua estrutura e pode ser determinada por cinco fatores: reatividade como agente doador de H e elétrons, estabilidade do radical flavanoil formado, reatividade frente a outros antioxidantes, capacidade de quelar metais de transição e solubilidade e interação com as membranas. A atividade de seqüestro está diretamente ligada ao potencial de oxidação dos flavonóides e das espécies a serem seqüestradas. Quanto menor o potencial de oxidação do flavonóide, maior é sua atividade como seqüestrador de radicais livres. Flavonóides com potencial de oxidação menor que o do Fe +3 e Cu +2 e seus complexos podem reduzir esses metais, sendo potencialmente prooxidantes, tendo em vista que o Fe +2 e o Cu + participam da reação de Fenton geradora de radicais livres 39. Quanto maior o número de hidroxilas, maior a atividade como agente doador de H e de elétrons 40. Flavonóides monoidroxilados apresentam atividade muito baixa, por ex. a 5-hidroxi-flavona tem atividade abaixo dos limites de detecção. Flavonas possuindo apenas uma hidroxila em 3, 6, 3 ou 4, assim como flavanonas apresentando apenas uma hidroxila em 2 -OH, 3 -OH, 4 -OH, 6-OH também mostram fraca atividade. A 7-hidroxi-flavanona representa uma exceção, que pode ser justificada pela tendência maior da 7-OH em doar H devido à estabilização do radical formado por deslocalização com a carbonila em C-4 (110 e 111) (Figura 11). Figura 11. Flavonóides antioxidantes e mecanismo da estabilização elétron desemparelhado Entretanto, apesar dessa exceção, para proteger os lisossomos e outras membranas contra o estresse oxidativo foi constatada a necessidade de no mínimo duas hidroxilas fenólicas no flavonóide, demonstrando que os monoidroxiflavonóides não são efetivos. Entre os flavonóides diidroxilados, destacam-se aqueles que possuem o sistema catecol (3,4 -diidroxi) no anel B. Os flavonóides com múltiplas hidroxilas como a miricetina (118), quecertina (117), luteolina (119), fustina (120), eriodictiol (121) e taxifolina (122) possuem forte atividade antioxidante quando comparados ao α-tocoferol, ácido ascórbico, β-caroteno, glutationa, ácido úrico e bilirrubina 40,41 (Figura 11). A estabilidade do radical livre flavanoil formado depende da habilidade do flavonóide em deslocalizar o elétron desemparelhado. A presença de hidroxilas em orto é o principal fator que auxilia nessa deslocalização. Os outros fatores são a presença de insaturação no anel C e hidroxila em C-4 em B conjugada com a carbonila; ângulo do anel B do flavonóide e do radical formado em relação ao restante da estrutura, sendo que esse ângulo é regulado pela presença ou ausência de hidroxila em C-3; presença de duas insaturações em C; conjugação da carbonila em C-4 com hidroxila em C-5 e, presença de hidroxila em C A doação do H ocorre principalmente nas posições 7-OH > 4 -OH > 5-OH, seguindo a seqüência das constantes de dissociação 42. Os flavonóides, devido ao seu caráter fracamente ácido encontram-se, em geral, parcialmente ionizados, o que aumenta a estabilidade na posição C-4 e favorece a deslocalização do elétron desemparelhado do radical formado entre os anéis A, B e C [por ex., quercetina parcialmente ionizada em C-4 (112)]. A doação do H radicalar para o radical livre ocorre principalmente nas posições C-4 (113) e C-7 (114). Ambos os radicais livres formados podem ter seu elétron deslocalizado pela estrutura, com maior estabilidade para os radicais 113, 115 e 116, devido à estabilização resultante das ligações de hidrogênio 4,42,43. A remoção de metais de transição livres no meio biológico é fundamental para a proteção antioxidante do organismo, visto que esses catalisam as reações de Fenton (Equação 3) e de Haber- Weiss (Equação 15). Para a atividade de quelação de metais de transição é fundamental a presença de grupos orto-difenólicos, onde o mais comum é o sistema 3,4 -diidroxi, unidade catecol em B e/ou estruturas cetol como 4-ceto-3-hidroxi e 4-ceto-5- hidroxi. A substituição de qualquer uma das hidroxilas envolvidas na quelação de metais reduz essa atividade devido, principalmente, ao impedimento estérico provocado. Outros sistemas ortodifenólicos em flavonóides menos comuns também podem quelar os metais de transição, como por ex. o 6,7-diidroxi ou 7,8- diidroxi 4,39,43. O último fator importante que influencia a atividade antioxidante dos flavonóides é a sua interação com as biomembranas. A lipofilicidade do flavonóide indica a incorporação desse pela membrana, que é alvo da maioria das ERO e ERN. Assim, deve haver uma concentração mínima do flavonóide por ácido graxo, de modo a assegurar a presença de uma de suas moléculas próxima ao sítio de ataque do radical 44. Flavonóides que possuem uma cadeia de açúcares ligada em sua estrutura são muito polares, não sendo assimilados pela membrana, porém, nesta forma eles podem ser armazenados em vesículas, possuindo um tempo maior de permanência no organismo. Os flavonóides que são assimilados pelas membranas exercem a função de moduladores de fluidez. Restringindo essa fluidez os flavonóides geram um impedimento físico para a difusão das ERO e ERN, de modo que decresce a cinética das reações responsáveis pelo estresse oxidativo. Esse tipo de atividade antioxidante é similar ao relatado para o α-tocoferol e o colesterol 45.
11 Vol. 29, No. 1 Estresse Oxidativo: Relação entre Geração de Espécies Reativas 123 CONSIDERAÇÕES FINAIS O organismo humano está sujeito ao estresse oxidativo causado por ERO e ERN provenientes do meio ambiente ou geradas pelo próprio organismo. Entre as biomoléculas alvo dessas espécies encontram-se as que compõem membranas celulares, proteínas DNA e RNA. Hoje em dia sabe-se que a ação de espécies oxidantes sobre o DNA é responsável por mutação ou mesmo oncogênese. No entanto, o organismo é protegido em parte por macro e micromoléculas de origem endógenea ou obtidas diretamente da dieta. A proteção enzimática baseia-se quase que exclusivamente na decomposição de ânion superóxido ou dismutação de peróxido de hidrogênio, agentes oxidantes brandos. Cabe às micromoléculas, tais como tocoferóis, carotenóides e flavonóides entre outros, o papel de impedir o ataque de ERO e ERN ou regenerar os danos causados em sistemas biológicos essenciais. O mecanismo complexo de atividade anti e pró-oxidante destas substâncias é alvo de extensos estudos científicos contemporâneos, tendo em vista que o sucesso destas investigações está diretamente relacionado com a melhoria da qualidade de vida do ser humano. AGRADECIMENTOS Ao CNPq, à FAPESB e ao IMSEAR pelas bolsas e auxílios. LISTA DE ABREVIATURAS 8OHdA 5-8-ciclo-2 -desoxiadenosina 8OHdG 5-8-ciclo-2 -desoxiguanosina 8-oxoA 8-oxo-7,8-diidro-2 -desoxiadenosídeo 8-oxoG 8-oxo-7,8-diidro-2 -desoxiguanosídeo AG-CoA Ácido graxo coenzima A CAT - Catalase ERN Espécies Reativas de Nitrogênio ERO Espécies Reativas de Oxigênio FapyA 4,6-diamino-5-formamido-pirimidina FapyG 2,6-diamino-4-hidroxi-5-formamidopirimidina GPx Se-glutationa peroxidase GR Glutationa Redutase GSH Glutationa HPODE Ácido hidroperoxioctadecadienóico PMHC 2,2,5,7,8-pentametil-6-hidroxicromano S H i Substituição Homolítica Intramolecular SOD Superóxido dismutase TMMP 2,3,5,6-tetrametil-4-metoxifenol REFERÊNCIAS 1. Visioli, F.; Keaney Jr., J. F.; Halliwell, B.; Cardiovasc. Res. 2000, 47, Finkel, T.; Holbrook, N. J.; Nature 2000, 408, Halliwell, B.; The Lancet 2000, 355, Pietta, P.; J. Nat. Prod. 2000, 63, Husain, S. R.; Cillard, J.; Cillard, P.; Phytochemistry 1987, 26, Halliwell, B.; Gutteridge, J. M. C.; Cross, C. E.; J. Lab. Clin. Med. 1992, 119, Halliwell, B.; Aeschbach, R.; Loliger, J.; Arouma, O. I.; Food Chem. Toxicol. 1995, 33, Ho, C. T.; Ferraro, T.; Chen, Q.; Hosen, R. T.; Huang, M. T. Em Food Phytochemicals for Cancer Prevention II; Ho, C. T.; Osawa, T.; Huang, M. T.; Hosen, R. T., eds.; American Chemical Society: Washington DC, 1994, p Fauré, M.; Lessi, E.; Torres, R.; Videla, C. A.; Phytochemistry 1984, 29, Halliwell, B.; Mutat. Res. 1999, 443, 37; Chatgilialoglu, C.; O neill, P.; Exp. Gerontol. 2001, 36, 1459; Wiseman, H.; Kaur, H.; Halliwell, B.; Cancer Lett. 1995, 93, 113; Cadet, J.; Delatour, T.; Douki, T.; Gasparutto, D.; Pouget, J. P.; Ravanat J. L.; Sauvaigo, S.; Mutat. Res. 1999, 424, Berger, P.; Leitner, N. K. V.; Doré, M.; Legube B.; Water Res.1999, 33, Schöneich, C.; Exp. Gerontol. 1999, 34, Zhao, F.; Ghezzo-Schöneich, E.; Aced, G. I.; Hong, J.; Milby, T.; Schöneich C.; J. Biol. Chem. 1997, 272, Vogt, W.; Free Radical Biol. Med. 1995, 18, Blair, I. A.; Exp. Gerontol. 2001, 36, Larson, R. A.; Naturally Occurring Antioxidants, Lewis Publishers: New York, 1997, p Jin, F.; Leitich, J.; Sonntag, C. V.; J. Photochem. Photobiol., A 1995, 92, Halliwell, B.; Clement, M. V.; Long, L. H.; FEBS Lett. 2000, 486, 10; Babior, B. M.; Am. J. Med. 2000, 109, Babior, B. M.; Braz. J. Med. Biol. Res. 1997, 30, Kehrer, J. P.; Toxicology 2000, 149, Tamir, S.; Tannenbaum, S. R.; Biochim. Biophys. Acta 1996, 1288, F Eiserich, J. P.; Cross, C. E.; Jones, A. D.; Halliwell, B.; Vliet, A. V.; J. Biol. Chem. 1996, 271, Denicola, A.; Freeman, B. A.; Trujillo, M.; Radi, R.; Arch. Biochem. Biophys. 1996, 333, Halliwell, B.; Trends Biochem. Sci. 1999, 24, 255; Levine, M.; Daruwala, R. C.; Park, J. B.; Rumsey, S. C.; Wang, Y.; Nature 1998, 395, 231; Podmore, I. D.; Griffiths, H. R.; Herbert, K. E.; Mistry, N.; Mistry, P.; Lunec, J.; Nature 1998, 392, Buettner, G. R.; Arch. Biochem. Biophys. 1993, 300, Theriault, A.; Chao, J-T.; Wang, Q.; Gapor, A.; Adeli, K.; Clin. Biochem. 1999, 32, Jacob, R. A.; Nutr. Res. 1995, 15, Burton, G. W.; Ingold, K. U.; J. Am. Chem. Soc. 1981, 103, Burri, B. J.; Nutr. Res. 1997, 17, 547; Palace, V. P.; Khaper, N.; Qin, Q.; Singal, P. K.; Free Radical Biol. Med. 1999, 26, Mordi, R. C.; Walton, J. C.; Tetrahedron 1993, 49, Woodall, A. A.; Lee, S. W-M.; Weesie, R. J.; Jackson, M. J.; Britton, G.; Biochim. Biophys. Acta 1997, 1336, 33; Woodall, A. A.; Britton, G.; Jackson, M. J.; Biochim. Biophys. Acta 1997, 1336, Lehninger, A. L.; Nelson, D. C.; Cox, M. M.; Princípios de Bioquímica, 2 a ed.; Sarvier Ed. Ltda.: São Paulo, 1995, p Dallner, G.; Sindelar, P. J.; Free Radical Biol. Med. 2000, 29, 285; Nohl, H.; Kozlov, A. V.; Staniek, K.; Gille, L.; Bioorg. Chem. 2001, 29, Nohl, H.; Gille, L.; Kozlov, A. V.; Free Radical Biol. Med. 1998, 25, 666; Bliznakov, E. G.; Cardiovasc. Res. 1999, 43, Kagan, V. E.; Arroyo, A.; Tyurin, V. A.; Tyurina, Y. Y.; Villalba, J. M.; Navas, P.; FEBS Lett. 1998, 428, Nieto, F. J.; Iribarren, C.; Gross, M. D.; Comstock, G. W.; Cutler, R. G.; Atherosclerosis 2000, 148, 131; Simic, M. G.; Jovanovic, S. V.; J. Am. Chem. Soc. 1989, 111, Dailly, E.; Urien, S.; Barré, J.; Reinert, P.; Tillement, J. P.; Biochem. Biophys. Res. Commun. 1998, 248, Asad, S. F.; Sing, S.; Ahmad, A.; Khan, N. U.; Hadi, S. M.; Chem.-Biol. Interact. 2001, 137, Rice-Evans, C. A.; Miller, N. J.; Paganga, G.; Trends Plant Sci. 1997, 2, Cao, G.; Sofic, E.; Prior, R. L.; Free Radical Biol. Med. 1997, 22, Yang, B.; Koiani, A.; Arai, K.; Kusu, F.; Chem. Pharm. Bull. 2001, 49, Rice-Evans, C. A.; Miller, N. J.; Paganga, G.; Free Radical Biol. Med. 1996, 20, Bors, W.; Heller, W.; Michel, C.; Saran, M.; Methods in Enzimology, Academic Press: New York, 1990, vol. 186, p. 343; van Acker, S. A. B. E.; van Balen, G. P.; van den Berg, D-J.; Bast, A.; van der Vijgh, W. J. F.; Biochem. Pharmacol. 1998, 56, van Acker, S. A. B. E.; van den Berg, D-J.; Tromp, M. N. J. L.; Griffioen, D. H.; van Bennekom, W. P.; van der Vugh, W. J. F.; Bast, A.; Free Radical Biol. Med. 1996, 20, Arora, A.; Byrem, T. M.; Nair, M. G.; Strasburg, G. M.; Arch. Biochem. Biophys. 2000, 373, 102; Arora, A.; Nair, M. G.; Strasburg, G. M. Arch. Biochem. Biophys. 1998, 356, Stanley, L. L.; Mazier, M. J. P.; Nutr. Res. 1999, 19, 3.
Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I. Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas.
 Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I Acompanhe! Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas. Introdução: A proteína é o composto orgânico mais abundante
Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I Acompanhe! Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas. Introdução: A proteína é o composto orgânico mais abundante
METABOLISMO ENERGÉTICO RESPIRAÇÃO CELULAR FERMENTAÇÃO FOTOSSÍNTESE QUIMIOSSÍNTESE
 METABOLISMO ENERGÉTICO RESPIRAÇÃO CELULAR FERMENTAÇÃO FOTOSSÍNTESE QUIMIOSSÍNTESE RESPIRAÇÃO CELULAR Processo de produção de energia a partir da degradação completa de compostos orgânicos energéticos (ex.:
METABOLISMO ENERGÉTICO RESPIRAÇÃO CELULAR FERMENTAÇÃO FOTOSSÍNTESE QUIMIOSSÍNTESE RESPIRAÇÃO CELULAR Processo de produção de energia a partir da degradação completa de compostos orgânicos energéticos (ex.:
METABOLISMO ENERGÉTICO RESPIRAÇÃO CELULAR FERMENTAÇÃO FOTOSSÍNTESE QUIMIOSSÍNTESE
 METABOLISMO ENERGÉTICO RESPIRAÇÃO CELULAR FERMENTAÇÃO FOTOSSÍNTESE QUIMIOSSÍNTESE RESPIRAÇÃO CELULAR Processo de produção de energia a partir da degradação completa de compostos orgânicos energéticos (ex.:
METABOLISMO ENERGÉTICO RESPIRAÇÃO CELULAR FERMENTAÇÃO FOTOSSÍNTESE QUIMIOSSÍNTESE RESPIRAÇÃO CELULAR Processo de produção de energia a partir da degradação completa de compostos orgânicos energéticos (ex.:
Biologia-Prof.Barão. Metabolismo Energético: Respiração Celular e Fermentação
 Biologia-Prof.Barão Metabolismo Energético: Respiração Celular e Fermentação Metabolismo Energético I Conceitos básicos: 1-Metabolismo 2-Reações Exergônicas e Endergônicas 3-Reação de Redox(Oxidação-Redução)
Biologia-Prof.Barão Metabolismo Energético: Respiração Celular e Fermentação Metabolismo Energético I Conceitos básicos: 1-Metabolismo 2-Reações Exergônicas e Endergônicas 3-Reação de Redox(Oxidação-Redução)
BASES MACROMOLECULARES DA CONSTITUIÇÃO CELULAR
 BASES MACROMOLECULARES DA CONSTITUIÇÃO CELULAR As moléculas que constituem as células são formadas pelos mesmos átomos encontrados nos seres inanimados. Todavia, na origem e evolução das células, alguns
BASES MACROMOLECULARES DA CONSTITUIÇÃO CELULAR As moléculas que constituem as células são formadas pelos mesmos átomos encontrados nos seres inanimados. Todavia, na origem e evolução das células, alguns
Na aula de hoje, iremos ampliar nossos conhecimentos sobre as funções das proteínas. Acompanhe!
 Aula: 21 Temática: Funções bioquímicas das proteínas parte III Na aula de hoje, iremos ampliar nossos conhecimentos sobre as funções das proteínas. Acompanhe! 1) Função Estrutural (Arquitetônica): Os materiais
Aula: 21 Temática: Funções bioquímicas das proteínas parte III Na aula de hoje, iremos ampliar nossos conhecimentos sobre as funções das proteínas. Acompanhe! 1) Função Estrutural (Arquitetônica): Os materiais
(2) converter as moléculas dos nutrientes em unidades fundamentais precursoras das macromoléculas celulares;
 INTRODUÇÃO AO METABOLISMO Metabolismo é o conjunto das reações químicas que ocorrem num organismo vivo com o fim de promover a satisfação de necessidades estruturais e energéticas. O metabolismo tem quatro
INTRODUÇÃO AO METABOLISMO Metabolismo é o conjunto das reações químicas que ocorrem num organismo vivo com o fim de promover a satisfação de necessidades estruturais e energéticas. O metabolismo tem quatro
BIOFÍSICA DAS RADIAÇÕES IONIZANTES
 BIOFÍSICA DAS RADIAÇÕES IONIZANTES DANOS RADIOINDUZIDOS NA MOLÉCULA DE DNA Por ser responsável pela codificação da estrutura molecular de todas as enzimas da células, o DNA passa a ser a molécula chave
BIOFÍSICA DAS RADIAÇÕES IONIZANTES DANOS RADIOINDUZIDOS NA MOLÉCULA DE DNA Por ser responsável pela codificação da estrutura molecular de todas as enzimas da células, o DNA passa a ser a molécula chave
Profa. Alessandra Barone www.profbio.com.br
 Profa. Alessandra Barone www.profbio.com.br Digestão de lipídeos A maior parte de nossa ingestão de lipídeos é feita sob a forma de triacilgliceróis Hidrólise inicia-se pela ação da lipase lingual, ativada
Profa. Alessandra Barone www.profbio.com.br Digestão de lipídeos A maior parte de nossa ingestão de lipídeos é feita sob a forma de triacilgliceróis Hidrólise inicia-se pela ação da lipase lingual, ativada
RANCIDEZ OXIDATIVA ALIMENTOS
 A RANCIDEZ OXIDATIVA EM ALIMENTOS Os lipídios ocorrem em quase todas as matérias-primas alimentícias, sendo as principais classes os triglicérides (também conhecidos como triacilgliceróis), que ocorrem
A RANCIDEZ OXIDATIVA EM ALIMENTOS Os lipídios ocorrem em quase todas as matérias-primas alimentícias, sendo as principais classes os triglicérides (também conhecidos como triacilgliceróis), que ocorrem
Proteínas. As proteínas são o centro da acção em todos os processos biológicos. Voet & Voet Biochemistry
 Proteínas As proteínas são o centro da acção em todos os processos biológicos. Voet & Voet Biochemistry As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (~50% do peso sêco)
Proteínas As proteínas são o centro da acção em todos os processos biológicos. Voet & Voet Biochemistry As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (~50% do peso sêco)
BANCO DE QUESTÕES - BIOLOGIA - 1ª SÉRIE - ENSINO MÉDIO ==============================================================================================
 PROFESSOR: Leonardo Mariscal BANCO DE QUESTÕES - BIOLOGIA - 1ª SÉRIE - ENSINO MÉDIO ============================================================================================== Assunto: Organelas citoplasmáticas
PROFESSOR: Leonardo Mariscal BANCO DE QUESTÕES - BIOLOGIA - 1ª SÉRIE - ENSINO MÉDIO ============================================================================================== Assunto: Organelas citoplasmáticas
C 5 H 12 O álcool 88g/mol. x 12,5g x = 9,94g 5CO 2 + 5H 2 O
 Questão 1 O esquema abaixo mostra compostos que podem ser obtidos a partir de um alceno de fórmula molecular C 5 H 10. A seguir, responda às questões relacionadas a esse esquema, considerando sempre o
Questão 1 O esquema abaixo mostra compostos que podem ser obtidos a partir de um alceno de fórmula molecular C 5 H 10. A seguir, responda às questões relacionadas a esse esquema, considerando sempre o
UFMG - 2003 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR
 UFMG - 2003 3º DIA QUÍMICA BERNULLI CLÉGI E PRÉ-VESTIBULAR Química Questão 01 A glicose, C 6 6, é uma das fontes de energia mais importantes para os organismos vivos. A levedura, por exemplo, responsável
UFMG - 2003 3º DIA QUÍMICA BERNULLI CLÉGI E PRÉ-VESTIBULAR Química Questão 01 A glicose, C 6 6, é uma das fontes de energia mais importantes para os organismos vivos. A levedura, por exemplo, responsável
Metais em água. metais tem um papel crucial em. como espécies hidroxiladas, ex.: FeOH(H 2 O)
 Metais em água Para a estabilização dos elétrons mais externos os cátions metálicos em água são ligados (coordenados) a outras espécies. Assim, os metais em soluções aquosas procuram a máxima estabilidade
Metais em água Para a estabilização dos elétrons mais externos os cátions metálicos em água são ligados (coordenados) a outras espécies. Assim, os metais em soluções aquosas procuram a máxima estabilidade
METABOLISMO DAS PROTEÍNAS. Bioquímica Básica Ciências Biológicas 3º período Cátia Capeletto
 METABOLISMO DAS PROTEÍNAS Bioquímica Básica Ciências Biológicas 3º período Cátia Capeletto Aminoácido Os aminoácidos livres são obtidos da degradação da proteína da dieta, da renovação constante das proteínas
METABOLISMO DAS PROTEÍNAS Bioquímica Básica Ciências Biológicas 3º período Cátia Capeletto Aminoácido Os aminoácidos livres são obtidos da degradação da proteína da dieta, da renovação constante das proteínas
BASES NITROGENADAS DO RNA
 BIO 1E aula 01 01.01. A determinação de como deve ser uma proteína é dada pelos genes contidos no DNA. Cada gene é formado por uma sequência de códons, que são sequências de três bases nitrogenadas que
BIO 1E aula 01 01.01. A determinação de como deve ser uma proteína é dada pelos genes contidos no DNA. Cada gene é formado por uma sequência de códons, que são sequências de três bases nitrogenadas que
Biologia. Sistema circulatório
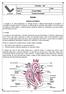 Aluno (a): Série: 3ª Turma: TUTORIAL 10R Ensino Médio Equipe de Biologia Data: Biologia Sistema circulatório O coração e os vasos sanguíneos e o sangue formam o sistema cardiovascular ou circulatório.
Aluno (a): Série: 3ª Turma: TUTORIAL 10R Ensino Médio Equipe de Biologia Data: Biologia Sistema circulatório O coração e os vasos sanguíneos e o sangue formam o sistema cardiovascular ou circulatório.
NUTRIÇÃO DE GATOS. DUTRA, Lara S. 1 ; CENTENARO, Vanessa B. 2 ; ARALDI, Daniele Furian 3. Palavras-chave: Nutrição. Gatos. Alimentação.
 NUTRIÇÃO DE GATOS DUTRA, Lara S. 1 ; CENTENARO, Vanessa B. 2 ; ARALDI, Daniele Furian 3 Palavras-chave: Nutrição. Gatos. Alimentação. Introdução Nutrição veterinária é a ciência que tem por objetivo descobrir
NUTRIÇÃO DE GATOS DUTRA, Lara S. 1 ; CENTENARO, Vanessa B. 2 ; ARALDI, Daniele Furian 3 Palavras-chave: Nutrição. Gatos. Alimentação. Introdução Nutrição veterinária é a ciência que tem por objetivo descobrir
3ª Série / Vestibular
 3ª Série / Vestibular 01. Uma característica típica de todo o tecido conjuntivo é: (A) apresentar células em camadas unidas; (B) apresentar poucas camadas de células; (C) apresentar muito material intersticial;
3ª Série / Vestibular 01. Uma característica típica de todo o tecido conjuntivo é: (A) apresentar células em camadas unidas; (B) apresentar poucas camadas de células; (C) apresentar muito material intersticial;
SANGUE (composição, células, coagulação, hemograma)
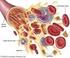 SANGUE (composição, células, coagulação, hemograma) Introdução A função básica do sistema cardiovascular é comunicação das células entre si, produzindo um fluxo, e com o meio externo, havendo uma integração
SANGUE (composição, células, coagulação, hemograma) Introdução A função básica do sistema cardiovascular é comunicação das células entre si, produzindo um fluxo, e com o meio externo, havendo uma integração
Membranas Biológicas e Transporte
 Universidade Federal do Ceará Centro de Ciências Departamento de Bioquímica e Biologia Molecular Disciplina de Introdução a Bioquímica Membranas Biológicas e Transporte 1. Introdução 2. Os Constituintes
Universidade Federal do Ceará Centro de Ciências Departamento de Bioquímica e Biologia Molecular Disciplina de Introdução a Bioquímica Membranas Biológicas e Transporte 1. Introdução 2. Os Constituintes
CADERNO DE EXERCÍCIOS 2F
 CADERNO DE EXERCÍCIOS 2F Ensino Médio Ciências da Natureza Questão 1. 2. Conteúdo Extração do ferro a partir do minério, representações químicas das substâncias e reações químicas Habilidade da Matriz
CADERNO DE EXERCÍCIOS 2F Ensino Médio Ciências da Natureza Questão 1. 2. Conteúdo Extração do ferro a partir do minério, representações químicas das substâncias e reações químicas Habilidade da Matriz
Aula: 12 Temática: Metabolismo das principais biomoléculas parte IV. Na aula de hoje iremos estudar a fermentação. Boa aula!
 Aula: 12 Temática: Metabolismo das principais biomoléculas parte IV Na aula de hoje iremos estudar a fermentação. Boa aula! Fermentação O Piruvato, produto da glicólise, pode continuar sendo processado
Aula: 12 Temática: Metabolismo das principais biomoléculas parte IV Na aula de hoje iremos estudar a fermentação. Boa aula! Fermentação O Piruvato, produto da glicólise, pode continuar sendo processado
Protocolos de Tratamento
 !"#$%$%&'()*+,"-)'(*).(/'"+%$/'"/0$+/1%*"2')0$#+ 0"+ 3456+ 789+ :",0"6+ ;#
!"#$%$%&'()*+,"-)'(*).(/'"+%$/'"/0$+/1%*"2')0$#+ 0"+ 3456+ 789+ :",0"6+ ;#
Profº André Montillo www.montillo.com.br
 Profº André Montillo www.montillo.com.br Definição: É a soma de todas as reações químicas envolvidas na manutenção do estado dinâmico das células, onde milhares de reações ocorrem ao mesmo tempo, determinando
Profº André Montillo www.montillo.com.br Definição: É a soma de todas as reações químicas envolvidas na manutenção do estado dinâmico das células, onde milhares de reações ocorrem ao mesmo tempo, determinando
UFMG - 2005 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR
 UFMG - 2005 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR Química Questão 01 Carbono é um elemento cujos átomos podem se organizar sob a forma de diferentes alótropos. Alótropos H de combustão a 25
UFMG - 2005 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR Química Questão 01 Carbono é um elemento cujos átomos podem se organizar sob a forma de diferentes alótropos. Alótropos H de combustão a 25
EXERCÍCIOS DE REVISÃO CITOPLASMA E METABOLISMO
 Componente Curricular: Biologia Professor: Leonardo Francisco Stahnke Aluno(a): Turma: Data: / /2015 EXERCÍCIOS DE REVISÃO CITOPLASMA E METABOLISMO 1. A respeito da equação ao lado, que representa uma
Componente Curricular: Biologia Professor: Leonardo Francisco Stahnke Aluno(a): Turma: Data: / /2015 EXERCÍCIOS DE REVISÃO CITOPLASMA E METABOLISMO 1. A respeito da equação ao lado, que representa uma
Questão 41. (Valor: 10 pontos)
 Questão 41 (Valor: 10 pontos) O superóxido, o peróxido de hidrogênio e o radical livre hidroxil são exemplos de moléculas que compõem as espécies reativas de oxigênio (ERO). Esses compostos são formados
Questão 41 (Valor: 10 pontos) O superóxido, o peróxido de hidrogênio e o radical livre hidroxil são exemplos de moléculas que compõem as espécies reativas de oxigênio (ERO). Esses compostos são formados
Dra. Kátia R. P. de Araújo Sgrillo. sgrillo.ita@ftc.br
 Dra. Kátia R. P. de Araújo Sgrillo sgrillo.ita@ftc.br A glicólise é provavelmente a via bioquímica mais bem compreendida. Desempenha uma função central no metabolismo energético, fornecendo uma porção
Dra. Kátia R. P. de Araújo Sgrillo sgrillo.ita@ftc.br A glicólise é provavelmente a via bioquímica mais bem compreendida. Desempenha uma função central no metabolismo energético, fornecendo uma porção
CONTROLE E INTEGRAÇÂO
 CONTROLE E INTEGRAÇÂO A homeostase é atingida através de uma série de mecanismos reguladores que envolve todos os órgãos do corpo. Dois sistemas, entretanto, são destinados exclusivamente para a regulação
CONTROLE E INTEGRAÇÂO A homeostase é atingida através de uma série de mecanismos reguladores que envolve todos os órgãos do corpo. Dois sistemas, entretanto, são destinados exclusivamente para a regulação
MEMBRANA PLASMÁTICA. Modelo do mosaico fluido caráter dinâmico à estrutura da membrana (as proteínas estão em constante deslocamento lateral)
 MEMBRANA PLASMÁTICA Modelo do mosaico fluido caráter dinâmico à estrutura da membrana (as proteínas estão em constante deslocamento lateral) ESTRUTURA DA MEMBRANA Formada por fosfolipídios e (nas animais
MEMBRANA PLASMÁTICA Modelo do mosaico fluido caráter dinâmico à estrutura da membrana (as proteínas estão em constante deslocamento lateral) ESTRUTURA DA MEMBRANA Formada por fosfolipídios e (nas animais
Reações orgânicas. Mestranda: Daniele Potulski Disciplina: Química da Madeira I
 Reações orgânicas Mestranda: Daniele Potulski Disciplina: Química da Madeira I Introdução Quase todos os compostos orgânicos tem moléculas apolares ou com baixa polaridade; Essa característica é um fator
Reações orgânicas Mestranda: Daniele Potulski Disciplina: Química da Madeira I Introdução Quase todos os compostos orgânicos tem moléculas apolares ou com baixa polaridade; Essa característica é um fator
Lembrete: Antes de começar a copiar cada unidade, coloque o cabeçalho da escola e a data!
 Lembrete: Antes de começar a copiar cada unidade, coloque o cabeçalho da escola e a data! Use canetas coloridas ou escreva palavras destacadas, para facilitar na hora de estudar. E capriche! Não se esqueça
Lembrete: Antes de começar a copiar cada unidade, coloque o cabeçalho da escola e a data! Use canetas coloridas ou escreva palavras destacadas, para facilitar na hora de estudar. E capriche! Não se esqueça
2. Nesse sistema, ocorre uma relação de protocooperação entre algas e bactérias.
 PROVA DE BIOLOGIA QUESTÃO 01 Entre os vários sistemas de tratamento de esgoto, o mais econômico são as lagoas de oxidação. Essas lagoas são reservatórios especiais de esgoto, que propiciam às bactérias
PROVA DE BIOLOGIA QUESTÃO 01 Entre os vários sistemas de tratamento de esgoto, o mais econômico são as lagoas de oxidação. Essas lagoas são reservatórios especiais de esgoto, que propiciam às bactérias
SISTEMA DIGESTÓRIO. Quitéria Paravidino
 SISTEMA DIGESTÓRIO Quitéria Paravidino PROCESSOS DIGESTÓRIOS Ingestão:captar alimento pela boca; Mistura e movimentação do alimento:contrações musculares misturam o alimento e as secreções e movimentam
SISTEMA DIGESTÓRIO Quitéria Paravidino PROCESSOS DIGESTÓRIOS Ingestão:captar alimento pela boca; Mistura e movimentação do alimento:contrações musculares misturam o alimento e as secreções e movimentam
Ciências E Programa de Saúde
 Governo do Estado de São Paulo Secretaria de Estado da Educação Ciências E Programa de Saúde 13 CEEJA MAX DADÁ GALLIZZI PRAIA GRANDE SP Vai e avisa a todo mundo que encontrar que ainda existe um sonho
Governo do Estado de São Paulo Secretaria de Estado da Educação Ciências E Programa de Saúde 13 CEEJA MAX DADÁ GALLIZZI PRAIA GRANDE SP Vai e avisa a todo mundo que encontrar que ainda existe um sonho
01 Processos Químicos. Prof. Dr. Sergio Pilling Aluno: Will Robson Monteiro Rocha
 Física e a Química do Meio Interestelar Mestrado e Doutorado em Física e Astronomia Livro texto: Physics and chemistry of the interestellar medium A. G. G. M. Tielens (2004) Prof. Dr. Sergio Pilling Aluno:
Física e a Química do Meio Interestelar Mestrado e Doutorado em Física e Astronomia Livro texto: Physics and chemistry of the interestellar medium A. G. G. M. Tielens (2004) Prof. Dr. Sergio Pilling Aluno:
- TERCEIRÃO 2012. COLÉGIO CEC CENTRO EDUCACIONAL CIANORTE ED. INFANTIL, ENS. FUNDAMENTAL E MÉDIO - SISTEMA ANGLO DE ENSINO. PROF.
 - TERCEIRÃO 2012. COLÉGIO CEC CENTRO EDUCACIONAL CIANORTE ED. INFANTIL, ENS. FUNDAMENTAL E MÉDIO - SISTEMA ANGLO DE ENSINO. PROF. NANNI 01) (UFPE) O esquema abaixo representa o elo entre os processos de
- TERCEIRÃO 2012. COLÉGIO CEC CENTRO EDUCACIONAL CIANORTE ED. INFANTIL, ENS. FUNDAMENTAL E MÉDIO - SISTEMA ANGLO DE ENSINO. PROF. NANNI 01) (UFPE) O esquema abaixo representa o elo entre os processos de
Os lipídeos se encontram distribuídos em todos os tecidos, principalmente nas membranas celulares.
 LIPÍDEOS Os lipídeos se encontram distribuídos em todos os tecidos, principalmente nas membranas celulares. Por convenção (Congresso Internacional de Bioquímica em 1922) ésteres de ácidos graxos, ou seja,
LIPÍDEOS Os lipídeos se encontram distribuídos em todos os tecidos, principalmente nas membranas celulares. Por convenção (Congresso Internacional de Bioquímica em 1922) ésteres de ácidos graxos, ou seja,
Onze superalimentos que você deveria consumir mais
 1 Onze superalimentos que você deveria consumir mais Eles são pouco populares, mas enchem o prato de vitaminas, minerais e proteínas Por Fernando Menezes - atualizado em 07/05/2012 http://www.minhavida.com.br/alimentacao/galerias/12441-onze-superalimentos-que-voce-deveria-consumirmais?utm_source=news_mv&utm_medium=alimentacao&utm_campaign=785913
1 Onze superalimentos que você deveria consumir mais Eles são pouco populares, mas enchem o prato de vitaminas, minerais e proteínas Por Fernando Menezes - atualizado em 07/05/2012 http://www.minhavida.com.br/alimentacao/galerias/12441-onze-superalimentos-que-voce-deveria-consumirmais?utm_source=news_mv&utm_medium=alimentacao&utm_campaign=785913
Estresse Oxidativo e Interface com Doenças Crônicas
 Estresse Oxidativo e Interface com Doenças Crônicas Karin Argenti Simon karsimon.unifesp@gmail.com VII Simpósio Internacional de Alergia Alimentar em Pediatria IX Jornada de Atualização em Nutrição Pediátrica
Estresse Oxidativo e Interface com Doenças Crônicas Karin Argenti Simon karsimon.unifesp@gmail.com VII Simpósio Internacional de Alergia Alimentar em Pediatria IX Jornada de Atualização em Nutrição Pediátrica
METABOLISMO CELULAR. Professor Felipe Abs
 METABOLISMO CELULAR Professor Felipe Abs O que é ENERGIA??? Físicos energia é a capacidade de realizar trabalhos; Biólogos energia é a capacidade de provocar mudanças; É indispensável para os seres vivos;
METABOLISMO CELULAR Professor Felipe Abs O que é ENERGIA??? Físicos energia é a capacidade de realizar trabalhos; Biólogos energia é a capacidade de provocar mudanças; É indispensável para os seres vivos;
Zinco quelato. Identificação. Peso molecular: Não aplicável. CAS: Não aplicável
 Material Técnico Zinco quelato Identificação Fórmula Molecular: Não aplicável DCB / DCI: Não aplicável INCI: Não aplicável Peso molecular: Não aplicável CAS: Não aplicável Denominação botânica: Não aplicável
Material Técnico Zinco quelato Identificação Fórmula Molecular: Não aplicável DCB / DCI: Não aplicável INCI: Não aplicável Peso molecular: Não aplicável CAS: Não aplicável Denominação botânica: Não aplicável
Vida saudável. Dicas e possibilidades nos dias de hoje.
 CENTRO UNIVERSITÁRIO ASSUNÇÃO- Vida saudável. Dicas e possibilidades nos dias de hoje. Profa. Dra. Valéria Batista O que é vida saudável? O que é vida saudável? Saúde é o estado de complexo bem-estar físico,
CENTRO UNIVERSITÁRIO ASSUNÇÃO- Vida saudável. Dicas e possibilidades nos dias de hoje. Profa. Dra. Valéria Batista O que é vida saudável? O que é vida saudável? Saúde é o estado de complexo bem-estar físico,
DOSSIER INFORMATIVO. Descodificar o conceito dos antioxidantes
 DOSSIER INFORMATIVO Descodificar o conceito dos antioxidantes 1 QUADRO RESUMO aos antioxidantes ajudam o organismo a combater os efeitos nefastos dos radicais livres; aos radicais livres são elementos
DOSSIER INFORMATIVO Descodificar o conceito dos antioxidantes 1 QUADRO RESUMO aos antioxidantes ajudam o organismo a combater os efeitos nefastos dos radicais livres; aos radicais livres são elementos
VITAMINA K2. Saúde Óssea e Cardiovascular
 Informações Técnicas VITAMINA K2 Saúde Óssea e Cardiovascular FÓRMULA MOLECULAR: C 46H 64O 2 PESO MOLECULAR: 648,99 CAS NUMBER: 2124-57-4 INTRODUÇÃO A vitamina K ocorre naturalmente em 2 formas principais:
Informações Técnicas VITAMINA K2 Saúde Óssea e Cardiovascular FÓRMULA MOLECULAR: C 46H 64O 2 PESO MOLECULAR: 648,99 CAS NUMBER: 2124-57-4 INTRODUÇÃO A vitamina K ocorre naturalmente em 2 formas principais:
São catalisadores biológicos de alta especificidade. Catalisar uma reação química é alterar a sua
 Profa Alessandra Barone Enzimas São catalisadores biológicos de alta especificidade. Catalisar uma reação química é alterar a sua velocidade, ou seja, a quantidade de massa de reagentes (S) transformada
Profa Alessandra Barone Enzimas São catalisadores biológicos de alta especificidade. Catalisar uma reação química é alterar a sua velocidade, ou seja, a quantidade de massa de reagentes (S) transformada
CLOROPLASTOS E FOTOSSÍNTESE
 CLOROPLASTOS E FOTOSSÍNTESE Cloroplastos Plastos ou plastídeos com pigmentos coloridos (cromoplastos), sendo o pigmento predominante a clorofila, responsável pela absorção de energia luminosa. Nos vegetais
CLOROPLASTOS E FOTOSSÍNTESE Cloroplastos Plastos ou plastídeos com pigmentos coloridos (cromoplastos), sendo o pigmento predominante a clorofila, responsável pela absorção de energia luminosa. Nos vegetais
TESTES REFERENTES A PARTE 1 DA APOSTILA FUNDAMENTOS DA CORROSÃO INDIQUE SE AS AFIRMAÇÕES A SEGUIR ESTÃO CERTAS OU ERRADAS
 TESTES REFERENTES A PARTE 1 DA APOSTILA FUNDAMENTOS DA CORROSÃO INDIQUE SE AS AFIRMAÇÕES A SEGUIR ESTÃO CERTAS OU ERRADAS 1) Numa célula eletroquímica a solução tem que ser um eletrólito, mas os eletrodos
TESTES REFERENTES A PARTE 1 DA APOSTILA FUNDAMENTOS DA CORROSÃO INDIQUE SE AS AFIRMAÇÕES A SEGUIR ESTÃO CERTAS OU ERRADAS 1) Numa célula eletroquímica a solução tem que ser um eletrólito, mas os eletrodos
Marcos Luppi Engº Ambiental. Desinfecção da Água
 Marcos Luppi Engº Ambiental Desinfecção da Água Um dos principais problemas que surgiram neste século é a crescente contaminação da água, recurso que vem sendo poluído de tal maneira que em muitos casos
Marcos Luppi Engº Ambiental Desinfecção da Água Um dos principais problemas que surgiram neste século é a crescente contaminação da água, recurso que vem sendo poluído de tal maneira que em muitos casos
PROVA DE BIOLOGIA. Observe o esquema, que representa o transporte de lipoproteína LDL para dentro da célula. Receptores de LDL.
 11 PROVA DE BIOLOGIA Q U E S T Ã O 1 6 Observe o esquema, que representa o transporte de lipoproteína LDL para dentro da célula. Partícula de LDL (Lipoproteína de baixa densidade) Receptores de LDL Endossomo
11 PROVA DE BIOLOGIA Q U E S T Ã O 1 6 Observe o esquema, que representa o transporte de lipoproteína LDL para dentro da célula. Partícula de LDL (Lipoproteína de baixa densidade) Receptores de LDL Endossomo
Bolsa limitada por duas membranas semelhantes à membrana plasmática. A interna forma uma série de dobras ou septos, as cristas mitocondriais, entre
 Bolsa limitada por duas membranas semelhantes à membrana plasmática. A interna forma uma série de dobras ou septos, as cristas mitocondriais, entre as quais há uma solução gelatinosa, a matriz mitocondrial.
Bolsa limitada por duas membranas semelhantes à membrana plasmática. A interna forma uma série de dobras ou septos, as cristas mitocondriais, entre as quais há uma solução gelatinosa, a matriz mitocondrial.
Matéria: Biologia Assunto: Ciclos Biogeoquímicos Prof. Enrico Blota
 Matéria: Biologia Assunto: Ciclos Biogeoquímicos Prof. Enrico Blota Biologia Ecologia Ciclos biogeoquímicos Ciclo da água Proporção de água doce e água salgada no planeta A água encontrada na atmosfera
Matéria: Biologia Assunto: Ciclos Biogeoquímicos Prof. Enrico Blota Biologia Ecologia Ciclos biogeoquímicos Ciclo da água Proporção de água doce e água salgada no planeta A água encontrada na atmosfera
9/9/2008 CONSIDERAÇÕES GERAIS. Toxicidade. Faixa terapêutica. Concentrações sub-terapêuticas. - Não sofre efeito de primeira passagem
 CONSIDERAÇÕES GERAIS Princípios de Farmacologia: Farmacocinética Farmacodinâmica Concentração plasmática Toxicidade Faixa terapêutica Concentrações sub-terapêuticas Tempo VIAS DE ADMINISTRAÇÃO DE MEDICAMENTOS
CONSIDERAÇÕES GERAIS Princípios de Farmacologia: Farmacocinética Farmacodinâmica Concentração plasmática Toxicidade Faixa terapêutica Concentrações sub-terapêuticas Tempo VIAS DE ADMINISTRAÇÃO DE MEDICAMENTOS
ESTUDO DA FARMACOLOGIA Introdução - Parte II
 NESP UNIVERSIDADE ESTADUAL PAULISTA "JÚLIO DE MESQUITA FILHO UNESP ESTUDO DA FARMACOLOGIA Introdução - Parte II A Terapêutica é um torrencial de Drogas das quais não se sabe nada em um paciente de que
NESP UNIVERSIDADE ESTADUAL PAULISTA "JÚLIO DE MESQUITA FILHO UNESP ESTUDO DA FARMACOLOGIA Introdução - Parte II A Terapêutica é um torrencial de Drogas das quais não se sabe nada em um paciente de que
UNIVERSIDADE COMUNITÁRIA DA REGIÃO DE CHAPECÓ ÁREA DE CIÊNCIAS DA SAÚDE CURSO DE FISIOTERAPIA CIÊNCIAS MORFOLÓGICAS II
 UNIVERSIDADE COMUNITÁRIA DA REGIÃO DE CHAPECÓ ÁREA DE CIÊNCIAS DA SAÚDE CURSO DE FISIOTERAPIA CIÊNCIAS MORFOLÓGICAS II Respiração Celular 1º estágio: GLICÓLISE 2º estágio: CK Ciclo de Krebs 3º estágio:
UNIVERSIDADE COMUNITÁRIA DA REGIÃO DE CHAPECÓ ÁREA DE CIÊNCIAS DA SAÚDE CURSO DE FISIOTERAPIA CIÊNCIAS MORFOLÓGICAS II Respiração Celular 1º estágio: GLICÓLISE 2º estágio: CK Ciclo de Krebs 3º estágio:
LIGAÇÕES INTERATÔMICAS
 UNIDADE 2 - LIGAÇÕES INTERATÔMICAS 2.1. FORÇAS DE LIGAÇÃO FORTES Importante conhecer-se as atrações que mantêm os átomos unidos formando os materiais sólidos. Por exemplo, uma peça de cobre contém 8,4x10
UNIDADE 2 - LIGAÇÕES INTERATÔMICAS 2.1. FORÇAS DE LIGAÇÃO FORTES Importante conhecer-se as atrações que mantêm os átomos unidos formando os materiais sólidos. Por exemplo, uma peça de cobre contém 8,4x10
AULA 1 Organização Celular Tipos de Célula. CÉLULAS ANIMAL E VEGETAL Pág. 71
 AULA 1 Organização Celular Tipos de Célula CÉLULAS ANIMAL E VEGETAL Pág. 71 CÉLULAS As células são os menores e mais simples componentes do corpo humano. A maioria das células são tão pequenas, que é necessário
AULA 1 Organização Celular Tipos de Célula CÉLULAS ANIMAL E VEGETAL Pág. 71 CÉLULAS As células são os menores e mais simples componentes do corpo humano. A maioria das células são tão pequenas, que é necessário
PROVA DE BIOLOGIA 2 o BIMESTRE 2012
 PROVA DE BIOLOGIA 2 o BIMESTRE 2012 PROFª. VERA NOME N o 1 a SÉRIE A compreensão do enunciado faz parte da questão. Não faça perguntas ao examinador. A prova deve ser feita com caneta azul ou preta. É
PROVA DE BIOLOGIA 2 o BIMESTRE 2012 PROFª. VERA NOME N o 1 a SÉRIE A compreensão do enunciado faz parte da questão. Não faça perguntas ao examinador. A prova deve ser feita com caneta azul ou preta. É
Ciclo do Ácido Cítrico
 Ciclo do Ácido Cítrico e denominado Ciclo de Krebs ou ciclo do Ácido Ciclo do Ácido Cítrico O ciclo do ácido cítrico, também denominado Ciclo de Krebs ou ciclo do Ácido Tricarboxílico (TCA) realiza a oxidação
Ciclo do Ácido Cítrico e denominado Ciclo de Krebs ou ciclo do Ácido Ciclo do Ácido Cítrico O ciclo do ácido cítrico, também denominado Ciclo de Krebs ou ciclo do Ácido Tricarboxílico (TCA) realiza a oxidação
O CICLO DO ERITRÓCITO
 O CICLO DO ERITRÓCITO Rassan Dyego Romão Silva Faculdade Alfredo Nasser Aparecida de Goiânia GO Brasil rassandyego@hotmail.com Orientador: Amarildo Lemos Dias de Moura RESUMO: Os eritrócitos são discos
O CICLO DO ERITRÓCITO Rassan Dyego Romão Silva Faculdade Alfredo Nasser Aparecida de Goiânia GO Brasil rassandyego@hotmail.com Orientador: Amarildo Lemos Dias de Moura RESUMO: Os eritrócitos são discos
www.aliancaprevestibular.com
 Professor Juliana Villa-Verde Disciplina Bio I Lista nº Assuntos Texto I Intodução à Citologia CITOLOGIA É o ramo da biologia que estuda a célula, unidade básica dos seres vivos. Hans e Zacarias Jensen
Professor Juliana Villa-Verde Disciplina Bio I Lista nº Assuntos Texto I Intodução à Citologia CITOLOGIA É o ramo da biologia que estuda a célula, unidade básica dos seres vivos. Hans e Zacarias Jensen
Yerba mate extrato EXTRATO DE MATE PADRONIZADO CAFEÍNA POLIFENÓIS TEOBROMINA
 Yerba mate extrato EXTRATO DE MATE PADRONIZADO CAFEÍNA POLIFENÓIS TEOBROMINA Ilex paraguariensis extract Coadjuvante tratamento obesidade, redução colesterol, antioxidante, estimulante Se tratando de fitoterápico:
Yerba mate extrato EXTRATO DE MATE PADRONIZADO CAFEÍNA POLIFENÓIS TEOBROMINA Ilex paraguariensis extract Coadjuvante tratamento obesidade, redução colesterol, antioxidante, estimulante Se tratando de fitoterápico:
Fisiologia e Crescimento Bacteriano
 UNIVERSIDADE FEDERAL DE JUIZ DE FORA DEPARTAMENTO DE PARASITOLOGIA, MICROBIOLOGIA E IMUNOLOGIA Fisiologia e Crescimento Bacteriano Disciplina: Biologia de Microrganismos Professora: Alessandra Machado
UNIVERSIDADE FEDERAL DE JUIZ DE FORA DEPARTAMENTO DE PARASITOLOGIA, MICROBIOLOGIA E IMUNOLOGIA Fisiologia e Crescimento Bacteriano Disciplina: Biologia de Microrganismos Professora: Alessandra Machado
Principais propriedades físicas da água.
 BIOQUÍMICA CELULAR Principais propriedades físicas da água. Muitas substâncias se dissolvem na água e ela é comumente chamada "solvente universal". Por isso, a água na natureza e em uso raramente é pura,
BIOQUÍMICA CELULAR Principais propriedades físicas da água. Muitas substâncias se dissolvem na água e ela é comumente chamada "solvente universal". Por isso, a água na natureza e em uso raramente é pura,
SECRETARIA DE SEGURANÇA PÚBLICA/SECRETARIA DE EDUCAÇÃO POLÍCIA MILITAR DO ESTADO DE GOIÁS COMANDO DE ENSINO POLICIAL MILITAR
 SECRETARIA DE SEGURANÇA PÚBLICA/SECRETARIA DE EDUCAÇÃO POLÍCIA MILITAR DO ESTADO DE GOIÁS COMANDO DE ENSINO POLICIAL MILITAR COLÉGIO DA POLÍCIA MILITAR SARGENTO NADER ALVES DOS SANTOS SÉRIE/ANO: 1ª TURMA(S):
SECRETARIA DE SEGURANÇA PÚBLICA/SECRETARIA DE EDUCAÇÃO POLÍCIA MILITAR DO ESTADO DE GOIÁS COMANDO DE ENSINO POLICIAL MILITAR COLÉGIO DA POLÍCIA MILITAR SARGENTO NADER ALVES DOS SANTOS SÉRIE/ANO: 1ª TURMA(S):
Água e Solução Tampão
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
Biologia 1. 01 Alternativa E. 02 Alternativa D. 01 Alternativa D. 02 Alternativa E. 03 Alternativa E. 04 Alternativa A.
 Biologia 1 Aula 1 21 Aula 2 Aula 3 1 Aula 4 a) A "Chlamydia trachomatis" é uma bactéria, pois, como mostra a tabela, não apresenta núcleo celular organizado, porém possui DNA, RNA, membrana plasmática
Biologia 1 Aula 1 21 Aula 2 Aula 3 1 Aula 4 a) A "Chlamydia trachomatis" é uma bactéria, pois, como mostra a tabela, não apresenta núcleo celular organizado, porém possui DNA, RNA, membrana plasmática
Nutrientes. E suas funções no organismo humano
 Nutrientes E suas funções no organismo humano O corpo humano necessita de uma série de substâncias básicas indispensáveis para a formação de tecidos, para obtenção de energia, para a realização de atividades
Nutrientes E suas funções no organismo humano O corpo humano necessita de uma série de substâncias básicas indispensáveis para a formação de tecidos, para obtenção de energia, para a realização de atividades
Associação Catarinense das Fundações Educacionais ACAFE PARECER RECURSO DISCIPLINA QUÍMICA
 33) Assinale a alternativa correta, na qual todas as substâncias são compostas e líquidas à temperatura ambiente. A O 3, O 2 ; CH 3 CH 2 OH B H 2 ; CO 2 ; CH 3 OH C H 2 O; NH 3 ; CO D H 2 O; CH 3 CH 2
33) Assinale a alternativa correta, na qual todas as substâncias são compostas e líquidas à temperatura ambiente. A O 3, O 2 ; CH 3 CH 2 OH B H 2 ; CO 2 ; CH 3 OH C H 2 O; NH 3 ; CO D H 2 O; CH 3 CH 2
www.elesapiens.com GLOSSÁRIO DE QUÍMICA ADUBO: É qualquer substância orgânica ou inorgânica que melhora a qualidade da terra.
 GLOSSÁRIO DE QUÍMICA ADUBO: É qualquer substância orgânica ou inorgânica que melhora a qualidade da terra. ALQUIMIA: A alquimia foi uma antiga prática que buscava encontrar o que chamavam de Pedra Filosofal,
GLOSSÁRIO DE QUÍMICA ADUBO: É qualquer substância orgânica ou inorgânica que melhora a qualidade da terra. ALQUIMIA: A alquimia foi uma antiga prática que buscava encontrar o que chamavam de Pedra Filosofal,
Metabolismo de Carboidratos. Profa.Dra. Leticia Labriola Abril 2012
 Metabolismo de Carboidratos. Profa.Dra. Leticia Labriola Abril 2012 Oxidação Completa da Glicose C 6 H 12 O 6 + 6O 2 + 36-38ADP + 36-38 P i 6CO 2 + 6H 2 O + 36-38ATP Via glicolítica gastou: 1 glicose,
Metabolismo de Carboidratos. Profa.Dra. Leticia Labriola Abril 2012 Oxidação Completa da Glicose C 6 H 12 O 6 + 6O 2 + 36-38ADP + 36-38 P i 6CO 2 + 6H 2 O + 36-38ATP Via glicolítica gastou: 1 glicose,
Visão Geral. Tecido conjuntivo líquido. Circula pelo sistema cardiovascular. Produzido na medula óssea, volume total de 5,5 a 6 litros (homem adulto)
 Tecido Sanguíneo Visão Geral Tecido conjuntivo líquido Circula pelo sistema cardiovascular Produzido na medula óssea, volume total de 5,5 a 6 litros (homem adulto) Defesa imunológica (Leucócitos) Trocas
Tecido Sanguíneo Visão Geral Tecido conjuntivo líquido Circula pelo sistema cardiovascular Produzido na medula óssea, volume total de 5,5 a 6 litros (homem adulto) Defesa imunológica (Leucócitos) Trocas
Você não é o que come. Você é o que absorve!
 Você não é o que come. Você é o que absorve! Sabe-se que o consumo de suplementos alimentares com finalidades específicas, como incremento de massa muscular,vem crescendo constantemente no Brasil e no
Você não é o que come. Você é o que absorve! Sabe-se que o consumo de suplementos alimentares com finalidades específicas, como incremento de massa muscular,vem crescendo constantemente no Brasil e no
Energia para a célula Fermentação Desnitrificação. Natália A. Paludetto nataliaapaludetto@gmail.com
 Energia para a célula Fermentação Desnitrificação Natália A. Paludetto nataliaapaludetto@gmail.com Respiração anaeróbia Processo em que energia é gerada a partir de quebra de uma molécula, porém sem a
Energia para a célula Fermentação Desnitrificação Natália A. Paludetto nataliaapaludetto@gmail.com Respiração anaeróbia Processo em que energia é gerada a partir de quebra de uma molécula, porém sem a
PROCESSO DE FERMENTAÇÃO CONTÍNUA ENGENHO NOVO - FERCEN
 PROCESSO DE FERMENTAÇÃO CONTÍNUA ENGENHO NOVO - FERCEN A ENGENHO NOVO, sempre atenta ao desenvolvimento de novas tecnologias para produção de etanol, pesquisou e desenvolveu um processo simples e eficiente
PROCESSO DE FERMENTAÇÃO CONTÍNUA ENGENHO NOVO - FERCEN A ENGENHO NOVO, sempre atenta ao desenvolvimento de novas tecnologias para produção de etanol, pesquisou e desenvolveu um processo simples e eficiente
SEGREDOS DO MUNDO DA QUÍMICA: OS MISTERIOSOS RADICAIS LIVRES
 Universidade de Évora Departamento de Química Vânia Pais Aluna do Curso de Mestrado em Química Aplicada SEGREDOS DO MUNDO DA QUÍMICA: OS MISTERIOSOS RADICAIS LIVRES Com o passar dos anos, o aumento da
Universidade de Évora Departamento de Química Vânia Pais Aluna do Curso de Mestrado em Química Aplicada SEGREDOS DO MUNDO DA QUÍMICA: OS MISTERIOSOS RADICAIS LIVRES Com o passar dos anos, o aumento da
Aulão: 20/06/2015 Conteúdo: Metabolismo Energético Profº Davi Vergara Profº Roberto Fonseca ONDA que apenas transportam energia.
 Aulão: 20/06/2015 Conteúdo: Metabolismo Energético Profº Davi Vergara O Sol é o principal responsável pela existência de vida na Terra. A energia luminosa captada por algas e plantas é utilizada na produção
Aulão: 20/06/2015 Conteúdo: Metabolismo Energético Profº Davi Vergara O Sol é o principal responsável pela existência de vida na Terra. A energia luminosa captada por algas e plantas é utilizada na produção
Definição. -organelas envoltas por uma única membrana; - diâmetro variável de 0,2 a 1,5 µm;
 Peroxissomos Histórico 1930 Análise bioquímica da catalase. 1950 - Inicia-se o estudo bioquímico da urato oxidase. 1954 Rodhin observou ao microscópio partículas inéditas (microcorpos). 1957 Thompson e
Peroxissomos Histórico 1930 Análise bioquímica da catalase. 1950 - Inicia-se o estudo bioquímico da urato oxidase. 1954 Rodhin observou ao microscópio partículas inéditas (microcorpos). 1957 Thompson e
Coffea arábica (Coffee) seed oil and Vegetable steryl esters. Modificador mecanobiológico da celulite e gordura localizada.
 Produto INCI Definição Propriedades SLIMBUSTER L Coffea arábica (Coffee) seed oil and Vegetable steryl esters Modificador mecanobiológico da celulite e gordura localizada. - Diminui a gordura localizada
Produto INCI Definição Propriedades SLIMBUSTER L Coffea arábica (Coffee) seed oil and Vegetable steryl esters Modificador mecanobiológico da celulite e gordura localizada. - Diminui a gordura localizada
Sistema Respiratório Introdução
 Introdução Nesse caso, o termo respiração é empregado incluindo as trocas gasosas através do corpo e as trocas gasosas nas células dos diferentes tecidos. As trocas gasosas são realizadas através da superfície
Introdução Nesse caso, o termo respiração é empregado incluindo as trocas gasosas através do corpo e as trocas gasosas nas células dos diferentes tecidos. As trocas gasosas são realizadas através da superfície
A natureza química do material genético Miescher nucleínas. ácidos nucleicos. ácido desoxirribonucleico ácido ribonucleico Avery MacLeod McCarty
 UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL COLÉGIO DE APLICAÇÃO Departamento de Ciências Exatas e da Natureza Disciplina: Biologia Professora: Lauren Valentim A natureza química do material genético A natureza
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL COLÉGIO DE APLICAÇÃO Departamento de Ciências Exatas e da Natureza Disciplina: Biologia Professora: Lauren Valentim A natureza química do material genético A natureza
AS QUESTÕES OBRIGATORIAMENTE DEVEM SER ENTREGUES EM UMA FOLHA À PARTE COM ESTA EM ANEXO.
 ENSINO MÉDIO Conteúdos da 1ª Série 1º/2º Bimestre 2015 Trabalho de Dependência Nome: N. o : Turma: Professor(a): Roberta/Marco Data: / /2015 Unidade: Cascadura Mananciais Méier Taquara Biologia Resultado
ENSINO MÉDIO Conteúdos da 1ª Série 1º/2º Bimestre 2015 Trabalho de Dependência Nome: N. o : Turma: Professor(a): Roberta/Marco Data: / /2015 Unidade: Cascadura Mananciais Méier Taquara Biologia Resultado
Aula 28.10.09: Síntese e degradação do glicogênio
 Aula 28.10.09: Síntese e degradação do glicogênio Glicogênio síntese e degradação As enzimas que catalisam a síntese e a degradação do glicogênio, além de proteínas reguladoras destes processos, estão
Aula 28.10.09: Síntese e degradação do glicogênio Glicogênio síntese e degradação As enzimas que catalisam a síntese e a degradação do glicogênio, além de proteínas reguladoras destes processos, estão
REDUÇÃO E OXIDAÇÃO EM SISTEMAS INORGÂNICOS
 REDUÇÃO E OXIDAÇÃO EM SISTEMAS INORGÂNICOS EXTRAÇÃO DE ELEMENTOS A definição original de oxidação foi a da reação que um elemento reage com oxigênio e é convertido em seu óxido. Comparativamente, redução
REDUÇÃO E OXIDAÇÃO EM SISTEMAS INORGÂNICOS EXTRAÇÃO DE ELEMENTOS A definição original de oxidação foi a da reação que um elemento reage com oxigênio e é convertido em seu óxido. Comparativamente, redução
VÍRUS (complementar o estudo com as páginas 211-213 do livro texto)
 COLÉGIO E CURSO INTELECTUS APOSTILA NOME: MAT.: Biologia I PROFº: EDUARDO SÉRIE: TURMA: DATA: VÍRUS (complementar o estudo com as páginas 211-213 do livro texto) Os vírus são os únicos organismos acelulares,
COLÉGIO E CURSO INTELECTUS APOSTILA NOME: MAT.: Biologia I PROFº: EDUARDO SÉRIE: TURMA: DATA: VÍRUS (complementar o estudo com as páginas 211-213 do livro texto) Os vírus são os únicos organismos acelulares,
QUÍMICA. 32. A neutralização equimolar do HClO com NaOH gera hipoclorito de sódio e água. Questão 21
 Questão 21 QUÍMICA A irradiação é uma técnica utilizada na conservação de alimentos para inibir a germinação, retardar o amadurecimento e destruir bactérias patogênicas. Os isótopos césio 137 e cobalto
Questão 21 QUÍMICA A irradiação é uma técnica utilizada na conservação de alimentos para inibir a germinação, retardar o amadurecimento e destruir bactérias patogênicas. Os isótopos césio 137 e cobalto
Biologia Professor Vianna 1ª série / 1º trimestre
 Biologia Professor Vianna 1ª série / 1º trimestre Módulo 3 ÁCIDOS NUCLEICOS E CITOLOGIA 1 Os itens abaixo referem-se à estrutura, composição e função dos ácidos nucleicos. Estrutura: I) Dupla hélice; II)
Biologia Professor Vianna 1ª série / 1º trimestre Módulo 3 ÁCIDOS NUCLEICOS E CITOLOGIA 1 Os itens abaixo referem-se à estrutura, composição e função dos ácidos nucleicos. Estrutura: I) Dupla hélice; II)
CPV o cursinho que mais aprova na fgv Fgv - 05/12/2004
 37 QUÍMICA 31. s irradiadores de alimentos representam hoje uma opção interessante na sua preservação. alimento irradiado, ao contrário do que se imagina, não se torna radioativo, uma vez que a radiação
37 QUÍMICA 31. s irradiadores de alimentos representam hoje uma opção interessante na sua preservação. alimento irradiado, ao contrário do que se imagina, não se torna radioativo, uma vez que a radiação
Educador: Mariana Borges Batista Componente Curricular: Biologia Data: / /2012 Estudante: 1ª Série
 Educador: Mariana Borges Batista Componente Curricular: Biologia Data: / /2012 Estudante: 1ª Série Questão 1 (UFMA) Das estruturas abaixo relacionadas, qual a alternativa que não está presente na célula
Educador: Mariana Borges Batista Componente Curricular: Biologia Data: / /2012 Estudante: 1ª Série Questão 1 (UFMA) Das estruturas abaixo relacionadas, qual a alternativa que não está presente na célula
Disciplina: Fisiologia Vegetal
 Universidade Federal Rural da Amazônia Instituto de Ciências Agrárias (ICA) Disciplina: Fisiologia Vegetal FISIOLOGIA DA SEMENTE Professor: Dr. Roberto Cezar Lobo da Costa Belém Pará 2012 GERMINAÇÃO Fonte:
Universidade Federal Rural da Amazônia Instituto de Ciências Agrárias (ICA) Disciplina: Fisiologia Vegetal FISIOLOGIA DA SEMENTE Professor: Dr. Roberto Cezar Lobo da Costa Belém Pará 2012 GERMINAÇÃO Fonte:
Dia Mundial do ovo 11 de outubro
 Importância do ovo na alimentação humana 7 de outubro de 2013 ULBRA Veterinária Zootecnia - Agronegócio Dia Mundial do ovo 11 de outubro Ovos aumentam o colesterol? Colesterol é ruim? Não é bem assim...
Importância do ovo na alimentação humana 7 de outubro de 2013 ULBRA Veterinária Zootecnia - Agronegócio Dia Mundial do ovo 11 de outubro Ovos aumentam o colesterol? Colesterol é ruim? Não é bem assim...
AVALIAÇÃO DIAGNÓSTICA
 Caderno N0901 AVALIAÇÃO DIAGNÓSTICA 2 BIMESTRE Ciências 9 ano do Ensino Fundamental Nome do Aluno(a): Orientações Você está recebendo um caderno com 27 questões. Você dispõe de 2 horas para responder a
Caderno N0901 AVALIAÇÃO DIAGNÓSTICA 2 BIMESTRE Ciências 9 ano do Ensino Fundamental Nome do Aluno(a): Orientações Você está recebendo um caderno com 27 questões. Você dispõe de 2 horas para responder a
DIGESTÃO HUMANA. Sistema Digestório. Professor: Fernando Stuchi. Enzimas Caminho da digestão Etapas da digestão
 DIGESTÃO HUMANA 1. 2. 3. Enzimas Caminho da digestão Etapas da digestão Sistema Digestório Professor: Fernando Stuchi Dúvidas sobre Digestão Afinal o que é digestão? Conjunto de transformações físico-químicas
DIGESTÃO HUMANA 1. 2. 3. Enzimas Caminho da digestão Etapas da digestão Sistema Digestório Professor: Fernando Stuchi Dúvidas sobre Digestão Afinal o que é digestão? Conjunto de transformações físico-químicas
 Tecido conjuntivo 1º ano Pró Madá Componentes da matriz extracelular A matriz é uma massa amorfa, de aspecto gelatinoso e transparente. É constituída principalmente por água e glicoproteínas e uma parte
Tecido conjuntivo 1º ano Pró Madá Componentes da matriz extracelular A matriz é uma massa amorfa, de aspecto gelatinoso e transparente. É constituída principalmente por água e glicoproteínas e uma parte
Biologia Fascículo 04 Lara Regina Parra de Lazzari
 Biologia Fascículo 04 Lara Regina Parra de Lazzari Índice Fotossíntese e Respiração... 1 Fotossíntese... 1 Respiração... 4 Exercícios... 5 Gabarito... 8 Fotossíntese e Respiração Fotossíntese Definição
Biologia Fascículo 04 Lara Regina Parra de Lazzari Índice Fotossíntese e Respiração... 1 Fotossíntese... 1 Respiração... 4 Exercícios... 5 Gabarito... 8 Fotossíntese e Respiração Fotossíntese Definição
CONTROLE DE POLUIÇÃO DE ÁGUAS
 CONTROLE DE POLUIÇÃO DE ÁGUAS NOÇÕES DE ECOLOGIA. A ÁGUA NO MEIO A ÁGUA É UM DOS FATORES MAIS IMPORTANTES PARA OS SERES VIVOS, POR ISSO É MUITO IMPORTANTE SABER DE QUE MANEIRA ELA SE ENCONTRA NO MEIO,
CONTROLE DE POLUIÇÃO DE ÁGUAS NOÇÕES DE ECOLOGIA. A ÁGUA NO MEIO A ÁGUA É UM DOS FATORES MAIS IMPORTANTES PARA OS SERES VIVOS, POR ISSO É MUITO IMPORTANTE SABER DE QUE MANEIRA ELA SE ENCONTRA NO MEIO,
COAGULAÇÃO DE PROTEÍNAS DO LEITE
 Universidade Federal do Rio de Janeiro Faculdade de Farmácia COAGULAÇÃO DE PROTEÍNAS DO LEITE Integrantes: Paula Floriano da Silva Virgínia Figueira Marques PROTEÍNAS PROTEÍNAS Ponto isoelétrico ou pi,
Universidade Federal do Rio de Janeiro Faculdade de Farmácia COAGULAÇÃO DE PROTEÍNAS DO LEITE Integrantes: Paula Floriano da Silva Virgínia Figueira Marques PROTEÍNAS PROTEÍNAS Ponto isoelétrico ou pi,
Nestas últimas aulas irei abordar acerca das vitaminas. Acompanhe!
 Aula: 31 Temática: Vitaminas parte I Nestas últimas aulas irei abordar acerca das vitaminas. Acompanhe! Introdução O termo vitamina refere-se a um fator dietético essencial requerido por um organismo em
Aula: 31 Temática: Vitaminas parte I Nestas últimas aulas irei abordar acerca das vitaminas. Acompanhe! Introdução O termo vitamina refere-se a um fator dietético essencial requerido por um organismo em
