Conclusões científicas
|
|
|
- Natan Estrela Chagas
- 6 Há anos
- Visualizações:
Transcrição
1 Anexo II Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado ou para a suspensão das Autorizações de Introdução no Mercado, conforme aplicável, tendo em conta as indicações aprovadas para cada medicamento 9
2 Conclusões científicas Resumo da avaliação científica de medicamentos contendo di-hidroergotoxina (ver Anexo I) Em 18 de janeiro de 2012, a França desencadeou um procedimento de consulta nos termos do artigo 31.º da Diretiva 2001/83/CE relativamente aos seguintes medicamentos contendo derivados da ergotamina: di-hidroergocriptina/cafeína, di-hidroergocristina, di-hidroergotamina, di-hidroergotoxina e nicergolina. Na sequência de uma revisão nacional de farmacovigilância realizada em 2011, novas notificações espontâneas relativas a alguns desses medicamentos identificaram casos graves de fibrose e ergotismo e a França considerou que esta preocupação de segurança não era compensada pelas evidências de eficácia limitadas. Por conseguinte, foi solicitado ao CHMP que desse o seu parecer sobre se as Autorizações de Introdução no Mercado para os medicamentos contendo derivados da ergotamina deviam ser mantidas, alteradas, suspensas ou retiradas em relação às seguintes indicações: Tratamento sintomático de patologias crónicas da função cognitiva ou perturbações neurossensoriais nos idosos (excluindo doença de Alzheimer e outras demências), Tratamento auxiliar da claudicação intermitente na doença oclusiva arterial periférica sintomática (DAOP estádio II), Tratamento auxiliar da doença de Raynaud, Tratamento auxiliar da acuidade visual diminuída e distúrbios no campo visual de origem presumivelmente vascular, Retinopatias agudas de origem vascular, Profilaxia da enxaqueca, Hipotensão ortostática, Tratamento sintomático da insuficiência veno-linfática. O mesilato de di-hidroergotoxina é um alcaloide da ergotamina, também conhecido como mesilato de codergocrina e mesilato de ergoloide, o qual é composto por partes iguais de mesilatos de di-hidroergocornina, di-hidroergocristina e di-hidroergocriptina. De momento, desconhece-se o mecanismo de ação principal da di-hidroergotoxina e de outros ergoloides. Funciona como um agonista dos recetores dopaminérgicos e serotoninérgicos e como um antagonista dos recetores adrenérgicos alfa. A di-hidroergotoxina modula os níveis dos neurotransmissores sinápticos e aumenta o fluxo sanguíneo para o cérebro; previamente, acreditava-se que este último mecanismo era o modo de ação principal por meio do qual a di-hidroergotoxina exerce efeitos clínicos. Entre as indicações aprovadas para os medicamentos contendo di-hidroergotoxina, as que se enquadram no âmbito deste procedimento de consulta e que estão aprovadas em pelo menos um Estado-Membro são as seguintes (a redação específica da indicação poderá variar consoante o medicamento): Tratamento sintomático de patologias crónicas da função cognitiva ou perturbações neurossensoriais nos idosos (excluindo doença de Alzheimer e outras demências), Tratamento auxiliar da doença de Raynaud, 10
3 Tratamento auxiliar da acuidade visual diminuída e distúrbios no campo visual de origem presumivelmente vascular, Profilaxia da enxaqueca, Tratamento sintomático da insuficiência veno-linfática. A demência e as indicações relacionadas com a demência, bem como o tratamento agudo das enxaquecas, não estão incluídos no âmbito deste procedimento de consulta. Os titulares das Autorizações de Introdução no Mercado (titulares das AIM) submeteram todos os dados de eficácia disponíveis que foram obtidos em ensaios clínicos e estudos observacionais, incluindo dados que foram disponibilizados após a concessão da Autorização de Introdução no Mercado inicial. Os titulares das AIM também submeterem as suas próprias descrições e resumos críticos relativos a todas as notificações espontâneas de reações fibróticas (cardíacas, com ou sem hipertensão arterial pulmonar, pulmonares, pleurais, peritoneais, retroperitoneais, etc.) e ergotismo com os seus medicamentos contendo derivados da ergotamina. Sempre que possível, foi fornecida uma revisão de todos os restantes dados disponíveis (ou seja, dados da literatura, dados pré-clínicos e outros dados clínicos, incluindo estudos epidemiológicos) que eram relevantes para avaliar o risco de fibrose. O CHMP teve em conta a totalidade dos dados disponíveis relacionados com a segurança e eficácia da di-hidroergotoxina. Eficácia clínica Relativamente à eficácia na indicação tratamento sintomático de patologias crónicas da função cognitiva ou perturbações neurossensoriais nos idosos (excluindo doença de Alzheimer e outras demências), o titular da AIM apresentou dados por subáreas das doenças da função cognitiva: perturbação vascular cerebral com arteriosclerose, insuficiência vascular cerebral e AVC; e outras causas com patologias em idosos/senis, perturbação primária ou não especificada e síndrome orgânica cerebral. O titular da AIM submeteu uma série de artigos com estudos clínicos de eficácia, 2 revisões (the medical letter, 1974, Mc Donald, 1979) e uma revisão de Cochrane (2009). A revisão de Cochrane não é relevante para a avaliação, dado que se centra na demência e em sintomas relacionados com demência. As publicações relativas a dados clínicos são antigas (de 1971 a 1995). Na sua maioria, os artigos não são relevantes (publicações não submetidas, estudos sem ocultação, sem controlo por placebo e/ou com uso do mesilato de di-hidroergotoxina por via intravenosa). Durante a revisão, o titular da AIM sugeriu restringir a indicação ao tratamento sintomático de patologias crónicas da função cognitiva nos idosos (excluindo doença de Alzheimer e outras demências). Entre os 19 estudos clínicos que são apresentados para fundamentar esta indicação restrita, e que incluíram populações heterogéneas, alguns não revelaram efeitos significativos da di-hidroergotoxina. Noutros, apenas determinados pontos da escala de avaliação da eficácia apresentaram uma melhoria significativa. Questões como a elevada taxa de abandonos, critérios de avaliação pouco claros ou subjetivos e um número reduzido de doentes também impedem que se chegue a uma conclusão relativamente à eficácia com base nestes dados. 11
4 O diagnóstico e a determinação da origem das perturbações cognitivas constituem tarefas difíceis para a medicina moderna. Com as atuais ferramentas de avaliação dos doentes, é difícil distinguir entre uma perturbação cognitiva ligeira ou moderada e uma fase precoce da doença de Alzheimer ou de outra demência. Nesses casos, a administração da di-hidroergotoxina pode atrasar a administração de um tratamento adequado para a demência. O CHMP constatou que os doentes incluídos nos estudos apresentavam sintomas diversos ou um diagnóstico putativo, que o efeito era essencialmente avaliado através de escalas subjetivas, que os sintomas observados eram extremamente heterogéneos e os resultados não eram consistentes em todos os estudos e que os dados de longo prazo não indicavam um efeito da di-hidroergotoxina em comparação com o placebo. Por conseguinte, o CHMP considerou que não era possível chegar a qualquer conclusão quanto à eficácia da di-hidroergotoxina como Tratamento sintomático adjuvante de patologias crónicas da função cognitiva ou perturbações neurossensoriais nos idosos (excluindo doença de Alzheimer e outras demências) ou noutra indicação. Além disso, em dezembro de 2012, um grupo de aconselhamento científico (SAG) reuniu-se a pedido do CHMP e, com base na sua experiência clínica, os especialistas discutiram se esta substância desempenha um papel no tratamento sintomático de patologias crónicas da função cognitiva ou perturbações neurossensoriais nos idosos (excluindo doença de Alzheimer e outras demências). O grupo realçou que a indicação reivindicada já não é utilizada na prática clínica e que, de um ponto de vista clínico, não existem atualmente evidências de que exista uma necessidade terapêutica relativamente a esta substância ativa no tratamento das perturbações cognitivas e neurossensoriais nos idosos. No que se refere à indicação tratamento auxiliar da doença de Raynaud, o CHMP constatou que a indicação reivindicada pelo titular da AIM é a doença vascular periférica e que, em alguns Estados-Membros, o tratamento auxiliar da doença de Raynaud com a di-hidroergotoxina está aprovado no âmbito desta indicação mais geral (ou seja, doença vascular periférica ). Contudo, os estudos apresentados avaliaram a di-hidroergotoxina oral em doenças venosas extremamente heterogéneas: insuficiência vascular cerebral e periférica, eczema varicoso crónico, ulcus cruris, varizes, insuficiência venosa, lesões vasculares cerebrais, tromboflebite das veias superficiais, síndromes pós-tromboflebite. Estes estudos apresentavam uma má qualidade metodológica: desenho sem controlo e em aberto e ausência de um parâmetro de avaliação final primário de eficácia bem definido. Por conseguinte, o CHMP não chegou a quaisquer conclusões científicas relativamente ao benefício da di-hidroergotoxina na doença vascular periférica com base nestes resultados de estudos e, subsequentemente, não foi possível chegar a conclusões relativamente ao tratamento auxiliar da doença de Raynaud. Relativamente à indicação tratamento auxiliar da acuidade visual diminuída e distúrbios no campo visual de origem presumivelmente vascular, foram submetidos sete estudos clínicos. Todos estes estudos antigos apresentavam falhas metodológicas. Cinco tinham um desenho sem controlo e em aberto, não incluíam um objetivo de eficácia primário bem definido, e foram realizados em doentes com patologias oculares heterogéneas. Os dois estudos comparativos descritos pelo titular da AIM 12
5 (Orma, 1958 e Vannas, 1958) apresentavam uma má qualidade metodológica; além do mais, não existem informações disponíveis sobre o desenho exato ou a aleatorização nos diferentes grupos avaliados. Além disso, ambos incluíram um número reduzido de doentes (n=48 e n=62) e ambos foram estudos de curto prazo (1-5 meses e 8 meses, respetivamente), sendo que uma duração de estudo curta é considerada inadequada para avaliar o resultado no que se refere às doenças de progressão lenta. Com base na totalidade da documentação fornecida, o CHMP concluiu que os estudos apresentam deficiências metodológicas substanciais que impedem que se chegue a qualquer conclusão relativamente à eficácia do medicamento. Quanto à indicação profilaxia da enxaqueca, duas publicações descrevem um estudo em dupla ocultação, com controlo ativo e não controlado por placebo sobre o efeito da di-hidroergocriptina (a di-hidroergotoxina é composta em um terço por di-hidroergocriptina) em comparação com o propranolol e a flunarizina. Embora o propranolol e a flunarizina sejam reconhecidos a nível da profilaxia da enxaqueca, a ausência de um grupo de placebo não permite chegar a qualquer conclusão quanto à eficácia da di-hidroergotoxina na profilaxia da enxaqueca. Além disso, em dezembro de 2012, um grupo de aconselhamento científico (SAG) reuniu-se a pedido do CHMP e, com base na sua experiência clínica, os especialistas discutiram se esta substância desempenha um papel na profilaxia da enxaqueca. Com base na experiência clínica, o grupo considerou que não existe uma população especial que possa beneficiar do tratamento com esta substância ativa para a profilaxia da enxaqueca. Por conseguinte, o grupo considerou que não existe uma população claramente definida que reaja de forma insatisfatória ao tratamento padrão de profilaxia da enxaqueca e em que exista uma necessidade terapêutica desta substância como tratamento alternativo/de último recurso. Não foram submetidos dados para fundamentar a indicação tratamento sintomático da insuficiência veno-linfática e, por conseguinte, o CHMP não chegou a qualquer conclusão relativamente à eficácia. Segurança clínica Reconhece-se que os derivados da ergotamina têm capacidade para induzir fibrose, sobretudo fibrose das válvulas cardíacas. A relação entre a fibrose e a ativação dos recetores serotoninérgicos, sobretudo dos recetores 5-HT 2B, por derivados da ergotamina está amplamente descrita na literatura. O agonismo dos recetores 5-HT 2B induz uma resposta proliferativa e a mitogenicidade das células que expressam este recetor, originando a fibrogénese. Globalmente, a variabilidade da afinidade dos diferentes derivados da ergotamina para os recetores serotoninérgicos e as doses terapêuticas utilizadas poderão explicar as diferenças observadas a nível das taxas de notificação de reações fibróticas. Por conseguinte, ainda que, em termos farmacológicos, seja altamente plausível que os derivados da ergotamina que atuam como agonistas dos recetores 5-HT 2B possam induzir valvulopatias serotoninérgicas semelhantes às induzidas por tumores carcinoides ou lesões fibróticas de outros tecidos, é necessário ter em conta que alguns derivados da ergotamina não são agonistas dos recetores 5-HT 2B. Por conseguinte, não se pode excluir outros mecanismos que induzem fibrose, o que sugere uma ligação causal entre a fibrose e o agonismo dos recetores 5-HT 2A e 5-HT 1B, bem como um efeito plausível no transportador da serotonina. 13
6 Os dados relativos aos casos de fibrose notificados (n=9) são limitados e não permitem que se chegue a conclusões concretas. Contudo, não é possível excluir a capacidade da di-hidroergotoxina para induzir reações fibróticas, localizadas na área retroperitoneal, pulmonar e cardíaca, nomeadamente devido à ausência de qualquer outra etiologia em alguns dos casos avaliados e ao mecanismo de ação dos derivados da ergotamina. Além do mais, três dos nove casos foram notificados durante o inquérito de farmacovigilância francês realizado em 2011, que revela que as medidas de minimização dos riscos atualmente em vigor não são suficientes para prevenir o risco de reações fibróticas. Além disso, a di-hidroergotoxina é composta por di-hidroergocriptina e di-hidroergocristina. Considera-se que estas duas substâncias também estarão associadas à indução de reações fibróticas. Com base nestes dados e na plausibilidade farmacológica, considera-se que a di-hidroergotoxina está associada a reações fibróticas. Além disso, deve destacar-se a gravidade de tais efeitos adversos, a possibilidade de serem fatais e o risco aumentado de desenvolvimento de uma patologia fibrótica na sequência da utilização prolongada, de acordo com as indicações autorizadas. Não foram comunicadas notificações de ergotismo. Porém, o CHMP questionou a adequação do método de recolha de dados (ou seja, não foi exaustivo e, por conseguinte, foi inconclusivo). Mais especificamente, o CHMP declarou que, além do ergotismo, outros termos preferenciais estão também relacionados com os sintomas de ergotismo (ou seja, parestesia, formigueiro, prurido, isquemia intestinal/vascular cerebral/periférica/da língua, angina de peito, coronaropatia, dor torácica, náuseas, vómitos, diarreia, dor abdominal, sensação de frio, trombose, AVC, gangrena, necrose, vasoconstrição/vasospasmo, cianose, mialgia, cãibras musculares, dor nas extremidades, vertigens, hipoestesia, entorpecimento, dor de cabeça, confusão, alucinações). Além disso, foram notificados na literatura diversos casos de sintomas de vasoconstrição periférica. O CHMP teve em conta as propostas de medidas de minimização dos riscos apresentadas pelos titulares das AIM. Estas incluíram a alteração da classificação do medicamento quanto à dispensa ao público, a limitação da duração do tratamento em determinadas condições, a contraindicação do medicamento em doentes com fibrose preexistente ou em associação com outros medicamentos, a emissão de uma comunicação direta aos médicos e profissionais de saúde (DHPC) em que é destacado o risco, uma lista de verificação para os prescritores e um estudo farmacológico in vitro sobre a afinidade dos recetores da subclasse 5-HT para o medicamento. Ainda que algumas das medidas propostas possam ajudar a identificar os doentes com fibrose preexistente, medicação concomitante relevante e risco aumentado, o Comité referiu que as mesmas são insuficientes para evitar que alguns doentes desenvolvam fibrose e ergotismo durante o tratamento. Globalmente, o CHMP considerou que, tendo em consideração os dados muito limitados sobre a eficácia, nenhuma situação pode justificar a exposição dos doentes ao risco de fibrose e ergotismo. 14
7 Relação risco-benefício O Comité concluiu que a relação risco-benefício dos medicamentos contendo di-hidroergotoxina não é favorável, nos termos do artigo 116.º da Diretiva 2001/83/CE, para o tratamento sintomático de patologias crónicas da função cognitiva ou perturbações neurossensoriais nos idosos (excluindo doença de Alzheimer e outras demências), tratamento auxiliar da doença de Raynaud, tratamento auxiliar da acuidade visual diminuída e distúrbios no campo visual de origem presumivelmente vascular, profilaxia da enxaqueca e tratamento sintomático da insuficiência veno-linfática. Procedimento de reexaminação Após a adoção do parecer do CHMP durante a reunião de junho de 2013 do Comité, foi recebido um pedido de reexaminação submetido por um dos titulares de AIM envolvidos no procedimento. O âmbito da reexaminação centrou-se na reavaliação da relação risco-benefício da di-hidroergotoxina na indicação restrita proposta pelo titular da AIM: tratamento sintomático de patologias da função cognitiva nos idosos, excluindo doença de Alzheimer e demência. O CHMP reviu todos os dados disponíveis para fundamentar o benefício e a segurança da di-hidroergotoxina e teve em conta a indicação restrita supramencionada proposta pelo titular da AIM. O CHMP sublinhou que patologias crónicas da função cognitiva, excluindo doença de Alzheimer e outras demências não é considerada uma definição geralmente aceite relativamente a uma patologia que deverá melhorar com o tratamento. O CHMP reiterou que os estudos apresentados para fundamentar a eficácia da di-hidroergotoxina foram publicados nas décadas de 70 e de 80, com o consequente risco de parcialidade da publicação, e apresentam diversas limitações. Na realidade, a heterogeneidade dos estudos submetidos é tal que não é possível chegar a conclusões concretas. O CHMP considerou que estes estudos não forneceram evidências sólidas que suportem a eficácia da di-hidroergotoxina na população alvo proposta. Por outro lado, o facto de estes estudos terem sido realizados há muitos anos resulta em preocupações metodológicas, tendo em conta os avanços que se verificaram a nível dos métodos de investigação clínica e as alterações a nível da definição de demência/estados de pré-demência desde então. Por conseguinte, permanece a incerteza quanto à possibilidade de a população avaliada nos estudos clínicos selecionados ser representativa da indicação proposta. Por esse motivo, mantêm-se as preocupações relativas à heterogeneidade da população estudada. Além disso, nos estudos que apresentam resultados positivos, são referidas melhorias a nível de diferentes parâmetros em escalas destinadas a detetar aspetos importantes de patologias da função cognitiva. As escalas utilizadas baseavam-se em grande medida na avaliação subjetiva e não tanto em testes formais. Os resultados a nível dos diferentes componentes incluídos nestas ferramentas de avaliação variam consideravelmente entre os estudos, não sendo possível chegar a quaisquer conclusões gerais relativamente à dimensão dos possíveis efeitos ou à relevância clínica. Tendo em conta o que foi acima referido, o CHMP considerou que os estudos submetidos não demonstraram que a di-hidroergotoxina tem um efeito clinicamente relevante nos doentes com patologias da função cognitiva. 15
8 O CHMP constatou que a incidência de acontecimentos adversos (ou seja, fibrose retroperitoneal, fibrose pulmonar, valvulopatias cardíacas, ergotismo) notificados pelo titular da AIM relativamente à di-hidroergotoxina é reduzida. Contudo, o CHMP constatou também que o titular da AIM apenas forneceu informações relativas ao seu medicamento (Hydergine) e que é provável a ocorrência de subnotificação. O CHMP considerou que, ainda que o risco de reações fibróticas e ergotismo associado à di-hidroergotoxina seja raro, esse risco está estabelecido e estes acontecimentos adversos são graves, com um possível resultado fatal. O CHMP teve em conta as medidas de minimização dos riscos propostas pelo titular da AIM. Globalmente, o CHMP reiterou que considera que as medidas de minimização dos riscos propostas pelo titular da AIM não reduzem de forma eficaz o risco de reações fibróticas e ergotismo. As reações fibróticas estão associadas ao uso crónico de derivados da ergotamina e, embora a taxa de notificação relativa à di-hidroergotoxina seja reduzida, o risco é suficientemente grave e não pode ser ignorado, sobretudo tendo em conta que poderá ser utilizada em tratamentos de longa duração numa vasta população de doentes. Além disso, o CHMP convocou outra reunião do grupo de aconselhamento científico (SAG), que teve lugar em 16 de outubro de O SAG concordou por unanimidade que não existe uma entidade clínica distinta no que se refere à patologia da função cognitiva sem demência (CIND), que os critérios de diagnóstico e as definições mudaram ao longo do tempo e que esta expressão não corresponde a um grupo clinicamente definido atual. O SAG considerou ainda que as evidências apresentadas pelo titular da AIM são de má qualidade. Segundo o SAG, não é de excluir a priori que o medicamento possa ser eficaz num subgrupo de doentes bem definido de acordo com os critérios atuais, mas o mesmo não pode ser determinado com base nas informações fornecidas, que incluem parâmetros de resultados de estudos e uma população de doentes altamente heterogéneos. De um modo geral, um fármaco investigado nas fases prodrómicas da demência teria de resultar numa melhoria da função cognitiva e num atraso da progressão para a demência. Globalmente, o SAG não concordou com a indicação nem com as definições da população alvo propostas pelo titular da AIM. Tendo em conta o que foi acima referido, o Comité considerou que existe um risco de reações fibróticas e ergotismo raros mas graves associado ao tratamento com a di-hidroergotoxina. O Comité considera que as evidências relativas à eficácia clinicamente significativa da di-hidroergotoxina na indicação proposta tratamento sintomático de patologias da função cognitiva nos idosos, excluindo doença de Alzheimer e demência são extremamente limitadas. Assim, o benefício demonstrado para os doentes na indicação proposta não é superior ao risco acima identificado. O Comité considerou que as medidas de minimização dos riscos propostas não reduzem de forma eficaz o risco relativo às duas reações referidas (fibrose e ergotismo) na indicação ampla proposta pelo titular da AIM. Por conseguinte, o Comité concluiu que a relação risco-benefício dos medicamentos contendo di-hidroergotoxina no tratamento sintomático de patologias da função cognitiva nos idosos, excluindo doença de Alzheimer e demência não é favorável. 16
9 Fundamentos para a suspensão/alteração dos termos das Autorizações de Introdução no Mercado Considerando que: O Comité teve em conta o procedimento realizado nos termos do artigo 31.º da Diretiva 2001/83/CE, relativamente aos medicamentos contendo derivados da ergotamina nas indicações em questão, O Comité teve em conta todos os dados e fundamentos apresentados pelos titulares das AIM e as conclusões dos grupos de aconselhamento científico, O Comité considerou que não se pode excluir uma potencial ligação causal entre as reações fibróticas ou o ergotismo e a di-hidroergotoxina. Os dados disponíveis são, de facto, indicativos dessa relação causal. Foi sublinhada a gravidade desses efeitos adversos e as suas possíveis consequências fatais, O Comité considera que as evidências relativas à eficácia clinicamente significativa da di-hidroergotoxina nas indicações atualmente avaliadas, bem como na indicação proposta pelo titular da AIM no âmbito do procedimento de reexaminação são muito limitadas e, por conseguinte, o potencial benefício para os doentes nestas indicações é superado pelo risco acima identificado, O Comité manteve o seu parecer de que a relação risco-benefício dos medicamentos contendo di-hidroergotoxina: não é favorável no tratamento sintomático de patologias crónicas da função cognitiva ou perturbações neurossensoriais nos idosos (excluindo doença de Alzheimer e outras demências) e na indicação posteriormente proposta de tratamento sintomático de patologias da função cognitiva nos idosos, excluindo doença de Alzheimer e demência, não é favorável no tratamento auxiliar da doença de Raynaud, não é favorável no tratamento auxiliar da acuidade visual diminuída e distúrbios no campo visual de origem presumivelmente vascular, não é favorável na profilaxia da enxaqueca, não é favorável no tratamento sintomático da insuficiência veno-linfática. Por conseguinte, o CHMP manteve o seu parecer de 27 de junho de 2013 e, de acordo com o artigo 116.º da Diretiva 2001/83/CE, recomenda: A alteração dos termos da Autorização de Introdução no Mercado para os medicamentos contendo di-hidroergotoxina referidos no Anexo I, a eliminação, na Informação do Medicamento, das indicações abaixo referidas (a redação específica da indicação poderá variar consoante o medicamento e consoante o país), bem como de qualquer referência relevante a essas indicações, quando existirem outras indicações terapêuticas aprovadas no âmbito da respetiva Autorização de Introdução no Mercado: 17
10 tratamento sintomático de patologias crónicas da função cognitiva ou perturbações neurossensoriais nos idosos (excluindo doença de Alzheimer e outras demências), tratamento auxiliar da doença de Raynaud, tratamento auxiliar da acuidade visual diminuída e distúrbios no campo visual de origem presumivelmente vascular, profilaxia da enxaqueca, tratamento sintomático da insuficiência veno-linfática, A suspensão da Autorização de Introdução no Mercado para os medicamentos contendo di-hidroergotoxina referidos no Anexo I, caso não existam outras indicações aprovadas no âmbito da respetiva Autorização de Introdução no Mercado. Para que a suspensão possa ser levantada, os titulares das AIM têm de identificar uma população específica de doentes na qual os benefícios do medicamento são superiores aos riscos. 18
Nome de fantasia Dosagem Forma farmacêutica. VASOBRAL, comprimido sulcado. VASOBRAL, A solução oral num frasco. 0.
 Anexo I Lista do(s) nome(s), forma(s) farmacêutica(s), dosagem(ns), via(s) de administração do(s) medicamento(s) do(s) titular(es) da(s) Autorização(ões) de Introdução no mercado nos Estados-Membros 1
Anexo I Lista do(s) nome(s), forma(s) farmacêutica(s), dosagem(ns), via(s) de administração do(s) medicamento(s) do(s) titular(es) da(s) Autorização(ões) de Introdução no mercado nos Estados-Membros 1
Anexo II. Conclusões científicas
 Anexo II Conclusões científicas 15 Conclusões científicas Haldol, que contém a substância ativa haloperidol, é um antipsicótico do grupo das butirofenonas. É um potente antagonista dos recetores de dopamina
Anexo II Conclusões científicas 15 Conclusões científicas Haldol, que contém a substância ativa haloperidol, é um antipsicótico do grupo das butirofenonas. É um potente antagonista dos recetores de dopamina
Conclusões científicas
 Anexo II Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado ou para a suspensão das Autorizações de Introdução no Mercado, conforme aplicável, tomando
Anexo II Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado ou para a suspensão das Autorizações de Introdução no Mercado, conforme aplicável, tomando
Ergomed - Tropfen (1:1:1) ERSILAN 1mg/ml solução oral em gotas oral mg/19.20 mg. ISKEDYL, comprimé 0.60 mg / 4.80 mg
 Anexo I Lista de nomes, forma(s) farmacêutica(s), dosagem(ns), via(s) de administração do(s) medicamento(s), do(s) titular(es) da(s) autorização(ões) de introdução no mercado nos estados-membros 1 Estado
Anexo I Lista de nomes, forma(s) farmacêutica(s), dosagem(ns), via(s) de administração do(s) medicamento(s), do(s) titular(es) da(s) autorização(ões) de introdução no mercado nos estados-membros 1 Estado
Mifepriston Linepharma. Mifepristone Linepharma. Mifepristone Linepharma 200 mg comprimé. Mifepristone Linepharma 200 mg Tafla
 Anexo I Lista dos nomes (de fantasia), forma farmacêutica, dosagem dos medicamentos, modo de administração, requerentes/titulares da autorização de introdução no mercado nos Estados-Membros 1 Estado-Membro
Anexo I Lista dos nomes (de fantasia), forma farmacêutica, dosagem dos medicamentos, modo de administração, requerentes/titulares da autorização de introdução no mercado nos Estados-Membros 1 Estado-Membro
Lipophoral Tablets 150mg. Mediator 150 mg Comprimido Via oral. Benfluorex Mylan 150 mg Comprimido Via oral. Benfluorex Qualimed
 ANEXO I LISTA DOS NOMES DE FANTASIA, FORMAS FARMACÊUTICAS, DOSAGENS DOS MEDICAMENTOS, VIA DE ADMINISTRAÇÃO E TITULARES DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO NOS ESTADOS-MEMBROS (EEE) 1 Estado-Membro
ANEXO I LISTA DOS NOMES DE FANTASIA, FORMAS FARMACÊUTICAS, DOSAGENS DOS MEDICAMENTOS, VIA DE ADMINISTRAÇÃO E TITULARES DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO NOS ESTADOS-MEMBROS (EEE) 1 Estado-Membro
Anexo II. Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado
 Anexo II Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado 13 Conclusões científicas e fundamentos para a alteração dos termos das Autorizações
Anexo II Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado 13 Conclusões científicas e fundamentos para a alteração dos termos das Autorizações
Anexo II. Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado
 Anexo II Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado 7 Conclusões científicas Resumo da avaliação científica do Kantos Master e nomes associados
Anexo II Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado 7 Conclusões científicas Resumo da avaliação científica do Kantos Master e nomes associados
Anexo I. Conclusões científicas e fundamentos da alteração dos termos da(s) autorização(ões) de introdução no mercado
 Anexo I Conclusões científicas e fundamentos da alteração dos termos da(s) autorização(ões) de introdução no mercado 1 Conclusões científicas Tendo em conta o relatório de avaliação do PRAC sobre os relatórios
Anexo I Conclusões científicas e fundamentos da alteração dos termos da(s) autorização(ões) de introdução no mercado 1 Conclusões científicas Tendo em conta o relatório de avaliação do PRAC sobre os relatórios
PROCEDIMENTO DE VERIFICAÇÃO DA INSTRUÇÃO DE UM PEDIDO DE RENOVAÇÃO DA AIM SUBMETIDO POR PROCEDIMENTO NACIONAL MÓDULO 1 INFORMAÇÕES ADMINISTRATIVAS
 PROCEDIMENTO DE VERIFICAÇÃO DA INSTRUÇÃO DE UM PEDIDO DE RENOVAÇÃO DA AIM SUBMETIDO POR PROCEDIMENTO NACIONAL Nome do medicamento Nº de processo Data de Entrada Substância ativa Forma farmacêutica Dosagem
PROCEDIMENTO DE VERIFICAÇÃO DA INSTRUÇÃO DE UM PEDIDO DE RENOVAÇÃO DA AIM SUBMETIDO POR PROCEDIMENTO NACIONAL Nome do medicamento Nº de processo Data de Entrada Substância ativa Forma farmacêutica Dosagem
Anexo II. Conclusões científicas e fundamentos para a recusa apresentados pela Agência Europeia de Medicamentos
 Anexo II Conclusões científicas e fundamentos para a recusa apresentados pela Agência Europeia de Medicamentos 4 Conclusões científicas Resumo da avaliação científica do Furosemide Vitabalans e nomes associados
Anexo II Conclusões científicas e fundamentos para a recusa apresentados pela Agência Europeia de Medicamentos 4 Conclusões científicas Resumo da avaliação científica do Furosemide Vitabalans e nomes associados
ANEXO III ALTERAÇÕES AO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO E FOLHETO INFORMATIVO
 ANEXO III ALTERAÇÕES AO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO E FOLHETO INFORMATIVO 43 ALTERAÇÕES A SEREM INCLUÍDAS NAS SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO PARA MEDICAMENTOS
ANEXO III ALTERAÇÕES AO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO E FOLHETO INFORMATIVO 43 ALTERAÇÕES A SEREM INCLUÍDAS NAS SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO PARA MEDICAMENTOS
RESUMO DA AVALIAÇÃO CIENTÍFICA DE MEDICAMENTOS CONTENDO ÁCIDO VALPRÓICO/VALPROATO (ver Anexo I)
 ANEXO II CONCLUSÕES CIENTÍFICAS E FUNDAMENTOS PARA A ALTERAÇÃO DOS RESUMOS DAS CARACTERÍSTICAS DO MEDICAMENTO E DOS FOLHETOS INFORMATIVOS APRESENTADOS PELA AGÊNCIA EUROPEIA DE MEDICAMENTOS 108 CONCLUSÕES
ANEXO II CONCLUSÕES CIENTÍFICAS E FUNDAMENTOS PARA A ALTERAÇÃO DOS RESUMOS DAS CARACTERÍSTICAS DO MEDICAMENTO E DOS FOLHETOS INFORMATIVOS APRESENTADOS PELA AGÊNCIA EUROPEIA DE MEDICAMENTOS 108 CONCLUSÕES
Anexo III. Adenda às secções relevantes do Resumo das Características do Medicamento e Folheto Informativo
 Anexo III Adenda às secções relevantes do Resumo das Características do Medicamento e Folheto Informativo Nota: Esta adenda às secções relevantes do Resumo das Características do Medicamento e Folheto
Anexo III Adenda às secções relevantes do Resumo das Características do Medicamento e Folheto Informativo Nota: Esta adenda às secções relevantes do Resumo das Características do Medicamento e Folheto
Titular da Autorização de Introdução no Mercado Nome de fantasia Dosagem Forma farmacêutica Via de administração
 ANEXO I LISTA DAS DENOMINAÇÕES, FORMA(S) FARMACÊUTICA(S), DOSAGEM(NS), VIA(S) DE ADMINISTRAÇÃO DO(S) MEDICAMENTO(S), TITULAR(ES) DA(S) AUTORIZAÇÃO(ÕES) DE INTRODUÇÃO NO MERCADO NOS ESTADOS-MEMBROS 1 Estado-Membro
ANEXO I LISTA DAS DENOMINAÇÕES, FORMA(S) FARMACÊUTICA(S), DOSAGEM(NS), VIA(S) DE ADMINISTRAÇÃO DO(S) MEDICAMENTO(S), TITULAR(ES) DA(S) AUTORIZAÇÃO(ÕES) DE INTRODUÇÃO NO MERCADO NOS ESTADOS-MEMBROS 1 Estado-Membro
Anexo II. Conclusões científicas e fundamentos para a suspensão das Autorizações de Introdução no Mercado
 Anexo II Conclusões científicas e fundamentos para a suspensão das Autorizações de Introdução no Mercado 12 Conclusões científicas e fundamentos para a suspensão das Autorizações de Introdução no Mercado
Anexo II Conclusões científicas e fundamentos para a suspensão das Autorizações de Introdução no Mercado 12 Conclusões científicas e fundamentos para a suspensão das Autorizações de Introdução no Mercado
Resumo das conclusões científicas relativas aos fármacos que contêm buflomedil (ver Anexo I)
 Anexo II Conclusões científicas e fundamentos para a suspensão da autorização de introdução no mercado e utilização dos produtos apresentados pela EMA 14 Conclusões científicas Resumo das conclusões científicas
Anexo II Conclusões científicas e fundamentos para a suspensão da autorização de introdução no mercado e utilização dos produtos apresentados pela EMA 14 Conclusões científicas Resumo das conclusões científicas
Anexo II. Conclusões científicas
 Anexo II Conclusões científicas 199 Conclusões científicas Na sequência da avaliação de um procedimento de partilha do trabalho do RPS sobre os medicamentos contendo ambroxol iniciada em janeiro de 2012
Anexo II Conclusões científicas 199 Conclusões científicas Na sequência da avaliação de um procedimento de partilha do trabalho do RPS sobre os medicamentos contendo ambroxol iniciada em janeiro de 2012
40 mg tablet uso oral. Furosemide Vitabalans 40 mg tablet uso oral. Furosemide Vitabalans 40 mg tablet uso oral
 Anexo I Lista das denominações, forma(s) farmacêutica(s), dosagem(ns), via(s) de administração do(s) medicamento(s), do(s) requerente(s) titular(es) da(s) autorização(ões) de introdução no mercado nos
Anexo I Lista das denominações, forma(s) farmacêutica(s), dosagem(ns), via(s) de administração do(s) medicamento(s), do(s) requerente(s) titular(es) da(s) autorização(ões) de introdução no mercado nos
ANEXO I. Lista das denominações, forma farmacêutica, dosagem, via de administração dos medicamentos e dos requerentes nos Estados-membros
 ANEXO I Lista das denominações, forma farmacêutica, dosagem, via de administração dos medicamentos e dos requerentes nos Estados-membros 1 Estado- Membro UE/EEE Requerente Nome (de fantasia) Dosagem Forma
ANEXO I Lista das denominações, forma farmacêutica, dosagem, via de administração dos medicamentos e dos requerentes nos Estados-membros 1 Estado- Membro UE/EEE Requerente Nome (de fantasia) Dosagem Forma
(Inventado) Loratadine Vitabalans 10 mg tablety. Loraxin 10 mg tablet uso oral. Loratadine Vitabalans. Loratadine Vitabalans 10 mg tabletes
 Anexo I Lista de nomes, forma farmacêutica, potência do medicamento, via de administração, requerente, titular da autorização de introdução no mercado nos Estados-Membros 1 Estado- Membro da UE/AEE República
Anexo I Lista de nomes, forma farmacêutica, potência do medicamento, via de administração, requerente, titular da autorização de introdução no mercado nos Estados-Membros 1 Estado- Membro da UE/AEE República
Curso Avançado em Gestão Pré-Hospitalar e Intra-Hospitalar Precoce do Enfarte Agudo de Miocárdio com Supradesnivelamento do Segmento ST
 Curso Avançado em Gestão Pré-Hospitalar e Intra-Hospitalar Precoce do Enfarte Agudo de Miocárdio com Supradesnivelamento do Segmento ST Perante a suspeita clínica de Síndrome coronária aguda (SCA) é crucial
Curso Avançado em Gestão Pré-Hospitalar e Intra-Hospitalar Precoce do Enfarte Agudo de Miocárdio com Supradesnivelamento do Segmento ST Perante a suspeita clínica de Síndrome coronária aguda (SCA) é crucial
Posologia: A posologia habitual corresponde à ingestão de uma cápsula, três vezes por dia, no momento das principais refeições.
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Venosmil 200 mg cápsula 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Composição por cápsula: Substância ativa: Cada cápsula contém 200 mg de
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Venosmil 200 mg cápsula 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Composição por cápsula: Substância ativa: Cada cápsula contém 200 mg de
Segurança. Salbutamol
 Anexo II Conclusões científicas e fundamentos para a revogação ou alteração, conforme aplicável, dos termos das autorizações de introdução no mercado e explicação detalhada das diferenças relativamente
Anexo II Conclusões científicas e fundamentos para a revogação ou alteração, conforme aplicável, dos termos das autorizações de introdução no mercado e explicação detalhada das diferenças relativamente
FARMACOVIGILÂNCIA A QUALIDADE FQM EM SUAS MÃOS ENTENDA MANUAL COMO E POR QUE. RELATAR EventoS AdversoS
 FARMACOVIGILÂNCIA A QUALIDADE FQM EM SUAS MÃOS MANUAL ENTENDA COMO E POR QUE RELATAR EventoS AdversoS Apresentação O desastre da Talidomida no final da década de 50 foi um marco mundial na história da
FARMACOVIGILÂNCIA A QUALIDADE FQM EM SUAS MÃOS MANUAL ENTENDA COMO E POR QUE RELATAR EventoS AdversoS Apresentação O desastre da Talidomida no final da década de 50 foi um marco mundial na história da
Monitorização de justificações técnicas e direito de opção - registo de casos
 Monitorização de justificações técnicas e direito de opção - registo de casos Comissão de Farmácia e Terapêutica - ARS Norte Porto,10 novembro de 2014 Índice 1. Introdução.... 4 2. Metodologia.... 5 2.1
Monitorização de justificações técnicas e direito de opção - registo de casos Comissão de Farmácia e Terapêutica - ARS Norte Porto,10 novembro de 2014 Índice 1. Introdução.... 4 2. Metodologia.... 5 2.1
Recomendações do PRAC relativamente aos sinais para atualização da informação do medicamento
 23 April 2015 EMA/PRAC/273916/2015 Pharmacovigilance Risk Assessment Committee Recomendações do PRAC relativamente aos sinais para atualização da informação do medicamento Adotadas a 7-10 de abril de 2015
23 April 2015 EMA/PRAC/273916/2015 Pharmacovigilance Risk Assessment Committee Recomendações do PRAC relativamente aos sinais para atualização da informação do medicamento Adotadas a 7-10 de abril de 2015
Agência Europeia de Medicamentos recomenda alterações à utilização da metoclopramida
 20 de dezembro de 2013 EMA/13239/2014 Corr. 1 Agência Europeia de Medicamentos recomenda alterações à utilização da As alterações destinam-se principalmente a reduzir o risco de efeitos secundários neurológicos
20 de dezembro de 2013 EMA/13239/2014 Corr. 1 Agência Europeia de Medicamentos recomenda alterações à utilização da As alterações destinam-se principalmente a reduzir o risco de efeitos secundários neurológicos
Informação importante para os profissionais de saúde acerca dos riscos graves associados a CAPRELSA
 CAPRELSA (vandetanib) Informação importante para os profissionais de saúde acerca dos riscos graves associados a CAPRELSA Estes materiais educacionais estão focados no risco de prolongamento do intervalo
CAPRELSA (vandetanib) Informação importante para os profissionais de saúde acerca dos riscos graves associados a CAPRELSA Estes materiais educacionais estão focados no risco de prolongamento do intervalo
Anexo III Resumo das características do medicamento, rotulagem e folheto informativo
 Anexo III Resumo das características do medicamento, rotulagem e folheto informativo Nota: Estas alterações ao Resumo das Características do Medicamento e ao Folheto Informativo são válidas no momento
Anexo III Resumo das características do medicamento, rotulagem e folheto informativo Nota: Estas alterações ao Resumo das Características do Medicamento e ao Folheto Informativo são válidas no momento
Úlceras de Perna. Definição Epidemiologia Etiologia Manifestações Clínicas Diagnóstico Diferencial Tratamento 2015 ENF.
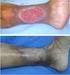 ÚLCERAS DE PERNA Úlceras de Perna Definição Epidemiologia Etiologia Manifestações Clínicas Diagnóstico Diferencial Tratamento 2015 ENF.ª MARTA MIRANDA 2 2015 ENF.ª MARTA MIRANDA 3 2015 ENF.ª MARTA MIRANDA
ÚLCERAS DE PERNA Úlceras de Perna Definição Epidemiologia Etiologia Manifestações Clínicas Diagnóstico Diferencial Tratamento 2015 ENF.ª MARTA MIRANDA 2 2015 ENF.ª MARTA MIRANDA 3 2015 ENF.ª MARTA MIRANDA
Anexo III. Alterações às secções relevantes do resumo das características do medicamento e folheto informativo
 Anexo III Alterações às secções relevantes do resumo das características do medicamento e folheto informativo Nota: Este Resumo das Características do Medicamento, rotulagem e folheto informativo é o resultado
Anexo III Alterações às secções relevantes do resumo das características do medicamento e folheto informativo Nota: Este Resumo das Características do Medicamento, rotulagem e folheto informativo é o resultado
fantasia Actocalcio D3 35 mg mg/880 IU Acrelcombi 35 mg mg/880 IU Fortipan Combi D
 ANEXO I LISTA DAS DENOMINAÇÕES, FORMA(S) FARMACÊUTICA(S), DOSAGEM(NS), VIA(S) DE ADMINISTRAÇÃO DO(S) MEDICAMENTO(S), DO(S) REQUERENTE(S) TITULAR(ES) DA(S) AUTORIZAÇÃO(ÕES) DE INTRODUÇÃO NO MERCADO NOS
ANEXO I LISTA DAS DENOMINAÇÕES, FORMA(S) FARMACÊUTICA(S), DOSAGEM(NS), VIA(S) DE ADMINISTRAÇÃO DO(S) MEDICAMENTO(S), DO(S) REQUERENTE(S) TITULAR(ES) DA(S) AUTORIZAÇÃO(ÕES) DE INTRODUÇÃO NO MERCADO NOS
Preditores de lesão renal aguda em doentes submetidos a implantação de prótese aórtica por via percutânea
 Preditores de lesão renal aguda em doentes submetidos a implantação de prótese aórtica por via percutânea Sérgio Madeira, João Brito, Maria Salomé Carvalho, Mariana Castro, António Tralhão, Francisco Costa,
Preditores de lesão renal aguda em doentes submetidos a implantação de prótese aórtica por via percutânea Sérgio Madeira, João Brito, Maria Salomé Carvalho, Mariana Castro, António Tralhão, Francisco Costa,
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO
 RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI Rotigotina N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM PVP 5943980 doseados
RELATÓRIO DE AVALIAÇÃO DO PEDIDO DE COMPARTICIPAÇÃO DE MEDICAMENTO PARA USO HUMANO DCI Rotigotina N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM PVP 5943980 doseados
CETIRIZINE DIHYDROCHLORIDE DERMAPHARM 10 mg E DESIGNACÕES ASSOCIADAS. Cetirizine dihydrochloride Dermapharm 10 mg filmomhulde tabletten
 ANEXO I LISTA DAS DENOMINAÇÕES, FORMA FARMACÊUTICA, DOSAGEM, VIA DE ADMINISTRAÇÃO DOS MEDICAMENTOS, DO REQUERENTE TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO NOS ESTADOS-MEMBROS 1 CETIRIZINE DIHYDROCHLORIDE
ANEXO I LISTA DAS DENOMINAÇÕES, FORMA FARMACÊUTICA, DOSAGEM, VIA DE ADMINISTRAÇÃO DOS MEDICAMENTOS, DO REQUERENTE TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO NOS ESTADOS-MEMBROS 1 CETIRIZINE DIHYDROCHLORIDE
SEÇÃO 1 IMPORTÂNCIA DO ACIDENTE VASCULAR CEREBRAL E DE SUA PREVENÇÃO
 SEÇÃO 1 Capítulo 1 IMPORTÂNCIA DO ACIDENTE VASCULAR CEREBRAL E DE SUA PREVENÇÃO 1 Epidemiologia da prevenção do acidente vascular cerebral e urgência do tratamento 2 Introdução / 2 Incidência e prevalência
SEÇÃO 1 Capítulo 1 IMPORTÂNCIA DO ACIDENTE VASCULAR CEREBRAL E DE SUA PREVENÇÃO 1 Epidemiologia da prevenção do acidente vascular cerebral e urgência do tratamento 2 Introdução / 2 Incidência e prevalência
Requerente Nome (de fantasia) Dosagem Forma Farmacêutica. Simvastatin Vale 20 mg/5 ml Suspension zum Einnehmen
 Anexo I Lista das denominações, forma(s) farmacêutica(s), dosagem(ns), via(s) de do(s) medicamento(s), titular(es) da(s) autorização(ões) de introdução no mercado nos estados-membros 1 Áustria 20 mg/5
Anexo I Lista das denominações, forma(s) farmacêutica(s), dosagem(ns), via(s) de do(s) medicamento(s), titular(es) da(s) autorização(ões) de introdução no mercado nos estados-membros 1 Áustria 20 mg/5
Delineamentos de estudos. FACIMED Investigação científica II 5º período Professora Gracian Li Pereira
 Delineamentos de estudos FACIMED 2012.1 Investigação científica II 5º período Professora Gracian Li Pereira Delineamentos de estudos Estudos descritivos Relato de caso Série de casos Transversal Ecológico
Delineamentos de estudos FACIMED 2012.1 Investigação científica II 5º período Professora Gracian Li Pereira Delineamentos de estudos Estudos descritivos Relato de caso Série de casos Transversal Ecológico
O Pradaxa é um medicamento que contém a substância ativa etexilato de dabigatran. Está disponível em cápsulas (75, 110 e 150 mg).
 EMA/47517/2015 EMEA/H/C/000829 Resumo do EPAR destinado ao público etexilato de dabigatran Este é um resumo do Relatório Público Europeu de Avaliação (EPAR) relativo ao. O seu objetivo é explicar o modo
EMA/47517/2015 EMEA/H/C/000829 Resumo do EPAR destinado ao público etexilato de dabigatran Este é um resumo do Relatório Público Europeu de Avaliação (EPAR) relativo ao. O seu objetivo é explicar o modo
Anexo C. (alteração a medicamentos autorizados nacionalmente)
 Anexo C (alteração a medicamentos autorizados nacionalmente) ANEXO I CONCLUSÕES CIENTÍFICAS E FUNDAMENTOS RECOMENDANDO A ALTERAÇÃO AOS TERMOS DA(S) AUTORIZAÇÃO(ÇÕES) DE INTRODUÇÃO NO MERCADO Conclusões
Anexo C (alteração a medicamentos autorizados nacionalmente) ANEXO I CONCLUSÕES CIENTÍFICAS E FUNDAMENTOS RECOMENDANDO A ALTERAÇÃO AOS TERMOS DA(S) AUTORIZAÇÃO(ÇÕES) DE INTRODUÇÃO NO MERCADO Conclusões
Forma farmacêutica. Dosagens. Clavulanic acid 10 mg. de 10 mg de amoxicilina / 2,5 mg de ácido clavulânico/kg de peso corporal República Checa
 Anexo I Lista dos nomes, forma farmacêutica, dosagem do medicamento veterinário, espécies-alvo, via de administração, requerente/titular da Autorização de Introdução no Mercado nos Estados-Membros 1/11
Anexo I Lista dos nomes, forma farmacêutica, dosagem do medicamento veterinário, espécies-alvo, via de administração, requerente/titular da Autorização de Introdução no Mercado nos Estados-Membros 1/11
Maio, Unidade de Cuidados na Comunidade de Castelo Branco. Hipertensão Arterial
 Maio, 2014 Unidade de Cuidados na Comunidade de Castelo Branco Hipertensão Arterial Sumário: O que é a Hipertensão Arterial (HTA)?; Causas da HTA; Fatores de Risco; Como prevenir a HTA; Sintomas; Problemas
Maio, 2014 Unidade de Cuidados na Comunidade de Castelo Branco Hipertensão Arterial Sumário: O que é a Hipertensão Arterial (HTA)?; Causas da HTA; Fatores de Risco; Como prevenir a HTA; Sintomas; Problemas
FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR
 FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR Veroven 20 mg/g gel Hidrosmina APROVADO EM Leia com atenção todo este folheto antes de começar a utilizar este medicamento pois contém informação importante
FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR Veroven 20 mg/g gel Hidrosmina APROVADO EM Leia com atenção todo este folheto antes de começar a utilizar este medicamento pois contém informação importante
Bromocriptina mesilato
 Material Técnico Identificação Fórmula Molecular: C 32 H 40 BrN 5 O 5.CH 4 O 3 S Peso molecular: 750.72 DCB/ DCI: 01466 - mesilato de bromocriptina / 3365 CAS: 22260-51-1 INCI: não aplicável Sinonímia:
Material Técnico Identificação Fórmula Molecular: C 32 H 40 BrN 5 O 5.CH 4 O 3 S Peso molecular: 750.72 DCB/ DCI: 01466 - mesilato de bromocriptina / 3365 CAS: 22260-51-1 INCI: não aplicável Sinonímia:
Novas abordagens terapêuticas na Doença de Parkinson
 Novas abordagens terapêuticas na Doença de Parkinson Ricardo Viana Soares Centro de Informação do Medicamento Ordem dos Farmacêuticos Lisboa, 5 de junho de 2017 Sumário 1. Fisiopatologia da DP 2. Tratamento
Novas abordagens terapêuticas na Doença de Parkinson Ricardo Viana Soares Centro de Informação do Medicamento Ordem dos Farmacêuticos Lisboa, 5 de junho de 2017 Sumário 1. Fisiopatologia da DP 2. Tratamento
8 sinais de má circulação sanguínea
 8 sinais de má circulação sanguínea Angiologista explica sinais que vão de alterações na pele até dor Se você tem pés e mãos frias e uma sensação de formigamento, pode ser que você esteja com sinais de
8 sinais de má circulação sanguínea Angiologista explica sinais que vão de alterações na pele até dor Se você tem pés e mãos frias e uma sensação de formigamento, pode ser que você esteja com sinais de
Anexo II. Conclusões científicas e fundamentos da recusa
 Anexo II Conclusões científicas e fundamentos da recusa 4 Conclusões científicas Resumo da avaliação científica do Levothyroxine Alapis e nomes associados (ver Anexo I) As indicações propostas para o Levothyroxine
Anexo II Conclusões científicas e fundamentos da recusa 4 Conclusões científicas Resumo da avaliação científica do Levothyroxine Alapis e nomes associados (ver Anexo I) As indicações propostas para o Levothyroxine
Agência Nacional de Vigilância Sanitária Anvisa Gerência-Geral de Tecnologia de Produtos para a Saúde - GGTPS
 Agência Nacional de Vigilância Sanitária Anvisa Gerência-Geral de Tecnologia de Produtos para a Saúde - GGTPS NOTA TÉCNICA N 004/2016/GGTPS/DIREG/ANVISA Objeto: Requisitos para determinar a necessidade
Agência Nacional de Vigilância Sanitária Anvisa Gerência-Geral de Tecnologia de Produtos para a Saúde - GGTPS NOTA TÉCNICA N 004/2016/GGTPS/DIREG/ANVISA Objeto: Requisitos para determinar a necessidade
DEMÊNCIA? O QUE é 45 MILHOES 70% O QUE É DEMÊNCIA? A DEMÊNCIA NAO É UMA DOENÇA EM 2013, DEMÊNCIA. Memória; Raciocínio; Planejamento; Aprendizagem;
 O QUE é APRESENTA DEMÊNCIA? O QUE É DEMÊNCIA? A demência é um distúrbio em um grupo de processos mentais que incluem: Memória; Raciocínio; Planejamento; Aprendizagem; Atenção; Linguagem; Percepção; Conduta.
O QUE é APRESENTA DEMÊNCIA? O QUE É DEMÊNCIA? A demência é um distúrbio em um grupo de processos mentais que incluem: Memória; Raciocínio; Planejamento; Aprendizagem; Atenção; Linguagem; Percepção; Conduta.
FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR
 FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR VASILIUM, 10 mg, Comprimidos Flunarizina Leia atentamente este folheto antes de tomar o medicamento. -Conserve este folheto. Pode ter necessidade de o
FOLHETO INFORMATIVO: INFORMAÇÃO PARA O UTILIZADOR VASILIUM, 10 mg, Comprimidos Flunarizina Leia atentamente este folheto antes de tomar o medicamento. -Conserve este folheto. Pode ter necessidade de o
Antipsicóticos 27/05/2017. Tratamento farmacológico. Redução da internação. Convivio na sociedade. Variedade de transtornos mentais
 Psicofarmacologia Antipsicóticos Psicose Variedade de transtornos mentais Delírios (crenças falsas) Prof. Herval de Lacerda Bonfante Departamento de Farmacologia Vários tipos de alucinações Esquizofrenia:
Psicofarmacologia Antipsicóticos Psicose Variedade de transtornos mentais Delírios (crenças falsas) Prof. Herval de Lacerda Bonfante Departamento de Farmacologia Vários tipos de alucinações Esquizofrenia:
ANEXO I. Perguntas e Respostas sobre a revisão benefício-risco do piroxicam
 ANEXO I Perguntas e Respostas sobre a revisão benefício-risco do piroxicam A Agência Europeia de Medicamentos (EMEA) completou recentemente a avaliação da segurança do anti-inflamatório não esteróide (AINE)
ANEXO I Perguntas e Respostas sobre a revisão benefício-risco do piroxicam A Agência Europeia de Medicamentos (EMEA) completou recentemente a avaliação da segurança do anti-inflamatório não esteróide (AINE)
Gestão da Medicação nas Estruturas Residenciais para Pessoas Idosas (ERPI)
 RECOMENDAÇÃO DA COMISSÃO SETORIAL PARA A SAÚDE DO SISTEMA PORTUGUÊS DA QUALIDADE CS/09 (REC CS09/01/2014) Gestão da Medicação nas Estruturas Residenciais para Pessoas Idosas (ERPI) Contexto O número de
RECOMENDAÇÃO DA COMISSÃO SETORIAL PARA A SAÚDE DO SISTEMA PORTUGUÊS DA QUALIDADE CS/09 (REC CS09/01/2014) Gestão da Medicação nas Estruturas Residenciais para Pessoas Idosas (ERPI) Contexto O número de
TROMBOEMBOLISMO PULMONAR EMERGÊNCIAS AÓRTICAS. Leonardo Oliveira Moura
 TROMBOEMBOLISMO PULMONAR EMERGÊNCIAS AÓRTICAS Leonardo Oliveira Moura Dissecção da Aorta Emergência aórtica mais comum Pode ser aguda ou crônica, quando os sintomas duram mais que 2 semanas Cerca de 75%
TROMBOEMBOLISMO PULMONAR EMERGÊNCIAS AÓRTICAS Leonardo Oliveira Moura Dissecção da Aorta Emergência aórtica mais comum Pode ser aguda ou crônica, quando os sintomas duram mais que 2 semanas Cerca de 75%
Anexo I. Lista das denominações, forma farmacêutica, dosagem, via de administração dos medicamentos e dos requerentes nos Estadosmembros
 Anexo I Lista das denominações, forma farmacêutica, dosagem, via de administração dos medicamentos e dos requerentes nos Estadosmembros 1 Estadomembro UE/EEE República Checa França República Eslovaca Requerente
Anexo I Lista das denominações, forma farmacêutica, dosagem, via de administração dos medicamentos e dos requerentes nos Estadosmembros 1 Estadomembro UE/EEE República Checa França República Eslovaca Requerente
Anexo I. Conclusões científicas e fundamentos da alteração dos termos da(s) autorização(ões) de introdução no mercado
 Anexo I Conclusões científicas e fundamentos da alteração dos termos da(s) autorização(ões) de introdução no mercado 1 Conclusões científicas Tendo em conta o relatório de avaliação do PRAC sobre os relatórios
Anexo I Conclusões científicas e fundamentos da alteração dos termos da(s) autorização(ões) de introdução no mercado 1 Conclusões científicas Tendo em conta o relatório de avaliação do PRAC sobre os relatórios
Benepali (etanercept): Breve formação sobre medidas adicionais de minimização do risco
 Benepali (etanercept): Breve formação sobre medidas adicionais de minimização do risco Conjunto de diapositivos para formação de Profissionais de Saúde (PdS) Versão 2.0; Data de aprovação do Infarmed:
Benepali (etanercept): Breve formação sobre medidas adicionais de minimização do risco Conjunto de diapositivos para formação de Profissionais de Saúde (PdS) Versão 2.0; Data de aprovação do Infarmed:
Anexo III. Alterações nas secções relevantes do resumo das caraterísticas do medicamento e do folheto informativo
 Anexo III Alterações nas secções relevantes do resumo das caraterísticas do medicamento e do folheto informativo Nota: As alterações ao Resumo das Características do Medicamento e ao Folheto Informativo
Anexo III Alterações nas secções relevantes do resumo das caraterísticas do medicamento e do folheto informativo Nota: As alterações ao Resumo das Características do Medicamento e ao Folheto Informativo
RECONSTITUIÇÃO, DOSAGEM E ADMINISTRAÇÃO
 PHPT/VEL/0317/0002 Informação importante relacionada com a RECONSTITUIÇÃO, DOSAGEM E ADMINISTRAÇÃO de VELCADE (bortezomib) 3,5 mg frasco para injetáveis para utilização subcutânea (SC) e intravenosa (IV)
PHPT/VEL/0317/0002 Informação importante relacionada com a RECONSTITUIÇÃO, DOSAGEM E ADMINISTRAÇÃO de VELCADE (bortezomib) 3,5 mg frasco para injetáveis para utilização subcutânea (SC) e intravenosa (IV)
- termo utilizado para designar uma Dilatação Permanente de um. - Considerado aneurisma dilatação de mais de 50% num segmento vascular
 Doenças Vasculares Aneurisma A palavra aneurisma é de origem grega e significa Alargamento. - termo utilizado para designar uma Dilatação Permanente de um segmento vascular. - Considerado aneurisma dilatação
Doenças Vasculares Aneurisma A palavra aneurisma é de origem grega e significa Alargamento. - termo utilizado para designar uma Dilatação Permanente de um segmento vascular. - Considerado aneurisma dilatação
VERTIGIUM. (dicloridrato de flunarizina)
 VERTIGIUM (dicloridrato de flunarizina) Brainfarma Indústria Química e Farmacêutica S.A. Comprimido 10mg I - IDENTIFICAÇÃO DO MEDICAMENTO: VERTIGIUM dicloridrato de flunarizina MEDICAMENTO SIMILAR EQUIVALENTE
VERTIGIUM (dicloridrato de flunarizina) Brainfarma Indústria Química e Farmacêutica S.A. Comprimido 10mg I - IDENTIFICAÇÃO DO MEDICAMENTO: VERTIGIUM dicloridrato de flunarizina MEDICAMENTO SIMILAR EQUIVALENTE
Anexo II. Conclusões científicas
 Anexo II Conclusões científicas 4 Conclusões científicas A fusafungina é um antibacteriano depsipéptido produzido pela estirpe 437 de Fusarium lateritium. A fusafungina, utilizada na forma de pulverização,
Anexo II Conclusões científicas 4 Conclusões científicas A fusafungina é um antibacteriano depsipéptido produzido pela estirpe 437 de Fusarium lateritium. A fusafungina, utilizada na forma de pulverização,
 IMPLEMENTANDO ESTUDOS ADAPTATIVOS marcelo.vaz@marcelovaz.med.br Marcelo.vaz@iconclinical.com Uma empresa propõe uma associação de 3 princípios ativos para tratar sintomaticamente afecções das vias aéreas
IMPLEMENTANDO ESTUDOS ADAPTATIVOS marcelo.vaz@marcelovaz.med.br Marcelo.vaz@iconclinical.com Uma empresa propõe uma associação de 3 princípios ativos para tratar sintomaticamente afecções das vias aéreas
Exame Farmacoterapia Época normal 2012
 Exame Farmacoterapia Época normal 2012 1. Sindrome metabólico explicar a diabetes, fármacos na terapêutica. 2. 4 antibióticos, num individuo com infecção urinaria resistente aos beta-lactamicos qual o
Exame Farmacoterapia Época normal 2012 1. Sindrome metabólico explicar a diabetes, fármacos na terapêutica. 2. 4 antibióticos, num individuo com infecção urinaria resistente aos beta-lactamicos qual o
PARÉSIA MONOMÉLICA COMPLICAÇÃO RARA E GRAVE
 Reunião do Núcleo de Acessos Vasculares SPACV - 2014 Mª TERESA VIEIRA Cirurgia Vascular CHLN Isquémia distal complicação conhecida da cirurgia dos acessos Incidência varia de 1 a 6% Sintomas variam desde
Reunião do Núcleo de Acessos Vasculares SPACV - 2014 Mª TERESA VIEIRA Cirurgia Vascular CHLN Isquémia distal complicação conhecida da cirurgia dos acessos Incidência varia de 1 a 6% Sintomas variam desde
Desenhos de estudos científicos. Heitor Carvalho Gomes
 Desenhos de estudos científicos Heitor Carvalho Gomes 2016 01 01 01 Desenhos de estudos científicos Introdução Epidemiologia clínica (Epidemiologia + Medicina Clínica)- trata da metodologia das
Desenhos de estudos científicos Heitor Carvalho Gomes 2016 01 01 01 Desenhos de estudos científicos Introdução Epidemiologia clínica (Epidemiologia + Medicina Clínica)- trata da metodologia das
Folheto informativo: Informação para o utilizador Thrombocid 15 mg/g gel Polisulfato sódico de pentosano
 Folheto informativo: Informação para o utilizador Thrombocid 15 mg/g gel Polisulfato sódico de pentosano Leia com atenção todo este folheto antes de começar a tomar este medicamento, pois contém informação
Folheto informativo: Informação para o utilizador Thrombocid 15 mg/g gel Polisulfato sódico de pentosano Leia com atenção todo este folheto antes de começar a tomar este medicamento, pois contém informação
SOCIEDADE RELATÓRIO PARA MICOFENOLATO DE MOFETILA E MICOFENOLATO DE SÓDIO PARA TRATAMENTO DA NEFRITE LÚPICA
 n. 67 publicado em setembro/2017 RELATÓRIO PARA SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS MICOFENOLATO DE MOFETILA E MICOFENOLATO DE SÓDIO PARA
n. 67 publicado em setembro/2017 RELATÓRIO PARA SOCIEDADE informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS MICOFENOLATO DE MOFETILA E MICOFENOLATO DE SÓDIO PARA
Pressão arterial alta
 4 Pressão arterial alta As recomendações de saúde celular do Dr. Rath para a prevenção e terapia complementar Os factos sobre a pressão arterial alta: As recomendações de saúde celular do Dr. Rath Benefícios
4 Pressão arterial alta As recomendações de saúde celular do Dr. Rath para a prevenção e terapia complementar Os factos sobre a pressão arterial alta: As recomendações de saúde celular do Dr. Rath Benefícios
Anexo II. Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado
 Anexo II Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado 14 Conclusões científicas Resumo da avaliação científica do Zinacef e nomes associados
Anexo II Conclusões científicas e fundamentos para a alteração dos termos das Autorizações de Introdução no Mercado 14 Conclusões científicas Resumo da avaliação científica do Zinacef e nomes associados
GUIA DE INFORMAÇÃO DE SEGURANÇA PARA OS PROFISSIONAIS DE SAÚDE
 GUIA DE INFORMAÇÃO DE SEGURANÇA PARA OS PROFISSIONAIS DE SAÚDE FLIXABI é um medicamento biológico. Para fins de rastreabilidade, é importante registar, sempre que possível, o nome de marca e o número de
GUIA DE INFORMAÇÃO DE SEGURANÇA PARA OS PROFISSIONAIS DE SAÚDE FLIXABI é um medicamento biológico. Para fins de rastreabilidade, é importante registar, sempre que possível, o nome de marca e o número de
DOR PROTOCOLO DO TRATAMENTO CLÍNICO PARA O NEUROLOGISTA. Laura Sousa Castro Peixoto
 DOR PROTOCOLO DO TRATAMENTO CLÍNICO PARA O NEUROLOGISTA Laura Sousa Castro Peixoto DOR Dor é uma sensação ou experiência emocional desagradável, associada com dano tecidual real ou potencial. IASP Tratamento
DOR PROTOCOLO DO TRATAMENTO CLÍNICO PARA O NEUROLOGISTA Laura Sousa Castro Peixoto DOR Dor é uma sensação ou experiência emocional desagradável, associada com dano tecidual real ou potencial. IASP Tratamento
Dimensão Segurança do Doente Check-list Procedimentos de Segurança
 1. 1.1 1.2 Cultura de Segurança Existe um elemento(s) definido(s) com responsabilidade atribuída para a segurança do doente Promove o trabalho em equipa multidisciplinar na implementação de processos relativos
1. 1.1 1.2 Cultura de Segurança Existe um elemento(s) definido(s) com responsabilidade atribuída para a segurança do doente Promove o trabalho em equipa multidisciplinar na implementação de processos relativos
Antipsicóticos 02/02/2016. Tratamento farmacológico. Redução da internação. Convivio na sociedade. Variedade de transtornos mentais
 Psicofarmacologia Psicose Variedade de transtornos mentais Delírios (crenças falsas) Prof. Herval de Lacerda Bonfante Departamento de Farmacologia Vários tipos de alucinações Esquizofrenia: tipo de psicose
Psicofarmacologia Psicose Variedade de transtornos mentais Delírios (crenças falsas) Prof. Herval de Lacerda Bonfante Departamento de Farmacologia Vários tipos de alucinações Esquizofrenia: tipo de psicose
DCI Nome de fantasia Dosagem Forma farmacêutica CAUSTINERF ARSENICAL. CAUSTINERF ARSENICAL, pâte pour usage dentaire
 Anexo I Lista dos nomes, formas farmacêuticas, dosagens dos medicamentos, vias de administração, titulares das Autorizações de Introdução no Mercado nos Estados-Membros 1 Estado-Membro (no EEE) Titular
Anexo I Lista dos nomes, formas farmacêuticas, dosagens dos medicamentos, vias de administração, titulares das Autorizações de Introdução no Mercado nos Estados-Membros 1 Estado-Membro (no EEE) Titular
Centro Hospitalar de Hospital São João, EPE. João Rocha Neves Faculdade de Medicina da UP CH - Hospital São João EPE
 Centro Hospitalar de Hospital São João, EPE João Rocha Neves Faculdade de Medicina da UP CH - Hospital São João EPE Doença carotídea Doença arterial periférica Isquemia aguda Estenose da artéria renal
Centro Hospitalar de Hospital São João, EPE João Rocha Neves Faculdade de Medicina da UP CH - Hospital São João EPE Doença carotídea Doença arterial periférica Isquemia aguda Estenose da artéria renal
parte 1 estratégia básica e introdução à patologia... 27
 Sumário parte 1 estratégia básica e introdução à patologia... 27 1 Terapêutica: estratégia geral... 29 terminologia de doenças... 29 História do caso... 34 Disposição do fármaco... 39 Seleção do fármaco...
Sumário parte 1 estratégia básica e introdução à patologia... 27 1 Terapêutica: estratégia geral... 29 terminologia de doenças... 29 História do caso... 34 Disposição do fármaco... 39 Seleção do fármaco...
MANEJO DOS CASOS SUSPEITOS E CONFIRMADOS DE INFLUENZA NO HIAE E UNIDADES
 MANEJO DOS CASOS SUSPEITOS E CONFIRMADOS DE INFLUENZA NO HIAE E UNIDADES AVANÇADAS Maio de 2013 Serviço de Controle de Infecção Hospitalar Conteúdo Definições atualmente utilizadas Diagnóstico Tratamento
MANEJO DOS CASOS SUSPEITOS E CONFIRMADOS DE INFLUENZA NO HIAE E UNIDADES AVANÇADAS Maio de 2013 Serviço de Controle de Infecção Hospitalar Conteúdo Definições atualmente utilizadas Diagnóstico Tratamento
Utilidade da discussão
 Lei 146 XII Utilidade da discussão REGULAMENTO DO PARLAMENTO EUROPEU E DO CONSELHO relativo aos ensaios clínicos de medicamentos para uso humano e que revoga a Diretiva 2001/20/CE Votação Março 2014 Necessidade
Lei 146 XII Utilidade da discussão REGULAMENTO DO PARLAMENTO EUROPEU E DO CONSELHO relativo aos ensaios clínicos de medicamentos para uso humano e que revoga a Diretiva 2001/20/CE Votação Março 2014 Necessidade
Quetiapina SR Zentiva
 Quetiapina SR Zentiva Minimização e gestão de riscos importantes Material educacional para profissionais de saúde Conteúdo O que é Quetiapina SR Zentiva?... 2 Quais os riscos importantes associados a Quetiapina
Quetiapina SR Zentiva Minimização e gestão de riscos importantes Material educacional para profissionais de saúde Conteúdo O que é Quetiapina SR Zentiva?... 2 Quais os riscos importantes associados a Quetiapina
ANEXO III ALTERAÇÕES ÀS SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO E DOS FOLHETOS INFORMATIVOS
 ANEXO III ALTERAÇÕES ÀS SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO E DOS FOLHETOS INFORMATIVOS Nota: As alterações ao Resumo das Características do Medicamento e aos folhetos informativos
ANEXO III ALTERAÇÕES ÀS SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO E DOS FOLHETOS INFORMATIVOS Nota: As alterações ao Resumo das Características do Medicamento e aos folhetos informativos
Com o apoio científico da Secção Regional do Norte da ORDEM DOS MÉDICOS. Compreender a Enxaqueca. e outras Cefaleias. Anne MacGregor.
 Com o apoio científico da Secção Regional do Norte da ORDEM DOS MÉDICOS Compreender a Enxaqueca e outras Cefaleias Anne MacGregor Oo Guia de Saúde Introdução às cefaleias comuns Apercentagem da população
Com o apoio científico da Secção Regional do Norte da ORDEM DOS MÉDICOS Compreender a Enxaqueca e outras Cefaleias Anne MacGregor Oo Guia de Saúde Introdução às cefaleias comuns Apercentagem da população
EXAME MÉDICO DE CONDUTORES OU CANDIDATOS A CONDUTORES DE VEÍCULOS A MOTOR. (artigo 26.º n.º 1 do Regulamento da Habilitação Legal para Conduzir)
 REGIÃO AUTÓNOMA DA MADEIRA GOVERNO REGIONAL SECRETARIA REGIONAL DA SAÚDE INSTITUTO DE ADMINISTRAÇÃO DA SAÚDE E ASSUNTOS SOCIAIS, IP-RAM EXAME MÉDICO DE CONDUTORES OU CANDIDATOS A CONDUTORES DE VEÍCULOS
REGIÃO AUTÓNOMA DA MADEIRA GOVERNO REGIONAL SECRETARIA REGIONAL DA SAÚDE INSTITUTO DE ADMINISTRAÇÃO DA SAÚDE E ASSUNTOS SOCIAIS, IP-RAM EXAME MÉDICO DE CONDUTORES OU CANDIDATOS A CONDUTORES DE VEÍCULOS
Guia para médicos sobre a prescrição de TOCTINO
 Guia para médicos sobre a prescrição de TOCTINO Queira ler atentamente este guia antes de discutir com a sua doente a possibilidade de tratamento com TOCTINO. Aqui encontrará informação acerca da contraceção,
Guia para médicos sobre a prescrição de TOCTINO Queira ler atentamente este guia antes de discutir com a sua doente a possibilidade de tratamento com TOCTINO. Aqui encontrará informação acerca da contraceção,
RECONSTITUIÇÃO, DOSAGEM E ADMINISTRAÇÃO
 Informação importante relacionada com a RECONSTITUIÇÃO, DOSAGEM E ADMINISTRAÇÃO de VELCADE (bortezomib) 3,5 mg frasco para injetáveis para utilização subcutânea (SC) e intravenosa (IV) INFORMAÇÃO DE SEGURANÇA
Informação importante relacionada com a RECONSTITUIÇÃO, DOSAGEM E ADMINISTRAÇÃO de VELCADE (bortezomib) 3,5 mg frasco para injetáveis para utilização subcutânea (SC) e intravenosa (IV) INFORMAÇÃO DE SEGURANÇA
HYDERGINE SRO mesilato de codergocrina
 HYDERGINE SRO mesilato de codergocrina Forma farmacêutica e apresentações Cápsulas. Embalagens com 14 e 28 cápsulas SRO de liberação lenta de 6 mg. USO ADULTO Composição O princípio ativo é o mesilato
HYDERGINE SRO mesilato de codergocrina Forma farmacêutica e apresentações Cápsulas. Embalagens com 14 e 28 cápsulas SRO de liberação lenta de 6 mg. USO ADULTO Composição O princípio ativo é o mesilato
Genes e Epilepsia: Epilepsia e Alterações Genéticas
 Faculdade de Medicina de São José do Rio Preto Genes e Epilepsia: Epilepsia e Alterações Genéticas Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo Rodrigo Nunes Cal Introdução Epilepsia
Faculdade de Medicina de São José do Rio Preto Genes e Epilepsia: Epilepsia e Alterações Genéticas Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo Rodrigo Nunes Cal Introdução Epilepsia
RESIDÊNCIA MÉDICA SUPLEMENTAR 2015 PRÉ-REQUISITO (R1) / CLÍNICA MÉDICA PROVA DISCURSIVA
 RESIDÊNCIA MÉDICA SUPLEMENTAR 0 PRÉ-REQUISITO (R) / CLÍNICA MÉDICA PROVA DISCURSIVA RESIDÊNCIA MÉDICA SUPLEMENTAR 0 PRÉ-REQUISITO (R) / CLÍNICA MÉDICA PROVA DISCURSIVA ) Idosa de 8 anos, ex-tabagista (carga
RESIDÊNCIA MÉDICA SUPLEMENTAR 0 PRÉ-REQUISITO (R) / CLÍNICA MÉDICA PROVA DISCURSIVA RESIDÊNCIA MÉDICA SUPLEMENTAR 0 PRÉ-REQUISITO (R) / CLÍNICA MÉDICA PROVA DISCURSIVA ) Idosa de 8 anos, ex-tabagista (carga
ANEXO III SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO E FOLHETO INFORMATIVO
 ANEXO III SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO E FOLHETO INFORMATIVO Nota: Estas alterações ao Resumo das Características do Medicamento e ao Folheto Informativo são válidas
ANEXO III SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO E FOLHETO INFORMATIVO Nota: Estas alterações ao Resumo das Características do Medicamento e ao Folheto Informativo são válidas
Cada ml de Piridoxina Labesfal, 150 mg/ml, Solução injectável, contém 150 mg de cloridrato de piridoxina como substância activa.
 FOLHETO INFORMATIVO Leia atentamente este folheto antes de tomar o medicamento. Conserve este folheto. Pode ter necessidade de o reler. Caso tenha dúvidas, consulte o seu médico ou farmacêutico. Este medicamento
FOLHETO INFORMATIVO Leia atentamente este folheto antes de tomar o medicamento. Conserve este folheto. Pode ter necessidade de o reler. Caso tenha dúvidas, consulte o seu médico ou farmacêutico. Este medicamento
APROVADO EM INFARMED
 FOLHETO INFORMATIVO Leia atentamente este folheto antes de utilizar o medicamento - Conserve este folheto. Pode ter necessidade de o reler. - Caso tenha dúvidas, consulte o seu médico ou farmacêutico.
FOLHETO INFORMATIVO Leia atentamente este folheto antes de utilizar o medicamento - Conserve este folheto. Pode ter necessidade de o reler. - Caso tenha dúvidas, consulte o seu médico ou farmacêutico.
Grupo farmacoterapêutico: Antiparkinsónico, dopaminérgico (agonista da dopamina).
 FOLHETO INFORMATIVO Pergolida Teva 1 mg Comprimidos Pergolida Leia atentamente este folheto antes de tomar este medicamento: Conserve este folheto. Pode ter necessidade de o reler. Caso ainda tenha dúvidas,
FOLHETO INFORMATIVO Pergolida Teva 1 mg Comprimidos Pergolida Leia atentamente este folheto antes de tomar este medicamento: Conserve este folheto. Pode ter necessidade de o reler. Caso ainda tenha dúvidas,
www.printo.it/pediatric-rheumatology/pt/intro
 www.printo.it/pediatric-rheumatology/pt/intro Esclerodermia Versão de 2016 2. DIFERENTES TIPOS DE ESCLERODERMIA 2.1 Esclerodermia localizada 2.1.1 Como é diagnosticada a esclerodermia localizada? O aspeto
www.printo.it/pediatric-rheumatology/pt/intro Esclerodermia Versão de 2016 2. DIFERENTES TIPOS DE ESCLERODERMIA 2.1 Esclerodermia localizada 2.1.1 Como é diagnosticada a esclerodermia localizada? O aspeto
Anexo II. Conclusões científicas e fundamentos para as conclusões
 Anexo II Conclusões científicas e fundamentos para as conclusões 8 Conclusões científicas e fundamentos para as conclusões O CMDh, tendo avaliado a recomendação do PRAC datada de 5 de setembro de 2013
Anexo II Conclusões científicas e fundamentos para as conclusões 8 Conclusões científicas e fundamentos para as conclusões O CMDh, tendo avaliado a recomendação do PRAC datada de 5 de setembro de 2013
EXAME MÉDICO DE CONDUTORES OU CANDIDATOS A CONDUTORES DE VEÍCULOS A MOTOR (artigo 26.º n.º1 do RHLC)
 MINISTÉRIO DA SAÚDE DIREÇÃO-GERAL DA SAÚDE EXAME MÉDICO DE CONDUTORES OU CANDIDATOS A CONDUTORES DE VEÍCULOS A MOTOR (artigo 26.º n.º1 do RHLC) 1ª PARTE A PREENCHER PELO INTERESSADO IDENTIFICAÇÃO (Nome
MINISTÉRIO DA SAÚDE DIREÇÃO-GERAL DA SAÚDE EXAME MÉDICO DE CONDUTORES OU CANDIDATOS A CONDUTORES DE VEÍCULOS A MOTOR (artigo 26.º n.º1 do RHLC) 1ª PARTE A PREENCHER PELO INTERESSADO IDENTIFICAÇÃO (Nome
HIPERTENSÃO ARTERIAL
 HIPERTENSÃO ARTERIAL HIPERTENSÃO ARTERIAL A pressão arterial VARIA de batimento a batimento do coração, ajustando-se às atividades desenvolvidas ao longo do dia. Tais variações são fisiológicas e imperceptíveis,
HIPERTENSÃO ARTERIAL HIPERTENSÃO ARTERIAL A pressão arterial VARIA de batimento a batimento do coração, ajustando-se às atividades desenvolvidas ao longo do dia. Tais variações são fisiológicas e imperceptíveis,
Opioides: conceitos básicos. Dra Angela M Sousa CMTD-ICESP
 Opioides: conceitos básicos Dra Angela M Sousa CMTD-ICESP OPIOIDES OPIOIDES Classificação receptores opióides Receptor opióide clássico MECANISMO DE AÇÃO Conceitos da farmacologia opióide Receptores μ
Opioides: conceitos básicos Dra Angela M Sousa CMTD-ICESP OPIOIDES OPIOIDES Classificação receptores opióides Receptor opióide clássico MECANISMO DE AÇÃO Conceitos da farmacologia opióide Receptores μ
Vasculite sistémica primária juvenil rara
 www.printo.it/pediatric-rheumatology/br/intro Vasculite sistémica primária juvenil rara Versão de 2016 2. DIAGNÓSTICO E TRATAMENTO 2.1 Quais são os tipos de vasculite? Como é a vasculite classificada?
www.printo.it/pediatric-rheumatology/br/intro Vasculite sistémica primária juvenil rara Versão de 2016 2. DIAGNÓSTICO E TRATAMENTO 2.1 Quais são os tipos de vasculite? Como é a vasculite classificada?
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO. Cada saqueta de contém as seguintes substâncias activas:
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Molaxole pó para solução oral 2. COMPOSICÃO QUALITATIVA E QUANTITATIVA Cada saqueta de contém as seguintes substâncias activas: Macrogol
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO Molaxole pó para solução oral 2. COMPOSICÃO QUALITATIVA E QUANTITATIVA Cada saqueta de contém as seguintes substâncias activas: Macrogol
